Изобретение относится к медицине, конкретно к фармакологии и клеточным технологиям.
Существует большое количество способов стимуляции регенерации тканей с помощью различных фармакологических агентов [1, 2].
Известен способ стимуляции регенерации тканей (легочной ткани) с помощью введения SDF-1 - фактора (stromal cell derived factor-1) в зону повреждения на фоне предварительного курсового системного введения в организм G-CSF (granulocyte-colony stimulating factor) [3]. Данный способ является наиболее близким к заявляемому и выбран в качестве прототипа.
Недостатком способа-прототипа является его недостаточная эффективность и ограничение показания к применению при повреждении легочной ткани.
Задачей, решаемой данным изобретением, является повышение эффективности способа, а также расширение показаний к его применению.
Поставленная задача достигается техническим решением, заключающимся в стимуляции регенерации тканей при моделировании кожной раны с помощью наружного применения SDF-1 с 1-х по 7 сут раневого процесса 1 раз в день в дозе 5 нг (нанограмм) и подкожного введения G-CSF в течение 3-х сут 1 раз в день в дозе 125 мкг/кг (микрограмм/киллограмм) начиная с 5 сут после моделирования раны.
Новым в предлагаемом изобретении является стимуляция регенерации тканей при введении G-CSF 1 раз в день в дозе 125 мкг/кг в течение 3-х сут в организм начиная с 5 сут после моделирования раны на фоне наружного использования SDF-1 с 1-х по 7 сут раневого процесса в дозе 5 нг (нанограмм).
Полученные в последние годы сведения о свойствах и закономерностях жизнедеятельности поли(мульти)потентных клеток-предшественников открыли возможность развития нового направления в лечении многих заболеваний - клеточной терапии. При этом наиболее физиологичным подходом к решению задач регенеративной медицины является фармакологическая стимуляция эндогенных стволовых клеток (СК) [4].
Известна возможность стимуляции мобилизации стволовых клеток тканей депо в периферическую кровь с помощью гранулоцитарного колониестимулирующего фактора (G-CSF, Г-КСФ) [3, 4], а также способность SDF-1 связывать прогениторные клетки различных классов и тем самым влиять на их миграцию и хоминг [3]. Учитывая данные обстоятельства, был разработан способ стимуляции регенерации поврежденной легочной ткани путем введения SDF-1 в зону повреждения легкого после курсового системного введения G-CSF [3]. Использование описанной последовательности применения указанных веществ, а именно предварительного введения G-CSF, представляется обоснованным и целесообразным [3]. Так как предполагается, что SDF-1 обеспечивает хоминг уже мобилизованных в кровь с помощью G-CSF стволовых клеток (СК). При этом возможность повышения эффективности способа за счет изменения последовательности и сроков использования данных фармакологических веществ не изучена. Кроме того, известная значительная специфика функционирования различных тканей организма [4, 5] не позволяет рассчитывать на универсальность известного способа и возможность его эффективного применения в отношении кожи.
Факт стимуляции регенерации тканей при введении G-CSF после использования SDF-1 для достижения выраженных терапевтических эффектов для специалиста является неочевидным. Эксперимент показал непредсказуемые результаты.
Новые свойства не вытекают явным образом из уровня техники в данной области. Идентичной совокупности признаков не обнаружено при исследовании уровня техники по патентной и научно-медицинской литературе.
Предлагаемое изобретение может быть использовано в медицине.
Исходя из вышеизложенного, следует считать заявляемое техническое решение соответствующим критериям: «Новизна», «Изобретательский уровень», «Промышленная применимость».
Способ осуществляют следующим образом.
Лабораторному животному с 1-х по 7 сут после моделирования кожной раны наружно наносят SDF-1 в дозе 5 нг начиная с 5 сут после моделирования кожной раны, в течение 3-х сут подкожно вводят G-CSF 1 раз в день в дозе 125 мкг/кг.
Предлагаемый способ был изучен в экспериментах на беспородных мышах в количестве 56 штук, массой 20-22 г. Животные получены из отдела экспериментальных биологических моделей НИИФиРМ им. Е.Д. Гольдберга Томского НИМЦ. Исследования проводили в соответствии с правилами лабораторной практики (GLP), Приказом МЗСР РФ №708н от 23.08.2010 «Об утверждении правил лабораторной практики», Федеральным Законом от 12 апреля 2010 г. №61-ФЗ «Об обращении лекарственных средств», «Руководством по проведению доклинических исследований новых лекарственных средств» (Москва, 2013).
Пример 1
Эффективность регенерации тканей предлагаемого способа изучали на модели плоскостной кожной раны [6, 7]. На депилированном участке спины у мышей под легким эфирным наркозом вырезали лоскут кожи размером 10×10 мм. Для моделирования более длительного заживления струп с экспериментальной раны регулярно (через сутки) снимали.
Используемые вещества вводили экспериментальным животным по трем схемам.
1 схема. После моделирования кожной раны лабораторным животным с 1-х по 7 сут наружно наносили 50 микролитров раствора SDF-1 (SDF-1 alfa, STEMCELL Technologies, Канада) в дозе 5 нг. Начиная с 5 сут эксперимента в течение 3-х дней подкожно вводили раствор G-CSF (Нейпоген, «Hoffman-la Roche», Швейцария) 1 раз в день в дозе 125 мкг/кг (0,2 мл). Растворы фармакологических веществ готовили согласно прилагаемым к ним инструкциям к применению фирм-производителей.
2 схема. По способу прототипу после моделирования кожной раны лабораторным животным с 1-х по 7 сут наружно наносили 50 микролитров раствора SDF-1 (SDF-1 alfa, STEMCELL Technologies, Канада) в дозе 5 нг. Перед моделированием кожной раны животным в течение 5 дней подкожно вводили раствор G-CSF (Нейпоген, «Hoffman-la Roche», Швейцария) 1 раз в день в дозе 125 мкг/кг (0,2 мл).
3 схема. Кроме того, после моделирования кожной раны лабораторным животным с 1-х по 7 сут наружно наносили 50 микролитров раствора SDF-1 (SDF-1 alfa, STEMCELL Technologies, Канада) в дозе 5 нг на фоне подкожного введения (начиная одновременно с началом применения SDF-1) в течение 3 дней раствора G-CSF (Нейпоген, «Hoffman-la Roche», Швейцария) 1 раз в день в дозе 125 мкг/кг (0,2 мл).
Используемые дозы фармакологических средств были отобраны в предварительных экспериментах в качестве наиболее эффективных.
Контрольные животные в аналогичных режимах и аналогичными способами получали эквивалентные объемы физиологического раствора.
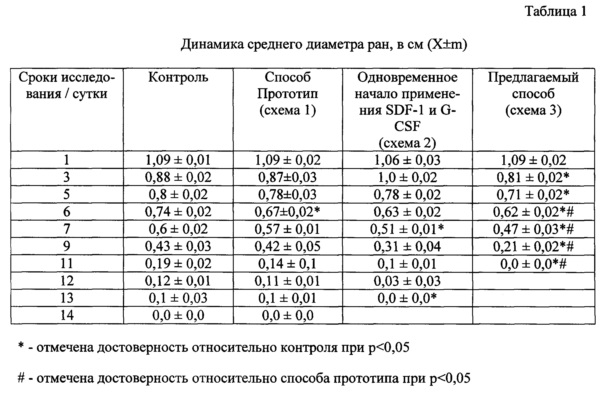
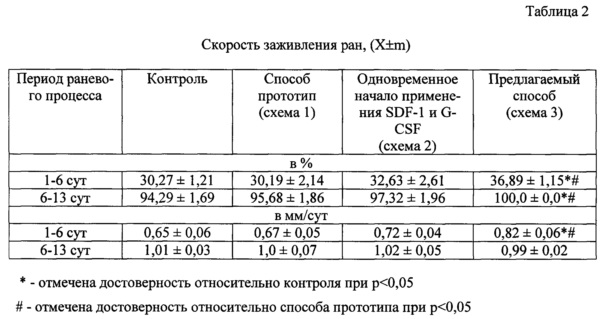
Критериями стимулирующего регенерацию действия служили средний диаметр раны на протяжении всего эксперимента, а также скорость заживления в % и мм/сут (миллиметрах в сутки) с 1 по 6 день и с 6 по 13 день раневого процесса. Обработку результатов проводили методом вариационной статистики с использованием t критерия Стьюдента и непараметрического U критерия Манна-Уитни.
В ходе эксперимента заживление ран у контрольных животных отмечалось к 14 сут опыта. Использование фармакологических веществ по способу-прототипу практически не влияло на показатели скорости регенерации кожи, исключение составляло лишь снижение среднего диаметра раны на 6-е сут эксперимента (табл. 1, 2). Вместе с тем одновременное начало использования фармакологических веществ приводило к ускоренному течению репаративных процессов и восстановлению повреждений к 13 сут (табл. 1). Однако статистически значимых различий в отношении расчетных показателей скорости заживления ран в первый (1-6 сут) и во второй (6-13 сут) между данной опытной и контрольной группами не наблюдалось (табл. 2).
В то же время использование фармакологических веществ по предлагаемому способу вызывало значительную стимуляцию регенерации кожи. Заживление дефекта в данном случае наблюдалось к 11 сут опыта. При этом на протяжении всего эксперимента регистрировалось выраженное снижение размера ран и возрастание скорости их заживления (табл. 1, 2).
В целом, полученные результаты свидетельствуют о максимально эффективном использовании SDF-1 и G-CSF для стимуляции процесса заживления кожи при введении G-CSF в организм во второй период раневого процесса - в фазу регенерации [2, 5] на фоне продолжения проведения терапии SDF-1 в зоне поражения, начинающейся сразу после моделирования дефекта кожи. В основе повышения эффективности предлагаемого способа, очевидно, лежит обеспечение максимальной синхронизации процессов эпителизации и созревания грануляционной ткани в ране. По-видимому, SDF-1 в таком случае способствует миграции преимущественно стромальных клеток-предшественников в зону поражения [4, 8] из близлежащих тканей, что обеспечивает быстрое формирование грануляций, необходимых для приживления и разрастания эпителиальных клеток [9], образующихся, в свою очередь, в дальнейшем из мигрирующих под влиянием G-CSF стволовых клеток тканей-депо [4, 8]. Изменение же последовательности применения данных средств, вероятно, сопровождается разобщением процессов эпителизации и созревания грануляционной ткани [9]. В случае предварительного введения G-CSF (или одновременного с началом терапии SDF-1), мобилизованные G-CSF клетки-предшественники, вероятно, из крови попадают в условия, в которых реализация их регенеративного потенциала существенно затруднена, вследствие отсутствия адекватного микроокружения - грануляционной ткани. При этом низкий уровень «приживаемости» мигрировавших в зону поражения СК, в конечном итоге, приводит к быстрому истощению циркулирующего в крови пула мобилизованных СК [4, 8] и дефициту родоначальных элементов эпителия в период достаточного развития грануляций.
Цитируемая литература
1. Машковский М.Д. Лекарственные средства: 15-е изд. - М.: ОО «Изд-во Новая Волна», 2008. - 1206 с.
2. Котельников В.П. Раны и их лечение. - М.: Знание. 1991. - 123 с.
3. Hannoush E.J., Sifri Z.C., Elhassan I.O., е.а. Impact of enhanced mobilization of bone marrow derived cells to site of injury // J Trauma. 2011, V.71, N2. - P. 283-289.
4. Дыгай A.M., Зюзьков Г.Н. Клеточная терапия: новые подходы // Наука в России. - Москва: Изд-во «Наука», 2009. - Том. 169. - №1. С. 4-8.
5. Бабаева А.Г. Регенерация: факты и перспективы. - М. Изд-во РАМН, 2009. - 336 с.
6. Методические рекомендации по изучению дерматотропных лекарственных средств // Руководство по проведению доклинических исследований новых лекарственных средств / Под ред. А.Н. Миронова. - М.: Гриф и К, 2013. - С. 738-745 (944 с.).
7. Зюзьков Г.Н., Поветьева Т.Н., Семенов А.А. и др. Патент (RU) на изобретение №2475260 «Средство, обладающее регенеративной активностью» (опубл. 20.02.2013, Бюл. №5).
8. Дыгай A.M., Зюзьков Г.Н., Жданов В.В. и др. Иммобилизированный гранулоцитарный колониестимулирующий фактор. Фармакологические свойства и перспективы использования. - Томск: Изд-во: ООО «Печатная мануфактура», 2011. - 149 с.
9. Аничков Н.Н., Волкова К.Г., Гаршин В.Г. Морфология заживления ран. - М.: Медгиз, 1951. - 123 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВА, СТИМУЛИРУЮЩИЕ РЕГЕНЕРАЦИЮ ТКАНЕЙ | 2013 |
|
RU2599289C2 |
| СПОСОБ СТИМУЛЯЦИИ МИЕЛОПОЭЗА | 2008 |
|
RU2366452C1 |
| СПОСОБ ПОЛУЧЕНИЯ КЛЕТОЧНОГО МАТЕРИАЛА ДЛЯ ТРАНСПЛАНТАЦИИ ПРИ МИЕЛОСУПРЕССИИ | 2008 |
|
RU2392947C1 |
| ГЕПАТОПРОТЕКТОРНОЕ СРЕДСТВО | 2010 |
|
RU2444569C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТЬЮ | 2012 |
|
RU2481836C1 |
| ЦЕРЕБРОПРОТЕКТОРНОЕ СРЕДСТВО | 2013 |
|
RU2517282C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИДИАБЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2313361C1 |
| Гемостимулирующее средство | 2017 |
|
RU2647833C1 |
| ГЕМОСТИМУЛИРУЮЩЕЕ СРЕДСТВО | 2013 |
|
RU2535021C1 |
| СПРЕЙ, ОБЛАДАЮЩИЙ РАНОЗАЖИВЛЯЮЩИМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ | 2021 |
|
RU2790489C2 |
Изобретение относится к медицине и может быть использовано для стимуляции регенерации тканей. Регенерацию тканей стимулируют при моделировании кожной раны у мыши с помощью наружного применения SDF-1 с 1-х по 7-е сутки раневого процесса 1 раз в день в дозе 5 нг (нанограмм) и подкожного введения G-CSF в течение 3 суток 1 раз в день в дозе 125 мкг/кг (микрограмм/килограмм) начиная с 5-х суток после моделирования раны. Изобретение позволяет стимулировать регенерацию кожных тканей. 2 табл., 1 пр.
Способ стимуляции регенерации тканей, заключающийся во введении в зону повреждения SDF-1 и в системном введении в организм мыши G-CSF, при котором стимулируют регенерацию тканей при моделировании кожной раны у мыши с помощью наружного применения SDF-1 с 1-х по 7-е сутки раневого процесса 1 раз в день в дозе 5 нг (нанограмм) и подкожного введения G-CSF в течение 3 суток 1 раз в день в дозе 125 мкг/кг (микрограмм/килограмм) начиная с 5-х суток после моделирования раны.
| HANNOUSH EJ et al | |||
| Impact of enhanced mobilization of bone marrow derived cells to site of injury // J Trauma | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| БИОКОМПОЗИТ ДЛЯ ОБЕСПЕЧЕНИЯ ВОССТАНОВИТЕЛЬНЫХ ПРОЦЕССОВ ПОСЛЕ ПОВРЕЖДЕНИЯ У МЛЕКОПИТАЮЩЕГО, СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ПРИМЕНЕНИЯ | 2011 |
|
RU2519326C2 |
| Стопорное приспособление к автоматическим раздатчикам жидкости | 1928 |
|
SU22360A1 |
| WO 2011067317 A1, 09.06.2011. | |||
Авторы
Даты
2017-10-31—Публикация
2016-10-24—Подача