Изобретение относится к области органической химии и касается разработки способа получения соединений общей формулы
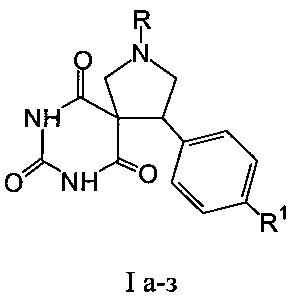
где R=CH3, R1=H (Iа); R=CH3, R1=СН3О (Iб); R=CH3, R1=(СН3)2N (Iв); R=CH3, R1=Cl (Iг); R=C6H5, R1=H (Iд); R=C6H5, R1=СН3О (Ie); R=C6H5, R1=(CH3)2N (Iж); R=С6Н5, R1=Cl (Iз)
Пиримидиновый цикл, спиросочлененный с пирролидиновым кольцом, является практически не исследованной системой. Тем не менее соединения, содержащие пиримидиновый или пирролидиновый циклы, могут в перспективе представлять интерес с точки зрения их практического применения. В частности, соединения, имеющие пиримидиновый цикл, обладают седативной активностью, а также применяются в качестве снотворных средств [М.Д. Машковский. Лекарственные средства, М.: Новая Волна, 2006, с. 21]. Вещества, содержащие в своей структуре пирролидиновое кольцо, проявляют антидепрессантную, анальгетическую и ноотропную активность [В.Г. Граник. Основы медицинской химии. М.: Вузовская книга, 2001, с. 168, 186].
Известен способ получения замещенных 2H-изоиндол-4,7-дионов, основанный на реакции трехкомпонентной гетероциклизации n-хинона с ароматическими альдегидами и иминокислотами [М. Schubert-Zsilavecz, А. Michelirsch, W. Likussar, D. Gusterhuber. Ann. Chem. 1993, 2, S. 147]. Наиболее близким техническим решением является способ получения замещенных 1H-пиррол-3-карбонитрилов, основанный на реакции трехкомпонентной гетероциклизации 2-бензилиденмалононитрила с альдегидами и иминокислотами [С.Б. Носачев, Е.А. Тыркова, А.Г. Тырков. Журн. орган, химии. 2009. 45 (4), 637].
Однако описанные соединения являются аналогами, так как не содержат в своей структуре спиросочлененные пиримидиновый и пирролидиновый циклы.
Техническим результатом является разработка способа получения серии ранее неизвестных 4-арил-2,7,9-триазаспиро[4.5]декан-6,8,10-трионов, основанный на проведении реакции трехкомпонентной гетероциклизации 5-(арилметилен)гексагидропиримидин-2,4,6-трионов, N-метилглицина или N-фенилглицина и формальдегида, позволяющий расширить базу веществ, которые могут быть использованы в качестве потенциальных седативных, антидепрессантных или ноотропных средств.
Для достижения технического результата в способе получения 4-арил-2,7,9-триазаспиро[4.5]декан-6,8,10-трионов общей формулы I
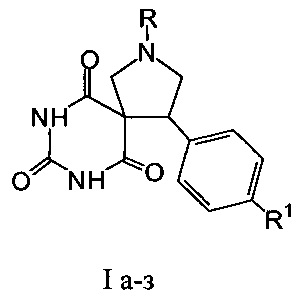
где R=CH3, R1=H (Ia); R=CH3, R1=СН3О (Iб); R=CH3, R1=(СН3)2N (Iв); R=CH3, R1=Cl (Iг); R=C6H5, R1=H (Iд); R=C6H5, R1=СН3О (Ie); R=C6H5, R1=(CH3)2N (Iж); R=С6Н5, R1=Cl (Iз),
проводят реакцию трехкомпонентной гетероциклизации, основанную на смешивании эквимольных количеств 5-(арилметилен)гексагидропиримидин-2,4,6-трионов IIа-з, N-метилглицина IIIа или N-фенилглицина IIIб и формальдегида IV в осушенном толуоле и последующем кипячении реакционной смеси в течение 17 ч, схема
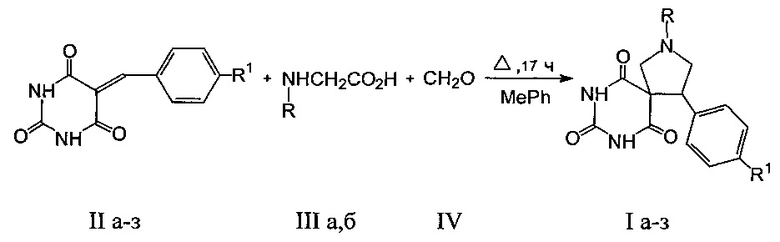
где, R=CH3, R1=H (Ia, IIа, IIIа); R=CH3, R1=СН3О (Iб, IIб, IIIа); R=CH3, R1=(СН3)2N (Iв, IIв, IIIа); R=CH3, R1=Cl (Iг, IIг, IIIа); R=C6H5, R1=H (Iд, IIд, IIIб); R=C6H5, R1=СН3О (Iе, IIе, IIIб); R=C6H5, R1=(CH3)2N (Iж, IIж, IIIж); R=С6Н5, R1=Cl (Iз, IIз, IIIз).
Иное соотношение исходных реагентов (примеры 2-5) не позволяют достигнуть лучшего результата.
Полученный технический результат позволяет получать 4-арил-2,7,9-триазаспиро[4.5]декан-6,8,10-трионы с выходом 38-53%, в структуре которых присутствуют спиросочлененные пиримидиновый и пирролидиновый циклы.
Исходные 5-(арилметилен)гексагидропиримидин-2,4,6-трионы IIа-з могут быть получены по методике [патент RU №2572081] из пиримидин-2,4,6-триона и соотвествующих ароматических альдегидов.
Примеры способа получения соединений общей формулы Iа-з, заключающегося в смешивании эквимольных количеств 5-(арилметилен) гексагидропиримидин-2,4,6-трионов IIа-з, N-метилглицина IIIа или N-фенилглицина IIIб и формальдегида IV в осушенном толуоле и последующем кипячении реакционной смеси в течение 17 ч, приведены ниже.
Пример 1.
2-Метил-4-фенил-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iа).
К суспензии 5 ммоль (1.08 г) 5-(фенилметилен)-2,4,6-пиримидинтриона IIа в 100 мл осушенного толуола добавляли 5 ммоль (0.45 г) N-метилглицина IIIа и 5 ммоль (0.15 г) параформа IV. Реакционную смесь кипятили 17 ч с обратным холодильником, соединенным через насадку Дина-Старка до полного прекращения выделения воды, затем растворитель упаривали под вакуумом, остаток обрабатывали 25 мл диэтилового эфира и нерастворимый остаток хроматографировали на нисходящей стеклянной колонке, заполненной активированным силикагелем марки Silicagel 100/400 мкм, элюент - этанол.
Получают 0.57 г (42%) целевого соединения с т.разл. 281-283°С.
Найдено, %: С 61.37; Н 5.41; N 15.21. C14H15N3O3.
Вычислено, %: С 61.53; Н 5.50; N 15.38.
ИКС, ν, см-1 (группа): 3550 (NH); 1770, 1750 (С=O).
ЯМР1Н, δ, м.д. (группа): 11.35 уш (1H, NH); 11.22 уш (1H, NH); 8.10-7.45 м (5Наром., С6Н5); 3.80 с (2Н, СН2); 3.65 т (1H, СН, 3J 9.0 Гц); 3.10-3.05 дд (2Н, СН2); 2.41 с (3Н, СН3).
ЯМР13С, δ, м.д. (группа): 163.4 (С6); 161.6 (С10); 154.7 (С8); 133.1 (C12); 132.7 (С11); 132.2 (С13); 128.1 (С14); 61.8 (С3); 61.5 (C1); 57.1 (С5); 55.1 (С4); 41.5 (СН3).
Пример 2.
2-Метил-4-фенил-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iа).
Получают аналогично примеру 1, только берут 10 ммоль (0.90 г) N-метилглицина IIIа и 10 ммоль (0.30 г) параформа IV. Выход соединения Iа составляет 35%.
Пример 3.
2-Метил-4-фенил-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iа).
Получают аналогично примеру 1, только берут 3 ммоль (0.267 г) N-метилглицина IIIа и 3 ммоль (0.09 г) параформа IV. Выход соединения Iа составляет 38%.
Пример 4.
2-Метил-4-фенил-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iа).
Получают аналогично примеру 1, только берут 10 ммоль (0.90 г) N-метилглицина IIIа и 3 ммоль (0.09 г) параформа IV. Выход соединения Iа составляет 35%.
Пример 5.
2-Метил-4-фенил-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iа).
Получают аналогично примеру 1, только берут 3 ммоль (0.267 г) N-метилглицина IIIа и 10 ммоль (0.30 г) параформа IV. Выход соединения Iа составляет 34%.
Пример 6.
2-Метил-4-(4-метоксифенил)-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iб).
Получают аналогично примеру 1, только берут 5 ммоль (1,23 г) 5-(4-метоксифенилметилен)-2,4,6-пиримидинтриона IIб, 5 ммоль (0.45 г) N-метилглицина IIIа и 5 ммоль (0.15 г) параформа IV. Получают 0,78 г (51%) целевого соединения с т.разл. 275-277°С.
Найдено, %: С 59.25; Н 5.44; N 13.71. C15H17N3O4.
Вычислено, %: С 59.41; Н 5.61; N 13.86.
ИКС, ν, см-1 (группа): 3550 (NH); 1770, 1750 (С=O).
ЯМР1Н, δ, м.д. (группа): 11.25 уш (1H, NH); 11.12 уш (1H, NH); 7.03-6.83 м (4Наром., C6H4, 3J 8.0 Гц); 3.81 с (2Н, СН2); 3.72 с (3Н, СН3О); 3.64 т (1H, СН, 3J 9.0 Гц); 3.02-2.99 дд (2Н, СН2); 2.40 с (3Н, СН3).
ЯМР13С, δ, м.д. (группа): 163.9 (С6); 163.4 (С10); 162.3 (С14); 155.0 (С8); 137.4 (C12); 125.3 (С11); 113.8 (C13); 61.7 (С3); 61.4 (C1); 56.8 (С5); 55.8 (СН3О); 54.9 (С4);41.4 (СН3).
Пример 7.
4-(4-Диметиламинофенил)-2-метил-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iв).
Получают аналогично примеру 1, только берут 5 ммоль (1,30 г) 5-(4-диметиламинофенилметилен)-2,4,6-пиримидинтриона IIв, 5 ммоль (0.45 г) N-метилглицина IIIа и 5 ммоль (0.15 г) параформа IV. Получают 0,84 г (53%) целевого соединения с т.разл. 301-303°С.
Найдено, %: С 60.59; Н 6.18; N 17.56. C16H20N4O3.
Вычислено, %: С 60.76; Н 6.33; N 17.72.
ИКС, ν, см-1 (группа): 3550 (NH); 1770, 1750 (С=O).
ЯМР1Н, δ, м.д. (группа): 11.20 уш (1Н, NH); 11.05 уш (1H, NH); 8.25-6.91 м (4Наром., С6Н4, 3J 8.0 Гц); 3.79 с (2Н, СН2); 3.62 т (1Н, СН, 3J 9.0 Гц); 2.99-2.96 дд (2Н, СН2); 2.94 с (6Н, CH3N); 2.40 с (3Н, СН3).
ЯМР13С, δ, м.д. (группа): 163.4 (С6); 161.6 (С10); 155.1 (С8); 151.1 (С14); 130.7 (С12); 121.9 (С11); 112.3 (C13); 61.6 (С3); 61.3 (C1); 56.9 (С5); 55.2 (С4); 41.5 (СН3); 40.1(СН3).
Пример 8.
2-Метил-4-(4-хлорфенил)-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iг).
Получают аналогично примеру 1, только берут 5 ммоль (1,25 г) 5-(4-хлорфенилметилен)-2,4,6-пиримидинтриона IIг, 5 ммоль (0.45 г) N-метилглицина IIIа и 5 ммоль (0.15 г) параформа IV. Получают 0,61 г (40%) целевого соединения с т.разл. 285-288°С.
Найдено, %: С 54.48; Н 4.38; N 13.51. C14H14ClN3O3.
Вычислено, %: С 54.63; Н 4.55; N 13.66.
ИКС, ν, см-1 (группа): 3550 (NH); 1770, 1750 (С=O).
ЯМР1Н, δ, м.д. (группа): 11.45 уш (1Н, NH); 11.35 уш (1Н, NH); 8.20-7.58 м (4Наром., С6Н4, 3J 8.0 Гц); 3.82 с (2Н, СН2); 3.68 т (1Н, СН, 3J 9.0 Гц); 3.11-3.07 дд (2Н, СН2); 2.40 с (3Н, СН3).
ЯМР13С, δ, м.д. (группа): 163.3 (С6); 162.9 (С10); 155.2 (С8); 135.7 (С14); 133.2 (С11); 129.7 (С13); 129.3 (C12); 62.6 (С3); 62.1 (С1); 58.2 (С5); 55.8 (С4); 41.6 (СН3).
Пример 9.
2,4-Дифенил-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iд).
Получают аналогично примеру 1, только берут 5 ммоль (1.08 г) 5-(фенилметилен)-2,4,6-пиримидинтриона IIа, 5 ммоль (0.76 г) N-фенилглицина IIIб и 5 ммоль (0.15 г) параформа IV. Получают 0,69 г (41%) целевого соединения с т.разл. 294-297°С.
Найдено, %: С 67.91; Н 4.93; N 12.38. C19H17N3O3.
Вычислено, %: С 68.06; Н 5.07; N 12.54.
ИКС, ν, см-1 (группа): 3550 (NH); 1770, 1750 (С=O).
ЯМР1Н, δ, м.д. (группа): 11.34 уш (1Н, NH); 11.24 уш (1Н, NH); 8.15-7.44 м (10Наром., 2С6Н5, 3J 8.0 Гц); 3.81 с (2Н, СН2); 3.64 т (1Н, СН, 3J 9.0 Гц); 3.11-3.04 дд (2Н, СН2).
ЯМР13С, δ, м.д. (группа): 163.5 (С6); 161.4 (С10); 154.8 (С8); 144.7 (С'11); 133.8 (С'12); 132.5 (С'13); 133.2 (С12); 132.5 (С11); 132.4 (С13); 128.6 (С'14); 128.2 (С14); 61.7 (С3); 61.3 (C1); 57.2 (С5); 55.2 (С4).
Пример 10.
4-(4-Метоксифенил)-2-фенил-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Ie).
Получают аналогично примеру 1, только берут 5 ммоль (1,23 г) 5-(4-метоксифенилметилен)-2,4,6-пиримидинтриона IIб, 5 ммоль (0.76 г) N-фенилглицина IIIб и 5 ммоль (0.15 г) параформа IV. Получают 0,78 г (43%) целевого соединения с т.разл. 287-290°С.
Найдено, %: С 65.59; Н 5.08; N 11.34. C20H19N3O4.
Вычислено, %: С 65.75; Н 5.21; N 11.51.
ИКС, ν, см-1 (группа): 3550 (NH); 1770, 1750 (С=O).
ЯМР1Н, δ, м.д. (группа): 11.22 уш (1Н, NH); 11.15 уш (1Н, NH); 8.10-6.84 м (9Наром., С6Н4, С6Н5); 3.83 с (2Н, СН2); 3.74 с (3Н, СН3О); 3.65 т (1Н, СН, 3J 9.0 Гц); 3.05-3.01 дд (2Н, СН2).
ЯМР13С, δ, м.д. (группа): 163.8 (С6); 163.6 (С10); 162.4 (С14); 155.2 (С8); 144.5 (С'11); 137.6 (С12); 133.6 (С'12); 132.2 (С'13); 128.9 (С'14); 125.5 (С11); 113.9 (С13); 61.8 (С3); 61.6 (С1); 56.9 (С5); 55.9 (СН3О); 54.8 (С4).
Пример 11.
4-(4-Диметиламинофенил)-2-фенил-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iж).
Получают аналогично примеру 1, только берут 5 ммоль (1,30 г) 5-(4-диметиламинофенилметилен)-2,4,6-пиримидинтриона IIв, 5 ммоль (0.76 г) N-фенилглицина IIIб и 5 ммоль (0.15 г) параформа IV. Получают 0,85 г (45%) целевого соединения с т.разл. 307-310°С.
Найдено, %: С 66.51; Н 5.67; N 14.65. C21H22N4O3.
Вычислено, %: С 66.67; Н 5.82; N 14.81.
ИКС, ν, см-1 (группа): 3550 (NH); 1770, 1750 (С=O).
ЯМР1Н, 8, м.д. (группа): 11.20 уш (1Н, NH); 11.08 уш (1Н, NH); 8.26-6.93 м (9Наром., С6Н4, С6Н5); 3.82 с (2Н, СН2); 3.61 т (1Н, СН, 3J 9.0 Гц); 3.04-2.98 дд (2Н, СН2); 2.94 с (6Н, CH3N).
ЯМР13С, δ, м.д. (группа): 163.5 (С6); 161.3 (С10); 155.2 (С8); 151.2 (С14); 144.3 (С'11); 133.6 (С'12); 132.4 (С'13); 130.5 (С12); 128.8 (С'14); 121.8 (С11); 112.5 (С13); 61.7 (С3); 61.2 (C1); 56.8 (С5); 55.4 (С4); 40.1 (СН3).
Пример 12.
2-Фенил-4-(4-хлорфенил)-2,7,9-триазаспиро[4.5]декан-6,8,10-трион (соединение Iз).
Получают аналогично примеру 1, только берут 5 ммоль (1,25 г) 5-(4-хлорфенилметилен)-2,4,6-пиримидинтриона IIг, 5 ммоль (0.76 г) N-фенилглицина IIIб и 5 ммоль (0.15 г) параформа IV. Получают 0,70 г (38%) целевого соединения с т.разл. 290-293°С.
Найдено, %: С 61.54; Н 4.19; N 11.22. C19H16ClN3O3.
Вычислено, %: С 61.71; Н 4.33; N 11.37.
ИКС, ν, см-1 (группа): 3550 (NH); 1770, 1750 (С=O).
ЯМР1Н, δ, м.д. (группа): 11.50 уш (1Н, NH); 11.37 уш (1H, NH); 8.25-7.60 м (9Наром., С6Н4, С6Н5); 3.81 с (2Н, СН2); 3.65 т (1Н, СН, 3J 9.0 Гц); 3.08-3.02 дд (2Н, СН2).
ЯМР13С, δ, м.д. (группа): 163.4 (С6); 162.8 (С10); 155.4 (С8); 144.5 (С'11); 135.6 (С14); 133.6 (С'12); 133.4 (С11); 132.6 (С'13); 129.9 (С13); 129.4 (С12); 128.9 (С'14); 62.5 (С3); 62.3 (C1); 58.5 (С5); 55.6 (С4); 41.5 (СН3).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1'-АРИЛГЕКСАГИДРО-1Н-СПИРО[ПИРИМИДИН-5,2'-ПИРРОЛИЗИН]-2,4,6(1Н,3Н,5Н)-ТРИОНОВ | 2016 |
|
RU2647240C1 |
| ПРОИЗВОДНЫЕ 2-ТИОУРАЦИЛА, ОБЛАДАЮЩИЕ ПРОТИВОАДЕНОВИРУСНОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2670204C1 |
| Применение 9-ароил-8-гидрокси-6-(2-гидроксиалкил)-2-тиоксо-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов в качестве средств, обладающих высокой противомикробной активностью в отношении S. aureus и C. albicans | 2024 |
|
RU2831126C1 |
| АГЕНТ, АКТИВИРУЮЩИЙ РЕЦЕПТОР, АКТИВИРУЕМЫЙ ПРОЛИФЕРАТОРАМИ ПЕРОКСИСОМ δ | 2007 |
|
RU2435764C2 |
| НОВЫЕ 2',5'-ДИАРИЛСПИРО[ИНДОЛ-3,3'-ПИРРОЛИДИН]-2(1Н)-ОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2019 |
|
RU2730287C1 |
| СПИРОАЗАЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СПОСОБ ИНГИБИРОВАНИЯ АКТИВНОСТИ ИЛИ АКТИВАЦИИ СЕРОТОНИНОВОГО 5-НТ2А РЕЦЕПТОРА, СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНЕННОГО СОСТОЯНИЯ, СВЯЗАННОГО С СЕРОТОНИНОВЫМ 5-НТ2А РЕЦЕПТОРОМ, И ИХ ПРИМЕНЕНИЕ | 2002 |
|
RU2315051C2 |
| Четвертичные аммониевые соли на основе производных витамина В6 | 2015 |
|
RU2607522C1 |
| КАТИОННЫЕ ДИМЕРНЫЕ АМФИФИЛЫ В КАЧЕСТВЕ АГЕНТОВ ТРАНСФЕКЦИИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2233834C2 |
| Способ получения аммонийных солей 3-амино-8-гидрокси-1,6-диоксо-4-циано-2,7-диазаспиро[4.4]нон-3-ен-2-идов | 2016 |
|
RU2631856C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЗАМЕЩЕННЫХ 2-ОКСО-1,2-ДИГИДРОПИРИДИН-3,4-ДИКАРБОНИТРИЛОВ | 2015 |
|
RU2577526C1 |
Изобретение относится к способу получения новых 4-арил-2,7,9-триазаспиро[4.5]декан-6,8,10-трионов общей формулы I, которые могут быть использованы в качестве потенциальных седативных, антидепрессантных или ноотропных средств. В общей формуле I
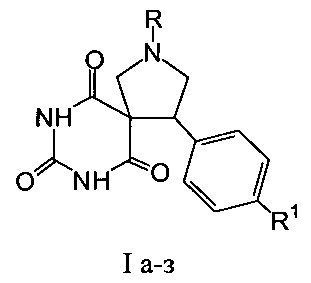
R=CH3, R1=H (Ia); R=CH3, R1=СН3О (Iб); R=CH3, R1=(СН3)2N (Iв); R=CH3, R1=Cl (Iг); R=C6H5, R1=H (Iд); R=C6H5, R1=СН3О (Ie); R=C6H5, R1=(CH3)2N (Iж); R=С6Н5, R1=Cl (Iз). Способ основан на реакции трехкомпонентной гетероциклизации и заключается в том, что осуществляют смешивание эквимольных количеств 5-(арилметилен)гексагидропиримидин-2,4,6-трионов, N-метилглицина или N-фенилглицина и формальдегида в осушенном толуоле с последующим кипячением реакционной смеси в течение 17 ч. 12 пр.
Способ получения 4-арил-2,7,9-триазаспиро[4.5]декан-6,8,10-трионов общей формулы I
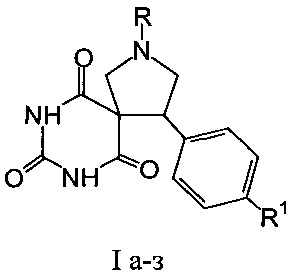
где R=CH3, R1=H (Ia); R=CH3, R1=CH3O (Iб); R=CH3, R1=(CH3)2N (Iв); R=CH3, R1=Cl (Iг); R=C6H5, R1=H (Iд); R=C6H5, R1=CH3O (Ie); R=C6H5, R1=(CH3)2N (Iж); R=C6H5, R1=Cl (Iз),
путем реакции трехкомпонентной гетероциклизации, в основе которой лежит смешивание эквимольных количеств 5-(арилметилен)гексагидропиримидин-2,4,6-трионов, N-метилглицина или N-фенилглицина и формальдегида в осушенном толуоле с последующим кипячением реакционной смеси в течение 17 ч.
| 1,6'-ДИАРИЛ-3-АРОИЛ-4-ГИДРОКСИ-1',3'-ДИМЕТИЛСПИРО[ПИРРОЛ-2,5'-ПИРРОЛО[2,3-d]ПИРИМИДИН]-2',4',5(1Н,1'Н,3'Н)-ТРИОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2502738C2 |
| WO 2006023630 A2, 02.03.2006 & RU 2387647 C9, 27.05.2011 | |||
| С.Б.Носачев и др., 2-Фенил-1,1-дицианоэтен в трехкомпонентной гетероциклизации с альдегидами и иминокислотами", Журнал органической химии, 2009, т.45, (4), 237-238. | |||
Авторы
Даты
2017-11-09—Публикация
2016-07-15—Подача