ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001] Настоящее изобретение относится к аттенуированному мутантному штамму сальмонеллы, содержащему рекомбинантную молекулу ДНК, кодирующую рецепторный белок VEGF. В частности, настоящее изобретение относится к применению указанного аттенуированного мутантного штамма сальмонеллы в иммунотерапии злокачественных опухолей.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
[0002] Аттенуированные производные сальмонеллы энтерика являются перспективными носителями для доставки гетерологичных антигенов, таких как опухолевые антигены или антигены стромы опухоли, к иммунной системе млекопитающего. Возможна доставка штаммов сальмонеллы энтерика посредством иммунизации слизистых оболочек, т.е. перорально или назально, что обеспечивает преимущества, заключающиеся в простоте и безопасности, по сравнению с парентеральным введением. Кроме того, штаммы сальмонеллы вызывают сильный гуморальный и клеточный иммунный ответ на уровне как системного, так и мукозального компартментов. Затраты на смесеприготовление являются относительно низкими, и составы живых бактериальных вакцин обладают высокой устойчивостью. Аттенуацию можно осуществить посредством делеции различных генов, включая вирулентные, регуляторные и метаболические гены.
[0003] Доказано, что несколько штаммов сальмонеллы тифимуриум, аттенуированных посредством мутаций aro, являются безопасными и эффективными средствами доставки для гетерологичных антигенов в моделях животных.
[0004] Методики доставки конструкций ДНК, кодирующих антигены, в частности рецепторные белки VEGF, посредством живых аттенуированных штаммов сальмонеллы тифимуриум к клеткам-мишеням мыши описаны в WO 03/073995. В Niethammer et al. (Nature Medicine 2002, 8(12), 1369) описан аттенуированный штамм сальмонеллы тифимуриум aroA SL7207, который содержит экспрессирующий вектор, кодирующий рецептор-2 фактора роста эндотелия сосудов мыши (VEGFR-2 или FLK-1), и его применение в качестве вакцины против злокачественной опухоли.
[0005] Однако существует только один аттенуированный штамм сальмонеллы энтерика серовар, а именно сальмонеллы энтерика серовар тифи Ty21a (сокращенно: сальмонеллы тифи Ty21a), который принят к применению на людях.
[0006] Эта хорошо переносимая, живая пероральная вакцина против тифоидной лихорадки была получена посредством химического мутагенеза вирулентного бактериального изолята сальмонеллы тифи Ty2 дикого типа и содержит мутацию с потерей функции в гене galE, а также другие менее распознанные мутации. Она залицензирована как тифозная вакцина во многих странах после получения доказательств ее эффективности и безопасности при производственных испытаниях.
[0007] Ангиогенез способствует росту плотной опухоли и метастаза. Было обнаружено, что такие соединения, как бевацизумаб и другие, например, низкомолекулярные соединения, такие как сунитиниб и акситиниб, которые имеют определенную направленность на новообразованные сосуды в опухоли, эффективны при различных указаниях на опухоль (Powles et al., Br J Cancer 2011, 104(5):741-5); Rini et al., Lancet 2011, 378:1931-1939).
[0008] Новообразованные сосуды в опухоли расположены с эндотелиальными клетками, которые сверхэкспрессируют рецептор-2 фактора роста эндотелия сосудов (VEGFR) и легкодоступны через кровоток. Генетическая стабильность этих клеток и их способность поддерживать сотни опухолевых клеток на эндотелиальную клетку делает их основной целью противоопухолевой терапии, или через антитела, ингибиторов тирозинкиназы, или вакцины (Augustin, Trends Pharmacol Sci 1998, 19:216-222). В недавнее время завоевала клинический успех иммунотерапия на основе Т-клеток при раке предстательной железы и подтвердила потенциал вакцинации против злокачественной опухоли, который часто показывали доклинические исследования (Sharma et al., Nat Rev Cancer 2011, 11:805-812). Активация иммунной системы против злокачественных клеток сталкивается с различными проблемами. Например, злокачественные образования часто являются поликлональными, и злокачественные клетки обладают способностью к мутированию. Антиген-специфичная терапия часто приводит только к отбору клеток, не содержащих антиген. Дополнительные затруднения включают инкапсуляцию опухоли и потерю или отрицательную регуляцию MHC молекул. Подходы к вакцинации, направленные на новообразованные сосуды в опухоли, теоретически должны преодолеть эти затруднения.
ЦЕЛИ ИЗОБРЕТЕНИЯ
[0009] Ввиду известного уровня техники целью настоящего изобретения является обеспечение новой безопасной пероральной вакцины против злокачественной опухоли, направленной против рецептора VEGF. Такая вакцина против злокачественной опухоли, направленная против рецептора VEGF, обеспечила бы основное преимущество, заключающееся в усовершенствовании вариантов лечения пациентов со злокачественной опухолью.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0010] Настоящее изобретение является сочетанием антиангиогенной терапии и вакцинации, направленным на VEGFR-2, с использованием новой вакцины (VXM01), которая является аттенуированным и реконструированным бактериальным штаммом сальмонеллы тифи Ty21a, содержащим плазмиду, кодирующую рецепторный белок VEGF-2.
[0011] VXM01 представляет собой новую стратегию посредством направленности не на антиген, находящийся в опухолевых клетках, а на антиген, находящийся в строме опухоли, сверхэкспрессированный незлокачественными эндотелиальными клетками новообразованных сосудов опухоли.
[0012] Посредством направления генетически устойчивых и легкодоступных эндотелиальных клеток этот продукт имеет целью устранение ограничений, встречающихся ранее при вакцинах, направленных непосредственно на опухолевые клетки, таких как гетерогенность опухолевых клеток, потеря MHC, иммуносупрессия на клеточном уровне и инкапсуляция опухоли, а также физиологических барьеров, таких как гематоэнцефалический барьер. Кроме того, ввиду независимости терапевтической цели от типа опухоли, вакцина может обладать потенциальной активностью против многих различных плотных злокачественных новообразований. Данный продукт представляет собой пациентнезависимую, «имеющуюся в готовом виде» пероральную вакцину, которую можно хранить и распространять для применения среди клинических баз. Несмотря на то, что уже была доказана эффективность антиангиогенной терапии либо посредством низкомолекулярных соединений, либо посредством антител, подход по настоящему изобретению существенно отличается благодаря активации собственной иммунной системы пациента против новообразованных сосудов опухоли и по существу потенциально создает эффект запоминания Т-клеток, что обеспечивает длительную эффективность. Исследования с помощью бевацизумаба при раке толстой кишки и раке яичника позволяют предположить, что для поддержания полезного эффекта в лечении в долгосрочной перспективе необходимо непрерывное антиангиогенное давление (Allegra et al., J Clin Oncol 2011, 29:11-16; Burger et al., N Engl J Med 2011, 365:2473-2483; Perren et al., N Engl J Med 2011, 365:2484-2496).
[0013] Насколько известно авторам, это первое клиническое испытание пероральной вакцины против злокачественной опухоли. Кроме того, эта вакцина обладает потенциальной эффективностью против многих различных типов опухолей.
[0014] В ходе первого клинического испытания было доказано, что вакцина по настоящему изобретению (VXM01) обладает высокой эффективностью в вызове иммунного ответа, который существенно влияет на рост опухоли у пациента. Это удивительный и неожиданный факт, что иммунный ответ можно вызвать очень низкими дозами перорально вводимой VXM01. Вакцина является эффективной при дозах, начиная уже с 1×105 или 1×106 до 1×107 колониеобразующих единиц (КОЕ). Первые результаты указывают на то, что вакцинация с помощью VXM01 может привести к нарушению существующей опухолевой сосудистой системы и может поддержать развитие памяти иммунной системы против пролифелирующих эндотелиальных клеток.
[0015] Вакцина эффективна в монотерапии, а также в комбинированном лечении с помощью стандартных химиотерапевтических средств, лучевой терапии и/или биологической терапии злокачественных опухолей.
[0016] В современном клиническом испытании пациентов со стадией IV обрабатывали предварительно и/или одномоментно с помощью химиотерапевтического средства гемцитабин и VXM01. Лечение с помощью VXM01, однако, также является эффективным при развитии у пациентов резистентности к химиотерапии (пациенты с рефрактерностью к химиотерапии).
[0017] В одном из аспектов настоящее изобретение относится к аттенуированному мутантному штамму сальмонеллы тифи, содержащему, по меньшей мере, одну копию рекомбинантной молекулы ДНК, содержащую экспрессирующую кассету, кодирующую рецепторный белок VEGF для применения в качестве вакцины.
[0018] В конкретных вариантах осуществления рецепторный белок VEGF выбран из группы, состоящей из VEGFR-2 человека и его гомолога, степень гомологии которых составляет, по меньшей мере, приблизительно 80%.
[0019] В конкретных вариантах осуществления рецепторный белок VEGF является VEGFR-2 человека с аминокислотной последовательностью, как представлено в SEQ ID NO:1.
[0020] В другом аспекте настоящее изобретение относится к ДНК-вакцине, содержащей аттенуированный мутантный штамм сальмонеллы тифи по настоящему изобретению.
[0021] В конкретных вариантах осуществления аттенуированный мутантный штамм сальмонеллы тифи является сальмонеллой тифи Ty21a.
[0022] В конкретных вариантах осуществления экспрессирующей кассетой является эукариотическая экспрессирующая кассета.
[0023] В конкретных вариантах осуществления ДНК-вакцина по настоящему изобретению предназначена для применения в иммунотерапии злокачественных опухолей.
[0024] В конкретных вариантах осуществления ДНК-вакцина содержит аттенуированный штамм сальмонеллы тифи Ty21a, трансформированный плазмидой, которая содержит ДНК, кодирующую белок VEGFR-2 с SEQ ID NO:1.
[0025] В конкретных вариантах осуществления ДНК-вакцина предназначена для применения в антиангиогенной иммунотерапии злокачественных опухолей.
[0026] В конкретных вариантах осуществления плазмида представляет собой pVAX10.VR2-1 размером 7580 п.н., как изображено на Фиг. 2, и имеет последовательность, как представлено в SEQ ID NO:3, и ДНК-вакцина обозначена как VXM01.
[0027] В конкретных вариантах осуществления злокачественной опухолью является рак поджелудочной железы.
[0028] В конкретных вариантах осуществления указанный рак поджелудочной железы находится на стадии IV или является местнораспространенным раком поджелудочной железы.
[0029] В конкретных вариантах осуществления злокачественная опухоль включает метастазы.
[0030] В конкретных вариантах осуществления лечение проводится в сопровождении химиотерапии и/или лучевой терапии.
[0031] В конкретных вариантах осуществления химиотерапевтическим средством является гемцитабин.
[0032] В конкретных вариантах осуществления иммунотерапевтическое лечение с помощью вакцины проводят в ходе цикла лечения химиотерапией.
[0033] В конкретных вариантах осуществления вакцину вводят перорально.
[0034] В конкретных вариантах осуществления однократная доза вакцины составляет 1×105, 1×106, 1×107, 1×108, 1×109, 1×1010 или 1×1011 колониеобразующих единиц (КОЕ).
[0035] В конкретных вариантах осуществления однократная доза вакцины составляет менее чем 1×109 КОЕ. В конкретных вариантах осуществления однократная доза вакцины составляет от 1×108 до 1×109 КОЕ.
[0036] В конкретных вариантах осуществления однократная доза вакцины составляет менее чем 1×108 КОЕ. В конкретных вариантах осуществления однократная доза вакцины составляет от 1×105 до 1×108 КОЕ, более конкретно - однократная доза вакцины составляет от 1×106 дo 1×107 КОЕ.
[0037] В конкретных вариантах осуществления однократная доза содержит приблизительно от 105 до приблизительно 1011, в частности, приблизительно от 106 до приблизительно 1010, более конкретно - приблизительно от 106 до приблизительно 109, более конкретно - приблизительно от 106 до приблизительно 108, наиболее конкретно - от 106 до приблизительно 107 колониеобразующих единиц (КОЕ).
[0038] В другом аспекте настоящее изобретение относится к ДНК-вакцине VXM01, содержащей аттенуированный штамм сальмонеллы тифи Ty21a, трансформированный плазмидой, которая содержит ДНК, кодирующую белок VEGFR-2 с SEQ ID NO:1, где плазмида представляет собой плазмиду ДНК размером 7580 п.н. и содержит кДНК VEGFR-2 под контролем промотора ЦМВ, канамицин-устойчивого гена и pMB1 ori, и обозначена как pVAX10.VR2-1.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0039] Настоящее изобретение может стать более доступным для понимания посредством ссылки на следующее подробное описание изобретения и включенные в него примеры.
[0040] В одном из аспектов настоящее изобретение относится к аттенуированному мутантному штамму сальмонеллы тифи, содержащему, по меньшей мере, одну копию рекомбинантной молекулы ДНК, содержащей экспрессирующую кассету, кодирующую рецепторный белок VEGF.
[0041] По изобретению аттенуированный мутантный штамм сальмонеллы тифи выполняет функцию бактериального носителя рекомбинантной молекулы ДНК, содержащей экспрессирующую кассету, кодирующую рецепторный белок VEGF, для доставки указанной рекомбинантной молекулы ДНК в клетку-мишень.
[0042] В контексте настоящего изобретения термин «аттенуированный» относится к бактериальному штамму пониженной вирулентности по сравнению с родительским бактериальным штаммом, не содержащим аттенуирующую мутацию. Аттенуированные бактериальные штаммы предпочтительно утратили свою вирулентность, но сохранили способность вызывать защитный иммунитет. Аттенуацию можно осуществить посредством делеции различных генов, включая вирулентные, регуляторные и метаболические гены. Аттенуированные бактерии можно найти в природе, или их можно получать искусственно в лабораторных условиях, например, посредством адаптирования к новой среде или культуре клеток, или их можно получать посредством технологии рекомбинантных ДНК.
[0043] В контексте настоящего изобретения термин «мутантный штамм» относится к бактериальному штамму, содержащему мутацию в своем геноме. В этом контексте термин «мутация» относится к изменению в последовательности нуклеиновой кислоты, включая точечные мутации, вставки, делеции, транслокации и инверсии.
[0044] В контексте настоящего изобретения термин «содержит» или «содержащий» означает «включая, но не ограничиваясь ими». Предполагается, что это неограничивающий термин для уточнения присутствия какой-либо из указанных характеристик, элементов, целых чисел, стадий или компонентов, но не для исключения присутствия или добавления одной или нескольких других характеристик, элементов, целых чисел, стадий, компонентов или групп. Термин «cодержащий», таким образом, включает более ограничивающие термины «состоящий из» и «по существу состоящий из». В одном из вариантов осуществления термин «cодержащий», употребляемый на всем протяжении заявки и, в частности, в рамках формулы изобретения, можно заменить термином «состоящий из».
[0045] В контексте настоящего изобретения термин «рекомбинантная молекула ДНК» относится к созданной конструкции ДНК, предпочтительно состоящей из частей ДНК различного происхождения. Рекомбинантной молекулой ДНК может быть линейная нуклеиновая кислота или, предпочтительно, кольцевая рекомбинантная ДНК плазмида, образованная посредством введения открытой рамки считывания, кодирующей рецепторный белок VEGF в экспрессирующую векторную плазмиду.
[0046] В контексте настоящего изобретения термин «экспрессирующая кассета» относится к единице нуклеиновой кислоты, содержащей, по меньшей мере, рецепторный белок VEGF под контролем регуляторных последовательностей, контролирующих его экспрессию. Экспрессирующая кассета, содержащаяся в аттенуированном мутантном штамме сальмонеллы, может предпочтительно содействовать транскрипции включенной открытой рамки считывания, кодирующей рецепторный белок VEGF в клетке-мишени. Экспрессирующие кассеты, как правило, содержат промотор, по меньшей мере, одну открытую рамку считывания и сигнал терминации транскрипции.
[0047] Рецепторные белки VEGF являются рецепторными тирозинкиназами, специфичными эндотелиальным клеткам, которые могут быть соединены лигандом фактора роста эндотелия сосудов (VEGF), который вызывает их димеризацию и активируется посредством трансфосфорилирования. Семейство факторов роста VEGF (Kd 75-760 пМ) включает 6 представителей семейства, VEGF-A (также известный как VEGF) посредством E и PLGF (плацентарного фактора роста, также известного как PGF или PIGF-2). Факторы роста VEGF регулируют рост и дифференцировку многочисленных компонентов сосудистой системы, в особенности кровеносных и лимфатических сосудов. Существует три основных подтипа VEGFR, VEGFR-1 (или FLT1), VEGFR-2 (или KDR, FLK1) и VEGFR-3 (или FLT4). Мембраносвязанные рецепторы VEGF имеют внеклеточную часть, состоящую из 7 иммуноглобулин-подобных доменов, единичного трансмембранного участка и внутриклеточной части, содержащей расщепленный тирозин-киназный домен. Транскрипты VEGFR также способствуют возникновению альтернативных вариантов сплайсинга, кодирующих растворимые рецепторные белки VEGF.
[0048] Как представляется, VEGFR-2, также известный как рецептор, имеющий в составе домен, содержащий киназу (KDR), опосредует почти все известные клеточные реакции на VEGF. Например, как представляется, роль VEGF в ангиогенезе опосредована взаимодействием этого белка с VEGFR-2. VEGFR-2 является высокоаффинным рецептором с длиной 1356 аминокислот, с молекулярной массой 200-230 кДа для VEGF, а также для VEGF-C и VEGF-D. При определении посредством скрининга эндотелиальной кДНК для тирозинкиназных рецепторов у людей степень идентичности последовательности VEGFR-2 составляет 85% с ранее выявленной киназой печени плода мыши 1 (Flk-1). VEGFR-2 обычно экспрессируется в эндотелиальных и гемопоэтических клетках-предшественниках, а также в эндотелиальных клетках, растущих гемопоэтических стволовых клетках и строме пуповины. Однако во взрослой сосудистой системе в состоянии покоя наблюдается регуляция в сторону уменьшения VEGFR-2 мРНК.
[0049] Внеклеточный домен VEGFR-2 содержит 18 потенциальных N-связанных гликозилированных участков. VEGFR-2 изначально синтезировали как белок с массой 150 кДа и быстро гликозилировали до формы промежуточного соединения с массой 200 кДа, а затем дополнительно гликозилировали при более медленной скорости до зрелого белка с массой 230 кДа, экспрессированного на поверхности клеток.
[0050] Аминокислотная последовательность VEGFR-2 человека кодирующей последовательности кДНК, клонированной в плазмиду pVAX10.VR2-1, представлена на Фиг. 1.
[0051] В конкретных вариантах осуществления аттенуированный мутантный штамм сальмонеллы тифи по настоящему изобретению предназначен для применения в качестве лекарственного средства.
[0052] В конкретных вариантах осуществления аттенуированный мутантный штамм сальмонеллы тифи по настоящему изобретению предназначен для применения в качестве вакцины.
[0053] В контексте настоящего изобретения термин «вакцина» относится к средству, которое способно вызывать иммунный ответ у индивидуума при введении. Вакцина может предпочтительно предотвращать, улучшать состояние или лечить заболевание. Вакцина в соответствии с настоящим изобретением содержит аттенуированный мутантный штамм сальмонеллы тифи, предпочтительно сальмонеллы тифи Ty21a. Вакцина в соответствии с настоящим изобретением дополнительно содержит, по меньшей мере, одну копию рекомбинантной молекулы ДНК, содержащую экспрессирующую кассету, предпочтительно эукариотическую экспрессирующую кассету, кодирующую рецепторный белок VEGF, предпочтительно выбранный из VEGFR-2 человека или белка, степень идентичности последовательности которых составляет, по меньшей мере, приблизительно 80%.
[0054] Живой аттенуированный мутантный штамм сальмонеллы по настоящему изобретению, содержащий рекомбинантную молекулу ДНК, кодирующую рецепторный белок VEGF, можно использовать в качестве носителя для пероральной доставки этой рекомбинантной молекулы ДНК. Такой вектор доставки, содержащий молекулу ДНК, кодирующую гетерологичный антиген, такой как рецепторный белок VEGF, называется ДНК-вакциной.
[0055] Генетическая иммунизация может быть более предпочтительной относительно общепринятой вакцинации. Целевую ДНК можно детектировать в течение значительного периода времени, таким образом, она выполняет функцию депо антигена. Мотивы в последовательности некоторых плазмид, таких как островки GpC, являются иммунностимулирующими и могут функционировать как адъюванты под действием иммуностимуляции посредством полиполисахаридов и других бактериальных компонентов. Живые бактериальные векторы производят свои собственные иммуномодулирующие факторы, такие как липополисахариды (LPS) in situ, которые могут обеспечивать преимущество над другими формами введения, такими как микрокапсулирование. Кроме того, как оказывается, использование естественного пути введения обеспечивает преимущество, так как многие бактерии, такие как сальмонелла, выходят из просвета кишечника через M-клетки пейеровых бляшек и в конечном итоге мигрируют в лимфоузлы и селезенку, таким образом, обеспечивая направленность вакцин на индуктивные участки иммунной системы.
[0056] Кроме того, аттенуированные производные сальмонеллы энтерика представляют интерес в качестве носителей для доставки гетерологичных антигенов иммунной системы млекопитающего, так как штаммы сальмонеллы энтерика S потенциально можно доставлять с помощью мукозальных способов иммунизации, т.е. перорально или назально, что обеспечивает преимущества, заключающиеся в простоте и безопасности, по сравнению с парентеральным введением. Кроме того, штаммы сальмонеллы вызывают сильный гуморальный и клеточный иммунный ответ на уровне как системного, так и мукозального компартментов.
[0057] В конкретных вариантах осуществления аттенуированным мутантным штаммом сальмонеллы тифи является сальмонелла тифи Ty21a. В настоящее время доказано, что вакцинный штамм Ty21a имеет отличный профиль безопасности. При выходе из просвета кишечника через M-клетки бактерии подхватывают фагоцитарные клетки, такие как макрофаги и дендритные клетки. С помощью патогена происходит активация этих клеток, и начинается их дифференцировка, и, возможно, миграция в лимфоузлы и селезенку. В связи с аттенуирующими мутациями бактерии штамма сальмонеллы тифи Ty21a не способны продолжать существовать в этих фагоцитарных клетках и погибают в этот момент. Происходит высвобождение рекомбинантных молекул ДНК, и затем их перенос в цитозоль фагоцитарных иммунных клеток, или через определенную систему транспортировки, или посредством эндосомальной системы. В конечном итоге, рекомбинантные молекулы ДНК поступают в ядро, где они транскрибируются, приводя в результате к экспрессии рецептора VEGF в цитозоле фагоцитарных клеток. Определенные цитотоксические T-клетки против рецепторного белка VEGFR вызывают активированные антигенпрезентирующие клетки (APC).
[0058] В настоящее время не представлено данных, указывающих на способность сальмонеллы тифи Ty21a поступать в системный кровоток. Живой аттенуированный вакцинный штамм сальмонеллы тифи Ty21a, таким образом, обеспечивает конкретную направленность иммунной системы, в то же время, показывая отличный профиль безопасности.
[0059] В конкретных вариантах осуществления рецепторный белок VEGF выбран из группы, состоящей из VEGFR-2 человека и его гомолога, степень гомологии которых составляет, по меньшей мере, приблизительно 80%.
[0060] В этом контексте термин «приблизительно» означает в пределах от 80% до 120%, альтернативно в пределах от 90% до 110%, включая предел от 95% до 105% указанного значения или диапазона.
[0061] В контексте настоящего изобретения термин «белок, степень идентичности последовательности которого с VEGFR-2 человека составляет, по меньшей мере, приблизительно 80%» относится к белку, у которого отличается аминокислотная последовательность и/или последовательность нуклеиновой кислоты, кодирующая аминокислотную последовательность VEGFR-2 человека. Белок может быть природного происхождения, например, гомологом различных видов VEGFR-2, или сконструированным белком, например, сконструированным производным VEGFR-2. Известно, что использование кодонов отличается применительно к различным видам. Таким образом, при экспрессировании гетерологичного белка в клетке-мишени может быть необходимым, или, по меньшей мере, может быть целесообразным, адаптация последовательности нуклеиновой кислоты к использованию кодона клетки-мишени. Способы определения и конструирования производных указанного белка хорошо известны любому специалисту в данной области.
[0062] Белок, степень идентичности последовательности которого с VEGFR-2 человека составляет, по меньшей мере, приблизительно 80%, может содержать одну или несколько мутаций, содержащих добавление, удаление и/или замещение одной или нескольких аминокислот. Согласно идее по настоящему изобретению, указанные удаленные, добавленные и/или замещенные аминокислоты могут быть последовательными аминокислотами или могут чередоваться на протяжении аминокислотной последовательности белка, степень идентичности последовательности которого с VEGFR-2 человека составляет, по меньшей мере, приблизительно 80%. Согласно идее по настоящему изобретению, ряд аминокислот можно добавлять, удалять и/или замещать, при условии, что степень идентичности последовательности которого с VEGFR-2 человека составляет, по меньшей мере, приблизительно 80%. В конкретных вариантах осуществления степень идентичности последовательности с VEGFR-2 человека составляет, по меньшей мере, приблизительно 80%, по меньшей мере, приблизительно 85%, по меньшей мере, приблизительно 90%, или наиболее конкретно, по меньшей мере, приблизительно 95%. Способы и алгоритмы определения степени идентичности последовательности, включая сравнение родительского белка и его производных с удалениями, добавлениями и/или замещениями относительно родительской последовательности, хорошо известны среднему специалисту в данной области. На уровне ДНК последовательности нуклеиновой кислоты, кодирующей белок, степень идентичности последовательности с VEGFR-2 человека которых составляет, по меньшей мере, приблизительно 80%, могут отличаться в большей степени ввиду вырожденности генетического кода.
[0063] В конкретных вариантах осуществления рецепторным белком VEGF является VEGFR-2 человека с аминокислотной последовательностью, как представлено в SEQ ID NO:1.
[0064] В другом аспекте настоящее изобретение относится к ДНК-вакцине, содержащей аттенуированный мутантный штамм сальмонеллы тифи по настоящему изобретению.
[0065] В конкретных вариантах осуществления аттенуированным мутантным штаммом сальмонеллы тифи является сальмонелла тифи Ty21a. Аттенуированный штамм сальмонеллы тифи Ty21a является активным компонентом Typhoral L®, также известным как Vivotif® (производства Berna Biotech Ltd., a Crucell Company, Швейцария). В настоящее время это единственная лицензированная живая пероральная вакцина против тифоидной лихорадки. Эта вакцина прошла всесторонние испытания и доказана ее безопасность относительно токсичности для пациента, а также передачи третьим лицам (Wahdan et al., J. Infectious diseases 1982, 145:292-295). Вакцина лицензирована в более чем 40 странах. Номером регистрационного свидетельства Typhoral L® является PL 15747/0001 от 16 декабря 1996 года. Одна доза вакцины содержит, по меньшей мере, 2×109 колониеобразующих единиц жизнеспособной сальмонеллы тифи Ty21a и, по меньшей мере, 5×109 клеток нежизнеспособной сальмонеллы тифи Ty21a.
[0066] Одним из биохимических свойств бактериального штамма сальмонеллы тифи Ty21a является его неспособность метаболизировать галактозу. Аттенуированный мутантный штамм также не способен восстанавливать сульфат до сульфита, что отличает его от штамма сальмонеллы Ty2 дикого типа. В отношении его серологических характеристик, штамм сальмонеллы тифи Ty21a содержит антиген О9, который является полисахаридом наружной мембраны бактерий, и в нем отсутствует антиген O5, который, в свою очередь, является компонентом, характерным для сальмонеллы тифимуриум. Эта серологическая характеристика поддерживает основание для включения соответствующего теста в ряде тестов на идентичность для разрешения на выпуск серии.
[0067] В конкретных вариантах осуществления экспрессирующей кассетой является эукариотическая экспрессирующая кассета. В контексте настоящего изобретения термин «эукариотическая экспрессирующая кассета» относится к экспрессирующей кассете, обеспечивающей экспрессию открытой рамки считывания в эукариотической клетке. Показано, что количество гетерологичного антигена, необходимого для вызова соответствующего иммунного ответа, может быть токсичным для бактерии и привести к гибели клеток, сверхаттенуации или к потере экспрессии гетерологичного антигена. Использование эукариотической экспрессирующей кассеты, которая не экспрессируется в бактериальном векторе, а только в клетке-мишени, может устранить эту проблему токсичности, и экспрессированный белок может показать эукариотический профиль гликозилирования.
[0068] Эукариотическая экспрессирующая кассета содержит регуляторные последовательности, способные контролировать экспрессию открытой рамки считывания в эукариотической клетке, предпочтительно промоторе и сигнале полиаденилирования. Промоторы и сигналы полиаденилирования, включенные в рекомбинантные молекулы ДНК, имеющие в составе аттенуированный мутантный штамм сальмонеллы по настоящему изобретению, предпочтительно отобраны в качестве функциональных в рамках клеток индивидуума, которому необходима иммунизация. Примеры подходящих промоторов, в особенности для получения ДНК-вакцины для людей, в качестве неограничивающих примеров включают промоторы из цитомегаловируса (ЦМВ), такие как сильный предранний промотор ЦМВ, вируса обезьян 40 (SV40), вируса опухоли молочной железы мышей (MMTV), вируса иммунодефицита человека (ВИЧ), такие как промотор длинного концевого повтора (ДКП) HIF, вируса Молони, вируса Эпштейна-Барра (ВЭБ), и из вируса саркомы Рауса, а также промоторы из генов человека, таких как актин человека, миозин человека, гемоглобин человека, креатин мышцы человека и металлотионеин человека. В конкретном варианте осуществления эукариотическая экспрессирующая кассета содержит промотор ЦМВ. В контексте настоящего изобретения термин «промотор ЦМВ» относится к сильному предраннему промотору ЦМВ.
[0069] Примеры подходящих сигналов полиаденилирования, в особенности для получения ДНК-вакцины для людей, в качестве неограничивающих примеров включают участок полиаденилирования гормона роста быка (BGH), сигналы полиаденилирования SV40 и сигналы полиаденилирования ДКП. В конкретном варианте осуществления эукариотическая экспрессирующая кассета, включенная в рекомбинантные молекулы ДНК, имеющие в составе аттенуированный мутантный штамм сальмонеллы по настоящему изобретению, содержит участок полиаденилирования BGH.
[0070] В дополнение к регуляторным элементам, необходимым для экспрессии рецепторного белка VEGF, таким как промотор и сигнал полиаденилирования, другие элементы также могут быть включены в рекомбинантную молекулу ДНК. Такие дополнительные элементы включают энхансеры. Энхансером может быть, например, энхансер актина человека, миозина человека, гемоглобина человека, креатин мышцы человека и вирусные энхансеры, такие как из ЦМВ, ВСР и ВЭБ.
[0071] Регуляторные последовательности и кодоны, как правило, зависят от вида, поэтому с целью максимального получения белка регуляторные последовательности и кодоны предпочтительно отбирают для эффективности у видов, которым необходима иммунизация. Специалист в данной области может получить рекомбинантные молекулы ДНК, которые являются функциональными у указанного вида индивидуума.
[0072] В конкретных вариантах осуществления ДНК-вакцина по настоящему изобретению предназначена для применения в иммунотерапии злокачественных опухолей.
[0073] В конкретных вариантах осуществления ДНК-вакцина содержит аттенуированный штамм сальмонеллы тифи Ty21a, трансформированный плазмидой, которая содержит ДНК, кодирующую белок VEGFR-2 с SEQ ID NO:1.
[0074] В конкретных вариантах осуществления ДНК-вакцина предназначена для применения в антиангиогенной иммунотерапии злокачественных опухолей.
[0075] В конкретных вариантах осуществления рекомбинантная молекула ДНК содержит ген, устойчивый к антибиотику канамицину, pMB1 ori и эукариотическую экспрессирующую кассету, кодирующую VEGFR-2 человека или белок, степень гомологии последовательности которых составляет, по меньшей мере, 80%, под контролем промотора ЦМВ. В конкретных вариантах осуществления VEGFR-2 человека имеет последовательность нуклеиновой кислоты, как представлено в SEQ ID NO:2.
[0076] Предранний эукариотический промотор ЦМВ обеспечивает эффективную трансляцию белка VEGFR-2 в клетку-хозяина, и прокариотическая точка начала репликации (ori) содействует размножению в пределах бактериального хозяина.
[0077] В конкретных вариантах осуществления рекомбинантную молекулу ДНК получают из коммерчески доступной pVAX1™ плазмиды экспрессии (Invitrogen, Сан-Диего, штат Калифорния). Этот экспрессирующий вектор модифицировали посредством замены точки начала репликации многокопийной pUC на точку начала репликации pBR322 малокопийной pMB1. Малокопийная модификация была произведена с целью снижения метаболической нагрузки и обеспечения большей стабильности конструкции. Детальное изображение конструкции плазмиды pVAX10.VR2-1 представлено на Фиг. 2. Образованный остов экспрессирующего вектора обозначен как pVAX10. В результате вставки последовательности нуклеиновой кислоты VEGFR-2 человека, как представлено в SEQ ID NO:2, в этот остов экспрессирующего вектора получили плазмиду экспрессии pVAX10.VR2-1.
[0078] Схематическое изображение плазмиды экспрессии pVAX10.VR2-1 представлено на Фиг. 2. В конкретных вариантах осуществления плазмидой является pVAX10.VR2-1 размером 7580 п.н., как изображено на Фиг. 2, и имеет последовательность, как представлено в SEQ ID NO:3, и ДНК-вакцина обозначена как VXM01. VXM01 является пероральной вакциной против злокачественной опухоли, состоящей из аттенуированного штамма сальмонеллы энтерика серовар тифи Ty21a, несущий, по меньшей мере, одну копию плазмиды ДНК, pVAX10.VR2-1, кодирующей эукариотическую экспрессирующую кассету рецептора-2 фактора роста эндотелия сосудов человека (VEGFR-2).
[0079] В конкретных вариантах осуществления злокачественной опухолью является рак поджелудочной железы.
[0080] В конкретных вариантах осуществления указанный рак поджелудочной железы находится на стадии IV или является местнораспространенным раком поджелудочной железы.
[0081] В конкретных вариантах осуществления злокачественная опухоль включает метастазы.
[0082] В конкретных вариантах иммунотерапия осуществления злокачественных опухолей дополнительно содержит введение одного или нескольких дополнительного(ых) аттенуированного(ых) мутантного(ых) штамма(ов) сальмонеллы, содержащего(их), по меньшей мере, одну копию рекомбинантной молекулы ДНК, содержащей экспрессирующую кассету, кодирующую опухолевый антиген и/или антиген стромы опухоли. В конкретных вариантах осуществления указанный(ые) один или несколько дополнительный(ых) мутантный(ых) штамм(ов) сальмонеллы является/являются сальмонеллой тифи Ty21a, содержащей эукариотическую экспрессирующую кассету. В конкретных вариантах осуществления указанный(ые) один или несколько дополнительный(ых) мутантный(ых) штамм(ов) сальмонеллы содержит(ат) аттенуированный мутантный штамм сальмонеллы, кодирующий WT1 человека.
[0083] Комбинация аттенуированного мутантного штамма сальмонеллы по настоящему изобретению со вторым аттенуированным мутантным штаммом, содержащим молекулу ДНК, кодирующую второй антиген стромы опухоли или опухолевый антиген, может оказать синергический противоопухолевый эффект. В частности, одномоментная направленность на опухоль и строму опухоли может свести к минимуму риск ускользания опухоли. Комбинация иммунотерапии на основе VEGFR-2 с иммунотерапией злокачественных опухолей на основе WT1 может оказаться особенно эффективной в связи с одновременной атакой на сверхэкспрессирующие клетки человека WT1 и опухолевую сосудистую систему.
[0084] В конкретных вариантах осуществления аттенуированный мутантный штамм сальмонеллы вводят совместно с указанным(и) одним или несколькими дополнительным(и) аттенуированным(и) мутантным(и) штаммом(ами) сальмонеллы.
[0085] В контексте настоящего изобретения термин «совместное введение» или «совместно вводить» означает введение двух различных аттенуированных мутантных штаммов сальмонеллы в пределах трех последующих суток, более конкретно - в пределах двух последующих суток, более конкретно - в те же сутки, более конкретно - в пределах 12 часов. Наиболее конкретно - в контексте настоящего изобретения, термин «совместное введение» относится к одномоментному введению двух различных аттенуированных мутантных штаммов сальмонеллы.
[0086] В конкретных вариантах осуществления лечение проводят в сопровождении химиотерапии и/или лучевой терапии, и/или биологической терапии злокачественных опухолей. Для лечения злокачественной опухоли может потребоваться полное уничтожение злокачественных стволовых клеток. С целью достижения максимальной эффективности может оказать благоприятное действие комбинация различных терапевтических подходов.
[0087] В контексте настоящего изобретения термин «биологическая терапия злокачественных опухолей» или «иммунотерапия злокачественных опухолей» относится к стимуляции иммунной системы пациента для атаки злокачественных опухолевых клеток или стромы опухоли. Подходы (методика) биологической терапии злокачественных опухолей включают доставку опухолевых антигенов, доставку терапевтических антител в качестве лекарственных средств, введение иммуностимулирующих цитокинов и введение иммунных клеток.
[0088] Химиотерапевтическими средствами, которые можно использовать в комбинации с аттенуированным мутантным штаммом сальмонеллы по настоящему изобретению, могут являться, например: амифостин (этиол), кабазитаксел, цисплатин, дакарбазин (DTIC), дактиномицин, доцетаксел, мехлоретамин, стрептозоцин, циклофосфамид, кармустин (BCNU), ломустин (CCNU), доксорубицин (адриамицин), инкапсулированный в липосомы доксорубицин (доксил), фолиниевая кислота, гемцитабин (гемзар), даунорубицин, даунорубицин липо (дауноксом), прокарбазин, кетоконазол, митомицин, цитарабин, этопозид, метотрексат, 5-фторурацил (5-FU), винбластин, винкристин, блеомицин, паклитаксел (таксол), доцетаксел (таксотер), альдеслейкин, аспарагиназа, бусульфан, карбоплатин, кладрибин, камптотецин, CPT-11, 10-гидрокси-7-этил-камптотецин (SN38), дакарбазин, флоксуридин, флударабин, гидроксимочевина, ифосфамид, идарубицин, месна, интерферон альфа, интерферон бета, иринотекан, митоксантрон, топотекан, лейпролид, мегестрол, мелфалан, меркаптопурин, оксалиплатин, пликамицин, митотан, пэгаспаргаза, пентостатин, пипоброман, пликамицин, стрептозоцин, тамоксифен, тенипозид, тестолактон, тиогуанин, тиотепа, урамустин, винорелбин, хлорамбуцил и их сочетания.
[0089] Наиболее предпочтительными химиотерапевтическими средствами по изобретению в комбинации с VXM01 являются кабазитаксел, карбоплатин, оксалиплатин, цисплатин, циклофосфамид, доцетаксел, гемцитабин, доксорубицин, паклитаксел (таксол), иринотекан, винкристин, винбластин, винорелбин, фолиниевая кислота, 5-фторурацил и блеомицин, в особенности гемцитабин.
[0090] В конкретных вариантах осуществления химиотерапевтическим средством является гемцитабин.
[0091] Включение лечения с помощью антибиотиков или противовоспалительных средств также может оказывать благоприятное действие в зависимости от возникновения возможных побочных эффектов.
[0092] В случае возникновения нежелательных явлений, схожих с реакциями гиперчувствительности, опосредованными гистамином, лейкотриенами или цитокинами, пригодными для применения являются варианты лечения лихорадки, анафилаксии, нестабильности артериального давления, бронхоспазма и диареи. Варианты лечения в случае нежелательной аутоагрессии Т-клеток получают из стандартных схем лечения при остром и хронической болезни «трансплантат против хозяина», применяемых после трансплантации стволовых клеток. В качестве вариантов лечения предлагают циклоспорин и глюкокортикоиды.
[0093] При маловероятном случае системной инфекции типа сальмонеллы тифи Ty21a рекомендуется надлежащая антибиотикотерапия, например, с помощью фторхинолонов, включая ципрофлоксацин или офлоксацин. Бактериальные инфекции желудочно-кишечного тракта подлежат лечению соответствующими средствами, такими как рифаксимин.
[0094] В конкретных вариантах осуществления аттенуированный мутантный штамм сальмонеллы вводят в ходе цикла лечения химиотерапией или лучевой терапией или в ходе биологической терапии злокачественных опухолей. В конкретных вариантах осуществления иммунотерапевтическое лечение с помощью вакцины проводят в ходе цикла лечения химиотерапией.
[0095] В конкретных вариантах осуществления аттенуированный мутантный штамм сальмонеллы вводят перед циклом лечения химиотерапией или лучевой терапией или перед биологической терапией злокачественных опухолей. Данный подход может иметь преимущество, заключающееся в том, что химиотерапию или лучевую терапию можно проводить в условиях повышенного иммунитета к злокачественной опухоли.
[0096] В конкретных вариантах осуществления аттенуированный мутантный штамм сальмонеллы вводят после цикла лечения химиотерапией или лучевой терапией или после биологической терапии злокачественных опухолей.
[0097] В конкретных вариантах осуществления вакцину вводят перорально. Пероральное введение является более простым, более безопасным и более удобным, чем парентеральное введение. Неблагоприятные воздействия парентерального, подкожного или интрадермального введения можно избежать посредством перорального введения ДНК-вакцины по настоящему изобретению. Аттенуированный мутантный штамм сальмонеллы по настоящему изобретению, однако, можно также вводить любым другим подходящим способом. Предпочтительно, терапевтически эффективную дозу вводят индивидууму, и эта доза зависит от конкретного применения, типа злокачественного новообразования, массы, возраста, пола и состояния здоровья индивидуума, способа введения и состава и т.д. Введение может быть однократным или многократным по необходимости.
[0098] Аттенуированный мутантный штамм сальмонеллы по настоящему изобретению может быть представлен в форме раствора, суспензии, лиофилизата или в любой другой подходящей форме. Он может быть представлен в комбинации с фармацевтически приемлемыми носителями, разбавителями и/или эксципиентами. Можно также включать средства для корректировки значения pH, буферы, средства для корректировки токсичности и т.п. В контексте настоящего изобретения термин «фармацевтически приемлемый» относится к молекулярным структурам и к другим ингредиентам фармацевтических композиций, которые являются физиологически переносимыми и которые, как правило, не вызывают нежелательных реакций при введении млекопитающему (например, человеку). Термин «фармацевтически приемлемый» может также означать одобренный федеральным или государственным регулирующим органом или числящийся в перечне Фармакопеи США или другой общепризнанной фармакопеи для применения на млекопитающих и, более конкретно, на людях.
[0099] Удивительным образом, вакцина по настоящему изобретению является эффективной в относительно низких дозах. В конкретных вариантах осуществления однократная доза вакцины составляет приблизительно 1×105, приблизительно 1×106, приблизительно 1×107, приблизительно 1×108, приблизительно 1×109, приблизительно 1×1010 или приблизительно 1×1011 колониеобразующих единиц(КОЕ). Введение низких доз этой живой бактериальной вакцины сводит к минимуму риск экскреции и, таким образом, к передаче третьим лицам.
[00100] В этом контексте термин «приблизительно» означает в пределах 3-кратного увеличения, альтернативно в пределах 2-кратного увеличения, включая увеличение в 1,5 раза указанного значения или диапазона.
[00101] В конкретных вариантах осуществления однократная доза вакцины составляет менее чем приблизительно 1×109 КОЕ. В конкретных вариантах осуществления однократная доза вакцины составляет от 1×108 до 1×109 КОЕ.
[00102] В конкретных вариантах осуществления однократная доза вакцины составляет менее чем приблизительно 1×108 КОЕ. В конкретных вариантах осуществления однократная доза вакцины составляет от 1×105 до 1×108 КОЕ, более конкретно - однократная доза вакцины составляет от 1×106 до 1×107 КОЕ.
[00103] В конкретных вариантах осуществления однократная доза содержит приблизительно от 105 до приблизительно 1011, в частности, приблизительно от 106 до приблизительно 1010, более конкретно приблизительно от 106 до приблизительно 109, более конкретно приблизительно от 106 до приблизительно 108, наиболее конкретно приблизительно от 106 до приблизительно 107 колониеобразующих единиц (КОЕ).
[00104] В конкретных вариантах осуществления аттенуированный мутантный штамм сальмонеллы предназначен для применения в индивидуальной иммунотерапии злокачественных опухолей. Индивидуальная иммунотерапия злокачественных опухолей может содержать стадию оценки профиля экспрессии антиген стромы опухоли и/или профиля экспрессии опухолевого антигена пациента. Индивидуальная иммунотерапия злокачественных опухолей может также содержать стадию оценки предиммунных ответов на антиген стромы опухоли или опухолевый антиген, предпочтительно предиммунного ответа на VEGFR-2. В соответствии с этим, было доказано, что предсуществующие иммунные ответы на VEGFR-2 сильно коррелируют с положительной клинической эффективностью VXM01, в частности, с уменьшением перфузии опухоли.
[00105] VXM01 можно использовать - или самостоятельно, или в комбинации с другими вакцинами против злокачественной опухоли на основе сальмонеллы тифи Ty21a, содержащими эукариотические экспрессирующие системы - для лечения различных типов злокачественных опухолей. В конкретных вариантах осуществления VXM01 можно использовать индивидуальное персонифицированное лечение злокачественных опухолей. С этой целью профиль экспрессии стромального и/или опухолевого антигена пациента можно оценивать на первой стадии, например, посредством сопровождающей диагностики, направленной на конкретный стромальный и/или опухолевый антигенный профиль пациента. Альтернативно, можно оценивать предсуществующие иммунные ответы на стромальные и/или опухолевые антигены. В зависимости от профиля экспрессии стромального и/или опухолевого антигена пациента, VMX01 можно вводить или в отдельности, или в комбинации с одной или несколькими подходящей(ими) дополнительной(ыми) вакциной(ами) против злокачественной опухоли на основе сальмонеллы тифи Ty21a, содержащей(ими) эукариотические экспрессирующие системы. Комбинации VXM01 с одной или несколькими дополнительной(ыми) вакциной(ами) против злокачественной опухоли на основе сальмонеллы тифи Ty21a можно, однако, также вводить в качестве фиксированных комбинаций. Эти смеси, сочетающие две или более вакцин против злокачественной опухоли на основе сальмонеллы тифи Ty21a, можно составлять из отдельных имеющихся в готовом виде продуктов. Комбинации или фиксированные, или индивидуальные, могут содержать VXM01 в качестве антиангиогенной базовой терапии.
[00106] В другом аспекте настоящее изобретение относится к ДНК-вакцине VXM01, содержащей аттенуированный штамм сальмонеллы тифи Ty21a, трансформированный плазмидой, которая содержит ДНК, кодирующую белок VEGFR-2 с SEQ ID NO:1, где плазмида представляет собой плазмиду ДНК размером 7580 п.н. и содержит кДНК VEGFR-2 под контролем промотора ЦМВ, канамицин-устойчивого гена и pMB1 ori, и обозначена как pVAX10.VR2-1.
КРАТКОЕ ОПИСАНИЕ ФИГУР И ТАБЛИЦ
Фиг. 1: Аминокислотная последовательность кДНК VEGFR-2, клонированная в плазмиде pVAX10.VR2-1
Фиг. 2: Карты плазмиды pVAX10.VR2-1
Фиг. 3: Схема с увеличением дозы вакцины VXM01
Фиг. 4: Общая схема исследования
Фиг. 5: VMX01-специфическая T-клеточная иммунная реакция
Фиг. 6: Воздействие VXM01 на перфузию опухоли
Фиг. 7: Воздействие VXM01 на уровень VEGF A в сыворотке
Фиг. 8: Воздействие VXM01 на уровень коллагена IV в сыворотке
Фиг. 9: Воздействие VXM01 на артериальное давление
Фиг. 10: VXM01-индуцированный иммунитет против носителя
Фиг. 11: Каскадный анализ экскреции VXM01
Фиг. 12: Экскреция VXM01
Таблица 1: Критерии отбора пациентов
Таблица 2: VMX01-специфическая T-клеточная иммунная реакция
ПРИМЕРЫ
Пример 1. Получение штамма сальмонеллы тифи Ty21a и получение плазмиды
[00107] Первая стадия получения посевной серии для исследования (RSL) состояла из отделения аттенуированного штамма сальмонеллы тифи Ty21a с последующей трансформацией аттенуированных бактерий с плазмидой ДНК (pVAX10.VR2-1).
[00108] Жидкую среду для культивирования инокулировали с помощью изолята сальмонеллы тифи Ty21a, и затем жидкую культуру наносили на агарную среду с целью отделения единичных бактериальных колоний. Единичные колонии отделяли и выращивали в жидкой среде для культивирования. Затем две культуры, а именно VAX.Ty21-1 и VAX.Ty21-2, объединяли с глицерином с разделением на аликвоты (1 мл) и хранили при -75°C ± 5°C для дальнейшего использования. Идентичность каждой из двух культур была дополнительно подтверждена.
[00109] Принцип синтеза плазмиды был основан на синтезе двухцепочечного гена in vitro со следующими стадиями:
- Всю последовательность плазмиды pVAX10-VR2,1 размером 7,58 т.п.н. подразделяли (посредством анализа программного обеспечения) на 5 секций по ~1,5 т.п.н. Каждую секцию подразделяли на олигонуклеотиды размером 40-50 п.н., в каждой из которых были перекрывающие области между олигонуклеотидами обеих цепей
- Затем синтезированные in vitro олигонуклеотиды фосфорилировали посредством инкубации с T4 полинуклеотидом киназы
- После процесса отжига перекрывающих олигонуклеотидов при подходящих условиях фермент Taq ДНК-лигазы соединяли с выстроенными олигонуклеотидами
- По завершении стадии лигирования проводили ПЦР с использованием праймеров, отожженных на внешних положениях, для увеличения выхода лигированных фрагментов плазмиды (~1,5 т.п.н.)
- Препаративный электрофорез в агарозном геле проводили для отделения продуктов ПЦР
- Отделенные продукты ПЦР клонировали в векторы TOPO (Invitrogen K#4575-40) и трансформировали в клетки E. coli TOP10 для воспроизводства
- После отделения плазмиды TOPO проводили проверку ограничения и последовательности
- Отделенные выстроенные фрагменты собирали с помощью перекрывающейся ПЦР. После этого процесса осуществляли линейный сбор плазмиды pVAX10.VR2-1
- После фрагментов рестрикции XhoI (единичный участок рестрикции, присутствующий в плазмиде pVAX10.VR2-1, см. Фиг. 2) и ковалентного связывания посредством лигазы T4 E. coli трансформировали с помощью кольцевой плазмиды для воспроизводства
- После окончательной проверки последовательности плазмиды плазмиду pVAX10.VR2-1 трансформировали в бактериальный штамм сальмонеллы тифи Ty21a.
[00110] Таким образом, плазмиду pVAX10.VR2-1 успешно синтезировали (без отклонения от эталонной последовательности). Затем эту плазмиду использовали для трансформации бактериального штамма сальмонеллы тифи Ty21a.
Пример 2. VXM01 - I-фазное клиническое испытание; описание исследования
[00111] В ходе этого I-фазного испытания проводили проверку безопасности, переносимости и иммунологического и клинического ответа на VXM01. Рандомизированное, плацебо-контролируемое исследование с увеличением дозы двойным слепым методом включало 45 пациентов с местнораспространенным или находящимся в IV стадии раком поджелудочной железы. Пациенты получали четыре дозы VXM01 или плацебо в дополнение к гемцитабину в качестве стандарта лечения. В исследовании оценивали дозы VXM01 от 106 КОЕ до 1010 КОЕ. В принятии решений по увеличению доз участвовал независимый комитет по мониторингу данных (DSMB). В дополнение к безопасности в качестве основного конечного показателя, оценивали показатели VXM01-специфического иммунного ответа, а также клинического ответа.
Оценка доклинической эффективности:
[00112] Эффективность и безопасность этого подхода у животных многократно подтверждена авторами изобретения. Дополнительные эксперименты, проводимые авторами изобретения, доказали активность этой вакцины на двух различных моделях рака поджелудочной железы.
[00113] VXM01, вакцина, используемая в этом испытании, является гуманизированной версией вакцины против VEGFR-2, ранее протестированной на мышах. Она кодирует полноразмерный VEGFR-2 человека и использует залицензированный штамм сальмонеллы тифи Ty21a вместо сальмонеллы тифимуриум в качестве носителя. Предполагается, что вакцина приводит к экспрессии белка VEGFR-2 в моноцитах и дендритных клетках после поступления VXM01 в пейеровые бляшки с помощью кишечных M-клеток, и интернализации с помощью антигенпрезентирующих клеток с последующей трансляцией кодированной ДНК.
Доклиническая оценка безопасности:
[00114] Доклиническое исследование токсичности на мышах включало, но не ограничивалось им, исследование токсичности однократной дозы на мышах, проведенное с помощью вакцины VXM01 человека. Ввиду специфичности VXM01 для хозяина человека исследование вакцины человека на мышах было направлено на выявление возможных эффектов примесей, связанных с процессом, и соответствующих признаков и симптомов возможной пригодности для нарушений сердечно-сосудистой, дыхательной или центральной нервной системы. С целью определения профиля токсичности T-клеточной иммунной реакции против VEGFR-2 исследование токсичности многократных доз проводили с использованием аналога конструкции VXM01 мыши, который индуцировал дозозависимую T-клеточную иммунную реакцию у мышей. Согласно предыдущим наблюдениям авторов изобретения, не наблюдалось случаев смерти, связанных с проводимым лечением, и токсикологически важных клинических симптомов на всем протяжении этих исследований, которые проводили в соответствии с надлежащей лабораторной практикой.
[00115] Вектором сальмонеллы тифи Ty21a, используемым в настоящем изобретении, является живой, аттенуированный бактериальный носитель, обеспечивающий пероральную доставку вакцины VXM01. Он сам по себе является одобренной вакциной против тифоидной лихорадки (Vivotif®, ранее называвшейся Crucell, Berna Biotech Ltd., Швейцария), прошедшей всесторонние испытания и продемонстрировавшей свою безопасность в отношении токсичности для пациента, а также передачи третьим лицам (Wahdan et al., J. Infectious diseases 1982, 145:292-295). VXM01 классифицирована как лекарственный препарат с переносом генов, и на нее распространяются действие соответствующих руководящих принципов и норм.
Описание и задачи исследования:
[00116] Проведенное исследование представляло собой одноцентровое, плацебо-контролируемое исследование с увеличением дозы двойным слепым методом экспериментальной вакцины VXM01 на пациентах с неоперабельным или находящимся на IV стадии раком поджелудочной железы. Вакцину применяли в качестве дополнения к стандартному лечению с помощью гемцитабина.
[00117] Задачи заключались в исследовании безопасности и переносимости иммунологического и клинического ответов на исследуемую вакцину VXM01 против VEGFR-2, а также в определении максимально переносимой дозы (МПД) VXM01. МПД определена как самая высокая доза, при которой менее чем два из шести пациентов, проходящих лечение с помощью VXM01, испытывают дозолимитирующую токсичность (ДЛТ).
[00118] Ниже представлены основные конечные показатели безопасности и переносимости: количество случаев ДЛТ, определенное как любое нежелательное явление (НЯ), связанное с исследуемым лекарственным средством 4 класса или выше, или 3 класса или выше для желудочно-кишечного свища, диареи, гастроинтестинальной перфорации, полиорганной недостаточности, анафилаксии, любого аутоиммунного расстройства, синдрома высвобождения цитокинов, кишечного кровотечения, почечной недостаточности, протеинурии, тромбоэмболических явлений, инсульта, сердечной недостаточности или васкулита, согласно критериям оценки степени тяжести наиболее частых нежелательных явлений Национального института злокачественных новообразований (CTCAE).
[00119] Вспомогательные конечные показатели, с помощью которых оценивают эффективность вызова экспериментальной вакциной специфического иммунного ответа на VEGFR-2, включали количество пациентов с иммуноположительным ответом.
[00120] Дополнительным вспомогательным конечным показателем являлся клинический ответ: оценка стадии распространения опухоли в соответствии с оценкой критериев плотных опухолей (RECIST), частота общего ответа, выживаемость без прогрессирования, общая выживаемость и изменения в перфузии опухоли. Перфузию опухоли определяли с помощью магнитно-резонансной томографии с динамическим контрастированием (DCE-MRI) на системе 1,5 Тесла (Magnetom Aera, Siemens, город Эрланген, Германия).
[00121] Производство VXM01 соответствовало Надлежащей Производственной Практике и было представлено в буферном растворе. Плацебо-контроль состоял из изотонического раствора хлорида натрия.
Отбор пациентов и план клинического исследования:
[00122] Исследование включало максимум 45 пациентов или с местнораспространенным и неоперабельным, или находящимся на IV стадии раком поджелудочной железы. Критерии отбора приведены в таблице 1.
Таблица 1
Критерии включения
1. Письменное информированное согласие с поставленной подписью и датой
2. Пациенты с местнораспространенным, неоперабельным и находящимся на IV стадии раком поджелудочной железы в соответствии с Международным союзом борьбы против рака, основанном на диагностической визуализации с использованием компьютерной томографии (КТ) или гистологических исследований
3. Мужчина или женщина в постменопаузе
4. Возраст ≥18 лет
5. Пациенты, ранее не проходившие курс химиотерапии в течение 60 суток до скринингового визита, за исключением лечения с помощью гемцитабина
6. Индекс Карновского >70
7. Продолжительность жизни >3 месяцев
8. Адекватная функция почек, печени и костного мозга
9. Абсолютное число нейтрофилов >1500/мкл
10. Гемоглобин >10 г/дл
11. Тромбоциты >75000/мкл
12. Протромбиновое время и международное нормализованное отношение (МНО) <1,5 раза выше верхней границы нормы (за исключением проведения лечения антикоагулянтом)
13. Аспартатаминотрансфераза <4 раза выше верхней границы нормы
14. Аланинаминотрансфераза <4 раза выше верхней границы нормы
15. Общий билирубин <3 раза выше верхней границы нормы
16. Клиренс креатинина согласно оценке по Кокрофту-Голту >30 мл/мин
17. Протеинурия <1 г белка в моче, собранной за 24 часа
Критерии исключения
18. Состояние после резекции поджелудочной железы (полной или частичной)
19. Резектабельное заболевание
20. Участие в испытании лекарственного средства за 60 суток до скринингового визита
21. Другое предыдущее или текущее злокачественное новообразование, за исключением базального или плоскоклеточного рака кожи, in situ рака шейки матки или любой другой злокачественной опухоли, при которой у пациента отсутствовали признаки заболевания в течение <2 лет
22. Состояние с проведенной ранее вакцинацией с помощью Ty21a после резекции поджелудочной железы (полной или частичной)
23. Резектабельное заболевание
24. Участие в испытании лекарственного средства за 60 суток до скринингового визита
25. Другое ранее перенесенное или переносимое в настоящее время злокачественное новообразование, за исключением базального или плоскоклеточного рака кожи, in situ рака шейки матки или любой другой злокачественной опухоли, при которой у пациента отсутствовали признаки заболевания в течение <2 лет
26. Проведенная ранее вакцинация с помощью Ty21a
27. Сердечно-сосудистое заболевание, определенное как: неконтролируемая гипертензия (систолическое артериальное давление >160 мм рт.ст. или диастолическое артериальное давление >100 мм рт.ст.) артериальное тромбоэмболическое осложнение за 6 месяцев до рандомизации, включая:
- инфаркт миокарда
- нестабильную стенокардию
- нарушение мозгового кровообращения
- транзиторную ишемическую атаку
28. Застойная сердечная недостаточность III - IV класса согласно классификации Нью-Йоркской кардиологической ассоциации
29. Серьезная желудочковая аритмия, требующая лечения
30. Клинически значимое заболевание периферических артерий > класса 2b согласно Фонтейну
31. Гемоптизис за 6 месяцев до рандомизации
32. Расширение вен пищевода
33. Кровотечение из верхних или нижних отделов желудочно-кишечного тракта за 6 месяцев до рандомизации
34. Серьезное травматическое повреждение за 4 недели до рандомизации
35. Незаживающая рана, перелом кости или язвы желудочно-кишечного тракта в анемнезе за три года до включения, или положительный результат гастроскопии за 3 месяца до включения
36. Желудочно-кишечный свищ
37. Тромболизисная терапия за 4 недели до рандомизации
38. Кишечная непроходимость за последние 30 суток до скринингового визита
39. Цирроз печени ≥ класса B согласно классификация по Чайлд-Пью
40. Присутствие любой острой или хронической системной инфекции
41. Лучевая терапия, проведенная за 4 недели до рандомизации
42. Серьезные хирургические вмешательства или операционная биопсия за 4 недели до рандомизации
43. Тонкоигольная аспирационная биопсия за 7 суток до рандомизации
44. Продолжительная сопутствующая терапия за 2 недели до и в течение периода исследования двойным слепым методом с помощью:
- кортикостероидов (за исключением стероидов для адреналовой недостаточности) или иммуносупрессирующих средств
- антибиотиков
- бевацизумаба
- любого ингибитора рецептора эпидермального фактора роста
45. Химиотерапия, за исключением гемцитабина, до 10 суток грамотрицательного микроба с множественной лекарственнной резистентностью
46. Беременность
47. Лактация
48. Неспособность соблюдения процедур исследования и/или процедур последующего врачебного наблюдения
49. Наличие в анамнезе другого заболевания, метаболического нарушения, данные физического обследования или клинико-лабораторных исследований, дающие обоснованные подозрения на наличие заболевания или состояния, которое является противопоказанием к применению исследуемого лекарственного препарата или которое может повлиять на интерпретацию результатов исследования или представлять высокий риск осложнений при лечении для пациента
50. Женщины репродуктивного возраста
51. Любая гиперчувствительность к лекарственному средству в анамнезе
52. Любое состояние, приводящее к неоправданному риску для пациента во время участия в исследовании согласно исследователю
[00123] Общее число пациентов, прошедших скрининг для исследования, составило 371. 326 пациентов являлись неподходящими ввиду исключенной лекарственной терапии (179), предсуществующего медицинского состояния (129) в истории болезни (анамнезе) пациента и по личным причинам (18). 45 пациентов, включенных и рандомизированных в исследовании, успешно прошли 10-суточную фазу исследования в лабораторных условиях в клиническом отделении клиники при университете города Хайдельберг (KliPS), в соответствии с протоколом исследования. Демографические показатели исходного заболевания пациентов не имели существенных различий в двух группах, но период времени с момента постановки диагноза был более продолжительным в группе VXM01 (8 по сравнению с 6 месяцами), и опухоль у пациентов в группе VXM01 находилась на более поздней стадии во время включения (CA19,9 >1000 у 40% в противоположность 20% и метастазирующая опухоль у 83% в противоположность 53%).
[00124] В это исследование были включены пациенты мужского пола и женского пола в постменопаузе. Однако не проводилось исследование различий между двумя полами. Средняя продолжительность выживания пациентов, участвовавших в этом испытании, не превышала 6 месяцев. Однако период последующего наблюдения за пациентами, прошедшими курс лечения, согласно протоколу составил до 24 месяцев. Исследуемый вид лечения применяли как терапию первой линии дополнительно к стандартному лечению. Принимая также во внимание другие факторы, в том числе комплексные первичные и вторичные фармакодинамические предклинические исследования, предполагалось, что анализ соотношения риск-ожидаемая польза приведет к благоприятному результату для отобранной популяции пациентов.
[00125] Начальная доза состояла из раствора, содержащего 106 колониеобразующих единиц (КОЕ) VXM01 или плацебо. Эта доза VXM01 была выбрана по соображениям безопасности, и предполагалось, что она ниже минимальной эффективной дозы для вызова иммунного ответа. Для сравнения, одна доза Typhoral® залицензированной вакцины против тифоидной лихорадки содержит от 2×109 до 6×109 КОЕ сальмонеллы тифи Ty21a, что в эквиваленте превышает начальную дозу VXM01 приблизительно в тысячу раз. Дозу увеличивали в 10 раз на каждой логарифмической стадии, что, как представляется, оправдано для живой бактериальной вакцины. Схема с увеличением дозы показана на Фиг. 3.
[00126] При соблюдении руководящих принципов для первого испытания на человеке пациенты из группы однократной дозы получали лечение по когортам. Первое введение VXM01 в любой дозовой группе произвели одному пациенту, сопровождаемому только одним пациентом, получавшим плацебо. Вторая когорта каждой дозовой группы состояла из двух пациентов, получавших VXM01, и одного пациента, получавшего плацебо. Такое шахматное введение с одним ведущим пациентом, т.е. только одним пациентом, получавшим VXM01 первым, способствовало снижению рисков.
[00127] Третью когорту пациентов (трех, получавших VXM01, и одного, получавшего плацебо) включили в группу с дозами 108, 109 и 1010. Такой подход сводил к минимуму воздействие доз VXM01, которые предположительно являлись субтерапевтическими. Третья когорта и первые две когорты следующей экспериментальной группы более высокого порядка получали лечение параллельно с учетом четко определенной стратегии рандомизации. Эта стратегия обеспечивала набор имеющихся пациентов и позволяла избежать ошибки отбора пациентов, получавших лечение параллельно в группе с более низкой и более высокой дозой. В группах с дозами 106 и 107 третью когорту пациентов включали, только если один пациент из трех первых пациентов, получавших VXM01 из соответствующей дозовой группы, испытывал ДЛТ, и требовалось подтверждение решения независимого комитета по мониторингу данных и безопасности субъектов исследования (DSMB).
[00128] Все пациенты прошли семисуточный курс вакцинации, состоявший из 4 доз на каждые вторые сутки в соответствии с протоколом без какого-либо уменьшения дозы. В связи с отсутствием наблюдений дозолимитирующей токсичности (ДЛТ), не была достигнута максимально переносимая доза. Хорошая переносимость VXM01 была отмечена на всех уровнях дозирования. Одинаковое распределение НЯ и СНЯ представлено в обеих группах, и в этих группах отсутствовали заметные признаки дозозависимых побочных эффектов.
[00129] Опасностью для окружающей среды, связанной с пероральной вакциной, является возможность экскреции в окружающую среду и последующая вакцинация людей за пределами целевой популяции. Место нахождения всех исследуемых пациентов ограничивалось исследовательским центром (KliPS) на период, в течение которого проводили вакцинацию, плюс дополнительные трое суток. Фекалии всех исследуемых пациентов собирали и сжигали. Образцы физиологических жидкостей и кала исследовали на выведение VXM01. Экскрецию VXM01 с калом наблюдали у двух пациентов, одного в дозовой группе 109 и одного в дозовой группе 1010. Экскреция VXM01 с калом у обоих пациентов была неустановившейся в одном случае после первого или второго введения, соответственно, и исчезла без лечения антибиотиком. В других физиологических жидкостях экскрецию не определяли.
[00130] Гигиенические меры предосторожности применяли для защиты исследовательской группы от случайного поглощения. Исследовательская группа прошла специальный инструктаж по этому аспекту исследования.
[00131] Пациентов выписывали из больницы только при отрицательных результатах тестирования на экскрецию вакцины после последнего введения исследуемого препарата. В случае положительного результата тестирования пациента на экскрецию после последнего введения проводили деконтаминацию желудочно-кишечного тракта с помощью антибиотика перед выпиской пациента. Последующий контроль экскреции проводили до получения отрицательного результата. Как представляется, эти меры являются оправданными и достаточными для защиты окружающей среды и исследовательской группы от воздействия VXM01 до установления профиля выделения.
[00132] VXM01 применяли параллельно с основным лечением с помощью гемцитабина, как показано на Фиг. 4 (общей схеме исследования). Вкратце, гемцитабин давали на 1, 8 и 15 сутки из 28 суток цикла химиотерапии. Вакцину давали четыре раза на 1, 3, 5 и 7 суток, начиная спустя трое суток после последней дозы гемцитабина. Фазу исследования двойным слепым методом завершили через 31 сутки после последнего введения последнему пациенту.
[00133] Для этого I-фазового испытания отбирали популяцию пациентов (пациентов с местнораспространенным или находящимся на IV стадии раком поджелудочной железы) с неблагоприятным прогнозом и выбирали относительно щадящим стандартом лечения в отношении иммуносупрессии. Совместные режимы химиотерапевтического средства гемцитабина с вакцинацией против опухоли могут быть синергетическими. Кроме того, в этой выборке пациентов измеряли специфическую T-клеточную активацию, которая продемонстрировала эффективность вакцины VXM01. Контроль плацебо включили в настоящее испытание с целью получения дополнительных знаний о конкретных проблемах безопасности, связанных с активной вакциной по сравнению с основным лечением. Кроме того, объединенные плацебо-контролируемые пациенты служили в качестве весомой базы сопоставления для оценки специфичной активации иммунной системы и других признаков клинической эффективности. В случае и при переходе в фазу II можно рассматривать различных пациентов с более длительной продолжительностью жизни в зависимости от наблюдаемого профиля безопасности. Такие исследования также включают типы опухоли, проявившие восприимчивость к антиангиогенному лечению.
Пример 3. VXM01-специфическая T-клеточная иммунная реакция
[00134] Реакцию на VXM01 оценивали посредством мониторинга частоты VEGFR2-специфических Т-клеток в периферической крови VXM01 и пациентов, получавших плацебо, детектированных посредством INFγ ELISpot, в различные моменты времени до, во время и после вакцинации.
[00135] Сначала T-клетки и дендритные клетки, сенсибилизированные пептидом, добавляли в лунки, покрытые антителами к INFγ. После периода инкубации клетки удаляли с помощью секретируемого INFγ, оставленного для связывания с антителами оболочки. Затем детекторное антитело добавляли для детектирования связанного INFγ, и после сигнальной амплификации конечный выход можно было рассматривать как «цветные точки», представляющие собой единичные активированные и специфичные T-клетки.
[00136] Положительность образцов посредством ELISpot оценивали в соответствии с предварительно установленными правилами, определяющими полученное увеличение сигнала от 0 до 3 степени на образец:
Без увеличения: 0 степень
Явное увеличение, но <3x: 1 степень
≥3x но <5x увеличение: 2 степень
≥5x увеличение: 3 степень
[00137] Иммунный ответ исследуемых пациентов посредством ELISpot показан в таблице 2:
КОЕ/введение
КОЕ/введение
КОЕ/введение
КОЕ/введение
[00138] Результаты иммунного ответа исследуемых пациентов посредством ELISpot графически изображены на Фиг. 5.
Пример 4. Воздействие на перфузию опухоли
[00139] Перфузию опухоли оценивали посредством времени нахождения контрастного средства (Ktrans) во время динамической магнитно-резонансной томографии с контрастным усилением (DCEMRI) для характеризации эффекта лечения. Проводили динамическое контрастное усиление T1-взвешенных изображений. DCEMRI оценивали на системе 1,5 Тесла (Magnetom Aera, Siemens, город Эрланген, Германия) на 0, 38 сутки и через 3 месяца после лечения. Динамическую магнитно-резонансную томографию с контрастным усилением проводили с помощью последовательностей VIBE (объемно-интерполированного обследования с задержкой дыхания). С этой целью инъецировали дозу 8 мл гадовиста.
[00140] Для каждого обследования исследуемые области вручную очерчивали в пределах опухолевой ткани с последующим проведением поэлеметного анализа с использованием комплекса программного обеспечения Siemens (Tissue 4D). Моделирование исследуемой области было основано на модели Tofts с предполагаемым T10 (1000мс) и Parker AIF. Для оценки перфузии опухоли константу перехода объема рассматривали в качестве основного конечного показателя.
[00141] Изменения среднего значения в перфузии опухоли составляли -9% в группе VXM01 (n=26) по сравнению с +18% в группе плацебо (n=11). Снижение более чем на 33% в перфузии опухоли детектировали у 35% подлежащих оценке пациентов, получивших лечение с помощью VXM01, по сравнению с 10% в группе плацебо. Данные пациентов с самым сильным клиническим ответом дополнительно анализировали в подгрупповом анализе. Максимальное среднее воздействие детектировали во временной точке на 38 сутки. Воздействие различных доз VXM01 на перфузию опухоли графически изображено на Фиг. 6.
Пример 5. Биомаркеры ангиогенеза
[00142] С целью дальнейшей характеризации VEGFR-2-специфической, опосредованной Т-клетками антиангиогенной активности VXM01 проводили наблюдения за сопутствующими изменениями в биомаркерах ангиогенеза - VEGF A, коллагене IV и артериальном давлении человека.
VEGF A:
[00143] VEGF A измеряли в образцах сыворотки человека посредством ELISA с использованием коммерческого набора для анализа (ELISA Kit Quantikine Human VEGF A Immunoassay, R&D Systems, кат. номер: DVE00). Анализ использовали, как описано на вкладыше в упаковке и с учетом изменений в плане исследования согласно указанному выше валидационному исследованию 580.132.2786.
[00144] В этом анализе применяли методику количественного ферментного иммунологического сэндвич-анализа. Моноклональное антитело, специфичное к VEGF A человека, предварительно наносили на микропланшет. Стандарты, образцы контроля качества (коммерчески полученные) и образцы отмеряли пипеткой в лунки, и любой присутствующий VEGF A связывали с помощью иммобилизованного антитела. Калибровочный стандарт, образцы контроля качества и образцы анализировали как копии. После смывки всех несвязанных веществ в лунки добавляли фермент-связанное поликлональное антитело, специфичное к VEGF A. После промывки для удаления любого реагента антитела с ферментом раствор субстрата добавляли в лунки, и формирование цвета происходило пропорционально количеству VEGF A, связанного на начальной стадии. Формирование цвета останавливали, и интенсивность цвета измеряли с использованием спектрометрического планшета для микротитрационного считывающего устройства при 450 нм. Стандартную кривую получали посредством нанесения оптической плотности относительно соответствующей концентрации VEGF A для каждого стандарта. Концентрацию VEGF A в образце определяли непосредственно по этой кривой.
[00145] Уровень VEGF-A в сыворотке повысился в группе VXM01 на 235% как на 38 сутки, так и в 3 месяц по сравнению с 17% и 31% в группе плацебо (p=0,05 в 3 месяц). Количественное выражение VEGF A в образцах сыворотки пациента графически изображено на Фиг. 7.
Коллаген IV:
[00146] Коллаген IV человека измеряли в образцах сыворотки человека посредством ELISA с использованием коммерческого набора для анализа (коллаген IV человека для ELISA, сыворотка, KAMIYA BIOMEDICAL COMPANY, кат. номер: KT-035). Анализ использовали, как описано на вкладыше в упаковке и с учетом изменений в плане исследования согласно указанному выше валидационному исследованию 580.132.3645.
[00147] ELISA коллагена IV человека представлял собой твердофазный одноэтапный сэндвич-ELISA. Коллаген IV в образце одномоментно связывали посредством твердофазного моноклонального антитела и моноклонального конъюгата антитела с ферментом, каждый из которых направляли на различные антигенные сайты. Это привело к тому, что молекула коллагена IV оказалась между твердофазными и фермент-мечеными антителами. После удаления несвязанного фермент-меченого антитела и образца посев инкубировали с хромогенным субстратом (TMB). Полученное в результате формирование цвета было прямопропорционально количеству коллагена IV в образце.
[00148] Уровень коллагена IV в сыворотке повысился на 38 сутки и в 3 месяце в среднем на 7% и 22%, соответственно, в группе VXM01 по сравнению с изменениями, составившими 2% и -7% в группе плацебо (p=0,02 на 3 месяц). Количественное выражение коллагена IV в образцах сыворотки пациента графически изображено на Фиг. 8.
Артериальное давление:
[00149] Артериальное давление (систолическое и диастолическое) и частоту пульса в качестве фармакодинамических показателей антиангиогенной эффективности измеряли по прошествии 5 минут покоя в лежачем положении. Изменения среднего значения систолического артериального давления составляли +3,6 мм рт.ст. и +3,9 мм рт.ст. в экспериментальной группе по сравнению с -8,8 мм рт.ст. и 9,1 мм рт.ст. при плацебо (p=0,08 на 38 сутки). Воздействие на среднее артериальное давление после первой дозы вакцинации (вплоть до 38 суток) графически изображено на Фиг. 9.
Пример 6. Иммунитет против носителя
[00150] Для оценки иммунного ответа на бактериальный носитель детектировали иммуноглобулины против сальмонеллы тифи IgG и IgM посредством ELISA с использованием двух коммерческих наборов для анализа (ELISA для сальмонеллы тифи IgG с каталожным номером ST0936G и ELISA для сальмонеллы тифи IgM ELISA с каталожным номером ST084M; Calbiotech. Inc., 10461 Austin Dr, Spring Valley, CA 91978, США). Эти анализы являлись количественными анализами. Анализы использовали, как описано на вкладыше в упаковках, соответственно, App., I/I) и с учетом изменений в плане исследования согласно указанному выше валидационному исследованию 580.132.2785.
[00151] В обоих анализах использовали метод твердофазного иммуноферментного анализа. Калибровочный стандарт, отрицательный контроль, положительный контроль и образцы анализировали как дубликаты. Разбавленную сыворотку пациента (при разведении 1:101) добавляли в лунки, покрытые очищенным антигеном. Специфическое антитело IgG или IgM, при его присутствии, связывали с антигеном. Все несвязанные материалы смывали и добавляли ферментный конъюгат для связывания комплекса антитело-антиген, при его присутствии. Избыток ферментного конъюгата смывали и добавляли субстрат. Планшет инкубировали для обеспечения гидролиза субстрата с помощью фермента. Интенсивность цветообразования была пропорциональна количеству специфического антитела IgG или IgM в образце. Интенсивность цветообразования измеряли с использованием спектрофотометрического планшета для микротитрационного считывающего устройства при 450 нм. Границу пропускания рассчитывали следующим образом:
Калибровочная оптическая плотность × калибровочный коэффициент.
[00152] Индекс антител каждого результата определяли посредством деления значения оптической плотности каждого образца на значение границы пропускания.
[00153] Расшифровка индекса антител:
<0,9 отсутствие детектируемого антитела к сальмонелле тифи IgG или IgM посредством ELISA
0,9-1,1 пограничное положительное значение
>1,1 детектируемое антитело к сальмонелле тифи IgG или IgM посредством ELISA
[00154] Количество пациентов с детектируемыми иммуноглобулинами против сальмонеллы тифи IgG изображены на Фиг. 10.
Пример 7. Экскреция
[00155] Выделение бактерий в стуле и физиологических жидкостях, слезах, слюне, моче и крови наблюдали в исследовании VXM01-01-DE в соответствии со способами, утвержденными переданными в качестве ранее проверенных в соответствии с GLP в учрежденной централизованной лаборатории (Huntingdon Life Sciences, город Хантингдон, Великобритания). Выделение и биораспределение VXM01 в физиологических жидкостях определяли посредством культивирования на чашках и обогатительного культивирования. Идентичность бактерии-носителя VXM01 определяли посредством серологической агглютинации и ПЦР.
[00156] Тестируемые образцы (кровь, слезы, мочу, слюну и кал) собирали в исследовательском центре города Гейдельберг и осуществили доставку образцов после вакцинации в MicroMol GmbH, находящемся в городе Карлсруэ, Германия, на те же сутки. Каскадный анализ выделения бактериального вектора и биораспределения разработали с целью обнаружения живых КОЕ VXM01 или горизонтального переноса плазмиды. Он состоит из двух отдельных частей анализа (части I и части II):
Часть I: Чашечный метод для детектирования горизонтального переноса плазмиды
Часть II: Жидкая обогатительная культура для детектирования живых КОЕ VXM01
[00157] После каскадного анализа применяют матрицу принятия решений с целью определения экскреции живых бактерий VXM01 или наблюдения горизонтального переноса плазмиды. Каскад обозначен на Фиг. 11.
Часть анализа I для детектирования горизонтального переноса плазмиды:
- Сутки 0: культивирование 5 тестируемых образцов на каждые 3 чашки с триптон-соевым агаром (+ канамицин), инкубация в течение ночи при 37°C
- Сутки 1: визуальное различение между морфотипами VXM01 (Ty21a) и не VXM01 на отобранных чашках. Отбор морфотипов не VXM01 (по 9 колоний), размазывание по чашкам с агаром (+ канамицин) для агглютинации и параллельной жидкой культуре (+ канамицин) для каждого объединенного морфотипа для анализа ПЦР на следующие сутки
- Сутки 2: ПЦР каждой совокупности жидких морфотипов
Часть анализа II для детектирования VXM01:
- Сутки 0: Получение жидких обогатительных культур (+ канамицин) для каждого из 5 тестируемых образцов
- Сутки 1: ПЦР непосредственно на каждую жидкую обогатительную культуру. Размазывание каждой обогатительной культуры по чашкам с агаром (+ канамицин) для серологического анализа на следующие сутки в случае положительной ПЦР для плазмиды
- Сутки 2: серологическое подтверждение присутствия VXM01 (Ty21a)
[00158] Ввиду того факта, что ПЦР любого тестируемого образца не различают между живыми КОЕ и/или свободной плазмидой или геномной ДНК Ty21a и в качестве агглютинации не может быть применена непосредственно к тестируемым образцам, ПЦР, а также способы агглютинации, использовали в качестве способов второй линии после применения чашечного метода. Выявленные живые колонии, выращенные на канамицин-содержащих чашках, были дополнительно охарактеризованы с помощью этих способов. Только чашечный метод способствует дифференцировке между живыми и мертвыми клетками (или VXM01, или чужими трансформантами не VXM01 плазмиды ввиду горизонтального переноса плазмиды).
[00159] Выведение VXM01 с калом наблюдали у двух пациентов - одного в дозовой группе 109 и одного в дозовой группе 1010. Экскреция VXM01 с калом у обоих пациентов была неустановившейся в одном случае после первого или второго введения, соответственно, и исчезла без лечения антибиотиком. Количество пациентов с экскрецией VMX01 в различных дозовых группах графически изображено на Фиг. 12.
[00160] Подводя итог, следует отметить, что VXM01 обладает потенциалом направленности на различные типы опухоли и устранения многих препятствий, возникающих при других современных подходах к получению вакцин против злокачественной опухоли. Представляется заманчивой перспективой возможность комбинации вакцины по настоящему изобретению с многими другими средствами против злокачественных опухолей и иммуномодулирующими средствами. Результаты исследования, приведенные в настоящем документе, побуждают авторов изобретения к дальнейшему продвижению этого подхода, представляющего большой интерес.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВЫСОКОПРОДУКТИВНЫЙ СПОСОБ ПОЛУЧЕНИЯ ОСЛАБЛЕННЫХ ШТАММОВ SALMONELLA | 2012 |
|
RU2631924C2 |
| ДНК-ВАКЦИНА ПРОТИВ ПРОЛИФЕРИРУЮЩИХ ЭНДОТЕЛИАЛЬНЫХ КЛЕТОК И СПОСОБЫ ЕЕ ПРИМЕНЕНИЯ | 2003 |
|
RU2318019C2 |
| КОМПОЗИЦИЯ ДНК ДЛЯ ВЫЗОВА ИММУННОГО ОТВЕТА ПРОТИВ ОПУХОЛЕАССОЦИИРОВАННЫХ МАКРОФАГОВ | 2007 |
|
RU2459631C2 |
| МИКРООРГАНИЗМЫ В КАЧЕСТВЕ НОСИТЕЛЕЙ НУКЛЕОТИДНЫХ ПОСЛЕДОВАТЕЛЬНОСТЕЙ, КОДИРУЮЩИХ КЛЕТОЧНЫЕ АНТИГЕНЫ, ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕЙ | 2003 |
|
RU2319741C2 |
| АТТЕНУИРОВАННЫЕ ВИРУСЫ С МИНУС-ЦЕПЬЮ С ИЗМЕНЕННОЙ АНТАГОНИСТИЧЕСКОЙ В ОТНОШЕНИИ ИНТЕРФЕРОНА АКТИВНОСТЬЮ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ВАКЦИН И ФАРМАЦЕВТИЧЕСКИХ ВЕЩЕСТВ | 1999 |
|
RU2236252C2 |
| СПОСОБ ПОЛУЧЕНИЯ АТТЕНУИРОВАННОГО ШТАММА БАКТЕРИЙ SALMONELLA | 1988 |
|
RU2114172C1 |
| СПОСОБ ПОЛУЧЕНИЯ АТТЕНУИРОВАННОГО ШТАММА БАКТЕРИЙ SALMONELLA И ВАКЦИНА | 1992 |
|
RU2126447C1 |
| ИММУНИЗАЦИЯ ВЕКТОРОМ НА ОСНОВЕ ВИРУСА БЕШЕНСТВА, ЭКСПРЕССИРУЮЩИМ ЧУЖЕРОДНЫЙ БЕЛКОВЫЙ АНТИГЕН | 2013 |
|
RU2660566C2 |
| АКТИВНАЯ ИММУНОТЕРАПИЯ ПРОТИВ АНГИОГЕНЕЗА | 2003 |
|
RU2329824C2 |
| Полиэпитопная противоопухолевая вакцинная конструкция, содержащая эпитопы опухоль-ассоциированных антигенов, фармацевтическая композиция и ее применение для стимуляции специфического противоопухолевого иммунного ответа | 2016 |
|
RU2684235C2 |














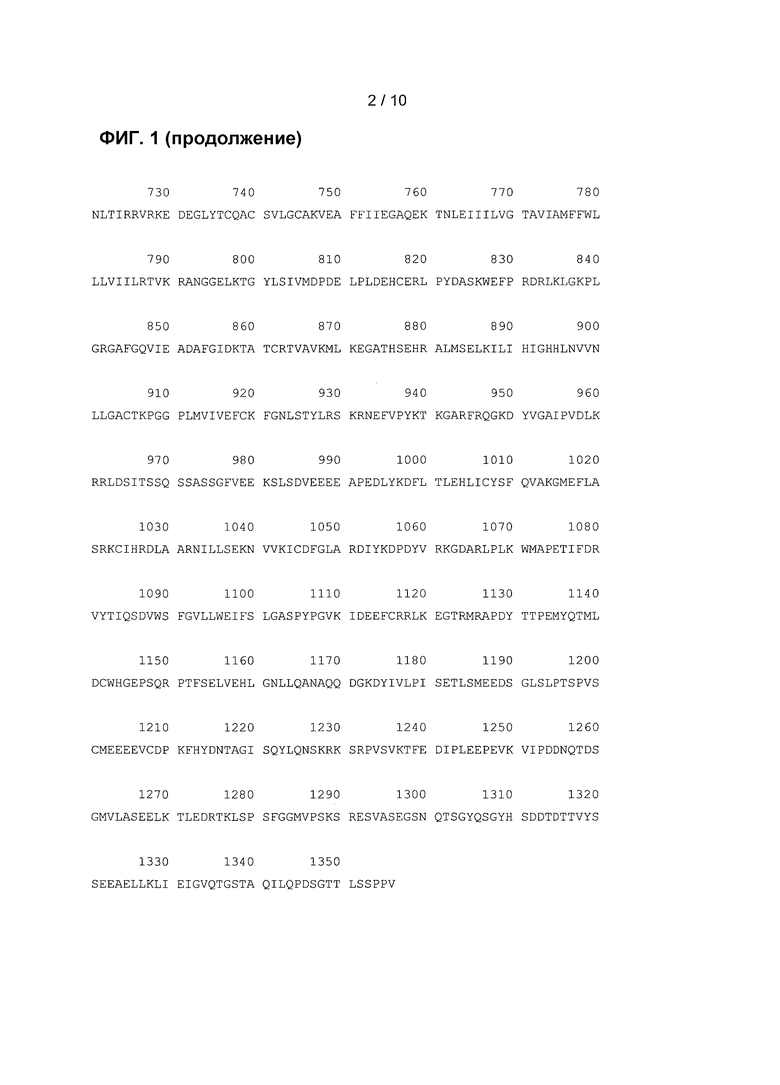
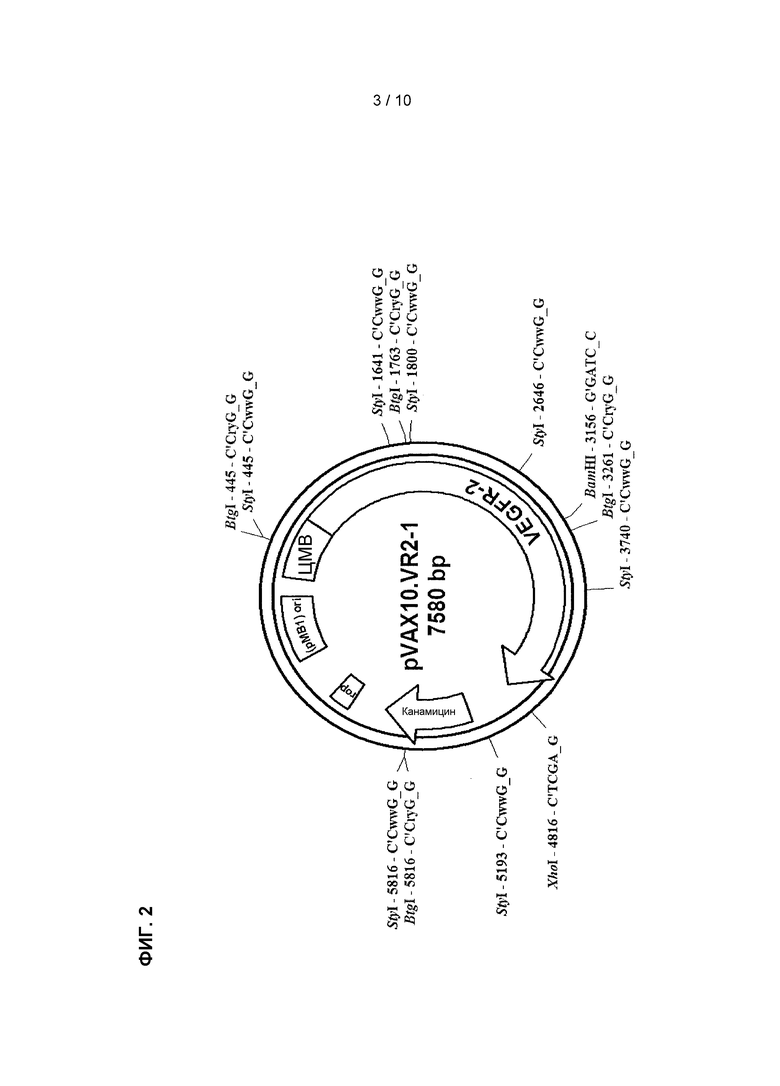
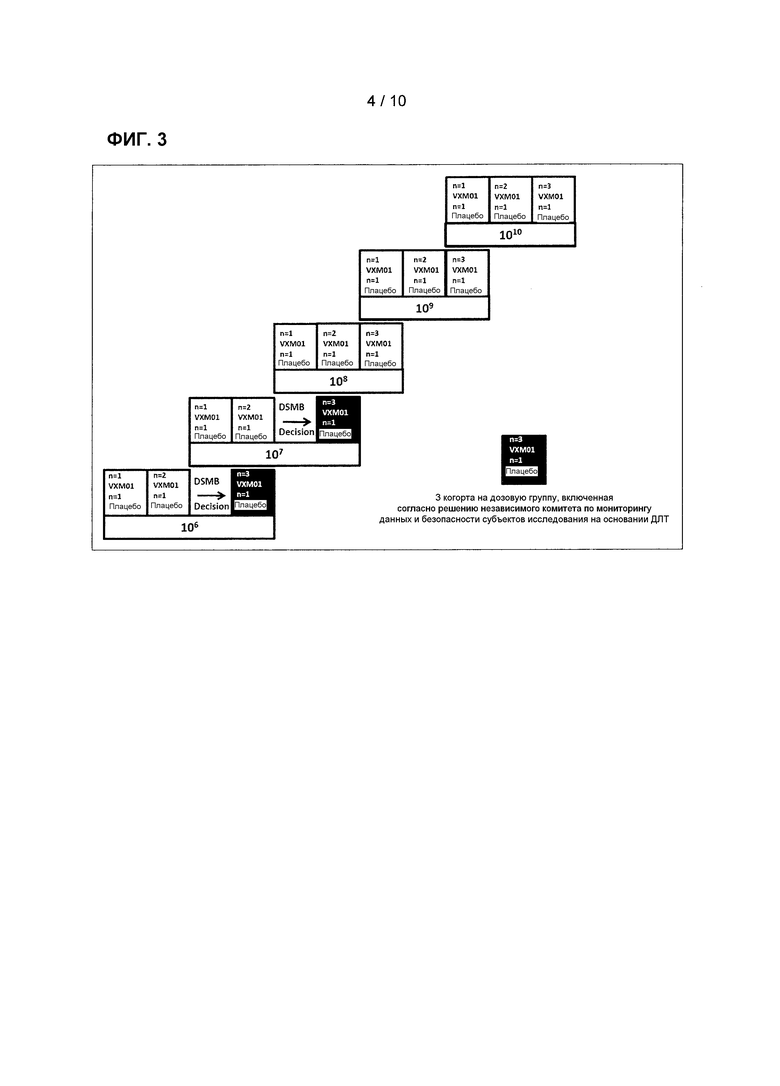
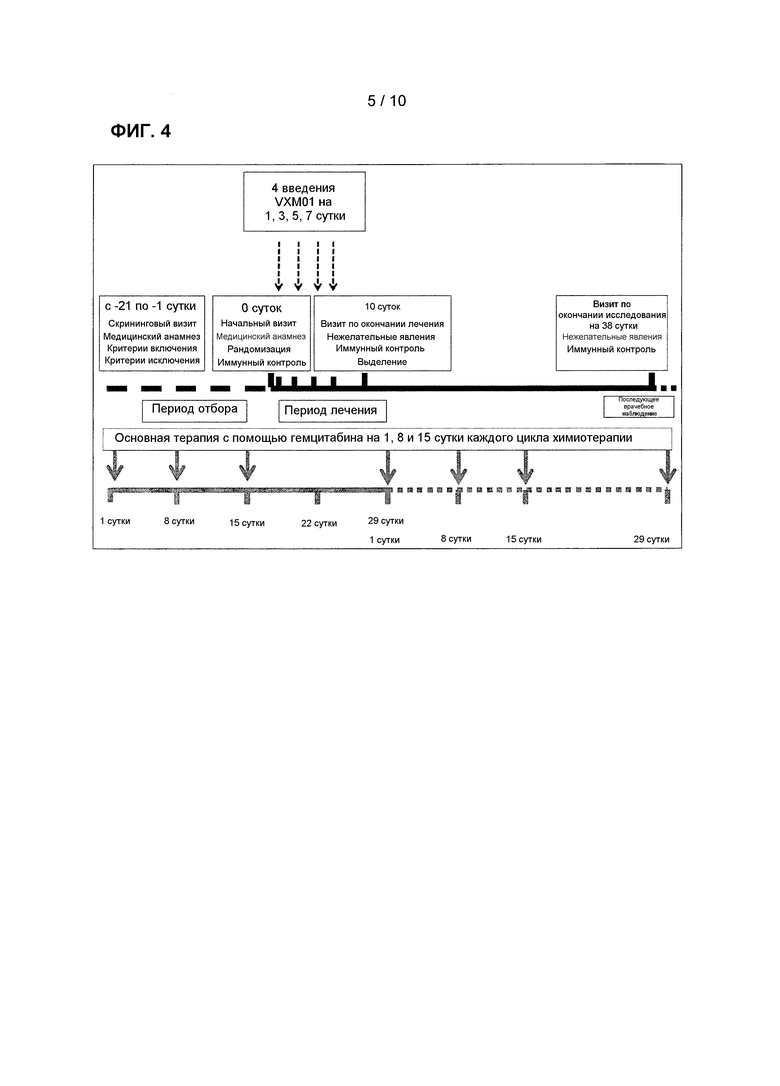
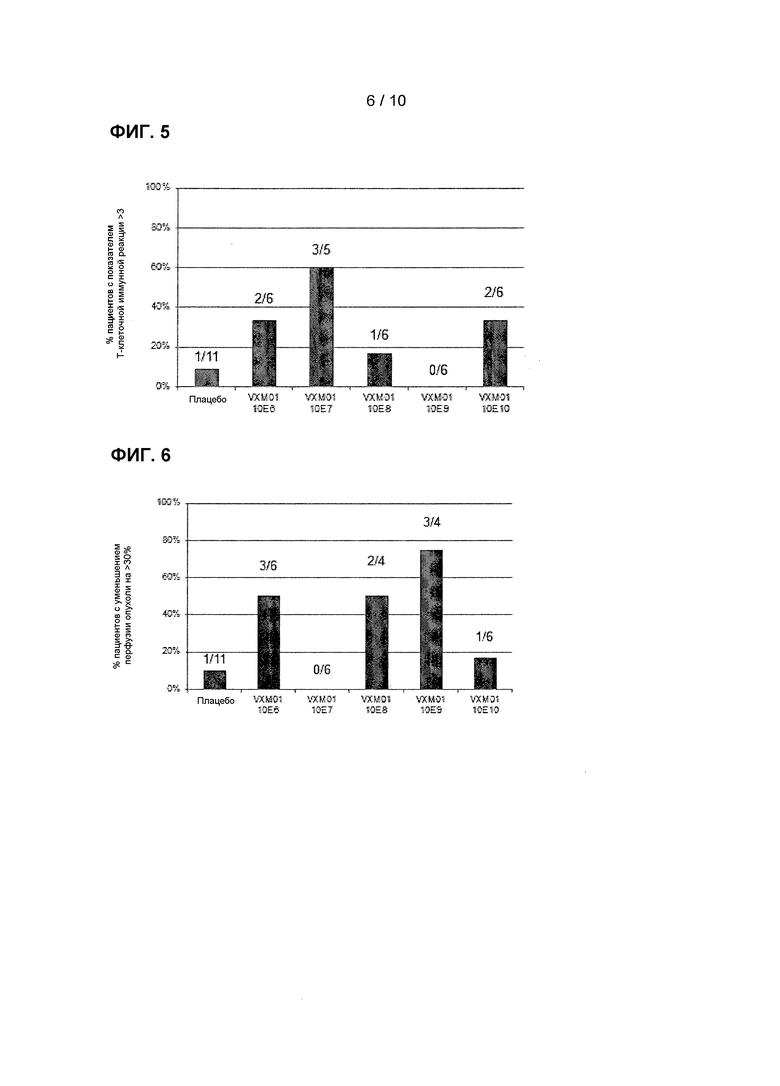
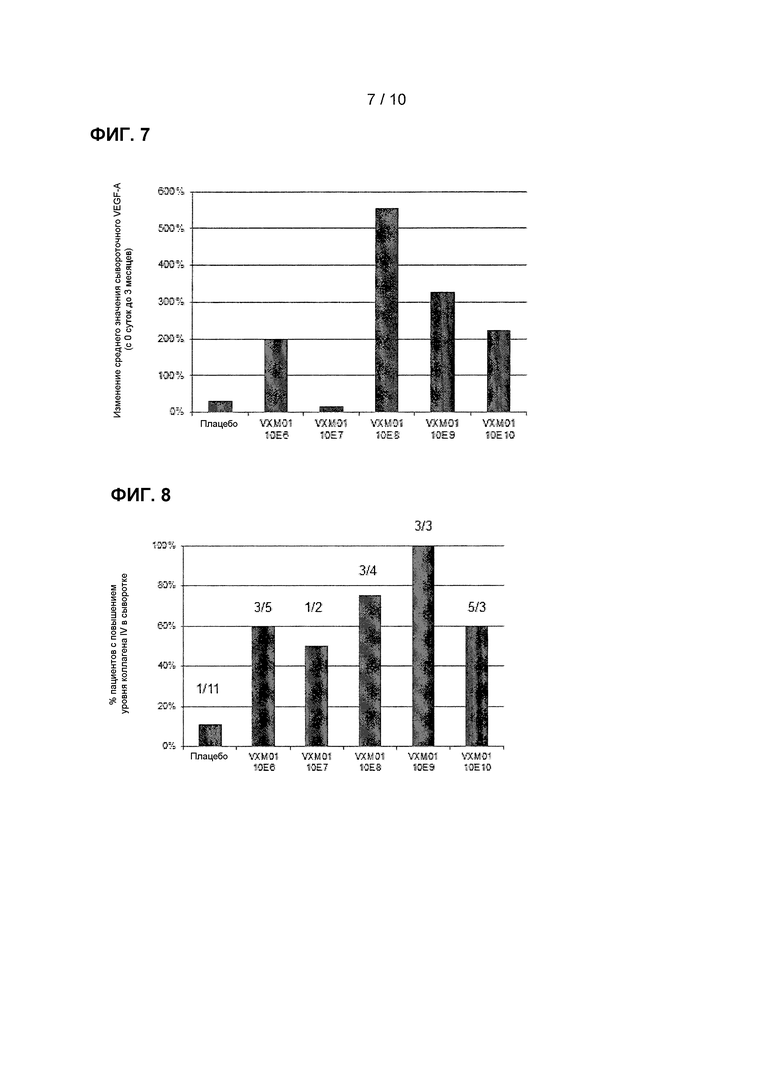
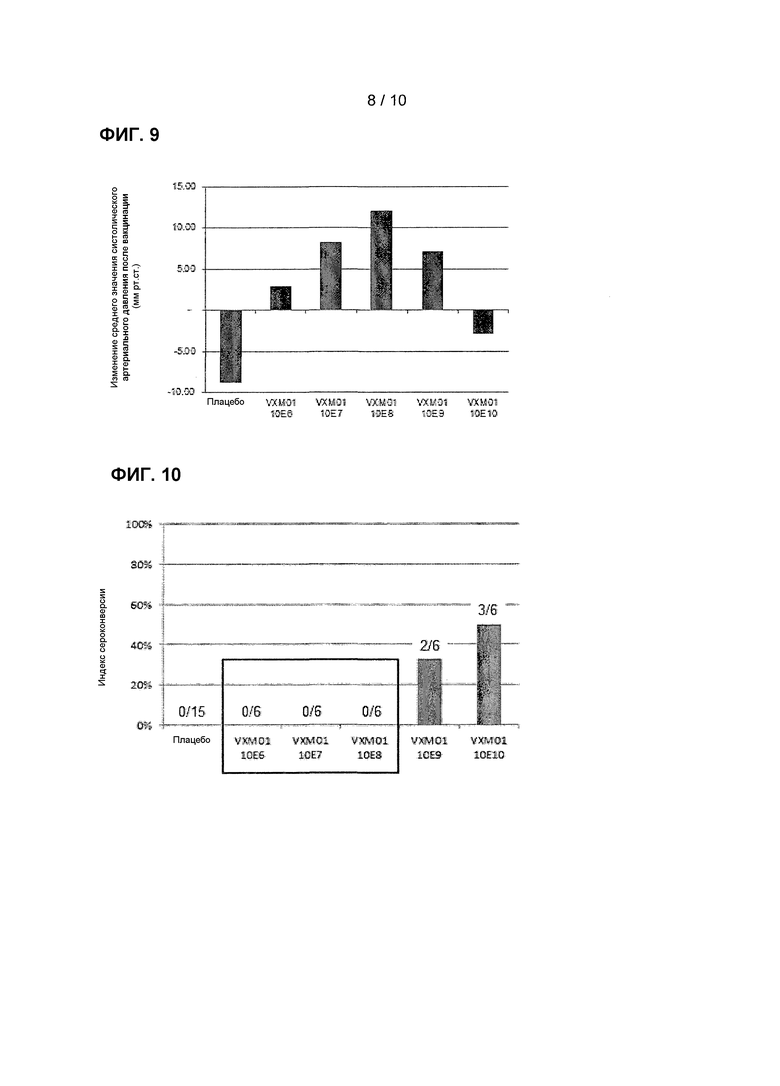
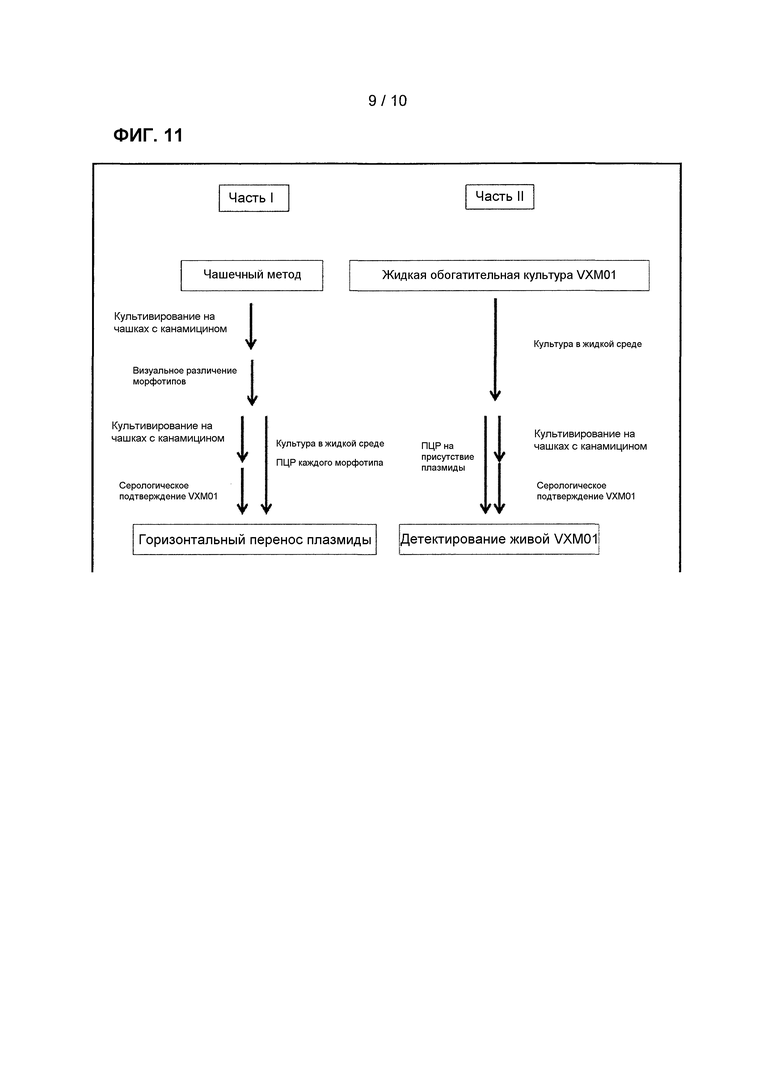

Изобретения относятся к аттенуированному мутантному штамму Salmonella enterica серовар typhi Ту21а и вакцине, содержащей такой штамм. Представленный штамм содержит по меньшей мере одну копию рекомбинантной молекулы ДНК, которая содержит эукариотическую экспрессирующую кассету, кодирующую рецепторы белка VEGF, где рецепторный белок VEGF представлен VEGFR-2 человека, который имеет аминокислотную последовательность, как представлено в SEQ ID NO: 1, для применения в качестве вакцины в иммунотерапии злокачественных опухолей, где однократная доза вакцины составляет 1×109 или менее чем 1×109 КОЕ. Изобретения позволяют получать необходимый иммунологический и клинический ответы при очень низких дозах. 3 н. и 13 з.п. ф-лы, 12 ил., 2 табл., 7 пр.
1. Аттенуированный мутантный штамм Salmonella enterica серовар typhi Ту21а, содержащий по меньшей мере одну копию рекомбинантной молекулы ДНК, которая содержит эукариотическую экспрессирующую кассету, кодирующую рецепторы белка VEGF, где рецепторный белок VEGF представлен VEGFR-2 человека, который имеет аминокислотную последовательность, как представлено в SEQ ID NO: 1, для применения в качестве вакцины в иммунотерапии злокачественных опухолей, где однократная доза вакцины составляет 1×109 или менее чем 1×109 КОЕ.
2. ДНК-вакцина, содержащая аттенуированный мутантный штамм Salmonella enterica серовар typhi Ту21а по п. 1, для применения в иммунотерапии злокачественных опухолей.
3. ДНК-вакцина по п. 2, где ДНК-вакцина содержит аттенуированный штамм Salmonella typhi Ту21а, трансформированный плазмидой, которая содержит эукариотическую экспрессирующую кассету, кодирующую белок VEGFR-2 с SEQ ID NO: 1, для применения в антиангиогенной иммунотерапии злокачественных опухолей.
4. ДНК-вакцина по п. 3, где плазмида имеет последовательность, как представлено в SEQ ID NO: 3.
5. ДНК-вакцина по п. 2, где злокачественной опухолью является рак поджелудочной железы.
6. ДНК-вакцина по п. 5, где указанный рак поджелудочной железы находится на IV стадии или является местнораспространенным раком поджелудочной железы.
7. ДНК-вакцина по п. 2, где злокачественная опухоль включает метастазы.
8. ДНК-вакцина по п. 2, где лечение проводится в сопровождении химиотерапии и/или лучевой терапии.
9. ДНК-вакцина по п. 8, где химиотерапевтическим средством является гемцитабин.
10. ДНК-вакцина по п. 8, где иммунотерапевтическое лечение с помощью вакцины проводят в ходе цикла лечения химиотерапией.
11. ДНК-вакцина по п. 2, где вакцину вводят перорально.
12. ДНК-вакцина по п. 2, где однократная доза вакцины составляет 1×105, 1×106, 1×107, 1×108 или 1×109 колониеобразующих единиц (КОЕ).
13. ДНК-вакцина для применения по п. 9, где однократная доза вакцины составляет от 1×108 до 1×109 КОЕ.
14. ДНК-вакцина для применения по п. 9, где однократная доза вакцины составляет менее чем 1×108 КОЕ, в частности, где однократная доза вакцины составляет от 1×105 до 1×108 КОЕ, более конкретно, где однократная доза вакцины составляет от 1×106 до 1×107 КОЕ.
15. ДНК-вакцина по п. 2, где однократная доза содержит от приблизительно 106 до приблизительно 109, более конкретно, от приблизительно 106 до приблизительно 108, наиболее конкретно, от приблизительно 106 до приблизительно 107 колониеобразующих единиц (КОЕ).
16. ДНК-вакцина VXM01, содержащая аттенуированный штамм Salmonella enterica серовар typhi Ту21а, трансформированный плазмидой, содержащей ДНК, кодирующую белок VEGFR-2 с SEQ ID NO: 1, где плазмида представляет собой плазмиду ДНК размером 7580 п.н. и содержит кДНК VEGFR-2 под контролем промотора цитомегаловируса (ЦМВ), канамицин-устойчивого гена и pMB1 ori, и имеет последовательность, как представлено в SEQ ID NO: 3, для применения в иммунотерапии злокачественных опухолей, где однократная доза вакцины составляет 1×109 или менее чем 1×109 КОЕ.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| CHRISTIAN HOTZ et al., Improvement ofthelivevaccinestrain Salmonella enterica serovar Typhi Ty21aforantigendeliveryviathehemolysinsecretionsystem of Escherichia coli, International Journal of Medical Microbiology, 2009, Vol.299, pp.109-119 | |||
| DOMINIQUE FRAILLERY et al., Salmonella enterica Serovar Typhi Ty21a Expressing Human Papillomavirus Type 16 L1 as a Potential Live Vaccine against Cervical Cancer and Typhoid Fever, CLINICAL AND VACCINE IMMUNOLOGY, Oct | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Спринклерная головка для водяных и химических огнетушителей с сигнализацией | 1924 |
|
SU1285A1 |
| BIN YU et al., A method to generate recombinant Salmonella typhi Ty21a strains expressing multiple heterologous genes using an improved recombineering strategy, Appl Microbiol Biotechnol, 2011, Vol.91, pp.177-188 | |||
| ДНК-ВАКЦИНА ПРОТИВ ПРОЛИФЕРИРУЮЩИХ ЭНДОТЕЛИАЛЬНЫХ КЛЕТОК И СПОСОБЫ ЕЕ ПРИМЕНЕНИЯ | 2003 |
|
RU2318019C2 |
Авторы
Даты
2017-11-22—Публикация
2013-06-26—Подача