Изобретение относится к новому производному в ряду 2,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазола, а именно к неописанному ранее гидрогалогениду 1-(3,4-диметоксифенил)-2-(7,8-диметил-2,3,4,5-тетрагадро[1,3]диазепино[1,2-а]бензимидазол-11-ил)этанону формулы 1:
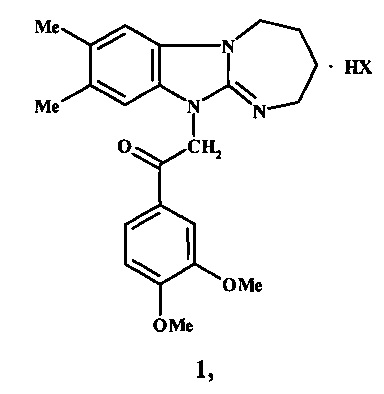
где X=Cl, Br,
обладающему одновременно обезболивающей и анксиолитической активностью.
Боль - это типовой, эволюционно выработанный процесс, возникающий в результате воздействия на организм ноцицептивных факторов или ослабления противоболевой системы. Он включает в себя соматический, вегетативный, эмоциональный, поведенческий, двигательный, антиноцицептивный компоненты и направлен на защиту организма от повреждений и на устранение боли. Международная ассоциация по изучению боли определяет боль как "неприятное сенсорное и эмоциональное ощущение, связанное с действительным или возможным повреждением тканей или описываемое в терминах такого повреждения". Любой болевой синдром сопровождается эмоциональным расстройством и невротическим состоянием. Поэтому в клинической практике применяют сочетанную терапию анальгетическими средствами и анксиолитиками [1]. Наиболее выраженные невротические расстройства возникают при синдроме хронической боли, которую чаще всего купируют наркотическими анальгетиками, однако выраженные побочные явления в виде дыхательной депрессии, развития толерантности к анальгетическому эффекту и наркогенного потенциала существенно ограничивают их применение [2]. В связи с этим поиск средств как с обезболивающим, так и с транквилизирующим действием становится одним из перспективных направлений для создания новых средств.
Современная медицина располагает большим количеством разнообразных препаратов для предупреждения и лечения нервно-психических заболеваний: агонисты бензодиазепиновых рецепторов (диазепам, феназепам и др.), агонисты серотониновых рецепторов (буспирон), вещества разного типа действия (бенактизин и др.) [3]. Большинство препаратов обладает неблагоприятными побочными эффектами, заключающимися в угнетении ЦНС: сонливость в дневное время, вялость, мышечная слабость, притупление эмоций, головная боль, головокружение, атаксия и др. Возможно нарушение когнитивных функций, а при длительном применении - привыкание, лекарственная зависимость [4, 5].
Известны производные бензимидазола, проявляющие анксиолитическую и обезболивающую активности [6].
Однако их активность остается недостаточно высокой.
Наиболее близкими по структуре среди производных 2,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазола являются гидрохлориды 11-фенацилпроизводных 2,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазола, обладающие гипотензивным действием [7], и гидрогалогениды 11-феноксиэтил- и бензилзамещенных 2,3,4,5-тетерагидро[1,3]диазепино[1,2-а]бензимидазола, обладающие антиагрегантной активностью [8].
В ряду 2,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазола не известны соединения, проявляющие одновременно обезболивающую и анксиолитическую активность.
Техническим результатом изобретения является новое соединение в ряду 2,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазола, проявляющее неизвестную для данного ряда совокупность активностей - обезболивающую и анксиолитическую.
Технический результат достигается соединением 1.
Синтез соединения 1 заключается в алкилировании 7,8-диметил-,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазола [9] (2) 2-галоген-1-(3,4-диметоксифенил)этаноном при кипячении в нитрометане:
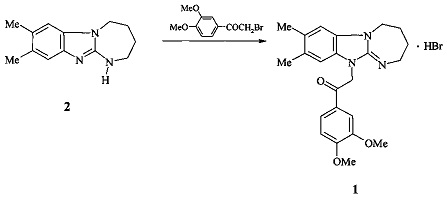
Ниже приведен пример синтеза соединения.
Пример. Гидробромид 1-(3,4-диметоксифенил)-2-(7,8-диметил-2,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазол-11-ил)этанона (1). Раствор 0.44 г (2 ммоль) 2,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазола (2) и 0.52 г (2 ммоль) 2-бром-1-(3,4-диметоксифенил)этанона в 15 мл нитрометана кипятили в течение 12 ч. Охлаждали, выделившийся осадок отфильтровывали. Выход 0.85 г (90%). Бесцветные кристаллы с т.пл. 246-248°C (из изопропанола).
Спектр ЯМР 1Н, (300 МГц), δ, м.д. (ДМСО-d6): 1.92-2.06 м (4Н, С(3)Н2, С(4)Н2); 2.07 с (3Н, CH3); 2.26 с (3Н, СН3); 3.42-3.44 м (2Н, С(5)Н2); 3.84 с (3Н, ОСН3); 3.89 с (3Н, ОСН3); 4.30-4,31 м (2Н, С(2)Н2); 5.90 с (2Н, СН2Ar); 7.20 д (1Н, Н(5'), J 8.5 Гц)1 (1 Здесь и далее цифрами со штрихом показаны протоны арильного заместителя в положении 11 диазепинобензимидазола 1.); 7.38 с (1Н, Н(10) или Н(7)), 7.52 с (2Н, Н(7) или Н(10), Н(2')); 7.78 д.д (1H, H(6'), J 8.4, 2.0 Гц); 8.66 с (1Н, +NH). Найдено, (%): С 58.00; Н 5.56; Br 16.791; N 10.00. C23H27N3O3⋅HBr. Вычислено, (%): С 58.23; Н 5.95; Br 16.84; N 10.12.
Исследование фармакологической активности.
Материалы и методы.
Эксперименты проводили на половозрелых мышах-самцах массой 18-23 г. Животные содержались в условиях вивария с естественным световым режимом на стандартной диете лабораторных животных, без ограничения доступа к еде и воде (ГОСТ Р 50258-92) с соблюдением Международных рекомендаций по защите позвоночных животных, используемых при экспериментальных исследованиях (1997). Животных разделили на группы по 10 животных в каждой.
Изучаемые вещества вводили за 30 минут до начала теста. Животным опытных групп внутрибрюшинно вводили либо исследуемое вещество в эквимолярных дозах (диазепаму 2 мг/кг), либо препараты сравнения. Контрольным группам крыс вводился изотонический раствор хлорида натрия.
Оценку болевой чувствительности проводили в тесте «горячая пластина». Животные помещались на пластину, нагретую до температуры 55°C. Время наблюдения составляло 60 секунд. О наличии обезболивающего действия судили по увеличению латентного периода облизывания задней лапки. В качестве препарата сравнения был выбран буторфанол в дозе 1.0 мг/кг, внутрибрюшинно [10].
Метод изучения анксиолитической активности в тесте «приподнятый крестообразный лабиринт» был основан на естественном предпочтении грызунами темных нор, а также на страхе нахождения на открытых площадках и падения с высоты [11].
Животных помещали в приподнятый крестообразный лабиринт и в течение 3-х минут регистрировали следующие показатели анксиолитической активности: латентный период до выхода в открытый рукав (сек), количество выходов в открытый рукав, суммарное время, проведенное в открытых рукавах лабиринта (сек), общее число переходов из рукава в рукав (с указанием переходов типов рукавов), количества свешиваний, реактивность, время ухода из центра (сек), общее время нахождения в центре (сек), количество выглядываний из закрытого рукава, количество болюсов. Препарат сравнения - диазепам был исследован в дозах 0.5, 1.0 и 2.0 мг/кг [12, 13].
Для изучения локомоторной активности животных помещали в актометр Activity cage 7401, в камере которого расположены датчики, фиксирующие горизонтальную активность животного. Информация передается на самописец, в котором есть возможность установки таймера с автоматической фиксацией поученных результатов. Препарат сравнения - диазепам в дозе 2.0 мг/кг [12, 13].
Для определения ректальной температуры использовали термодатчики (AnD DT-623). Температура определяется при погружении электрода на глубину 1.5-1.8 см [10].
Оценку прогипногенного эффекта проводили с использованием теста «гексеналового сна». Об уровне нейролептического действия судили по изменению продолжительности сна в опытных группах по сравнению с контрольной. Регистрировали время засыпания (принятие «бокового положения») и окончания сна (появление первых признаков активности, выход из бокового положения). Отсутствие у изучаемого вещества влияния на длительность гексеналового сна позволяет предположить, что он не оказывает угнетающего влияния на микросомальные системы печени, метаболизирующие барбитураты. Препарат сравнения - диазепам в дозе 2.0 мг/кг [10-12].
Статистическая обработка результатов исследования проводилась с использованием теста Вилкоксона, критерия Краскела-Уолиса с постобработкой тестом Данна, либо с использованием однофакторного дисперсионного анализа и теста Ньюмана-Кеулса, в случае нормального распределения данных. Расчет показателя LD50 проводили с помощью линейного и нелинейного однофакторного регрессионного анализа с определением доверительных интервалов для среднего значения. Обсчет реализован в программе GraphPad Prism 5.0.
Результаты исследований
Об уровне обезволивающего и транквилизирующего действия судили по изменению фиксируемых показателей в опытных группах по сравнению с контрольной.
При изучении анальгетической активности на установке «горячая пластина» диазепин 1 не уступал препарату сравнения - буторфанолу (табл. 1), так у животных в обоих группах увеличивался латентный период облизывания задней лапки на 40% в сравнении с контрольной группой мышей. В группе, получавшей диазепам, изучаемый показатель не имел статистически значимых изменений с результатами интактных животных, а также уступал группе диазепин 1 и буторфанолу.
В ходе работы соединение 1, полученное по вышеприведенному примеру, увеличило количество переходов между рукавами приподнятого крестообразного лабиринта, что свидетельствует о повышении исследовательской активности. Время нахождения животных, которым вводился диазепинобензимидазол 1, в светлом рукаве превосходило препарат сравнения диазепам (2 мг/кг) в эквимолярной дозе в 2 раза и контроль почти в 6 раз. Количество выходов в светлый рукав опытной группы диазепина 1 сопоставимо с препаратом сравнения, который в 2 раза превосходил контрольную группу. Таким образом, соединение 1 проявило анксиолитическую активность в тесте приподнятого крестообразного лабиринта, по эффективности превосходило препарат сравнения - диазепам (табл. 2).

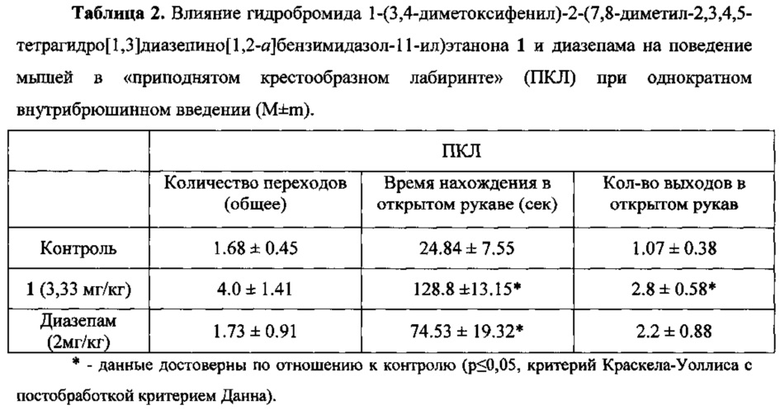
При дальнейшем изучении было выявлено, что диазепинобензимидазол 1 слабо влияет на локомоторную активность животных (табл. 3), незначительно снижая количество переходов в актометре в сравнении с контрольной группой (на 21.0%), при этом диазепам (2 мг/кг) достоверно угнетал двигательную активность мышей (в 4.4 раза в сравнении с группой контроля), а следовательно, диазепинобензимидазол 1 в отличие от препарата сравнения не обладает миорелаксирующим эффектом.
В результате исследования влияния соединения 1 на показатели термометрии достоверных изменений выявлено не было. Так, средняя температура у мышей имеет существенные колебания и в среднем составляет 36.5°C, в группе, в которой вводился диазепам, исследуемый параметр был несколько ниже, но статистически не отличался от уровня контрольной группы.
На продолжительность сна и латентное время засыпания в гексеналовом тесте исследуемое соединение не оказывает влияния, что позволяет сделать вывод об отсутствии прогипногенного действия и позволяет предположить, что вещество не оказывает угнетающего влияния на микросомальные системы печени в отличие от препарата сравнения диазепама.

Таким образом, гидробромид 1-(3,4-диметоксифенил)-2-(7,8-диметил-2,3,4,5-тетрагидро[1,3]диазепино[1,2-а] бензимидазол-11-ил)этанона 1 - производное бензимидазола, имеющее в своей структуре диазепиновый фрагмент, сочетает в себе анальгетические и анксиолитические свойства.
Литература
1. Хабиров Ф.А., Есин Р.Г., Кочергина О.С., Хайбуллин Т.И., Ахметова Г.И., Васильева М.А., Еникеева Г.И., Исмагилова А.А., Каменев В.М., Хабирова Ю.Ф., Хузяшева Э.И. Пребалгин при лечении вертеброгенной корешковой боли // Неврология, приложение к журналу Consilium Medicum». 2011. №15. С. 36-41.
2. Бурчинский С.Г. Анксиолитики нового поколения - новые возможности лечения тревожных состояний в общемедицинской практике // Новости медицины и фармации. 2007. №14. С. 220.
3. Соловьева И.К. Анксиолитики: вчера, сегодня, завтра // Русский медицинский журнал. 2006. Т. 14. №5. С. 385-388.
4. Гурович И.Я., Шмуклер А.Б. Купирующая терапия атипичными антипсихотиками больных с впервые возникшими психотическими состояниями // Социальная и клиническая психиатрия. 2011. Т. 21 №4. С. 51-57.
5. Фаттахов Ш.А. Направленный синтез N-содержащих производных фосфорилуксусных кислот, обладающих биологической активностью: автореф. дис. канд. хим. наук / Ш.А. Фаттахов - Казань: КГТУ. 2010.
6. Спасов А.А., Иежица И.Н., Бугаева Л.И., Анисимова В.А. Спектр фармакологической активности и токсикологические свойства производных бензимидазола // Хим. фарм. ж 1999. Т. 33. №5. С. 6-17.
7. Anisimova V.A., Osipova M.M, Kuzmenko T.A., Caignard D.-H., Renard P., Manechez D. Nouveaux derives tricycliques de benzimidazoles, leur procede de preparation et les compositions pharma-ceutiques qui les contiennent // Fr. Pat. 2765223 (1998); WO 9900390 (1999).
8. Диваева Л.Н., Кузьменко T.A., Спасов A.A., Морковник А.С., Анисимова В.А., Кучерявенко А.Ф., Сиротенко B.C. Пат. РФ 2582618. 2016.
9. Морковник А.С., Спасов А.А., Кузьменко Т.А., Кучерявенко А.Ф., Диваева Л.Н., Кощиенко Ю.В., Анисимова В.А., Таран А.С., Кузьмина Л.Г., Рогова Н.В., Кузнецова В.А., Чепляева Н.И., Воробьева Е.С., Алешин Д.А., Соловьева О.А., Сиротенко B.C., Гайдукова К.А., Богославцева М.В. Прототропное равновесие в 1(11)Н-2,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазоле, синтез и фармакологические свойства его N-замещенных производных // Изв. АН РФ Сер. хим. 2015. №11. С. 2622-2631.
10. Миронов А.Н. Руководство по проведению доклинических исследований лекарственных средств. Часть первая. М.: Гриф и К. 2012. С. 944.
11. Воронина Т.А., Середенин С.Б. Методические указания по изучению транквилизирующего (анксиолитического) действия фармакологических веществ // Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. М.: Ремедиум. 2000. С. 126-136.
12. Yakovlev D., Kolobrodova N., Spasov A., Anisimova V. Anxiolytic profile of 5-HT3-antagonist RU 1204 versus tropisetron and diazepam // European neuropsychopharmacology. 2011. Vol. 21. Supp.2. P. S147.
13. Maltsev D.V., Yakovlev D.S., Matokhin D.G., Samsonik Y.V., Spasov A.A., Anisimova V.A. Anxiolytic action of a new 5-HT2A antagonist RU-476 // European neuropsychopharmacology. 2013. Vol. 23. Supp. 2. P. S519-S520.
| название | год | авторы | номер документа |
|---|---|---|---|
| 11-(4-трет-Бутилбензил)- и фенацилзамещённые 2, 3, 4, 5-тетрагидро[1, 3]диазепино [1, 2-а]бензимидазола, обладающие анксиолитической активностью | 2016 |
|
RU2629022C1 |
| Гидробромид 11-(4-трет-бутилбензил)-2,3,4,5-тетрагидро[1,3]диазепино[1,2-a]бензимидазола, обладающий анксиолитической и противосудорожной активностью | 2017 |
|
RU2662242C1 |
| Способ получения 1(11)H-2,3,4,5-тетрагидро[1,3]диазепино[1,2-a]бензимидазола | 2023 |
|
RU2814769C1 |
| ГИДРОГАЛОГЕНИДЫ 11-[(4-ТРЕТ-БУТИЛФЕНОКСИ)ЭТИЛ]- И 11-БЕНЗИЛЗАМЕЩЁННЫХ 2,3,4,5-ТЕТРАГИДРО[1,3]ДИАЗЕПИНО[1,2-A]БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ АЛЬФА-ГЛЮКОЗИДАЗА ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ | 2015 |
|
RU2602504C1 |
| ГИДРОГАЛОГЕНИДЫ 11-ФЕНОКСИЭТИЛ- И 11-БЕНЗИЛЗАМЕЩЁННЫХ 2,3,4,5-ТЕТРАГИДРО[1,3]ДИАЗЕПИНО[1,2-а]БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ АНТИАГРЕГАНТНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2582618C1 |
| Диметоксибензилсульфопроизводное хиназолин-4(3Н)-она, обладающее анальгезирующей, противопаркинсонической, анксиолитической, психостимулирующей активностью | 2021 |
|
RU2758333C1 |
| 2-бензилпроизводное 4-(3Н)хиназолинона, обладающее анальгезирующим, противопаркинсоническим, антигипоксантным, транквилизирующим действием | 2019 |
|
RU2715884C1 |
| Анксиолитическое средство | 2017 |
|
RU2655929C1 |
| НОВОЕ N-АРИЛСУЛЬФАМИДНОЕ ПРОИЗВОДНОЕ О-БЕНЗОИЛАМИНОБЕНЗОЙНОЙ КИСЛОТЫ, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКОЙ, АКТОПРОТЕКТОРНОЙ И АНТИДЕПРЕССИВНОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2643356C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКИМ ДЕЙСТВИЕМ, НА ОСНОВЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-b)ИНДОЛОВ (ВАРИАНТЫ), ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2007 |
|
RU2338533C1 |
Изобретение относится к области органической химии, а именно к гидрогалогениду 1-(3,4-диметоксифенил)-2-(7,8-диметил-2,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазол-11-ил)этанона формулы 1, обладающему одновременно обезболивающей и анксиолитической активностью. Технический результат: получено новое гетероциклическое соединение, обладающее полезными биологическими свойствами. 1 з.п. ф-лы, 3 табл., 1 пр.
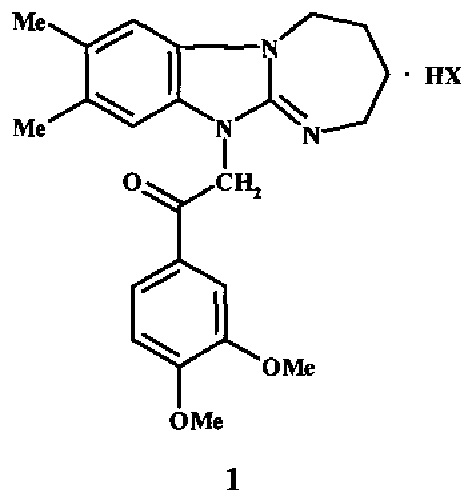
1. Гидрогалогенид 1-(3,4-диметоксифенил)-2-(7,8-диметил-2,3,4,5-тетрагидро[1,3]диазепино[1,2-а]бензимидазол-11-ил)этанона формулы 1:
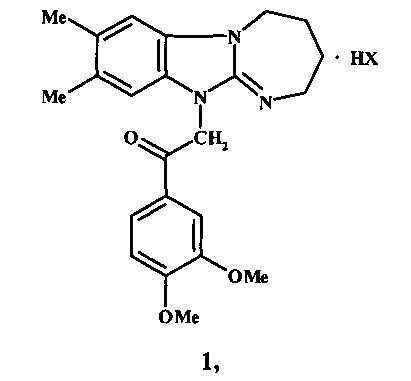
где X = Cl, Br.
2. Гидрогалогенид по п. 1, проявляющий обезболивающую и анксиолитическую активность.
| WO 1999000390 A1, 07.01.1999 | |||
| ИМИДАЗОБЕНЗОДИАЗЕПИНЫ ИЛИ ИХ АДДИТИВНЫЕ СОЛИ С КИСЛОТАМИ | 1992 |
|
RU2041225C1 |
Авторы
Даты
2017-12-01—Публикация
2016-11-21—Подача