Изобретение относится к сельскому хозяйству, а именно к методам определения физико-химических свойств почвы с помощью тепловых средств.
Известен способ определения энергии активации процесса десорбции [Method for measuring clay dispersion average binding free energy and adsorption free energy to cation: пат. CN 100510727 (C) Китай: МПК51 G01N 27/06 / Yujun Wang, Chengbao Li, Dongmei Zhou, Wei Wang, Jiang Jun; заявитель и патентообладатель Nanjing Institute Soil Science CAS - № CN 200613904820060324; заявл. 24.03.2006; опубл. 08.07.2009]. В этом способе суспензию частиц глины размером менее 2 мкм на дистиллированной воде помещают в одпородное электрическое поле напряженностью менее 15 кВ/см, постепенно повышают напряженность электрического поля, одновременно измеряя электропроводности суспензии, строят график зависимости электропроводности от напряженности поля и рассчитывают среднюю энергию связи обменных катионов и почвенных частиц ΔGbo по формуле

где R - универсальная газовая постоянная, Дж/(моль⋅K);
T - абсолютная температура, K;
CEC - емкость катионного обмена, моль-экв./кг;
ср - концентрация частиц в суспензии кг/л;
λ - эквивалентная проводимость обменных ионов См⋅л/(моль-экв.⋅м),
а также свободной энергии адсорбции ΔGad но формуле

где EC и EC0 - электропроводность суспензии в сильном и слабом электрическом поле соответственно, См/м.
Данный способ позволяет получить как среднюю энергию связи обменных ионов с поверхностью частиц глины (почвы) по формуле (1), так и получить распределение количества ионов по энергии связи? используя формулу (2).
Этому способу присущ ряд недостатков. Во первых, это - сложность измерения, требующая создания электрического поля высокой напряженности (вплоть до 200 кВ/см) и соответствующее искажение полученных значений из-за нагрева суспензии во время измерения. Во вторых, в этом способе используется разбавленная суспензия частиц размером менее 2 мкм, что делает его непригодным для определения энергии связи в концентрированных суспензиях, а тем более в ненарушенных образцах глины (почвы). Однако самым большим недостатком этого способа следует признать недостаточную обоснованность формулы (1) - коэффициент «2» в ней следует из предположения о том, что ровно половина электропроводности суспензии обусловлена обменными катионами, а вторая - анионами, что для суспензий частиц глины в общем случае несправедливо.
Наиболее близким по технической сущности к предлагаемому способу является способ определения энергии активации, основанный на ее определении, исходя из температурной зависимости коэффициента диффузии [Глесстон С. Теория абсолютных скоростей реакций. Кинетика химических реакций, вязкость, диффузия и электрохимические явления / С. Глесстон, К. Лейдлер, Г. Эйринг; пер. с англ. под ред. А.А. Баландина, Н.Д. Соколова. - М.: ИЛ, 1948. - 583 с.] по формуле:

где D - коэффициент диффузии, м2/с;
D0 - предэкспоненциальный множитель, м2/с;
Ea - энергия активации, Дж/моль.
При определении энергии активации но этому способу сначала определяют зависимость коэффициента диффузии от температуры, строят график этой зависимости в координатах (lnD; 1/T) и определяют энергию активации по наклону полученной прямой (угловой коэффициент равен -Ea/R).
Коэффициент диффузии может быть определен различными методами, например, по способу определения скорости диффузии веществ в почвах [Пакшина С.М. Миграция солей в микропорах почвы. Автореферат дис. докт. биол. наук. - Новосибирск: СО АН СССР, 1990. с. 3], заключающемуся в помещении почвенного образца на поверхность источника диффундирующего вещества на определенное время с последующим разделением почвенного образца на отдельные слои и определением содержания диффундирующего вещества в каждом из слоев. Основным недостатком такого способа измерения скорости диффузии ионов в почвах являются длительность проведения эксперимента и трудоемкость, связанные с разделением образца почвы на отдельные слои с последующим анализом этих слоев, так как в связи с неодпородностью почв толщина одного слоя не может быть меньше 4…5 мм, а для получения достоверных данных количество слоев должно быть больше 7-8.
Существуют и другие методы определения коэффициента диффузии, однако наиболее простым и удобным в применении оказывается определение его через электропроводность [Глесстон С. Теория абсолютных скоростей реакций. Кинетика химических реакций, вязкость, диффузия и электрохимические явления / С. Глесстон, К. Лейдлер, Г. Эйринг; пер. с англ. под ред. А.А. Баландина, Н.Д. Соколова. - М.: ИЛ, 1948. - 583 с.] по формуле:

где γ - электропроводность, См/м;
z - заряд ионов;
F - постоянная Фарадея, Кл/моль.
Если измерения производятся в небольшом температурном интервале, то энергию активации можно полагать постоянной и тогда из формул (3) и (4) можно определить энергию активации по электропроводностям γ1 и γ2, измеренным при температурах T1 и Т2 соответственно:

К недостатку этого способа определения энергии активации следует отнести то, что в этом случае энергия активации относится ко всему процессу электропроводности в суспензии, включая процессы диссоциации обменных ионов и их движение в объеме жидкости.
Целью изобретения является повышение достоверности определения энергии активации процесса десорбции обменных ионов с поверхности частиц почвы.
Цель достигается тем, что способ определения энергии активации десорбции обменных ионов почвы заключается в ее определении по измеренным значениям электропроводности почвенного образца при различных температурах и фиксированной влажности, отличающийся тем, что расчет энергии активации десорбции обменных ионов производят одним из двух равноценных приемов:
- по угловому коэффициенту наклона аппроксимирующей прямой зависимости электропроводности от температуры, построенной в координатах 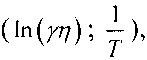 при этом угловой коэффициент прямой равен
при этом угловой коэффициент прямой равен 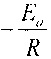 ;
;
- по электропроводности почвенного образца, измеренной при двух значениях температуры по формуле

где Ea - энергии активации десорбции обменных ионов Дж/моль;
R - универсальная газовая постоянная Дж/(моль⋅K);
T1 и T2 - абсолютные температуры, при которых проводится измерение, K;
γ1 и γ2 - электропроводность почвенного образца при температурах;
T1 и T2 - соответственно, См/м;
η1 и η2 - вязкость воды при температурах T1 и T2 соответственно, Па⋅с.
Основанием для осуществления изобретения являются следующие предпосылки.
Электропроводность почвы складывается из электропроводности твердой фазы и порового раствора. Первой составляющей, как правило, можно пренебречь в виду ее очень малой величины [Heimovaara Т.J. Assessing temporal variations in soil water composition with time domain reflectometry / Т.J. Heimovaara, A.G. Focke, W. Boute, J.M. Verstraten // Soil Science Society of America Journal. - 1995. - №59. - p. 689-698]. Электропроводность порового раствора определяется концентрацией ионов и их подвижностью [Сивухин Д.В. Термодинамика и молекулярная физика. - 3-е изд., испр. и доп. - М: Наука. Гл. ред. физ.-мат. лит., - 1990. - 592 с.]:

где zi - заряд i-x ионов;
e - элементарный заряд, Кл;
ni - концентрация i-х ионов, м-3;
bi - подвижность i-x ионов, м2/(В⋅с).
Подвижность ионов порового раствора в первую очередь определяется вязкостью воды. Если считать ионы шарами с радиусом, равным радиусу гидратированного иона, и применить закон вязкого трения Стокса, то подвижность определяется выражением

где η - вязкость воды, Па⋅с;
r - радиус гидратированного иона, м.
Поэтому в первом приближении, при расчете температурной зависимости электропроводности почвы, влияние температуры на подвижность ионов можно учесть ее влиянием на вязкость воды и считать электропроводность, так же как и подвижность, обратно пропорциональной вязкости воды [Балданова Д.М. Плазменно-гидродииамическая концепция состояния ионов в растворах электролитов в оценке некоторых свойств: монография / Д.М. Балданова, Б.Б. Танганов. - М.: Издательский дом Академии Естествознания, 2012. - 100 с.].
Электропроводность порового раствора обессоленной почвы (например, многократно очищенной декантацией дистиллированной водой) определяется обменными ионами, диссоциировавшими с поверхности коллоидных частиц [Бадесса Толера Седа. Перенос многозарядных ионов через ионообменные мембраны при электродиализе: диссертация … кандидата химических наук: 02.00.05. - Воронеж, 2015. - 143 с.]. При физической адсорбции (что справедливо для адсорбции обменных ионов) энергией активации адсорбции по сравнению с энергией активации десорбции Еа можно пренебречь. Следовательно, концентрация ионов в поровом растворе будет

где ni0 - максимально возможная концентрация i-x ионов.
Из уравнений (7)-(9) следует выражение для электропроводности порового раствора

Для моноионной почвы выражение (10) имеет вид

Записав это выражение для двух разных температур и разделив друг на друга, получаем расчетную формулу для расчета энергии десорбции обменных ионов через электропроводность и температуру почвы:

где индексами отмечены значения для первого и второго измерения.
Способ осуществляется следующим образом.
1. Почва переводится в моноионную форму по методике Гедройца (многократная обработка заданным солевым раствором с многократной очисткой декантацией дистиллированой водой) [Злочевская Р.И. Электроповерхностные явления в глинистых породах / Р.И. Злочевская, В.А. Королев. - М., Изд-во МГУ, - 1988. - 177 с.]. Если почва не переводится в моноионную форму, то будет получено усредненное значение энергии активации, относящееся ко всему комплексу поглощенных ионов.
2. Почвенный образец насыщается дистиллированной водой до необходимой влажности и помещается в герметичную кювету с инертными электродами. Кювета помещается в термостат. Производится измерение установившегося значения электропроводности образца на переменном токе при двух температурах (ориентировочно в диапазоне от 1°C до 25°C).
3. Производится расчет энергии активации десорбции по формуле (12) по значениям электропроводности и вязкости воды при двух значениях температуры почвы.
Способ позволяет определить энергию активации процесса десорбции обменных ионов для моноионной почвы, хотя он применим и для полиионных образцов для определения среднего значения энергии активации.
Приводимый далее пример раскрывает суть предлагаемого изобретения.
Почвенный образец переводился в моноионную форму по методике Гедройца путем многократной обработки солевым раствором с многократной очисткой декантацией дистиллированой водой. Обработка образца производилась раствором хлорида натрия (чда) и последующей промывкой дистиллированной водой до исчезновения реакции на ионы хлора (проверка реакцией нитратом серебра). Определялась электропроводность легкосуглинистой серой лесной почвы горизонта B1, насыщенная ионами Na+.
Массу образца выбирали из условия надежности определения электропроводности, и чтобы крупные фракции не влияли на контакт почвенного образца и электродов (обычно достаточно навески сухой почвы 25÷50 г). При этих условиях масса навески не влияет на результат определения энергии активации.
Почвенный образец насыщался дистиллированной водой до необходимой влажности (в данном примере 4,9%) и помещался в герметичную кювету с инертными электродами. В описываемом примере кювета представляла собой стеклянный стакан для взвешивания с притертой стеклянной крышкой (СН 50×30 мм), в который установлены электроды из инертного сплава ПдВ-20.Т.0,15. Кювета подключалась к измерителю электропроводности и помещалась в термостат. Измерение установившегося значения электропроводности образца производилось на переменном токе (1000 Гц).
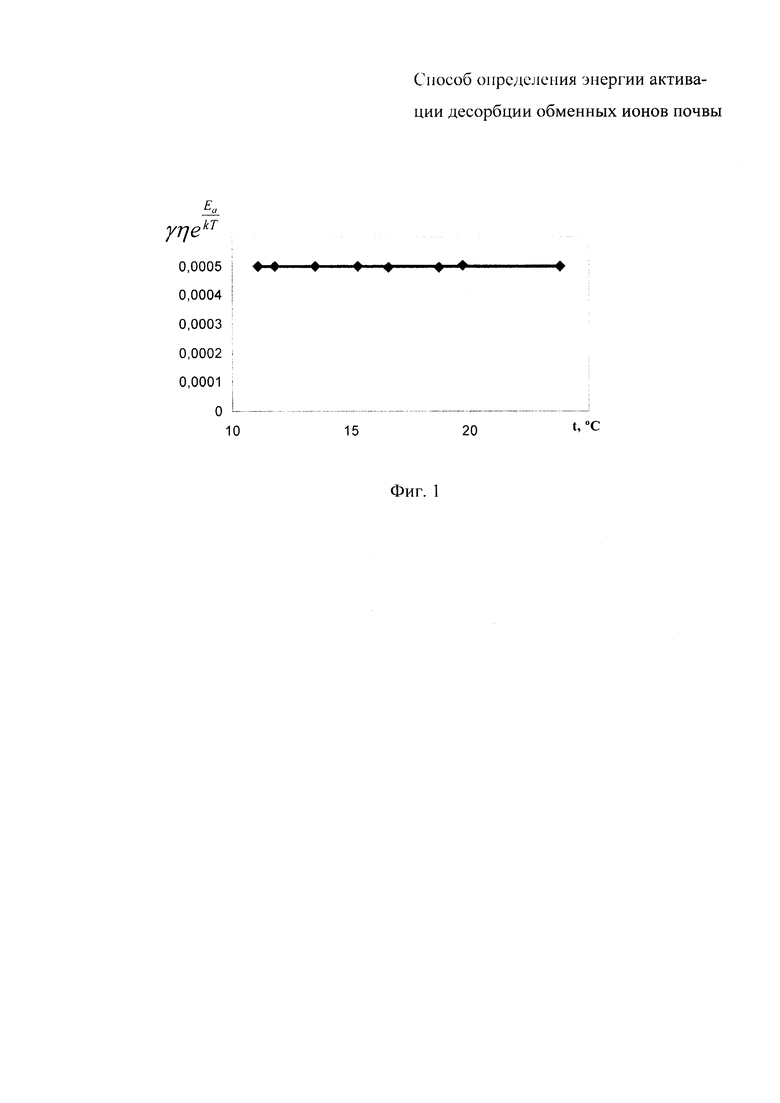
Согласно формуле (11) должно выполняться равенство 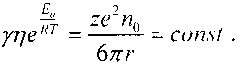 Как показали предварительные эксперименты, для всех почв можно подобрать значение Еа, при котором величина
Как показали предварительные эксперименты, для всех почв можно подобрать значение Еа, при котором величина 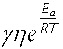 не зависит от температуры. График этой зависимости для данного примера показан на фиг. 1. Независимость величины
не зависит от температуры. График этой зависимости для данного примера показан на фиг. 1. Независимость величины 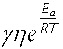 от температуры подтверждает справедливость формул (11) и (12) и возможность определения энергии активации, используя измерения при различных температурах. Для обеспечения малости ошибки температурный диапазон должен быть достаточно широк - для точности 5% необходимо использовать диапазон шириной не менее 10°C, например - 10÷20°C, а измерение должно производиться с точностью ±0,01°C.
от температуры подтверждает справедливость формул (11) и (12) и возможность определения энергии активации, используя измерения при различных температурах. Для обеспечения малости ошибки температурный диапазон должен быть достаточно широк - для точности 5% необходимо использовать диапазон шириной не менее 10°C, например - 10÷20°C, а измерение должно производиться с точностью ±0,01°C.
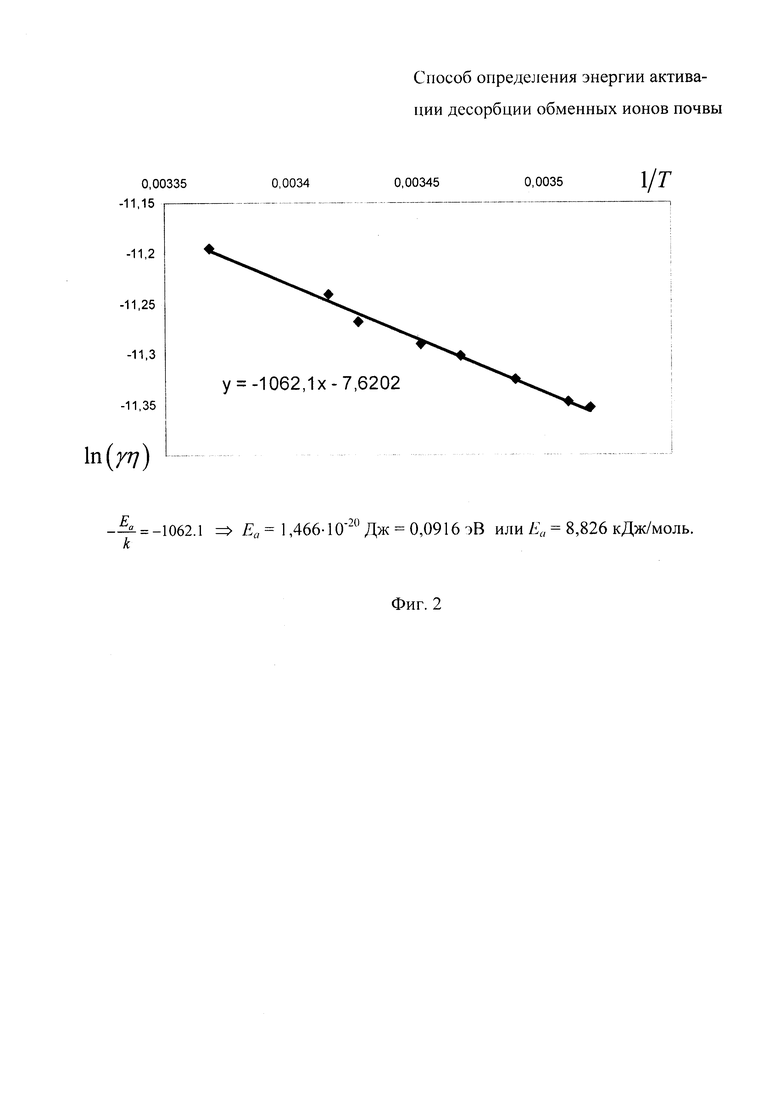
Определенная по формуле (12) энергия активации для рассматриваемого образца составила 0,092 эВ или 8,8 кДж/моль. Значение вязкости воды было использовано из справочной литературы [Физические величины: справочник / А.П. Бабичев, Н.А. Бабушкина, А.М. Братковский [и др.]; под ред. И.С. Григорьева, Е.Е. Мелихова. - М.: Энергоатомиздат, 1991. - 1223 с.].
Энергию активации обменных ионов составляет десятые доли эВ. Так, для катионобменных мембран Бадесса приводит данные от 0,24 эВ до 0,42 эВ. Значения, полученные для почв экспериментально Logsdon, составляют от 0,24 эВ до 0,44 эВ [Logsdon, S.D. Activation energies and temperature effects from electrical spectra of soil // Soil Sci. №173, - 2008, - p. 359-367]. Приведенные значения характеризуют суммарную энергию - требуемую для отрыва ионов от адсорбционных центров и необходимую для перемещения ионов в поровом растворе. Этим и объясняется различие полученных результатов. Энергия активации 0,092 эВ, полученная в приведенном примере, не возмущена поведением ионов в растворе, а относится только к отрыву ионов от адсорбционных центров и характеризует только их. Таким образом, предлагаемый способ определения энергии активации позволяет исключить влияние свойств растворителя (воды) на ее определение.
В данном случае энергия активации была вычислена по формуле (12), используя крайние температурные точки измерения. Однако возможно определять энергию активации, используя ряд точек зависимости электропроводности от температуры. Это позволяет уменьшить влияние случайных ошибок. Из формулы (11) следует, что

То есть в координатах 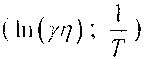 график будет представлять собой прямую с угловым коэффициентом
график будет представлять собой прямую с угловым коэффициентом 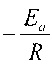 (см. фиг. 2), что позволяет графически определить энергию активации но наклону аппроксимационной прямой.
(см. фиг. 2), что позволяет графически определить энергию активации но наклону аппроксимационной прямой.
Приведенные приемы определения энергии активации дают одинаковые результаты. Расчет по двум точкам измерения проще, но требует большей точности при измерениях. Графический расчет по ряду точек требует большего числа измерений, но позволяет снизить погрешность, вызванную случайными ошибками.
Источники информации:
1. Method for measuring clay dispersion average binding free energy and adsorption free energy to cation: пат. CN 100510727 (C), Китай: МПК51 G01N 27/06 / Y. Wang, C. Li, D. Zhou, W. Wang, J. Jun; заявитель и патентообладатель Nanjing Institute Soil Science CAS - № CN 200613904820060324; заявл. 24.03.2006; опубл. 08.07.2009.
2. Глесстон С. Теория абсолютных скоростей реакций. Кинетика химических реакций, вязкость, диффузия и электрохимические явления / С. Глесстон, К. Лейдлер, Г. Эйринг; пер. с англ., под ред. А.Л. Баландина, Н.Д. Соколова. - М.: ИЛ. - 1948. - 583 с.
3. Пакшина С.М. Миграция солей в микропорах почвы. Автореферат дис. докт. биол. наук. - Новосибирск: СО АН СССР, - 1990.
4. Сивухин Д.В. Термодинамика и молекулярная физика. 3-е изд., испр. и доп. - М: Наука. Гл. ред. физ.-мат. лит., - 1990. - 592 с.
5. Балданова Д.М. Плазменно-гидродинамическая концепция состояния ионов в растворах электролитов в оценке некоторых свойств: монография / Д.М. Балданова, Б.Б. Танганов. - М.: Издательский дом Академии Естествознания, 2012. - 100 с.
6. Бадесса Толера Седа. Перенос многозарядных ионов через ионообменные мембраны при электродиализе: диссертация … кандидата химических наук: 02.00.05. - Воронеж, 2015. - 143 с.
7. Злочевская Р.И. Электроповерхностные явления в глинистых породах / Р.И. Злочевская, В.Л. Королев. - М., Изд-во МГУ, - 1988. - 177 с.
8. Физические величины: справочник / А.П. Бабичев, Н.А. Бабушкина, A.M. Братковский [и др.]; под ред. И.С. Григорьева, Е.Е. Мелихова. - М.: Энергоатомиздат, 1991. - 1223 с.
9. Logsdon, S.D. Activation energies and temperature effects from electrical spectra of soil // Soil Sci. №173, - 2008, - p. 359-367.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭКСПРЕСС-ОЦЕНКИ СОСТАВА ОБМЕННЫХ ИОНОВ ПОЧВЫ ПО ИХ ЭНЕРГИИ АКТИВАЦИИ ДЕСОРБЦИИ | 2016 |
|
RU2649074C2 |
| Способ определения электропроводности почв | 1982 |
|
SU993855A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНСТАНТЫ СКОРОСТИ ИЗМЕНЕНИЯ СОДЕРЖАНИЯ РАДИОНУКЛИДА В ПОЧВЕ | 1996 |
|
RU2103684C1 |
| Способ определения кажущейся энергии активации процессов гидратации в мелкозернистых цементных бетонах в начальный период твердения | 2024 |
|
RU2825857C1 |
| Способ оценки энергий активации диффузии ионов кислорода в филаменте мемристора | 2019 |
|
RU2729978C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДИФФУЗИОННЫХ КОНСТАНТ В ПОЛИКРИСТАЛЛИЧЕСКИХ ТЕЛАХ | 1999 |
|
RU2169914C2 |
| СПОСОБ ПРОГНОЗА ВЫБРОСООПАСНОСТИ УГОЛЬНОГО ПЛАСТА | 2016 |
|
RU2643868C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДИФФУЗИОННЫХ КОНСТАНТ В ПОЛИКРИСТАЛЛИЧЕСКИХ МАТЕРИАЛАХ | 2004 |
|
RU2260787C1 |
| СПОСОБ УМЕНЬШЕНИЯ НАМАГНИЧЕННОСТИ МАГНИТНЫХ ОКСИДНЫХ МАТЕРИАЛОВ | 1992 |
|
RU2077618C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПАРАМЕТРОВ МАТЕРИАЛОВ | 1995 |
|
RU2120613C1 |
Изобретение относится к сельскому хозяйству, а именно к методам определения свойств почвы. Предложен способ определения энергии активации десорбции обменных ионов почвы, заключающийся в ее определении по измеренным значениям электропроводности почвенного образца при различных температурах и фиксированной влажности. Расчет энергии активации десорбции обменных ионов производят одним из двух равноценных приемов:
- по угловому коэффициенту наклона аппроксимирующей прямой зависимости электропроводности от температуры, построенной в координатах 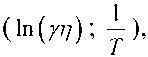 при этом угловой коэффициент прямой равен
при этом угловой коэффициент прямой равен 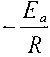 ;
;
- по электропроводности почвенного образца, измеренной при двух значениях температуры по формуле
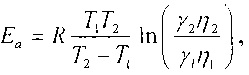
где Еа - энергии активации десорбции обменных ионов Дж/моль;
R - универсальная газовая постоянная Дж/(моль⋅K);
T1 и T2 - абсолютные температуры, при которых проводится измерение, K;
γ1 и γ2 - электропроводность почвенного образца при температурах;
T1 и T2 соответственно, См/м;
η1 и η2 - вязкость воды при температурах T1 и T2 соответственно, Па⋅с. Технический результат - повышение достоверности определения энергии активации десорбции обменных ионов почвы. 2 ил.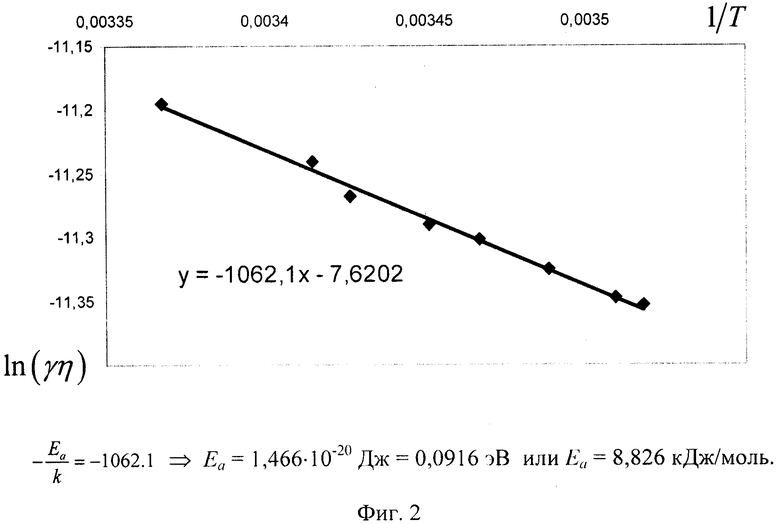
Способ определения энергии активации десорбции обменных ионов почвы, заключающийся в ее определении по измеренным значениям электропроводности почвенного образца при различных температурах и фиксированной влажности, отличающийся тем, что расчет энергии активации десорбции обменных ионов производят одним из двух равноценных приемов:
- по угловому коэффициенту наклона аппроксимирующей прямой зависимости электропроводности от температуры, построенной в координатах 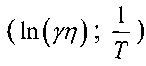 , при этом угловой коэффициент прямой равен -
, при этом угловой коэффициент прямой равен - 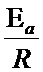
- по электропроводности почвенного образца, измеренной при двух значениях температуры по формуле
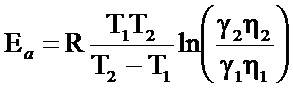
где Еа - энергии активации десорбции обменных ионов Дж/моль;
R - универсальная газовая постоянная Дж/(моль⋅K);
Т1 и Т2 - абсолютные температуры, при которых проводится измерение, K;
γ1 и γ2 - электропроводность почвенного образца при температурах Т1 и Т2 соответственно, См/м;
η1 и η2 - вязкость воды при температурах Т1 и T2 соответственно, Па⋅с.
| СПОСОБ ОПРЕДЕЛЕНИЯ ЭНЕРГИИ АКТИВАЦИИ ПРОЦЕССА ДЕСОРБЦИИ | 2011 |
|
RU2469299C1 |
| Способ определения содержания ионов водорастворимых солей в почве | 1987 |
|
SU1492275A1 |
| ФЕРАПОНТОВ Ю.А., ПУТИН С.Б., и др., "ИЗУЧЕНИЕ КИНЕТИКИ ТОПОХИМИЧЕСКИХ ПРОЦЕССОВ В НЕИЗОТЕРМИЧЕСКОМ РЕЖИМЕ ДЕРИВАТОГРАФИЧЕСКИМ МЕТОДОМ", ВЕСТНИК ТГГУ, 2009, ТОМ 15, НОМЕР 4, С.826-835 | |||
| CN 100510727 C, 08.07.2009 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ ГИДРОФОБИЗИРУЮЩИХ СВОЙСТВ ХИМРЕАГЕНТОВ | 2000 |
|
RU2183319C2 |
Авторы
Даты
2018-01-11—Публикация
2016-09-12—Подача