ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к предупреждению, лечению и диагностике нейродегенеративных заболеваний, в частности болезни Альцгеймера, и другого сходного заболевания. Более точно, данное изобретение относится к антителам с высокой аффинностью 10-7 М, предпочтительно 10-8 М, даже менее чем 10-9 М или менее чем 10-10 М или 10-11 М, селективным в отношении амилоидного бета-белка (Аβ) в его протофибриллярной конформации и относящимся к классу IgG и подклассам IgG1 или IgG4 или их комбинациям, сохраняющим высокое связывание Fc-рецептора и низкое связывание С1 (С1q), эффективным в клиренсе профибрилл Аβ и уменьшающим риск воспаления.
УРОВЕНЬ ТЕХНИКИ
Болезнь Альцгеймера (AD) является прогрессирующим и необратимым нейродегенеративным нарушением, вызывающим когнитивные, связанные с памятью и поведенческие нарушения. Она является наиболее обычной причиной деменции в популяции пожилого возраста, поражающей приблизительно 5% популяции с возрастом 65 лет и 20% с возрастом 80 лет. AD характеризуется незаметно подкрадывающимся появлением и прогрессирующей деградацией множественных когнитивных функций. Невропатология включает в себя как внеклеточные, так и внутриклеточные аргирофильные белковые отложения. Внеклеточные отложения, называемые невритными бляшками, в основном состоят из амилоидного бета-белка (Aβ), окруженного дистрофическими невритами (набухшими, искаженными выступами нейронов). Aβ в этих внеклеточных отложениях могут окрашиваться определенными красителями, например, Конго Красным, и обнаруживают фибриллярную ультраструктуру. Эти характеристики, приобретаемые Aβ в его фибриллярной структуре в невритных бляшках, являются определением общего термина «амилоид». Это классическое патологическое изменение AD является нейрофибриллярным клубком (NFT), который состоит из волокнистых структур, называемых спаренными спиральными филаментами (PHFs), составленными из скрученных тяжей гиперфосфорилированного связанного с микротрубочками белка тау. Часто встречающиеся невритные бляшки и отложения нейрофибриллярных клубков в головном мозге являются диагностическими критериями для AD при проведении аутопсии. Головной мозг при AD также проявляет макроскопическую атрофию головного мозга, потерю нервных клеток, местное воспаление (микроглиоз и астроцитоз) и часто церебральную амилоидную ангиопатию (CAA) в стенках сосудов головного мозга.
Две формы Aβ-пептидов, Aβ40 и Aβ42, являются доминантными разновидностями в невритных бляшках AD, тогда как Aβ40 является важной разновидностью в цереброваскулярном амилоиде, связанным с AD. Ферментативные активности позволяют Aβ непрерывно образовываться из большего белка, называемого амилоидным белком-предшественником (APP) как в здоровых, так и в пораженных AD субъектах во всех клетках тела. Два основных события процессинга APP посредством активностей β- и γ-секретаз делает возможным образование Aβ, тогда как третий фермент, называемый α-секретазой, предотвращает генерирование Aβ расщеплением внутри последовательности Aβ (Selkoe, 1994; Ester 2001; US5604102). Aβ42 является пептидом из сорока двух аминокислот, т.е. на две аминокислоты более длинным на С-конце в сравнении с Aβ40. Aβ42 является более гидрофобным и действительно более легко агрегируется в более крупные структуры Aβ-пептидов (Jarret 1993), такие как Aβ-димеры, Aβ-тримеры, Aβ-тетрамеры, Aβ-олигомеры, Aβ-протофибриллы или Aβ-фибриллы. Aβ-фибриллы являются гидрофобными и нерастворимыми, тогда как другие структуры являются менее гидрофобными и растворимыми. Все эти более высокомолекулярные пептиды Aβ индивидуально определяются на основе из биофизического и структурного вида, например, в электронной микроскопии, и их биохимических характеристик, например, анализом при помощи вытеснительной хроматографии/вестерн-блоттинга. Эти пептиды Aβ, в частности, Aβ42, будут постепенно собираться в различные более высокомолеклярные структуры Aβ на протяжении продолжительности жизни. AD, которая является в сильной степени зависимым от возраста нарушением, будет встречаться раньше в жизни, если этот процесс сборки происходит более быстро. Это является центральной частью «гипотезы амилоидного каскада» AD, которая заявляет, что процессинг APP, уровни Aβ42 и их сборка в более высокомолекулярные структуры являются центральной причиной AD. Вся другая невропатология головного мозга больных AD и симптомы AD, такие как деменция, каким-то образом вызываются Aβ или его собранными формами.
Aβ может существовать в различных длинах, т.е. 1-39, 1-40, 1-42 и 1-43, и размерах фрагментов, т.е. 1-28 и 25-35. Укорочения могут иметь место на N-конце этого пептида. Все эти пептиды могут агрегироваться и образовывать растворимые промежуточные продукты и нерастворимые фибриллы, причем каждая молекулярная форма имеет уникальную структурную конформацию и биофизические свойства. Например, мономерный Aβl-42 является растворимым и нетоксичным пептидом с длиной 42 аминокислоты, который, как предполагается, участвует в нормальной функции синапса. При определенных условиях, Aβ1-42 может агрегироваться в димеры, тримеры, тетрамеры, пентамеры до 12-мерных и более высокоолигомерных форм, все из которых имеют различные физико-химические свойства, такие как молекулярный размер, ЭМ-структура и молекулярная форма в AFM (микроскопии на основе атомных сил). Примером более высокомолекулярной растворимой олигомерной формы Aβ является протофибрилла (Walsh 1997), которая имеет среднюю молекулярную массу >100 кДа и криволинейную структуру 4-11 нм в диаметре и <200 нм в длину. Недавно было продемонстрировано, что растворимые олигомерные Aβ-пептиды, такие как протофибриллы Aβ, нарушают долгосрочное потенциирование (LTP), показатель синаптической пластичности, который, как предполагается, отражает формирование памяти в гиппокампе (Walsh 2002). Кроме того, олигомерные Аβ-пептиды Arctic проявляют гораздо большее ингибирующее действие, чем wtAβ, на LTP в головном мозгу, по-видимому, вследствие их сильной склонности к образованию протофибрилл Aβ (Klyubin 2003).
Имеются также другие растворимые олигомерные формы, описанные в литературе, которые заметно отличаются от протофибрилл. Одной такой олигомерной формой является ADDL (полученный из амилоида диффундируемый лиганд) (Lambert 1998). AFM-анализ ADDL выявил преимущественно малые глобулярные виды 4,7-6,2 нм вдоль z-оси с молекулярными массами 17-42 кДа (Stine 1996). Другая форма названа ASPD (Амилоидсфероиды) (Hoshi 2003). ASPD являются сферическими олигомерами Aβ1-40. Исследования токсичности показали, что сферические ASPD >10 нм были более токсичными, чем более низкомолекулярные формы (Hoshi 2003). Эта идея получила поддержку из недавнего открытия мутации АРР Arctic (E693), которая вызывает раннее появление AD (US 2002/0162129 Al; Nilsberth et al., 2001). Эта мутация локализована внутри последовательности пептида Aβ. Носители мутации будут посредством этого генерировать варианты пептидов Aβ, например, Arctic Aβ40 и Arctic Aβ42. Как Arctic Aβ40, так и Arctic Aβ42 будут гораздо более легко собираемыми в более высокомолекулярные структуры, т.е. протофибриллы. Таким образом, патогенный механизм мутации Arctic предполагает, что эти растворимые, высокомолекулярные протофибриллы вызывают AD и содержит специфический уникальный эпитоп, т.е. “эпитоп болезни AD”.
В головном мозге в случае болезни Альцгеймера (AD) внеклеточные амилоидные бляшки обычно обнаруживают в паренхиме и стенках сосудов. Эти бляшки состоят из амилоида (гидрофобных и самоагрегирующихся пептидов Aβ38-43 с длиной 38-43 аминокислот, которые постепенно полимеризуются перед отложением бляшек). Было сделано предположение, что растворимые олигомерные разновидности Aβ являются лучшими коррелятами заболевания, чем сами амилоидные бляшки (McLean et al., 1999; Nаslund et al., 2000). Было показано, что среди этих префибриллярных промежуточных разновидностей Aβ олигомерные формы вызывают вредные биологические эффекты как in vitro, так и in vivo (Walsh et al., 2002) и, следовательно, могут играть центральную роль в патогенезе заболевания. Известно несколько разновидностей олигомерных Aβ с различными молекулярными размерами. Важно, что конформации мономерных, олигомерных и фибриллярных форм Aβ являются различными и могут быть мишенями конформационно селективных антител. Идентичность основного патогена Aβ не выяснена, хотя некоторые данные предполагают, что высокомолекулярные олигомеры Aβ являются особенно нейротоксичными (Hoshi et al., 2003).
Были описаны патогенные мутации гена амилоидного белка-предшественника (АРР), вызывающие раннее появление AD. Одна из них, мутация АРР Swedish (Mullan et al., 1992), вызывает увеличенные уровни Aβ. Было обнаружено, что другая мутация АРР Arctic (E693G), расположенная в домене Aβ, усиливает образование протофибрилл, больших олигомеров Aβ, что предполагает, что эти промежуточные продукты Aβ являются особенно патогенными (US 2002/0162129 Al; Nilsberth et al., 2001). Идентификация мутации АРР и выяснение токсических действий в отношении протофибрилл Aβ заставили сосредоточить внимание на олигомерах Aβ в патогенезе AD.
Активная иммунизация в качестве терапевтической стратегии для болезни Альцгеймера была впервые сообщена Schenk et al. 1999. Мишенью этой стратегии иммунизации была фибриллярная форма Aβ, обнаруженная в бляшках болезни Альцгеймера. Недавнее исследование клинической фазы I/II активной вакцинации Aβ, использующей фибриллизированный Aβ в качестве вакцины (AN-1792), должно было быть приостановлено вследствие менингоэнцефалита в небольшом количестве пациентов (Bayer et al., 2005). Побочные действия, наблюдаемые в этом исследовании, были, по-видимому, вызваны анти-Aβ-антителами, реагирующими против фибриллярного амилоида в стенках сосудов. Этот фибриллярный амилоид в САА находится в тесной близости с гематоэнцефалическим барьером (ВВВ), и, следовательно, реакция антиген-антитело могла генерировать повреждение ВВВ, приводя к инфильтрации Т-лимфоцитов в ЦНС (Pfeifer et al., 2002; Racke et al., 2005). Кроме того, только небольшая часть участвующих пациентов обнаруживала иммунную реакцию на эту вакцину Aβ. Хотя это исследование было закончено преждевременно, оно позволяет предполагать, что активная иммунизация Aβ может быть полезной только для субпопуляции пациентов с AD.
Были описаны моноклональные антитела, селективные в отношении протофибрилл Aβ человека (US 2002/0162129 Al). Способ генерирования высокоочищенных и стабильных протофибрилл Aβ человека включает в себя использование синтетических пептидов Aβ с мутацией Arctic (Glu22Gly). Эта мутация облегчает иммунизацию и скрининг гибридом на селективные в отношении протофибрилл Aβ антитела. Важно, что эти антитела связывают как протофибриллы Aβ дикого типа, так и протофибриллы Aβ-Arc (PCT/SE 2005/000993).
Были описаны антитела, которые являются селективными в отношении других конформаций Aβ, таких как фибриллы Aβ (O'Nuallain 2002), мицеллярный Aβ (Kayed 2003), ADDL (Lambert 2001). Однако ни одни из них не являются селективными в отношении протофибрилл Aβ.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение относится к улучшенным антителам, т.е. имеющим высокую аффинность (менее 10-7 М), селективным в отношении протофибрилл Aβ антителам класса IgG и подкласса IgG1 или IgG2 или их комбинации, или их мутациям, с уменьшенным риском воспаления, для улучшенной профилактики, лечения и диагностики болезни Альцгеймера, синдрома Дауна или других нейродегенеративных нарушений. Указанные антитела были разработаны классическими гибридомными способами и генной инженерией антител.
Это изобретение раскрывает консенсусную аминокислотную последовательность районов CDR1-3 на цепях VL и VH из антител, которые селективно связывают олигомерные формы Aβ, т.е. профибриллы Aβ, составляющие “эпитоп болезни Альцгеймера”, объединенную с модификациями Fc-района для уменьшения риска активации комплемента и воспаления.
Константная область антитела имеет многие важные функции, в особенности связывание рецепторов Fc и фактора комплемента С1q. Последнюю функцию инактивировали во избежание воспалительных реакций.
Таким образом, этот тип высокоаффинных селективных в отношении протофибрилл антител имеет явные преимущества в сравнении с другими известными иммунотерапевтическими способами лечения:
1) действует на заболевание, объединяясь с протофибриллами Aβ с высокой аффинностью,
2) уменьшает риск воспалительных побочных эффектов, т.е. менингоэнцефалита, вследствие низкого связывания или отсутствия связывания с фактором комплемента С1q,
3) высокоаффинное антитело уменьшает клиническую дозу, необходимую для эффективного лечения,
4) обеспечивает способ с точным дозированием,
5) меньшее связывание антитела с фибриллами Aβ в стенке кровеносных сосудов, т.е. САА, уменьшающее риск в отношении воспалительных побочных эффектов,
6) меньшее количество антител связываются в периферии, следовательно, большее количество антител будут пересекать гематоэнцефалический барьер и будут доступными для связывания и элиминации олигомерных форм Aβ в головном мозге.
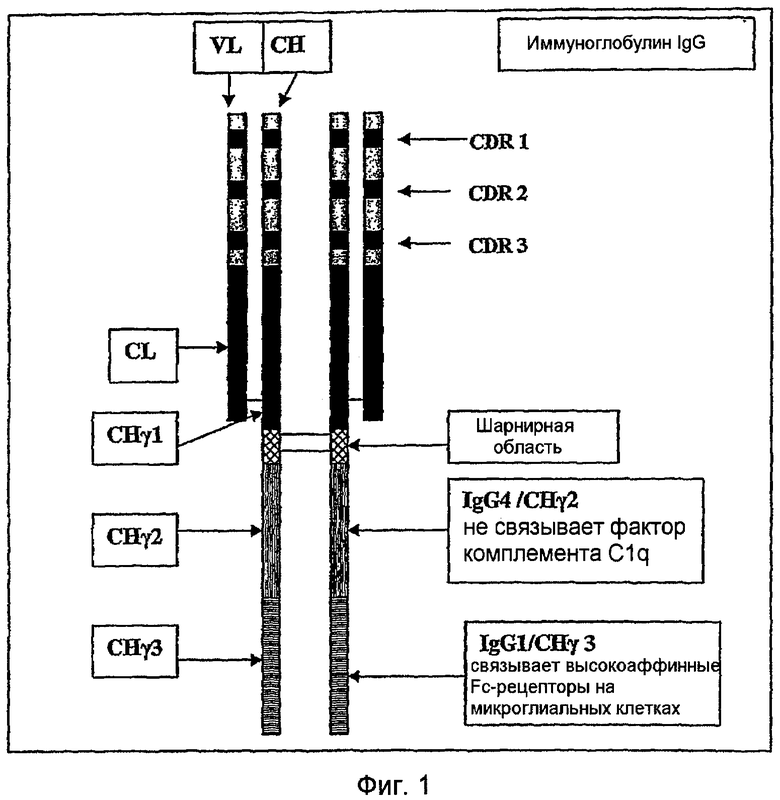
Одним аспектом этого изобретения является раскрытие консенсусной аминокислотной последовательности антитела районов CDR, которые связывают протофибриллы Aβ дикого типа человека (пример 1). Это раскрытие определяет сайты связывания (районы CDR), которые придают высокую аффинность и высокую селективность в отношении протофибрилл Aβ человека дикого типа, для использования в качестве терапевтических средств или диагностических средств. Основная структура молекулы иммуноглобулина (IgG) содержит две идентичные легкие цепи и две идентичные тяжелые цепи, связанные вместе дисульфидными мостиками (фигура 1). Легкая цепь, которая является либо лямбда, либо каппа, имеет вариабельную область (VL) и константную область (CL) из приблизительно 110 аминокислотных остатков, каждая. Тяжелая цепь имеет вариабельную область (VH) из приблизительно 110 аминокислотных остатков, но гораздо большую константную область (CH) из 300-400 аминокислотных остатков, содержащую районы или домены CHγl, CHγ2 и CHγ3.
Константная область (Fc) активирует систему комплемента и связывается с рецептором Fc на макрофагах, микроглии и нейтрофилах, которые поглощают и разрушают инфицирующие микроорганизмы или чужеродные/неаутологичные антигены. Эта функция имеет особенно важное значение, так как она является частью терапевтического принципа этого антитела, т.е. опосредованного рецептором Fc микроглиального фагоцитоза и клиренса протофибрилл Aβ. Другими опосредуемыми антителом механизмами клиренса являются также оперативные, т.е. противоагрегирующие свойства Aβ-антител и клиренс протофибрилл Aβ в периферии, в соответствии с гипотезой стока. Вариабельная область тяжелой и легкой цепей содержит 3 гипервариабельных района, называемых определяющими комплементарность районами или CDR. Эти районы CDR являются короткими участками с длиной приблизительно 13-23 аминокислот, расположенными в областях VL и VH. Шесть районов CDR на одном «плече» антитела образуют «карман», который связывает антиген. Фигура 1 показывает эту основную структуру иммуноглобулина IgG и его субдоменов.
Другой аспект этого изобретения относится к селективным в отношении протофибрилл антителам высокой аффинности. Описаны аффинности в диапазоне 10-7 М, предпочтительно 10-8 М, даже менее чем 10-9 М, менее чем 10-10 М, или менее чем 10-11 М в отношении протофибрилл (пример 2). Эти антитела имеют то преимущество, что они могут вводиться при более низких дозах в сравнении с антителами с аффинностями в диапазоне 10-6 М. Это имеет существенное клиническое преимущество, заключающееся в том, что эти высокоаффинные антитела, которые вводят инъекцией, могут предоставляться подкожно, так как только низкое количество этого антитела требуется для достижения эффективности. Способы введения не ограничиваются подкожными инъекциями. Кроме того, более низкие дозы, необходимые для эффективности, будут уменьшать расходы на покупку материалов для получения этого антитела.
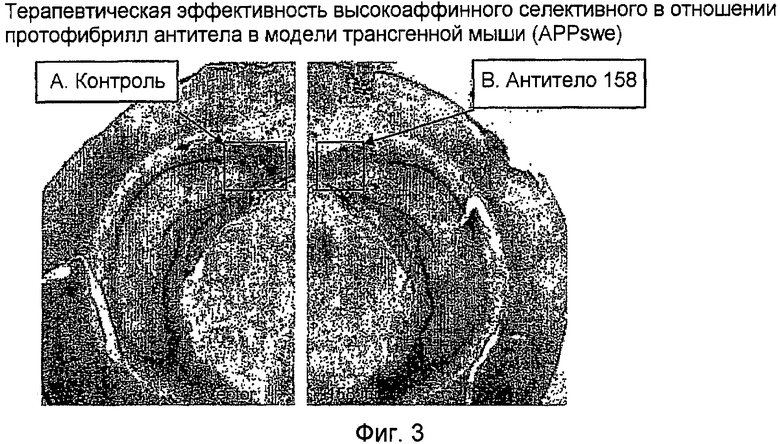
Другой аспект этого изобретения заключается в том, что эти антитела являются антителами класса IgG, подходящего для терапевтического использования, так как IgG может проходить через гематоэнцефалический барьер. Клиренс протофибрилл Aβ в паренхиме головного мозга достигается опосредованным Fc-рецептором фагоцитозом клетками микроглии. По-видимому, действуют также и другие механизмы клиренса анти-Aβ-антител. Этот клиренс растворимых протофибрилл Aβ является центральным механизмом этого лечения. Протофибриллы Aβ считаются высоко нейротоксичными, запускающими процесс заболевания и управляющими процессом заболевания. Клиренс протофибрилл Aβ в головном мозге имеет существенное клиническое значение. Кроме клиренса протофибрилл Aβ, другие олигомерные формы Aβ, в том числе фибриллы Aβ, будут снижаться непосредственно посредством удаления протофибрилл Aβ, так как различные агрегированные формы Aβ, т.е. димеры, тримеры, тетрамеры и более высокие олигомерные формы, в том числе протофибриллы и фибриллы, находятся в равновесии. Пример уменьшения бляшек, которые содержат фибриллы Aβ, показан в модели болезни Альцгеймера трансгенной мыши (APPswe) после 72-часовой обработки высокоаффинным селективным в отношении протофибрилл антителом (mAb 158) (пример 3). Таким образом, клиренс протофибрилл Aβ указанным антителом будет также выгодным для опосредованного уменьшения других агрегированных или олигомерных форм Aβ.
Еще одним аспектом этого изобретения является высокоаффинное селективное в отношении протофибрилл человека антитело подкласса IgG1, которое имеет высокую аффинность в отношении рецепторов FcγRI человека, присутствующих на микроглиальных клетках в головном мозге. Высокоаффинное антитело будет приводить к эффективному клиренсу протофибрилл Aβ, что будет иметь существенную терапевтическую пользу. Таким образом, эти антитела будут обнаруживать клиренс протофибрилл Aβ как в ЦНС, так и в периферии в сравнении с другими иммунотерапевтическими стратегиями, такими как вакцинация или лечение моноклональными антителами с использованием других моноклональных антител подкласса IgG1, мишенями которых являются другие формы Aβ. Важно, что это лечение будет эффективным рано в процессе этого заболевания, когда токсичные растворимые разновидности Aβ, такие как протофибриллы Aβ, присутствуют при повышенных уровнях, но также и позднее в процессе этого заболевания. Повышенные уровни олигомерных форм Aβ были описаны в трансгенной мышиной модели, обнаруживающей мутации Swedish и Arctic APP swearc (Lord A. et al. 2006).
Еще одним аспектом этого изобретения является то, что высокоаффинные селективные в отношении протофибрилл Aβ антитела могут снижать или ингибировать агрегацию Aβ, уменьшая посредством этого уровни растворимых олигомерных форм Aβ в головном мозге.
Кроме того, другим аспектом этого изобретения является то, что высокоаффинные селективные в отношении протофибрилл Aβ антитела могут связывать олигомерные формы Aβ, т.е. протофибриллы Aβ, также вне ЦНС, смещая посредством этого равновесие указанных форм Aβ через гематоэнцефалический барьер таким образом, что уровни в ЦНС указанных форм Aβ снижаются (дренаж).
Как обсуждалось выше, клиническое исследование Elan с использованием вакцины Aβ (AN-1792), селективной в отношении фибрилл Aβ, для лечения пациентов с болезнью Альцгеймера приводило к побочному действию, т.е. менингоэнцефалиту, в 6% этих случаев. Стратегия нацеливания на фибриллы Aβ, которые являются сердцевиной амилоидных бляшек, присутствующих в паренхиме головного мозга, но, что является важным, также в стенках кровеносных сосудов, приводила к тяжелым побочным эффектам. Эти побочные эффекты были, наиболее вероятно, вызваны связыванием этих антител с САА (церебральной амилоидной ангиопатией) в стенках сосудов головного мозга, начинающим воспалительный процесс. Эта существенная клиническая проблема устраняется улучшенными высокоаффинными селективными в отношении протофибрилл антителами с уменьшенной активностью активации комплемента. Эти антитела будут сохранять высокую эффективность клиренса протофибрилл Aβ, уменьшая риск побочных эффектов, т.е. менингоэнцефалита.
Другой аспект этого изобретения заключается в том, что высокоаффинные селективные в отношении протофибрилл Aβ антитела имеют низкое связывание фибрилл Aβ (см. пример 2), уменьшая риск побочных действий, но меньшее связывание с фибриллами Aβ, присутствующими в САА.
Еще один аспект этого изобретения заключается в том, что конструируют высокоаффинные селективные в отношении протофибрилл Aβ IgG-антитела для уменьшения связывания фактора комплемента С1q с доменом CH2 IgG1 и уменьшения активации комплемента и риска воспаления. Эта модификация может выполняться несколькими различными путями. Одним путем является получение химерного антитела, где домен CHγ2 константной области IgG1 был удален и заменен соответствующим доменом из IgG4 или частью домена, которая придает способность связывания С1q. Хорошо установлено, что IgG4 не связывает С1q и, следовательно, не активирует каскад комплемента. Для достижения этого константную область тяжелой цепи (СН) конструируют таким образом, чтобы объединить высокоаффинный домен Fc-рецептора (CHγ3) на IgG1 с доменом (CHγ2) IgG4, который не может связываться с фактором комплемента С1q. Это новое антитело, содержащее химерную константную область тяжелой цепи (IgG1:CHγ1, CHγ2:IgG4, CHγ3:IgGl), будет иметь важные свойства как эффективного клиренса протофибрилл Aβ через опосредованный Fc-рецептором фагоцитоз, так и уменшенный риск побочных действий, т.е. воспаления, такого как менингоэнцефалит.
Еще одним путем уменьшения риска воспаления является изменение структуры олигосахаридов этого антитела, которая будет уменьшать связывание фактора С1q и активацию комплемента. Были описаны 30 различных структур комплексных биантенных олигосахаридов при Asn-297 в IgG1 человека. Считается, что СН2-ассоциированные углеводы вызывают конформационное изменение в «шарнирной» области антитела, уменьшая эффективности взаимодействия с эффекторными молекулами и потерю функции активации комплемента и связывания С1q.
Эта модификация высокоаффинного селективного в отношении протофибрилл Aβ человека антитела сайт-направленным мутагенезом Asn-297 в любую другую аминокислоту будет генерировать антитело с сохраненным связыванием Fc-рецептора с меньшим связыванием С1q и, следовательно, уменьшенным риском воспаления, в частности, в гематоэнцефалическом барьере. Альтернативой модификации гликозилирования на этом антителе является экспрессия этого антитела в клеточном типе, в котором был инактивирован фермент N-aцетилглюкозаминилтрансфераза I. Это даст антитело с измененной углеводной структурой при Asn-297. Образуется структура Man5GlcNAc2, но не только эта структура. Эта углеводная модификация будет уменьшать связывание фактора С1q и ингибировать воспаление (Wright at al. 1998). Альтернативно, гликозилированные селективные в отношении протофибрилл антитела могут быть получены культивированием клеток, экспрессирующих антитела, в присутствии туникамицина, который ингибирует гликозилирование. Эти антитела будут иметь измененную активность активации комплемента, а также измененную функцию Fc-рецептора (Leatherbarrow el al. 1985). Скрининг клонов, экспрессирующих антитела с низкой активацией комплемента и высоким связыванием Fc-рецептора, будет генерировать селективные в отношении протофибрилл антитела, которые обнаруживают высокий Fc-опосредованный клиренс профибрилл Aβ и низкое связывание С1q.
Еще одним аспектом этого изобретения является высокоаффинное селективное в отношении протофибрилл антитело человека, подкласса IgG1, где был модифицирован сайт связывания фактора С1q, т.е. Pro33l>Ser331 (Xu et al. 1994) таким образом, чтобы уменьшить или ингибировать связывание фактора комплемента С1q, для лечения или предупреждения AD. Остаток пролина в положении 331 IgG1 человека может быть изменен на треонин или глицин или любую другую полярную аминокислоту. Эта модификация может быть получена стандартными способами молекулярной биологии, такими как сайт-направленный мутагенез или делеции ДНК.
Другим аспектом этого изобретения является применение высокоаффинных селективных в отношении протофибрилл Aβ человека антител для специфического определения уровней протофибрилл в тканях человека, в частности в цереброспинальной жидкости, крови, моче или слюне, в качестве диагностического инструмента или биомаркера в отношении болезни Альцгеймера. Уровни протофибрилл Aβ человека в CSF или крови являются, по-видимому, отличающимися в сравнении с соответствующей пожилой контрольной группой, не имеющей болезни Альцгеймера. Человек с развивающейся болезнью Альцгеймера, по-видимому, имеет увеличенные уровни протофибрилл в CSF или в крови. Таким образом, посредством определения уровней протофибрилл Aβ в CSF или крови может быть выполнена ранняя диагностика этого заболевания. Это может быть достигнуто с новыми высокоаффинными селективными в отношении протофибрилл Aβ антителами в комбинации со способом сэндвич-ELISA (пример 2А), где протофибриллы Aβ определяли до уровня 10 пМ. Интерференция других форм Aβ, таких как фибриллы Aβ, мономеры Aβ и фрагменты Aβ (1-16; 17-40) в этом анализе, составляет 10% или менее.
Это изобретение дополнительно относится к применению высокоаффинных специфических в отношении протофибрилл антител для определений протофибрилл Aβ в тканях человека и животных, таких как, например, цереброспинальная жидкость, кровь, сыворотка, моча и ткань головного мозга, но не только в этих тканях, обеспечивающему возможный диагностический способ для болезни Альцгеймера. Подходящими способами для анализа протофибрилл в этих тканях, а также в культурах клеток, использующими антитело против протофибрилл Aβ, являются иммуноанализы, такие как ELISA, RIA, вестерн-блоттинг или дот-блоттинг. Этот способ мог бы применяться для прослеживания эффективности лечения (уменьшения протофибрилл) в клинических исследованиях и быть пригодным в качестве диагностического теста на болезнь Альцгеймера или синдрома Дауна.
Поскольку уровни протофибрилл Aβ являются очень низкими в CSF и крови, в диагностическом тесте на основе способа ELISA необходимо высокоаффинное селективное в отношении протофибрилл антитело для возможности измерения очень низких уровней протофибрилл Aβ. Другие сверхчувствительные способы, такие как лигирование на основе близости (пример 4) (Gullberg 2004) или аналогичные системы амплификации или Biacore или сходные способы, могут быть использованы для увеличения чувствительности. Способ лигирования на основе близости основан на обнаружении того, что различные антитела, индуцированные против различных эпитопов на аналите (в этом случае на белке), могут связываться вблизи каждого из них на указанном аналите. Если указанные различные антитела конъюгируют с олигонуклеотидами, расстояние между указанными олигонуклеотидами будет достаточно коротким для того, чтобы олигонуклеотид-коннектор, при помощи компонентов лигирования, образовал мостик между этими олигонуклеотидами. Добавляют также компоненты амплификации, после чего может выполняться ОТ-ПЦР. По этому принципу генерируют амплифицируемую ДНК-последовательность, отражающую идентичность и количество белка-мишени. Этот способ позволяет получать усиленную реакцию сигнала и, следовательно, детектировать более низкие концентрации аналита.
Авторы данного изобретения неожиданно обнаружили, что модифицированный способ лигирования на основе близости может быть также использован с их специфическими в отношении протофибрилл Aβ антителами для детектирования низких концентраций более крупных структур Aβ-пептида, т.е. протофибрилл Aβ, но не мономеров Aβ. Они обнаружили, что Aβ-пептиды, в конформации протофибрилл, обнаруживают структуру (повторяющиеся звенья), которая делает возможным для двух антител, в соответствии с данным изобретением, достаточное связывание поблизости друг от друга на этой протофибрилле. Если указанные антитела конъюгируют с олигонуклеотидами, указанные олигонуклеотиды могут быть связаны мостиками с использованием олигонуклеотида-коннектора. Выполняют ПЦР с использованием компонентов амплификации. По этому принципу генерируют амплифицируемую ДНК-последовательность, отражающую идентичность и количество протофибриллы-мишени (см. фиг. 4А).
Лигирование на основе близости или версия этого способа, называемая «катящимся кольцом», является высокочувствительным способом и особенно хорошо подходящим для детектирования полимерных структур с повторяющимися последовательностями, таких как протофибриллы Aβ, при использовании для диагностики болезни Альцгеймера и других нейродегенеративных нарушений.
Это изобретение относится дополнительно к применению высокоаффинных специфических в отношении протофибрилл антител в томографии для детектирования, определения местоположения и количественного определения протофибрилл Aβ в тканях человека и животных. Это антитело может быть помечено радиоактивным лигандом, таким как I131, C14, H3 или галлий68, но без ограничения этими радиоактивными изотопами, для целей детектирования. Этот способ будет пригоден в качестве диагностического инструмента для болезни Альцгеймера или синдрома Дауна.
Еще одним аспектом этого изобретения является получение разновидностей антител, специфических для применения в ветеринарии. Эти диагностические способы описаны также для применения в ветеринарии.
Другим аспектом этого изобретения является гуманизация указанных антител во избежание побочного действия, т.е. во избежание иммунной реакции против указанных антител в людях при использовании в качестве терапевтического или диагностического агента.
Другим аспектом является приготовление этого антитела в физиологическом буфере, например, ЗФР, подходящем для введения людям и животным. Этот содержащий антитело продукт может быть лиофилизирован для лучшей стабильности. Лиофилизированная готовая форма может содержать эксципиент, например, маннит, но не ограничивающийся маннитом, для стабилизации этого продукта после лиофилизации.
Этот продукт антитела может содержать антибактериальный агент.
Антитела или фрагменты в соответствии с этим изобретением могут иметь делеции, замены и инсерции аминокислот в указанных CDR-районах и/или их каркасе. Встроенными или замененными аминокислотами могут быть также производные аминокислот при условии, что аффинность и специфичность этого антитела все еще является интактной.
ПРИМЕРЫ
Следующие примеры приведены для иллюстрации и не предназначены для ограничения этого изобретения этими конкретными примерами.
Пример 1
Селективные в отношении протофибрилл Aβ моноклональные антитела дикого типа человека клонировали и секвенировали. Аминокислотная последовательность вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL) показаны в таблице 1. Положения CDR-районов 1-3 подчеркнуты и показаны также в таблицах 2 и 3. Аминокислотные последовательности этих CDR-районов образуют структурную основу для связывания протофибрилл Aβ дикого типа, составляющую «эпитоп болезни Альцгеймера».
Аминокислотная последовательность CDR-районов 1-3 цепей VL и VH для высокоаффинного специфического в отношении профибрилл антитела BA9/158 показана в таблицах 1, 2 и 3. Данные секвенирования других селективных в отношении протофибрилл антител (BA2, BA3, BA4 и BA7) обеспечивают альтернативные аминокислотные последовательности CDR-районов, но не ограничиваются ими. Объединенные аминокислотные последовательности районов CDR1-3 цепей VH и VL создают молекулярный «карман», который связывает протофибриллы Aβ дикого типа человека с высокой аффинностью и специфичностью. Этот «карман» образует структурную основу для «эпитопа болезни Альцгеймера». Вариации в длине аминокислотных последовательностей CDR, наблюдаемые как в цепи VH, так и в цепи VL, являются совместимыми с протофибриллами Aβ человека (таблицы 2 и 3). Более короткий CDR-район обеспечивает более ограниченную трехмерную структуру кармана связывания этого антитела, в то время как более длинный является более гибким.
Авторы изобретения заявляют как последовательности CDR, показанные в таблицах 1, 2 и 3, так и аминокислотные последовательности в областях «мышиного каркаса» цепей VH и VL, т.е. вне CDR-районов, а также каркасных областях VL и VH человека для специфических в отношении протофибрилл антител, показанных в таблице 4 и 5, но не ограничивающиеся ими.
Аминокислотная последовательность каркасного района областей VL и VH 1-3 VL- и VH-цепей из высокоаффинного специфического в отношении протофибрилл антитела BA9/158 показана в таблице 4 и 5.
Другие аминокислотные замены в CDR-районах, чем те, которые показаны в таблицах 1, 2 и 3, являются совместимыми с высокой аффинностью и высокой специфичностью связывания с протофибриллами Aβ дикого типа человека. Если полярная аминокислота присутствует в конкретном положении в CDR-районе, эта конкретная аминокислота может быть заменена другой полярной аминокислотой с сохраненной или улучшенной высокой аффинностью и специфичностью связывания с протофибриллами Aβ. Подобным образом, если неполярная или отрицательно или положительно заряженная аминокислота присутствует в определенном положении, эта аминокислота может быть заменена сходной аминокислотой из той же самой группы. Конкретную аминокислоту или конкретные аминокислоты заменяют также в любом положении в CDR-районах функциональными эквивалентами, которые придают аналогичную функцию и структуру этому антителу.
Пример 2. Характеристика высокоаффинного селективного в отношении протофибрилл Aβ дикого типа человека моноклонального антитела при помощи ELISA
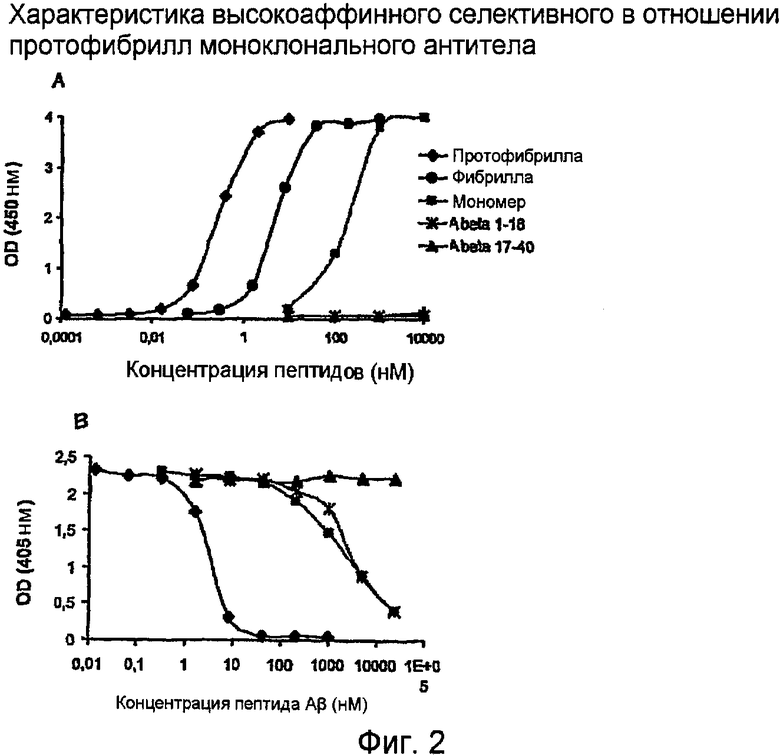
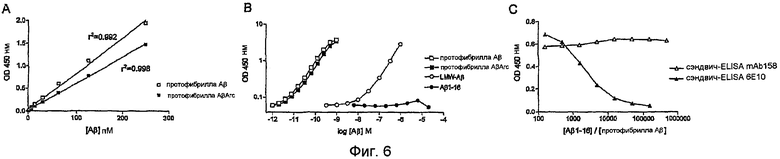
Пример 2 показывает высокоаффинное селективное в отношении протофибрилл антитело, которое перекрестно реагирует в 200-100 раз менее с мономерами Aβ и менее, чем в 40 раз, с фибриллами Aβ, как измерено сэндвич-ELISA (фиг. 2,А). На основании экспериментов с конкурентным ELISA это антитело имеет высокую аффинность в отношении протофибрилл дикого типа AB42 человека, но только очень слабую аффинность в отношении N-концевой части пептида Aβ и мономеров Aβ. Связывания не наблюдали с С-концевым фрагментом Aβ (фиг. 2,B). Кроме того, это антитело не реагирует перекрестно с другими типами амилоидов, такими как медин или транстиретин. Кроме того, это антитело не узнает АРР человека, обильный предшественник Aβ.
На фигуре 2,А показан сэндвич-ELISA. Антитело 158 было нанесено в виде покрытия в лунки и затем различные формы Aβ добавляли в лунки в увеличивающихся концентрациях. Измерение связанных форм A,β выполняли добавлением биотинилированного mAb 158 и HRP-меченого стрептавидина. Развитие окраски измеряли в соответствии с процедурой, рекомендованной изготовителем.
На фигуре 2,В показан конкурентный ELISA. Планшет ELISA покрывали протофибриллами Aβ человека. Затем антитело 158 инкубировали с увеличивающимися количествами различных форм Aβ (конкуренция). Инкубационную смесь добавляли в лунки этого микротитрационного планшета и свободному антителу давали связываться с иммобилизованными протофибриллами в этих лунках. Связанное антитело 158 измеряли вторым антителом с использованием стандартных процедур.
Пример 3
Эффективность высокоаффинного селективного в отношении протофибрилл Aβ антитела определяли в трансгенной мышиной модели болезни Альцгеймера (APPswe) посредством острой внутричерепной инъекции. Трансгенные мыши, используемые для оценки эффективности, экспрессировали АРР человека с мутацией Swedish (APPSwe). В этом примере антитела инъецировали непосредственно в богатые бляшками участки паренхимы головного мозга и действия на неврологию оценивали спустя 72 часа (Wilcock et al., 2003). Другие исследования показали, что прямое применение анти-Aβ-антител приводит к быстрому клиренсу амилоидных отложений in vivo (Bacskai et al., 2001; Brendza et al., 2005). Инъекция высокоаффинного селективного в отношении протофибрилл Aβ антитела приводит к значимому уменьшению бляшек в модели мыши APPswe (фигура 3).
На фигуре 3 испытывали терапевтическую эффективность высокоаффинного селективного в отношении протофибрилл антитела в модели трансгенной мыши (APPswe). A: 14-месячной трансгенной мыши APPSwe интракраниально инъецировали ЗФР, и В: высокоаффинное селективное в отношении протофибрилл антитело (158) при 1 мкг/мкл и испытывали спустя 72 часа после инъекции. Заметный клиренс нагрузки Aβ был обнаружен в подлежащей ткани вблизи места инъекции (B; стрелка) в сравнении с контрольной стороной (A; стрелка).
Пример 4
Лигирование на основе близости в комбинации с высокоаффинным селективным в отношении протофибрилл Aβ антителом для измерения протофибрилл Aβ
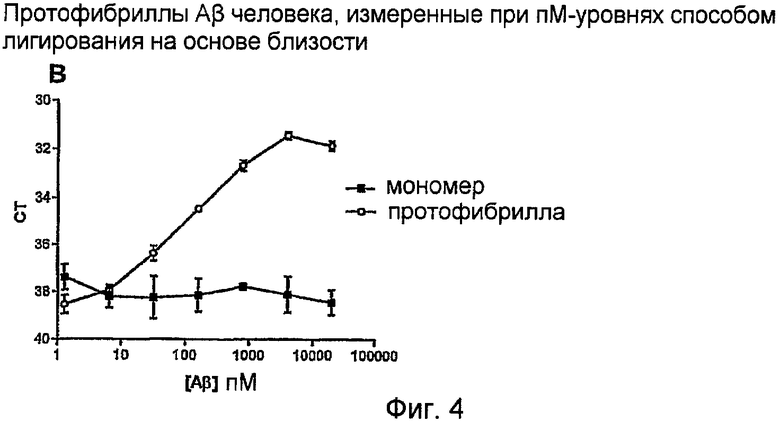
Протофибриллы Aβ дикого типа человека детектировали до диапазона 10 пМ, тогда как препарат мономеров Aβ вообще не детектировался. Комбинирование сверхчувствительного способа лигирования на основе близости и высокоаффинного антитела является особенно выгодным, так как оно обеспечивает систему для определения только олигомерных форм аналита, которая особенно пригодна при диагностике болезни Альцгеймера и других заболеваний с «агрегацией белка», например, вызываемых прионами заболеваний, болезни Крейтцфельда-Якоба, амилоидоза и болезни Паркинсона.
На фигуре 4 протофибриллы Aβ человека измеряют при пМ-уровнях способом лигирования на основе близости. Анализ лигирования на основе близости: Описание способа: (из Gullberg et al., 2004): стадия 1 - инкубирование пробы с парой зондов близости (~1 ч); стадия 2 - добавление всех компонентов, необходимых для лигирования и детектирования количественной ПЦР (время лигирования ~5 мин). В этом анализе использовали высокоаффинное селективное в отношении протофибрилл моноклональное антитело; стадия 3 - количественная ПЦР (~2 ч). Препараты синтетического мономера Aβ и протофибрилл Aβ разбавляли и испытывали на их реактивность в анализе лигирования на основе близости, описанного выше.
Пример 5
mAb 158 не узнает общий амилоидный эпитоп
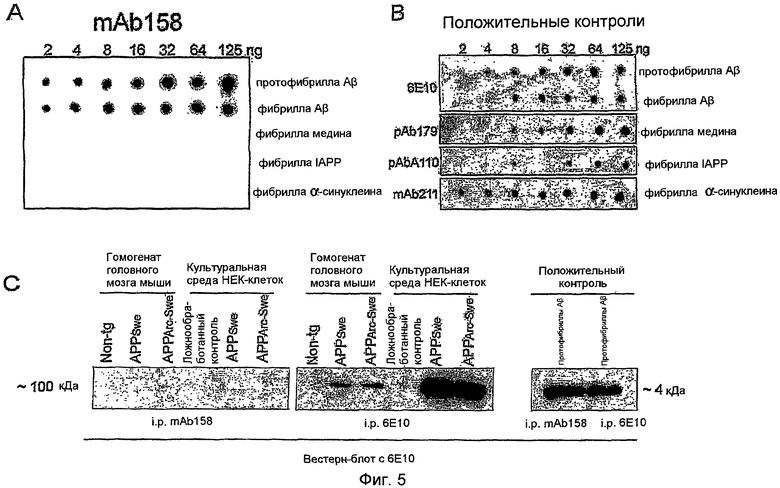
Было показано, что сообщенные ранее зависимые от конформации Aβ антитела связывают олигомеры и фибриллы других амилоидогенных белков, что предполагает наличие общего эпитопа, присутствующего на всех амилоидных агрегатах. Вследствие технических трудностей в генерировании протофибрилл из других амилоидогенных белков, чем Aβ, mAb158 тестировали вместо этого против различных амилоидных фибрилл. Для этих экспериментов использовали дот-блот-анализ, так как ELISA на основе ингибирования, где реакции антитело-антиген происходят в растворе, не пригоден для нерастворимых антигенов, таких как фибриллы. Однако дот-блот-анализ не пригоден для оценки специфичности антител в отношении разных форм Aβ, т.е. для измерения различий в селективности в отношении протофибрилл и фибрилл. Фибриллы медина, островкового амилоидного полипептида (IAPP) и α-синуклеина иммобилизовали на нитроцеллюлозной мембране для поддержания их нативных конформаций. mAbl58 не обнаруживал реактивности ни с одним амилоидом, другим, чем фибрилла Aβ (фиг. 5,A). Связывание mAb158 с фибриллами Aβ предполагает, что часть эпитопа протофибриллы Aβ присутствует также в структуре фибрилл Aβ. В качестве положительных контролей использовали антитела 6E10 (Aβ), pAbl79 (медин), pAbAl10 (IAPP) и mAb211 (α-синуклеин) (фиг. 5,B). Репрезентативные блоты из повторяемых экспериментов (n=3).
mAbl58 не связывает APP
Уровни APP и растворимых фрагментов APP обычно превышали уровни Aβ в биологических пробах, таких как CSF и гомогенат головного мозга, и, следовательно, перекрестная реактивность Aβ-антитела с APP могла ингибировать лечение связыванием с APP, приводя к меньшему количеству свободного антитела для связывания и элиминации протофибрилл Aβ и/или олигомеров Aβ. Она могла также нарушать измерения протофибрилл Aβ в биологических пробах при анализе Aβ сэндвич-ELISA. Для выяснения, связывается ли mAb158 с нативным APP, выполняли эксперименты с использованием иммунопреципитации. Культуральную среду HEK-клеток (контроль, APPSwe и APPArc-Swe) и гомогенаты головного мозга мыши (нетрансгенной, APPSwe и APPArc-Swe) иммунопреципитировали mAb158 или 6E10, с последующим денатурирующим вестерн-блоттингом с 6E10 в качестве детектирующего антитела (фиг. 5,C). Как видно на фигуре 5,C, mAbl58 не иммунопреципитировал αAPP из культуральной среды клеток или полноразмерный APP из гомогенатов головного мозга мыши, тогда как 6E10 иммунопреципитировал, как и ожидалось. Синтетические протофибриллы Aβ, используемые в качестве контроля, иммунопреципитировались равным образом хорошо обоими антителами (фиг. 5,С). Репрезентативные блоты из повторяемых экспериментов (n=3).
Пример 6
Установление специфического в отношении протофибрилл Aβ сэндвич-ELISA
Для обеспечения возможности измерений протофибрилл Aβ в биологических пробах был разработан сэндвич-ELISA с использованием mAbl58 в качестве как захватывающего, так и детектирующего антитела. Этот анализ измеряет протофибриллы Aβ с пределом детектирования 1 пМ и с линейным диапазоном 250 пМ (фиг. 6,А, линии указывают линейную регрессию калибровочных кривых). Вследствие неопределенности в отношении размера протофибрилл Aβ, используемых в калибровочной кривой, концентрация 1 пМ основывалась на молекулярной массе одного мономера Aβ (4514 г/моль), хотя, поскольку молекулярная масса протофибриллы была оценена как равная по меньшей мере 100 кДа, предел детектирования, рассчитанный как молярные протофибриллы Aβ, мог быть таким низким, как 50 фМ. Калибровочная кривая протофибрилл AβArc давала более низкий сигнал, чем протофибриллы Aβ дикого типа, возможно, вследствие различий в размере протофибрилл Aβ. (фиг. 6,A, 6,B). Использовали синтетический LMW-Aβ (низкомолекулярный Aβ) с определенными концентрациями. Под термином «низкомолекулярный Aβ» имеют в виду мономеры, димеры и триммеры Aβ, имеющие молекулярную массу приблизительно 4-12 кДа. Протофибриллы Aβ и Aβl-16 использовали для валидизации конформационной специфичности этого ELISA (фиг. 6,B), где использовали этот гидрофильный пептид Aβl-16, так как не ожидали, что он агрегируется. Этот анализ ELISA, состоящий из двух идентичных антител, требует по меньшей мере димера белка для продуцирования сигнала, и, как предсказывалось, Aβl-16 не детектировался mAbl58-сэндвич-ELISA даже при мкМ концентрациях (фиг. 6,B). При предобработке LMW-Aβ и протофибрилл Aβ 70% муравьиной кислотой (FA), которая, как известно, диссоциирует агрегированный Aβ на мономеры, этот сигнал сэндвич-ELISA был потерян (данные не показаны). Таким образом, детектирование LMW-Aβ при высоких нМ концентрациях (Fig 6B) обусловлено, возможно, малым содержанием агрегатов этого пептидного препарата.
Большой избыток мономерного Aβ, holoAPP и APP-фрагментов, природно-встречающийся в биологических пробах, мог бы препятствовать анализу протофибрилл Aβ занятием сайтов связывания захватывающей оболочки антитела, ингибируя связывание протофибрилл. Эту проблему исследовали добавлением увеличивающегося избытка Aβ1-16 к фиксированной концентрации протофибрилл Aβ (50 пМ, в расчете на мономерные звенья) и анализом этой проблемы с использованием как mAb158-ELISA, так и 6E10-6E10-сэндвич-ELISA (фиг. 6,C). 500000-кратный молярный избыток Aβ1-16, в сравнении с протофибриллами Aβ, не нарушал измерений с использованием mAbl58-сэндвич-ELISA, как и ожидалось, так как Aβl-16 связывается слабо с этим захватывающим антителом. В противоположность этому, 500-кратный избыток Aβ1-16 был достаточным для уменьшения сигнала в 6E10-6E10-ELISA, где Aβl-16 связывается с высокой аффинностью с захватывающим антителом (фиг. 6,C). Кроме того, при добавлении синтетических протофибрилл Aβ к контрольной культуральной среде клеток НЕК или гомогенатам головного мозга нетрансгенной мыши получали 90% этого сигнала (данные не показаны).
Пример 7
Измерение протофибрилл Aβ в биологических пробах
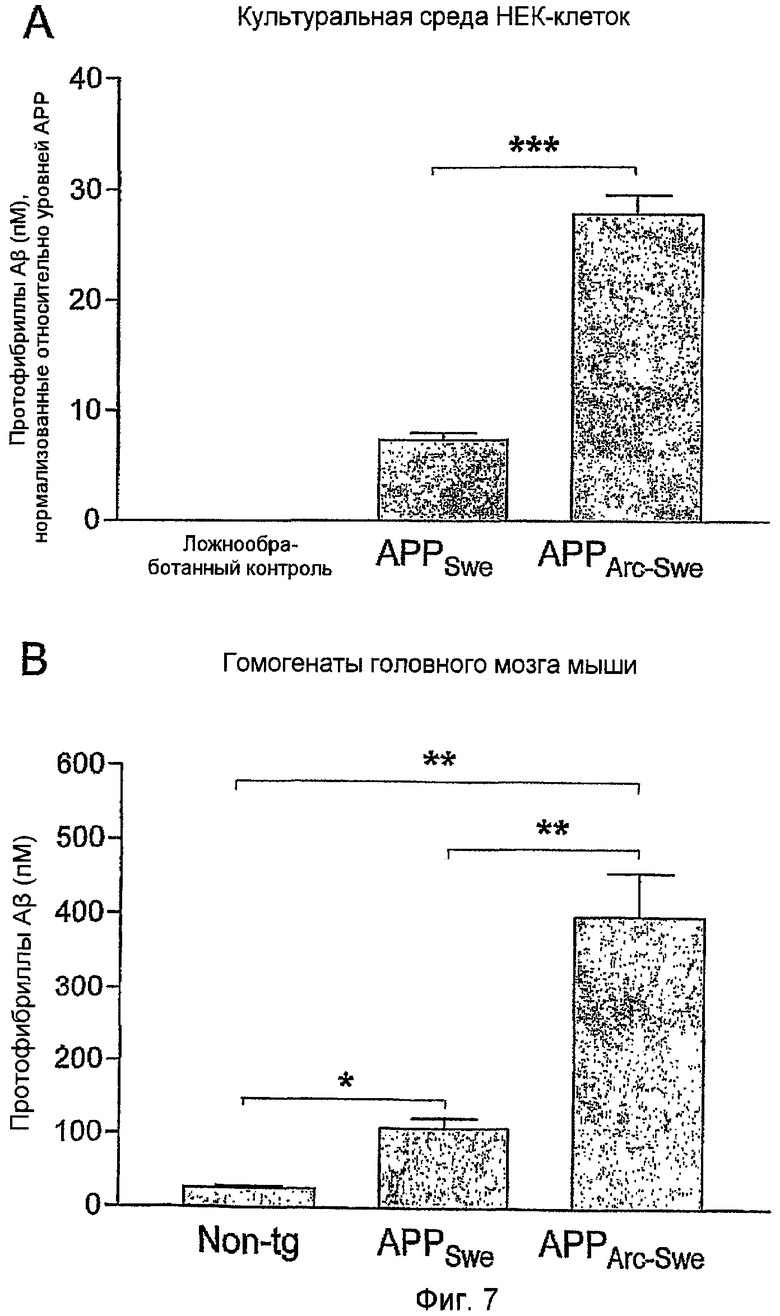
Было предположено присутствие протофибрилл Aβ в клетках и мышиных моделях, несущих мутацию Arctic, хотя до настоящего времени не было способа для прямого анализа протофибрилл Aβ в биологических пробах. Таким образом, mAbl58-сэндвич-ELISA обеспечивает первую возможность измерения уровня протофибрилл Aβ в таких клетках и мышиных моделях и сравнения их с моделями без внутренней мутации Aβ. Пробы из клеток и мышей, несущих только мутацию Swedish, сравнивали с калибровочной кривой протофибрилл Aβ дикого типа, тогда как пробы из клеток и мышей, экспрессирующих Aβ с мутацией Arctic, сравнивали с калибровочной кривой протофибрилл AβArc (фиг. 6,A). Для гарантии, что весь Aβ, измеренный в этом анализе, находился в растворимым состоянии, и для исключения какого-либо вмешательства со стороны фибрилл Aβ, все пробы центрифугировали в течение 5 минут при 17900 x g перед анализом. Группы клеточных сред от транзиторно трансфицированных APPSwe- и APPArc-Swe-HEK-клеток анализировали и сравнивали с контрольными культуральными средами НЕК-клеток. Уровни протофибрилл Aβ рассчитывали из калибровочных кривых (фиг. 6,A) в виде средней величины из трех повторностей и затем нормализовали относительно уровней АРР для компенсации в отношении различий в уровнях транскрипции (в соответствии с Stenh et al.). Концентрация протофибрилл Aβ в культуральных средах APPArc-Swe-HEK-клеток была равна 28 пМ (±2), значимо более высокая (p<0,0001), чем 8,2 пМ (±0,3), наблюдаемая в APPSwe (фиг. 7,A). В контрольных средах протофибриллы Aβ не детектировались. Уровни протофибрилл Aβ измеряли также в головном мозге из 10-месячных APPSwe- и APPArc-Swe-трансгенных мышей как с бляшками, так и с патологией с внутринейронным Aβ (в соответствии с Lord et al.). Головной мозг в каждом случае гомогенизировали в TBS и центрифугировали перед анализом для получения растворимой фракции Aβ. Аналогично этому анализу с использованием культуральных сред клеток, уровни протофибрилл Aβ значимо (р=0,005) различались между этими группами, с 397 пМ (±59) в головном мозгу APPArc-Swe- и 108 пМ (±14) в головном мозгу APPswе-трансгенных мышей (фиг. 7,B).
В вышеупомянутых фигурах (фиг. 6 и 7) исследовали следующее количество проб: контрольные клетки (n=3) и транзиторно трансфицированные APPSwe (n=8) и APPArc-Swe (n=11). Уровни протофибрилл Aβ в APPArc-Swe-средах были приблизительно в 9 раз более высокими, чем в средах APPSwe-средах, в то время как контрольные среды не давали сигнала (A). Измерения уровней протофибрилл Aβ в TBS-растворимой фракции гомогенатом головного мозга нетрансгенных мышей (n=6) сравнивали с трансгенными мышами (APPSwe, n=3, и APPArc-Swe, n=6) (B). Аналогично культуральным средам клеток, уровни протофибрилл Aβ APPArc-Swe-мышей были в 7 раз более высокими, чем в APPSwe-мышах. Столбики ошибок показывают ± SEM.
Пример 8
mAbl58 значимо снижает протофибриллы Aβ и общий Aβ в трансгенных мышах АРРswearc после i.p. введения
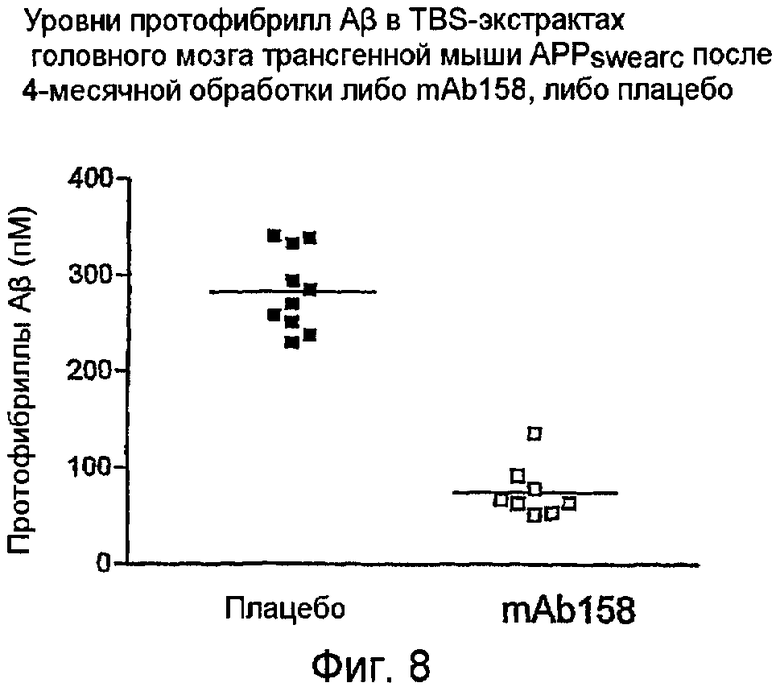
mAbl58 (12 мг/кг) инъецировали i.p. один раз в неделю в течение 18 недель в 9-10-месячных мышей APPswearc. После этого исследования головной мозг каждой мыши выделяли и гомогенизировали в TBS и затем центрифугировали для осаждения нерастворимого материала. Этот нерастворимый материал солюбилизировали в муравьиной кислоте. Таким образом, получали две фракции из головного мозга мыши, т.е. фракцию TBS и фракцию муравьиной кислоты. Уровни протофибрилл Aβ во фракциях TBS определяли при помощи ELISA. Обнаруживали значимое уменьшение протофибрилл Aβ в группе обработки mAbl58 в сравнении с группой плацебо (фиг. 8). Фигура 8 показывает уровни протофибрилл в экстрактах TBS головного мозга трансгенных мышей АРРswearc после 4-месячной обработки либо mAb158, либо плацебо.
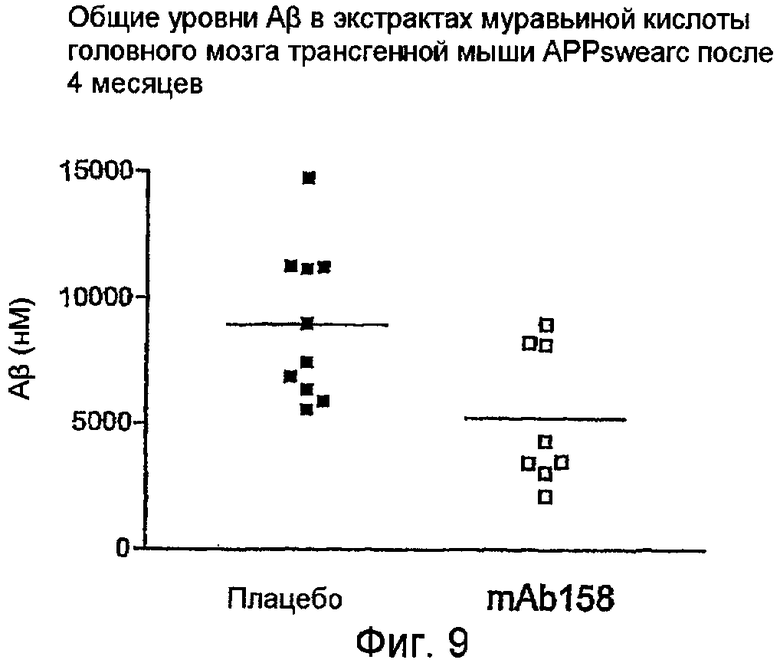
Общий Aβ во фракции муравьиной кислоты определяли при помощи ELISA (муравьиную кислоту использовали для солюбилизации всех форм Aβ, чтобы сделать все формы Aβ детектируемыми). Значимое уменьшение общего Aβ наблюдали в группе обработки в сравнении с группой плацебо (фиг. 9). Фигура 9 показывает уровни общего Aβ в экстрактах TBS головного мозга трансгенных мышей АРРswearc после 4-месячной обработки либо mAb158, либо плацебо.
Примеры 9-11
Аббревиатуры
Материалы
Оборудование
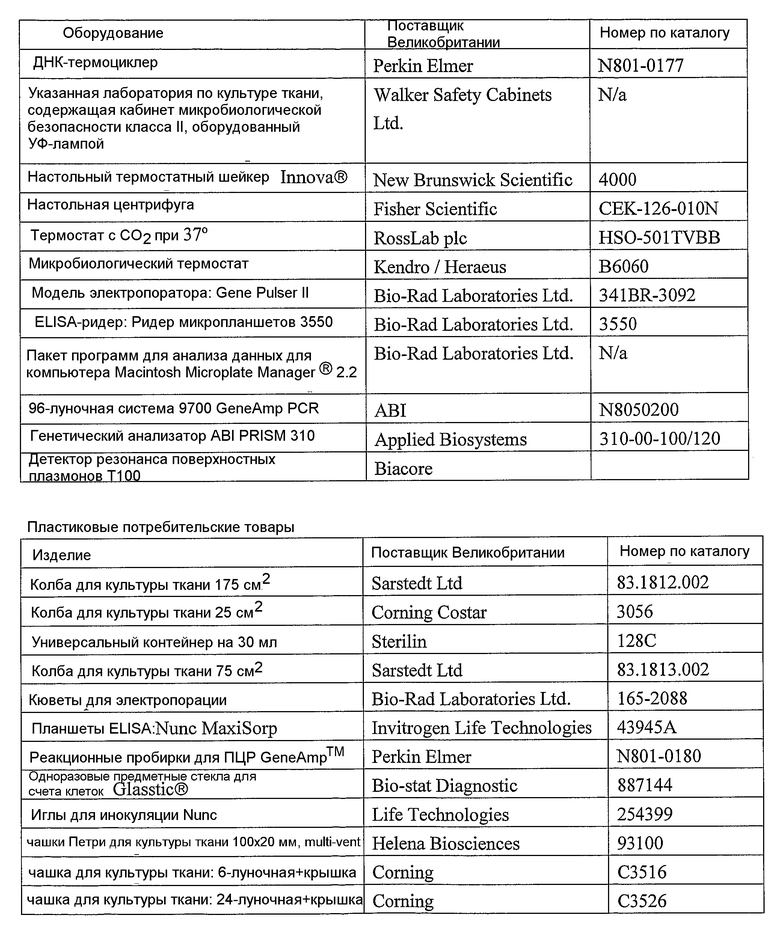
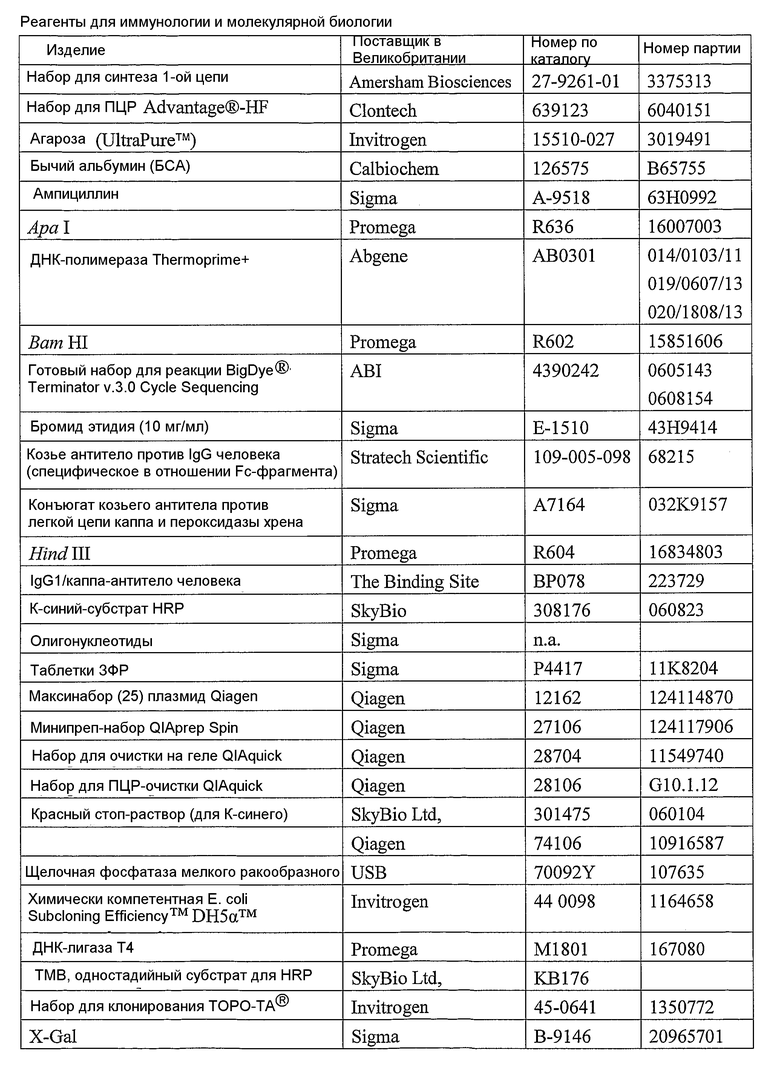
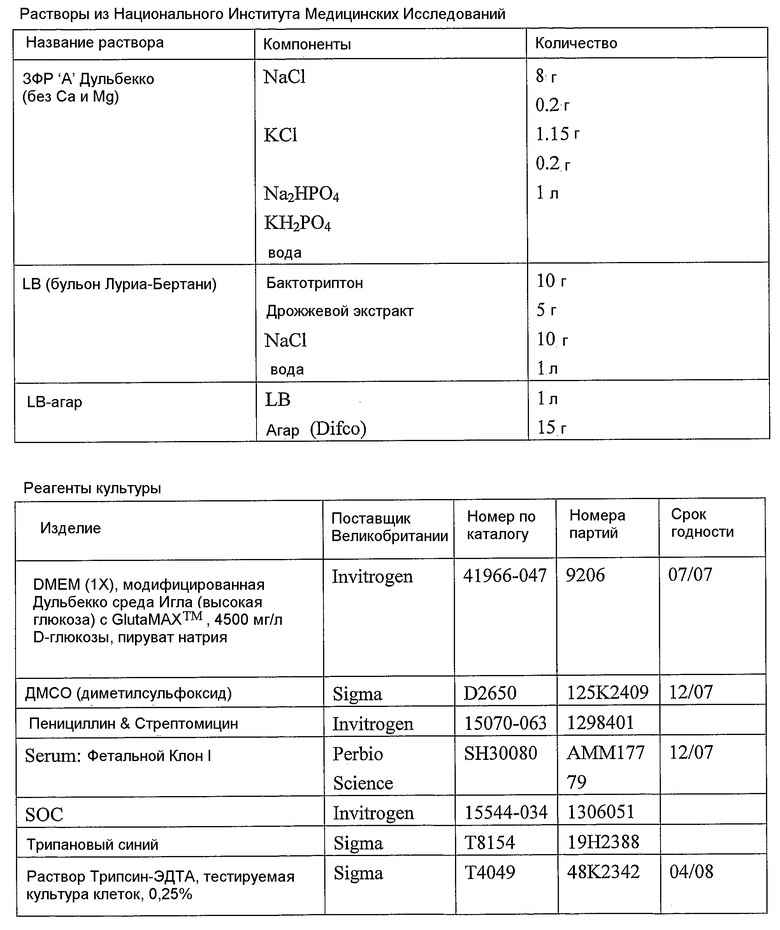
Пример 9. ДНК-последовательность антитела 158
9.1 - Получение РНК
Быстро замороженные осадки клеток мышиной гибридомы 158 (флаконы, помеченные как 060824#158 5×106 клеток) получали посредством TAG 3 октября 2006 года. Эти клетки хранили в замороженном виде до обработки с использованием мидинабора Qiagen RNeasy для выделения РНК по протоколу изготовителей.
9.2 - Синтез 1-й цепи
Приблизительно 5 микрограммов РНК 158 подвергали обратной транскрипции с получением кДНК 158 с применением набора для синтеза 1-й цепи Amersham Biosciences в соответствии с протоколом изготовителей. Это повторяли для получения 3 независимых кДНК-продуктов (раунды 1, 2 и 3) во избежание мутаций ДНК вследствие реакции обратной транскриптазы (RT).
9.3 - Клонирование кДНК иммуноглобулина 158
кДНК гибридомы 158 амплифицировали при помощи ПЦР в 23 отдельных реакциях кДНК вариабельной области каппа-цепи (VK) иммуноглобулина амплифицировали с использованием 11 VK-праймеров (МКV1-11) в комбинации с праймером МКС константной области каппа (таблица 6). Аналогично, кДНК вариабельной области тяжелой цепи (VH) иммуноглобулина амплифицировали при помощи ПЦР с использованием 12 различных VH-праймеров (MHV1-12) в комбинации со смесью четырех праймеров константной области IgG (MHCG l/2a/2b/3: таблица 7).
Результатом начального набора ПЦР-реакций IgН был единственный продукт амплификации, полученный с использованием праймера MHV5. Ни одна из остальных 11 пар праймеров не давала продукта ПЦР. Продукт этой реакции ПЦР, праймированной олигонуклеотидными праймерами: MHV5 + (смесь MHCGl/2a/2b/3), лигировали в вектор pCR2.1®-TOPO® с использованием набора для клонирования TOPO-TA®. Результатом начального набора ПЦР-реакций IgK были два отдельных продукта амплификации с использованием праймеров MKV1 и MKV2 с MKC. Другие 9 пар праймеров не генерировали продукт. Продукты ПЦР-реакции, праймированной олигонуклеотидными праймерами: MKV1 или MKV2 + MKC, лигировали в вектор pCR2.1®-TOPO® с использованием набора для клонирования TOPO-TA®.
Бактерии E.coli TOP10, трансформированные этим лигированным вектором, клонировали на чашках с LB/ампициллин/Х-gal-агаром, выскребанием капилляром на агаровую сеточку и в смесь для ПЦР-скрининга. Эти клонированные плазмидные инсерты подвергали скринингу ПЦР-амплификацией. Продукты ПЦР подвергали гель-электрофорезу и идентифицировали клоны, продуцирующие продукт ПЦР-амплификации правильного размера (приблизительно 500 п.н.). Ночные культуры (5 мл) каждого клона обрабатывали с использованием протокола набора QIAprep Spin Miniprep, с получением мини-препаратов ДНК-плазмид.
9.4 - Определение последовательности кДНК
Полный цикл ОТ-ПЦР, клонирования и анализа последовательности ДНК повторяли для получения трех независимых наборов информации последовательности для каждой цепи иммуноглобулина. Плазмидные клоны из каждого независимого набора реакций ОТ-ПЦР секвенировали в обоих направлениях с использованием праймеров 1212 и 1233 (таблица 10). Плазмиды секвенировали с использованием набора BigDye® Terminator v. 3.0 Cycle Sequencing Ready Reaction Kit (ABI), циклы повторяли на приборе GeneAmp9600 PCR и анализировали на капиллярном секвенаторе ABI 310.
9.5 - ДНК-последовательность VK 158
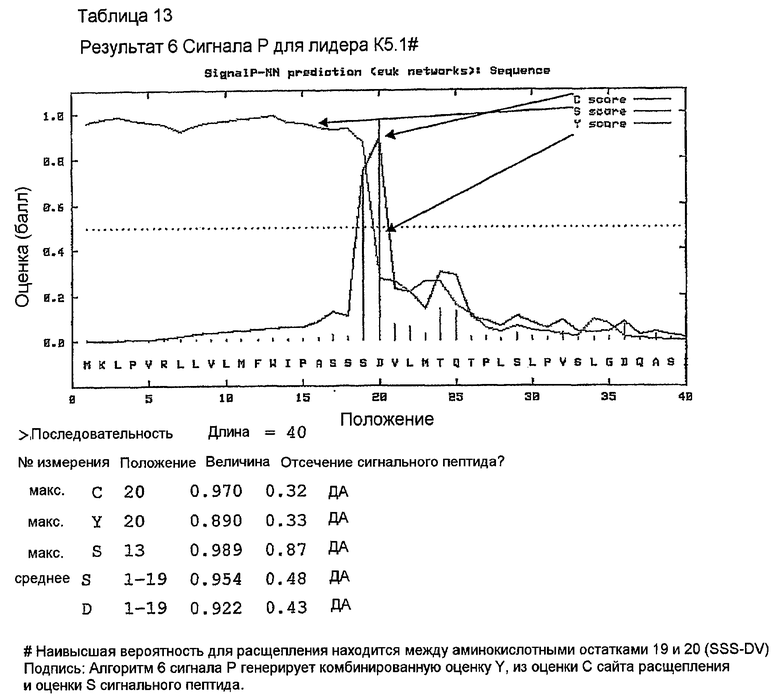
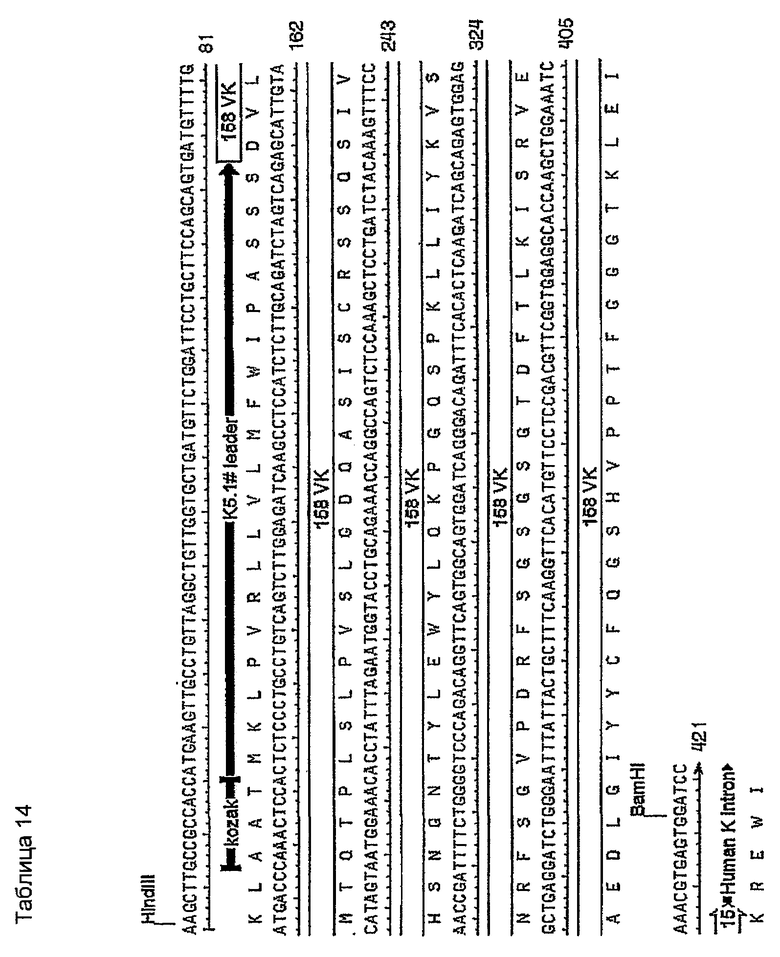
Последовательности клонов VK, генерированные с использованием праймеров ПЦР MKV2 и MKC в раундах 1 и 2 на кДНК 1-й цепи, были идентичны стерильному каппа-транскрипту из миеломного партнера слияния, такого как MOPC-21, SP2 и Ag8. Это стерильный транскрипт. Консенсусная последовательность (VK 158) клонов VK, генерированная с использованием праймеров ПЦР MKV1 и MKC в раундах 1-3 на кДНК 1-й цепи, показана в таблице 11. Это является функциональной реаранжировкой. Таблица 11 показывает некоторые отличия от последовательности, показанной в таблицах 1, 4 и 5. Эти отличия находятся в районе FW1, где расположен праймер ПЦР. Мышиной лидерной последовательностью VK, наиболее идентичной фрагменту лидера в VK 158, не кодируемой праймерами авторов изобретения, была K5.1# (таблица 12). Предсказание в отношении сигнального пептида для точного отщепления сигнальной последовательности #K5.1 выполняли с использованием программы предсказания. Наиболее вероятно предсказанный сайт расщепления находился точно между аминокислотными остатками 19 и 20 (таблица 13). Химерный белок 158VK и ДНК-последовательность показаны в таблице 14.
9.6 - ДНК-последовательность VH 158
Консенсусная последовательность (VН 158) клонов VН, генерированная с использованием праймеров ПЦР MKV5 и смеси MHCGl/2a/2b/3 в раундах 1-3 на кДНК 1-й цепи, показана в таблице 15. Как и в случае с VK 158, имелись некоторые отличия от последовательности FW1, показанные в таблицах 1, 4 и 5. Наиболее идентичной мышиной лидерной последовательностью VH относительно этого фрагмента лидера, не кодируемой праймерами авторов изобретения, была NL-1 (таблица 16).
Пример 10 - Конструирование химерных экспрессирующих векторов
Конструирование химерных экспрессирующих векторов влечет за собой добавление подходящей лидерной последовательности к VH и VK, перед которой находятся сайт рестрикции HindIII и последовательность Козака. Эта последовательность Козака (таблица 8) гарантирует эффективную трансляцию последовательности вариабельной области. Она определяет правильный кодон AUG, от которого рибосома может начинать трансляцию, и наиболее критическим основанием является аденин в положении -3, слева от стартового кодона AUG. Эта лидерная последовательность выбрана как наиболее сходная мышиная лидерная последовательность в базе данных Кабата. Эти добавления закодированы в прямых праймерах (таблица 9). Кроме того, конструирование химерных экспрессирующих векторов влечет за собой введение 5'-фрагмента константной области γ1 человека, до природного сайта рестрикции Apa I, смежного с 3'-концом J-области 158. Этот СН кодируется в экспрессирующем векторе справа от встроенной последовательности VH, но не содержит интрона V-C. Для легкой цепи справа от V-области добавляют природный донорный сайт сплайсинга (таблица 8) и сайт BamHI. Эта донорная последовательность сплайсинга облегчает сплайсинг интрона каппа V:C, который является необходимым для присоединения в рамке считывания VK к константной области.
Мышиные гены VH и VK анализировали для идентификации любых нежелательных донорных сайтов сплайсинга, последовательностей Козака и на присутствие каких-либо лишних субклонирующих сайтов рестрикции, которые могли бы в дальнейшем мешать субклонированию и/или экспрессии функционального полноразмерного антитела. В этом случае ни один из этих компонентов не был обнаружен.
10.1 - Экспрессирующие векторы
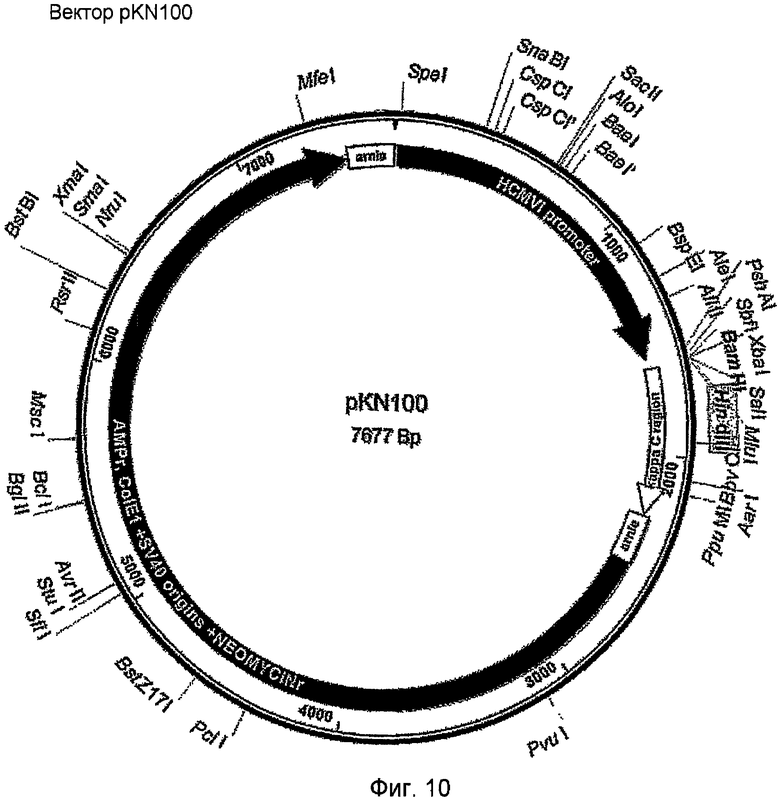
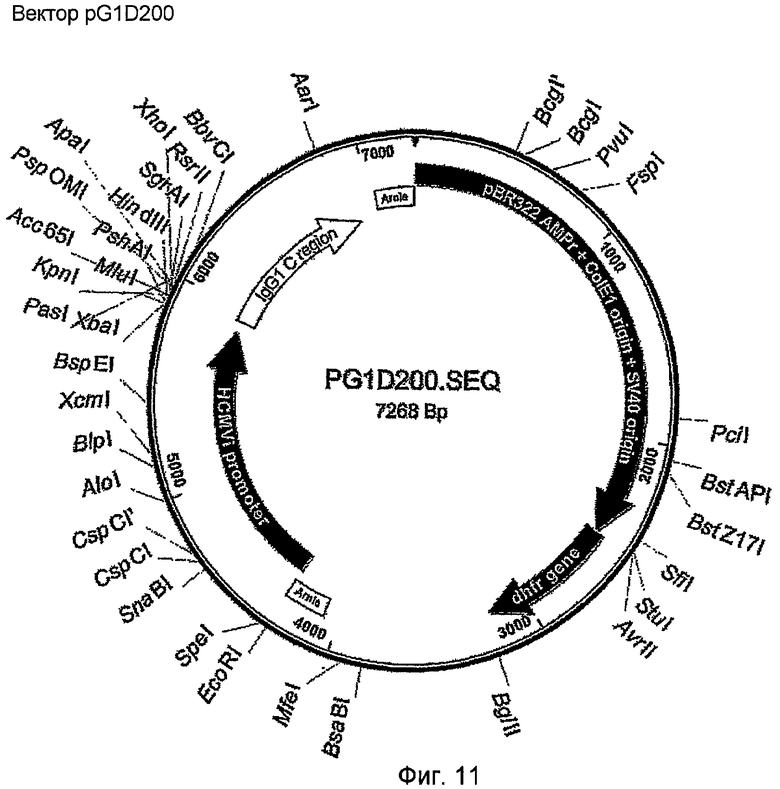
Препараты плазмидных ДНК экспрессирующих векторов pKN100 и pG1D200 очищали с использованием наборов Qiagen Maxi в соответствии с протоколом изготовителей. Плазмидную ДНК очищали с использованием наборов QIAGEN Plasmid Midi и Maxi из культур 500 мл бактерий TOP10, трансфицированных каждым вектором. Карты векторов показаны на фигурах 10 и 11.
10.2 - Праймеры химеризации легкой цепи
Мышиную лидерную последовательность K5.1# включали в конструкцию химерной VK 158. Праймеры конструировали таким образом, что они генерировали ПЦР-продукт, содержащий полный лидер и VK 158 с концевыми сайтами рестрикции HindIII и BamHI, для клонирования в экспрессирующий вектор pKN100 (таблица 9). Прямой праймер 158vl вводит сайт рестрикции HindIII, сайт Козака и лидерную последовательность K5.1#. Обратный праймер 158vlrev вводит донорный сайт сплайсинга и сайт рестрикции BamHI.
10.3 - Праймеры химеризации тяжелой цепи
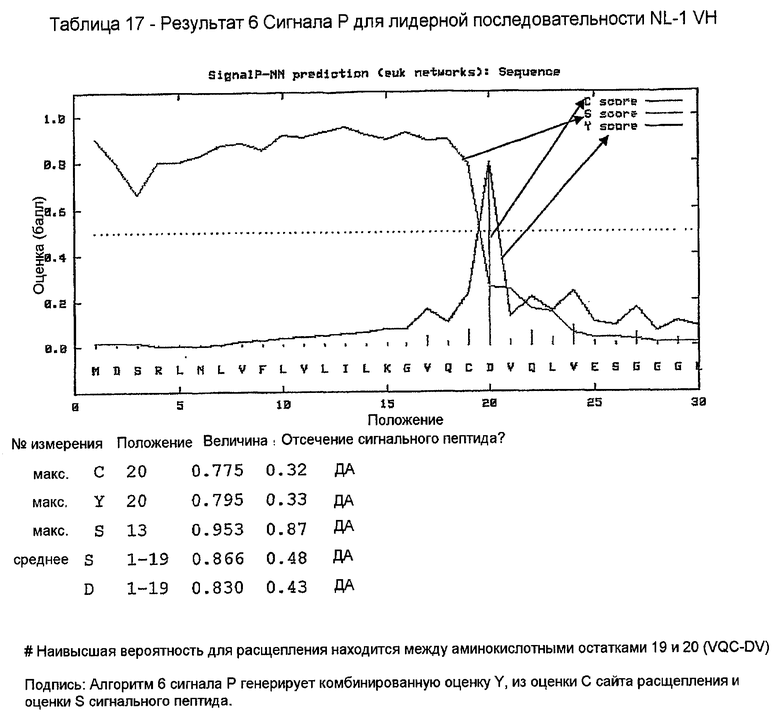
Лидерную последовательность NL-1 включали в конструкцию химерной VH 158. Праймеры конструировали таким образом, что они генерировали ПЦР-продукт, содержащий этот лидер и VH-область с концевыми сайтами рестрикции HindIII и Apa I, для клонирования в экспрессирующий вектор pG1D200. Они показаны в таблице 9. Прямой праймер 158vh1 вводит сайт рестрикции HindIII, сайт инициации трансляции Козака и лидерную последовательность NL-1. Обратный праймер 158vhrev вводит 5'-конец С-области γ1 и природный сайт рестрикции ApaI. Предсказание сайта отщепления сигнального пептида для лидерной последовательности K5.1 VK показано в таблице 17.
10.4 - Генерирование химерной конструкции VH 158: pG1D200158VH
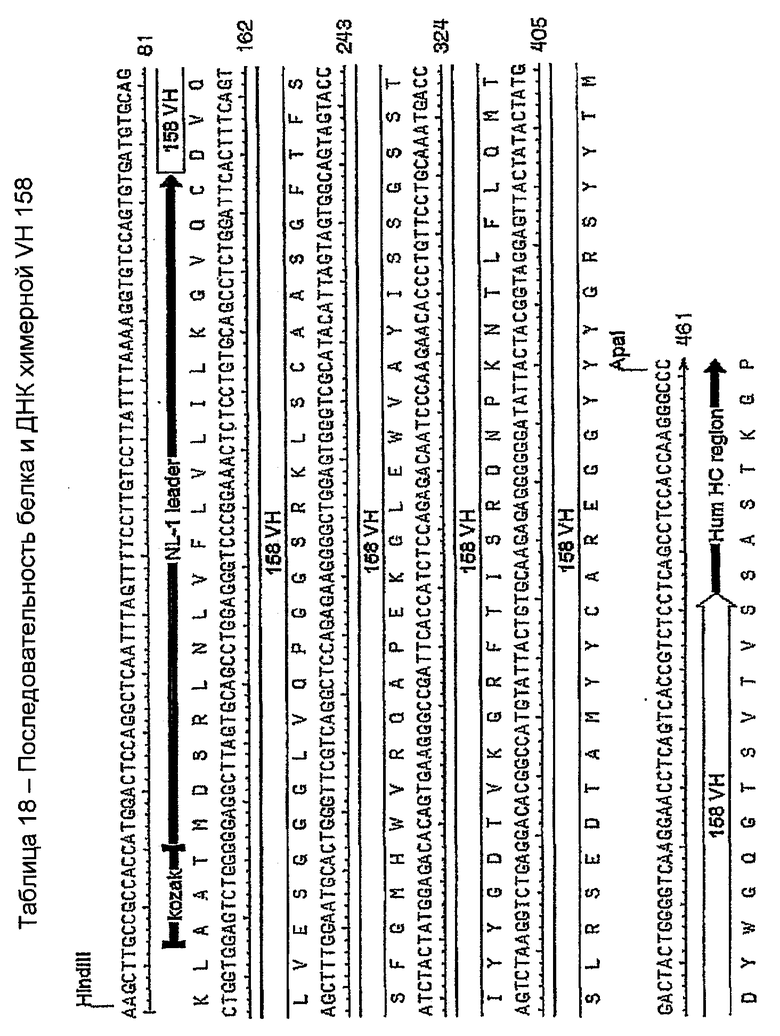
ДНК-фрагмент VH 158 амплифицировали с праймерами 158vh и 158vhrev (таблица 9). Продукт ПЦР 450 п.н. (приблизительно) лигировали T-A в вектор pCR2.1 и использовали для трансформации химически компетентных бактерий TOP10. Клоны отбирали по правильному размеру инсерта и секвенировали с использованием праймера 1212 (таблица 10). Правильно экспрессированный инсерт субклонировали в экспрессирующий вектор pG1D200 и правильный субклон отбирали с использованием секвенирования ДНК с использованием праймера BDSH61R (таблица 10). Этот клон выращивали в 200 мл культуры с получением плазмидной ДНК с использованием набора Qiagen Maxi Kit в соответствии с протоколом изготовителей. Этот химерный белок VH 158 и последовательность ДНК показаны в таблице 18.
10.5 - Генерирование химерной конструкции VK 158: pKN100158VK
ДНК-фрагмент VК 158 амплифицировали с праймерами 158vl и 158vlrev (таблица 9). Продукт ПЦР 450 п.н. (приблизительно) лигировали T-A в вектор pCR2.1 и использовали для трансформации химически компетентных бактерий TOP10. Клоны отбирали по правильному размеру инсерта и секвенировали с использованием праймера 1212 (таблица 10). Правильно экспрессированный инсерт субклонировали в экспрессирующий вектор pKN100. Правильный субклон отбирали скринингом на размер инсерта и секвенированием ДНК с использованием праймера Hu-K2 (таблица 10). Этот клон выращивали в 200 мл культуры с получением плазмидной ДНК с использованием набора Qiagen Maxi Kit в соответствии с протоколом изготовителей.
Пример 11 - Получение и свойства связывания химерного антитела 158
11.1 - Трансформация клеток COS 7 и культура клеток
Один флакон клеток COS 7 оттаивали и выращивали в DMEM, дополненной 10% фетальной сывороткой клона I и антибиотиками. Спустя одну неделю клетки (0,8 мл при 107/мл) электропорировали с использованием плазмид pGlD200158VH + pKN100158VK (10 мкг ДНК, каждой). Эти клетки выращивали в 8 мл среды для выращивания в чашках Петри в течение 3 дней.
11.2 - Получение химерного антитела
Сэндвич-ELISA использовали для измерения концентраций антител в супернатантах COS 7. Химерное антитело VH 158 x VK 158 экспрессировалось при 0,3 мкг/мл и затем при 3,7 мкг/мл (таблица 19) в кондиционированных транзиторно котрансфицированными COS-клетками средах.
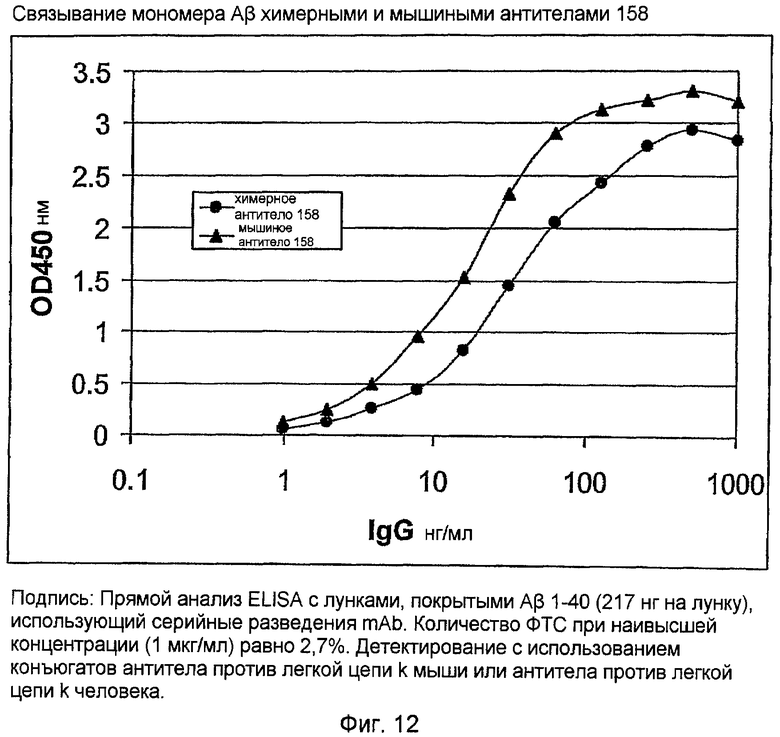
11.3 - Активность химерного антитела
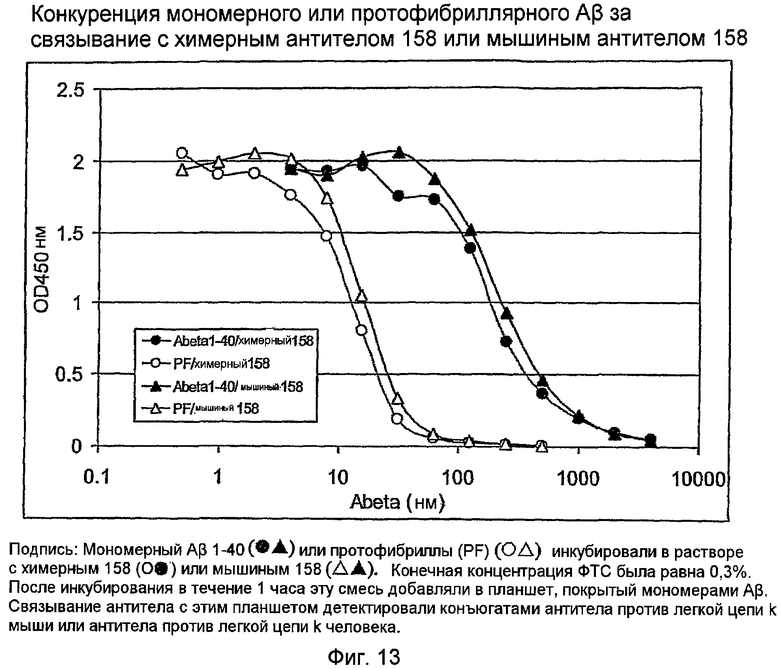
Два ELISA использовали для анализа связывания антигена химерного 158. С использованием кондиционированной 3,7 мкг/мл химерного антитела среды, связывание с мономером Aβ измеряли по протоколу прямого ELISA (фигура 12) и сравнивали с мышиным IgG 158. Кроме того, выполняли конкурентный ELISA с использованием либо мономера, либо протофибриллы, смешанных в водной фазе с антителом, которое затем связывали с мономером в твердой фазе (фигура 13). Эти ELISA показали, что химерное антитело 158 связывается с мономером амилоида Aβ и протофибриллой аналогично связыванию с первоначальным мышиным антителом 158
Примечание
Более позднее секвенирование показало, что данные относительно последовательности мышиного антитела, показанные в таблицах 1 и 4, содержат ошибки как в цепи VH, так и в цепи VK на 5'-конце. Авторы изобретения предполагают, что это вызвано использованием праймеров, расположенных в V-области. В более позднем секвенировании использовали праймеры, расположенные в лидерных последовательностях, которые не могут вводить мутации в этих V-областях. Это более позднее секвенирование показало различия последовательности (см. таблицы 15 и 11). Однако указанные различия не находятся в CDR-областях.
Это химерное антитело связывает мономер и протофибриллы амилоида Aβ, как показано прямым ELISA связывания и конкурентным ELISA соответственно. Этот результат подтверждает, что комбинация цепей VH 158 и VK 158 кодирует анти-LSAP-антитело 158, и показывает, что эти последовательности подходят для процедуры гуманизации для генерирования гуманизированного антитела 158.
Пример 12 - Конструирование и обсуждение гуманизированного антитела
Аббревиатуры и определения
V-область Сегмент цепей IgG, который является вариабельным по последовательности между различными антителами. Он простирается до остатка 109 Кабата в легкой цепи и до остатка 113 в тяжелой цепи
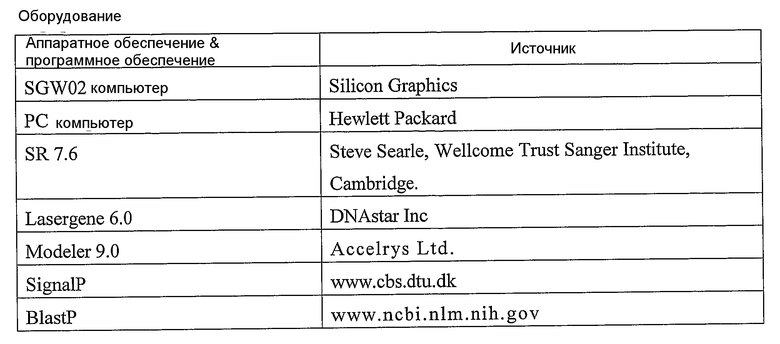
12.1 - Базы данных V-генов человека
Белковые последовательности иммуноглобулинов человека и мыши из International Immunogenetics Database 2006 и Kabat Database Release 5 of Sequences of Proteins of Immunological Interest (последняя корректировка 17 ноября 1999 года) использовали для компилирования базы данных белковых последовательностей иммуноглобулинов в сопоставлении Кабата. База данных авторов изобретения содержит 9322 последовательностей VH человека и 2689 последовательностей VK человека. Программу анализа последовательности, SR 7.6, использовали для запроса этих баз данных VH и VK человека с использованием белковых последовательностей VH 158 и VK 158 (таблица 20).
12.2 - Выбор каркасной области человека для 158RHA
12.2.1 - Сравнение VH 158 с последовательностями VH человека
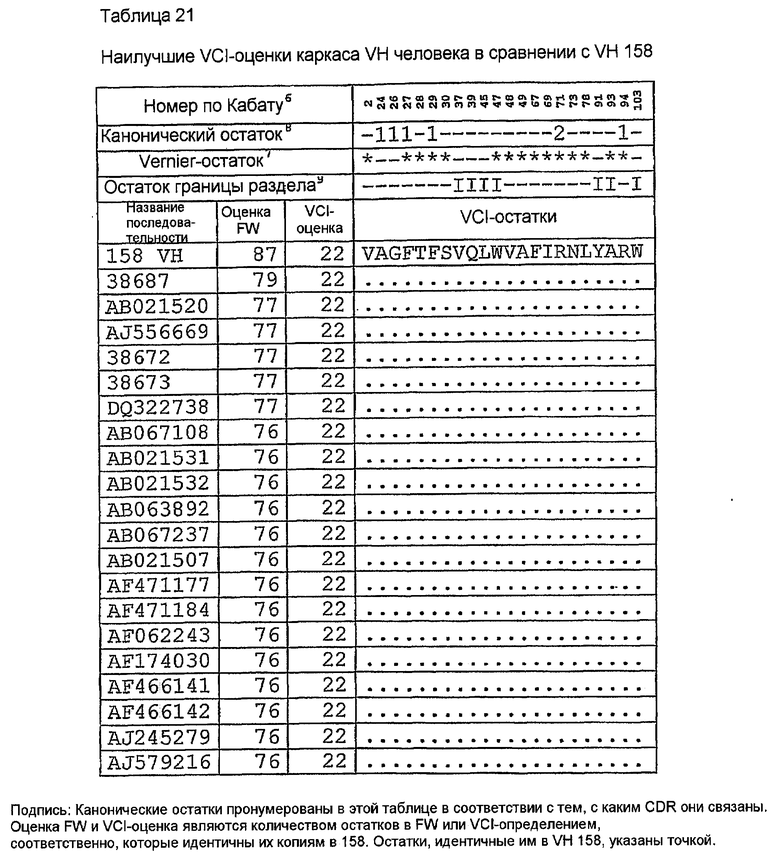
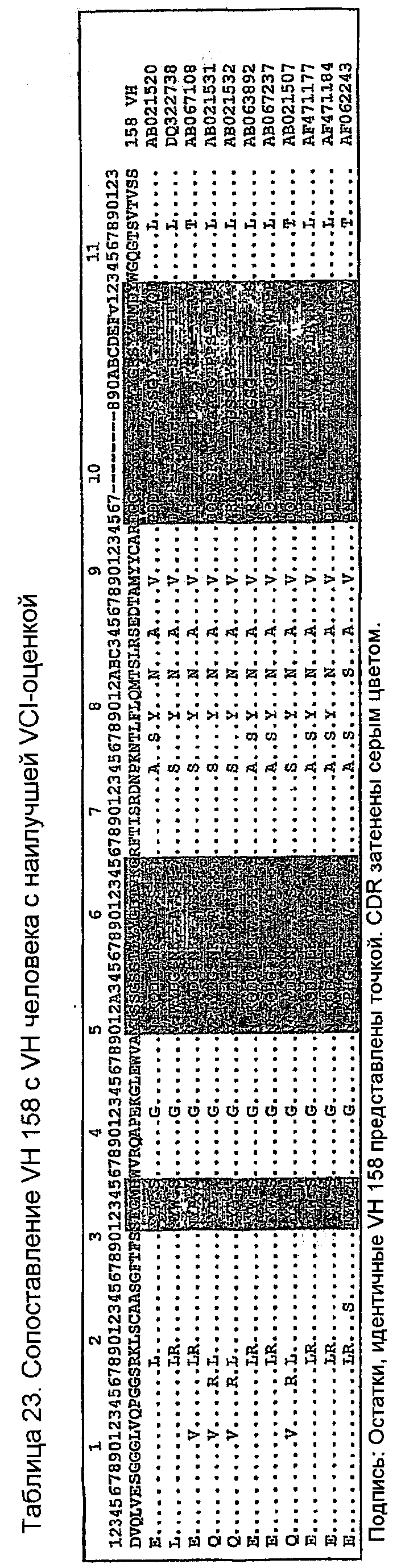
Последовательности VH человека с наивысшей идентичностью VH 158 в остатках Vernier (Foote, J. and G. Winter. 1992. Antibody framework residues affecting the conformation of the hypervariable loops. JMol.Biol. 224:487-499.). Канонических остатках (Canonical) (Morea,V., A.M.Lesk, and A.Tramontano. 2000. Antibody modeling: implications for engineering and design. Methods 20:267-279) и остатках VH-VL-границы раздела (VH-VL Interface) (Chothia,C, J.Novotny, R.Bruccoleri, and M.Karplus. 1985. Domain association in immunoglobulin molecules. The packing of variable domains. JMol.Biol. 186:651-663.), т.е. (VCI)-остатках, расположенных в каркасе (FW) V-области, показаны в таблице 21. Показаны также количество VCI-остатков (оценка VCI) и количество остатков FW (оценка FW), идентичных 158. Все эти VH-последовательности имеют общие идентичные VCI-остатки и длины CDR, как показано в таблице 22. AJ556669 имеет необычный Pro74, не наблюдаемый в других последовательностях человека в этом наборе данных, что приводит авторов изобретения к не принятию его в расчет в первоначальном анализе. Однако Pro74 присутствует в последовательности VH 158, и, следовательно, AJ556669 мог бы рассматриваться как альтернативный FW для гуманизации, если конструкция VH на основе AF062243 не связывает антиген. Сопоставление этих последовательностей (таблица 23) ясно показывает их различия. AF062243, единственный в этом наборе данных, имеет консервативное изменение T(82a)S и консервативный F79. Другими признаками AF062243 являются консервативные изменения D1E, K19R, A23S, T77S, S118T. Все другие изменения FW были общими для всех каркасов в таблице 23. AF062243 был выбран в качестве каркаса, на котором должен быть основан 158RHA.
12.3 - Генерирование 158RHA
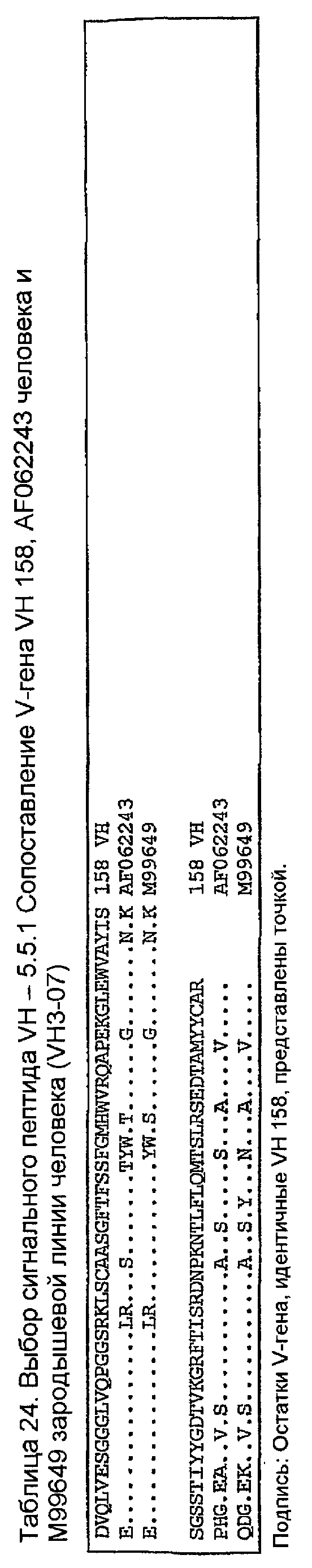
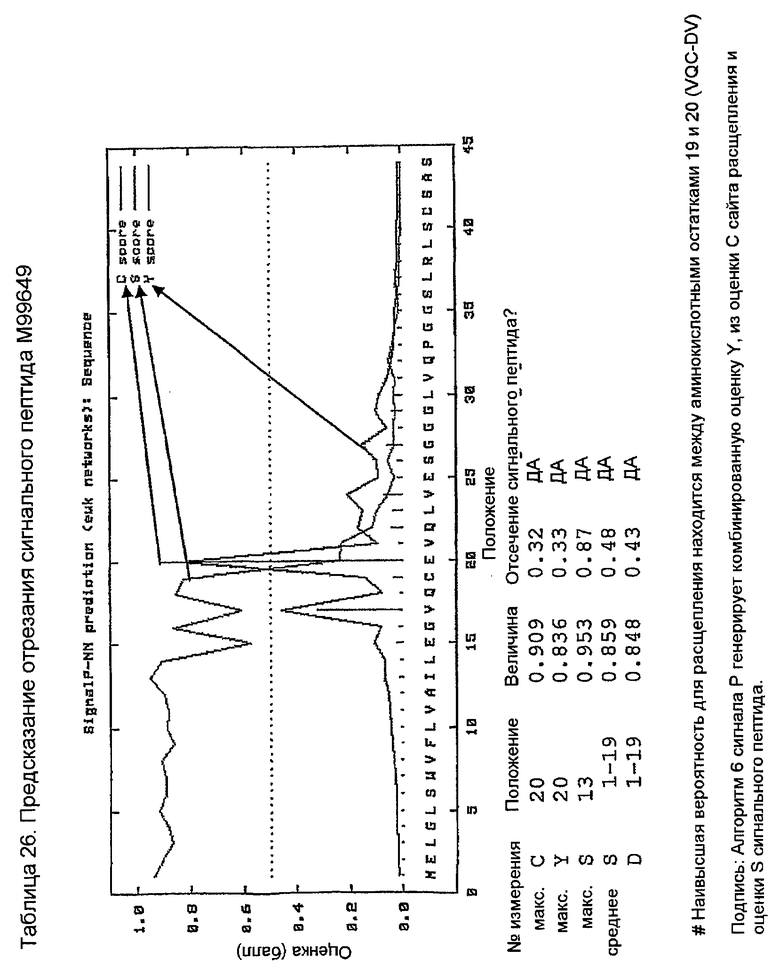
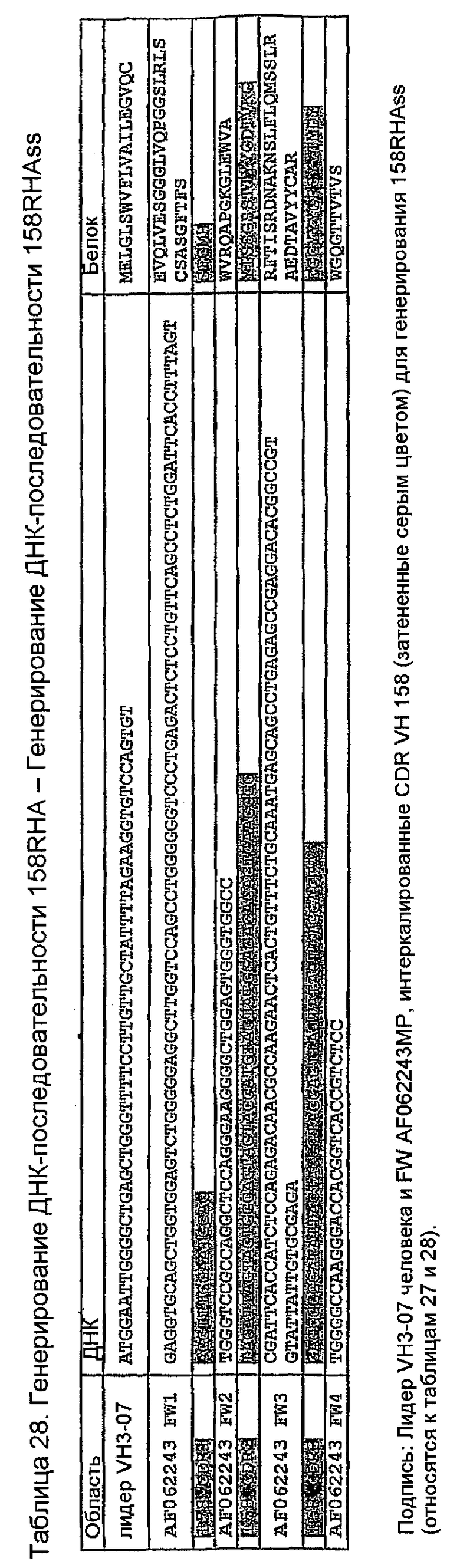
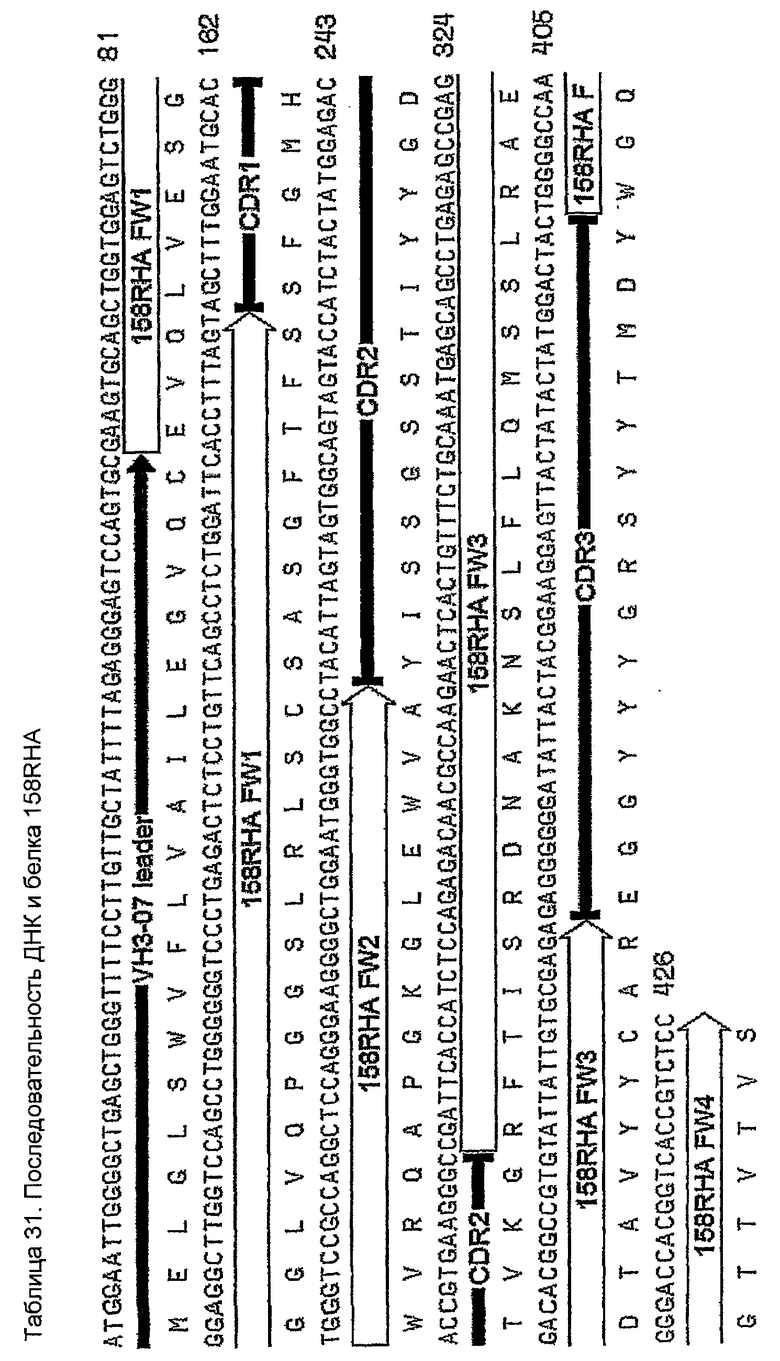
Конструирование 158RHA является просто трансплантацией CDR 1, 2 и 3 из VH 158 в акцепторный FW AF062243. V-геном зародышевой линии человека, наиболее идентичным AF062243 является VH M99649 (VH3-07) (таблица 24), из которого извлекали лидерный пептид (таблица 25). Алгоритм SignalP (Nielsen,H., J.Engelbrecht, S.Brunak, and G.von Heijne. 1997. Identification of prokaryotic and eukaryotic signal peptides and prediction of their cleavage sites. Protein Eng 10:1-6.) предсказывал, что он мог бы быть вырезан подходящим образом пептидазой сигнальной последовательности (таблица 26). Таблица 27 показывает схему трансплантации CDR 1, 2 и 3 VH 158 в FW AF062243 FW для генерирования последовательности белка 158RHA. Таблица 28 показывает генерирование ДНК-последовательности 158RHAss из природных ДНК-последовательностей VH 158 и AF062243. Анализ ДНК-последовательности 158RHAss предсказывал присутствие донорных сайтов сплайсинга, оценки предсказаний которых показаны в таблице 29. Некодирующие мутации вводили для инактивации этих предсказанных сайтов сплайсинга, как показано в таблице 30, для генерирования конечной ДНК-последовательности 158RHA (таблица 31).
12.4 - Выбор каркаса иммуноглобулина человека для 158RKA
12.4.1 - Сравнение VK 158 с последовательностями VK человека
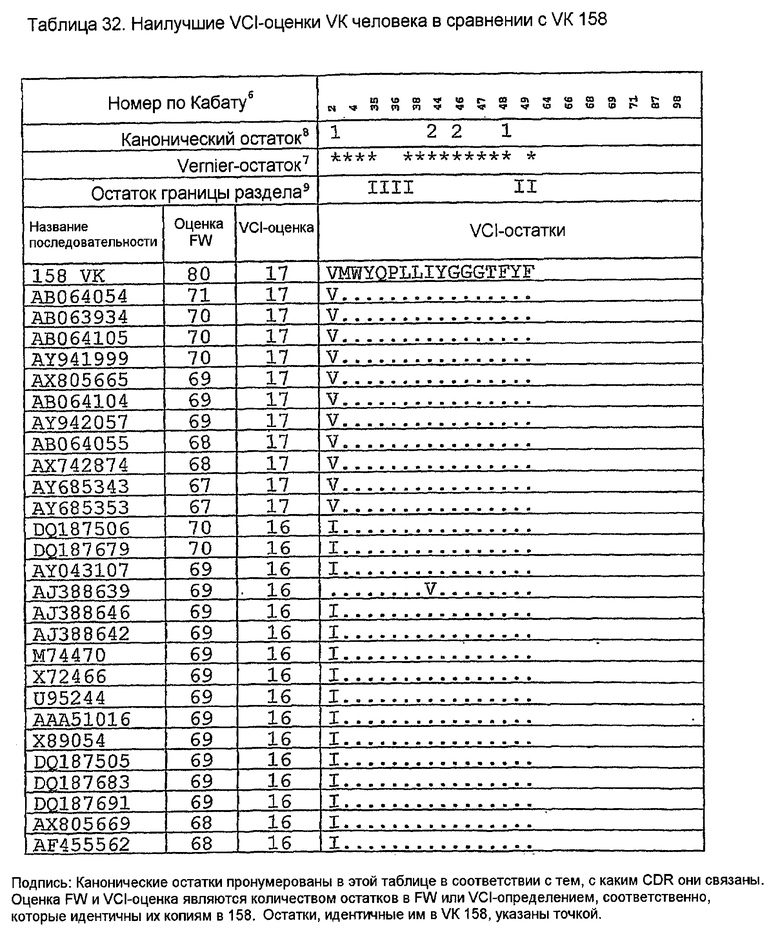
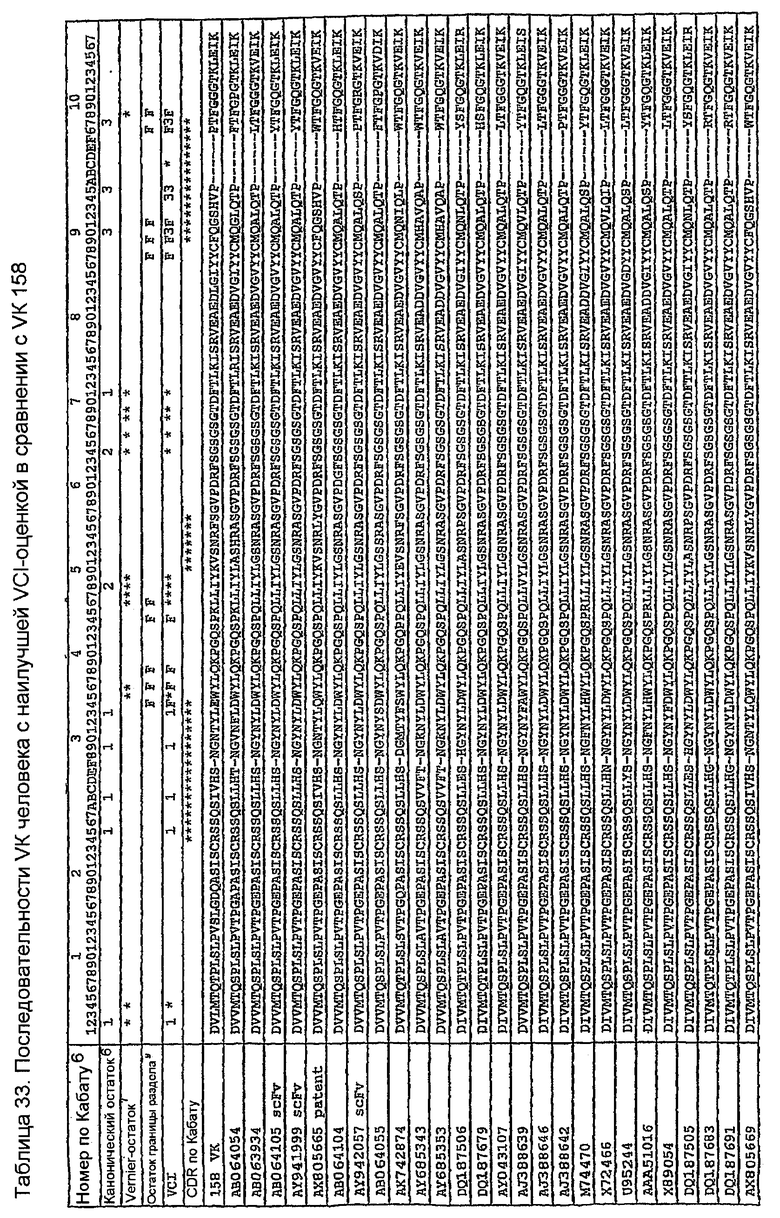
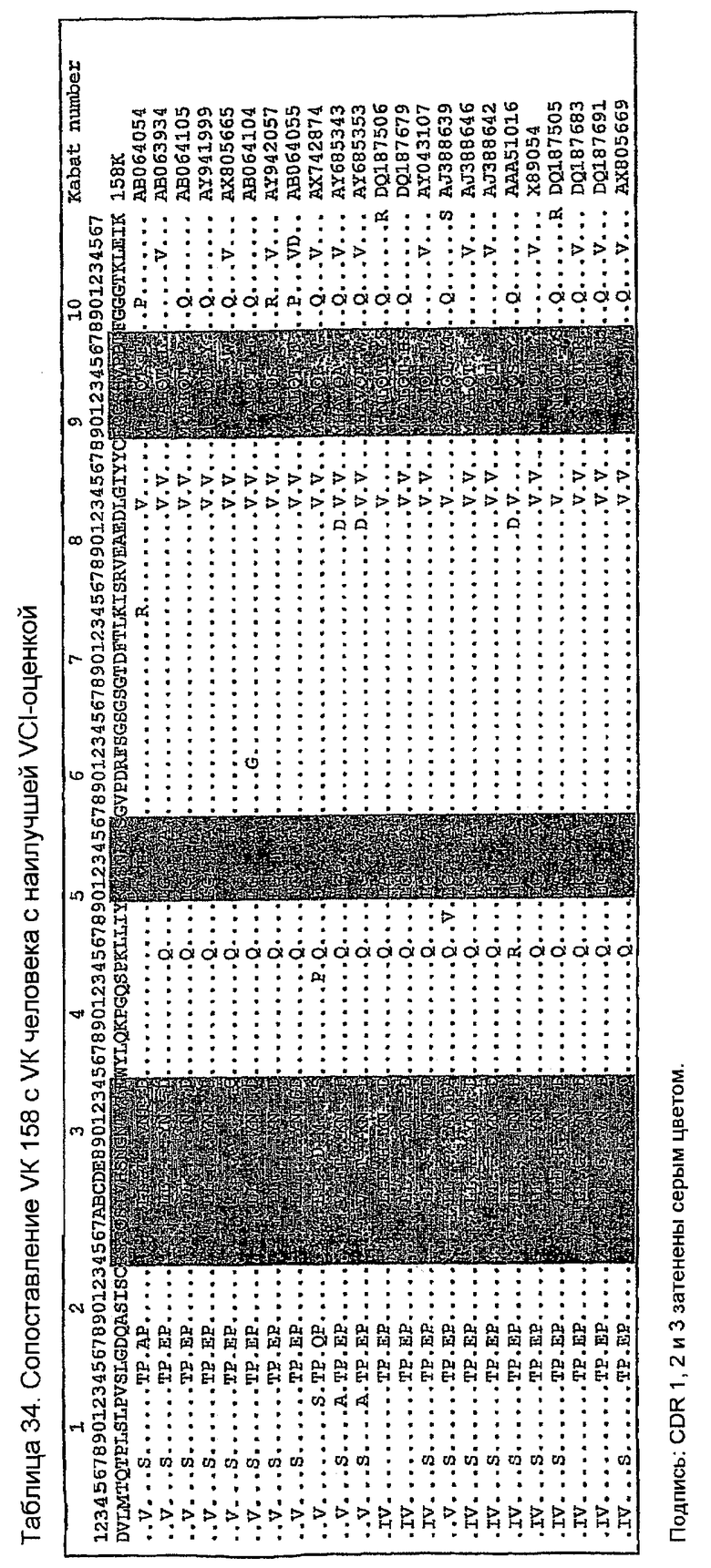
Последовательности VK человека с наивысшей идентичностью с VK 158 в VCI-остатках показаны в таблице 32 вместе с количеством VCI-остатков (оценкой VCI) и остатков FW (оценкой FW), идентичных VK 158. Одиннадцать последовательностей имеют все VCI-остатки, идентичные VK 158. Таблица 33 показывает, что все эти последовательности имеют длины CDR, идентичные VK 158. Таблица 34 ясно показывает их различия, показывая, что K45 сохраняется только в AB064054, который сохраняет также I85. Изменение G100P является неудивительным, так как P100 является обычным, имеющим инцидентность 15% в базе данных VK человека авторов изобретения. Две замены T7S и K74R являются консервативными заменами, а все другие замены являются общими для всех последовательностей в таблице 34. По этим причинам для генерирования 158RКA был выбран AB064054.
12.5 - Генерирование 158RKA
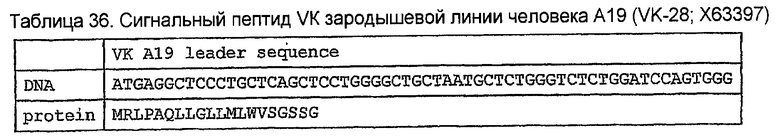
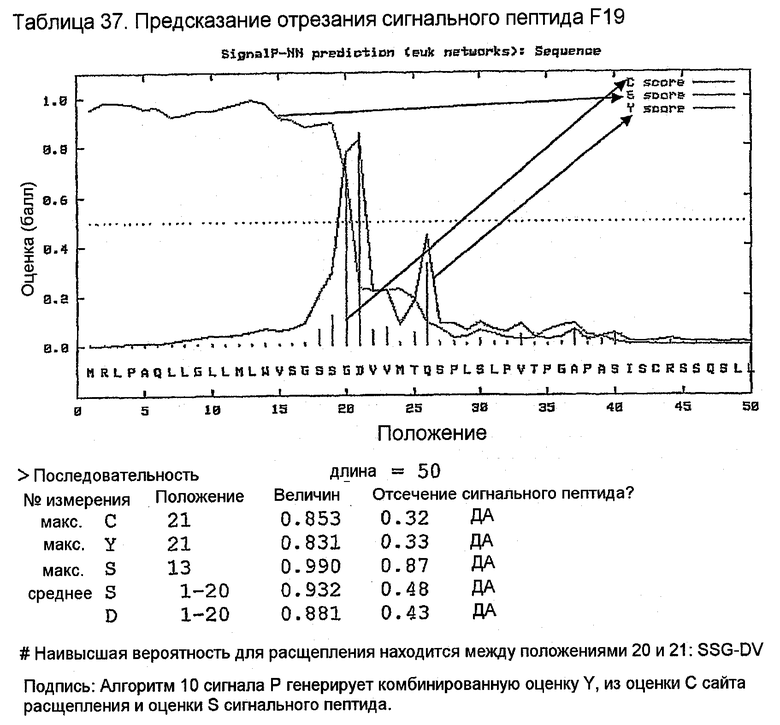
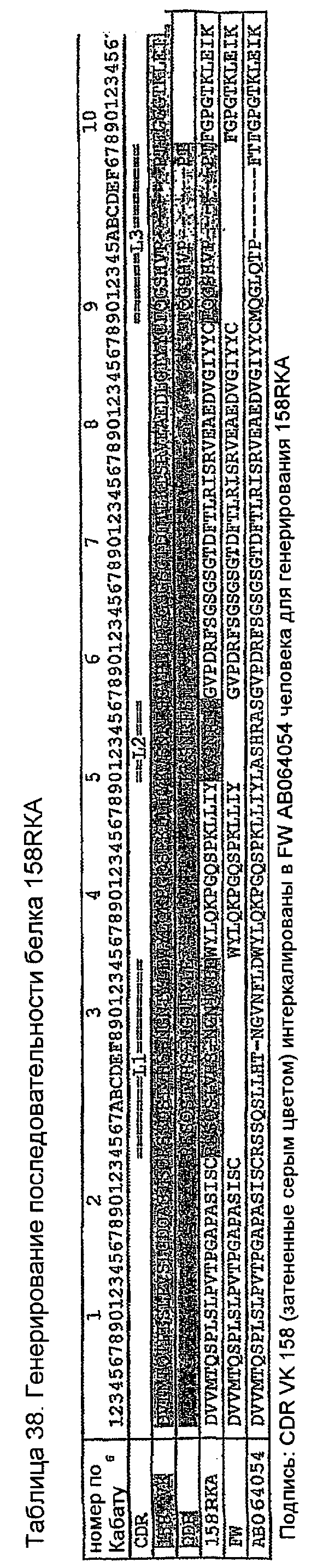
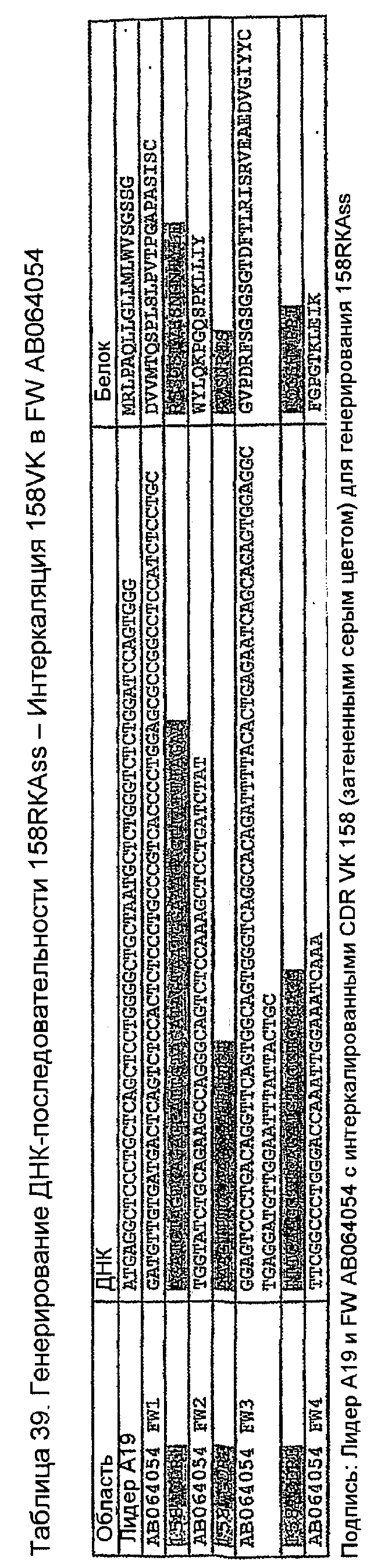
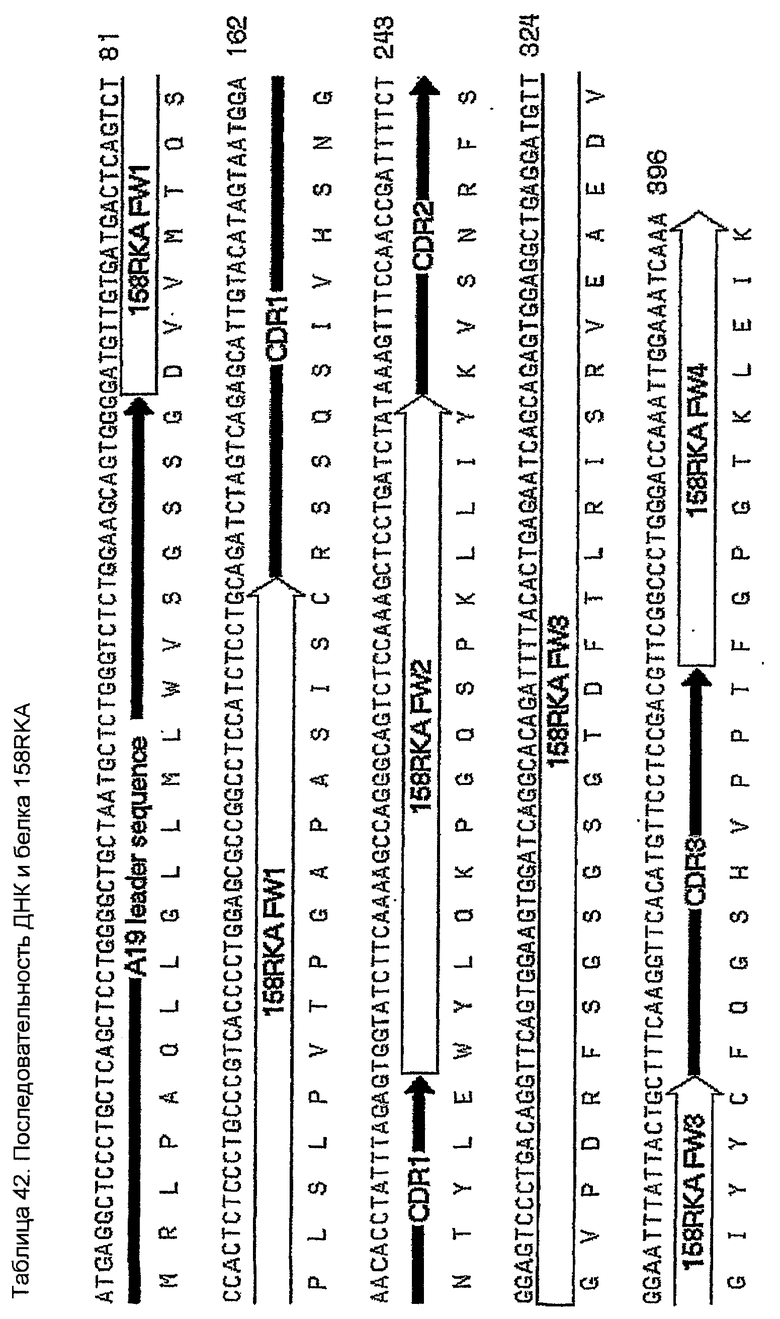
Конструирование 158RКA является просто трансплантацией CDR 1, 2 и 3 из VК 158 в акцепторный FW AВ064054 человека. Ближайшим V-геном зародышевой линии к АВ064054 является А19 (таблица 35), из которого извлекали лидерный пептид (таблица 36). Алгоритм SignalP предсказывал подходящее вырезание (таблица 37) этого лидерного пептида. Таблица 38 показывает генерирование белковой последовательности 158RKA интеркаляцией CDR VK 158 в FW AB064054. Таблица 39 показывает генерирование ДНК-последовательности 158RKAss из природной ДНК-последовательности VK 158 и AB064054. Анализ 158RKAss предсказывал присутствие донорных сайтов сплайсинга, оценки которых показаны в таблице 40. Некодирующие мутации (41) вводили для инактивации этих сайтов и генерирования конечной ДНК-конструкции 158RKA (таблица 42).
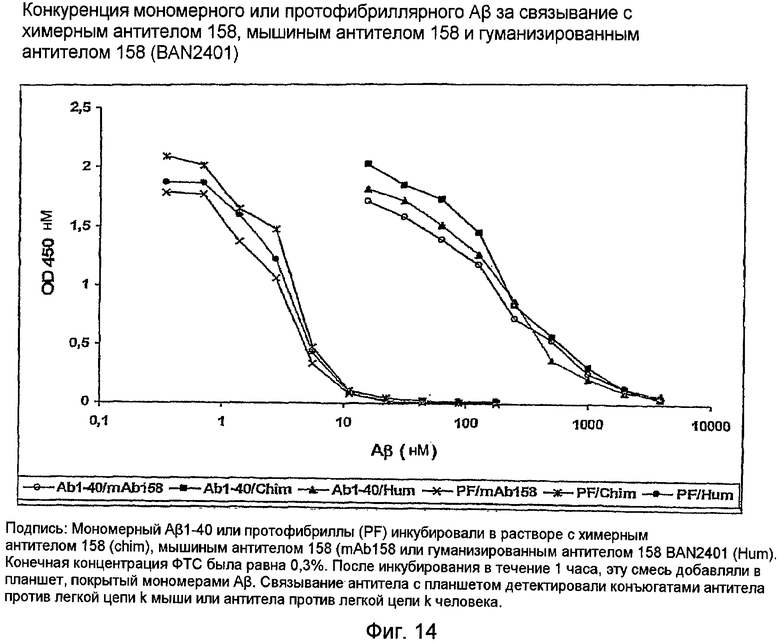
12.6 - Связывающая активность гуманизированного антитела (BAN2401)
Гены 158RKA и 158RHA встраивали в экспрессирующий вектор, содержащий константную область IgG1. Эту конструкцию экспрессировали в клетках COS для генерирования гуманизированного антитела 158. Это гуманизированное антитело испытывали на активность и специфичность связывания в конкурентном ELISA. Это гуманизированное антитело проявляло свойства связывания, идентичные свойствам связывания mAb158 и химерного антитела 158 (см. фигуру 14).
12.7 - Дополнительные мутации в цепях 158RHA и 158RKA
Сравнением V-генов VH зародышевой линии мыши AAK71612 с VH 158 идентифицировали единственную соматическую мутацию A60G в CDR2. Кроме того, молекулярная модель антитела 158 содержит три остатка FW VH в пределах 5 Ангстрем остатков CDR, которые являются не сохраненными в 158RHA. Этими заменами являются D1E, P74A и T82S (таблица 43). Аналогично, имеются два остатка FW VK в пределах 5 Ангстрем остатков CDR, которые являются не сохраненными в 158RKA. Этими заменами являются L3V и G100P (таблица 44). Введение обратных мутаций в положениях VH-I, VH-74, VH-82, VK-3 и VK-100 в 158RHA и 158RKA в гуманизированных версиях 158RHB, 158RHC, 158RHD, 158RKB и 158RKC показано в таблицах 43 и 44.
ССЫЛКИ
Bacskai et al., Nat. Med. 7:369-372, 2001.
Bard et al., Nat. Med. 6:916-919, 2000.
Bayer et al., Neurology 64:94-101, 2005.
Brendza et al., J. Clin. Invest. 115:428-33, 2005.
Chen et al., Nature, 408:975-9, 2000.
Chothia,C. et al, J Mol. Biol., 186:651-663, 1985.
Ester W.P. Science 293, 1449-1459, 2001.
Gullberg et al., Proc. Natl Acad Sci, 101:8420-4, 2004.
Foote,J. et al., J Mol. Biol, 224:487-499, 1992.
Hoshi et al. Proc. Natl Acad. Sci, 100:6370-6375, 2003.
Jarret J.T., Biochemistry, 32, 4693-4697, 1993.
Leatherbarrow R.J. et al., Mol. Immunol. 22, 407, 1985.
Lord et al., Neurobiol. Aging, 27:67-77, 2006.
McLean et al., Ann. Neurol. 46:860-866, 1999.
Morea,V. et al., Methods 20:267-279, 2000.
Mullan et al., Nat Genet. 1:345-347, 1992.
Nielsen,H. et al. Protein Eng 10: 1-6, 1997.
Nilsberth et al., Nat Neurosci. 4:887-893, 2001.
Naslund et al., JAMA, 283:1571-1577, 2000.
Pfeifer et al., Science 298:1379, 2002.
Racke et al., J. Neurosci 25:629-36, 2005.
Schenk D. et al. Nature, 400, 173-177, 1999.
Stenh et al., Ann. Neurol. 58:147-50, 2005.
Walsh D. M. et al., 272, 22364-22372, 1997
Walsh D. M.et al., Nature, 416, 535-9, 2002.
Wilcock et al., J. Neurosci., 23:3745-51, 2003.
Wright A. et al., J. of Immunology, 3393-3402, 1998.
Xu Y. et al. J. Biol. Chem. 269, 3469-3474, 1994.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С ПРОТОФИБРИЛЛАМИ, И ИХ ПРИМЕНЕНИЕ В МЕТОДАХ ТЕРАПИИ И ДИАГНОСТИКИ БОЛЕЗНИ ПАРКИНСОНА, ДЕМЕНЦИИ, АССОЦИИРОВАННОЙ С ОБРАЗОВАНИЕМ ДИФФУЗНЫХ ТЕЛЕЦ ЛЕВИ, И ДРУГИХ АЛЬФА-СИНУКЛЕИНОПАТИЙ | 2011 |
|
RU2555526C2 |
| АНТИТЕЛА ПРОТИВ ГЛОБУЛОМЕРА Аβ, ИХ АНТИГЕНСВЯЗЫВАЮЩИЕ ЧАСТИ, СООТВЕТСТВУЮЩИЕ ГИБРИДОМЫ, НУКЛЕИНОВЫЕ КИСЛОТЫ, ВЕКТОРЫ, КЛЕТКИ-ХОЗЯЕВА, СПОСОБЫ ПОЛУЧЕНИЯ УКАЗАННЫХ АНТИТЕЛ, КОМПОЗИЦИИ, СОДЕРЖАЩИЕ УКАЗАННЫЕ АНТИТЕЛА, ПРИМЕНЕНИЯ УКАЗАННЫХ АНТИТЕЛ И СПОСОБЫ ИСПОЛЬЗОВАНИЯ УКАЗАННЫХ АНТИТЕЛ | 2006 |
|
RU2442793C2 |
| ПРОДУЦИРУЮЩИЕ АНТИТЕЛА МЛЕКОПИТАЮЩИЕ, НЕ ЯВЛЯЮЩИЕСЯ ЧЕЛОВЕКОМ | 2009 |
|
RU2731084C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА И ИХ ПРИМЕНЕНИЯ | 2006 |
|
RU2432362C2 |
| ПРОДУЦИРУЮЩИЕ АНТИТЕЛА МЛЕКОПИТАЮЩИЕ, НЕ ЯВЛЯЮЩИЕСЯ ЧЕЛОВЕКОМ | 2020 |
|
RU2820926C2 |
| ПРОДУЦИРУЮЩИЕ АНТИТЕЛА МЛЕКОПИТАЮЩИЕ, НЕ ЯВЛЯЮЩИЕСЯ ЧЕЛОВЕКОМ | 2009 |
|
RU2559524C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА К β-АМИЛОИДНОМУ ПЕПТИДУ | 2008 |
|
RU2475500C2 |
| АНТИТЕЛА К РЕЦЕПТОРУ КОНЕЧНЫХ ПРОДУКТОВ ГЛУБОКОГО ГЛИКИРОВАНИЯ (RAGE) И ИХ ПРИМЕНЕНИЯ | 2009 |
|
RU2518351C2 |
| БИБЛИОТЕКА FV НА ОСНОВЕ КОМБИНАЦИЙ БЕЛКОВ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2014 |
|
RU2639505C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ АМИЛОИДОЗОВ | 2018 |
|
RU2746812C1 |


























Изобретение относится к биотехнологии и представляет собой антитело или его фрагмент, имеющие высокую аффинность в отношении протофибрилл Аβ. Также представлены композиции, содержащие антитело, способ детектирования протофибрилл Аβ in vitro, а также применения антитела. Изобретение может эффективно использоваться для лечения болезни Альцгеймера, синдрома Дауна, деменции с тельцами Леви и сосудистой деменции. 6 н. и 22 з.п. ф-лы, 14 ил., 44 табл.
1. Антитело или его фрагмент, являющиеся селективными и имеющими высокую аффинность в отношении протофибрилл Аβ человека, причем это антитело или фрагмент в его шести участках CDR имеет следующие консенсусные последовательности:
2. Антитело по п.1, где указанное антитело является моноклональным.
3. Антитело по п.1, где аминокислота пролин в положении 331 в человеческом IgG1 заменена серином или другой полярной аминокислотой.
4. Антитело по п.1, где указанное антитело является антителом класса IgG.
5. Антитело по п.4, где указанное антитело является антителом подкласса IgG1 или IgG4.
6. Антитело по п.5, где указанное антитело является химерой подкласса IgG1 или IgG4, где константная область СН2 или часть СН2 тяжелой цепи произведена из IgG4, а области СН1 и СН3 произведены из IgG1, для уменьшенной активации комплемента.
7. Антитело по п.1, где указанное антитело содержит полную последовательность тяжелой цепи в соответствии с таблицей 31 (SEQ ID NO. 178) и полную последовательность легкой цепи в соответствии с таблицей 42 (SEQ ID NO. 264).
8. Антитело, которое связывается с человеческими Аβ протофибриллами, где антитело содержит тяжелую цепь и легкую цепь, причем тяжелая цепь содержит аминокислотную последовательность 158RHA в таблице 27 (SEQ ID NO. 158), и легкая цепь содержит аминокислотную последовательность 158RKA в таблице 38 (SEQ ID NO. 244).
9. Антитело по п.1, где указанное антитело содержит мутации в тяжелой цепи (VH) в соответствии с таблицей 43 (SEQ ID NO. 265), причем указанные мутации выбраны из (по Kabat): от Е до D позиция 1 (E1D в SEQ ID NO. 265), от А до Р позиция 74 (А75Р в SEQ ID NO. 265) и от S до Т позиция 82А (S84T в SEQ ID NO. 265) и/или мутации в легкой цепи (VK) в соответствии с таблицей 44 (SEQ ID NO. 269), причем указанные мутации выбраны из (по Kabat): от V до L позиция 3 (V3L в SEQ ID NO. 269) и от Р до G позиция 100 (P105G в SEQ ID NO. 269), или комбинации этих мутаций VH и VK.
10. Антитело по п.1, где указанное антитело содержит полную последовательность тяжелой цепи в соответствии с таблицей 31 (SEQ ID NO. 178) и полную последовательность легкой цепи в соответствии с таблицей 42 (SEQ ID NO. 264), за исключением того, что в тяжелую цепь внесена мутация S23A (S42A в SEQ ID NO. 178).
11. Антитело по любому из пп.1 или 8, где указанное антитело является антителом человека или гуманизированным или мутированным антителом для уменьшения антигенности в людях.
12. Антитело по любому из пп.1 или 8, где индекс специфичности между мономерами и протофибриллами Аβ равен по меньшей мере 1:200, как определено конкурентным ELISA.
13. Антитело по п.1, где указанное антитело является антителом мыши.
14. Антитело по п.13, где указанное антитело содержит полную последовательность легкой цепи, закодированную ДНК последовательностью VK 158 в соответствии с таблицей 11 (SEQ ID NO. 97), и полную последовательность тяжелой цепи, закодированную ДНК последовательностью VH 158 в соответствии с таблицей 15 (SEQ ID NO. 106).
15. Композиция, содержащая антитело, определенное в любом из предыдущих пунктов в терапевтически эффективном количестве, и фармацевтически приемлемый буфер, где композиция является селективной и имеет высокую аффинность в отношении протофибрилл Аβ человека.
16. Композиция по п.15, дополнительно включающая антибактериальный агент.
17. Композиция по любому из пп.15 или 16, где эта композиция является лиофилизированной.
18. Композиция по п.17, где эта композиция лиофилизирована вместе с эксципиентом для увеличения стабильности этого антитела во время и после лиофилизации.
19. Композиция по п.18, где этим эксципиентом является маннит или трегалоза.
20. Способ детектирования протофибрилл Аβ in vitro, включающий стадии:
- добавления антитела, определенного в любом из пп.1-14, в биологическую пробу, содержащую протофибриллы Аβ или предположительно содержащую протофибриллы Аβ,
- измерения концентрации комплекса, образованного между указанной протофибриллой Аβ и указанным антителом.
21. Способ по п.20, где указанным способом детектирования является иммуноанализ.
22. Способ по п.20, где указанным способом детектирования является анализ лигирования на основе близости.
23. Антитело по любому из пп.1 или 8 для применения при диагностике заболевания Альцгеймера.
24. Антитело по любому из пп.1 или 8 для применения при диагностике синдрома Дауна, деменции с тельцами Леви или сосудистой деменции.
25. Применение антитела, определенного в любом из пп.1-14, или композиции, определенной в любом из пп.15-19, для получения лекарственного средства для лечения болезни Альцгеймера.
26. Применение антитела, определенного в любом из пп.1-14, или композиции, определенной в любом из пп.15-19, для получения лекарственного средства для лечения синдрома Дауна, деменции с тельцами Леви, сосудистой деменции.
27. Композиция по п.15 для применения при лечении болезни Альцгеймера.
28. Композиция по п.15 для применения при лечении синдрома Дауна, деменции с тельцами Леви, сосудистой деменции.
| WO 2005123775 А1, 29.12.2005 | |||
| Kayed R, et al, "Common structure of soluble amyloid oligomers implies common mechanism of pathogenesis" | |||
| Science | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Chromy BA, et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Biochemistry | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Кудинова Н.В | |||
| и др | |||
| В-АМИЛОИД: БОЛЕЗНЬ АЛЬЦГЕЙМЕРА И В-АМИЛОИДОЗЫ МОЗГА | |||
| Биохимия, 1999, 64, с 899-905. | |||
Авторы
Даты
2011-09-20—Публикация
2007-03-23—Подача