Перекрестная ссылка на родственные заявки
Настоящая заявка испрашивает приоритет Международной заявки PCT/US 2014/022984, поданной 11 марта 2014 года, которая испрашивает приоритет Временной заявки на патент США № 61/790231, поданной 15 марта 2013 года, каждая из них тем самым и включается в качестве ссылки во всей своей полноте.
Информация относительно исследований, финансируемых федеральным правительством
Нет
Имена участников объединенного исследовательского соглашения
Нет
Включение в качестве ссылки материала поданного на компакт-диске
Нет
Уровень техники
Область техники, к которой относится изобретение
Настоящее изобретение относится к амин-функциональным полиамидам. Амин-функциональные полиамиды содержат аминовые и аммониевые группы вдоль полимерной цепи. Кроме того, настоящее изобретение относится к применению амин-функциональных полиамидов в качестве фармацевтических агентов и в фармацевтических композициях.
Мукозит определяется как воспаление и/или изъязвление мембраны слизистой оболочки в пищеварительном тракте. Мукозит может возникать в желудке, кишечнике и в ротовой полости. Расстройство отличается разрушением слизистой оболочки, что приводит в результате к покраснению, отеку и/или образованию язвенных повреждений.
Мукозит слизистой оболочки полости рта является обычным токсичным повреждением, ограничивающим дозу при лекарственной и радиационной терапии рака; он возникает до некоторой степени у более трети всех пациентов, принимающих лекарственную терапию против новообразований. У гранулоцитопенических пациентов, изъязвления, которые сопровождают мукозит, часто являются воротами для входа собственных бактерий ротовой полости, приводящих к сепсису или бактериемии. Имеется примерно один миллион случаев мукозита слизистой оболочки полости рта в год в Соединенных Штатах. Мукозит также включает мукозит, который развивается самопроизвольно у здорового пациента, не принимающего противораковую терапию, как в случае афтозного стоматита или язвы рта. Необходима улучшенная терапия для лечения мукозита.
Хирургическая раневая инфекция (SSI) представляет собой инфекцию, связанную с хирургической процедурой.
Послеоперационные SSI являются главным источником расстройств, а реже смерти хирургических пациентов (Nichols RL, 2001). The Guideline for Prevention of Surgical Site Infection (1999) приводит рекомендации для предотвращения SSI.
Предоперационные меры, включая правильную подготовку пациента, антисептику для хирургического персонала, перераспределение хирургического персонала, который проявляет признаки передающегося инфекционного заболевания, и противомикробную профилактику.
Меры во время операции, включая соответствующую вентиляцию операционного помещения, очистку и дезинфекцию поверхностей в хирургической окружающей среде, отбор микробиологических проб, стерилизацию хирургических инструментов, соответствующую хирургическую одежду и простыни или салфетки, и соответствующую асептику и хирургическую технику.
Соответствующую послеоперационную обработку хирургического шва, включая стерильные перевязки и мытье рук до и после смены повязок.
Непрерывное наблюдение хирургической раны во время процесса заживления.
Несмотря на эти рекомендации, SSI развивается примерно у 1-3 из каждых 100 пациентов после операции (CDC.gov, 2011). Эти инфекции могут давать в результате большие осложнения, которые увеличивают стоимость и продолжительность послеоперационного пребывания в госпитале. Соответственно, необходимы новые подходы к борьбе SSI.
Кистозный фиброз (CF) представляет собой генетическое заболевание, вызываемое мутацией в регуляторе трансмембранной проводимости кистозного фиброза (CFTR), которая дает в результате аномально густую и липкую слизь (Yu Q, et al, 2012). Густая, липкая слизь пациента с CF приводит к ослаблению прозрачности слизи и к легочной инфекции. Хронические инфекции дыхательных путей являются одним из наиболее распространенных и ослабляющих проявлений CF (Tummler B, C Kiewitz, 1999). Застойная слизь становится почвой для размножения бактерий, подобных Pseudomonas aeruginosa, которые вызывают хронические инфекции дыхательных путей (Moreau-Marquis S, GA O'Toole и BA Stanton, 2009). Несмотря на использование традиционной антибактериальной терапии для пациентов с CF, большинство пациентов с CF подвержены хронической инфекции P. aeruginosa в подростковом и взрослом возрасте, что приводит к увеличению заболеваемости и смертности (Hoiby N, B Frederiksen B, T Pressler, 2005). При хронической инфекции P. aeruginosa, P. aeruginosa образует биопленки, что приводит в результате к повышению толерантности к антибиотикам и к повышению сложности лечения (Yu Q, et al., 2012). Необходимы эффективные новые способы лечения для борьбы с воздействиями бактериальной инфекции и образования биопленки у пациентов с CF.
Определения
Как используется в настоящем документе, термин "амино" обозначает функциональную группу, имеющую атом азота и 1-2 атома водорода. "Амино", как правило, может использоваться в настоящем документе для описания первичного, вторичного или третичного амина, и специалисты в данной области смогут легко определить какая именно идентификация имеется в виду в контексте, в котором этот термин используется в настоящем описании. Термин "амин" или "аминовая группа" или "аммиачная группа" обозначает функциональную группу, содержащую атом азота, полученную из аммиака (NH3). Аминовые группы предпочтительно представляют собой первичные амины, это означает, что азот связан с двумя атомами водорода и с одной группой заместителем, включающей замещенную или незамещенную алкильную или арильную группу или алифатическую или ароматическую группу. Аминовые группы могут представлять собой вторичные амины, это означает, что азот связан с одним атомом водорода и двумя группами заместителями, включающими замещенные или незамещенные алкильные или арильные группы или алифатическую или ароматическую группу, как определено ниже. Аминовые группы могут представлять собой третичные амины, это означает, что азот связан с тремя группами заместителями, включающими замещенные или незамещенные алкильные или арильные группы или алифатическую или ароматическую группу. Аминовые группы могут также представлять собой четвертичные амины, это означает, что обозначенная аминовая группа связана с четвертой группой, давая в результате положительно заряженную аммониевую группу.
Как используется в настоящем документе, термин "амидная группа" обозначает функциональную группу, содержащую карбонильную группу, связанную с азотом. "Карбонильная группа" обозначает функциональную группу, содержащую атом углерода, связанный двойной связью с атомом кислорода, представленным как (C=O).
Термин "алкан" обозначает насыщенный углеводород, связанный с помощью одинарных связей. Алканы могут быть линейными и разветвленными. "Циклоалканы" представляют собой насыщенные углеводородные кольца, связанные с помощью одинарных связей.
Как используется в настоящем документе, термин "(C1-C10)алкил" обозначает насыщенный прямоцепной или разветвленный или циклический углеводород, состоящий в основном из 1-10 атомов углерода и из соответствующего количества атомов водорода. Как правило, прямоцепные или разветвленные группы имеют от одного до десяти атомов углерода, или чаще, от одного до пяти атомов углерода. Иллюстративные (C1-C10)алкильные группы включают метил (представленный -CH3), этил (представленный -CH2-CH3), н-пропил, изопропил, н-бутил, изобутил, и тому подобное. Другие (C1-C10)алкильные группы будут очевидны специалистам в данной области, имеющим преимущество настоящего описания.
Как используется в настоящем документе, термин "(C2-C9)гетероалкил" обозначает насыщенный прямоцепной или разветвленный или циклический углеводород, состоящий в основном из 2-10 атомов, где 2-9 атомов представляют собой углерод, а оставшийся атом (атомы) выбирают из группы, состоящей из азота, серы и кислорода. Иллюстративные (C2-C9)гетероалкильные группы будут очевидны специалистам в данной области, имеющим преимущество настоящего описания.
Как используется в настоящем документе, термин "(C3-C10)циклоалкил" обозначает неароматическую насыщенную углеводородную группу, образующую по меньшей мере одно кольцо, состоящее в основном из 3-10 атомов углерода и из соответствующего количества атомов водорода. (C3-C10)циклоалкильные группы могут быть моноциклическими или мультициклическими. Индивидуальные кольца мультициклических циклоалкильных групп могут иметь различные способы соединения, например, быть слитыми, соединяться с помощью мостика, представлять собой спиро соединения, и тому подобное, в дополнение к замещению с помощью ковалентной связи. Иллюстративные (C3-C10)циклоалкильные группы включают циклопропил, циклобутил, циклопентил, циклогексил, норборнанил, бицикло-октанил, октагидропенталенил, спиродеканил, циклопропил, замещенный циклобутилом, циклобутил, замещенный циклопентилом, циклогексил, замещенный циклопропилом, и тому подобное. Другие (C3-C10)циклоалкильные группы будут очевидны специалистам в данной области, имеющим преимущество настоящего описания.
Как используется в настоящем документе, термин "(C2-C9)гетероциклоалкил" обозначает неароматическую группу, имеющую 3-10 атомов, которые образуют по меньшей мере одно кольцо, где 2-9 кольцевых атомов представляют собой углерод, а оставшийся кольцевой атом (атомы) выбирают из группы, состоящей из азота, серы и кислорода. (C2-C9)гетероциклоалкильные группы могут быть моноциклическими или мультициклическими. Индивидуальные кольца таких мультициклических гетероциклоалкильных групп могут иметь различные способы соединения, например, быть слитыми, соединяться с помощью мостика, представлять собой спиро соединения, и тому подобное, в дополнение к замещению с помощью ковалентной связи. Иллюстративные (C2-C9)гетероциклоалкильные группы включают пирролидинил, тетрагидрофуранил, дигидрофуранил, тетрагидропиранил, пиранил, тиопиранил, азиридинил, азетидинил, оксиранил, метилендиоксил, хроменил, барбитурил, изоксазолидинил, 1,3-оксазолидин-3-ил, изотиазолидинил, 1,3-тиазолидин-3-ил, 1,2-пиразолидин-2-ил, 1,3-пиразолидин-l-ил, пиперидинил, тиоморфолинил, 1,2-тетрагидротиазин-2-ил, 1,3-тетрагидротиазин-3-ил, тетрагидротиадиазинил, морфолинил, 1,2-тетрагидродиазин-2-ил, 1,3-тетрагидродиазин-l-ил, тетрагидроазепинил, пиперазинил, пиперизин-2-онил, пиперизин-3-онил, хроманил, 2-пирролинил, 3-пирролинил, имидазолидинил, 2-имидазолидинил, 1,4-диоксанил, 8-азабицикло[3.2.1]октанил, 3-азабицикло[3.2.1]октанил, 3,8-диазабицикло [3.2.1] октанил, 2,5-диазабицикло [2.2.1] гептанил, 2,5-диазабицикло[2.2.2]октанил, октагидро-2H-пиридо[1,2-a]пиразинил, 3-азабицикло[4.1.0]гептанил, 3-азабицикло[3.1.0]гексанил, 2-азаспиро[4.4]нонанил, 7-окса-l-аза-спиро[4.4]нонанил, 7-азабицикло[2.2.2]гептанил, октагидро-1H-индолил, и тому подобное. (C2-C9)гетероциклоалкильная группа, как правило, присоединяется к главной структуре через атом углерода или атом азота. Другие (C2-C9)гетероциклоалкильные группы будут очевидны специалистам в данной области, имеющим преимущество настоящего описания.
Термин "алифатическая группа" или "алифатический" обозначает неароматическую группу, состоящую из углерода и водорода, и может необязательно включать одну или несколько двойных и/или тройных связей. Алифатическая группа может быть прямоцепной, разветвленной или циклической, и, как правило, она содержит в пределах примерно от одного и примерно до 24 атомов углерода.
Термин "арильная группа" может использоваться взаимозаменяемо с "арилом", "арильным кольцом", "ароматическим соединением", "ароматической группой" и "ароматическим кольцом". Арильные группы включают карбоциклические ароматические группы, как правило, с шестью - четырнадцатью кольцевыми атомами углерода. Арильные группы также включают гетероарильные группы, которые, как правило, имеют пять - четырнадцать кольцевых атомов, с одним или несколькими гетероатомами, выбранными из азота, кислорода и серы.
Как используется в настоящем документе, термин "(С6-С14)арил" обозначает ароматическую функциональную группу, имеющую 6-14 атомов углерода, которые образуют по меньшей мере одно кольцо.
Как используется в настоящем документе, термин "(C2-C9)гетероарил" обозначает ароматическую функциональную группу, имеющую 5-10 атомов, которые образуют по меньшей мере одно кольцо, где 2-9 кольцевых атомов представляют собой углерод, а оставшийся кольцевой атом (атомы) выбирают из группы, состоящей из азота, серы и кислорода. (C2-C9)гетероарильные группы могут быть моноциклическими или мультициклическими. Индивидуальные кольца таких мультициклических гетероарильных групп могут иметь различные способы соединения, например, быть слитыми, и тому подобное, в дополнение к замещению с помощью ковалентной связи. Иллюстративные (C2-C9)гетероарильные группы включают фурил, тиенил, тиазолил, пиразолил, изотиазолил, оксазолил, изоксазолил, пирролил, триазолил, тетразолил, имидазолил, 1,3,5-оксадиазолил, 1,2,4-оксадиазолил, 1,2,3-оксадиазолил, 1,3,5-тиадиазолил, 1,2,3-тиадиазолил, 1,2,4-тиадиазолил, пиридил, пиримидил, пиразинил, пиридазинил, 1,2,4-триазинил, 1,2,3-триазинил, 1,3,5-триазинил, пиразоло[3,4-b]пиридинил, циннолинил, птеридинил, пуринил, 6,7-дигидро-5H-[l]пиридинил, бензо[b]тиофенил, 5,6,7,8-тетрагидро-хинолин-3-ил, бензоксазолил, бензотиазолил, бензизотиазолил, бензизоксазолил, бензимидазолил, тианафтенил, изотианафтенил, бензофуранил, изобензофуранил, изоиндолил, индолил, индолизинил, индазолил, изохинолил, хинолил, фталазинил, хиноксалинил, хиназолинил и бензоксазинил, и тому подобное. (C2-C9)гетероарильная группа, как правило, присоединяется к главной структуре через атом углерода, однако специалисты в данной области увидят, когда определенные другие атомы, например, кольцевые гетероатомы, могут быть присоединены к главной структуре. Другие (C2-C9)гетероарильные группы будут очевидны специалистам в данной области, имеющим преимущество настоящего описания.
Как используется в настоящем документе, термин "алкиламин" обозначает (C1-C10)алкил, содержащий первичную, вторичную или третичную аминовую группу вместо одного атома водорода, представленный как (C1-C10)алкиламин и ((C1-C10)алкил)2 амин.
Термин "сложный алкиловый эфир" обозначает (C1-C10)алкил, содержащий сложноэфирную группу вместо одного атома водорода, представленный как -O(O)C-(C1-C10)алкил.
Термин "алкиловая кислота" обозначает (C1-C10)алкил, содержащий группу карбоновой кислоты вместо одного атома водорода, представленный как (C1-C10)алкил-COOH.
Термин "алифатическая кислота" обозначает кислоту из неароматических углеводородов, представленную как (C3-C10)циклоалкил-COOH.
Термин "галоген" обозначает ион фтора (F), хлора (Cl, брома (Br), йода (I) или астатина (At).
Термин "метокси" обозначает (C1)алкил, содержащий кислород вместо одного атома водорода, представленный как -(O)CH3.
Термин "полиол" обозначает спирт, содержащий множество гидроксильных (-OH) групп. "Замещенный" обозначает замещение углерода в алкильных, гетероциклических или арильных группах одним или несколькими неуглеродными заместителями. Неуглеродные заместители выбирают из азота, кислорода и серы.
"Незамещенный" обозначает группу, состоящую только из атомов водорода и углерода.
Термин "полимер" обозначает молекулу, состоящую из повторяющихся единиц. Термин "повторяющаяся единица" или "мономер" обозначает группу в полимере, которая повторяется или появляется множество раз в полимере. Полимер может представлять собой сополимер, если повторяющиеся единицы или "сомономеры" являются химически и структурно отличными друг от друга.
Термин "фармацевтически приемлемый анион" обозначает анион, который является пригодным для фармацевтического использования. Фармацевтически приемлемые анионы включают, но, не ограничиваясь этим, галогениды, карбонат, бикарбонат, сульфат, бисульфат, гидроксид, нитрат, персульфат, сульфит, ацетат, аскорбат, бензоат, цитрат, дигидрогенцитрат, гидрогенцитрат, оксалат, сукцинат, тартрат, таурохолат, гликохолат и холат.
Термин "фармацевтически приемлемая конечная группа" обозначает конечную группу, которая является пригодной для фармацевтического использования. Примеры фармацевтически приемлемых конечных групп включают, но, не ограничиваясь этим, H, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил, (C1-C10)алкиламин, -O(O)C-(C1-C10)алкил, (C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амид, гуанидино группу, группу гуанидиния хлорида, гуанидинобензольную группу, дигидрокси группу и полиэтиленгликолевую группу.
"Гуанидино группа" представлена Формулой (A):
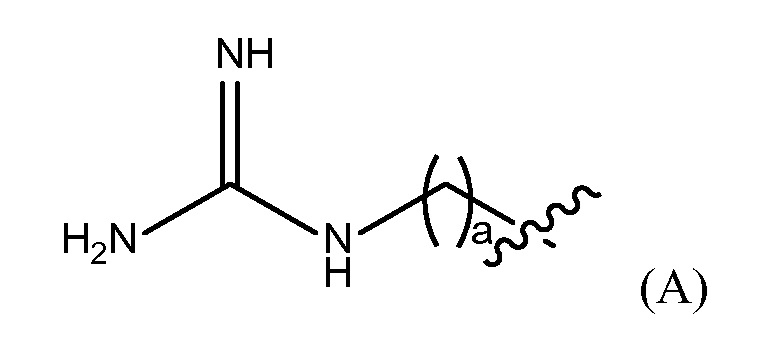
где a представляет собой целое число от 0 до 25,
"группа гуанидиния хлорида" представлена Формулой (B),
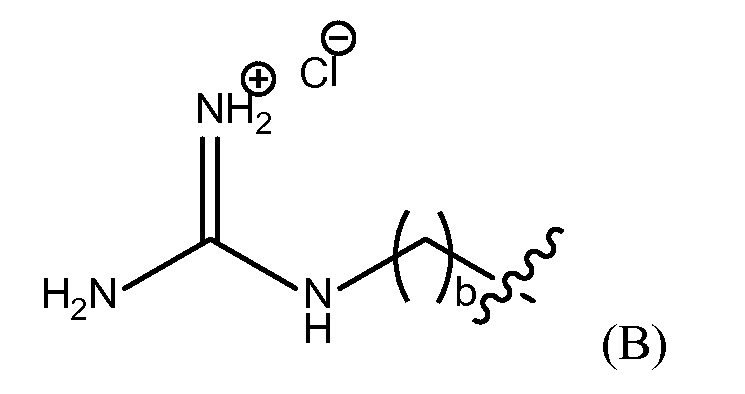
где b представляет собой целое число от 0 до 25,
"гуанидинобензольная группа" представлена Формулой (C),
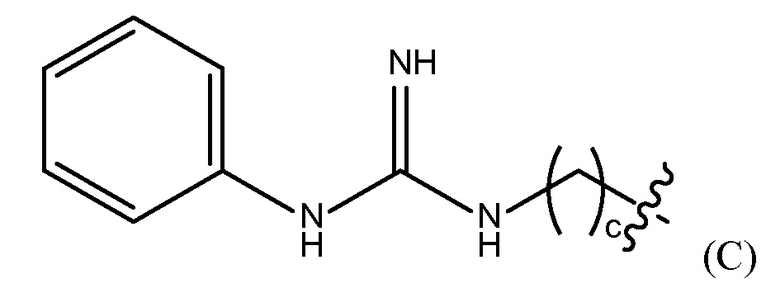
где c представляет собой целое число от 0 до 25,
"дигидргокси группа" представлена Формулой (D),
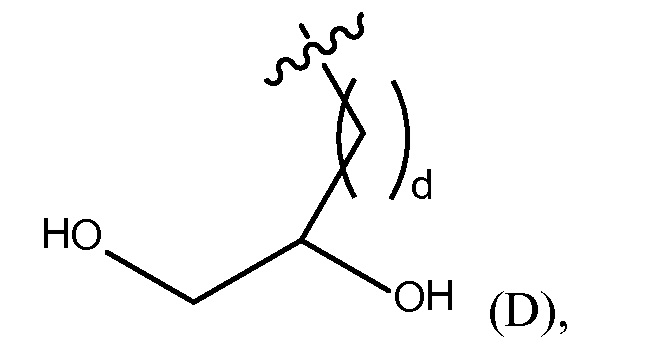
где d представляет собой целое число от 0 до 25, или
"полиэтиленгликолевая группа" (PEG) представлена Формулой (E)
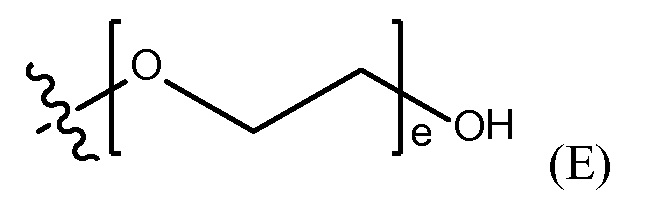
где e представляет собой целое число от 1 до 400.
Термин "эффективное количество" описанных амин-функциональных полиамидов представляют собой количество достаточное для достижения терапевтического и/или профилактического воздействие на конкретное состояние, которое лечится, такое как количество, которое дает в результате предотвращение или уменьшение симптомов, связанных с мукозитом, мукозитом слизистой оболочки полости рта, инфекцией и хирургической раневой инфекцией, и инфекцией легких, связанной с кистозным фиброзом. Точное количество описанных амин-функциональных полиамидов, которое вводится, будет зависеть от типа и тяжести мукозита или инфекции, которая лечится, и от характеристик индивидуума, таких как общее состояние здоровья, возраст, пол, масса тела и толерантность по отношению к лекарственным средствам.
Предшествующий уровень техники
Нет
Сущность изобретения
В одном из аспектов настоящего изобретения, амин-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (I):
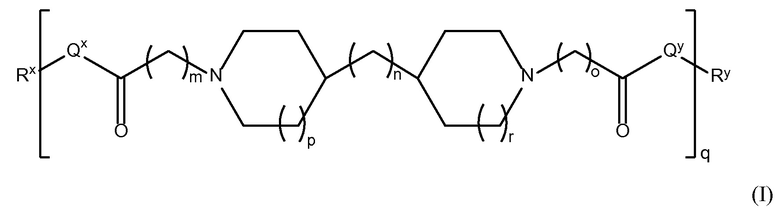
где:
i) m равно 0, 1, 2 или 3;
ii) n равно 0, 1, 2 или 3;
iii) o равно 0, 1, 2 или 3;
iv) p равно 0 или 1;
v) r равно 0 или 1;
vi) q представляет собой целое число от 1 до 400;
vii) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
viii) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
ix) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу.
В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (II):
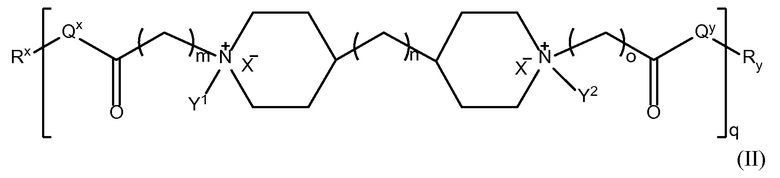
где:
i) m равно 0, 1, 2 или 3;
ii) n равно 0, 1, 2 или 3;
iii) o равно 0, 1, 2 или 3;
iv) p равно 0 или 1;
v) r равно 0 или 1;
vi) q представляет собой целое число от 1 до 400;
vii) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
viii) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
ix) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу;
x) X-, каждый, независимо представляет собой галоген или любой фармацевтически приемлемый анион;
xi) Y1 и Y2, каждый, независимо представляют собой H или (C1-C10)алкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из (C1-C10)алкила, (C2-C9)гетероалкила, (C3-C10)циклоалкила, (C2-C9)гетероциклоалкила, (C6-C14)арила, (C2-C9)гетероарила, (C1-C10)алкиламина, -S-O-(C1-C10)алкила, -O(O)C-(C1-C10)алкила, -(C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амида, дигидрокси группы, представленной Формулой (D),
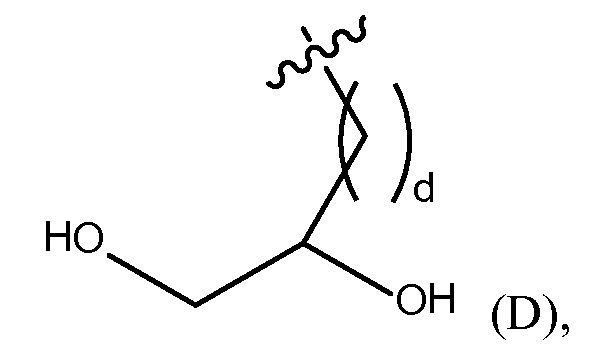
где d представляет собой целое число от 0 до 25, или
полиэтиленгликолевой группы, представленной Формулой (E)
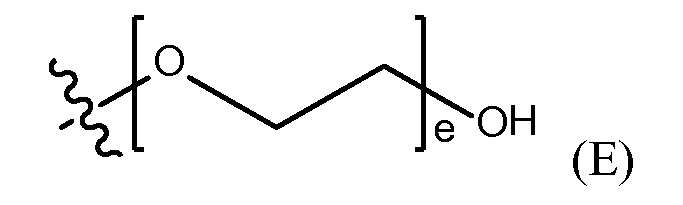
где e представляет собой целое число от 1 до 25.
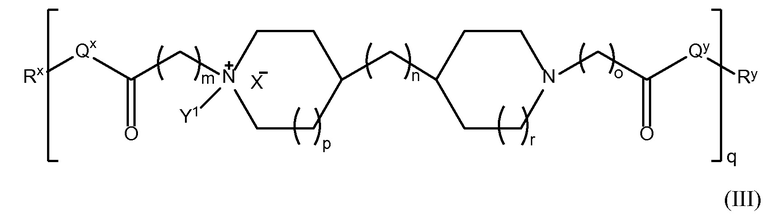
В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (III):
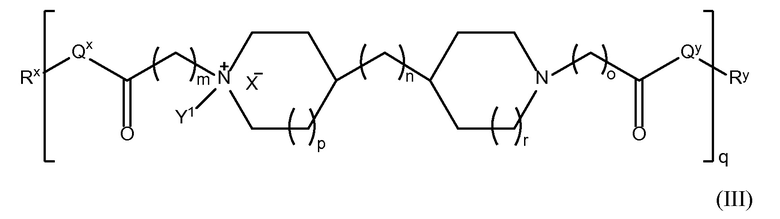
где:
i) m равно 0, 1, 2 или 3;
ii) n равно 0, 1, 2 или 3;
iii) o равно 0, 1, 2 или 3;
iv) p равно 0 или 1;
v) r равно 0 или 1;
vi) q представляет собой целое число от 1 до 400;
vii) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
viii) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
ix) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу;
x) X- представляет собой галоген или любой фармацевтически приемлемый анион;
xi) Y1 представляет собой H или (C1-C10)алкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из (C1-C10)алкила, (C2-C9)гетероалкила, (C3-C10)циклоалкила, (C2-C9)гетероциклоалкила, (C6-C14)арила, (C2-C9)гетероарила, (C1-C10)алкиламина, -S-O-(C1-C10)алкила, -O(O)C-(C1-C10)алкила, -(C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амида, дигидрокси группы, представленной Формулой (D),
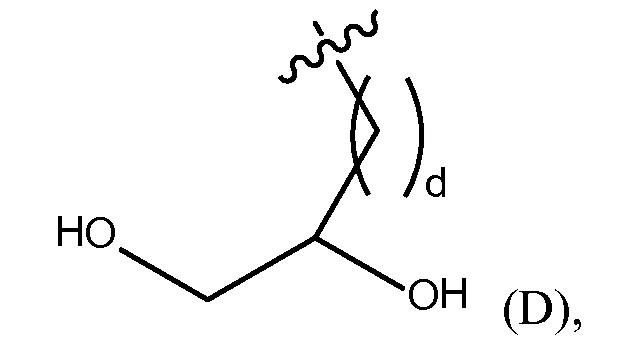
где d представляет собой целое число от 0 до 25, или
полиэтиленгликолевой группы, представленной Формулой (E),
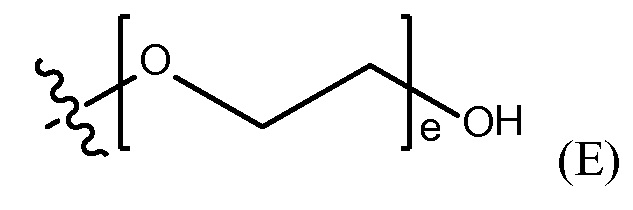
где e представляет собой целое число от 1 до 400.
В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (IV):
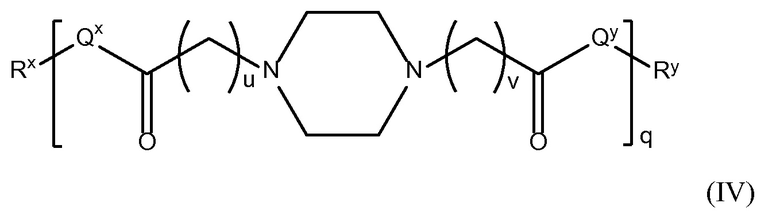
где:
i) u равно 0, 1, 2, или 3;
ii) v равно 0, 1, 2, или 3;
iii) q представляет собой целое число от 1 до 400;
iv) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
v) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
vi) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу.
В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (V):
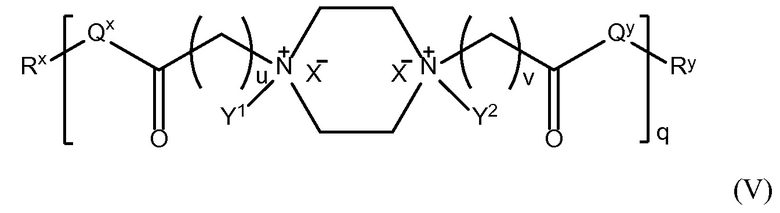
где:
i) u равно 0, 1, 2 или 3;
ii) v равно 0, 1, 2 или 3;
iii) q представляет собой целое число от 1 до 400;
iv) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
v) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
vi) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу;
vii) X- независимо представляет собой галоген или любой фармацевтически приемлемый анион,
viii) Y1 и Y2 независимо представляют собой H или (C1-C10)алкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из (C1-C10)алкила, (C2-C9)гетероалкила, (C3-C10)циклоалкила, (C2-C9)гетероциклоалкила, (C6-C14)арила, (C2-C9)гетероарила, (C1-C10)алкиламина, -S-O-(C1-C10)алкила, -O(O)C-(C1-C10)алкила, -(C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амида, дигидрокси группы, представленной Формулой (D),
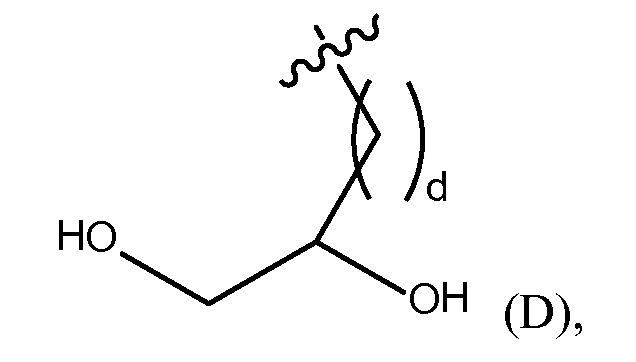
где d представляет собой целое число от 0 до 25, или
полиэтиленгликолевой группы, представленной Формулой (E),
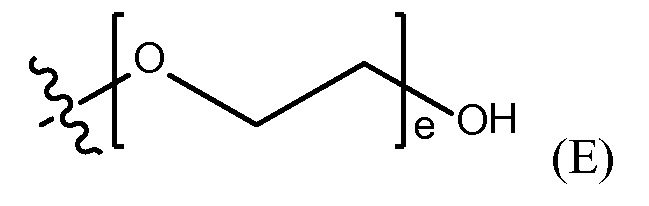
где e представляет собой целое число от 1 до 400.
В одном из аспектов настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (I). В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (II). В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (III). В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (IV). В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (V).
В одном из аспектов настоящего изобретения, амин-функциональные полиамиды используются для лечения мукозита. В другом аспекте настоящего изобретения, амин-функциональные полиамиды используются для лечения мукозита слизистой оболочки полости рта. В другом варианте осуществления настоящего изобретения, амин-функциональные полиамиды используются для лечения инфекций. В другом варианте осуществления настоящего изобретения, амин-функциональные полиамиды используются для лечения хирургической раневой инфекции. В другом варианте осуществления настоящего изобретения, амин-функциональные полиамиды используются для лечения инфекции легких, связанной с кистозным фиброзом. В другом варианте осуществления настоящего изобретения, амин-функциональные полиамиды используются для лечения легочной инфекции P. aeruginosa и у пациентов с CF. В другом варианте осуществления настоящего изобретения, амин-функциональные полиамиды используются для лечения легочной инфекции P. aeruginosa и у пациентов с CF, где образуются биопленки.
Еще один аспект настоящего изобретения представляет собой способ лечения состояния, выбранного из мукозита, мукозита слизистой оболочки полости рта и инфекций, включающий введение амин-функционального полиамида.
Краткое описание нескольких видов чертежей
Нет
Подробное описание изобретения
Настоящее изобретение относится к новым амин-функциональным полиамидам. Полимеры или сополимеры амин-функциональных полиамидов имеют различные структуры и содержат аминовые и аммониевые группы вдоль полимерной цепи.
Амин-функциональные полиамиды содержат повторяющиеся единицы амидных групп и аминовых групп; аминовые группы могут представлять собой группы вторичного, третичного и четвертичного аммония.
Кроме того, амин-функциональные полиамиды по настоящему изобретению имеют различные молекулярные массы.
Амин-функциональные полиамиды являются водорастворимыми.
Настоящее изобретение относится к фармацевтическим композициям, содержащим полимеры или сополимеры амин-функциональных полиамидов. Настоящее изобретение также относится к способам лечения и предотвращения мукозита и инфекции, включая SSI, легочные инфекции у пациентов с CF и легочные инфекции C. aeruginosa у пациентов с CF с образованием биопленки или без него, с помощью амин-функциональных полиамидов. Амин-функциональные полиамиды и фармацевтические композиции, содержащие полимеры или сополимеры амин-функциональных полиамидов, могут вводиться в виде множества дозированных форм и посредством системного или местного введения.
Настоящее изобретение относится к применению амин-функциональных полиамидов и фармацевтических композиций, содержащих полимеры или сополимеры амин-функциональных полиамидов в качестве противоинфекционных агентов. Амин-функциональные полиамиды и фармацевтические композиции, содержащие полимеры или сополимеры амин-функциональных полиамидов, можно использовать для лечения бактериальных, грибковых и вирусных инфекций, включая мукозит, инфекции и, конкретно, хирургические раневые инфекции, легочные инфекции, связанные с CF, и легочные инфекции C. aeruginosa у пациентов с CF с образованием биопленки или без него.
Амин-функциональные полиамиды можно также использовать для нанесения покрытия на поверхности различных медико-биологических устройств и другие поверхностей для предотвращения инфекций.
В одном из аспектов настоящего изобретения, амин-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (I):
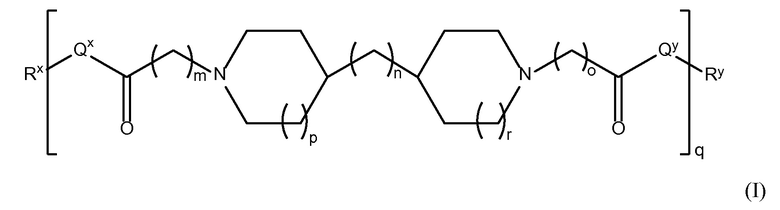
где:
i) m равно 0, 1, 2 или 3;
ii) n равно 0, 1, 2 или 3;
iii) o равно 0, 1, 2 или 3;
iv) p равно 0 или 1;
v) r равно 0 или 1;
vi) q представляет собой целое число от 1 до 400;
vii) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
viii) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
ix) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу.
В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (II):
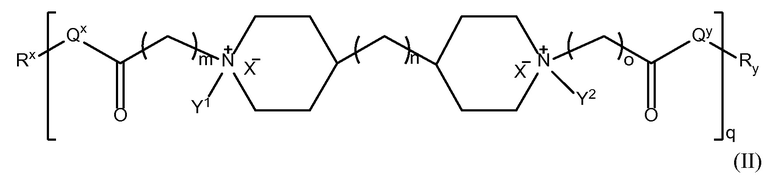
где:
i) m равно 0, 1, 2 или 3;
ii) n равно 0, 1, 2 или 3;
iii) o равно 0, 1, 2 или 3;
iv) p равно 0 или 1;
v) r равно 0 или 1;
vi) q представляет собой целое число от 1 до 400;
vii) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
viii) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
ix) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу;
x) X-, каждый, независимо представляет собой галоген или любой фармацевтически приемлемый анион;
xi) Y1 и Y2, каждый, независимо представляют собой H или (C1-C10)алкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из (C1-C10)алкила, (C2-C9)гетероалкила, (C3-C10)циклоалкила, (C2-C9)гетероциклоалкила, (C6-C14)арила, (C2-C9)гетероарила, (C1-C10)алкиламина, -S-O-(C1-C10)алкила, -O(O)C-(C1-C10)алкила, -(C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амида, дигидрокси группы, представленной Формулой (D),
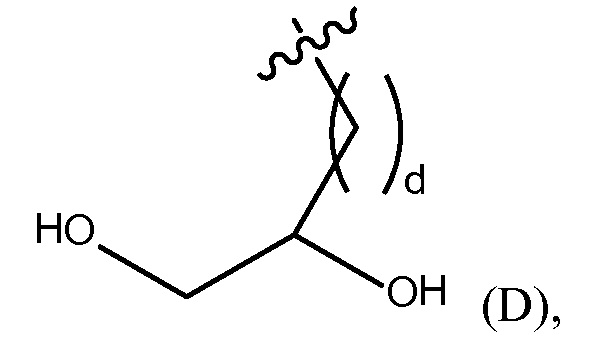
где d представляет собой целое число от 0 до 25, или
полиэтиленгликолевой группы, представленной Формулой (E)
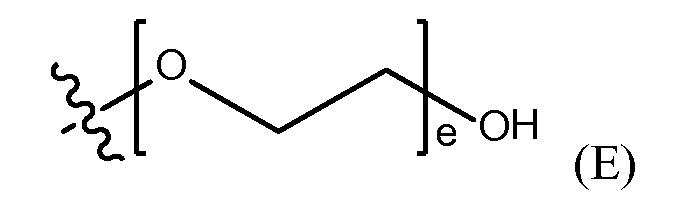
где e представляет собой целое число от 1 до 25.
В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (III):
где:
i) m равно 0, 1, 2 или 3;
ii) n равно 0, 1, 2 или 3;
iii) o равно 0, 1, 2 или 3;
iv) p равно 0 или 1;
v) r равно 0 или 1;
vi) q представляет собой целое число от 1 до 400;
vii) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
viii) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
ix) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу;
x) X- представляет собой галоген или любой фармацевтически приемлемый анион;
xi) Y1 представляет собой H или (C1-C10)алкил, необязательно замещенный одним или нескольким заместителями, выбранными из группы, состоящей из (C1-C10)алкила, (C2-C9)гетероалкила, (C3-C10)циклоалкила, (C2-C9)гетероциклоалкила, (C6-C14)арила, (C2-C9)гетероарила, (C1-C10)алкиламина, -S-O-(C1-C10)алкила, -O(O)C-(C1-C10)алкила, -(C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амида, дигидрокси группы, представленной Формулой (D),

где d представляет собой целое число от 0 до 25, или
полиэтиленгликолевой группы, представленной Формулой (E)
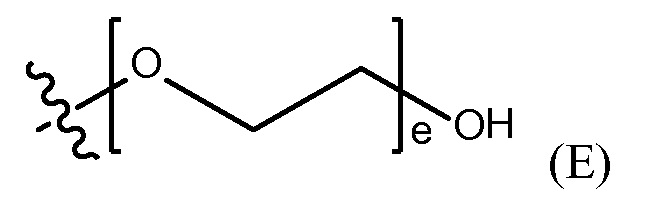
где e представляет собой целое число от 1 до 400.
В предпочтительных вариантах осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой соединения Формулы (I), Формулы (II) или Формулы (III), где как p, так и r равны 0 и как p, так и r равны 1. В других предпочтительных вариантах осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой соединения Формулы (I), Формулы (II) или Формулы (III), где n, p и r, все, равны 0, n равно 0 и как p, так r равны 1, и n равно 3 и как p, так и r равны 1.
В предпочтительном варианте осуществления настоящего изобретения, амид-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (1).
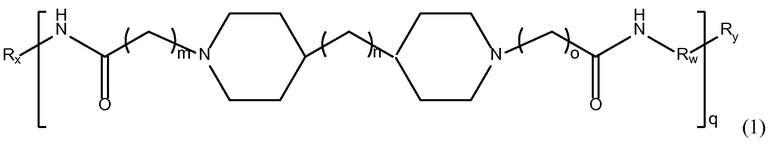
где Rw представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил.
В другом предпочтительном варианте осуществления настоящего изобретения, амид-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (2) или Формулы (3):
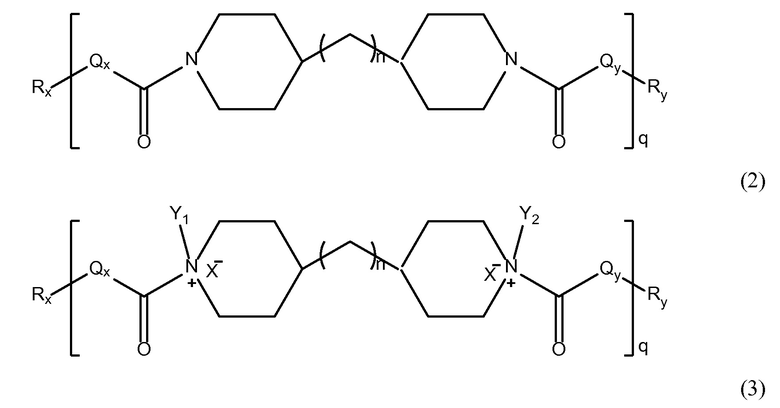
В другом предпочтительном варианте осуществления настоящего изобретения, амин-функциональные полиамиды состоят из соединения, содержащего структуру Формулы (I), Формулы (II), Формулы (III), Формулы (1), Формулы (2) или Формулы (3), где Rx и Ry независимо выбирают из метокси группы, гуанидино группы или гуанидинобензольной группы.
В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (IV):
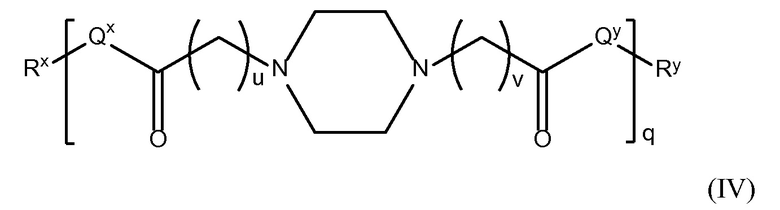
где:
i) u равно 0, 1, 2 или 3;
ii) v равно 0, 1, 2 или 3;
iii) q представляет собой целое число от 1 до 400;
iv) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
v) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
vi) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу.
В другом аспекте настоящего изобретения, амид-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (V):
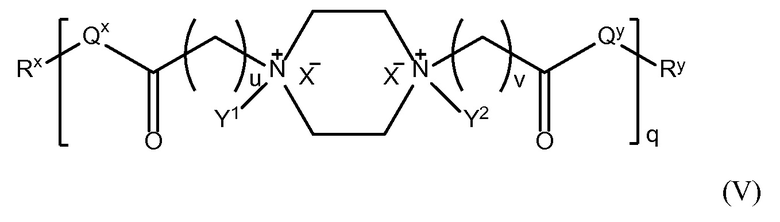
i) u равно 0, 1, 2 или 3;
ii) v равно 0, 1, 2 или 3;
iii) q представляет собой целое число от 1 до 400;
iv) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
v) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
vi) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу;
vii) X- независимо представляет собой галоген или любой фармацевтически приемлемый анион,
vi) Y1 и Y2 независимо представляют собой H или (C1-C10)алкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из (C1-C10)алкила, (C2-C9)гетероалкила, (C3-C10)циклоалкила, (C2-C9)гетероциклоалкила, (C6-C14)арила, (C2-C9)гетероарила, (C1-C10)алкиламина, -S-O-(C1-C10)алкила, -O(O)C-(C1-C10)алкила, -(C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амида, дигидрокси группы, представленной Формулой (D),
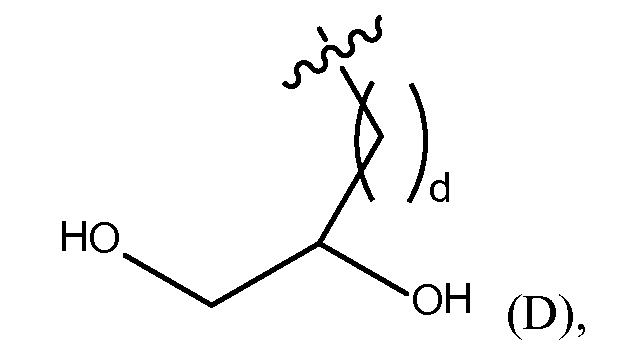
где d представляет собой целое число от 0 до 25 25, или
полиэтиленгликолевой группы, представленной Формулой (E)
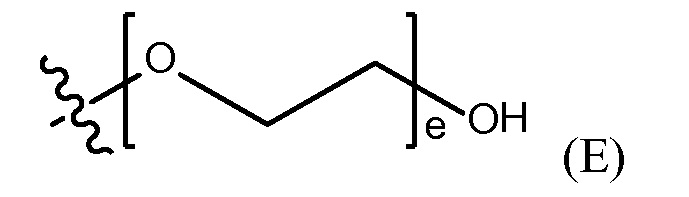
где e представляет собой целое число от 1 до 400.
В предпочтительном варианте осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой соединения Формулы (IV) или Формулы (V), где как u и, так v равны 2.
В предпочтительном варианте осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой соединение, содержащее структуру Формулы (4).
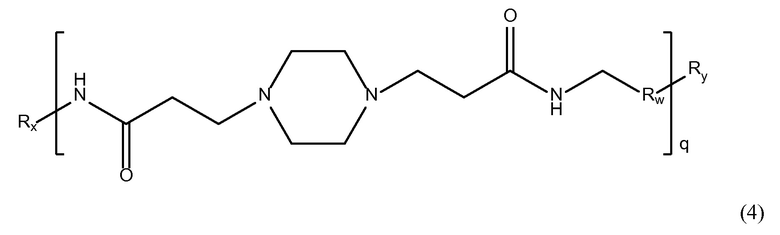
В одном из аспектов настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (I). В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (II). В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (III). В предпочтительных вариантах осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (1), Формулы (2) или Формулы (3). В другом предпочтительном варианте осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (I), Формулы (II), Формулы (III), Формулы (1), Формулы (2) или Формулы (3), где Rx и Ry независимо выбирают из метокси группу, гуанидино группу или гуанидинобензольную группу.
В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (IV). В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (V). В предпочтительном варианте осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (4).
В другом предпочтительном варианте осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (I), (II), (III), (IV), (V), (1), (2), (3) или (4), для применения при лечении или предотвращении состояний, выбранных из мукозита, мукозита слизистой оболочки полости рта и инфекции. В другом предпочтительном варианте осуществления, амин-функциональные полиамиды представляют собой фармацевтическую композицию, содержащую соединение, содержащее структуру Формулы (I), (II), (III), (IV), (V), (1), (2), (3) или (4), для применения при лечении или предотвращении хирургической раневой инфекции, легочной инфекции, связанной с кистозным фиброзом, легочной инфекции Pseudomonas aeruginosa и легочной инфекции Pseudomonas aeruginosa, легочной инфекции, где присутствуют биопленки.
В одном из вариантов осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой полимеры.
В некоторых вариантах осуществления, полимеры могут содержать мономер, включающий соединение, имеющее повторяющиеся единицы в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4).
В одном из вариантов осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой сополимеры. В некоторых вариантах осуществления, сополимеры могут содержать мономер, содержащий соединение, имеющее по меньшей мере одну единицу в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4), которая сополимеризуется с одним или несколькими другими сомономерами или олигомерами или другими полимеризуемыми группами. Неограничивающие примеры соответствующих сомономеров, которые можно использовать по отдельности или в сочетании по меньшей мере с одной единицей в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4), с образованием амин-функциональных полиамидов, представлены в Таблице 1.
В одном из вариантов осуществления настоящего изобретения, амин-функциональные полиамиды представляют собой полимеры или сополимеры, состоящие примерно из 1 - примерно 400 повторяющихся единиц, в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4). В одном из аспектов настоящего изобретения, амин-функциональные полиамиды представляют собой полимеры или сополимеры, состоящие примерно из 1 - примерно 200 повторяющихся единиц, в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4). В другом аспекте настоящего изобретения, амин-функциональные полиамиды представляют собой полимеры или сополимеры, состоящие примерно из 1 - примерно 100 повторяющихся единиц, в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4). В некоторых вариантах осуществления, амин-функциональные полиамиды представляют собой полимеры или сополимеры, состоящие примерно из 1 - примерно 50 повторяющихся единиц, в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4). В дополнительном варианте осуществления, амин-функциональные полиамиды представляют собой полимеры или сополимеры, состоящие примерно из 1 - примерно 25 повторяющихся единиц, в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4). В другом варианте осуществления, амин-функциональные полиамиды представляют собой полимеры или сополимеры, состоящие примерно из 1 - примерно 10 повторяющихся единиц, в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4). В других вариантах осуществления, амин-функциональные полиамиды представляют собой полимеры или сополимеры, состоящие примерно из 5 примерно - 40 повторяющихся единиц, в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4). В одном из вариантов осуществления, амин-функциональные полиамиды представляют собой полимеры или сополимеры, состоящие примерно из 5 примерно - 30 повторяющихся единиц, в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4). В другом варианте осуществления, амин-функциональные полиамиды представляют собой полимеры или сополимеры, состоящие примерно из 5 примерно - 25 повторяющихся единиц, в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4). В другом варианте осуществления, амин-функциональные полиамиды представляют собой полимеры или сополимеры, состоящие примерно из 5 примерно - 10 повторяющихся единиц, в соответствии с любой из формул (I), (II), (III), (IV), (V), (1), (2), (3) или (4).
В одном из аспектов настоящего изобретения, амин-функциональные полиамиды имеют молекулярную массу меньше примерно чем 10000 г/моль. В другом аспекте настоящего изобретения, амин-функциональные полиамиды имеют молекулярную массу меньше примерно чем 9000 г/моль. В дополнительном аспекте настоящего изобретения, амин-функциональные полиамиды имеют молекулярную массу меньше примерно чем 8000 г/моль. В другом аспекте настоящего изобретения, амин-функциональные полиамиды имеют молекулярную массу меньше примерно чем 7000 г/моль.
В одном из аспектов настоящего изобретения, амин-функциональные полиамиды независимо необязательно имеют окончания (Rx и Ry) в виде фармацевтически приемлемой конечной группой.
Репрезентативные примеры фармацевтически приемлемых конечных групп будут понятны специалистам в данной области, они включают H, (C1-C10)алкил, (C2-C0)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил, (C1-C10)алкиламин, -O(O)C-(C1-C10)алкил, (C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амид, гуанидино группу представленную Формулой (A)
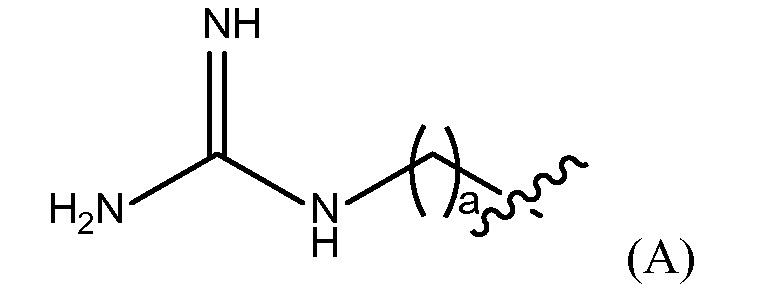
где a представляет собой целое число от 0 до 25,
группу гуанидиния хлорида, представленную Формулой (B),
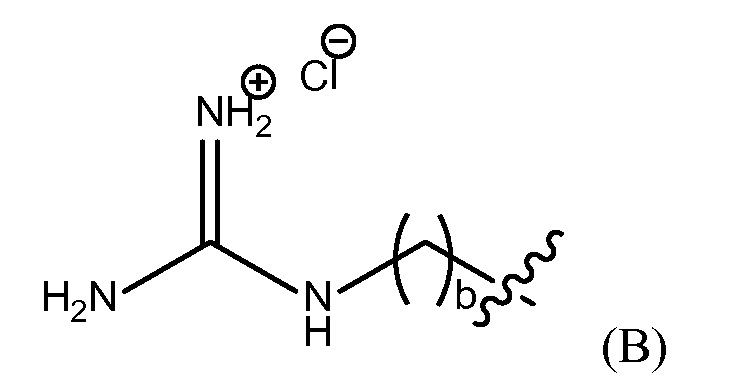
где b представляет собой целое число от 0 до 25, гуанидинобензольную группу, представленную Формулой (C),
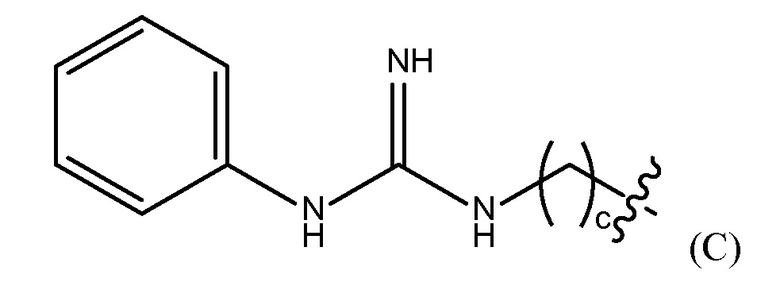
где c представляет собой целое число от 0 до 25,
дигидрокси группу, представленную Формулой (D),
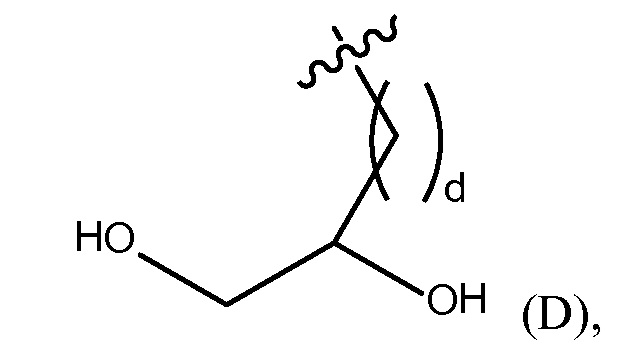
где d представляет собой целое число от 0 до 25, или полиэтиленгликолевую группу, представленную Формулой (E)
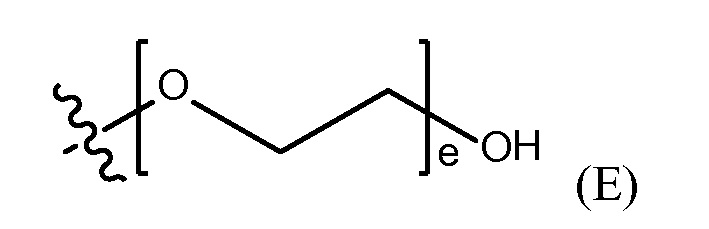
где e представляет собой целое число от 1 до 400.
Количество повторяющихся единиц и молекулярная масса амин-функциональных полиамидов контролируются посредством синтеза соединения. Способы получения предпочтительных амин-функциональных полиамидов по настоящему изобретению и контроля количества повторяющихся единиц и молекулярной массы описаны в Примере 3.
Амин-функциональные полиамиды
дипиперидин
биспропановая
кислота-N,N'-диметил-1,3-диаминопропан)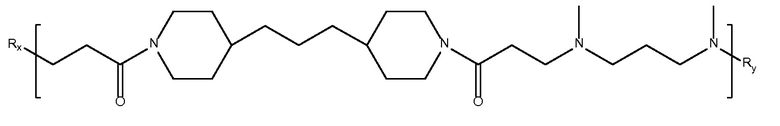
дипиперидин
биспропановая кислота-4,4'-триметилен
дипиперидин)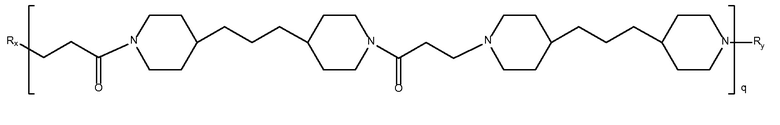
дипиперидин
биспропановая
кислота-пиперазин)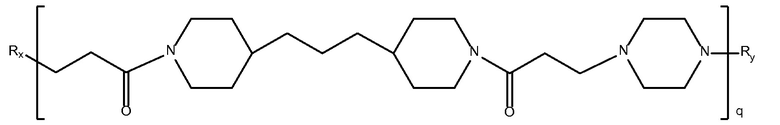
триметилен
дипиперидин
биспропановая
кислота-диаминоэтан)
Mw<10K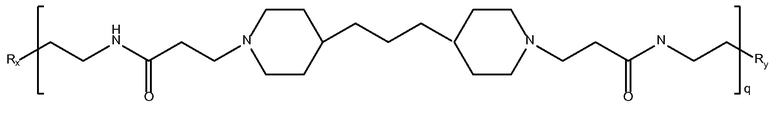
дипиперидин
биспропановая кислота-диаминопропан)
Mw<10K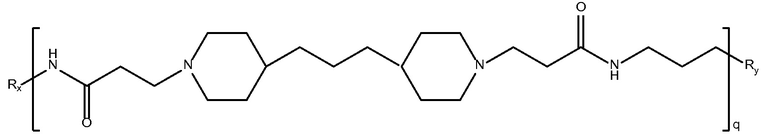
дипиперидин
биспропановая кислота-диаминопропан)
Mw>10K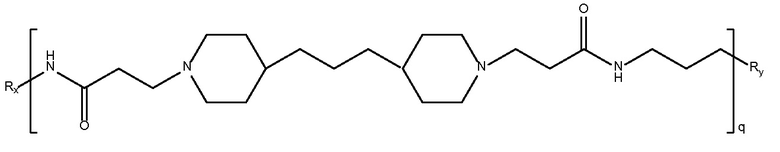
дипиперидин
биспропановая кислота-диаминопропан)
Mw 1650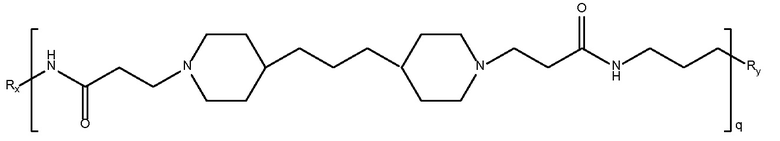
дипиперидин
биспропановая кислота-диаминопропан)
Mw 7,7K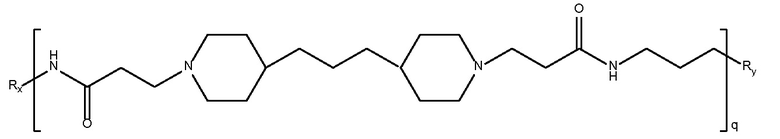
дипиперидин
биспропановая кислота-диаминопропан)
Mw 3K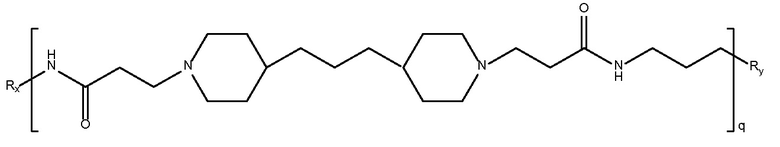
дипиперидин
биспропановая кислота-диаминопропан)
Mw 5K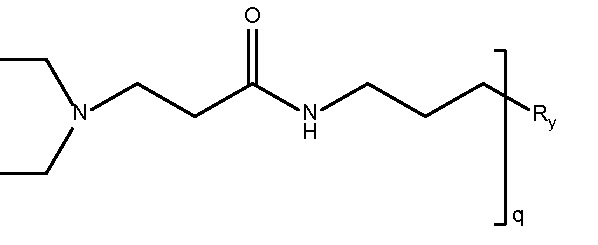
дипиперидин
биспропановая кислота-диаминопропан),
Mw 3250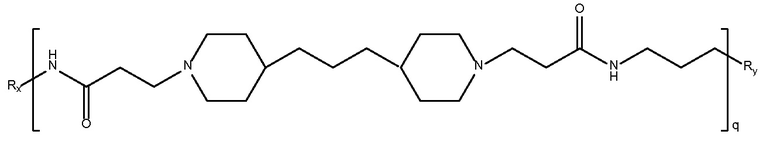
дипиперидин
биспропановая кислота-диаминопропан),
Mw 4700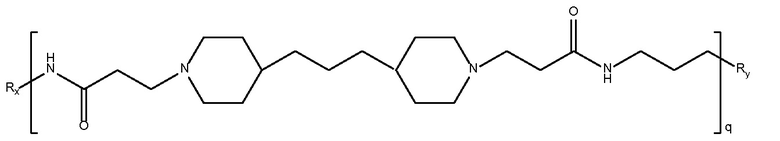
дипиперидин
биспропановая кислота-диаминопропан),
Mw 2500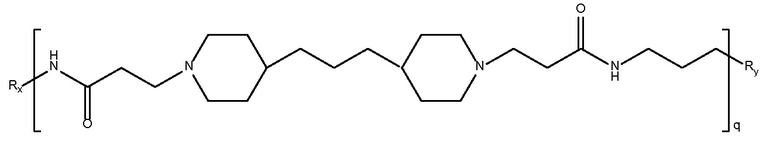
дипиперидин
биспропановая кислота-диаминопропан)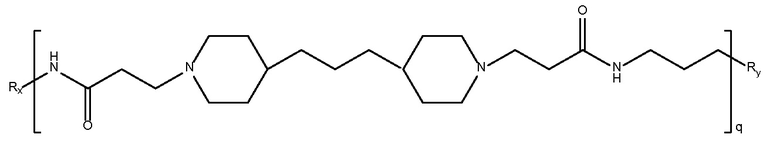
дипиперидин
биспропановая кислота-диаминопропан)
Mw 1400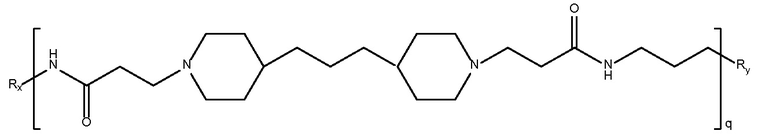
дипиперидин
биспропановая кислота-диаминобутан)
Mw <10K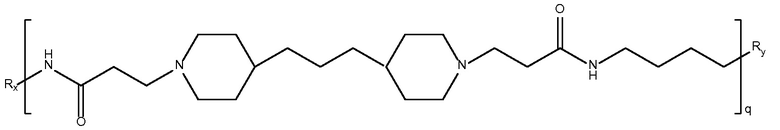
Дипиперидин
биспропановая кислота-диаминобутан)
Mw>10K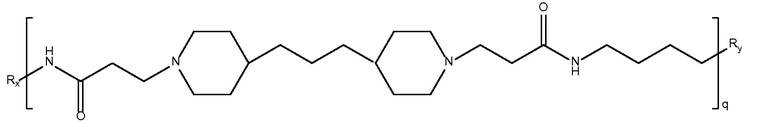
дипиперидин
биспропановая кислота-диаминотриPEG)
Mw<10K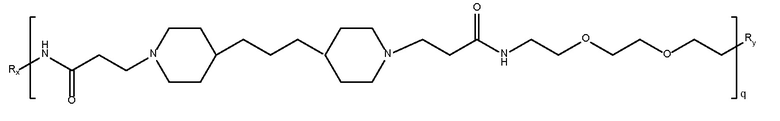
дипиперидин
биспропановая кислота-диаминотриPEG)
Mw>10K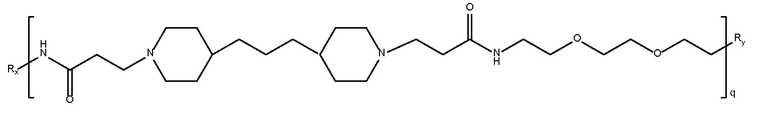
дипиперидин
биспропановая кислота-N(2-аминоэтил)-диаминоэтан)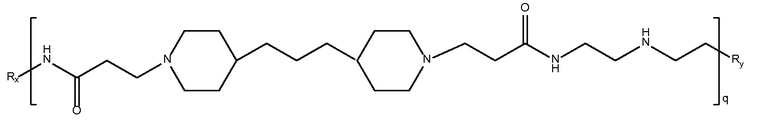
дипиперидин
биспропановая кислота-2,2'-диамино диэтиламин)
Mw 5,5K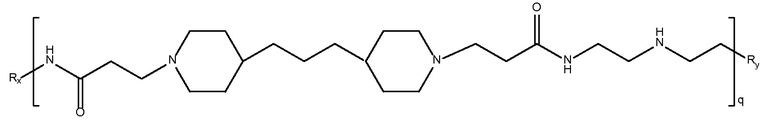
триметилен
дипиперидин
биспропановая кислота-2,2'-диамино диэтиламин)
Mw~14000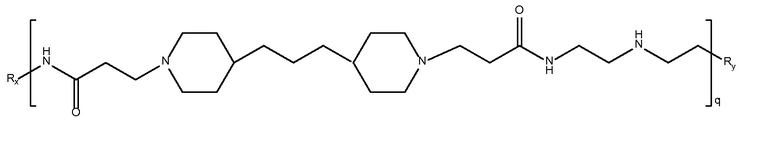
триметилен
дипиперидин
биспропановая кислота-1,4-бензиламин)
Mw<10K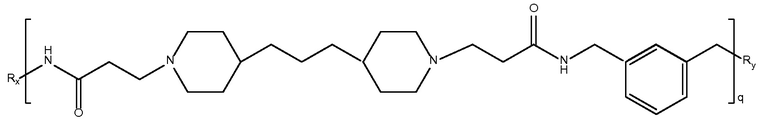
дипиперидин
биспропановая кислота-N(3-аминопропил)-1,3-пропандиамин)
Mw<10K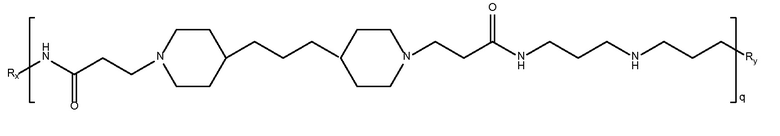
дипиперидин
биспропановая кислота-3,3'-диамино-N-
метил-дипропиламин)
Mw<10K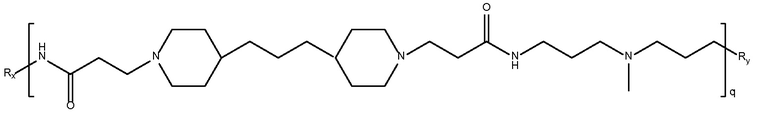
дипиперидин
биспропановая кислота-2,2'-диамино-N-метил-диэтиламин)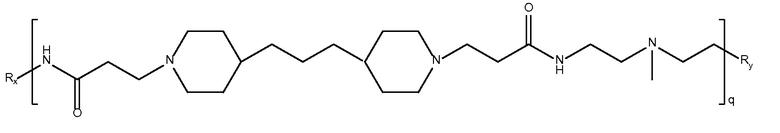
биспропановая кислота-1,2-бис(2-аминоэтокси)этан)
Mw<10K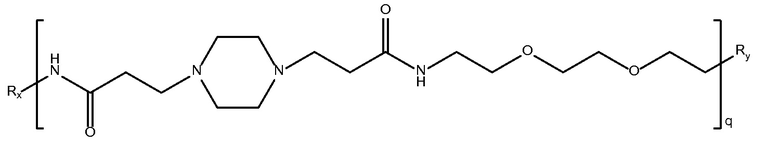
биспропановая кислота-2,2-диаминодиэтиламин)
Mw<10K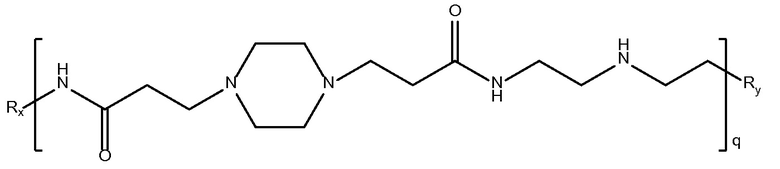
биспропановая кислота-N-метил-2,2-диаминодиэтиламин)
Mw<10K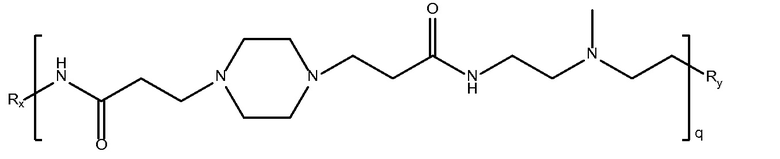
биспропановая кислота-N(3-аминопропил)-1,3-пропандиамин)
Mw<10K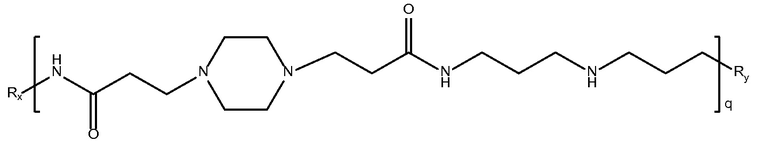
биспропановая кислота-3,3'-диамино-N-метил-дипропиламин)
Mw<10K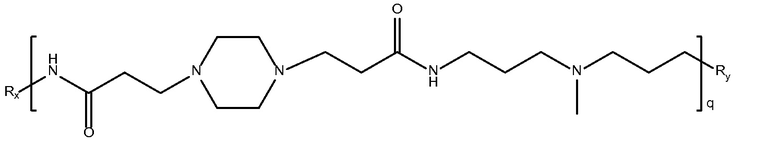
биспропановая кислота-1,3-диаминопропан)
Mw~3700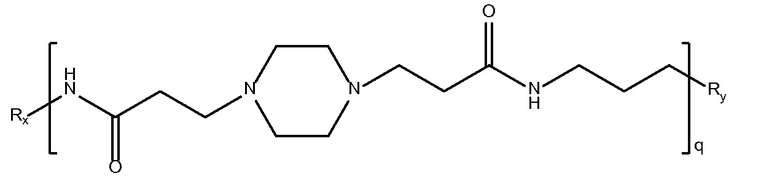
биспропановая кислота-1,4-диаминобутан)
Mw~4400
биспропановая кислота-2,2'-диаминодиэтиламин)
Mw<5K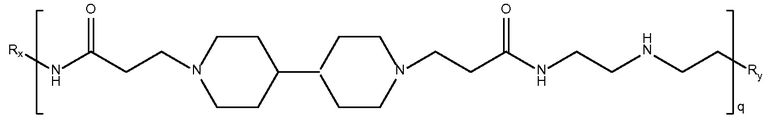
биспропановая кислота-2,2'-диамино
диэтиламин)
Mw 5,1K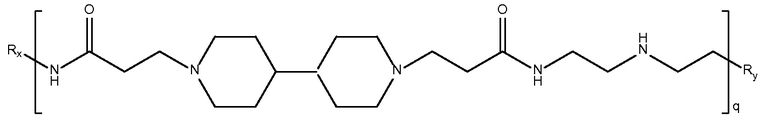
биспропановая кислота-2,2'-диамино N-
метилдиэтиламин)
Mw<5K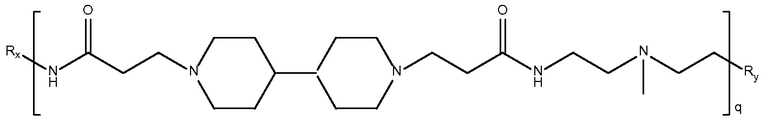
дипиперидин
биспропановая кислота-2,2'-диамино N-
метилдиэтиламин)
Mw<5K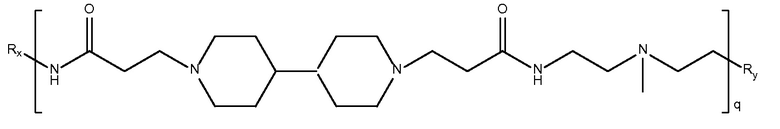
дипиперидин
биспропановая кислота-3,3'-диамино-
дипропиламин)
Mw<5K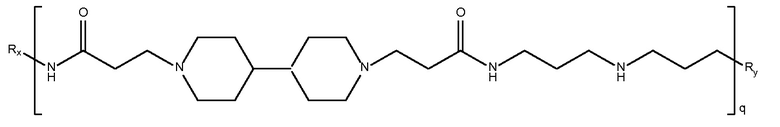
дипиперидин
биспропановая кислота-3,3'-диамино-
дипропиламин)
Mw<5K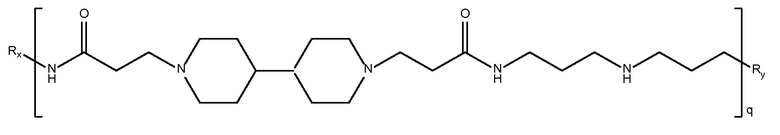
дипиперидин
биспропановая кислота-3,3'-диамино-N-
метилдипропиламин)
Mw<5K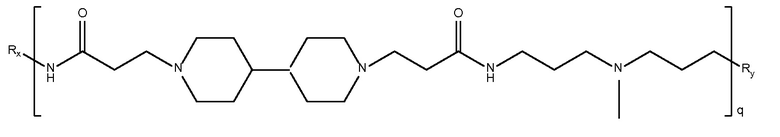
дипиперидин
биспропановая кислота-3,3'-диамино-N-метил-дипропиламин)
Mw~5,5K
биспропионовая кислота-этилендиамин)
Mw<5K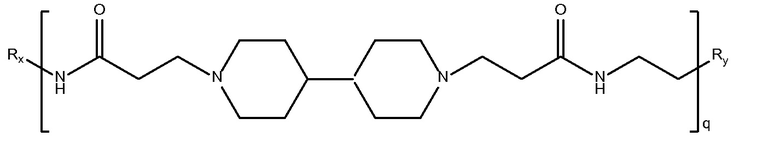
биспропионовая кислота-1,3-диаминопропан)
Mw<5K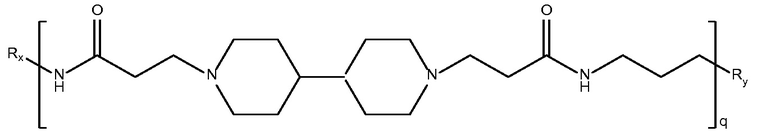
биспропионовая кислота-1,4-диаминобутан)
Mw<5K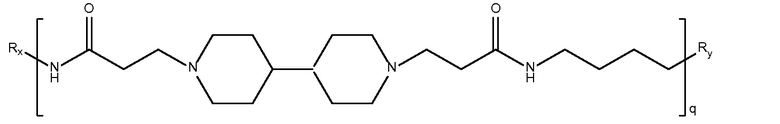
дипиперидин
биспропионовая кислота-простой бис(4-аминобутиловый эфир)
Mw<5K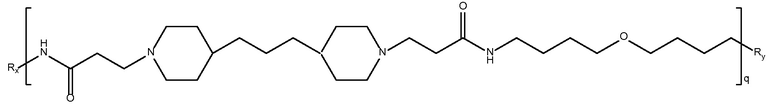
триметилен
дипиперидин
биспропионовая кислота-2-дигдрокси-1,3-
диаминопропан)
Mw<5K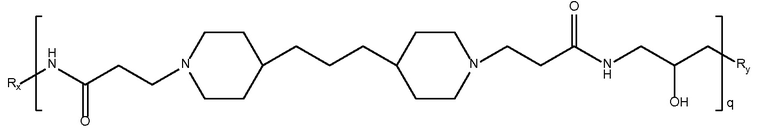
триметилен
дипиперидин-1,3-
диаминопропан-N,N'-ди-3-
пропионовая кислота)
Mw<5K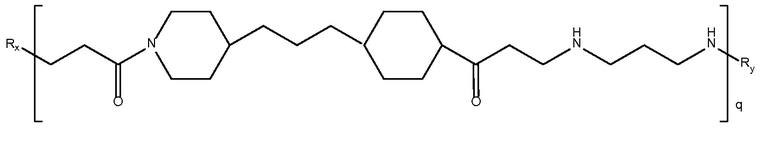
триметилен
дипиперидин
биспропановая
кислота--N,N'-
диметил-1,3-
диаминопропан),
Mw 1K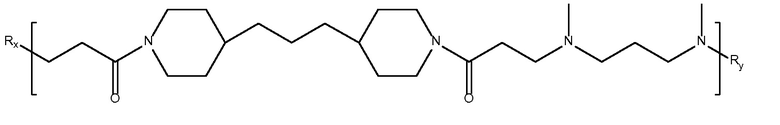
дипиперидин
биспропановая кислота-4,4'-дипиперидин),
Mw 10631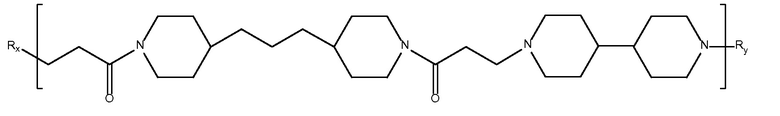
дипиперидин
биспропановая кислота-гистамин),
Mw 2,3K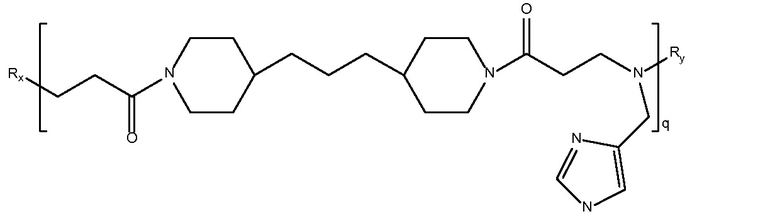
глицидола
поли(4,4-триметилен
дипиперидин
биспропановая кислота-диаминопропан),
Mw 8000
где x равно 0,6 и
Rx и Ry представляют собой 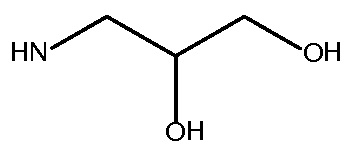 или NH2
или NH2
глицидола
поли(4,4-триметилен
дипиперидин
биспропановая кислота-
диаминопропан),
Mw 4700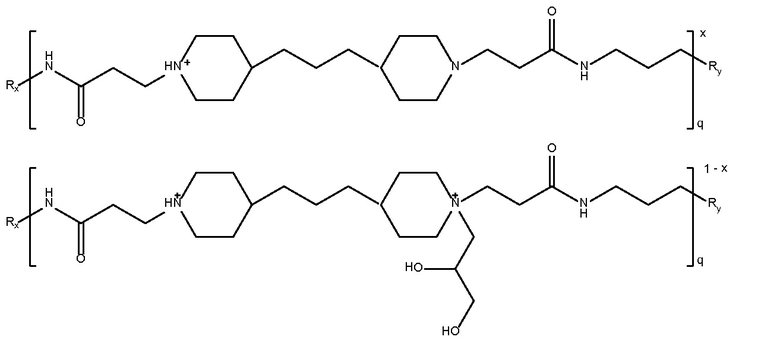
где x равно 0,6 и
Rx и Ry представляют собой 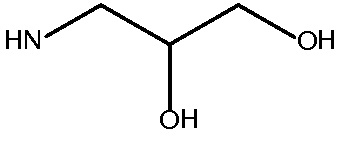 или NH2
или NH2
40% моль
глицидола поли(4,4-
триметилен
дипиперидин
биспропановая кислота-диаминопропан)
Mw 5000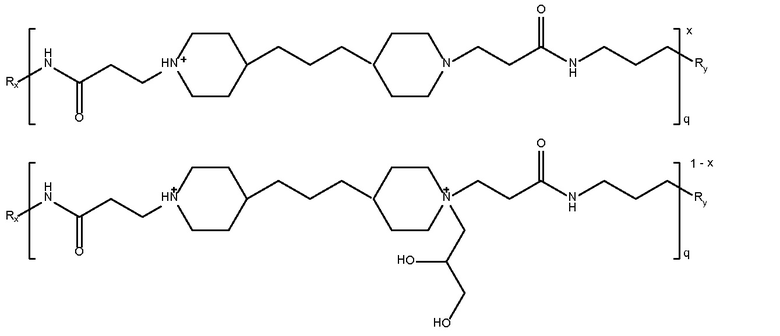
где x равно 0,6 и
Rx и Ry представляют собой 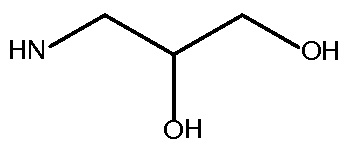 или NH2
или NH2
глицидола
поли(4,4-триметилен
дипиперидин
биспропановая кислота-
диаминопропан)
Mw 5000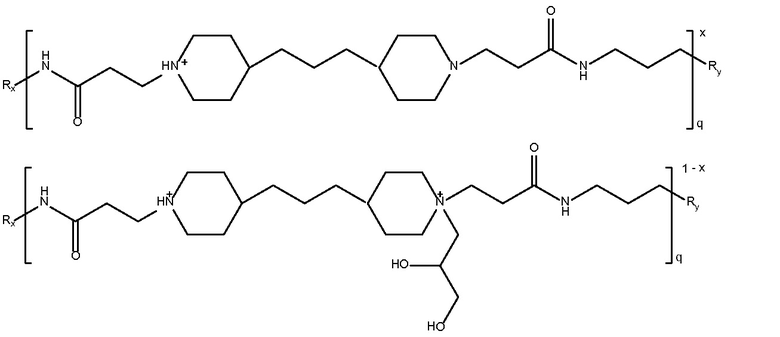
где x равно 0,6 и
Rx и Ry представляют собой 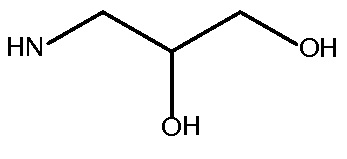 или NH2
или NH2
моль глицидола
поли(4,4-триметилен
дипиперидин
биспропановая кислота-диаминопропан),
Mw 8K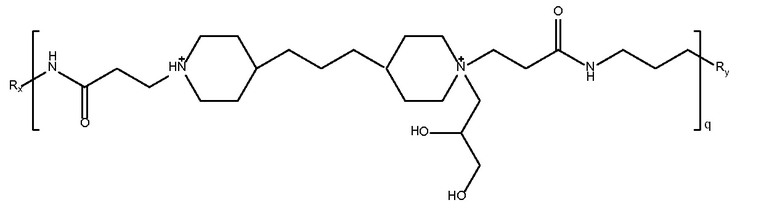
где Rx и Ry представляют собой 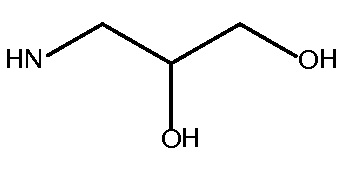 или NH2
или NH2
поли(4,4-триметилен
дипиперидин
биспропановая кислота-
диаминопропан),
Mw 7800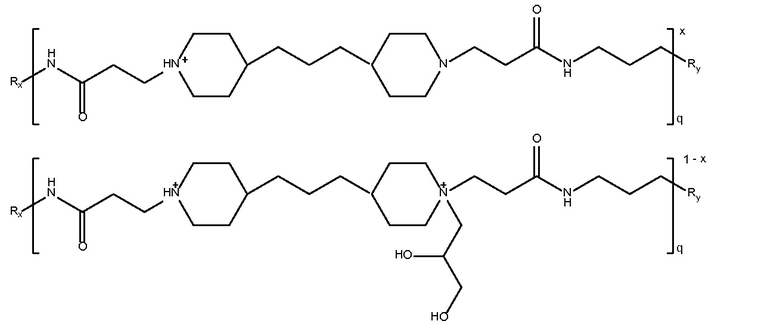
где x равно 0,75 и
Rx и Ry представляют собой 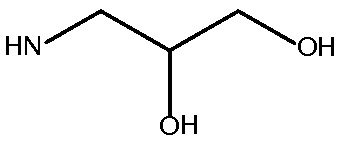 или NH2
или NH2
глицидола
поли(4,4-триметилен
дипиперидин
биспропановая кислота-
диаминопропан),
Mw 7800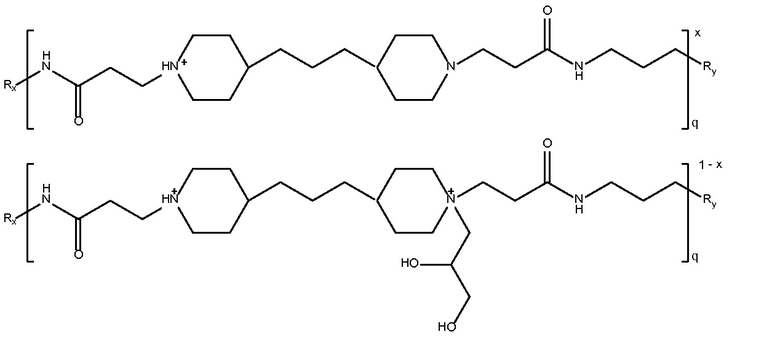
где x равно 0,5 и
Rx и Ry представляют собой 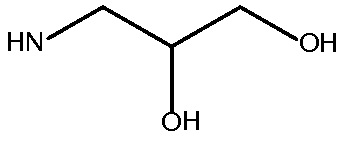 или NH2
или NH2
моль глицидола
поли(4,4-триметилен
дипиперидин
биспропановая кислота-диаминопропан),
Mw 7800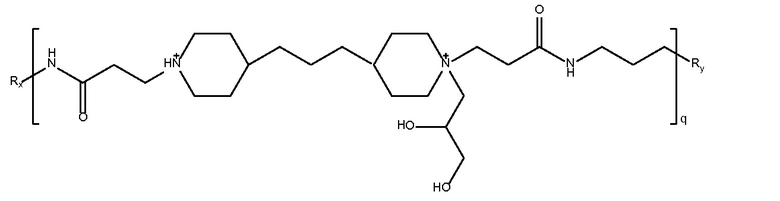
Rx и Ry представляют собой  или NH2
или NH2
дипиперидин
биспропановая кислота-диаминопропан),
Mw 7800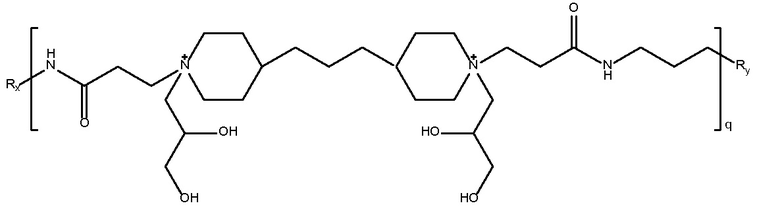
Rx и Ry представляют собой 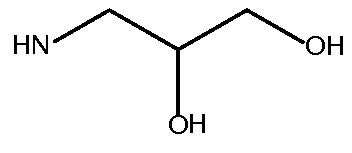 или NH2
или NH2
дипиперидин
биспропановая
кислота-3-(диметиламино) 1-пропиламин),
Mw 1K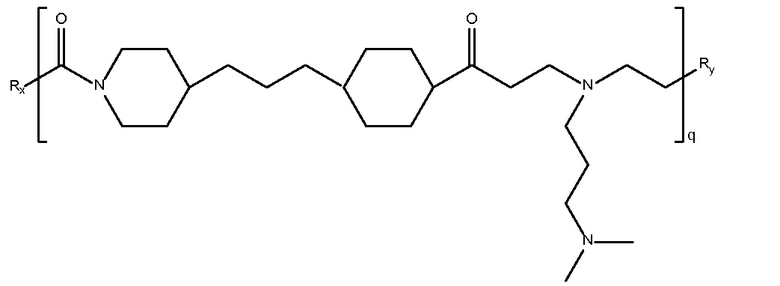
биспропановая кислота-диаминопропан),
Mw 2,5K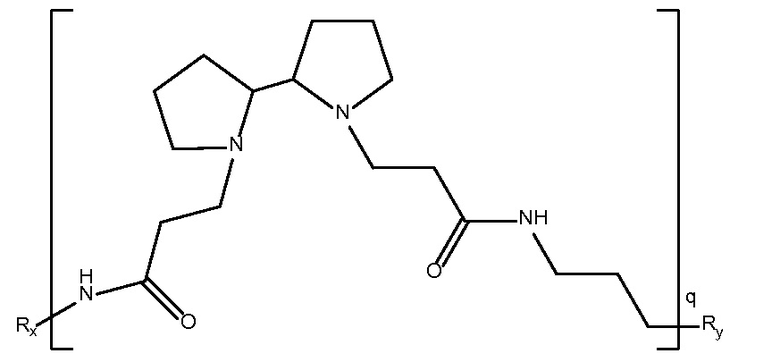
биспропановая кислота-бутилдиамин)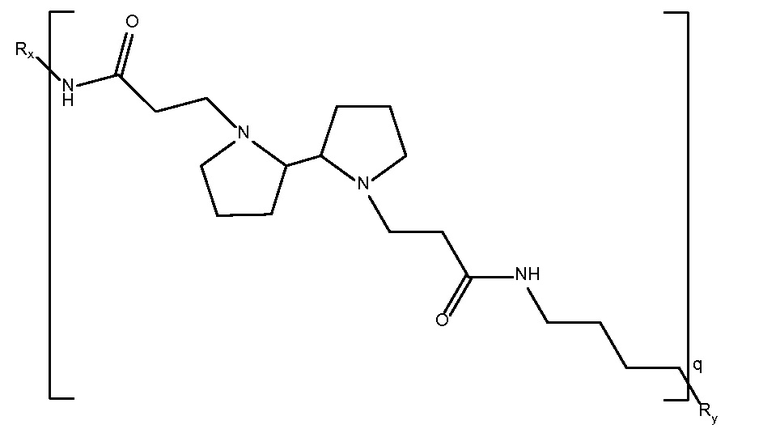
биспропановая кислота-
пентадиамин)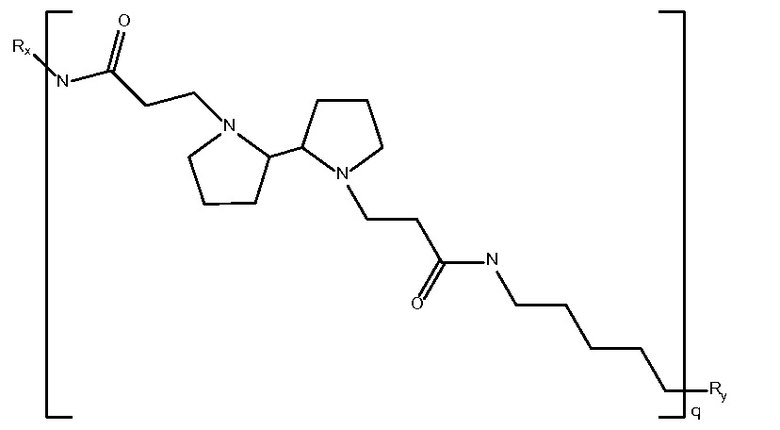
биспропановая кислота-этилдиамин)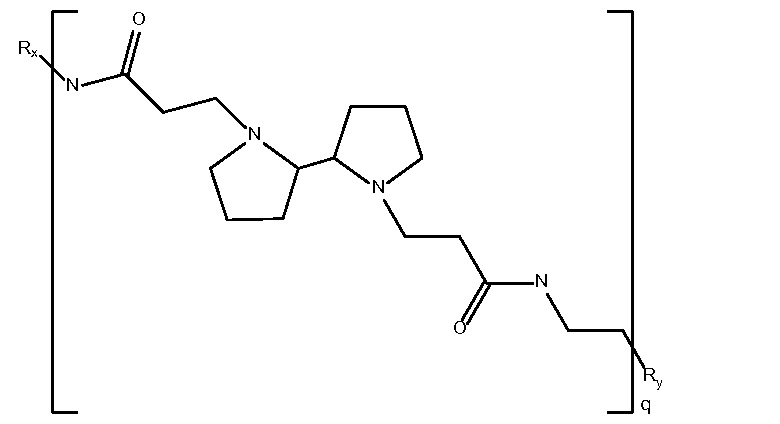
дипиперидин
биспропановая кислота-
аминометилбензол)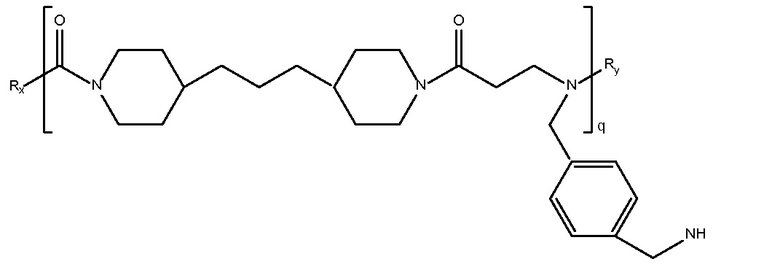
дипиперидин
биспропановая кислота-(1-аминометил-4-
гуанидинметил
бензол)]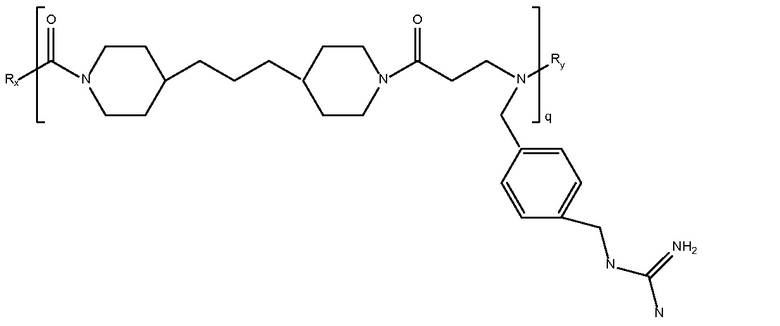
дипиперидин
биспропановая кислота-
диаминопропан)
с карбокси окончаниями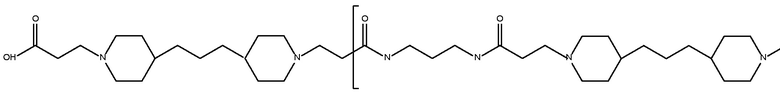
дипиперидин
биспропановая кислота-
диаминопропан)
с окончаниями сложного метилового эфира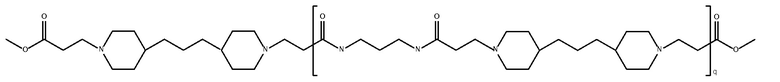
триметилен
дипиперидин
биспропановая кислота-
диаминопропан)
с окончаниями гуанидина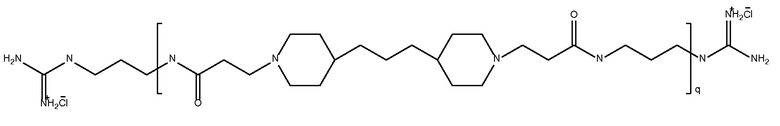
дипиперидин
биспропановая кислота-диаминопропан)
с окончаниями гуанидина
Mw 4700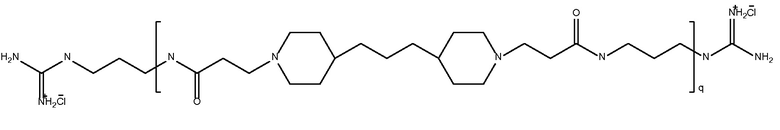
дипиперидин
биспропановая кислота-
диаминопропан)
с окончаниями гуанидина
Mw 7700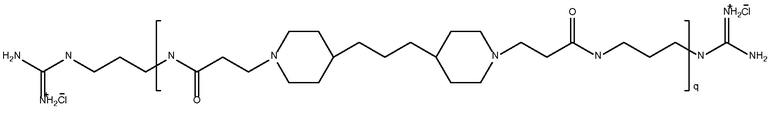
дипиперидин
биспропановая кислота-
диаминопропан)
(с окончаниями гуанидина)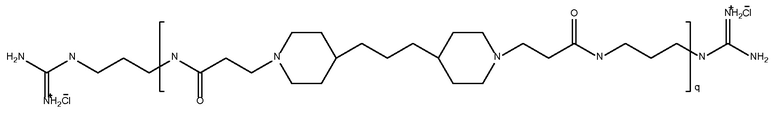
дипиперидин
биспропановая кислота-диаминопропан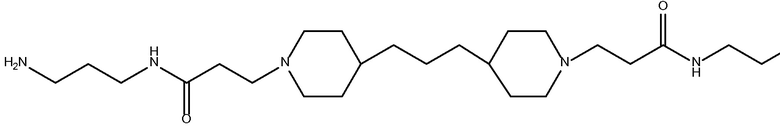
дипиперидин
биспропановая кислота-диаминопропан) с окончаниями 4-гуанидинобензола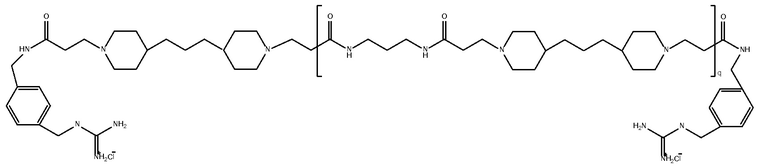
триметилен
дипиперидин
бисэтилакриламид-со-1,3-
диаминпропан)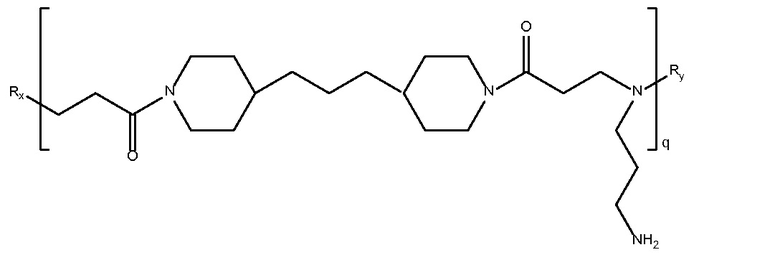
триметилен
дипиперидин
бисэтилакриламид-со-1-амино-3-гуанидинпропан)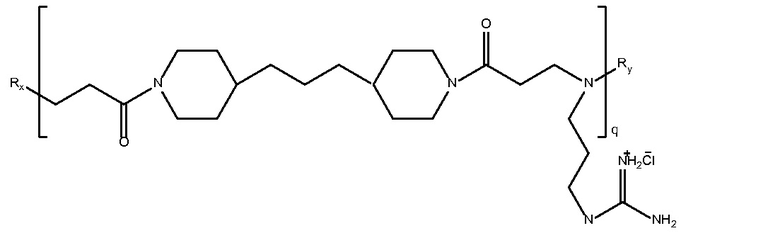
дипиперидин
биспропановая кислота-1-амино-3-гуанидинпропан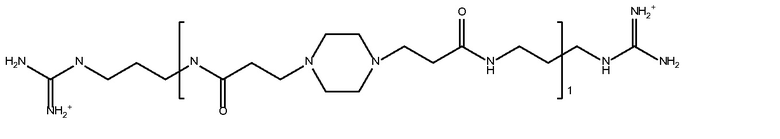
триметилен
дипиперидин
бисэтилакриламид-1,3-диамин
пропан)-со-
поли(4,4'-
триметилен
дипиперидин
бисэтилакриламид-1-аминобутил-3-карбамоил-
пиридиний)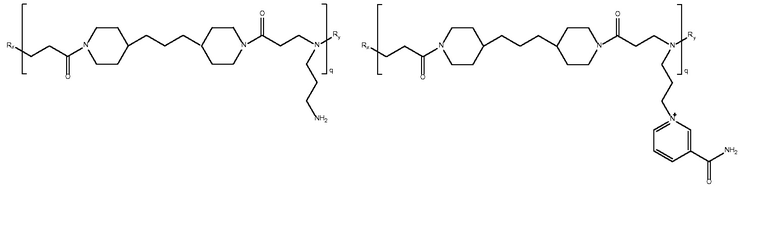
триметилен
дипиперидин
бисэтилакриламин-1-аминобутил-3-карбамоил-
пиридиний)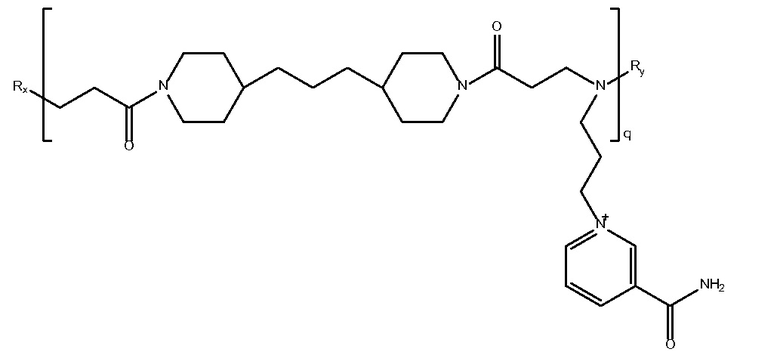
дипиперидин
биспропановой кислоты-диаминопропана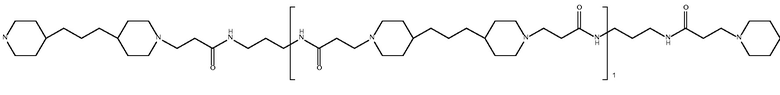
дипиперидин
биспропановой кислоты-диаминопропана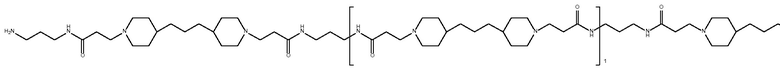
дипиперидин
биспропановая кислота-N-
глицидолди
пропилентриамин)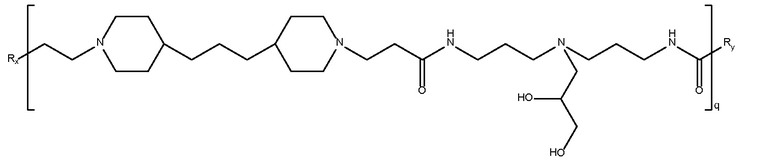
дипиперидин
биспропановая кислота-N-
глицидолди
этилентриамин)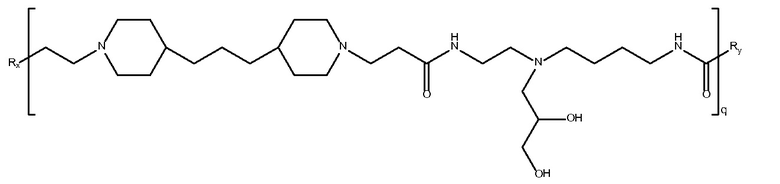
дипиперидин
биспропановая кислота-N-
глицидолди
этилентриамин)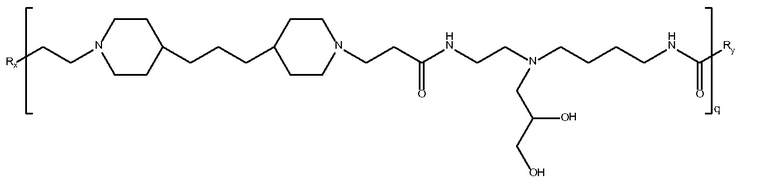
В одном из вариантов осуществления настоящего изобретения, амин-функциональные полиамиды вводятся в качестве фармацевтической композиции. В другом варианте осуществления настоящего изобретения, амин-функциональные полиамиды вводятся в эффективном количестве для достижения желаемого терапевтического эффекта. Специалист в данной области будет способен определить эффективное количество амин-функциональных полиамидов в зависимости от индивидуума и от состояния, которое лечится.
В одном из вариантов осуществления настоящего изобретения, амин-функциональные полиамиды используются при лечении всех форм мукозита и являются особенно эффективным, когда используются для лечения мукозита слизистой оболочки полости рта. Лечение включает профилактическое и терапевтическое применение, описанных амин-функциональных полиамидов и использования описанных фармацевтических композиций, содержащих амин-функциональные полиамиды. Желаемые профилактические воздействия включают предотвращение и замедление развития мукозита, уменьшение тяжести мукозита, уменьшение размера повреждений, связанных с мукозитом, и уменьшение вероятности развития мукозита посредством нанесения или введения амин-функциональных полиамидов или фармацевтических композиций, содержащих амин-функциональные полиамиды. Желаемые терапевтические воздействия включают облегчение дискомфорта, связанного с мукозитом, и/или увеличение скорости заживления повреждений при мукозите.
В одном из вариантов осуществления, амин-функциональные полиамиды и фармацевтические композиции, содержащие амин-функциональные полиамиды, могут использоваться для лечения всех форм инфекций, включая, но, не ограничиваясь этим, SSI, легочную инфекцию у пациентов с CF и легочную инфекцию C. aeruginosa у пациентов с CF с образованием биопленки или без него. Амин-функциональные полиамиды и фармацевтические композиции, содержащие амин-функциональные полиамиды, могут использоваться при профилактических и терапевтических применениях для лечения и предотвращения инфекции.
В другом варианте осуществления, амин-функциональные полиамиды и фармацевтические композиции, содержащие амин-функциональные полиамиды, могут использоваться для лечения всех форм SSI. Лечение включает профилактические и терапевтические применения описанных амин-функциональных полиамидов и применения описанных фармацевтических композиций, содержащих амин-функциональные полиамиды. Желаемое профилактическое применение представляет собой непосредственное введение амин-функциональных полиамидов или фармацевтических композиций, содержащих амин-функциональные полиамиды, в послеоперационную рану после операции для предотвращения и/или уменьшения вероятности развития SSI. Другое желательное профилактическое применение представляет собой введение амин-функциональных полиамидов или фармацевтических композиций, содержащих амин-функциональные полиамиды, перед операцией для предотвращения и/или уменьшения вероятности развития SSI. Желаемые терапевтические воздействия включают лечение существующего SSI посредством нанесения или введения амин-функциональных полиамидов или фармацевтических композиций, содержащих амин-функциональные полиамиды.
В другом варианте осуществления, амин-функциональные полиамиды и фармацевтические композиции, содержащие амин-функциональные полиамиды, можно использовать для лечения всех форм легочных инфекций и хронических легочных инфекций, связанных с CF, включая легочные инфекции C. aeruginosa у пациентов с CF, с образованием биопленки или без него. Лечение включает профилактические и терапевтические применения описанных амин-функциональных полиамидов и применения описанных фармацевтических композиций, содержащих амин-функциональные полиамиды. Желаемые терапевтические воздействия включают лечение существующих легочных инфекций или хронических легочных инфекций посредством введения амин-функциональных полиамидов или фармацевтических композиций, содержащих амин-функциональные полиамиды. В одном из вариантов осуществления, амин-функциональные полиамиды и фармацевтические композиции, содержащие амин-функциональные полиамиды, используют для лечения инфекций P. Aeruginosa, связанных с CF, без образования биопленки. В другом варианте осуществления, амин-функциональные полиамиды и фармацевтические композиции, содержащие амин-функциональные полиамиды, используют для лечения инфекций P. Aeruginosa, связанных с CF, с образованием биопленки. Желательное профилактическое применение представляет собой введение амин-функциональных полиамидов или фармацевтических композиций, содержащих амин-функциональные полиамиды, пациенту с CF для предотвращения и/или уменьшения вероятности развития легочной инфекции, включая легочную инфекцию C. aeruginosa. Желаемые терапевтические воздействия включают лечение существующей легочной инфекции или хронической легочной инфекции посредством введения амин-функциональных полиамидов или фармацевтических композиций, содержащих амин-функциональные полиамиды.
Амин-функциональные полиамиды по настоящему изобретению могут вводиться сами по себе или в фармацевтической композиции, содержащей амин-функциональные полиамиды. Соответствующие фармацевтические композиции могут содержать амин-функциональный полиамид и один или несколько фармацевтически приемлемых наполнителей. Форма, в которой вводятся полимеры, например, порошок, таблетка, капсула, раствор или эмульсия, зависит отчасти от способа, с помощью которого он вводится. Амин-функциональные полиамиды могут вводиться, например, местным образом, перорально, интраназально, посредством аэрозоля или ректально. Соответствующие наполнители включают, но, не ограничиваясь этим, неорганические или органические материалы, такие как желатин, альбумин, лактоза, крахмал, стабилизаторы, агенты для понижения температуры плавления, эмульгирующие агенты, соли и буферы. Соответствующие фармацевтически приемлемые наполнители для препаратов для местного введения, таких как мази, кремы и гели, включают, но, не ограничиваясь этим, коммерчески доступные инертные гели или жидкости, дополненные альбумином, метилцеллюлозой или коллагеновой матрицей.
Амин-функциональные полиамиды и фармацевтические композиции, содержащие амин-функциональные полиамиды, могут вводиться сами по себе или в сочетании с одним или несколькими дополнительными лекарственными средствами. Дополнительные лекарственные средства, которые вводятся в сочетании с амин-функциональными полиамидами и фармацевтическими композициями, содержащими амин-функциональные полиамиды, по настоящему изобретению, включают антибиотики и другие соединения, включая соединения, используемыми для профилактически и/или терапевтически, для лечения или предотвращения мукозита и инфекции, включая SSI и легочную инфекцию, и хроническую легочную инфекцию, связанную с CF, в частности, инфекцию P. aeruginosa, с образованием биопленки или без него. Дополнительные лекарственные средства могут вводиться одновременно с амин-функциональным полиамидом или фармацевтическими композициями, содержащими амин-функциональные полиамиды. Дополнительные лекарственные средства могут также вводиться последовательно с амин-функциональным полиамидом или фармацевтическими композициями, содержащими амин-функциональные полиамиды. Фармацевтическая композиция, содержащая амин-функциональные полиамиды, может также дополнительно содержать лекарственное средство, используемое профилактически и/или терапевтически, для лечения или предотвращения мукозита и инфекции, включая SSI и легочную инфекцию, и хроническую легочную инфекцию, связанную с CF, в частности, инфекцию P. aeruginosa, с образованием биопленки или без него.
Примеры
Пример 1: Исследования in vitro
Пример 1-1: Анализ цитотоксичности, клетки RPTEC и клетки NHDF
Анализы цитотоксичности для клеток млекопитающих осуществляют с использованием двух первичных линий клеток человека: эпителиальных клеток проксимальных почечных канальцев (RPTEC - Cambrex CC-2553) и нормальных дермальных фибробластов человека (NHDF - Cambrex CC-2509). Клетки размещают при плотности 3000 клеток/лунка (RPTEC) или 5000 клеток/лунка (NHDF) в 96-луночных планшетах и инкубируют в течение ночи при 37°C. В лунки добавляют соединения, и клетки инкубируют в течение 4 дней. К одному набору планшетов добавляют Alomar Blue, и их инкубируют в течение 4 часов. Планшеты считывают, когда добавляют соединение (время ноль) и в конце исследования. Флуоресценцию считывают с использованием 530 нм (возбуждение) и 590 нм (испускание) в соответствии с инструкциями производителя. 50% ингибиторную концентрацию (IC50) вычисляют как 50% от максимального сигнала минус его значение при времени ноль. 50% летальную концентрацию (LC50) вычисляют как 50% от значения при времени ноль минус минимальный сигнал.
Таблица 2 показывает значения IC50 и LC50 для эпителиальных клеток проксимальных почечных канальцев и для нормальных дермальных фибробластов человека для выбранных соединений.
Пример 1-2: Анализ цитотоксичности, эпителиальные клетки легких человека
Анализ цитотоксичности полимеров по отношению к эпителиальным клеткам легких человека осуществляют с использованием линии клеток эпителиальной карциномы легких человека (A 549-ATCC # CCL-185). Клетки инкубируют в течение 96 часов при 7°C с 5% CO2 в 96-луночном планшете. В планшеты добавляют реагент CellTiter-Glo® (Promega). Планшеты считывают посредством измерения люминесценции, возникающей при катализируемой люциферазой реакции люциферина с ATP в соответствии с протоколом, предлагаемым производителем. Концентрация ATP прямо пропорциональна выживаемости клеток; соответственно, более высокая люминесценция является мерой высокой выживаемости клеток.
Таблица 2 показывает IC50 эпителиальных клеток легких человека для выбранных соединений.
Пример 1-3: Анализ лизирования эритроцитов
Соединения инкубируют в течение ночи при 37°C в солевом фосфатном буфере Дюльбекко, содержащем свежие промытые эритроциты при гематокрите 1%. После инкубирования, планшеты центрифугируют и супернатант переносят в плоскодонные 96-луночные планшеты. Супернатант анализируют с использованием набора QuantiChrom Hemoglobin kit в соответствии с инструкциями производителя. Значения IC50 вычисляют с использованием GraphPad Prism.
Таблица 2 показывает IC50 значения для выбранных соединений.
Пример 1-4: Анализ минимальной ингибиторной концентрации
Анализ минимальной ингибиторной концентрации (MIC) определяет самую низкую концентрацию противомикробного агента, необходимую для ингибирования роста исследуемых организмов после инкубирования. Анализ MIC осуществляют с использованием внутреннего стандарта, панели организмов для идентификации соединений с противомикробной активностью. Анализ MIC впоследствии повторяют по отношению к другим специализированным микробным панелям. Анализы осуществляют по отношению к следующим клинически важным микроорганизмам: Staphylococcus aureus subsp. aureus, Staphylococcus epidermis, Escherichia coli, Pseudomonas aeruginosa, Haemophilius influenzae. Соединения исследуют на бактерицидную активность, временную зависимость гибели, токсичность по отношению к культуре клеток ткани, выращенной in vitro, а в некоторых случаях их исследуют на противомикробную активность in vivo.
Анализ MIC осуществляют в соответствии с Performance Standards for Antimicrobial Susceptibility Testing, 2006, vol. M100-S15, Fifteenth Informational Supplement, NCCLS, 940 West Valley Road, Suite 1400, Wayne, PA 19087.
Исследуемые полимеры растворяют в 0,85% солевом растворе до конечной концентрации либо 830, либо 1000 мкг/мл, и pH доводят до 7,0. Затем раствор стерилизуют фильтрованием через 0,22-мкм фильтр. Двукратные последовательные разбавления полимера приготавливают в бульоне Мюллера-Хинтона с катионами, аликвотированном в 96-луночных микротитровальных планшетах. Затем планшеты инокулируют при 5×105 клеток/мл целевого организма и инкубируют 18-24 часа при 35°C. Оптическую плотность (OD) считывают на 590 нм, и оценивают рост микроорганизмов (OD>0,1 считается ростом; OD<0,1 считается ингибирование роста). Значение MIC представляет собой самую низкую концентрацию соединения, которая ингибирует рост; соответственно, более высокое значение MIC указывает на меньшее сильнодейстие, в то время как более низкое значение MIC указывает на более высокое сильнодейстие.
Значения MIC репрезентативных амин-функциональных полиамидов по отношению к клинически важным микроорганизмам представлены в Таблице 2.
Результаты анализов цитотоксичности репрезентативных амин-функциональных полиамидов [IC50 и LC50 для эпителиальных клеток почек и дермальных фибробластов человека], анализа лизирования эритроцитов in vitro [IC50 гемолиза] и значения MIC относительно клинически важных микроорганизмов
(IC50 Эпит. клеток почек)
(LC50 Эпит. клеток почек)
(IC50 дерм. фибробласты чел.)
(IC50 дерм. фибробласты чел.)
(IC50 гемолиза)
aureus (MIC)
Epidermic
(MIC)
aeruginosa (MIC)
influenza (MIC)
дипиперидин
биспропановая кислота-
диаминопропан)
<10K
триметилен
дипиперидин
биспропановая кислота-
диаминобутан)
>10K
дипиперидин
биспропановая кислота-
диаминобутан)
<10K
триметилен
дипиперидин
биспропановая кислота-
диаминоэтан)
<10K
триметилен
дипиперидин
биспропановая кислота-
диаминотриPEG)<10K
триметилен
дипиперидин
биспропановая кислота-диаминотриPEG)>10K
триметилен
дипиперидин
биспропановая кислота-диаминопропан)<10K
триметилен
дипиперидин биспропановая кислота-N(2-аминоэтил)-диаминоэтан)
триметилен
дипиперидин
биспропановая кислота-N(3-
аминопропил)
1,3-пропандиамин)<10K
триметилен
дипиперидин
биспропановая кислота-
диаминопропан)<10K
триметилен
дипиперидин
биспропановая кислота-3,3'-
диамино-N-метил-
дипропиламин)
<10K
триметилен
дипиперидин
биспропановая
кислота-2,2'-
диамино-N-
метил-диэтиламин)
триметилен
дипиперидин
биспропановая кислота-1,4-бензиламин)
<10K
биспропановая кислота-1,2-бис(2-аминоэтокси)этан)
<10K
биспропановая кислота-2,2-диаминоди-этиламин)
<10K
биспропановая
кислота-3,3'-
диамино-N-метил-
дипропиламин)
<10K
биспропановая
кислота-N(3-
аминопропил)
1,3-пропандиамин)<10K
биспропановая
кислота-N-
метил-2,2-
диаминодиэтиламин)
<10K
триметилен
дипиперидин
биспропановая кислота-
2,2'-диамино
диэтиламин)
5,5K
дипиперидин
биспропановая
кислота-2,2'-диамино
диэтиламин)
5,1K
дипиперидин
биспропановая кислота-2,2'-
диамино N-метил
диэтиламин)<5K
дипиперидин
биспропановая
кислота-2,2'-
диамино N-метил
диэтиламин)
<5K
дипиперидин
биспропановая кислота-2,2'-
диамино N-метилдиэтиламин)
~5K
дипиперидин
биспропановая
кислота-3,3'-
диамино-дипропиламин)
<5K
дипиперидин
биспропановая
кислота-3,3'-
диамино-
дипропиламин)
~5K
дипиперидин
биспропановая кислота-3,3'-
диамино-N-
метил-дипропиламин) ~5K
дипиперидин
биспропановая кислота-3,3'-
диамино-N-
метил-
дипропиламин)
>5K
триметилен
дипиперидин
биспропановая кислота-
2,2'-диамино
диэтиламин)
~14000
биспропановая кислота-1,3-диаминопропан)~3700
биспропановая кислота-1,4-диаминобутан)
~4400
биспропионовая кислота-1,3-диаминопропан)<5K
биспропионовая кислота-1,4-диаминобутан)<5K
биспропионовая кислота-
этилендиамин)<5K
дипиперидин-1,3-диаминопропан-N,N'-ди-S-пропионовая кислота)<5K
триметилен
дипиперидин
биспропионовая кислота-2-дигидрокси
1,3-диаминопропан)
<5K
дипиперидин
биспропионовая кислота-простой бис(4-аминобутиловый эфир)<5K
триметилен
дипиперидин
биспропановая
кислота-4,4'-
триметилен
дипиперидин)
триметилен
дипиперидин
биспропановая
кислота--N,N'-
диметил-1,3-
диаминопропан)
дипиперидин
биспропановая
кислота-
пиперазин)
триметилен
дипиперидин
биспропановая кислота-
диаминопропан), модифицированный
40% моль
глицидола 8K
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), 1650
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), 5K
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), 7,7K
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), 3K
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), модифицированный 100% моль
глицидола, 8K
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), модифицированный 200% моль глицидола,
7800
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), модифицированный
150% моль глицидола,
7800
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), модифицированный 50% моль глицидола, 7800
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), 2500
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), модифицированный 25% моль глицидола, 7800
триметилен
дипиперидин
биспропановая
кислота-3-
(диметиламино)1-
пропиламин), 11K
триметилен
дипиперидин
биспропановая
кислота--N,N'-
диметил-1,3-
диаминопропан), 1K
биспропановая кислота-
диаминопропан), 2,5K
бипирролидин
биспропановая
кислота-бутилдиамин)
бипирролидин
биспропановая
кислота-этилдиамин)
бипирролидин
биспропановая
кислота-пентадиамин)
триметилен
дипиперидин
биспропановая кислота-
диаминопропан, пентамер
триметилен
дипиперидин
биспропановая кислота-
диаминопропан, гептамер
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан)
(с окончаниями гуанидина)
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), модифицированный
40% моль
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), модифицированный
40% моль
триметилен
дипиперидин
биспропановая
кислота-N-
глицидолдиэтилен
триамин)
триметилен
дипиперидин
биспропановая
кислота-N-
глицидол
диэтилентриамин)
триметилен
дипиперидин
биспропановая
кислота-N-
глицидол
дипропилен
триамин)
триметилен
дипиперидин
бисэтилакриламид-
со-1,3-диаминпропан)
триметилен
дипиперидин
бисэтилакриламид-со-1-амино-3-
гуанидинпропан)
триметилен
дипиперидин
биспропановая
кислота-l-амино-
3-гуанидинпропан
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), 1400
триметилен
дипиперидин
бисэтилакриламид-1,3-диамин
пропан)-со-поли(4,4'-триметилен-дипиперидин
бисэтилакриламид-1-
аминобутил-3-
карбамоил-
пиридиний)
триметиленди
пиперидин
бисэтилакриламин-1-
аминобутил-3-
карбамоил-пиридиний)
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), модифицированный
40 % моль глицидола
4700
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан) с окончаниями гуанидина 4700
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), с окончаниями гуанидина 7700
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан) с карбокси окончаниями
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан) с окончаниями сложного метилового эфира
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), с окончаниями гуанидина 2200
триметилен
дипиперидин
биспропановая
кислота-
аминометилбензол)
дипиперидин
биспропановая кислота-
диаминопропан
триметилен
дипиперидин
биспропановая
кислота-(1-
аминометил-
4-гуанидинметил бензол)]
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), с окончаниями 4-гуанидинобензола
триметилен
дипиперидин
биспропановая
кислота-
диаминопропан), <10K
Пример 1-5: Ингибирование Pseudomonas aeruginosa в бронхиальных эпителиальных клетках кистозного фиброза
Бронхиальные эпителиальные клетки кистозного фиброза (CFBE) выращивают в 12-луночных планшетах в течение 7-9 дни. Клетки промывают дважды проявляющей средой перед тем как Pseudomonas aeruginosa (мукоидный штамм, SMC 1585) инокулируют в каждую лунку при количестве инфицирований (MOI) ~30 (~6×106 к.о.е./лунка). Планшеты инкубируют при 37°C, 5% CO2 в течение 1 часа, чтобы сделать возможным присоединение бактерий к клеткам дыхательных путей. Затем супернатант заменяют проявляющей средой, содержащей 0,4% аргинина, а затем инкубируют в течение 5 часов для образования биопленок на клетках CFBE. Для оценки эффективности противомикробного лечения полимером на полученных биопленках, планшеты промывают дважды проявляющей средой и противомикробным агентом (противомикробный полимер или тобрамицин [положительный контроль]) наносят при обозначенных концентрациях для разрушения установившихся биопленок в течение 16 часов. Затем супернатант удаляют и промывают дважды проявляющей средой. Клетки CFBE лизируют 0,1% Triton X-100 в течение приблизительно 15 минут. Лизат перемешивают на вихревой мешалке в течение 3 минут перед последовательным разбавлением и спотовым тированием на LB планшетах для определения величины к.о.е./лунка. Бактериальный штамм определяется как 'восприимчивый' к лечению антибиотиками в модели статичного совместного культивирования, если монослои CFBE не разрушаются после лечения антибиотиками в течение ночи и имеется разница более чем 2 log10 в выходе к.о.е. между отсутствием лечения и лечением противомикробным агентом антибиотиком.
Для исследования способности антибиотиков к предотвращению образования биопленки, эти соединения наносят после периода в 1 час для присоединения бактерий. Планшеты инкубируют в течение 5 часов, и определяют значения к.о.е./лунка, как описано выше. Предел детектирования анализа статичного совместного культивирования составляет 200 к.о.е./лунка. Все эксперименты осуществляют по меньшей мере по три раза. Восприимчивость биопленки Pseudomonas aeruginosa к поли(4,4-триметилен-дипиперидинбиспропановой кислоте-диаминопропану) <10K показана на Фигуре I, ниже.
Пример 2: Исследования in vivo
Пример 2-1: Токсичность - максимальная переносимая доза
Острые 24-часовые исследования токсичности для определения максимальной переносимой дозы соединения осуществляют на самцах крыс и мышей возрастом приблизительно 8-10 недель.
Животных содержат поодиночке в стандартных поликарбонатных клетках и кормят нормальным кормом. После одной недели акклиматизации, соединения вводят в виде одной внутрибрюшинной (LP.) или внутривенной (I.V.) дозы, как правило, в носителе из PBS. Дозы, как правило, находятся в диапазоне от 1 мг/кг до достигающих 400 мг/кг. Животные наблюдаются относительно признаков боли, страдания и локальных или системных признаков токсичности в течение одного часа после дозирования, а затем через 1-часовые интервалы в течение 6 часов после дозирования. На следующий день, через 24 часа после дозирования, животных умерщвляют и удаляют кровь для химического анализа сыворотки. Осуществляемые химические анализы сыворотки включают: ALT, AST, креатинин и азот мочевины. Главные органы также исследуют на признаки аномалий.
Таблица 3 показывает максимальную переносимую дозу (MTD) для выбранных исследуемых соединений при выбранных способах введения.
Максимальная переносимая доза (MTD)
введения
дипиперидинбиспропановая кислота-со-1,3-диаминопропан), MW=4700
дипиперидинбиспропановая кислота-со-1,3-диаминопропан), MW=2500
дипиперидинбиспропановая кислота-диаминопропан),
MW<10K
дипиперидинбиспропановая кислота-со-1,3-диаминопропан), MW=2500
Пример 2-2: Эффективность - хирургическая раневая инфекция
Исследуемое соединение, поли(4,4-триметилендипиперидинбиспропановая кислота-диаминопропан), модифицированный 40% моль глицидола, оценивают на противоинфекционную активность против Staphylococcus aureus, стойких к метицилину (MRSA), и Escherichia coli (E. coli) у мышей. Самцы мышей ICR весящие приблизительно 22 г используются для оценки противоинфекционной активности против каждой бактерии.
Пример 2-2(a): MRS A
Пять группы по 10 самцов мышей инокулируют внутрибрюшинно LD90-100 MRSA (1,90×108 к.о.е./мышь), суспедированным в 0,5 мл бульона с сердечно-мозговой вытяжкой (BHI), содержащего 5% муцина. Через час после инокулирования бактерий, группам по 10 животных внутрибрюшинно вводят один из следующих препаратов:
0,2 мг/кг поли(4,4-триметилендипиперидинбиспропановой кислоты-диаминопропана), модифицированного 40% моль глицидола, суспендированного в 0,9% NaCl,
5 мг/кг поли(4,4-триметилендипиперидинбиспропановой кислоты-диаминопропана), модифицированного 40% моль глицидола, суспендированного в 0,9% NaCl,
1 мг/кг офлоксацина,
3 мг/кг офлоксацина и
5 мл/кг носителя (0,9% NaCl).
Смертность регистрируют раз в день в течение 7 дней и оценивают увеличение выживаемости по отношению к контрольной группе с носителем.
Таблица 4 показывает результаты по отношению к MRSA для исследуемых соединений.
Активность по отношению к MRSA
дипиперидин
биспропановая кислота-диаминопропан), модифицированный 40% моль глицидола
Пример 2-2(b): E. coli
Пять групп по 10 самцов мышей инокулируют внутрибрюшинно LD90-100 E. coli (2,20×105 к.о.е./мышь), суспендированного в 0,5 мл бульона BHI, содержащего 5% муцина. Через час после инокулирования бактерий, группам по 10 животных вводят внутрибрюшинно один из следующих препаратов:
0,2 мг/кг поли(4,4-триметилендипиперидинбиспропановой кислоты-диаминопропана), модифицированного 40% моль глицидола, суспендированного в 0,9% NaCl,
5 мг/кг поли(4,4-триметилендипиперидинбиспропановой кислоты-диаминопропана), модифицированного 40% глицидола, суспендированного в 0,9% NaCl,
0,3 мг/кг гентамицина,
1 мг/кг гентамицина и
5 мг/кг носителя (0,9% NaCl).
Смертность регистрируют раз в день в течение 7 дни и оценивают увеличение выживаемости по сравнению с контрольной группой с носителем.
Таблица 5 показывает результаты по отношению к E. coli для исследуемых соединений.
Активность по отношению к E. coli
дипиперидин
биспропановая кислота-диаминопропан), модифицированный 40% моль глицидола
Исследуемое соединение, поли(4,4-триметилендипиперидинбиспропановая кислота-диаминопропан), модифицированное 40% моль глицидола, обеспечивает значительную противомикробную защиту, демонстрируя 60% и 80% увеличение доли выживаемости для моделей, указанных выше, инфицированных MRSA и E. coli.
Пример 2-3: Эффективность - мукозит
Целью этого исследования является изучение роли временного графика и способа введения для наблюдаемой эффективности поли(4,4-триметилен-дипиперидинбиспропановой кислоты-диаминопропана) (1 мг/мл) по отношению к частоте, тяжести и продолжительности мукозита слизистой оболочки полости рта, вызванного облучением. Самцы сирийского золотистого хомячка LVG, возрастом 5-6 недель, со средней массой тела 86,3 г при начале исследований используются для оценки активности каждого из соединений по отношению к вызванному облучением мукозита слизистой оболочки полости рта. Конечными целями исследований являются оценка мукозита, изменения веса и выживаемости.
Самцы сирийского золотистого хомячка произвольно и с возможностью замены разделяют на группы лечения по семь (7) животных на группу (предмет исследования) и одну группу из десяти (10) животных (контроль).
В день 0, все животные получают острую дозу облучения 40 Гр, направленного на их левый ротовой защечный мешок. В день 0, животные дозируются местным образом один раз. От дня 0 до дня 20, дозы по 0,5 мл наносят местным образом на левый ротовой защечный мешок по три раза в день.
Для оценки тяжести мукозита, животных анестезируют с помощью ингаляции анестетика, и левый ротовой защечный мешок выворачивают наизнанку. Мукозит оценивают визуально посредством сравнения с сертифицированной фотографической шкалой; шкала находится в диапазоне от 0 для нормального состояния до 5 для тяжелого изъязвления. Дескриптивная версия шкалы для оценки мукозита, используемая в настоящем исследовании, представлена в Таблице 6.
Шкала для оценки мукозита
Балл 1 или 2 представляет умеренную стадию повреждения, балл 3, 4 или 5 указывает на мукозит, от умеренного до тяжелого. После визуальной оценки делают цифровую фотографию слизистой оболочки каждого животного с использованием стандартизованной методики. В заключение эксперимента, все изображения нумеруются случайным образом и сортируются слепым образом с помощью по меньшей мере двух независимых тренированных наблюдателей с использованием описанной выше шкалы (слепая оценка).
Гибель животных оценивают в ходе исследования. На модели, гибель чаще всего приписывают отрицательным воздействиям, связанным с анестезией, как правило, осуществляемой во время облучения, или токсичности экспериментального соединения. Нет смертей, связанных с экспериментальными соединениями.
Изменение веса также оценивают, поскольку оно представляет собой вторичный способ изучения потенциальной токсичности экспериментального лечения. Животные взвешиваются ежедневно в течение исследования; изменение массы были сходны во всех группах. Средний процент набора массы во время исследования приведен в Таблице 7.
Для оценки значимости этих различий, средняя площадь под кривой (AUC) вычисляется для каждого животного из данных по проценту набора массы, и средние значения и стандартные отклонения изображаются в виде графика. Используя односторонний тест ANOVA, не наблюдают статистически значимой разницы в изменении массы для любой из групп.
Для оценки эффективности, средние баллы группы с мукозитом сравнивают с контрольной группой в каждом эксперименте. Балл для клинического мукозита равный 3 у хомячков указывает на присутствие язвы. Изъязвление представляет собой момент в развитии мукозита, где нарушается физическая целостность слизистой оболочки ротовой полости. В клинике, пациент, присутствующий с тяжелыми изъязвлениями ротовой полости, может потребовать госпитализации для анальгетической, наркотической и/или использующей антибиотики терапии или для восполнения жидкости. Средняя стоимость ухода за больным является значительной. Запущенный мукозит у людей (с язвенными поражениями, коррелирующими с баллом 3 или выше) часто требует перерыва в терапии для пациентов, принимающих облучение, и, если возникает сепсис, для этих пациентов возникает риск гибели. Терапия, которая значительно уменьшает время, в течение которого пациент с мукозитом слизистой оболочки полости рта имеет язвы, была бы очень ценной для клинического врача. Кумулятивное количество дней, когда животное имеет балл 3 или выше, определяется благодаря его клинической значимости.
Значимость групповых различий при баллах 3 или выше определяют с использованием анализа различий с критерием Хи-квадрат (χ2) относительно общего количества для животных с баллом 3 или выше в ходе всего исследования; эти результаты представлены в Таблице 7. Тяжесть и ход мукозита благоприятно уменьшаются в группе с поли(4,4-триметилендипиперидин-биспропановой кислотой-диаминопропаном).
Безопасность и эффективность при мукозите
(дни 0-20)
с баллом
мукозита ≥ 3
дипиперидин
биспропановая кислота-диаминопропан), местно, три раза в день
(1 мг/мл)
Пример 3: Синтез амин-функциональных полиамидов
Пример 3-1: Синтез ацетата 4,4'-триметилен- дипиперидинбиспропановой кислоты
К 5,0 г 4,4'-триметилендипиперидина в 20 мл метанольного раствора (20 мл), добавляют по каплям 4,6 г метилакрилата. Полученную в результате реакционную смесь перемешивают при комнатной температуре в течение 16 часов. Растворитель удаляют при пониженном давлении, и остаток очищают с помощью колоночной хроматографии с использованием системы с градиентом растворителей, содержащей от 100% гексана до 100% этилацетата. Удаление растворителя при пониженном давлении дает 7 г желаемого продукта в виде белого твердого продукта.
Пример 3-2: Синтез ацетата 4,4'-дипиперидинбиспропановой кислоты
К 10,0 г 4,4'-дипиперидина HCl, растворенного в 80 мл метанола, добавляют 12,6 г карбоната калия. Реакционную смесь перемешивают при комнатной температуре в течение 3 часов, за это время медленно добавляют 8,03 г метилакрилата. Затем полученный в результате реакционный раствор перемешивают при комнатной температуре в течение 18 часов. Реакционную смесь фильтруют, и фильтрат выпаривают досуха при пониженном давлении. Остаток обрабатывают 300 мл этилацетата. Полученную в результате суспензию перемешивают при комнатной температуре в течение 2 часов с последующим фильтрованием. Фильтрат выпаривают досуха при пониженном давлении. Полученную в результате массу сушат при комнатной температуре в вакууме с получением 11,34 г желаемого продукта в виде беловатого твердого продукта.
Пример 3-3: Синтез ацетата пиперазинбиспропановой кислоты
К 10 г пиперазина гексагидрата, растворенного в 40 мл метанола, капельным образом добавляют 9,97 г метилакрилата. Реакционную смесь перемешивают при комнатной температуре в течение 18 часов. По прохождении этого времени, реакционную смесь выпаривают досуха при пониженном давлении. Остаток перекристаллизуют из гексана/метиленхлорида (1:1 объем/объем). После фильтрования и сушки при комнатной температуре при пониженном давлении, получают 12,2 г желаемого продукта в виде белого твердого продукта.
Пример 3-4: Синтез 1,1-диакрил-4,4'-триметилендипиперидина
К 3,8 г акрилоилхлорида, растворенного в 50 мл дихлорметана, капельным образом добавляют раствор 4,0 г 4,4-триметилендипиперидина, растворенного в 20 мл дихлорметана, при 0°C. К этому раствору с помощью шприца медленно добавляют 4,23 г триэтиламина. Полученную в результате реакционную смесь перемешивают в течение 18 часов и дают ей возможность для нагрева до комнатной температуры. Реакционную смесь фильтруют, и фильтрат собирают. После удаления растворителя при пониженном давлении, остаток обрабатывают 100 мл этилацетата. Раствор экстрагируют 1M HCl (1×100 мл), насыщенным раствором NaHCO3 (2×100 мл) и, наконец, насыщенным раствором соли (2×100 мл). Органический слой собирают и сушат над Na2SO4. После фильтрования, фильтрат выпаривают досуха при пониженном давлении. Остаток очищают с помощью колоночной хроматографии с использованием системы с градиентом растворителей от 100% гексана до 100% этилацетата. При удалении растворителя, получают 3 г желаемого продукта в виде вязкого масла.
Пример 3-5: Синтез ацетата 2,2'-бипирролидинбиспропановой кислоты
К раствору 5 г 2,2'-бипирролидина в 20 мл метанола капельным образом добавляют 6,9 г метилакрилата (6,9 г, 80 ммоль). Полученную в результате реакционную смесь перемешивают при комнатной температуре в течение 16 часов. Реакционную смесь выпаривают досуха с получением 10 г желаемого продукта в виде вязкого масла.
Пример 3-6: Синтез поли(4,4'-триметилендипиперидин- биспропановой кислоты-со-1,3-диаминопропана)
Реакционную смесь, состоящую из 1 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты (Пример 3-1) и 0,387 г 1,3-диаминопропана, нагревают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. После отфильтровывания растворителя, остаток растворяют в 20 мл деионизованной (DI) воды. pH раствора доводят до 2 посредством добавления HCl. Полученный в результате раствор диализируют с помощью DI воды в течение 24 часов с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализном мешке, сушат посредством лиофилизации с получением 90 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-7: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-диаминоэтана)
Реакционную смесь, содержащую 0,5 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты (Пример 3-1) и 0,157 г диаминоэтана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 50 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-8: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,4-диаминобутана)
Реакционную смесь, содержащую 0,5 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,23 г 1,4-диаминобутана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл CH2Cl2, а затем преципитируют в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 60 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-9: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,2-бис(2-аминоэтокси)этана)
Реакционную смесь, содержащую 0,5 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,26 г 1,2-бис(2-аминоэтокси)этана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 60 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-10: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,4-бис(аминометил)бензола)
Реакционную смесь, содержащую 0,5 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,7 г 1,4-бис(аминометил)бензола (0,7 г, 5,1 ммоль), перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 40 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-11: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-2,2'диаминодиэтиламина)
Реакционную смесь, содержащую 0,5 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,35 г 2,2'-диаминодиэтиламина, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 63 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-12: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-N-метил-2,2'-диаминодиэтиламина)
Реакционную смесь, содержащую 1 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,61 г N-метил-2,2' диаминодиэтиламина (0,61 г, 5,2 ммоль) перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 130 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-13: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-N-(3-аминопропил)-1,3-пропандиамина)
Реакционную смесь, содержащую 1 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,68 г N-(3-аминопропил)-1,3-пропандиамина (0,68 г, 5,2 ммоль), перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 180 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-14: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-3,3'-диамино-N-метилдипропиламина)
Реакционную смесь, содержащую 1 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,76 г 3,3'-диамино-N-метилдипропиламина, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 110 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-15: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диамино-2-пропанола)
Реакционную смесь, содержащую 1 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,47 г 1,3-диамино-2-пропанола (0,47 г, 5,2 ммоль), перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 60 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-16: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-4-(4-амино-бутоксил)бутиламина)
Соль 4-(4-амино-бутоксил)бутиламина и HCl (1 г) растворяют в 20 мл метанола. К этому раствору добавляют 0,72 г водного раствора гидроксида натрия (50% масс/масс). Реакционную смесь перемешивают при комнатной температуре в течение 1 часа. После отфильтровывания твердых продуктов, фильтрат выпаривают досуха. Остаток обрабатывают 20 мл этанола. Реакционную смесь фильтруют, и фильтрат выпаривают досуха с получением 0,55 г беловатого твердого продукта. Этот твердый продукт объединяют с 0,75 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты, и полученную в результате реакционную смесь перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 90 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-17: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-3,5-диамино-1,2,4-триазола)
Реакционную смесь, содержащую 1 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,31 г 3,5-диамино-1,2,4-триазола, обрабатывают 1 мл DMSO. Полученную в результате реакционную смесь перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 10 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-18: Синтез поли(пиперазинбиспропановой кислоты-со-диаминоэтана)
Реакционную смесь, содержащую 1 г ацетата пиперазинбиспропановой кислоты (Пример 3-3) и 0,47 г диаминоэтана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 10 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-19: Синтез поли(пиперазинбиспропановой кислоты-со-1,3-диаминопропана)
Реакционную смесь, содержащую 1 г ацетата пиперазинбиспропановой кислоты (Пример 3-3) и 0,5 г 1,3-диаминопропана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 30 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-20: Синтез поли(пиперазинбиспропановой кислоты-со-1,4-диаминобутана)
Реакционную смесь, содержащую 1 г ацетата пиперазинбиспропановой кислоты (Пример 3-3) и 0,6 г 1,4-диаминобутана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 60 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-21: Синтез поли(пиперазинбиспропановой кислоты-со-1,2-бис (2-аминоэтокси)этана)
Реакционную смесь, содержащую 1 г ацетата пиперазинбиспропановой кислоты (Пример 3-3) и 1,15 г 1,2-бис(2-аминоэтокси)этана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 30 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-22: Синтез поли(пиперазинбиспропановой кислоты-со-2,2'-диаминодиэтиламина)
Реакционную смесь, содержащую 1 г ацетата пиперазинбиспропановой кислоты (Пример 3-3) и 0,8 г 2,2'-диаминодиэтиламина, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 60 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-23: Синтез поли(пиперазинбиспропановой кислоты-со-N-метил-2,2'-диаминодиэтиламина)
Реакционную смесь, содержащую 1 г ацетата пиперазинбиспропановой кислоты (Пример 3-3) и 0,9 г N-метил-2,2'-диаминодиэтиламина, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 50 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-24: Синтез поли(пиперазинбиспропановой кислоты-со-N-(3-аминопропил)-1,3-пропандиамина)
Реакционную смесь, содержащую 1 г ацетата пиперазинбиспропановой кислоты (Пример 3-3) и 1,02 г N-(3-аминопропил)-1,3-пропандиамина, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 90 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-25: Синтез поли(пиперазинбиспропановой кислоты-со-3,3'-диамино-N-метилдипропиламина)
Реакционную смесь, содержащую 1 г ацетата пиперазинбиспропановой кислоты (Пример 3-3) и 1,12 г 3,3'-диамино-N-метилдипропиламина, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 120 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-26: Синтез поли(4,4'-дипиперидинбиспропановой кислоты-со-диаминоэтана)
Реакционную смесь, содержащую 1 г ацетата 4,4'-дипиперидинбиспропановой кислоты (Пример 3-2) и 0,31 г диаминоэтана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 90 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-27: Синтез поли(4,4'-дипиперидинбиспропановой кислоты-со-1,3-диаминопропана)
Реакционную смесь, содержащую 1 г ацетата 4,4'-дипиперидинбиспропановой кислоты (Пример 3-2) и 0,38 г 1,3-диаминопропана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 60 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-28: Синтез поли(4,4'-дипиперидинбиспропановой кислоты-со-1,4-диаминобутана)
Реакционную смесь, содержащую 1 г ацетата 4,4'-дипиперидинбиспропановой кислоты (Пример 3-2) и 0,45 г 1,4-диаминобутана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 90 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-29: Синтез поли(4,4'-дипиперидинбиспропановой кислоты-со-1,2-бис(2-аминоэтокси)этана)
Реакционную смесь, содержащую 1 г ацетата 4,4'-дипиперидинбиспропановой кислоты (Пример 3-2) и 0,76 г 1,2-бис(2-аминоэтокси)этана, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 100 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-30: Синтез поли(4,4'-дипиперидинбиспропановой кислоты-со-2,2'-диаминодиэтиламина)
Реакционную смесь, содержащую 1 г ацетата 4,4'-дипиперидинбиспропановой кислоты и 0,45 г 2,2'-диаминодиэтиламина, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 310 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-31: Синтез поли(4,4'-дипиперидинбиспропановой кислоты-со-N-метил-2,2'-диаминодиэтиламина)
Реакционную смесь, содержащую 1 г ацетата 4,4'-дипиперидинбиспропановой кислоты и 0,52 г N-метил-2,2'-диаминодиэтиламина, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 480 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-32: Синтез поли(4,4'-дипиперидинбиспропановой кислоты-со-N-(3-аминопропил)-1,3-пропандиамина)
Реакционную смесь, содержащую 1 г ацетата 4,4'-дипиперидинбиспропановой кислоты и 0,58 г N-(3-аминопропил)- 1,3-пропандиамина, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 540 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-33: Синтез поли(4,4'-дипиперидинбиспропановой кислоты-со-3,3'-диамино-N-метилдипропиламина)
Реакционную смесь, содержащую 1 г ацетата 4,4'-дипиперидинбиспропановой кислоты и 0,64 г 3,3'-диамино-N-метилдипропиламина, перемешивают при 100°C в атмосфере азота в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 420 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-34: Синтез поли(1,1-диакрил-4,4'-триметилендипиперидина-со-1,3-диаминопропана)
Реакционную смесь, содержащую 1 г 1,1'-диакрил-4,4'-триметилендипиперидина, 0,35 г 1,3-диаминопропана и 1 мл метанола, перемешивают при комнатной температуре в течение 18 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 640 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-35: Синтез поли(1,1-диакрил-4,4'-триметилендипиперидина-со-N,N'-диметил-1,3-пропандиамина)
Реакционную смесь, содержащую 1 г 1,1'-диакрил-4,4'-триметилендипиперидина, 0,36 г N,N'-диметил-1,3-пропандиамина и 1 мл метанола, перемешивают при 60°C в течение 24 часов. Растворитель удаляют при пониженном давлении, и остаток растворяют в 20 мл DI воды. pH раствора доводят до 2 посредством добавления HCl. Раствор полимера диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 180 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-36: Синтез поли(1,1-диакрил-4,4'-триметилендипиперидина-со-4,4'-триметилендипиперидина)
Реакционную смесь, содержащую 1 г 1,1'-диакрил-4,4'-триметилендипиперидина, 0,99 г 4,4'-триметилендипиперидина, 1 мл метанола, перемешивают при 60°C в течение 12 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 220 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-37: Синтез поли(1,1-диакрил-4,4'-триметилендипиперидина-со-пиперазина)
Реакционную смесь, содержащую 1 г 1,1'-диакрил-4,4'-триметилендипиперидина, 0,91 г пиперазина гексагидрата и 1 мл метанола, перемешивают при 60°C в течение 12 часов. Полученный в результате продукт растворяют в 5 мл дихлорметана и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 80 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-38: Синтез поли(1,1-диакрил-4,4'-триметилендипиперидина-со-4,4'-бипиперидина)
Раствор, содержащий 1,14 г 4,4'-дипиперидина HCl и 5 мл метанола, обрабатывают 1,14 г карбоната калия. Реакционную смесь перемешивают при комнатной температуре в течение 2 часов. Реакционную смесь фильтруют, и фильтрат объединяют с 1 г 1,1'-диакрил-4,4'-триметилендипиперидина, растворенного в 3 мл метанола. Полученную в результате реакционную смесь перемешивают при 60°C в течение 15 часов. Полученный в результате продукт выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 140 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-39: Синтез поли(1,1'-диакрил-4,4'-триметилендипиперидина-со-гистамина)
Реакционную смесь, содержащую 1 г 1,1'-диакрил-4,4'-триметилендипиперидина, 0,5 г гистамина и 1 мл метанола, перемешивают при 60°C в течение 18 часов. Полученный в результате продукт выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 120 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-40: Синтез поли(1,1'-диакрил-4,4'-триметилендипиперидина-со-3-(диметиламино)-1-пропиламина)
Реакционную смесь, содержащую 1 г 1,1'-диакрил-4,4'-триметилендипиперидина, 0,53 г 3-(диметиламино)-1-пропиламина и 1 мл метанола, перемешивают при 50°C в течение 10 часов. Полученный в результате продукт выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 1 г желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-41: Синтез поли(1,1'-диакрил-4,4'-триметилендипиперидина-со-пропиламина)
Реакционную смесь, содержащую 0,64 г 1,1'-диакрил-4,4'-триметилендипиперидина, 0,35 г пропиламина и 1 мл метанола, перемешивают при 60°C в течение 20 часов. Полученный в результате продукт выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 740 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-42: Синтез поли(1,1'-диакрил-4,4'-триметилендипиперидина-со-1-аминобутил-3-карбамоилпиридиния
Реакционную смесь, содержащую 0,5 г 1,1'-диакрил-4,4'-триметилендипиперидина, 0,35 г 1-аминобутил-3-карбамоилпиридиния и 3 мл метанола, перемешивают при 50°C в течение 20 часов. Полученный в результате продукт выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 20 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-43: Синтез поли(1,1-диакрил-4,4'-триметилендипиперидина-со-1-аминобутил-3-карбамоилпиридиния)-со-4,4'-триметилендипиперидинбиспропановой кислоты-2-дигидрокси-1,3-диаминопропана)
Реакционную смесь, содержащую 1,0 г 1,1'-диакрил-4,4'-триметилендипиперидина, 0,36 г 1-аминобутил-3-карбамоилпиридиния, 0,27 г моно N-boc-1,3-диаминопропана и 3 мл метанола, перемешивают при 50°C в течение 20 часов. Реакционную смесь выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования. Остаток промывают этилацетатом (3×50 мл) и сушат при пониженном давлении.
Указанный выше продукт растворяют в 5 мл метанола и смешивают с 0,5 г 4,4'-триметилендипиперидинбиспропановой кислоты и 0,25 мл концентрированной HCl. Полученную в результате реакционную смесь перемешивают при 50°C в течение 6 часов. Полученный в результате продукт выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 210 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-44: Синтез поли(2,2'-бипирролидинбиспропановой кислоты-со-диаминоэтана)
Реакционную смесь, содержащую 1,0 г ацетата 2,2'-бипирролидинбиспропановой кислоты и 0,38 г диаминоэтана, перемешивают при 100°C в атмосфере азота в течение 20 часов. Полученный в результате продукт растворяют в 3 мл метанола и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 10 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-45: Синтез поли(2,2'-бипирролидинбиспропановой кислоты-со-1,3-диаминопропана)
Реакционную смесь, содержащую 1,0 г ацетата 2,2'-бипирролидинбиспропановой кислоты и 0,47 г 1,3-диаминопропана, перемешивают при 100°C в атмосфере азота в течение 20 часов. Полученный в результате продукт растворяют в 3 мл метанола и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 540 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-46: Синтез поли(2,2'-бипирролидинбиспропановой кислоты-со-1,3-диаминобутана)
Реакционную смесь, содержащую 1,0 г ацетата 2,2'-бипирролидинбиспропановой кислоты и 0,56 г 1,4-диаминобутана, перемешивают при 100°C в атмосфере азота в течение 20 часов. Полученный в результате продукт растворяют в 3 мл метанола и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 380 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-47: Синтез поли(2,2'-бипирролидинбиспропановой кислоты-со-1,5-диаминопентана)
Реакционную смесь, содержащую 1,0 г ацетата 2,2'-бипирролидинбиспропановой кислоты и 0,65 г 1,5-диаминопентана, перемешивают при 100°C в атмосфере азота в течение 20 часов. Полученный в результате продукт растворяют в 3 мл метанола и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 10 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-48: Синтез поли(2,2'-бипирролидинбиспропановой кислоты-со-1,6-диаминогексана)
Реакционную смесь, содержащую 1,0 г ацетата 2,2'-бипирролидинбиспропановой кислоты и 0,74 г 1,6-диаминогексана, перемешивают при 100°C в атмосфере азота в течение 20 часов. Полученный в результате продукт растворяют в 3 мл метанола и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 10 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-49: Синтез поли(4,4-триметилендипиперидинбиспропановой кислоты-со-4-(1,2-диол)-1,4,7-триазагептана)
Пример 3-49(a): Синтез 4-(1,2-диол)-1,4,7-триазагептана
В 5 мл этанола 1 г 1,7-бис-Boc-1,4,7-триазагептана и 0,3 г глицидола добавляют и реакционную смесь нагревают с обратным холодильником в течение 15 часов. Полученный в результате продукт очищают с помощью колоночной хроматографии с использованием системы с градиентом растворителей в пределах от 100% гексан до 100% этилацетата с получением 0,4 г 1,7-бис-boc-4-(1,2-диол)-1,4,7-триазагептана. К 0,4 г 1,7-бис-boc-4-(1,2-диол)-1,4,7-триазагептана, растворенного в 2 мл метанола добавляют 0,3 мл концентрированной HCl. Реакционную смесь перемешивают при 50°C в течение 24 часов. После удаления растворителя при пониженном давлении, остаток растворяют в 10 мл смеси метанол:вода (1:1 объем/объем). К этому раствору добавляют 5,0 г смолы Amberlyst OH 26. После перемешивания при комнатной температуре в течение 3 часов, смолу отфильтровывают. Растворитель выпаривают при пониженном давлении. Полученное в результате масло лиофилизируют досуха с получением 0,15 г желаемого продукта в виде вязкой жидкости.
Пример 3-49(b): Синтез поли(4,4-триметилендипиперидинбиспропановой кислоты-со-4-(1,2-диол)-1,4,7-триазагептана)
Реакционную смесь, содержащую 0,288 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,15 г 4-(1,2-диол)-1,4,7-триазагептана (Пример 3-49(a)), перемешивают при 100°C в течение 18 часов. Полученный в результате продукт растворяют в 3 мл метанола и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 160 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-50: Синтез поли(4,4-триметилендипиперидинбиспропановой кислоты-со-4-(1,2-диол)-1,4,7-триазагептан-со-1,3-диаминопропана)
Реакционную смесь, содержащую 0,25 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты, 0,09 г 4-(1,2-диол)-1,4,7-триазагептана (Пример 3-49(a)) и 0,05 г 1,3-диаминопропана, перемешивают при 100°C в течение 18 часов. Полученный в результате продукт растворяют в 3 мл метанола и выливают в 50 мл этилацетата. Преципитат выделяют посредством фильтрования и растворяют в 20 мл DI воды. После доведения pH раствора до 2, этот раствор диализируют с помощью DI воды с использованием диализной мембраны с порогом отсечки по молекулярной массе 1000 Да. Раствор, остающийся в диализной мембране, лиофилизируют досуха с получением 150 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-51: Синтез поли(4,4-триметилендипиперидинбиспропановой кислоты-со-5-(1,2-диол)-1,5,9-триазанонана)
Пример 3-51(a): Синтез 5-(1,2-диол)-1,5,9-триазанонана
Реакционную смесь, содержащую 1,5 г 1,9-бис-BOC-1,5,9-триазанонана, 0,34 г глицидола и 10 мл этанола, нагревают с обратным холодильником в течение 15 часов. После удаления растворителя, остаток очищают с помощью колоночной хроматографии с использованием системы с градиентом растворителей в пределах от 100% гексан до 100% этилацетата с получением 0,7 г 1,9-бис-boc-5-(1,2-диол)-1,5,9-триазанонана. К 0,7 г 1,9-бис-boc-5-(1,2-диол)-1,5,9-триазанонана, растворенного в 2 мл метанола, добавляют 0,25 мл концентрированной HCl, и реакционную смесь перемешивают при 50°C в течение 24 часов. После удаления растворителя при пониженном давлении, остаток растворяют в 10 мл смеси метанол/вода (1:1) и к ним добавляют 5 г смолы Amberlyst OH 26. После перемешивания при комнатной температуре в течение 3 часов, смолу отфильтровывают. Растворитель удаляют при пониженном давлении, и остаток лиофилизируют досуха с получением 0,28 г желаемого продукта в виде светло-желтого масла.
Пример 3-51(b): Синтез поли(4,4-триметилендипиперидинбиспропановой кислоты-со-5-(1,2-диол)-1,5,9-триазанонана)
Реакционную смесь, содержащую 0,23 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты и 0,15 г 5-(1,2-диол)-1,5,9-триазанонана, перемешивают при 100°C в течение 18 часов. Полученную в результате реакционную смесь растворяют в 5 мл метанола и выливают в 50 мл этилацетата. После отфильтровывания растворителя, остаток растворяют в 20 мл DI воды. pH раствора доводят до 2 посредством добавления разбавленной HCl, и раствор подвергают воздействию центрифугирования с использованием мембранного фильтра Microsep с порог отсечки по молекулярной массе 1000 Да. Фракцию с молекулярной массой выше чем 1000 Да собирают и лиофилизируют досуха с получением 100 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-52: Синтез поли(4,4-триметилендипиперидинбиспропановой кислоты-со-5-(1,2-диол)-1,5,9-триазанонана-со-1,3-диаминопропана).
Реакционную смесь, содержащую 0,125 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты (Пример 3-1), 0,05 г 5-(1,2-диол)-1,5,9-триазанонана (Пример 3-51(a)) и 0,3 г 1,3-диаминопропана, перемешивают при 100°C в течение 18 часов. Полученную в результате реакционную смесь растворяют в 5 мл метанола, вылитого в 50 мл этилацетата. После отфильтровывания растворителя, остаток растворяют в 20 мл DI воды. pH раствора доводят до 2 посредством добавления разбавленной HCl, и раствор подвергают воздействию центрифугирования с использованием мембранного фильтра Microsep с порогом отсечки по молекулярной массе 1000 Да. Фракцию с молекулярной массой выше чем 1000 Да собирают и лиофилизируют досуха с получением 90 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-53: Синтез модифицированного глицидолом поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диаминопропана)
К 0,26 г поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диаминопропана) (Пример 3-6), растворенного в 2 мл этанола, добавляют 16,5 мг глицидола. Реакционную смесь нагревают при 140°C в течение 30 минут с использованием микроволнового реактора. Полученную в результате реакционную смесь выливают в 50 мл этилацетата. После фильтрования, остаток промывают этилацетатом (3×50 мл). Впоследствии, его растворяют в 10 мл DI воды и подвергают воздействию центрифугирования с использованием мембранного фильтра Microsep с порогом отсечки по молекулярной массе 1000 Да. Фракцию с молекулярной массой выше чем 1000 Да собирают и лиофилизируют досуха с получением 126 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-54: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диаминопропана) с окончаниями гуанидина
К 0,3 г поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диаминопропана) (Пример 3-6), растворенного в 2 мл метанола, добавляют 0,1 г 1H-пиразол-1-карбоксамидина и 0,11 г Ν,Ν'-диизопропилэтиламина. Реакционную смесь перемешивают при 60°C в течение 8 часов. Полученную в результате реакционную смесь выливают в 50 мл этилацетата. После фильтрования, остаток промывают этилацетатом (3×50 мл). Полученный в результате твердый продукт растворяют в 2 мл DI воды и пропускают через колонку PD-10 Sephadex. Желаемую фракцию собирают, лиофилизируют досуха с получением 0,19 г полимера в виде светло-желтого твердого продукта.
Пример 3-55: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диаминопропана) с окончаниями полиэтиленгликоля (PEG-4).
К 0,128 г поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диаминопропана) (Пример 3-6), растворенного в 5 мл метанольного раствора добавляют 0,2 мл триэтиламина, а затем 0,075 г сложного эфира m-dPEG4-NHS. Реакционный раствор перемешивают при комнатной температуре в течение 22 часов. Полученную в результате реакционную смесь выливают в 50 мл этилацетата. После фильтрования, остаток промывают этилацетатом (5×50 мл). Впоследствии остаток растворяют в 2 мл DI воды, и pH полученного в результате раствора доводят до 2 с использованием разбавленной HCl, и подвергают этот раствор воздействию центрифугирования с использованием мембранного фильтра Microsep с порогом отсечки по молекулярной массе 1000 Да. Фракцию с молекулярной массой выше чем 1000 Да собирают и лиофилизируют досуха с получением 50 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-56: Синтез поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диаминопропана) с окончаниями полиэтиленгликоля (PEG-12)
К 0,1 г поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диаминопропана) (Пример 3-6), растворенного в 5 мл метанола, добавляют 0,2 мл триэтиламина, а затем 0,12 г сложного эфира m-dPEG12-NHS. Реакционный раствор перемешивают при комнатной температуре в течение 22 часов. Полученную в результате реакционную смесь выливают в 50 мл этилацетата. После фильтрования, остаток промывают этилацетатом (5×50 мл). Впоследствии остаток растворяют в 2 мл DI воды, и pH полученного в результате раствора доводят до 2 с использованием разбавленной HCl, и этот раствор подвергают воздействию центрифугирования с использованием мембранного фильтра Microsep с порогом отсечки по молекулярной массе 1000 Да. Фракцию с молекулярной массой выше чем 1000 Дальтон собирают и лиофилизируют досуха с получением 60 мг желаемого продукта в виде светло-желтого твердого продукта.
Пример 3-57: Синтез монодисперсного полимера (гептамера) поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диаминопропана)
Пример 3-57(a): Синтез тримера 4,4'-триметилендипиперидинбиспропановой кислоты-1,3-диаминопропана
Реакционную смесь, содержащую 3 г ацетата 4,4'-триметилендипиперидинбиспропановой кислоты (Пример 3-2) и 4,1 г моно N-boc-1,3-диаминопропана, перемешивают при 100°C в течение 18 часов. Полученную в результате реакционную смесь очищают с помощью колоночной хроматографии с использованием колонки с амин-модифицированным диоксидом кремния и системы с градиентом растворителей в пределах от 100% гексана до смеси этилацетат/гексан (50/50)). Соответствующие фракции собирают, и растворитель удаляют при пониженном давлении, с получением 2,6 г 4,4'-триметилендипиперидинбиспропановой кислоты-бис-BOC-1,3-диаминопропана.
К 0,55 г 4,4'-триметилендипиперидинбиспропановой кислоты-бис-boc-1,3-диаминопропана, растворенной в 5 мл метанола, добавляют 0,5 мл концентрированной HCl, и реакционную смесь перемешивают при 50°C в течение 10 часов. После удаления растворителя при пониженном давлении, остаток растворяют в смеси 10 мл метанол/вода (1:1) и обрабатывают с помощью 5 г смолы Amberlyst OH 26. После перемешивания при комнатной температуре в течение 3 часов, смолу отфильтровывают. Фильтрат выпаривают досуха, и остаток лиофилизируют с получением 0,5 г продукта в виде белого твердого продукта.
Пример 3-57(b): Синтез 1-BOC-4,4'-триметилен-1'-пропановой кислоты
К 2 г сложного метилового эфира 1-BOC-4,4'-триметилен-1'-пропановой кислоты, добавляют 0,9 г 50% масс водного раствора гидроксида натрия и реакционную смесь перемешивают при 60°C в течение 15 часов. К этой реакционной смеси добавляют концентрированную HCl до тех пор, пока pH реакционной смеси не достигнет 7,5. Реакционную смесь выпаривают досуха, и остаток лиофилизируют до полной сухости. К этому сухому остатку добавляют 10 мл дихлорметана, и полученную в результате смесь перемешивают при комнатной температуре в течение 30 минут. После отфильтровывания нерастворившихся частиц фильтрат выпаривают досуха с получением 0,7 г белого твердого продукта.
Пример 3-57(c): Синтез пентамера бис-boc-4,4'-триметилендипиперидинбиспропановой кислоты-1,3-диаминопропана
К 90 мг 1-boc-4,4'-триметилен-1'-пропановой кислоты (Пример 3-57(b)), растворенной в 2 мл смеси дихлорметан/DMF (1:1 объем/объем) добавляют 38 мг 1,1-карбонилдиимидазола. После перемешивания при комнатной температуре в течение 1 часа, к реакционной смеси добавляют 0,05 г тримера 4,4'-триметилендипиперидинбиспропановой кислоты-1,3-диаминопропана (Пример 3-57(a)). Полученную в результате реакционную смесь перемешивают при комнатной температуре в течение 20 часов. После удаления растворителя при пониженном давлении, остаток очищают с помощью колоночной хроматографии с использованием колонки с амин-модифицированным диоксидом кремния, с использованием системы с градиентом растворителей в пределах от 100% этилацетата до смеси этилацетат/метанол (95/5)) с получением 80 мг продукта в виде бесцветного масла. Это масло растворяют 2 мл метанола с последующим добавлением 0,5 мл концентрированной HCl. Реакционную смесь перемешивают при 50°C в течение 10 часов. Растворитель выпаривают при пониженном давлении и остаток лиофилизируют досуха с получением 60 мг желаемого продукта в виде желтого вязкого масла.
Пример 3-57(d): Синтез гептамера поли(4,4'-триметилендипиперидинбиспропановой кислоты-со-1,3-диаминопропана)
К 35 мг пентамера 4,4'-триметилендипиперидинбиспропановой кислоты-1,3-диаминопропана (Пример 3-57(c)), растворенной в 1 мл метанола, добавляют 0,08 мл триэтиламина и 24 мг boc-(3-акриламидо)пропиламина. Реакционную смесь перемешивают при комнатной температуре в течение ночи. Реакционную смесь выливают в 10 мл этилацетата. Остаток выделяют посредством фильтрования и промывают этилацетатом (3×10 мл). Остаток сушат при комнатной температуре при пониженном давлении с получением 40 мг белого твердого продукта. К этому остатку твердого продукта добавляют 2 мл метанола и 0,5 мл концентрированной HCl. Полученную в результате реакционную смесь дополнительно перемешивают при 50°C в течение 10 часов. После удаления растворителя при пониженном давлении, остаток очищают с помощью препаративной ВЭЖХ с получением 10 мг желаемого продукта в виде светло-желтого вязкого масла.
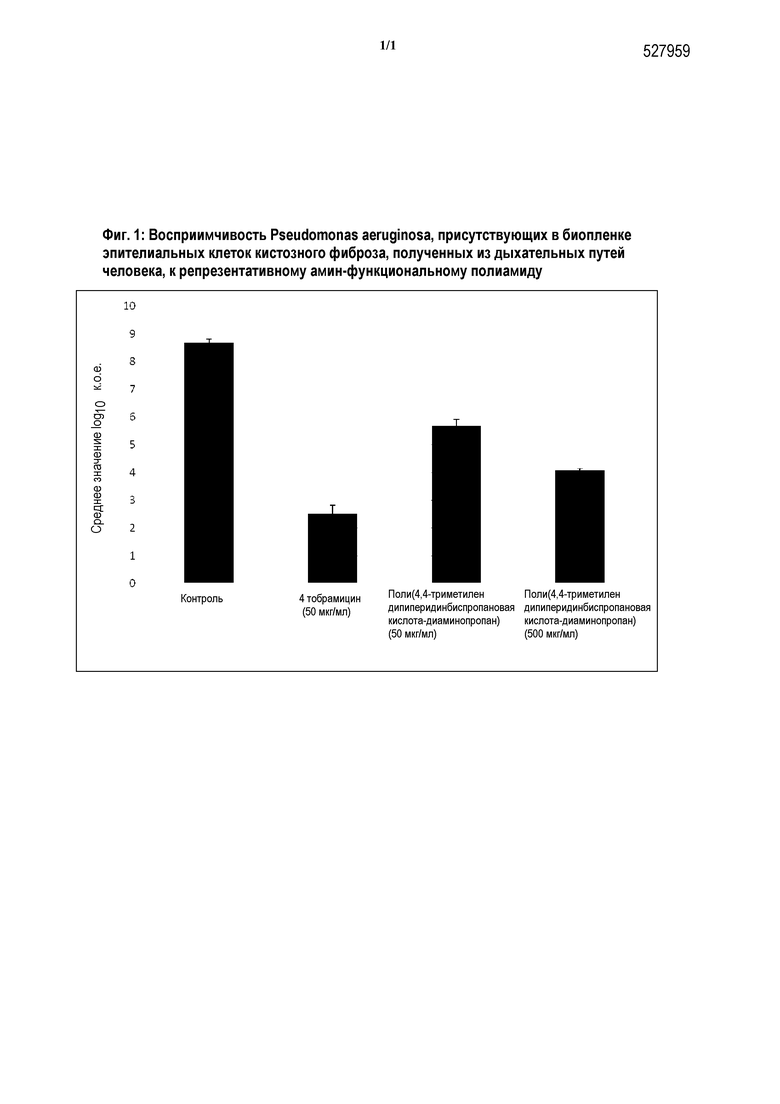
Изобретение относится к соединению формулы (I) и его вариантам, которые могут использоваться в качестве фармацевтических агентов, а также к фармацевтическим композициям, содержащим такие соединения, которые могут быть использованы для лечения или предотвращении мукозита или инфекции. В формуле(I) m равно 0, 1, 2 или 3; n равно 0, 1, 2 или 3; o равно 0, 1, 2 или 3; p равно 0 или 1; r равно 0 или 1; q представляет собой целое число от 1 до 400; Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил; Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил; Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил; Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу. Изобретение позволяет получить фармацевтическую композицию, обладающую высокой противомикробной активностью, и использовать ее при лечении мукозита слизистой оболочки полости рта, хирургической раневой инфекции и легочной инфекции, связанной с кистозным фиброзом. 6 н. и 84 з.п. ф-лы., 1 ил., 7 табл., 57 пр.
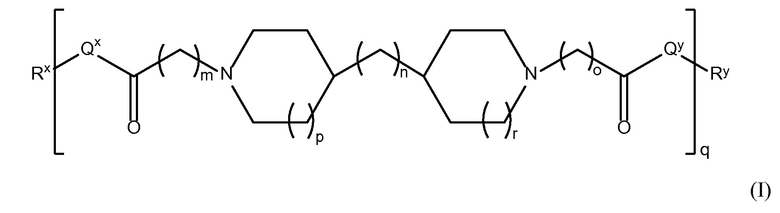
1. Соединение, содержащее структуру Формулы (I):
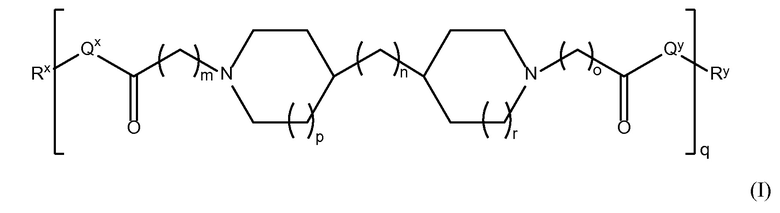
где:
i) m равно 0, 1, 2 или 3;
ii) n равно 0, 1, 2 или 3;
iii) o равно 0, 1, 2 или 3;
iv) p равно 0 или 1;
v) r равно 0 или 1;
vi) q представляет собой целое число от 1 до 400;
vii) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
viii) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
ix) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу.
2. Соединение, содержащее структуру Формулы (II):
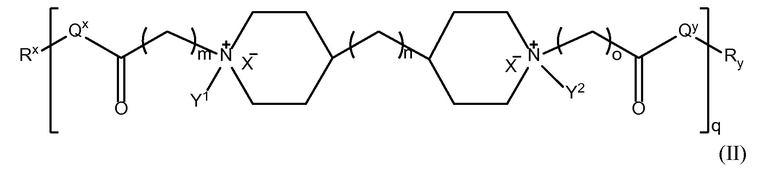
где:
i) m равно 0, 1, 2 или 3;
ii) n равно 0, 1, 2 или 3;
iii) o равно 0, 1, 2 или 3;
iv) p равно 0 или 1;
v) r равно 0 или 1;
vi) q представляет собой целое число от 1 до 400;
vii) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
viii) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил,
(C6-C14)арил или (C2-C9)гетероарил;
ix) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу;
x) X-, каждый, независимо представляет собой галоген или любой фармацевтически приемлемый анион;
xi) Y1 и Y2, каждый, независимо представляют собой H или (C1-C10)алкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из (C1-C10)алкила, (C2-C9)гетероалкила, (C3-C10)циклоалкила, (C2-C9)гетероциклоалкила, (C6-C14)арила, (C2-C9)гетероарила, (C1-C10)алкиламина, -S-O-(C1-C10)алкила, -O(O)C-(C1-C10)алкил, -(C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амида, дигидрокси группы, представленной Формулой (D),
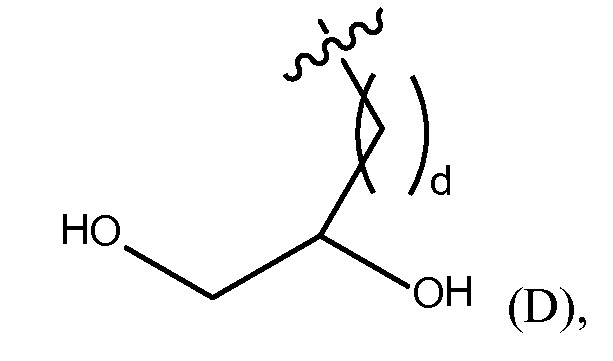
где d представляет собой целое число от 0 до 25, или
полиэтиленгликолевой группы, представленной Формулой (E)
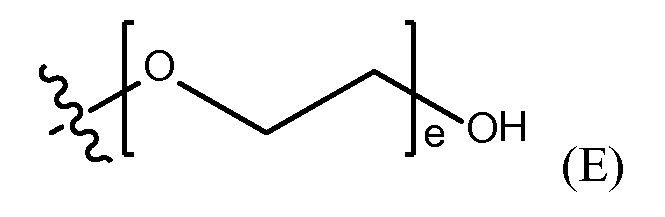
где e представляет собой целое число от 1 до 25.
3. Соединение, содержащее структуру Формулы (III):
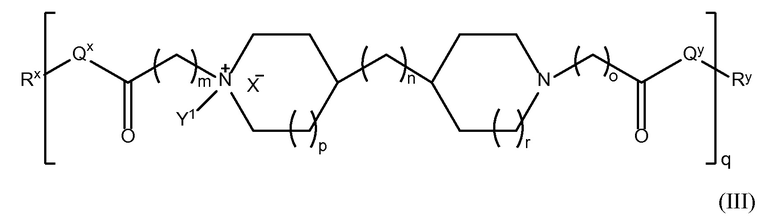
где:
i) m равно 0, 1, 2, или 3;
ii) n равно 0, 1, 2, или 3;
iii) o равно 0, 1, 2, или 3;
iv) p равно 0 или 1;
v) r равно 0 или 1;
vi) q представляет собой целое число от 1 до 400;
vii) Qx представляет собой NH, (C1-C10)алкил, (C2-C9)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил;
viii) Qy представляет собой NH-RW, NH-CH2-RW, (C1-C10)алкил или (C6-C14)арил,
где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил;
ix) Rx и Ry, каждый, независимо представляют собой фармацевтически приемлемую конечную группу;
x) X- представляет собой галоген или любой фармацевтически приемлемый анион;
xi) Y1 представляет собой H или (C1-C10)алкил, необязательно замещенный один или несколькими заместителями, выбранными из группы, состоящей из (C1-C10)алкила, (C2-C9)гетероалкила, (C3-C10)циклоалкила, (C2-C9)гетероциклоалкила, (C6-C14)арила, (C2-C9)гетероарила, (C1-C10)алкиламина, -S-O-(C1-C10)алкила, -O(O)C-(C1-C10)алкила, -(C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH, -OH, амида, дигидрокси группы, представленной Формулой (D),
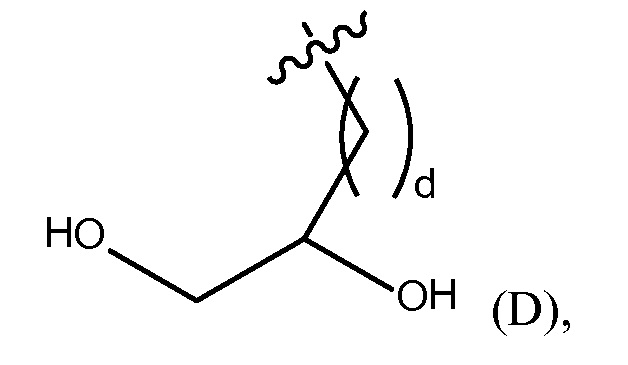
где d представляет собой целое число от 0 до 25, или
полиэтиленгликолевой группы, представленной Формулой (E)
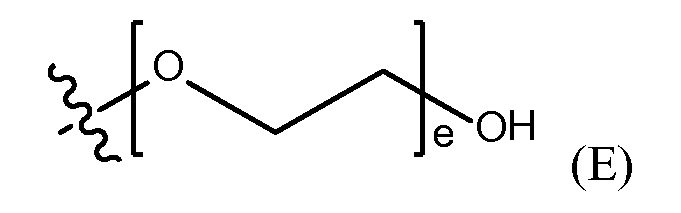
где e представляет собой целое число от 1 до 400.
4. Соединение по п. 1, где n равно 0.
5. Соединение по п. 2, где n равно 0.
6. Соединение по п. 3, где n равно 0.
7. Соединение по п. 1, где n равно 1.
8. Соединение по п. 2, где n равно 1.
9. Соединение по п. 3, где n равно 1.
10. Соединение по п. 1, где n равно 2.
11. Соединение по п. 2, где n равно 2.
12. Соединение по п. 3, где n равно 2.
13. Соединение по п. 1, где n равно 3.
14. Соединение по п. 2, где n равно 3.
15. Соединение по п. 3, где n равно 3.
16. Соединение по п. 1, где p равно 0.
17. Соединение по п. 2, где p равно 0.
18. Соединение по п. 3, где p равно 0.
19. Соединение по п. 1, где p равно 1.
20. Соединение по п. 2, где p равно 1.
21. Соединение по п. 3, где p равно 1.
22. Соединение по п. 1, где r равно 0.
23. Соединение по п. 2, где r равно 0.
24. Соединение по п. 3, где r равно 0.
25. Соединение по п. 1, где r равно 1.
26. Соединение по п. 2, где r равно 1.
27. Соединение по п. 3, где r равно 1.
28. Соединение по п. 1, где p равно 0 и r равно 0.
29. Соединение по п. 2, где p равно 0 и r равно 0.
30. Соединение по п. 2, где p равно 0 и r равно 0.
31. Соединение по п. 1, где p равно 1 и r равно 1.
32. Соединение по п. 2, где p равно 1 и r равно 1.
33. Соединение по п. 3, где p равно 1 и r равно 1.
34. Соединение по п. 1, где n равно 3; p равно 1 и r равно 1.
35. Соединение по п. 2, где n равно 3; p равно 1 и r равно 1.
36. Соединение по п. 3, где n равно 3; p равно 1 и r равно 1.
37. Соединение по п. 1, где n равно 0; p равно 1 и r равно 1.
38. Соединение по п. 2, где n равно 0; p равно 1 и r равно 1.
39. Соединение по п. 3, где n равно 0; p равно 1 и r равно 1.
40. Соединение по п. 1, где n равно 0; p равно 0 и r равно 0.
41. Соединение по п. 2, где n равно 0; p равно 0 и r равно 0.
42. Соединение по п. 3, где n равно 0; p равно 0 и r равно 0.
43. Соединение по п. 31, где
i) Qx представляет собой -NH и
ii) Qy представляет собой NH-RW-, где Rw представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил.
44. Соединение по п. 32, в котором:
i) Qx представляет собой -NH и
ii) Qy представляет собой NH-RW-, где Rw представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил.
45. Соединение по п. 33, в котором:
i) Qx представляет собой -NH и
ii) Qy представляет собой NH-RW-, где Rw представляет собой
(C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил.
46. Соединение по п. 34, где:
i) m равно 2;
ii) o равно 2;
iii) Qx представляет собой NH и
iv) Qy представляет собой NH-RW-, где Rw представляет собой (C3)алкил.
47. Соединение по п. 35, где:
i) m равно 2;
ii) o равно 2;
iii) Y1 представляет собой H и
iv) Y2 представляет собой дигидрокси группу, представленную Формулой (D),
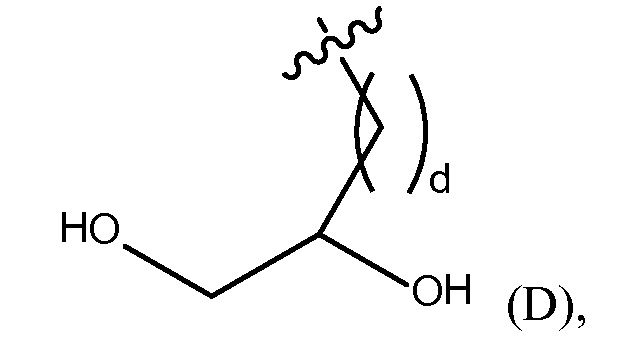
где d равно 1.
48. Соединение по п. 36, где:
i) m равно 2;
ii) o равно 2;
iii) Qx представляет собой NH и
iv) Qy представляет собой NH-RW, где Rw представляет собой (C3)алкил.
49. Соединение по п. 47, где соединение представляет собой полимер.
50. Соединение по п. 48, где соединение представляет собой полимер.
51. Соединение по п. 49, где полимер представляет собой сополимер с соединением по п. 50.
52. Соединение по п. 31, где:
i) m равно 0 и
ii) o равно 0.
53. Соединение по п. 32, где:
i) m равно 0 и
ii) o равно 0.
54. Соединение по п. 33, где:
i) m равно 0 и
ii) o равно 0.
55. Соединение по п. 40, где:
i) Qx представляет собой NH и
ii) Qy представляет собой N-Rw, где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил.
56. Соединение по п. 41, где:
i) Qx представляет собой NH и
ii) Qy представляет собой N-Rw, где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил.
57. Соединение по п. 42, где:
i) Qx представляет собой NH и
ii) Qy представляет собой N-Rw, где Rw отсутствует или представляет собой (C1-C10)алкил, (C2-C9)гетероалкил, (C6-C14)арил или (C2-C9)гетероарил.
58. Соединение по п. 34, где:
i) m равно 2;
ii) o равно 2;
iii) Qx представляет собой NH;
iv) Qy представляет собой NH-RW-, где Rw представляет собой (C3)алкил
v) Rx представляет собой группу гуанидиния хлорида, представленную Формулой (B),
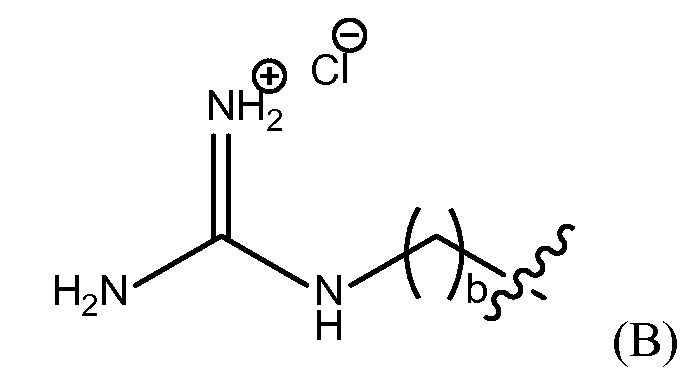
где b равно 3; и
vi) Ry представляет собой группу гуанидиния хлорида, представленную Формулой (B),
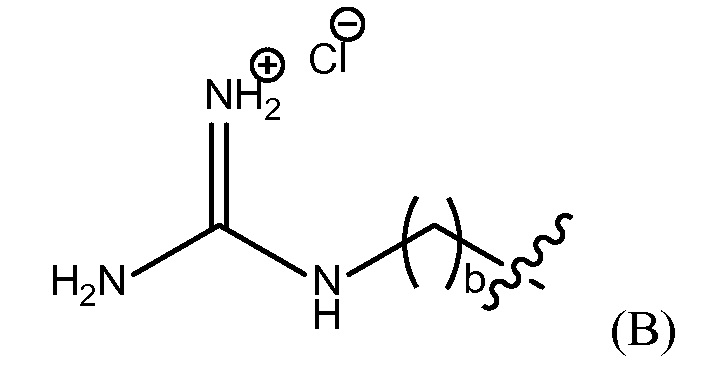
где b равно 0.
59. Соединение по п. 35, где:
i) m равно 2;
ii) o равно 2;
iii) Qx представляет собой NH;
iv) Qy представляет собой NH-RW-, где Rw представляет собой (C3)алкил;
v) Rx представляет собой группу гуанидиния хлорида, представленную Формулой (B),
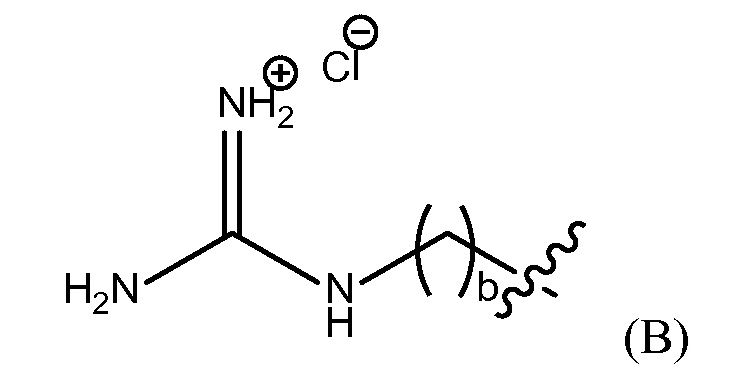
где b равно 3; и
vi) Ry представляет собой группу гуанидиния хлорида, представленную Формулой (B),
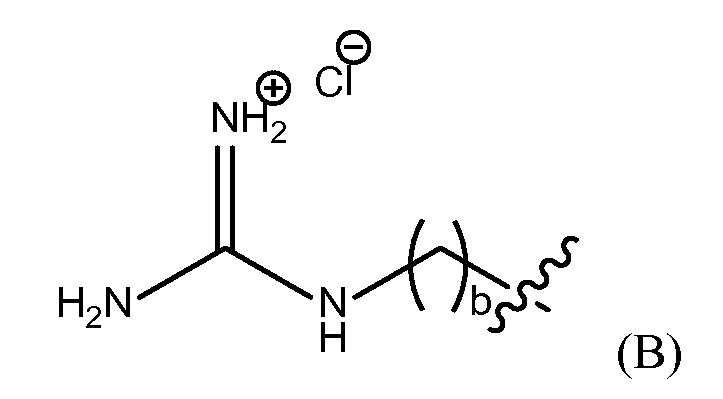
где b равно 0.
60. Соединение по п. 36, где:
i) m равно 2;
ii) o равно 2;
iii) Qx представляет собой NH;
iv) Qy представляет собой NH-RW-, где Rw представляет собой (C3)алкил;
v) Rx представляет собой группу гуанидиния хлорида, представленную Формулой (B),
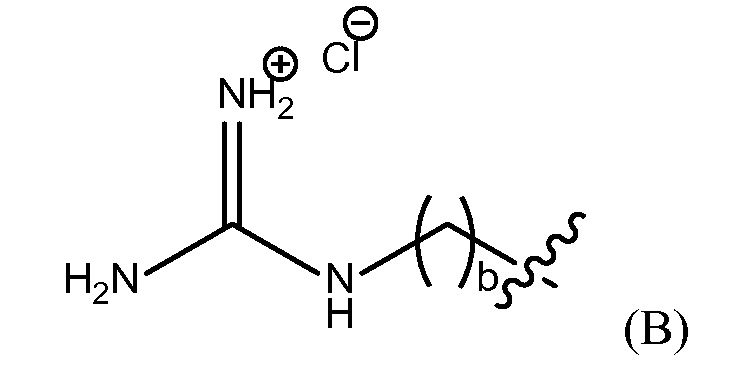
где b равно 3; и
vi) Ry представляет собой группу гуанидиния хлорида, представленную Формулой (B),
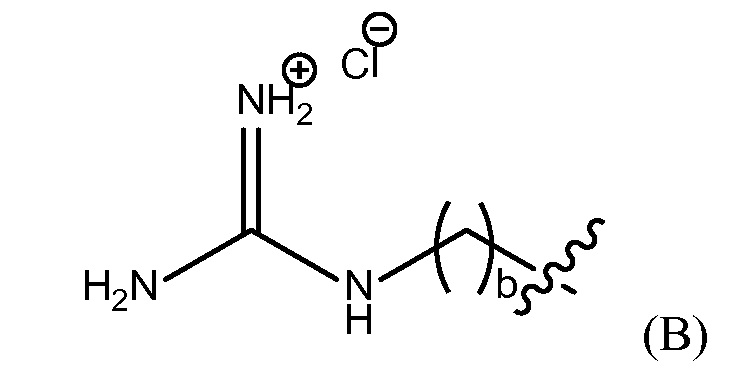
где b равно 0.
61. Соединение по п. 1, где Rx и Ry, каждый, независимо представляют собой H, (C1-C10)алкил, (C2-C0)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил, (C1-C10)алкиламин, -O(O)C-(C1-C10)алкил, (C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амид, гуанидино группу, представленную Формулой (A)
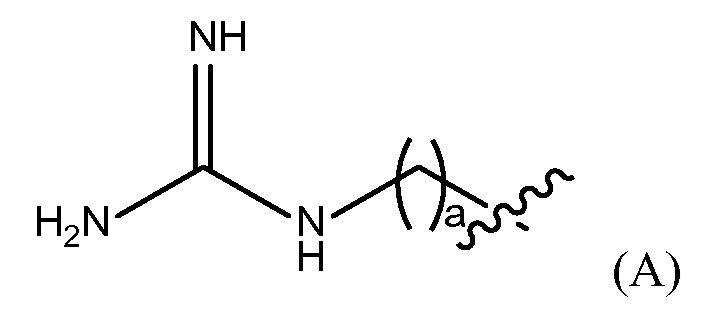
где a представляет собой целое число от 0 до 25,
группу гуанидиния хлорида, представленную Формулой (B),
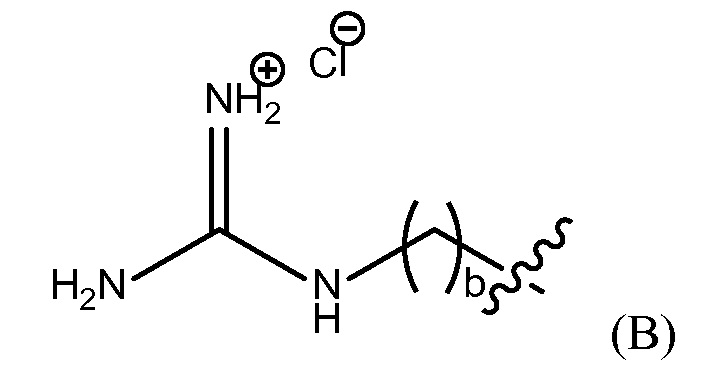
где b представляет собой целое число от 0 до 25,
гуанидинобензольную группу, представленную Формулой (C),
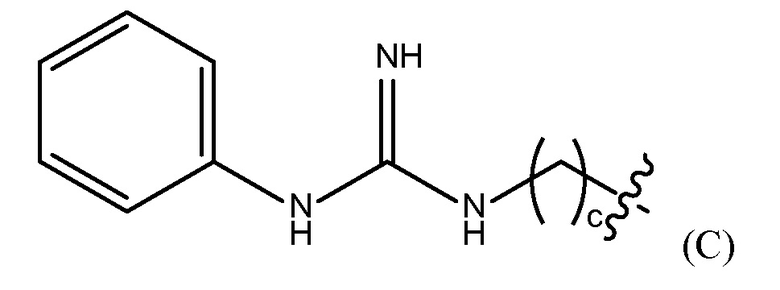
где c представляет собой целое число от 0 до 25.
дигидрокси группу, представленную Формулой (D),
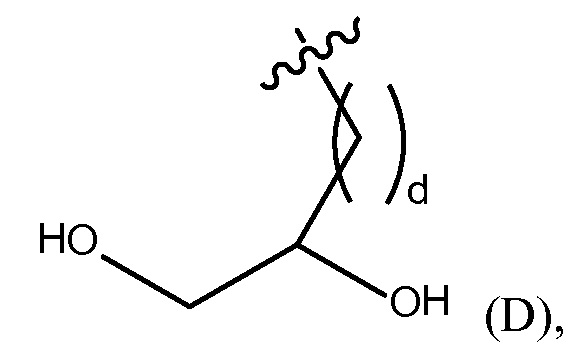
где d представляет собой целое число от 0 до 25, или
полиэтиленгликолевую группу, представленную Формулой (E)
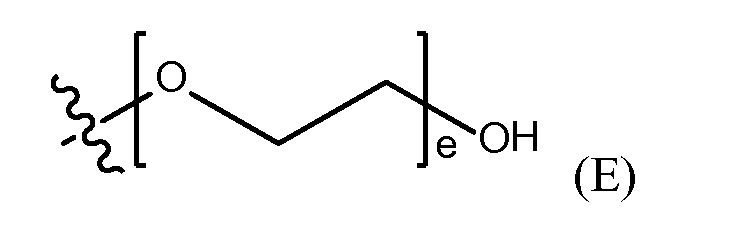
где e представляет собой целое число от 1 до 400.
62. Соединение по п. 61, где Rx и Ry, каждый независимо выбирают из -(O)CH3, гуанидино группы, представленной Формулой (A)
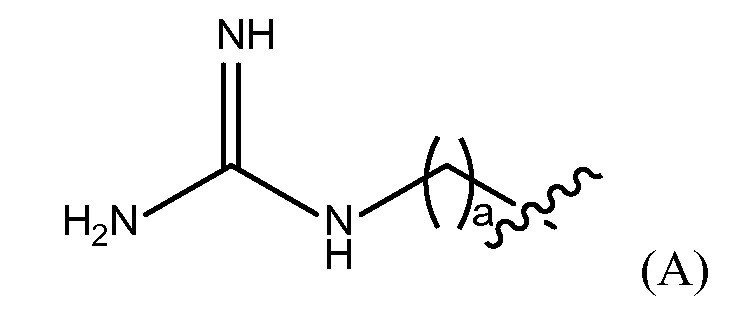
где a представляет собой целое число от 0 до 25, или
гуанидинобензольной группы, представленной Формулой (C),
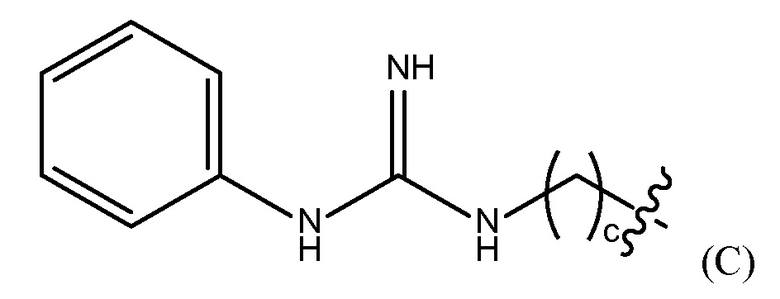
где c представляет собой целое число от 0 до 25.
63. Соединение по п. 2, где Rx и Ry, каждый, независимо представляют собой H, (C1-C10)алкил, (C2-C0)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил, (C1-C10)алкиламин, -O(O)C-(C1-C10)алкил, (C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амид, гуанидино группу, представленную Формулой (A)
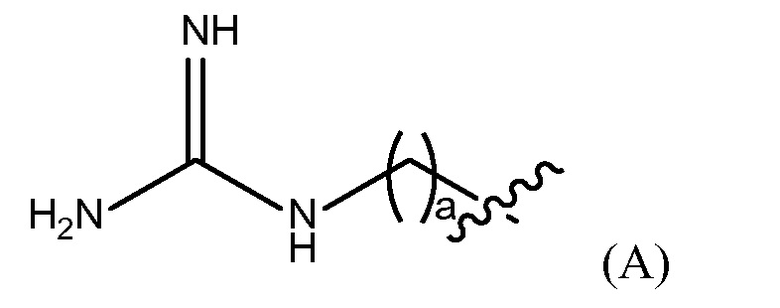
где a представляет собой целое число от 0 до 25,
группу гуанидиния хлорида, представленную Формулой (B),
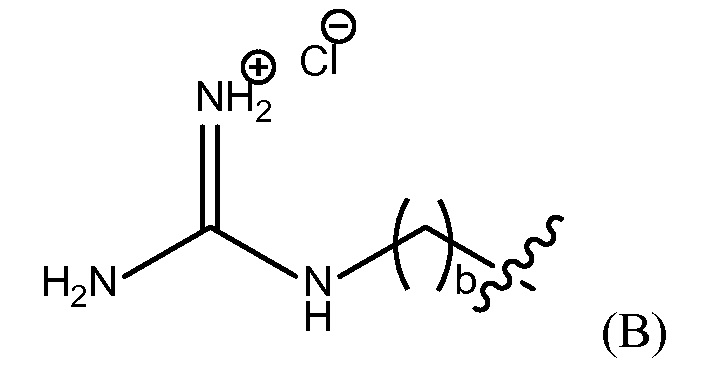
где b представляет собой целое число от 0 до 25,
гуанидинобензольную группу, представленную Формулой (C),
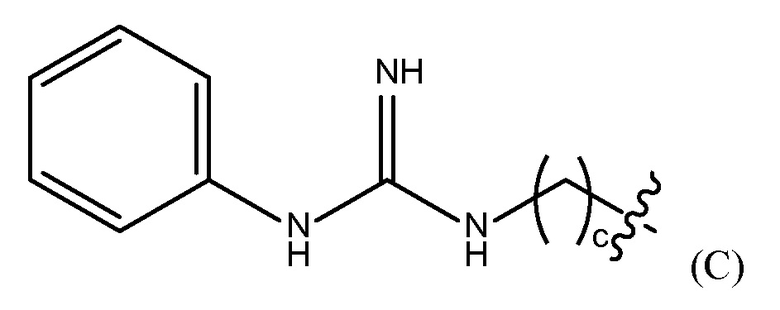
где c представляет собой целое число от 0 до 25,
дигидрокси группу, представленную Формулой (D),
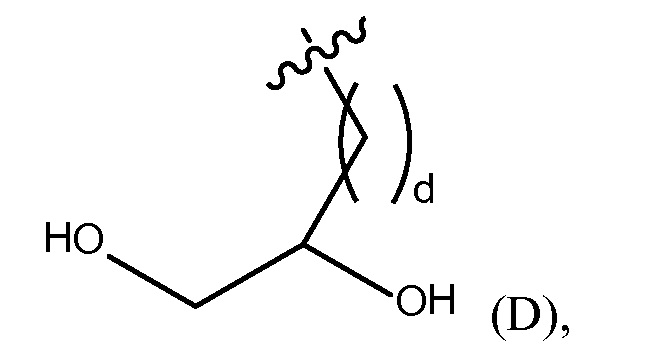
где d представляет собой целое число от 0 до 25, или
полиэтиленгликолевую группу, представленную Формулой (E)
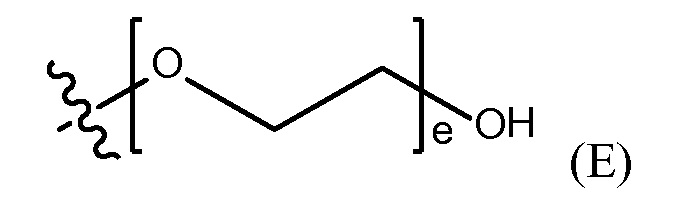
где e представляет собой целое число от 1 до 400.
64. Соединение по п. 63, где Rx и Ry, каждый, независимо выбирают из -(O)CH3, гуанидино группы, представленной Формулой (A)
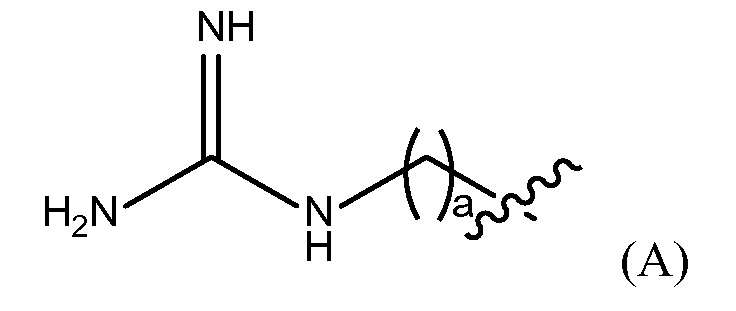
где a представляет собой целое число от 0 до 25, или
гуанидинобензольной группы, представленной Формулой (C),
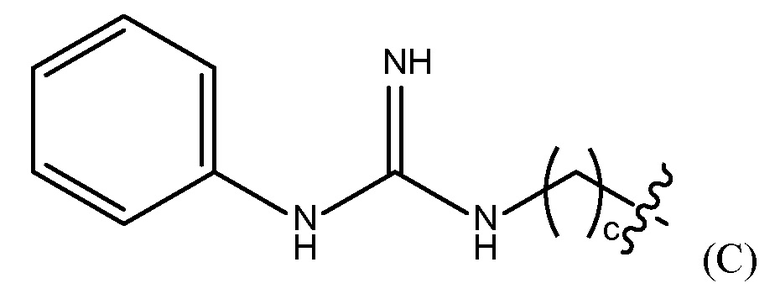
где c представляет собой целое число от 0 до 25.
65. Соединение по п. 3, где Rx и Ry, каждый, независимо представляют собой H, (C1-C10)алкил, (C2-C0)гетероалкил, (C3-C10)циклоалкил, (C2-C9)гетероциклоалкил, (C6-C14)арил, (C2-C9)гетероарил, (C1-C10)алкиламин, -O(O)C-(C1-C10)алкил, (C1-C10)алкил-COOH, (C3-C10)циклоалкил-COOH, -(O)CH3, -OH, амид, гуанидино группу, представленную Формулой (A)
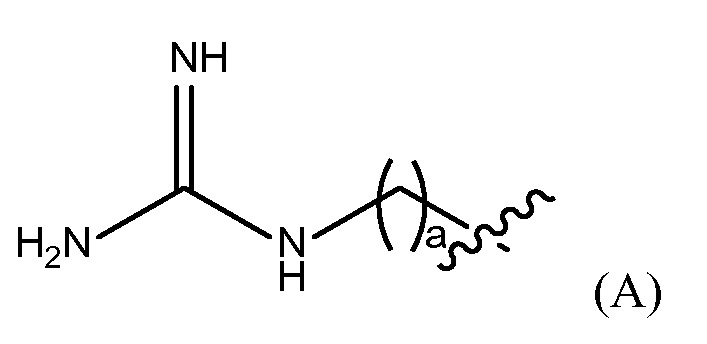
где a представляет собой целое число от 0 до 25, группу гуанидиния хлорида, представленную Формулой (B),
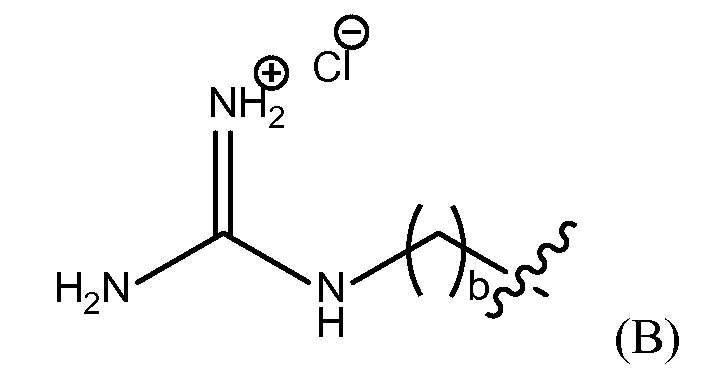
где b представляет собой целое число от 0 до 25,
гуанидинобензольную группу, представленную Формулой (C),
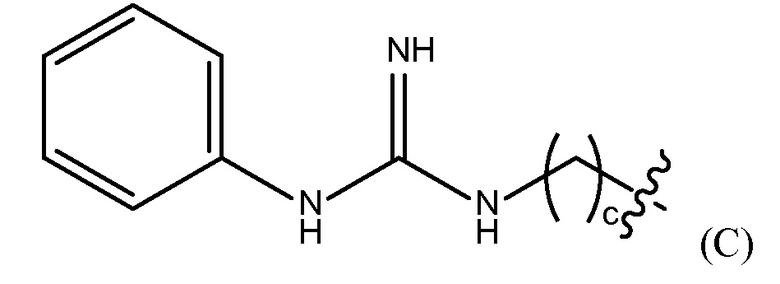
где c представляет собой целое число от 0 до 25, дигидрокси группу, представленную Формулой (D),
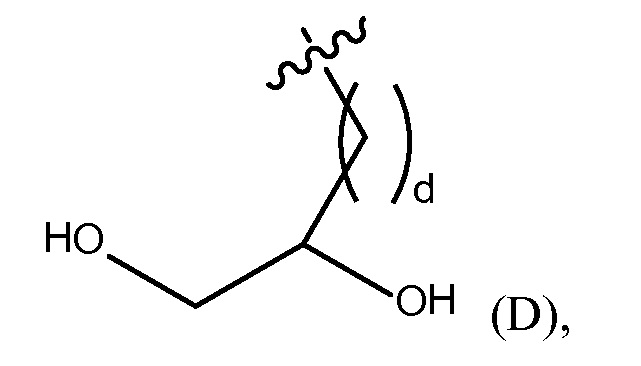
где d представляет собой целое число от 0 до 25, или
полиэтиленгликолевую группу, представленную Формулой (E)
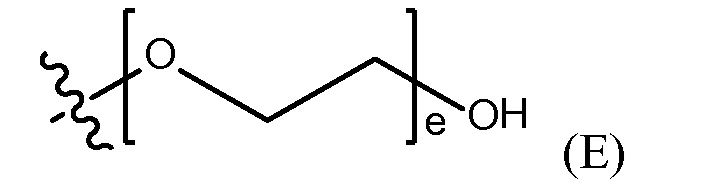
где e представляет собой целое число от 1 до 400.
66. Соединение по п. 65, где Rx и Ry, каждый, независимо выбирают из -(O)CH3, гуанидино группы, представленной Формулой (A)
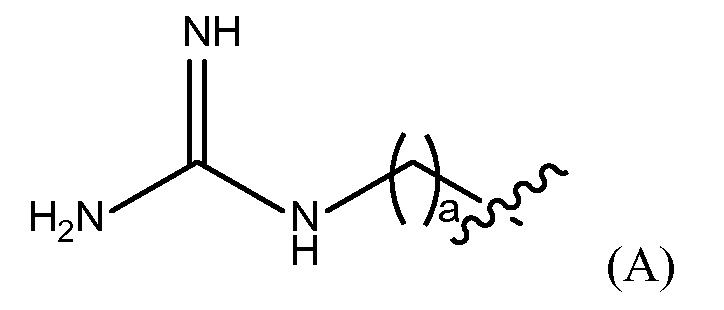
где a представляет собой целое число от 0 до 25, или
гуанидинобензольной группы, представленной Формулой (C),
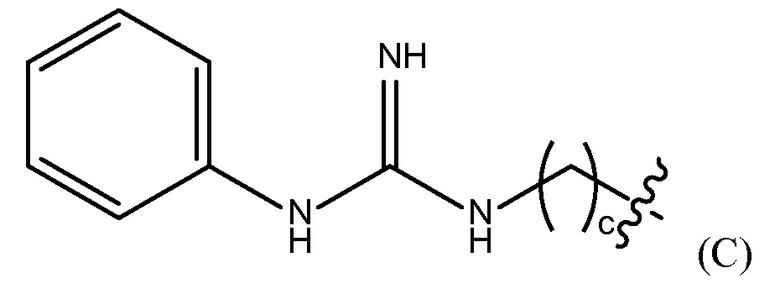
где c представляет собой целое число от 0 до 25.
67. Фармацевтическая композиция, содержащая соединение по п. 1.
68. Фармацевтическая композиция, содержащая соединение по п. 2.
69. Фармацевтическая композиция, содержащая соединение по п. 3.
70. Фармацевтическая композиция по п. 67 для применения при лечении мукозита.
71. Фармацевтическая композиция по п. 68 для применения при лечении мукозита.
72. Фармацевтическая композиция по п. 69 для применения при лечении мукозита.
73. Фармацевтическая композиция по п. 67 для применения при лечении мукозита слизистой оболочки полости рта.
74. Фармацевтическая композиция по п. 68 для применения при лечении мукозита слизистой оболочки полости рта.
75. Фармацевтическая композиция по п. 69 для применения при лечении мукозита слизистой оболочки полости рта.
76. Фармацевтическая композиция по п. 67 для применения при лечении инфекции.
77. Фармацевтическая композиция по п. 68 для применения при лечении инфекции.
78. Фармацевтическая композиция по п. 69 для применения при лечении инфекции.
79. Фармацевтическая композиция по п. 76, где инфекция представляет собой хирургическую раневую инфекцию.
80. Фармацевтическая композиция по п. 76, где инфекция представляет собой легочную инфекцию, связанную с кистозным фиброзом.
81. Фармацевтическая композиция по п. 80, где инфекция представляет собой легочную инфекцию Pseudomonas aeruginosa.
82. Фармацевтическая композиция по п. 81, где при легочной инфекции Pseudomonas aeruginosa присутствуют биопленки.
83. Фармацевтическая композиция по п. 77, где инфекция представляет собой хирургическую раневую инфекцию.
84. Фармацевтическая композиция по п. 77, где инфекция представляет собой легочную инфекцию, связанную с кистозным фиброзом.
85. Фармацевтическая композиция по п. 84, где инфекция представляет собой легочную инфекцию Pseudomonas aeruginosa.
86. Фармацевтическая композиция по п. 85, где при легочной инфекции Pseudomonas aeruginosa присутствуют биопленки.
87. Фармацевтическая композиция по п. 78, где инфекция представляет собой хирургическую раневую инфекцию.
88. Фармацевтическая композиция по п. 78, где инфекция представляет собой легочную инфекцию, связанную с кистозным фиброзом.
89. Фармацевтическая композиция по п. 88, где инфекция представляет собой легочную инфекцию Pseudomonas aeruginosa.
90. Фармацевтическая композиция по п. 89, где при легочной инфекции Pseudomonas aeruginosa присутствуют биопленки.
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2018-02-13—Публикация
2014-03-11—Подача