Короткий пептид, обладающий цитотоксическим действием
Изобретение относится к фармацевтической химии и непосредственно касается новых коротких пептидов, обладающих цитотоксической активностью, которые могут быть применены для лечения онкологических заболеваний.
Как известно, к коротким пептидам относят пептидный белок - Соматостатин (SRIF) -пептидный гормон, обнаруженный в 1973 г. (Brazeau P. et al. Science. 1973, Vol. 179, No 4068, P. 77-79). SRIF представляет собой циклический тетрадекапептидный гормон, содержащий дисульфидный мостик между положением 3 и положением 14 (Heiman, et al., Neuroendocrinology, 1987, Vol. 45, P. 429-436). Выявлено, что Соматостатин вырабатывается дельта-клетками поджелудочной железы, желудка и кишечника и также является одним из гормонов гипоталамуса. Он обладает способностью ингибировать высвобождение гормона роста (ГР, GH) и тиреотропного гормона (ТТГ, TSH), ингибировать высвобождение амилина, инсулина и глюкагона, снижать секрецию желудочного сока и высвобождение нейротрансмиттеров. SRIF действует также в качестве нейромодулятора в центральной нервной системе.
Наряду с этим соматостатин обладает широким спектром биологического действия - угнетает выделение пролактина, инсулина, глюкагона, гормонов поджелудочной железы и желудочно-кишечного тракта, стимулирующих пролиферативные процессы в клетке (Buscail L., Vernejoul F., Faure P., Torrisani J., Susini C. Ann Endocrinol. - 2002. - Vol. 63. - P. 2S13-8).
Соматостатин оказывает свое биологическое влияние через взаимодействие с рецепторами, расположенными на мембранах клеток. В настоящее время различают 5 типов рецепторов к соматостатину: SST1, SST2, SST3, SST4 и SST5, которые имеются как в тканях различных областей ЦНС, так и в периферических тканях (Adams R.L., Adams I.P., Lindow S.W. et al. Br. J. Cancer. - 2005. - 92. - P. 1493-1498; Kilian M., Gregor J. I., Heukamp I. et al. Clin. Exp.Metastasis. - 2009. - 26. - P. 719-727).
Несмотря на полученные положительные результаты, применение соматостатина сильно ограничено из-за его короткого периода жизни в плазме (1-3 мин) (Chapman I. М., Helfgott A., Willoughby J. О. J. Endocrinol. - 1991. - 128. - P. 369-374). Метаболизм соматостатина аминопептидазами и карбоксипептидазами сокращает период его действия. В связи с коротким сроком жизни нативного соматостатина разрабатываются различные аналоги соматостатина, например, для лечения акромегалии (Raynor, et al., Molecular Pharmacol. 43:838 (1993)).
Оказалось, что для сохранения активности критически важным является наличие в циклической части молекулы последовательности Phe7-Trp8-Lys9-Thr10. Остаток Trp8-Lys9 образует часть β-изгиба, который обычно стабилизируется заменой L-Trp на D-Trp, циклизацией скелета, дисульфидным мостиком или всеми ограничениями (Veber, D. F.. Freidinger, R. М., Schwenk-Perlow, D. et al. Nature (Lond.). 1981. - 292. - P. 55-58.). Аминокислотные фрагменты Trp и Lys обязательны, a Phe и Thr могут быть заменены, например, на Tyr и Ser или Val соответственно.
Пептидные аналоги соматостатина имеют ряд ограничений в клиническом применении, таких как низкая оральная биодоступность, относительно короткий период полураспада и иммуногенность. Практическое применение синтетических пептидных аналогов также лимитируется наличием тахифилаксии (быстрое снижение лечебного эффекта при повторном применении) и значительных антисереторных эффектов. Поэтому поиск новых метаболически стабильных синтетических агонистов соматостатина является актуальной задачей в целях улучшения клинического профиля.
Одним из путей поиска эффективных аналогов соматостатина является синтез пептидов линейной структуры.
Исследованы N-замещенные нипекотиновые и изонипекотиновые амиды дипептида beta-methylTrp-Lys-OBu-t, среди которых найдены новые селективные агонисты рецептора соматостатина 2 типа (Zhou С. et al. Bioorg. Med. Chem. Lett. 2001, Vol. 11, P. 415-417). Конъюгаты замещенной мочевины и дипептидов D-Trp-Lys-OH и D-Trp-Lys-NH2 также показали высокую активность и селективность к рецептору соматостатина 2 типа (Yang L., Guo L., Pasternak A. et al. Journal of Medicinal Chemistry, 1998, Vol. 41, No. 13, P. 2175-2179).
С целью уменьшения размеров пептида и сохранения антипролиферативной активности на основе биологически значимой аминокислотной последовательности Tyr-D-Trp-Lys пептида ТТ-232 были синтезированы короткие пептиды и пептидомиметики линейной структуры с двумя или тремя аминокислотами и Вос-защищенной аминогруппой, где Boc обозначает трет-бутилоксикарбоксильную группу (Kuriyama I. et al. Biorg. Med. Chem. 2013, Vol. 21, №2, P. 403-411). Наиболее активным признано соединение - Boc-Tyr-Ile-1-naphthylamide, которое ингибирует ДНК полимеразу-β млекопитающих, значительно подавляет рост раковых клеток карциномы толстой кишки человека (НСТ116). В процессе исследования активности амидов дипептидов (Boc-Tyr-D-Trp-1-адамантиламид) и (Вос-Tyr-D-Trp-2-адамантиламид) выявлено, что они сильно подавляют рост клеток НСТ116 (Kuriyama I. et al. Anticancer Res. 2010, Vol. 30, №12, P. 4841-4849). Необходимо отметить, что при удалении Вос-группы в данных пептидах их активность значительно снижается. Часто модификация молекул адамантановым фрагментом осуществляется для повышения липофильности и стабильности лекарственных средств, тем самым улучшая их фармакокинетику. Введение жесткого диаминоадамантанового фрагмента и D-триптофана в сверхмалый цикл одного из аналогов соматостатина для стабилизации конформационного бета-поворота пептида привело к увеличению селективности к рецепторам sst2 (Blakeney J. S., Reid R. C., Le G. Т., Fairlie D. P. Nonpeptidic Ligands for Peptide-Activated G Protein-Coupled Receptors. Chem. Rev. 2007, 107, 2960-3041). Этот аналог имеет высокое сродство к рецепторам sst2 (KD=63 нМ) и ингибирует высвобождение гормона роста in vitro и in vivo в опытах на крысах.
Наиболее сходными по своей структуре к предлагаемым коротким пептидам являются известные аналоги соматостатина линейной структуры с защитными группами, общей формулы R(R1)Cys-Phe-D-Trp-Lys(R2)-Thr-R3, основанные на фрагменте октреотида: Phe7-D-Trp8-Lys9-Thr10, входящие в качестве активного компонента в средство, обладающее противоопухолевым действием (RU 2254139, А61К 38/08, 2005). Эти пептиды частично сохраняют специфические гормональные свойства соматостатина, что проявляется подавлением секреции гормона роста (СТГ), пролактина и инсулина соответствующими эндокринными железами, наряду со значительным противоопухолевым эффектом in vitro и in vivo (Кубасова И.Ю., Борисова Л.М., Киселева М.П. и др. Российский биотерапевтический журнал. 2006. Т. 5, №3. С. 128-133; Балаев А.Н., Осипов В.Н., Федоров В.Е. и др. Российский биотерапевтический журнал. 2012. Т. 11, №4. С. 47-53; Балаев А.Н., Осипов В.Н., Федоров В.Е. и др. Российский биотерапевтический журнал. 2013. Т. 12, №3. С. 57-60). Выявлено, что наиболее активным является пентапептид Boc-Cys(Thp)-Phe-D-Trp-Lys(Z)-Thr-ОМе, который проявляет более высокую цитотоксическую активность, чем нативный соматостатин (Михаевич Е.И., Красильников М.А. Бюллетень экспериментальной биологии и медицины. 2012. Т. 154, №11. С. 629-632). В данной работе показано, что индуцированный пептидом апоптоз развивается по р53-независимому механизму и сопровождается ранним подавлением активности NF-kB. Благодаря защите всех реакционно-способных групп этот пептид частично сохраняется в кислой среде желудка, что дает возможность орального применения. Данное свойство в сочетании с небольшим размером молекулы и высокой цитотоксической активностью делает этот класс соединений потенциально перспективным для терапии опухолей.
Получение пептидов, рассматриваемых как аналоги заявляемым, описано ранее в ряде публикаций.
Одним из ключевых полупродуктов для синтеза новых заявляемых соединений является пептид H-Phe-D-Trp-Lys(Boc)-Thr-OMe, синтез которого описан ранее в статьях: «Балаев А.Н., Охманович К.А., Осипов В.Н. и др. Получение H-Phe-D-Trp-Lys(ε-Boc)-Thr-ОМе - тетрапептидного фрагмента синтеза аналогов соматостатина // Российский биотерапевтический журнал. 2011 г. Т. 10, №4, С. 43-47», «Балаев А.Н., Осипов В.Н., Охманович, Фёдоров В.Е. Использование F-комплекса при получении Z-Phe-D-Trp-Lys(ε-Вос)ОН в полупромышленном масштабе // Химико-фармацевтический журнал. 2014. Т. 48, №5. С. 40-42». Синтез проводился по оригинальной схеме с использованием F-комплекса для получения активированного пентафторфенилового эфира дипептида H-Phe-D-Trp-OPfp с последующим присоединением к нему гамма-Бок-лизина и метилового эфира треонина по С-концу. Дальнейшее удаление бензилоксикарбонильной группы гидрированием на палладиевом катализаторе приводило к целевому соединению.
Синтез другого структурного аналога - пептида - Boc-Cys(Acm)-Phe-D-Trp-Lys(Boc)-Thr-OMe описан ранее в статье «Балаев А.Н., Осипов В.Н., Фёдоров В.Е. и др. Синтез и изучение цитотоксической активности аналогов гипоталамического гормона соматостатина // Российский биотерапевтический журнал. 2012. Т. 11, №4. С. 47-53» Синтез проводился карбодиимидным методом взаимодействием Boc-Cys(Acm)-OH с тетрапептидом H-Phe-D-Trp-Lys(Boc)-Thr-OMe.
Целью настоящего изобретения является получение новых производных коротких адамантилпроизводных пептидов, обладающих цитотоксическим действием, низкой токсичностью, с возможностью орального применения и с расширенным спектром противоопухолевого действия.
В качестве таких соединений предлагается короткий пептид, обладающий цитотоксическим действием, общей формулы:
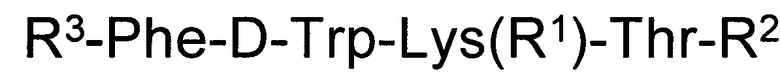 ,
,
где R1 представляет собой Н или трет-бутилоксикарбонил;
R2 представляет собой 1-аминоадамантильную, 1-амино-(1-адамантил)этильную группу;
R3 представляет собой R4-Cys(R5)- или 3-R4-тиазолидин-4-карбонил,
где R4 представляет собой Н или трет-бутилоксикарбонил;
R5 представляет собой Н, или трет-бутилоксикарбонил, или ацетомидометил.
Предлагается короткий пептид, обладающий цитотоксическим действием, выбранный из группы:
Boc-Cys(Acm)-Phe-D-Trp-Lys(Вос)-Thr-1-(1 адамантил)-этиламид,
Вос-Thz-Phe-D-Trp-Lys(Вос)-Thr-1-(1 адамантил)-этиламид,
Boc-Cys(Boc)-Phe-D-Trp-Lys(Boc)-Thr-1-адамантиламид,
Boc-Cys(Acm)-Phe-D-Trp-Lys(Boc)-Thr-1-адамантиламид,
Boc-Thz-Phe-D-Trp-Lys(Boc)-Thr-NH-1-адамантиламид,
где Boc обозначает трет-бутилкарбоксильную группу, Acm - ацетамидометильную группу,
Thz - остаток тиазолидин-4-карбоновой кислоты.
Все заявляемые и полученные соединения содержат общую аминокислотную последовательность из четырех аминокислот Phe-D-Trp-Lys-Thr, которая важна для сохранения активности как аналогов соматостатина. Также полученные соединения содержат цистеин или циклическое производное цистеина - тиазолидин-4-карбоновую кислоту (тиопролин), которое получают в результате взаимодействия цистеина и формальдегида, а также адамантильную группу, которая повышает цитотоксическую активность пептидов, а также их липофильность и протеолитическую стабильность.
В представленных формулах:
Boc обозначает трет-бутилкарбоксильную группу,
Acm обозначает ацетамидометильную группу,
Thz обозначает остаток тиазолидин-4-карбоновой кислоты: 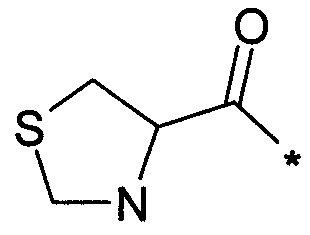 ,
,
1-адамантиламид обозначает 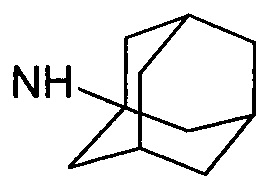 ,
,
1-(1-адамантил)этиламид обозначает 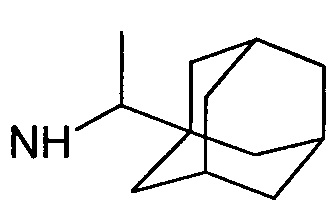 .
.
Наличие адамантанового фрагмента значительно усиливает цитотоксическое действие заявляемых соединений, при этом токсичность по отношению к нераковым клеткам - эмбриональным фибробластам человека остается низкой. Кроме того, добавление фрагмента адамантана в молекулу значительно повышает липофильность и стабильность пептидов, увеличивает проницаемость их через различные биологические мембраны, тем самым улучшая фармакокинетику лекарственных препаратов.
Особым преимуществом новых соединений является их высокая устойчивость к ферментативному разложению и возможность орального применения.
Введение может быть осуществлено любым из способов, принятых для фармацевтических, предпочтительно онкологических, средств, включая оральные и парентеральные способы, как, например, введение подкожно, внутривенно, внутримышечно и внутрибрюшинно.
Соединения могут быть введены по отдельности или в виде фармацевтических композиций.
Новые соединения получают известными методами синтеза, применимыми в пептидной химии. Пептиды синтезируют последовательным соединением аминокислот или путем связывания подходящих небольших пептидных фрагментов. При последовательном соединении, начиная с С-конца, пептидная цепь удлиняется постепенно, каждый раз на одну аминокислоту. При взаимодействии олигопептидов соединяют вместе фрагменты различной длины, а последние в свою очередь могут быть получены путем последовательного наращивания пептидной цепочки из аминокислот или из более коротких пептидов через образование амидных связей.
Химические способы для синтеза новых пептидов подробно описаны в «Synthesis of Peptides and Peptidomimetics in Houben-Weyl Methods in Organic Chemis-try Vol. E-22a / Eds. Goodman M., Felix A., Moroder L., and Toniolo C., Thieme Verlag, Stuttgart, Germany. - 2002».
Одними из ключевых полупродуктов для синтеза новых соединений являются:
пептид H-Phe-D-Trp-Lys(Boc)-Thr-OMe и пептид Вос-Cys(Acm)-Phe-D-Trp-Lys(Вос)-ThrOMe, синтез которых описан выше. Новые адамантилпроизводные пептиды синтезируют путем жидкофазного синтеза с использованием стандартной методики с Z- и Вос-защитными группами.
Ниже приводятся примеры осуществления изобретения:
Пример 1
Получение Вос-Cys(Acm)-Phe-D-Trp-Lys(Вос)-Thr-ОН
Растворяют 500 мг Вос-Cys(Acm)-Phe-D-Trp-Lys(Вос)-Thr-ОМе в 7 мл метанола. При 0°С прибавляют раствор 20 мг гидроксида лития в 3 мл воды. Перемешивают реакционную массу 30 мин при комнатной температуре, добавляют 10 мл 5%-ного раствора лимонной кислоты. Отфильтровывают выпавший осадок, промывают на фильтре 5 мл воды и 5 мл гексана, сушат на воздухе. Получают 390 мг белого твердого вещества.
Пример 2
Получение Вос-Cys(Acm)-Phe-D-Trp-Lys(Вос)-Thr-1-(1-адамантил)-этиламид
К раствору 955 мг (1 ммоль) Вос-Cys(Acm)-Phe-D-Trp-Lys(Вос)-Thr-ОН, 269 мг (1.5 ммоль) 1-(1-адамантил)этиламина, 170 мг (1.1 ммоль) моногидрата N-гидроксибензотриазола в 10 мл диметилформамида при 0°С прибавляют по каплям раствор 227 мг (1.1 ммоль) дициклогексилкарбодиимида в 5 мл диметилформамида. Реакционную массу перемешивают 12 ч при комнатной температуре. Фильтруют выпавшие кристаллы, промывают 5 мл этилацетата, фильтрат разбавляют водой (1 объем фильтрата - 2 объема воды). Экстрагируют 2 раза по 15 мл этилацетата, органический слой промывают 10 мл 5%-ной лимонной кислотой, 10 мл воды, 10 мл насыщенного раствора бикарбоната натрия, затем 2 раза по 10 мл насыщенного раствора хлористого натрия. Органическую фазу сушат над сульфатом натрия и отгоняют растворитель в вакууме (40°С, 15 мм рт. ст.), остаток растирают и сушат на воздухе до постоянного веса. Получают 831 мг (74.2%) белого твердого вещества
Пример 3
Получение Вос-Thz-Phe-D-Trp-Lys(Вос)-Thr-ОМе
В 30 мл диметилформамида последовательно растворяют 2.1 г (3 ммоль) H-Phe-D-Trp-Lys(Boc)-Thr-OMe, 0.76 г (3.1 ммоль) Boc-Thz-OH и 0.51 г (3.1 ммоль) моногидрата N-гидроксибензотриазола. Охлаждают до 0°С и при этой температуре прибавляют по каплям раствор 0.62 г (3.0 ммоль) дициклогексилкарбодиимида в 5 мл диметилформамида. Реакционную массу перемешивают при этой температуре 2 ч, затем 12 ч при комнатной температуре. Отфильтровывают выпавшие кристаллы, промывают 5 мл диметилформамида, к фильтрату добавляют 50 мл 1%-ной лимонной кислоты. Экстрагируют 2 раза по 15 мл этилацетата, органический слой промывают 10 мл воды, 10 мл 5%-ного бикарбоната натрия, 2 раза по 10 мл насыщенного раствора хлористого натрия. Органическую фазу сушат над сульфатом натрия и отгоняют растворитель в вакууме (40°С, 15 мм рт. ст.), остаток растирают и сушат на воздухе до постоянного веса. Получают 2.4 г белого твердого вещества.
Пример 4
Получение Boc-Thz-Phe-D-Trp-Lys(Boc)-Thr-OH
Растворяют 500 мг Вос-Cys(Acm)-Phe-D-Trp-Lys(Вос)-Thr-ОМе в 7 мл метанола. При 0°С прибавляют раствор 20 мг гидроксида лития в 3 мл воды. Перемешивают реакционную массу 30 мин при комнатной температуре, добавляют 10 мл 5%-ного раствора лимонной кислоты. Отфильтровывают выпавший осадок, промывают на фильтре 2 раза по 5 мл воды и 5 мл гексана, сушат на воздухе. Получают 420 мг белого твердого вещества.
Пример 5
Получение Boc-Thz-Phe-D-Trp-Lys(Boc)-Thr-1-(1 адамантил)-этиламид
К раствору 896 мг (1 ммоль) Boc-Thz-Phe-D-Trp-Lys(Boc)-Thr-OH, 269 мг (1.5 ммоль) 1-(1-адамантил)этиламина, 170 мг (1.1 ммоль) моногидрата N-гидроксибензотриазола в 10 мл диметилформамида при 0°С прибавляют по каплям раствор 227 мг (1.1 ммоль) дициклогексилкарбодиимида в 5 мл диметилформамида. Реакционную массу перемешивают 12 ч при комнатной температуре. Фильтруют выпавшие кристаллы, промывают 5 мл этилацетата, фильтрат разбавляют водой (1 объем фильтрата - 2 объема воды). Экстрагируют 2 раза по 15 мл этилацетата, органический слой промывают 10 мл 5%-ной лимонной кислотой, 10 мл воды, 10 мл насыщенного раствора бикарбоната натрия, затем 2 раза по 10 мл насыщенного раствора хлористого натрия. Органическую фазу сушат над сульфатом натрия и отгоняют растворитель в вакууме (40°С, 15 мм рт. ст.), остаток растирают и сушат на воздухе до постоянного веса. Получают 797 мг (75.4%) белого твердого вещества.
Пример 6
Получение Boc-Cys(Boc)-Phe-D-Trp-Lys(Boc)-Thr-OMe
В 150 мл диметилформамида при перемешивании последовательно растворяют 20.80 г (30 ммоль) H-Phe-D-Trp-Lys(Boc)-Thr-OMe, 4.59 г (30 ммоль) моногидрата N-гидроксибензотриазола, 10.59 г (33 ммоль) Boc-Cys(Boc)-OH. Охлаждают до 0°С и при этой температуре добавляют по каплям раствор 6.78 г (33 ммоль) дициклогексилкарбодиимида в 25 мл диметилформамида. Реакционную массу перемешивают при этой температуре 2 ч и еще 12 ч при комнатной температуре. Фильтруют выпавшие кристаллы, промывают 20 мл этилацетата, фильтрат разбавляют водой (1 объем фильтрата - 2 объема воды). Экстрагируют 2 раза по 100 мл этилацетата, органический слой промывают 25 мл 5%-ной лимонной кислотой, 25 мл воды, 25 мл насыщенного раствора бикарбоната натрия, затем 2 раза по 25 мл насыщенного раствора хлористого натрия. Органическую фазу сушат над сульфатом натрия и отгоняют растворитель в вакууме (40°С, 15 мм рт. ст.), остаток растирают и сушат на воздухе до постоянного веса. Получают 27.54 г (92.1%) белого мелкокристаллического вещества.
Пример 7
Получение Boc-Cys(Boc)-Phe-D-Trp-Lys(Boc)-Thr-OH
Растворяют 10.00 г Boc-Cys(Acm)-Phe-D-Trp-Lys(Boc)-Thr-OMe в 150 мл метанола. При 0°С прибавляют раствор 400 мг гидроксида лития в 50 мл воды. Перемешивают реакционную массу 30 мин при комнатной температуре, добавляют 200 мл 5%-ного раствора лимонной кислоты. Отфильтровывают выпавший осадок, промывают на фильтре 2 раза по 50 мл воды и 50 мл гексана, сушат на воздухе. Получают 8.94 г белого твердого вещества.
Пример 8
Получение Boc-Cys(Boc)-Phe-D-Trp-Lys(Boc)-Thr-1-(1 адамантил)-этиламид
К раствору 984 мг (1 ммоль) Boc-Cys(Boc)-Phe-D-Trp-Lys(Boc)-Thr-OH, 269 мг (1.5 ммоль) 1-(1-адамантил)этиламина, 170 мг (1.1 ммоль) моногидрата N-гидроксибензотриазола в 10 мл диметилформамида при 0°С прибавляют по каплям раствор 227 мг (1.1 ммоль) дициклогексилкарбодиимида в 5 мл диметилформамида. Реакционную массу перемешивают 12 ч при комнатной температуре. Фильтруют выпавшие кристаллы, промывают 5 мл этилацетата, фильтрат разбавляют водой (1 объем фильтрата - 2 объема воды). Экстрагируют 2 раза по 15 мл этилацетата, органический слой промывают 10 мл 5%-ной лимонной кислотой, 10 мл воды, 10 мл насыщенного раствора бикарбоната натрия, затем 2 раза по 10 мл насыщенного раствора хлористого натрия. Органическую фазу сушат над сульфатом натрия и отгоняют растворитель в вакууме (40°С, 15 мм рт. ст.), остаток растирают и сушат на воздухе до постоянного веса. Получают 906 мг (79.1%) белого твердого вещества
Пример 9
Получение Boc-Cys(Boc)-Phe-D-Trp-Lys(Boc)-Thr-1- адамантиламид
К раствору 984 мг (1 ммоль) Boc-Cys(Boc)-Phe-D-Trp-Lys(Boc)-Thr-OH, 281 мг (1.5 ммоль) 1-адамантиламина гидрохлорида, 170 мг (1.1 ммоль) моногидрата N-гидроксибензотриазола и 150 мг (1.5 ммоль) N-метилморфолина в 10 мл диметилформамида при 0°С прикапывают раствор 227 мг (1.1 ммоль) дициклогексилкарбодиимида в 5 мл диметилформамида. Реакционную массу перемешивают 12 ч при комнатной температуре. Фильтруют выпавшие кристаллы, промывают 5 мл этилацетата, фильтрат разбавляют водой (1 объем фильтрата - 2 объема воды). Экстрагируют 2 раза по 15 мл этилацетата, органический слой промывают 10 мл 5%-ной лимонной кислотой, 10 мл воды, 10 мл насыщенного раствора- бикарбоната натрия, затем 2 раза по 10 мл насыщенного раствора хлористого натрия. Органическую фазу сушат над сульфатом натрия и отгоняют растворитель в вакууме (40°С, 15 мм рт. ст.), остаток растирают и сушат на воздухе до постоянного веса. Получают 900 мг (80.5%) белого твердого вещества
Пример 10
Получение Вос-Cys(Acm)-Phe-D-Trp-Lys(Вос)-Thr-1- адамантиламид
К раствору 955 мг (1 ммоль) Вос-Cys(Acm)-Phe-D-Trp-Lys(Вос)-Thr-ОН, 281 мг (1.5 ммоль) 1-адамантиламина гидрохлорида, 170 мг (1.1 ммоль) моногидрата N-гидроксибензотриазола и 150 мг (1.5 ммоль) N-метилморфолина в 10 мл диметилформамида при 0°С прикапывают раствор 227 мг (1.1 ммоль) дициклогексилкарбодиимида в 5 мл диметилформамида. Реакционную массу перемешивают 12 ч при комнатной температуре. Фильтруют выпавшие кристаллы, промывают 5 мл этилацетата, фильтрат разбавляют водой (1 объем фильтрата - 2 объема воды). Экстрагируют 2 раза по 15 мл этилацетата, органический слой промывают 10 мл 5%-ной лимонной кислотой, 10 мл воды, 10 мл насыщенного раствора бикарбоната натрия, затем 2 раза по 10 мл насыщенного раствора хлористого натрия. Органическую фазу сушат над сульфатом натрия и отгоняют растворитель в вакууме (40°С, 15 мм рт. ст.), остаток растирают и сушат на воздухе до постоянного веса. Получают 856 мг (76.5%) белого твердого вещества
Пример 11
Получение Вос-Thz-Phe-D-Trp-Lys(Вос)-Thr-NH-1 - адамантиламид
К раствору 896 мг (1 ммоль) Вос-Thz-Phe-D-Trp-Lys(Вос)-Thr-ОН, 281 мг (1.5 ммоль) 1-адамантиламина гидрохлорида, 170 мг (1.1 ммоль) моногидрата N-гидроксибензотриазола и 150 мг (1.5 ммоль) N-метилморфолина в 10 мл диметилформамида при 0°С прикапывают раствор 227 мг (1.1 ммоль) дициклогексилкарбодиимида в 5 мл диметилформамида. Реакционную массу перемешивают 12 ч при комнатной температуре. Фильтруют выпавшие кристаллы, промывают 5 мл этилацетата, фильтрат разбавляют водой (1 объем фильтрата - 2 объема воды). Экстрагируют 2 раза по 15 мл этилацетата, органический слой промывают 10 мл 5%-ной лимонной кислотой, 10 мл воды, 10 мл насыщенного раствора бикарбоната натрия, затем 2 раза по 10 мл насыщенного раствора хлористого натрия. Органическую фазу сушат над сульфатом натрия и отгоняют растворитель в вакууме (40°С, 15 мм рт. ст.), остаток растирают и сушат на воздухе до постоянного веса. Получают 785 мг (76.1%) белого твердого вещества
Синтезированные пептиды были очищены и проанализированы.
Препаративная ВЭЖХ
Очистку проводили с помощью препаративной обращено-фазовой высокоэффективной жидкостной хроматографии (ОФ ВЭЖХ). Для очистки тетрапептидов использовалась хроматографическая система, состоящая из 2 насосов GILSON 306 производительностью до 25 мл в минуту, манометрического модуля GILSON 805 и спектрофотометрического детектора UVV-105 (производство фирмы JET chrom). Разделение производилось на колонке ReproSil-PurAQ С18 5 мкм, размером 250*10 мм с предколонкой ReproSil-PurAQ С18 10 мкм, размером 30*8 мм. Элюент: 60% водный ацетатно-аммонийный буфер (рН=5)/40% ацетонитрил.
Все соединения были очищены до содержания основного вещества выше 98%.
ВЭЖХ-МС:
Чистоту полученных соединений определяли при помощи аналитической высокоэффективной жидкостной хроматографии на хроматографической системе Agilent LC/MS 1200 (колонка - ReproSil-Pur Basic С18 5 мкм размером 250×4,6 мм с предколонкой SecurityGuard Cartridges Widepore C18 4×2 мм; подвижная фаза: градиент с 95% вода +5% ацетонитрил до 100% ацетонитрил с буферизацией 0,01% трифторуксусной кислотой за 20 минут). Детектирование на УФ-детекторе с длиной волны 220 нм.
Содержание основного вещества в образце определяли по относительной величине площади пика на хроматограмме.
Спектры ESI-MS регистрировались на MS детекторе Agilent Ion Trap 6310. Ионизация пробы с помощью электроспрея, регистрация в режиме положительных ионов, в некоторых случаях в режиме отрицательных ионов.
Настройки масс-детектора:
- давление на нибулайзере 40 psi;
- напряжение на нибулайзере 3500 вольт;
- поток шторного газа 7 л в минуту;
- температура газа носителя 360°С;
- детекция масс в диапазоне от 70 до 1500 атомных единиц массы.
Параметром, характеризующим анализируемое вещество, является молекулярный вес иона, определенный МС детектором.
Структуры и физико-химические характеристики полученных соединений приведены в таблице 1.
Синтезированные соединения были испытаны на цитотоксическую активность.
Цитотоксическую активность заявляемых соединений определяли с помощью МТТ-теста. Концентрацию полумаксимального ингибирования (IC50) для синтезированных веществ определяли на клетках рака молочной железы линии MCF-7, клетках аденокарциномы простаты линии РС-3, клетках колоректального рака линии НСТ-116 и ФЭЧ (фибробласты эмбриональные человека). Клетки MCF-7 и ФЭЧ культивировали в среде DMEM, клетки РС-3 и НСТ-116 - в среде RPMI1640 (ПанЭко, Россия) с добавлением 10% эмбриональной бычьей сыворотки (GE Healthcare LifeSciences) и гентамицина в концентрации 40 мг/мл.
Клетки MCF-7, РС-3 и НСТ-116 рассевали в 96-луночные планшеты по 5×103 клеток в лунку в 90 мкл культуральной среды.
Исследуемые вещества растворяли в ДМСО до получения концентрации 1×10-2 М, для последующего разведения веществ использовалась бессывороточная культуральная среда.
Через сутки в лунки с клетками добавляли растворы испытуемых веществ в объеме 10 мкл на лунку в различных концентрациях. Использовалась линейка из 10 концентраций, от 1×10-4М до 2×10-7М, каждая концентрация добавлялась в 3-4 повторах. В контрольные лунки добавляли 10 мкл бессывороточной среды. Клетки культивировали в СО2-инкубаторе в атмосфере 5% СО2, при 100% влажности и температуре 37°С в течение 72 часов. Затем в лунки добавляли реагент МТТ в концентрации 5 мг/мл в объеме 20 мкл на лунку. После 1,5-2 часовой инкубации в атмосфере 5% СО2, при 100% влажности и температуре 37°С планшеты центрифугировали при 1500 об/мин в течение 5 минут, удаляли супернатант и в каждую лунку добавили по 60 мкл ДМСО для растворения осадка кристаллов фармазана. Через 30 минут инкубации при комнатной температуре, после полного растворения кристаллов формазана, уровень оптической плотности определяли с помощью спектрофотометра Multiskan FC (Thermo Scientific), при длине волны 594 нм.
Далее в компьютерной программе строился график зависимости уровня оптической плотности (проценты от контроля) от концентрации исследуемого вещества и рассчитывалась концентрация IC50.
Результаты испытаний приведены в Таблице 2.
Как показали исследования, особым преимуществом новых соединений перед известными аналогами является их высокая цитотоксическая активность и устойчивость к ферментативному разложению, что дает возможность их орального введения в организм, дополнительно к парентеральному, осуществляемому подкожно, внутривенно, внутримышечно и внутрибрюшинно. Кроме повышения цитотоксичности добавление фрагмента адамантана в молекулу также значительно повышает липофильность и протеолитическую стабильность пептидов, тем самым улучшая их фармакокинетику.
К изобретению «Короткий пептид, обладающий цитотоксическим действием»
| название | год | авторы | номер документа |
|---|---|---|---|
| КОРОТКИЕ ПЕПТИДЫ С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2648357C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТА BOC-THZ-PHE-D-TRP-LYS(BOC)-THR-NHCHCHNH-DOTA, ЯВЛЯЮЩЕГОСЯ ПРЕКУРСОРОМ ДЛЯ ПРОТИВООПУХОЛЕВЫХ РАДИОФАРМПРЕПАРАТОВ | 2022 |
|
RU2795447C1 |
| ЗАЩИЩЕННЫЕ ПРОИЗВОДНЫЕ ОКТРЕОТИДА | 2001 |
|
RU2196144C1 |
| ТВЕРДОФАЗНЫЙ СИНТЕЗ ПЕПТИДОВ С ЗАЩИТНЫМИ ГРУППАМИ ВОС И FMOC | 2007 |
|
RU2439075C2 |
| Способ получения пептидов | 1976 |
|
SU639446A3 |
| ПЕПТИДНЫЕ ВЕКТОРЫ | 2004 |
|
RU2361876C2 |
| ХИМЕРНЫЕ АНАЛОГИ СОМАТОСТАТИНА-ДОФАМИНА | 2002 |
|
RU2277539C2 |
| ПРОИЗВОДНОЕ ПЕПТИДА, СПОСОБ ЛЕЧЕНИЯ РАКА У ПАЦИЕНТА | 1994 |
|
RU2133252C1 |
| ПЕПТИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2067000C1 |
| КОНЪЮГАТЫ ЦИТОТОКСИЧЕСКИХ СРЕДСТВ С ПЕПТИДАМИ | 2007 |
|
RU2457218C2 |
Изобретение относится к медицине и касается коротких пептидов, обладающих цитотоксическим действием, общей формулы R3-Phe-D-Trp-Lys(R1)-Thr-R2, где R1 представляет собой Н или трет-бутилоксикарбонил; R2 представляет собой 1-аминоадамантильную, 1-амино-(1-адамантил)этильную группу; R3 представляет собой R4-Cys(R5)- или 3-R4-тиазолидин-4-карбонил, где R4 - Н или трет-бутилоксикарбонил; R5 - Н или трет-бутилоксикарбонил или ацетомидометил. Изобретение обеспечивает высокую устойчивостью пептидов к ферментативному разложению; возможность как орального, так и парентерального введения в организм. 1 з.п. ф-лы, 2 табл., 11 пр.
1. Короткий пептид, обладающий цитотоксическим действием, общей формулы:
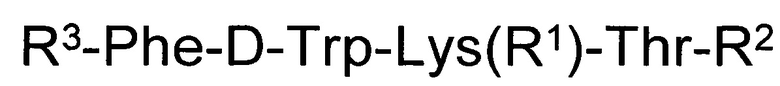 ,
,
где R1 представляет собой Н или трет-бутилоксикарбонил;
R2 представляет собой 1-аминоадамантильную, 1-амино-(1-адамантил)этильную группу;
R3 представляет собой R4-Cys(R5)- или 3-R4-тиазолидин-4-карбонил,
где R4 - Н или трет-бутилоксикарбонил;
R5 - Н или трет-бутилоксикарбонил или ацетомидометил.
2. Короткий пептид, обладающий цитотоксической активностью по п. 1, выбранный из группы:
Boc-Cys(Acm)-Phe-D-Trp-Lys(Boc)-Thr-1-(1 адамантил)-этиламид,
Boc-Thz-Phe-D-Trp-Lys(Boc)-Thr-1-(1 адамантил)-этиламид
Boc-Cys(Boc)-Phe-D-Trp-Lys(Boc)-Thr-1-адамантиламид,
Вос-Cys(Acm)-Phe-D-Trp-Lys(Вос)-Thr-1-адамантиламид,
Boc-Thz-Phe-D-Trp-Lys(Boc)-Thr-NH-1-адамантиламид,
где Boc обозначает трет-бутилкарбоксильную группу, Acm - ацетамидометильную группу,
Thz - остаток тиазолидин-4-карбоновой кислоты.
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2254139C1 |
| БАЛАЕВ А | |||
| Н | |||
| и др | |||
| Синтез и изучение цитотоксической активности аналогов гипоталамического гормона соматостатина | |||
| Российский биотерапевтический журнал | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| БАЛАЕВ А | |||
| Н | |||
| и др | |||
| Синтетические пептидные аналоги соматостатина: стратегии синтеза и перспективы поиска новых противоопухолевых препаратов | |||
| Химико-фармацевтический журнал | |||
| Т | |||
| Способ смешанной растительной и животной проклейки бумаги | 1922 |
|
SU49A1 |
| БАЛАЕВ А | |||
| Н | |||
| и др | |||
| Эффект синтетических пептидных агонистов соматостатина на рост перевиваемых опухолей мышей | |||
| Российский биотерапевтический журнал | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
2018-03-07—Публикация
2016-09-23—Подача