Изобретение относится к ветеринарной микробиологии и может быть использовано при индикации и количественном учете S-, R-форм бактерий Yersinia enterocolitica.
Бактерии Yersinia enterocolitica при инфицировании восприимчивых видов реализуют факторы вирулентности, детерминированные хромосомами и плазмидой вирулентности иерсиний - «plasmid asociated with Yersinia virulence» (pYV), характеризуются психрофильностью, метаболической пластичностью, ростом на обедненных средах, являясь убиквитарными, выделены из объектов внешней среды, обнаружены в воде, почве (Поздеев O.К., Федоров Р.В., 2007). Наличие перекрестных серологических реакций между бактериями Y. enterocolitica 09 и Brucella abortus обусловливает получение ложноположительных результатов при исследовании сыворотки крови животных из благополучных по бруцеллезу хозяйств. При бессимптомной персистенции иерсиний в организме бактерионосителей может происходить контаминация пищевого сырья, что обусловливает социальную значимость профилактических мероприятий в начале «пищевой цепи» (Санитарные правила. 3.1.094-96; Ветеринарные правила 13.3.1318-96). При воздействии физических и химических факторов наблюдается внутрипопуляционная изменчивость иерсиний, выражающаяся диссоциацией на S-R-формы, снижением процессов метаболизма и переходом популяции в «некультивируемое состояние», что обусловливает длительность и ретроспективность бактериологических исследований (Е.М. Ленченко и соавт., 2014). Для оптимизации индикации и идентификации иерсиний приоритетным направлением представляется разработка способа культивирования, позволяющего проводить учет количества S-, R-форм бактерий Y. enterocolitica.
Известна питательная среда для выделения бактерий Y. enterocolitica (Патент РФ №2251570, питательная среда для выделения возбудителей кишечного иерсиниоза и псевдотуберкулеза, МПК C12N 1/20, C12Q 1/10, C12Q 1/10, C12R 1:01, Бюл. №13, 10.05.2005), содержащая пептон, дрожжевой экстракт, маннит, натрия пируват, натрия хлорид, магния сульфат, натрия дезоксихолат, нейтральный красный, кристаллический фиолетовый, агар-агар, иргасан и дистиллированную воду при следующем содержании компонентов, г/л:
Известная питательная среда не позволяет выделить в быстрые сроки из патологического материала S-, R-формы иерсиний, необходимые для опытов по изучению особенностей вызываемого инфекционного процесса. Недостатком указанной среды также является сложность приготовления вследствие необходимости раздельного автоклавирования компонентов.
Задачей изобретения является повышение качества идентификации S-, R-форм иерсиний в исследуемом материале, кроме того, позволяющей упростить и ускорить способ идентификации S- и R-форм иерсиний.
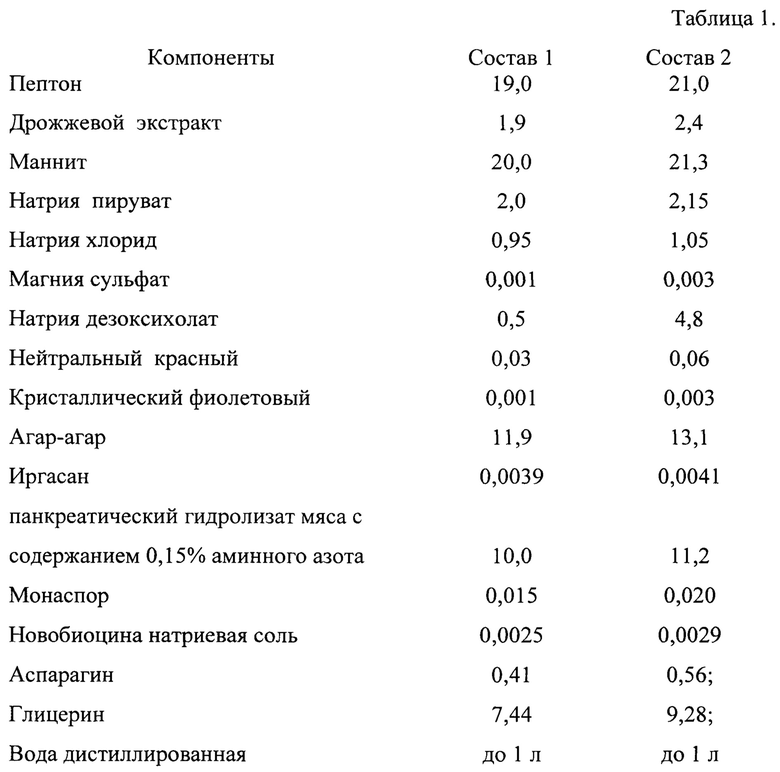
Поставленная задача решается тем, что питательная среда для идентификации Yersinia enterocolitica, содержащая пептон, дрожжевой экстракт, маннит, натрия пируват, натрия хлорид, магния сульфат, натрия дезоксихолат, нейтральный красный, кристаллический фиолетовый, агар-агар, иргасан и дистиллированную воду, согласно изобретению дополнительно содержит панкреатический гидролизат мяса с содержанием 0,15% аминного азота, «Монаспор», новобиоцина натриевую соль, аспарагин и глицерин, при следующем содержании компонентов, г/л:
Известен панкреатический гидролизат мяса с содержанием 0,15% аминного азота (ГОСТ 29311-92), который используется для питательных сред.
Панкреатический гидролизат мяса получают при продолжительной варке мясного фарша в автоклаве с последующей выпаркой мясного бульона в вакуум-аппарате до образования пастообразного продукта. Содержит воды 18,0%, органических веществ - 61,0%, минеральных - 21,0% (http://mspolyak.narod.ru/books/culture_medium_2002.pdf).
«Монаспор» (Цефсулодин натрия) относится к полусинтетическим антибиотикам из группы цефалоспоринов III поколения (http://www.medmoon.ru/rebenok/), предназначен для парентерального введения и обладает бактерицидным действием с выраженной активностью в отношении бактерий Pseudomonas aeruginosa (http://polyntrava.ru/lekarstva/arhiv/monaspor.html).
Новобиоцина натриевая соль (международное название - новобиоцин (Novobiocin)) - мононатриевая соль антибиотика новобиоцина, продуцируемого микроорганизмами Streptomyces spheroides или Streptomyces niveus. Новобиоцина натриевая соль применяется при пневмонии, септицемии, энтероколитах, инфекциях мочевых путей, флегмонах, раневых инфекциях, абсцессах и инфекционных заболеваниях, вызванных стафилококками, устойчивыми к другим антибиотикам. Химическое название: 7-[4-(карбамоил-окси)-тетрагидро-3-окси-5-метокси-6,6-диметилпиранил-2-окси]-4-окси-3-(3-метил-2-бутенил)-бензамидо-8-метилкумарат натрия - гигроскопический порошок белого цвета, горького вкуса, хорошо растворимый в воде (http://www.etolen.com/index.php?option=com_content&view=article&id=2936& Itemid=101).
Аспарагин - H2NOCCH2CHNH2COOH, амид аспарагиновой кислоты. Молекулярная масса 132,12. Кристаллизуется в виде ромбических призм, растворимых в горячей воде. Входит в состав многих белков. Содержится в свободном состоянии в жидкостях и тканях растений и животных. В больших количествах накапливается в проростках бобовых. Играет важную роль в жизни растений, являясь резервом азота и соединением, обезвреживающим аммиак, образующийся в процессе превращения белков (Большая советская энциклопедия. - М.: Советская энциклопедия, 1969-1978, с. 84).
Среда позволяет избирательно выделять и дифференцировать S-, R-формы Y. enterocolitica. Способ является оригинальным в решении, простым в осуществлении, информативным, дает статистически достоверные результаты, позволяет значительно сократить расход питательных сред, стерильной бактериологической посуды и времени проведения анализа. Анализ известной литературы свидетельствует о соответствии заявленного технического решения критерию «новизна». Сравнение заявленного способа с известными показывает, что эффективность питательной среды не зависит от уровня технического оснащения, что свидетельствует о соответствии заявленного технического решения критерию «изобретательский уровень».
Изобретение иллюстрируется на следующих примерах.
Пример 1. Получают составы 1-2, согласно прописи таблицы 1.
Способ приготовления: Растворение навесок проводят последовательно согласно прописи питательной среды в таблице, доводя конечный объем питательной среды дистиллированной водой до 1 л. Каждую последующую навеску растворяют только после полного растворения предыдущей; L-аспарагин растворяют отдельно в небольшом количестве дистиллированной воды при нагревании до кипения с добавлением по каплям концентрированной соляной кислоты до полного просветления раствора. Нагревают до кипения и кипятят в течение 5 мин на медленном огне. Фильтруют через ватно-марлевый фильтр, вновь кипятят 1-2 мин, охлаждают до 45-50°С и разливают в чашки Петри. Хранят среду в течение 7-10 суток при 4-7°С.
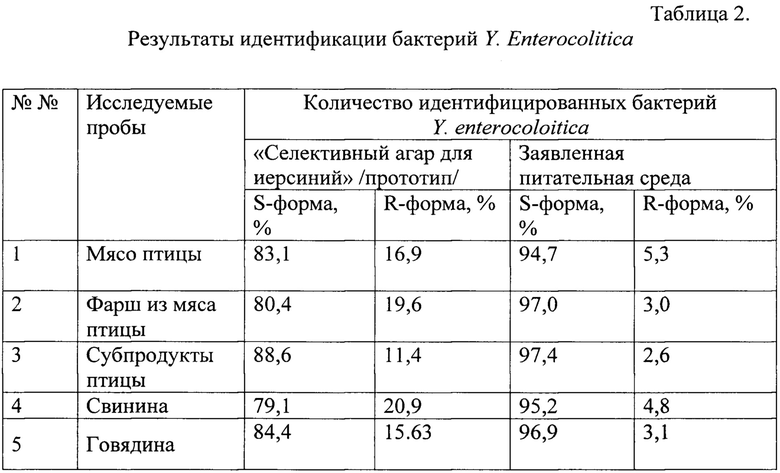
Применение разработанной среды (см. табл. 2) позволяет снизить диссоциацию S-, R- форм колоний бактерий, избирательно выделять и дифференцировать S-, R-формы Y. enterocolitica, изучать внутрипопуляционные процессы изменчивости бактерий.
Пример 2. Учет количества S-, R- форм бактерий Y. enterocolitica, выделенных при вторичной контаминации мяса птицы. Отбор проб производили в соответствии с ГОСТ Р 50396.0-2013 «Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка к микробиологическим исследованиям». При проведении анализа применяли два способа.
Способ 1. Исследуемые пробы помещали в известную среду обогащения (прототип) в соотношении 1:9 (масса/объем) и культивировали при 37°С 18-24 ч, из основного разведения готовили ряд серийных разведения в 0,85% NaCl. Из среды обогащения делали высев на дифференциально-диагностические питательные среды в чашки Петри, при культивировании бактерий при 22-28°С через 18-48 ч выявлено формирование S-, R- форм колоний Y. enterocolitica; S-формы колоний имели округлую форму, были прозрачными, с ровными краями; R-формы - плоские неправильной формы, складчатые, непрозрачные, с шероховатыми краями.
Способ 2 (использовали состав 1, полученный по примеру 1) включает подготовку препарата следующим образом: на предметное стекло наносили стерильной нагретой пипеткой 0,2-0,3 мл горячей питательной среды («Селективный агар для иерсиний» и разработанная питательная среду для определения S-, R-форм бактерий Y. enterocolitica), распределяли по всей поверхности стекла. Затем на поверхность тонкой агаровой пленки стерильной препаровальной иглой наносили суспензию клеток микроорганизмов. Полученные препараты помещали во влажную камеру-чашка Петри с влажной фильтровальной бумагой. Посев производили параллельно на два стекла, одно из которых культивировали при 37°С, другое - при 22-28°С в течение 48 ч. Для иерсиний характерным является полиморфизм колоний как по размеру, форме, так и по цвету, особенно при культивировании при 37°С. В этом случае наряду с колониями S-формы (колонии круглые умеренно выпуклые, прозрачные в виде росинок) можно наблюдать образование R-форм колоний, имеющих бугристую форму с изрезанными краями, коричнево-желтоватого цвета. При росте в жидкой питательной среде диссоциированные культуры бактерий Y. enterocolitica образуют хлопьевидный осадок, гладкие вызывают равномерное помутнение среды. При исследовании колоний при малом увеличении микроскопа дифференцировали округлой формы колонии: светлые с ровными краями - S-форма, фиолетовые с изрезанными краями - R-форма.
Пример 3. Учет количества S-, R- форм бактерий Y. enterocolitica, выделенных при вторичной контаминации фарша из мяса птицы. Пробы отбирали в соответствии с ГОСТ Р 50396.0-2013 «Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка к микробиологическим исследованиям». При проведении анализа применяли два способа.
Способ 1. Исследуемые пробы помещали в известную среду обогащения (прототип) в соотношении 1:9 (масса/объем) и культивировали при 37°С 18-24 ч, из основного разведения готовили ряд серийных разведения в 0,85% NaCl. Из среды обогащения делали высев на дифференциально-диагностические питательные среды в чашки Петри, при культивировании бактерий при 22-28°С через 18-48 ч выявлено формирование S-, R- форм колоний Y. enterocolitica; S-формы колоний имели округлую форму, были прозрачными, с ровными краями; R-формы -плоские неправильной формы, складчатые, непрозрачные, с шероховатыми краями.
Способ 2 (использовали состав 2, полученный по примеру 1) включает подготовку препарата следующим образом: на предметное стекло наносили стерильной нагретой пипеткой 0,2-0,3 мл горячей питательной среды («Селективный агар для иерсиний» и разработанная питательная среда для определения S-, R-форм бактерий Y. enterocolitica), распределяли по всей поверхности стекла. Затем на поверхность тонкой агаровой пленки стерильной препаровальной иглой наносили суспензию клеток микроорганизмов. Полученные препараты помещали во влажную камеру - чашка Петри с влажной фильтровальной бумагой. Посев производили параллельно на два стекла, одно из которых культивировали при 37°С, другое - при 22-28°С в течение 48 ч. Для иерсиний характерным является полиморфизм колоний как по размеру, форме, так и по цвету, особенно при культивировании при 37°С. В этом случае наряду с колониями S-формы (колоний круглые умеренно выпуклые, прозрачные в виде росинок) можно наблюдать образование R-форм колоний, имеющих бугристую форму с изрезанными краями, коричнево-желтоватого цвета. При росте в жидкой питательной среде диссоциированные культуры бактерий Y. enterocolitica образуют хлопьевидный осадок, гладкие вызывают равномерное помутнение среды. При исследовании колоний при малом увеличении микроскопа дифференцировали округлой формы колонии: светлые с ровными краями - S-форма, фиолетовые с изрезанными краями - R-форма.
Пример 4. Учет количества S-, R- форм бактерий Y. enterocolitica, выделенных при вторичной контаминации субпродуктов птицы. Пробы отбирали в соответствии с ГОСТ Р 50396.0-2013 «Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка к микробиологическим исследованиям». При проведении анализа применяли два способа.
Способ 1. Исследуемые пробы помещали в известную среду обогащения (прототип) в соотношении 1:9 (масса/объем) и культивировали при 37°С 18-24 ч, из основного разведения готовили ряд серийных разведения в 0,85% NaCl. Из среды обогащения делали высев на дифференциально-диагностические питательные среды в чашки Петри, при культивировании бактерий при 22-28°С через 18-48 ч выявлено формирование S-, R- форм колоний Y. enterocolitica; S-формы колоний имели округлую форму, были прозрачными, с ровными краями; R-формы -плоские неправильной формы, складчатые, непрозрачные, с шероховатыми краями.
Способ 2 (использовали состав 1, полученный по примеру 1) включает подготовку препарата следующим образом: на предметное стекло наносили стерильной нагретой пипеткой 0,2-0,3 мл горячей питательной среды («Селективный агар для иерсиний» и разработанная питательная среда для определения S-, R-форм бактерий Y. enterocolitica), распределяли по всей поверхности стекла. Затем на поверхность тонкой агаровой пленки стерильной препаровальной иглой наносили суспензию клеток микроорганизмов. Полученные препараты помещали во влажную камеру - чашка Петри с влажной фильтровальной бумагой. Посев производили параллельно на два стекла, одно из которых культивировали при 37°С, другое - при 22-28°С в течение 48 ч. Для иерсиний характерным является полиморфизм колоний как по размеру, форме, так и по цвету, особенно при культивировании при 37°С. В этом случае наряду с колониями S-формы (колоний круглые умеренно выпуклые, прозрачные в виде росинок) можно наблюдать образование R-форм колоний, имеющих бугристую форму с изрезанными краями, коричнево-желтоватого цвета. При росте в жидкой питательной среде диссоциированные культуры бактерий Y. enterocolitica образуют хлопьевидный осадок, гладкие вызывают равномерное помутнение среды. При исследовании колоний при малом увеличении микроскопа дифференцировали округлой формы колонии: светлые с ровными краями - S-форма, фиолетовые с изрезанными краями - R-форма.
Пример 5. Учет количества S-, R- форм бактерий Y. enterocolitica, выделенных при вторичной контаминации свинины. Пробы отбирали в соответствии с ГОСТ Р 51448-99 «Мясо и мясные продукты. Методы подготовки проб для микробиологических исследований». При проведении анализа применяли два способа.
Способ 1. Исследуемые пробы помещали в известную среду обогащения (прототип) в соотношении 1:9 (масса/объем) и культивировали при 37°С 18-24 ч, из основного разведения готовили ряд серийных разведения в 0,85% NaCl. Из среды обогащения делали высев на дифференциально-диагностические питательные среды в чашки Петри, при культивировании бактерий при 22-28°С через 18-48 ч выявлено формирование S-, R- форм колоний Y. enterocolitica; S-формы колоний имели округлую форму, были прозрачными, с ровными краями; R-формы - плоские неправильной формы, складчатые, непрозрачные, с шероховатыми краями.
Способ 2 (использовали состав 2, полученный по примеру 1) включает подготовку препарата следующим образом: на предметное стекло наносили стерильной нагретой пипеткой 0,2-0,3 мл горячей питательной среды («Селективный агар для иерсиний» и разработанная питательная среда для определения S-, R-форм бактерий Y. enterocolitica), распределяли по всей поверхности стекла. Затем на поверхность тонкой агаровой пленки стерильной препаровальной иглой наносили суспензию клеток микроорганизмов. Полученные препараты помещали во влажную камеру - чашка Петри с влажной фильтровальной бумагой. Посев производили параллельно на два стекла, одно из которых культивировали при 37°С, другое - при 22-28°С в течение 48 ч. Для иерсиний характерным является полиморфизм колоний как по размеру, форме, так и по цвету, особенно при культивировании при 37°С. В этом случае наряду с колониями S-формы (колоний круглые умеренно выпуклые, прозрачные в виде росинок) можно наблюдать образование R-форм колоний, имеющих бугристую форму с изрезанными краями, коричнево - желтоватого цвета. При росте в жидкой питательной среде диссоциированные культуры бактерий Y. enterocolitica образуют хлопьевидный осадок, гладкие вызывают равномерное помутнение среды. При исследовании колоний при малом увеличении микроскопа дифференцировали округлой формы колонии: светлые с ровными краями - S-форма, фиолетовые с изрезанными краями - R-форма.
Пример 6. Учет количества S-, R- форм бактерий Y. enterocolitica, выделенных при вторичной контаминации говядины. Пробы отбирали в соответствии с ГОСТ Р 51448-99 «Мясо и мясные продукты. Методы подготовки проб для микробиологических исследований».
Способ 1. Исследуемые пробы помещали в известную среду обогащения (прототип) в соотношении 1:9 (масса/объем) и культивировали при 37°С 18-24 ч, из основного разведения готовили ряд серийных разведения в 0,85% NaCl. Из среды обогащения делали высев на дифференциально-диагностические питательные среды в чашки Петри, при культивировании бактерий при 22-28°С через 18-48 ч выявлено формирование S-, R- форм колоний Y. enterocolitica; S-формы колоний имели округлую форму, были прозрачными, с ровными краями; R-формы - плоские неправильной формы, складчатые, непрозрачные, с шероховатыми краями.
Способ 2 (использовали состав 1, полученный по примеру 1) включает подготовку препарата «агаровая пленка» или «микрокультура» следующим образом: на предметное стекло наносили стерильной нагретой пипеткой 0,2-0,3 мл горячей питательной среды, распределяли по всей поверхности стекла. Затем на поверхность тонкой агаровой пленки стерильной препаровальной иглой наносили суспензию клеток микроорганизмов. Полученные препараты помещали во влажную камеру - чашка Петри с влажной фильтровальной бумагой. Посев производили параллельно на два стекла, одно из которых культивировали при 37°С, другое - при 22-28°С в течение 48 ч. Для иерсиний характерным является полиморфизм колоний как по размеру, форме, так и по цвету, особенно при культивировании при 37°С. В этом случае наряду с колониями S-формы (колоний круглые умеренно выпуклые, прозрачные в виде росинок) можно наблюдать образование R-форм колоний, имеющих бугристую форму с изрезанными краями, коричнево-желтоватого цвета. При росте в жидкой питательной среде диссоциированные культуры бактерий Y. enterocolitica образуют хлопьевидный осадок, гладкие вызывают равномерное помутнение среды. При исследовании колоний при малом увеличении микроскопа дифференцировали округлой формы колонии: светлые с ровными краями - S-форма, фиолетовые с изрезанными краями - R-форма.
Предлагаемый способ позволяет в три раза уменьшить количество используемой питательной среды и затрат рабочего времени, а также за счет применения разработанной среды снизить диссоциацию S-, R- форм колоний бактерий, избирательно выделять и дифференцировать S-, R-формы Y. enterocolitica (т.е. повысить чувствительность идентификации S- (на 10-20%), R-формы (на 15,3-22,3%) Y. enterocolitica), изучать внутрипопуляционные процессы с использованием световой микроскопии.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ВОЗБУДИТЕЛЕЙ КИШЕЧНОГО ИЕРСИНИОЗА И ПСЕВДОТУБЕРКУЛЕЗА | 2002 |
|
RU2251570C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИТАТЕЛЬНОЙ СРЕДЫ ДЛЯ КУЛЬТИВИРОВАНИЯ YERSINIA ENTEROCOLITICA | 2005 |
|
RU2300560C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ СЕЛЕКТИВНОГО НАКОПЛЕНИЯ YERSINIA ENTEROCOLITICA И YERSINIA PSEUDOTUBERCULOSIS | 2004 |
|
RU2264455C2 |
| СПОСОБ ИДЕНТИФИКАЦИИ YERSINIA ENTEROCOLITICA | 2011 |
|
RU2460802C1 |
| Способ дифференциации иерсиний серовара 09 от бруцелл | 1989 |
|
SU1703119A1 |
| ДИФФЕРЕНЦИАЛЬНО-ДИАГНОСТИЧЕСКАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ВОЗБУДИТЕЛЕЙ КИШЕЧНОГО ИЕРСИНИОЗА И ПСЕВДОТУБЕРКУЛЕЗА | 1995 |
|
RU2101342C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ ВОЗБУДИТЕЛЯ КИШЕЧНОГО ИЕРСИНЕОЗА БАКТЕРИОФАГОМ YERSINIA ENTEROCOLITICA 2021 (ФК-115) | 2021 |
|
RU2787399C1 |
| НАБОР ШТАММОВ БАКТЕРИЙ, ИСПОЛЬЗУЕМЫЙ ДЛЯ ОБУЧЕНИЯ ВОПРОСАМ МИКРОБИОЛОГИИ И МЕТОДАМ ЛАБОРАТОРНОЙ ДИАГНОСТИКИ ЧУМЫ | 2016 |
|
RU2642322C1 |
| Способ выделения бактерий p. Bacillus из ризопланы и ризосферы прикорневой зоны растений | 2019 |
|
RU2713120C1 |
| Способ идентификации у.pSeUDo-тULеRеULоSIS U у.ентеRосоLIтIса | 1981 |
|
SU988865A1 |
Изобретение относится к ветеринарной микробиологии. Питательная среда для выделения бактерий Yersinia enterocolitica содержит пептон, дрожжевой экстракт, маннит, натрия пируват, натрия хлорид, магния сульфат, натрия дезоксихолат, нейтральный красный, кристаллический фиолетовый, агар-агар, иргасан, дополнительно содержит гидролизат панкреатический мяса с содержанием аминного азота 0,15%, «Монаспор», новобиоцина натриевую соль, аспарагин, глицерин и дистиллированную воду при заданном соотношении компонентов. Изобретение позволяет упростить и повысить точность способа идентификации S- и R-форм Yersinia. 2 табл., 5 пр.
Питательная среда для идентификации Yersinia enterocolitica, содержащая пептон, дрожжевой экстракт, маннит, натрия пируват, натрия хлорид, магния сульфат, натрия дезоксихолат, нейтральный красный, кристаллический фиолетовый, агар-агар, иргасан и дистиллированную воду, отличающаяся тем, что дополнительно содержит панкреатический гидролизат мяса с содержанием 0,15% аминного азота, «Монаспор», новобиоцина натриевую соль, аспарагин и глицерин, при следующем содержании компонентов, г/л:
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ВОЗБУДИТЕЛЕЙ КИШЕЧНОГО ИЕРСИНИОЗА И ПСЕВДОТУБЕРКУЛЕЗА | 2002 |
|
RU2251570C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИТАТЕЛЬНОЙ СРЕДЫ ДЛЯ КУЛЬТИВИРОВАНИЯ YERSINIA ENTEROCOLITICA | 2005 |
|
RU2300560C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ СЕЛЕКТИВНОГО НАКОПЛЕНИЯ YERSINIA ENTEROCOLITICA И YERSINIA PSEUDOTUBERCULOSIS | 2004 |
|
RU2264455C2 |
| ДИФФЕРЕНЦИАЛЬНО-ДИАГНОСТИЧЕСКАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ВОЗБУДИТЕЛЕЙ КИШЕЧНОГО ИЕРСИНИОЗА И ПСЕВДОТУБЕРКУЛЕЗА | 1995 |
|
RU2101342C1 |
| Штриховальный прибор | 1928 |
|
SU9829A1 |
Авторы
Даты
2018-03-22—Публикация
2016-06-29—Подача