Предлагаемое изобретение относится к медицинской микробиологии и может быть использовано в лабораторной диагностике заболевания иерсиниозом, вызываемым Yersinia enterocolitica для ее идентификации и дифференциации.
В настоящее время во всем мире, в течение последних 30 лет, в центре внимания остается проблема заболеваемости иерсиниозами. Главными причинами этого можно считать: повсеместное распространение инфекции и растущую заболеваемость; выраженный полиморфизм клинических проявлений, в результате которого некоторые случаи остаются нераспознанными и скрываются под диагнозами других инфекционных заболеваний, что приводит к частому развитию осложнений в ходе инфекционного процесса; генотипическую и фенотипическую близость Yersinia enterocolitica и Yersinia pseudotuberculosis к Yersinia pestis. В связи с этим настоящее время увеличился процент обнаружения иерсиний в объектах внешней среды, где они могут достаточно долго сохраняться, создавая угрозу передачи инфекции [1, 2, 3].
В связи с вышеизложенным, большое значение придают лабораторной диагностике возбудителя, в том числе и фагодиагностике. Поиск новых методов в лабораторной диагностике Yersinia enterocolitica актуален и связан с необходимостью выделить специфические свойства бактерии достоверным, быстрым и простым способом [4, 5].
Известен способ детекции и дифференциации бактерий рода Yersinia методом мультиплексной полимеразной цепной реакции (6), заключающийся в том, что в способе используют мультиплексную ПЦР с последующим гель-электрофорезным анализом длин амплифицированных фрагментов, при этом дифференциальную диагностику не патогенных видов рода Yersinia от патогенных видов, проводят с помощью набора праймеров [V-F (SEQ ID NO: 1), Y-R(SEQ ID NO: 2), YP-R (SEQ ID NO: 5)], образуя только один специфический ПЦР-продукт, а у патогенных видов иерсиний (Y. enterocolitica и Y. pseudotuberculosis и Y. pestis) образуются два специфических ПЦР-продукта.
Недостатком данного метода является сложность в его проведении, так как для этого способа требуются смысловые радиоспецифические пары праймеров, кодирующие пептиды RLGFAGhK и антисмысловые видоспецифические праймеры, обладающие гомологией на 95-100% с нуклеотидной последовательностью.
Известен способ идентификации холерных вибрионов 01 двух биоваров (7), заключающийся в том, что определяют чувствительность холерных вибрионов к полимиксину В и диагностическим холерным фагам (классическому и эльтор). Холерные вибрионы биовара cholerae чувствительны к полимиксину и не растут на агаре с добавлением 50 мкг/мл полимиксина, а холерные вибрионы биовара eltor устойчивы к полимиксину В. Далее определяют биовар на основании лизабельности диагностическими фагами (классическим или эльтор).
Недостатком данного способа является невозможность его применения для диагностики возбудителя Y. enterocolitica, что связано с оптимальной температурой роста вибрионов при 37°С, а это не соответствует условиям роста бактерий Y. enterocolitica при 28°С; также отсутствие роста на щелочном агаре рН 7,6-7,8, а иерсиниям требуется агар Хоттингера рН 7,1-7,2.
За прототип был выбран способ идентификации Yersinia enterocolitica (8), заключающийся в том, что в данном способе определяют чувствительность Y. pseudotuberculosis и Y. enterocolitica к кишечноиерсиниозному фагу и антибиотику ампициллину. Штаммы Y.pseudotuberculosis не способны расти на среде с антибиотиком и устойчивы к бактериофагу.
Недостатком данного способа является то, что невозможно провести дифференциацию Y. enterocolitica от Y. pestis, а также для постановки анализа необходим дополнительный препарат - ампициллин.
Следовательно фагодиагностика, используемая в данном случае требует для Y. enterocolitica определенного специфического фага, способного дифференцировать Y. enterocolitica от Y.pseudotuberculosis и Y. pestis, а также наличие ампициллина.
Таким образом, для фагодиагностики иерсиниозов, требуется определенный специфический бактериофаг, чувствительный к данному виду иерсиний.
Технической задачей предполагаемого изобретения является разработка способа позволяющего достоверно и быстро осуществлять идентификацию и дифференциацию кишечного иерсиниоза путем использования диагностического бактериофага Y. enterocolitica 2021 (ФК-115).
Поставленная задача достигается тем, что в способе идентификации возбудителя кишечного иерсинеоза бактериофагом Y. enterocolitica 2021 (ФК-115), включающем инкубирование исследуемого штамма и использование лизабельности диагностического фага на агаровой среде, отличие заключается в том, что в качестве диагностического препарата используют фаг Yersinia enterocolitica 2021(ФК-115), который наносят в виде дорожки на двуслойный газон, нижний слой которого представляет собой 1,5% агаровую среду Хотингера в чашках Петри, а верхний слой получают из исследуемого штамма, который предварительно выращивают на агаре Хоттингера (рН7,2) в чашках Петри, затем культуру засевают в 4,5 мл бульона Хотингера и ставят в термостат на 24 часа при 28°С до конечной концентрации n⋅108 м.к./мл, после этого 0,5 мл бульонной культуры вносят в 4,5 мл 0,7% агара Хоттингера, предварительно растопленного и охлажденного до 45°С, далее полученную смесь выливают вторым слоем на поверхность нижнего слоя, а после застывания верхнего слоя наносят бактериофаг Y. enterocolitica 2021 (ФК-115), посевы инкубируют в термостате 24 часа при 28°С, далее визуально учитывают результат по наличию зоны лизиса на исследуемой культуре и делают вывод о присутствии возбудителя Y. enterocolitica.
Для проведения способа использован кишечноиерсиниозный бактериофаг 2021, который депонирован в коллекции-депозитарии фагов ФКУЗ Ростовский-на-Дону противочумный институт Роспотребнадзора под номером ФК-115.
В качестве контроля проверки литического действия фага применяют фагочувствительный индикаторный штамм Y. enterocolitica 2012 (депонированный в НИПЧИ «Микроб» г. Саратов под номером КМ-206). Штамм Y. enterocolitica 2012 выделен от человека (Бельгия), в 1966 году получен в музей ФКУЗ Ростовский-на-Дону противочумный институт Роспотребнадзора.
Фаг Y. enterocolitica 2021 на газоне индикаторной культуры КМ 206 образует точечные мутные и полупрозрачные негативные колонии диаметром около 1 мм. По данным электронно-микроскопического исследования бактериофаг имеет полигональную головку размером 59 нм и длинный сокращающийся хвост, размером 100 нм. и относится к V морфогруппе по Тихоненко А.С., к типу А семейства Myoviridae.
Физические свойства. Данный бактериофаг устойчив к действию хлороформа. Обработка хлороформом в течение суток не оказывала инактивирующего воздействия на фаговые частицы. Прогревание при 56° не изменяло титр свежевыделейного фага. При температуре 60° в течение 30 минут наблюдалось резкое уменьшению числа корпускул, при 65° и 70° фаг погибал.
Антигенные свойства. В опыте используют экспериментальные кроличьи антифаговые сыворотки к кишечноиерсиниозным (I-III серотипов) фагам при постановке прямых и перекрестных реакций нейтрализации бактериофага при его типизации. Рабочее разведение каждой антифаговой сыворотки составляет 1:100. В результате иммунизации кроликов фагом в их крови образуются специфические антитела. Полученная антифаговая сыворотка II серотипа нейтрализовала фаг Y. enterocolitica 2021. Проведенные исследования показали, что бактериофаг относится ко II серологическому типу и является ДНК-содержащим фагом.
Таким образом, было установлено, что данный фаг обладает антигенной специфичностью, позволяющей использовать этот биологический признак при идентификации бактерий Y. enterocolitica.
Специфичность и диапазон литической активности. Специфичность фага Y. enterocolitica 2021 в отношении хозяина подтверждена на большом наборе представителей близкородственных микроорганизмов семейства Enterobacteriaceae, включающих 7 видов (Y. pestis, Y. pseudotuberculosis, Y. enterocolitica,S. typhi, S. paratyphi, Sh. dysenteriae, E.coli), которые не лизировались испытуемым фагом. Изучение литического действия фага выявили его специфичность в отношении гомологичного вида, так как он не лизирует представителей других видов семейства Enterobacteriaceae. По литической активности к гомологичным культурам фаг обладает высоким показателем, так как он лизирует 84,0% из 25 штаммов наиболее распространенного 03 серовара, а также 4 из 5 штаммов O1 серовара и по 1 штамму O9, O10, O12, O17 - сероваров.
Таким образом, бактериофаг Y. enterocolitica 2021 имеет индивидуальные особенности, которые могут быть использованы при идентификации и дифференциации бактерий Y. enterocolitica.
Способ осуществляется следующим образом.
Для идентификации исследуемой культуры применяют фаг Y. enterocolitica 2021 (ФК-115). Штаммы Y. enterocolitica, Y.pseudotuberculosis и Y. pestis выращивают на агаре Хоттингера (рН 7,2) в чашке Петри в течение суток в термостате при температуре 28°С (в данном исследовании было изучено 15 штаммов Y. pestis, 22 штамма Y.pseudotuberculosis и 39 штаммов Y. enterocolitica). Все штаммы взяты из коллекции музея Ростовского противочумного института Роспотребнадзора. Способ проводят поэтапно.
Первый этап - в чашках Петри образуют нижний слой, который представляет 1,5% агара Хоттингера;
Второй этап- выращивают на агаре Хотингера (рН7,2) в чашках Петри исследуемую культуру в течение суток в термостате при температуре 28°С, затем одну петлю суточной агаровой культуры засевают в количестве 4,5 мл бульона Хоттингера и выращивают 24 часа при 28°С до конечной концентрации n⋅108 частиц/мл. Далее 0,5 мл бульонной культуры вносят в 4,5 мл 0,7% агара Хоттингера, предварительно растопленного и охлажденного до 45°С. Полученную Смесь выливают вторым слоем на поверхность 1,5% агара Хоттингера в чашки Петри (нижний слой).
Третий этап - после застывания верхнего слоя наносят бактериофаг Y. enterocolitica 2021 (ФК-115) в виде дорожки на газон засеянной культуры. Посев инкубируют в термостате 24 часа при температуре 28°С.
Четвертый этап- учитывают результат визуально по наблюдениям роста культуры и присутствия зоны лизиса культуры в местах нанесения бактериофага, подтверждая или отрицая присутствие штамма Y. Enterocolitica.
Пример 1. Лизис кишечноиерсиниозным бактериофагом штамма Y. enterocolitica 2012.
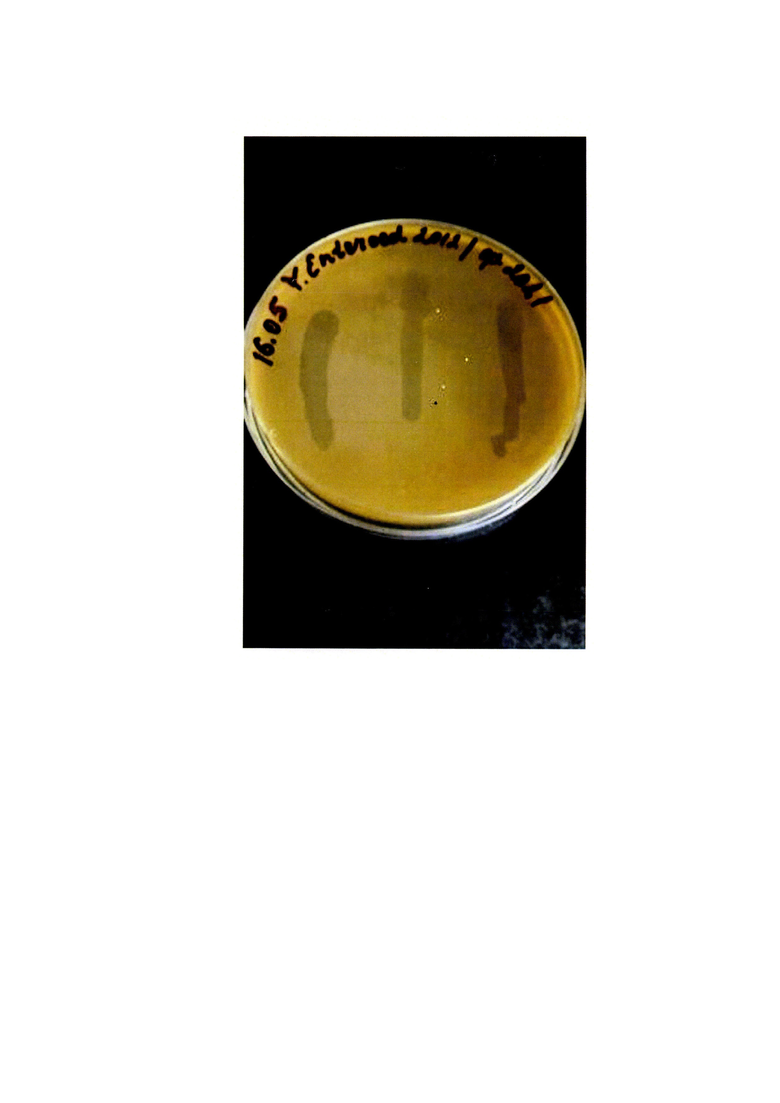
Штамм Y. enterocolitica 2012 (КМ-206) выращивают на агаре Хоттингера (рН 7,2) в чашке Петри в течение суток в термостате при температуре 28°С. Одну петлю суточной агаровой культуры засевают в 4,5 мл бульона Хоттингера и выращивают 24 часа при 28°С до конечной концентрации n⋅108 частиц/мл. Далее 0,5 мл бульонной культуры вносят в 4,5 мл 0,7% агара Хоттингера, предварительно растопленного и охлажденного до 45°С. Полученную смесь выливают вторым слоем на поверхность 1,5% агара Хоттингера в чашки Петри. После застывания верхнего слоя наносят бактериофаг Y. enterocolitica 2021 (ФК-115) в виде «дорожки» на газон засеянной культуры. Посев инкубируют в термостате 24 часа при температуре 28°С и учитывают результат (см. рисунок).
На рисунке видно, что наблюдается рост культуры и присутствие зоны лизиса культуры в месте нанесения бактериофага, что подтверждает присутствие штамма Y. enterocolitica Пример 2. Литическая активность кишечноиерсиниозного бактериофага в отношении штаммов Y. enterocolitica, Y. pestis, Y. pseudotuberculosis.
Исследуемые штаммы бактерий (Y. enterocolitica, Y. pestis, Y. pseudotuberculosis) наносят секторами на 1,5% агар Хоттингера в ч. Петри. Посевы культивируем в течение суток при температуре 28°С, далее на выросшую культуру наносим каплю исследуемого бактериофага, чашки ставим в термостат на 24 часа при 28°С. Оценку литической активности фага проводим по 4-х бальной системе. За положительный результат принимаем любую степень лизиса (см. таблицу 1).
«4+» - сливной полный лизис культуры с прозрачным дном литического пятна;
«3+» - прозрачное пятно с единичными колониями вторичного роста или множество изолированных литических пятен;
«2+» - прозрачное пятно лизиса со значительным вторичным ростом или единичные изолированные пятна лизиса;
«1+» - слабозаметное пятно лизиса культуры.
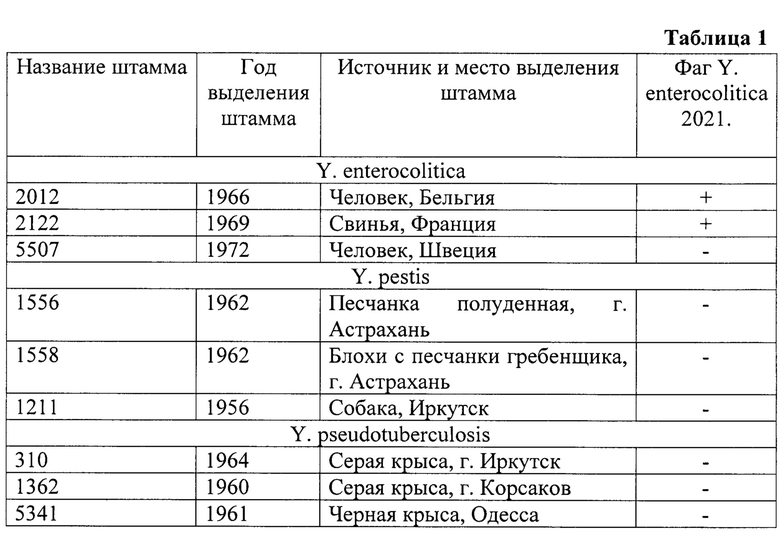
Таким образом, бактериофаг Y. enterocolitica 2021 лизирует большинство культур Y. enterocolitica и не наблюдается зон лизиса на всех исследуемых культурах Y. pestis, Y. pseudotuberculosis. Данный признак может использоваться для дифференциации бактерий внутри рода Yersinia (Y. enterocolitica от Y. Pestisn и Y. pseudotuberculosis).
Пример 3. Изучение специфичности бактериофага Y. enterocolitica 2021.
Специфичность фага изучаем путем постановки прямой пробы с фагом (титр 107-108 БОЕ/мл.). Для этого исследуемые штаммы (Y. pestis, Y. pseudotuberculosis, Y. enterocolitica,S. typhi, S. paratyphi, Sh. dysenteriae, E.coli)), выращенные на агаре Хоттингера (рН 7,2) в чашках Петри, засеваем в 4,5 мл бульона Хоттингера, затем ставим в термостат на 24 часа при 28°С и 37°С соответственно. Далее 0,5 мл каждой бульонной культуры вносим в 4,5 мл 0,7% агара Хоттингера, предварительно растопленного и охлажденного до 45°С. Полученную смесь выливаем вторым слоем на поверхность 1,5% агара Хоттингера в чашки Петри. После застывания верхнего слоя наносим бактериофаг Y. enterocolitica 2021 (ФК-115). Посевы инкубируем в термостате 24 часа и учитываем результат (см. таблицу 2).


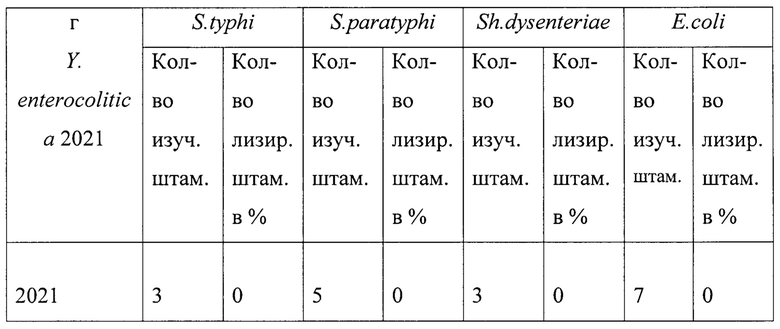
Вывод: изучение литического действия кишечноиерсиниозного фага выявляет его специфичность в отношении гомологичного вида, так как он не лизирует представителей других видов семейства Enterobacteriaceae.
Пример 4. Изучение диапазона литической активности бактериофага Y. enterocolitica 2021.
Для этого исследуемые штаммы Y. enterocolitica разных сероваров, выращенные на агаре Хоттингера (рН 7,2) в чашках Петри, засеваем в 4,5 мл бульона Хоттингера, затем ставим в термостат на 24 часа при 28°С. Далее 0,5 мл каждой бульонной культуры вносим в 4,5 мл 0,7% агара Хоттингера, предварительно растопленного и охлажденного до 45°С. Полученную смесь выливаем вторым слоем на поверхность 1,5% агара Хоттингера в чашки Петри. После застывания верхнего слоя наносим бактериофаг Y. enterocolitica 2021 (ФК-115). Посевы инкубируем в термостате 24 часа при 28°С и учитываем результат. Оценку степени литической активности фага проводим по четырех крестовой системе (см. таблицу 4).
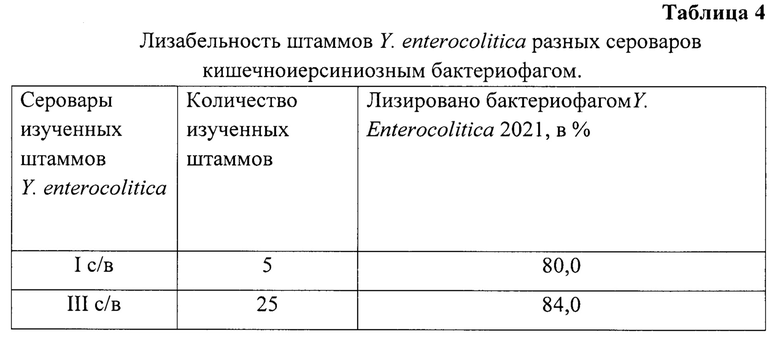
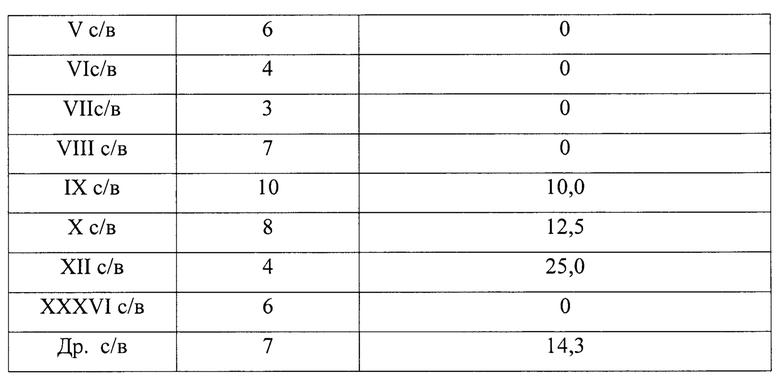
Следовательно делаем вывод что, фаг обладает высокой литической активностью, так как он лизирует 84,0% из 25 штаммов наиболее распространенного O3 серовара, а также 4 из 5 штаммов O1 серовара и по 1 штамму O9, O10, O12, O17 - сероваров и данный признак может быть использован при дифференциации внутри вида Y. enterocolitica
Использование предложенного способа позволяет за счет применения диагностического фага ФК-115 на двойном слое агара Хоттингера достоверно и быстро проводить идентификацию и дифференциации Y. enterocolitica. Сам способ прост в исполнении и не требует дополнительных реагентов и оборудования.
Кроме того предложенный способ позволяет эффективно применять его в лабораторной диагностике, так как чувствительность к фагу ФК-115 зависит от вида штаммов, на которых он культивируется, что позволяет его применять в качестве дополнительного теста идентификации и дифференциации возбудителей кишечного иерсинеоза.
Источники информации
1. Адаме М. Бактериофаги. - М: Медгиз, 1961. - 521 с.
2. Смирнов И.В. Возбудитель иерсиниоза и близкие к нему микроорганизмы // Клин, микробиол. антимикроб, химиотер. - 2004. - Том 6. - №1. - С. 10-21.
3. Ценева Г.Я. Псевдотуберкулез и иерсиниоз // Эпидемиология, клиника, диагностика, терапия. - Спб, ВМедА, 2005. - С. 52.
4. Leon-Velarde C.G., Jun J.W., Skurnik M. Yersinia Phages and Food Safety // Viruses. - 2019. - Nov. 28. - №11(12). - P. 1105. doi: 10.3390/v11121105.
5. Дарсавелидзе M.A., Капанадзе Ж.С., Чанишвили Т.Г. Биологические свойства бактериофагов, активных в отношении Yersinia enterocolitica II Журнал микробиол., эпидемиол. и иммунобиол. - 2004. - №6. - С. 10-13.
6. Патент RU №2385941, кл. C12Q 1/100 (опубликовано 10.04.2010 г).
7. МУК 4.2.2 218-07 «Лабораторная диагностика холеры». - Москва, 2007. - с 40-41.
8. Патент RU №2460802 С1, кл. C12Q 1/08, C12Q 1/70 (опубликовано 10.09.2012 г.).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИДЕНТИФИКАЦИИ YERSINIA ENTEROCOLITICA | 2011 |
|
RU2460802C1 |
| ШТАММ БАКТЕРИЙ Yersinia enterocolitica, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ ИНДИКАТОРНОЙ КУЛЬТУРЫ ДЛЯ ВЫЯВЛЕНИЯ УМЕРЕННЫХ БАКТЕРИОФАГОВ ЛИЗОГЕННЫХ ШТАММОВ О1, О3, О12 СЕРОВАРОВ | 2010 |
|
RU2425872C1 |
| Способ идентификации холерных вибрионов O1 серогруппы биоваров Classical и El Tor | 2019 |
|
RU2729575C1 |
| НАБОР ШТАММОВ БАКТЕРИЙ, ИСПОЛЬЗУЕМЫЙ ДЛЯ ОБУЧЕНИЯ ВОПРОСАМ МИКРОБИОЛОГИИ И МЕТОДАМ ЛАБОРАТОРНОЙ ДИАГНОСТИКИ ЧУМЫ | 2016 |
|
RU2642322C1 |
| Штамм РнаGUм реSтIS для внутривидовой дифференциации возбудителя чумы | 1987 |
|
SU1578194A1 |
| Способ идентификации Vibrio cholerae 01 серогруппы биовара El Tor | 2022 |
|
RU2797369C1 |
| СПОСОБ ОБНАРУЖЕНИЯ МИКРООРГАНИЗМА ВИДА VIBRIO PARAHAEMOLYTICUS | 2013 |
|
RU2531236C1 |
| СПОСОБ ДИФФЕРЕНЦИАЦИИ ВОЗБУДИТЕЛЕЙ ЧУМЫ И ПСЕВДОТУБЕРКУЛЕЗА ПО N-АЦЕТИЛ-БЕТА-D-ГЛЮКОЗАМИНИДАЗНОЙ АКТИВНОСТИ | 2014 |
|
RU2566559C1 |
| ШТАММ БАКТЕРИОФАГА Escherichia coli V32 ДЛЯ ИДЕНТИФИКАЦИИ БАКТЕРИЙ Escherichia coli СЕРОГРУППЫ О157 | 2010 |
|
RU2425877C1 |
| Штамм @ @ @ -1,используемый для внутривидовой дифференциации иерсиний чумы | 1983 |
|
SU1106834A1 |
Изобретение относится к области биотехнологии. Сущность предлагаемого изобретения заключается в том, что в качестве диагностического препарата используют фаг Yersinia enterocolitica 2021 (ФК-115), который наносят в виде дорожки на двуслойный газон, нижний слой которого представляет собой 1,5% агаровую среду Хоттингера в чашках Петри, а верхний слой получают из исследуемого штамма, который предварительно выращивают на агаре Хоттингера (рН 7,2) в чашках Петри, затем культуру засевают в 4,5 мл бульона Хоттингера и ставят в термостат на 24 часа при 28°С до конечной концентрации n⋅108 м.к./мл, после этого 0,5 мл бульонной культуры вносят в 4,5 мл 0,7% агара Хоттингера, предварительно растопленного и охлажденного до 45°С, далее полученную смесь выливают вторым слоем на поверхность нижнего слоя, а после застывания верхнего слоя наносят бактериофаг Y. enterocolitica 2021 (ФК-115), посевы инкубируют в термостате 24 часа при 28°С, далее визуально учитывают результат по наличию зоны лизиса на исследуемой культуре и делают вывод о присутствии возбудителя Y. enterocolitica. Изобретение может быть использовано в лабораторной диагностике заболевания иерсиниозом, вызываемым Yersinia enterocolitica для ее идентификации и дифференциации. 1 ил., 4 табл., 1 пр.
Способ идентификации возбудителя кишечного иерсинеоза бактериофагом Y. enterocolitica 2021 (ФК-115), включающий инкубирование исследуемого штамма и использование лизабельности диагностического фага на агаровой среде, отличающийся тем, что в качестве диагностического препарата используют фаг Yersinia enterocolitica 2021 (ФК-115), который наносят в виде дорожки на двуслойный газон, нижний слой которого представляет собой 1,5% агаровую среду Хоттингера в чашках Петри, а верхний слой получают из исследуемого штамма, который предварительно выращивают на агаре Хоттингера (рН7,2) в чашках Петри, затем культуру засевают в 4,5 мл бульона Хоттингера и ставят в термостат на 24 часа при 28°С до конечной концентрации n⋅108 м.к./мл, после этого 0,5 мл бульонной культуры вносят в 4,5 мл 0,7% агара Хоттингера, предварительно растопленного и охлажденного до 45°С, далее полученную смесь выливают вторым слоем на поверхность нижнего слоя, а после застывания верхнего слоя наносят бактериофаг Y. enterocolitica 2021 (ФК-115), посевы инкубируют в термостате 24 часа при 28°С, далее визуально учитывают результат по наличию зоны лизиса на исследуемой культуре и делают вывод о присутствии возбудителя Y. enterocolitica.
| СПОСОБ ИДЕНТИФИКАЦИИ YERSINIA ENTEROCOLITICA | 2011 |
|
RU2460802C1 |
| СПОСОБ ДЕТЕКЦИИ БАКТЕРИЙ РОДА Yersinia И ДИФФЕРЕНЦИАЦИИ ПАТОГЕННЫХ ДЛЯ ЧЕЛОВЕКА ВИДОВ ИЕРСИНИЙ МЕТОДОМ МУЛЬТИПЛЕКСНОЙ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2008 |
|
RU2385941C1 |
| LEON-VELARDE C.G., Yersinia Phages and Food Safety, Viruses., 2019., Nov | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| СПОСОБ ПОСЛЕДОВАТЕЛЬНОГО СОЕДИНЕНИЯ ДВУХ ИЛИ НЕСКОЛЬКИХ ЭЛЕКТРОДВИГАТЕЛЕЙ ПОСТОЯННОГО ТОКА, СНАБЖЕННЫХ КОНТАКТНЫМИ КОЛЬЦАМИ, ДЛЯ ПОЛУЧЕНИЯ СИНХРОННОГО ИХ ВРАЩЕНИЯ | 1919 |
|
SU1105A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
2023-01-09—Публикация
2021-12-16—Подача