Настоящее изобретение относится к новому способу синтеза соединений, которые могут быть использованы в лечении инфекции, вызываемой вирусом папилломы, описанному, в частности, в заявке WO 2007/135106.
Соединения, описанные в заявке WO 2007/135106, имеют следующую структуру:

в которой:
• А представляет собой необязательно замещенную арильную, циклоалкильную, циклоалкенильную или гетероциклическую группу,
• В представляет собой необязательно замещенные арил или гетероцикл,
• R1 и R2 независимо друг от друга представляют собой атом водорода или различные заместители,
• R3 представляет собой кислотную функциональную группу, или радикал пролекарства, или биоизостер этой функциональной группы,
• G1 представляет собой связь или углеводородную цепь и
• G2 представляет собой группу 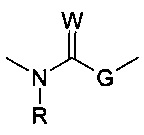 , в которой R является атомом водорода или различными заместителями, W представляет собой O, S или NH и G представляет собой связь или углеводородную цепь.
, в которой R является атомом водорода или различными заместителями, W представляет собой O, S или NH и G представляет собой связь или углеводородную цепь.
В способе синтеза этих соединений, описанном в заявке WO 2007/135106, в качестве промежуточного соединения используют гидразин со следующей структурой:

который получают из амина со следующей структурой:
Получение гидразина из соответствующего амина проводят путем нитрозирования амина в присутствии NaNO2 с получением соответствующего N-нитрозосоединения, которое затем восстанавливают с получением гидразина. Однако такой путь синтеза непригоден с промышленной точки зрения, поскольку нитрозосоединения опасны для применения. Кроме того, довольно строгие стандарты, касающиеся приемлемых остаточных концентраций нитрозосоединений в фармацевтических продуктах, ведут к рассмотрению другого пути синтеза.
Поэтому изобретатели обнаружили, что целевой гидразин может быть получен из соответствующего амина с использованием в качестве промежуточного соединения мочевины, а не N-нитрозосоединения.
Таким образом, предметом настоящего изобретения является способ получения гидразина с общей формулой (I):

и его фармацевтически приемлемых солей,
где
• G1 представляет собой связь, либо линейную или разветвленную, насыщенную или ненасыщенную углеводородную цепь, содержащую от 1 до 4 атомов углерода, необязательно замещенную одной или двумя предпочтительно одинаковыми алкильными группами,
• А представляет собой арильную группу, такую как фенил, необязательно замещенный:
- в мета- или пара-положении:
• атомом галогена или цианогруппой, алкоксигруппой, галогеналкоксигруппой, ациламиноалкильной группой или -XR группой, где X представляет собой -O-, -S-, -SO-, -SO2- или -CO-, a R представляет собой арилалкил, циклоалкил или арил, каждый из которых необязательно замещен одним или двумя одинаковыми или различными заместителями, такими как атом галогена, алкоксигруппа или ацильная группа, или
• циклоалкильной, арильной или арилалкильной группой, каждая из которых необязательно замещена одним или двумя одинаковыми или различными заместителями, такими как ацильная группа или алкоксигруппа,
- и/или в орто- или метаположении алкильной группой, и
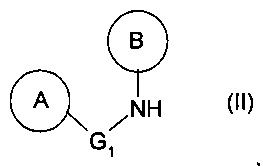
• В представляет собой арильную группу, предпочтительно фенил, замещенный в орто-положении гетероциклом, предпочтительно N-циклоалкилом, таким как пиперидин-1-ильная группа, и необязательно замещенный в орто'-положении алкильной группой, например метилом, из амина с формулой (II):

в котором G1, А и B являются такими, как определено выше,
отличающийся тем, что упомянутый способ использует мочевину с формулой (III) в качестве промежуточного соединения синтеза:
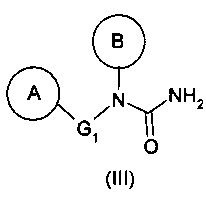
в котором G1, А и B являются такими, как определено выше.
В настоящем изобретении термин «фармацевтически приемлемый» означает, что объект может быть использован в производстве фармацевтической композиции и, как правило, безопасен, нетоксичен и не является ни биологически, ни иным образом нежелательным, приемлем для использования в ветеринарии, а также для фармацевтического применения у человека.
Термин «фармацевтически приемлемые» какого-либо соединения предназначен в настоящем изобретении для обозначения солей, которые являются, как определено здесь, фармацевтически приемлемыми и обладают заданной фармакологической активностью исходного соединения.
Такие соли включают:
(1) гидраты и сольваты,
(2) кислотно-аддитивные соли, образованные неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и им подобные; или образованные органическими кислотами, такими как уксусная кислота, бензолсульфоновая кислота, бензойная кислота, камфорсульфоновая кислота, лимонная кислота, этансульфоновая кислота, фумаровая кислота, глюкогептоновая кислота, глюконовая кислота, глутаминовая кислота, гликолевая кислота, оксинафтойная кислота, 2-гидроксиэтансульфокислота, молочная кислота, малеиновая кислота, яблочная кислота, миндальная кислота, метансульфоновая кислота, муконовая кислота, 2-нафталинсульфоновая кислота, пропионовая кислота, салициловая кислота, янтарная кислота, дибензоил-L-винная кислота, винная кислота, п-толуолсульфоновая кислота, триметилуксусная кислота, трифторуксусная кислота и им подобные; и
(3) соли, образующиеся в том случае, когда кислотный протон, присутствующий в исходном соединении, либо заменяется ионом металла, например ионом щелочного металла (например, Na+, К+ или Li+), ионом щелочноземельного металла (таким как Са2+ или Mg2+), или ионом алюминия; либо координируется с органическим или неорганическим основанием. Приемлемые органические основания включают диэтаноламин, этаноламин, N-метилглюкамин, триэтаноламин, трометамин и им подобные. Приемлемые неорганические основания включают гидроксид алюминия, гидроксид кальция, гидроксид калия, карбонат натрия и гидроксид натрия.
Термин «ненасыщенный» означает, в контексте настоящего изобретения, что группа содержит одну или более ненасыщенных связей.
Под «ненасыщенностью» подразумевается, в контексте настоящего изобретения, двойная или тройная связь.
Под «галогеном», в контексте настоящего изобретения, понимают фтор, бром, хлор или иод. Предпочтительно, это фтор, бром или хлор.
Термин «алкильная группа» означает, в контексте настоящего изобретения, линейную или разветвленную насыщенную углеводородную цепь, содержащую от 1 до 6 атомов углерода, в частности метильную, этильную, н-пропильную, изопропильную, н-бутильную, изобутильную, втор-бутильную, трет-бутильную, н-пентильную или н-гексильную группу. Предпочтительно она является метильной группой.
Термин «циклоалкильная группа» означает, в контексте настоящего изобретения, насыщенную моноциклическую или полициклическую систему, предпочтительно насыщенную моно-, би- или трициклическую систему, содержащую от 3 до 12 атомов углерода, причем пары колец могут быть конденсированными или соединенными при помощи мостика, например циклопропильную, циклопентильную, циклогексильную, циклогептильную, циклооктильную, адамантильную, декалинильную или норборнильную группу.
Термин «N-циклоалкильная группа» означает, в контексте настоящего изобретения, циклоалкильную группу, как определено выше, в которой атом углерода замещен атомом азота, а связь с молекулой образуется посредством этого атома азота. Предпочтительно она является пиперидин-1-ильной или пирролидин-1-ильной группой.
Под термином «ацильная группа», в контексте настоящего изобретения, понимают группу с формулой -C(O)-Z, где Z означает алкильную группу, как определено выше, или фенил. Предпочтительно она представляет собой ацетильную, этилкарбонильную или бензоильную группу.
Термин «алкоксигруппа» означает, в контексте настоящего изобретения, алкильную группу, как определено выше, связанную с молекулой посредством атома кислорода. Она может быть, в частности, метокси-, этокси-, н-пропокси-, изопропокси-, н-бутокси-, изо-бутокси-, втор-бутокси- или трет-бутоксигруппой.
Термин «галогеналкоксигруппа» означает, в контексте настоящего изобретения, алкоксигруппу, как определено выше, замещенную одним или более атомом (атомами) галогена, как определено выше. Предпочтительно она представляет собой фторалкоксигруппу, то есть алкоксигруппу, замещенную одним или более атомом (атомами) фтора, например группу -OCF3 или -OCH2CF3.
Термин «арильная группа» означает, в контексте настоящего изобретения, ароматическую группу, предпочтительно содержащую от 5 до 10 атомов углерода и одно или более соединенных между собой колец, например, такую группу как фенильная или нафтильная. Предпочтительно она представляет собой фенил.
Под «гетероциклом», в контексте настоящего изобретения, понимают насыщенную, ненасыщенную или ароматическую моноциклическую или полициклическую систему, причем, предпочтительно, насыщенную, ненасыщенную или ароматическую моно- или бициклическую систему, включающую от 3 до 12 членов, в которой пары колец могут быть сопряженными, спиро-конденсированными или соединенными при помощи мостика, и содержащую от 1 до 4 одинаковых или различных гетероатомов, выбранных из O, S и N, и необязательно содержащую одну или две оксо- или тиоксогрупп, с учетом того, что в случае полициклической системы одно из колец может быть ароматическим, тогда как другое (другие) может быть ароматическим, насыщенным или ненасыщенным. Предпочтительно, она представляет собой пиперидильную, пиперазильную, фурильную, тиенильную, пирролильную, пиразолильную, имидазолильную, пиридильную, пиримидильную, пиразинильную, пиридазинильную, бензофурильную, бензотиенильную, индолильную, хинолильную, изохинолинильную, бензодиоксолильную, бензодиоксинильную, бензо[1,2,5]тиадиазолильную, бензо[1,2,5]оксадиазолильную, [1,2,3]триазолильную и [1,2,4]триазолильную группы.
Термин «арилалкильная группа» означает, в контексте настоящего изобретения, арильную группу, как определено выше, связанную с молекулой при помощи алкильной группы, как определено выше. Предпочтительно, она представляет собой бензильную группу.
Под «ациламиноалкилом» подразумевают, в контексте настоящего изобретения, группу с формулой -Alk-NHCO-Alk', где Alk и Alk' независимо друг от друга представляют собой алкильную группу, как определено выше.
Гидразин с формулой (I), как определено выше, может, таким образом, быть получен из мочевины с формулой (III), как определено выше, путем перегруппировки Шестакова.
Эта реакция описана в литературе для различных замещенных соединений мочевины (Viret J. et al. Tetrahedron 1987, 43, 891-894; Murakami Y. et al. Chem. Pharm. Bull. 1983, 31, 423-428; Murakami Y. and Yokotama Y. Heterocycles 1979, 12, 1571-1574).
Такую перегруппировку Шестакова предпочтительно проводить в присутствии агента, индуцирующего перегруппировку, выбранного из NaOCl и KOCl, и предпочтительно являющегося NaOCl.
Предпочтительно, чтобы агент, индуцирующий перегруппировку, вводили ступенчато. Таким образом, индуцирующий агент может быть введен несколькими порциями, разнесенными во времени, или по каплям, или непрерывно и медленно так, чтобы это добавление в достаточной мере распределить по времени. Специалист в данной области техники сможет сам адаптировать параметр добавления (например, скорость добавления при непрерывной подаче) индуцирующего агента, такой, чтобы добавление являлось оптимальным.
По меньшей мере 1 молярный эквивалент предпочтительно между 1 и 1,5 молярными эквивалентами и предпочтительно примерно 1 молярный эквивалент агента, индуцирующего перегруппировку, используют в этой реакции для получения 1 молярного эквивалента мочевины с формулой (III).
Изобретатели неожиданно заметили, что лучшие выходы были получены, когда агент, индуцирующий перегруппировку, добавляли к реакционной среде постепенно, по сравнению с однократным добавлением.
Очевидно, что количество добавленных порций и продолжительность добавления, будет зависеть от масштаба, в котором проводят реакцию; такие адаптации являются обычной практикой специалиста в данной области техники.
Перегруппировку Шестакова можно проводить в смеси диоксан/вода или в спирте в качестве растворителя и предпочтительно в трет-бутаноле.
Термин «спирт», в контексте настоящего изобретения означает соединение с формулой Alk-OH, где Alk представляет собой алкильную группу, как определено выше. Предпочтительно он представляет собой метанол, этанол или трет-бутанол.
Такая перегруппировка осуществляется преимущественно в щелочных условиях, в частности в присутствии гидроксида натрия или гидроксида калия и предпочтительно в присутствии гидроксида калия.
Кроме того, мочевина с формулой (III), как определено выше, может быть получена из амина с формулой (II), как определено выше, в соответствии со следующими этапами:
(1) реакция амина с формулой (II) и трихлорацетилизоцианата (Cl3CC(O)-N=C=O) для того, чтобы получить соединение с формулой (IV):

в которой G1, А и B являются такими, как определено выше, и
(2) обработка в щелочной среде соединения с формулой (IV), полученного на предыдущем этапе, для того, чтобы получить мочевину с формулой (III).
Этап (1) может быть проведен в растворителе, таком как ацетонитрил, тетрагидрофуран, дихлорметан или диоксан и предпочтительно в ацетонитриле.
Этап (1) может быть проведен при комнатной температуре, то есть при температуре, изменяющейся от 20 до 40°C и предпочтительно при температуре примерно 25°C.
Гидроксид натрия или калия, и, предпочтительно, КОН, может быть использован в качестве основания на этапе (2).
Растворитель, используемый на этапе (2) должен представлять собой спирт, как определено выше, и предпочтительно является метанолом; этап (2) проводиться, в частности, в противотоке этого растворителя.
Таким образом, в соответствии с конкретной формой осуществления настоящего изобретения, касающейся способа, гидразин с предыдущей формулой (I) может быть получен согласно следующим последовательным этапам:
(1) реакция амина с формулой (II), как определено выше, и Cl3CC(O)-N=C=O для того, чтобы получить соединение с формулой (IV), как определено выше,
(2) обработка в щелочной среде соединения с формулой (IV), полученного на предыдущем этапе, для того, чтобы получить мочевину с формулой. (III), как определено выше,
(3) реакция Шестакова, начинающаяся от мочевины с формулой (III), полученной на предыдущем этапе, для того, чтобы получить гидразин с формулой (I), как определено выше, и
(4) выделение из реакционной среды гидразина с формулой (I), полученного на предыдущем этапе.
Выделение конечного продукта может быть осуществлено методами, хорошо известными специалистам в данной области техники, такими как, например, экстракция, выпаривание растворителя или осаждение и фильтрование.
Полученный таким образом гидразин может быть дополнительно очищен, если необходимо, с помощью способов, хорошо известных специалистам в данной области техники, например, путем перекристаллизации, если соединение является кристаллическим, или путем перегонки.
Предпочтительно, чтобы G1 представлял собой связь или линейную и насыщенную углеводородную цепь, содержащую от 1 до 4 атомов углерода и предпочтительно, чтобы он представлял собой связь.
Предпочтительно, чтобы радикал А, определенный выше, представлял собой арил, предпочтительно фенил, замещенный в мета- или пара-положении, предпочтительно в пара-положении, алкоксигруппой, такой как метоксигруппа, либо арильной или арилалкильной группой, такой как фенил или бензил, необязательно замещенный одним или двумя одинаковыми или различными заместителями, такими как ацил или алкоксигруппа.
Предпочтительно, чтобы В представлял собой арильную группу, предпочтительно фенил, замещенный в орто-положении гетероциклом, предпочтительно N-циклоалкилом, таким как пиперидин-1-ильная группа, и необязательно замещенный в орто'-положении алкильной группой, например метилом.
В частности, гидразин с формулой (I) представляет собой N-(4-бензил-фенил)-N-(2-метил-6-пиперидин-1-ил-фенил) гидразин (гидразин (Ia)).
Следовательно, предшествующий гидразин (Ia) получают из 1-(4-бензил-фенил)-1-(2-метил-6-пиперидин-1-ил-фенил) мочевины (соединение (IIIа)), причем последнюю получают из (4-бензил-фенил)-(2-метил-6-пиперидин-1-ил-фенил)амина (соединение (IIа)).
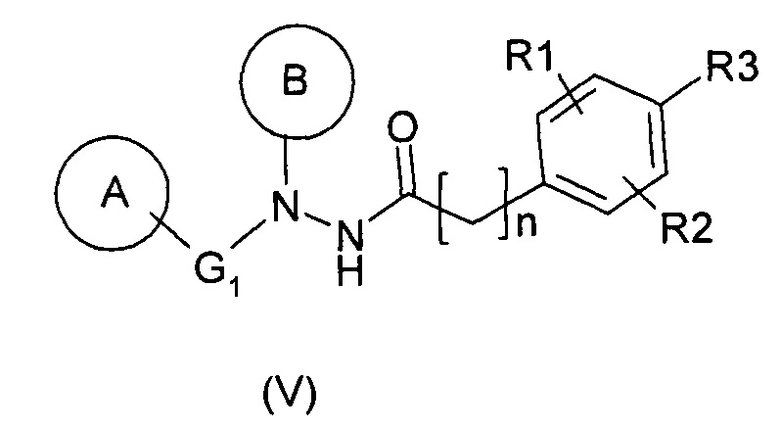
Другим предметом настоящего изобретения является способ получения соединения с нижеследующей формулой (V):
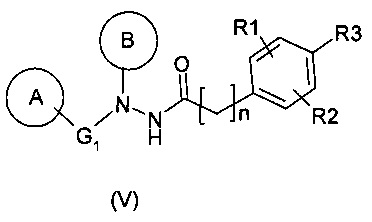
и его фармацевтически приемлемых солей,
где
- R1 обозначает алкоксигруппу, например, метоксигруппу, предпочтительно в орто-положении по отношению к R3,
- R2 обозначает атом водорода или галогена, такой как хлор или бром, или алкильную группу, такую как метил, предпочтительно в мета-положении по отношению к R3,
- R3 обозначает кислотную или сложноэфирную группу и предпочтительно является кислотной группой,
- n представляет собой целое число от 1 до 4, предпочтительно от 1 до 2 и более предпочтительно 1,
• G1 представляет собой связь, либо линейную или разветвленную, насыщенную или ненасыщенную углеводородную цепь, содержащую от 1 до 4 атомов углерода, необязательно замещенную одной или двумя предпочтительно одинаковыми алкильными группами,
• А представляет собой арильную группу, такую как фенил, необязательно замещенный:
- в мета- или пара-положении:
• атомом галогена или цианогруппой, алкоксигруппой, галогеналкоксигруппой, ациламиноалкильной группой или -XR группой, где X представляет собой -O-, -S-, -SO-, -SO2- или -СО-, a R представляет собой арилалкил, циклоалкил или арил, каждый из которых необязательно замещен одним или двумя одинаковыми или различными заместителями, такими как атом галогена, алкоксигруппа или ацильная группа, или
• циклоалкильной, арильной или арилалкильной группой, каждая из которых необязательно замещена одним или двумя одинаковыми или различными заместителями, такими как ацил или алкоксигруппа,
- и/или в орто- или мета положении алкильной группой, и
• В представляет собой арильную группу, предпочтительно фенил, замещенный в орто-положении гетероциклом, предпочтительно N-циклоалкилом, таким как пиперидин-1-ильная группа, и необязательно замещенный в орто'-положении алкильной группой, например метилом,
отличающийся тем, что этот способ включает способ получения соединения с формулой (I), как определено выше.
Соединения с формулой (V) соответствуют соединениям, которые могут быть использованы при лечении инфекции, вызываемой вирусом папилломы, описанным в заявке WO 2007/135106. Данная патентная заявка дополнительно описывает способ получения соединений с формулой (V) из гидразина с формулой (I), а также способ получения аминов с формулой (II).
Под «кислотой», в контексте настоящего изобретения, подразумевают группу COOH.
Под «сложным эфиром», в контексте настоящего изобретения, подразумевают группу -CO-O-Alk, где Alk представляет собой алкильную группу, как определено выше.
Предпочтительно, чтобы R2 представлял собой атом галогена, такой как атом брома, предпочтительно в мета-положении по отношению к R3.
Предпочтительно, чтобы G1 представлял собой связь или линейную и насыщенную углеводородную цепь, содержащую от 1 до 4 атомов углерода, и предпочтительно, чтобы он представлял собой связь.
Предпочтительно, чтобы радикал А, определенный выше, являлся арилом, предпочтительно фенилом, замещенным в мета- или пара-положении, предпочтительно в пара-положении, алкоксигруппой, такой как метоксигруппа, либо арильная или арилалкильная группа, например, фенил или бензил, необязательно замещенный одним или двумя одинаковыми или различными заместителями, такими как ацил или алкоксигруппа.
Предпочтительно, чтобы В представлял собой арильную группу, предпочтительно фенил, замещенный в орто-положении гетероциклом, предпочтительно N-циклоалкилом, таким как пиперидин-1-ильная группа, и необязательно замещенный в орто'-положении алкильной группой, например метилом.
Предпочтительно, чтобы соединение формулы (V) имело следующие особенности:
- А представляет собой фенильную группу, замещенную в пара-положении бензильной группой,
- В представляет собой фенильную группу, замещенную в орто-положении пиперидин-1-ильной группой, а в орто'-положении метильной группой,
- G1 представляет собой связь, и
- R1, R2, R3 и n являются такими, как определено выше.
В частности, соединение формулы (V) является 4-[N'-(4-бензил-фенил)-N'-(2-метил-6-пиперидин-1-ил-фенил)-гидразинокарбонил метил]-5-бром-2-метоксибензойной кислоты гидрохлоридом (соединение (Va)).
Следовательно, соединение (Va) может быть получено из промежуточных соединений (Ia), (IIа) и (IIIa), упомянутых выше.
Другим предметом настоящего изобретения является соединение с общей формулой (III):
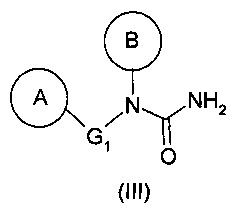
в которой
• G1 представляет собой связь, либо линейную или разветвленную, насыщенную или ненасыщенную углеводородную цепь, содержащую от 1 до 4 атомов углерода, необязательно замещенную одной или двумя предпочтительно одинаковыми алкильными группами,
• А представляет собой арильную группу, такую как фенил, необязательно замещенный:
- в мета- или пара-положении:
• атомом галогена или цианогруппой, алкоксигруппой, галогеналкоксигруппой, ациламиноалкильной группой или -XR группой, где X представляет собой -O-, -S-, -SO-, -SO2- или -CO-, a R представляет собой арилалкил, циклоалкил или арил, каждый из которых необязательно замещен одним или двумя одинаковыми или различными заместителями, такими как атом галогена, алкоксигруппа или ацильная группа, или
• циклоалкильной, арильной или арилалкильной группой, каждая из которых необязательно замещена одним или двумя одинаковыми или различными заместителями, такими как ацил или алкоксигруппа,
- и/или в орто- или метаположении алкильной группой, и
• В представляет собой арильную группу, предпочтительно фенил, замещенный в орто-положении гетероциклом, предпочтительно N-циклоалкилом, таким как пиперидин-1-ильная группа, и необязательно замещенный в орто'-положении алкильной группой, например, метилом.
Предпочтительно, чтобы G1 представлял собой связь или линейную и насыщенную углеводородную цепь, содержащую от 1 до 4 атомов углерода, и предпочтительно, чтобы он представлял собой связь.
Предпочтительно, чтобы радикал А, определенный выше, являлся арилом, предпочтительно фенилом, замещенным в мета- или пара-положении, предпочтительно в пара-положении, алкоксигруппой, такой как метоксигруппа, либо арильная или арилалкильная группа, например фенил или бензил, необязательно замещенный одним или двумя одинаковыми или различными заместителями, такими как ацил или алкоксигруппа.
Предпочтительно, чтобы В представлял собой арильную группу, предпочтительно фенил, замещенный в орто-положении гетероциклом, предпочтительно N-циклоалкилом, таким как пиперидин-1-ильная группа, и необязательно замещенный в орто'-положении алкильной группой, например метилом.
В частности, соединение (III) должно представлять собой 1-(4-бензил-фенил)-1-(2-метил-6-пиперидин-1-ил-фенил)-мочевину (соединение (IIIа)).
Настоящее изобретение станет более понятным в свете следующих ниже неограничивающих примеров.

Синтез соединения (Va)
Стадия 1: Синтез амина (IIа)
Это соединение синтезировали в соответствии с методикой, описанной в заявке WO 2007/135106. Оно соответствует соединению, полученному в Стадии 3 Примера 27 этой заявки (стр. 90-91).
Стадия 2: Синтез мочевины (IIIа)
Этап 1
К суспензии амина (Iа) (4,00 г, 11,23 ммоль, 1,0 экв) в безводном ацетонитриле (100 мл), в атмосфере аргона и при перемешивании добавляли трихлорацетилизоцианат (2,53 г, 13,48 ммоль, 1,2 экв) по каплям при 18°C в течение 10 минут. Полученный прозрачный желтый раствор перемешивали в течение добавочных 15 мин при комнатной температуре. После полного израсходования амина (IIа) (контролировали с помощью ТСХ и ВЭЖХ) растворитель выпаривали при пониженном давлении. Полученный таким образом прозрачный бурый неочищенное промежуточное соединение (6,2 г, количественный выход) использовали непосредственно на следующей стадии без дополнительной очистки.
Выход: количественный
ВЭЖХ: 92.24%.
1Н-ЯМР (CDCl3, 200 МГц) δ (м.д.): 8,80 (широкий синглет, 1Н), 6,95-7,31 (мультиплет, 12Н), 3,92 (синглет, 2Н), 2,86 (м, 2Н), 2,73 (м, 2Н), 2,03 (с, 3H), 1,53 (м, 6Н).
Этап 2
К раствору неочищенного промежуточного соединения, полученного на Этапе 1 выше (6,13 г, 11,2 ммоль, 1,0 экв), в метаноле (120 мл) добавляли водный раствор КОН (12,73 г КОН, 224,0 ммоль, 20 экв в 25 мл воды) при перемешивании. Затем реакционную смесь нагревали при 75°C со встряхиванием в течение 1,5 ч при той же температуре. После полного израсходования промежуточного соединения (контролировали с помощью ТСХ) реакционную смесь концентрировали досуха. Затем полученную сырую смесь переносили в воду (100 мл) и экстрагировали этилацетатом (3×100 мл). Объединенные органические фазы высушивали над сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением целевой мочевины (IIIa) (4,43 г, 11,1 ммоль, 99% выход) в виде бесцветной смолы с чистотой 83%, определенной при помощи ВЭЖХ. Затем эту мочевину использовали в том же виде на следующем этапе.
Выход: 99%
МС: МН+ 400
ВЭЖХ: 83,01%
1Н-ЯМР (CDCl3, 200 МГц) δ (м.д.): 6,94-7,30 (м, 12Н), 4,77 (с, 2Н), 3,91 (с, 2Н), 2,91 (м, 2Н), 2,60 (м, 2Н), 2,26 (с, 3Н), 1,48 (м, 6Н).
Стадия 3: Синтез гидразина (Ia)
К раствору неочищенной мочевины (IIIа), полученной на предыдущем Этапе 2 (4,43 г, 11,1 ммоль, 1 экв), в трет-бутаноле (50 мл) добавляли КОН (водный раствор 12,58 г КОН, 222,1 ммоль, 20 экв в 25 мл воды) при 18°C с перемешиванием в течение 10 мин. К полученной реакционной смеси добавляли водный раствор NaOCl (8,21 мл, 11,1 ммоль, 10% активного хлора) порциями (по 1 мл каждые 15 минут) в течение 2,25 ч. После энергичного перемешивания при 18°C в течение добавочных 15 минут разделяли фазы. Реакционную смесь экстрагировали этилацетатом (3×100 мл). Объединенные органические фазы концентрировали досуха при пониженном давлении с получением целевого гидразина (4 г, с чистотой 83%, определенной методом ВЭЖХ). Затем полученный таким образом остаток очищали флэш-хроматографией на колонке с силикагелем (элюент: 95/5 циклогексан/этилацетат) с получением целевого гидразина (3,4 г, 9,1 ммоль, общий выход 81%) в виде твердого вещества кремового цвета с чистотой 95,6%, определенной при помощи ВЭЖХ.
Общий выход: 81%
МС: МН+ 372
ВЭЖХ: 95,60%
1Н-ЯМР (CDCl3, 400 МГц) δ (м.д): 7,25 (м, 2Н), 7,14 (м, 4Н), 6,97 (м, 4Н), 6,73 (м, 2Н), 4,83 (широкий синглет, 2Н), 3,87 (с, 2Н), 2,80 (широкий синглет, 4Н), 2,08 (с, 3Н), 1,46-1,57 (м, 6Н).
Стадия 4: Синтез соединения (Va)
Это соединение получают из гидразина (Ia), полученного на предыдущей стадии 3 в соответствии с протоколом, описанным в заявке WO 2007/135106. Этот протокол описан в Примере 27 упомянутой заявки и соответствует стадии 5 и 6 данного примера (стр. 91-92).
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ИНГИБИТОРА ПАПИЛЛОМАВИРУСА | 2013 |
|
RU2661007C2 |
| ПРОИЗВОДНЫЕ ТЕТРАГИДРОПИРИМИДИН-2-ОНА И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2334741C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ РЕЦЕПТОРА EP4 В ЛЕЧЕНИИ IL-23-ОПОСРЕДУЕМЫХ ЗАБОЛЕВАНИЙ | 2011 |
|
RU2571816C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ | 2006 |
|
RU2383539C2 |
| АЗОТСОДЕРЖАЩИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ | 2009 |
|
RU2477281C2 |
| СПОСОБ АСИММЕТРИЧЕСКОГО ГИДРИРОВАНИЯ ПРОИЗВОДНЫХ АКРИЛОВОЙ КИСЛОТЫ, КАТАЛИЗИРУЕМОГО ПЕРЕХОДНЫМИ МЕТАЛЛАМИ, И НОВАЯ КАТАЛИТИЧЕСКАЯ СИСТЕМА ДЛЯ АСИММЕТРИЧЕСКОГО КАТАЛИЗА ПЕРЕХОДНЫМИ МЕТАЛЛАМИ | 2005 |
|
RU2415127C2 |
| ТЕРАПЕВТИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ИЛИ ПРОФИЛАКТИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ОТ ДИАБЕТИЧЕСКОЙ НЕФРОПАТИИ | 2017 |
|
RU2735538C1 |
| ПРОИЗВОДНЫЕ (ТИО)МОЧЕВИНЫ, ИНГИБИРУЮЩИЕ ФАКТОР VIIa, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2286337C2 |
| ПРОИЗВОДНЫЕ ПИРИДАЗИНОНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2131419C1 |
| 3-АЛКИЛИДЕНГИДРАЗИНО-ЗАМЕЩЕННЫЕ ГЕТЕРОАРИЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ АКТИВАТОРОВ РЕЦЕПТОРА ТРОМБОПОЭТИНА | 2004 |
|
RU2358970C2 |
Изобретение относится к способу получения соединения общей формулы (I) и его фармацевтически приемлемых солей из амина формулы (II) с использованием мочевины формулы (III) в качестве промежуточного соединения синтеза. Согласно предлагаемому способу мочевину формулы (III) получают из амина формулы (II) в соответствии со следующими этапами: (1) реакция амина формулы (II) и Cl3CC(O)-N=C=O с получением соединения, имеющего формулу (IV); (2) обработка в щелочной среде соединения формулы (IV), полученного на предыдущем этапе, с получением мочевины формулы (III). Затем из мочевины формулы (III) получают соединение формулы (I) с помощью перегруппировки Шестакова. Способ позволяет получать гидразины формулы (I), которые могут найти применение в синтезе соединений с формулой (V), используемых при лечении инфекции, вызываемой вирусом папилломы. Изобретение относится также к способу получения соединения формулы (V) и соединению формулы (III). В формулах (I)-(V) G1 представляет собой связь, А представляет собой арильную группу, такую как фенил, замещенный в пара-положении (С5-10)арил-(С1-6)алкильной группой, и В представляет собой арильную группу, такую как фенил, замещенный в орто-положении гетероциклом, таким как пиперидин-1-ильная группа, и замещенный в орто'-положении алкильной группой, такой как метил. 3 н. и 5 з.п. ф-лы, 4 пр.

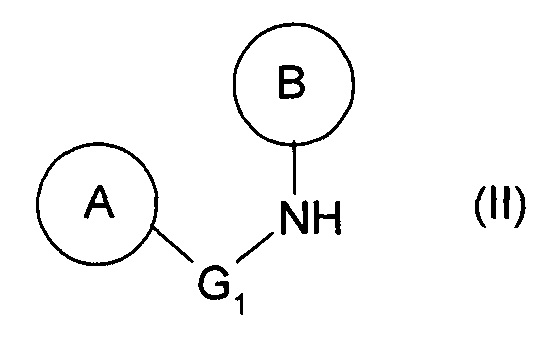


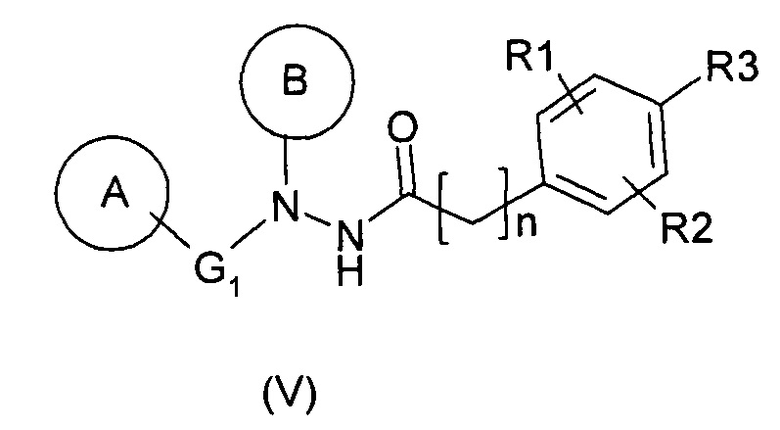
1. Способ получения соединения общей формулы (I)
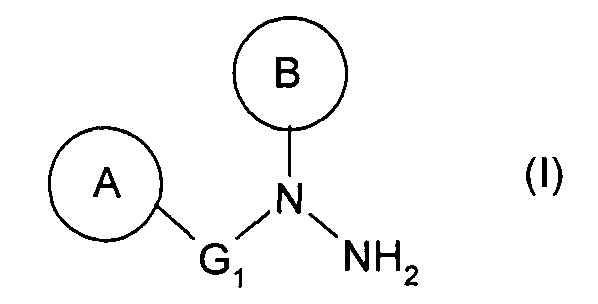
и его фармацевтически приемлемых солей,
где
G1 представляет собой связь,
А представляет собой арильную группу, такую как фенил, замещенный в пара-положении (С5-10)арил-(С1-6)алкильной группой,
и
В представляет собой арильную группу, такую как фенил, замещенный в орто-положении гетероциклом, таким как пиперидин-1-ильная группа, и замещенный в орто'-положении алкильной группой, такой как метил,
из амина формулы (II)
 ,
,
где G1, А и В являются такими, как определено выше,
отличающийся тем, что используют мочевину формулы (III) в качестве промежуточного соединения синтеза
 ,
,
где G1, А и В являются такими, как определено выше,
где мочевину формулы (III) получают из амина формулы (II) в соответствии со следующими этапами:
(1) реакция амина формулы (II) и Cl3CC(O)-N=C=O с получением соединения, имеющего следующую формулу (IV):
 ,
,
где G1, А и В являются такими, как определено выше, и
(2) обработка в щелочной среде соединения формулы (IV), полученного на предыдущем этапе, с получением мочевины формулы (III),
и из мочевины формулы (III) получают соединение формулы (I) с помощью перегруппировки Шестакова.
2. Способ по п.1, отличающийся тем, что перегруппировку Шестакова осуществляют в присутствии индуцирующего перегруппировку агента, выбранного из NaOCl и KOCl, предпочтительно NaOCl.
3. Способ по п.2, отличающийся тем, что индуцирующий перегруппировку агент вводят ступенчато.
4. Способ по п.1, отличающийся тем, что соединение формулы (I) представляет собой N-(4-бензил-фенил)-N-(2-метил-6-пиперидин-1-ил-фенил)гидразин.
5. Способ получения соединения формулы (V)
и его фармацевтически приемлемых солей,
где
R1 обозначает (C1-6)алкоксигруппу в орто-положении по отношению к R3,
R2 обозначает атом галогена, такой как хлор или бром, в мета-положении по отношению к R3,
R3 обозначает карбоксигруппу,
n представляет собой целое число от 1 до 4,
G1 представляет собой связь,
А представляет собой арильную группу, такую как фенил, замещенный в пара-положении (С5-10)арил-(С1-6)алкильной группой,
и
В представляет собой арильную группу, такую как фенил, замещенный в орто-положении гетероциклом, таким как пиперидин-1-ильная группа, и замещенный в орто'-положении алкильной группой, такой как метил,
отличающийся тем, что включает способ по любому из пп.1-4.
6. Способ по п.5, отличающийся тем, что соединение с формулой (V) является 4-[N'-(4-бензил-фенил)-N'-(2-метил-6-пиперидин-1-ил-фенил)гидразинокарбонилметил]-5-бром-2-метоксибензойной кислоты гидрохлоридом.
7. Соединение формулы (III)
 ,
,
в которой
G1 представляет собой связь,
А представляет собой арильную группу, такую как фенил, замещенный в пара-положении (С5-10)арил-(С1-6)алкильной группой,
и
В представляет собой арильную группу, такую как фенил, замещенный в орто-положении гетероциклом, таким как пиперидин-1-ильная группа, и замещенный в орто'-положении алкильной группой, такой как метил.
8. Соединение по п.7, отличающееся тем, что оно представляет собой 1-(4-бензил-фенил)-1-(2-метил-6-пиперидин-1-ил-фенил)мочевину.
| Колосоуборка | 1923 |
|
SU2009A1 |
| J | |||
| VIRET ET AL, Practical synthesis of optically active α -hydrazino acids from α -amino acids, TETRAHEDRON, 1987, vol | |||
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Способ получения губчатого свинца и приготовления из него аккумуляторных пластин без прессования | 1921 |
|
SU891A1 |
| АЗОТСОДЕРЖАЩИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ КАРБОКСАМИДА ИЛИ ИХ СОЛИ И ПРОТИВОВИРУСНЫЕ СРЕДСТВА, ВКЛЮЧАЮЩИЕ ИХ | 1999 |
|
RU2224520C2 |
Авторы
Даты
2018-03-29—Публикация
2013-12-27—Подача