Изобретение относится к области медицины, а именно к терапии воспалительных заболеваний, и может быть использовано в качестве противовоспалительного средства. Предложено противовоспалительное средство, представляющее собой 70%-ную настойку из высушенной и измельченной надземной части копеечника кустарникового (Hedysarum fruticosum), полученную методом перколяции в соотношении сырье : экстрагент 1:10.
Фармакологическая регуляция воспалительных процессов является актуальной проблемой медицинской науки и практики. В настоящее время известны синтетические противовоспалительные препараты, например, ацетилсалициловая кислота (АСК), индометацин и некоторые др. (Машковский М.Д. Лекарственные средства: Т. 2. - М., 1998. - 592 с.). Однако в некоторых случаях их применение ограничено из-за высокой возможности развития нежелательных лекарственных реакций, плохой переносимости. Кроме синтетических препаратов известны фитопрепараты из лекарственных растений, обладающие противовоспалительным действием. Они имеют ряд преимуществ: лучшая переносимость, меньшая токсичность, полифункциональность.
Задачей предлагаемого изобретения является получение настойки на основе природного растительного сырья, обладающего высокой противовоспалительной активностью и низкой токсичностью.
Сущность изобретения состоит в том, что предложена настойка из высушенной и измельченной надземной части копеечника кустарникового, получаемая методом перколяции с использованием в качестве экстрагента 70%-ного этилового спирта в соотношении в весовых частях сырье : экстрагент 1:10. Способ изготовления противовоспалительного средства включает получение настойки методом перколяции, отличающийся тем, что на 1 этапе перколяции 10 г высушенной и измельченной надземной части копеечника кустарникового заливают 11,29 мл 70%-ного этилового спирта.
Перколяция - процеживание экстрагента через растительный материал с целью извлечения растворимых в экстрагенте веществ. Метод перколяции включает три последовательно протекающие стадии: намачивание сырья (набухание), настаивание и собственно перколяция.
Намачивание (набухание) проводят вне перколятора. Для намачивания используют от 50 до 100% экстрагента по отношению к массе сырья. После перемешивания сырье оставляют на 4-5 ч в закрытой емкости. За это время экстрагент проникает между частицами растительного материала и внутрь клеток, сырье набухает, увеличиваясь в объеме. При этом происходит растворение действующих веществ внутри клетки.
Настаивание - вторая стадия процесса перколяции. Набухший или сухой материал загружают в перколятор и заливают экстрагентом до образования «зеркала», высота слоя которого над сырьем должна быть около 30-40 мм, и проводят настаивание 24-48 ч, в течение которых будет достигнута равновесная концентрация. Для многих видов сырья время настаивания может быть сокращено.
Собственно перколяция - непрерывное прохождение экстрагента через слой сырья и сбор перколята. При этом слив перколята и одновременная подача сверху экстрагента проводится со скоростью, не превышающей 1/24 части используемого объема перколятора за 1 ч. При этом насыщенная вытяжка вытесняется из растительного материала током свежего экстрагента и создается разность концентраций экстрагируемых веществ в сырье и экстрагенте. Скорость перколяции должна быть такой, чтобы успевала произойти диффузия экстрагируемых веществ в вытяжку. При приготовлении настоек перколирование заканчивают получением пяти или десяти объемов (в зависимости от свойств сырья) вытяжки по отношению к массе загруженного сырья (Промышленная технология лекарств: Учебник. В 2-х т. Том 2 / В.И. Чуешов, М.Ю. Чернов, Л.М. Хохлова и др.; Под ред. В.И. Чуешова. - Харьков: МТК-Книга; Издательство НФАУ, 2002. - 716 с.).
Предложено противовоспалительное средство, представляющее собой настойку из высушенной и измельченной надземной части копеечника кустарникового в соотношении сырье : экстрагент 1:10, полученную методом перколяции с использованием в качестве экстрагента 70%-ного этилового спирта.
Предлагаемое средство изготавливается следующим образом: собранную надземную часть копеечника кустарникового высушивают и измельчают с помощью мельницы. Просеивают сквозь сито с диаметром отверстий 3 мм. 10 г измельченного сырья заливают 11,29 мл 70%-ного этилового спирта (для намачивания используют 100% экстрагента по отношению к массе сырья, с учетом значения плотности спирта 70%-ной концентрации, равной 0,8854 г/мл), перемешивают и оставляют на 4 часа в закрытой емкости. Набухшее сырье помещают в перколятор, заливают экстрагентом до образования «зеркала» и настаивают в течение 24 часов. По истечении времени проводят собственно перколяцию. Слив перколята и одновременная подача экстрагента проводится со скоростью, не превышающей 1/24 части используемого объема перколятора за 1 час. Хранят полученную настойку в темном прохладном месте.
Использование в качестве экстрагента 70%-ного этилового спирта обусловлено тем, что максимальное количество действующих веществ извлекается из высушенной и измельченной надземной части копеечника кустарникового именно этиловым спиртом 70%-ной концентрации.
Фитохимический скрининг настойки показал наличие следующих групп биологически активных веществ (БАВ): флавоноиды (1,6%), фенольные соединения ((галловая кислота (14,6%) протокатеховая кислота (11,2%), кофейная кислота (7,9%), хлорогеновая кислота (24,4%)), органические кислоты, в пересчете на яблочную кислоту (3,5%), дубильные вещества (около 8,5%), аскорбиновая кислота (0,0096%), свободные сахара (галактоза, глюкоза, фруктоза, рамноза), полисахариды (12,5%), тритерпеновые сапонины (2,6% в пересчете на астрагалозид), каротиноиды (в пересчете на β-каротин 0,00428%), аминокислоты (3,2% в пересчете на глутаминовую кислоту). Выраженное противовоспалительное действие предлагаемой настойки обусловлено наличием в ней фенольных соединений в растительном сырье (Йорданов Д., Николов П., Бойчинов Асп. Фитотерапия. Лечение травами. - София, 1970. - 344 с.). Присутствие в качестве сопутствующих соединений аскорбиновой кислоты и дубильных веществ также оправдывает применение настойки копеечника кустарникового в качестве противовоспалительного средства.
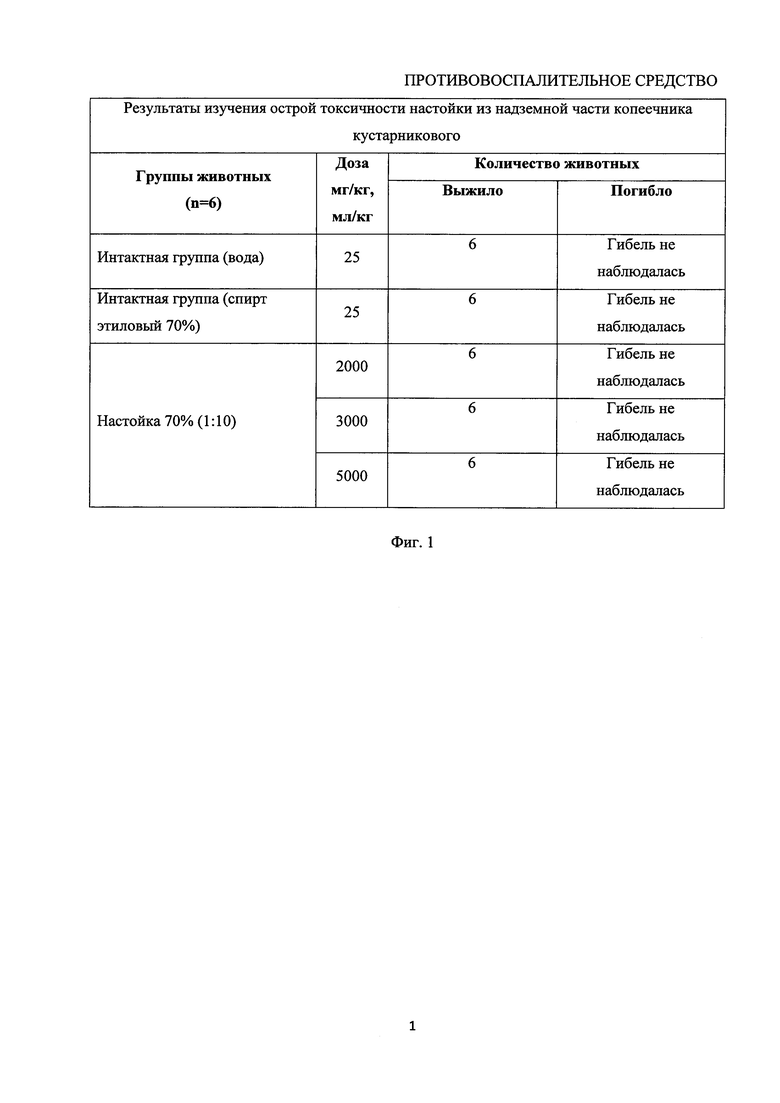
Для определения острой токсичности использовали методику Б.М. Штабского (Штабский Б.М. К методике определения средне-смертельных доз и концентраций химических веществ / Б.М. Штабский и др. // Гигиена и санитария. - 1980. - №10. С. 49-51.). Исследования проводили на беспородных белых мышах обоего пола массой 18,0-26,0 г. Предлагаемую настойку вводили однократно внутрижелудочно в дозах от 1 до 5 г/кг (в пересчете на сухое сырье) в объеме 0,5 мл. После введения каждую группу животных (не менее 6 животных) помещали в изолированную клетку при стандартном температурном и пищевом режиме и вели наблюдение в течение 24 часов (Сернов Л.Н. Элементы экспериментальной фармакологии / Л.Н. Сернов, В.В. Гацура. - М., 2000. - 352 с.).
В эксперименте установлено, что однократное введение настойки копеечника кустарникового в дозах 2000-5000 мг/кг не влияет на общее состояние животных, симптомы острого отравления не регистрировались, падеж животных отсутствовал. Так как исследуемая доза настойки не привела к гибели ни одного животного, сделан вывод, что LD50>2000 мг/кг и, в соответствии смодифицированной классификацией Организации экономического содействия и развития (OECD), анализируемая настойка на основе высушенной и измельченной надземной части копеечника кустарникового относится к IV классу опасности (малотоксичные вещества), как и практически все суммарные фитопрепараты (Лобанова И.Ю. Изучение острой токсичности и антиоксидантной активности экстракта листьев осины сухого / И.Ю. Лобанова, В.Ф. Турецкова, Я.Ф. Зверев, О.С. Талалаева // Фундаментальные исследования. - 2012. - №9. - С. 308-312).
В течение всего периода наблюдения поведенческие реакции животных экспериментальной группы были в пределах физиологической нормы: отмечались обычное питьевое и пищевое поведение, нормальная координация движений, обычная частота и глубина дыхательных движений, нормальная консистенцию фекальных масс, частота мочеиспускания и окраска мочи. За это время мыши прибавили в весе (таблица на фиг. 1).
Для доказательства противовоспалительной активности 70%-ной настойки из высушенной и измельченной надземной части копеечника кустарникового было проведено исследование на модели формалинового отека (Хабриев Р.У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. - М.: Медицина, 2005. - 832 с.). Экспериментальную работу выполняли на белых крысах-самцах линии Wistar с массой 183,0-226,0 г. В эксперименте было задействовано 42 животных, которых содержали в стандартных условиях вивария ФГБОУ ВО СГМУ Минздрава России при 12-часовом режиме освещения и свободном доступе к воде и корму. Каждая группа состояла из животных приблизительно одинаковой массы в количестве 6 особей.
Результаты статистической обработки химического и фармакологического экспериментов вели по Государственной Фармакопее (ГФ) XIII издания. Обработку данных осуществляли с использованием пакетов Microsoft Excel 2016. Независимые группы сравнивали с помощью непараметрического U-теста Манна-Уитни, различия считали достоверными при р≤0,01 и р≤0,05 (Гублер Е.В. Вычислительные методы анализа и распознавания патологических процессов. - Л., 1978 - С. 72).
Пример конкретного выполнения эксперимента №1 (модель формалинового отека).
Опыты проводят на белых крысах-самцах линии Wistar массой 196-219 г. Животных отбирают таким образом, чтобы исходный средний объем лапок во всех экспериментальных группах был примерно одинаков.
В ходе выполнения эксперимента 70%-ную настойку из высушенной и измельченной надземной части копеечника кустарникового (25 мл/кг), ацетилсалициловую кислоту (300 мг/кг), 70%-ный этиловый спирт и дистиллированную воду вводят через зонд в желудок в объеме из расчета 5 мл на 200 г массы животного, соблюдая временной интервал до введения формальдегида за 2 часа и через 5 часов и 18 часов после его введения, а затем ежедневно в течение 7 дней.
Острую воспалительную реакцию воспроизводят путем субплантарного введения (под апоневроз лапки) 0,1 мл 2% раствора формалина в виде водного раствора в левую лапу крысе. Это вызывает, развивающийся во времени отек лапки. Степень отека отражает интенсивность воспаления. Величину отека измеряют по количеству вытесненной воды при погружении в нее лапки.
Экспериментальных животных разбивают на 7 групп по 6 особей в каждой. Животные первой группы являются интактными, второй группе перорально вводят воду очищенную, третьей - 70%-ный этиловый спирт. Четвертой и пятой группе создают воспаление, на фоне которого вводят соответствующие растворители: воду очищенную и этиловый спирт 70%-ной концентрации. Животным шестой группы на фоне введения формалина дают настойку копеечника кустарникового. Животные седьмой группы в аналогичных условиях совместно с формалином получают препарат сравнения, которым служит ацетилсалициловая кислота в дозе 300 мг/кг. Измерение объема лапки проводят через 3, 24, 72, 120, 168 часов после введения в лапку формалина.
Антиэкссудативное действие изучают методом онкометрии (Тринус Ф.П., Мохорт Н.А., Клебанов Б.М. Нестероидные противовоспалительные средства. - Киев: Здоровья, 1975. - С. 205). Развитие отека оценивают по формуле 1:
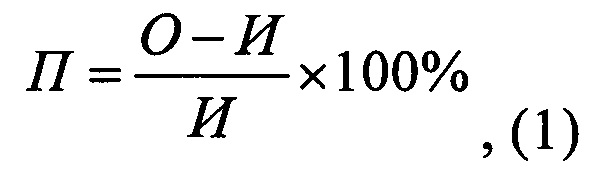
где П - прирост отека;
О - величина объема лапы после введения индуктора воспаления;
И - величина объема лапы до введения индуктора воспаления.
Эффект терапевтического воздействия (торможение воспаления) оценивали по степени угнетения воспалительной реакции по сравнению с контролем и рассчитывали по формуле 2:
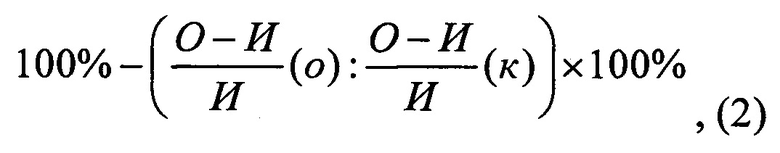
где И - величина объема лапы до введения индуктора воспаления;
О - величина объема лапы после введения индуктора воспаления;
о - группа животных, получавшая фармакологический препарат;
к - группа животных, получавшая индуктор воспаления.
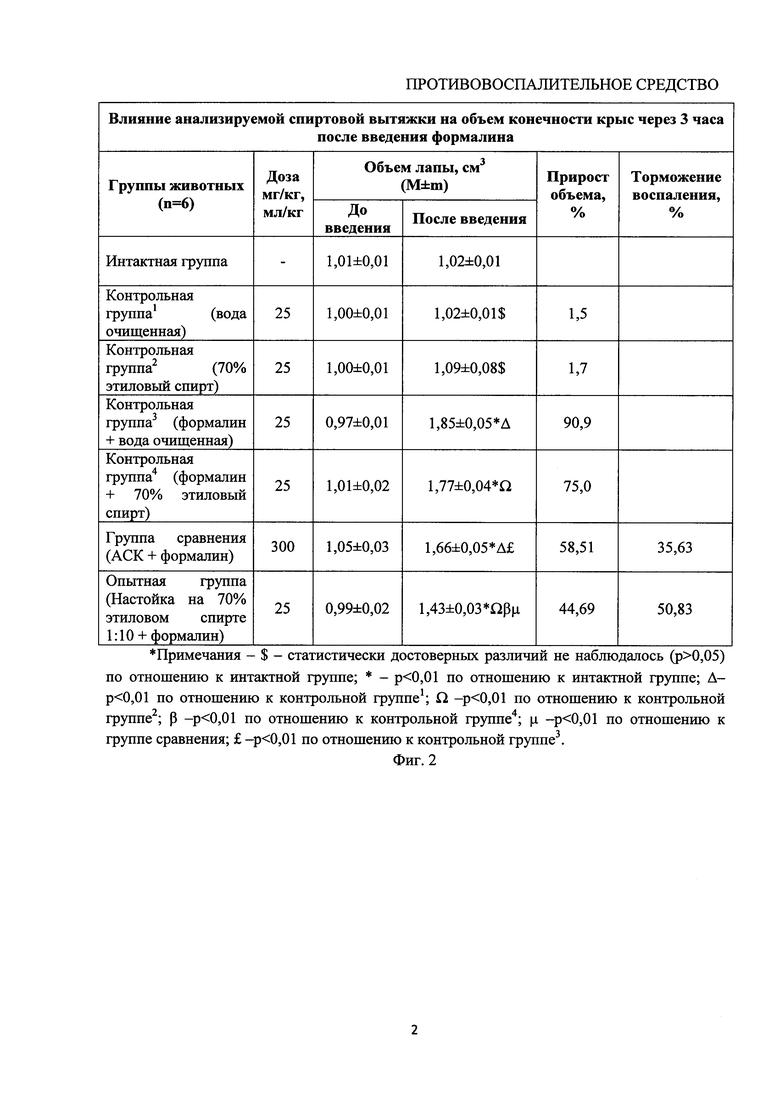
Результаты сравнительного исследования влияния профилактического введения настойки на развитие формалин-индуцированного отека лапы крысы представлены в таблице на фиг. 2.
Исходный объем конечности интактных крыс составил 1,01±0,01 см3 (вода очищенная). В группе контрольных животных - 1,00±0,01 см3 (70% этиловый спирт). Как видно исходный объем лапок крыс во всех группах был примерно одинаков и статистически достоверных различий не наблюдалось (р>0,05), это согласуется с данными литературы (Мосесова Н.С., Ковалева В.Л., Ларенцова Л.И. Экспериментальное исследование противовоспалительных свойств Мексидола // Сборник трудов III Всероссийской научно-практической конференции «Образование, наука и практика в стоматологии» - Москва. - 2006. - С. 108-110.). При индукции воспаления формалином через 3 часа наблюдалось увеличение объема конечности на 0,88±0,04 см3 (р<0,01). На фоне введения АСК объем конечности у крыс увеличивался по сравнению с контролем до 1,66±0,05 см3 (р<0,01), торможение воспаления составило 35,63%).
При введении анализируемой настойки объем конечности увеличился по сравнению с контролем соответственно до 1,43±0,03 см3 (р<0,01), а торможение воспаления составило 50,83%.
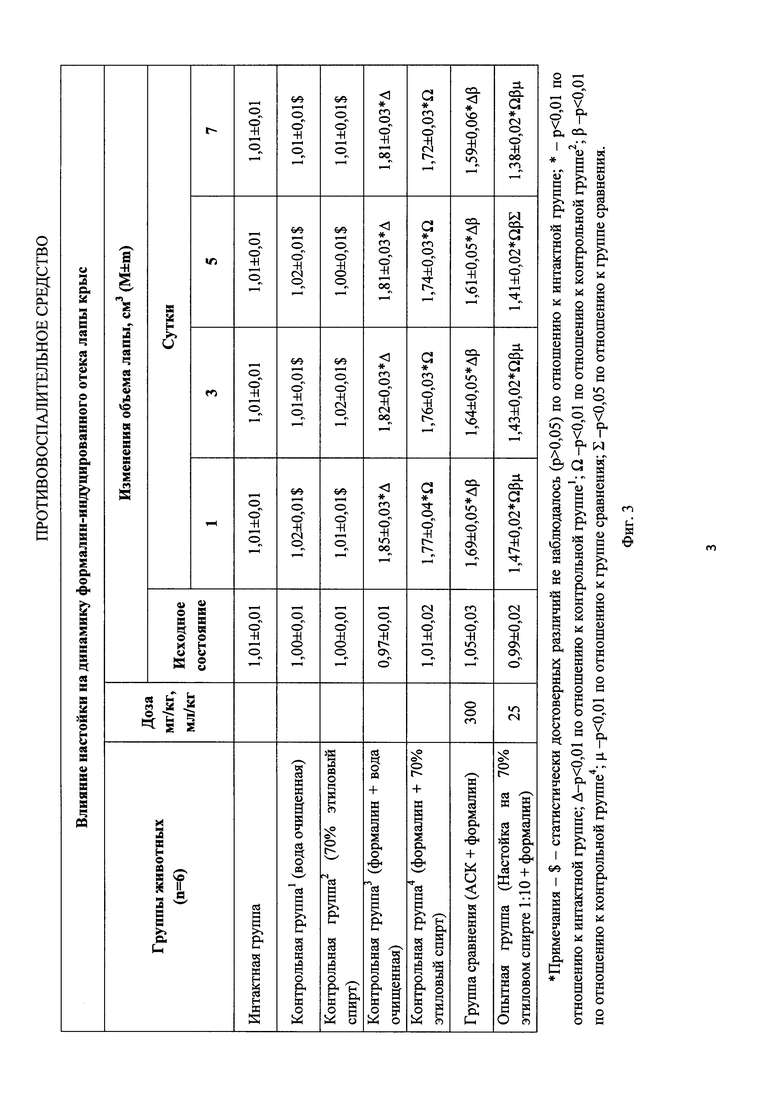
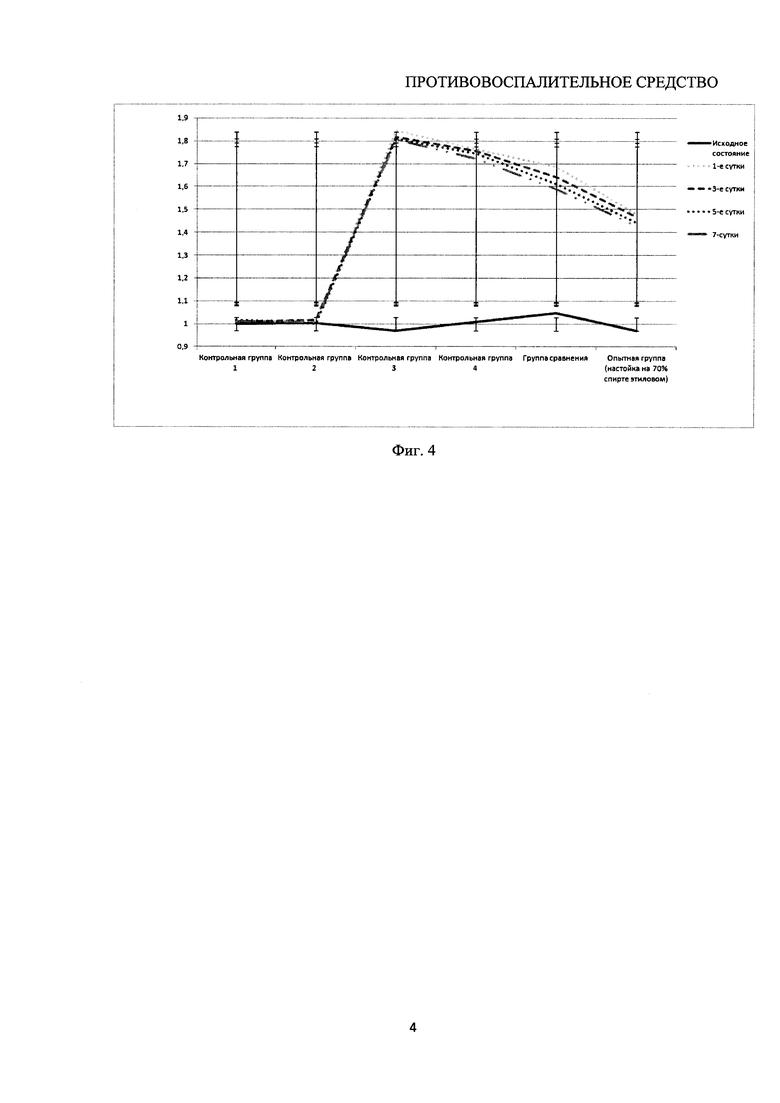
Далее было изучено влияние настойки на динамику формалин-индуцированного воспаления. Данные этих исследований представлены на фиг. 3 и фиг. 4.
При индукции воспаления формалином установлено, что воспалительная реакция формировалась в течение 3 часов (фиг. 2). Данный эффект достигал максимума в первые сутки (1,85±0,03 см3 (р<0,01), 1,77±0,04 см3 (р<0,01)) и сохранялся в течение 7 суток.
При использовании у опытных животных АСК объем конечности через сутки достоверно увеличился до 1,69±0,05 см3 (р<0,01), при этом тенденция к его уменьшению наблюдалась на 3-е сутки. Возврат к исходному значению отмечен спустя 7 суток. В опытной группе, где применялась настойка объем конечности через 1 сутки после введения формалина составил 1,47±0,02 см3 (р<0,01), динамика снижения объема конечности отмечалась на 3-е сутки, к 7-му дню объем конечности уменьшился до 1,38±0,02 см3 (р<0,01).
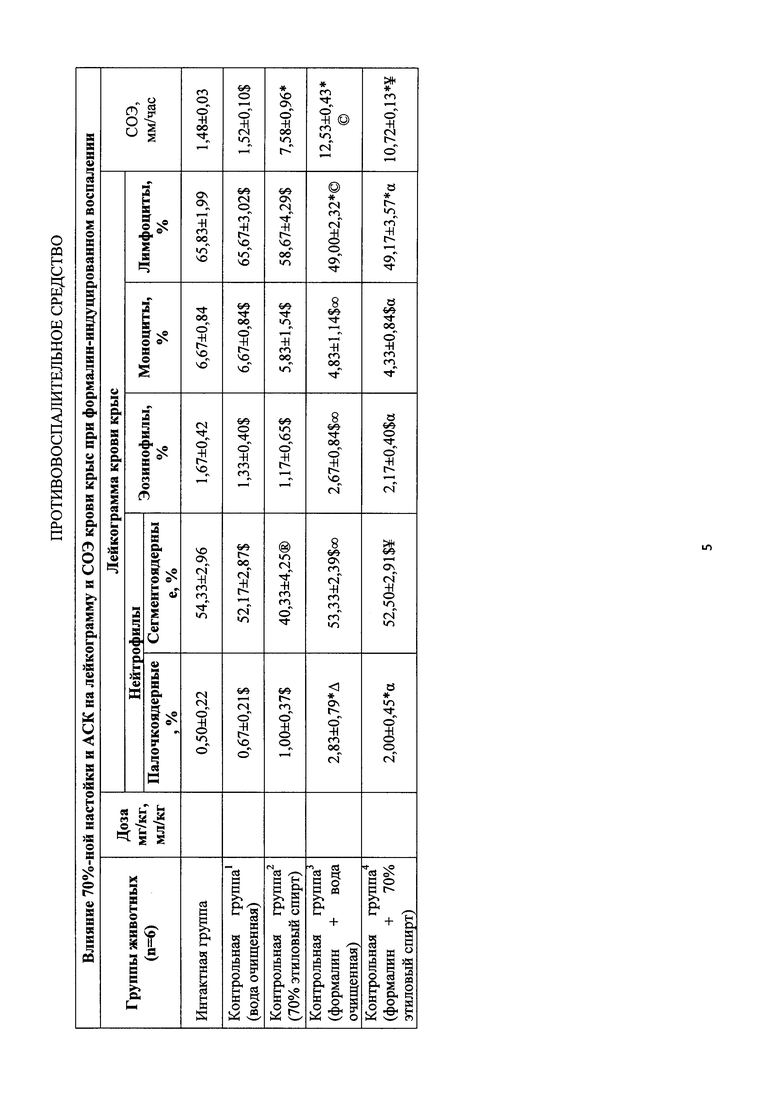
Острое воспаление проявляется характерными изменениями лейкограммы крови и скорости оседания эритроцитов (СОЭ). Были изучены эти показатели у контрольных и опытных животных через 3 часа после введения формалина.
Для изучения лейкограммы крови проводили подсчет общего числа лейкоцитов стандартным методом в камере Горяева. Мазки крови фиксировали метанолом в течение 10 минут и окрашивали по Романовскому-Гимзе. Подсчет клеток крови осуществляли под иммерсионным объективом ×90, окуляр ×5. Забор крови животных производили путем частичного обрезания кончика хвоста, через 18 часов после индукции воспаления.
По показателям лейкограммы производили расчет агранулоцитарно/гранулоцитарного индекса (индекс противовоспалительной активности - I), который представляет собой соотношение суммы агранулоцитов (лимфоциты и моноциты) к сумме гранулоцитов (нейтрофилы и эозинофилы):
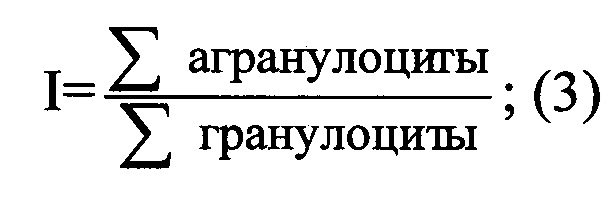
Как видно из таблицы на фиг. 4, во всех контрольных группах животных введение флогогена вызывало увеличение количества нейтрофилов, что характерно для острого воспалительного процесса. Количество зрелых форм нейтрофилов и эозинофилов в крови животных, которым вводили формалин, возросло соответственно до 53,33±2,39% и 2,67±0,84%; 52,50±2,91% и 2,17±0,40% (р>0,05), по сравнению с интактными группами. Количество моноцитов и лимфоцитов уменьшилось соответственно до 4,83±1,14%, 4,33±0,84% (р>0,05) и 49,00±2,32%, 49,17±3,57% (р<0,01).
В группах животных, получавших лекарственные препараты после введения формалина, наблюдались противоположные изменения, так, например, под действием АСК и настойки 70% количество нейтрофилов уменьшилось до 38,5±2,11%, 33,83±2,8% (р<0,01), лимфоцитов уменьшилось соответственно до 65,50±2,28%, 49,33±4,31% (р>0,05). При этом количество моноцитов и эозинофилов при введении этих же препаратов увеличилось до 7,00±1,29%, 7,33±1,23% (р>0,05) и 0,67±0,33%, 1,17±0,48% (р<0,05) соответственно.
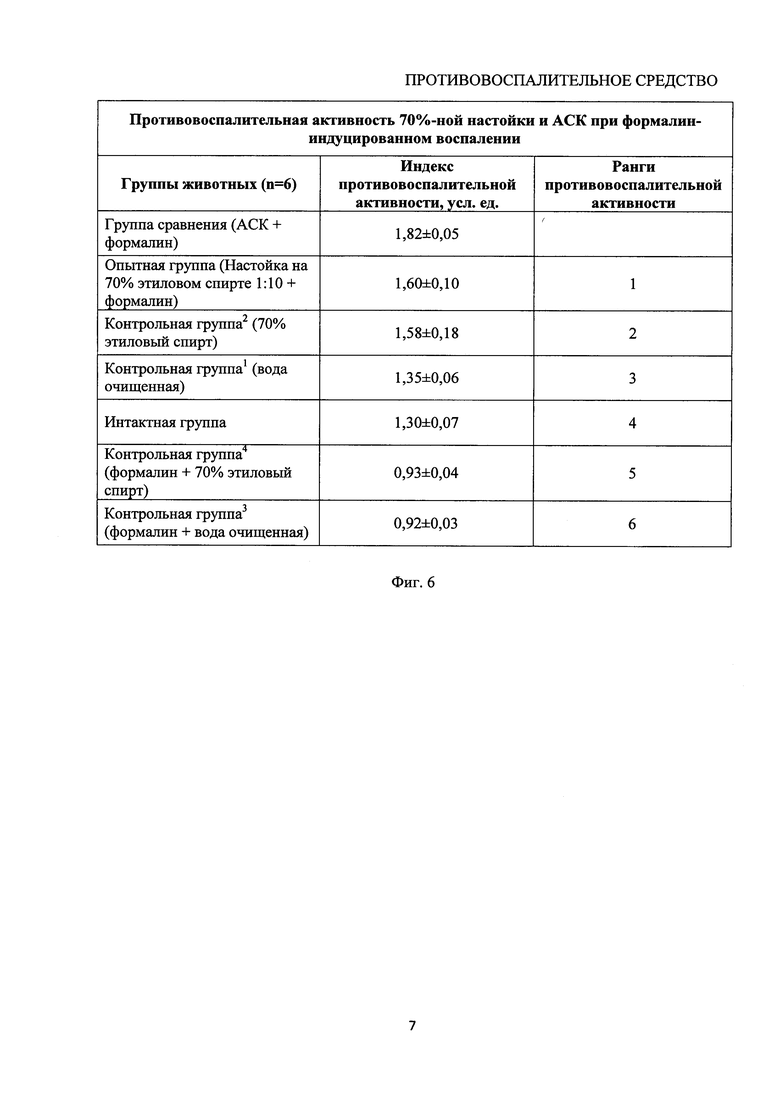
Для оценки противовоспалительной активности настойки и АСК на модели формалин-индуцированного воспаления был рассчитан индекс противовоспалительной активности по формуле 3.
Наибольшее значение индекса противовоспалительной активности отмечено у АСК - 1,82±0,05, а наименьшее при моделировании воспаления у воды - 0,92±0,03. При наличии воспаления предлагаемый индекс уменьшается, а его величина зависит от тяжести патологического процесса (таблица на фиг. 5).
На основании величины значения агранулоцитарно/гранулоцитарного индекса произведено ранжирование препаратов по их противовоспалительной активности (в порядке убывания активности) на модели формалин-индуцированного воспаления (фиг. 6). Таким образом, наибольшая противовоспалительная активность на модели формалин-индуцированного воспаления выявлена у предлагаемой настойки, а наименьшая - у воды, которая практически не оказывает противовоспалительного действия.
Признаком воспалительной реакции также является повышение скорости оседания эритроцитов (СОЭ). Это связано с увеличением содержания фибриногена (одного из белков острой фазы воспаления), что приводит к агглютинации эритроцитов. Определение СОЭ проводили сразу же после взятия крови (не позднее 2-х часов) с помощью микрометода Панченкова.
Показатель СОЭ в группе животных, где применялся формалин, составил 12,53±0,43 мм/ч, что в 8,5 раз больше, чем в интактной группе. На фоне настойки 70% и АСК СОЭ достоверно снизилась до 7,60±0,16 мм/ч и 5,47±0,18 мм/ч (р<0,01) соответственно (фиг. 5).
Анализ полученных результатов проведенных исследований показывает, что предлагаемая нами настойка оказывает более выраженное действие, чем у препарата сравнения (ацетилсалициловая кислота) и достоверное в сравнении с результатами, полученными в контрольной группе животных.
Таким образом, экспериментально установлена возможность использования 70%-ной настойки из высушенной и измельченной надземной части копеечника кустарникового в соотношении сырье : экстрагент 1:10 в качестве противовоспалительного средства в медицине. Предлагаемая нами настойка обладает выраженной противовоспалительной активностью. При сравнении с ацетилсалициловой кислотой настойка копеечника кустарникового 70%-ная не уступает по эффективности, а в некоторых случаях превосходит ее.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФИТОСУБСТАНЦИИ С АДАПТОГЕННОЙ И АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ (ВАРИАНТЫ) | 2024 |
|
RU2836177C1 |
| АДАПТОГЕННЫЙ, ТОНИЗИРУЮЩИЙ, ИММУНОМОДУЛИРУЮЩИЙ, ГИПОГЛИКЕМИЧЕСКИЙ, АНТИГИПОКСИЧЕСКИЙ, ПРОТИВОВОСПАЛИТЕЛЬНЫЙ, НООТРОПНЫЙ, РАДИОПРОТЕКТОРНЫЙ, ФЕРВОПРОТЕКТОРНЫЙ, АКТОПРОТЕКТОРНЫЙ ПРЕПАРАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2195950C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2372934C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2637414C1 |
| НАСТОЙКА ЭХИНАЦЕИ ПУРПУРНОЙ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2014 |
|
RU2552919C2 |
| ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО | 2002 |
|
RU2210380C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОМЕТАСТАТИЧЕСКОЙ АКТИВНОСТЬЮ | 2001 |
|
RU2189832C1 |
| Способ получения настойки листьев дуба черешчатого, обладающей антимикробной активностью | 2021 |
|
RU2781430C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГУСТОГО ЭКСТРАКТА НА ОСНОВЕ ПЛОДОВ ЛАБАЗНИКА ВЯЗОЛИСТНОГО, ОБЛАДАЮЩЕГО АНТИДЕПРЕССАНТНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2726794C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГИПОГЛИКЕМИЧЕСКОЙ И ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2506091C1 |

Изобретение относится к фармацевтической промышленности, а именно к противовоспалительному средству. Противовоспалительное средство, представляющее собой настойку из высушенной и измельченной надземной части копеечника кустарникового, полученную методом перколяции с использованием в качестве экстрагента 70% этилового спирта, при соотношении сырье : экстрагент 1:10, при этом на стадии намачивания 10 г сырья заливают 11,29 мл 70%-го этилового спирта. Полученное средство выдерживает испытания на острую токсичность, обладает высоким противовоспалительным действием. 6 ил.
Противовоспалительное средство, представляющее собой настойку из высушенной и измельченной надземной части копеечника кустарникового, полученную методом перколяции с использованием в качестве экстрагента 70% этилового спирта, при соотношении сырье:экстрагент 1:10, при этом на стадии намачивания 10 г сырья заливают 11,29 мл 70% этилового спирта.
| CN 104127751 A, 05.11.2014 | |||
| CN 103709266 A, 09.04.2014 | |||
| РАСТИТЕЛЬНЫЙ СБОР "АНАСТАСИЯ" | 2006 |
|
RU2371194C2 |
| WO 2005063273 A1, 17.12.2008 | |||
| УСТРОЙСТВО ДЛЯ ЗАКРЕПЛЕНИЯ ШТУЧНЫХ ЗАГОТОВОК С БАЗИРОВАНИЕМ ИХ ПО ЦЕНТРАЛЬНОМУ ОСЕВОМУ ОТВЕРСТИЮ | 2009 |
|
RU2411114C2 |
Авторы
Даты
2018-05-22—Публикация
2017-04-26—Подача