Изобретение относится к медицине, биотехнологии и пищевой промышленности, в частности к созданию функциональных продуктов питания для реабилитации онкологических больных на основе симбиотических консорциумов пробиотических бактерий и биологически активных пептидов.
Питание является очень важной составляющей здоровья человека. У больного с онкологическим заболеванием в организме происходят изменения метаболических процессов, поэтому ему требуется особый питательный рацион.
Онкологические пациенты нуждаются в повышенном потреблении белковой пищи. Имеющиеся на сегодняшний день данные свидетельствуют о том, что пептидная диета наиболее эффективно поддерживает работу печени и, следовательно, способствует синтезу белков. Биологически активные пептиды, используемые в качестве пребиотиков, представляют собой короткие цепочки из аминокислот и обладают иммуномодифицирующими и противоопухолевыми свойствами.
Систематическое употребление пробиотиков в питании стимулирует иммунную систему организма, подавляет патогенную и условно-патогенную микрофлору, оказывает противоопухолевый и другие положительные эффекты на организм человека.
На сегодняшний день созданию новых функциональных продуктов питания для обеспечения населения необходимыми полезными веществами, придающими им лечебные и профилактические свойства, уделяется особое внимание.
Так, известен пищевой лечебно-профилактический функциональный продукт (RU, патент 2453132, опубл. 20.06.2012), обладающий иммуномодулирующим действием. Получение пищевого функционального продукта заключается в смешивании в следующем соотношении исходных компонентов, мас. %: растительных фосфолипидов - 6,00; витамина Е - 0,40; β-каротина - 0,10 и отдельно аскорбиновой кислоты - 2,50; витамина В1 - 0,06; витамина В2 - 0,04; витамина В6 - 0,10; сульфата железа - 0,05; сухого водорастворимого экстракта шиповника - 45,00; сухого водорастворимого экстракта корня солодки голой - 43,75; заменителя сахара - 2,00.
Недостатком известного продукта являются недостаточно высокие иммуномодулирующие свойства.
Известен продукт детского питания для иммуномодулирующего эффекта (RU, патент 2402226, опубл. 27.10.2010). Основу иммуномодулирующей леденцовой карамели составляет экстракт из слоевища лишайника семейства пармелиевых Xanthoparmelia camtschadalis - 67%, к которому добавлены, сахар-песок - 22%, патока - 10%, лимонная кислота - 0,7%, эссенция - 0,3%.
Недостатком известного продукта следует признать использование редкого сырья - экстракта из слоевища лишайника семейства пармелиевых Xanthoparmelia camtschadalis.
Известно мороженое (RU, патент 2294647, опубл. 10.03.2007) с повышенными пробиотическими, профилактическими и биологическими свойствами. В состав мороженого помимо молока, сливок, сахара-песка, стабилизатора, также вносят бакконцентрат, который включает культуры микроорганизмов Bifidobacterium longum В 379 М, Lactobacillus acidophilus 97, Propionibacterium shermanii 12 AE, в соотношении 1:1:1.
Недостатком данного продукта можно считать невысокую пищевую и биологическую ценность.
Известен жидкий ферментированный и пастеризованный натуральный продукт (RU, патент 2452243, опубл. 10.06.2012), изготовленный на основе фруктов, овощей, бобовых, трав и/или орехов и содержащий живые пробиотические микроорганизмы в количестве от 105 до 1015 клеток/мл и неживые пробиотические микроорганизмы. Микроорганизмы находятся в натуральном продукте в виде смеси бактерий Lactobacillus rhamnosus с другими пробиотическими микроорганизмами.
Основной недостаток продукта заключается в том, что, несмотря на относительно широкий спектр действия, он недостаточно эффективен к иммуностимулирующим механизмам в организме.
Известен штамм Bifidobacterium longum infantis для приготовления пробиотика (RU, патент 2308483, опубл. 20.10.2007), выделенный из иссеченного и промытого желудочно-кишечного тракта человека. Препарат с данным штаммом может применяться при профилактике или лечении нежелательной воспалительной активности. Штамм Bifidobacterium оказывает существенное противовоспалительное действие после перорального потребления и вызывает изменения в иммунологическом маркере при введении в систему, содержащую клетки, которые взаимодействуют с иммунной системой. А также предложен препарат (RU, патент 2308483, опубл. 20.10.2007), содержащий штамм Bifidobacterium, который может включать другой пробиотический материал - Lactobacillus salivarius, выделенный из иссеченного и промытого желудочно-кишечного тракта человека.
Недостатком известных препаратов можно считать узкий спектр действия предлагаемого штамма.
Предложена фармацевтическая композиция (RU, патент 2362579, опубл. 27.07.2009), обладающая противоопухолевым действием, содержащая в качестве действующего вещества эффективное количество пептида глутамил-аспартил-глицин формулы: H-Glu-Asp-Gly-OH и фармацевтически приемлемый носитель. Пептид получают классическим методом пептидного синтеза в растворе.
Недостатком предложенной композиции следует признать трудоемкость процедуры получения биопептида.
Предлагается пептид структуры Tyr-Ser-Leu (RU, патент 2305107, опубл. 27.08.2007), характеризующийся аминокислотной
последовательностью SEQ ID No: 16, и фармацевтическая композиция на его основе для стимулирования противоопухолевого иммунного ответа. Фармацевтическая композиция состоит из эффективного количества пептида и фармацевтически приемлемого носителя.
Недостатком известной композиции являются недостаточно высокие противоопухолевые свойства.
Известен лекарственный препарат (RU, заявка 94040451, опубл. 20.09.1996), содержащий живую культуру молочнокислых бактерий Streptococcus faecium 3185-М ВКПМ В-3491 и Streptococcus faecium М ВКПМ В-3490, производимые в виде сухого концентрата монокультур и смешиваемые в соотношении 0,6…1,4:0,6…1,4 по количеству жизнеспособных клеток. Предлагаемый лекарственный препарат обладает высокой биологической активностью, в том числе иммуностимулирующей способностью и способностью к подавлению патогенной и условно-патогенной микрофлоры.
Недостатком предлагаемого препарата является ограниченный видовой состав микроорганизмов.
В ходе проведения патентного поиска не выявлено техническое решение, которое может быть признано ближайшим аналогом.
Техническая задача, решаемая использованием разработанного способа, состоит в расширении ассортимента продуктов питания функционального назначения для онкологических больных в период реабилитации.
Технический результат, достигаемый при реализации разработанного способа, состоит в получении функционального продукта питания для реабилитации онкологических больных, состоящего из пробиотических бактерий - представителей нормальной кишечной микрофлоры человека и биологически активных пептидов, выделенных из белков молока, с выраженными противоопухолевыми, антиоксидантными и иммуномодулирующими свойствами.
Для достижения указанного технического результата предложено использовать разработанный способ получения функционального продукта питания для реабилитации онкологических больных, согласно которому сначала проводят выделение биологически активных пептидов из белков молока путем внесения в него фосфатов, пастеризацию при температуре 74±2°С с выдержкой 15-20 секунд с целью уничтожения микроорганизмов, содержащихся в казеине, охлаждения до температуры 37+2°С, внесения энзиматической системы, и дальнейшего выделения и очистки биологически активных пептидов посредством ультрафильтрации, препаративного электрофореза и обращенно-фазовой высокоэффективной жидкостной хроматографии. Для достижения необходимой консистенции биологически активных пептидов их сгущают на вакуум-выпарной установке до массовой доли сухих веществ от 40 до 45% и проводят распылительную сушку с температурой воздуха на входе 175±5°С, на выходе 90±5°С.
С целью получения консорциума пробиотических бактерий проводят первичное выделение бактерий из фекалий человека, их культивирование на жидкой питательной среде в анаэробных условиях при Т=37,0±2,0°С, рН 7,2±0,2 в течение 12,0 ч, с последующим центрифугированием и лиофилизацией. Далее проводят смешивание компонентов функционального продукта (консорциум пробиотических бактерий и биологически активный пептид), готовый продукт фасуют и упаковывают.
Разработанный способ реализуют следующим образом.
Выделение биологически активных пептидов осуществляют из белков молока. Проводят приемку сырья и оценку его качества (показатели качества и безопасности сырого молока должны соответствовать требованиям, установленным в Техническом регламенте Таможенного союза «О безопасности молока и молочной продукции» TP ТС 033/2013, принятом решением Совета Евразийской экономической комиссии от 9 октября 2013 года №67). Вносят фосфорнокислый натрий (35%-ный раствор) до достижения рН молока 7,5 и проводят пастеризацию при температуре 74±2°С с выдержкой 15-20 секунд с целью уничтожения микроорганизмов, содержащихся в казеине, охлаждают до температуры 37+2°С, вносят энзиматическою систему, включающую трипсин, химотрипсин и термолизин в соотношении 1:1:1.
Ферментативный гидролиз ведут при температуре 37+2°С в течение 8,00±0,05 ч при рН 7,5±0,1, фермент-субстратное соотношение 1:50. С целью инактивации комплекса ферментов и удаления патогенной микрофлоры полученный гидролизат подогревают до 95±2°С в течение 30 с.
Выделение и очистку биологически активных пептидов осуществляют путем последовательных стадий ультрафильтрации, препаративного электрофореза и обращенно-фазовой высокоэффективной жидкостной хроматографии. На первой стадии очистки ферментативные гидролизаты казеина подвергают ультрафильтрации с использованием мембран с диаметром пор 10 и 15 кДа при рН 6,0-6,5. Полученный материал, содержащий пептиды и низкомолекулярные белки с молекулярными массами менее 10-12 кДа, наносят на электрофоретическую колонку (предварительно добавив в пробу мочевину до концентрации 3 М) для разделения белков с помощью препаративного электрофореза.
Препаративный электрофорез при непрерывной элюции белков проводят в 12,5%-ном полиакриламидном геле в кислой буферной системе в присутствии мочевины. Элюированные с колонки белковые фракции анализируют с помощью аналитического электрофореза в присутствии додецилсульфата натрия. Содержащиеся в белковых фракциях пептиды разделяют с помощью нескольких последовательных циклов обращенно-фазовой высокоэффективной жидкостной хроматографии, элюируя пептиды в градиенте концентраций ацетонитрила с использованием различных противоионов, при скорости потока 0,8 мл/мин.
Для достижения необходимой консистенции биологически активных пептидов их сгущают на вакуум-выпарной установке до массовой доли сухих веществ от 40 до 45% и сушат в распылительной сушилке с температурой воздуха на входе 175±5°С, на выходе 90±5°С.
Источником выделения пробиотических бактерий являются фекалии взрослого здорового субъекта, который в течение 3 месяцев перед выделением не принимает ни антибиотические, ни пробиотические препараты.
Подготовку содержимого кишечника проводят следующим образом: 1 г фекалий вносят в 9 мл стерильного изотонического раствора хлорида натрия (NaCl) и тщательно суспендируют путем встряхивания в течение 20-30 минут. Затем отстаивают и через 1 час из надосадочной жидкости готовят разведения в изотоническом растворе хлорида натрия 102, 103, 104, 105. Из разведений 103, 104, 105 делают посев бактериологической петлей на питательные среды.
Для первичного выделения бактерий родов Bifidobacterium, Lactobacillus, Streptococcus и Enterococcus используют бифидум-среду, среду МРС, селективный агар для стрептококков, среду Сланец-Бартли для энтерококков. Культивирование бактерий осуществляют на агаризованных питательных средах в анаэробном режиме при температуре 37°С в течение 24,0 часов. С суммарных газонов на чашках Петри с видимым ростом микроорганизмов проводят истощающие рассевы. Выделенные микроорганизмы культивируют в жидких питательных средах в анаэробном режиме при температуре 37°С в течение 1,20-24,0 часов до достижения концентрации микроорганизмов 1,0⋅108 КОЕ/мл.
По окончании культивирования биомассу отделяют от культуральной жидкости центрифугированием при 8000 об/мин в течение 20 минут.
Культуры микроорганизмов, выделенных из желудочно-кишечного тракта человека, хранятся в сублимационно-высушенном состоянии в ампулах при температуре 4±2°С не менее 24 месяцев. Параметры сублимационной сушки: температура замораживания в защитной среде, содержащей 5% глицерина, -25°С при продолжительности 90 минут; температура сушки 30°С; продолжительность сушки 6 часов; тепловая нагрузка 5,45 кВт/м2; остаточное давление 0,6-0,8 кПа, толщина слоя сушки - 2 мм.
Лиофилизированные культуры микроорганизмов, выделенных из желудочно-кишечного тракта человека, восстанавливают путем переноса содержимого ампул в определенном соотношении в пробирки с питательными средами, соответствующими культивированию консорциумов пробиотических бактерий.
Для получения функционального продукта питания проводят смешивание компонентов в соответствии с рецептурой: консорциум пробиотических бактерий + биологически активный пептид.
Изобретение иллюстрируется следующими примерами.
Пример 1
Для получения биологически активных пептидов при температуре 37+2°С, рН 7,5±0,1 и фермент-субстратном соотношении 1:50 проводят ферментативный гидролиз подготовленного молока энзиматической системой, включающей трипсин, химотрипсин и термолизин в течение 8,00±0,05 ч. Полученный гидролизат подогревают до 95±2°С в течение 30 с.
Для очистки ферментативные гидролизаты казеина подвергаются ультрафильтрации с использованием мембран с диаметром пор 10 и 15 кДа при рН 6,0-6,5. Полученный материал наносят на электрофоретическую колонку. Препаративный электрофорез при непрерывной элюции белков проводят в 12,5%-ном полиакриламидном геле в кислой буферной системе в присутствии мочевины. Элюированные с колонки белковые фракции анализируют с помощью аналитического электрофореза в присутствии додецилсульфата натрия. Содержащиеся в белковых фракциях пептиды Leu-Leu-Tyr и Trp-Tre-Ala-Glu-Glu-Lys-Glu-Leu разделяют с помощью нескольких последовательных циклов обращенно-фазовой высокоэффективной жидкостной хроматографии, элюируя пептиды в градиенте концентраций ацетонитрила с использованием различных противоионов, при скорости потока 0,8 мл/мин.
Полученные биологически активные пептиды сгущают на вакуум-выпарной установке до массовой доли сухих веществ от 40 до 45% и сушат в распылительной сушилке с температурой воздуха на входе 175±5°С, на выходе - 90±5°С.
Для получения консорциума пробиотических бактерий лиофилизированные культуры, выделенные из желудочно-кишечного тракта человека, восстанавливают путем переноса содержимого ампул с бактериями видов Bifidobacterium bifidum, Bifidobacterium breve, Lactobacillus plantarum, Lactobacillus acidophilus, Lactobacillus rhamnosus, Lactobacillus paracasei (соотношение 1:1:1:1:1:1) в чашку Петри с питательной средой состава, г/л: дрожжевой экстракт - 5,0; папаиновый перевар соевой муки - 10,0; натрия гидрофосфат - 1,0; Твин-80 - 0,2; аммония цитрат - 1,0; цистеина гидрохлорид - 0,5; магния хлорид - 0,5; кислота аскорбиновая - 0,5; глюкоза - 10,0; мясной экстракт - 20,0; марганца сульфат - 0,05; натрия азид - 0,2; агар-агар - 15,0. Посевы инкубируют при температуре 37,0±2,0°С, рН 6,8±0,2 в течение 12,0 ч.
По окончании культивирования консорциум пробиотических бактерий подвергают сублимационной сушке при следующих параметрах: температура замораживания в защитной среде, содержащей 5% глицерина, -25°С при продолжительности 90 минут; температура сушки 30°С; продолжительность сушки 6 часов; тепловая нагрузка 5,45 кВт/м2; остаточное давление 0,6-0,8 кПа, толщина слоя сушки - 2 мм.
Для получения функционального продукта питания проводят смешивание консорциума пробиотических бактерий и биологически активных пептидов в соответствии с рецептурой, мас. %:
консорциум пробиотических бактерий - 25,0;
пептид Leu-Leu-Tyr - 37,5;
пептид Trp-Tre-Ala-Glu-Glu-Lys-Glu-Leu - 37,5.
Для полученного функционального продукта питания в экспериментах in vitro и in vivo определяли противоопухолевые, антиоксидантные и иммуномодулирующие свойства.
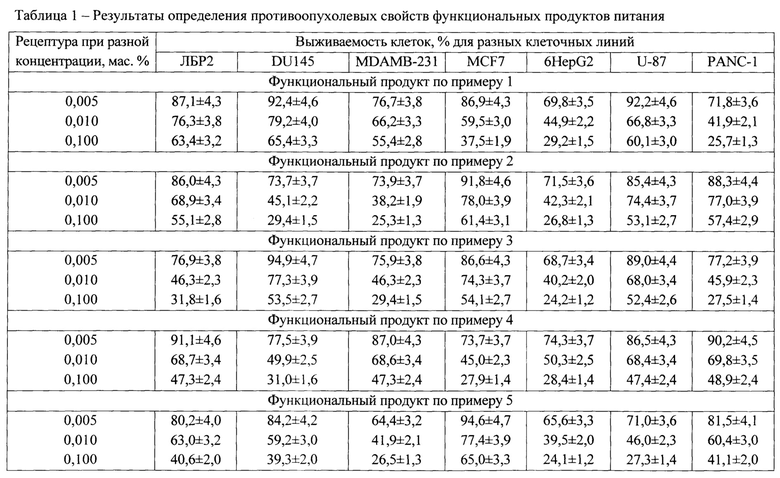
Результаты определения противоопухолевых свойств функционального продукта питания представлены в таблице 1.
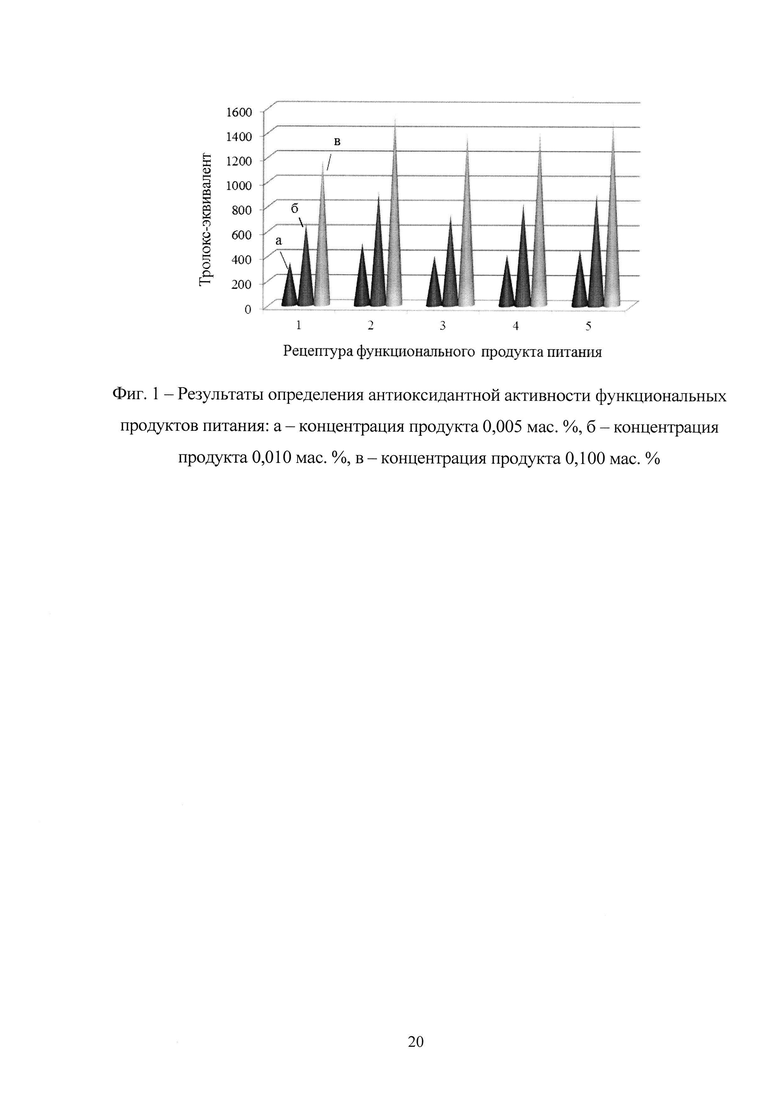
Результаты определения антиоксидантных свойств функционального продукта питания представлены на фиг. 1.
Результаты оценки влияния функционального продукта питания на гуморальный иммунный ответ представлены в таблице 2.
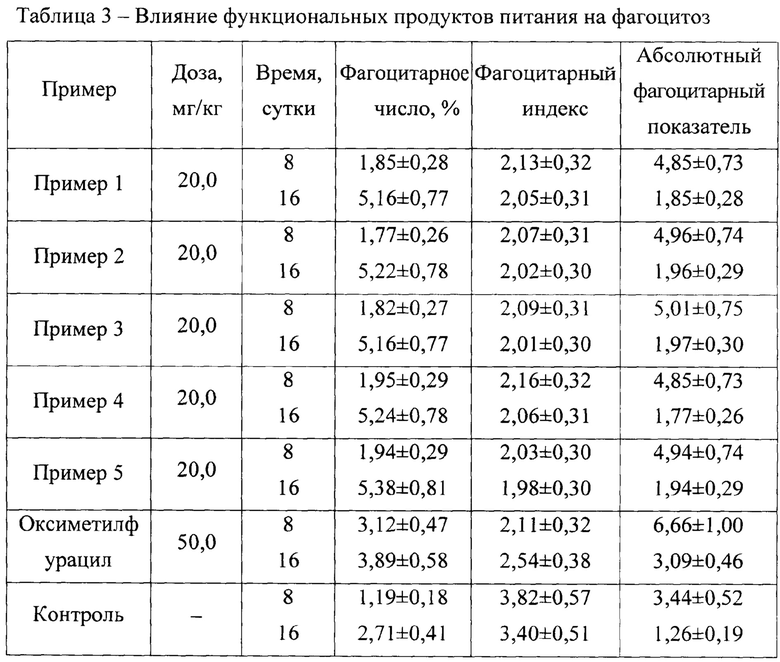
Результаты оценки влияния функционального продукта питания на фагоцитоз представлены в таблице в таблице 3.
Пример 2
Биологически активные пептиды из белков молока выделяют аналогично примеру 1.
Содержащиеся в белковых фракциях пептиды Tre-Gly-Glu-Asn-His-Asp и Lys-Val-Leu-Pro-Val-Pro-Glu разделяют с помощью нескольких последовательных циклов обращенно-фазовой высокоэффективной жидкостной хроматографии, элюируя пептиды в градиенте концентраций ацетонитрила с использованием различных противоионов, при скорости потока 0,8 мл/мин.
Полученные биологически активные пептиды сгущают и подвергают распылительной сушке при параметрах, указанных в примере 1.
Для получения консорциума пробиотических бактерий лиофилизированные культуры, выделенные из желудочно-кишечного тракта человека, восстанавливают путем переноса содержимого ампул с бактериями видов Bifidobacterium breve, Lactobacillus fermentum, Lactobacillus plantarum, Lactobacillus acidophilus, Lactobacillus salivarius, Streptococcus agalactiae, Lactobacillus paracasei, Lactobacillus casei (соотношение 1:1:1:1:1:1:1:1) в чашку Петри с питательной средой состава, г/л: протеозопептон - 15,0; папаиновый перевар соевой муки - 10,0; натрия гидрофосфат - 1,5; Твин-80 - 1,0; аммония цитрат - 2,0; цистеина гидрохлорид - 1,0; магния хлорид - 0,5; кислота аскорбиновая - 0,2; натрия хлорид - 2,5; глюкоза - 10,0; мясной экстракт - 10,0; натрия азид - 0,2; агар-агар - 15,0. Посевы инкубируют при температуре 37,0±2,0°С, рН 7,0±0,2 в течение 12,0 ч.
По окончании культивирования консорциум пробиотических бактерий подвергают сублимационной сушке при параметрах, указанных в примере 1.
Для получения функционального продукта питания проводят смешивание консорциума пробиотических бактерий и биологически активных пептидов в соответствии с рецептурой, мас. %:
консорциум пробиотических бактерий - 50,0;
пептид Tre-Gly-Glu-Asn-His-Asp - 25,0;
пептид Lys-Val-Leu-Pro-Val-Pro-Glu - 25,0.
Для полученного функционального продукта питания в экспериментах in vitro и in vivo определяли противоопухолевые, антиоксидантные и иммуномодулирующие свойства.
Результаты определения противоопухолевых свойств функционального продукта питания представлены в таблице 1.
Результаты определения антиоксидантных свойств функционального продукта питания представлены на фиг. 1.
Результаты оценки влияния функционального продукта питания на гуморальный иммунный ответ представлены в таблице 2.
Результаты оценки влияния функционального продукта питания на фагоцитоз представлены в таблице в таблице 3.
Пример 3
Биологически активные пептиды из белков молока выделяют аналогично примеру 1.
Содержащиеся в белковых фракциях пептиды Lys-Glu-Asn и Leu-Leu-Tyr-Glu-Glu-Pro-Val-Leu-Gly-Pro-Val-Gly-Pro-Pro-Pro-Ile-Ile-Val разделяют с помощью нескольких последовательных циклов обращенно-фазовой высокоэффективной жидкостной хроматографии, элюируя пептиды в градиенте концентраций ацетонитрила с использованием различных противоионов, при скорости потока 0,8 мл/мин.
Полученные биологически активные пептиды сгущают и подвергают распылительной сушке при параметрах, указанных в примере 1.
Для получения консорциума пробиотических бактерий лиофилизированные культуры, выделенные из желудочно-кишечного тракта человека, восстанавливают путем переноса содержимого ампул с бактериями видов Lactobacillus fermentum, Lactobacillus plantarum, Lactobacillus acidophilus, Lactobacillus salivarius, Streptococcus agalactiae, Lactobacillus rhamnosus, Lactobacillus paracasei (соотношение 1:1:1:1:1:1:1) в чашку Петри с питательной средой состава, г/л: дрожжевой экстракт - 5,0; протеозопептон - 3,0; панкреатический гидролизат казеина - 25,0; папаиновый перевар соевой муки - 7,5; натрия гидрофосфат - 2,0; лактоза - 2,0; аммония цитрат -2,0; цистеина гидрохлорид - 0,5; магния хлорид - 0,5; кислота аскорбиновая - 0,2; натрия хлорид - 4,0; глюкоза - 5,0; мясной экстракт - 15,0; марганца сульфат - 0,02; натрия азид - 0,1; агар-агар - 15,0. Посевы инкубируют при температуре 37,0±2,0°С, рН 7,0±0,2 в течение 12,0 ч.
По окончании культивирования консорциум пробиотических бактерий подвергают сублимационной сушке при параметрах, указанных в примере 1.
Для получения функционального продукта питания проводят смешивание консорциума пробиотических бактерий и биологически активных пептидов в соответствии с рецептурой, мас. %:
консорциум пробиотических бактерий - 50,0;
пептид Lys-Glu-Asn - 25,0;
пептид Leu-Leu-Tyr-Glu-Glu-Pro-Val-Leu-Gly-Pro-Val-Gly-Pro-Pro-Pro-Ile-Ile-Val - 25,0.
Для полученного функционального продукта питания в экспериментах in vitro и in vivo определяли противоопухолевые, антиоксидантные и иммуномодулирующие свойства.
Результаты определения противоопухолевых свойств функционального продукта питания представлены в таблице 1.
Результаты определения антиоксидантных свойств функционального продукта питания представлены на фиг. 1.
Результаты оценки влияния функционального продукта питания на гуморальный иммунный ответ представлены в таблице 2.
Результаты оценки влияния функционального продукта питания на фагоцитоз представлены в таблице 3.
Пример 4
Биологически активные пептиды из белков молока выделяют аналогично примеру 1.
Содержащиеся в белковых фракциях пептиды Tyr-Pro-Pro-Pro-Gly-Pro-Ile и Lys-Val-Leu-Pro-Val-Pro-Glu разделяют с помощью нескольких последовательных циклов обращенно-фазовой высокоэффективной жидкостной хроматографии, элюируя пептиды в градиенте концентраций ацетонитрила с использованием различных противоионов, при скорости потока 0,8 мл/мин.
Полученные биологически активные пептиды сгущают и подвергают распылительной сушке при параметрах, указанных в примере 1.
Для получения консорциума пробиотических бактерий лиофилизированные культуры, выделенные из желудочно-кишечного тракта человека, восстанавливают путем переноса содержимого ампул с бактериями видов Bifidobacteriu longum, Bifidobacterium bifidum, Lactobacillus salivarius, Streptococcus agalactiae, Bifidobacterium adolescentis, Lactobacillus paracasei (соотношение 1:1:1:1:1:1) в чашку Петри с питательной средой состава, г/л: дрожжевой экстракт - 5,0; панкреатический гидролизат казеина - 30,0; папаиновый перевар соевой муки - 5,0; натрия гидрофосфат - 1,0; Твин-80 - 1,0; лактоза - 2,5; аммония цитрат - 2,0; цистеина гидрохлорид - 1,0; магния хлорид - 0,5; кислота аскорбиновая - 0,5; натрия ацетат - 0,3; натрия хлорид - 2,0; глюкоза - 7,5; мясной экстракт - 10,0; марганца сульфат - 0,05; натрия азид - 0,2; агар-агар - 12,0. Посевы инкубируют при температуре 37,0±2,0°С, рН 7,2±0,2 в течение 12,0 ч.
По окончании культивирования консорциум пробиотических бактерий подвергают сублимационной сушке при параметрах, указанных в примере 1.
Для получения функционального продукта питания проводят смешивание консорциума пробиотических бактерий и биологически активных пептидов в соответствии с рецептурой, мас. %:
консорциум пробиотических бактерий - 30,0;
пептид Tyr-Pro-Pro-Pro-Gly-Pro-Ile - 35,0;
пептид Lys-Val-Leu-Pro-Val-Pro-Glu - 35,0.
Для полученного функционального продукта питания в экспериментах in vitro и in vivo определяли противоопухолевые, антиоксидантные и иммуномодулирующие свойства.
Результаты определения противоопухолевых свойств функционального продукта питания представлены в таблице 1.
Результаты определения антиоксидантных свойств функционального продукта питания представлены на фиг. 1.
Результаты оценки влияния функционального продукта питания на гуморальный иммунный ответ представлены в таблице 2.
Результаты оценки влияния функционального продукта питания на фагоцитоз представлены в таблице в таблице 3.
Пример 5
Биологически активные пептиды из белков молока выделяют аналогично примеру 1.
Содержащиеся в белковых фракциях пептиды Lys-Glu и Tre-Gly-Glu-Asn-His-Asp разделяют с помощью нескольких последовательных циклов обращенно-фазовой высокоэффективной жидкостной хроматографии, элюируя пептиды в градиенте концентраций ацетонитрила с использованием различных противоионов, при скорости потока 0,8 мл/мин.
Полученные биологически активные пептиды сгущают и подвергают распылительной сушке при параметрах, указанных в примере 1.
Для получения консорциума пробиотических бактерий лиофилизированные культуры, выделенные из желудочно-кишечного тракта человека, восстанавливают путем переноса содержимого ампул с бактериями видов Lactobacillus reuteri, Bifidobacterium bifidum, Lactobacillus fermentum, Lactobacillus plantarum, Lactobacillus salivarius, Streptococcus agalactiae, Enterococcus faecium (соотношение 1:1:1:1:1:1:1) в чашку Петри с питательной средой состава, г/л: дрожжевой экстракт - 10,0; панкреатический гидролизат казеина - 20,0; натрия гидрофосфат - 2,5; Твин-80 - 0,7; лактоза - 5,0; аммония цитрат - 0,5; цистеина гидрохлорид - 1,0; магния хлорид - 1,0; кислота аскорбиновая - 0,1; натрия ацетат - 0,2; натрия хлорид - 3,0; глюкоза - 5,0; мясной экстракт - 15,0; марганца сульфат - 0,1; натрия азид - 0,2; агар-агар - 12,0. Посевы инкубируют при температуре 37,0±2,0°С, рН 7,0±0,2 в течение 12,0 ч.
По окончании культивирования консорциум пробиотических бактерий подвергают сублимационной сушке при параметрах, указанных в примере 1.
Для получения функционального продукта питания проводят смешивание консорциума пробиотических бактерий и биологически активных пептидов в соответствии с рецептурой, мас. %:
консорциум пробиотических бактерий - 30,0;
пептид Lys-Glu - 35,0;
пептид Tre-Gly-Glu-Asn-His-Asp - 35,0.
Для полученного функционального продукта питания в экспериментах in vitro и in vivo определяли противоопухолевые, антиоксидантные и иммуномодулирующие свойства.
Результаты определения противоопухолевых свойств функционального продукта питания представлены в таблице 1.
Результаты определения антиоксидантных свойств функционального продукта питания представлены на фиг. 1.
Результаты оценки влияния функционального продукта питания на гуморальный иммунный ответ представлены в таблице 2.
Результаты оценки влияния функционального продукта питания на фагоцитоз представлены в таблице в таблице 3.
Из таблицы 1 следует, что функциональные продукты питания на основе консорциумов пробиотических бактерий и биологически активных пептидов, полученные в соответствии с описанными примерами, характеризуются противоопухолевой активностью по отношению к тестируемым клеточным линиям: лимфомы Беркитта ЛБР2, рака предстательной железы человека DU 145, рака молочной железы человека MDAMB-231 и MCF7, гепатоцеллюлярной карциномы HepG2, рака головного мозга U-87, рака поджелудочной железы человека PANC-1.
Данные фиг.1 свидетельствуют о том, что функциональные продукты питания на основе консорциумов пробиотических бактерий и биологически активных пептидов, полученные в соответствии с описанными примерами, характеризуются выраженными антиоксидантными свойствами (величина тролокс-эквивалента/109 клеток находится в диапазоне от 345 до 1488). При этом максимальная антиоксидантная активность обнаружена у функционального продукта, приготовленного по примеру 2 (от 500 до 1545).
Из таблицы 2 видно, что все функциональные продукты питания на основе консорциумов пробиотических бактерий и биологически активных пептидов, полученные в соответствии с описанными примерами, вызывают увеличение антителообразующих клеток в селезенке крыс в 1,26-1,33 раз по сравнению с контролем. В пересчете на 1 млн спленоцитов исследуемые функциональные продукты питания стимулируют антителогенез. Кроме того, из таблицы 2 видно, что исследуемые продукты ослабляют гиперчувствительностью замедленного типа к эритроцитам барана, что может объясняться наличием у разработанных продуктов противовоспалительного эффекта.
Из таблицы 3 следует, что при введении лабораторным животным функциональных продуктов питания на основе консорциумов пробиотических бактерий и биологически активных пептидов, полученных в соответствии с описанными примерами, в течение 16 дней наблюдается увеличение числа фагоцитирующих клеток (3,89-5,38%) по сравнению с контролем (2,71%). Активность фагоцитов у животных, получавших исследуемые продукты, аналогична фагоцитарному индексу животных, которым вводят оксиметилурацил (2,02 и 2,54, соответственно). На основании анализа абсолютного фагоцитарного показателя установлено, что все изучаемые функциональные продукты питания обладают способностью стимулировать фагоцитоз.
Таким образом, установлено, что разработанные продукты на основе консорциумов пробиотических бактерий и биологически активных пептидов, характеризуются выраженными противоопухолевыми, антиоксидантными и иммуномодулирующими свойствами, что позволяет использовать их в качестве функционального питания в восстановительной терапии онкологических больных.
Получены предварительные результаты клинических исследований, свидетельствующие о том, что включение в рацион питания больных колоректальным раком функциональных продуктов питания на основе консорциумов пробиотических бактерий и биологически активных пептидов, выделенных из белков молока, полученных в соответствии с примерами 1-5, приводит к положительной динамике в бактериальном составе микрофлоры желудочно-кишечного тракта у онкологических больных, что выражается в увеличении количества полезной микрофлоры (бифидобактерий, лактобактерий, молочнокислых бактерий, энтерококков, эшерихий с нормальной ферментацией) и уменьшении содержания условно-патогенных бактерий (Klebsiella pneumoniae, Enterobacter spp., Proteus spp., Staphylococcus aureus, Pseudomonas aeruginosa, Acinetobacter, Clostridium).

| название | год | авторы | номер документа |
|---|---|---|---|
| ФЕРМЕНТЫ ЛАКТАЗЫ С УЛУЧШЕННЫМИ СВОЙСТВАМИ | 2018 |
|
RU2788608C2 |
| Ферменты лактазы с улучшенными свойствами | 2018 |
|
RU2806709C2 |
| Ферменты лактазы с улучшенными свойствами при кислом pH | 2019 |
|
RU2814542C2 |
| ХЛОРИД-ИНДУЦИРУЕМАЯ ПРОКАРИОТИЧЕСКАЯ СИСТЕМА ЭКСПРЕССИИ | 2019 |
|
RU2812766C2 |
| МОДИФИЦИРОВАННЫЕ ГРАМПОЛОЖИТЕЛЬНЫЕ БАКТЕРИИ И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2773435C2 |
| САХАРОЗООТРИЦАТЕЛЬНЫЙ ШТАММ STREPTOCOCCUS THERMOPHILUS ДЛЯ ПРИМЕНЕНИЯ ПРИ ПРИГОТОВЛЕНИИ ФЕРМЕНТИРОВАННЫХ ПРОДУКТОВ | 2020 |
|
RU2839701C1 |
| МУКОАДГЕЗИВНЫЙ МИКРООРГАНИЗМ | 2017 |
|
RU2762940C2 |
| Ферменты лактазы с улучшенной активностью при низких температурах | 2018 |
|
RU2800427C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА 1 ТИПА | 2017 |
|
RU2760997C2 |
| ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫЕ БАКТЕРИИ, СТАБИЛЬНО ЭКСПРЕССИРУЮЩИЕ ИЛ-10 И ИНСУЛИН | 2017 |
|
RU2768027C2 |
Изобретение относится к пищевой промышленности, в частности к созданию функциональных продуктов питания на основе симбиотических консорциумов пробиотических бактерий и биологически активных пептидов для реабилитации онкологических больных. Способ получения функционального продукта питания для реабилитации онкологических больных включает получение биологически активных пептидов из белков молока, а также консорциума пробиотических бактерий, выделенных из желудочно-кишечного тракта человека, с последующим смешиванием компонентов функционального продукта питания. При этом процесс получения биологически активных пептидов из белков молока осуществляют согласно схеме, включающей следующие операции: приемка, оценка качества, подготовка сырья, внесение фосфатов, растворение казеина, доведение рН до 7,5, пастеризация при температуре 74±2°С с выдержкой 15-20 с с целью уничтожения микроорганизмов, содержащихся в казеине, охлаждение до температуры 37±2°С, внесение энзиматической системы, включающей трипсин, химотрипсин и термолизин. Далее осуществляют последовательные стадии выделения и очистки биологически активных пептидов путем ультрафильтрации, препаративного электрофореза и обращенно-фазовой высокоэффективной жидкостной хроматографии. Затем для достижения необходимой консистенции биологически активных пептидов их сгущают на вакуум-выпарной установке до массовой доли сухих веществ от 40 до 45%. Изобретение позволяет получить функциональный продукт питания для реабилитации онкологических больных, обладающий выраженными противоопухолевыми, антиоксидантными и иммуномодулирующими свойствами. 5 з.п. ф-лы, 1 ил., 3 табл., 5 пр.
1. Способ получения функционального продукта питания для реабилитации онкологических больных, характеризующийся тем, что получают биологически активные пептиды из белков молока, получают консорциум пробиотических бактерий, выделенных из желудочно-кишечного тракта человека с последующим смешиванием компонентов функционального продукта питания, при этом процесс получения биологически активных пептидов из белков молока осуществляют согласно схеме, включающей следующие операции: приемка, оценка качества, подготовка сырья, внесение фосфатов, растворение казеина, доведение рН до 7,5, пастеризация при температуре 74±2°С с выдержкой 15-20с с целью уничтожения микроорганизмов, содержащихся в казеине, охлаждение до температуры 37±2°С, внесение энзиматической системы, включающей трипсин, химотрипсин и термолизин, далее осуществляют последовательные стадии выделения и очистки биологически активных пептидов путем ультрафильтрации, препаративного электрофореза и обращенно-фазовой высокоэффективной жидкостной хроматографии, затем для достижения необходимой консистенции биологически активных пептидов их сгущают на вакуум-выпарной установке до массовой доли сухих веществ от 40 до 45%.
2. Способ получения функционального продукта питания для реабилитации онкологических больных по п. 1, отличающийся тем, что для его получения используют следующие компоненты в определенном соотношении, мас. %:
консорциум пробиотических бактерий Bifidobacterium bifidum, Bifidobacterium breve, Lactobacillus plantarum, Lactobacillus acidophilus, Lactobacillus rhamnosus, Lactobacillus paracasei (соотношение 1:1:1:1:1:1) - 25,0;
пептид Leu-Leu-Tyr - 37,5;
пептид Trp-Tre-Ala-Glu-Glu-Lys-Glu-Leu - 37,5.
3. Способ получения функционального продукта питания для реабилитации онкологических больных по п. 1, отличающийся тем, что для его получения используют следующие компоненты в определенном соотношении, мас. %:
консорциум пробиотических бактерий Bifidobacterium breve, Lactobacillus fermentum, Lactobacillus plantarum, Lactobacillus acidophilus, Lactobacillus salivarius, Streptococcus agalactiae, Lactobacillus paracasei, Lactobacillus casei (соотношение 1:1:1:1:1:1:1:1) - 50,0;
пептид Tre-Gly-Glu-Asn-His-Asp - 25,0;
пептид Lys-Val-Leu-Pro-Val-Pro-Glu - 25,0.
4. Способ получения функционального продукта питания для реабилитации онкологических больных по п. 1, отличающийся тем, что для его получения используют следующие компоненты в определенном соотношении, мас. %:
консорциум пробиотических бактерий Lactobacillus fermentum, Lactobacillus plantarum, Lactobacillus acidophilus, Lactobacillus salivarius, Streptococcus agalactiae, Lactobacillus rhamnosus, Lactobacillus paracasei (соотношение 1:1:1:1:1:1:1)- 50,0;
пептид Lys-Glu-Asn - 25,0;
пептид Leu-Leu-Tyr-Glu-Glu-Pro-Val-Leu-Gly-Pro-Val-Gly-Pro-Pro-Pro-Ile-Ile-Val-25,0.
5. Способ получения функционального продукта питания для реабилитации онкологических больных по п. 1, отличающийся тем, что для его получения используют следующие компоненты в определенном соотношении, мас. %:
консорциум пробиотических бактерий Bifidobacteriu longum, Bifidobacterium bifidum, Lactobacillus salivarius, Streptococcus agalactiae, Bifidobacterium adolescentis, Lactobacillus paracasei (соотношение 1:1:1:1:1:1) - 30,0;
пептид Tyr-Pro-Pro-Pro-Gly-Pro-Ile - 35,0;
пептид Lys-Val-Leu-Pro-Val-Pro-Glu - 35,0.
6. Способ получения функционального продукта питания для реабилитации онкологических больных по п. 1, отличающийся тем, что для его получения используют следующие компоненты в определенном соотношении, мас. %: консорциум пробиотических бактерий Lactobacillus reuteri, Bifidobacterium bifidum, Lactobacillus fermentum, Lactobacillus plantarum, Lactobacillus salivarius, Streptococcus agalactiae, Enterococcus faecium (соотношение 1:1:1:1:1:1:1) - 30,0;
пептид Lys-Glu - 35,0;
пептид Tre-Gly-Glu-Asn-His-Asp - 35,0.
| WO 2010033424 A2, 25.03.2010 | |||
| US 20140271553 A1, 18.09.2014 | |||
| US 20070298144 A1, 27.12.2007 | |||
| WO 2014150571 A1, 25.09.2014 | |||
| ШТАММ BIFIDOBACTERIUM LONGUM INFANTIS ДЛЯ ПРИГОТОВЛЕНИЯ ПРОБИОТИКА, АНТИМИКРОБНЫЙ АГЕНТ И ПРЕПАРАТ НА ОСНОВЕ ШТАММА BIFIDOBACTERIUM LONGUM INFANTIS С ИММУНОМОДУЛИРУЮЩИМИ СВОЙСТВАМИ | 2000 |
|
RU2308483C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ПЕПТИДА, ОБЛАДАЮЩЕГО ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ | 2007 |
|
RU2362579C1 |
Авторы
Даты
2018-06-29—Публикация
2016-05-23—Подача