Настоящее изобретение относится к каталитическому способу получения олефинов, диенов, полиенов посредством дегидратации спиртов.
Олефины, также называемые этиленовыми углеводородами или алкенами, состоят из углеводородов общей формулы CnH2n, с n больше чем или равным 2. Диены или полиены состоят из углеводородов, молекула которых содержит две или более этиленовые связи. Данное общее определение применимо к любому углеводороду, имеющему одну или несколько этиленовых связей и включающему любую функциональную группу, такую как, например, первичная, вторичная и третичная аминогруппы, первичная, вторичная и третичная спиртовые группы, карбонильные группы, из которых альдегидные группы сопряжены или не сопряжены с одной из указанных этиленовых связей.
Легкие олефины, такие как этилен, пропен и бутены, а также бутадиен, представляют собой основное углеводородное сырье для химического синтеза и для нефтехимической промышленности. Многочисленные реакции присоединения, которым они могут подвергаться, ставят их в центр множества промышленных отраслей большой производительности для получения функциональных промежуточных соединений. Например, этилен можно окислить до эпоксиэтана (этиленоксид) или представить как исходное вещество для гликоля, этаноламинов, простых и сложных гликолевых эфиров, или его можно окислить до этаналя (ацетальдегид), подвергнуть хлорированию и дегидрохлорированию до винилхлорида, добавить к бензолу и затем дегидрогенизировать до стирола или даже полимеризовать до полиэтилена. Пропен позволяет получать большое разнообразие нефтехимических продуктов, таких как полипропен, акролеин, акрилонитрил, кумол, оксоспирты (бутанол, 2-этилбутанол, 2-этилгексанол), оксид пропена, акриловая кислота, изопропиловый спирт и полигазовые химические продукты. При использовании в качестве синтона в установках алкилирования, установках каталитической полимеризации и установках димеризации, он позволяет получать смеси бензинов с высоким октановым числом. Пропен и бутены также превращаются в функциональные промежуточные продукты. Их полимеризации и сополимеризации приводят к получению макромолекул, которые обладают практически важными свойствами. Изобутилен, также известный как изобутен или 2-метилпропен, представляет собой исходный мономер для бутилкаучука (сополимер изобутилена и небольших количеств изопрена). Изопрен, также известный как 2-метилбута-1,3-диен или терпен, представляет собой предшественник синтетического каучука (полиизопрен), блок-сополимеров стирола-изопрена-стирола и бутилкаучука. Бута-1,3-диен, часто прямо называемый бутадиеном, главным образом используют в изготовлении синтетического каучука, лака, нейлона и (растительных) латексных красок. Большое число автомобильных шин изготовляют с помощью каучука «буна», который представляет собой сополимер бутадиена и стирола. Бутадиен также представляет собой основной реагент для синтеза хлоропрена посредством хлорирования с последующей изомеризацией и дегидрохлорированием. Данные диены также используют для получения адипонитрила и гексаметиленадиамина посредством реакции с синильной кислотой. В нескольких способах бутадиен используют для получения бутан-1,4-диола. Бутадиен представляет собой прекрасный реагент для реакции Дильса-Альдера, и он делает возможным синтез 4-винилциклогексена (реагент для получения стирола), 1,5-циклооктадиена и 1,5,9-циклодекатриена.
В настоящее время, данные синтетические сырьевые и промежуточные вещества главным образом получают из горючих природных ископаемых посредством парового крекинга, каталитического крекинга, каталитической дегидрогенизации и метатезиса. В данных способах потребляется большое количество энергии и выделяется большое количество CO2, который представляет собой парниковый газ.
Этилен, который представляет собой основу мировой химической промышленности, главным образом происходит из жидких нефтепродуктов парового крекинга (нафта или газойль) или газоконденсатных жидкостей (этан, пропан и бутан), где его сопровождают его первые гомологи: пропен или пропилен, бут-1-ен и цис- и транс-бут-2-ены, изобутилен и бута-1,3-диен, и от которых его отделяют посредством фракционной перегонки.
Подобно этилену, пропен представляет собой краеугольный камень нефтехимической промышленности. В настоящее время пропен получают исключительно из природных горючих ископаемых. Он представляет собой основной сопродукт при получении этилена посредством термического крекинга. Установки парового крекинга нафты или газойля являются более селективными в отношении пропена, чем те, в которых в качестве сырья используется сжиженный углеводородный газ. Нефтеперерабатывающие заводы также генерируют значительные количества пропена в качестве промежуточного продукта разрыва пласта, коксования и каталитических процессов висбрекинга. Пропен можно также получать посредством каталитической дегидрогенизации пропана или посредством метатезиса этилена и бут-2-енов.
Диены и полиены очень редко находят в природном состоянии. Одним из самых простых диенов является изопрен, CH2=C(CH3)-CH=CH2, который образуется в результате пиролиза нескольких природных терпенов и политерпенов. Другие доступны посредством многочисленных способов синтеза. Бутадиен, который возникает при крекинге углеводородов (5% бутадиена образуется при крекинге легкого бензина), выделяют из смеси путем перегонки C4 фракций. Получение чистого бутадиена невозможно посредством простой перегонки данной фракции, так как бутан и бутадиен образуют азеотроп. Данное разделение обычно требует проведения экстракции жидкости жидкостью или экстрактивной перегонки. Бутадиен также промышленно синтезируют посредством дегидрогенизации бутана или смесей бутенов и бутана.
Последние технологические разработки прогнозируют все более и более значительную доступность, в краткосрочной перспективе, чистых или смешанных спиртов, способных снижать зависимость от горючих природных ископаемых и уменьшать вред окружающей среде, в частности, в отношении выбросов диоксида углерода (см. отчет EPA/600/R-07/144,  2007, biomass conversion: emerging technologies, feedstocks, and products; SRI BIOTECHNOLOGY-BASED CHEMICALS Hossein Janshekar, KazuteruYokose, Marifaith Hackett and Xiaomeng Ma, консалтинговый отчет SRI, CHEMICAL BUILDING BLOCKS FROM RENEWABLES, Marifaith Hackett, September 2011).
2007, biomass conversion: emerging technologies, feedstocks, and products; SRI BIOTECHNOLOGY-BASED CHEMICALS Hossein Janshekar, KazuteruYokose, Marifaith Hackett and Xiaomeng Ma, консалтинговый отчет SRI, CHEMICAL BUILDING BLOCKS FROM RENEWABLES, Marifaith Hackett, September 2011).
Метанол получают коммерчески посредством реагирования синтетического газа под давлением и в присутствии катализатора (см. отчет о маркетинговом исследовании СЕН METHANOL, Guillermo A. Saade, June 2009). Синтетический газ представляет собой смесь газов, которая состоит главным образом из оксида углерода и водорода, с небольшими количествами диоксида углерода и других газов. Главным образом его получают из природного газа, а также из других источников углеводородов (нафта, нефтяные остатки, угольные остатки и по меньшей мере возможно газы с мест хранения отходов, которые содержат метан). Для ограничения производственных затрат на метанол многочисленные производственные площадки увеличивают свои производственные мощности для получения пользы от положительного влияния эффекта масштаба, тогда как другие направляют свои исследования на одностадийную реакцию метана и кислорода без промежуточного образования синтетического газа.
Все продукты, которые происходят из биомассы, независимо от их происхождения, позволяют получать, как непосредственно, так и в виде промежуточных продуктов, как посредством ферментации, так и посредством химического процесса, функционализированные химические соединения, такие как С6, C5 и C4 спирты, диолы, полиолы и даже С1, С2 и C3 синтоны. В частности, можно заметить возобновившийся интерес в отношении бутандиола, полученного из биологического сырья, включая бутан-1,4-диол и бутан-2,3-диол. Недавний отчет, опубликованный американской компанией Transparency Market Research, сфокусирован на том, что бутан-2,3-диол, полученный из биологического сырья, позволит заместить свой вариант ископаемого происхождения. Можно предложить хорошее альтернативное решение при конкурентных издержках на основе данного диола. Одним из самых крупных применений бутан-2,3-диола, полученного из биологического сырья, остается получение бута-1,3-диена, который представляет собой быстрорастущее сырье. Другим очень известным примером является этанол, который продолжают получать главным образом посредством ферментации углевода (крахмал, сахар или целлюлоза) с последующей перегонкой и обработками, подходящими для его конечного применения (топливо, растворитель, химическое сырье…). Таким образом, он имеется в продаже, в чистой форме (99,9% безводный этанол) или в водном растворе в концентрации выше, чем 80%. Многие исследователи уделяют большое внимание разработке способов, которые позволяют получать этанол при низких затратах из непищевого сырья. Это особенно справедливо в отношении целлюлозного этанола (см. отчет о маркетинговом исследовании СЕН, ETHANOL, Eric Linak, Hossein Janshekar and Yoshio Inoguchi, April 2009).
Ферментация АБЭ (ацетон-бутанол-этанол) представляет собой способ, в котором применяется бактериальная ферментация с образованием ацетона, н-бутанола и этанола из крахмала. Промышленное использование данной ферментации АБЭ началось в 1916 году, когда Хаим Вейцман выделил бактерию Clostridium acetobutylicum, как описано в патенте US1315585A. В способе образуется смесь ацетона, н-бутанола и этанола в соотношениях, находящихся в интервале около 3-6-1. Сырье и штамм, которые используются, прямо влияют на состав смеси на выходе ферментного реактора. Таким образом, например, Cobalt Technologies, Inc. в своей заявке на патент US 2010330633 A1 заявляют о достижении 80% выхода бутанола в результате ферментации сахарозы и использования Clostridium saccharubutylium, тогда как Lanzatech New Zealand LTD в своем патенте US8119844B2 заявляет о достижении 63% выхода в результате ферментации глицерина и использования Clostridium pasteurianum. Для того чтобы сделать ферментацию АБЭ прибыльной, были разработаны многочисленные системы выделения продуктов in-situ. В частности, они включают перегонку, разделение первапорацией, мембранная экстракция, адсорбция и обратный осмос. Еще одно более релевантное улучшение было бы нацелено непосредственно на использование полученной смеси.
Европейские директивы 2001/77/ЕС и 2003/30/ЕС, которые будут введены в ближайшем будущем, планируют вводить 10% Diester® (или VOME, сложные метиловые эфиры растительных масел) в газойль к 2015. Данный биодизель получают в результате переэтерификации метанолом триглицеридов, которые содержаться в масляных жидкостях, в частности, в пальмовом, рапсовом и подсолнечном растительных маслах. В зависимости от рассматриваемых способов, примерно 100 кг глицерина на тонну Diester® получают в виде побочного продукта реакции. Существенное увеличение количества биодизеля, которое будут производить в течение следующих лет, будет образовывать значительные количества глицерина, эквивалентные нескольким сотням тысяч тонн в год. В общем, глицерин, полученный данном способом, имеет чистоту 75-90%. Вода и остаточные соли (часто происходящие из катализаторов) представляют собой основные загрязняющие примеси данного глицерина. В зависимости от предполагаемого применения его будут очищать в большей или меньшей степени. Уже найдено 1500 способов применения глицерина, среди которых нижеприведенные применения, в качестве примеров, иллюстрируют его присутствие в многочисленных и различных композициях:
- увлажнители для фармацевтического применения (в суппозиториях и сиропах) или для косметического применения в увлажняющих кремах, глицериновых мылах, зубных пастах,
- растворители в пищевой промышленности,
- пластификаторы и смазывающие вещества в химической промышленности.
Данных способов применения будет явно недостаточно для освоения количеств глицерина, которые будут образовываться в случае биодизелей, и, несмотря на то, что традиционный рынок глицерина (мыла, фармацевтика…) развивается, он не будет способен переработать такой избыток. Вследствие этого, необходимо найти новые способы применения, которые позволят получать пользу от больших объемов глицерина. В этой связи, за последние годы были изучены многочисленные возможности (см. М. Pagliaro, М. Rossi: The Future of Glycerol, RSC Publishing, Cambridge (2008)), в частности, в отношении конверсии с образованием пропан-1,3-диола и пропан-1,2-диола, которых используют, в частности, в качестве основных мономеров при синтезе сложных полиэфиров и полиуретанов.
Dupont и Tate & Lyle разработали биоферментативный способ, который позволяет получать пропан-1,3-диол (фермент, разработанный совместно с Genencor (Danisco)) из кукурузного крахмала, без обязательного прохождения через получение глицерина.
Рассматривая недавние разработки, которые должны облегчать доступ к многочисленным спиртам, наблюдают возобновившийся интерес к очень давней реакции Гербе. Данная реакция позволяет получать спирты из более короткоцепочечных спиртов посредством кислотно-основного катализатора. В патенте US 7807857 B2 Dupont предлагает способ получения спиртов Гербе (бутанол и высшие спирты) из этанола. В US 7989664 B2, Virent Energy Systems описывает способ получения полиолов, который может включать спирты, такие как метанол, этанол, изопропиловый спирт, пропанол, бутанол, пентанол и гексанол. В своем патенте US 8187347 B2, Kabushiki Kaisha Sangi предлагает способ, который позволяет получать смесь спиртов и олефинов из спиртов, и в своем патенте US 8080695 B2 описывает способ получения из этанола смеси бутан-1-ола, гексанола, октанола и деканола.
Следует отметить, что преобразование биомассы не является единственным путем получения спиртов в больших количествах. Таким образом, способы на основе сингаза модифицируют так, чтобы в результате получать спирты, отличные от метанола, такие как этанол, пропан-1-ол и пропан-2-ол и бутанолы. Катализаторы представляют собой катализаторы на основе металлов, таких как Cu, Zn, Mo или Cr, легированные щелочными металлами. Способы получения смесей спиртов, отличных от метанола, таким образом, были разработаны компаниями Snamprogetti, Topsoe, Lurgi, Dow и IFP-Idemitsu. Реакции, которые вовлечены в данные способы, включают реакцию конверсии водяного газа, бета-соприсоединение, гомологизации этанола и других более длинноцепочечных спиртов, конденсацию, дегидратацию, образование разветвленных изо-спиртов и сложных метиловых эфиров.
Таким образом, некоторые спирты, такие как, например, метанол, этанол и бутанол, уже были получены промышленно в крупных масштабах. Технологии будущего предоставят доступ к данным спиртам и ко многим другим спиртам, как чистым, так и смешанным, при низких затратах. При возрастании потребности в олефинах, истощении традиционного ископаемого сырья и разработке доступа к альтернативному сырью селективная дегидратация спиртов до олефинов, по-видимому, является многообещающим альтернативным промышленным способом, тем более что он позволит перерабатывать смеси спиртов.
По общему правилу, реакции гидратации предпочтительно проводить при низкой температуре, тогда как реакции дегидратации предпочтительно проводить при высокой температуре. Вследствие этого, для получения желательных продуктов дегидратации необходимо применять достаточную температуру реакции, и/или частичный вакуум, для сдвига равновесия реакции. Реакцию дегидратации можно проводить в жидкой фазе или в газовой фазе. Известно, что данный тип реакции катализируется неорганическими кислотами или твердыми кислотами.
Многие кислотные катализаторы являются эффективными при дегидратации этанола. В основе большей части данных катализаторов лежит легированный оксид алюминия, фосфорная кислота на подложке, алюмосиликаты или цеолиты (см. A. Morschbacker, Journal of Macromolecular Science, Part C: Polymer Reviews, 49 (2009) 79-84; O. Winter, E. Ming-Teck, Hydrocarb. Process Nov (1976) 125-133; C.B. Phillips, R. Datta, Ind. Eng. Chem. Res. 36 (1997) 4466-4475; T.M. Nguyen, R.L.V. Mao, Appl. Catal. 58 (1990) 119-129, X. Zhang, R. Wang, X. Yang, F. Zhang, Micro and Meso Materials 116 (2008) 210-215.). Почти все из первых промышленных катализаторов, которые были предложены, были основаны на фосфорной кислоте на подложке, но они были быстро вытеснены оксидами алюминия или алюмосиликатами из-за их более высокой продуктивности и отсутствия характерной коррозии при их применении.
Тем не менее, данные катализаторы требуют высоких температур реакции (430-450°C), и они являются менее эффективными в случае, когда спиртовые растворы содержат большие количества воды. В силу данных причин, в качестве катализаторов были разработаны синтетические цеолиты, такие как HZSM5 [см. С.В. Phillips, R. Datta, Ind. Eng. Chem. Res. 36 (1997) 4466-4475 et T.M. Nguyen, R.L.V. Mao, Appl. Catal. 58 (1990) 119-129]. Их использовали только для дегидратации этанола, и они позволяют снижать температуру реакции (300°C) без какой-либо потери эффективности (например, на катализаторе на основе HZSM55 можно получать селективность 95% в отношении этилена при конверсии этанола 98%). Также успешно были использованы цеолиты типа SAPO-34. Однако, дегидратация спиртов происходит на кислотных центрах, которые являются слабыми или средней силы, и наличие неоднородно распределенных сильных кислотных центров, так же, как и в данных цеолитных материалах, вызывает образование нежелательных продуктов и значительное коксообразование на катализаторе (см. X. Zhang, R. Wang, X. Yang, F. Zhang, Micro and Meso Materials 116 (2008) 210-215). Вследствие этого, цеолиты нужно модифицировать посредством легирования фосфором (см. D.S. Zhang, R.J. Wang, Х.Х. Yang, Catal. Lett. 124 (2008) 384-391 et K. Ramesh, LM. Hui, Y.F. Han, A. Borgna, Catal. Commun. 10 (2009) 567-571), редкоземельными металлами (см. J. Ouyang, F.X. Kong, G.D. Su, Y.C. Hu, Q.L. Song, Catal. Lett. 132 (2009) 64-72; US 4873392 A; N. Zhan, Y. Ни, H. Li, D. Yu, Y. Han, H. Huang, Catal. Comm. 11 (2010) 633-637) или еще, так же, как в случае SAPO-34, никелем (см. X. Zhang, R. Wang, X. Yang, F. Zhang, Micro and Meso Materials 116 (2008) 210-215) для устранения избыточно сильных кислотных центров и увеличения количества умеренно сильных или даже слабых кислотных центров.
Данные модификации улучшают селективность и стабильность катализаторов, но, тем не менее, имеют недостаток, связанный с необходимостью использования относительно низкой часовой объемной скорости подачи сырья.
В то время, как дегидратацию пропанола-2 обычно используют для характеристики кислотности всех типов катализаторов, дегидратация н-пропанола не была достаточно изучена. Наилучшие катализаторы, которые были получены, обеспечивают выход 100% при 380°C (см. P. Brandao, А. Philippou, J. Rocha, M.W. Anderson, Catal. Letters 80 (2002) 99) на катализаторах на основе цеолита.
Исследование получения бутанола ферментацией стало более интенсивным за последние несколько лет, и были сделаны значительные успехи. Данные успехи связаны, в то же самое время, со штаммами микроорганизмов и технологией ферментации, качеством исходных продуктов, которые могут состоять из остатков биомассы, и методиками, используемыми для разделения полученных продуктов [А.Р. Mariano, R. MacielFilho, J. Bioenerg. Res. 5 (2012) 504.Et V. Menon, M. Rao, Progress in Energy and Combustion Science 38 (2012) 522]. В настоящее время считают, что биобутанол является возможным биотопливом, поскольку его можно получать в масштабе миллионов тонн.
Было разработано много способов применения для извлечения пользы от данного биобутанола. Его можно каталитически дегидрогенизировать или дегидратировать. В первом случае, получают бутанон (или метилэтилкетон), который представляет собой обычный растворитель в химической промышленности [C.F. Turner, J.W. McCreery, The Chemistry of Fire and Hazardous Materials. Boston, Massachusetts: Allyn and Bacon, Inc. (1981) 118.]. Bo втором случае, получают разные изомеры бутена (бут-1-ен, цис-бут-2-ен, транс-бут-2-ен и изобутен). Распределение данных разных бутенов зависит от исходного спирта (бутан-1-ол, бутан-2-ол и изобутанол), температуры (термодинамическое равновесие) и катализатора. Бутены используют в получении пластмассы, например, бут-1-ен, или смазывающих веществ, например, бут-2-ен, или гумми (бутилкаучук) и метил-трет-бутилового эфира (МТБЭ) или изооктана, например, изобутен.
Бут-2-ен можно также использовать для получения пропена посредством реакции метатезиса с этиленом. Полагают, что данный способ производства на основе метатезиса в ближайшем будущем будет развиваться, так как он предоставляет доступ к пропену, полностью полученному из биологического сырья. Тем не менее, так как основным продуктом большинства способов получения бутанола посредством ферментации является бутан-1-ол, бутен, который необходим для реакции метатезиса, представляет собой бут-2-ен. В связи с этим, важно обеспечить каталитический способ селективной конверсии бутан-1-ола в бут-2-ены. По данным, сообщений о катализаторе, который позволяет получать приемлемую селективность, еще не было.
Фундаментальный научный успех заключался бы в разработке катализатора, который делает возможной селективную дегидратацию бутан-1-ола до бут-2-ена в сочетании с селективной дегидратацией этанола до этилена, причем чтобы данный катализатор можно было использовать для селективного превращения двух спиртов при одной и той же температуре. Кроме того, если бы катализатор был также селективным в отношении превращения бутан-2-ола в бут-2-ены, не было бы больше необходимости в разделении спиртов или обогащении реакции одним из них. Дегидратацию смеси спиртов можно было бы проводить за одну единственную стадию, и она могла бы приводить непосредственно к оптимальной смеси для реакции метатезиса.
Если существует какой-либо особый интерес к превращению этанола и бутанола одновременно на одном и том же катализаторе, могло бы быть интересно превращать другие смеси из двух или большего количества спиртов одновременно на одном и том же катализаторе, при одной и той же температуре, для получения, скорее селективно, смеси алкенов, не допуская при этом какого-либо мешающего крекинга или реакций образования простого эфира. Катализатор, который используют в такой реакции, должен быть довольно активным и селективным для дегидратации всех рассматриваемых спиртов в одном и том же интервале температур.
Цель настоящего изобретения заключается в применении катализаторов, которые являются надежными, активными, селективными и регенерируемыми, и которые позволяют получать олефины, диены и/или пол иены из спиртов, диолов, полиолов как чистых, так и смешанных, в соответствии с реакцией дегидратации. Авторы настоящего изобретения разработали высокоселективные, регенерируемые и активные катализаторы при более низкой температуре, чем катализаторы, которые были описаны в предшествующем уровне техники для дегидратации спиртов.
Таким образом, изобретение относится к способу получения одного или нескольких олефинов, диенов или полиенов посредством каталитической конверсии по меньшей мере одного спирта, имеющего углеродную цепь по меньшей мере из трех атомов углерода и отличного от пропан-2-ола, в присутствии по меньшей мере одного катализатора на основе по меньшей мере одного фосфата металла или нескольких металлов М, причем М выбран из 15 лантанидов (лантан, церий, празеодим, неодим, прометий, самарий, европий, гадолиний, тербий, диспрозий, гольмий, эрбий, тулий, иттербий, лютеций), иттрия, скандия и бора.
Под спиртом согласно настоящему изобретению подразумевается углеводородная цепь, как насыщенная, так и ненасыщенная, линейная или разветвленная, которая несет одну или несколько гидроксильных групп, например, диолы и все другие полиолы.
Ниже в данном документе настоящее изобретение описано более подробно, обращая особое внимание на варианты и преимущества способа по изобретению, а также на способы его применения.
Предпочтительно, катализатор основан по меньшей мере на одном фосфате одного или нескольких металлов М, выбранных из лантана, празеодима, неодима, прометия, самария, европия, гадолиния, тербия, диспрозия, гольмия, эрбия, тулия, иттербия, лютеция, иттрия и скандия.
Согласно еще одному предпочтительному воплощению катализатор основан по меньшей мере на одном фосфате одного или нескольких металлов М, выбранных из лантана, неодима, гадолиния и самария.
Катализатор по изобретению может быть легирован по меньшей мере одним щелочным металлом, выбранным из цезия, рубидия и калия, и/или переходным металлом, выбранным из групп 4-7.
Преимущественно, молярное отношение Р/М варьирует от 0,5 до 2, и еще лучше от 0,9 до 1,5, причем М представляет металл или сумму металлов М, которые образуют указанных катализатор.
Способ по изобретению представляет большой интерес, заключающийся в том, что он позволяет перерабатывать один или более чем один спирт, как чистый, частично очищенный, неочищенный, так и в форме азеотропных композиций, а также их любую смесь. Они могут быть переработаны в инертном газе, независимо от того, присутствует газ-окислитель (O2, H2O, CO2, O3…) или нет. Присутствие такого газа позволяет повышать стабильность катализатора со временем. Спирт(ы) может(гут) находиться в форме водного раствора, предпочтительно в концентрации по меньшей мере 1 мас.%.
Исходя из их доступности и/или продукта, который получается в результате их дегидратации, предпочтительные спирты выбраны из пропан-1-ола, бутан-1-ола, бутан-2-ола, изобутанола, бут-3-ен-1-ола, бут-2-ен-1-ола, бут-3-ен-1,2-диола, бутан-2,3-диола, бутан-1,3-диола, бутан-1,4-диола, глицерина, пропан-1,2-диола, пропан-1,3-диола, эритритола и их смесей.
Согласно изобретению, полученный олефин, диен или полиен имеет углеродную цепь из такого же числа атомов углерода, как и у спирта(ов), из которого(ых) они были получены; таким образом, целью изобретения является способ получения по меньшей мере одного олефина, диена или полнена, имеющих углеродную цепь по меньшей мере из трех атомов углерода, и которых получают посредством каталитической конверсии спирта или смеси соответствующих спиртов, имеющих углеродную цепь из такого же числа атомов углерода.
Другая интересная цель изобретения заключается в реализации описанного выше способа получения смеси олефинов, диенов и/или полиенов.
Более конкретно, он позволяет получать смесь по меньшей мере двух олефинов, диенов и/или полиенов, из по меньшей мере одного спирта, имеющего углеродную цепь по меньшей мере из трех атомов углерода и отличного от пропан-2-ола. Согласно варианту изобретения, способ позволяет получать смесь по меньшей мере двух олефинов, диенов и/или полиенов из смеси спиртов, содержащей по меньшей мере один спирт, имеющий углеродную цепь по меньшей мере из трех атомов углерода и отличный от пропан-2-ола, и любой другой спирт.
Таким образом, другой целью изобретения является способ получения смеси по меньшей мере двух олефинов, диенов и/или полиенов, согласно которому по меньшей мере один из олефинов, диенов и/или полиенов получают способом по изобретению. По меньшей мере другой(ие) олефин(ы), диен(ы) и/или полиен(ы) может(гут) быть или не может(гут) быть получен(ы) способом по изобретению; они могут быть получены посредством каталитической конверсии спирта или смеси спиртов, в присутствии по меньшей мере одного катализатора, как определено выше.
Получение указанных олефинов, диенов и/или полиенов можно осуществлять посредством каталитической конверсии спирта или смеси спиртов, в присутствии одного и того же катализатора или в присутствии разных катализаторов.
Их можно получать в одном и том же реакторе, в присутствии одного и того же катализатора или в присутствии разных катализаторов; их можно так же получать в разных реакторах, в присутствии идентичного катализатора или разных катализаторов.
Оказалось, что катализаторы по изобретению способны селективно превращать несколько спиртов притом, что данные спирты смешаны.
Преимущественно, указанный(ые) катализатор(ы), который(ые) используют для получения данных олефинов/диенов/полиенов, содержит(ат) активную фазу и подложку и/или связующее вещество. Они также могут быть образованы, возможно, в присутствии связующего вещества. Их можно также регенерировать.
Чистые или смешанные спирты можно обрабатывать в инертном газе, независимо от того, присутствует газ-окислитель (O2, H2O, CO2, O3, …) или нет. Присутствие такого газа позволяет улучшать стабильность катализатора со временем.
По сравнению с предшествующим уровнем техники, согласно описанному изобретению предложен способ получения C4 олефинов, который является более эффективным и более селективным в отношении бут-2-ена, чем в отношении бут-1-ена, посредством дегидратации C4 спиртов в присутствии катализатора, который при условии полной конверсии исходного C4 спирта может быть очень легко регенерирован и имеет длительный срок службы. Реакцию можно проводить в жидкой фазе, в газовой фазе или в двухфазной смешанной среде.
В случае реакции в газовой фазе после дегидратации реакционный газ охлаждают в колонне с водой для охлаждения, которая разделяет основную часть продуктов от воды и спирта, который не прореагировал. Последующая обработка потока олефина, диена и/или полнена зависит от уровня чистоты, который требуется от конечного продукта, в частности, в соответствии с ожидаемым применением.
Таким образом, данная альтернатива предусматривает выгодный способ синтеза олефинов, диенов и/или полиенов или кетонов, который в меньшей степени зависит от традиционных ископаемых ресурсов при уменьшении вреда окружающей среде. Недавние технологические и биотехнологические разработки обещают в краткосрочной перспективе повышенную доступность чистых или смешанных спиртов. Данные научные разработки позволили бы снизить вред окружающей среде посредством уменьшения выбросов тепличных газов, в частности, диоксида углерода.
Ниже в данном документе, описаны примеры по существу интересных применений способа по изобретению:
Селективное получение бут-2-ена из бутан-1-ола, бутан-2-ола и их смесей;
Получение пропена посредством осуществления любого из следующих способов:
- получение пропена способом по изобретению, при этом спирт выбран из пропан-1-ола, возможно смешанного с пропан-2-олом;
- получение бутена способом по изобретению, при этом спирт выбран из бутан-1-ола, бутан-2-ола и их смесей, и затем конверсия бутена в пропен посредством метатезиса;
- получение смеси этилена и бутена способом по изобретению, при этом по меньшей мере один спирт состоит из этанола, а другой спирт выбран из бутан-1-ола, бутан-2-ола и их смесей, и затем конверсия смеси этилена и бутена в пропен посредством метатезиса.
Получение бутадиена посредством осуществления способа по изобретению, при этом спирт выбран из бут-2-ен-1-ола, бут-3-ен-1-ола, бут-1-ен-3-ола, бут-3-ен-1,2-диола, бутан-2,4-диола, бутан-2,3-диола, бутан-1,3-диола и бутан-1,4-диола и их смесей;
Получение изобутена из изобутанола;
Получение пентена и изопрена из спиртов, в частности, из соответствующих диолов;
Получение акролеина, акриловой кислоты, акрилонитрила и полипропилена из пропена, который был получен согласно настоящему изобретению;
Получение альдегид-3-(метилтио)пропионовой кислоты (ММР), нитрила 2-гидрокси-4-метилтиомасляной кислоты (HMTBN), метионина, 2-гидрокси-4-метилтиомасляной кислоты (НМТВА), сложных эфиров данных соединений или 2-оксо-4-метилтиобутановой кислоты (КМВ) из акролеина, полученного, как описано выше, или из пропена.
Метионин, НМТВА и сложные эфиры последней и их аналоги используют для кормления животных, и в промышленных способах их синтеза акролеин обычно получают путем окисления пропена и/или пропана. Окисление пропена до акролеина воздухом в присутствии воды является частичным, и получающийся неочищенный продукт, в основе которого лежит акролеин, также содержит пропен и пропан, которые не прореагировали, воду и промежуточные продукты реакции окисления, в частности, кислоты, альдегиды и спирты.
Традиционно, акролеин и акриловую кислоту получают посредством контролируемого окисления пропена атмосферным кислородом в газовой фазе в присутствии катализаторов на основе молибдена и/или оксидов висмута. Акролеин, который получают данным образом, можно либо прямо включать в способ получения акриловой кислоты, акрилонитрила, либо использовать в качестве промежуточного продукта синтеза.
Рынки акролеина, который представляет собой один из самых простых ненасыщенных альдегидов, акрилонитрила и акриловой кислоты являются огромными, так как данные мономеры входят в состав многочисленных продуктов массового спроса.
Кроме того, акролеин, который является высокореакционноспособным соединением благодаря своей структуре, имеет множество применений, в частности, в качестве промежуточного продукта синтеза. Как указано ранее, он особенно используется в качестве ключевого промежуточного соединения, участвующего в синтезе D,L-метионина и его аналогичного гидроксипроизводного, 2-гидрокси-4-метилтиомасляной кислоты (НМТВА). Данные кормовые добавки массово используют, так как они входят в состав кормовых добавок, которые являются необходимыми для роста животных (домашней птицы, свиней, жвачных животных, рыбы, …).
В некоторых случаях, может быть прибыльной возможность увеличения, и даже обеспечения, производственных мощностей существующих промышленных установок посредством введения разнообразия используемого сырья. Вследствие этого, по-видимому, особенна интересна возможность повышать продуктивность в отношении акролеина, уменьшая при этом зависимость в отношении данного ресурса на масляной основе, который представляет собой пропен, и уменьшать вред, наносимый окружающей среде. Таким образом, пропен можно получать посредством метатезиса этилена и н-бутена, полученных отдельно или в виде смеси посредством дегидратации спиртов или непосредственно посредством дегидратации пропан-1-ола, также называемого н-пропанолом, или посредством крекинга высших олефинов.
Получение пропена посредством метатезиса этилена и н-бутенов можно обобщенно представить в соответствии со следующим равновесным уравнением:
Этилен + Бут-2-ен = >Пропен
Данная реакция является термодинамически предпочтительной, но она является равновесной. Использование избытка этилена позволяет стимулировать образование пропена. Данная реакция остается селективной, но требует отсутствия всех органических примесей. Следовательно, нужно обеспечить предварительную очистку реагентов, в противном случае, реакцию следует проводить с высокоочищенными реагентами. Данная реакция эффективна только с бут-2-еном. Побочная реакция между двумя молекулами бут-1-ена приводила бы к получению гекс-3-ена и этилена. Следовательно, необходимо либо добавлять изомеризатор, который превращает нереакционноспособный бут-1-ен в частично бут-2-ен, либо использовать фракцию, которая была заранее обогащена бут-2-еном. Получение пропена с хорошей селективностью и с хорошей скоростью протекания реакции стимулируют избытком бут-2-ена в отношении бут-1-ена и избытком этилена. Например, в заявке на патент US 2005/0124839 A1, от имени LUMMUS, рекомендуется проведение реакции с молярным соотношением «этилен/сумма бутенов», находящимся в диапазоне от 0,9 до 2. Согласно способу Meta-4 IFP (Французский институт нефти), предложен непрерывный способ получения пропена из этилена и бут-2-ена посредством метатезиса при низкой температуре в жидкой фазе в присутствии гетерогенного катализатора на основе рения (см. US 6075173 A). При равновесии сообщают о скорости конверсии 63% при 35°C.
Применение изобретения, обладающее большим преимуществом, заключается в синтезе фракции, которая обогащена бут-2-еном, или потока, который стимулирует селективное получение пропена посредством метатезиса этилена и бутена.
По сравнению с предшествующим уровнем техники, согласно описанному изобретению предложен способ получения С4 олефинов, который является более селективным в отношении бут-2-ена, чем в отношении бут-1-ена, и который включает каталитическую дегидратацию С4 спиртов в присутствии катализатора, который, при обеспечении полной конверсии исходного С4 спирта, довольно легко может быть регенерирован и имеет значительный срок службы.
Аналогично, согласно описанному изобретению можно получать смесь этилена и бутенов, которые стимулируют получение пропена в результате метатезиса, посредством каталитической дегидратации смеси этанола и С4 спирта, и предпочтительно бутан-1-ола.
Катализатор можно получать различными способами (соосаждение, гидротермальный синтез…), хорошо известными специалистам в данной области техники. В частности, специалисты в данной области техники могут обратиться к следующим статья: М. Anbia, М.К. Rofouel, S.W. Husain, Chin. J. Chem. 24 (2006) 1026-1030; J.A. Diaz-Guillen, A.F. Fuentes, S. Gallini, M.T. Colomer, J. Alloys and Compounds 427 (2007) 87-93; K. Rajesh, P. Shajesh, O. Seidel, P. Mukundan, K.G.K. Warrier, Adv. Funct. Mater. 17 (2007) 1682-1690.
Исходный предшественник на основе фосфора может быть выбран из нескольких соединений, таких как фосфаты аммония и гидрофосфаты аммония, фосфаты щелочных металлов и предпочтительно фосфаты натрия, фосфорные кислоты и предпочтительно ортофосфорные кислоты, безводный оксид фосфора, или органических соединений фосфора, таких как эфиры фосфорной кислоты.
Кроме того, катализатор, который был ранее описан, может соответствовать следующим предпочтительным характеристикам, рассматриваемым по отдельности или в комбинации:
- катализаторы главным образом образованы фосфатами и смешанными фосфатами, как определено выше, которые составляют основную(ые) активную(ые) фазу(ы) катализаторов.
- катализаторы главным образом состоят из ортофосфатной фазы как чистой, так и в смеси.
- молярное отношение Р/М варьирует в диапазоне от 0,5 до 2, более преимущественно оно варьирует в диапазоне от 0,9 до 1,5, причем М представляет металл или сумму металлов М, которые составляют указанный катализатор.
Указанный катализатор может также содержать активную фазу на основе фосфата и по меньшей мере одно связующее вещество или подложку для данной активной фазы. Подложка или связующее вещество могут быть образованы чистым диоксидом кремния (SiO2), силикатом (диоксид кремния щелочного металла, щелочноземельного металла или редкоземельных металлов), возможно смешанными друг с другом или с глинами, оксидом титана (TiO2), оксидом бора (B2O3) или смолами (сульфоновые смолы, перфторсульфоновые смолы). Предпочтительные связующие вещества или подложки содержат в своей основе диоксид кремния, во всех формах, которые известны специалистам в данной области техники, в своей основе оксид титана и их смеси. Массовое содержание связующего вещества или подложки в катализаторе находится в диапазоне от 0 до 80%, более предпочтительно от 5 до 50%.
Подложку можно получать посредством формования, независимо от того, присутствует связующее вещество или нет, с помощью любой методики, известной специалистам в данной области техники. Например, формование можно осуществлять посредством экструзии, посредством пеллетирования, способом коагуляции капель (масляная капля), посредством грануляции с использованием вращающегося гранулятора или любым другим способом, хорошо известным специалистам в данной области техники. По меньшей мере одну кальцинацию можно проводить после любой из стадий получения, ее обычно проводят на воздухе при температуре по меньшей мере 150°C, предпочтительно при по меньшей мере 300°C.
Как сказано ранее, катализатор по изобретению интересен тем, что он может быть легко регенерирован, таким образом не влияя ни на выход дегидратации, ни селективность в отношении получаемых олефина, диена и полнена, соответственно. Например, данную регенерацию проводят на воздухе, разреженном воздухе, обогащенном воздухе, in situ или ex situ. Преимущественно, она происходит in situ.
Реакцию согласно изобретению можно проводить в газовой фазе или в жидкой фазе, и предпочтительно в газовой фазе. В случае, когда реакцию проводят в газовой фазе, можно использовать разные технологии способа, а именно, способ с использованием неподвижного слоя, способ с использованием псевдоожиженного слоя или способ с использованием циркулирующего псевдоожиженного слоя, например, в реакторе TZFBR (двухзонный реактор с псевдоожиженным слоем). В первых двух способах, то есть способе с использованием неподвижного слоя или способе с использованием псевдоожиженного слоя, регенерацию катализатора можно отделить от каталитической реакции. Например, ее можно проводить ex situ традиционными способами регенерации, такими как сжигание на воздухе или с газовой смесью, содержащей молекулярный кислород или любой другой окислитель. Согласно способу по изобретению регенерацию можно проводить in situ, так как температуры и давления, под которыми проводят регенерацию, совместимы с условиями реакции по способу.
Помимо данной регенерации, которая в первую очередь нацелена на устранение кокса, который образовался на поверхности катализаторов, непрерывную или периодическую регенерацию катализатора можно проводить для повышения долговременной стабильности и образования оптимального молярного соотношения фосфор/редкоземельные металлы (RE). Для данной цели, катализатор можно приводить в контакт с соединением на основе фосфора, которое было добавлено к реагентам во время каталитической реакции, регенерации или во время заранее определенной стадии. В качестве примеров, соответствующие соединения на основе фосфора выбраны из триэтилфосфата или других алкилфосфатов, таких как триметилфосфат, фосфитов, таких как триметилфосфит и триэтилфосфит, и других фосфинов. Данные соединения можно добавлять с водой или без нее; все же присутствие воды является предпочтительным.
Так как указанная реакция представляет собой жидкофазный способ, ее можно проводить в традиционном реакторе, используемом для реакций в жидкой фазе на твердом катализаторе. Тем не менее, принимая во внимание значительное различие между точками кипения спиртов и точками кипения соответствующих олефинов, диенов и полиенов, реакцию можно проводить в реакторе, используемом для каталитических перегонок. Кроме того, также целесообразно рассмотреть жидкофазный способ при относительно низкой температуре, которая делает возможной непрерывную перегонку полученных продуктов, ограничивая, таким образом, последовательные реакции распада.
Предпочтительно, экспериментальные условия газофазной реакции включают в себя температуру, находящуюся в интервале от 150 до 450°C, при давлении, находящемся в интервале от 1 до 10 бар (от 100 до 1000 кПа). В жидкой фазе реакцию проводят при температуре от 50 до 200°C и при давлении, которое может изменяться в интервале от 3 до 70 бар (от 300 до 7000 кПа).
Другое преимущество способа по изобретению заключается в форме исходных спиртов, которые могут быть чистыми, частично очищенными или в растворе, в частности, в водном растворе или в смесях. Кроме того, растворы спиртов не следует слишком разбавлять вследствие непозволительных энергетических затрат, которые являлись бы результатом испарения спиртов. Во всех случаях целесообразно регулировать концентрацию спиртового раствора посредством частичной или полной рециркуляции воды, которую получали в результате рассматриваемой реакции. Возможно оптимизировать энергопотребление в процессе синтеза посредством рекуперации тепла на выходе реактора и использовать его для упаривания потока спирта(ов), который подают в реактор. Таким образом, в оставшейся части описания будут главным образом ссылаться на конверсию чистого спирта или смеси спиртов, независимо от их происхождения и степени чистоты.
В зависимости от рассматриваемого приложения возможно рассматривать очистку олефинов, диенов и полиенов или смеси олефинов, диенов и/или полиенов, которые были получены посредством традиционных методик, известных специалистам в данной области техники.
Другим объектом изобретения является способ получения альдегид-3-(метилтио)пропионовой кислоты (ММР), нитрила 2-гидрокси-4-метилтиомасляной кислоты (HMTBN), метионина, 2-гидрокси-4-метилтиомасляной кислоты (НМТВА), сложных эфиров последней, в частности, изопропилового сложного эфира, и 2-оксо-4-метилтиобутановой кислоты (КМВ), из пропена, который был получен способом, описанным выше. Затем пропен подвергают контролируемому окислению атмосферным кислородом в газовой фазе в присутствии катализаторов на основе молибдена и/или оксидов висмута для образования акролеина.
После очистки акролеин, который был получен непосредственно согласно изобретению или после очистки, вступает в реакцию с метилмеркаптаном (MSH) для получения альдегид-3-(метилтио)пропионовой кислоты (ММР). На последующей стадии ММР приводят в контакт с синильной кислотой для получения нитрила 2-гидрокси-4-метилтиомасляной кислоты (HMTBN). После синтеза HMTBN в результате различных стадий реакции получают метионин, его аналогичное гидроксипроизводное (НМТВА), сложные эфиры последнего или его аналогичное оксопроизводное (КМВ). Все данные стадии, начиная с синтеза пропена, хорошо известны специалистам в данной области техники.
Другая цель настоящего изобретения заключается в получении акриловой кислоты, акрилонитрила и полипропилена из пропена, который был получен любым из описанных выше способов, согласно способам, которые хорошо известны специалистам в данной области техники.
Ниже в данном документе изобретение проиллюстрировано следующими примерами, которые показывают его подробности и его преимущества по сравнению с предшествующим уровнем техники, и со ссылкой на графические материалы.
На Фиг. 1 представлено сравнение изменения конверсии бутан-1-ола в соответствии с температурой реакции для трех катализаторов по изобретению и для оксида алюминия в условиях, которые описаны в Примере 1.
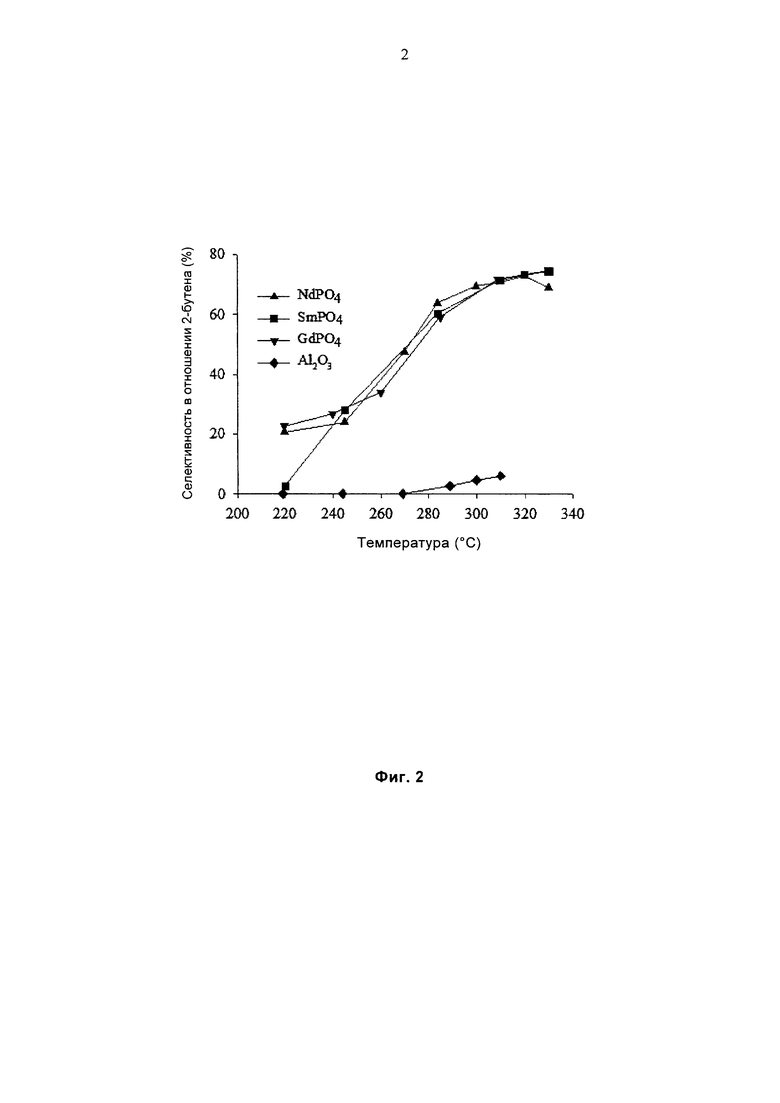
На Фиг. 2 представлено сравнение селективности в отношении бут-2-ена в соответствии с температурой реакции для тех же трех катализаторов по изобретению и для того же оксида алюминия, как на Фиг. 1, в условиях, которые описаны в Примере 1.
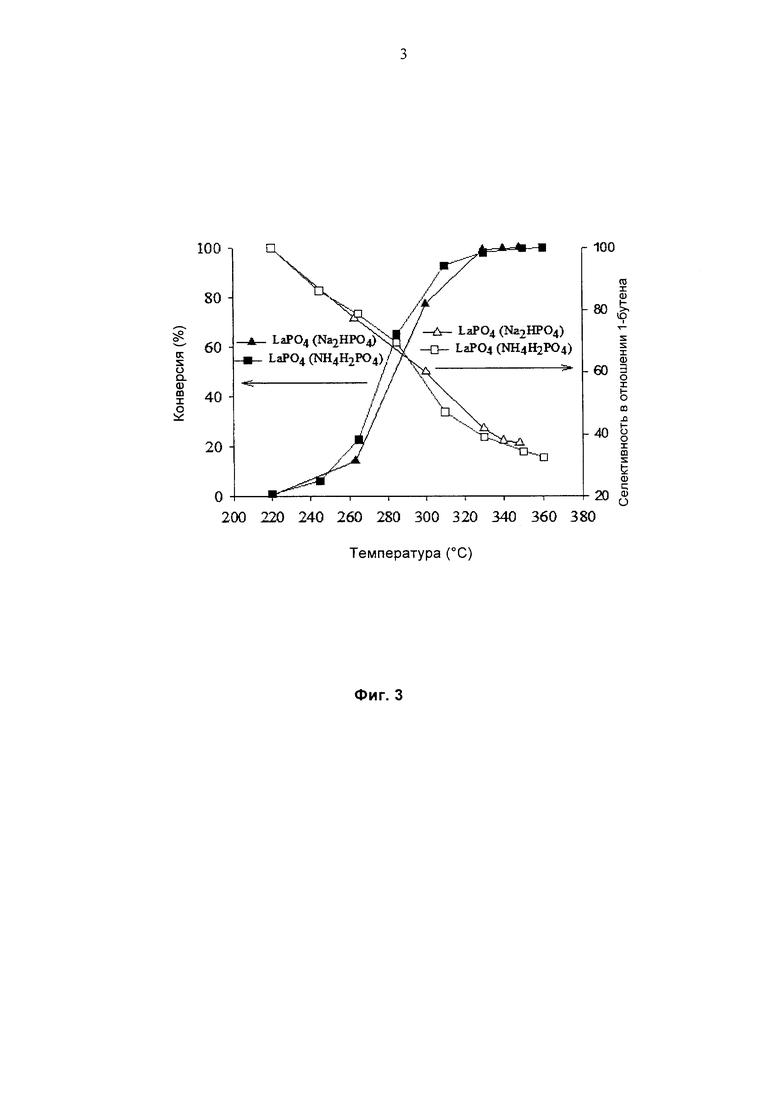
На Фиг. 3 представлено сравнение конверсии бутан-1-ола и селективности в отношении бут-2-ена в соответствии с температурой реакции для катализатора по изобретению, который был получен согласно двум разным способам в условиях, которые описаны в Примере 2.
На Фиг. 4 показано влияние воды на дегидратацию бутан-2,3-ола до бутадиена в условиях, которые описаны в Примере 15.
Проиллюстрированные катализаторы характеризуются следующими параметрами:
- Удельная поверхность, выраженная в м2/г и измеренная способом БЭТ (метод Брунауэра, Эммета и Теллера),
- содержание фосфора и содержание металла(ов) М, выраженные молярным соотношением Р/М и измеренные ICP-OES (оптическая эмиссионная спектроскопия с индуктивно-связанной плазмой); в следующих примерах данное отношение варьирует в пределах предпочтительного диапазона, который был ранее определен, от 0,9 до 1,5; более конкретно, для катализаторов по изобретению, которые тестируют ниже в данном документе, молярное соотношение P/La составляет 1,10 для LaPO4, и молярное соотношение P/Nd составляет 1,14 для NdPO4.
Реакцию дегидратации спиртов проводили на указанных катализаторах при атмосферном давлении и при существенно более высоком давлении в реакторе с неподвижным слоем. Реактор помещают в печь, которая позволяет выдерживать катализатор при температуре реакции, которая варьирует от 130 до 390°C. В реактор подают спирт посредством сатуратора или шприцевого насоса в присутствии потока азота. Для каждого примера указано относительное молярное соотношение спирта к азоту. Среднечасовая скорость подачи сырья (WHSV) выражена в граммах вводимого спирта на граммы катализатора в час.
ПРИМЕР 1
Ряд ортофосфатов редкоземельных металлов (Nd, Sm, Gd) тестировали в реакции дегидратации бутан-1-ола для конверсии бутан-1-ола в бут-2-ен и сравнивали с гамма-оксидом алюминия.
Удельная поверхность каждого тестируемого катализатора составляла 117 м2/г для NdPO4, 82 м2/г для SmPO4, 95 м2/г для GdPO4 и 270 м2/г для Al2O3.
Реакцию проводили при атмосферном давлении в следующих условиях: WHSV = 2,38 ч-1; бутан-1-ол/N2 = 1/82,6.
На Фиг. 1 и 2 соответственно показаны конверсия бутан-1-ола и селективность в отношении бут-2-ена в зависимости от температуры реакции согласно следующим условным обозначениям:
▲ - NdPO4
■ - SmPO4
▼ - GdPO4
♦ - Al2O3
По-видимому, фосфаты являются активными при более низкой температуре, чем контрольный оксид алюминия. Кроме того, измерили заметно более высокую селективность в отношении бут-2-ена.
ПРИМЕР 2
В данном примере ортофосфат лантана получают из двух разных предшественников, соответственно, Na2HPO4 в соответствии со способом получения, описанным в J.A. Diaz-Guillen, A.F. Fuentes, S. Gallini, M.T. Colomer, J. All. and Comp. 427 (2007) 87-98, и (NH4)H2PO4 согласно способу Pavel.
Удельная поверхность каждого тестируемого катализатора составляет 128 м2/г для LaPO4, который получали из Na2HPO4, и 112 м2/г для LaPO4, который получали из (NH4)H2PO4.
Данные катализаторы тестировали при дегидратации бутан-1-ола в следующих условиях тестирования: WHSV = 2,38 ч-1; бутан-1-ол/N2 = 1/82,6.
На Фиг. 3 показано изменение конверсии спирта и селективности в отношении бут-1-ена в зависимости от температуры согласно следующим условным обозначениям:
▲ (конверсия) и ∆ (селективность): LaPO4, полученный из Na2HPO4
■ (конверсия) и □ (селективность): LaPO4, полученный из (NH4)H2PO4
Отмечено, что каталитические свойства катализаторов по изобретению не зависят от используемых предшественников.
ПРИМЕР 3
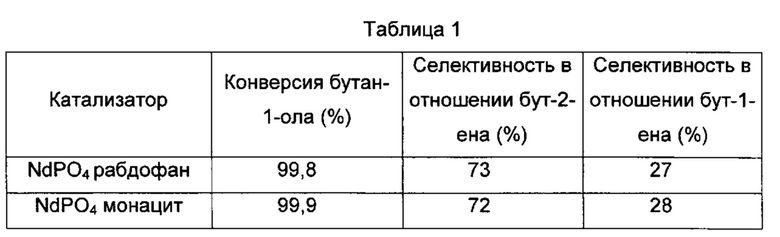
В данном примере ортофосфат неодима в двух разных полиморфных формах (рабдофан и монацит) тестировали в реакции дегидратации бутан-1-ола.
Условия тестирования были следующими: WHSV = 2,38 ч-1; бутан-1-ол/N2 = 1/82,6.
В Таблице 1 показана конверсия спирта и селективность в отношении бут-2-ена при 320°C:
ПРИМЕР 4
50/50 молярную смесь этанола и бутан-1-ола дегидратировали на катализаторе GdPO4 по изобретению и на гамма-оксиде алюминия. Результаты по катализаторам, полученные при 360°C, показаны ниже в Таблице 2.
Удельная поверхность катализатора GdPO4 по изобретению составляет 95 м2/г, и удельная поверхность оксида алюминия составляет 270 м2/г.
Условия тестирования были следующие: WHSV = 2,34 ч-1; N2 = 100 мл.
Оба спирта полностью превращали на фосфатном катализаторе. Данное превращение приводит к получению смеси этилен/бут-2-ен, которая характеризуется молярным соотношением 1,4 и которую можно использовать непосредственно в реакции метатезиса для образования пропена. Также отмечено, что фосфатный катализатор является очень стабильным.

ПРИМЕР 5
Катализаторы LaPO4 и NdPO4 сравнивали с оксидом алюминия в дегидратации бут-3-ен-1-ола.
Удельная поверхность катализаторов NdPO4 и NdPO4 по изобретению составляет 117 м2/г и 124 м2/г соответственно и удельная поверхность оксида алюминия составляет 270 м2/г.
Условия реакции были следующие: WHSV = 2,49 ч-1; 3-бут-1-ен-ол/N2 = 1/76,8.
В Таблице 3 ниже показана конверсия спирта и селективность в отношении бутадиена при 286°C.

ПРИМЕР 6
NdPO4 тестировали и сравнивали с оксидом алюминия в дегидратации изобутанола.
Удельная поверхность катализатора NdPO4 по изобретению составляет 117 м2/г и удельная поверхность оксида алюминия составляет 270 м2/г.
Условия реакции были следующие: WHSV = 2,38 ч-11; изобутанол/N2 = 1/82,6.
Конверсия изобутанола и селективность в отношении изобутена и в отношении бут-2-ена при 245°C приведены в следующей Таблице 4.

ПРИМЕР 7
NdPO4 тестировали в реакции дегидратации бутан-2-ола и сравнивали с оксидом алюминия.
Удельная поверхность катализатора NdPO4 по изобретению составляет 117 м2/г и удельная поверхность оксида алюминия составляет 270 м2/г.
Реакцию проводили при атмосферном давлении в следующих условиях: WHSV = 2,38 ч-1; бутан-2-ол/N2 = 1/82,6; температура реактора = 200°C.

ПРИМЕР 8
В данном примере фосфат неодима тестировали в дегидратации пропан-1-ола.
Удельная поверхность катализатора NdPO4 по изобретению составляет 117 м2/г.
Реакцию проводили при атмосферном давлении в следующих условиях: WHSV = 3,04 ч-1; пропан-1-ол/N2 = 1/49,5; температура реактора = 330°C.
Конверсия пропан-1-ола и селективность в отношении пропена показана в следующей Таблице 6.

ПРИМЕР 9
Фосфат неодима тестировали в качестве катализатора в дегидратации бутан-2,3-диола.
Удельная поверхность катализатора NdPO4 по изобретению составляет 117 м2/г.
Реакцию проводили в следующих условиях:
WHSV = 2,95 ч-1; бутан-2,3-ол/N2 = 1/80,3; температура реактора = 320°C. Результаты по катализатору, которые получали, показаны в следующей Таблице 7.
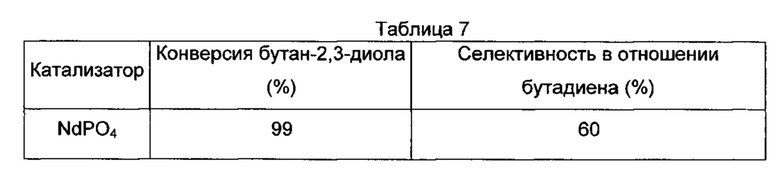
Катализатор является очень активным и селективным в отношении бутадиена.
ПРИМЕР 10
Фосфаты лантана, неодима и гадолиния тестировали в качестве катализаторов в дегидратации бутан-2,3-ола (2,3-BDO).
Условия реакции были следующие: WHSV = 2,98 ч-1; mката = 101 мг, время контакта (W/F) = 30,28 гката⋅ч⋅моль2,3-BDO-1; N2 = 100 мл⋅мин-1 и газовая смесь бутан-2,3-ол/N2 = 1/80,3.
Результаты по катализаторам, которые получали, показаны в следующей Таблице 8.

Катализаторы являются очень активными и селективными в отношении бутадиена.
ПРИМЕР 11
Катализатор GdPO4 тестировали в дегидратации 3-бутен-2-ола.
Условия реакции были следующие: mката = 101 мг; время контакта (W/F) = 28,97 гката⋅ч⋅моль-1; 3-бутен-2-ол/N2 = 1/76,8.
В Таблице 9 показана конверсия 3-бутен-2-ола и селективность в отношении бутадиена при 230°C.

Катализатор является очень активным и селективным в отношении бутадиена.
ПРИМЕР 12
Катализатор GdPO4 тестировали в качестве катализатора для дегидратации бут-3-ен-1,2-диола.
Условия реакции были следующие: mката = 118 мг; время контакта (W/F) = 30,3 гката⋅ч⋅моль-1; спирт/N2 = 1/68; Т = 310°C.
Результаты по катализатору, которые получали, показаны в следующей Таблице 10.

ПРИМЕР 13
SmPO4 тестировали в реакции совместной дегидратации этанола, пропанола и бутанола.
Реакцию проводили при атмосферном давлении в следующих условиях:
время контакта (W/F) = 28,33 гката⋅ч⋅моль-1;
этанол/1-пропанол/2-пропанол/2-бутанол = 10/15/15/60;
N2 = 100 мл⋅мин-1.
Температура реактора = 330°C.
Как указано в следующей Таблице 11, при данной температуре отмечена 100% конверсия всех спиртов и практически 100% селективность в отношении соответствующих алкенов.
ПРИМЕР 14
Катализаторы SmPO4 и NdPO4 исследовали в дегидратации смеси АБЭ (ацетон/бутанол/этанол), которую получали посредством ферментации.
Тест проводили при атмосферном давлении в следующих условиях:
mката = 101 МГ;
время контакта (W/F) = 28,1 гката⋅ч⋅моль-1;
ацетон/1-бутанол/этанол = 3/6/1;
N2 = 100 мл⋅мин-1.
Температура реактора = 330°C.
Результаты показаны в следующей Таблице 12.

ПРИМЕР 15
При получении посредством ферментации бутан-2,3-ол (2,3-BDO) смешивали со значительным количеством воды, которое нужно было устранить выпариванием. Если бы данного разделения можно было бы полностью или частично избежать перед стадией дегидратации до бутадиена, то это, конечно, было бы интересно с экономической точки зрения.
Фосфат гадолиния тестировали в присутствии воды.
Реакцию проводили в следующих условиях:
Температура = 300°C; mката = 101 мг; время контакта (W/F) = 30,28 гката⋅ч⋅моль2,3-ВDO-1; N2 = 100 мл⋅мин-1.
Результаты показаны в следующей Таблице 13 и проиллюстрированы на Фиг. 4.
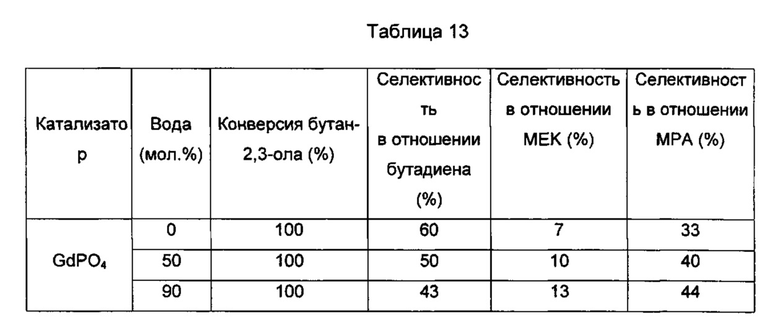
Отмечено, что увеличение количества воды значительно не модифицирует каталитические свойства, но немного снижает селективность в отношении бутадиена.
Влияние воды на стабильность катализатора в условиях реакции также исследовали. Вода имеет весьма положительный эффект на данную стабилизацию.
ПРИМЕР 16
50/50 молярную смесь этанола и 1-бутанола дегидратировали на фосфатах гадолиния, самария и неодима.
Условия каталитической реакции были следующие:
mката = 101 мг; время контакта (W/F) = 25 гката⋅ч⋅моль-1; N2 = 100 мл⋅мин-1.
Результаты по катализаторам, которые получали, показаны ниже в Таблице 14.
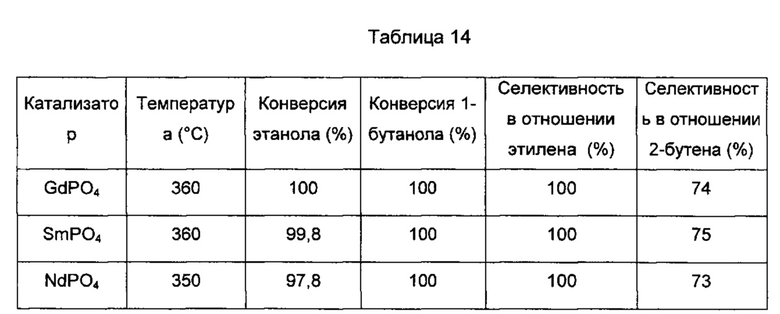
Оба спирта полностью превращали на катализаторах. В случае обеих реакций дегидратации катализаторы являются очень активными и селективными. Катализатор SmPO4 является более селективным в отношении 2-бутена.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОЛЕФИНОВ | 2008 |
|
RU2422420C1 |
| Способ получения диенов | 2016 |
|
RU2692477C2 |
| СПОСОБ ДЕГИДРАТАЦИИ КИСЛОРОДСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 2016 |
|
RU2701863C2 |
| СПОСОБ ПРЕДВАРИТЕЛЬНОЙ ОБРАБОТКИ В УСТАНОВКЕ МЕТАТЕЗИСА С ОБРАЗОВАНИЕМ ОКТЕНА | 2008 |
|
RU2460713C1 |
| Способ получения олефинов @ - @ | 1980 |
|
SU1186084A3 |
| СПОСОБ ПОЛУЧЕНИЯ ОЛЕФИНОВ | 2006 |
|
RU2367644C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКООКТАНОВОГО БЕНЗИНА ИЗ УГЛЕВОДОРОДОВ C4-, СОДЕРЖАЩИХ ОЛЕФИНЫ И БУТАДИЕН | 2004 |
|
RU2277525C1 |
| ИЗОМЕРИЗАЦИЯ В ЖИДКОЙ ФАЗЕ ДЛЯ ПРОЦЕССА МЕТАТЕЗИСА | 2018 |
|
RU2783161C2 |
| БОЛЕЕ ЭНЕРГОЭФФЕКТИВНЫЙ СПОСОБ ГИДРОГЕНИЗАЦИИ С5 | 2013 |
|
RU2627657C2 |
| СПОСОБ РЕГИОСЕЛЕКТИВНОГО ПОЛУЧЕНИЯ Н-ПЕНТАНАЛЯ | 2013 |
|
RU2536048C2 |


Изобретение относится к способу получения олефина, диена или полиена посредством каталитической конверсии по меньшей мере одного спирта, имеющего углеродную цепь по меньшей мере из трех атомов углерода, отличного от пропан-2-ола и глицерина, в присутствии по меньшей мере одного катализатора на основе по меньшей мере одного фосфата металла М или нескольких металлов М, причем М выбран из лантана, празеодима, неодима, прометия, самария, европия, гадолиния, тербия, диспрозия, гольмия, эрбия, тулия, иттербия и лютеция. Также изобретение относится к способам, использующим описанный. Настоящее изобретение предоставляет применение катализаторов, которые являются надежными, активными, селективными и регенерируемыми. 14 н. и 19 з.п. ф-лы, 16 пр., 14 табл., 4 ил.
1. Способ получения олефина, диена или полнена посредством каталитической конверсии по меньшей мере одного спирта, имеющего углеродную цепь по меньшей мере из трех атомов углерода, отличного от пропан-2-ола и глицерина, в присутствии по меньшей мере одного катализатора на основе по меньшей мере одного фосфата металла М или нескольких металлов М, причем М выбран из лантана, празеодима, неодима, прометия, самария, европия, гадолиния, тербия, диспрозия, гольмия, эрбия, тулия, иттербия и лютеция.
2. Способ по п. 1, отличающийся тем, что металл(ы) выбран(ы) из лантана, неодима, гадолиния и самария.
3. Способ по п. 1 или 2, отличающийся тем, что указанный катализатор легирован по меньшей мере одним щелочным металлом, выбранным из цезия, рубидия и калия, и/или переходным металлом, выбранным из групп 4-7.
4. Способ по п. 1, отличающийся тем, что молярное соотношение Р/М варьирует в диапазоне от 0,5 до 2, причем М представляет металл или комбинацию металлов М, которые образуют указанный катализатор.
5. Способ по п. 4, отличающийся тем, что молярное отношение Р/М варьирует в диапазоне от 0,9 до 1,5.
6. Способ по п. 1, отличающийся тем, что катализатор регенерируют, например, на воздухе или разреженном воздухе, который обогащали in situ или ex situ.
7. Способ по п. 1, отличающийся тем, что катализатор содержит активную фазу и подложку и/или связующее вещество, и/или катализатор образован возможно в присутствии связующего вещества.
8. Способ по п. 7, отличающийся тем, что подложка и/или связующее вещество образованы чистым диоксидом кремния (SiO2), диоксидом кремния щелочного металла, щелочноземельного металла или редкоземельных металлов, возможно смешанными друг с другом или с глинами, оксидом титана (TiO2), оксидом бора (В2О2) или смолами (сульфоновые смолы, перфторсульфоновые смолы или другие) или их смесями.
9. Способ по п. 1, отличающийся тем, что конверсию проводят в газовой фазе.
10. Способ по п. 9, отличающийся тем, что конверсию проводят в реакторе с неподвижным слоем, реакторе с псевдоожиженным слоем или реакторе с циркулирующим псевдоожиженным слоем с резервуаром с окислителем (О2, СО2, Н2О и т.д.), или реакторе TZFBR зонального типа (двухзонный реактор с псевдоожиженным слоем).
11. Способ по п. 1, отличающийся тем, что конверсию проводят в жидкой фазе.
12. Способ по п. 1, отличающийся тем, что спирт или спирты являются чистыми, частично очищенными, неочищенными или находятся в форме азеотропных композиций или их смесей.
13. Способ по п. 1, отличающийся тем, что спирт или спирты находятся в водном растворе в концентрации по меньшей мере 1 мас.%.
14. Способ по п. 1, отличающийся тем, что спирт или спирты выбраны из пропан-1-ола, бутан-1-ола, бутан-2-ола, изобутанола, бут-3-ен-1-ола, бут-2-ен-1-ола, бут-3-ен-1,2-диола, бутан-2,3-диола, бутан-1,3-диола, бутан-1,4-диола, пропан-1,2-диола, пропан-1,3-диола, эритритола и их смесей.
15. Способ по п. 1, отличающийся тем, что олефин, диен или полиен имеет углеродную цепь по меньшей мере из трех атомов углерода, и их получают посредством каталитической конверсии спирта или смеси соответствующих спиртов, имеющих углеродную цепь из такого же числа атомов углерода.
16. Способ селективного получения бут-2-ена из бутан-1-ола, бутан-2-ола и их смесей, по любому из пп. 1-15.
17. Способ получения изобутена из изобутанола по любому из пп. 1-15.
18. Способ получения смеси олефинов, диенов и/или полиенов по любому из пп. 1-17.
19. Способ получения смеси по меньшей мере двух олефинов, диенов и/или полиенов, отличающийся тем, что один из олефинов, диенов и/или полиенов получают способом по любому из пп. 1-17.
20. Способ по п. 19, отличающийся тем, что по меньшей мере другой(ие) олефин(ы), диен(ы) и/или полиен(ы) получают посредством каталитической конверсии спирта или смеси спиртов в присутствии по меньшей мере одного катализатора на основе по меньшей мере одного фосфата по меньшей мере одного металла М, причем указанный металл М выбран из лантана, церия, празеодима, неодима, прометия, самария, европия, гадолиния, тербия, диспрозия, гольмия, эрбия, тулия, иттербия и лютеция.
21. Способ по п. 20, отличающийся тем, что катализаторы являются идентичными или разными.
22. Способ по п. 20 или 21, отличающийся тем, что указанный катализатор, используемый для получения другого(их) олефина(ов), диена(ов), полиена(ов), содержит активную фазу и подложку и/или связующее вещество, и/или катализатор образован возможно в присутствии связующего вещества.
23. Способ по п. 19, отличающийся тем, что указанный катализатор, используемый для получения другого(их) олефина(ов), диена(ов), полиена(ов), регенерируют.
24. Способ по п. 18 или 19, отличающийся тем, что по меньшей мере два олефина, диена, полиена получают в одном и том же реакторе или в разных реакторах.
25. Способ получения пропена, включающий получение пропена способом по любому из пп. 1-15, при этом спирт выбран из пропан-1-ола, возможно смешанного с пропан-2-олом.
26. Способ получения пропена, включающий получение бутена способом по любому из пп. 1-16, при этом спирт выбран из бутан-1-ола, бутан-2-ола и их смесей, и затем конверсию данного бутена в пропен посредством метатезиса.
27. Способ получения пропена, включающий получение смеси этилена и бутена способом по любому из пп. 19-24, при этом по меньшей мере один спирт выбран из этанола, а другой спирт выбран из бутан-1-ола, бутан-2-ола и их смесей, и затем конверсию смеси этилена и бутена в пропен посредством метатезиса.
28. Способ получения бутадиена, отличающийся тем, что в нем осуществляют способ по любому из пп. 1-16, при этом спирт выбран из бут-2-ен-1-ола, бут-3-ен-1-ола, бут-1-ен-3-ола, бут-3-ен-1,2-диола, бутан-2,4-диола, бутан-1,3-диола, бутан-2,3-диола и бутан-1,4-диола и их смесей.
29. Способ получения акролеина из пропена, отличающийся тем, что в нем осуществляют способ по любому из пп. 1-27.
30. Способ получения альдегид-3-(метилтио)пропионовой кислоты (ММР) из акролеина, отличающийся тем, что в нем осуществляют способ по п. 29.
31. Способ получения нитрила 2-гидрокси-4-метилтиомасляной кислоты (HMTBN) из акролеина, отличающийся тем, что в нем осуществляют способ по п. 29.
32. Способ получения 2-гидрокси-4-метилтиомасляной кислоты (НМТВА) и ее сложных эфиров из акролеина, отличающийся тем, что в нем осуществляют способ по п. 29.
33. Способ получения 2-оксо-4-метилтиобутановой кислоты (KMB) из акролеина, отличающийся тем, что в нем осуществляют способ по п. 29.
| 0 |
|
SU317500A1 | |
| JEWUR S.S | |||
| et al., The role of acidity of boron phosphate in the activity and selectivity of the dehydration of alcohols, JOURNAL OF CATALYSIS, 01.01.1979, vol | |||
| Способ получения на волокне оливково-зеленой окраски путем образования никелевого лака азокрасителя | 1920 |
|
SU57A1 |
| Прибор для запора стрелок | 1921 |
|
SU167A1 |
| СПОСОБ ПРОИЗВОДСТВА ГОРОХОВОГО КОНЦЕНТРАТА БЫСТРОГО ПРИГОТОВЛЕНИЯ | 1998 |
|
RU2157074C2 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| СПОСОБ ПОЛУЧЕНИЯ АКРОЛЕИНА И/ИЛИ АКРИЛОВОЙ КИСЛОТЫ | 2001 |
|
RU2285690C2 |
Авторы
Даты
2018-07-10—Публикация
2014-02-04—Подача