Предлагаемое изобретение относится к фармакологии и медицине, может быть использовано для создания лекарственных препаратов, применяемых с целью лечения и профилактики тромбоза.
В качестве средств лечения состоявшегося тромбоза в зависимости от локализации в сосудистом русле и давности возникновения применяют препараты из групп антикоагулянтов и антиагрегантов [Bates SM, Jaeschke R, Stevens SM, Goodacre S, Wells PS, Stevenson MD, Kearon C, Schunemann HJ, Crowther M, Pauker SG, Makdissi R, Guyatt GH. Diagnosis of DVT: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012;141(2 Suppl):e351S-e418S.].
Наиболее близким аналогом изобретения является ацетилсалициловая кислота, применение которой показано при остром инфаркте миокарда [Uzu К, Shinke Т, Otake Н, Takaya Т, Osue Т, et al. Morphological and pharmacological determinants of peri-procedural myocardial infarction following elective stent implantation: Optical coherence tomography sub-analysis of the PRASFIT-Elective study. J Cardiol. 2017: S0914-5087(17)30146-6.], тромбоэмболии легочной артерии [Poullis M. Aspirin for the treatment of pulmonary embolism: vasoconstriction versus physical obstruction. Am Heart J2000;140:E22.] и ишемическом инсульте [Zhou X, Tian J, Zhu MZ, He CK.A systematic review and meta-analysis of published randomized controlled trials of combination of clopidogrel and aspirin in transient ischemic attack or minor stroke. Exp Ther Med. 2017;14(l):324-332.].
Задачей изобретения является расширение арсенала биологически активных веществ, в том числе обладающих профилактической и терапевтической эффективностью при тромбозе.
Технический результат - получение биологически активного вещества, проявляющего профилактическую и терапевтическую эффективность при тромбозе посредством блокирования ГП IIb-IIIa рецепторов тромбоцитов.
Сущность изобретения: применение 3-метил-8-(пиперазин-1-ил)-7-(тиетан-3-ил)-1-этил-1H-пурин-2,6(3H,7H)-диона гидрохлорида (I) формулы:
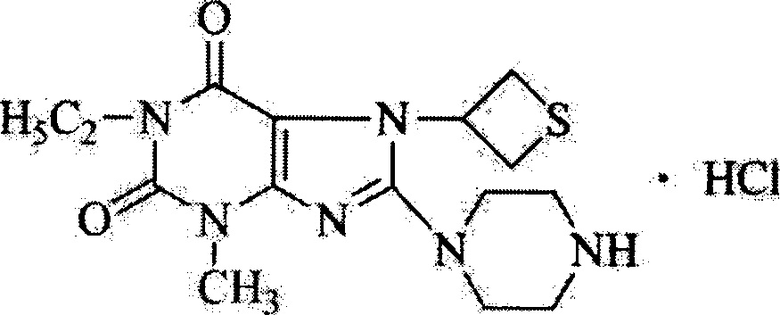
I
в качестве средства для лечения профилактики и лечения тромбоза посредством блокирования ГП IIb-IIIa рецепторов тромбоцитов.
Синтез соединения I осуществляется по методике [Халиуллин Ф.А. 3-Метил-8-пиперазино-7-(тиетанил-3)-1-этилксантина гидрохлорид, проявляющий антиагрегационную и дезагрегационную активность / Ф.А. Халиуллин, Ю.В. Шабалина, Г.А. Тимирханова, Ф.Х. Камилов, А.В. Самородов, P.M. Шарафутдинов // Патент РФ №2404181 от 20.11.2010.].
Известно, что пентоксифиллин и эуфиллин, которые по химической природе являются производными ксантина, проявляют высокую антиагрегационную и дезагрегационную фармакологическую активность [Государственный реестр лекарственных средств. / Официальное издание. - М.: Медицина, 2004. - Т. 2. - 1791 с.]. Необходимо отметить, что подавляющее большинство лекарственных препаратов с установленной антиагрегационной и/или дезагрегационной активностью (в т.ч. и группа метилксантинов) не применяются в качестве средств профилактики и лечения тромбоза. А последнее поколение антиагрегационных препаратов, селективные блокаторы рецепторов тромбоцитов ГП IIb-IIIa, применяются только в одном случае - в условиях сопровождения эндоваскулярного вмешательства на коронарных артериях и не могут выступать в качестве препаратов-прототипов в данной заявке. Известно, что соединение I проявляет антиагрегационную и дезагрегационную активность в отношении тромбоцитов в условиях in vitro на донорской крови здоровых добровольцев [Халиуллин Ф.А. 3-Метил-8-шшеразино-7-(тиетанил-3)-1-этилксантина гидрохлорид, проявляющий антиагрегационную и дезагрегационную активность / Ф.А. Халиуллин, Ю.В. Шабалина, Г.А. Тимирханова, Ф.Х. Камилов, А.В. Самородов, P.M. Шарафутдинов // Патент РФ №2404181 от 20.11.2010.]. Применение 3-метил-8-(пиперазин-1 -ил)-7-(тиетан-3-ил)-1-этил-1H-пурин-2,6(3H,7H)-диона гидрохлорида в качестве средства профилактики и/или лечения тромбоза посредством блокирования рецепторов тромбоцитов ГП IIb-IIIa не известно.
Так как тромбоз нижней каудальной (полой) вены у крыс является эквивалентом тромбоза глубоких вен (основным источником тромбоэмболов при возникновении тромбоэмболии легочной артерии), мезентериального тромбоза и тромбоза нижней полой вены у человека, профилактическую и терапевтическую эффективность соединения I оценили на модели тромбоза нижней полой вены у крыс. Для изучения эффективности соединения I и препаратов сравнения в качестве средств для профилактики тромбоза проводили внутривенное введение исследуемых веществ за 1 час до моделирования тромбоза нижней полой вены. Терапевтическая эффективность препаратов оценивалась моделированием тромбоза нижней полой вены с последующим внутривенным введением изучаемых веществ через каждые 24 часа в течение 7 суток в эквимолярных дозировках. Животных опытной группы предварительно взвешивали и вводили однократно внутривенно исследуемый препарат. Животным контрольной группы вводили соответствующее количество стерильного 0,9% раствора NaCl. Вторая группа контроля была представлена группой ложнооперированных крыс (ЛОК): животных подвергали наркотизации и лапаротомии без инициации тромбоза.
Моделирование тромбоза нижней полой вены.
Экспериментальным животным под наркозом (тиопентал натрия 50 мг/кг внутрибрюшинно) проводили срединную лапаротомию. Освобождали от соединительной ткани участок нижней полой вены длиной 3 см в каудальном направлении от места впадения левой почечной вены, подводили под нижнюю полую вену лигатуру и завязывали ее, полностью перекрывая просвет сосуда. Рану ушивали [Henke РК et al, 2007]. Моделирование тромбоза нижней полой вены проведено на 80 белых лабораторных крысах. До начала лечения погибло 8 крыс, что полностью соответствует данным литературы о закономерном летальном исходе вследствие острого тромбоза. Выжившие крысы распределились на группы лечения (по 20 особей), каждая из которых были разделены для отбора материала на две подгруппы: 1-е и 7-е сутки (по 10 животных в каждой подгруппе) лечения.
После вывода животных из эксперимента оценивали эффективность терапевтического эффекта по следующим показателям: выживаемость-падеж, разница масс влажного и сухого тромбов, результаты гистологических исследований, маркеры внутрисосудистого тромбоза.
Для определения массы тромбов у одной половины крыс каждой группы крыс в условиях общей анестезии открывали брюшную полость, продольным разрезов вскрывали просвет нижней полой вены, извлекали образовавшийся тромб. Извлеченный тромб взвешивали на аналитических весах: массу влажного тромба определяли непосредственно после изъятия, массу сухого тромба - через 7 суток высушивания при 37°С в сухожаровом шкафу ГП 20 СПУ (ОАО "Смоленское СКТБ СПУ", Россия).
Определение циркулирующих агрегатов проводили по методу Wu & Hoak в модификации FH Kohanna. Для этого кровь из вены набирали в две пробирки, в одной из которых содержится раствор ЭДТА, а в другой -смесь такого же раствора ЭДТА с 4% раствором формалина. После перемешивания содержимое пробирок отстаивали 30 мин при комнатной температуре. Во время отстаивания агрегаты оседают, а отдельные тромбоциты остаются в надосадочном слое. После отстаивания подсчитывали число тромбоцитов в надосадочном слое в каждой из пробирок.
Оценка связывания с тромбоцитарными рецепторами ГП IIb-IIIa.
Эффект связывания соединения I и аграстата с тромбоцитарными рецепторами ГП IIb-IIIa определяли методом проточной цитометрии на крови здоровых доноров-мужчин в возрасте 18-24 лет. Исследование было одобрено этическим комитетом ФГБОУ ВО «Башкирский государственный медицинский университет» Минздрава России (№2 от 17.10.2012). Информированное согласие было получено у всех участников исследования до забора крови. Взятие крови проводили из локтевой вены в стерильных условиях с использованием систем вакуумного забора крови BD Vacutainer® (Dickinson and Company, США). В качестве стабилизатора венозной крови использовали 3,8% раствор цитрата натрия в соотношении 9:1. Для исключения влияния других форменных элементов крови вся исследовательская работа была проведена на образцах обогащенной тромбоцитами плазмы (PRP). Образцы богатой тромбоцитами плазмы получали центрифугированием цитратной крови при 100g в течение 10 минут. В работе использовалась центрифуга ОПН-3.02 (ОАО ТНК «ДАСТАН», Киргизия). Далее определяли эффект связывания с тромбоцитарными рецепторами ГП IIb-IIIa флюоресцентно-мечеными антителами против CD61 и CD41a. Для этого вносили по 10 мкл PRP в пластиковые пробирки, разводили в 100 раз фосфатно-солевым буферным раствором (PBS). Образцы инкубировали 5 мин при комнатной температуре. После инкубации с исследуемым веществом и препаратами сравнения образцы PRP инкубировали 20 мин при комнатной температуре с моноклональными антителами CD41a, мечеными РЕ (фикоэритрином) и CD61, мечеными FITC (флюоресцеинизотиоционатом), (Becton Dickinson, США), согласно рекомендациям производителя. Цитофлюориметрический анализ проводили на приборе BD FACSCanto II (Becton Dickinson Immunocytometry Systems, США), используя программное обеспечение «FACSDiva». Параметры настройки прибора были одинаковы для всех измерений. Для каждой пробы собирали не менее 10000 событий. «Тромбоцитарное окно» выделяли по параметрам прямого (FCS) и малоугольного (SSC) светорассеяния в логарифмической шкале координат. Оценивали количество позитивных клеток (%) по CD41a и CD61. Результат представлен в IC50 - концентрации, связывающей 50% тромбоцитарных рецепторов ГП IIb-IIIa по интегринам CD41a и CD61.
В качестве препаратов сравнения были выбраны: препараты из группы антиагрегантов - К-(бутилсульфонил)-4-[4-(4-пиперидин)бутокси]-α-фенилаланина моногидрохлорид моногидрат («Аграстат», Correvio, Великобритания), L-цистеинамид, М6-(аминоиминометил)-N2-(3-меркапто-1-оксопропил)-L-лизилглицил-L-α-аспартил-L-триптофи-L-пропил-,циклический(1-6)-дисульфид (Эптифибатид, «Интегрилин», Glaxo Operations UK Limited, Великобритания) и 2-ацетилоксибензойная кислота («Ацетилсалициловая кислота», Фармацевтическая фабрика Шандонг Ксинхуа Фармасьютикал Ко., ЛТД, Китай) и из группы антикоагулянтов - эноксипарин натрия ("Клексан", Санофи-Авентис Франс, Франция).
Результаты исследования обработаны с применением статистического пакета Statistica 10,0 (StatSoft Inc, США). Проверку на нормальность распределения фактических данных выполняли с помощью критерия Шапиро-Уилка. Выявлено, что вид распределения полученных данных отличается от нормального, поэтому при дальнейшей работе использовались непараметрические методы. Данные представлены в виде медианы, 25 и 75 процентилей. Дисперсионный анализ проводили с помощью критерия Краскела-Уоллиса (для независимых наблюдений) и Фридмена (для повторных наблюдений). Анализ выживаемости проведен при помощи метода Каплана-Мейера. Различия выживаемости между группами оценивались при помощи критерия Вилкоксона. Критический уровень значимости р для статистических критериев принимали равным 0,05.
Оценка соединения I, как средства профилактики тромбоза.
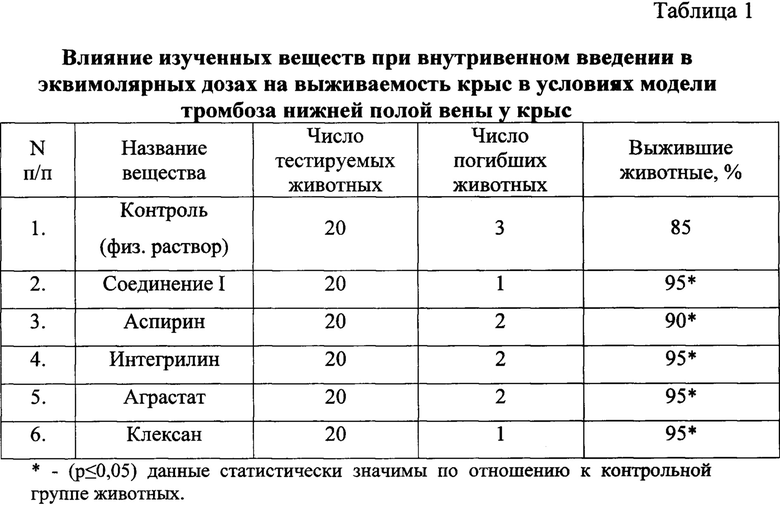
Анализ суточной выживаемости (таблица 1) демонстрирует, что в группе ложнооперированных крыс падеж отсутствовал, в группе физиологического раствора летальность животных от тромбоза составила 15%, в группах лекарственных препаратов и соединения I убыль животных до вывода из эксперимента не превышала 10%.
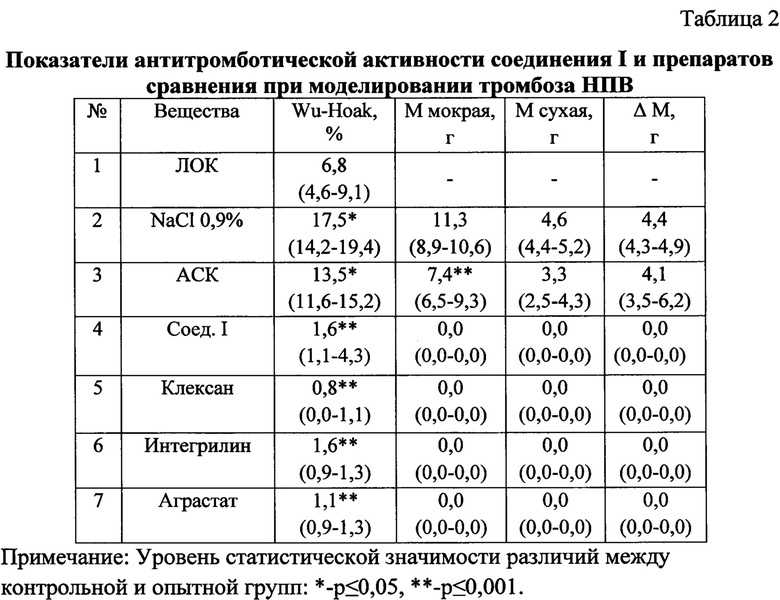
Объективные показатели тромбоза представлены в таблице 2. Из данных таблицы 2 видно, что аспирин снижал массивность тромбоза по данным масс свежих и сухих тромбов соответственно на 34,5% и 27,4% в сравнении с контролем, несмотря на регистрацию циркулирующих тромбоцитарных агрегатов ≥15% по методу Wu-Hoak. Однако разница масс свежих и сухих тромбов для групп физиологического контроля и аспирина статистически не имела различий и в среднем составляла 4,4%. Введение аграстата, клексана и соединения I эффективно препятствовало образованию тромба в условиях полной окклюзии - при визуальном осмотре участков нижней полой вены признаков тромбоза нет. Количество тромбоцитарных агрегатов, рассчитанных по методу Wu-Hoak, при перевязке нижней полой вены оставались в пределах контрольных значений.
Оценка соединения I, как средства лечения тромбоза.
Показатели 7 дневной выживаемости представлены в таблице 3. Из данных таблицы 3 видно, применение аспирина увеличивает продолжительность жизни на 41,6%, а аграстата и клексана на 47,3% и 48,9% соответственно по сравнению с группой физиологического контроля. Летальность в группе соединения I не регистрировалась и продолжительность жизни соответствовала группе ложнооперированных крыс без тромбоза.
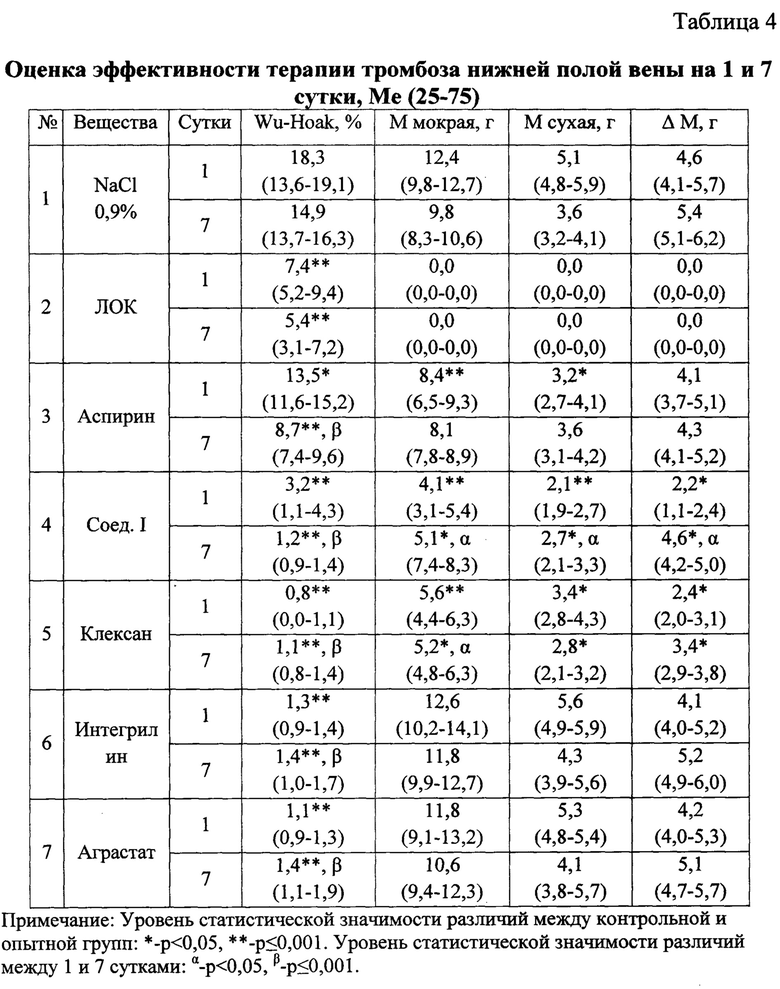
В таблице 4 представлены результаты исследования масс тромбов и содержание циркулирующих тромбоцитарных агрегатов. Установлено, что на фоне терапии аграстатом количество тромбоцитарных агрегатов по Wu-Hoak оставались на уровне значений интактных крыс. Однако массы свежих и сухих тромбов соответствуют группе физиологического раствора. Количество тромбоцитарных агрегатов по Wu-Hoak в группе аспирина на первые сутки лечения меньше на 26,3%, а на седьмые сутки на 41,6% в сравнении с группой физиологического раствора. Масса свежих тромбов в группе аспирина уже на первые сутки составляла 41,3% массы тромбов группы физиологического раствора, однако на 7 сутки разницы в данном показателе не регистрировалось. Терапия клексаном значительно снижает количество циркулирующих тромбоцитарных агрегатов по методу Wu-Hoak: данный показатель в первые сутки в 22,3 раза, на 7 сутки терапии в 13,5 раз меньше значений крыс, получивших физиологический раствор. Показатели масс тромбов в группе клексана составляла 46,4% в первые и 58,6% на седьмые сутки терапии от свежих тромбов группы физиологического раствора. Применение соединения I в качестве средства лечения тромбоза демонстрирует его наибольшую эффективность - содержание тромбоцитарных агрегатов, рассчитанных по методу Wu-Hoak, регистрируются на уровне значений интактных крыс, а показатель массы свежеизвлеченных тромбов снижается эффективнее, чем при использовании других препаратов сравнения.
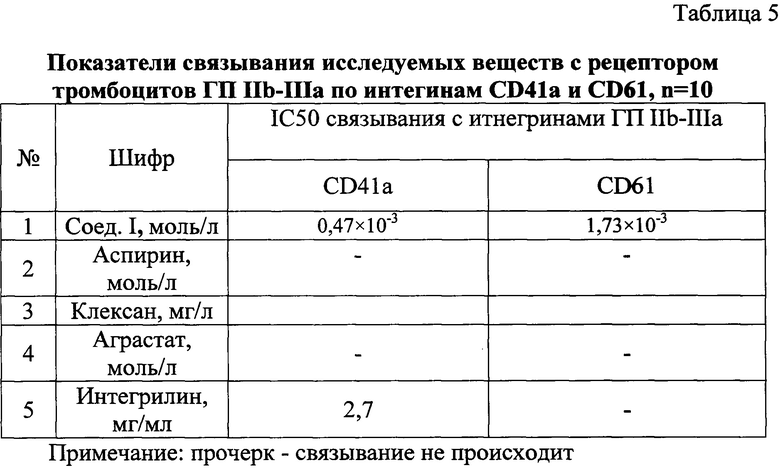
Оценка связывания соединения I с рецепторами ГП IIb-IIIa тромбоцитов.
Аспирин и клексан, используемые на данном этапе исследования в качестве отрицательного контроля, не имеют сродство к рецептору ГП IIb-IIIa тромбоцитов. Применяемые в клинической практике препараты группы блокаторов рецепторов тромбоцитов ГП IIb-IIIa имеют разное сродство с этим рецептором по интегринам CD41a и CD61. Аграстат не обладает эффектом связывания с рецептором ГП IIb-IIIa по интегринам CD41a и CD61. Интегрилин связывается с рецептором только по интегрину CD41a. Соединение I имеет более селективное сродство с тромбоцитарным рецептором ГП IIb-IIIa по интегринам CD41a и CD61 (таблица 5).
Таким образом, установлено, что соединение I эффективнее, и как средство профилактики и как средство лечения тромбоза, препарата прототипа - ацетилсалициловой кислоты и всех выбранных препаратов сравнения. В сравнении с последним поколением антиагрегационных препаратов - блокаторов рецептора тромбоцита ГП IIb-IIIa, соединение I характеризуется более эффективным связыванием по интегринам CD41a и CD61 с рецептором ГП IIb-IIIa, что и обуславливает его очевидную эффективность.

| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ АНТИТРОМБОТИЧЕСКИЙ ЭФФЕКТ ПОСРЕДСТВОМ БЛОКИРОВАНИЯ РЕЦЕПТОРОВ ТРОМБОЦИТОВ ГП IIb-IIIa (ВАРИАНТЫ) | 2016 |
|
RU2643336C1 |
| ГИДРОХЛОРИДЫ 1-АЛКИЛ-3-МЕТИЛ-8-ПИПЕРАЗИНО-7-(ТИЕТАНИЛ-3)КСАНТИНА, ПРОЯВЛЯЮЩИЕ АНТИТРОМБОТИЧЕСКИЙ ЭФФЕКТ ПОСРЕДСТВОМ БЛОКИРОВАНИЯ РЕЦЕПТОРОВ ТРОМБОЦИТОВ ГП IIb-IIIa | 2017 |
|
RU2640579C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ У КРЫС | 2015 |
|
RU2610212C1 |
| Средство с антиагрегационной активностью и способ его получения | 2021 |
|
RU2778686C1 |
| АНТИТРОМБОТИЧЕСКИЙ ПРЕПАРАТ И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ТРОМБОЗОВ | 2002 |
|
RU2205027C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ВНУТРИСОСУДИСТОЙ АКТИВАЦИИ ТРОМБОЦИТОВ | 2009 |
|
RU2416796C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИАГРЕГАНТНОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2709017C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ АНТИАГРЕГАНТНОГО ПРЕПАРАТА В ОБРАЗЦАХ ЦЕЛЬНОЙ ПЕРИФЕРИЧЕСКОЙ КРОВИ | 2022 |
|
RU2800671C1 |
| Производные триазола, проявляющие антиагрегационную активность | 2021 |
|
RU2770405C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ДЕЙСТВИЯ АНТИАГРЕГАНТНЫХ ПРЕПАРАТОВ, ВЛИЯЮЩИХ НА МЕТАБОЛИЗМ АРАХИДОНОВОЙ КИСЛОТЫ ПУТЕМ ИНГИБИРОВАНИЯ ЦИКЛООКСИГЕНАЗЫ-1 КАК В ОТДЕЛЬНОСТИ, ТАК И СОВМЕСТНО С АНТАГОНИСТОМ РЕЦЕПТОРА АДФ P2Y НА ТРОМБОЦИТАРНЫХ МЕМБРАНАХ, НА СОСТОЯНИЯ ТРОМБОЦИТОВ КРОВИ ПАЦИЕНТА, ПРИНИМАЮЩЕГО АНТИАГРЕГАНТНЫЕ ПРЕПАРАТЫ УКАЗАННОЙ ГРУППЫ | 2010 |
|
RU2442167C1 |
Изобретение относится к фармацевтической промышленности и медицине и представляет собой применение 3-метил-8-(пиперазин-1-ил)-7-(тиетан-3-ил)-1-этил-1H-пурин-2,6(3H,7H)-диона гидрохлорида в качестве средства для лечения и профилактики тромбоза посредством блокирования рецептора тромбоцитов ГП IIb-IIIa. Изобретение обеспечивает расширение арсенала средств, обладающих терапевтической и профилактической активностями в отношении тромбоза посредством блокирования рецептора тромбоцитов ГП IIb-IIIa. 5 табл.
Применение 3-метил-8-(пиперазин-1-ил)-7-(тиетан-3-ил)-1-этил-1H-пурин-2,6(3H,7H)-диона гидрохлорида в качестве средства для лечения и профилактики тромбоза.
| Инструкция по медицинскому применению препарата Аспирин, дата регистрации 13.12.2007, найдено в Интернете на сайте: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=712d0942-5c3e-4391-96b3-08f47af0de08&t=; | |||
| АНТИТРОМБОТИЧЕСКИЙ ПРЕПАРАТ И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ТРОМБОЗОВ | 2002 |
|
RU2205027C1 |
| Способ получения молибдата кальция | 1931 |
|
SU26701A1 |
| ПРОИЗВОДНЫЕ ЦИННАМОИЛ-ПИПЕРАЗИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ PAR-1 | 2007 |
|
RU2440997C2 |
| 3-МЕТИЛ-8-ПИПЕРАЗИНО-7-(ТИЕТАНИЛ-3)-1-ЭТИЛКСАНТИНА ГИДРОХЛОРИД, ПРОЯВЛЯЮЩИЙ АНТИАГРЕГАЦИОННУЮ И ДЕЗАГРЕГАЦИОННУЮ АКТИВНОСТЬ | 2009 |
|
RU2404181C1 |
| US 4218476 A1, 19.08.1980. | |||
Авторы
Даты
2018-07-25—Публикация
2017-12-25—Подача