Область техники
Настоящее изобретение относится к новой кристаллической форме метансульфоната 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида и содержащей его фармацевтической композиции.
Настоящее изобретение выполнено в рамках национального научно-исследовательского проекта (конкретный номер проекта: KDDF-201210-04; идентификационный номер проекта: 1345193908; название научно-исследовательской работы: разработка нового терапевтического средства для ингибирования фактора свертывания крови Xa).
Уровень техники
Метансульфонат 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида следующей формулы (1) известен как ингибитор фактора свертывания крови Xa и используется для лечения и предупреждения тромбоза, инфаркта миокарда, артериосклероза, воспаления, инсульта, стенокардии, рецидивирующей стриктуры после ангиопластики и тромбоэмболии, в частности перемежающейся хромоты (см. патент США № 817825).
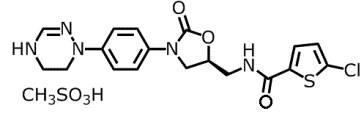
(1)
Согласно рекомендациям и инструкциям, опубликованным органом по регулированию лекарственных средств в различных странах, для получения предпродажного одобрения лекарственного препарата требуется стабильность кристаллического лекарственного средства. Соответственно, существует потребность в разработке новой кристаллической формы метансульфоната 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида, обладающей превосходной скоростью растворения и стабильностью даже при высокой температуре и во влажной окружающей среде.
Сущность изобретения
Цель настоящего изобретения состоит в разработке новой кристаллической формы метансульфоната 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида, однородной и стабильной.
Другая цель настоящего изобретения состоит в разработке содержащей новую кристаллическую форму фармацевтической композиции для лечения или предупреждения, по меньшей мере, одного из заболеваний или симптомов, выбранных из группы, состоящей из тромбоза, инфаркта миокарда, артериосклероза, воспаления, инсульта, стенокардии, рецидивирующей стриктуры после ангиопластики и тромбоэмболии, в частности, перемежающейся хромоты.
Согласно одному из аспектов настоящего изобретения предоставляется безводный кристаллический метансульфонат 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида, рентгеновский порошковый спектр дифракции которого с использованием Cu-Kα-излучения содержит пики при угле дифракции 2θ, равном 4,302, 8,621, 9,606, 12,103, 12,879, 15,648, 17,353, 17,949, 19,26, 19,577, 20,252, 21,792, 23,108, 23,356, 25,76 и 27,463.
Согласно еще одному аспекту настоящего изобретения предоставляется безводный кристаллический метансульфонат 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида, рентгеновский порошковый спектр дифракции которого с использованием Cu-Kα-излучения содержит пики при угле дифракции 2θ, равном 12,022, 15,721, 15,971, 18,125, 18,928, 19,979, 20,311, 20,726, 21,66, 22,805, 23,18, 23,985, 25,857, 27,25, 27,829, 28, 28,189 и 29,753.
Настоящее изобретение также предоставляет фармацевтическую композицию, содержащую в качестве активного ингредиента безводный кристаллический метансульфонат 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида.
Новое кристаллическое соединение по изобретению обладает превосходной скоростью растворения и стабильностью даже при высокой температуре и во влажной окружающей среде, и поэтому может эффективно применяться для предупреждения или лечения, по меньшей мере, одного из заболеваний или симптомов, выбранных из группы, состоящей из тромбоза, инфаркта миокарда, артериосклероза, воспаления, инсульта, стенокардии, рецидивирующей стриктуры после ангиопластики и тромбоэмболии, в частности, перемежающейся хромоты.
Краткое описание чертежей
Вышеуказанные и другие цели и отличительные признаки настоящего изобретения станут очевидными из следующего описания изобретения, рассматриваемого вместе с сопровождающими чертежами, которые соответственно представляют:
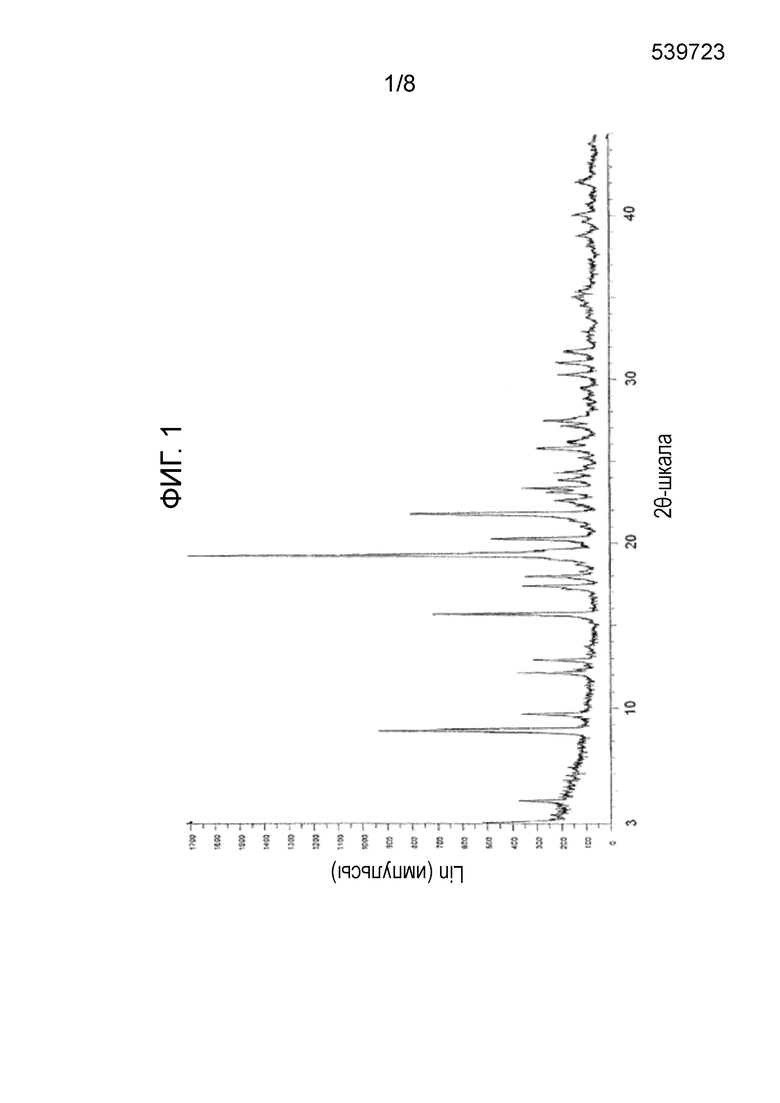
Фиг. 1 показывает результаты анализа порошковой рентгеновской дифракцией (PXRD) кристаллической формы 1.
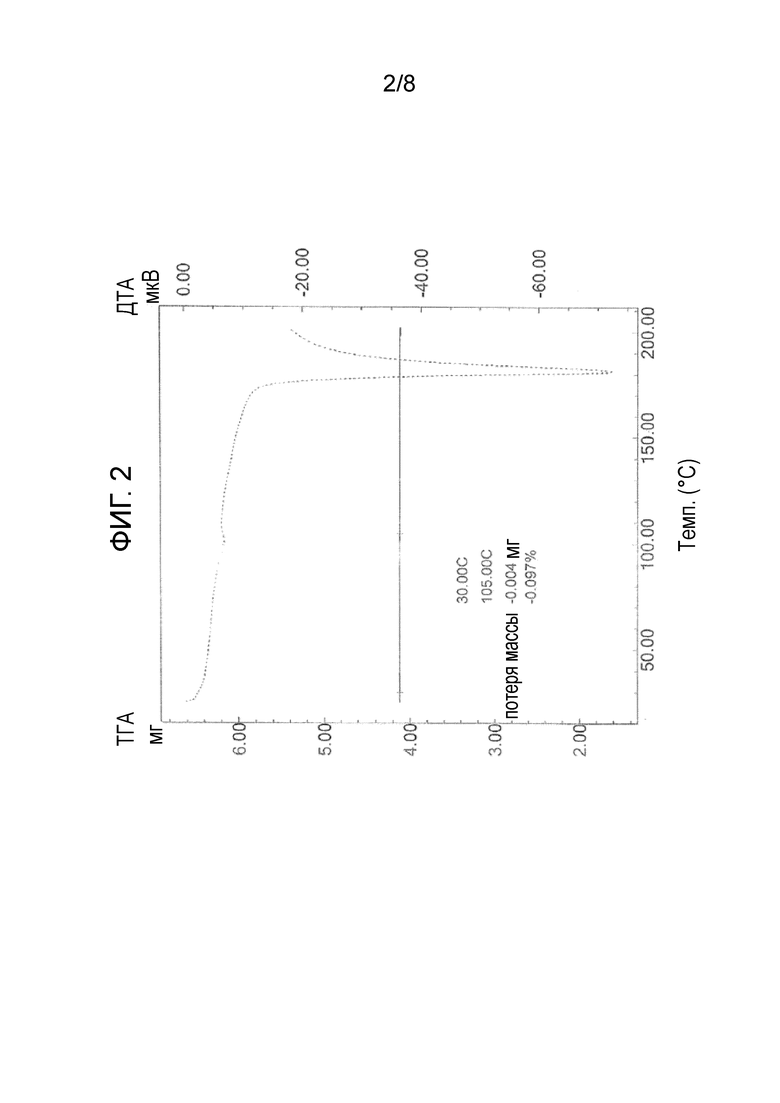
Фиг. 2 показывает результаты термогравиметрического анализа (ТГА) кристаллической формы 1.
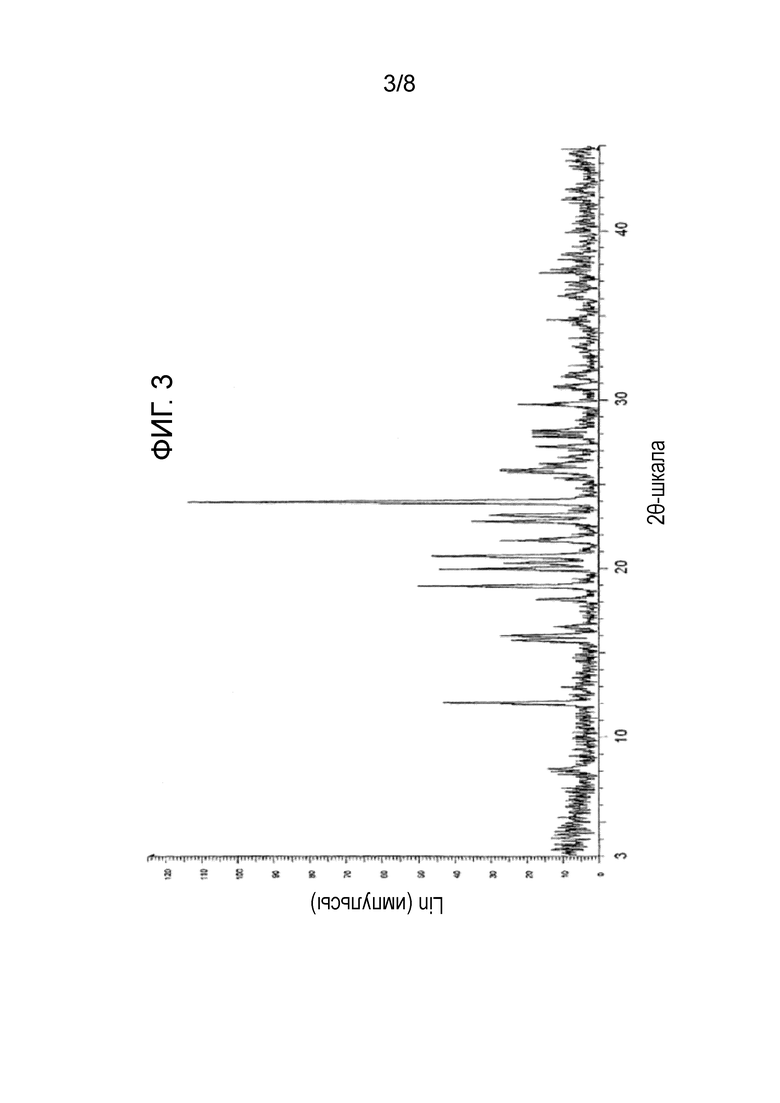
Фиг. 3 показывает результаты анализа порошковой рентгеновской дифракцией кристаллической формы 5.
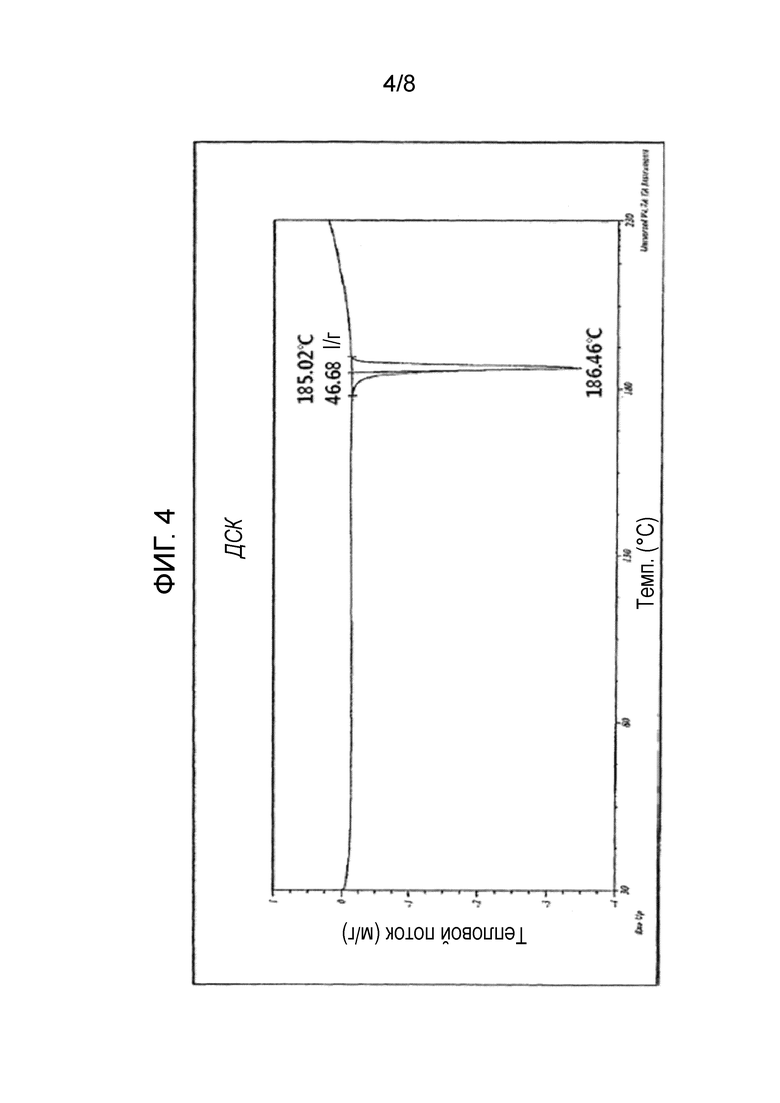
Фиг. 4 показывает результаты анализа дифференциальной сканирующей калориметрией кристаллической формы 5.
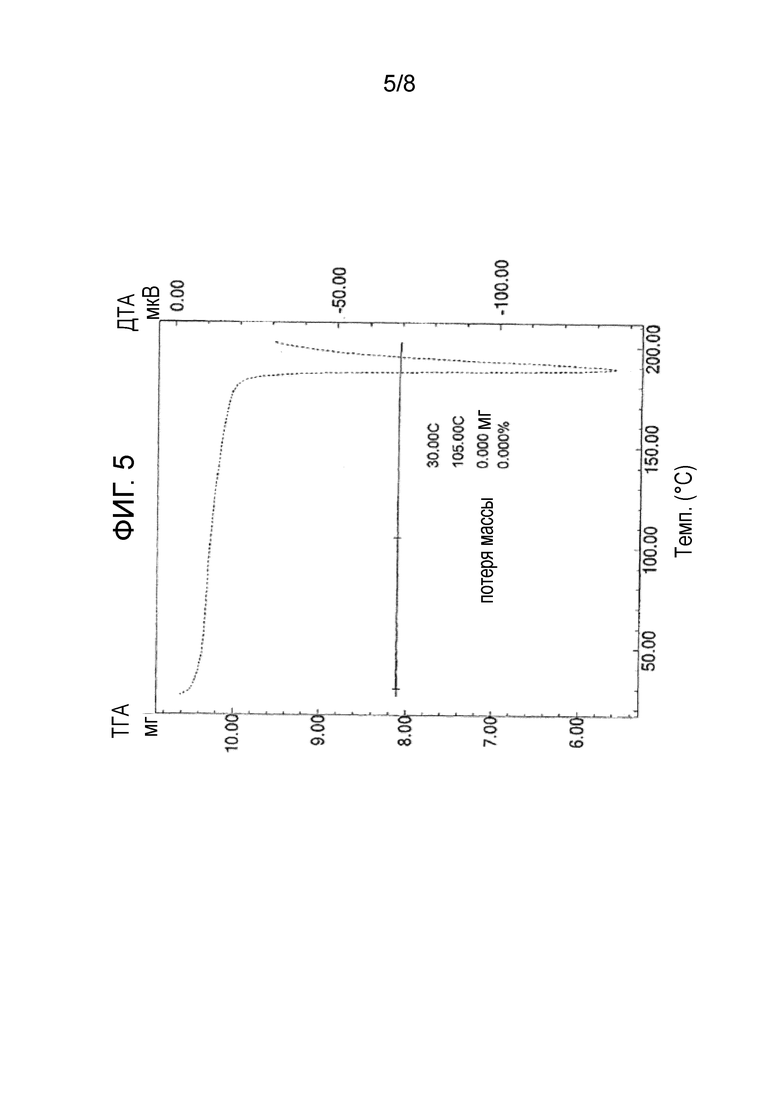
Фиг. 5 показывает результаты термогравиметрического анализа кристаллической формы 5.
Фиг. 6 представляет фотографии кристаллических форм 1 и 5, сделанные с помощью поляризационного микроскопа.
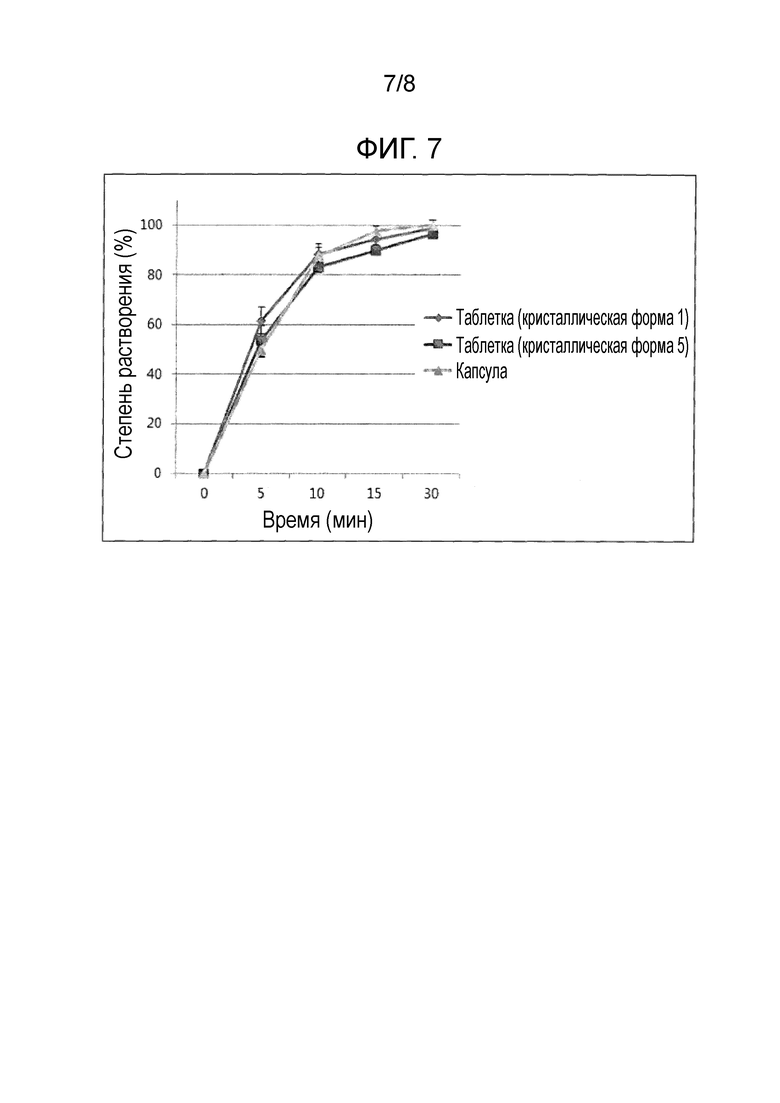
Фиг. 7 представляет график сравнения скоростей растворения капсул и таблеток, содержащих кристаллическую форму 1 или 5 по настоящему изобретению.
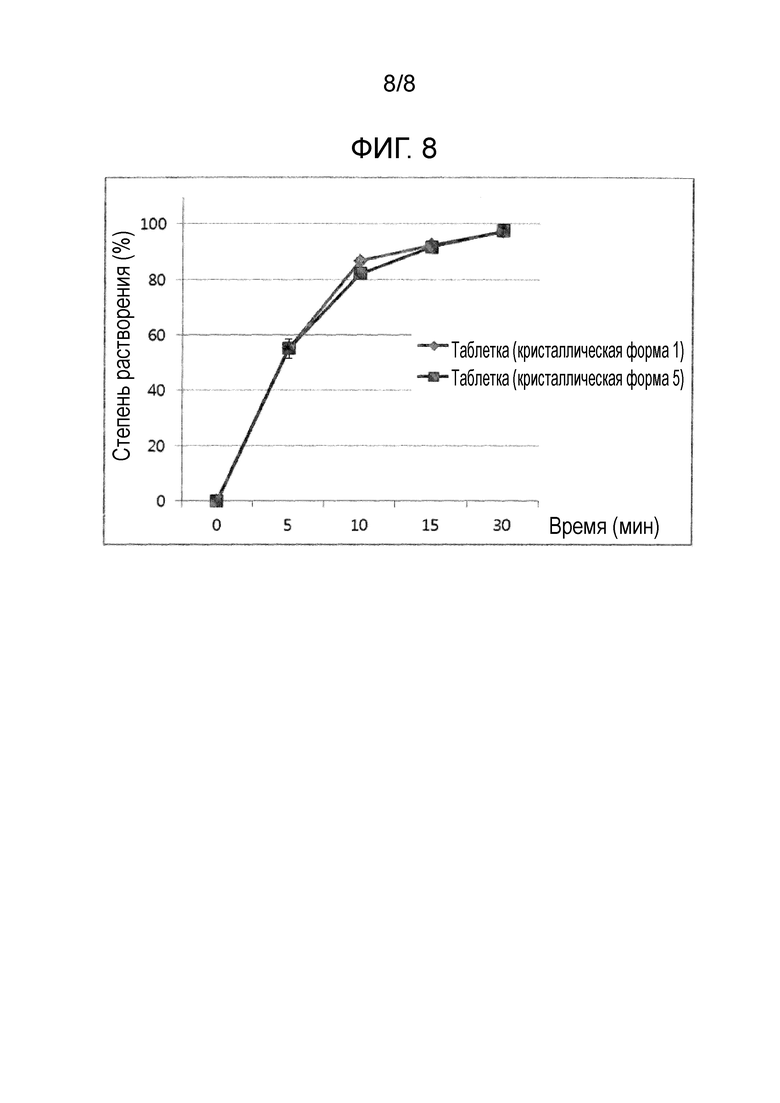
Фиг. 8 представляет собой график, показывающий зависимость скоростей растворения таблеток, содержащих кристаллическую форму 1 или 5 по настоящему изобретению, от кристаллических форм.
Наилучший вариант осуществления изобретения
Ниже настоящее изобретение раскрыто более подробно.
Новая кристаллическая форма метансульфоната 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида (далее называемого ʺGCC-4401Cʺ) по настоящему изобретению обладает превосходной растворимостью и стабильностью при высокой температуре и во влажной окружающей среде.
Новая кристаллическая форма GCC-4401C легко может быть получена методом кристаллизации путем охлаждения органического растворителя, методом вакуумной кристаллизации или методом кристаллизации из растворителя-антирастворителя.
GCC-4401C, используемый в качестве реакционного материала, может быть получен описанным в WO 2011/005029 способом. Новое кристаллическое соединение по настоящему изобретению может быть получено растворением реакционного материала в органическом растворителе, добавлением антирастворителя и охлаждением смеси, с последующим фильтрованием и сушкой образовавшихся кристаллов.
Органические растворители, которые могут быть использованы, выбирают из группы, состоящей из метанола, диметилацетамида (DMA), диметилсульфоксида (DMSO) и их комбинаций, и предпочтителен метанол. Антирастворители, которые могут быть использованы, выбирают из группы, состоящей из изопропилового спирта (IPA), н-бутанола, этилацетата, толуола и их комбинаций, и предпочтителен н-бутанол.
Антирастворитель можно использовать в количестве 1-10-кратного объема, предпочтительно 2-3 кратного объема, из расчета на объем органического растворителя.
Кристаллы, полученные, добавлением антирастворителя и охлаждением смеси, могут быть отфильтрованы общепринятым способом фильтрования и затем высушены при температуре в диапазоне от 55 до 65°C за 3-4 часа для удаления остаточного растворителя, с получением нового кристаллического соединения по настоящему изобретению.
Согласно одному из вариантов осуществления настоящего изобретения новое кристаллическое соединение, именуемое кристаллической формой 1, может быть получено способом, по которому GCC-4401C растворяют в органическом растворителе (напр., метаноле), добавляют антирастворитель (напр., н-бутанол) и смесь охлаждают, а затем кристаллы, полученные на предыдущей стадии, фильтруют и сушат при 60±5°C в течение 3-4 часов.
Согласно другому варианту осуществления настоящего изобретения новое кристаллическое соединение, именуемое кристаллической формой 5, может быть получено способом, по которому GCC-4401C растворяют в органическом растворителе (напр., метаноле), образовавшийся раствор нагревают до температуры 45°C или выше, добавляют антирастворитель (напр., н-бутанол) и смесь охлаждают, а затем кристаллы, полученные на предыдущей стадии, фильтруют и сушат при 60±5°C в течение 3-4 часов.
Согласно одному из аспектов настоящего изобретения кристаллическая форма 1 имеет кристаллическую структуру, рентгеновский порошковый спектр дифракции которой с использованием Cu-Kα-излучения содержит пики при угле дифракции 2θ, равном 4,302, 8,621, 9,606, 12,103, 12,879, 15,648, 17,353, 17,949, 19,26, 19,577, 20,252, 21,792, 23,108, 23,356, 25,76 и 27,463. Каждый пик при угле дифракции 2θ имеет относительную интенсивность 10% или больше. Кроме того, анализ дифференциальной сканирующей калориметрией (ДСК) показывает пик при 178±2°C (см. пример 1).
Согласно другому аспекту настоящего изобретения кристаллическая форма 5 имеет кристаллическую структуру, рентгеновский порошковый спектр дифракции которой с использованием Cu-Kα-излучения содержит пики при угле дифракции 2θ, равном 12,022, 15,721, 15,971, 18,125, 18,928, 19,979, 20,311, 20,726, 21,66, 22,805, 23,18, 23,985, 25,857, 27,25, 27,829, 28, 28,189 и 29,753. Каждый пик при угле дифракции 2θ имеет относительную интенсивность 10% или больше. Кроме того, анализ дифференциальной сканирующей калориметрией (ДСК) показывает пик при 186±2°C (см. пример 2).
Как подтверждают результаты рентгеновской порошковой дифрактометрии, кристаллические формы 1 и 5 по настоящему изобретению представляют собой безводные кристаллические формы и обладают стабильностью без изменения кристаллических форм даже будучи размолотыми или при воздействии влажных условий (см. пример испытания 1). Кроме того, кристаллические формы по настоящему изобретению показывают превосходную скорость растворения, равную 80% или более за 10 минут, независимо от фармацевтических лекарственных форм, таких как таблетки и капсулы, содержащие кристаллические формы (см. пример испытания 2). Таким образом, новые кристаллические формы по настоящему изобретению, кристаллические формы 1 и 5 GCC-4401C, эффективны для лечения тромбоза, инфаркта миокарда, артериосклероза, воспаления, инсульта, стенокардии, рецидивирующей стриктуры после ангиопластики и тромбоэмболии, в частности, перемежающейся хромоты.
Согласно другому аспекту настоящее изобретение относится к фармацевтической композиции, содержащей новую кристаллическую форму метансульфоната 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида в качестве активного ингредиента.
Фармацевтическая композиция по настоящему изобретению может дополнительно содержать фармацевтически приемлемый носитель или вспомогательное вещество. Фармацевтически приемлемый носитель, вспомогательное вещество или их комбинации могут быть выбраны в зависимости от способа введения, используемого для лечения конкретного пациента, типов медицинских показаний или болезненных состояний.
Примеры фармацевтически приемлемого носителя или вспомогательного вещества следующие: вспомогательные вещества, такие как крахмалы, сахар, лактоза, декстрин, маннит, сорбит, кристаллическая целлюлоза, гидроксипропилцеллюлоза с низкой степенью замещения, натрийкарбоксиметилцеллюлоза, гуммиарабик, амилопектин, легкая безводная кремниевая кислота и синтетический алюмосиликат; наполнители или увеличивающие в объеме средства, такие как фосфат кальция и производные диоксида кремния; связующие вещества, такие как крахмалы, сахар, маннит, трегалоза, декстрин, амилопектин, сахароза, глютен, гуммиарабик, метилцеллюлоза, карбоксиметилцеллюлоза, натрийкарбоксиметилцеллюлоза, кристаллическая целлюлоза, производные целлюлозы (напр., включая гидроксипропилцеллюлозу и гидроксипропилметилцеллюлозу), желатин, соль альгиновой кислоты и поливинилпирролидон; скользящие вещества, такие как тальк, стеарат магния или кальция, гидрогенизированное касторовое масло, порошок талька и полиэтиленгликоль в твердой форме; разрыхлители, такие как повидон, кроскармеллоза натрия и кросповидон; и поверхностно-активные вещества, такие как полисорбат, цетиловый спирт и глицеринмоностеарат.
Фармацевтическая композиция по настоящему изобретению может быть получена любым общепринятым способом. В отношении обычно применяемых технологий составления композиций см. [Remington: The Science and Practice of Pharmacy, 20th Edition, Lippincott Williams & White, Baltimore, Maryland (2000)] и [H. C. Ansel et al., Pharmaceutical Dosage Forms and Drug Delivery Systems, 7th Edition, Lippincott Williams & White, Baltimore, Maryland (1999)].
Фармацевтическая композиция по настоящему изобретению может содержать в качестве активного ингредиента кристаллическую форму 1 или 5 метансульфоната 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида в количестве 0,1-95% масс., предпочтительно 1-70% масс., из расчета на общую массу композиции.
Фармацевтическая композиция по настоящему изобретению может быть составлена в виде перорального или парентерального препарата и т.д. и введена пациенту подходящими способами введения. Предпочтительно композиция по изобретению может быть составлена в виде капсул, таблеток, дисперсий, суспензий и проч. и затем введена перорально.
Фармацевтическая композиция по настоящему изобретению может быть введена в виде однократной дозы или раздельными дозами в течение суток, и типичная суточная доза для человека может находиться в диапазоне от 2,5 до 80 мг, из расчета на количество активного ингредиента, кристаллической формы 1 или 5 метансульфоната 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида.
Варианты осуществления изобретения
Далее настоящее изобретение подробно поясняется примерами. Следующие примеры предназначены для дополнительной иллюстрации настоящего изобретения без ограничения его объема.
[Пример]
Аналитические данные, приведенные в нижеописанных примерах, получали в следующих условиях.
1) Спектр порошковой рентгеновской дифракции (PXRD) получали на рентгеновском дифракционном спектрометре (Bruker Corporation, Germany), используя Cu-Kα-излучение. Приборы и условия, используемые для измерения PXRD-спектра, перечислены ниже в таблице 1.
[Таблица 1]
2) Дифференциальную сканирующую калориметрию (ДСК) выполняли, используя дифференциальный сканирующий калориметр (TA Instruments Q2000) приблизительно при 50 мл/мин в инертной атмосфере азота. Температуру устанавливали на 30°C-220°C и затем повышают на 10°C в минуту.
3) ТГА выполняли, используя Shimadzu DTG-60 приблизительно при 30 мл/мин в инертной атмосфере азота. Температуру устанавливали от комнатной температуры до 220°C со скоростью подъема 10°C/мин, и результаты интегрировали в диапазоне от 30°C до 105°C.
Пример 1: получение кристаллической формы 1
н-Бутанол загружали в автоматизированный многоблочный реактор (8-блочный (параллельный реактор) POLYBLOCK, производитель: HEL) при комнатной температуре (30±5°C). 15 г метансульфоната 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида (чистота: 99,7%), полученного способом, описанным на страницах 28-35 в WO 2011/005029, растворяли в 8-кратном объеме метанола. Полученный раствор медленно добавляли в реактор. н-Бутанол использовали в количестве 20-кратного объема.
Реагент перемешивали при комнатной температуре (30±5°C) в течение 1 часа и затем медленно охлаждали до температуры 0±5°C при скорости 0,5°C/мин. Полученный продукт перемешивали при той же температуре в течение 3 часов и фильтровали. Отфильтрованное вещество собирали и сушили при 60±5°C в течение 3-4 часов, получая 10,5 г (99,7%) белого кристаллического вещества. Полученное кристаллическое вещество фотографировали на поляризационном микроскопе (Nikon). Фиг. 6 представляет фотографии полученных кристаллов, выполненные с помощью поляризационного микроскопа.
Спектр порошковой рентгеновской дифракции (PXRD) полученного таким образом кристаллического вещества дает углы дифракции (2θ), межплоскостные расстояния (величину d) и относительные интенсивности (%) пиков, как показаны на Фиг. 1 и в таблице 2, ниже. Кристаллическое соединение, имеющее характеристические углы дифракции (2θ) с относительной интенсивностью 10% или больше, обозначали как ʺкристаллическая форма 1.ʺ
[Таблица 2]
ДСК-пик, потеря массы при ТГА, ИК-спектр и данные 13C-ЯМР для кристаллического вещества приведены ниже. Фиг. 2 показывает результаты ТГА кристаллической формы 1.
ДСК-пик: 179,33°C
Потеря массы при ТГА: 0,09% (м/м)
ИК (KBr, см-1): 3301, 3453, 3066, 2939, 2357, 2124, 2018, 1962, 1742, 1670, 1644, 1552, 1509, 1486, 1429, 1411, 1361, 1344, 1323, 1301, 1287, 1217, 1196, 1160, 1146, 1105, 1085, 1032, 991, 930, 882, 839, 821, 803, 776, 751, 729, 707, 683, 667.
13C-ЯМР: 160,81, 154,16, 148,00, 143,43, 138,47, 134,06, 133,25, 128,45, 128,18, 119,35, 118,08, 71,32, 47,53, 45,94, 42,17, 40,13, 35,71,
Пример 2: получение кристаллической формы 5
Метанол загружали в автоматизированный многоблочный реактор (8-блочный (параллельный реактор) POLYBLOCK, производитель: HEL) при комнатной температуре (30±5°C). В реактор добавляли 20 г метансульфоната 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида (чистота: 99,7%), полученного способом, описанным на страницах 28-35 в WO 2011/005029. Реагент нагревали при 45±2°C, получая прозрачный раствор.
н-Бутанол медленно добавляли к полученному таким образом раствору в количестве 20-кратного объема. Полученный продукт перемешивали при той же температуре в течение 4-6 часов и фильтровали при той же температуре. Собранный продукт сушили при 60±5°C в течение 3-4 часов, получая 15 г (99,7%) белого кристаллического вещества. Полученное кристаллическое вещество фотографировали на поляризационном микроскопе (Nikon). Фиг. 6 представляет фотографии полученных кристаллов, выполненные с помощью поляризационного микроскопа.
Спектр порошковой рентгеновской дифракции (PXRD) полученного таким образом кристаллического вещества дает углы дифракции (2θ), межплоскостные расстояния (величину d) и относительные интенсивности (%) пиков, как показаны на Фиг. 2 и в таблице 3, ниже. Кристаллическое соединение, имеющее характеристические углы дифракции (2θ) с относительной интенсивностью 10% или больше, обозначали как ʺкристаллическая форма 5.ʺ
[Таблица 3]
ДСК-пик, потеря массы при ТГА, ИК-спектр и данные 13C-ЯМР для кристаллического вещества приведены ниже. Фиг. 4 и 5 показывают результаты ДСК и результаты ТГА для кристаллической формы 5, соответственно.
ДСК-пик: 186°C
Потеря массы при ТГА: 0,00% (м/м)
ИК (KBr, см-1): 3315, 3236, 3050, 2963, 2439, 2144, 2167, 2135, 2055, 2015, 1892, 1708, 1656, 1572, 1550, 1514, 1479, 1438, 1419, 1429, 1322, 1303, 1273, 1236, 1226, 1202, 1169, 1150, 1082, 1058, 1038, 1018, 996, 943, 882, 821, 807, 777, 757, 723, 685, 671, 655.
13C-ЯМР: 160,81, 154,16, 148,00, 143,43, 138,47, 134,06, 133,25, 128,45, 128,18, 119,35, 118,08, 71,32, 47,53, 45,94, 42,17, 40,13, 35,71,
Пример испытания 1: стабильность новых кристаллических форм
Стабильность новых кристаллических форм, полученных по примерам 1 и 2, оценивали следующими методами.
1) Оценка стабильности суспензионной системы в растворителе
Чтобы определить, происходит ли взаимопревращение одной кристаллической формы в другую кристаллическую форму в перемешиваемой суспензии, проводили испытание суспензии в различных растворителях при комнатной температуре.
Сначала автоматизированный многоблочный реактор заполняли каждым из растворителей, перечисленных ниже в таблице 4, при комнатной температуре (30±5°C). Кристаллическую форму 1 добавляли в реактор при 30±5°C и нагревали и перемешивали до получения прозрачного раствора. После чего антирастворители, перечисленные ниже в таблице 4 (н-бутанол или IPA), добавляли в реактор за 30±15 минут и перемешивали в течение 30±15 минут до получения прозрачного раствора. Образовавшийся раствор охлаждали до температуры 0±5°C, перемешивали 2-3 часа и затем фильтровали при 0±5°C. Полученное вещество сушили при 60±5°C в течение 3-4 часов в VTD и затем выполняли ДСК-анализ полученного образца для идентификации конечной кристаллической формы.
Другое испытание суспензии выполняли тем же способом, что описан выше, для кристаллической формы 5, используя нижеперечисленные в таблице 4 растворители. Выполняли ДСК-анализ полученного образца для идентификации конечной кристаллической формы. Результаты приведены в таблице 4.
[Таблица 4]
Как показано в таблице 4, кристаллическая форма 1 имеет тенденцию к превращению в кристаллическую форму 5 при перемешивании ее в растворителе в течение 24 часов, тогда как кристаллическая форма 5 сохраняет первоначальную форму даже когда ее перемешивают в различных комбинациях растворителей в течение 24 часов, что указывает на стабильность кристаллической формы 5.
2) Оценка взаимопревращения при высокой температуре
Чтобы выяснить взаимопревращение кристаллических форм при высокой температуре, каждую из кристаллических форм 1 и 5 сушили при 80±5°C без вакуума и затем охлаждали до температуры 30±5°C. Выполняли ДСК-анализ полученных образцов для идентификации конечной кристаллической формы. Результаты приведены в таблице 5.
[Таблица 5]
Как показано в таблице 5, подтверждается, что кристаллические формы 1 и 5 по настоящему изобретению стабильны при высокой температуре.
3) Оценка стабильности при воздействии физического стимула
Выполняли испытание кристаллических форм по настоящему изобретению многократным размалыванием, измельчением вручную и увлажнением для подтверждения их стабильности при воздействии физических стимулов. Для испытания многократным размалыванием каждую из кристаллических форм 1 и 5 размалывали при 3.000 об/мин, используя опытный образец мультимельницы (Sreenex Machines Pvt. Ltd.). Для измельчения вручную каждую из кристаллических форм последовательно измельчали, используя пестик и ступку. Для испытания увлажнением кристаллические формы 1 и 5 хранили при 30°C и относительной влажности 90% в течение 24 часов.
Выполняли ДСК-анализ полученных при испытаниях кристаллических форм для идентификации конечной кристаллической формы. Результаты приведены в таблице 6.
[Таблица 6]
Как показано в таблице 6, подтверждается, что обе кристаллические формы 1 и 5 по настоящему изобретению стабильны при воздействии физических стимулов, таких как размалывание, измельчение и увлажнение.
4) Растворимость
Оценивали растворимость каждой из кристаллических форм 1 и 5 по настоящему изобретению после растворения в растворителе-метаноле. В результате, растворимость кристаллической формы 1 составляла 70 мг/мл, тогда как растворимость кристаллической формы 5 составляла 30 мг/мл, это указывает на то, что кристаллическая форма 5 более стабильна, чем кристаллическая форма 1.
Пример испытания 2: испытание на растворение новых кристаллических форм
1) Получение капсул
Капсулы, содержащие кристаллическую форму 1 по настоящему изобретению, получали общепринятым методом капсулирования. Сначала 20 мг кристаллической формы 1 по настоящему изобретению и 279,1 мг лактозы добавляли в V-миксер, который обычно используют в процедуре смешения для изготовления лекарственных препаратов, и затем перемешивали при 20 об/мин в течение 20 минут. Добавляли 0,9 мг стеарата магния и смесь дополнительно перемешивали при 20 об/мин в течение 5 минут. Твердые желатиновые капсулы заполняли смесью, получая капсулы кристаллической формы 1.
2) Получение таблеток
Таблетки, содержащие кристаллическую форму 1 по настоящему изобретению, получали общепринятым методом таблетирования.
А именно, 20 мг кристаллической формы 1, 175,5 мг лактозы, 7 мг примойела, 5 мг гидроксипропилметилцеллюлозы (HPMC) и 1,5 мг Aerosil 200 добавляли в V-миксер, который обычно используют в процедуре смешения для изготовления лекарственных препаратов, и затем перемешивали при 20 об/мин в течение 20 минут. Добавляли 1 мг стеарата магния и смесь дополнительно перемешивали при 20 об/мин в течение 5 минут. Смесь прессовали в таблетки, используя таблеточный пресс. Покрытые оболочкой таблетки, содержащие кристаллическую форму 1, получали, покрывая полученные таблетки приблизительно 10 мг Opadry.
Вышеуказанную процедуру продолжали за тем исключением, что использовали кристаллическую форму 5 вместо кристаллической формы 1, получая покрытые оболочкой таблетки, содержащие кристаллическую форму 5.
3) Испытание на растворение
Выполняли испытание на растворение капсул и таблеток, полученных как указано выше, для оценки скорости их растворения (%).
Испытание на растворение выполняли способом с использованием лопастной мешалки в аппарате U.S.P. Apparatus 2, при скорости лопасти 50 об/мин. В качестве раствора для растворения использовали ацетатный буфер, pH 4,0, и капсулы или таблетки добавляли, когда 900 мл раствора для растворения достигали 37±0,5°C. В заданное время (5 минут, 10 минут, 15 минут и 30 минут) из раствора для растворения забирали по 1 мл каждой пробы и фильтровали. Скорость растворения измеряют, используя ВЭЖХ. Испытание проводили однократно (N=6). Средние значения и стандартные отклонения (S.D.) для скоростей растворения приведены ниже в таблице 7 и на Фиг. 7.
[Таблица 7]
Обычно капсулы не требуют большого количества носителя, и преимущество их состоит в простом способе изготовления. Однако существуют проблемы стабильности капсул, поскольку сама капсула легко повреждается влагой и компоненты в капсуле не спрессованы, то это приводит к большой площади поверхности, следовательно, к подверженности влиянию окружающей среды. Таблетки могут устранять недостатки капсул, и преимущества их состоят в превосходной эффективности производства и низкой стоимости производства. Между тем, полиморфы имеют одну и ту же составляющую единицу кристалла, но различное расположение, и растворимость их может изменяться в зависимости от расположения.
Как показано в таблице 7 и на Фиг. 7, и таблетки, и капсулы по настоящему изобретению имеют превосходную скорость растворения, равную 80% или более за 10 минут.
Кроме того, кристаллические формы по настоящему изобретению в капсуле показывают скорости растворения, схожие со скоростями для таблеточной формы, что подтверждает эквивалентность растворимости капсул и таблеток. Таблетки, содержащие кристаллическую форму 1, дают график растворения, подобный графику для таблеток, содержащих кристаллическую форму 5, который подтверждает, что кристаллические формы 1 и 5 по настоящему изобретению обладают аналогичной растворимостью и фармакологическими эффектами.
4) Испытание на растворение при массовом производстве
Таблетки, содержащие кристаллические формы 1 и 5 по настоящему изобретению, производили массово (в увеличенном масштабе), чтобы подтвердить сходство зависимости графиков растворения от кристаллических форм при массовом производстве. Испытание на растворение выполняли на полученных таким образом таблетках по тем же методикам, что описаны выше. Результаты приведены в таблице 8 и на Фиг. 8.
[Таблица 8]
Как показано в таблице 8 и на Фиг. 8, таблетки, содержащие кристаллические формы 1 и 5 по настоящему изобретению, дают уменьшенное отклонение в зависимости графика растворения от кристаллических форм, которое подтверждает, что кристаллические формы по настоящему изобретению имеют схожую растворимость и фармакологические эффекты при массовом производстве.
Хотя изобретение раскрыто на приведенных выше конкретных примерах, следует понимать, что специалистом в данной области могут быть сделаны различные модификации и изменения относительно изобретения, которые также находятся в пределах объема изобретения, как определено приложенной формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВОЕ КРИСТАЛЛИЧЕСКОЕ ТВЕРДОЕ СОЕДИНЕНИЕ ГИДРОХЛОРИДА 3-ФЕНИЛ-4-ПРОПИЛ-1-(ПИРИДИН-2-ИЛ)-1Н-ПИРАЗОЛ-5-ОЛА | 2018 |
|
RU2754255C2 |
| СОЛИ ПРОИЗВОДНЫХ ПИРРОЛОПИРИМИДИНОНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2448967C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА α МОНОБЕНЗОАТА СОЕДИНЕНИЯ А, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ЕЕ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2015 |
|
RU2677660C2 |
| ТВЕРДАЯ ДИСПЕРСИЯ С УЛУЧШЕННОЙ РАСТВОРИМОСТЬЮ, СОДЕРЖАЩАЯ ПРОИЗВОДНОЕ ТЕТРАЗОЛА В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2013 |
|
RU2662819C2 |
| Кристалл (6S,9aS)-N-бензил-8-({ 6-[3-(4-этилпиперазин-1-ил)азетидин-1-ил]пиридин-2-ил} метил)-6-(2-фтор-4-гидроксибензил)-4,7-диоксо-2-(проп-2-ен-1-ил)гексагидро-2H-пиразино[2,1-c][1,2,4]триазин-1(6H)-карбоксамида | 2016 |
|
RU2723551C2 |
| Способ получения полиморфной формы 4-(3-этокси-4-гидроксибензил)-N-(2,4-дифторфенил)-5-оксо-5,6-дигидро-4H-1,3,4-тиадиазин-2-карбоксамида | 2022 |
|
RU2785195C1 |
| НОВЫЕ КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ПРОИЗВОДНЫХ ПИРРОЛИЛГЕПТАНОВОЙ КИСЛОТЫ | 2008 |
|
RU2421445C1 |
| Соединение на основе оксазолидина и содержащий его селективный агонист андрогенового рецептора | 2015 |
|
RU2702001C2 |
| ТОЗИЛАТНАЯ СОЛЬ ПРОИЗВОДНОГО 5-ПИРАЗОЛИЛ-2-ПИРИДОНА, ПОЛЕЗНАЯ В ЛЕЧЕНИИ COPD | 2010 |
|
RU2526038C2 |
| ИНГИБИТОРЫ ДИАЦИЛГЛИЦЕРОЛ-АЦИЛТРАНСФЕРАЗЫ 2 | 2017 |
|
RU2719589C1 |

Изобретение относится к кристаллической форме метансульфоната 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида (GCC-4401C), охарактеризованного рентгеновским порошковым спектром дифракции с использованием Cu-Kα-излучения, содержащим пики при угле дифракции 2θ, равном 12,022, 15,721, 15,971, 18,125, 18,928, 19,979, 20,311, 20,726, 21,66, 22,805, 23,18, 23,985, 25,857, 27,25, 27,829, 28, 28,189 и 29,753. Также изобретение относится к фармацевтической композиции, обладающей свойствами ингибитора фактора свертывания крови Xa, содержащей безводный кристаллический метансульфонат 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида по изобретению, в качестве активного ингредиента. Кристаллическая форма соединения по изобретению обладает превосходной стабильностью и может эффективно применяться для предупреждения или лечения заболеваний, таких как тромбоз, инфаркт миокарда, артериосклероз, воспаление, инсульт, стенокардия, рецидивирующая стриктура после ангиопластики и тромбоэмболия. 2 н. и 3 з.п. ф-лы., 8 ил., 8 табл., 4 пр.
1. Безводный кристаллический метансульфонат 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида (GCC-4401C), рентгеновский порошковый спектр дифракции которого с использованием Cu-Kα-излучения содержит пики при угле дифракции 2θ, равном 12,022, 15,721, 15,971, 18,125, 18,928, 19,979, 20,311, 20,726, 21,66, 22,805, 23,18, 23,985, 25,857, 27,25, 27,829, 28, 28,189 и 29,753.
2. Безводный кристаллический GCC-4401C по п.1, который дает пик 186±2°C при анализе дифференциальной сканирующей калориметрией (ДСК).
3. Фармацевтическая композиция, обладающая свойствами ингибитора фактора свертывания крови Xa, содержащая безводный кристаллический метансульфонат 5-хлор-N-({(5S)-2-оксо-3-[4-(5,6-дигидро-4H-[1,2,4]триазин-1-ил)фенил]-1,3-оксазолидин-5-ил}метил)тиофен-2-карбоксамида по любому из пп.1 и 2 в качестве активного ингредиента.
4. Фармацевтическая композиция по п.3, где фармацевтическая композиция дополнительно содержит фармацевтически приемлемый носитель или вспомогательное вещество.
5. Фармацевтическая композиция по п. 3, где фармацевтическая композиция применяется для предупреждения или лечения, по меньшей мере, одного из заболеваний или симптомов, выбранных из группы, состоящей из тромбоза, инфаркта миокарда, артериосклероза, воспаления, инсульта, стенокардии, рецидивирующей стриктуры после ангиопластики и тромбоэмболии.
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| ИНГИБИТОРЫ FXa С ЦИКЛИЧЕСКИМ АМИДОКСИМОМ ИЛИ ЦИКЛИЧЕСКИМ АМИДРАЗОНОМ В КАЧЕСТВЕ P4 СУБЪЕДИНИЦЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ПРОИЗВОДНЫЕ | 2009 |
|
RU2468024C2 |
| US 8178525 B2, 15.05.2012. | |||
Авторы
Даты
2018-08-07—Публикация
2014-07-18—Подача