ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
Данная заявка заявляет приоритет согласно 35 U.S.С. § 119(e) предварительной заявки на патент США №61/642358, поданной 3 мая 2012 г., которая включена в данный документ во всей своей полноте посредством ссылки.
ИНФОРМАЦИЯ О ПЕРЕЧНЕ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Перечень последовательностей, приложенный к данной заявке, представлен в текстовом формате вместо бумажной копии и, таким образом, включен посредством ссылки в настоящее описание. Название текстового файла, содержащего перечень последовательностей, 360056_412WO_SEQUENCE_LISTING.TXT. Текстовый файл имеет размер 129KB, был создан 2 мая 2013 г. и подается в электронном виде посредством EFS-Web.
ИНФОРМАЦИЯ О ПРАВИТЕЛЬСТВЕННОЙ ПОДДЕРЖКЕ
Настоящее изобретение выполнено при поддержке правительства согласно контракту № Р01 СА 18029, заключенному с Национальными институтами здравоохранения/Национальным институтом онкологии. Правительство обладает определенными правами на настоящее изобретение.
ПРЕДПОСЫЛКИ
Область техники
Настоящее раскрытие относится к Т-клеточным рецепторам с повышенным сродством (TCR) и, более конкретно, к применению отбора с помощью агонистов гемопоэтических клеток-предшественников, экспрессирующих антиген-специфическую TCRα, для обеспечения повышенного сродства TCR и их применениям.
Описание уровня техники
Генная терапия с использованием TCR является новым терапевтическим подходом, который может преодолеть многие затруднения, связанные с традиционной Т-клеточной адоптивной иммунотерапией, такие как длительное время и значительные трудозатраты, необходимые для выделения, получения характеристик и увеличения количества специфических в отношении опухолевых антигенов Т-клеточных клонов (Schmitt, Ragnarsson, & Greenberg, 2009, Hum. Gene Ther. 20:1240-1248). Дополнительные преимущества генной терапии включают возможность использования популяций Т-клеток, характеристики которых были определены, способных к длительному существованию in vivo (Berger et al., 2008, J. Clin. Invest. 118:294-305; Hinrichs et al., 2009, Proc. Natl. Acad. Sci. USA 106:17469-17474). Такие Т-клетки могут быть трансдуцированы посредством генов, кодирующих хорошо изученные TCR, которые характеризуются высоким сродством к опухолевым антигенам, таким образом увеличивая вероятность содействия противоопухолевому эффекту. Фактически, недавний доклад по терапии, направленной на В-клеточный лейкоз поздней стадии при помощи генетически модифицированных Т-клеток, экспрессирующих химерный рецептор с высоким сродством, нацеленный на "собственный"/опухолевый антиген, подчеркнул потенциал применения разработанных с помощью генной инженерии Т-клеток с высокой авидностью для лечения лейкоза (Kalos et al., 2011, Sci. Transl. Med. 3:95ra73). Однако, поскольку большинство опухолевых антигенов, на которые нацелена Т-клеточная иммунотерапия, сверхэкспрессируют собственные белки, Т-клетки с высоким сродством, специфичные в отношении этих антигенов, как правило, подвергаются негативной селекции в тимусе. Таким образом, одним значительным ограничением видов Т-клеточной иммунотерапии в целом является ограниченное количество Т-клеток, экспрессирующих эндогенный TCR с достаточно высоким сродством в отношении немутировавших опухолевых антигенов.
Было разработано несколько стратегий повышения сродства TCR, которые предполагается применять в генной терапии с использованием TCR (Richman & Kranz, 2007, Biomol. Eng. 24:361-373; Udyavar et al., 2009, J. Immunol. 182:4439-4447; Zhao et al., 2007, J. Immunol. 179:5845-5854). Данные подходы в целом предполагают создание библиотек мутантных TCR, которые подверглись нескольким циклам мутагенеза и последующего скрининга в отношении мутаций, которые придают большее сродство к целевому пептиду/МНС-лиганду. Мутации, как правило, осуществляют в участках CDR, которые, как известно, взаимодействуют с пептидом/МНС. Участки CDR1 и CDR2 преимущественно контактируют с молекулой МНС, тогда как гипервариабельный участок CDR3 главным образом контактирует с пептидом (Wucherpfennig et al., 2010, Cold Spring Harbor Perspectives in Biology 2:a005140-a005140). Стратегии сайт-направленного мутагенеза, как правило, направлены на выбранные части всех трех из этих участков, однако не являются всегда успешными в получении варианта с более высоким сродством, и улучшения ограничены изменениями только в участках особого целенаправленного воздействия. Более того, введение мутаций в остатки, контактирующие с МНС, связано с риском потенциального увеличения сродства TCR к МНС, при этом уменьшая общую специфичность рецептора в отношении родственного пептида. По этой причине, в идеальном случае, большинство мутаций, введенных для повышения сродства TCR, будут рестриктированы по участку CDR3. Однако существующие в настоящее время методики ограничены в возможности получения разнообразия CDR3, поскольку сайт-направленный мутагенез ограничен первоначальной длиной участка CDR3.
Учитывая сложность выделения Т-клеток с высоким сродством, которые распознают характерные опухоль-ассоциированные антигены, существует постоянная необходимость в альтернативных способах получения TCR с повышенным сродством.
КРАТКОЕ ОПИСАНИЕ
В одном аспекте настоящее раскрытие предусматривает способ получения TCR с повышенным сродством, включающий а) приведение гемопоэтических клеток-предшественников в контакт со стромальными клетками и пептидным антигеном при условиях и в течение времени, достаточных для индукции дифференцировки гемопоэтических клеток-предшественников в DN TCRαβ+ тимоциты, где гемопоэтические клетки-предшественники содержат неэндогенную последовательность нуклеиновой кислоты, кодирующую TCRα-цепь из исходного TCR, специфичного в отношении пептидного антигена, и где стромальные клетки содержат неэндогенную последовательность нуклеиновой кислоты, кодирующую Delta-like-1 или Delta-like-4, и последовательность нуклеиновой кислоты, кодирующую молекулу МНС; b) выделение последовательностей нуклеиновой кислоты, кодирующих различные TCRβ-цепи из DN TCRαβ+ тимоцитов, и введение последовательностей нуклеиновой кислоты, кодирующих TCRβ-цепи, в клетки, способные экспрессировать TCR на клеточной поверхности и содержащие последовательность нуклеиновой кислоты, кодирующую TCRα-цепь из этапа а); и идентификацию TCR с повышенным сродством (например, путем выявления или отбора кандидатных TCRαβ с высоким сродством с помощью анализа с использованием МНС-тетрамеров, а затем измерения сродства связывания с таковым исходного TCRαβ).
В дополнительных аспектах предусматриваются TCR с повышенным сродством, полученные с помощью способов, раскрываемых в данном документе, которые могут быть фиксированными на клетках или могут находиться в растворимой форме и могут дополнительно быть кодон-оптимизированными для повышения экспрессии в Т-клетках.
В других дополнительных аспектах TCR с повышенным сродством по настоящему раскрытию можно применять для лечения заболевания (такого как рак, инфекционное заболевание или аутоиммунное заболевание) у субъекта путем введения композиции, содержащей TCR с повышенным сродством. В дополнительных вариантах осуществления TCR с повышенным сродством по настоящему раскрытию можно применять в диагностических способах или способах визуализации, включая такие способы, используемые применительно к показаниям или условиям, указанным в данном документе.
Эти и другие аспекты настоящего изобретения станут очевидными при обращении к нижеследующим подробному описанию и приложенным графическим материалам. Все ссылки, раскрываемые в данном документе, включены, таким образом, посредством ссылки во всей их полноте, как если бы каждая была включена индивидуально.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигуры 1A-D. Тимоциты от трансгенных мышей ОТ-1 сортировали в отношении TCRβ-TCRγδ-CD4-CD8-CD117+CD44+ DN1 и DN2 клеток-предшественников и культивировали на клетках OP9-DL1, экспрессирующих молекулу МНС класса I Н-2Kb, в течение 20 дней в присутствии различных концентраций пептида овальбумина SIINFEKL (SEQ ID NO: 1), как указано. (А, В, С) Культуры анализировали с помощью проточной цитометрии в указанные моменты времени. (D) Общую насыщенность клетками каждой культуры определяли в день 20 культивирования.
Фигура 2. Отсортированные CD69- DP тимоциты, которые пока не подвергались позитивной селекции, полученные от трансгенных мышей В6 или ОТ-1, культивировали на клетках OP9-DL1, экспрессирующих молекулу МНС класса I Н-2Kb в присутствии пептида овальбумина SIINFEKL (SEQ ID NO: 1).
Фигуры 3А-С. Тимоциты В6 сортировали в отношении CD4-CD8-CD117+CD44+ DN1 и DN2 клеток-предшественников, и трансдуцировали посредством TCRα-цепи клона 3D WT1-специфического TCR с повышенным сродством, и культивировали на клетках OP9-DL1, экспрессирующих молекулу МНС класса I H-2Db в присутствии или при отсутствии 1 мкМ пептида WT1 с последовательностью RMFPNAPYL (SEQ ID NO: 2). (А) В день 16 культивирования трансдуцированные (hCD2+) и нетрансдуцированные (hCD2-) клетки анализировали с помощью проточной цитометрии. (В) В день 21 культивирования OP9-DL1 в присутствии 1 мкМ пептида WT1 с последовательностью RMFPNAPYL (SEQ ID NO: 2) DN TCRαβ+ клетки сортировали согласно указанной схеме. (С) Отсортированные клетки лизировали, выделяли ДНК и проводили ПЦР с использованием Vb10-специфического прямого праймера и Cb2-специфического обратного праймера. Vb10-продукт ПЦР затем клонировали посредством прямого ТОРО-клонирования в вектор pENTR/D-TOPO, переносили в ретровирусный вектор MigR1-attR с помощью технологии Gateway® и ретровирусный супернатант получали и использовали для трансдукции мышиных 58-/- клеток для скрининга библиотеки, как описано.
Фигуры 4А-С. Ретровирусную библиотеку TCRβ использовали для трансдукции CD8+3Dα+ 58-/- клеток. (А) Трансдуцированные клетки сначала сортировали в отношении экспрессии только GFP (данные не показаны) с последующими двумя сортировками в отношении GFP и экспрессии на высоком уровне тетрамера МНС-пептид WT1, как указано. Отсортированные 58-/- клетки также анализировали на предмет окрашивания посредством неспецифического, но специфичного в отношении GP33 тетрамера МНС Н-2Db-пептид в качестве контроля для выявления неспецифического связывания тетрамера. (В) Анализ последовательности выделенных TCRβ-цепей. (С) Четыре кандидатные TCRβ-цепи идентифицировали с помощью анализа последовательности и переносили обратно в ретровирусный вектор MigR1-attR. Получали ретровирусный супернатант и использовали для трансдукции CD8+3Dα+ 58-/- клеток.
Фигуры 5А-С. (А) Относительное сродство трех TCR с наиболее высоким сродством определяли путем окрашивания каждой трансдуцированной клеточной линии посредством тетрамера МНС-пептид с последующей проточной цитометрией. Измерения KD осуществляли с использованием шести 2-кратных разведений РЕ-конъюгированных тетрамеров, и наблюдаемые значения KD определяли на основе кривых связывания, построенных с использованием нелинейной регрессии, как концентрацию лиганда, полученную после полумаксимального связывания. (В) TCRβ-цепь с наиболее высоким сродством (клон №1) подвергали кодон-оптимизации, и связывание с тетрамером сравнивали с первоначальной конструкцией 3Dαβ с повышенным сродством. (С) 58-/- клетки, трансдуцированные посредством каждой из кандидатных TCRβ-цепей, образующих пару с 3Dα, окрашивали посредством специфического тетрамера МНС-пептид WT1, а также посредством нескольких неспецифических тетрамеров МНС H-2Db-пептид для оценки потенциальной пептид-независимой реактивности в отношении МНС.
Фигуры 6А-В. Анализ экспрессии CD4 и CD8 TCRβ+ тимоцитами (А) и спленоцитами (В), полученными от ретрогенных 3D-PYYα-IRES-hCD2 и 7431α-IRES-hCD2 мышей. Экспрессия Vβ10 и Vβ9 TCRβ+ тимоцитами (А), полученными от ретрогенных 3D-PYYα-IRES-hCD2 и 7431α-IRES-hCD2 мышей.
Фигура 7. Анализ спленоцитов от ретрогенных мышей через 6 дней стимуляции посредством пептида WT1 мезотелина +IL2 in vitro.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее раскрытие предусматривает способы и композиции для получения TCR с повышенным или высоким сродством, в которых TCRα-цепь из антиген-специфического TCR используется для отбора de novo образованных TCRβ-цепей, которые образуют пару с антиген-специфической TCRα-цепью, в ходе развития Т-клеток in vitro с образованием новых рецепторов с повышенным сродством, которые могут преимущественно управлять созреванием Т-клеток независимо от негативной селекции с помощью нового способа отбора для целенаправленного воздействия на антиген, представляющий интерес.
В одном аспекте настоящее раскрытие предусматривает способ получения Т-клеточного рецептора (TCR) с повышенным сродством путем культивирования гемопоэтических клеток-предшественников (содержащих неэндогенную последовательность нуклеиновой кислоты, кодирующую антиген-специфическую TCRα-цепь) со стромальными клетками (содержащими неэндогенную последовательность нуклеиновой кислоты, кодирующую Delta-like-1 или Delta-like-4, и последовательность нуклеиновой кислоты, кодирующую молекулу МНС) в присутствии пептидного антигена, что будет индуцировать дифференцировку гемопоэтических клеток-предшественников в DN TCRαβ+ тимоциты. Затем последовательности нуклеиновой кислоты, кодирующие различные TCRβ-цепи из DN TCRαβ+ тимоцитов выделяют и вводят в клетки, которые способны экспрессировать TCR на клеточной поверхности, а также экспрессируют TCRα-цепь, указанную выше. Наконец, TCR с повышенным сродством идентифицируют путем сравнения сродства связывания кандидатного TCRαβ с исходным TCRαβ.
Кроме того, настоящее раскрытие предусматривает TCR с повышенным сродством, полученные с помощью таких способов, а также композиции и способы для применения TCR с повышенным сродством по настоящему раскрытию в различных терапевтических применениях, включая лечение заболевания у субъекта (например, рака, инфекционного заболевания, аутоиммунного заболевания).
Перед тем, как перейти к более подробному изложению настоящего раскрытия, для его понимания может быть полезным привести определения некоторых выражений, используемых в данном документе. Дополнительные определения изложены на всем протяжении настоящего раскрытия.
В настоящем описании выражения "приблизительно" и "фактически состоящий из" означают ±20% к указанному диапазону, значению или позиции, если не указано иное. Следует понимать, что формы единственного числа, используемые в данном документе, относятся к "одному или нескольким" перечисленным компонентам. Использование предлогов альтернативы (например, "или") следует понимать как обозначение одной, как одной, так и другой или любой комбинации альтернатив. Как используется в данном документе, выражения "включает", "имеет" и "содержит" применяются синонимически, при этом выражения и их варианты предполагается толковать как неограничивающие.
"Т-клеточный рецептор" (TCR) относится к молекуле, находящейся на поверхности Т-клеток (или Т-лимфоцитов), которая совместно с CD3 в целом отвечает за распознавание антигенов, связанных с молекулами главного комплекса гистосовместимости (МНС). В большинстве Т-клеток TCR представляет собой связанный дисульфидными связями гетеродимер высоковариабельных α- и β-цепей (также известных как TCRα и TCRβ, соответственно). В меньшей субпопуляции Т-клеток TCR представляет собой гетеродимер вариабельных γ- и δ-цепей (также известных как TCRγ и TCRδ, соответственно). Каждая цепь TCR является представителем суперсемейства иммуноглобулинов и содержит один N-концевой вариабельный домен иммуноглобулина, один константный домен иммуноглобулина, трансмембранный участок и короткий цитоплазматический "хвост" на С-концевой области (см. Janeway et al., Immunobiology: The Immune System in Health and Disease, 3rd Ed., Current Biology Publications, p. 4:33, 1997). TCR, как используется в настоящем раскрытии, может быть получен от различных видов животных, включая человека, мышь, крысу или других млекопитающих. TCR может быть фиксированным на клетке или находиться в растворимой форме.
TCR и его связывающие домены по настоящему раскрытию могут быть "иммуноспецифическими" или способными связываться с необходимой степенью, в том числе "связываться специфически или селективно" с мишенью, при этом не характеризуются значительным связыванием с другими компонентами, присутствующими в исследуемом образце, если они связываются с целевой молекулой со сродством или Ka (т.е. равновесной константой ассоциации конкретного взаимодействия связывания с единицами 1/М), например, большей или равной приблизительно 105 М-1, 106 М-1, 107 М-1, 108 М-1, 109 М-1, 1010 М-1, 1011 М-1, 1012 М-1 или 1013 М-1. Домены, характеризующиеся "высоким сродством" связывания, относятся к связывающим доменам с Ka по меньшей мере 107 М-1, по меньшей мере 108 М-1, по меньшей мере 109 М-1, по меньшей мере 1010 М-1, по меньшей мере 1011 М-1, по меньшей мере 1012 М-1, по меньшей мере 1013 М-1 или более. Альтернативно, сродство может быть определено как равновесная константа диссоциации (Kd) конкретного взаимодействия связывания с единицами М (например, от 10-5 М до 10-13 М). Значения сродства TCR и полипептидов связывающих доменов согласно настоящему раскрытию могут быть без труда определены с помощью традиционных методик (см., например, Scatchard et al. (1949) Ann. N.Y. Acad. Sci. 51:660; и патенты США №№5283173; 5468614, анализ Biacore® или аналогичную систему). Следовательно, "Т-клеточный рецептор с повышенным сродством" (TCR с повышенным сродством) относится к подвергнутому отбору или разработанному с помощью генной инженерии TCR с более сильным связыванием с целевым антигеном, чем у TCR дикого типа (или исходного). Повышенное сродство может быть определено как TCR с Ka (равновесной константой ассоциации) в отношении целевого антигена более высокой, чем таковая у TCR дикого типа (также называемого исходным или первоначальным), TCR с Kd (константой диссоциации) в отношении целевого антигена меньшей, чем таковая у TCR дикого типа (также называемого исходным или первоначальным) или со скоростью диссоциации (Koff) в отношении целевого антигена меньшей, чем таковая у TCR дикого типа (или исходного).
"Молекулы главного комплекса гистосовместимости" (молекулы МНС) относятся к гликопротеинам, которые доставляют пептидные антигены на клеточную поверхность. Молекулы МНС класса I являются гетеродимерами, состоящими из трансмембранной α-цепи (с тремя α-доменами) и нековалентно связанного β2 микроглобулина. Молекулы МНС класса II состоят из двух трансмембранных гликопротеинов, α и β, оба из которых проходят через мембрану. Каждая цепь имеет два домена. Молекулы МНС класса I доставляют пептиды, находившиеся в цитозоле, на клеточную поверхность, где комплекс пептид : МНС распознается CD8+ Т-клетками. Молекулы МНС класса II доставляют пептиды, находившиеся в везикулярной системе, на клеточную поверхность, где они распознаются CD4+ Т-клетками. Молекула МНС может быть получена от различных видов животных, включая человека, мышь, крысу или других млекопитающих.
"Гемопоэтическая клетка-предшественник" представляет собой клетку, полученную из гемопоэтической стволовой клетки или фетальной ткани, способную к дальнейшей дифференцировке в зрелые типы клеток (например, клетки Т-клеточной линии дифференцировки). В конкретном варианте осуществления используют CD24lo Lin- CD117+ гемопоэтические клетки-предшественники. Как определено в данном документе, гемопоэтические клетки-предшественники могут включать эмбриональные стволовые клетки, способные к дальнейшей дифференцировке в клетки Т-клеточной линии дифференцировки. Гемопоэтические клетки-предшественники могут быть получены от различных видов животных, включая человека, мышь, крысу или других млекопитающих.
"Клетка-предшественник тимоцит" или "тимоцит" представляет собой гемопоэтическую клетку-предшественника, присутствующую в тимусе.
"Гемопоэтические стволовые клетки" относятся к недифференцированным гемопоэтическим клеткам, способным к практически неограниченному размножению либо in vivo, либо ex vivo и способным к дифференцировке в другие типы клеток, включая клетки Т-клеточной линии дифференцировки. Гемопоэтические стволовые клетки могут быть выделены, например, из печени плода, костного мозга и пуповинной крови.
"Клетки Т-клеточной линии дифференцировки" относятся к клеткам, у которых наблюдается по меньшей мере одна фенотипическая характеристика Т-клетки, или ее клетки ранней стадии дифференцировки или ее предшественника, который отличает клетки от других лимфоидных клеток и клеток эритроидной или миелоидной линий дифференцировки. Такие фенотипические характеристики могут включать экспрессию одного или нескольких белков, специфичных по отношению к Т-клеткам (например, CD8+), или физиологический, морфологический, функциональный или иммунологический признак, характерный для Т-клеток. Например, клетками Т-клеточной линии дифференцировки могут быть предшественники или клетки ранней стадии дифференцировки, коммитированные в направлении Т-клеточной линии дифференцировки; незрелые и неактивированные CD25+ Т-клетки; клетки, которые прошли коммитирование в направлении CD4 или CD8 линии дифференцировки; клетки-предшественники тимоциты, которые являются CD4+CD8+ дважды положительными; моноположительными CD4+ или CD8+; TCRαβ или TCR γδ или зрелые и функционально способные или активированные Т-клетки.
"Стромальные клетки" представляют собой клетки соединительной ткани любого органа. В конкретном варианте осуществления стромальные клетки являются стромальными клетками костного мозга. Примеры клеточных линий стромальных клеток, которые могут быть разработаны с помощью генной инженерии экспрессирующими DLL1 или DLL4, включают мышиную клеточную линию стромальных клеток MS5 (Itoh, et al., Exp. Hematol. 1989, 17:145-153) и S17 и человеческие клеточные линии стромальных клеток HGS2.11, HGS2.52, HGS.18, HGS3.30, HGS3.65, HGS.3.66, HGS3.103 и HGS3.114 (доступные от Human Genome Sciences Inc., MD, см. опубликованную заявку на патент США 20020001826). В конкретном варианте осуществления используют клетки ОР9 (Kodama et al., 1994, Exp. Hematol. 22:979-984; доступные из депозитария клеточных культур RIKEN). Клетки ОР9, экспрессирующие DLL1 и DLL4, были описаны ранее (см., например, Schmitt et al., 2002, Immunity: 17:749-756; патент США №7575925).
"Дважды отрицательные TCRαβ тимоциты" (DN TCRαβ тимоциты) относятся к популяции тимоцитов, не экспрессирующих корецепторы CD4 и CD8, но экспрессирующих TCRα- и β-цепи.
"Пептидный антиген" относится к аминокислотной последовательности с длиной в диапазоне от приблизительно 7 аминокислот до приблизительно 25 аминокислот, которая специфически распознается TCR или его связывающими доменами как антиген и которая может быть получена из или на основе фрагмента более длинной целевой биологической молекулы (например, полипептида, белка), или ее производному. Антиген может экспрессироваться на клеточной поверхности, внутри клетки или как интегральный мембранный белок. Антиген может быть получен из организма хозяина (например, опухолевый антиген, аутоиммунный антиген) или может быть экзогенного происхождения (например, бактериальный, вирусный).
"Последовательность нуклеиновой кислоты" или полинуклеотиды, могут быть в форме РНК или ДНК, которая включает кДНК, геномную ДНК и синтетическую ДНК. Последовательность нуклеиновой кислоты может быть двунитевой или однонитевой и в случае однонитевой может представлять собой кодирующую нить или некодирующую (антисмысловую нить). Кодирующая последовательность может быть идентичной кодирующей последовательности, известной в уровне техники, или может быть отличной кодирующей последовательностью, которая в результате избыточности или вырожденности генетического кода, или в результате сплайсинга кодирует тот же полипептид.
"Неэндогенный" относится к молекуле (например, последовательности нуклеиновой кислоты), которая не присутствует в клетке-хозяине (клетках-хозяевах)/образце, в которые вводят молекулу, например, вводят с помощью методик рекомбинантных ДНК. Неэндогенная молекула может быть получена от того же вида или от другого вида.
Лиганды Notch "Delta-like-1" (DL1 или DLL1) и "Delta-like-4" (DL4 или DLL4) являются гомологами лигандов Notch Delta и являются представителями семейства белков delta/serrate/jagged. Они играют роль в опосредовании выбора судьбы клеток в ходе гемопоэза и могут играть роль в межклеточной коммуникации. Иллюстративные последовательности Delta-like-1 включают таковые с номерами доступа в Genbank NM_005618.3 (SEQ ID NO: 3) и NP_005609.3 (SEQ ID NO: 4) (последовательности транскрипта и белка Homo sapiens, соответственно) и с номером доступа в Genbank NM_007865.3 (SEQ ID NO: 5) и NP_031891.2 (SEQ ID NO: 6) (последовательности транскрипта и белка Mus musculus, соответственно). Иллюстративные последовательности Delta-like-4 включают таковые с номером доступа в Genbank NM_019074.3 (SEQ ID NO: 7) и NP_061947.1 (SEQ ID NO: 8) (последовательности транскрипта и белка Homo sapiens, соответственно) и с номером доступа в Genbank NM_019454.3 (SEQ ID NO: 9) и NP_062327.2 (SEQ ID NO: 10) (последовательности транскрипта и белка Mus musculus, соответственно). Лиганды Notch коммерчески доступны или могут быть получены с помощью стандартных методик рекомбинантных ДНК и очищены до различной степени.
"Эмбриональные стволовые клетки", или "ES-клетки", или "ESC", относятся к недифференцированным эмбриональным стволовым клеткам, обладающим способностью интегрироваться и становиться частью зародышевой линии развивающегося эмбриона. Эмбриональные стволовые клетки способны к дифференцировке в гемопоэтические клетки-предшественники. Эмбриональные стволовые клетки, пригодные для использования в данном документе, включают клетки из клеточной линии J1 ES, клеточной линии 129J ES, мышиной клеточной линии стволовых клеток D3 (номер в каталоге Американской коллекции типовых культур CRL 1934), клеточных линий R1 или E14K, полученных от мышей 129/Sv, клеточных линий, полученных от мышей Balb/c и С57В 1/6, и человеческие эмбриональные стволовые клетки (например, из WiCell Research Institute, Висконсин или ES cell International, Мельбурн, Австралия).
"WT1" означает опухоль Вильмса 1, фактор транскрипции, который содержит четыре мотива "цинковые пальцы" на С-конце и богатый пролином/глутамином ДНК-связывающий домен на N-конце. WT1 играет важную роль в нормальном развитии мочеполовой системы и является мутировавшим у небольшой субпопуляции пациентов с опухолями Вильмса. Высокий уровень экспрессии WT1 наблюдается при различных формах рака, включая рак молочной железы, рак яичника, формы острого лейкоза, сосудистые новообразования, формы меланомы, рак толстой кишки, рак легкого, рак щитовидной железы, саркому кости и мягких тканей и рак пищевода. Альтернативный сплайсинг был описан для WT1. Иллюстративные последовательности WT1 включают таковые с номерами доступа в Genbank NM_000378.4 (SEQ ID NO: 11) (человеческий транскрипт), NP_000369.3 (SEQ ID NO: 12) (человеческий белок); NM_024424.3 (SEQ ID NO: 13) (человеческий транскрипт), NP_077742.2 (SEQ ID NO: 14) (человеческий белок); NM_024426.4 (SEQ ID NO: 15) (человеческий транскрипт), NP_077744.3 (SEQ ID NO: 16); NM_001198552.1 (SEQ ID NO: 17), NP_001185481.1 (SEQ ID NO: 18) (человеческий белок); NM_001198551.1 (SEQ ID NO: 19) (человеческий транскрипт), NP_001185480.1 (SEQ ID NO: 20) (человеческий белок); NM_144783.2 (SEQ ID NO: 21) (мышиный транскрипт) и NP_659032.3 (SEQ ID NO: 22) (мышиный белок).
"Мезотелин" (MSLN) относится к гену, который кодирует белок-предшественник, который расщепляется на два продукта: фактор стимуляции мегакариоцитов и мезотелин. Фактор стимуляции мегакариоцитов действует как цитокин, который может стимулировать колониеобразование мегакариоцитов в костном мозге. Мезотелин представляет собой закрепленный с помощью гликозилфосфатидилинозита белок на клеточной поверхности, который может действовать как белок клеточной адгезии. Этот белок сверхэкспрессируется в эпителиальных мезотелиомах, формах раковых опухолей яичников и в отдельных формах плоскоклеточных карцином. Альтернативный сплайсинг дает в результате множество вариантов транскриптов. Иллюстративные последовательности мезотелина включают таковые с номерами доступа в Genbank NM_001177355.1 (SEQ ID NO: 23), NP_001170826.1 (SEQ ID NO: 24) (последовательности человеческого транскрипта и белка-предшественника, соответственно); NM_005823.5 (SEQ ID NO: 25), NP_005814.2 (SEQ ID NO: 26) (последовательности человеческого транскрипта и белка-предшественника, соответственно); NM_013404.4 (SEQ ID NO: 27), NP_037536.2 (SEQ ID NO: 28) (последовательности человеческого транскрипта и белка-предшественника, соответственно); NM_018857.1 (SEQ ID NO: 29), NP_061345.1 (SEQ ID NO: 30) (последовательности мышиного транскрипта и белка-предшественника, соответственно).
"Окрашивание посредством тетрамера МНС-пептид" относится к анализу, используемому для выявления антиген-специфических Т-клеток, главным элементом которого является тетрамер из молекул МНС, каждая из которых содержит идентичный пептид с аминокислотной последовательностью, которая является родственной (например, идентичной или близкой) по меньшей мере одному антигену, где комплекс способен связываться с Т-клетками, специфичными в отношении родственного антигена. Каждая из молекул МНС может быть меченой молекулой биотина. Биотинилированные МНС/пептиды тетрамеризуют путем добавления стрептавидина, который, как правило, имеет флуоресцентную метку. Тетрамер может быть выявлен посредством проточной цитометрии с помощью флуоресцентной метки. В определенных вариантах осуществления анализ с использованием тетрамера МНС-пептид используют для выявления или отбора TCR с высоким сродством по настоящему раскрытию.
Способы получения TCR с повышенным сродством
В качестве вводной информации: в ходе развития Т-клеток в тимусе тимоциты-предшественники проходят ряд TCR-опосредованных контрольных точек. Первая из них называется β-селекция и происходит на двойной негативной 3 (DN3) стадии развития мышиных Т-клеток. DN3 клетки, в которых успешно осуществилась реаранжировка в генном локусе Tcrb, могут экспрессировать на клеточной поверхности белок TCRβ, образующий пару с инвариантным белком пре-Тα. Этот рецептор носит название пре-TCR и он дает сигнал лиганд-независимым образом, способствуя пролиферации, дифференцировке клеток αβ линии дифференцировки в CD4/CD8 двойной позитивной (DP) стадии и реаранжировке в генном локусе Tcra (Boehmer et al., 1999, Curr. Opin. Immunol. 11:135-142). Хотя локус TCRα неактивен и закрыт для генных реаранжировок TCR до β-селекции, и TCRγ-, и δ-локусы также подвергаются реаранжировкам на DN3 стадии развития, и успешные реаранжировки в обоих этих локусах приводят в результате к экспрессии зрелых γδ-TCR, которые могут обеспечивать сигналы, которые направляют дифференцировку в направлении γδ Т-клеточной линии дифференцировки - γδ Т-клетки не проходят в ходе дифференцировки через DP стадию развития и, как правило, остаются DN или CD8αα+. Выбор судьбы клеток αβ/γδ определяется силой TCR-сигналов на данной стадии развития, так как развитие Т-клеток с пре-TCR-сигналом отличается от такового с γδ TCR-сигналом более сильным сигналом, ассоциированный со зрелыми γδ TCR (Pennington, Silva-Santos, & Hayday, 2005, Curr. Opin. Immunol. 17:108-115). Интересно, что, у многих трансгенных мышей с αβ TCR присутствует большая популяция зрелых CD24 TCRαβ-положительных CD4/CD8 дважды отрицательных (DN) клеток в тимусе, что, как было показано, обозначает клетки с "γδ-предрасположенностью", которые развиваются как результат более сильного сигнала от трансгенных TCR со зрелыми αβ в контрольной точке β-селекции (Egawa et al., 2000, PLOS One 3:1512).
В данном документе раскрывается способ получения TCR с повышенным сродством, где эктопическая экспрессия антиген-специфической TCRα-цепи до β-селекции обеспечивает возможность развития Т-клеток, экспрессирующих TCR с высоким сродством к тому же антигену при дифференцировке в присутствии родственного антигена в ходе in vitro дифференцировки Т-клеток. С помощью данного способа Т-клетки, экспрессирующие рецепторы с высоким сродством, обходят негативный отбор, принимая выбор DN TCRαβ+ линии дифференцировки в ответ на агонистические сигналы на DN3 стадии развития Т-клеток.
В определенных вариантах осуществления настоящее раскрытие предусматривает способ получения TCR с повышенным сродством, включающий а) приведение гемопоэтических клеток-предшественников в контакт со стромальными клетками и пептидным антигеном при условиях и в течение времени, достаточных для индукции дифференцировки гемопоэтических клеток-предшественников в DN TCRαβ+ тимоциты, где гемопоэтические клетки-предшественники содержат неэндогенную последовательность нуклеиновой кислоты, кодирующую TCRα-цепь из исходного TCR, специфичного в отношении пептидного антигена, и где стромальные клетки содержат неэндогенную последовательность нуклеиновой кислоты, кодирующую Delta-like-1 или Delta-like-4, и последовательность нуклеиновой кислоты, кодирующую молекулу МНС; b) выделение последовательностей нуклеиновой кислоты, кодирующих различные TCRβ-цепи из DN TCRαβ+ тимоцитов, и введение последовательностей нуклеиновой кислоты, кодирующих TCRβ-цепи, в клетки, способные экспрессировать TCR на клеточной поверхности и содержащие последовательность нуклеиновой кислоты, кодирующую TCRα-цепь из этапа а); и идентификацию TCR с повышенным сродством (например, путем выявления или отбора кандидатных TCRαβ с высоким сродством с помощью анализа с использованием МНС-тетрамеров, а затем измерения сродства связывания с таковым исходного TCRαβ).
В определенных вариантах осуществления гемопоэтические клетки-предшественники включают клетки-предшественники тимоциты или эмбриональные стволовые клетки. В других вариантах осуществления гемопоэтические клетки-предшественники получены из ткани печени плода. В других вариантах осуществления гемопоэтические клетки-предшественники включают гемопоэтические стволовые клетки, полученные или имеющие происхождение из костного мозга, пуповинной крови или периферической крови. В других вариантах осуществления гемопоэтические клетки-предшественники получены от человека, мыши, крысы или других млекопитающих. В конкретном варианте осуществления используют CD24lo Lin- CD117+ клетки-предшественники тимоциты.
Гемопоэтические клетки-предшественники были модифицированы таким образом, что они содержат неэндогенную последовательность нуклеиновой кислоты, кодирующую TCRα-цепь из исходного TCR, специфичного в отношении пептидного антигена. В конкретном варианте осуществления TCRβ-цепь также выделена из исходного TCR. Клонирование TCRα- и β-цепей можно осуществлять с помощью стандартных методик молекулярной биологии, известных в данной области. Способы клонирования цепей TCR известны в данной области (см., например, Walchli et al., 2011, PLoS ONE 6:e27930; Birkholz et al., 2009, J. Immunol. Methods 346:45-54; Kurokawa et al, 2001, Clin. Exp. Immunol. 123:340-345).
"Стромальная клетка" представляет собой клетку соединительной ткани любого органа. Стромальные клетки, которые можно использовать согласно настоящему изобретению, включают человеческие и мышиные стромальные клетки. Примеры линий стромальных клеток, которые могут быть разработаны с помощью генной инженерии экспрессирующими DL1 или DL4, включают мышиную клеточную линию стромальных клеток MS5 (Itoh, et al., Exp. Hematol. 1989, 17:145-153) и S17 и человеческие клеточные линии стромальных клеток HGS2.11, HGS2.52, HGS.18, HGS3.30, HGS3.65, HGS.3.66, HGS3.103 и HGS3.114 (доступные от Human Genome Sciences Inc., Мэриленд, см. опубликованную заявку на патент США 20020001826). В определенных вариантах осуществления стромальные клетки являются стромальными клетками костного мозга. В дополнительных вариантах осуществления используют клетки ОР9.
В определенных вариантах осуществления стромальные клетки содержат неэндогенные последовательности нуклеиновой кислоты, кодирующие DL1, такой как человеческий DL1. Иллюстративные последовательности Delta-like-1 включают таковые с номером доступа в Genbank NM_005618.3 (SEQ ID NO: 3) и NP_005609.3 (SEQ ID NO: 4) (последовательности транскрипта и белка Homo sapiens, соответственно) и с номером доступа в Genbank NM_007865.3 (SEQ ID NO: 5) и NP_031891.2 (SEQ ID NO: 6) (последовательности транскрипта и белка Mus musculus, соответственно). В определенных вариантах осуществления стромальные клетки содержат неэндогенные последовательности нуклеиновой кислоты, кодирующие DL4, такой как человеческий DL4. Иллюстративные последовательности Delta-like-4 включают таковые с номером доступа в Genbank NM_019074.3 (SEQ ID NO: 7) и NP_061947.1 (SEQ ID NO: 8) (последовательности транскрипта и белка Homo sapiens, соответственно) и с номером доступа в Genbank NM_019454.3 (SEQ ID NO: 9) и NP_062327.2 (SEQ ID NO: 10) (последовательности транскрипта и белка Mus musculus, соответственно). Лиганды Notch коммерчески доступны или могут быть получены с помощью стандартных методик рекомбинантных ДНК и очищены до различной степени.
В дополнительных вариантах осуществления стромальные клетки представляют собой клетки ОР9 или их производные, экспрессирующие DL1, такой как человеческий DL1. Клетки ОР9, экспрессирующие DL1 и DL4, были описаны ранее (Schmitt et al., 2002, Immunity 17:749-756; патент США №7575925).
В определенных вариантах осуществления стромальные клетки также содержат последовательность нуклеиновой кислоты, кодирующую молекулу МНС. В конкретных вариантах осуществления стромальные клетки содержат последовательность нуклеиновой кислоты, кодирующую молекулу МНС класса I и могут необязательно также содержать последовательность нуклеиновой кислоты, кодирующую β2-микроглобулин. Молекулы МНС класса I и β2-микроглобулина могут быть получены из молекул МНС класса I человека, мыши, крысы или других видов млекопитающих, последовательности генов и белков которых известны в данной области. В других вариантах осуществления стромальные клетки содержат последовательность нуклеиновой кислоты, кодирующую молекулу МНС класса И. Молекула МНС класса II может быть получена из молекул МНС человека, мыши, крысы или другого вида млекопитающих, последовательности генов и белков которых известны в данной области.
Данная Т-клетка будет распознавать пептидный антиген, только когда она связана с молекулой МНС клетки-хозяина (МНС-рестриктированное распознавание антигена). Выбирают исходный TCR со специфичностью в отношении известного пептидного антигена для повышения сродства TCR с помощью раскрываемых способов. Следовательно, молекулу МНС, которая связывается с конкретным пептидным антигеном, также выбирают, и она экспрессируется в стромальных клетках для обеспечения возможности МНС-рестриктированного распознавания антигена в раскрываемой in vitro системе. Способы идентификации молекулы МНС, которая связывается с пептидным антигеном, известны в данной области (см., например, Akatsuka et al., 2002, Tissue Antigens 59:502-511). В определенных вариантах осуществления молекула МНС содержит HLA-A2 и бета-2-микроглобулин, предпочтительно источником которого является человек, который может связываться, например, с пептидом WT1 с последовательностью RMFPNAPYL (SEQ ID NO: 2). В других вариантах осуществления молекула МНС содержит мышиный H-2Db, который может связываться, например, с пептидом WT1 с последовательностью RMFPNAPYL или различными мезотелиновыми пептидами, как раскрыто на фиг. 3А в Hung et al., 2007, Gene Therapy 14:921-929, или H-2Kb, который может связываться, например, с различными мезотелиновыми пептидами, как раскрыто на фиг. 3А в Hung et al. Возможные рестриктированные по H-2Db эпитопы мезотелина, раскрытые у Hung et al., включают ISKANVDVL (SEQ ID NO: 42), GQKMNAQAI (SEQ ID NO: 43), SAFQNVSGL (SEQ ID NO: 44) и LLGPNIVDL (SEQ ID NO: 45). Возможные рестриктированные по H-2Kb эпитопы мезотелина, раскрытые у Hung et al., включают EIPFTYEQL (SEQ ID NO: 46) и GIPNGYLVL (SEQ ID NO: 47).
Пептидный антиген, используемый в раскрываемых способах, относится к пептидной последовательности антигена или целевой биологической молекуле (например, полипептиду, белку), с которыми исходный TCR специфически связывается. Пептидная последовательность может быть получена из антигена, который экспрессируется на клеточной поверхности, внутри клетки или который является интегральным мембранным белком. Антиген может представлять собой антиген, полученный из организма хозяина (например, опухолевый/раковый антиген и аутоиммунный антиген), или экзогенный антиген (например, вирусный, бактериальный антиген, антиген простейших). Опухолевый или раковый антиген может быть получен из различных раковых опухолей, таких как упомянутые в данном документе. В некоторых вариантах осуществления раковый антиген включает антиген, ассоциированный с лейкозом. В определенных вариантах осуществления пептидный антиген получен из опухоли Вильмса 1 (WT1), например, пептид WT1, содержащий аминокислотную последовательность RMFPNAPYL (SEQ ID NO: 2). В других вариантах осуществления пептидный антиген получен из мезотелина, например, мезотелиновые пептиды, раскрытые на фиг. 3А в Hung et al., 2007, Gene Therapy 14:921-929. В некоторых вариантах осуществления пептид мезотелин содержит аминокислотную последовательность GQKMNAQAI (SEQ ID NO: 31). В других вариантах осуществления пептид мезотелин содержит аминокислотную последовательность, включающую ISKANVDVL (SEQ ID NO: 42), GQKMNAQAI (SEQ ID NO: 43), SAFQNVSGL (SEQ ID NO: 44) и LLGPNIVDL (SEQ ID NO: 45), EIPFTYEQL (SEQ ID NO: 46) или GIPNGYLVL (SEQ ID NO: 47). Аутоиммунные антигены представляют собой антигены, которые распознаются аутореактивными TCR, специфичными в отношении собственных антигенов, выполняющие, как следствие, иммунноэффекторные функции, вызывающие появление аутоиммунного заболевания, вызывающие обострение аутоиммунного заболевания, способствующие прогрессированию аутоиммунного заболевания, вызывающие появление или ухудшение симптомов, ассоциированных с аутоиммунным заболеванием. Например, аутореактивные TCR, специфичные в отношении пептида коллагена, могут быть пригодными в супрессивной генной терапии с помощью Treg при ревматоидном артрите. Аутоиммунные антигены могут также представлять собой антигены, расположенные на других иммунных клетках, которые обуславливают аутоиммунное заболевание или опосредуют симптомы аутоиммунного заболевания (например, В-клетках, продуцирующих аутоантитела). Например, пептидные антигены CD20 могут быть пригодными для получения TCR с повышенным сродством, которые целенаправленно воздействуют на В-клетки, вовлеченные или ассоциированные с ревматоидным артритом. Пептидный антиген может быть добавлен в культуральную систему к гемопоэтическим клеткам-предшественникам и стромальным клеткам, как описано в данном документе. Альтернативно, стромальные клетки, содержащие последовательность нуклеиновой кислоты, кодирующую пептидный антиген, представляющий интерес, можно использовать для экспрессии такого антигена в клеточной культуре. Не вдаваясь в теорию, пептидный антиген, либо добавленный как экзогенный пептидный антиген в культуральную систему, либо экспрессируемый стромальными клетками, образует комплекс с молекулой МНС, экспрессируемой стромальными клетками, с образованием комплекса МНС-пептидный антиген. Комплекс МНС-пептидный антиген обеспечивает возможность МНС-рестриктированного распознавания пептидного антигена TCR в культуральной системе. В определенных вариантах осуществления клетки ОР9 трансдуцированы посредством последовательности нуклеиновой кислоты для экспрессии антигенного пептида WT1 с последовательностью RMFPNAPYL (SEQ ID NO: 2). В других вариантах осуществления клетки ОР9 трансдуцированы посредством последовательности нуклеиновой кислоты для экспрессии антигенного пептида мезотелина GQKMNAQAI (SEQ ID NO: 31).
Пептиды, которые связываются с молекулами МНС класса I, составляют, как правило, от приблизительно 7 до приблизительно 10 аминокислот в длину. Длина пептидов, которые связываются с молекулами МНС класса II, варьирует, как правило, они составляют приблизительно 10-25 аминокислот в длину. В определенных вариантах осуществления специфичность исходного TCR в отношении пептидного антигена известна. В других вариантах осуществления специфичность исходного TCR в отношении пептидного антигена необходимо определить с помощью способов, известных в данной области (Borras et al., 2002, J. Immunol. Methods 267:79-97; Hiemstra et al., 2000, Cur. Opin. Immunol. 12:80-4). Например, если целевой антиген для исходного TCR известен, даже если не известна конкретная пептидная последовательность, пептидные библиотеки, полученные из полипептидной последовательности целевого антигена, могут быть использованы для скрининга и идентификации специфического пептидного антигена для исходного TCR.
"Вектор" представляет собой молекулу нуклеиновой кислоты, способную переносить другую нуклеиновую кислоту. Векторами могут быть, например, плазмиды, космиды, вирусы или фаги. "Вектор экспрессии" представляет собой вектор, способный управлять экспрессией белка, кодируемого одним или несколькими генами, находящимися в векторе, когда он находится в соответствующем окружении.
"Ретровирусы" представляют собой вирусы, содержащие РНК-геном. "Гаммаретровирус" относится к роду семейства Retroviridae. Иллюстративные гаммаретровирусы включают, но без ограничений, вирус, поражающий стволовые клетки мышей, вирус мышиного лейкоза, вирус лейкоза кошек, вирус саркомы кошек и вирусы ретикулоэндотелиоза птиц.
"Лентивирус" относится к роду ретровирусов, способных инфицировать делящиеся и неделящиеся клетки. Некоторые примеры лентивирусов включают HIV (вирус иммунодефицита человека: в том числе HIV 1 типа и HIV 2 типа); вирус инфекционной анемии у лошадей; кошачий вирус иммунодефицита (FIV); бычий вирус иммунодефицита (BIV) и вирус иммунодефицита обезьян (SIV).
Вектор, кодирующий нуклеокапсид вируса, также известен как "вирусный вектор". Существует большое число доступных вирусных векторов, пригодных для применения в настоящем изобретении, в том числе векторы, идентифицированные для применений, связанных с генной терапией у человека, такие как векторы, описанные Pfeifer и Verma (Pfeifer, A. and I.М. Verma. 2001. Ann. Rev. Genomics Hum. Genet. 2:177-211). Пригодные вирусные векторы включают векторы на основе РНК-вирусов, такие как векторы, полученные на основе ретровируса, например, вируса мышиного лейкоза Молони, векторы, полученные на основе (MLV), и включают более сложные векторы, полученные на основе ретровируса, например, векторы, полученные на основе лентивируса. Векторы, полученные на основе HIV-1, относятся к этой категории. Другие примеры включают лентивирусные векторы, полученные из HIV-2, FIV, вируса инфекционной анемии у лошадей, SIV и вируса меди/висна. Способы применения вирусных векторов на основе ретровируса и лентивируса и упаковывающих клеток для трансдукции целевых клеток млекопитающих посредством вирусных частиц, содержащих трансгены TCR, хорошо известны в данной области и были описаны ранее, например, в патенте США 8119772; Walchli et al., 2011, PLoS One 6:327930; Zhao et al., J. Immunol., 2005, 174:4415-4423; Engels et al., 2003, Hum. Gene Ther. 14:1155-68; Frecha et al., 2010, Mol. Ther. 18:1748-57; Verhoeyen et al., 2009, Methods Mol. Biol. 506:97-114. Конструкции на основе ретровирусного и лентивирусного вектора и системы экспрессии также коммерчески доступны.
В конкретном варианте осуществления вирусный вектор применяют для введения неэндогенной последовательности нуклеиновой кислоты, кодирующей TCRα-цепь, специфичную в отношении пептидного антигена, в гемопоэтические клетки-предшественники. В другом варианте осуществления вирусный вектор применяют для введения неэндогенной последовательности нуклеиновой кислоты, кодирующей DL1 или DL4, и последовательности нуклеиновой кислоты, кодирующей молекулу МНС, в стромальные клетки. Вирусный вектор может представлять собой ретровирусный вектор или лентивирусный вектор. Вирусный вектор может также включать последовательность нуклеиновой кислоты, кодирующую маркер трансдукции. Маркеры трансдукции для вирусных векторов известны в данной области и включают маркеры отбора, которые могут придавать резистентность к лекарственному средству, или выявляемые маркеры, такие как флуоресцентные маркеры или белки клеточной поверхности, которые могут быть выявлены с помощью таких способов, как проточная цитометрия. В конкретном варианте осуществления вирусный вектор дополнительно содержит генный маркер трансдукции, включающий зеленый флуоресцентный белок или внеклеточный домен CD2 человека. Если геном вирусного вектора содержит более одной последовательности нуклеиновой кислоты, которую необходимо экспрессировать в клетке-хозяине в виде отдельных транскриптов, вирусный вектор может также содержать дополнительную последовательность между двумя (или более) транскриптами, что обеспечивает возможность бицистронной или мультицистронной экспрессии. Примеры таких последовательностей, применяемых в вирусных векторах, включают внутренние сайты связывания рибосомы (IRES), сайты расщепления фурином, вирусный пептид 2А.
Другие векторы также можно применять для доставки полинуклеотидов, в том числе векторы на основе вирусной ДНК, включая, например, векторы на основе аденовируса и векторы на основе адено-ассоциированного вируса (AAV); векторы, полученные из вирусов простого герпеса (HSV), в том числе ампликон-векторы, HSV с дефективной репликацией и аттенуированный HSV (Krisky et al., 1998, Gene Ther. 5: 1517-30).
Другие векторы, которые были разработаны в недавнее время для применений в генной терапии, также можно применять в способах по настоящему раскрытию. Такие векторы включают векторы, полученные из бакуловирусов и альфавирусов. (Jolly D J. 1999. Emerging viral vectors. pp 209-40 в Friedmann T. ed. 1999. The development of human gene therapy. New York: Cold Spring Harbor Lab).
Гемопоэтические клетки-предшественники культивируют со стромальными клетками, содержащими последовательность нуклеиновой кислоты, кодирующую неэндогенный DL1 или DL4, и последовательность нуклеиновой кислоты, кодирующую молекулу МНС, при условиях и в течение времени, достаточных для индукции дифференцировки гемопоэтических клеток-предшественников в DN TCRαβ+ тимоциты. В определенных вариантах осуществления гемопоэтические клетки-предшественники культивируют в чашке для обработки тканевых культур на 6 см или 10 см. Концентрация гемопоэтических клеток-предшественников в культуре может составлять 1-109, или от 1×102 до 1×106, или от 1×103 до 1×104. В некоторых вариантах осуществления гемопоэтические клетки-предшественники (приблизительно 1-5×104 клеток) культивируют на монослое клеток ОР9, экспрессирующих DL1.
Один или несколько цитокинов, содействующих коммитированию и дифференцировке гемопоэтических клеток-предшественников, могут быть также добавлены в культуру. Цитокины могут быть получены от человека или другого вида. Концентрация цитокина в культуре может находиться в диапазоне от приблизительно 1 нг/мл до приблизительно 50 нг/мл. Типичные примеры цитокинов, которые можно применять, включают всех представителей семейства FGF, включая FGF-4 и FGF-2; Flt-3-лиганд, фактор стволовых клеток (SCF), тромбопоэтин (ТРО) и IL-7. Цитокины можно применять в комбинации с гликозаминогликаном, таким как гепарин сульфат. Цитокины коммерчески доступны или могут быть получены с помощью методик рекомбинантных ДНК и очищены до различной степени. Некоторые цитокины могут быть очищены от культуральных сред клеточных линий с помощью стандартных биохимических методик.
Гемопоэтические клетки-предшественники можно культивировать в культуральной среде, включая кондиционированную среду, некондиционированную среду или клеточную среду с эмбриональными стволовыми клетками. Примеры пригодной кондиционированной среды включают IMDM, DMEM или αМЕМ, кондиционированные эмбриональными клетками фибробластами (например, человеческими эмбриональными клетками фибробластами), или аналогичную среду. Примеры пригодной некондиционированной среды включают среду Дульбекко, модифицированную по способу Исков (IDMD), DMEM или αМЕМ или аналогичную среду. Культуральная среда может содержать сыворотку (например, бычью сыворотку, фетальную бычью сыворотку, телячью сыворотку, лошадиную сыворотку, человеческую сыворотку или искусственный заменитель сыворотки), или она может не содержать сыворотку.
Условия культивирования подразумевают культивирование гемопоэтических клеток-предшественников в течение времени, достаточного для индукции дифференцировки гемопоэтических клеток-предшественников в DN TCRαβ+ тимоциты. Клетки содержат в культуре, как правило, в течение приблизительно 4-5 дней, предпочтительно от приблизительно 5 до 20 дней. Понятно, что клетки можно содержать в течение соответствующего количества времени, необходимого для получения желаемого результата, т.е. желаемой клеточной композиции. Например, для получения клеточной композиции, содержащей главным образом незрелые и неактивированные Т-клетки, клетки можно содержать в культуре в течение от приблизительно 5 до 20 дней. Клетки можно содержать в культуре в течение от 20 до 30 дней для получения клеточной композиции, содержащей главным образом зрелые Т-клетки. Неадгезивные клетки также можно собирать из культуры в различные моменты времени, например, от приблизительно нескольких дней до приблизительно 25 дней. Способы культивирования гемопоэтических стволовых клеток на клеточных линиях стромальных клеток были описаны ранее (патент США №7575925; Schmitt et al., 2004, Nat. Immunol. 5:410-417; Schmitt et al., 2002, Immunity 17:749-756).
Дифференцировка гемопоэтических клеток-предшественников в DN TCRαβ+ тимоциты может быть выявлена, и данные клетки могут быть выделены с помощью стандартных способов проточной цитометрии. Одну или несколько сортировок клеток можно использовать для выделения DN TCRαβ+ тимоцитов. Например, с помощью первой сортировки клеток можно идентифицировать гемопоэтические клетки-предшественники, экспрессирующие маркер трансдукции (т.е. маркер экспрессии TCRα). В определенных вариантах осуществления маркером трансдукции является внеклеточный домен CD2 человека. В дополнительных вариантах осуществления клетки, положительные по маркеру трансдукции, можно подвергать второй сортировке клеток для скрининга в отношении клеток с фенотипом CD4- и CD8-. С помощью третьей сортировки клеток, проводимой среди DN клеток, можно осуществлять скрининг в отношении клеток, экспрессирующих TCRβ. Специалисту в данной области будет понятно, что можно спроектировать ряд таких сортировок, или одну, или несколько сортировок клеток с помощью разных комбинаций маркеров клеточной поверхности или маркеров трансдукции с целью идентификации желаемой субпопуляции DN TCRαβ+ тимоцитов. Способы сортировки DN TCRαβ+ клеток известны в данной области (патент США №7575925 и Schmitt et al., 2002, Immunity: 17:749-756).
Последовательности нуклеиновой кислоты, кодирующие различные TCRβ-цепи из DN TCRαβ+ тимоцитов, выделяют и вводят в Т-клетки, содержащие последовательность нуклеиновой кислоты, кодирующую TCRα-цепь из исходного TCR. Как рассматривалось в данном документе, способы клонирования TCRβ-цепей из клеток хорошо известны в данной области и были описаны ранее. В определенных вариантах осуществления, как только последовательности нуклеиновой кислоты, кодирующие кандидатные TCRβ-цепи, были выделены из DN TCRαβ+ тимоцитов, последовательности нуклеиновой кислоты можно подвергать процессу дополнительного отбора, посредством которого TCRβ-цепи с таким же Vβ-геном, что и задействованный в исходных TCRβ-цепях, отбирают для введения в Т-клетки. Исходный Vβ-ген, содержащий TCRβ-цепь, может быть идентифицирован в отсортированной популяции клеток с помощью специфичных для Vβ-гена праймеров для ПЦР. Одна сложность, связанная с повышением сродства антиген-специфических TCR in vitro, заключается в том, что некоторые модификации могут повысить сродство рецептора только к МНС, а не к пептиду/МНС, увеличивая, таким образом, вероятность того, что TCR будет аутореактивным. Сокращение числа кандидатных TCRβ-цепей до таковых, содержащих исходный Vβ-ген, увеличивает вероятность сохранения доменов CDR1 и CDR2 TCR, контактирующих с МНС, и ограничения вариабельности CDR3. Как рассматривалось ранее, вирусные векторы, такие как ретровирусные векторы и лентивирусные векторы, пригодны для введения последовательностей нуклеиновой кислоты, кодирующих различные TCRβ-цепи и/или исходную TCRα, в Т-клетки. В некоторых вариантах осуществления вирусный вектор дополнительно содержит генный маркер трансдукции (например, зеленый флуоресцентный белок).
Клетки, способные экспрессировать TCR на клеточной поверхности, используют для трансформации или трансдукции посредством последовательностей нуклеиновой кислоты, кодирующих различные TCRβ-цепи из DN TCRαβ+ тимоцитов. Клетки, способные экспрессировать TCR на клеточной поверхности, экспрессируют молекулу CD3. "CD3" представляет собой мультипротеиновый комплекс из шести цепей, которые устойчиво связаны с TCR на клеточной поверхности. У млекопитающих комплекс содержит CD3γ-цепь, CDδ-цепь, две CD3ε и гомодимер CD3ζ-цепей. CD3γ, CD3δ и CD3ε представляют собой близкородственные белки клеточной поверхности суперсемейства иммуноглобулинов, содержащие один иммуноглобулиновый домен. Трансмембранные участки CD3γ, CD3δ и CD3ε отрицательно заряжены, что является характеристикой, обеспечивающей возможность соединения данных цепей с положительно заряженными цепями TCR. Цитоплазматические домены цепей CD3γ, CD3δ и CD3ε содержат иммунорецепторные тирозиновые активирующие мотивы (ITAM), обеспечивающие возможность их соединения с цитозольными белковыми тирозинкиназами после стимуляции рецептора и, таким образом, посылать сигнал внутрь клетки. CD3-белки необходимы для экспрессии TCR на клеточной поверхности (см. Janeway et al., Immunobiology: The Immune System in Health and Disease, 3rd Ed., Current Biology Publications, p. 4:39, 1997).
В некоторых вариантах осуществления клетками, способными экспрессировать TCR на клеточной поверхности, являются Т-клетки, включая первичные клетки или клеточные линии, полученные от человека, мыши, крысы или других млекопитающих. В случае если Т-клетка получена от млекопитающего, она может быть получена из разнообразных источников, включая кровь, костный мозг, лимфатический узел, тимус или другие ткани или жидкости. Т-клетки могут быть обогащены или очищены. Т-клеточные линии хорошо известны в данной области, некоторые из них описаны в Sandberg et al., 2000, Leukemia 21:230-237. В определенных вариантах осуществления используют Т-клетки, у которых отсутствует эндогенная экспрессия TCRα- и β-цепей. У таких Т-клеток может естественным образом отсутствовать эндогенная экспрессия TCRα- и β-цепей, или они могли быть модифицированы для блокировки экспрессии (например, Т-клетки от трансгенной мыши, не экспрессирующие TCR α- и β-цепи, или клеточная линия, подвергнутая манипуляциям для ингибирования экспрессии TCRα- и β-цепей). В определенных вариантах осуществления используют 58 α-β- клетки, мышиную Т-клеточную линию, в которой отсутствуют эндогенные TCRα- и TCRβ-цепи (Letourneur and Malissen, 1989, Eur. J. Immunol. 19:2269-74). В других вариантах осуществления используют Т-клеточную линию Н9 (номер в каталоге НТВ-176, АТСС, Манассас, Виргиния). В определенных вариантах осуществления клетки, способные экспрессировать TCR на клеточной поверхности, не являются Т-клетками или клетками Т-клеточной линии дифференцировки, но являются клетками, которые были модифицированы для экспрессии CD3 с обеспечением возможности экспрессии TCR на клеточной поверхности (например, клетки 293 или клетки 3Т3). Экспрессия TCR на клеточной поверхности клеток, которые не относятся к Т-клеточной линии дифференцировки, была описана ранее (Szymczak et al., 2004, Nat. Biotechnol. 22:589-594).
Для идентификации предполагаемого TCR с повышенным сродством после того, как клетки, способные экспрессировать TCR на клеточной поверхности, которые также экспрессируют исходную TCRα-цепь, были трансформированы или трансдуцированы посредством библиотеки кандидатных TCRβ-цепей, антиген-специфические клетки сортируют или идентифицируют с помощью окрашивания посредством тетрамера МНС-пептид. В окрашивании посредством тетрамера МНС-пептид главным элементом является тетрамер из молекул МНС, каждая из которых содержит идентичный пептид с аминокислотной последовательностью, которая является родственной (например, идентичной или близкой) по меньшей мере одному антигену, где комплекс способен связываться с Т-клетками, специфичными в отношении родственного антигена. Каждая из молекул МНС может быть меченой молекулой биотина. Биотинилированные МНС/пептиды тетрамеризуют путем добавления стрептавидина, который, как правило, имеет флуоресцентную метку. Тетрамер может быть выявлен посредством проточной цитометрии с помощью флуоресцентной метки. Способы окрашивания посредством тетрамера МНС-пептид для выявления антиген-специфических Т-клеток хорошо известны в данной области (например, Altman et al, 1996, Science 274:94-96; Kalergis et al., 2000, J. Immunol. Methods 234:61-70; Xu and Screaton, 2002, J. Immunol. Methods 268:21-8; James et al., J. Vis. Exp. 25:1167). В определенных вариантах осуществления тетрамер МНС-пептид содержит молекулы МНС класса I. В других вариантах осуществления тетрамер МНС-пептид содержит молекулы МНС класса II. В дополнительных вариантах осуществления на этапе культивирования раскрываемого способа используют такой же пептидный антиген, что и пептид, включаемый в тетрамер МНС-пептид. В других вариантах осуществления молекула МНС, экспрессируемая стромальными клетками на этапе культивирования раскрываемого способа, является одинаковой с молекулой МНС в тетрамере МНС-пептид. Клетки, окрашенные посредством тетрамера МНС-пептид, можно один или несколько раз подвергать сортировке с помощью проточной цитометрии. С помощью первой сортировки можно отобрать трансдуцированные клетки, экспрессирующие выявляемый маркер трансдукции (например, зеленый флуоресцентный белок). Положительные по признаку трансдукции клетки также можно один или несколько раз подвергать сортировке в отношении клеток, экспрессирующих такую же Vβ-цепь, что и в исходном TCR. Специалисту в данной области будет понятно, что можно спроектировать ряд таких сортировок, или одну, или несколько сортировок клеток с помощью разных комбинаций маркеров клеточной поверхности или маркеров трансдукции с целью идентификации желаемой субпопуляции клеток.
TCR с повышенным сродством идентифицируют путем сравнения сродства связывания кандидатного TCRαβ с таковым исходного TCRαβ. Антиген-специфические Т-клетки могут затем быть клонированы и секвенированы с помощью стандартных методик молекулярной биологии. Кандидатные TCRβ-клоны могут затем быть использованы для трансдукции Т-клеток, содержащих исходную TCRα-цепь, и можно применять окрашивание посредством тетрамера МНС-пептид для сравнения степени окрашивания с таковым исходного TCRαβ, как описано ранее. Увеличение степени окрашивания, наблюдаемое в случае кандидатного TCRβ, может указывать на повышенное сродство по сравнению с исходным TCRαβ. Однако, если исходный TCRαβ был кодон-оптимизирован для увеличения экспрессии в Т-клетках, прямое сравнение степени окрашивания посредством тетрамера с таковой кандидатного TCRβ может быть невозможным. Кандидатные TCRβ-цепи также могут быть кодон-оптимизированы для прямого сравнения с исходными TCRβ.
Кандидатный TCRαβ имеет повышенное сродство по сравнению с исходным TCRαβ, если он характеризуется более сильным связыванием с пептидным антигеном, чем исходный TCRαβ. Повышенное сродство может быть определено как TCR с Ka (равновесной константой ассоциации) в отношении целевого антигена более высокой, чем таковая исходного TCR, TCR с KD (константой диссоциации) в отношении целевого антигена меньшей, чем таковая исходного TCR или со скоростью диссоциации (Koff) в отношении целевого антигена меньшей, чем таковая TCR дикого типа (или исходного). Способы измерения сродства связывания TCR были описаны ранее (например, Laugel et al., 2007, J. Biol. Chem. 282:23799-23810; Garcia et al., 2001, Proc. Natl. Acad. Sci. USA 98:6818-6823).
TCR с повышенным сродством и композиции
В другом аспекте предусматриваются TCR с повышенным сродством, полученные с помощью способов, раскрываемых в данном документе. TCR с повышенным сродством может быть фиксированным на клетке (например, экспрессированным на поверхности зрелой Т-клетки) или находиться в растворимой форме. В определенных вариантах осуществления TCR с повышенным сродством могут быть кодон-оптимизированными для повышения экспрессии в Т-клетках (Scholten et al., 2006, Clin. Immunol. 119:135-145).
В других вариантах осуществления TCR с повышенным сродством могут также быть компонентом слитого белка, который может дополнительно содержать цитотоксический компонент (например, химиотерапевтические лекарственные средства, такие как виндезин, антифолаты; бактериальные токсины, рицин, антивирусные лекарственные средства), пригодный для специфического уничтожения или повреждения раковой клетки или инфицированной клетки, или выявляемый компонент (например, биотин, флуоресцентный фрагмент, радионуклид), пригодный для визуализации раковых клеток, инфицированных клеток или тканей, подвергшихся аутоиммунному воздействию.
Настоящее раскрытие также предусматривает фармацевтические композиции, содержащие TCR с повышенным сродством, полученный с помощью способов, раскрываемых в данном документе, и фармацевтически приемлемый носитель, разбавители или наполнитель. Пригодные наполнители включают воду, солевой раствор, декстрозу, глицерин, этанол или подобные им и их комбинации.
Применения
TCR с повышенным сродством, полученные с помощью способов по настоящему раскрытию, можно применять для лечения заболевания (такого как рак, инфекционное заболевание или аутоиммунное заболевание) у субъекта путем введения композиции, содержащей TCR с повышенным сродством.
Заболевания, которые можно лечить посредством терапии с использованием TCR с повышенным сродством, включают рак, инфекционные заболевания (вирусные, бактериальные, протозойные инфекции) и аутоиммунные заболевания. Генная терапия с использованием TCR является перспективным видом лечения различных типов рака (Morgan et al., 2006, Science 314:126-129; пересмотрено в Schmitt et al, 2009, Human Gene Therapy; пересмотрено в июне 2007 г., J. Clin. Invest. 117:1466-1476) и инфекционного заболевания (Kitchen et al., 2009, PLoS One 4:38208; Rossi et al., 2007, Nat. Biotechnol. 25:1444-54; Zhang et al., PLoS Pathog. 6:e1001018; Luo et al., 2011, J. Mol. Med. 89:903-913). Иммуносупрессивная генная терапия аутоиммунных заболеваний с помощью регуляторных Т-клеток, включая аутореактивные TCR, также является перспективным видом лечения (Fujio et al., 2006, J. Immunol. 177:8140-8147; Brusko et al., 2008, Immunol. Rev. 223:371-390).
Широкий круг форм рака, включая солидные опухоли и формы лейкоза, восприимчивы к композициям и способам, раскрываемым в данном документе. Типы рака, которые можно лечить, включают формы аденокарциномы молочной железы, предстательной железы и толстой кишки; все формы бронхогенной карциномы легкого; поражение миелоидной ткани; меланому; гепатому; нейробластому; папиллому; апудому; хористому; бранхиогенный рак; карциноидный синдром; карциноидную болезнь сердца и карциному (например, карциному Уолкера, базалиому, базальную плоскоклеточную карциному, карциному Брауна-Пирс, внутрипротоковый рак, карциному Эрлиха, карциному Кребса - 2, карциному из клеток Меркеля, коллоидный рак, немелкоклеточный рак легкого, овсяноклеточный рак, папиллярную карциному, скирр, рак бронха, бронхогенный рак, плоскоклеточный рак и переходноклеточный рак). Дополнительные типы рака, которые можно лечить, включают гистиоцитарные расстройства; лейкоз; злокачественный гистиоцитоз; болезнь Ходжкина; иммунопролиферативную болезнь тонкого кишечника; неходжкинскую лимфому; плазмоцитому; ретикулоэндотелиоз; меланому; хондробластому; хондрому; хондросаркому; фиброму; фибросаркому; гигантоклеточные опухоли; гистиоцитому; липому; липосаркому; мезотелиому; миксому; миксосаркому; остеому; остеосаркому; хордому; краниофарингиому; дисгерминому; гамартому; мезенхимому; мезонефрому; миосаркому; амелобластому; цементому; одонтому; тератому; тимому; трофобластическую болезнь. Кроме того, следующие типы рака также предполагаются как восприимчивые к лечению: аденома; холангиома; холестеатома; циклиндрома; цистаденокарцинома; цистаденома; гранулезоклеточная опухоль; гинандробластома; гепатома; гидраденома; инсулома; опухоль из клеток Лейдига; папиллома; опухоль из клеток Сертоли; текома; лейомиома; лейомиосаркома; миобластома; миома; миосаркома; рабдомиома; рабдомиосаркома; эпендимома; ганглионеврома; глиома; медуллобластома; менингиома; невринома; нейробластома; нейроэпителиома; нейрофиброма; неврома; параганглиома; нехромаффинная параганглиома. Типы рака, которые можно лечить, также включают ангиокератому; ангиолимфоидную гиперплазию с эозинофилией; склерозирующую ангиому; ангиоматоз; гломангиому; гемангиоэндотелиому; гемангиому; гемангиоперицитому; гемангиосаркому; лимфангиому; лимфангиомиому; лимфангиосаркому; пинеалому; карциносаркому; хондросаркому; листовидную цистосаркому; фибросаркому; гемангиосаркому; лейомиосаркому; лейкосаркому; липосаркому; лимфангиосаркому; миосаркому; миксосаркому; карциному яичника; рабдомиосаркому; саркому; новообразования; нейрофиброматоз и цервикальную дисплазию.
Примером ряда гиперпролиферативных нарушений, восприимчивых к терапии с использованием TCR с повышенным сродством, служат формы В-клеточного рака, включая В-клеточные лимфомы (такие как различные формы болезни Ходжкина, неходжкинских лимфом (NHL) или лимфом центральной нервной системы), формы лейкоза (такие как острый лимфоцитарный лейкоз (ALL), хронический лимфоцитарный лейкоз (CLL), волосатоклеточный лейкоз и хронический миелоцитарный лейкоз) и формы миеломы (такие как множественная миелома). Дополнительные формы В-клеточного рака включают мелкоклеточную лимфоцитарную лимфому, В-клеточный пролимфоцитарный лейкоз, лимфоплазмоцитарную лимфому, лимфому маргинальной зоны селезенки, плазмоклеточную миелому, солитарную плазмацитому кости, экстраоссальную плазмоцитому, экстранодальную В-клеточную лимфому маргинальной зоны мукозоассоциированной лимфоидной ткани (MALT), нодальную В-клеточную лимфому маргинальной зоны, фолликулярную лимфому, мантийноклеточную лимфому, диффузную В-клеточную крупноклеточную лимфому, медиастинальную (тимическую) В-клеточную крупноклеточную лимфому, интраваскулярную В-клеточную крупноклеточную лимфому, первичную выпотную лимфому, лимфому/лейкоз Беркитта, пролиферацию В-клеток с неясным злокачественным потенциалом, лимфогранулематоз и посттрансплантационные лимфопролиферативные нарушения.
Аутоиммунные заболевания включают: артрит, ревматоидный артрит, ювенильный ревматоидный артрит, остеоартрит, полихондрит, псориатический артрит, псориаз, дерматит, полимиозит/дерматомиозит, миозит с тельцами включения, воспалительный миозит, токсический эпидермальный некролиз, системную склеродермию и склероз, CREST-синдром, реакции, ассоциированные с воспалительным заболеванием кишечника, болезнь Крона, язвенный колит, респираторный дистресс-синдром, респираторный дистресс-синдром взрослых (ARDS), менингит, энцефалит, увеит, колит, гломерулонефрит, аллергические состояния, экзему, астму, состояния, сопровождающиеся Т-клеточной инфильтрацией, и хронические воспалительные реакции, атеросклероз, аутоиммунный миокардит, нарушение адгезии лейкоцитов, системную красную волчанку (SLE), подострую кожную красную волчанку, дискоидную волчанку, волчаночный миелит, волчаночный энцефалит, ювенильный сахарный диабет, рассеянный склероз, аллергический энцефаломиелит, нейромиелит зрительного нерва, ревматическую атаку, хорея Сиденгама, иммунные реакции, ассоциированные с гиперчувствительностью немедленного и замедленного типа, опосредованные цитокинами и Т-лимфоцитами, туберкулез, саркоидоз, гранулематоз, включая гранулематоз Вегенера и синдром Черджа-Стросс, агранулоцитоз, васкулит (включая аллергический васкулит/ангиит, ANCA и ревматоидный васкулит), апластическую анемию, анемию Даймонда-Блекфена, иммунную гемолитическую анемию, включая аутоиммунную гемолитическую анемию (AIHA), пернициозную анемию, истинную эритроцитарную аплазию (PRCA), недостаточность фактора VIII, гемофилию А, аутоиммунную нейтропению, панцитопению, лейкопению, заболевания, сопровождающиеся диапедезом лейкоцитов, воспалительные нарушения центральной нервной системы (ЦНС), синдром полиорганной недостаточности, миастению гравис, заболевания, опосредованные комплексами антиген-антитело, заболевание с поражением антителами базальной мембраны клубочков, антифосфолипидный синдром, аллергический неврит, болезнь Бехчета, болезнь Кастлемана, синдром Гудпасчера, миастенический синдром Ламберта-Итона, синдром Рейно, синдром Шегрена, синдром Стивенса-Джонсона, отторжения трансплантата после пересадки солидного органа, реакцию "трансплантат против хозяина" (GVHD), буллезный пемфигоид, пемфигус, аутоиммунные полиэндокринопатии, серонегативные спондилоартропатии, болезнь Рейтера, синдром мышечной скованности, гигантоклеточный артериит, иммунокомплексный нефрит, IgA-нефропатию, IgM-полинейропатии или IgM-опосредованную нейропатию, идиопатическую тромбоцитопеническую пурпуру (ITP), тромботическую тромбоцитопеническую пурпуру (ТТР), пурпуру Шенлейна-Геноха, аутоиммунную тромбопению, аутоиммунное заболевание яичка и яичника, включая аутоиммунный орхит и оофорит, первичный гипотиреоз; аутоиммунные эндокринные заболевания, включая аутоиммунный тиреоидит, хронический тиреоидит (тиреоидит Хашимото), подострый тиреоидит, идиопатический гипотиреоз, болезнь Аддисона, болезнь Грейвса, аутоиммунные полигландулярные синдромы (или полигландулярные эндокринопатии), сахарный диабет I типа, также называемый инсулинозависимым сахарным диабетом (IDDM), и синдром Шихана; аутоиммунный гепатит, лимфоидный интерстициальный пневмонит (HIV), облитерирующий бронхиолит (нетрансплантационный) или NSIP, синдром Гийена-Барре, васкулит крупных сосудов (включая ревматическую полимиалгию и гигантоклеточный артериит (Такаясу)), васкулит сосудов среднего размера (включая болезнь Кавасаки и узелковый полиартериит), узелковый полиартериит (PAN) и анкилозирующий спондилит, болезнь Бергера (IgA-нефропатия), быстропрогрессирующий гломерулонефрит, первичный биллиарный цирроз, целиакию спру (глютеновую энтеропатию), криоглобулинемию, криоглобулинемию, ассоциированную с гепатитом, амиотрофический латеральный склероз (ALS), заболевание коронарных артерий, семейную средиземноморскую лихорадку, микроскопический полиангиит, синдром Когана, синдром Вискотта-Олдрича и облитерирующий тромбангиит.
В конкретных вариантах осуществления способ лечения субъекта с помощью TCR с повышенным сродством, полученных с помощью способов, раскрываемых в данном документе, предусматривает субъекта с острым миелоцитарным лейкозом, острым лимфоцитарным лейкозом или хроническим миелоцитарным лейкозом.
Инфекционные заболевания включают заболевания, ассоциированные с возбудителями инфекции, и они включают любые из множества бактерий (например, патогенные Е. coli, S. typhimurium, P. aeruginosa, В. anthracis, С. botulinum, С. difficile, С. perfringens, Н. pylori, V. cholerae, Listeria spp., Rickettsia spp., Chlamydia spp. и т.п.), микобактерий и паразитов (включая любых известных паразитов-представителей Protozoa). Инфекционные вирусы включают эукариотические вирусы (например, аденовирус, буньявирус, герпесвирус, паповавирус, парамиксовирус, пикорнавирус, рабдовирус (например, бешенства), ортомиксовирус (например, гриппа), поксвирус (например, осповакцины), реовирус, ретровирусы, лентивирусы (например, HIV), флавивирусы (например, HCV) и т.п.). В определенных вариантах осуществления инфекцию, вызванную цитоплазматическими патогенами, антигены которых процессируются и выставляются с молекулами МНС класса I, лечат с помощью TCR с повышенным сродством по настоящему изобретению.
TCR с повышенным сродством можно вводить субъекту в форме фиксированных на клетке TCR (т.е. генная терапия целевой популяции клеток (зрелые Т-клетки (например, CD8+ Т-клетки) или другие клетки Т-клеточной линии дифференцировки)). В конкретном варианте осуществления вводимые субъекту клетки Т-клеточной линии дифференцировки, содержащие TCR с повышенным сродством, являются аутологическими клетками. В другом варианте осуществления TCR с повышенным сродством можно вводить субъекту в растворимой форме. Растворимые TCR известны в данной области (см., например, Molloy et al., 2005, Curr. Opin. Pharmacol. 5:438-443; патент США №6759243).
"Лечить" и "лечение" относится к оказанию медицинской помощи при заболевании, нарушении или состоянии у субъекта (т.е. индивидуума, которым может быть человек или млекопитающее, не являющееся человеком (например, примат, мышь, крыса)). В целом, соответствующая доза и схема лечения предусматривают описанные в данном документе TCR с повышенным сродством и необязательно адъювант в количестве, достаточном для обеспечения терапевтического или профилактического полезного эффекта. Терапевтический и профилактический полезный эффекты включают улучшение результатов лечения; уменьшение или смягчение симптомов, ассоциированных с заболеванием; снижение частоты симптомов; улучшение качества жизни; большая продолжительность состояния без заболевания; уменьшение длительности заболевания, стабилизация состояния при заболевании; замедление прогрессирования заболевания; ремиссия; выживаемость или увеличение выживаемости.
Фармацевтические композиции, включающие рецепторы с повышенным сродством, можно вводить способом, соответствующим заболеванию или состоянию, лечение (или предупреждение) которого предполагается, что определяют специалисты в области медицины. Соответствующая доза, подходящая длительность и частота введения композиций будут определяться такими факторами, как состояние пациента, размеры тела, тип и тяжесть заболевания, конкретная форма активного ингредиента и способ введения.
В дополнительных вариантах осуществления TCR с повышенным сродством по настоящему раскрытию можно применять в диагностических способах или способах визуализации, включая такие способы, используемые применительно к показаниям или условиям, указанным в данном документе.
ПРИМЕРЫ
Следующие примеры показывают, что, как предусматривается настоящим раскрытием, например, TCR-трансгенные тимоциты эффективно дифференцируются в "γδ подобную" CD4-CD8-CD24-TCRβ+ линию дифференцировки при воздействии родственного антигена в культурах ОР9-DL1. Кроме того, тимоциты-предшественники, экспрессирующие только TCRα-цепь из Т-клеточного клона, специфичного в отношении опухолевого антигена WT1, могут также дифференцироваться в данную зрелую TCRαβ+ линию дифференцировки в культуре OP9-DL1. Библиотеку TCRβ-цепей получали из популяции DN TCRαβ+ клеток, отсортированных из этих культур и подвергнутых скринингу на предмет реактивности в отношении тетрамера WT1 МНС, когда они образуют пару с антиген-специфической TCRα-цепью. Используя данный подход, идентифицировали несколько TCRβ-цепей, которые могут образовывать пару с антиген-специфической TCRα-цепью, для получения TCR со сродством в отношении пептида WT1, до 10 раз превосходящего сродство первоначального TCR.
Пример 1. Посредством применения пептида-агониста в ходе дифференцировки на клетках OP9-DL1 можно управлять дифференцировкой зрелых TCRαβ+ DN клеток из очищенных предшественников Т-клеток от TCR-трансгенных мышей
Агонистические сигналы посредством αβ TCR до β-селекции приводят в результате к дифференцировке "γδ-подобных" дважды отрицательных (DN) TCRαβ+ клеток в ходе развития Т-клеток in vivo, а перекрестное связывание TCR на DN3 стадии ведет к дифференцировке аналогичной линии дифференцировки в ходе in vitro дифференцировки Т-клеток на клетках OP9-DL1. Для того, чтобы определить, могут ли предшественники Т-клеток от TCR-трансгенных мышей также дифференцироваться в DN TCRαβ+ линию дифференцировки в ответ на родственный пептидный антиген на DN3 стадии, сортировали TCRαβ-CD4-CD8-CD117+CD44+ DN1 и DN2 тимоциты-предшественники от трансгенных мышей ОТ-1 (экспрессирующие TCR, специфичный в отношении пептидной последовательности овальбумина SIINFEKL (SEQ ID NO: 1), представленной на МНС класса I Н-2Kb; сток №003831, Jackson Laboratory, ME; см. также Hogquist et al., 1994, Cell 76:17-27) и культивировали с клетками OP9-DL1 (Schmitt et al., 2002, Immunity 17:749-756; патент США №7575925), трансдуцированными для экспрессии мышиных молекул МНС класса I Н-2Kb, либо при отсутствии пептида, либо с увеличивающимися концентрациями овальбумин-специфического пептида (SEQ ID NO: 1) в течение 20 дней и анализировали в различные моменты времени с помощью проточной цитометрии. При отсутствии пептида дважды положительные (DP) Т-клетки могли быть выявлены ко дню 16 и составляли основную фракцию культуры ко дню 20 (фиг. 1А). Однако развитие или выживаемость DP Т-клеток снижалась даже при очень низких концентрациях пептида (0,0001 мкМ), и DP полностью отсутствовали в культурах, содержащих 0,01 мкМ или более пептида (фиг. 1А), что указывало на то, что DP клетки подверглись негативной селекции посредством сильных агонистических сигналов в культурах OP9-DL1.
Для того, чтобы определить, управляют ли агонистические сигналы возрастающей силы развитием TCRαβ+ DN клеток, DN популяцию анализировали на предмет экспрессии CD24, маркера созревания, экспрессирующегося на высоком уровне во всех незрелых популяциях предшественников Т-клеток, и TCRβ. Большая часть клеток, как было обнаружено, экспрессировала на высоком уровне CD24, и у них отсутствовала экспрессия TCRβ на день 5 (фиг. 1В), но ко дню 16 большая часть DN клеток из всех условий культивирования экспрессировала TCRβ, хотя значительно большее количество CD24- клеток наблюдалось из культур, которые содержали 0,01 мкМ или более пептида (38,2% и 31,4% TCR+CD24- клеток в культурах, содержащих 0,01 и 1,0 мкМ пептида, соответственно, по сравнению с 6,9% TCR+CD24- в культуре без пептида) (фиг. 1В). Ко дню 20 ~60% всех DN клеток были TCRβ+CD24- из культур, содержащих 0,01 мкМ или 1,0 мкМ пептида, тогда как в культурах, в которые не вносили пептид, или в культурах с низкой концентрацией (0,0001 мкМ) пептида только ~20% DN были TCRβ+CD24-, и около 50% были TCRβ- (фиг. 1В, 1С). Кроме того, при сравнении уровня экспрессии TCR на поверхности при разных условиях культивирования TCRβ+ клетки, развившиеся в ответ на высокие уровни пептида, экспрессировали более высокие уровни TCRβ на клеточной поверхности (фиг. 1С). Не вдаваясь в теорию, возможно, что развитие некоторых TCRαβ+ DN клеток в культурах без добавленного пептида происходит благодаря перекрестной реактивности с другими лигандами пептид-МНС в культуральной системе OP9-DL1. Для подтверждения того, что TCRαβ+ DN клетки, наблюдавшиеся в этих культурах, не проходили при развитии через DP стадию, сортировали полученные из тимуса В6 или ОТ-1 CD69- DP клетки, которые пока не подвергались позитивной селекции, и культивировали в присутствии или при отсутствии пептида овальбумина SIINFEKL (SEQ ID NO: 1). На DP клетки В6 не оказывало эффект присутствие пептида SIINFEKL (SEQ ID NO: 1), но если тимоциты ОТ-1 DP культивировали на клетках OP9-DL1 в присутствии SIINFEKL (SEQ ID NO: 1), наблюдались все признаки негативного отбора, включая значительное уменьшение насыщенности клетками и снижение модуляции корецептора (фиг. 2). Важным является то, что DN клетки, наблюдавшиеся в этих культурах были одинаково TCR-отрицательными (фиг. 2).
Эти данные указывают на то, что посредством применения пептида-агониста в ходе дифференцировки на клетках OP9-DL1 можно управлять дифференцировкой зрелых TCRαβ+ DN клеток из очищенных предшественников Т-клеток, полученных от TCR-трансгенных мышей.
Пример 2. Трансгенная TCRα-цепь образует пару с эндогенными TCRβ-цепями и управляет развитием DN CD24- TCRαβ+ клеток с "γδ-предрасположенностью" в культуральной системе QP9-DL1
Для того, чтобы определить, будет ли экспрессия только TCRα-цепи до β-селекции также приводить в результате к отклонению линии дифференцировки DN3 предшественников Т-клеток, экспрессирующих эндогенную TCRβ-цепь, которая образует пару с введенной TCRα-цепью, способной к взаимодействию с лигандом пептид-МНС в культуральной системе OP9-DL1, превышающему определенный порог сродства, сортировали полученные от мышей В6 CD4-CD8-CD117+CD44+ DN1 и DN2 тимоциты-предшественники и трансдуцировали посредством TCRα-цепи из клона 3D специфичных в отношении антигена опухоли Вильмса (WT1) Т-клеток, которые были ранее идентифицированы как вариант с повышенным сродством, выделенный из библиотеки, полученной с помощью насыщающего мутагенеза участка CDR3 3Dα. Конструкция экспрессии 3Dα содержит мотив последовательности внутреннего сайта связывания рибосомы, следующий за ним внеклеточный домен CD2 человека (номер доступа в Genbank NM_001767.3 (SEQ ID NO: 48) и NP_001758.2 (SEQ ID NO: 49) (последовательности транскрипта и белка CD2 полной длины, соответственно)) (IRES-hCD2) в качестве маркера трансдукции. Трансдуцированные тимоциты-предшественники культивировали в присутствии или при отсутствии 1,0 мкМ рестриктированного по МНС класса I H-2Db пептида WT1 с последовательностью RMFPNAPYL (SEQ ID NO: 2) в течение 14 дней, а затем анализировали с помощью проточной цитометрии. DN клетки в hCD2-отрицательной фракции включали меньше TCRαβ+ клеток вне зависимости от присутствия пептида в условиях культивирования. Напротив, hCD2-положительная фракция (которая экспрессировала 3Dα-ген) из культур, в которые не вносили пептид, содержала 6,8% TCRβ+ клеток, и количество TCRαβ+ клеток возрастало до 16,6% при добавлении 1,0 мкМ пептида WT1 (фиг. 3А). Эти данные указывают на то, что значительная популяция TCRαβ+ DN клеток может развиваться из ранних тимоцитов-предшественников, эктопически экспрессирующих TCRα-цепь до β-селекции. Кроме того, факт того, что популяция TCRαβ+ DN клеток увеличивается, если присутствует родственный пептид (в отношении введенной TCRα-цепи), означает, что большая фракция этих клеток развилась в ответ на антиген WT1-специфические сигналы.
Вместе взятые, эти данные указывают на то, что TCRαβ+ DN популяция могла потенциально содержать клетки, экспрессирующие TCRβ-цепь, которая может образовывать пару с введенным 3Dα с образованием TCR с более высоким сродством в отношении тетрамера МНС-пептид WT1, чем у первоначального рецептора с повышенным сродством, и значительно более высоким, чем у того, который может быть выделен из обычного репертуара Т-клеток.
Следовательно, 3Dα-трансдуцированные CD4-CD8-CD117+CD44+ DN1 и DN2 тимоциты-предшественники дифференцировались на клетках OP9-DL1, экспрессирующих мышиные МНС класса 1 H-2Db и также трансдуцированных для экспрессии WT1. Неадгезивные Т-клетки собирали в течение нескольких дней вплоть до дня 21 и сортировали в отношении hCD2+CD4-CD8-TCRβ+ клеток в реагенте TRIzol (Invitrogen) (фиг. 3В). Клетки, полученные в результате сортировок в отдельные дни, объединяли; очищали РНК и получали кДНК. В исходном TCR 3D используется вариабельный участок Vb10. Для того, чтобы сохранить домены TCR CDR1 и CDR2, контактирующие с МНС, кандидатные TCRβ-цепи ограничили таковыми, содержащими данный вариабельный участок. Следовательно, Vβ10-содержащие TCRβ-цепи в отсортированной популяции клеток выделяли с помощью ПЦР с использованием Vβ10-специфического прямого праймера и Сβ2-специфического обратного праймера (фиг. 3С). Конструировали Vb10-специфический прямой праймер, таким образом, чтобы он содержал последовательность САСС, что обеспечивало возможность прямого ТОРО-клонирования в вектор pENTR™/D-TOPO® (Invitrogen) с последующим переносом с использованием технологии для рекомбинации Gateway® (Invitrogen) в ретровирусный вектор MigR1-attR (вариант вектора MigR1 (Pear et al., 1998, Blood 92:3780-3792), который был модифицирован таким образом, чтобы он содержал сайты attR и ген ccdB для клонирования с помощью Gateway®). Библиотеку MigR1-TCRβ использовали для трансдукции PlatE ретровирусных упаковывающих клеток (Morita et al., 2000, Gene Therapy 7:1063-1066; Cell Biolabs, Inc.) с получением ретровирусного супернатанта, который затем использовали для трансдукции посредством ретровируса 58 α-β- клеток мышиной Т-клеточной линии, в которой отсутствовали эндогенные TCRα- и TCRβ-цепи, (58-/-) (Letourneur and Malissen, 1989, Eur. J. Immunol. 19:2269-74).
Супернатант, содержащий ретровирусную библиотеку TCRβ, титровали и использовали разведение, которое обеспечивало наличие менее 20% трансдуцированных клеток после трансдукции, для того, чтобы обеспечить, что большинство клеток содержали только одну ретровирусную интеграцию. Трансдуцированные клетки сортировали сначала в отношении GFP-положительных клеток, а затем повторно сортировали еще два раза в отношении Vβ10+ клеток, которые также характеризовались высокой степенью окрашивания посредством тетрамера МНС-пептид WT1 (фиг. 4А). После второй сортировки клетки анализировали на предмет окрашивания посредством неродственного, но специфичного в отношении GP33 тетрамера МНС H-2Db-пептид для того, чтобы оценить, связывались ли клетки, положительные в отношении тетрамера МНС-пептид WT1, пептид-независимым образом с остатками МНС (фиг. 4А).
После третьей сортировки в отношении окрашенных с высокой степенью посредством тетрамера МНС-пептид WT1, трансдуцированных посредством библиотеки 58-/- клеток увеличивали количество отсортированных клеток, лизировали и выделяли ДНК. Ретровирусные вставки извлекали с помощью ПЦР с использованием специфичных в отношении вектора MigR1-attR праймеров, сконструированных таким образом, чтобы они включали сайты клонирования AttB Gateway® из вектора. Применяя двухэтапный подход, вставки клонировали сначала в вектор pDONR™ (Invitrogen) с использованием технологии рекомбинантного клонирования Gateway®, а затем обратно в MigR1-attR. Отдельные бактериальные колонии выбирали из реакции рекомбинантного клонирования и секвенировали. После анализа последовательности >30 клонов четыре наиболее распространенные TCRβ-цепи идентифицировали для дополнительного анализа. Интересно, что некоторые из клонов содержали последовательности CDR3β, в которых было множество таких же консервативных остатков, что и в первоначальной 3Dβ-цепи (фиг. 4В). Один из клонов (клон №1), как было обнаружено, практически идентичен первоначальной 3Dβ, за исключением замены P108Q и замены G112S (фиг. 4В). Четыре кандидатные TCRP-цепи трансдуцировали посредством ретровируса в 3Dα+58-/- клетки и анализировали с помощью проточной цитометрии (фиг. 4С). Все четыре кандидатных клона связывались с тетрамером МНС-пептид WT1, будучи трансдуцированными в 3Dα+58-/- клетки, хотя клон №4 связывался с тетрамером MHC-WT1 пептид на значительно более низком уровне, чем остальные, и его не анализировали дополнительно. Исходная 3Dβ цепь была ранее кодон-оптимизирована и в связи с этим обеспечивала экспрессию TCR на более высоком уровне на клеточной поверхности, что делало невозможным прямое сравнение степени окрашивания посредством тетрамера между 3Dβ и выделенными клонами.
Для того, чтобы наиболее точно оценить относительное сродство каждой из TCRβ-цепей в отношении тетрамера МНС-пептид WT1, 3Dα+58-/- клетки трансдуцировали посредством 3Dα, и каждую из кандидатных TCRβ-цепей окрашивали с использованием шести 2-кратных серийных разведений тетрамера МНС-пептид WT1, и значения MFI подставляли в кривую насыщения связывания, построенную с использованием нелинейной регрессии, как концентрацию лиганда, которая обеспечивала полумаксимальное связывание (фиг. 5А). Наблюдаемые значения сродства всех трех кандидатных TCRβ-цепей в случае, когда они образовывали пару с 3Dα, как было обнаружено, являлись более высокими, чем у исходной 3Dβ, и клон №1 имел ~10-кратно превосходящее сродство (фиг. 5А). Таким образом, чтобы напрямую сравнить окрашивание посредством тетрамера 3Dα, образовавшей пару с клоном №1, и таковое исходной 3Dβ, клон №1 кодон-оптимизировали таким образом, что единственное отличие в последовательности между первоначальной 3Dβ и клоном №1 было в участке CDR3. Обе конструкции трансдуцировали в 58-/- клетки и с помощью проточной цитометрии оценивали на предмет окрашивания посредством тетрамера МНС-пептид WT1. В случае, когда клон №1 был кодон-оптимизирован, было обнаружено, что он связывался с тетрамером на более высоком уровне, чем первоначальная 3Dβ, как и ожидалось (фиг. 5В).
Одна сложность, связанная с повышением сродства антиген-специфических TCR in vitro, заключается в том, что некоторые модификации могут повысить сродство рецептора только к МНС, а не к пептиду/МНС, увеличивая, таким образом, вероятность того, что TCR будет аутореактивным. Данный риск минимизировали, ограничивая библиотеку TCRβ TCRβ-цепями, которые содержали один и тот же вариабельный домен (Vb10), для того, чтобы ограничить вариабельность CDR3. Для того, чтобы определить, придает ли какая-либо из кандидатных TCRβ-цепей повышенную предрасположенность к связыванию с молекулой МНС H-2Db пептид-независимым образом, трансдуцированные 58-/- клетки окрашивали с использованием панели тетрамеров МНС H-2Db (пептиды WT1, GP33, Е4, MESN, SQV). Все три кандидатные TCRβ-цепи окрашивались в высокой степени посредством тетрамера МНС-пептид WT1 в случае, когда они образовывали пару с 3Dα, сходной с первоначальной 3Dβ (фиг. 5С). При окрашивании посредством четырех других тетрамеров МНС H-2Db-пептид все три TCRβ-цепи были одинаково отрицательными в отношении окрашивания посредством тетрамера, что означало, что возрастание сродства, наблюдавшееся у этих рецепторов, не являлось результатом возросшего сродства в отношении МНС отдельно (фиг. 5С).
Пример 3. Получение WT1-специфических Т-клеток с высоким сродством посредством эктопической экспрессии антиген-специфической TCRα-цепи в ходе раннего развития человеческих Т-клеток in vitro
Антиген опухоли Вильмса (WT1) экспрессируется на патологически высоком уровне на поверхности лейкозных клеток. Осуществляли скрининг клонов HLA A2/WT1-специфических Т-клеток в отношении клонов с высоко специфичной активностью. Выделяли TCRα- и TCRβ-цепи из клона С4, который, как было определено, имел наиболее высокое сродство в отношении WT1. Лентивирусный вектор, содержащий С4 TCR и обеспечивающий экспрессию на высоком уровне, является объектом клинического испытания, посвященного генной терапии с использованием TCR, которое планировалось проводить в 2012 г. Для того, чтобы дополнительно повысить сродство С4 TCR в отношении антигена WT1, систему дифференцировки in vitro, описанную в предыдущих примерах, применяли по отношению к клеткам-предшественникам из пуповинной крови человека, экспрессирующим С4 TCRα-цепь.
Получение WT1-специфических Т-клеток
Получали вариант клеточной линии OP9-DL1, описанной в примере 1, экспрессирующей молекулу HLA-A2 МНС класса I человека (номер доступа в Genbank U18930.1 (SEQ ID NO: 50) и ААА87076.1 (SEQ ID NO: 51), последовательности транскрипта и белка, соответственно) и молекулу β2-микроглобулина МНС класса I (β2М) человека (номер доступа в Genbank NM_004048.2 (SEQ ID NO: 52) и NP_004039.1 (SEQ ID NO: 53), последовательности транскрипта и белка, соответственно). TCRα-цепь клона С4 TCR устойчиво трансдуцировали в гемопоэтические клетки-предшественники, полученные из пуповинной крови, путем ретровирусной трансдукции с использованием ретровирусного вектора, который также кодирует зеленый флуоресцентный белок (GFP) в качестве маркера трансдукции. Клетки-предшественники, экспрессирующие GFP, сортировали с помощью проточной цитометрии и культивировали на стромальных клетках OP9-DL1-A2/β2M в присутствии или при отсутствии пептида WT1 с последовательностью RMFPNAPYL (SEQ ID NO: 2). Человеческие гемопоэтические клетки-предшественники без труда пролиферировались и дифференцировались в культуре OP9-DL1 до стадии развития человеческих Т-клеток, характеризующейся фенотипом CD34+CD1a+CD4+ (La Motte-Mohs et al., 2005, Blood 105:1431-1439), в этот момент они подвергались реаранжировкам TCR-генов в β-, γ- и δ-локусах (Spits, 2002, Nat. Rev. Immunol. 2:760-772). Существует гипотеза, что как и их мышиные аналоги, человеческие TCRα-экспрессирующие предшественники Т-клеток, в которых происходит реаранжировка в TCRβ-локусе внутри рамки считывания, примут один из двух вариантов выбора судьбы клеток: клетки, экспрессирующие TCRβ-цепь, которая не образует легко пару с трансгенной TCRα или которая образует пару с трансгенной TCRα, но не получает сильный сигнал посредством данного αβTCR, будут дифференцироваться на DP стадии в ответ на сигналы посредством пре-TCR; с другой стороны, клетки, на которых образуется TCRβ-цепь, которая может образовывать пару с трансгенной TCRα и получать достаточно сильный сигнал посредством этого зрелого αβTCR, получат сигнал к дифференцировке в направлении DN TCRαβ+ γδ-подобной линии дифференцировки. Поскольку DP клетки выживают только ~3-4 дня без сигнала позитивной селекции и поскольку эффективная позитивная селекция не происходит в культурах OP9-DL1, подавляющее большинство клеток, не получивших агонистический сигнал посредством αβ TCR, будут элиминироваться из культуры, обеспечивая возможность накопления γδ-подобных клеток, которые развиваются благодаря ранним γδ TCR-сигналам.
Выделение кандидатных TCRβ-цепей
В различные моменты культивирования неадгезивные клетки, которые имеют DN TCRαβ+ γδ-подобный фенотип и являются положительными в отношении тетрамера пептид WT1/A2 МНС, собирают посредством сортировки клеток. Выявление WT1-тетрамер-положительных клеток может быть невозможным, поскольку длительное присутствие антигена в культурах может привести в результате к снижению модуляции TCR, что может уменьшить окрашивание посредством тетрамера ниже порога выявления. Кроме того, поскольку эти клетки вероятно не экспрессируют CD8αβ, рецепторы с высоким сродством, которые не являются CD8-независимыми, невозможно выявить с помощью окрашивания посредством тетрамера. Следовательно, может быть необходимым осуществлять скрининг в отношении TCRβ-цепей из всех DN TCRαβ+ клеток, которые появляются в культуре (см. ниже). Также может быть желательно ограничить кандидатные Т-клетки клетками, в которых задействован тот же Vβ-сегмент, который задействован в первоначальной С4 TCRβ-цепи (Vβ17), для того, чтобы сохранить CDR1 и CDR2, контактирующие с МНС, исходного С4 TCR.
После сортировки клеток эндогенные TCRβ-цепи клонируют посредством очистки общей РНК путем проведения RACE ОТ-ПЦР последовательности полной длины с С-β1 или С-β2 праймерами и клонируют продукты ПЦР в вектор pENTR™/D-TOPO® (Invitrogen), что обеспечивает возможность прямого ТОРО-клонирования и включения сайтов attL, что обеспечивает возможность быстрого и эффективного переноса в ретровирусный вектор Mig-attR (вариант MigR1 (Pear et al., 1998, Blood 92:3780-3792), который содержит сайты attR для вставки гена, представляющего интерес) с использованием системы технологии для рекомбинации Gateway® от Invitrogen. Продукты реакции рекомбинации внедряют посредством электропорации в высокопроизводительные бактерии и колонии накапливают вместе и подвергают максимальной предварительной подготовке для получения ретровирусной библиотеки потенциально WT1-реактивных TCRβ-цепей.
Скрининг WT1-специфических TCR с высоким сродством
TCRβ цепи, которые могут образовывать пары с С4 TCRα-цепью с образованием WT1-специфического TCR с высоким сродством, идентифицировали путем трансдукции посредством библиотеки TCRβ в человеческую Т-клеточную линию Н9 (номер в каталоге НТВ-176, АТСС, Манассас, Виргиния), которая была трансдуцирована для экспрессии С4 TCRα-цепи (Н9-С4α). Трансдуцированные клетки сортировали с помощью проточной цитометрии в отношении высокой степени окрашивания посредством тетрамера МНС-пептид WT1 и ретровирусные вставки амплифицировали с помощью ПЦР из отсортированной популяции. Кандидатные TCRβ-цепи идентифицировали посредством ТОРО-клонирования продукта ПЦР с последующим анализом последовательности. Отобранные TCRβ-цепи и исходные С4α трансдуцировали в Н9-С4α клетки и рассчитывали значения относительного сродства в отношении тетрамера МНС-пептид WT1 путем окрашивания трансдуцированных клеток с использованием серийных 2-кратных разведений РЕ-конъюгированных тетрамеров (как описано в примере 2). Значения сродства определяли, подставляя значение MFI для каждого разведения в кривую связывания, построенную с использованием нелинейной регрессии, и KD определяли как концентрацию тетрамера, которая обеспечивала полумаксимальное связывание. TCRβ-цепи, которые могут образовывать пару с С4 TCRα, с получением TCR с более высоким сродством при окрашивании посредством тетрамера МНС-пептид, чем таковое С4 рецептора дикого типа, дополнительно исследовали в отношении безопасности и эффективности.
Пример 4. Исследовали эффективность и безопасность кандидатных TCR с высоким сродством с использованием in vivo мышиной модели WT1-направленной генной терапии с использованием TCR
Человеческие WT1-специфические TCR с повышенным сродством, которые идентифицировали как в примере 3, тестировали на безопасность и эффективность на модели WT1-направленной генной терапии на HLA-A2 трансгенных мышах.
Оценка TCR с повышенным сродством в отношении нецелевой активности
Случайную активацию TCR с высоким сродством оценивали путем измерения продуцирования цитокина TCR-трансдуцированными Т-клетками в ответ на панель А2-экспрессирующих целевых клеток в присутствии или при отсутствии пептида WT1. TCR, которые проявляют нецелевое распознавание WT1-отрицательных целевых клеток по сравнению с исходным С4 TCR, не проходят на дополнительное изучение.
Активность TCR с повышенным сродством в нормальной ткани in vivo
Экспрессия WT1 в нормальной ткани сходна у мыши и у человека, и пептид WT1, распознаваемый С4 TCR, идентичен у мышей и, как известно, процессируется и презентируется мышиными клетками (Gaiger et al., 2000, Blood 96:1480-9). HLA-A2-трансгенных мышей использовали для изучения распознавания нормальных тканей Т-клетками, экспрессирующими человеческие WT1-специфические TCR с высоким сродством (Kuball et al., 2009, J. Exp. Med. 206:463-475).
Для того, чтобы оценить безопасность TCR с повышенным сродством, полученных in vitro, как раскрывается в предыдущем примере, CD8+ Т-клетки от мышей B6.A2/Db, которые экспрессируют трансген, кодирующий домены α1 и α2 из А2, слитые с α3 из Db (для связывания мышиных CD8) (Newberg et al., 1996, J. Immunol. 156:2473-2480), трансдуцировали для экспрессии кандидатных TCR с повышенным сродством. TCR модифицировали перед трансдукцией таким образом, чтобы они содержали мышиные, а не человеческие домены Сα и Сβ, что повышало экспрессию в мышиных Т-клетках (Pouw et al., 2007, J. Gene Med. 9:561-570). Приблизительно через 4-6 недель после переноса TCR-трансдуцированных Т-клеток мышам ткани, которые, как известно, естественным образом экспрессируют WT1 (например, легких и почки) анализировали с помощью гистологических методов на предмет Т-клеточной инфильтрации и повреждения ткани, а костный мозг оценивали с помощью проточной цитометрии на предмет сокращения числа WT1-экспрессирующих гемопоэтических клеток-предшественников.
Корреляция повышенного сродства с улучшенным распознаванием цели и выполнением функций
Есть данные о том, что может существовать порог сродства для TCR, дополнительное повышение свыше которого не будет увеличивать выполнение функций Т-клетками и может фактически уменьшить чувствительность в отношении антигена (Schmid et al., 2010, J. Immunol. 184:4936-46). Таким образом, ответ TCR-трансдуцированных CD8+ Т-клеток с высоким сродством на целевые клетки, сенсибилизированные пептидом в ограничивающих концентрациях, сравнивали с таковым Т-клеток, экспрессирующих исходный С4 TCR. Анализировали продукцию цитокина (IFNγ/IL-2) и пролиферацию, а также литическую активность. TCR, проявляющие увеличенное сродство и повышенное выполнение функций, проходили на дополнительное исследование и испытания, посвященные потенциальному применению в генной терапии с использованием TCR.
Пример 5. Получение WT1-специфических Т-клеток с высоким сродством in vivo
In vivo мышиную модель (ретрогенные TCRα мыши) применяли для того, чтобы определить, могут ли TCRβ+ дважды отрицательные (DN) клетки развиваться в тимусе. Ретрогенные (транедуцированные посредством ретровируса) мыши обеспечивают возможность быстрого, по сравнению со способами трансгенеза, получения специфического TCR-трансгена, экспрессируемого мышами. Способы получения ретрогенных мышей известны в данной области (см., например, Hoist et al., 2006, Nat. Protoc. 1:406-417; Hoist et al., 2006, Nat. Methods 3:191-197; Bettini et al., 2012, Immunology 136:265-272). Вкратце, гемопоэтический предшественник/стволовые клетки, полученные из костного мозга мышей В6, очищали и трансдуцировали для экспрессии TCRα-цепи либо из WT1-специфического 3D-PYY TCR с высоким сродством, либо из мезотелин-специфического TCR 7431 с низким сродством. 3D-PYY TCR представляет собой TCR с более высоким сродством, разработанный с помощью генной инженерии на основе 3D TCR, идентифицированный с использованием системы Т-клеточного дисплея и отбора при помощи WT1/Db Ig DimerX (BD Biosciences) (Stone et al., 2011, J. Immunol. 186:5193-5200; Chervin et al., 2008, J. Immunol. Methods 339:175-184). Ретровирусная конструкция, содержащая трансгены 3D-PYY TCRα или 7431α, также включала внеклеточный домен CD2 человека в качестве маркера трансдукции с IRES между двумя трансгенами. Трансдуцированные предшественники, полученные из костного мозга, переносили в тело мышей-хозяев В6, получивших летальную дозу облучения, с получением химерных организмов, в костном мозге которых экспрессировались введенные TCRα-цепи. Через шесть недель после in vivo переноса TCRα-трансдуцированных клеток костного мозга мышей умерщвляли. Клетки из тимуса и селезенки анализировали в отношении экспрессии CD4 и CD8 с помощью проточной цитометрии (фигуры 6А, 6В). Анализ экспрессии CD4 и CD8 TCRβ+ клетками в тимусе (фигура 6А) показывает, что большая популяция дважды отрицательных TCRβ+клеток может быть выявлена in vivo в трансдуцированных тимоцитах, которые эктопически экспрессируют TCRα-цепь на ранней стадии развития, и что данная популяция представлена в большем количестве у мышей, экспрессирующих TCRα из TCR с высоким сродством (например, 3D-PYYα). DN TCRβ+ тимоциты из ретрогенных мышей, экспрессирующих 3D-PYYα и 7431α, также анализировали в отношении экспрессии Vβ10 и Vβ9, соответственно (фигура 6А). Эти данные показывают, что DN TCRβ+ популяция обогащена клетками, в которых задействован такой же сегмент Vβ-гена, что и в первоначальном антиген-специфическом TCR. Вместе взятые, эти данные подтверждают гипотезу о том, что DN TCRβ+ клетки развиваются в ответ на относительно сильные TCR-сигналы, образующиеся в результате родственных взаимодействий с целевым антигеном (т.е. WT1 или мезотелином), экспрессирующимся в тимусе. Анализ экспрессии CD4 и CD8 ретрогенными TCRβ+ спленоцитами показывает, что эти DN TCRβ+ клетки также присутствуют в периферических тканях ретрогенных мышей (фигура 6В).
Спленоциты от ретрогенных 3D-PYYα и 7431α мышей стимулировали пептидом WT1 и пептидом мезотелином, соответственно, и культивировали in vitro в присутствии IL-2 в течение 6 дней. IL-2 добавляли в культуру для того, чтобы потенциально увеличить количество антиген-специфических клеток таким образом, чтобы они могли быть выявлены с помощью окрашивания посредством тетрамера. Культуры анализировали в отношении экспрессии CD4 и CD8 с помощью проточной цитометрии в пределах гейта TCRβ+, а также в отношении экспрессии исходного Vβ-гена TCR (фигура 7). Опять наблюдалось обогащение в отношении исходного семейства Vβ-генов, в особенности в отношении 3D-PYY с высоким сродством. Культивируемые Т-клетки также анализировали в отношении присутствия антиген-специфических Т-клеток с помощью окрашивания посредством тетрамеров пептид WT1 или мезотелин/МНС (фигура 7). Эти данные показывают, что значительное количество антиген-специфических Т-клеток присутствовало в этих культурах, в особенности у ретрогенных мышей с 3D-PYYα с высоким сродством. Факт того, что тетрамер-положительные клетки обнаруживают в TCRα-трансдуцированной (hCD2+) популяции, указывает на то, что данные клетки развились в результате ранней экспрессии TCRα-цепи. Это показывает, что DN TCRβ+ клетки, развившиеся в организме этих мышей, действительно содержат антиген-специфические Т-клетки с высоким сродством. Поскольку они являются DN клетками, CD8 не вносят вклад, способствуя их связыванию с тетрамером - следовательно, эти TCR являются "CD8--независимыми" - для CD8-независимого связывания с тетрамером требуется TCR с высоким сродством.
Различные варианты осуществления, описанные выше, можно комбинировать для обеспечения дополнительных вариантов осуществления. Все патенты США, публикации заявок на патент США, заявки на патент США, иностранные патенты, иностранные заявки на патент и непатентные публикации, упоминаемые в настоящем описании и/или перечисленные в листе сведений о заявке, включены в данный документ во всей своей полноте посредством ссылки. Аспекты вариантов осуществления могут быть модифицированы, если необходимо применить идеи различных патентов, заявок и публикаций для обеспечения дополнительных вариантов осуществления.
Эти и другие изменения могут быть произведены с вариантами осуществления в свете подробно изложенного выше описания. В целом, в следующей далее формуле изобретения используемые выражения не следует толковать как ограничивающие формулу изобретения конкретными вариантами осуществления, раскрываемыми в описании и формуле изобретения, но следует толковать как включающие все возможные варианты осуществления наряду с полным объемом эквивалентов, право на которые обеспечивается такой формулой изобретения. Таким образом, настоящая формула изобретения не ограничивается настоящим раскрытием.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОПОСРЕДОВАННЫЕ ГУМАНИЗИРОВАННЫМИ Т-КЛЕТКАМИ ИММУННЫЕ ОТВЕТЫ У НЕ ОТНОСЯЩИХСЯ К ЧЕЛОВЕКУ ЖИВОТНЫХ | 2016 |
|
RU2732628C2 |
| ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫЕ В ОТНОШЕНИИ Т-КЛЕТОЧНОГО РЕЦЕПТОРА МЫШИ | 2012 |
|
RU2661106C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЙ РЕЦЕПТОР, И РОДСТВЕННЫЕ КОМПОЗИЦИИ | 2019 |
|
RU2835579C2 |
| МЕЧЕНЫЕ ХИМЕРНЫЕ ЭФФЕКТОРНЫЕ МОЛЕКУЛЫ И ИХ РЕЦЕПТОРЫ | 2014 |
|
RU2729463C2 |
| ЖИВОТНЫЕ, НЕ ЯВЛЯЮЩИЕСЯ ЧЕЛОВЕКОМ, ЭКСПРЕССИРУЮЩИЕ ЭКЗОГЕННУЮ ТЕРМИНАЛЬНУЮ ДЕЗОКСИНУКЛЕОТИДИЛТРАНСФЕРАЗУ | 2017 |
|
RU2753585C2 |
| ХИМЕРНЫЕ КОНСТРУКЦИИ АНТИТЕЛО/Т-КЛЕТОЧНЫЙ РЕЦЕПТОР И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2767209C2 |
| СПОСОБ ЛЕЧЕНИЯ АУТОИММУННОГО ЗАБОЛЕВАНИЯ С ИСПОЛЬЗОВАНИЕМ БИОСОВМЕСТИМЫХ БИОАБСОРБИРУЕМЫХ НАНОСФЕР | 2011 |
|
RU2635537C2 |
| Химерные антигенные рецепторы, нацеленные на антиген созревания B-клеток | 2016 |
|
RU2706582C2 |
| СПОСОБЫ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ИСТОЩЕНИЯ TCRαβ КЛЕТОК | 2020 |
|
RU2829624C2 |
| ГЕНЫ РЕЦЕПТОРОВ АНТИГЕНСПЕЦИФИЧНЫХ ХЕЛПЕРНЫХ Т-КЛЕТОК | 2013 |
|
RU2680588C2 |





































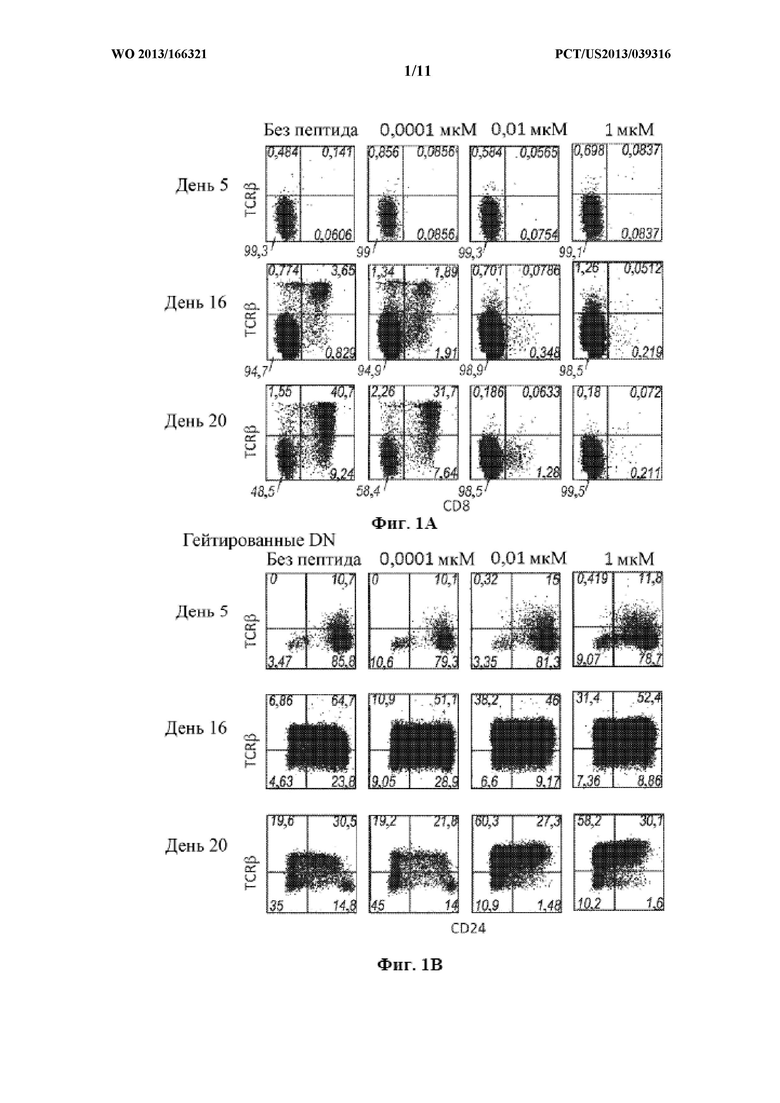
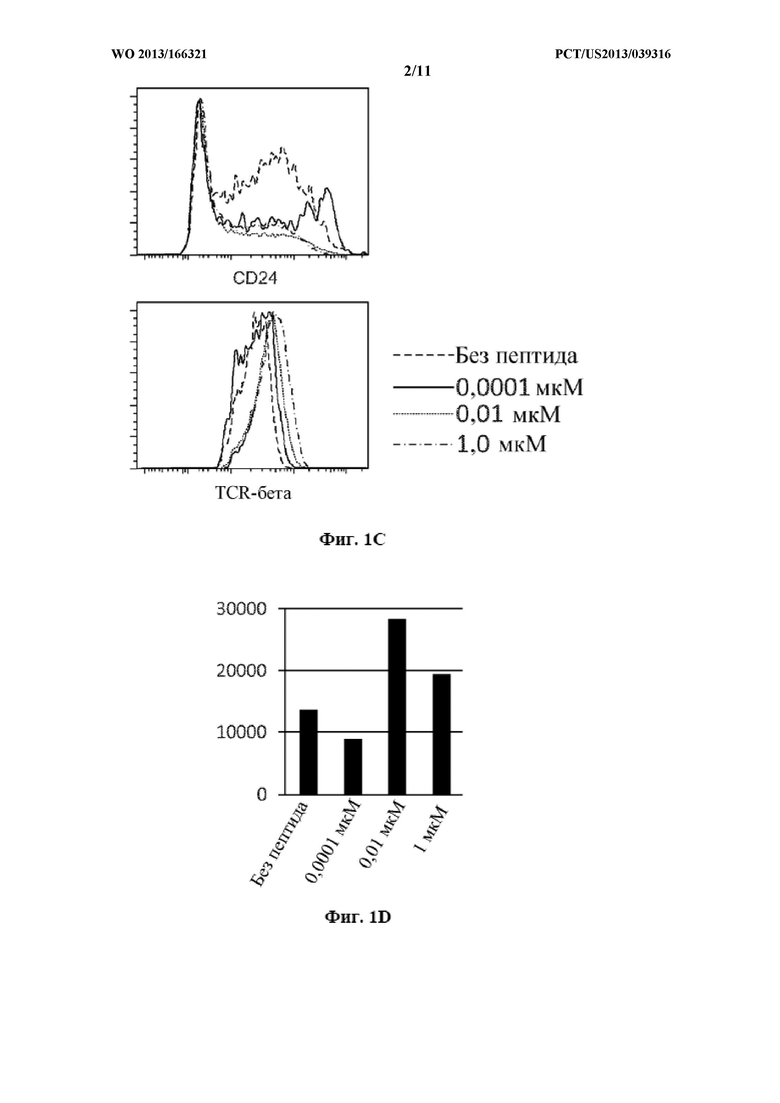
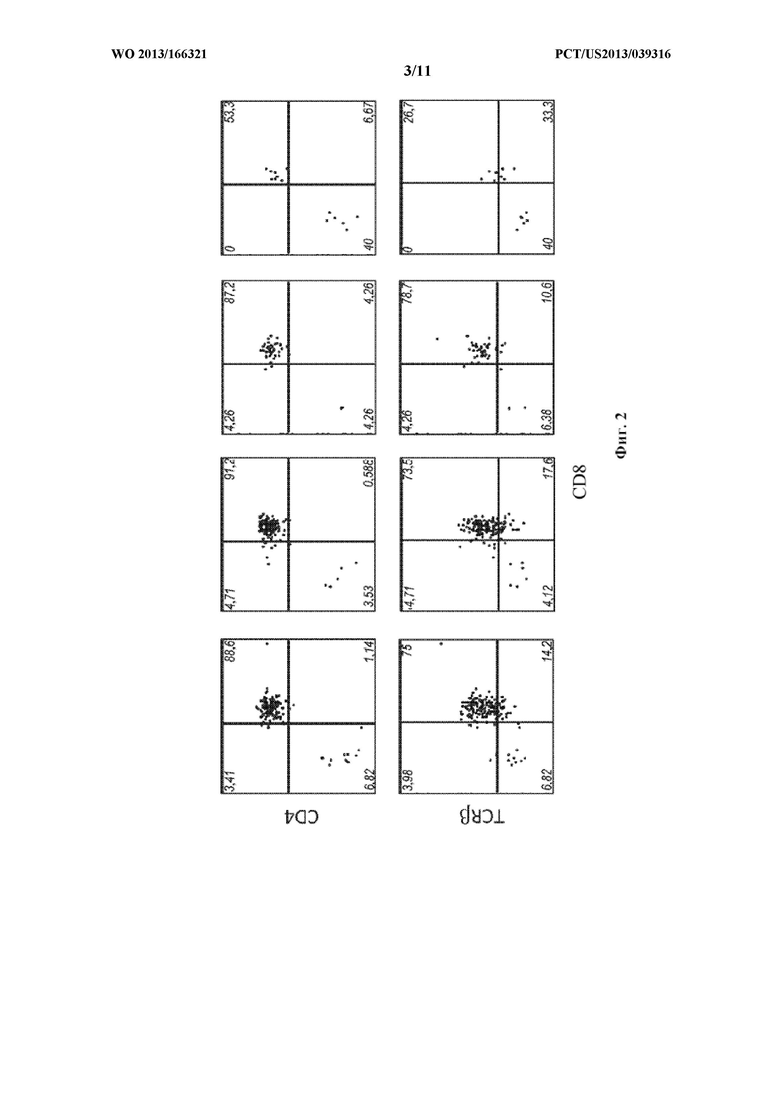
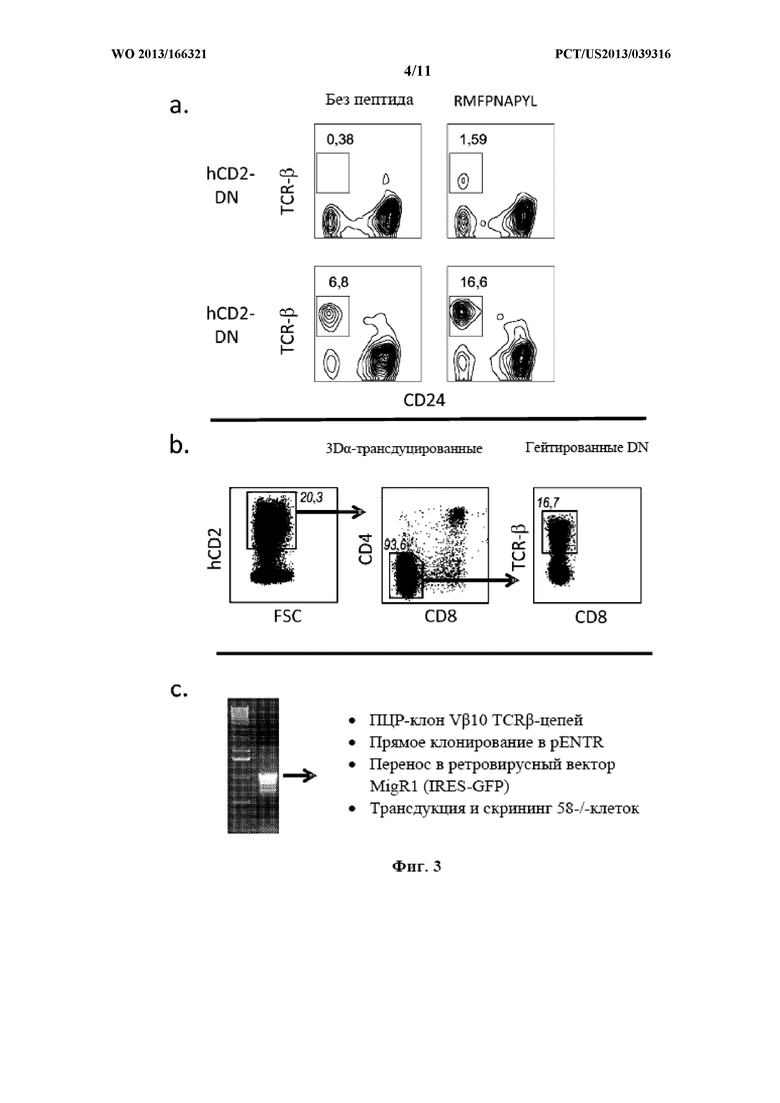
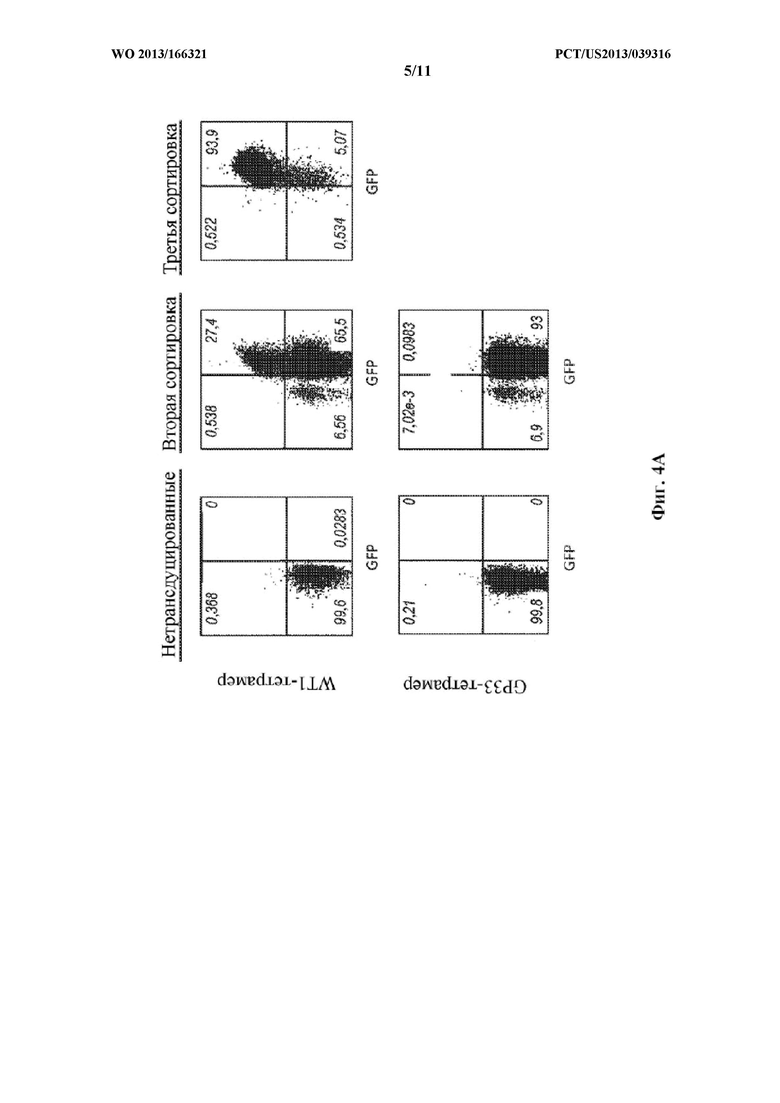


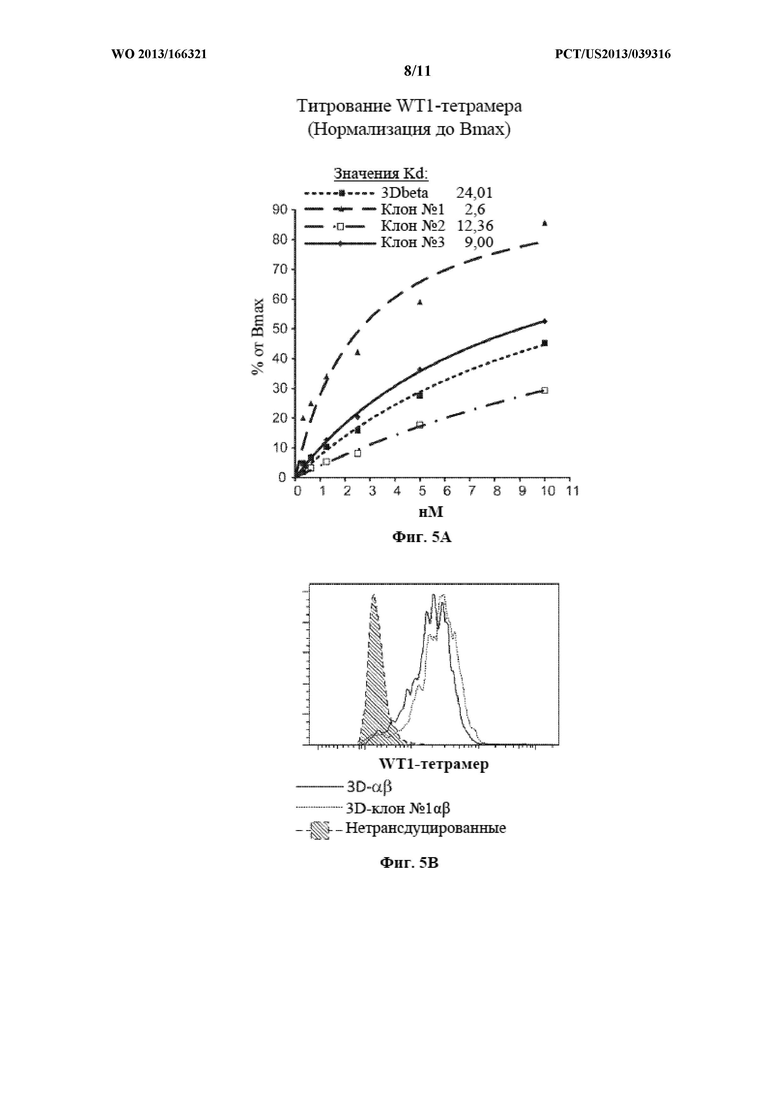
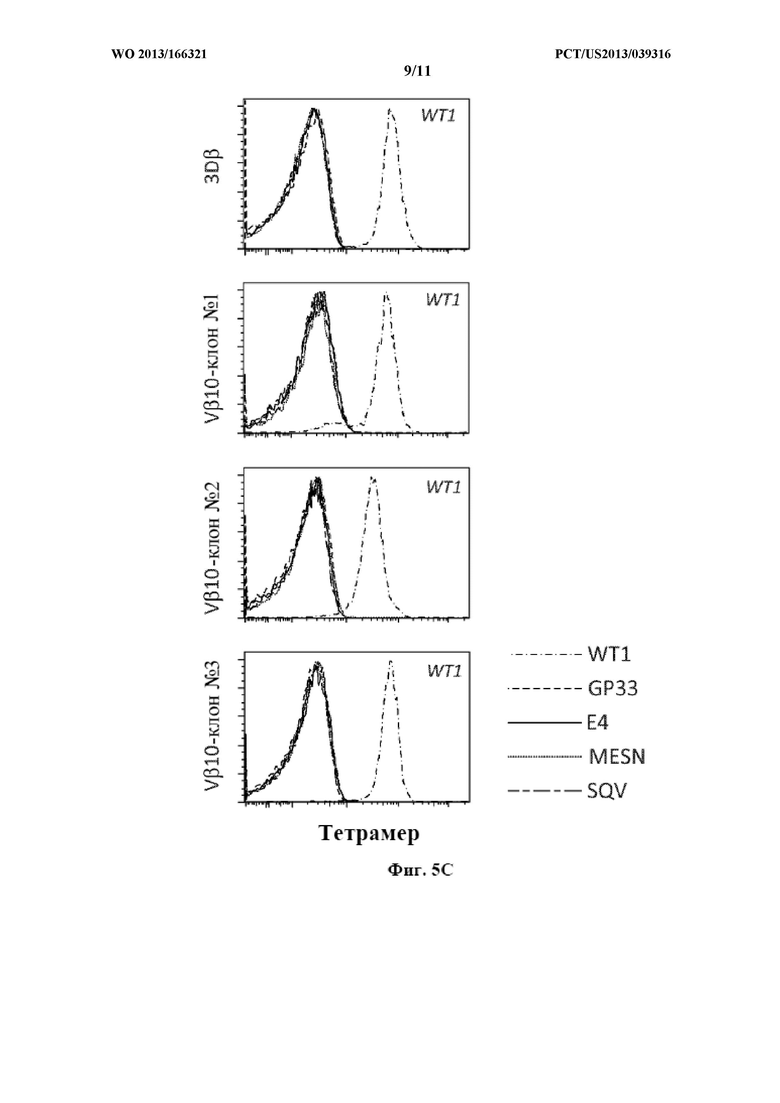
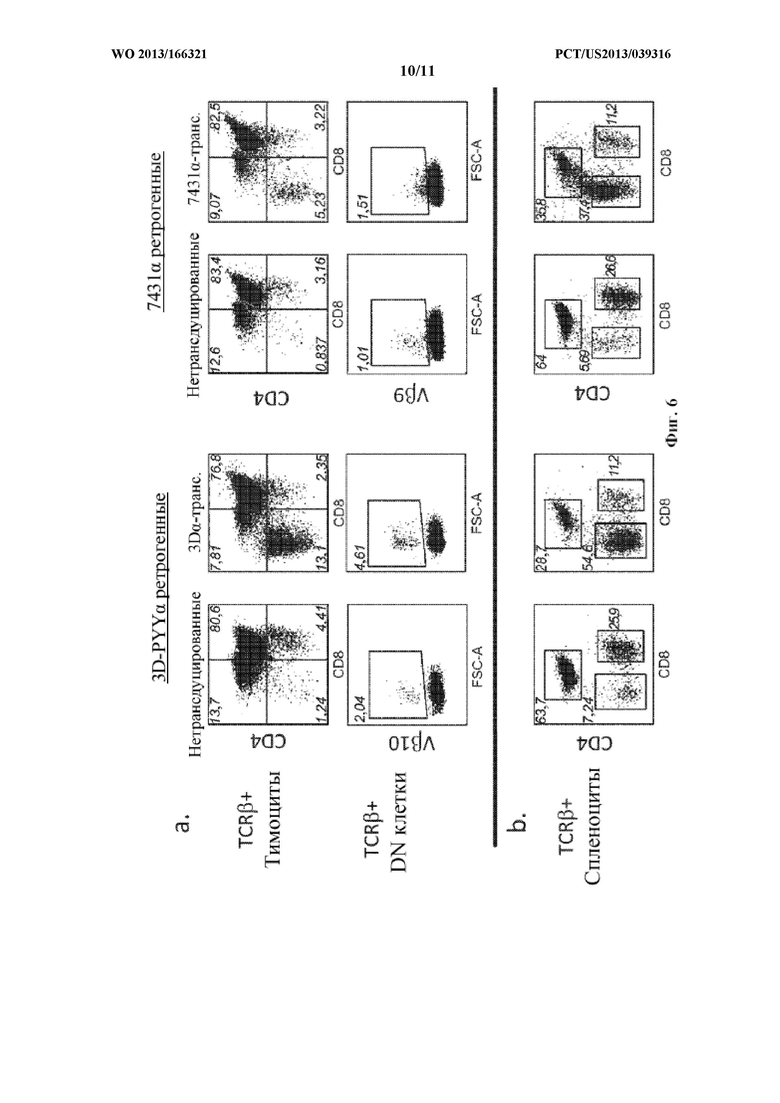
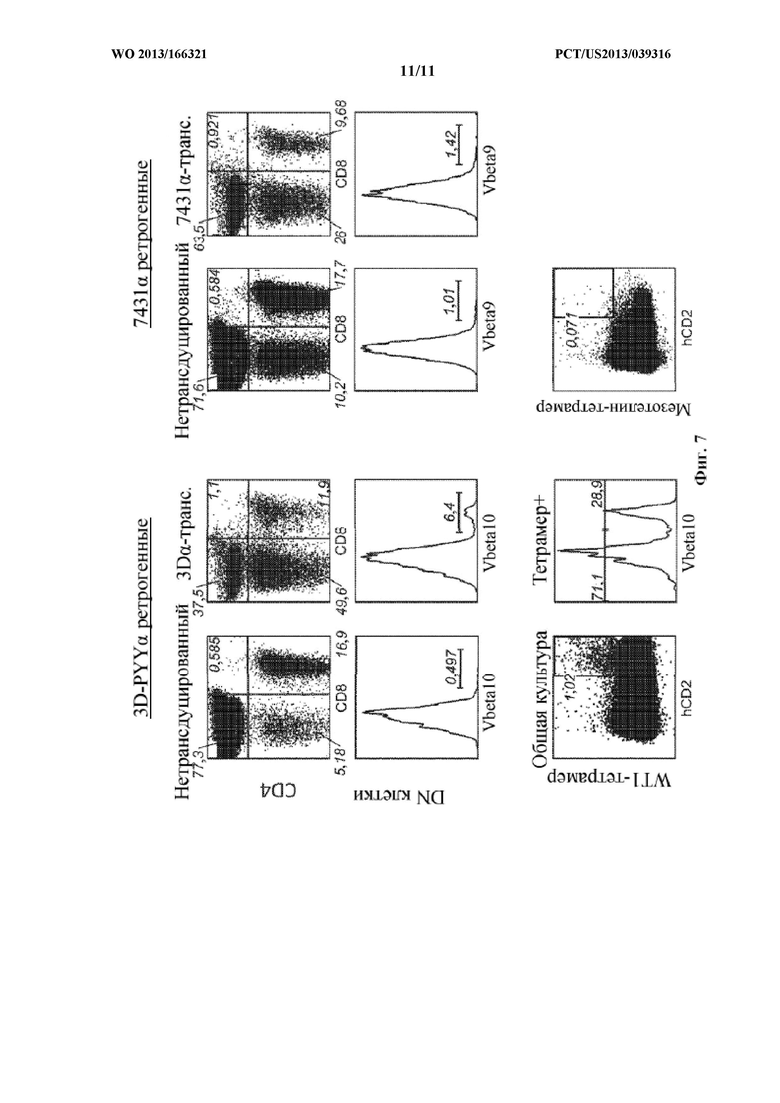
Изобретение относится к области клеточной биологии и биотехнологии, а именно к способу получения клеток, экспрессирующих Т-клеточный рецептор (TCR). Способ включает приведение клеток, способных к дифференцировке в клетки Т-клеточной линии, в контакт со стромальными клетками и пептидным антигеном для дифференцировки в DN TCRαβ+ тимоциты. При этом клетки, способные к дифференцировке в клетки Т-клеточной линии, содержат нуклеиновую кислоту, кодирующую TCRα-цепь из исходного TCR, специфичного в отношении пептидного антигена, а стромальные клетки содержат нуклеиновую кислоту, кодирующую Delta-like-1 или Delta-like-4, и нуклеиновую кислоту, кодирующую МНС. Далее, в полученные ранее клетки, содержащие нуклеиновую кислоту, кодирующую TCRα-цепь, и способные экспрессировать TCR на клеточной поверхности, вводят нуклеиновую кислоту, кодирующую TCRβ-цепи из DN TCRαβ+ тимоцитов. Изобретение позволяет получать клетки, экспрессирующие TCR. 32 з.п. ф-лы, 7 ил., 5 пр.
1. Способ получения клеток, экспрессирующих Т-клеточный рецептор (TCR), включающий
a. приведение клеток, способных к дифференцировке в клетки Т-клеточной линии, в контакт со стромальными клетками и пептидным антигеном при условиях и в течение времени, достаточных для индукции дифференцировки клеток, способных к дифференцировке в клетки Т-клеточной линии, в DN TCRαβ+ тимоциты,
где клетки, способные к дифференцировке в клетки Т-клеточной линии, содержат неэндогенную последовательность нуклеиновой кислоты, кодирующую TCRα-цепь из исходного TCR, специфичного в отношении пептидного антигена, и
где стромальные клетки содержат неэндогенную последовательность нуклеиновой кислоты, кодирующую Delta-like-1 или Delta-like-4, и последовательность нуклеиновой кислоты, кодирующую молекулу МНС; и
b. введение последовательностей нуклеиновой кислоты, кодирующих TCRβ-цепи из DN TCRαβ+ тимоцитов, полученных на этапе (а), в клетки, способные экспрессировать TCR на клеточной поверхности и которые содержат последовательность нуклеиновой кислоты, кодирующую TCRα-цепь из этапа (а); тем самым получая клетки, экспрессирующие TCR.
2. Способ по п. 1, дополнительно включающий оценку сродства связывания одного или нескольких TCR, экспрессируемых клетками из этапа (b).
3. Способ по п. 1, где клетки, способные к дифференцировке в клетки Т-клеточной линии, включают гематопоэтические стволовые клетки, клетки-предшественники тимоциты или эмбриональные стволовые клетки, где эмбриональные стволовые клетки выбраны из (а) клеток J1 ES, (b) клеток 129 J ES, (с) клеток D3, (d) клеток R1, (е) клеток E14K, (f) клеток, полученных из мышей Balb/c, (g) клеток, полученных из мышей C57B1/6, или их комбинации.
4. Способ по п. 1, где клетки, способные к дифференцировке в клетки Т-клеточной линии, включают гемопоэтические стволовые клетки, полученные из костного мозга или пуповинной крови.
5. Способ по п. 1, где неэндогенную последовательность нуклеиновой кислоты, кодирующую TCRα-цепь, специфичную в отношении пептидного антигена, вводят в клетки, способные к дифференцировке в клетки Т-клеточной линии, с использованием вирусного вектора, и/или указанная неэндогенная последовательность нуклеиновой кислоты содержится в вирусном векторе.
6. Способ по п. 5, где вирусный вектор является ретровирусным вектором.
7. Способ по п. 5, где вирусный вектор является лентивирусным вектором.
8. Способ по п. 5, где вирусный вектор дополнительно содержит генный маркер трансдукции.
9. Способ по п. 8, где генный маркер трансдукции включает зеленый флуоресцентный белок или внеклеточный домен CD2 человека.
10. Способ по п. 1, где стромальные клетки экспрессируют Delta-like-1.
11. Способ по п. 1, где стромальные клетки представляют собой стромальные клетки костного мозга или получены из них.
12. Способ по п. 1, где способ дополнительно включает отбор клеток, способных экспрессировать TCR на клеточной поверхности, полученных на этапе (b), с помощью окрашивания посредством тетрамера МНС-пептид.
13. Способ по п. 12, где клетки, способные экспрессировать TCR на клеточной поверхности, полученные на этапе (b), отбирают с помощью многократного окрашивания посредством тетрамера МНС-пептид.
14. Способ по п. 1, где последовательности нуклеиновой кислоты, кодирующие TCRβ-цепи из этапа (b), вводят в клетки, способные экспрессировать TCR на клеточной поверхности, с использованием вирусного вектора, и/или содержатся в вирусном векторе.
15. Способ по п. 14, где вирусный вектор является ретровирусным вектором.
16. Способ по п. 14, где вирусный вектор является лентивирусным вектором.
17. Способ по п. 14, где вирусный вектор дополнительно содержит генный маркер трансдукции.
18. Способ по п. 17, где генный маркер трансдукции включает зеленый флуоресцентный белок.
19. Способ по п. 1, где клетки, способные экспрессировать TCR на клеточной поверхности, получают из TCRα-/β- 58 Т-клеточной гибридомы.
20. Способ по п. 1, где TCR является человеческим TCR.
21. Способ по п. 1, где молекула МНС содержит молекулу МНС класса I или молекулу МНС класса II.
22. Способ по п. 21, где молекула МНС содержит HLA-A2 и человеческий бета-2-микроглобулин (β2М).
23. Способ по п. 1, где пептидный антиген выбирают из группы, включающей вирусный антиген, бактериальный антиген, раковый антиген и аутоиммунный антиген.
24. Способ по п. 23, где пептидный антиген представляет собой пептидный антиген WT1 или пептидный антиген мезотелин.
25. Способ по п. 24, где пептидный антиген WT1 содержит аминокислотную последовательность RMFPNAPYL (SEQ ID NO:2).
26. Способ по п. 24, где пептидный антиген мезотелин содержит аминокислотную последовательность GQKMNAQAI (SEQ ID NO:31).
27. Способ по п. 1, где пептидный антиген добавляют к клеткам, способным к дифференцировке в клетки Т-клеточной линии, и стромальным клеткам в культуре.
28. Способ по п. 1, где стромальные клетки содержат последовательность нуклеиновой кислоты, кодирующую пептидный антиген.
29. Способ по п. 1, дополнительно включающий перед введением на этапе (b) выделение последовательностей нуклеиновой кислоты, кодирующих TCRβ-цепи из DN TCRαβ+ тимоцитов, где выделение дополнительно включает отбор последовательностей нуклеиновой кислоты, которые кодируют TCRβ-цепи и содержат такой же Vβ-ген, что и в исходной TCRβ-цепи, перед введением отобранных последовательностей нуклеиновой кислоты в клетки, способные экспрессировать TCR на клеточной поверхности.
30. Способ по п. 11, где стромальные клетки костного мозга получены из MS5, S17, HGS2.11, HGS2.52, HGS.18, HGS3.30, HGS3.65, HGS.3.66, HGS3.103, HGS3.114, ОР9 или любой их комбинации.
31. Способ по п. 30, где стромальные клетки костного мозга получены из ОР9.
32. Способ по п. 2, дополнительно включающий идентификацию TCR, имеющим большее связывание с пептидным антигеном, чем исходный TCR.
33. Способ по п. 1, где TCR дополнительно содержит цитотоксический или выявляемый компонент.
| US 20090217403 A1, 27.08.2009 | |||
| Автоматический парный сцепной прибор для железнодорожных повозок | 1928 |
|
SU12507A1 |
| SCHMITT TM et al | |||
| "T cell receptor gene therapy for cancer", Human Gene Therapy | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| DOSSETT ML et al., "Adoptive immunotherapy of disseminated leukemia with TCR-transduced, CD8+ T cells expressing a known endogenous TCR", Molecular Therapy | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
Авторы
Даты
2018-08-30—Публикация
2013-05-02—Подача