Перекрестная ссылка на родственные заявки
Представленная заявка испрашивает приоритет и преимущество заявки на патент США №13/925,509 и предварительной заявки на патент США №61/838,784, обе поданы 24 июня 2013.
Область техники, к которой относится изобретение
Настоящее изобретение относится к способам лечения острого или хронического зуда антагонистом рецептора NK-1. Настоящее изобретение, кроме того, относится к фармацевтическим композициям, которые содержат антагонист рецептора NK-1.
Уровень техники
Зуд, или чесотка, является неприятным кожным ощущением, которое провоцирует желание чесать. Хотя чесотка может быть острой, например, от укуса насекомого, хронический зуд возникает из-за множества различных причин. Это серьезное изнурительное состояние, сопоставимое с хронической болью, которое отрицательно сказывает на качестве жизни.
Хронический зуд затрагивает миллионы людей во всем мире, хотя достоверные эпидемиологические данные очень ограничены. Например, одно исследование сообщало, что 8-10% населения Осло страдают от хронического зуда из-за всех вместе взятых причин (F. Dalgard et al., J. Investig. Dermatol. Symp. Proc., 2004, 9(2): 120-5). Пациенты с определенными заболеваниями и состояниями сообщают о высокой частоте возникновений хронической чесотки, включая тех, у кого псориаз (78-84%), болезнь Ходжкина (25-35%), диализные пациенты (22%, и истинная полицитемия (48%) (М. Metz and S.  , CME Dermatol., 2008; 3(3): 124-143). Хронический зуд также является широко распространенным симптомом при кожной Т-клеточной лимфоме (68-93%), заболевании, которое включает грибовидный микоз и синдром Сезари (N. Meyer et al., Acta Derm. Venereol., 2010, 90:12-17). Зуд является наиболее распространенной дерматологической жалобой у пациентов пожилого возраста (S. Beauregard and В. А. Gilchrest, Arch. Dermatol., 1987, 123:1638-43). Чесотка часто является побочным эффектом некоторых лекарственных средств, таких как антагонистов рецептора EGF.
, CME Dermatol., 2008; 3(3): 124-143). Хронический зуд также является широко распространенным симптомом при кожной Т-клеточной лимфоме (68-93%), заболевании, которое включает грибовидный микоз и синдром Сезари (N. Meyer et al., Acta Derm. Venereol., 2010, 90:12-17). Зуд является наиболее распространенной дерматологической жалобой у пациентов пожилого возраста (S. Beauregard and В. А. Gilchrest, Arch. Dermatol., 1987, 123:1638-43). Чесотка часто является побочным эффектом некоторых лекарственных средств, таких как антагонистов рецептора EGF.
Антигистаминные средства иногда могут эффективно лечить чесотку, связанную с острой крапивницей, но многие хронические зудящие заболевания плохо реагируют на общепринятые антагонисты рецептора H1 (Tey H.L. and G. Yosipovitch; Br. J. Dermatol., 2011, 165(1):5-17). В дополнение к предельной эффективности, антигистаминные средства также могут вызывать невыносимую сонливость. Другие действующие в настоящий момент терапии обладают различными ограничениями. Например, противосудорожные средства, такие как габапентин, ингибируют спинномозговые механизмы в ощущении чесотки, но их использование ограничивается из-за их медленного начала действия (5-6 недель) (Metz and Stander, 2008). Антагонисты опиатных рецепторов, такие как налоксон, налмефен и налтрексон, снижали симптомы зуда у пациентов с заболеванием печени и почек, несмотря на то, что имели место значительные побочные эффекты со стороны центральной нервной системы и желудочно-кишечного тракта (Metz and  , 2008; N.V. Bergasa et al., Hepatology, 2006, 44(5): 1317-23).
, 2008; N.V. Bergasa et al., Hepatology, 2006, 44(5): 1317-23).
Субстанция P, эндогенный лиганд для рецептора нейрокинина-1 (NK-1), является значительным медиатором зуда (Т. Andoh et al., J. Pharmacol. Exp. Ther., 1998, 286:1140-5). Внутрикожная инъекция субстанции P вызывает ощущение чесотки у субъектов-людей, и связанный с чесоткой ответ у мышей. Индуцированный субстанцией Р связанный с чесоткой ответ у мышей не ингибируется антигистаминными средствами (В. Amatya et al., Skin Pharmacol. Physiol., 2010; 23:133-138; C. Weidner et al., J. Invest. Dermatol., 2000, 115:1015-1020). В эксперименте, предназначенном для изучения роли субстанции Р в зуде, Ohmura et al. сообщил, что антагонист тахикининового рецептора NK-1, BIEF 1149 CL, ингибировал поведение чесания в индуцированной пикрилхлоридом модели дерматита у мышей NC/Nga (Eur. J. Pharmacol., 2004, 491:191-194; заявка на патент США №2003/100565).
Апрепитант (Emend®), антагонист рецептора NK-1, одобрен FDA для использования в профилактике химически индуцированной тошноты и рвоты (позывов рвоты) после химиотерапии. Duval и Dubertret впервые сообщили, что пероральный прием апрепитанта (80 мг ежедневно) имел благоприятный эффект в лечении зуда у трех пациентов с синдромом Сезари (N. Engl. J. Med.., 2009, 361(14): 1415-6). Torres et al. раскрыли аналогичные результаты (J. Am. Acad. Dermatol., 2012; 66(1): e14-5).  et al. провели небольшое открытое исследование, которое продемонстрировало, что апрепитант значительно снижал хронический зуд, вызванный такими состояниями, как атопический диатез и узловатый пруриго. В данном исследовании, двадцать ранее неизлечимых пациентов получали ежедневную дозу 80 мг в течение от 3 до 13 дней. Восемьдесят процентов пациентов испытывали значительное снижение интенсивности чесотки (S.
et al. провели небольшое открытое исследование, которое продемонстрировало, что апрепитант значительно снижал хронический зуд, вызванный такими состояниями, как атопический диатез и узловатый пруриго. В данном исследовании, двадцать ранее неизлечимых пациентов получали ежедневную дозу 80 мг в течение от 3 до 13 дней. Восемьдесят процентов пациентов испытывали значительное снижение интенсивности чесотки (S.  , et al., PLoS One, 2010, 5:6, e10968). Тем не менее, Wallengren провел дополнительное двойное слепое исследование, основанное на работе Stander, которое исследовало единичную дозу апрепитанта для местного применения, смешанного в концентрации 5% с липофильной основой, на пациентах, страдающих от хронического зуда различной этиологии. Хотя лекарственное средство абсорбировалось в кожу, чесотка у пациентов не ослаблялась (J. Wallengren, Arch. Dermatol., 2012, 148(8): 957-9).
, et al., PLoS One, 2010, 5:6, e10968). Тем не менее, Wallengren провел дополнительное двойное слепое исследование, основанное на работе Stander, которое исследовало единичную дозу апрепитанта для местного применения, смешанного в концентрации 5% с липофильной основой, на пациентах, страдающих от хронического зуда различной этиологии. Хотя лекарственное средство абсорбировалось в кожу, чесотка у пациентов не ослаблялась (J. Wallengren, Arch. Dermatol., 2012, 148(8): 957-9).
Несмотря на то что пероральный прием апрепитанта, как правило, хорошо переносится, он очень дорогой, что ограничивает его применение при хроническом зуде (Tey, 2011). Кроме того, апрепитант является умеренным ингибитором, а также индуктором CYP3A4 и CYP2C9, который показывает, что должны рассматриваться взаимодействия лекарственное средство - лекарственное средство с химиотерапевтическими агентами и кортикостероидами (Torres, 2012). Mir и Coriat предположили, что риск взаимодействий лекарственное средство - лекарственное средство с апрепитантом является высоким, потому что это может изменить активность изоформы цитохрома Р450 3А4 (CYP-3A4), фермента, принимающего участие в метаболизме ряда обычно прописываемых лекарственных средств, включая ингибиторы тирозинкиназы, или индуцирование или ингибирование CYP-3A4, в зависимости от того, какие лекарственные средства даются одновременно. Ингибиторы тирозинкиназы не вызывают частую тошноту и роту; таким образом, клинический опыт одновременного введения апрепитанта и данных лекарственных средств является недостаточным. Более того, фармакокинетика ингибиторов тирозинкиназы широко варьирует между пациентами, и взаимодействия лекарственное средство - лекарственное средство являются общими (О. Mir and R. Coriat, The Lancet, 2012, 13: 964-965). Таким образом, существует потребность в дополнительных, безопасных способах лечения острого и хронического зуда.
Сущность изобретения
В одном аспекте, настоящее изобретение предусматривает способ лечения зуда у пациента, который нуждается в таком лечении, включающий стадию, на которой вводят указанному пациенту терапевтически эффективное количество 3-[(3aR,4R,5S,7aS)-5-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси]-4-(4-фторфенил)-1,3,3а,4,5,6,7,7а-октагидроизоиндол-2-ил]циклопент-2-ен-1-она или его фармацевтически приемлемой соли, сольвата или полиморфа. В одном варианте осуществления, терапевтически эффективное количество включает дозировку 0,10 мг, 0,15 мг, 0,20 мг, 0,25 мг, 0,5 мг, 0,75 мг, 1 мг, 2 мг, 2,5 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 15 мг, 20 мг, 25 мг или 30 мг один или более раз в день. В другом варианте осуществления, терапевтически эффективное количество включает дозировку 0,25 мг, 1 мг или 5 мг один раз в день. В еще одном варианте осуществления, терапевтически эффективное количество включает дозировку от приблизительно 0,1 мг до приблизительно 30 мг или от приблизительно 1 мг до приблизительно 7,5 мг. В другом варианте осуществления, терапевтически эффективное количество вводят перорально в форме таблетки. В еще одном варианте осуществления, терапевтически эффективное количество вводят один раз в день перед сном. В другом варианте осуществления, терапевтически эффективное количество вводят один раз в день, один раз в два дня, один раз в три дня, один раз в четыре дня или один раз в неделю. В других вариантах осуществления, серлопитант вводят при длительном режиме дозирования. В некоторых вариантах осуществления, терапевтически эффективное количество серлопитанта вводят в течение периода, по меньшей мере, 2 недели, 3 недели, 1 месяц, 1,5 месяца, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев или дольше.
В другом аспекте, настоящее изобретение предусматривает способ лечения зуда, включающий стадию, на которой 3-[(3aR,4R,5S,7aS)-5-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси]-4-(4-фторфенил)-1,3,3а,4,5,6,7,7а-октагидроизоиндол-2-ил]циклопент-2-ен-1-он (серлопитант) или его фармацевтически приемлемую соль, сольват или полиморф вводят пациенту, который нуждается в таком лечении, в соответствии со схемой, по которой сначала вводят, по меньшей мере, одну насыщающую дозу, и, затем вводят, по меньшей мере, одну терапевтически эффективную поддерживающую дозу. В одном варианте осуществления, насыщающая доза представляет собой пятикратную, четырехкратную, трехкратную или двукратную поддерживающую дозу. В другом варианте осуществления, насыщающая доза представляет собой трехкратную поддерживающую дозу. В еще одном варианте осуществления, насыщающую дозу вводят на день 1 и поддерживающую дозу вводят на день 2 и в дальнейшем. В другом варианте осуществления, насыщающую дозу и поддерживающую дозу вводят перед сном. В другом варианте осуществления, способ дополнительно включает стадию, на которой вводят вторую насыщающую дозу перед введением поддерживающей дозы. В одном варианте осуществления, насыщающая доза представляет собой трехкратную поддерживающую дозу, и вторая насыщающая доза представляет собой двукратную поддерживающую дозу. В еще одном варианте осуществления, терапевтически эффективная поддерживающая доза составляет 0,10 мг, 0,15 мг, 0,20 мг, 0,25 мг, 0,5 мг, 0,75 мг, 1 мг, 2 мг, 2,5 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 15 мг, 20 мг, 25 мг или 30 мг, вводимые один или более раз в день. В другом варианте осуществления, терапевтически эффективная поддерживающая доза включает дозировку 0,25 мг, 1 мг или 5 мг, вводимую один раз в день. В еще одном варианте осуществления, терапевтически эффективная поддерживающая доза включает дозировку от приблизительно 0,1 мг до приблизительно 30 мг или от приблизительно 1 мг до приблизительно 7,5 мг. В другом варианте осуществления, терапевтически эффективную поддерживающую дозу вводят один раз в день, один раз в два дня, один раз в три дня, один раз в четыре дня или один раз в неделю. В других вариантах осуществления, серлопитант вводят при длительном режиме дозирования. В некоторых вариантах осуществления, терапевтически эффективную поддерживающую дозу серлопитанта вводят в течение периода, по меньшей мере, 2 недели, 3 недели, 1 месяц, 1,5 месяца, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев или дольше. В определенных вариантах осуществления, серлопитант вводят перорально.
В одном аспекте, настоящее изобретение предусматривает фармацевтическую композицию для лечения зуда, содержащую 3-[(3aR,4R,5S,7aS)-5-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси]-4-(4-фторфенил)-1,3,3а,4,5,6,7,7а-октагидроизоиндол-2-ил]циклопент-2-ен-1-он или его фармацевтически приемлемую соль, сольват или полиморф и фармацевтически приемлемый носитель. В одном варианте осуществления, фармацевтическую композицию составляют в форме таблетки, которая содержит соединение 1 или его фармацевтически приемлемую соль, сольват или полиморф и один или более разбавителей, дезинтегрантов, поверхностно-активных веществ или смазывающих веществ. В другом варианте осуществления, композиция содержит капсулу, наполненную раствором, содержащим соединение 1 или его фармацевтически приемлемую соль, сольват или полиморф и амфифильный агент. В еще одном варианте осуществления, амфифильный агент представляет собой сложный эфир жирной кислоты и глицерина, пропиленгликоля или сорбита. В другом варианте осуществления, фармацевтическая композиция содержит 0,10 мг, 0,15 мг, 0,20 мг, 0,25 мг, 0,5 мг, 0,75 мг, 1 мг, 2 мг, 2,5 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 15 мг, 20 мг, 25 мг или 30 мг соединения 1 или его фармацевтически приемлемой соли, сольвата или полиморфа. В другом варианте осуществления, композиция содержит 0,25 мг, 1 мг или 5 мг соединения 1 или его фармацевтически приемлемой соли, сольвата или полиморфа.
В другом аспекте, настоящее изобретение предусматривает способ лечения острого или хронического зуда у пациента, который нуждается в таком лечении, включающий стадию, на которой вводят указанному пациенту терапевтически эффективное количество фармацевтической композиции, содержащей 3-[(3aR,4R,5S,7aS)-5-[1R)-1-[3,5-бис(трифторметил)фенил]этокси]-4-(4-фторфенил)-1,3,3а,4,5,6,7,7а-октагидроизоиндол-2-ил]циклопент-2-ен-1-он или его фармацевтически приемлемую соль, сольват или полиморф и фармацевтически приемлемый носитель. В одном варианте осуществления, способ включает лечение фармацевтической композицией, составленной в форме таблетки, которая содержит соединение 1 или его фармацевтически приемлемую соль, сольват или полиморф и один или более разбавителей, дезинтегрантов, поверхностно-активных веществ или смазывающих веществ. В другом варианте осуществления, способ включает стадию, на которой вводят композицию, содержащую капсулу, наполненную раствором, содержащим соединение 1 или его фармацевтически приемлемую соль, сольват или полиморф и амфифильный агент. В еще одном варианте осуществления, амфифильный агент представляет собой сложный эфир жирной кислоты и глицерина, пропиленгликоля или сорбита. В другом варианте осуществления, способ включает лечение фармацевтической композицией, содержащей 0,10 мг, 0,15 мг, 0,20 мг, 0,25 мг, 0,5 мг, 0,75 мг, 1 мг, 2 мг, 2,5 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 15 мг, 20 мг, 25 мг или 30 мг соединения 1 или его фармацевтически приемлемой соли, сольвата или полиморфа. В другом варианте осуществления, композиция содержит 0,25 мг, 1 мг или 5 мг соединения 1 или его фармацевтически приемлемой соли, сольвата или полиморфа.
В еще одном варианте осуществления, связанное с зудом состояние лечат путем введения серлопитанта (соединения 1) и дополнительного противозудного агента. В еще одном варианте осуществления, проблему со сном или расстройство сна лечат путем введения серлопитанта, необязательно в комбинации с дополнительным способствующим сну агентом.
Другие цели настоящего изобретения могут быть очевидными для специалиста в данной области техники после прочтения нижеследующего описания и формулы изобретения.
Краткое описание чертежей
Новые отличительные признаки настоящего изобретения изложены с подробностями в прилагаемой формуле изобретения. Лучшее понимание отличительных признаков и преимуществ настоящего изобретения будет получено путем ссылки на следующее подробное описание, которое представляет иллюстративные варианты осуществления, в которых используются принципы настоящего изобретения, и прилагаемые чертежи, при этом:
ФИГ. 1 изображает схему синтеза серлопитанта, соединения 1.
ФИГ. 2 иллюстрирует диффузионную ячейку Франца для исследования проникновения в кожу лекарственного средства in vitro.
ФИГ. 3 показывает совокупное высвобождение серлопитанта из составов для местного применения В и С в камере рецептора диффузионной ячейки Франца в различные моменты времени в исследовании проникновения в кожу in vitro.
ФИГ. 4 показывает количество серлопитанта (называемое «VPD737»), удерживаемое в коже в конце исследования диффузионной ячейки Франца. Каждый столбик представляет мкг серлопитанта/г кожи в 250 мкм слоях кожи. Для каждого из составов для местного применения В и С, столбики слева направо представляют собой количество серлопитанта, удерживаемое в слоях кожи от рогового слоя эпидермиса до дермы.
Подробное описание изобретения
Если не указано другое, все технические и научные термины, использованные в данной заявке, имеют те же самые значения, как это обычно понимается специалистом в данной области техники, к которой принадлежит данная заявка. Необходимо отметить, что как используется в данной заявке и в прилагаемой формуле изобретения, форма единственного числа включает множественное число, если из контекста явно не указано другое.
Сейчас будет сделана подробная ссылка для определенных предпочтительных способов лечения, соединений и способов введения данных соединений. Настоящее изобретение не ограничивается теми предпочтительными соединениями и способами, но скорее определяется формулой изобретения, вытекающей из данной заявки.
Введение
Серлопитант представляет собой антагонист рецептора нейрокинина-1 (NK-1).
Настоящее изобретение предусматривает способ лечения хронического зуда и связанных с ним состояний, с использованием серлопитанта или его фармацевтически приемлемой соли или гидрата. Химически, международное непатентованное название серлопитант относится к соединению соединения 1:

Согласно номенклатуре IUPAC соединение имеет название 3-[(3aR,4R,5S,7aS)-5-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси]-4-(4-фторфенил)-1,3,3а,4,5,6,7,7а-октагидроизоиндол-2-ил]циклопент-2-ен-1-он. Альтернативно, соединение 1 может быть названо как 3-[(3aR,4R,5S,7aS)-5-{(1R)-1-[3,5-бис(трифторметил)фенил]этокси}-4-(4-фторфенил)октагидро-2Н-изоиндол-2-ил]циклопент-2-ен-1-он. Для целей настоящего изобретения, следует понимать, что любое из этих обозначений соединения 1 может взаимозаменяемо использоваться и иметь одинаковое значение. Кроме того, следует понимать, что настоящее изобретение также охватывает рацемическую форму серлопитанта (соединения 1).
Серлопитант ранее был раскрыт как антагонист рецептора нейрокинина-1 (NK-1), ингибитор тахикинина и, в частности, субстанции Р (J. Jiang, et al., J. Med. Chem., 2009, 52:3039-3046)). Рецепторы нейрокинина представляют собой часть большого семейства сопряженных с G-белком рецепторов, которые вызывают многие из своих эффектов за счет активации инозитфосфатного пути передачи сигнала. Рецепторы NK-1 присутствуют как в центральной, так и периферической нервной системе и в сосудистых эндотелиальньгх клетках, мышцах и клетках иммунной системы. Соединение 1 является необыкновенно селективным (>39000 раз) для клонированного рецептора NK-1 человека по отношению к клонированным рецепторам NK-2 и NK-3 человека, как продемонстрировано, используя клетки яичника китайского хомячка, стабильно экспрессирующие соответствующие рецепторы (Jiang et al., 2009). Jiang et al. показали, что серлопитант связывается с рецептором NK-1 человека с Kd 46 пМ, и что он вытесняет субстанция P, связываясь с тем же самым рецептором с IC50 61 пМ.
Соединение 1 является слабым обратимым ингибитором ферментов CYP-3A4, 2С8, 2С9, 2С19, 2D6 и 1А2 человека, значения IC50 которых составляют 39, 58, 30, 29, 35 и > 100 мкМ, соответственно. Серлопитант не значительно индуцировал CYP-3A4 мРНК в трех индивидуальных препаратах гепатоцитов человека. Эти данные дают основание предположить, что серлопитант будет иметь минимальную предрасположенность к взаимодействию лекарственное средство - лекарственное средство в организме человека, и что любые взаимодействия лекарственное средство - лекарственное средство будут снижены по сравнению с другими антагонистами рецептора NK-1. Хотя универсальный датчик-скрининг серлопитанта в более, чем 145 анализах идентифицировал ряд слабых активностей от 1 до 10 мкМ, ни один из анализов, для которых IC50 < 1 мкмМ, не наблюдался. Таким образом, нецелевые активности были более, чем в 20000 раз менее эффективными, чем активность hNK-1 (Jiang et al., 2009).
Предполагается, что серлопитант и его аналоги должны быть полезными в профилактике и лечении различных клинических состояний, характеризующихся присутствием избытка активности тахикинина, в частности, субстанции Р. Серлопитант был раскрыт как средство для лечения рвоты и недержания мочи (патенты США №№US 7,217,731, US 7,345,083, US 7,544,815, US 7,645,790 и US 7,893,091, раскрытия которых включены в данную заявку путем ссылки; опубликованные заявки США №№US 2009/0270477, US 2010/0113469 и US 2010/0209496, раскрытия которых включены в данную заявку путем ссылки; и публикация РСТ WO 2007/146224, раскрытие которой включено в данную заявку путем ссылки).
Безопасность и переносимость серлопитанта были оценены в нескольких клинических испытаниях на людях касательно лечения или профилактики гиперактивности мочевого пузыря (ОАВ). В одном исследовании, в общей сложности 557 пациентов с ОАВ были распределены по группам случайным образом в данном двойном слепом, плацебо-контролируемом и контролируемом по активному веществу (толтеродин) исследовании с подбором дозы. Серлопитант в дозе 0,25 и 4 мг ежедневно значительно снизил количество ежедневных мочеиспусканий по сравнению с плацебо. Не существовало никаких связанных с лекарственным средством серьезных неблагоприятных действий, и лекарственное средство, как правило, хорошо переносилось. Тем не менее, серлопитант не показал соотношения ответа на дозу с частотой мочеиспускания, и не оказывал значительного влияния на конечные точки вторичной эффективности сильной потребности в мочеиспускании, недержании мочи и общего недержания. Толтеродин был номинально более эффективным, чем серлопитант на всех конечных точках эффективности и статистически значительно более эффективным, чем плацебо. Серлопитант не был связан с неблагоприятным действием сухости полости рта, характерного для пациентов, получающих толтеродин, антагонист мускариновых рецепторов. (См.: Frenkl, Т.L. et al., J. Urology, 2009, 181(4), Suppl. S, p. 676; Frenkl, T. L. et al., Neurourol. Urodyn., 2009, 28(2): 143-144; Frenkl, T. L. et al., European Urology Supplements, 2009, 8(4):134; Frenkl, Tara L, et al., J. Urology, 2010, 184(2): 616-622.)
Химическое описание серлопитанта
Термин «фармацевтически приемлемые соли» относится к солям, полученным из фармацевтически приемлемых нетоксичных оснований или кислот, включая неорганические или органические основания и неорганические или органические кислоты. Соли, полученные из неорганических оснований, включают соли алюминия, аммония, кальция, меди, трехвалентного железа, двухвалентного железа, лития, магния, трехвалентного марганца, двухвалентного марганца, калия, натрия, цинка и т.п. Особенно предпочтительными являются соли аммония, кальция, магния, калия и натрия. Соли в твердой форме могут существовать в более, чем одной кристаллической структуре, и также могут находиться в форме гидратов. Соли, полученные из фармацевтически приемлемых органических нетоксичных оснований, включают соли первичных, вторичных и третичных аминов, замещенных аминов, включая встречающиеся в природе замещенные амины, циклические амины, и основные ионообменные смолы, такие как аргинин, бетаин, кофеин, холин, N,N'-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, морфолин, пиперазин, пиперидин, полиаминовые смолы, прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин, трометамин и т.п. Когда соединение в соответствии с настоящим изобретением является основным, соли могут быть получены из фармацевтически приемлемых нетоксичных кислот, включая неорганические и органические кислоты. Такие кислоты включают уксусную, бензолсульфоновую, бензойную, камфорсульфоновую, лимонную, этансульфоновую, фумаровую, глюконовую, глутаминовую, бромистоводородную, хлористоводородную, изетионовую, молочную, малеиновую, яблочную, миндальную, этансульфоновую, слизевую, азотную, памовую, пантотеновую, фосфорную, янтарную, серную, винную, п-толуолсульфоновую кислоту и т.п. Особенно предпочтительными являются лимонная, бромистоводородная, хлористоводородная, малеиновая, фосфорная, серная, фумаровая и винная кислоты. Следует понимать, что, как используется в данной заявке, ссылки на соединения в соответствии с настоящим изобретением предназначены, чтобы также включать фармацевтически приемлемые соли.
Термин «сольват» относится к агрегату, который состоит из растворенного иона или молекулы с одной или более молекулами растворителя. «Сольваты» включают гидраты, то есть, агрегаты интересующего соединения с водой. Следует понимать, что, как используется в данной заявке, ссылки на соединения в соответствии с настоящим изобретением предназначены, чтобы также включать сольваты.
Термин «полиморф» относится к кристаллической форме соединения, которое может кристаллизоваться в различных формах. Настоящее изобретение также охватывает полиморфы серлопитанта. Примеры полиморфов серлопитанта включают без ограничения безводные кристаллические формы I и II серлопитанта в виде свободного основания, как описано в публикации заявки на патент США №2009/0270477 Kuethe et al. Форма I характеризуется дифракционными пиками, полученными из рентгеновской порошковой дифрактограммы, которые соответствуют d-межплоскостным расстояниям 10,4, 9,9, 9,2, 5,5, 5,0, 4,1, 3,9, 3,6 и 3,5 ангстрем. Форма II характеризуется дифракционными пиками, полученными из рентгеновской порошковой дифрактограммы, которые соответствуют d-межплоскостным расстояниям 7,7, 5,3, 4,9, 4,8, 4,6, 4,2, 3,9, 3,8 и 2,8 ангстрем. US 2009/0270477 включена в данную заявку путем ссылки в полном объеме.
Химический синтез. Серлопитант может быть получен, как описано Jiang et al. (J. Med. Chem. 2009, 52:3039-3046), который включен в данную заявку путем ссылки в полном объеме. Альтернативно, может быть использован способ Kuethe et al., как описано в патенте США №7,544,815, или Bunda et al., как описано в патенте США №7,217,731, оба из которых включены в данную заявку путем ссылки в полном объеме.
Способ Kuethe et al. изображен на фигуре 1. Коротко говоря, коммерчески доступную 4-фторфенилуксусную кислоту (2) (Sigma-Aldrich Co. LLC, St. Louis, МО) подвергают реакции с тионилхлоридом в ДМФ/толуоле с получением хлорида кислоты (3). Хлорид кислоты (3) затем подвергают реакции с гидрохлоридной солью амина Вайнреба (CH3NHOCH3⋅HCl) в присутствии гидроксида натрия с получением 2-(4-фторфенил)-N-метокси-N-метилацетамида (4). Реакция с винилом Гриньяра преобразовывает (4) в 1-(4-фторфенил)бут-3-ен-2-он (5). TES диениловый эфир (6) получают по реакции (5) с хлортриэтилсиланом (TESC1) в присутствии iPr2NEt2.
Коммерчески доступные фумароилхлорид и два эквивалента (-)-ментола (оба от Sigma-Aldrich) подвергают реакции с получением ди-(-)-ментилфумарата (7). Реакция Дильса-Альдера между (6) и (7) дает (8). Какой-либо Е-изомер диена (<5%), который присутствует, не принимает участия в реакции Дильса-Альдера. Снятие защиты и эпимеризация (8) в кислоту дает (9). Десилилирование (8) сначала давало смесь 2,3-цис- и 2,3-транс-кетонов, которая, под воздействием кристаллизации желаемого (9), изомеризовалась преимущественно в транс-соединение. Восстановление (9) три-трет-бутоксиалюмогидридом лития (Li(t-BuO)3AlH), с последующим алюмогидридом лития (LiAlH4), дает триол (10). который затем защищают н-пропилсульфонилхлоридом (н-PrSO2Cl2) с получением (11).
S-ВТВА ((S)-1-[3,5-бис(трифторметил)]фенилэтанол)) (12) подвергают реакции с трихлорацетонитрилом (Sigma-Aldrich) в присутствии основания 1,8-диазабициклоундец-7-ена (DBU) с получением имидата (13). HBF4 используют, чтобы катализировать реакцию (11) с (13) с получением эфира (14). Обработка аллиламином и бис-пропилсульфонатом циклизует (14) до аллиламин-защищенного пирролидина (15). Удаление аллильной защитной группы тиосалициловой кислотой и 1,4-бис(дифенилфосфин)бутаном (dppb), с последующим бис(дибензилиденацетон)палладием (Pd2(dba)3) и выделение с уксусной кислотой дает кристаллическую структуру (16). В заключение, (16) подвергают реакции с 1,3-циклопентандионом (Sigma-Aldrich) в изопропиловом спирте с получением соединения 1. Соединение 1 представляет собой порошок от белого до почти белого цвета. Он легко растворим в метаноле, растворим в этаноле, незначительно растворим в изопропилацетате, умеренно растворим в изопропиловом спирте, этилацетате и ацетонитриле, и нерастворим в воде.
Фармацевтические композиции
Композиции, содержащие серлопитант или его фармацевтически приемлемую соль, сольват или полиморф, как активный ингредиент, могут быть преимущественно использованы для лечения хронического зуда. В то время, как существует возможность вводить серлопитант или его фармацевтически приемлемую соль, сольват или полиморф самостоятельно, предпочтительным является, чтобы он был представлен как состав. Композиции, или лекарственные формы, могут вводить или применять самостоятельно, или в комбинации с другими агентами. Составы также могут доставлять серлопитант пациенту в комбинации с другим фармацевтически активным агентом.
Термин «композиция», как используется в данной заявке, предназначен для того, чтобы охватить продукт, содержащий конкретные ингредиенты в предварительно установленных количествах или пропорциях, а также любой продукт, который в результате получают, непосредственно или опосредованно, из комбинации конкретных ингредиентов в конкретных количествах. Данный термин по отношению к фармацевтическим композициям предназначен для того, чтобы охватить продукт, содержащий один или более активных ингредиентов и необязательный фармацевтически приемлемый носитель, содержащий инертные ингредиенты, а также любой продукт, который в результате получают, непосредственно или опосредованно, из комбинации, комплексообразования или агрегации любых двух или более ингредиентов, или из диссоциация одного или более ингредиентов, или из других типов реакций или взаимодействий одного или более ингредиентов. Как правило, фармацевтические композиции получают путем равномерного и непосредственного внесения активного ингредиента в сочетании с жидким носителем или высокодисперсным твердым носителем или обоими, и затем, если необходимо, формирования продукта в желаемый состав. В фармацевтической композиции активное целевое соединение включают в количестве, достаточном для получения желаемого эффекта в процессе или состоянии заболеваний. Соответственно, фармацевтические композиции в соответствии с настоящим изобретением охватывают любую композицию, полученную смешиванием соединения в соответствии с настоящим изобретением и фармацевтически приемлемого носителя. Указанные композиции получают в соответствии с общепринятыми способами смешивания, гранулирования или покрытия, соответственно, и содержат приблизительно от 0,1 до 75%, предпочтительно приблизительно от 1 до 50%, активного ингредиента.
Под «фармацевтически приемлемым» подразумевают, что носитель, разбавитель или эксципиент должен быть совместимым с другими ингредиентами состава и безвредным для его реципиента. Фармацевтические композиции, предназначенные для перорального применения, могут быть получены в соответствии с любым способом, известным в данной области с уровня техники для производства фармацевтических композиций, и такие композиции могут содржать один или более агентов, выбранных из группы, состоящей из подсластителей, ароматизирующих агентов, окрашивающих агентов и консервирующих агентов, для того чтобы обеспечить фармацевтически лучшие и приятные на вкус препараты.
Табетки содержат активный ингредиент в смеси с нетоксичными фармацевтически приемлемыми эксципиентами, которые являются приемлемыми для производства таблеток. Данные эксципиенты, например, могут представлять собой инертные разбавители, такие как карбонат кальция, карбонат натрия, лактозу, фосфат кальция или фосфат натрия; гранулирующие агенты и дезинтегранты, например, кукурузный крахмал или альгиновую кислоту; связывающие агенты, например, крахмал, желатин или камедь, и смазывающие агенты, например стеарат магния, стеариновую кислоту или тальк. Таблетки могут быть непокрытыми, или они могут быть покрыты, используя известные методики, чтобы задерживать распад и абсорбцию в желудочно-кишечном тракте, и, тем самым, обеспечивают продолжительное действие в течение более длительного периода. Таблетка может быть получена путем прессования или формования активного ингредиента необязательно с одним или более фармацевтически приемлемыми ингредиентами. Прессованные таблетки могут быть получены путем прессования, с использованием приемлемого оборудования, активного ингредиента в высокосыпучей форме, такой как порошок или гранулы, необязательно смешанного со связывающим агентом, смазывающим веществом, инертным разбавителем, поверхностно-активным веществом или диспергирующим агентом. Формованные таблетки могут быть получены путем формования, с использованием приемлемого оборудования, смеси порошкообразного активного ингредиента и приемлемого носителя, увлажненного инертным жидким разбавителем.
Композиции для перорального применения также могут быть представлены в форме твердых желатиновых капсул, в которых активный ингредиент смешивают с инертным твердым разбавителем, например, карбонатом кальция, фосфатом кальция или каолином, или в форме мягких желатиновых капсул, в которых активный ингредиент смешивают с водной или масляной средой, например, арахисовым маслом, жидким парафином или оливковым маслом. В частности, фармацевтическая композиция в соответствии с настоящим изобретением может содержать наполненную жидкостью капсульную лекарственную форму, в которой активный ингредиент находится в растворе в определенных комбинациях жидких и мягких эксципиентов. В одном варианте осуществления, настоящее изобретение направлено на раствор, содержащий активный агент 3-[(3aR,4R,5S,7aS)-5-{(1R)-1-[3,5-бис(трифторметил)фенил]этокси}-4-(4-фторфенил)-октагидро-2Н-изоиндол-2-ил]циклопент-2-ен-1-он (соединение 1) или его фармацевтически приемлемую соль, сольват или полиморф, и амфифильный агент, при этом указанный амфифильный агент представляет собой сложный эфир жирной кислоты и глицерина, пропиленгликоля или сорбита, как описано в опубликованной заявке на патент США №2010/0209496 (Dakou et al.), которая включена в данную заявку путем ссылки в полном объеме. Предпочтительно, амфифильный агент состоит в значительной степени из моно- и диглицеридов С8-С12 насыщенных жирных кислот и их смесей.
Композиции для перорального введения также могут быть составлены в форме водных суспензий, содержащих активный ингредиент в смеси с эксципиентами, приемлемыми для производства водных суспензий. Маслянистые суспензии могут быть составлены путем суспендирования активного ингредиента в приемлемом масле. Также могут применяться эмульсии типа масло-в-воде. Диспергируемые порошки и гранулы, приемлемые для получения водной суспензии путем добавления воды, обеспечивают активный ингредиент в смеси с диспергирующим или увлажняющим агентом, суспендирующим агентом и одним или более консервантами.
Активный ингредиент в соответствии с настоящим изобретением может быть введен в пероральный состав с продолжительным высвобождением. «Продолжительное высвобождение» относится к высвобождению активного агента из лекарственной формы со скоростью, эффективной для того, чтобы достичь терапевтическое количество агента или его активного метаболита, в большом круге кровообращения в течение длительного периода времени по сравнению с тем, которое достигается при пероральном введении общепринятого состава агента. Высвобождение агента происходит в течение продолжительного периода времени, например, в течение периода, по меньшей мере, 6 часов, в течение периода, по меньшей мере, 8 часов, в течение периода, по меньшей мере, 12 часов, или в течение периода, по меньшей мере, 24 часа.
Приемлемые составы для местного применения и лекарственные формы включают мази, кремы, гели, лосьоны, пасты и т.п., как описано в Remington: The Science and Practice of Pharmacy (21st Edition, University of the Sciences in Philadelphia, 2005). Мази представляют собой мягкие препараты, которые, как правило, основаны на вазелине или других продуктах переработки углеводородного сырья. Основа конкретной мази, которая используется, как будет понятно квалифицированным специалистам в данной области техники, представляет собой основу, которая будет обеспечивать оптимальную доставку лекарственного средства, и, предпочтительно, будет обеспечивать другие желаемые характеристики, в том числе, например, смягчение или т.п. Кремы представляют собой вязкие жидкости или мягкие эмульсии, или типа масло-в-воде или вода-в-масле. Основы крема являются такими, которые смываются водой, и содержат масляную фазу, эмульгатор и водную фазу. Масляная фаза, которая также называется «внутренней» фазой, как правило, состоит из вазелина и жирного спирта, такого как цетиловый или стеариловый спирт. Водная фаза, как правило, хотя и необязательно, превышает масляную фазу по объему, и, как правило, содержит увлажнитель. Эмульгатор в кремовом составе, как правило, представляет собой неионное, анионное, катионное или амфотерное поверхностно-активное вещество. Гели представляют собой мягкие системы суспензионного типа. Однофазные гели содержат органические макромолекулы (полимеры) распределенные, по существу, однородно по всему носителю-жидкости, который, как правило, является водным, но, также, предпочтительно, содержит спирт, такой как этанол или изопропанол, и, необязательно, масло. Для того, чтобы получить однородный гель, могут быть добавлены диспергирующие агенты, такие как спирт или глицерин, или гелеобразующий агент может быть диспергирован путем растирания, механического перемешивания или встряхивания, или их комбинаций. Лосьоны представляют собой препараты, которые должны наноситься на поверхность кожи без растирания, и, как правило, представляют собой жидкие или полужидкие препараты, в которых твердые частицы, включая активный агент, присутствуют в водной или спиртовой основе. Лосьоны, как правило, представляют собой суспензии высокодисперсных твердых веществ, и, как правило, будут содержать суспендирующие агенты для получения более подходящих дисперсий, а также соединений, приемлемых для локализации и удержания активного агента при контакте с кожей. Пасты представляют собой мягкие лекарственные формы, в которых активный агент суспендирован в приемлемой основе. В зависимости от природы основы, пасты делят на жирные пасты или те, которые получены из однофазных водных гелей.
Различные добавки, известные квалифицированным специалистам в данной области техники, могут быть включены в составы для местного применения. Например, растворители, включая относительно небольшие количества спирта, могут быть использованы для растворения определенных веществ лекарственного средства. Другие необязательные добавки включают замутнители, антиоксиданты, ароматизирующее вещество, краситель, гелеобразующие агенты, загущающие агенты, стабилизаторы, поверхностно-активные вещества и т.п. Также могут быть добавлены другие агенты, такие как противомикробные агенты, для предотвращения ухудшения качества при хранении, то есть, для ингибирования роста микробов, таких как дрожжевые грибы и плесневые грибы. Для таких лекарственных средств, которые имеют необычно низкую скорость проникновения через кожу или слизистую ткань, может быть желательным, чтобы в состав был включен усилитель проницаемости. Состав может также содержать уменьшающие раздражение добавки для минимизации или исключения возможности раздражения кожи или повреждения кожи в результате действия лекарственного средства, усилителя или других компонентов лекарственной формы. Составы также могут содержать эфирные физиологически приемлемые эксципиенты или другие незначительные добавки, такие как ароматизирующие вещества, красители, эмульгаторы, буферы, охлаждающие агенты (например, ментол), антибиотики, стабилизаторы или т.п. В некоторых случаях, один компонент может выполнять более, чем одну функцию.
Концентрация активного агента в составе для местного применения может изменяться в больших пределах и будет зависеть от различных факторов, включая заболевание или состояние, подлежащее лечению, природу и активность активного агента, желаемый эффект, возможные неблагоприятные реакции, способность и скорость активного агента достигать намеченной цели, и другие факторы в пределах конкретного знания пациента и врача. Составы, как правило, будут содержать ориентировочно приблизительно от 0,1 мас. % до 50 мас. % активного агента, предпочтительно приблизительно от 0,1 мас. % до 5 мас. % активного агента, оптимально приблизительно от 5 мас. % до 20 мас. % активного агента.
В некоторых вариантах осуществления, лекарственную форму серлопитанта для местного применения составляют как буккальную или сублингвальную таблетку или пилюлю. Преимущества буккальной или сублингвальной таблетки или пилюли включают предотвращение пресистемного метаболизма и обход желудочно-кишечной абсорбции. В дополнение к терапевтически эффективному количеству серлопитанта, буккальная или сублингвальная таблетка или пилюля может содержать приемлемые эксципиенты, включая, без ограничения любую комбинацию наполнителей и разбавителей (например, маннит и сорбит), связывающие агенты (например, карбонат натрия), увлажняющие агенты (например, карбонат натрия), дезинтегранты (например, кросповидон и кроскармеллозу натрия), смазывающие вещества (например, диоксид кремния [включая коллоидный диоксид кремния] и стеарилфумарат натрия), стабилизаторы (например, бикарбонат натрия), ароматизирующие агенты (например, мятный ароматизатор), подсластители (например, сукралозу) и окрашивающие агенты (например, желтый оксид железа). Буккальная или сублингвальная таблетка или пилюля, содержащая серлопитант, может быть использована для лечения, например, любого связанного с зудом состояния, описанного в данной заявке.
Фармацевтические композиции в соответствии с настоящим изобретением могут быть составлены как депо-состав для введения путем внутримышечной или подкожной инъекции. Депо-составы являются эффективными, хорошо переносимыми, продолжительного или замедленного высвобождения композициями активного ингредиента, которые являются терапевтически эффективными в течение нескольких недель, таких как, по меньшей мере, одна неделя, по меньшей мере, две недели, по меньшей мере, три недели, по меньшей мере, четыре недели, по меньшей мере, пять недель или, по меньшей мере, шесть недель или более. В дополнение к активному агенту, дополнительные ингредиенты могут быть использованы в депо-составах в соответствии с настоящим изобретением, включая поверхностно-активные вещества, солюбилизаторы, эмульгаторы, консерванты, изотонические агенты, диспергирующие агенты, увлажняющие агенты, наполнители, растворители, буферы, стабилизаторы, смазывающие вещества и загущающие агенты. Также может использоваться комбинация дополнительных ингредиентов. Количество активного ингредиента в депо-составе будет зависеть от степени тяжести зуда, подлежащего лечению.
Композиции в соответствии с настоящим изобретением могут быть представлены в единичной лекарственной форме и могут быть получены с помощью любого способа, хорошо известного в области фармации. Термин «единичная лекарственная форма» используется для обозначения единичной дозы, в которой все активные и неактивные ингредиенты объединены в приемлемую систему, таким образом, что пациент или индивидуум, вводящий лекарственное средство пациенту, может открыть один контейнер или упаковку со всей дозой, которая содержится в нем, и не должен смешивать какие-либо компоненты вместе из двух или больше контейнеров или упаковок. Типичные примеры единичных лекарственных форм представляют собой таблетки или капсулы для перорального введения. Данные примеры единичных лекарственных форм не предназначены для того, чтобы ограничить каким-либо образом, а исключительно для того, чтобы представить типичные примеры в области фармации единичных лекарственных форм.
Композиции в соответствии с настоящим изобретением также могут быть представлены в виде набора, в соответствии с которым два или более компонентов, которые могут быть активными или неактивными ингредиентами, носителями, разбавителями и т.п., обеспечиваются инструкциями для получения фактической лекарственной формы пациентом или индивидуумом, вводящим лекарственное средство пациенту. Такие наборы могут быть обеспечены всеми необходимыми веществами и ингредиентами, содержащимися в них, или они могут содержать инструкции по применению или получению веществ или компонентов, которые должны быть получены независимо пациентом или индивидуумом, вводящим лекарственное средство пациенту.
Композиции для местного применения, содержащие серлопитант
Составы для местного применения для нанесения на кожу или слизистую оболочку могут быть полезными для лечения состояний верхних слоев кожи или слизистой оболочки, и для трансдермального или трансмукозального введения активного агента в местную ткань, лежащую под кожей или слизистой оболочкой, и, если необходимо, в кровь для системного распределения. Преимущества местного введения могут включать предотвращение пресистемного метаболизма, обход желудочно-кишечной абсорбции, доставку активного агента с относительно коротким биологическим периодом полувыведения, более контролируемое высвобождение активного агента, введение более однородного плазменного дозирования активного агента и улучшение в соблюдении предписанного режима терапии пользователем.
В целом и в дополнение к раскрытию составов для местного применения, описанных где-либо еще в данной заявке, композиции приемлемые для местного введения включают без ограничения жидкие или полужидкие препараты, такие как спреи, гели, линименты, лосьоны, эмульсии типа масло-в-воде или вода-в-масле, такие как кремы, пены, мази и пасты, и растворы или суспензии, такие как капли (например, глазные капли, назальные капли и ушные капли). В некоторых вариантах осуществления, композиция для местного применения содержит активный агент, растворенный, диспергированный или суспендированный в носителе. Носитель может находиться в форме, например, раствора, суспензии, эмульсии, мазевой или гелевой основы, и может содержать, например, вазелин, ланолин, воск (например, пчелиный воск), минеральное масло, длинноцепочечный спирт, полиэтиленгликоль или полипропиленгликоль, разбавитель (например, воду и/или спирт [например, этанол или пропиленгликоль]), эмульгатор, стабилизатор или загущающий агент, или их комбинацию. Композиция для местного применения может включать, или состав для местного применения может вводиться с помощью, например, трансдермального пластыря, микроигольного пластыря или ионтофорезного устройства. Трансдермальный пластырь может содержать, например, микропористую мембрану, изготовленную из приемлемого материала (например, нитрата или ацетата целлюлозы, пропилена или поликарбоната), кожный адгезивный материал и материал основы. Композиция для местного применения может доставлять активный агент трансдермально (включая чрескожно и трансмукозально) с помощью градиента концентрации или активного механизма (например, ионосфер).
Репрезентативные виды композиций для местного применения описываются ниже с целью иллюстрации.
I. Композиции для местного применения, содержащие усилитель проницаемости
В некоторых вариантах осуществления, композиция для местного применения содержит серлопитант и усилитель проницаемости. Композиция необязательно может содержать дополнительный терапевтический агент. В определенных вариантах осуществления, композиция содержит серлопитант в виде свободного основания.
Усилитель проницаемости повышает проницаемость кожи или слизистой оболочки к терапевтическому агенту(ам). В определенных вариантах осуществления, усилитель проницаемости представляет собой N-лауроилсаркозин, октилсульфат натрия, метиллаурат, изопропилмиристат, олеиновую кислоту, глицерилолеат или лаурилсульфоацетат натрия, или их комбинацию. В определенных вариантах осуществления, композиция содержит по массе/объему (мас./об.) усилителя проницаемости в количестве приблизительно 1-20%, 1-15%, 1-10% или 1-5%. Для дальнейшего повышения способности терапевтического агента(ов) проникать в кожу или слизистую оболочку, композиция также может содержать поверхностно-активное вещество, азон-подобное соединение, спирт, жирную кислоту или сложный эфир, или алифатический тиол.
Композиция может дополнительно содержать один или более дополнительных эксципиентов. Приемлемые эксципиенты включают без ограничения солюбилизаторы (например, C2-C8 спирты), увлажняющие средства или увлажнители (например, глицерол [глицерин], пропиленгликоль, аминокислоты и их производные, полиаминокислоты и их производные, и пирролидоновые карбоновые кислоты и их соли и производные), поверхностно-активные вещества (например, лауретсульфат натрия и монолаурат сорбитана), эмульгаторы (например, цетиловый спирт и стеариновый спирт), загустители (например, метилцеллюлозу, этилцеллюлозу, гидроксиметилцеллюлозу, гидроксипропилцеллюлозу, поливинилпирролидон, поливиниловый спирт и акриловые полимеры), и основы или носители состава (например, полиэтиленгликоль как мазевую основу). В качестве неограничивающего примера, основа или носитель композиции может содержать этанол, пропиленгликоль и полиэтиленгликоль (например, ПЭГ 300), и необязательно водную жидкость (например, изотонический фосфатный буферный солевой раствор).
Композиция для местного применения может иметь любую приемлемую лекарственную форму, такую как раствор (например, глазные капли, назальные капли или ушные капли), суспензия, эмульсия, крем, лосьон, гель, мазь, паста, желе, пена, шампунь или спрей. В некоторых вариантах осуществления, композицию наносят на кожу или слизистую оболочку, покрывая площадь поверхности приблизительно 10-800 см2, 10-400 см2 или 10-200 см2. Композиция может доставлять терапевтический агент(ы) в кожу или слизистую оболочку, или нижележащую ткань. Композиция также может быть составлена для трансдермального введения терапевтического агента(ов) в большой круг кровообращения, например, в виде трансдермального пластыря или микроигольного пластыря.
II. Композиции для местного применения, содержащие усилитель проницаемости и летучую жидкость
В еще одних вариантах осуществления, композиция для местного применения содержит серлопитант, усилитель проницаемости и летучую жидкость. Композиция необязательно может содержать дополнительный терапевтический агент. В определенных вариантах осуществления, композиция содержит серлопитант в виде свободного основания.
Усилитель проницаемости повышает проницаемость кожи или слизистой оболочки к терапевтическому агенту(ам). В некоторых вариантах осуществления, усилитель проницаемости выбирают из группы, состоящей из C8-C18 алкиламинобензоатов (например, C8-C18 алкил-п-аминобензоатов), C8-C18 алкилдиметиламинобензоатов (например, C8-C18 алкил-п-диметиламинобензоатов), C8-C18 алкилциннаматов, C8-C18 алкилметоксициннаматов (например, C8-C18 алкил-п-метоксициннаматов) и C8-C18 алкилсалицилатов. В определенных вариантах осуществления, усилитель проницаемости представляет собой октилсалицилат, октил-п-диметиламинобензоат или октил-п-метоксициннамат, или их комбинацию.
Летучая жидкость может быть любым летучим, хорошо переносимым кожей или слизистой оболочкой растворителем. В определенных вариантах осуществления, летучая жидкость представляет собой С2-С5 спирт или его водный раствор, такой как этанол или изопропанол, или их водный раствор. Аэрозольный пропеллент (например, диметиловый эфир) может рассматриваться как летучая жидкость. В некоторых вариантах осуществления, летучая жидкость действует в качестве носителя или основы композиции.
Композиция необязательно может содержать загущающий агент. Неограничивающие примеры загущающих агентов включают целлюлозные загущающие агенты (например, этилцеллюлозу, гидроксипропилцеллюлозу и гидроксипропилметилцеллюлозу), повидон, полиакриловые кислоты/полиакрилаты (например, Carbopol® полимеры), Sepigel® (полиакриламид/изопарафин/лаурет-7) и Gantrez® серии сополимеров полиметилвинилового эфира/малеинового ангидрида (например, бутиловый сложный эфир PMV/MA сополимера Gantrez® А-425).
В некоторых вариантах осуществления, композиция содержит по массе приблизительно 0,5-10%, 0,5-5% или 1-5% серлопитанта, приблизительно 1-20%, 1-15% или 1-10%) усилителя проницаемости и приблизительно 40-98%, 45-95%, 50-90% или 60-80% летучей жидкости. В еще одних вариантах осуществления, композиция необязательно содержит по массе приблизительно 1-40%, 1-30%, 1-20% или 5-20% воды и/или приблизительно 0,1-15%, 0,5-10% или 1-5% загущающего агента.
Для целей иллюстрации, в определенных вариантах осуществления спреевая композиция для местного применения содержит приблизительно 0,5-5% мас./об. серлопитанта, приблизительно 2-10% мас./об. октилсалицилата или октил-п-метилоксициннамата, и приблизительно 95% водного этанола в качестве носителя. В еще одних вариантах осуществления, гелевая композиция для местного применения содержит приблизительно 0,5-5% мас./об. серлопитанта, приблизительно 1-10% мас./об. октилсалицилата или октил-п-метилоксициннамата, приблизительно 0,5-5% мас./об. Carbopol® полиакриловой кислоты и приблизительно 70% водного этанола в качестве носителя, и необязательно приблизительно 1-10% мас./об. основного раствора (например, 0,1 N NaOH). В дополнительных вариантах осуществления, лосьонная композиция для местного применения содержит приблизительно 0,5-5% мас./об. серлопитанта, приблизительно 1-10% мас./об. октилсалицилата или октил-п-метилоксициннамата, приблизительно 1-5% мас./об. этилцеллюлозы или гидроксипропилцеллюлозы и приблизительно 90% водного этанола в качестве носителя.
Композиция дополнительно может содержать другие эксципиенты, такие как соединяющий агент (например, парафиновое масло, силиконовое масло, растительное масло или сложный эфир жирной кислоты, такой как изопропилмиристат), разбавитель, сорастворитель (например, ацетон или гликолевый эфир, такой как диэтиленгликольмоноэтиловый эфир), эмульгатор, поверхностно-активное вещество (например, этоксилированный жирный спирт, глицеролмоностеарат или фосфатный сложный эфир), стабилизатор, антиоксидант или консервант (например, гидроксибензоатный сложный эфир), или их комбинацию. Например, сорастворитель и/или поверхностно-активное вещество могут использоваться для поддержания терапевтического агента(ов) в растворе или суспензии в требуемой концентрации.
Композиция для местного применения может иметь любую приемлемую лекарственную форму, такую как крем, лосьон, гель, мазь, мусс, спрей или аэрозоль, или любое трансдермальное устройство (например, пластырь), которое вводит лекарственное средство путем абсорбции через кожу или слизистую оболочку. В некоторых вариантах осуществления, композицию для местного применения наносят на кожу или слизистую оболочку, покрывая площадь поверхности приблизительно 10-800 см2, 10-400 см2 или 10-200 см2.
III. Композиции для местного применения, содержащие усилитель проницаемости и другой эксципиент
В еще одних вариантах осуществления, композиция для местного применения содержит серлопитант, усилитель проницаемости и, по меньшей мере, один липофильный растворитель, основу состава и загуститель. В некоторых вариантах осуществления, композиция содержит липофильный растворитель и основу состава, или одно и тоже вещество может действовать в качестве как липофильного растворителя, так и основы состава. В еще одних вариантах осуществления, композиция содержит липофильный растворитель, основу состава и загуститель. Композиция может, необязательно, содержать дополнительный терапевтический агент. В определенных вариантах осуществления, композиция содержит серлопитант в виде свободного основания.
Усилитель проницаемости повышает проницаемость кожи или слизистой оболочки к терапевтическому агенту(ам). Неограничивающие примеры усилителей проницаемости включают диметилсульфоксид (ДМСО), децилметилсульфоксид, лаурокапрам, пирролидоны (например, 2-пирролидон и N-метил-2-пирролидин), поверхностно-активные вещества, спирты (например, олеиловый спирт), полиэтиленгликоль (например, ПЭГ 400), диэтиленгликольмоноэтиловый эфир, олеиновую кислоту и сложные эфиры жирных кислот (например, изопропилмиристат, метиллаурат, глицеролмоноолеат и пропиленгликольмоноолеат).
Неограничивающие примеры липофильных растворителей включают липофильные спирты (например, гексиленгликоль, октилдодеканол, олеиловый спирт и стеариловый спирт), полиэтиленгликоль (например, ПЭГ 100, ПЭГ 300, ПЭГ 400 и ПЭГ 3350), диэтиленгликольмоноэтиловый эфир, полисорбаты (например, Tween® от 20 до 80), Labrasol®, сложные эфиры жирных кислот (например, изопропилмиристат и диизопропиладипат), диэтилсебацинат, пропиленгликоля монокаприлат, пропиленгликоля лаурат, моно- и диглицериды (например, Capmul® MCM), среднецепочечные триглицериды, каприловый/каприновый триглицерид, глицерилмонокаприлат, глицерилмоноолеат, глицерилмонолинолеат, глицерололеат/пропиленгликоль, минеральное масло и растительные масла.
Липофильный растворитель также может действовать в качестве основы состава или носителя. Например, полиэтиленгликоль (например, от ПЭГ 100 до ПЭГ 3500, такие как ПЭГ 300, ПЭГ 400 и ПЭГ 3350) может действовать в качестве липофильного растворителя и основы состава.
Композиция также может содержать гидрофильный растворитель, такой как C1-C5 спирт (например, этанол, изопропанол, глицерин, пропиленгликоль и 1,2-пентандиол) и/или вода.
Композиция может содержать загуститель, чтобы повысить вязкость и/или физическую стабильность композиции. Примеры загустителей включают без ограничения глицерин, стеариловый спирт и полимеры (например, полидиметилсилоксан [диметикон] и Carbopol® полимеры).
В некоторых вариантах осуществления, композиция дополнительно содержит антиоксидант.Неограничивающие примеры антиоксидантов включают бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), токоферолы (например, витамин Е и его сложные эфиры), флавиноиды, глутатион, аскорбиновую кислоту и ее сложные эфиры, ДМСО и хелатирующие агенты (например, ЭДТА и лимонную кислоту).
В определенных вариантах осуществления, композиция для местного применения содержит по мас./мас. приблизительно 0,5-10% или 1-5% серлопитанта, приблизительно 2-30%) или 5-20% усилителя проницаемости, приблизительно 20-80% или 30-70% липофильного растворителя, который также может действовать в качестве основы состава, приблизительно 0,1-10% или 1-7,5% загустителя и приблизительно 0,01-2% или 0,05-1% антиоксиданта. Как неограничивающий пример, композиция для местного применения может содержать серлопитант, ПЭГ 400 и/или ПЭГ 3350, как липофильный растворитель(и) и основу(ы) состава, диэтиленгликольмоноэтиловый эфир, олеиловый спирт и/или изопропилмиристат, как усилитель(и) проницаемости, стеариловый спирт, как загуститель, и ВНТ, как антиоксидант.
Композиция для местного применения может иметь любую приемлемую лекарственную форму, такую как крем, лосьон, гель, мазь, желе, паста или любое трансдермальное устройство (например, пластырь), которое вводит лекарственное средство путем абсорбции через кожу или слизистую оболочку.
IV. Композиции для местного применения, содержащие усилитель проницаемости и адгезив
В дополнительных вариантах осуществления, композиция для местного применения содержит серлопитант, усилитель проницаемости и адгезив. Композиция необязательно может содержать дополнительный терапевтический агент. В определенных вариантах осуществления, композиция содержит серлопитант в виде свободного основания.
Усилитель проницаемости повышает проницаемость кожи или слизистой оболочки к терапевтическому агенту(ам). Усилитель проницаемости может представлять собой, например, сложный эфир жирных кислот, имеющий жирную ацильную цепь длиной C8-C20 или C12-C18 и C1-C6 или C2-C4 спиртовый компонент (например, изопропанол). В определенных вариантах осуществления, усилитель проницаемости представляет собой изопропилмиристат или изопропилпальмитат. В некоторых вариантах осуществления, усилитель проницаемости находится в количестве приблизительно 0,1-20%, 0,5-15%, 1-15%, 2-12% или 4-10% по массе композиции или контактирующего с кожей слоя трансдермального пластыря.
Адгезив поддерживает контакт композиции для местного применения с кожей или слизистой оболочкой. Неограничивающие примеры адгезивов включают акриловые смолы/акрилаты (например, полиакрилаты, включая полиалкилакрилаты и Duro-Tak® полиакрилаты), поливинилацетат, этиленвинилацетатные сополимеры, полисилоксаны, полиуретаны, пластифицированные полиэфирные блок-амидные сополимеры, природные и синтетические куачуки, пластифицированные стирол-бутадиеновые каучуковые блок-сополимеры (например, Duro-Tak® 87-6173) и их смеси.
Композиция для местного применения может содержать один или более дополнительных эксципиентов. Дополнительный эксципиент(ы) может представлять собой, например, разбавитель, смягчающее средство, пластификатор или агент, который уменьшает раздражение кожи или слизистой оболочки, или их комбинацию.
В определенных вариантах осуществления, композиция для местного применения перед нанесением на кожу или слизистую оболочку является по существу свободной от воды, тетрагликоля (гликофурола) и/или гидрофильного органического растворителя (например, C1-C5 спирта).
Композиция может вводить терапевтический агент(ы) трансдермально (включая чрескожно и трансмукозально) через поверхность тела или мембраны, такие как неповрежденная здоровая кожа или неповрежденная здоровая ткань слизистой оболочки в большой круг кровообращения.
В некоторых вариантах осуществления, композиция для местного применения находится в форме трансдермального пластыря для нанесения на кожу или слизистую оболочку. Пластырь имеет контактирующий с кожей или слизистой оболочкой слой («контактирующий с кожей слой» для простоты), ламинированный или иным образом прикрепленный к слою-подложке. Контактирующий с кожей слой может быть покрыт удаляемым перед использованием защитным покрытием, чтобы защитить контактирующую с кожей поверхность и сохранить ее чистой до тех пор, пока ее не нанесут на кожу или слизистую оболочку.
Слой-подложка пластыря действует как подложка для контактирующего с кожей слоя и как барьер, который предотвращает потерю терапевтического агента(ов) в контактирующем с кожей слое в окружающую среду. Материал слоя-подложки является совместимым с терапевтическим агентом(ами), усилителем проницаемости и адгезивом, и является минимально проницаемым для компонентов пластыря. Слой-подложка может быть непрозрачным, чтобы защитить компоненты пластыря от разложения посредством воздействия ультрафиолетового света. Слой-подложка также способен связываться с и поддерживать слой адгеза, еще является достаточно пластичным, для того, чтобы приспосабливаться к движениям субъекта, который использует пластырь. Материал слоя-подложки может представлять собой, например, металлическую фольгу, металлизированную полифольгу или композитную фольгу или пленку, содержащую полимер (например, сложный полиэфир [такой как сложный полиэфирный терефталат] или алюминизированный сложный полиэфир, полиэтилен, полипропилен, политетрафторэтилен, полиэтиленметилметакрилатный блок-сополимер, полиэфирный блок-амидный сополимер, полиуретан, поливинилиден хлорид, нейлон, силиконовый эластомер, полиизобутилен на основе каучука, стирол, или стирол-бутадиеновый или стирол-изопреновый сополимер). Защитное покрытие может быть выполнено из того же материала, что и слой-подложка, или может быть пленкой, покрытой соответствующей высводождающей поверхностью.
Зуд
Зуд является физиологическим восприятием в пределах сенсорной нейронной сети в коже, которая, наряду с болью и физическими или механическими стимулами, может служить в качестве системы предупреждения против возможных угроз организму. Чесотка является неприятным ощущением, которое может привести к чесанию, но не зависит от боли. Международная федерация по изучению чесотки (IFSI) определяет хронический зуд (в отличие от острого зуда) как чесотку, которая имеет продолжительность шесть недель или дольше (S.  et al., Acta Derm. Venereol., 2007, 87(4): 291-4). Несколько факторов в и на коже могут активировать сенсорные нервные волокна или модулировать их активность и, таким образом, вызывать, подавлять или усугублять чесотку. Физические стимулы, такие как холод и тепло, модулируют восприятие чесотки; причиняющее боль тепло и холод могут значительно ее уменьшать, в то время как умеренный холод усиливает ее (Valet et al., J. Invest. Dermatol., 2008, 128(2): 426-33.). Механические факторы, такие как трение или чесание кожи, коротко говоря, могут подавлять чесотку путем активирования нервных волокон, которые селективно активируют и деактивируют определенные участки мозга (Yosipovitch et al., J. Invest. Dermatol, 2008, 128(7): 1806-11).
et al., Acta Derm. Venereol., 2007, 87(4): 291-4). Несколько факторов в и на коже могут активировать сенсорные нервные волокна или модулировать их активность и, таким образом, вызывать, подавлять или усугублять чесотку. Физические стимулы, такие как холод и тепло, модулируют восприятие чесотки; причиняющее боль тепло и холод могут значительно ее уменьшать, в то время как умеренный холод усиливает ее (Valet et al., J. Invest. Dermatol., 2008, 128(2): 426-33.). Механические факторы, такие как трение или чесание кожи, коротко говоря, могут подавлять чесотку путем активирования нервных волокон, которые селективно активируют и деактивируют определенные участки мозга (Yosipovitch et al., J. Invest. Dermatol, 2008, 128(7): 1806-11).
Хронический зуд может серьезно ухудшит качество жизни у тех, кто от него страдает, поскольку он может быть труднопреодолимым и инвалидизирующим. Он является серьезным изнурительным состоянием, сравнимым с хронической болью, которое может привести к растройству, отчаянию и депрессии. Кроме того, хроническое чесание часто приводит к открытым повреждениям кожи, склонным к первичному или вторичному инфицированию, рубцеванию и потенциальному обезображиванию. Хронический зуд часто является признаком первопричинного заболевания и всегда присутствует при заболеваниях, таких как крапивница и атопический дерматит. Диагностирование первопричинного заболевания является необходимым и клиническое проявление, история болезни пациента и самоанализ пациента формируют важные части такого диагностирования.
В соответствии с руководствами Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) (Ассоциация научных медицинских обществ Германии), заболевания и расстройства с хроническим зудом, как симптомом, могут быть классифицированы по тому, является ли кожа воспаленной или невоспаленной (S.  , Clin. Exp. Dermatol., 2006, 31(6):762-7). Кроме того, IFSI характеризует зуд как дерматологический, системный, нейрогенный, психогенный, смешанный и другой. Хронических зуд на невоспаленной коже может быть результатом дерматологических заболеваний, в том числе атопического диатеза, астеатоза, порфирии, субуртикарных стадий солнечной травмы, холинергической, адренергической крапивницы, начальной стадии мастоцитоза, буллезного пемфигоида и болезни Дюринга (герпетиформного дерматита); эндокринных и метаболических расстройств, таких как хроническая почечная недостаточность и диализ, необходимый для ее лечения, гепатопатии с холестазом, сахарный диабет, растройства мальабсорбции, анорексия, глютеновая энтеропатия, гипертиреоз, гипотиреоз, гиперпаратиреоз и перименопаузальный зуд; инфекций, включая ВИЧ-инфекцию, паразитные, Helicobacter pylori и связанную с гельминтами; гематологических и лимфопролиферативных заболеваний, таких как дефицит железа, истинная полицитемия, синдром гиперэозинофилии, миелодиспластический синдром, болезнь Ходжкина, неходжкинская лимфома, плазмоцитома и системный мастоцитоз; твердых злокачественных опухолей, включая рак шейки матки, молочной железы, предстательной железы или толстого кишечника, и карциноидные опухоли; неврологических расстройств, таких как плечелучевой зуд, парестетическая боль в спине, невралгия после опоясывающего лишия, вульводиния, невропатии различного происхождения, рассеянный склероз, опухоли, абсцессы, при перфузии, инфаркты, включающие ЦНС/спинномозговой столб; психогенных расстройств, таких как депрессия, шизофрения и тактильные галлюцинации; и внутрипеченочного холестаза у беременных (зуд беременных).
, Clin. Exp. Dermatol., 2006, 31(6):762-7). Кроме того, IFSI характеризует зуд как дерматологический, системный, нейрогенный, психогенный, смешанный и другой. Хронических зуд на невоспаленной коже может быть результатом дерматологических заболеваний, в том числе атопического диатеза, астеатоза, порфирии, субуртикарных стадий солнечной травмы, холинергической, адренергической крапивницы, начальной стадии мастоцитоза, буллезного пемфигоида и болезни Дюринга (герпетиформного дерматита); эндокринных и метаболических расстройств, таких как хроническая почечная недостаточность и диализ, необходимый для ее лечения, гепатопатии с холестазом, сахарный диабет, растройства мальабсорбции, анорексия, глютеновая энтеропатия, гипертиреоз, гипотиреоз, гиперпаратиреоз и перименопаузальный зуд; инфекций, включая ВИЧ-инфекцию, паразитные, Helicobacter pylori и связанную с гельминтами; гематологических и лимфопролиферативных заболеваний, таких как дефицит железа, истинная полицитемия, синдром гиперэозинофилии, миелодиспластический синдром, болезнь Ходжкина, неходжкинская лимфома, плазмоцитома и системный мастоцитоз; твердых злокачественных опухолей, включая рак шейки матки, молочной железы, предстательной железы или толстого кишечника, и карциноидные опухоли; неврологических расстройств, таких как плечелучевой зуд, парестетическая боль в спине, невралгия после опоясывающего лишия, вульводиния, невропатии различного происхождения, рассеянный склероз, опухоли, абсцессы, при перфузии, инфаркты, включающие ЦНС/спинномозговой столб; психогенных расстройств, таких как депрессия, шизофрения и тактильные галлюцинации; и внутрипеченочного холестаза у беременных (зуд беременных).
Хронический зуд на воспаленной коже может наблюдаться у пациентов с воспалительным заболеванием кожи, включая, но не ограничиваясь приведенным, атопический дерматит, аллергический, раздражающий контактный дерматит, дерматит высушивания, монетоподобный и дисгидротический дерматит, красный плоский лишай, склеротический атрофический лишай, полиморфный фотодерматозный псориаз, болезнь Гровера, муциноз, мастоцитоз и крапивница; инфекционными заболеваниями кожи, такими как микозы, бактериальные и вирусные инфекции, чесотка, педикулез, укусы насекомых и фолликулит; аутоиммунными заболеваниями кожи, в том числе буллезными кожными растройствами, в частности герпетиформным дерматитом (болезнью Дюринга) и буллезным пемфигоидом; генодерматозами, такими как болезнь Дарье и болезнь Хейли-Хейли; кожными заболеваниями связанными с беременностью, включая полиморфный дерматоз беременных (PEP, ранее известный как PUPPP), атопический дерматоз беременных и пемфигоид беременных; и новообразованиями, такими как кожная Т-клеточная лимфома (в частности эритродермическая форма).
Узловатый пруриго (PN), или узелковый пруриго, является особенно тяжелой формой хронической чесотки, который может лечиться с помощью способов и композиций в соответствии с настоящим изобретением. Характеризуемый зудящими, экскориированными, лихенированными папулами и узелками, PN может возникнуть в любом возрасте, но наиболее часто обнаруживается у пациентов среднего и пожилого возраста на их руках и ногах (Е. Weisshaar and S.  , Acta Derm. Venereol., 2012, 92:532-533). Этиология PN неизвестна, но он, как правило, возникает у пациентов с личной или семейной историей атопического дерматита, и часто с сопутствующими медицинскими состояниями, такими как печеночная или почечная функция, местная травма или повреждение кожи, инфекция и ВИЧ или другие иммунодефицита. PN в результате может привести к постоянным изменениям кожи, в том числе узелковой лихенификации, гиперкератозу, гиперпигментации и утолщению кожи.
, Acta Derm. Venereol., 2012, 92:532-533). Этиология PN неизвестна, но он, как правило, возникает у пациентов с личной или семейной историей атопического дерматита, и часто с сопутствующими медицинскими состояниями, такими как печеночная или почечная функция, местная травма или повреждение кожи, инфекция и ВИЧ или другие иммунодефицита. PN в результате может привести к постоянным изменениям кожи, в том числе узелковой лихенификации, гиперкератозу, гиперпигментации и утолщению кожи.
Комбинированные терапии с серлопитантом и другими противозудными агентами
Серлопитант, самостоятельно или в комбинации с одним или более дополнительными противозудными агентами, может быть использован для лечения зуда (включая острый и хронический зуд), связанный с любым состоянием. Ощущение чесотки может возникать, например, в периферической нервной системе (например, кожная или нейропатическая чесотка) или в центральной нервной системе (например, нейропатическая, нейрогенная или психогенная чесотка).
Примеры связанных с зудом состояний, включают без ограничения те, которые описаны в другом месте в данной заявке и следующие:
дерматологические расстройства и состояния (в том числе воспалительные и невоспалительные состояния кожи), включая, но не ограничиваясь приведенным, блашкит у взрослых, амилоидозы (например, первичный кожный амилоидоз [включая макулярный амилоидоз, узелковый амилоидоз и узловой амилоидоз]), ожоги (например, химические ожоги и солнечные ожоги), дерматит {например, атопический дерматит, контактный дерматит (в том числе аллергический контактный дерматит, контактный дерматит вследствие раздражения и фотодерматит), экзему (например, аутосенсибилизационный дерматит, герпетиформный дерматит [болезнь Дюринга], дискоидную экзему, дисгидроз [водяницу], экзему рук, ауточувствительный дерматит [генерализованную экзему], монетоподобную экзему, статический дерматит [гравитационную экзему], венозную экзему и ксеротическую экзему), гнойничковый дерматит (например, эозинофильный гнойничковый фолликулит [болезнь Офуджи], реактивный артрит [болезнь Рейтера] и субкорнеальный пустулезный дерматоз [болезнь Снеддона-Уилкинсона]), и себорейный дерматит (например, детский себорейный дерматит, болезнь Лейнера и питириаз простой волосянистый [перхоть])}, эритродермию (эксфолиативный дерматит), фолликулит, псевдофолликулит зоны роста бороды (псевдофолликулит волос бороды), гнойный гидраденит, ихтиозы (например, ихтиоз обыкновенный, врожденный ихтиоз, эпидермолитический гиперкератоз и пластинчатый ихтиоз), красный плоский лишай (например, кожный красный плоский лишай и оральный красный плоский лишай), склероатрофический лишай (например, склеротический атрофический лишай вульвы), простой лишай (например, простой хронический лишай [нейродерматит]), линеарный IgA буллезный дерматоз (линеарный IgA дерматоз), эритематозную волчанку (например, кожную эритематозную волчанку, дискоидную эритематозную волчанку и системную эритематозную волчанку), потницу (потовую сыпь), ладонно-подошвенную кератодермию (например, точечную ладонно-подошвенную кератодермию), питириаз (например, асбестовидный лишай, лихеноидный парапсориаз [включая хронический лихеноидный парапсориаз и острый лихеноидный и вариолиформный парапсориаз], розовый питириаз, красный волосистый питириаз [болезнь Девержи] и разноцветный питириаз), пруриго (например, солнечный пруриго, пруриго Бенье, узловатый пруриго, пруриго пигментарный и пруриго простой), анальный зуд, зуд мошонки, зуд вульвы, псориаз (например, эритродермический псориаз, каплевидный псориаз [сопровождающийся сыпью псориаз], псориаз обыкновенный [хронический стационарный псориаз], гнойничковых псориаз и ладонно-подошвенный пустулез), парапсориаз (например, большой бляшковидный парапсориаз и малый бляшковидный парапсориаз [хронический поверхностный дерматит]), зудящее пятно (зудящие точки), высыпания (например, опрелость и периоральный дерматит), розовые угри, крапивницу (например, контактную крапивницу [включая сыпь] и идиопатическую крапивницу), витилиго, ксероз (сухую кожу), потрескавшуюся кожу (например, потрескавшиеся ноги), зуд волосистой части головы, заживление под струпом, развитие шрама, и развитие невоидных опухолей, прыщи и вросшие волосы;
медицинские расстройства и состояния (включая периферийные и системные расстройства), включая, но не ограничиваясь приведенным, атопический диатез, аутоиммунные расстройства (например, глютеиновую болезнь, дерматомиозит, болезнь Грейвса, пемфигоид [например, буллезный пемфигоид], склеродермию и синдром Шегрена), заболевания крови (например, анемию [например, железодефицитную анемию и серповидно-клеточную анемию], гиперкальцемию, миелодиспластические синдромы и полицитемию [например, истинную полицитемию]), болезнь Крейтцфельда-Якоба (например, прионов зуд), сахарный диабет, генетические заболевания (например, синдром Алажиля, болезнь Дарье, буллезный эпидермолиз, болезнь Хейли-Хейли и синдром Шегрена-Ларссона), болезнь Гровера, ВИЧ/СПИД, заболевания почек (например, диабетическую нефропатию, гломерулонефрит, хроническое заболевание почек, болезни терминальной стадии заболевания почек и хроническую почечную недостаточность), уремию (например, уремический зуд [почечный зуд]), заболевания печени (например, цирроз печени [например, первичный билиарный цирроз печени], гепатит [включая гепатит А, В, С, D и Е и их хронические состояния] и печеночную недостаточность), холестаз (например, холестатический зуд), желтуху (например, желчный зуд), лимфаденопатию (например, увеличенные лимфатические узлы), заболевания тучных клеток (например, синдром активации тучных клеток и мастоцитоз), рассеянный склероз, невропатии (например, периферическую невропатию [например, плечелучевой зуд, парестезическую боль в спине, полинейропатию и периферическую невропатию мелких волокон]), нервное раздражение, защемление нервов, расстройства паращитовидной железы (например, гиперпаратиреоз и гипопаратиреоз), расстройства щитовидной железы (например, гипертиреоз, гипотиреоз и микседему), инсульт, рак {например, карциноидный синдром, лейкоз (например, поражение кожи при лейкозе и лимфолейкоз), лимфомы (например, болезнь Ходжкина и неходжкинские лимфомы [например, кожную В-клеточную лимфому и кожную Т-клеточную лимфому (включая грибовидный микоз и синдром Сезари)]), саркому Капоши, множественную миелому и рак кожи}, опухоли (например, опухоль головного мозга, плазмоцитому и твердые опухоли шейки матки, толстой кишки и предстательной железы), паранеопластический зуд, психические расстройства (например, стресс, тревожные расстройства, галлюцинаторный бред, депрессию, обсессивно-компульсивные расстройства [например, невротические экскориации], и тактильные галлюцинации), старение (например, сенильный зуд) и изменения в гормональных равновесиях, связанные со старением (например, перименопаузу и менопаузу);
инфекции и инвазии, включая, но не ограничиваясь приведенным, синдром Свиммерса (чесотка Свиммерса), укусы и ужаления насекомых (например, муравьев, пчел, клещей, блох, вшей [включая нательных вшей, головных вшей и лобковых вшей], клещей, комаров, пауков, иксодовых клещей и ос), чесотку, бактериальные инфекции (например, абсцесс, гангренозный дерматит, эктиму, эритразму, импетиго и болезнь Лайма), грибковые инфекции (например, кандидоз, дерматофитоз, дерматомикоз гладкой кожи [стригущий лишай тела], паховый дерматомикоз [паховую эпидермофитию] и грибковое заболевание ног [эпидермофитию стопы]), вирусные инфекции {например, герпес (включая опоясывающий герпес [опоясывающий лишай] и постгерпетический зуд), корь, парвовирусные инфекции (например, парвовирус B19), ветряную оспу (ветрянку) и желтую лихорадку}, и гельминтные инфекции {например, гельминты (например, гельминтоз [заражение глистами]), нематоды (например, кожные ларвальные личиночные гельминтозы), гельминты Onchocerca (например, онхоцеркоз [речная слепота]), острицы, аскариды (например, филяриоз и трихинеллез) и гельминты Schistosoma (например, шистосомоз)};
реакции на аллергены и раздражители, включая, но не ограничиваясь приведенным, аллергический ринит (например, поллиноз [включая сенную лихорадку]), астму, аллергены животных (например, перхоть кошки и перхоть собаки), химические аллергены (например, кислоты [например, абиетиновую кислоту и сорбиновую кислоту], косметику, моющие средства, красители, смягчители тканей, фунгициды, гидроксиэтилкрахмал и латекс), пищевые аллергены (например, молочные белки, арахис, лесные орехи, морепродукты, специи, консерванты [например, нитраты], витамины [например, витамины А и В], спирт, кофеин и глутамат мононатрия), аллергены металлов и солей металлов (например, хром, кобальт, золото и никель, и их соли), растительные аллергены (например, бальзам Перу и урушиол [например, в яде плюща, яде дуба и яде сумах]), химические раздражители (например, кислоты, щелочи, смазочно-охлаждающие жидкости, растворители, поверхностно-активные вещества, моющие средства, мыла, чистящие средства, косметику, парфюмерию, дезодоранты, антиперспиранты, пищевые ароматизаторы, специи, консерванты [например, формальдегид и парабены], мономеры и полимеры [например, акриловые смолы, эпоксидные смолы, этиленоксид, латекс и лаки], и масла [например, керосин]), ткани (например, шерсть), растительные раздражители (например, алкилрезорцины [например, в Grevillea banksii, Grevillea «Robyn Gordon» и Gingko biloba]), и физические раздражители (например, воду [например, аквадынию и аквагенный зуд), низкую влажность от кондиционирования воздуха и холодную температуру);
зуд, вызванный лекарственными средствами/медикаментами, включая, но не ограничиваясь приведенным, хлорохин, гидроксиэтилцеллюлозу, гидроксиэтилкрахмал, ингибиторы ангиотензинконвертирующего фермента, ингибиторы ксантиноксидазы (например, аллопуринол), антибиотики (изониазид, неомицин, пенициллин, сульфаниламиды и ванкомицин), противогрибковые средства (например, флуконазол, гризеофульвин, итраконазол и кетоконазол), нейролептики/антипсихотические средства (например, фенотиазины), антиаритмические лекарственные средства (например, амиодарон и хинидин), химиотерапевтические лекарственные средства, мочегонные лекарственные средства (например, гидрохлортиазид), статины (например, симвастатин), и лекарственные средства (например, опиоиды), которые активируют рецептор гистамина H1 или вызывают высвобождение гистамина; и
состояния, связанные с беременностью, включая, но не ограничиваясь приведенным, гестационный пемфигоид, импетиго герпетиформный, внутрипеченочный холестаз беременных (зуд беременных), полиморфный дерматоз беременных, пруриго беременных, зудящий фолликулит беременных и зудящие уртикарные папулы и бляшки беременных.
Один или более дополнительних противозудных агентов необязательно могут быть использованы в комбинации с серлопитантом для лечения зуда (включая острый и хронический зуд). Примеры противозудных агентов включают без ограничения:
антигистаминные средства, включая, но не ограничиваясь приведенным, антигистаминные средства, которые ингибируют действие рецептора гистамина H1 (например, акривастин, антазолин, азеластин, биластин, бромфенирамин, буклизин, бромдифенгидрамин, карбиноксамин, цетиризин, хлорпромазин, циклизин, хлорфенирамин, хлордифенгидрамин, клемастин, ципрогептадин, дезлоратадин, дексбромфенирамин, дексхлорфенирамин, дименгидринат, диметинден, дифенгидрамин, доксепин, доксиламин, эбастин, эмбрамин, фексофенадин, гидроксизин, левоцетиризин, лоратадин, меклозин, мепирамин, миртазапин, олопатадин, орфенадрин, фениндамин, фенирамин, фенилтолоксамин, прометазин, пириламин, кветиапин, рупатадин, трипеленнамин и трипролидин), и антигистаминные средства, которые ингибируют действие рецептора гистамина H4 (например, тиоперамид, JNJ 7777120 и VUF-6002), и их аналоги и производные;
антагонисты рецептора серотонина, включая, но не ограничиваясь приведенным, антагонисты 5-HT2 (например, клозапин, ципрогептадин, кетансерин, пизотифен и кветиапин) и антагонисты 5-НТ3 (например, алосетрон, силансетрон, доласетрон, гранисетрон, ондансетрон, палоносетрон и трописетрон), и их аналоги и производные;
антагонисты рецептора нейрокинина-1 (NK-1), включая, но не ограничиваясь приведенным, апрепитант, касопитант (GW679769), дапитант, эзлопитант, фосапрепитант, ланепитант (LY-303870), маропитант, нетупитант, нолпитант, орвепитант, ролапитант, вестипитант, вофопитант, AV-818, BIIF 1149CL, СР122,721, DNK-333, GSK-424887, L-733060, L-759274, LY-686017, М516102 и ТА-5538, и их аналоги и производные;
антагонисты опиоидных рецепторов, включая, но не ограничиваясь приведенным, буторфанол, ципродим, леваллорфан (лорфан или налоксифан), нальбуфин, налорфин (летидрон или наллин), налоксон, налоксол, налмефен, налтрексон (например, налтрексон 1% крем) и налтрексол, и их аналоги и производные;
агонисты опиоидных рецепторов, включая, но не ограничиваясь приведенным, селективные агонисты каппа опиоидных рецепторов (например, асимадолин, бремазоцин, динорфин, энадолин, кетазоцин, налфурафин, сальвинорин А, 2-метоксиметилсальвинорин В, 2-этоксиметилсальвинорин В, 2-фторэтоксиметилсальвинорин В, спирадолин, тифлуадом, BRL-52537, FE 200665, GR-89696, HZ-2, ICI-199,441, ICI-204,448, LPK-26, U-50488 и U-69,593), и их аналоги и производные;
ингибиторы Янус-киназы (JAK), включая, но не ограничиваясь приведенным, ингибиторы JAK1 (например, GLPG0634 и GSK2586184), ингибиторы JAK2 (например, лестауртиниб, пакритиниб, CYT387 и TG101348), ингибиторы JAK1/JAK2 (например, бариситиниб и руксолитиниб) и ингибиторы JAK3 (например, тофаситиниб), и их аналоги и производные;
иммуномодуляторы и иммунодепрессанты, включая но не ограничиваясь приведенным, талидомид, антиметаболиты (например, антифолаты, такие как метотрексат), и ингибиторы кальциневрина (например, циклоспорин [циклоспорин], пимекролимус и такролимус), и их аналоги и производные;
антидепрессанты, включая, но не ограничиваясь приведенным, трициклические антидепрессанты (например, амитриптилин, амитриптилиноксид, амоксапин, досулепин [дотиепин], доксепин и мелитрацен), тетрациклические антидепрессанты (например, амоксапин, мапротилин, мазиндол, миансерин, миртазапин и сетиптилин), селективные ингибиторы обратного захвата серотонина (SSRI, например, циталопрам, дапоксетин, эсциталопрам, флуоксетин, флувоксамин, пароксетин и сертралин), и ингибиторы обратного захвата серотонина-норэпинефрина (SNRI, например, бицифадин, дулоксетин, милнаципран, левомилнаципран, сибутрамин, венлафаксин, дезвенлафаксин и SEP-227162), и их аналоги и производные;
противосудорожные средства, включая, но не ограничиваясь приведенным, карбамазепин, габапентин, прегабалин и вальпроевую кислоту и ее соли (например, вальпроат натрия), и их аналоги и производные;
кортикостероиды, включая, но не ограничиваясь приведенным, типы гидрокортизона (например, кортизон и его производные [например, кортизона ацетат], гидрокортизон и его производные [например, гидрокортизона ацетат, гидрокортизона-17-ацепонат, гидрокортизона-17-бутепрат, гидрокортизона-17-бутират и гидрокортизона-17-валерат], преднизолон, метилпреднизолон и его производные [например, метилпреднизолона ацепонат], преднизон и тиксокортол и его производные [например, тиксокортола пивалат]), типы бетаметазона (например, бетаметазон и его производные [например, бетаметазона дипропионат, бетаметазона натрия фосфат и бетаметазона валерат], дексаметазон и его производные [например, дексаметазона натрия фосфат], и флуокортолон и его производные [например, флуокортолона капроат и флуокортолона пивалат]), галогенированные стероиды (например, алклометазон и его производные [например, алклометазона дипропионат], беклометазон и его производные [например, беклометазона дипропионат], клобетазол и его производные [например, клобетазола-17-пропионат], клобетазон и его производные [например, клобетазона-17-бутират], дезоксиметазон и его производные [например, дезоксиметазона ацетат], дифлоразон и его производные [например, дифлоразона диацетат], дифлукортолон и его производные [например, дифлукортолона валерат], флупредниден и его производные [например, флупреднидена ацетат], флутиказон и его производные [например, флутиказона пропионат], галобетазол [улобетазол] и его производные [например, галобетазола пропионат], галометазон и его производные [например, галометазона ацетат], и мометазон и его производные [например, мометазона фуроат]), ацетониды и родственные вещества (например, амцинонид, будесонид, циклесонид, дезонид, флуоцинонид, флуоцинолона ацетонид, флурандренолид [флурандренолон или флудроксикортид], гальцинонид, триамцинолона ацетонид и триамцинолон-спирт), и карбонаты (например, предникарбат), и их аналоги и производные;
местные анестетики, включая, но не ограничиваясь приведенным, амиды (например, артикаин, бупивакаин, цинхокаин [дибукаин], этидокаин, левобупивакаин, лидокаин [например, лидокаин 2,5-5% крем], прилокаин [например, прилокаин 2,5% крем], EMLA [лидокаин 2,5%/прилокаин 2,5% крем], мепивакаин, ропивакаин и тримекаин), сложные эфиры (например, бензокаин, хлорпрокаин, кокаин, циклометикаин, диметокаин [ларокаин], пиперокаин, прокаин [новокаин], пропаракаин, пропоксикаин, стоваин и тетракаин [аметокаин]), эфиры (например, полидоканол [например, полидоканол 3% пена] и прамокаин [прамоксин] [например, прамоксин 1% крем]), и местные анестетики природного происхождения (например, кокаин, эвгенол, ментол, сакситоксин, неосакситоксин и тетродотоксин), и их аналоги и производные;
противораздражающие и охлаждающие агенты, включая, но не ограничиваясь приведенным, капсаицин, камфору, масло мяты, ментол (например, ментол 1-3% крем) и фенол (например, в жидкости от солнечных ожогов), и их аналоги и производные;
увлажняющие средства, включая, но не ограничиваясь приведенным, водные увлажняющие средства, увлажняющие средства с низким pH, содержащие кислоту (например, молочную кислоту), и увлажняющие средства, содержащие увлажнитель, который притягивает и удерживает воду (например, глицерин, сорбит, лактат, мочевину и гиалуроновую кислоту и ее соли), окклюзионный агент, который предотвращает испарение {например, масла (например, минеральное масло и силиконовое масло [например, диметикон]) и вазелиновое масло (вазелин)}, и/или смягчающее средство, которое обеспечивает частичную гидратацию и окклюзию (например, масла, воски [например, ланолин и парафин], липиды [например, фосфолипиды, керамиды, триглицериды, гликольстеарат, глицерилстеарат, жирные кислоты и сквален], и стеролы [например, холестерин и фитостерол]), и их аналоги и производные; и
другие виды противозудных агентов, включая, но не ограничиваясь приведенным, S-аденозилметионин, ботулотоксин (например, ботулотоксин типов А и В), витамин D и его аналоги и производные (например, кальцитриол и кальципотриол [кальципотриен]), нестероидные противовоспалительные лекарственные средства (НПВЛС, например, аспирин), агонисты каннабиноидного рецептора (например, агонисты CB2, такие как пальмитоилэтаноламид), ингибиторы цитокинов (например, антитела к интерлейкинам, такие как IL-31), антагонисты простагландинового рецептора D2 (DP1) и/или хемоаттрактантного рецептора гомологичного молекуле, которая экспрессируется на TH2 клетках (CRTH2) (например, TS-022), ингибиторы фосфодиэстеразы (PDE) (например, ингибиторы PDE4, такие как апремиласт), антагонисты активированного протеазой рецептора 2 (PAR2) (например, GB83), антагонисты переходного потенциального ванилоидного рецептора (TRPV) (например, TRPV1 антагонисты, такие как капсазепин и SB-705498), ингибиторы нейротрофических тирозинкиназных рецепторов (например, ингибиторы TrkA, такие как СТ327), противомикробные средства (включая антибиотики, противогрибковые средства, противовирусные средства и противопаразитарные средства, такие как кротамитон и рифампин [рифампицин]), восстанавливающие абсорбцию желчи или изолирующие желчь агенты (например, урсодезоксихолевую кислоту [урсодиол]), ультрафиолетовое излучение (например, ультрафиолет А и В), и терапевтические агенты, которые лечат первопричины связанных с зудом состояний, и их аналоги и производные.
При необходимости (например, для облегчения зуда в течение дня), может быть использован неседативный противозудный агент. Например, антигистаминные средства второго поколения и третьего поколения разрабатываются неседативными, или менее седативными, чем антигистаминные средства первого поколения. Неограничивающие примеры антигистаминных средств второго поколения и третьего поколения включают акривастин, астемизол, азеластин, бепотастин, биластин, цетиризин, левоцетиризин, эбастин, фексофенадин, кетотифен, левокабастин, лоратадин, дезлоратадин, мизоластин, олопатадин, хифенадин, рупатадин и терфенадин.
В некоторых вариантах осуществления, кортикостероид умеренной или средней активности используется в комбинации с серлопитантом для лечения связанного с зудом состояния. Примеры кортикостероидов, имеющих умеренную или среднюю активность включают кортикостероиды группы III, IV и V по системе классификации США из 7-групп и кортикостероиды класса II по Европейской системе классификации из 4-классов, включая без ограничения амцинонид 0,1% (например, крем), бетаметазона дипропионат 0,05% (например, Diprosone® крем/мазь), бетаметазона валерат 0,1% (например, крем/мазь), клобетазона бутират 0,05% (например, Eumovate® крем), дезонид 0,05% (например, Tridesilon® крем/мазь и DesOwen® крем/мазь), флуоцинолона ацетонид 0,01-0,2% (например, Synalar® крем/мазь и Synemol® крем), флурандренолид 0,05% (например, Cordran® лента), флутиказона пропионат 0,005% (например, Cutivate® мазь), флутиказона пропионат 0,05% (например, Cutivate® крем), галометазон 0,05% (например, крем), гидрокортизона бутират 0,1% (например, Locoid® крем/мазь), гидрокортизона валерат 0,2% (например, Westcort® крем/мазь), мометазона фуроат 0,1% (например, Elocon® крем/мазь), триамцинолона ацетонид 0,025-0,5% (например, Aristocort® крем/мазь, Kenacomb® крем/мазь, Kenalog® крем и Viaderm® КС крем/мазь) и триамцинолона диацетат 0,5% (например, крем/мазь).
Необязательный дополнительный противозудный агент(ы) может быть введен субъекту, страдающему от зуда, одновременно с (например, в той же композиции, что и серлопитант, или в отдельных композициях) или последовательно с (до или после) введением серлопитанта. Серлопитант и необязательный дополнительный противозудный агент(ы) независимо могут быть введены любым приемлемым способом, в том числе, без ограничения перорально, местно (например, дермально/накожно, трансдермально, мукозально, трансмукозапьно, интраназально [например, в виде назального спрея или капель], офтальмологично [например, в виде глазных капель], пульмонально [например, в виде ингаляции], буккально, сублингвально, ректально и вагинально), путем инъекции или инфузии (например, парентерально, включая внутримышечно, подкожно, внутрикожно, внутривенно/внутрисосудисто и интратекально), и путем имплантации (например, подкожно и внутримышечно). В некоторых вариантах осуществления, противозудный агент вводят местно (например, дермально), если зуд локализован, и вводят системно (например, перорально или внутривенно), если зуд обширный (генерализованный) или имеет системную причину. В определенных вариантах осуществления, серлопитант и/или необязательный дополнительный противозудный агент(ы) вводят перорально. В других вариантах осуществления, серлопитант и/или необязательный дополнительный противозудный агент(ы) вводят местно (например, дермально, муккозально, буккально или сублингвально).
Серлопитант и необязательный дополнительный противозудный агент(ы) независимо могут быть введены с любой приемлемой частотой, в том числе, без ограничения каждый день (один, два, три или более раз в день), один раз в два дня, два раза в неделю, три раза в неделю, еженедельно, один раз в две недели, один раз в три недели, ежемесячно, один раз в два месяца и один раз в три месяца. Частота дозирования может зависеть, например, от выбранного способа введения. Например, дермальный состав серлопитанта и/или того необязательного дополнительного противозудного агента(ов), может наноситься на кожу субъекта два, три или четыре раза в день. В некоторых вариантах осуществления, серлопитант вводят при длительном режиме дозирования. В определенных вариантах осуществления, серлопитант вводят в течение периода, по меньшей мере, 2 недели, 3 недели, 1 месяц, 1,5 месяца, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев или дольше.
Примеры лекарственных форм для местного применения включают без ограничения кремы, мази, гели, линименты, лосьоны, суппозитории (например, ректальные и вагинальные суппозитории), буккальные и сублингвальные таблетки и пилюли, спреи (например, дермальные и назальные спреи) и капли (например, глазные, назальные и ушные капли). Неограничивающие примеры пероральных лекарственных форм включают твердые лекарственные формы (например, саше, капсулы и таблетки) и жидкие лекарственные формы (например, растворы или суспензии в водной жидкости и/или неводной жидкости, и жидкие эмульсии типа масло-в-воде или жидкие эмульсии типа вода-в-масле). В неограничивающем примере состава для инъекций, состав находится в форме раствора и содержит противозудный агент (например, местный анестетик), основу (например, водную основу или стерильную воду), буфер, восстанавливающий агент/антиоксидант (например, метабисульфит натрия, если в качестве вазоконстриктора используют эпинефрин) и консервант (например, метилпарабен), и необязательно вазоконстриктор (например, эпинефрин), чтобы увеличить продолжительность фармакологического эффекта противозудного агента путем сужения кровеносных сосудов, тем самым концентрируя противозудный агент для увеличенной продолжительности и повышая максимальную дозу противозудного агента.
В таблице 4 представлены неограничивающие примеры комбинированных терапий, применяющих серлопитант и один или более дополнительных противозудных агентов для лечения зуда, связанного с различными состояниями. Таблица 4 также может показать другие терапевтические агенты, используемые для лечения первопричины состояний.



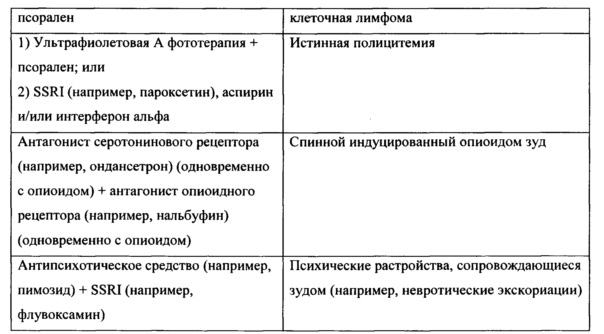
Применение серлопитанта в качестве способствующего сну средства
Настоящее изобретение также охватывает применение серлопитанта в качестве способствующего сну средства. Соответственно, настоящее изобретение предусматривает способ способствования сну, который включает стадию, на которой вводят субъекту, страдающему от проблем со сном или расстройства сна, эффективное количество серлопитанта или его фармацевтически приемлемой соли, сольвата или полиморфа. Также субъекту необязательно могут вводить дополнительный способствующий сну агент.
Серлопитант может способствовать сну у субъектов, которые, как правило, страдают от расстройства сна или проблемы со сном. В качестве способствующего сну средства, серлопитант может иметь седативный эффект (снижение раздражительности, беспокойства или волнения) и/или снотворный эффект (индукцию, поддержание и/или удлинение сна).
Примеры расстройств сна, которые серлопитант потенциально может облегчить, включают без ограничения бессонницу (включая первичную и вторичную бессонницу, и переходную, острую и хроническую бессонницу); сонную болезнь (африканский трипаносомоз); расстройства циркадного ритма сна (например, расстройство досрочной фазы сна [ASPD], расстройство запоздалой фазы сна [DSPD], нерегулярный ритм сна и бодрствования, расстройство не 24 часового сна и бодрствования, расстройство смены часовых поясов и сдвиг сна и работы [SWSD]); парасомнии (например, бруксизм, расстройство поведения сна с быстрым движением глаз [RBD], расстройство периодического движения конечностей [PLMD или ночной миоклонус], синдром беспокойных ног [RLS], паралич сна, синдром «взрывающейся головы», ужасы во время сна [ночной кошмар или ночные страхи], никтурию, синдром ночного питания, разговор во время сна [сомнилоквию], лунатизм [сомнамбулизм] и сомнифобию); и связанные со сном расстройства дыхания (например, апноэ во время сна [включая центральное, обструктивное и смешанное апноэ во время сна], синдром гипопноэ, связанная со сном гиповентиляция, храп и синдром сопротивления верхних дыхательных путей).
Для применения в качестве способствующего сну средства, серлопитант вводят, когда субъект желает спать (например, на ночь или приблизительно в то время, когда ложатся спать). Эффективное количество серлопитанта вводят для того, чтобы способствовать сну. Эффективное количество может зависеть от различных факторов, включая способ введения; возраст, массу тела, общее состояние здоровья, пол и диету субъекта; тяжесть проблемы со сном; и ответ субъекта на лечение. В определенных вариантах осуществления, доза серлопитанта как способствующего сну средства составляет приблизительно 0,1-500 мг, или приблизительно 0,25-400 мг, или приблизительно 0,5-300 мг, или приблизительно 1-200 мг, или приблизительно 2,5-100 мг, или приблизительно 5-50 мг, или как считает нужным лечащий врач. Единичная доза или несколько доз серлопитанта могут быть введены для того, чтобы способствовать сну. В еще одних вариантах осуществления, дозировка серлопитанта для того, чтобы способствовать сну, составляет приблизительно 0,01-10 мг/кг, 0,025-7,5 мг/кг, 0,05-5 мг/кг, 0,075-2,5 мг/кг или 0,1-1 мг/кг массы тела, или как считает нужным лечащий врач.
Серлопитант может быть введен любым приемлемым способом. Возможные способы введения серлопитанта включают без ограничения пероральный, парентеральный (включая внутримышечный, подкожный, внутрикожный, внутривенный, внутриартериальный, внутрикостномозговой и интратекальный), внутрибрюшинный и местный (включая дермальный/накожный, трансдермальный, мукозальный, трансмукозальный, интраназальный [например, в виде назального спрея или капель], внутриглазной [например, в виде глазных капель], пульмональный [например, в виде ингаляции], буккальный, сублингвальный, ректальный и вагинальный). В определенных вариантах осуществления, серлопитант вводят перорально.
В других вариантах осуществления, серлопитант вводят местно, применяя буккальную или сублингвальную таблетку или пилюлю. Буккальная или сублингвальная таблетка или пилюля может быть разработана для обеспечения более быстрого высвобождения серлопитанта для более быстрого захвата его в большой круг кровообращения. Кроме терапевтически эффективного количества серлопитанта, буккальная или сублингвальная таблетка или пилюля может содержать приемлемые эксципиенты, включая без ограничения любую комбинацию наполнителей и разбавителей (например, маннит и сорбит), связывающие агенты (например, карбонат натрия), увлажняющие агенты (например, карбонат натрия), дезинтегранты (например, кросповидон и кроскармеллозу натрия), смазывающие вещества (например, диоксид кремния [включая коллоидный диоксид кремния] и стеарилфумарат натрия), стабилизаторы (например, бикарбонат натрия), ароматизирующие агенты (например, мятный ароматизатор), подсластители (например, сукралозу) и окрашивающие агенты (например, желтый оксид железа). Неограничивающий пример группы пациентов, на которую может оказывать благоприятное действие буккальная или сублингвальная таблетка или пилюля способствующего сну средства представляет собой пациентов, которые просыпаются рано и имеют трудности с засыпанием снова.
В некоторых вариантах осуществления, (один или более) дополнительный способствующий сну агент вводят в комбинации с серлопитантом, чтобы способствовать сну. Дополнительный способствующий сну агент могут вводить одновременно с или последовательно с (до или после) введением серлопитанта. Если введен одновременно с серлопитантом, дополнительный способствующий сну агент может содержаться в той же композиции, что и серлопитант, или в отдельных композициях. Применение серлопитанта может уменьшить дозировку и/или длительность лечения дополнительным способствующим сну агентом, который, в противном случае, должен был бы требоваться, и, тем самым, минимизировать или избежать каких-либо неблагоприятных эффектов (например, зависимости или привыкания) дополнительного способствующего сну агента.
Дополнительный способствующий сну агент может быть выбран из-за его снотворного свойства или из-за его способности лечить расстройство сна или первопричину расстройства сна (например, стресс, тревогу, депрессию или неврологическое заболевание). В некоторых вариантах осуществления, дополнительный способствующий сну агент выбирают из группы, состоящей из снотворных средств, седативных средств, транквилизаторов, нейролептиков и антидепрессантов. Конкретный способствующий сну агент может иметь фармакологические эффекты, которые подпадают под несколько категорий (например, бензодиазепины могут иметь седативное или анксиолитическое действие в более низкой дозе и снотворное действие в более высокой дозе). В еще одних вариантах осуществления, дополнительный способствующий сну агент выбирают из группы, которая состоит из:
антидепрессантов, включая трициклические антидепрессанты (например, амитриптилин, амитриптилиноксид, амоксапин, кломипрамин, дезипрамин, досулепин [дотиепин], доксепин, имипрамин, лофепрамин, мелитрацен, нортриптилин, протриптилин и тримипрамин), тетрациклические антидепрессанты (например, амоксапин, мапротилин, мазиндол, миансерин, миртазапин и сетиптилин), селективные ингибиторы обратного захвата серотонина (SSRI, например, циталопрам, дапоксетин, эсциталопрам, флуоксетин, флувоксамин, пароксетин и сертралин), антагонист и ингибиторы обратного захвата серотонина (SARI, например, этоперидон, лорпипразол, лубазодон, мепипразол, нефазодон и тразодон), ингибиторы обратного захвата серотонина-норэпинефрина (SNRI, например, бицифадин, дулоксетин, милнаципран, левомилнаципран, сибутрамин, венлафаксин, дезвенлафаксин и SEP-227162), и ингибиторы моноаминоксидазы (МАО) (включая селективные ингибиторы МАО-А, такие как моклобемид, пирлиндол [пиразидол] и толоксатон [хуморил]), и их аналоги и производные;
антипсихотических средств, включая антипсихотические средства первого поколения (или типичные) (включая фенотиазины [например, хлорпромазин, флуфеназин, левомепромазин, перазин, перициазин, перфеназин, пипотиазин, прохлорперазин, промазин, прометазин, тиопроперазин, тиоридазин и трифлуоперазин] и тиоксантены [например, клопентиксол, зуклопентиксол, флупентиксол и тиотиксен]) и антипсихотические средства второго поколения (или нетипичные) (например, амисульприд, арипипразол, азенапин, клозапин, илоперидон, локсапин, амоксапин, луразидон, оланзапин, кветиапин, норкветиапин, рисперидон, палиперидон, сертиндол, тримипрамин, зипразидон и зотепин), и их аналоги и производные;
антигистаминных средств, которые ингибируют действие рецептора гистамина H1, включая антигистаминные средства первого поколения, такие как алимемазин (тримепразин), антазолин, азатадин, бромазин, карбиноксамин, хлорпромазин, клемастин, клоцинизин, циклизин, хлорциклизин, ципрогептадин, дименгидринат, диметинден, дифенгидрамин, бромодифенгидрамин, хлородифенгидрамин, доксиламин, гидроксизин, меклизин, мепирамин [пириламин], метдилазин, оксатомид, фениндамин, фенирамин, бромфенирамин, хлорфенирамин, фторфенирамин, орфенадрин, фенилтолоксамин, прометазин, трипеленнамин и трипролидин, и их аналоги и производные;
бензодиазепинов, которые усиливают эффект гамма-аминомасляной кислоты (ГАМК) в рецепторе ГАМКА путем положительной аллостерической модуляции рецептора, таких как адиназолам, алпразолам, хлордиазепоксид, климазолам, клоназепам, клоразепат, диазепам, эстазолам, этизолам (бензодиазепиновый аналог), флунитразепам, флуразепам, галазепам, лопразолам, лоразепам, лорметазепам, мидазолам, ниметазепам, нитразепам, оксазепам, празепам, квазепам, темазепам и триазолам, и их аналоги и производные;
небензодиазепинов (также называемых Z-лекарственные средства), которые являются положительными аллостерическими модуляторами рецептора ГАМКА, таких как бета-карболины (например, абекарнил, гедокарнил и ZK-93423), циклопирролоны (например, пагоклон, пазинаклон, супроклон, суриклон, зопиклон и эсзопиклон), имидазопиридины (например, алпидем, некопидем, сарипидем и золпидем), пиразолопиримидины (например, диваплон, фасиплон, индиплон, лоредиплон, оцинаплон, панадиплон, таниплон и залеплон) и триазолопиридазины (например, CL-218,872), и их аналоги и производные;
барбитуратов, которые являются положительными аллостерическими модуляторами рецептора ГАМКА, таких как аллобарбитал, амобарбитал, апробарбитал, алфенал, барбитал, браллобарбитал, бутабарбитал, мефобарбитал, пентобарбитал, фенобарбитал, секобарбитал и натрия тиопентал, и их аналоги и производные;
аналогов ГАМК, таких как габапентин и прегабалин, и их аналоги и производные;
агонистов мелатонинового рецептора (например, MT1 и/или МТ2), таких как мелатонин, агомелатин, LY-156,735, пиромелатин, рамелтеон и тасимелтеон, и их аналоги и производные;
антагонистов орексинового рецептора (например, OX1 и/или ОХ2), таких как альморексант, суворексант, SB-334,867, SB-408,124, SB-649,868, TCS-OX2-29 и N-этил-2-[(6-метоксипиридин-3-ил)-(толуол-2-сульфонил)амино]-N-пиридин-3-илметилацетамид (ЕМРА), и их аналоги и производные;
4-хиназолинонов, таких как афлоквалон, клороквалон, дипроквалон, этаквалон, меброквалон, меклоквалон, метаквалон, метилметаквалон и нитрометаквалон, и их аналоги и производные;
опиоидов (например, при расстройствах сна, связанных с болью), таких как бупренорфин, кодеин, фентанил, гидрокодон, гидроморфон, леворфанол, метадон, морфин, этилморфин, оксикодон, оксиморфон, петидин, пропоксифен, декстропропоксифен, тебаин и трамадол, и их аналоги и производные;
трав, таких как Cannabis (включая каннабиноиды, такие как каннабидиол [CBD] и тетрагидроканнабинол [ТНС]), Duboisia hopwoodii (кустарник), Hamulus lupulus (хмель обыкновенный), Hypericum perforatum (зверобой), Lactuca virosa (опиумный салат), Lavandula (лаванда), Matricaria chamomilla (ромашка), Nepeta cataria (кошачья мята), Passiflora (страстоцвет) (например, P. incarnata), Piper methysticum (кава), Prostanthera striatiflora (переполосный мятный куст), Sceletium tortuosum (канна), Scutellaria (шлемник) (например, S. canescens, S. cordifolia, S. galericulata и S. lateriflora), Valeriana officinalis (валериана) и Withania somnifera (ашвагандха); и
других видов веществ, таких как S-аденозил-L-гомоцистеин, L-триптофан, L-аргинин-L-аспартат, индуцирующий сон дельта пептид (DSIP), хлоральгидрат, этанол, 2-метил-2-бутанол, гамма-гидроксимасляная кислота (GHB), глютетимид, медетомидин, дексмедетомидин, ментилизовалерат (валидол), S32212, α2 адренергические агонисты (например, клонидин), и ингибиторы карбоангидразы (например, ацетазоламид и топирамат), и их аналоги и производные.
Дополнительный способствующий сну агент также может быть выбран из-за его способность лечить состояние, которое является одной из причин трудностей со сном (например, аномальное телесное движение или поведение). Например, противосудорожное средство может быть использовано в комбинации с серлопитантом для лечения парасомнии, такой как синдром беспокойных ног, расстройство периодических движений конечностей или синдромом ночного питания. Примеры противосудорожных средств включают без ограничения карбамазепин, габапентин, прегабалин, вальпроевую кислоту и ее соли (например, вальпроат натрия), и их аналоги и производные.
Дополнительный способствующий сну агент могут вводить любым приемлемым способом. В определенных вариантах осуществления, дополнительный способствующий сну агент вводят перорально, буккально или сублингвально.
Терапевтическое введение и дозы
Следует понимать, что термины «введение» или «вводить» соединение означают предоставление соединения в соответствии с настоящим изобретением индивидууму, который нуждается в лечении, в форме, которая может быть введена в организм индивидуумов в терапевтически приемлемой форме и терапевтически эффективном количестве, включая, но не ограничиваясь приведенным, пероральные лекарственные формы, такие как таблетки, капсулы, сиропы, суспензии и т.п.
Термины «лечить», «лечащий» и «лечение» хронического зуда все касаются уменьшения частоты симптомов острого или хронического зуда (включая устранение их полностью), предотвращения возникновения острого или хронического зуда, и/или уменьшения тяжести симптомов острого или хронического зуда.
Термин «терапевтически эффективное количество» относится к достаточному количеству соединений в соответствии с настоящим изобретением, в приемлемой композиции, и в приемлемой лекарственной форме для лечения указанных болезненных состояний. «Терапевтически эффективное количество» будет изменяться в зависимости от соединения, тяжести состояния, которое вызывает зуд, и возраста, массы, и т.д. пациента, подлежащего лечению.
Термин «насыщающая доза» относится к количеству соединений или композиций в соответствии с настоящим изобретением, которое часто превышает последующие дозы, вводимое с целью установления терапевтического уровня лекарственного средства. В более общем смысле, насыщающая доза представляет собой количество соединения I, или его фармацевтически приемлемой соли, сольвата или полиморфа, которое вводят пациенту с зудом, которое дается иногда после проявления, но перед введением одной или более поддерживающих доз. Альтернативно, насыщающая доза относится к одной или сериям доз, которые могут даваться в начале терапии для быстрого достижения целевой концентрации активного ингредиента.
Представленные способы лечения зуда требуют введения серлопитанта, или фармацевтической композиции, содержащей серлопитант, пациенту, который нуждается в таком лечении. Соединение и/или фармацевтические композиции предпочтительно вводятся перорально. Известны различные системы доставки (например, инкапсулирование в липосомы, микрочастицы, микрокапсулы, капсулы и т.п.), которые могут быть использованы для введения соединения и/или композиции серлопитанта. Соединение и/или фармацевтические композиции могут быть доставлены с помощью лекарственных форм с продолжительным высвобождением.
Количество серлопитанта, его фармацевтически приемлемой соли, сольвата или полиморфа, которое должно быть эффективным в лечении зуда у пациента, будет зависеть от конкретного характера состояния, и может быть определено согласно стандартным клиническим методикам, известным в данной области с уровня техники. Кроме того, in vitro или in vivo анализы могут необязательно использоваться, чтобы помочь идентифицировать оптимальные диапазоны дозирования. Конкретный уровень дозы для какого-либо конкретного индивидуума будет зависеть от множества факторов, включая активность композиции, возраст, массу тела, общее физическое и психическое здоровье, генетические факторы, влияния окружающей среды, пол, диету, время введения, способ введения, скорость выведения, и тяжесть зуда, подлежащего лечению.
Предпочтительно, лекарственные формы адаптируются для введения пациенту три, два или один раз в день. Более предпочтительно, терапевтически эффективное количество принимается один раз в день. Альтернативно, доза может приниматься через день, один раз в три дня, один раз в четыре дня или один раз в неделю. В некоторых вариантах осуществления, серлопитант вводят при длительном режиме дозирования. В определенных вариантах осуществления, терапевтически эффективное количество серлопитанта вводят в течение периода, по меньшей мере, 2 недели, 3 недели, 1 месяц, 1,5 месяца, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев или дольше.
Дозы могут приниматься в любое время, удобное для пациента. Тем не менее, чтобы свести к минимуму побочные эффекты, такие как головокружение или сонливость, суточная доза может быть принята перед сном. Показано, что антагонисты рецептора NK-1 вызывают сонливость у человека в клинических испытаниях по использованию, отличному от лечения зуда. Например, Ratti et al. сообщали, что у пациентов, которых лечили касопитантом большое депрессивное расстройство, в двое увеличивалась заболеваемость сонливостью, по сравнению с плацебо (J. Clin. Psychopharmacol., 2011, 31:727-733). Сонливость, кроме того, рассматривалась в аналогичном клиническом испытании по тестированию антагониста рецептора NK-1 L-759274, как антидепрессанта (М. S. Kramer et al., Neuropsychopharm., 2004, 29:385-392). Таким образом, в одном варианте осуществления настоящего изобретения, серлопитант вводят перед тем, как пациент ложится спать.
Дозирование может быть предусмотрено отдельно или в комбинации с другими лекарственными средствами и может продолжаться до тех пор, пока требуется для эффективного лечения зуда. Например, соединения в соответствии с настоящим изобретением могут вводиться в комбинации с другим веществом, которое имеет комплиментарный эффект к тахикинину и ингибирующий эффект к веществу Р в соответствии с настоящим изобретением. Соответствующие соединения включают другие антагонисты рецептора NK-1, такие как, но не ограничиваясь приведенным, касопитант (GW679769), L-759274, L-733060, CP 122,721, BIIF 1149CL, DNK333, М516102, эзлопитант, ролапитант, орвепитант, LY-686017, ланепитант (LY-303870), маропитант, вестипитант, вофопитант, апрепитант, фосапрепитант, AV-818 и ТА-5538.
Диапазоны дозировок соединений в соответствии с настоящим изобретением для перорального введения могут быть установлены по отношению к количеству лекарственного средства, введенного за определенный период времени. Определенное количество активного ингредиента может даваться один или более раз в день по мере необходимости в соответствии с факторами, описанными выше. Например, дозы могут приниматься один раз в день, два раза в день, три раза в день, четыре раза в день или более. Приемлемые диапазоны дозировок составляют от приблизительно 0,1 мг до приблизительно 30 мг, и предпочтительно, от приблизительно 1 мг до приблизительно 7,5 мг. Приемлемые дозировки, как правило, составляют 0,10 мг, 0,15 мг, 0,20 мг, 0,25 мг, 0,5 мг, 0,75 мг, 1 мг, 2 мг, 2,5 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 15 мг, 20 мг, 25 мг, 30 мг, 35 мг, 40 мг, 50 мг, 100 мг или 200 мг один или более раз в день. Предпочтительно, дозу 0,25 мг, 1 мг или 5 мг вводят один раз в день.
Альтернативно, приемлемые диапазоны дозировок соединений в соответствии с настоящим изобретением для перорального введения, как правило, составляют от приблизительно 0,001 мг до приблизительно 500 мг лекарственного средства на килограмм массы тела, предпочтительно от приблизительно 0,1 мг до приблизительно 200 мг лекарственного средства на килограмм массы тела, и более предпочтительно от приблизительно 1 до приблизительно 100 мг/кг массы тела в день. Диапазоны дозировок могут быть легко определены способами, известными квалифицированному специалисту в данной области техники. Количество активного ингредиента, которое может быть, например, объединено с веществами носителя для получения единичной лекарственной формы, будет изменяться в зависимости от пациента, котого лечат, и конкретного способа введения. Единичные лекарственные формы, как правило, будут содержать от приблизительно 0,25 мг до приблизительно 500 мг активного ингредиента.
В тех случаях, в которых желательным является долгосрочное сохранение эффекта активного лекарственного средства, например, но не ограничиваясь приведенным, при лечении хронического зуда, используется схема дозирования, в которой вводится насыщающая доза, с последующим введением или (i) второй насыщающей дозы, или доз, и поддерживающей дозы (или доз), или (ii) поддерживающей дозы или доз, без второй насыщающей дозы, как определяется при назначении квалифицированным специалистом в данной области техники. Схема введения насыщающих и поддерживающих доз может быть определена на основе индивидуальных требований конкретного пациента. В одном варианте осуществления настоящего изобретения, вводят одну насыщающую дозу с последующим введением терапевтически эффективной поддерживающей дозы через соответствующий промежуток времени, такой как через один день. В другом варианте осуществления, насыщающую дозу вводят на день 1, вторую насыщающую дозу на день 2 и поддерживающую дозу вводят на день 3 и после этого в течение всего срока терапии. Насыщающая доза можеть быть в пять, четыре, три или два раза больше поддерживающей дозы. Предпочтительно, насыщающая доза представляет собой трехкратную поддерживающую дозу. Активное лекарственное средство может вводиться любым приемлемым способом (например, перорально).
Определение терапевтической эффективности
Эффективность композиций в соответствии с настоящим изобретением может быть исследована на экспериментальных моделях зуда на животных, известных квалифицированным специалистам в данной области техники. Например, различные мышиные модели были использованы для оценки лечения для чесотки. Tsukumo et al. описывают модель, в которой 4-этоксиметилен-2-фенил-2-оксазолин-5-он (оксазолон) индуцирует хронический дерматит с ассоциированным ответом в виде чесотки у BALB/c мышей, которая может быть использована, чтобы определить является ли эффективным лечение зуда (J. Pharmacol. Sci., 2010, 113:255-262). Costa et al. сообщают об аналогичной модели, в которой яд паука Phoneutria nigriventer используется как индуктор чесотки (Vascul. Pharmacol., 2006, 45(4):209-14). Аналогично, Ohmura et al. используют пикрилхлорид на мышах NC/Nga, чтобы стимулировать поведение чесания (Eur. J. Pharmacol., 2004; 491:191-194). В значительной степени, у субъекта-животного индуцируется чесотка раздражающим агентом, вводится тестовое соединение или плацебо, и животное наблюдается в контролируемых условиях. Поведение чесания определяют количественно и анализируют, используя стандартные статистические методы. Тестовое соединение считается эффективным, если подавляется или постоянное, или сильное чесание.
Эффективность способов и композиций в соответствии с настоящим изобретением в лечении острого и хронического зуда также необязательно может быть оценена в клинических испытаниях людей, проводимых согласно соответствующему руководству по стандартам и этическим нормам, как представлено в Администрации США по пищевым продуктам и лекарственным веществам (FDA). После того, как определяется общая безопасность лекарственного средства в фазе I клинических испытаний, проведенных на здоровых добровольцах, проводят фазу II испытаний, оценивающую безопасность и эффективность лекарственного средства у пациентов с состоянием, которое подлежит лечению. Как правило, такие испытания являються двойными слепыми и плацебо-контролируемыми, и могут определять диапазоны дозировки. Исследование фазы III собирает больше информации о безопасности и эффективности при исследовании различных групп и различных дозировок, и с использованием лекарственного средства в комбинации с другими лекарственными средствами.
Поскольку облегчение зуда является субъективным собственным восприятием пациента, может быть трудным оценить его типичными клиническими конечными точками. Однако, были созданы и могут быть использованы в клинических испытаниях два стандартизованных инструмента оценки, демонстрирующих полезность настоящего изобретения. Визуальная аналоговая шкала (VAS) является наиболее общепринятым используемым инструментом для оценки интенсивности зуда (N. Q. Phan et al., Acta Derm. Venereol., 2012; 92:502-507). VAS представляет собой графический инструмент со 100-мм горизонтальной линией, с левого конца которой надписано «нет симптомов» и с правого конца надписано «худший вообразимый симптом». Пациента просят нарисовать вертикальную линию, чтобы указать на горизонтальной шкале точку, которая соответствует интенсивности симптома. Длина от левого конца до вертикальной отметки, сделанной пациентом, измеряется в миллиметрах. Отклонение в одну сотую считается достаточно чувствительным (R.С. Aitken, Proc. R. Soc. Med., 1969, 62:989-993). Результаты могут быть проанализированы с использованием стандартных статистических методов, известных квалифицированным специалистам в данной области техники.
В дополнение к VAS, индекс качества жизни при заболеваниях кожи (DLQI) может быть использован для оценки эффективности лечения хронического зуда. DLQI, сам по себе введенный в опросный лист общего качества жизни при заболеваниях кожи, был первоначально разработан и опубликован в дерматологической клинике в Университетской больнице Уэльса (A.Y. Finlay and G.К. Khan, Clin. Exper. Derm., 1994,19:210-216). Независимые исследования подтвердили, что DLQI является простым и эффективным способом для оценки качества жизни у пациентов с заболеваниями кожи (Н. В. Hahn et al., J. Am. Acad. Dermatol., 2001, 45(l):44-8). Текущая версия простого, утвержденного вопросника из десяти вопросов с инструкциями по использованию и оцениванию доступна от School of Medicine, Cardiff University, Wales, UK (world wide web URL dermatology.org.uk/quality/).
Следующие примеры предлагаются в качестве иллюстрации, а не в качестве ограничения.
ПРИМЕРЫ
Все неактивные фармацевтические ингредиенты в примерах ниже соответствуют требованиям United States Pharmacopeia и The National Formulary и тестируются и высвобождаются в соответствии с монографией для каждого ингредиента, заявленного в USP/NF компендиуме.
Пример 1. Получение таблеток серлопитанта
Серлопитант, 3-[(3aR,4R,5S,7aS)-5-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси]-4-(4-фторфенил)-1,3,3а,4,5,6,7,7а-октагидроизоиндол-2-ил]циклопент-2-ен-1-он, соединение 1, может быть составлен в форме таблетки для перорального применения. Таблица 1 показывает качественную/количественную композицию иллюстративных дозирований. Незначительные вариации в количествах эксципиентов (+/-10%) могут происходить во время процесса разработки лекарственного средства.


Таблетку, содержащую действующего вещества 0,25, 1 и 5 мг, получают в форме состава прессованной таблетки. Способ производства таблетки является одинаковым для всех предлагаемых содержаний действующего вещества. Способ состоит из следующих стадий, на которых: 1) смешивают соединение 1, маннит и лаурилсульфат натрия; 2) оставшийся маннит добавляют в смеситель и перемешивают; 3) микрокристаллическую целлюлозу, кроскармеллозу натрия и коллоидный диоксид кремния добавляют в смеситель, содержащий указанную выше смесь, чтобы завершить смешивание, и смесь деагломерируют, если это необходимо; 4) смесь смазывают стеаратом магния, который был предварительно просеян, если это необходимо; 5) смазанную смесь уплотняют валиком и измельчают, и затем смазывают стеаратом магния, который был предварительно просеян, если это необходимо; и 6) смесь затем прессуют в таблетки соответствующей массы.
Пример 2. Получение капсул серлопитанта
Серлопитант (соединение 1) также может поставляться в клиннику в форме наполненных жидкостью капсул. Таблица 2 показывает качественный/количественный состав иллюстративных дозировок. Незначительные вариации в количествах эксципиентов (+/-10%) могут происходить во время процесса разработки лекарственного средства.
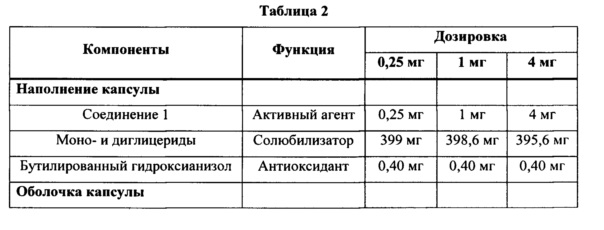
Состав получают путем растворения лекарственного вещества в моно- и диглицеридах. Кроме того, 0,1 мас. % бутилированного гидроксианизола добавляют в качестве антиоксиданта. Первоначальные дозировки капсулы распределяют в твердые желатиновые капсулы и герметично скрепляют с помощью распыления раствором вода:этанол 1:1 (мас./мас.). Последующие содержания действующего вещества, включая 0,25, 1 и 4 мг, распределяют в твердые желатиновые капсулы и герметично скрепляют с помощью полоски из желатина/полисорбата 80. Соответствующие составы плацебо получают аналогичным способом, но без добавления лекарственного вещества и антиоксиданта.
Способ производства капсул является одинаковым для всех содержаний действующего вещества. Способ состоит из следующих стадий, на которых: 1) моно- и диглицериды эксципиента расплавляют при 40°C в случае необходимости; 2) моно- и диглицериды добавляют в оснащенный рубашкой сосуд соответствующего размера и начинают перемешивание; 3) бутилированный гидроксианизол добавляют к моно- и диглицеридам, и перемешивают до растворения (минимум 10 мин.); 4) соединение 1 медленно добавляют к смеси и перемешивают до растворения (визуальное подтверждение); 5) наполняют раствором твердые желатиновые капсулы; 6) наполненные капсулы герметично скрепляют смесью желатина и полисорбата 80; 7) высушивают герметично скрепленные капсулы в течение ночи, и затем капсулы визуально проверяют на утечку; 8) приемлемые капсулы могут рассортировать по массе, в случае необходимости; и 9) конечный продукт затем упаковывают в соответствующие контейнеры.
Пример 3. Клиническое исследование серлопитанта при хроническом зуде
Хорошо контролированное клиническое испытание с участием людей по тестированию эффективности трех дозировок серлопитанта при лечении хронического зуда проводится в соответствии с руководством ICH для надлежащей клинической практики, Кодексом федеральных правил США, Законом о непрерывности действия и прозрачности медицинского страхования (HIPAA) и какими-либо местными регуляторными требованиями. Исследование является фазой II распределенного по группам случайным образом, двойного слепого, в параллельных группах, плацебо-контролируемого, многоцентрового исследования, предназначенного для тестирования эффективности и безопасности различных доз серлопитанта по сравнению с плацебо у пациентов с хроническим зудом. Исследуемая группа пациентов включает взрослых мужчин или женщин в возрасте от 18 до 72 лет. Пациентам предварительно должен быть поставлен диагноз хронического зуда, вызванного любой этиологией, за исключением уремии, печеночной недостаточности, рака или противораковой терапии, с хроническим зудом, определенным как зуд на протяжении более, чем 6 недель, и VAS оценкой более, чем 7.
Пациентов распределяют по группам случайным образом для того, чтобы получать либо плацебо, либо одну из трех доз активного агента. Пациенты принимают активное лекарственное средство или плацебо один раз в день перорально в общей сложности от 2 до 8 недель. Максимальная продолжительность исследования для каждого субъекта составляет приблизительно 14 недель и включает скрининговый период вплоть до 2 недель, период лечения 2-8 недель, и последующий период вплоть до 4 недель. Параметры исследования приведены в таблице 3.



Дополнительные клинические испытания в соответствии с аналогичной структурой могут быть проведены для тестирования различных уровней дозирования активного ингредиента или для установления различия между оптимальными дозами или схемами дозирования. Кроме того, эффективность лекарственного средства в конкретных группах, таких как пожилые люди, дети или пациенты с уремией, печеночной недостаточностью, раком, или пациенты, перенесшие противораковую терапию, могут быть определены в дополнительных клинических испытаниях, проведенных по аналогичной методике.
Пример 4. Составы для местного применения, содержащие серлопитант
Таблица 5 показывает различные составы для местного применения, содержащие серлопитант. Составы включают Vanicream™ Moisturizing Skin Cream («VM»), Vanicream™ Lite Lotion («VLL») или Aquaphor® Healing Ointment («АР» от Eucerin) как основа или носитель. VM и VLL представляют собой эмульсию типа масло-в-воде и АР имеет масляную основу. Исходный раствор серлопитанта в виде свободного основания (соединение 1 или «Соед. 1») в этаноле (EtOH) получали путем растворения серлопитанта в виде свободного основания в этаноле до максимальной степени и затем фильтрования полученного в результате раствора через Anotop® 25 неорганический фильтр, имеющий поры с размером 0,02 микрон. Серлопитант в виде свободного основания имеет максимальную растворимость в этаноле 64,5 мг/г EtOH, или 6,45% мас./мас. Для того, чтобы получить состав для местного применения, исходный раствор серлопитанта/этанола добавляли в тарированную пробирку, содержащую конкретное количество основания до получения в результате смеси, которая весит 25,0 г. Смесь интенсивно перемешивали в течение 2 минут, используя вибрационный стенд и затем медленно вращали в течение 4 дней. Для составов «С», этанол, не содержащий серлопитант, добавляли, таким образом, что составы «В» и «С» должны содержать одинаковое количество основания и этанола.

Определили, что АР является неприемлемой основой для этанольного раствора, содержащего серлопитант из-за нерастворимости этанола в такой основе. Основа VM является стабильной/неизменной при 15х увеличении микроскопа после 4 дней смешивания с 15,5% этанола. Основа VLL показала некоторую агрегацию пластинчатых структур при 15х увеличении микроскопа после 4 дней смешивания с 15,5% этанола, но общее изменение основы являлось незначительным. Составы VM и VLL могут быть протестированы, например, касательно проникновения в кожу серлопитанта.
Пример 5. Проникновение в кожу серлопитанта in vitro в составах для местного применения
Составы для местного применения A-D, использованные в исследованиях проникновения в кожу in vitro, показаны в таблице 6. Основы «VM» и «VLL» составов А-D описаны в примере 4. Составы A-D были получены в соответствии со способами, описанными в примере 4.


Проникновение в кожу серлопитанта in vitro в составах для местного применения A-D оценивали с использованием диффузионной ячейки Франца. ФИГ. 2 иллюстрирует диффузионную ячейку Франца. Диффузионная ячейка Франца, имеющая круговую зону проникновения 4,15 см2 и объем камеры рецептора 19 мл, была создана с терморегулируемой внешней водяной рубашкой, чтобы поддерживать температуру 37°С. Камеру рецептора наполняли 19 мл 1×PBS (рН 7,5), содержащим 10% этанола и 1% Tween® 80. Тестирование растворимости показало, что серлопитант оставался растворимым при концентрациях 0,5, 5 и 50 мкг/мл в данном растворе после 1 часа инкубирования при 37°С. Растворимость серлопитанта значительно снижалась, если не использовали Tween® 80, и незначительно снижалась, если не использовали этанол.
Кожу человека предварительно обрабатывали, чтобы удалить весь подкожный жир и очищали 70% о этанолом перед использованием. Кожу визуально проверяли, чтобы гарантировать, что на ней отсутствуют какие-либо поверхностные неровности или мелкие отверстия, и разделяли на одинаковые четыре части. Затем кожу устанавливали на камеру рецептора лицевой стороной рогового слоя эпидермиса. Приблизительно 100 мг состава для местного применения А, В, С или D наносили на кожу (фактическая масса: А, 103,8 мг; В, 101,3 мг; С, 103,2 мг; и D, 103,8 мг), которую затем покрывали парафином, чтобы избежать испарения.
Приблизительно 0,5 мл раствора отбирали через отверстие для отбора проб диффузионной ячейки Франца через 0,5, 1, 2, 4, 6, 18 и 22 часа. Камеру рецептора снова наполняли равным объемом свежего диффузионного буфера после каждого отбора проб. В конце эксперимента (через 22 часа инкубирования), кожу протирали начисто метанолом, и участок, обработанный составом, взвешивали и замораживали для изготовления срезов из замороженных тканей.
Все пробы подвергали обработке твердофазной экстракцией (SPE) перед анализом ЖХ-МС/МС. Коротко говоря, Strata-X 33 мкм полимерную колонку с обращенной фазой с массой сорбента 30 мг/1 мл объема (Phenomenex) подвергали обработке 1 мл метанола и уравновешивали 1 мл воды. 300 мкл пробы загружали в колонку с последующим промыванием 1 мл 30% метанола. Серлопитант элюировали 2% муравьиной кислотой в ацетонитриле. Пробу затем концентрировали путем сушки с обдувом азотом и повторно суспендировали в 50 мкл 50% метанола. Рабочий стандарт получали сначала, используя метод добавок диффузионного буфера с известными концентрациями серлопитанта, который затем подвергали обработке, используя тот же SPE способ. Достигали чувствительность 0,1 нг/мл. Концентрации серлопитанта в пробах, полученных из составов A-D, определяли путем сравнения со стандартом. Серлопитант не был обнаружен в пробах, полученных из составов для местного применения А и D, как и ожидалось. ФИГ. 3 показывает совокупное высвобождение серлопитанта из составов для местного применения В и С в камеру рецептора через 0,5, 1, 2, 4, 6, 18 и 22 часа. После начального отставания, серлопитант был обнаружен с помощью ЖХ-МС/МС в камере рецептора через 6 часов. ФИГ. 3 показывает, что состав для местного применения В в результате дал большее проникновение серлопитанта через кожу, чем состав для местного применения С в данном исследовании in vitro.
Количество серлопитанта, которое удерживается в коже, определяли в конце эксперимента. Кожу вытирали и промывали метанолом. Участок, обработанный составом, разрезали на горизонтальные участки 25 мкм, используя криостат. Каждые 10 участков объединяли, помещали в пробирки Эппендорф, взвешивали и обрабатывали дважды объемом 1 мг/мл либеразы при 37°C в течение 1 часа. Обработанные участки кожи затем гомогенизировали с использованием ультразвукового зонда. К 25 мкл кожного гомогената добавляли 25 мкл 50% метанола и 100 мкл ацетонитрила/метанола, чтобы экстрагировать серлопитант. Для маркированных стандартов, 25 мкл раствора серлопитанта в 50% метаноле (от 5 нг/мл до 5000 нг/мл) добавляли к 25 мкл сравнительного кожного гомогената с последующим добавлением 100 мкл ацетонитрила/метанола. Экстрагированный серлопитант количественно определяли с помощью ЖХ-МС/МС. ФИГ. 4 показывает количество серлопитанта (называемое «VPD737» на ФИГ. 4), которое удерживается в коже в конце эксперимента. Каждый столбик представляет мкг серлопитанта/г кожи в 250 мкм слоях кожи. Для каждого из составов для местного применения В и С, столбики слева направо представляют количество серлопитанта, которое удерживается в слоях кожи от рогового слоя эпидермиса до дермы.
Пример 6. Иллюстративные составы для местного применения, содержащие серлопитант
Таблица 7 представляет неограничивающие примеры составов для местного применения, которые могут быть получены с серлопитантом или его солью, сольватом или полиморфом, и, необязательно, дополнительным терапевтическим агентом.




Все публикации и патентные заявки, упомянутые в данном описании, включены в данную заявку путем ссылки в той же степени, как если бы каждая отдельная публикация или патентная заявка были конкретно и индивидуально указаны как включенные путем ссылки.
Из вышеизложенного следует понимать, что, несмотря на то, что конкретные варианты осуществления настоящего изобретения были описаны в данной заявке в целях иллюстрации, различные модификации могут быть выполнены не отходя от сущности и объема настоящего изобретения. Соответственно, настоящее изобретение не ограничивается ничем, кроме как прилагаемой формулой изобретения.
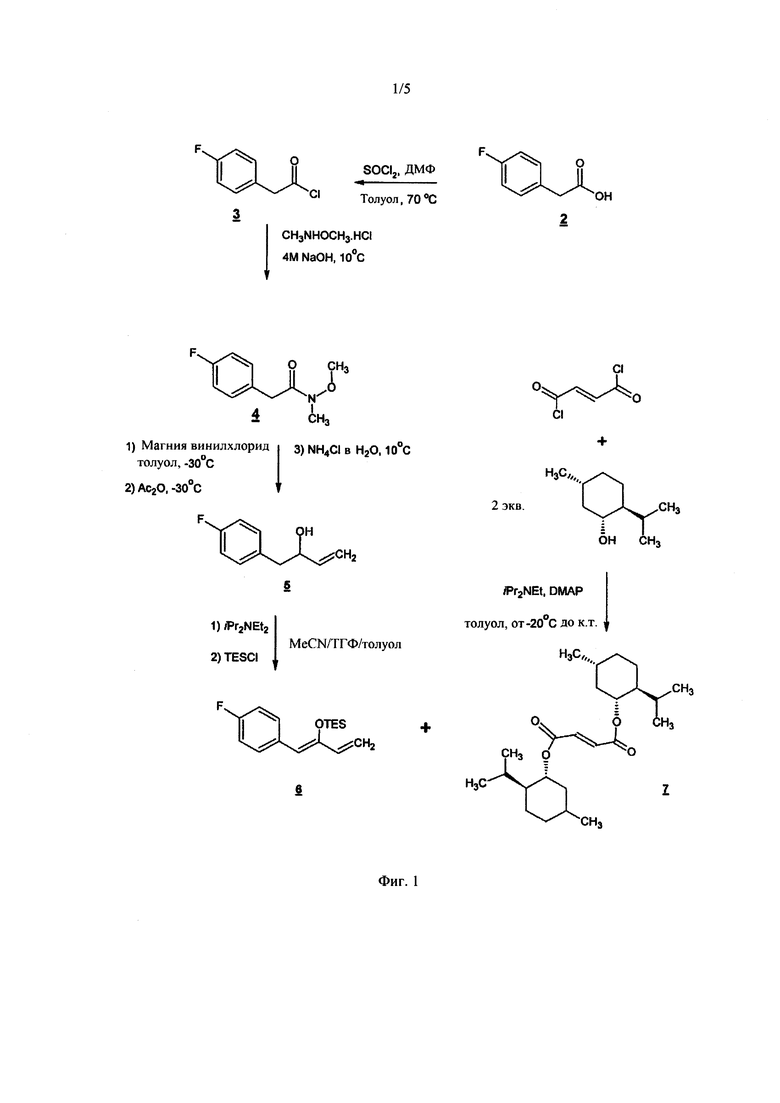
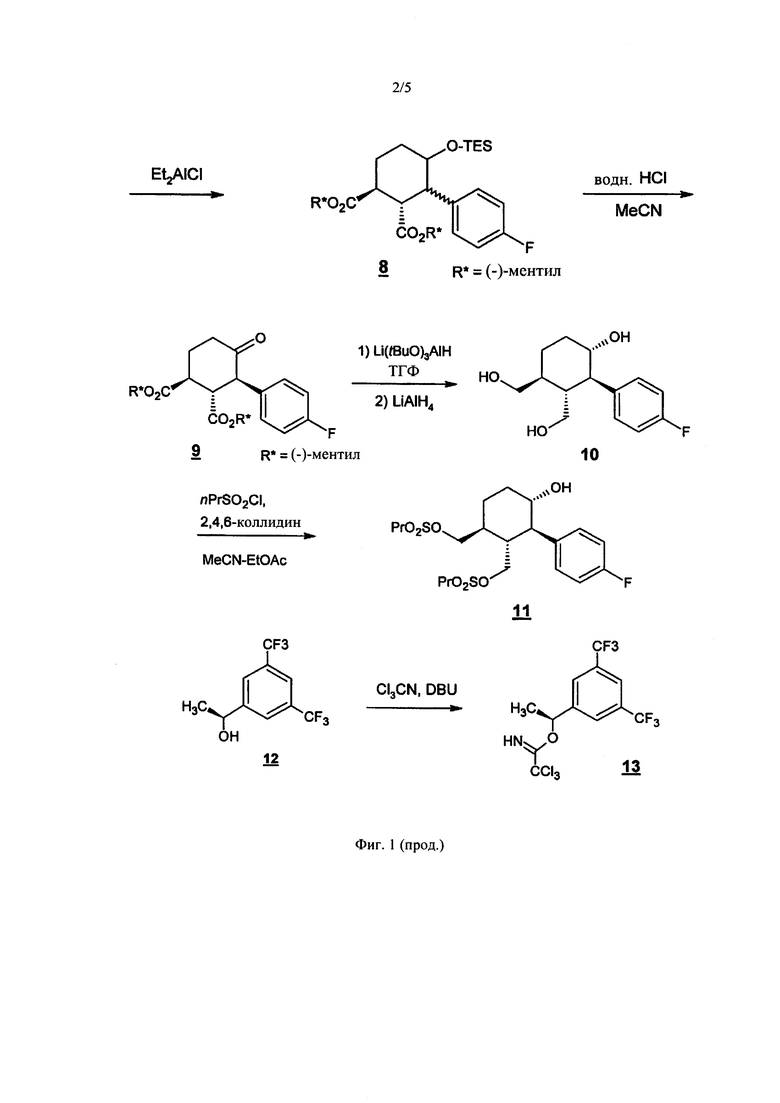
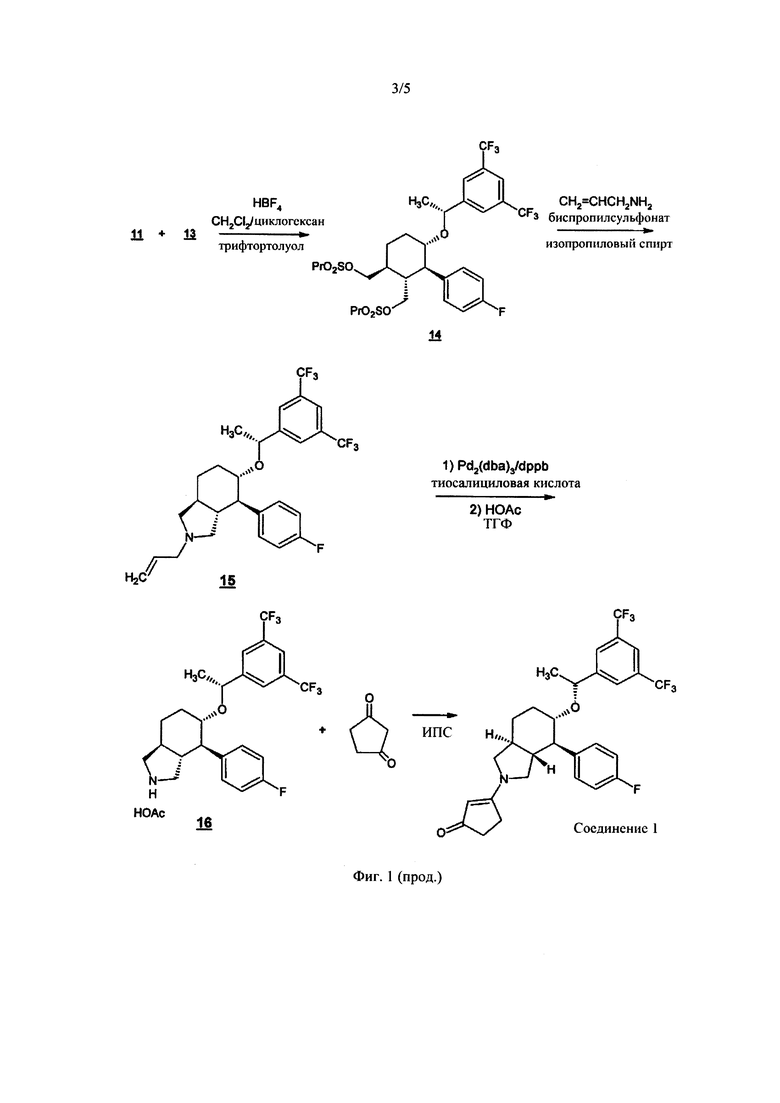

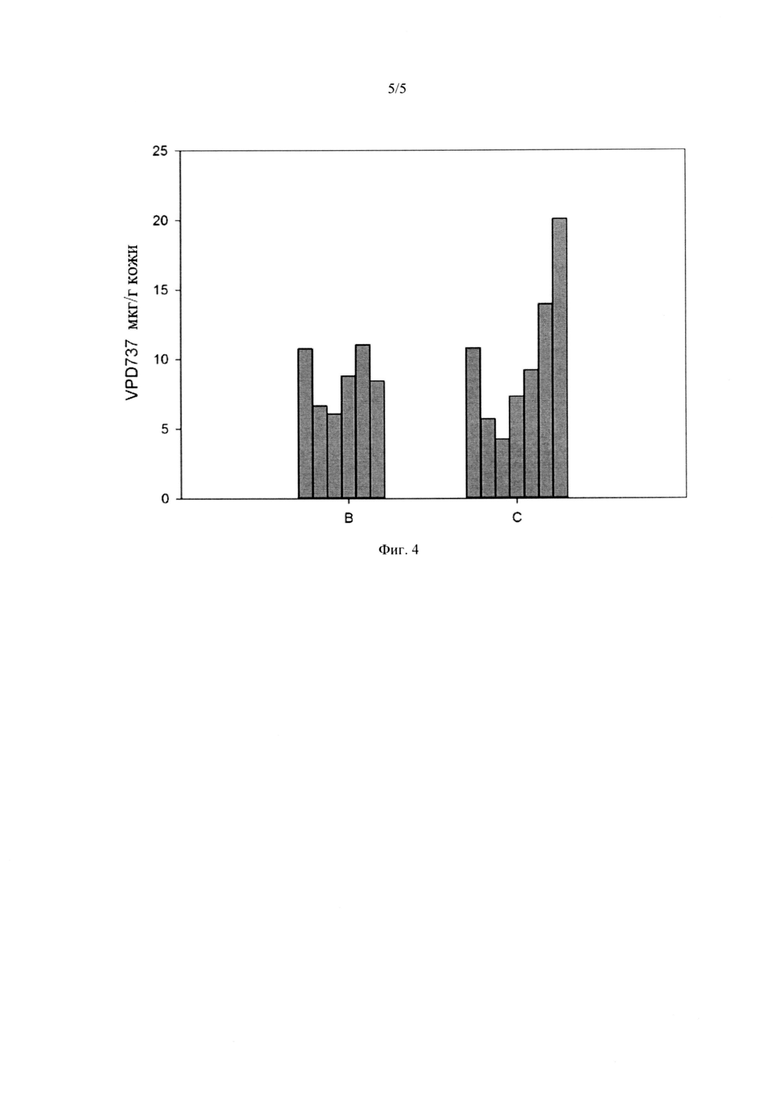
Группа изобретений относится к медицине и касается лечения зуда у пациента, который нуждается в таком лечении. Указанное лечение включает стадию, на которой вводят пациенту терапевтически эффективное количество 3-[(3aR,4R,5S,7aS)-5-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси]-4-(4-фторфенил)-1,3,3а,4,5,6,7,7а-октагидроизоиндол-2-ил]циклопент-2-ен-1-она (серлопитанта) или его фармацевтически приемлемой соли, сольвата или полиморфа. Также предложен способ введения серлопитанта пациенту. Группа изобретение обеспечивает лечение зуда разного генеза у пациента, при этом разработанная схема введения препарата обеспечивает продолжительный противозудный эффект. 2 н. и 32 з.п. ф-лы, 4 ил., 7 табл., 6 пр.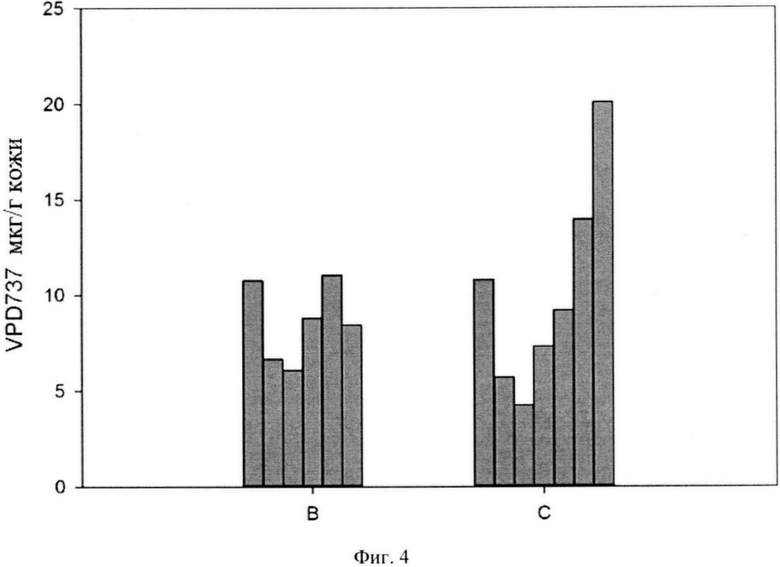
1. Способ лечения зуда у пациента, который нуждается в таком лечении, включающий стадию, на которой вводят указанному пациенту терапевтически эффективное количество 3-[(3aR,4R,5S,7aS)-5-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси]-4-(4-фторфенил)-1,3,3а,4,5,6,7,7а-октагидроизоиндол-2-ил]циклопент-2-ен-1-она (серлопитанта) или его фармацевтически приемлемой соли, сольвата или полиморфа.
2. Способ по п. 1, отличающийся тем, что терапевтически эффективное количество включает дозировку 0,10 мг, 0,15 мг, 0,20 мг, 0,25 мг, 0,5 мг, 0,75 мг, 1 мг, 2 мг, 2,5 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 15 мг, 20 мг, 25 мг или 30 мг один или более раз в день.
3. Способ по п. 2, отличающийся тем, что терапевтически эффективное количество включает дозировку 1 мг, 3 мг или 5 мг один раз в день.
4. Способ по п. 1, отличающийся тем, что терапевтически эффективное количество включает дозировку от приблизительно 0,1 мг до приблизительно 30 мг или от приблизительно 1 мг до приблизительно 7,5 мг.
5. Способ по п. 1, отличающийся тем, что терапевтически эффективное количество вводят перорально, например, в форме таблетки.
6. Способ по п. 1, отличающийся тем, что терапевтически эффективное количество вводят один раз в день перед сном.
7. Способ по п. 1, отличающийся тем, что терапевтически эффективное количество вводят один раз в день, один раз в два дня, один раз в три дня, один раз в четыре дня или один раз в неделю.
8. Способ лечения зуда, при этом указанный способ включает стадию, на которой вводят 3-[(3aR,4R,5S,7aS)-5-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси]-4-(4-фторфенил)-1,3,3а,4,5,6,7,7а-октагидроизоиндол-2-ил]циклопент-2-ен-1-он (серлопитант) или его фармацевтически приемлемую соль, сольват или полиморф пациенту, который нуждается в таком лечении, в соответствии со схемой, при этом указанная схема включает:
a) первое введение, по меньшей мере, одной насыщающей дозы; и
b) второе введение, по меньшей мере, одной терапевтически эффективной поддерживающей дозы,
причем указанная, по меньшей мере, одна насыщающая доза больше, чем указанная, по меньшей мере, одна терапевтически эффективная поддерживающая доза.
9. Способ по п. 8, отличающийся тем, что насыщающая доза в пять раз, четыре раза, три раза или два раза больше, чем поддерживающая доза.
10. Способ по п. 9, отличающийся тем, что насыщающая доза в три раза больше, чем поддерживающая доза.
11. Способ по п. 8, отличающийся тем, что насыщающую дозу вводят в день 1 и поддерживающую дозу вводят в день 2 и в дальнейшем.
12. Способ по п. 8, отличающийся тем, что насыщающую дозу и поддерживающую дозу вводят перед сном.
13. Способ по п. 8, отличающийся тем, что терапевтически эффективная поддерживающая доза составляет 0,10 мг, 0,15 мг, 0,20 мг, 0,25 мг, 0,5 мг, 0,75 мг, 1 мг, 2 мг, 2,5 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 15 мг, 20 мг, 25 мг или 30 мг, которые вводят один или более раз в день.
14. Способ по п. 13, отличающийся тем, что терапевтически эффективная поддерживающая доза включает дозировку 1 мг, 3 мг или 5 мг, которую вводят один раз в день.
15. Способ по п. 8, отличающийся тем, что терапевтически эффективная поддерживающая доза включает дозировку от приблизительно 0,1 мг до приблизительно 30 мг или от приблизительно 1 мг до приблизительно 7,5 мг.
16. Способ по п. 8, отличающийся тем, что терапевтически эффективную поддерживающую дозу вводят один раз в день, один раз в два дня, один раз в три дня, один раз в четыре дня или один раз в неделю.
17. Способ по п. 8, отличающийся тем, что серлопитант вводят перорально, например, в форме таблетки.
18. Способ по п. 1 или 8, отличающийся тем, что терапевтически эффективное количество или терапевтически эффективную поддерживающую дозу серлопитанта вводят в течение периода, составляющего, по меньшей мере, две недели, 1 месяц, 1,5 месяца или 2 месяца.
19. Способ по п. 1 или 8, отличающийся тем, что зуд связан с пруриго, генетическим заболеванием или заболеванием печени.
20. Способ по п. 19, отличающийся тем, что пруриго представляет собой узловатый пруриго, генетическое заболевание представляет собой буллезный эпидермолиз и заболевание печени представляет собой холестаз, первичный билиарный цирроз, гепатит (например, гепатит В или гепатит С), цирроз или печеночную недостаточность.
21. Способ по п. 1 или 8, отличающийся тем, что серлопитант вводят местно.
22. Способ по п. 21, отличающийся тем, что серлопитант вводят дермально или трансдермально.
23. Способ по п. 1 или 8, отличающийся тем, что дополнительно включает стадию, на которой вводят один или более дополнительных противозудных агентов.
24. Способ по п. 23, отличающийся тем, что один или более дополнительных противозудных агентов выбраны из группы, состоящей из антигистаминных средств, кортикостероидов, иммуномодуляторов, иммунодепрессантов, агонистов каппа-опиоидных рецепторов, антагонистов опиоидных рецепторов, антидепрессантов и противосудорожных средств.
25. Способ по п. 24, отличающийся тем, что:
антигистаминные средства выбраны из H1-антигистаминных средств (например, акривастин, антазолин, астемизол, азеластин, бепотастин, биластин, бромдифенгидрамин, бромфенирамин, буклизин, карбиноксамин, цетиризин, хлордифенгидрамин, хлорфенирамин, хлорпромазин, клемастин, циклизин, ципрогептадин, дезлоратадин, дексбромфенирамин, дексхлорфенирамин, дименгидринат, диметинден, дифенгидрамин, доксепин, доксиламин, эбастин, эмбрамин, фексофенадин, гидроксизин, кетотифен, левокабастин, левоцетиризин, лоратадин, меклозин, мепирамин, миртазапин, мизоластин, олопатадин, орфенадрин, фениндамин, фенирамин, фенилтолоксамин, прометазин, пириламин, кветиапин, квифенадин, рупатадин, терфенадин, трипеленнамин и трипролидин), и Н4-антигистаминных средств (например, тиоперамид, JNJ 7777120 и VUF-6002), и их фармацевтически приемлемых солей;
кортикостероиды представляют собой кортикостероиды, имеющие умеренную или среднюю эффективность, такие как амцинонид 0,1% (например, крем), бетаметазона дипропионат 0,05% (например, крем/мазь), бетаметазона валерат 0,1% (например, крем/мазь), клобетазона бутират 0,05% (например, крем), дезонид 0,05% (например, крем/мазь), флуоцинолона ацетонид 0,01-0,2% (например, крем/мазь), флурандренолид 0,05% (например, лента), флутиказона пропионат 0,005% (например, мазь), флутиказона пропионат 0,05% (например, крем), галометазон 0,05% (например, крем), гидрокортизона бутират 0,1% (например, крем/мазь), гидрокортизона валерат 0,2% (например, крем/мазь), мометазона фуроат 0,1% (например, крем/мазь), триамцинолона ацетонид 0,025-0,5% (например, крем/мазь) и триамцинолона диацетат 0,5% (например, крем/мазь);
иммуномодуляторы и иммунодепрессанты выбраны из талидомида, антиметаболитов (например, антифолатов, таких как метотрексат), ингибиторов кальциневрина (например, циклоспорин, пимекролимус и такролимус) и их фармацевтически приемлемых солей;
агонисты каппа опиоидных рецепторов выбраны из асимадолина, бремазоцина, динорфина, энадолина, кетазоцина, налфурафина, сальвинорина А, 2-метоксиметилсальвинорина В, 2-этоксиметилсальвинорина В, 2-фторэтоксиметилсальвинорина В, спирадолина, тифлуадома, BRL-52537, FE 200665, GR-89696, HZ-2, ICI-199,441, ICI-204,448, LPK-26, U-50488 и U-69,593), и их фармацевтически приемлемых солей;
антагонисты опиоидных рецепторов выбраны из буторфанола, ципродима, леваллорфана, нальбуфина, налорфина, налоксона, налоксола, налмефена, налтрексона, налтрексола и их фармацевтически приемлемых солей;
антидепрессанты выбраны из трициклических антидепрессантов (например, амитриптилин, амитриптилиноксид, амоксапин, досулепин, доксепин и мелитрацен), тетрациклических антидепрессантов (например, амоксапин, мапротилин, мазиндол, миансерин, миртазапин и сетиптилин), селективных ингибиторов обратного захвата серотонина (например, циталопрам, дапоксетин, эсциталопрам, флуоксетин, флувоксамин, пароксетин и сертралин), ингибиторов обратного захвата серотонина-норэпинефрина (например, бицифадин, дулоксетин, милнаципран, левомилнаципран, сибутрамин, венлафаксин, десвенлафаксин и SEP-227162) и их фармацевтически приемлемых солей; и
противосудорожные средства выбраны из карбамазепина, габапентина, прегабалина, вальпроевой кислоты и ее солей (например, натрия вальпроата) и их фармацевтически приемлемых солей.
26. Способ по п. 23, отличающийся тем, что один или более дополнительных противозудных агентов вводят местно.
27. Способ по п. 26, отличающийся тем, что один или более дополнительных противозудных агентов вводят дермально или трансдермально.
28. Способ по п. 24, отличающийся тем, что один или более дополнительных противозудных агентов вводят местно, например дермально или трансдермально.
29. Способ по п. 25, отличающийся тем, что один или более дополнительных противозудных агентов вводят местно, например дермально или трансдермально.
30. Способ по п. 23, отличающийся тем, что один или более дополнительных противозудных агентов вводят системно, например, орально.
31. Способ по п. 24, отличающийся тем, что один или более дополнительных противозудных агентов вводят системно, например, орально.
32. Способ по п. 25, отличающийся тем, что один или более дополнительных противозудных агентов вводят системно, например, орально.
33. Способ по п. 19 или 20, отличающийся тем, что зуд представляет собой холестатический зуд или билиарный зуд.
34. Способ по п. 1 или 8, отличающийся тем, что зуд представляет собой хронический зуд.
| WO2008030389 A2, 13.03.2008 | |||
| ГЕЛЬ, ОБЛАДАЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНЫМ И ПРОТИВОАЛЛЕРГИЧЕСКИМ ДЕЙСТВИЕМ | 2008 |
|
RU2370265C1 |
| TSUYOSHI OHMURA et al | |||
| Involvement of substance P in scratching behaviour in an atopic dermatitis model // EUROPEAN JOURNAL OF PHARMACOLOGY, 2004, vol | |||
| Бензиновая зажигалка | 1923 |
|
SU491A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| SONJA STANDER et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
Авторы
Даты
2018-09-06—Публикация
2014-06-24—Подача