ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет в соответствии с § 119(e) раздела 35 U.S.C. предварительной заявки на патент США 61/873,719, поданной 4 сентября 2013 года, и предварительной заявки на патент США 61/899,569, поданной 4 ноября 2013 года, содержание которых полностью включено в настоящую заявку посредством отсылки.
ССЫЛКА НА СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ, ПРЕДСТАВЛЕННЫЙ В ЭЛЕКТРОННОЙ ФОРМЕ
Официальная копия списка последовательностей представлена в электронной форме через систему EFS-Web в виде списка последовательностей в формате ASCII в файле под названием "226007_ST25.txt", созданном 04 ноября 2013 года и имеющем размер 68,6 килобайтов, и подана одновременно с описанием. Список последовательностей, содержащийся в данном документе в формате ASCII, является частью описания и полностью включен в настоящую заяку посредством отсылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее описание в общем относится к области молекулярной биологии и биохимии. Настоящее описание связано со способом анализа геномного участка вставки интегрированного донорного полинуклеотида. Способ может применяться для высокопроизводительного анализа интегрированного донорного полинуклеотида и может служить для минимизации обнаружения ложноположительных результатов. Кроме того, в способе применяется клеточный таргетинг и анализ, без необходимости получения или создания стабильно таргетированного растения.
УРОВЕНЬ ТЕХНИКИ
Направленная модификация генома растений являлась давней и недостижимой целью как прикладных, так и фундаментальных исследований. Направленное введение генов и пакетов генов в определенные положения в геноме растения улучшает качество трансгенных объектов, снижает затраты, связанные с получением трансгенных объектов, и обеспечивает новые способы создания трансгенных растительных продуктов, таких как последовательное пакетирование генов. В целом, направление трансгенов в определенные участки генома, вероятно, будет коммерчески выгодным. Значительные успехи были достигнуты в последние несколько лет в разработке способов и композиций для направленного воздействия и расщепления геномной ДНК с помощью сайт-специфических нуклеаз (например, цинк-пальцевых нуклеаз (ZFN), мегануклеаз, нуклеаз TALENS (от англ. transcription activator-like effector nucelases - подобные активаторам транскрипции эффекторные нуклеазы) и CRISPR-ассоциированной (от англ. clustered regularly interspaced short palindromic repeats - кластерные, разделенные регулярными интервалами, короткие палиндромные повторы) нуклеазы (CRISPR/Cas) со сконструированной crРНК/tracrРНК), для индукции направленного мутагенеза, индукции направленных делеций клеточных последовательностей ДНК и обеспечения направленной рекомбинации экзогенного донорного ДНК полинуклеотида в заданный геномный локус. См., например, патентные публикации США 20030232410; 20050208489; 20050026157; 20050064474 и 20060188987, и Международную патентную публикацию WO 2007/014275, описания которых полностью включены посредством отсылки во всех отношениях. В патентной публикации США 20080182332 описано применение неканонических цинк-пальцевых нуклеаз (ZFN) для направленной модификации геномов растений и в патентной публикации США 20090205083 описана ZFN-опосредованная направленная модификация геномного локуса EPSPs растений. Существующие способы направленной вставки экзогенной ДНК обычно включают котрансформацию растительной ткани донорным ДНК полинуклеотидом, содержащим по меньшей мере один трансген и сайт-специфическую нуклеазу (например, ZFN), которая создана для связывания и расщепления определенного геномного локуса. Это приводит к стабильной вставке донорного ДНК полинуклеотида в расщепленный геномный локус с направленным введением гена в указанный геномный локус.
К сожалению, описываемые и наблюдаемые частоты направленной геномной модификации указывают, что таргетинг в геномные локусы в растениях относительно неэффективен. Описываемая неэффективность требует проводить скрининг большого количества растительных объектов для идентификации специфического объекта, содержащего направленные геномные локусы. Способ скрининга также должен обеспечивать возможность применения в качестве высокопроизводительного способа быстрой идентификации растительных объектов, содержащих направленные геномные локусы. Кроме того, поскольку направленная вставка гена происходит в сочетании со случайной вставкой гена, должны быть разработаны способы скрининга для специфичной идентификации таргетинга геномных локусов в окружении случайных вставок и обнаружения геномной интеграции из экзогенной плазмидной ДНК, которая может давать ложноположительные результаты. Кроме того, анализ должен обладать достаточной чувствительностью для обнаружения события, происходящего в отдельной клетке, которая содержит единственное направленное событие, среди тысяч других неспецифических клеток. Наиболее часто описываемые анализы растительных объектов основаны на одном аналитическом методе для подтверждения таргетинга, что может приводить к неточной оценке частоты таргетинга и результатам с низкой достоверностью. Существует потребность в создании улучшенных способов молекулярного анализа, в особенности высокопроизводительного анализа, которые могут позволить обнаружить сайт-специфические хромосомные интеграции и отличить такие объекты от экзогенной плазмидной ДНК. Наконец, существующие способы оценки направленных геномных модификаций основаны на получении стабильных растений и требуют больших затрат времени и средств. Таким образом, существует потребность в способе анализа, который позволяет выполнить быструю оценку таргетинга в большом количестве геномных локусов и провести скрининг большого количества сайт-специфических нуклеаз для идентификации и подтверждения вставки донорной полинуклеотидной последовательности в геномных локусах-мишенях.
Предшествующие примеры из уровня техники и ограничения, связанные с ними, являются иллюстративными и не являются исчерпывающими. Другие ограничения из уровня техники будут очевидны специалистам в данной области при прочтении настоящего описания.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В варианте осуществления описание относится к анализу для обнаружения сайт-специфическаой интеграции донорной полинуклеотидной последовательности в целевой участок генома, где: геномную ДНК амплифицируют в первом раунде ПЦР с получением первого ампликона при использовании первого внешнего ПЦР-праймера, предназначенного для связывания с целевым участком геномной ДНК; первого внутреннего ПЦР-праймера, предназначенного для связывания интегрированной донорной полинуклеотидной последовательности, и первый ампликон амплифицируют во втором раунде ПЦР с использованием праймеров, специфичных к последовательностям, расположенным в первом ампликоне, с получением второго ампликона; и обнаруживают присутствие второго ампликона, где получение второго ампликона указывает на присутствие события сайт-спеифической интеграции.
В одном из аспектов данного варианта осуществления целевой участок генома включает эндогенный или сконструированный целевой участок генома. В другом аспекте данного варианта осуществления первый внутренний ПЦР-праймер представлен в более низкой концентрации, чем первый внешний ПЦР-праймер. В варианте осуществления первый раунд ПЦР проводят при использовании относительной концентрации первого внешнего ПЦР-праймера к первому внутреннему ПЦР-праймеру приблизительно 4:1, 3:1 или 2:1. В другом варианте осуществления первый внутренний ПЦР-праймер включает концентрацию 0,05-0,09 мкM, а первый внешний ПЦР-праймер включает концентрацию по меньшей мере 0,1 мкM.
В следующем аспекте варианта осуществления второй раунд ПЦР включает второй внешний ПЦР-праймер, предназначенный для связывания с целевым участком геномной ДНК первого ампликона, и второй внутренний ПЦР-праймер, предназначенный для связывания с интегрированной донорной полинуклеотидной последовательностью первого ампликона. В варианте осуществления второй внутренний ПЦР-праймер представлен в более низкой концентрации, чем второй внешний ПЦР-праймер. В другом варианте осуществления второй раунд ПЦР проводят при использовании относительной концентрации второго внешнего ПЦР-праймера ко второму внутреннему ПЦР-праймеру приблизительно 4:1, 3:1 или 2:1. В другом варианте осуществления второй внутренний ПЦР-праймер включает концентрацию 0,05-0,1 мкM, а второй внешний ПЦР-праймер включает концентрацию 0,2 мкM.
В другом аспекте данного варианта осуществления геномная ДНК, включающая сайт-специфическую интеграцию донорной полинуклеотидной последовательности в целевой участок генома, является растительной геномной ДНК. В качестве варианта осуществления, растительная геномная ДНК выделена из однодольного растения. В качестве другого варианта осуществления, растительная геномная ДНК выделена из двудольного растения.
В другом аспекте данного варианта осуществления расщепление целевого участка геномной ДНК сайт-специфической нуклеазой приводит к сайт-специфической интеграции донорной полинуклеотидной последовательности в целевой участок генома. В качестве варианта осуществления, сайт-специфическая нуклеаза выбрана из группы, состоящей из цинк-пальцевой нуклеазы, нуклеазы CRISPR, нуклеазы TALEN или мегануклеазы. В следующем варианте осуществления сайт-специфическая интеграция донорной полинуклеотидной последовательности в целевой участок генома проходит по механизму негомологичного соединения концов.
В аспекте варианта осуществления этапом обнаружения является агарозный гель второго ампликона или реакция секвенирования второго ампликона.
В еще одном аспекте варианта осуществления описание относится к способу обнаружения сайт-специфической интеграции донорной полинуклеотидной последовательности в целевом участке генома трансфицированных растительных клеток, включающему: амплификацию геномной ДНК в первом раунде ПЦР с получением первого ампликона, где указанную ПЦР проводят при использовании первого внешнего ПЦР-праймера, предназначенного для связывания с целевым участком генома, и первого внутреннего ПЦР-праймера, предназначенного для связывания с донорной полинуклеотидной последовательностью, а также где указанный первый внутренний ПЦР-праймер представлен в более низкой концентрации, чем первый внешний ПЦР-праймер; амплификацию первого ампликона во втором раунде ПЦР при использовании праймеров, специфичных к последовательностям, расположенным в первом ампликоне, с получением второго ампликона; и обнаружение присутствия второго ампликона, где получение второго ампликона указывает на присутствие события сайт-специфической интеграции. В других вариантах осуществления растительная клетка является протопластом растительной клетки. В варианте осуществления обнаружение сайт-специфической интеграции осуществляют на смешанной популяции целевых и нецелевых растительных клеток, где нецелевые растительные клетки не содержат донорную полинуклеотидную последовательность в целевом участке генома.
В дополнение к примерным аспектам и вариантам осуществления, описанным выше, другие аспекты и варианты осуществления станут очевидными при изучении следующих описаний.
КРАТКОЕ ОПИСАНИЕ ФИГУР
На Фигуре 1 показана карта плазмиды pDAB111845.
На Фигуре 2 показана карта плазмиды pDAB111846.
На Фигуре 3 показана карта плазмиды pDAB117415.
На Фигуре 4 показана карта плазмиды pDAB117416.
На Фигуре 5 показана карта плазмиды pDAB117417.
На Фигуре 6 показана карта плазмиды pDAB117419.
На Фигуре 7 показана карта плазмиды pDAB117434.
На Фигуре 8 показана карта плазмиды pDAB117418.
На Фигуре 9 показана карта плазмиды pDAB117420.
На Фигуре 10 показана карта плазмиды pDAB117421.
На Фигуре 11 показано изображение универсальной донорной полинуклеотидной последовательности для интеграции посредством NHEJ.
На Фигуре 12 показано изображение универсальной донорной полинуклеотидной последовательности для интеграции посредством HDR. Подпись "HA" обозначает плечи гомологии; и подпись "ZFN BS" обозначает сайт связывания ZFN (для мономера).
На Фигуре 13 показаны конструкции, используемые для таргетинга и подтверждения правильности интеграции универсальной донорной полинуклеотидной системы в выбранных целевых геномных локусах Zea mays. A) область конструирования ZFN с расположением пар ZFN. B) конфигурация экспрессионной конструкции ZFN. Подпись "NLS" обозначает сигнал ядерной локализации, подпись "ZFP" обозначает цинк-пальцвый белок. C) универсальный донорный полинуклеотид для NHEJ-опосредованного таргетинга выбранных геномных локусов Zea mays. Z1-Z6 представляют собой сайты связывания ZFN, специфические для выбранных целевых геномных локусов Zea mays. Количество сайтов ZFN может варьировать от 3 до 6. Вертикальные стрелки указывают уникальные сайты рестрикции, а горизонтальные стрелки представляют потенциальные сайты для ПЦР-праймеров. Универсальная донорная полинуклеотидная система представляет собой короткую (110 пн) последовательность, которая характерна для всех доноров, используемых для интеграции в выбранные геномные локусы Zea mays.
На Фигуре 14 показана карта плазмиды pDAB8393.
На Фигурах 15A и 15B показана активность расщепления ZFN в выбранных целевых геномных локусах Zea mays. Активность расщепления представлена как количество последовательностей с вставками-делециями в сайте расщепления ZFN на один миллион считанных последовательностей высокого качества. На Фигуре 15A представлены данные в форме гистограммы. На Фигуре 15B представлены данные в виде таблицы.
На Фигуре 16 показано подтверждение правильности выбранных целевых геномных локусов Zea mays с использованием способа быстрого анализа таргетинга на основе NHEJ.
На Фигуре 17 показаны конструкции плазмид, трансформированных в Zea mays посредством случайной интеграции, которые включают события, используемые для анализа фланкирующих последовательностей и исследований экспрессии трансгенов.
На Фигуре 18 показана донорная вставка посредством NHEJ по ELP в быстром анализе таргетинга протопластов. Вставка может проходить в прямой или обратной ориентации.
На Фигуре 19 показано расщепление по сайтам расщепления ZFN в ELP1. Расщепление представлено как ослабление сигнала кПЦР по отношению мишени к контролю. В среднем наблюдается снижение сигнала на 22% и 15% для ZFN1 и ZFN3, соответственно.
На Фигуре 20 показана последовательность амплифицированных продуктов внутренней-внешней ПЦР. Четыре клона из каждой внутренней-внешней ПЦР были секвенированы, и результаты продемонстрировали интактные целевые донорные соединения и процессированные концевые соединения. Перечисленные последовательности соответствуют SEQ ID NO: 248, как предсказано, SEQ ID NO:249 как A9-1, SEQ ID NO:250 как A9-2, SEQ ID NO:251 как A9-5, SEQ ID NO:252 как A9-6, SEQ ID NO:253 как G8-1, SEQ ID NO:254 как G8-2, SEQ ID NO:255 как G8-5, SEQ ID NO:256 как G8-6, SEQ ID NO:257 как G9-1, SEQ ID NO:258 как G9-2, SEQ ID NO:259 как G9-6, SEQ ID NO:260 как H9-1, SEQ ID NO:261 как H9-2, SEQ ID NO:262 как H9-5 и SEQ ID NO:263 как H9-6.
На Фигуре 21 показана донорная вставка посредством NHEJ по E32 в быстром анализе таргетинга протопластов. Вставка может проходить в прямой или обратной ориентации.
На Фигуре 22 представлена схема, на которой показано соотношение праймеров, подобранных к донорному полинуклеотиду и цинк-пальцевой связывающей последовательности.
На Фигуре 23 показана карта плазмиды pDAB7221.
На Фигуре 24 показана схема зондов/праймеров для анализа расщепления локуса. Указаны сайты связывания F2 ZFN для FAD2 2.3 и 2.6 генов и праймеры, используемые для анализа расщепления.
На Фигуре 25 представлена последовательность продуктов внутренней-внешней ПЦР, полученных в результате NHEJ таргетинга донорной последовательности при использовании F2, цинк-пальцевой нуклеазы ZFN2, в локусе FAD2 2.3. Референсная последовательность (верхняя часть фигуры) представляет конфигурацию направленной вставки донорного вектора в обратной ориентации. Одноцепочечные концы молекул ДНК, полученные при расщеплении FokI, заполняли с получением референсной последовательности. Показаны последовательности Сэнгера. Последовательности связывания ZFN F2, ZFN2 подчеркнуты. Клоны плазмид с последовательностью, аналогичной указанной последовательности, перечислены справа.
ПОДРОБНОЕ ОПИСАНИЕ
I. Обзор
Далее раскрыты новые способы быстрого скрининга, идентификации и исследования растительных объектов, подвергнутых направленному воздействию сайт-специфической нуклеазы. Указанные способы могут применяться для анализа интеграции донорного полинуклеотида в целевом локусе генома посредством первой и второй реакции амплификации. Первая и вторая реакции амплификации являются "внутренней-внешней" реакцией ПЦР амплификации для скрининга 3' и/или 5' соединительных последовательностей донорного ДНК полинуклеотида, который является мишенью в геномном локусе. Наличие амплифицированного продукта, который содержит 3' и/или 5' соединительные последовательности, указывает, что донорный ДНК полинуклеотид присутствует в геномном локусе-мишени.
Раскрытые скрининговые анализы описывают высококачественные, высокопроизводительные процессы для идентификации и получения объектов с направленной вставкой трансгена. Применение скринингового анализа позволяет проанализировать и провести скрининг большого количества растительных объектов с целью отбора специфических объектов, которые содержат вставку донорного ДНК полинуклеотида в геномном локусе-мишени, и отличить эти события от ложноположительных результатов. Кроме того, раскрытые способы могут быть применены в качестве высокопроизводительных анализов, которые позволяют проводить быструю и эффективную идентификацию субпопуляции образцов, которые могут быть затем также проанализированы с помощью других молекулярных методов подтверждения. Раскрытый настоящий объект изобретения включает растения и растительные клетки, включающие растительные объекты, подвергнутые направленному воздействию нуклеазы, отобранные с применением новых способов скрининга. Кроме того, данная методика может быть легко применена для анализа любых видов растений.
II. Термины
Если не определено иное, все технические и научные термины, используемые в настоящем описании, имеют такое же значение, под которым их обычно понимает средний специалист в данной области техники, к которой относится данное описание. В случае возникновения противоречий настоящая заявка, включая определения, будет иметь преимущественную силу. Если из контекста не следует иное, термины в форме единственного числа должны включать формы множественного числа, и термины в форме множественного числа должны включать формы единственного числа. Все публикации, патенты и другие источники, указанные в настоящем описании, полностью включены посредством отсылки во всех отношениях, как если бы каждая отдельная публикация или заявка на патент были прямо и индивидуально указаны, как включенные посредством отсылки, если только определенные разделы патентов или патентных публикаций не указаны, как включенные посредством отсылки.
Для дополнительного уточнения настоящего описания представлены следующие термины, сокращения и определения.
При использовании в настоящем описании предполагается, что термины "включают", "включающий", "имеет", "имеющий", "содержит" или "содержащий", или их любая другая вариация, являются неисключающими или открытыми. Например, композиция, смесь, процесс, способ, изделие или устройство, которые включают список элементов, не должны обязательно ограничиваться только указанными элементами, но могут включать и другие элементы, не перечисленные прямо или характерные для такой композиции, смеси, процесса, способа, изделия или устройства. Кроме того, если прямо не указано обратное, "или" относится к включающему или, а не к исключающему или. Например, условие A или B удовлетворено любым из следующего: A верно (или присутствует), а B ложно (или не присутствует), A ложно (или не присутствует), а B верно (или присутствует), и A и B верны (или присутствуют).
Термин "изобретение" или "настоящее изобретение", при использовании в настоящем описании, является неограничивающим термином и не должен относиться к какому-либо одному варианту осуществления конкретного изобретения, а охватывает все возможные варианты осуществления, как раскрыто в заявке.
При использовании в настоящем описании, термин "растение" включает целое растение и любое потомство, клетку, ткань или часть растения. Термин "части растения" включает любую часть(и) растения, в том числе, например, и без ограничения: семя (включая зрелое семя, незрелое семя и незрелый зародыш без семенной оболочки); черенки растения; клетку растения; культуру клеток растения; орган растения (например, пыльцу, зародыши, цветки, плоды, побеги, листья, корни, стебли и соответствующие экспланты). Ткань растения или орган растения могут быть семенем, каллусом или любой другой группой клеток растения, которые организованы в структурную или функциональную единицу. Растительная клетка или культура тканей могут быть способны к регенерации растения, обладающего физиологическими и морфологическими признаками растения, из которого была получена клетка или ткань, и регенерации растения, имеющего по существу такой же генотип, что и указанное растение. Напротив, некоторые растительные клетки не способны к регенерации с получением растения. Регенерируемые клетки в растительной клетке или культуре тканей могут быть зародышами, протопластами, меристематическими клетками, каллусом, пыльцой, листьями, пыльниками, корнями, корневыми кончиками, пестиками початков, цветками, зернами, початками, стержнями початков, обверткой початков или стеблями.
Части растения включают пригодные для сбора части и части, пригодные для размножения потомства растений. Части растения, пригодные для размножения, включают, например, и без ограничения: семя; плод; черенок; сеянец; клубень и корневище. Пригодная для сбора часть растения может быть любой полезной частью растения, включая, например, и без ограничения: цветок; пыльцу; сеянец; клубень; лист; стебель; плод; семя и корень.
Растительная клетка является структурной и физиологической единицей растения. Растительные клетки, при использовании в настоящем описании, включают протопласты и протопласты с неполной клеточной стенкой. Растительная клетка может быть в форме выделенной одиночной клетки или агрегата клеток (например, рыхлого каллуса и культивируемой клетки) и может быть частью более высокоорганизованной единицы (например, растительной ткани, органа растения и растения). Таким образом, растительная клетка может быть протопластом, гаметообразующей клеткой или клеткой или коллекцией клеток, которые могут регенерировать с образованием целого растения. Таким образом, семя, которое включает множество растительных клеток и способно к регенерации с образованием целого растения, считается "частью растения" в вариантах осуществления в настоящей заявке.
Термин "протопласт", при использовании в настоящем описании, относится к растительной клетке, у которой была полностью или частично удалена ее клеточная стенка, и ее липидная бислойная мембрана была обнажена. Как правило, протопласт представляет собой выделенную растительную клетку без клеточных стенок, которая обладает возможностью регенерации с получением клеточной культуры или целого растения.
При использовании в настоящем описании, "эндогенная последовательность" определяет нативную форму полинуклеотида, гена или полипептида в его естественном местоположении в организме или в геноме организма.
Термин "выделенный", при использовании в настоящем описании, означает удаленный из своего естественного окружения.
Термин "очищенный", при использовании в настоящем описании, относится к выделению молекулы или соединения в форме, которая по существу не содержит контаминирующих примесей, обычно связанных с молекулой или соединением в нативном или естественном окружении, и означает повышение чистоты в результате отделения от других компонентов исходной композиции. Термин "очищенная нуклеиновая кислота" используется в настоящем описании для описания последовательности нуклеиновой кислоты, которая была отделена от других соединений, в том числе, без ограничения перечисленными, полипептидов, липидов и углеводов.
При использовании в настоящем описании, термины "полинуклеотид", "нуклеиновая кислота" и "молекула нуклеиновой кислоты" используются попеременно и могут охватывать одну нуклеиновую кислоту; множество нуклеиновых кислот; фрагмент нуклеиновой кислоты, ее вариант или производное; и конструкцию нуклеиновой кислоты (например, матричную РНК (мРНК) и плазмидную ДНК (пДНК)). Полинуклеотид или нуклеиновая кислота могут содержать нуклеотидную последовательность полноразмерной последовательности кДНК или ее фрагмент, включая нетранслируемые 5' и/или 3' последовательности и кодирующую последовательность (и). Полинуклеотид или нуклеиновая кислота могут состоять из любого полирибонуклеотида или полидезоксирибонуклеотида, который может включать немодифицированные рибонуклеотиды или дезоксирибонуклеотиды или модифицированные рибонуклеотиды или дезоксирибонуклеотиды. Например, полинуклеотид или нуклеиновая кислота могут состоять из одно- и двухцепочечной ДНК; ДНК, которая является смесью одно- и двухцепочечных областей; одно- и двухцепочечной РНК; и РНК, которая является смесью одно- и двухцепочечных областей. Гибридные молекулы, включающие ДНК и РНК, могут быть одноцепочечными, двухцепочечными или смесью одно- и двухцепочечных областей. Предыдущие термины также включают химически, энзиматически и метаболически модифицированные формы полинуклеотида или нуклеиновой кислоты.
Подразумевается, что специфическая ДНК относится также к ее комплементарной последовательности, последовательность которой определяется согласно правилам спаривания дезоксирибонуклеотидных оснований.
При использовании в настоящем описании, термин "ген" относится к нуклеиновой кислоте, которая кодирует функциональный продукт (РНК или полипептид/белок). Ген может включать регуляторные последовательности до (5' некодирующие последовательности) и/или после (3' некодирующие последовательности) последовательности, кодирующей функциональный продукт.
При использовании в настоящем описании, термин "кодирующая последовательность" относится к последовательности нуклеиновой кислоты, которая кодирует определенную аминокислотную последовательность. "Регуляторная последовательность" относится к нуклеотидной последовательности, расположенной до (например, 5' некодирующая последовательность), в или после (например, 3' некодирующая последовательность) кодирующей последовательности, которая влияет на транскрипцию, процессинг или стабильность РНК, или трансляцию связанной с ней кодирующей последовательности. Регуляторные последовательности включают, например, и без ограничения: промоторы; трансляционные лидерные последовательности; интроны; распознаваемые последовательности полиаденилирования; участки процессинга РНК; участки связывания эффектора и структуры стебель-петля.
При использовании в настоящем описании, термин "полипептид" включает одиночный полипептид, множество полипептидов и их фрагменты. Данный термин относится к молекуле, состоящей из мономеров (аминокислот), линейно связанных амидными связями (также известными как пептидные связи). Термин "полипептид" относится к любой цепи или цепям двух или более аминокислот, и не относится к определенной длине или размеру продукта. Соответственно, пептиды, дипептиды, трипептиды, олигопептиды, белок, аминокислотная цепь и любой другой термин, используемый для указания цепи или цепей двух или более аминокислот, включены в рамки определения "полипептида", при этом предыдущие термины используются в настоящем описании попеременно с "полипептидом". Полипептид может быть выделен из природного биологического источника или получен с помощью рекомбинантной технологии, но при этом определенный полипептид не транслирован обязательно с определенной нуклеиновой кислоты. Полипептид может быть получен любым подходящим образом, включая, например, и без ограничения, химический синтез.
Напротив, термин "гетерологичный" относится к полинуклеотиду, гену или полипептиду, который обычно не находится в его местоположении в соответствующем организме (хозяине). Например, гетерологичная нуклеиновая кислота может быть нуклеиновой кислотой, которая обычно находится в соответствующем организме в другом местоположении в геноме. В качестве дополнительного примера гетерологичная нуклеиновая кислота может быть нуклеиновой кислотой, которая обычно не находится в соответствующем организме. Организм-хозяин, включающий гетерологичный полинуклеотид, ген или полипептид, может быть получен при введении гетерологичного полинуклеотида, гена или полипептида в организм-хозяин. В конкретных примерах гетерологичный полинуклеотид включает нативную кодирующую последовательность или ее часть, которую повторно вводят в исходный организм в форме, отличающейся от соответствующего нативного полинуклеотида. В конкретных примерах гетерологичный ген включает нативную кодирующую последовательность или ее часть, которую повторно вводят в исходный организм в форме, отличающейся от соответствующего нативного гена. Например, гетерологичный ген может включать нативную кодирующую последовательность, которая является частью химерного гена, включающего ненативные регуляторные области, который повторно вводят в нативный организм-хозяин. В конкретных примерах гетерологичный полипептид является нативным полипептидом, который повторно вводят в исходный организм в форме, отличающейся от соответствующего нативного полипептида.
Гетерологичный ген или полипептид могут быть геном или полипептидом, которые включают функциональный полипептид или последовательность нуклеиновой кислоты, кодирующую функциональный полипептид, которые слиты с другим геном или полипептидом с получением химерного полипептида или слитого полипептида, или гена, кодирующего их. Гены и белки согласно конкретным вариантам осуществления включают конкретные представленные примеры полноразмерных последовательностей и частей, сегментов, фрагментов (включающие непрерывные фрагменты и внутренние и/или концевые делеции по сравнению с полноразмерными молекулами), вариантов, мутантов, химерных и слитых последовательностей.
При использовании в настоящем описании, термин "модификация" может относиться к изменению в полинуклеотиде, раскрытом в настоящей заявке, которое приводит к снижению, существенному устранению или исчезновению активности полипептида, кодируемого полинуклеотидом, в также к изменению в полипептиде, раскрытом в настоящей заявке, которое приводит к снижению, существенному устранению или исчезновению активности полипептида. В альтернативе термин "модификация" может относиться к изменению в полинуклеотиде, раскрытом в настоящей заявке, которое приводит к увеличению или повышению активности полипептида, кодируемого полинуклеотидом, а также к изменению в полипептиде, раскрытом в настоящей заявке, которое приводит к увеличению или повышению активности полипептида. Такие изменения могут быть сделаны с помощью способов, известных в уровне техники, в том числе, без ограничения перечисленным, введения делеции, мутации (например, посредством спонтанного мутагенеза, случайного мутагенеза, мутагенеза, вызванного генами-мутаторами, или транспозонного мутагенеза), замены, вставки, посредством даун-регуляции, изменения клеточной локализации, изменения состояния полинуклеотида или полипептида (например, метилирование, фосфорилирование или убиквитинирование), удаления кофактора, введения антисмысловой РНК/ДНК, введения интерферирующей РНК/ДНК, химической модификации, ковалентной модификации, облучения УФ или рентгеновским излучением, гомологичной рекомбинации, митотической рекомбинации, с помощью методов замены промотора и/или комбинации перечисленного.
Термин "производное" при использовании в настоящем описании относится к модификации последовательности, представленной в настоящем описании. Примером таких модификаций будет замена, вставка и/или делеция одного или более оснований, относящихся к последовательности нуклеиновой кислоты, кодирующей последовательности, раскрытые в настоящей заявке, которые сохраняют, немного изменяют или усиливают функцию кодирующей последовательности, раскрытой в настоящей заявке, в видах сельскохозяйственных культур. Такие производные могут быть с легкостью определены специалистом в данной области техники, например, при использовании методик компьютерного моделирования для предсказания и оптимизации структуры последовательности. Термин "производное", таким образом, также включает последовательности нуклеиновой кислоты, обладающие существенной идентичностью последовательности с раскрытыми в настоящей заявке кодирующими последовательностями таким образом, что они способны обладать раскрытой функциональностью для применения в вариантах получения согласно настоящему описанию.
Термин "промотор" относится к последовательности ДНК, способной осуществлять регуляцию экспрессии кодирующей последовательности нуклеиновой кислоты или функциональной РНК. В примерах регулируемая кодирующая последовательность расположена 3' относительно последовательности промотора. Промотор может быть полностью получен из нативного гена, промотор может состоять из различных элементов, полученных из различных промоторов, обнаруживаемых в природе, или промотор может включать даже рационально созданные сегменты ДНК. Специалистам в данной области очевидно, что различные промоторы могут направлять экспрессию гена в различных тканях или типах клеток, или в различных стадиях развития, или в ответ на различные внешние или физиологические условия. Примеры всех предшествующих промоторов известны и используются в уровне техники для регуляции экспрессии гетерологичных нуклеиновых кислот. Промоторы, которые направляют экспрессию гена в большинстве типов клеток в большинстве случаев, обычно называют "конститутивными промоторами". Кроме того, хотя специалисты (во многих случаях неудачно) пытались определить точные границы регуляторных последовательностей, стало очевидно, что фрагменты ДНК различной длины могут обладать идентичной промоторной активностью. Промоторная активность конкретной нуклеиновой кислоты может быть установлена при использовании методик, известных из уровня техники.
Термин "функционально связанный" относится к ассоциации последовательностей нуклеиновых кислот в одной нуклеиновой кислоте, где на функцию одной из последовательностей нуклеиновых кислот влияет другая последовательность. Например, промотор является функционально связанным с кодирующей последовательностью, если промотор способен вызывать экспрессию указанной кодирующей последовательности (например, кодирующая последовательность находится под транскрипционным контролем промотора). Кодирующая последовательность может быть функционально связана с регуляторной последовательностью в смысловой или антисмысловой ориентации.
Термин "экспрессия" при использовании в настоящем описании может относиться к транскрипции и устойчивому накоплению смысловой (мРНК) или антисмысловой РНК, получаемых с ДНК. Экспрессия может также относиться к трансляции мРНК в полипептид. При использовании в настоящем описании, термин "оверэкспрессия" относится к экспрессии, которая является более высокой, чем эндогенная экспрессия того же гена или соответствующего гена. Таким образом, гетерологичный ген "оверэкспрессирован", если его экспрессия является более высокой, чем экспрессия сопоставимого эндогенного гена.
При использовании в настоящем описании, термин "трансформация" или "трансформирующий" относится к переносу и интеграции нуклеиновой кислоты или ее фрагмента в организм-хозяин с получением генетически стабильного наследования. Организмы-хозяева, содержащие трансформирующую нуклеиновую кислоту, именуются как "трансгенные", "рекомбинантные" или "трансформированные" организмы. Известные методы трансформации включают, например: Agrobacterium tumefaciens- или A. rhizogenes-опосредованную трансформацию; трансформацию с фосфатом кальция; трансформацию с полибреном; слияние протопластов; электропорацию; ультразвуковые методы (например, сонопорацию); липосомную трансформацию; микроинъекцию; трансформацию голой ДНК; трансформацию плазмидными векторами; трансформацию вирусными векторами; биолистическую трансформацию (бомбардировку микрочастицами); трансформацию, опосредованную нитями карбида кремния; трансформацию аэрозольным пучком и ПЭГ-опосредованную трансформацию.
При использовании в настоящем описании, термин "введенный" (в отношении введения нуклеиновой кислоты в клетку) включает трансформацию клетки, а также скрещивание растения, включающего нуклеиновую кислоту, со вторым растением, причем второе растение содержит нуклеиновую кислоту, что может быть выполнено при использовании стандартных методик селекции растений. Такие методики селекции известны в уровне техники. По поводу обсуждения методик селекции растения см. Poehlman (1995) Breeding Field Crops, 4th Edition, AVI Publication Co., Westport CT.
Методы обратного скрещивания могут использоваться для введения нуклеиновой кислоты в растение. Данную методику использовали в течение многих десятилетий для введения признаков в растения. Пример описания обратного скрещивания (и другие методики селекции растений) можно найти, например, в Poelman (1995), выше; и Jensen (1988) Plant Breeding Methodology, Wiley, New York, NY. В примерной методике обратного скрещивания исходное целевое растение ("рекуррентный родитель") скрещивают со вторым растением ("нерекуррентным родителем"), несущим нуклеиновую кислоту, которую требуется ввести. Полученное в результате этого скрещивания потомство затем снова скрещивают с рекуррентным родителем и повторяют процесс до тех пор, пока не будет получено измененное растение, в котором присутствуют по существу все требуемые морфологические и физиологические признаки рекуррентного родителя в дополнение к нуклеиновой кислоте из нерекуррентного родителя.
"Связывание" относится к сиквенс-специфическому, нековалентному взаимодействию между макромолекулами (например, между белком и нуклеиновой кислотой). Не все компоненты связывающего взаимодействия должны быть сиквенс-специфическими (например, контакты с фосфатными остатками в цепи ДНК) при условии, что взаимодействие в целом является сиквенс-специфическим. Такие взаимодействия обычно характеризуются константой диссоциации (Kd) 10-6 М-1 или ниже. "Аффинность" относится к силе связывания: повышение аффинности связывания согласуется с понижением Kd.
"Связывающий белок" является белком, который способен нековалентно связываться с другой молекулой. Связывающий белок может связываться, например, с молекулой ДНК (ДНК-связывающий белок), молекулой РНК (РНК-связывающий белок) и/или молекулой белка (белок-связывающий белок). В случае белок-связывающего белка он может связываться сам с собой (с образованием гомодимеров, гомотримеров и т.д.), и/или он может связываться с одной или более молекулами другого белка или белков. Связывающий белок может иметь больше одного типа связывающей активности. Например, цинк-пальцевые белки обладают ДНК-связывающей, РНК-связывающей и белок-связывающей активностью.
"Рекомбинация" относится к процессу обмена генетической информацией между двумя полинуклеотидами, включающему, без ограничения перечисленным, донорный захват при негомологичном соединении концов (NHEJ) и гомологичную рекомбинацию. В рамках настоящего описания, "гомологичная рекомбинация (ГР)" относится к специализированной форме такого обмена, который происходит, например, во время репарации двухцепочечных разрывов в клетках, осуществляемой посредством направленных гомологией механизмов репарации. Этот процесс требует гомологии нуклеотидной последовательности, использует "донорную" молекулу для матричной репарации молекулы "мишени" (то есть молекулы, в которой образовался двухцепочечный разрыв) и известен под разными названиями, такими как "некроссоверная конверсия генов" или "конверсия генов на коротких участках", поскольку он приводит к переносу генетической информации от донора к мишени. Без желания быть связанными какой-либо конкретной теорией, предполагают, что такой перенос может включать коррекцию неспаренных оснований гетеродуплекса ДНК, который образуется между расщепленной мишенью и донором, и/или "синтез-зависимый отжиг цепей", в котором донор используется для восстановления генетической информации, которая становится частью мишени, и/или подобные процессы. Такая специализированная ГР часто приводит к изменению последовательности молекулы-мишени, в результате чего часть или вся последовательность донорного полинуклеотида встраивается в целевой полинуклеотид. В отношении ГР-направленной интеграции, донорная молекула содержит по меньшей мере одну область гомологии с геномом ("плечи гомологии") длиной по меньшей мере 50-100 пар оснований. См., например, патентную публикацию США 20110281361.
В способах настоящего описания одна или более направленных нуклеаз, как описано в настоящей заявке, создают двухцепочечный разрыв в целевой последовательности (например, клеточный хроматин) на заданном участке, при этом "донорный" полинуклеотид, обладающий гомологией с нуклеотидной последовательностью в области разрыва, может быть введен в клетку. Присутствие двухцепочечного разрыва, как было показано, способствует интеграции донорной последовательности. Донорная последовательность может быть интегрирована физически или, в альтернативе, донорный полинуклеотид используется в качестве матрицы для репарации разрыва посредством гомологичной рекомбинации, что приводит к введению полной или части нуклеотидной последовательности, как в доноре, в клеточный хроматин. Таким образом, первая последовательность в клеточном хроматине может быть изменена и, в некоторых вариантах осуществления, может быть превращена в последовательность, присутствующую в донорном полинуклеотиде. Таким образом, использование терминов "заменяет" или "замена", как можно понимать, представляет замену одной нуклеотидной последовательности другой (то есть замену последовательности в информационном смысле) и не требует обязательно физической или химической замены одного полинуклеотида другим.
"Расщепление" относится к разрыву ковалентной цепи молекулы ДНК. Расщепление можно инициировать множеством способов, включающих, без ограничения перечисленным, ферментативный или химический гидролиз фосфодиэфирной связи. Возможно как одноцепочечное расщепление, так и двухцепочечное расщепление, причем двухцепочечное расщепление может происходить в результате двух отдельных событий одноцепочечного расщепления. Расщепление ДНК может приводить к образованию тупых концов или липких концов. В некоторых вариантах осуществления для направленного двухцепочечного расщепления ДНК используют слитые полипептиды.
Термины "плазмида" и "вектор", при использовании в настоящем описании, относятся к внехромосомному элементу, который может нести один или более генов, которые не являются частью центрального метаболизма клетки. Плазмиды и векторы обычно представляют собой кольцевые двухцепочечные молекулы ДНК. Впрочем, плазмиды и векторы могут быть линейными или кольцевыми нуклеиновыми кислотами, одно- или двухцепочечными ДНК или РНК, и могут нести ДНК, полученную по существу из любого источника, в которых множество нуклеотидных последовательностей были соединены или рекомбинированы в уникальную конструкцию, которая обеспечивает введение промоторного фрагмента и кодирующей последовательности ДНК вместе с любыми соответствующими 3' нетранслируемыми последовательностями в клетку. В примерах плазмиды и векторы могут включать автономно реплицирующиеся последовательности для размножения в бактериях-хозяевах.
Полипептид и "белок" используются попеременно в настоящем описании и включают молекулярную цепь из двух или более аминокислот, связанных через пептидные связи. Данные термины не относятся к определенной длине продукта. Таким образом, "пептиды" и "олигопептиды" включены в рамки определения полипептида. Данные термины включают посттрансляционные модификации полипептида, например, гликозилирования, ацетилирования, фосфорилирования и т.п. Кроме того, фрагменты белков, аналоги белков, мутированные белки или варианты белков, слитые белки и т.п. включены в рамки значения полипептида. Данные термины также включают молекулы, в которые включены один или более аналогов аминокислот или неканонические или неприродные аминокислоты, которые могут быть синтезированы или экспрессированы рекомбинантно с использованием известных методик инженерии белков. Кроме того, слитые белки согласно изобретению могут быть дериватизированы, как описано в настоящей заявке, с помощью известных методик органической химии.
Термин "слитый белок" указывает, что белок включает полипептидные компоненты, полученные больше чем из одного исходного белка или полипептида. Как правило, слитый белок экспрессируется со слитого гена, в котором нуклеотидная последовательность, кодирующая последовательность полипептида из одного белка, соединена в рамке считывания с, и необязательно отделена линкером от, нуклеотидной последовательности, кодирующей последовательность полипептида из другого белка. Слитый ген может быть затем экспрессирован рекомбинантной клеткой-хозяином в виде одного белка.
III. Варианты осуществления настоящего изобретения
В варианте осуществления описание относится к анализу для обнаружения сайт-специфической интеграции донорной полинуклеотидной последовательности в целевой участок генома.
В некоторых вариантах осуществления геномную ДНК анализируют с целью обнаружения сайт-специфической интеграции донорной полинуклеотидной последовательности в целевой участок генома. В аспектах варианта осуществления геномная ДНК включает: хромосомную геномную ДНК, митохондриальную геномную ДНК, геномную ДНК мобильного элемента, геномную ДНК, полученную в результате интеграции вируса, геномную ДНК искусственной хромосомы (см. PCT/US2002/017451 и PCT/US2008/056993, включенные в настоящее описание в качестве неограничивающих примеров) и другие источники геномной ДНК.
В некоторых вариантах осуществления геномную ДНК амплифицируют с помощью полимеразной цепной реакции (ПЦР). В аспектах варианта осуществления ПЦР обычно относится к методу увеличения концентрации сегмента целевой последовательности в смеси геномной ДНК без клонирования или очистки (патенты США 4,683,195; 4,683,202 и 4,965,188; включенные в настоящую заявку посредством отсылки). Этот процесс амплификации целевой последовательности включает введение избытка двух олигонуклеотидных праймеров в смесь ДНК, содержащую требуемую целевую последовательность, с последующим выполнением точной последовательности тепловых циклов в присутствии ДНК-полимеразы. Два праймера комплементарны их соответствующим цепям двухцепочечной целевой последовательности. Для выполнения амплификации смесь денатурируется и затем праймеры отжигаются на их комплементарных последовательностях в целевой молекуле. После отжига праймеры достраиваются полимеразой с образованием новой пары комплементарных цепей. Стадии денатурации, отжига праймера и достройки полимеразой могут быть повторены много раз (то есть денатурация, отжиг и достройка составляют один "цикл"; может быть многожество "циклов") для получения высокой концентрации амплифицированного сегмента требуемой целевой последовательности. Длина амплифицированного сегмента требуемой целевой последовательности определяется относительными положениями праймеров по отношению друг к другу и поэтому является регулируемым параметром. В силу повторяющегося аспекта процесса способ называют "полимеразной цепной реакцией" (в дальнейшем "ПЦР"). Поскольку требуемые амплифицированные сегменты целевой последовательности становятся преобладающими последовательностями (в выражении концентрации) в смеси, они называются "ПЦР амплифицированными".
В других вариантах осуществления реакция ПЦР дает ампликон. В качестве аспекта варианта осуществления ампликон относится к продукту реакции амплификации, полученному в результате достройки одного или обоих из пары амплификационных праймеров. Ампликон может содержать экспоненциально амплифицированные нуклеиновые кислоты, если оба используемых праймера гибридизуются с целевой последовательностью. В альтернативе ампликоны могут быть получены в результате линейной амплификации, если один из используемых праймеров не гибридизуется с целевой последовательностью. Таким образом, данный термин используется в настоящем описании в общем смысле и не подразумевает обязательно присутствие экспоненциально амплифицированных нуклеиновых кислот.
Амплификация выбранной или целевой последовательности нуклеиновой кислоты может быть выполнена любым подходящим методом. См. в общем Kwoh et al., Am. Biotechnol. Lab. 8, 14-25 (1990). Примеры подходящих методик амплификации включают, без ограничения перечисленным, полимеразную цепную реакцию, лигазную цепную реакцию, амплификацию с вытеснением цепи (см. в общем Г. G. Walker et al., Proc. Natl. Acad. Sci. USA 89, 392-396 (1992); G. Walker et al., Nucleic Acids Res. 20, 1691-1696 (1992)), транскрипционную амплификацию (см. D. Kwoh et al., Proc. Natl. Acad Sci. USA 86, 1173-1177 (1989)), самоподдерживающуюся репликацию последовательностей (или "3SR") (см. J. Guatelli et al., Proc. Natl. Acad. Sci. USA 87, 1874-1878 (1990)), Qβ-репликазную систему (см. P. Lizardi et al., BioTechnology 6, 1197-1202 (1988)), амплификацию на основе последовательности нуклеиновых кислот (или "NASBA") (см. R. Lewis, Genetic Engineering News 12 (9), 1 (1992)), репаративную цепную реакцию (или "RCR") (см. R. Lewis, выше) и амплификацию ДНК методом бумеранга (или "BDA") (см. R. Lewis, выше). Полимеразная цепная реакция обычно является предпочтительной.
В другом варианте осуществления амплификацию геномной ДНК проводят с помощью реакции ПЦР при использовании праймеров. В аспекте варианта осуществления праймеры могут включать первый набор праймеров, второй набор праймеров, третий набор праймеров и т.д. Таким образом, обозначение "первый", "второй", "третий" и т.д. указывает порядок, в котором наборы праймеров используются в реакции гнездовой ПЦР. Например, "первый" набор праймеров используется первоначально в первой реакции ПЦР для амплификации полинуклеотидной последовательности. Затем "второй" набор праймеров используется во второй реакции ПЦР для амплификации продукта первой реакции ПЦР. Затем "третий" набор праймеров используется в третьей реакции ПЦР для амплификации продукта второй реакции ПЦР и т.д. В других аспектах варианта осуществления праймеры могут быть внешним праймером, который предназначен для связывания целевого участка геномной ДНК, или внутренним праймером, который предназначен для связывания донорной полинуклеотидной последовательности, которая интегрирована в геном организма. В других вариантах осуществления первый набор праймеров может состоять из внутреннего и внешнего праймера, или может включать два разных внешних праймера или два разных внутренних праймера. В варианте осуществления термин праймер относится к олигонуклеотиду, который комплементарен ДНК матрице, амплифицируемой в подходящем амплификационном буфере. В определенном варианте осуществления праймеры могут иметь длину от 10 пн до 100 пн, от 10 пн до 50 пн или от 10 пн до 25 пн.
В варианте осуществления настоящего описания внутренний праймер представлен в более низкой концентрации, чем внешний праймер. Аспект варианта осуществления включает относительную концентрацию внешнего праймера к внутреннему праймеру приблизительно 10:1, 9:1, 8:1, 7:1, 6:1, 5:1, 4:1, 3:1 или 2:1. В другом аспекте вариант осуществления включает концентрацию внутреннего праймера 0,001, 0,005, 0,01, 0,02, 0,03, 0,04, 0,05, 0,06, 0,07, 0,008 или 0,09 мкМ и концентрацию внешнего праймера по меньшей мере 0,1 мкМ. В другом аспекте вариант осуществления включает концентрацию внутреннего праймера 0,01, 0,02, 0,03, 0,04, 0,05, 0,06, 0,07, 0,08, 0,09, 0,1, 0,11 0,12, 0,13, 0,14, 0,15, 0,16, 0,17, 0,18 или 0,19 мкМ и концентрацию внешнего праймера по меньшей мере 0,2 мкМ.
В некоторых вариантах осуществления участок геномной интеграции является геномной ДНК растения. В одном из аспектов растительные клетки, которые трансформируют в соответствии с настоящим описанием, включают, без ограничения перечисленным, любые высшие растения, в том числе двудольные и однодольные растения, и в особенности пригодные к употреблению пищу растения, включая сельскохозяйственные культуры. Такие растения могут включать, без ограничения перечисленными, например: люцерну, сою, хлопок, рапс (также описываемый как канола), лен, кукурузу, рис, ветвянку, пшеницу, сафлоровые, сорго, сахарную свеклу, подсолнечники, табак и газонные травы. Таким образом, могут быть выбраны любые виды растений или растительная клетка. В вариантах осуществления растительные клетки, используемые в настоящей заявке, и растения, выращенные или полученные из них, включают, без ограничения перечисленными, клетки, получаемые из рапса (Brassica napus); горчицы сарептской (Brassica juncea); горчицы абиссинской (Brassica carinata); репы (Brassica rapa); капусты огородной (Brassica oleracea); сои (Glycine max); льна обыкновенного (Linum usitatissimum); кукурузы сахарной (также описываемой как кукуруза) (Zea mays); сафлора (Carthamus tinctorius); подсолнечника (Helianthus annuus); табака (Nicotiana tabacum); Arabidopsis thaliana; бразильского ореха (Bertholettia excelsa); клещевины (Ricinus communis); кокосовой пальмы (Cocus nucifera); кориандра (Coriandrum sativum); хлопчатника (Gossypium spp.); арахиса (Arachis hypogaea); жожоба (Simmondsia chinensis); масличной пальмы (Elaeis guineensis); оливы европейской (Olea europaea); риса (Oryza sativa); тыквы гигантской (Cucurbita maxima); ячменя (Hordeum vulgare); сахарного тростника (Saccharum officinarum); риса (Oryza sativa); пшеницы (Triticum spp. включая Triticum durum и Triticum aestivum); и ряски (Lemnaceae sp.). В некоторых вариантах осуществления генетический фон в пределах видов растений может изменяться.
В отношении получения генетически модифицированных растений, в уровне техники известны методы генной инженерии растений. Например, были разработаны многочисленные методы трансформации растений, включая методики биологической и физической трансформации двудольных растений, а также однодольных растений (например, Goto-Fumiyuki et al., Nature Biotech 17:282-286 (1999); Miki et al., Methods in Plant Molecular Biology and Biotechnology, Glick, B. R. and Thompson, J. E. Eds., CRC Press, Inc., Boca Raton, pp. 67-88 (1993)). Кроме того, векторы и методы in vitro культивирования растительных клеток или трансформации ткани и регенерации растений доступны, например, в Gruber et al., Methods in Plant Molecular Biology and Biotechnology, Glick, B. R. and Thompson, J. E. Eds., CRC Press, Inc., Boca Raton, pp. 89-119 (1993).
Большое количество методик доступно для введения ДНК в растительную клетку-хозяина. Такие методики включают трансформацию обезоруженной T-ДНК с использованием Agrobacterium tumefaciens или Agrobacterium rhizogenes в качестве трансформирующего агента, трансфекцию с фосфатом кальция, трансформацию с полибреном, слияние протопластов, электропорацию, ультразвуковые методы (например, сонопорацию), липосомную трансформацию, микроинъекцию, голую ДНК, плазмидные векторы, вирусные векторы, биолистику (бомбардировку микрочастицами), трансформацию, опосредованную нитями карбида кремния, аэрозольным пучком или ПЭГ, а также другие возможные методы.
Например, конструкция ДНК может быть введена непосредственно в геномную ДНК растительной клетки при использовании таких методик, как электропорация и микроинъекция протопластов растительных клеток, или конструкции ДНК могут быть введены непосредственно в растительную ткань при использовании биолистических методов, таких как бомбардировка частицами с ДНК (см., например, Klein et al. (1987) Nature 327:70-73). Дополнительные методы трансформации растительной клетки включают микроинъекцию с захватом ДНК, опосредуемым нитями карбида кремния (Kaeppler et al. (1990) Plant Cell Reporter 9:415-418). В альтернативе конструкция ДНК может быть введена в растительную клетку с помощью трансформации наночастицами (см., например, заявку на патент США 12/245,685, которая полностью включена в настоящую заявку посредством отсылки).
Другим известным методом трансформации растений является трансформация, опосредованная ускоренными микрочастицами, где ДНК нанесена на поверхность микрочастиц. В этом методе вектор вводят в растительные ткани при помощи биолистического устройства, которое ускоряет микрочастицы до скорости, достаточной для проникновения через стенки и мембраны растительной клетки. Sanford et al., Part. Sci. Technol. 5:27 (1987), Sanford, J. C., Trends Biotech. 6:299 (1988), Sanford, J. C., Physiol. Plant 79:206 (1990), Klein et al., Biotechnology 10:268 (1992).
В альтернативе перенос генов и методы трансформации включают, без ограничения перечисленным, трансформацию протопластов посредством осаждения хлоридом кальция, опосредованный полиэтиленгликолем (ПЭГ) или электропорацией захват голой ДНК (см. Paszkowski et al. (1984) EMBO J 3:2717-2722, Potrykus et al. (1985) Molec. Gen. Genet. 199:169-177; Fromm et al. (1985) Proc. Nat. Acad. Sci. USA 82:5824-5828; и Shimamoto (1989) Nature 338:274-276) и электропорацию растительных тканей (D'Halluin et al. (1992) Plant Cell 4:1495-1505).
Широко применяемый метод введения вектора экспрессии в растения основан на природной системе трансформации агробактерии (Horsch et al., Science 227:1229 (1985)). A. tumefaciens и A. rhizogenes являются фитопатогенными почвенными бактериями, которые, как известно, применяются для генетической трансформации растительных клеток. Ti и Ri плазмиды A. tumefaciens и A. rhizogenes, соответственно, несут гены, ответственные за генетическую трансформацию растения (Kado, C. I., Crit. Rev. Plant. Sci. 10:1 (1991)). Описания агробактериальных векторных систем и методов опосредованного агробактерией переноса генов также можно найти, например, в Gruber et al., выше, Miki et al., выше, Moloney et al., Plant Cell Reports 8:238 (1989), а также в патентах США 4,940,838 и 5,464,763.
При использовании агробактерии для трансформации, вводимую ДНК нужно клонировать в специальные плазмиды, а именно либо в промежуточный вектор, либо в бинарный вектор. Промежуточные векторы не могут реплицироваться в агробактерии. Промежуточный вектор можно перенести в Agrobacterium tumefaciens при помощи хелперной плазмиды (конъюгации). Супербинарная система Japan Tobacco является примером такой системы (см. обзор Komari et al., (2006) в Methods in Molecular Biology (K. Wang, ed.) No. 343: Agrobacterium Protocols (2nd Edition, Vol. 1) Humana Press Inc., Totowa, NJ, стр. 15-41; и Komori et al., (2007) Plant Physiol. 145:1155-1160). Бинарные векторы могут реплицироваться и в E. coli, и в агробактерии. Они включают маркерный селективный ген и линкер или полилинкер, которые фланкированы правой и левой бордерными областями T-ДНК. Они могут быть трансформированы непосредственно в агробактерию (Holsters, 1978). Агробактерия, используемая в качестве клетки-хозяина, должна включать плазмиду, несущую vir-область. Ti или Ri плазмида также включают vir-область, необходимую для переноса T-ДНК. vir область необходима для переноса T-ДНК в растительную клетку. Может содержаться дополнительная T-ДНК.
Вирулентные функции хозяйской Agrobacterium tumefaciens будут направлять вставку T-цепи, содержащей конструкцию и сопряженный маркер, в ДНК растительной клетки при заражении клетки бактериями с использованием методик с бинарным T-ДНК вектором (Bevan (1984) Nuc. Acid Res. 12:8711-8721) или небинарным T-ДНК вектором (Horsch et al. (1985) Science 227:1229-1231). Как правило, система агробактериальной трансформации используется в инженерии двудольных растений (Bevan et al. (1982) Ann. Rev. Genet 16:357-384; Rogers et al. (1986) Methods Enzymol. 118:627-641). Система агробактериальной трансформации может также использоваться для трансформации, а также переноса ДНК в однодольные растения и растительные клетки. См. патент США 5,591,616; Hernalsteen et al. (1984) EMBO J 3:3039-3041; Hooykass-Van Slogteren et al. (1984) Nature 311:763-764; Grimsley et al. (1987) Nature 325:1677-179; Boulton et al. (1989) Plant Mol. Biol. 12:31-40; и Gould et al. (1991) Plant Physiol. 95:426-434. После введения генетической конструкции в специфические растительные клетки растительные клетки можно выращивать и после появления дифференцирующейся ткани, такой как побеги и корни, могут быть получены зрелые растения. В некоторых вариантах осуществления может быть получено множество растений. Методики регенерации растений известны средним специалистам в данной области и могут быть найдены, например, в Plant Cell and Tissue Culture, 1994, Vasil and Thorpe Eds. Kluwer Academic Publishers, и в Plant Cell Culture Protocols (Methods in Molecular Biology 111, 1999 Hall Eds Humana Press). Генетически модифицированное растение, описанное в настоящей заявке, можно культивировать в питательной среде или выращивать в подходящей среде, такой как почва. В некоторых вариантах осуществления подходящая среда для выращивания высших растений может включать любую среду для выращивания растений, в том числе, без ограничения перечисленным, почву, песок, любые другие дисперсные среды, которые поддерживают рост корней (например, вермикулит, перлит и т.д.), или гидропонную культуру, а также подходящее освещение, воду и питательные добавки, которые оптимизируют рост высшего растения.
Трансформированные растительные клетки, которые получены с помощью любой из вышеуказанных методик трансформации, можно культивировать с регенерацией целого растения, которое обладает трансформированным генотипом и, таким образом, требуемым фенотипом. Такие методики регенерации основаны на манипуляции некоторыми фитогормонами в среде для выращивания культур тканей, которые обычно основаны на применении биоцидного и/или гербицидного маркера, который был введен вместе с нужными нуклеотидными последовательностями. Регенерация растения из культивируемых протопластов описана в Evans, et al., "Protoplasts Isolation and Culture" в Handbook of Plant Cell Culture, стр. 124-176, Macmillian Publishing Company, New York, 1983; и Binding, Regeneration of Plants, Plant Protoplasts, стр. 21-73, CRC Press, Boca Raton, 1985. Регенерация также может быть получена из растительного каллуса, эксплантатов, органов, пыльцы, зародышей или их частей. Такие методики регенерации описаны в общем виде в Klee et al. (1987) Ann. Rev. of Plant Phys. 38:467-486.
В других вариантах осуществления растительные клетки, которые трансформированы, не способны к регенерации с получением растения. Такие клетки называют транзиентно трансформированными. Транзиентно трансформированные клетки могут быть получены для анализа экспрессии и/или функциональности определенного трансгена. Методики транзиентной трансформации известны в уровне техники и включают незначительные модификации в методиках трансформации, описанных выше. Специалисты в данной области техники могут выбрать применение транзиентной трансформации для быстрого анализа экспрессии и/или функциональности определенных трансгенов, поскольку транзиентная трансформация выполняется быстро и не требует так много ресурсов (например, культивирование растений для развития целых растений, самоопыления или скрещивания растений для фиксации трансгена в геноме и т.д.), как методики стабильной трансформации.
В варианте осуществления донорный полинуклеотид может быть введен по существу в любое растение. Большое разнообразие растений и систем растительных клеток может быть создано для сайт-специфической интеграции донорного полинуклеотида согласно настоящему описанию и различных методов трансформации, указанных выше. В варианте осуществления целевые растения и растительные клетки для конструирования включают, без ограничения перечисленными, однодольные и двудольные растения, такие как сельскохозяйственные культуры, в том числе зерновые культуры (например, пшеницу, кукурузу, рис, просо, ячмень), плодовые культуры (например, томат, яблоко, грушу, землянику, апельсин), кормовые культуры (например, люцерну), корневые растительные культуры (например, морковь, картофель, сахарные свеклы, ямс), листовые растительные культуры (например, салат, шпинат); цветковые растения (например, петунию, розу, хризантему), хвойные растения и сосны (например, сосну, ель); растения, используемые в фиторемедиации (например, растения, накапливающие тяжелые металлы); масличные культуры (например, подсолнечник, рапс) и растения, используемые в экспериментальных целях (например, резуховидку).
В других вариантах осуществления донорные полинуклеотидные последовательности вводят в растительную клетку для сайт-специфического таргетинга в целевой участок генома. В таких вариантах осуществления растительная клетка может быть протопластом растительной клетки. Протопласты могут быть получены из различных типов растительных клеток. Соответственно, средние специалисты в данной области техники могут использовать различные технологии или методики для получения протопласта растительной клетки. Например, создание и получение протопластов описано в: Green and Phillips, Crop Sc., 15 (1975) 417-421; Harms et al. Z. Pflanzenzuechtg., 77 (1976) 347-351; европейских патентах EP-0,160,390, Lowe and Smith (1985); EP-0,176,162, Cheng (1985); и EP-0,177,738, Close (1985); Cell Genetics in Higher Plants, Dudits et al., (eds), Akademiai Kiado, Budapest (1976) 129-140, а также в приведенных в них ссылках; Harms, "Maize and Cereal Protoplasts-Facts and Perspectives", Maize for Biological Research, W. F. Sheridan, ed. (1982); Dale, в: Protoplasts (1983); Potrykus et al (eds.) Lecture Proceedings, Experientia Supplementum 46, Potrykus et al., eds, Birkhauser, Basel (1983) 31-41, а также в приведенных в них ссылках. Регенерация растения из культивируемых протопластов описана в Evans et al. (1983) "Protoplast Isolation and Culture", Handbook of Plant Cell Cultures 1, 124-176 (MacMillan Publishing Co., New York; Davey (1983) "Recent Developments in the Culture and Regeneration of Plant Protoplasts", Protoplasts, стр. 12-29, (Birkhauser, Basel); Dale (1983) "Protoplast Culture and Plant Regeneration of Cereals and Other Recalcitrant Crops", Protoplasts, стр. 31-41, (Birkhauser, Basel); Binding (1985) "Regeneration of Plants," Plant Protoplasts, стр. 21-73, (CRC Press, Boca Raton, FL).
Выбор целевых участков; белки ZFP и способы создания и конструирования слитых белков (и полинуклеотидов, кодирующих их) известны специалистам в данной области и подробно описаны в патентах США 6,140,081; 5,789,538; 6,453,242; 6,534,261; 5,925,523; 6,007,988; 6,013,453; 6,200,759; WO 95/19431; WO 96/06166; WO 98/53057; WO 98/54311; WO 00/27878; WO 01/60970 WO 01/88197; WO 02/099084; WO 98/53058; WO 98/53059; WO 98/53060; WO 02/016536 и WO 03/016496.
В последующих вариантах осуществления ДНК-связывающий домен, включающий одну или более ДНК-связывающих последовательностей, связывается цинк-пальцевым связывающим белком, связывающим белком мегануклеазой, CRIPSR или TALEN связывающим белком.
В некоторых вариантах осуществления в композиции и способах, описанных в настоящей заявке, используется связывающий белок мегануклеаза (хоуминг-эндонуклеаза) или ДНК-связывающий домен мегануклеазы для связывания с донорной молекулой и/или связывания с целевой областью в геноме клетки. Природные мегануклеазы распознают участки расщепления длиной 15-40 пар оснований и обычно подразделяются на четыре семейства: семейство LAGLIDADG, семейство GIY-YIG, семейство His-Cyst бокса и семейство HNH. Примеры хоуминг-эндонуклеаз включают I-SceI, I-CeuI, PI-PspI, PI-Sce, I-SceIV, I-CsmI, I-PanI, I-SceII, I-PpoI, I-SceIII, I-CreI, I-TevI, I-TevII и I-TevIII. Распознаваемые ими последовательности известны. См. также патент США 5,420,032; патент США 6,833,252; Belfort et al. (1997) Nucleic Acids Res. 25:3379-3388; Dujon et al. (1989) Gene 82:115-118; Perler et al. (1994) Nucleic Acids Res. 22, 1125-1127; Jasin (1996) Trends Genet. 12:224-228; Gimble et al. (1996) J. Mol. Biol. 263:163-180; Argast et al. (1998) J. Mol. Biol. 280:345-353 и каталог New England Biolabs.
В некоторых вариантах осуществления в способах и композициях, описанных в настоящей заявке, используется нуклеаза, которая включает сконструированную (неприродную) хоуминг-эндонуклеазу (мегануклеазу). Распознаваемые последовательности хоуминг-эндонуклеаз и мегануклеаз, таких как I-SceI, I-CeuI, PI-PspI, PI-Sce, I-SceIV, I-CsmI, I-PanI, I-SceII, I-PpoI, I-SceIII, I-CreI, I-TevI, I-TevII и I-TevIII, известны. См. также патент США 5,420,032; патент США 6,833,252; Belfort et al. (1997) Nucleic Acids Res. 25:3379-3388; Dujon et al. (1989) Gene 82:115-118; Perler et al. (1994) Nucleic Acids Res. 22, 1125-1127; Jasin (1996) Trends Genet. 12:224-228; Gimble et al. (1996) J. Mol. Biol. 263:163-180; Argast et al. (1998) J. Mol. Biol. 280:345-353 и каталог New England Biolabs. Кроме того, специфичность связывания ДНК хоуминг-эндонуклеаз и мегануклеаз может быть изменена с помощью генной инженерии для связывания неприродных целевых участков. См., например, Chevalier et al. (2002) Molec. Cell 10:895-905; Epinat et al. (2003) Nucleic Acids Res. 31:2952-2962; Ashworth et al. (2006) Nature 441:656-659; Paques et al. (2007) Current Gene Therapy 7:49-66; патентная публикация США 20070117128. ДНК-связывающие домены хоуминг-эндонуклеаз и мегануклеаз могут быть изменены в контексте нуклеазы в целом (то есть таким образом, чтобы нуклеаза включала родственный расщепляющий домен).
В других вариантах осуществления ДНК-связывающий домен одной или более нуклеаз, используемых в способах и композициях, описанных в настоящей заявке, включает природный или сконструированный (неприродный) ДНК-связывающий домен TAL эффектора. См., например, патентную публикацию США 20110301073, полностью включенную в настоящую заявку посредством отсылки. Фитопатогенные бактерии рода Xanthomonas, как известно, вызывают множество болезней важных сельскохозяйственных растений. Патогенность Xanthomonas зависит от системы секреции консервативного типа III (T3S), которая вводит более 25 различных эффекторных белков в растительную клетку. Среди этих вводимых белков присутствуют подобные активаторам транскрипции эффекторы (TAL), которые имитируют активаторы транскрипции растения и управляют транскриптомом растения (см. Kay et al (2007) Science 318:648-651). Эти белки содержат ДНК-связывающий домен и домен активации транскрипции. Одним из наиболее хорошо описанных TAL-эффекторов является AvrBs3 из Xanthomonas campestgris pv. Vesicatoria (см. Bonas et al (1989) Mol Gen Genet 218: 127-136 и WO2010079430). TAL-эффекторы содержат централизованный домен тандемных повторов, каждый повтор содержит приблизительно 34 аминокислоты, которые являются ключевыми для ДНК-связывающей специфичности этих белков. Кроме того, они содержат последовательность ядерной локализации и кислотный домен активации транскрипции (см. обзор Schornack S, et al (2006) J Plant Physiol 163(3): 256-272). Кроме того, в фитопатогенных бактериях Ralstonia solanacearum были обнаружены два гена, обозначенные brg11 и hpx17, которые гомологичны семейству AvrBs3 Xanthomonas, в штамме GMI1000 биовар 1 и в штамме RS1000 биовар 4 R. solanacearum (см. Heuer et al (2007) Appl and Envir Micro 73(13): 4379-4384). Эти гены на 98,9% идентичны по нуклеотидной последовательности друг другу, но отличаются делецией 1575 пн в домене повторов hpx17. Однако оба продукта генов обладают менее чем 40% идентичностью последовательности с белками семейства AvrBs3 Xanthomonas. См., например, патентные публикации США 20110239315, 20110145940 и 20110301073, полностью включенные в настоящую заявку посредством отсылки.
Специфичность указанных TAL-эффекторов зависит от последовательностей, обнаруженных в тандемных повторах. Повторяющаяся последовательность содержит приблизительно 102 пн, при этом повторы обычно на 91-100% гомологичны друг другу (Bonas et al, там же). Полиморфизм повторов обычно расположен в положениях 12 и 13 и, по-видимому, имеется однозначное соответствие между идентичностью гипервариабельных динуклеотидов в положениях 12 и 13 с идентичностью смежных нуклеотидов в целевой последовательности TAL-эффектора (см. Moscou and Bogdanove, (2009) Science 326:1501 и Boch et al (2009) Science 326:1509-1512). Экспериментально был определен природный код для распознавания ДНК этих TAL-эффекторов, а именно последовательность HD в положениях 12 и 13 приводит к связыванию с цитозином (C), NG связывается с T, NI - с A, C, G или T, NN связывается с A или G, и ING связывается с T. Эти ДНК-связывающие повторы были собраны в белки с новыми комбинациями и числом повторов, в результате чего были получены искусственные факторы транскрипции, которые способны взаимодействовать с новыми последовательностями и активировать экспрессию неэндогенного репортерного гена в растительных клетках (Boch et al, там же). Сконструированные TAL-белки были связаны с расщепленной FokI половиной домена с получением слитой нуклеазы с TAL-эффекторным доменом (TALEN), которая проявляет активность в анализе дрожжей по репортеру (мишень на основе плазмиды). См., например, патентную публикацию США 20110301073; Christian et al ((2010) Genetics epub 10.1534/genetics.110.120717).
В других вариантах осуществления нуклеаза представляет собой систему, включающую CRISPR (кластерные, разделенные регулярными интервалами, короткие палиндромные повторы)/Cas (CRISPR ассоциированную) нуклеазную систему. CRISPR/Cas является недавно сконструированной нуклеазной системой, основанной на бактериальной системе, которая может применяться в геномной инженерии. Она основана на компоненте адаптивного иммунного ответа многих бактерий и археев. При приникновении вируса или плазмиды в бактерию, сегменты чужеродной ДНК превращаются в CRISPR РНК (crРНК) под воздействием 'иммунного' ответа. Такая crРНК затем связывается через область частичной комплементарности с другим типом РНК, называемой tracrРНК, которая направляет Cas9 нуклеазу к области, гомологичной crРНК, в ДНК-мишени рядом с примыкающим к протоспейсеру мотивом (PAM) NGG. Cas9 расщепляет ДНК с образованием тупых концов в разрывах двухцепочечной ДНК (DSB) по сайтам, обозначенным 20-нуклеотидной направляющей последовательностью, содержащейся в crРНК транскрипте. Для сайт-специфического распознавания и расщепления ДНК Cas9 требуется crРНК и tracrРНК. Эту систему недавно сконструировали таким образом, чтобы crРНК и tracrРНК могли быть объединены в одну молекулу ("одиночная направляющая РНК"), при этом эквивалентная crРНК часть одиночной направляющей РНК может быть сконструирована так, чтобы направлять нуклеазу Cas9 для направленного воздействия на любую требуемую последовательность, примыкающую к PAM (см. Jinek et al (2012) Science 337, стр. 816-821, Jinek et al, (2013), eLife 2:e00471, и David Segal, (2013) eLife 2:e00563). Таким образом, система CRISPR/Cas может быть спроектирована так, чтобы создавать DSB в требуемой мишени в геноме, при этом на репарацию DSB может воздействовать применение ингибиторов репарации, чтобы вызвать увеличение репарации, склонной к ошибкам.
В некоторых вариантах осуществления ДНК-связывающий домен одной или более нуклеаз, используемых для in vivo расщепления и/или направленного расщепления генома клетки, включает цинк-пальцевый белок. Предпочтительно, цинк-пальцевый белок не является природным в том отношении, что он сконструирован с возможностью связывания с выбранным целевым участком. См., например, Beerli et al. (2002) Nature Biotechnol. 20:135-141; Pabo et al. (2001) Ann. Rev. Biochem. 70:313-340; Isalan et al. (2001) Nature Biotechnol. 19:656-660; Segal et al. (2001) Curr. Opin. Biotechnol. 12:632-637; Choo et al. (2000) Curr. Opin. Struct. Biol. 10:411-416; патенты США 6,453,242; 6,534,261; 6,599,692; 6,503,717; 6,689,558; 7,030,215; 6,794,136; 7,067,317; 7,262,054; 7,070,934; 7,361,635; 7,253,273; и патентные публикации США 2005/0064474; 2007/0218528; 2005/0267061, полностью включенные в настоящую заявку посредством отсылки.
Сконструированный цинк-пальцевый связывающий домен может обладать новой специфичностью связывания по сравнению с природным цинк-пальцевым белком. Инженерные способы включают, без ограничения перечисленными, рациональное конструирование и различные типы отбора. Рациональное конструирование включает, например, использование баз данных, содержащих триплетные (или квадруплетные) нуклеотидные последовательности и индивидуальные аминокислотные последовательности цинковых пальцев, в которых каждая триплетная или квадруплетная нуклеотидная последовательность связана с одной или более аминокислотными последовательностями цинковых пальцев, которые связывают определенную триплетную или квадруплетную последовательность. См., например, находящиеся в совместном владении патенты США 6,453,242 и 6,534,261, полностью включенные в настоящую заявку посредством отсылки.
Примеры способов отбора, включающих фаговый дисплей и двухгибридные системы, раскрыты в патентах США 5,789,538; 5,925,523; 6,007,988; 6,013,453; 6,410,248; 6,140,466; 6,200,759 и 6,242,568; а также в WO 98/37186; WO 98/53057; WO 00/27878; WO 01/88197 и GB 2,338,237. Кроме того, повышение специфичности связывания цинк-пальцевых связывающих доменов было описано, например, в находящемся в совместном владении WO 02/077227.
Кроме того, как раскрыто в этой и других ссылках, цинк-пальцевые домены и/или многопальцевые цинк-пальцевые белки могут быть связаны друг с другом при использовании любых подходящих линкерных последовательностей, включающих, например, линкеры длиной пять или более аминокислот. См., также, патенты США 6,479,626; 6,903,185 и 7,153,949 по поводу примеров линкерных последовательностей длиной 6 или более аминокислот. Белки, описанные в настоящей заявке, могут включать любую комбинацию подходящих линкеров между отдельными цинковыми пальцами белка.
В настоящей заявке описаны композиции, в частности нуклеазы, которые могут применяться для in vivo расщепления донорной молекулы, несущей трансген, и нуклеазы для расщепления генома клетки таким образом, чтобы трансген направленно интегрировался в геном. В некоторых вариантах осуществления одна или более нуклеаз являются природными. В других вариантах осуществления одна или более нуклеаз не являются природными, то есть они сконструированы в ДНК-связывающем домене и/или расщепляющем домене. Например, ДНК-связывающий домен природной нуклеазы может быть изменен для связывания с выбранным целевым участком (например, мегануклеаза, которая была сконструирована для связывания с участком, отличающимся от исходного распознаваемого участка связывания). В других вариантах осуществления нуклеаза включает гетерологичные ДНК-связывающий и расщепляющий домены (например, цинк-пальцевые нуклеазы; ДНК-связывающие белки с TAL-эффекторным доменом; ДНК-связывающие домены мегануклеазы с гетерологичными расщепляющими доменами).
Любой подходящий расщепляющий домен может быть функционально связан с ДНК-связывающим доменом с формированием нуклеазы. Например, ДНК-связывающие домены белков ZFP были слиты с доменами нуклеаз с получением белков ZFN - функциональных молекул, которые способны распознавать свою заданную нуклеиновую кислоту-мишень посредством своего сконструированного (ZFP) ДНК-связывающего домена и производить разрезание ДНК около ZFP-связывающего участка посредством активности нуклеазы. См., например, Kim et al. (1996) Proc Natl Acad Sci USA 93(3):1156-1160. В последнее время белки ZFN использовались для модификации генома множества организмов. См., например, патентные публикации США 20030232410; 20050208489; 20050026157; 20050064474; 20060188987; 20060063231; и международную публикацию WO 07/014275. Аналогичным образом, ДНК-связывающие домены TALE были слиты с нуклеазными доменами с получением белков TALEN. См., например, патентную публикацию США 20110301073.
Как отмечено выше, расщепляющий домен может быть гетерологичен ДНК-связывающему домену, например, цинк-пальцевый ДНК-связывающий домен и расщепляющий домен из нуклеазы или ДНК-связывающий домен TALEN и расщепляющий домен, или ДНК-связывающий домен мегануклеазы и расщепляющий домен из другой нуклеазы. Гетерологичные расщепляющие домены могут быть получены из конкретной эндонуклеазы или экзонуклеазы. Примеры эндонуклеаз, из которых может быть получен расщепляющий домен, включают, без ограничения перечисленными, некоторые эндонуклеазы рестрикции и хоуминг-эндонуклеазы. См., например, 2002-2003 Catalogue, New England Biolabs, Beverly, MA; и Belfort et al. (1997) Nucleic Acids Res. 25:3379-3388. Известны дополнительные ферменты, которые расщепляют ДНК (например, нуклеаза S1; нуклеаза из бобов мунг; панкреатическая ДНКаза I; микрококковая нуклеаза; дрожжевая эндонуклеаза HO; см. также Linn et al. (eds.) Nucleases, Cold Spring Harbor Laboratory Press,1993). Один или более таких ферментов (или их функциональных фрагментов) могут использоваться в качестве источника расщепляющих доменов и расщепляющих полудоменов.
Аналогичным образом расщепляющий полудомен может быть получен из любой нуклеазы или ее части, как указано выше, что требует димеризации для расщепляющей активности. Как правило, для расщепления требуются два слитых белка, если слитые белки содержат расщепляющие полудомены. В альтернативе может использоваться один белок, включающий два расщепляющих полудомена. Два расщепляющих полудомена могут быть получены из одной эндонуклеазы (или ее функциональных фрагментов), или каждый расщепляющий полудомен может быть получен из разных эндонуклеаз (или их функциональных фрагментов). Кроме того, целевые участки для двух слитых белков предпочтительно расположены по отношению друг к другу таким образом, что связывание двух слитых белков с их соответствующими целевыми участками помещает расщепляющие полудомены в такую пространственную ориентацию друг относительно друга, которая позволяет расщепляющим полудоменам формировать функциональный расщепляющий домен, например, при димеризации. Таким образом, в некоторых вариантах осуществления близкие края целевых участков разделены 5-8 нуклеотидами или 15-18 нуклеотидами. Впрочем, любое целое число нуклеотидов или пар нуклеотидов может находиться между двумя целевыми участками (например, от 2 до 50 пар нуклеотидов или больше). Обычно участок расщепления находится между целевыми участками.
Эндонуклеазы рестрикции (рестриктазы) присутствуют у многих видов и способны к сиквенс-специфическому связыванию с ДНК (на участке распознавания) и расщеплению ДНК на участке связывания или около него. Некоторые рестриктазы (например, типа IIS) расщепляют ДНК на участках, удаленных от участка распознавания, и имеют разделяемые связывающий и расщепляющий домены. Например, фермент типа IIS Fok I катализирует расщепление двухцепочечной ДНК на удалении 9 нуклеотидов от ее участка распознавания на одной цепи и 13 нуклеотидов от ее участка распознавания на другой цепи. См., например, патенты США 5,356,802; 5,436,150 и 5,487,994; а также Li et al. (1992) Proc. Natl. Acad. Sci. USA 89:4275-4279; Li et al. (1993) Proc. Natl. Acad. Sci. USA 90:2764-2768; Kim et al. (1994a) Proc. Natl. Acad. Sci. USA 91:883-887; Kim et al. (1994b) J. Biol. Chem. 269:31,978-31,982. Таким образом, в одном варианте осуществления слитые белки включают расщепляющий домен (или расщепляющий полудомен) по меньшей мере из одного рестрикционного фермента типа IIS и один или более цинк-пальцевых связывающих доменов, которые могут быть сконструированными или нет.
Примером рестрикционного фермента типа IIS, расщепляющий домен которого может быть отделен от связывающего домена, является Fok I. Этот специфический фермент активен в виде димера. Bitinaite et al. (1998) Proc. Natl. Acad. Sci. USA 95: 10,570-10,575. Соответственно, в рамках настоящего описания часть фермента Fok I, используемая в раскрытых слитых белках, считается расщепляющим полудоменом. Таким образом, для направленного двухцепочечного расщепления и/или направленной замены последовательностей ДНК с использованием слитых цинк-пальцевых-Fok I белков, два слитых белка, каждый из которых включает расщепляющий полудомен FokI, могут использоваться для восстановления каталитически активного расщепляющего домена. В альтернативе может также использоваться одна полипептидная молекула, содержащая цинк-пальцевый связывающий домен и два расщепляющих полудомена Fok I. Параметры для направленного расщепления и направленного изменения последовательности при использовании слитых цинк-пальцевых-Fok I белков представлены в других частях настоящего описания.
Расщепляющий домен или расщепляющий полудомен могут быть любой частью белка, которая сохраняет расщепляющую активность или которая сохраняет способность к мультимеризации (например, димеризации) с образованием функционального расщепляющего домена.
Примеры рестрикционных ферментов типа IIS описаны в международной публикации WO 07/014275, которая полностью включена в настоящее описание. Дополнительные рестрикционные ферменты также содержат отдельные связывающий и расщепляющий домены и предусмотрены согласно настоящему описанию. См., например, Roberts et al. (2003) Nucleic Acids Res. 31:418-420.
В некоторых вариантах осуществления расщепляющий домен включает один или более сконструированных расщепляющих полудоменов (также называемых димеризационно мутантными доменами), которые минимизируют или предотвращают гомодимеризацию, как описано, например, в патентных публикациях США 20050064474; 20060188987; 20070305346 и 20080131962, описания которых полностью включены в настоящую заявку посредством отсылки. Аминокислотные остатки в положениях 446, 447, 479, 483, 484, 486, 487, 490, 491, 496, 498, 499, 500, 531, 534, 537 и 538 Fok I являются мишенями для воздействия на димеризацию расщепляющих полудоменов Fok I.
Примеры сконструированных расщепляющих полудоменов Fok, которые образуют облигатные гетеродимеры, включают пару, в которой первый расщепляющий полудомен включает мутации по аминокислотным остаткам в положениях 490 и 538 Fok I и второй расщепляющий полудомен включают мутации по аминокислотным остаткам 486 и 499.
Таким образом, в одном варианте осуществления мутация в положении 490 приводит к замене Glu (E)→Lys (K); мутация в положении 538 приводит к замене Iso (I)→Lys (K); мутация в положении 486 приводит к замене Gln (Q)→Glu (E); и мутация в положении 499 приводит к замене Iso (I)→Lys (K). В частности, сконструированные расщепляющие полудомены, описанные в настоящей заявке, были получены в результате мутации в положениях 490 (E→K) и 538 (I→K) в одном расщепляющем полудомене, с получением сконструированного расщепляющего полудомена, обозначенного "E490K:I538K", и в результате мутации в положениях 486 (Q→E) и 499 (I→L) в другом расщепляющем полудомене, с получением сконструированного расщепляющего полудомена, обозначенного "Q486E:I499L". Сконструированные расщепляющие полудомены, описанные в настоящей заявке, являются мутантными облигатными гетеродимерами, в которых нарушение расщепления минимизировано или устранено. См., например, патентную публикацию США 2008/0131962, описание которой полностью включено посредством отсылки во всех отношениях. В некоторых вариантах осуществления сконструированный расщепляющий полудомен включает мутации в положениях 486, 499 и 496 (нумеруемых относительно FokI дикого типа), например, мутации, которые приводят к замене остатка Gln (Q) дикого типа в положении 486 остатком Glu (E), остатка Iso (I) дикого типа в положении 499 остатком Leu (L) и остатка Asn (N) дикого типа в положении 496 остатком Asp (D) или Glu (E) (также обозначены как домены "ELD" и "ELE", соответственно). В других вариантах осуществления сконструированный расщепляющий полудомен включает мутации в положениях 490, 538 и 537 (нумеруемых относительно FokI дикого типа), например, мутации, которые приводят к замене остатка Glu (E) дикого типа в положении 490 остатком Lys (K), остатка Iso (I) дикого типа в положении 538 остатком Lys (K) и остатка His (H) дикого типа в положении 537 остатком Lys (K) или Arg (R) (также обозначены как домены "KKK" и "KKR", соответственно). В других вариантах осуществления сконструированный расщепляющий полудомен включает мутации в положениях 490 и 537 (нумеруемых относительно FokI дикого типа), например, мутации, которые приводят к замене остатка Glu (E) дикого типа в положении 490 остатком Lys (K) и остатка Его (H) дикого типа в положении 537 остатком Lys (K) или Arg (R) (также обозначены как домены "KIK" и "KIR", соответственно). См. патентную публикацию США 20110201055). В других вариантах осуществления сконструированный расщепляющий полудомен включает мутации "Sharkey" и/или "Sharkey'" (см. Guo и другие, (2010) Дж. Мол. Biol. 400 (1):96-107).
Сконструированные расщепляющие полудомены, описанные в настоящей заявке, могут быть получены при использовании любого подходящего способа, например, с помощью сайт-направленного мутагенеза расщепляющих полудоменов дикого типа (Fok I), как описано в патентных публикациях США 20050064474; 20080131962 и 20110201055.
В альтернативе нуклеазы могут собираться in vivo на целевом участке нуклеиновой кислоты при использовании так называемой технологии "сплит-энзим" (т.е. раздельный фермент, см. например, патентную публикацию США 20090068164). Компоненты таких сплит-энзимов могут экспрессироваться либо на отдельных экспрессионных конструкциях, либо могут быть связаны в одной открытой рамке считывания, где отдельные компоненты разделены, например, последовательностью саморасщепляющегося 2A пептида или IRES. Компоненты могут быть отдельными цинк-пальцевым связывающими доменами или доменами мегануклеазы, связывающими нуклеиновую кислоту.
Нуклеазы могут быть подвергнуты скринингу на активность перед применением, например, в дрожжевой хромосомной системе, как описано в WO 2009/042163 и 20090068164. Экспрессионные конструкции нуклеазы могут быть с легкостью разработаны при использовании способов, известных в уровне техники. См., например, патентные публикации США 20030232410; 20050208489; 20050026157; 20050064474; 20060188987; 20060063231 и международную публикацию WO 07/014275. Экспрессия нуклеазы может находиться под контролем конститутивного промотора или индуцируемого промотора, например галактокиназного промотора, который активируется (дерепрессируется) в присутствии рафинозы и/или галактозы и репрессируется в присутствии глюкозы.
В варианте осуществления полинуклеотидная донорная кассета включает последовательность, которая кодирует пептид. Для экспрессии пептида нуклеотидные последовательности, кодирующие последовательность пептида, обычно субклонируют в экспрессионный вектор, который содержит промотор, направляющий транскрипцию. Подходящие бактериальные и эукариотические промоторы известны в уровне техники и описаны, например, в Sambrook et al., Molecular Cloning, A Laboratory Manual (2nd ed. 1989; 3rd ed., 2001); Kriegler, Gene Transfer and Expression: A Laboratory Manual (1990); и Current Protocols in Molecular Biology (Ausubel et al., выше). Доступны бактериальные системы экспрессии для экспрессии пептида, например, в E. coli, Bacillus sp. и Salmonella (Palva et al., Gene 22:229-235 (1983)). Наборы для таких систем экспрессии коммерчески доступны. Эукариотические системы экспрессии для клеток млекопитающих, дрожжей и клеток насекомых известны специалистам в данной области и также являются коммерчески доступными.
В варианте осуществления полинуклеотидная донорная кассета включает кассету экспрессии гена, включающую трансген. Кассета экспрессии гена обычно содержит единицу транскрипции или кассету экспрессии, которая содержит все дополнительные элементы, требуемые для экспрессии нуклеиновой кислоты в клетках-хозяевах, прокариотических или эукариотических. Типичная кассета экспрессии гена, таким образом, содержит промотор, функционально связанный, например, с последовательностью нуклеиновой кислоты, кодирующей белок, и сигналы, требуемые, например, для эффективного полиаденилирования транскрипта, терминации транскрипции, участков связывания рибосомы или терминации трансляции. Дополнительные элементы кассеты могут включать, например, энхансеры и гетерологичные сигналы сплайсинга.
В варианте осуществления кассета экспрессии гена будет также включать на 3'-конце гетерологичной последовательности целевого нуклеотида область терминации транскрипции и трансляции, функциональную в растениях. Область терминации может быть нативной с нуклеотидной последовательностью промотора вариантов осуществления настоящего описания, может быть нативной с целевой последовательностью ДНК или может быть получена из другого источника. Подходящие области терминации доступны из Ti-плазмиды A. tumefaciens, такие как области терминации октопинсинтазы и нопалинсинтазы (nos) (Depicker et al., Mol. and Appl. Genet. 1:561-573 (1982) и Shaw et al. (1984) Nucleic Acids Research vol. 12, No. 20 pp7831-7846(nos)); см. также Guerineau et al. Mol. Gen. Genet. 262:141-144 (1991); Proudfoot, Cell 64:671-674 (1991); Sanfacon et al. Genes Dev. 5:141-149 (1991); Mogen et al. Plant Cell 2:1261-1272 (1990); Munroe et al. Gene 91:151-158 (1990); Ballas et al. Nucleic Acids Res. 17:7891-7903 (1989); Joshi et al. Nucleic Acid Res. 15:9627-9639 (1987).
В других вариантах осуществления кассеты экспрессии генов могут дополнительно содержать 5'-лидерные последовательности. Такие лидерные последовательности могут обеспечивать усиление трансляции. Лидерные последовательности трансляции известны в уровне техники и включают, в качестве примера, лидерные последовательности пикорнавирусов, лидерную последовательность EMCV (5'-некодирующую область вируса энцефаломиокардита), Elroy-Stein et al. Proc. Nat. Acad. Sci. USA 86:6126-6130 (1989); лидерные последовательности потивирусов, например, лидерную последовательность TEV (вируса гравировки табака), Carrington and Freed Journal of Virology, 64:1590-1597 (1990), лидерную последовательность MDMV (вируса карликовой мозаики кукурузы), Allison et al., Virology 154:9-20 (1986); белок, связывающий тяжелую цепь человеческого иммуноглобулина (BiP), Macejak et al. Nature 353:90-94 (1991); нетранслируемую лидерную последовательность из мРНК белка оболочки вируса мозаики люцерны (AMV RNA 4), Jobling et al. Nature 325:622-625 (1987); лидерную последовательность вируса табачной мозаики (ВТМ), Gallie et al. (1989) Molecular Biology of RNA, стр. 237-256; и лидерную последовательность вируса хлорозной пятнистости кукурузы (MCMV), Lommel et al. Virology 81:382-385 (1991). См. также Della-Cioppa et al. Plant Physiology 84:965-968 (1987). Конструкция может также содержать последовательности, которые повышают трансляцию и/или стабильность мРНК, такие как интроны. Примером одного такого интрона является первый интрон гена II варианта гистона H3.III Arabidopsis thaliana (Chaubet et al. Journal of Molecular Biology, 225:569-574 (1992)).
В варианте осуществления кассета экспрессии гена донорной полинуклеотидной последовательности содержит промотор. Промотор, используемый для направления экспрессии нуклеиновой кислоты, кодирующей пептид, зависит от конкретного применения. Например, для экспрессии и очистки белков обычно используется сильный конститутивный промотор, подходящий для клетки-хозяина. Неограничивающие примеры предпочтительных растительных промоторов включают последовательности промоторов, полученные из убиквитина-10 A. thaliana (ubi-10) (Callis, et al., 1990, J. Biol. Chem., 265:12486-12493); маннопинсинтазы A. tumefaciens (Δmas) (Petolino et al., патент США 6,730,824) и/или вируса мозаики жилок маниоки (CsVMV) (Verdaguer et al., 1996, Plant Molecular Biology 31:1129-1139).
В способах, раскрытых в настоящей заявке, может использоваться ряд промоторов, которые направляют экспрессию гена в растении. Такие промоторы могут быть выбраны из конститутивных, химически регулируемых, индуцируемых, тканеспецифических и семяпредпочтительных промоторов.
Конститутивные промоторы включают, например, 35S кор-промотор вируса мозаики цветной капусты (Odell et al. (1985) Nature 313:810-812); промотор актина риса (McElroy et al. (1990) Plant Cell 2:163-171); промотор убиквитина кукурузы (патент США 5,510,474; Christensen et al. (1989) Plant Mol. Biol. 12:619-632 и Christensen et al. (1992) Plant Mol. Biol. 18:675-689); промотор pEMU (Last et al. (1991) Theor. Appl. Genet. 81:581-588); промотор ALS (патент США 5,659,026); промотор гистона кукурузы (Chaboute et al. Plant Molecular Biology, 8:179-191 (1987)) и т.п.
Диапазон доступных совместимых растительных промоторов включает тканеспецифические и индуцируемые промоторы. Индуцируемый регуляторный элемент является элементом, который способен прямо или опосредованно активировать транскрипцию одной или более последовательностей ДНК или генов в ответ на индуктор. В отсутствие индуктора последовательности ДНК или гены не будут транскрибироваться. Обычно белковый фактор, который специфично связывается с индуцируемым регуляторным элементом для активации транскрипции, присутствует в неактивной форме, которая затем прямо или опосредованно переводится в активную форму индуктором. Индуктор может быть химическим агентом, таким как белок, метаболит, регулятор роста, гербицид или фенольное соединение, или физиологическим стрессом, который вызван теплом, холодом, солью или токсичными элементами непосредственно или опосредованно в результате воздействия патогена или болезнетворного агента, такого как вирус. Обычно белковый фактор, который специфично связывается с индуцируемым регуляторным элементом для активации транскрипции, присутствует в неактивной форме, которая затем прямо или опосредованно переводится в активную форму индуктором. Индуктор может быть химическим агентом, таким как белок, метаболит, регулятор роста, гербицид или фенольное соединение, или физиологическим стрессом, который вызван теплом, холодом, солью или токсичными элементами непосредственно или опосредованно в результате воздействия патогена или болезнетворного агента, такого как вирус. Растительная клетка, содержащая индуцируемый регуляторный элемент, может быть подвергнута воздействию индуктора путем применения индуктора к клетке или растению извне, например, с помощью распыления, орошения, нагрева или подобных методов.
В вариантах осуществления настоящего описания может использоваться любой индуцируемый промотор. См. Ward et al. Plant Mol. Biol. 22: 361-366 (1993). Примеры индуцируемых промоторов включают промоторы рецепторов экдизонов (патент США 6,504,082); промоторы из системы ACE1, которые реагируют на медь (Mett et al. PNAS 90: 4567-4571 (1993)); гены In2-1 и In2-2 из кукурузы, которые реагируют на антидоты бензолсульфонамидных гербицидов (патент США 5,364,780; Hershey et al., Mol. Gen. Genetics 227: 229-237 (1991) и Gatz et al., Mol. Gen. Genetics 243: 32-38 (1994)); Tet репрессор из Tn10 (Gatz et al., Mol. Gen. Genetics 227: 229-237 (1991); или промоторы из гена стероидного гормона, транскрипционную активность которых индуцирует глюкокортикостероидный гормон, Schena et al., Proc. Natl. Acad. Sci. U.S.A. 88: 10421 (1991) и McNellis et al., (1998) Plant J. 14(2):247-257; GST промотор кукурузы, который активируется гидрофобными электрофильными соединениями, которые применяются в качестве предвсходовых гербицидов (см. патент США 5,965,387 и публикацию международной заявки на патент WO 93/001294); а также промотор PR-1a табака, который активируется салициловой кислотой (см. Ono S, Kusama M, Ogura R, Hiratsuka K., "Evaluation of the Use of the Tobacco PR-1a Promoter to Monitor Defense Gene Expression by the Luciferase Bioluminescence Reporter System", Biosci Biotechnol Biochem. 2011 Sep 23;75(9):1796-800). Другие химически регулируемые промоторы, представляющие интерес, включают тетрациклин-индуцируемые и тетрациклин-репрессируемые промоторы (см., например, Gatz et al., (1991) Mol. Gen. Genet. 227:229-237 и патенты США 5,814,618 и 5,789,156).
Другие представляющие интерес регулируемые промоторы включают холодочувствительный регуляторный элемент или регуляторный элемент теплового шока, на транскрипцию которых может влиять воздействие холода или тепла, соответственно (Takahashi et al., Plant Physiol. 99:383-390, 1992); промотор гена алкогольдегидрогеназы (Gerlach et al., PNAS USA 79:2981-2985 (1982); Walker et al., PNAS 84(19):6624-6628 (1987)), индуцируемый анаэробными условиями; и светоиндуцируемый промотор, полученный из гена rbcS гороха или гена psaDb гороха (Yamamoto et al. (1997) Plant J. 12(2):255-265); светоиндуцируемый регуляторный элемент (Feinbaum et al., Mol. Gen. Genet. 226:449, 1991; Lam and Chua, Science 248:471, 1990; Matsuoka et al. (1993) Proc. Natl. Acad. Sci. USA 90(20):9586-9590; Orozco et al. (1993) Plant Mol. Bio. 23(6):1129-1138), индуцируемый фитогормонами регуляторный элемент (Yamaguchi-Shinozaki et al., Plant Mol. Biol. 15:905, 1990; Kares et al., Plant Mol. Biol. 15:225, 1990) и т.п. Индуцируемый регуляторный элемент также может быть промотором гена In2-1 или In2-2 кукурузы, который реагирует на антидоты бензолсульфонамидных гербицидов (Hershey et al., Mol. Gen. Gene. 227:229-237, 1991; Gatz et al., Mol. Gen. Genet. 243:32-38, 1994), и Tet репрессором транспозона Tn10 (Gatz et al., Mol. Gen. Genet. 227:229-237, 1991). Индуцируемые стрессом промоторы включают промоторы, индуцируемые в условиях солевого/водного стресса, такие как P5CS (Zang et al. (1997) Plant Sciences 129:81-89); индуцируемые холодом промоторы, такие как cor15a (Hajela et al. (1990) Plant Physiol. 93:1246-1252), cor15b (Wilhelm et al. (1993) Plant Mol Biol 23:1073-1077), wsc120 (Ouellet et al. (1998) FEBS Lett. 423-324-328), ci7 (Kirch et al. (1997) Plant Mol Biol. 33:897-909), ci21A (Schneider et al. (1997) Plant Physiol. 113:335-45); индуцируемые засухой промоторы, такие как Trg-31 (Chaudhary et al (1996) Plant Mol. Biol. 30:1247-57), rd29 (Kasuga et al. (1999) Nature Biotechnology 18:287-291); осмотически индуцируемые промоторы, такие как Rab17 (Vilardell et al. (1991) Plant Mol. Biol. 17:985-93) и осмотин (Raghothama et al. (1993) Plant Mol Biol 23:1117-28); а также индуцируемые теплом промоторы, такие как белки теплового шока (Barros et al. (1992) Plant Mol. 19:665-75; Marrs et al. (1993) Dev. Genet. 14:27-41), smHSP (Waters et al. (1996) J. Experimental Botany 47:325-338), и индуцируемый тепловым шоком элемент из промотора убиквитина петрушки (WO 03/102198). Другие индуцируемые стрессом промоторы включают rip2 (патент США 5,332,808 и патентная публикация США 2003/0217393) и rd29a (Yamaguchi-Shinozaki et al. (1993) Mol. Gen. Genetics 236:331-340). Некоторые промоторы индуцируются при пореждении, включая промотор pMAS (Guevara-Garcia et al. (1993) Plant J. 4(3):495-505) и промотор ORF13 агробактерии (Hansen et al., (1997) Mol. Gen. Genet. 254(3):337-343).
Тканепредпочтительные промоторы могут использоваться для направленного повышения транскрипции и/или экспрессии в определенной растительной ткани. При ссылке на предпочтительную экспрессию, это означает экспрессию в определенной растительной ткани на более высоком уровне, нежели в другой растительной ткани. Примеры таких типов промоторов включают семяпредпочтительную экспрессию, такую как обеспечивает промотор фазеолина (Bustos et al. 1989. The Plant Cell Vol. 1, 839-853) и гена глобулина-1 кукурузы (Belanger, et al. 1991 Genetics 129:863-972). В случае двудольных семяпредпочтительные промоторы включают, без ограничения перечисленными, промотор β-фазеолина фасоли, напина, β-конглицинина, лектина сои, круциферина и т.п. В случае однодольных семяпредпочтительные промоторы включают, без ограничения перечисленными, промотор 15 кДа зеина кукурузы, 22 кДа зеина, 27 кДа зеина, γ-зеина, waxy, shrunken 1, shrunken 2, глобулина-1 и т.д. Семяпредпочтительные промоторы также включают такие промоторы, которые направляют экспрессию генов преимущественно в определенных тканях семени, например, эндосперм-предпочтительный промотор γ-зеина, криптический промотор табака (Fobert et al. 1994. T-DNA tagging of a seed coat-specific cryptic promoter in tobacco. Plant J. 4: 567-577), промотор P-гена кукурузы (Chopra et al. 1996. Alleles of the maize P gene with distinct tissue specificities encode Myb-homologous proteins with C-terminal replacements. Plant Cell 7:1149-1158, Erratum in Plant Cell.1997, 1:109), промотор глобулина-1 кукурузы (Belenger and Kriz.1991. Molecular basis for Allelic Polymorphism of the maize Globulin-1 gene. Genetics 129: 863-972), и промоторы, которые направляют экспрессию в семенной оболочке или шелухе зерен кукурузы, например, перикарпий-специфический промотор глутаминсинтетазы (Muhitch et al.,2002. Isolation of a Promoter Sequence From the Glutamine Synthetase1-2 Gene Capable of Conferring Tissue-Specific Gene Expression in Transgenic Maize. Plant Science 163:865-872).
Кассета экспрессии гена может содержать 5'-лидерную последовательность. Такие лидерные последовательности могут вызывать повышение трансляции. Лидерные последовательности трансляции известны в уровне техники и включают, в качестве примера, лидерные последовательности пикорнавирусов, лидерную последовательность EMCV (5'-некодирующую область вируса энцефаломиокардита), Elroy-Stein et al. Proc. Nat. Acad. Sci. USA 86:6126-6130 (1989); лидерные последовательности потивирусов, например, лидерную последовательность TEV (вируса гравировки табака), Carrington and Freed Journal of Virology, 64:1590-1597 (1990), лидерную последовательность MDMV (вируса карликовой мозаики кукурузы), Allison et al., Virology 154:9-20 (1986); белок, связывающий тяжелую цепь человеческого иммуноглобулина (BiP), Macejak et al. Nature 353:90-94 (1991); нетранслируемую лидерную последовательность из мРНК белка оболочки вируса мозаики люцерны (AMV RNA 4), Jobling et al. Nature 325:622-625 (1987); лидерную последовательность вируса табачной мозаики (ВТМ), Gallie et al. (1989) Molecular Biology of RNA, стр. 237-256; и лидерную последовательность вируса хлорозной пятнистости кукурузы (MCMV), Lommel et al. Virology 81:382-385 (1991). См. также Della-Cioppa et al. Plant Physiology 84:965-968 (1987).
Конструкция может также содержать последовательности, которые повышают трансляцию и/или стабильность мРНК, такие как интроны. Примером одного такого интрона является первый интрон гена II варианта гистона H3.III Arabidopsis thaliana (Chaubet et al. Journal of Molecular Biology, 225:569-574 (1992)).
В тех случаях, когда желательно иметь экспрессируемый продукт гетерологичной нуклеотидной последовательности, направленный в определенную органеллу, в частности пластиду, амилопласт или в эндоплазматический ретикулум, или секретируемый на поверхности клетки или внеклеточно, кассета экспрессии может дополнительно включать кодирующую последовательность транзитного пептида. Такие транзитные пептиды известны в уровне техники и включают, без ограничения перечисленными, транзитный пептид ацилпереносящего белка, малой субъединицы RUBISCO, растительной EPSP синтазы и Helianthus annuus (см. Lebrun et al., патент США 5,510,417), транзитный пептид хлоропластов Brittle-1 Zea mays (Nelson et al. Plant Physiol 117(4):1235-1252 (1998); Sullivan et al. Plant Cell 3(12):1337-48; Sullivan et al., Planta (1995) 196(3):477-84; Sullivan et al., J. Biol. Chem. (1992) 267(26):18999-9004)) и т.п. Кроме того, в уровне техники известны химерные транзитные пептиды хлоропластов, такие как Оптимизированный транзитный пептид (см., патент США 5,510,471). Дополнительные транзитные пептиды хлоропластов были описаны ранее в патентах США 5,717,084 и 5,728,925. Специалист в данной области сумеет оценить множество опций, доступных при экспрессии продукта в конкретной органелле. Например, последовательность альфа-амилазы ячменя часто используется для направления экспрессии в эндоплазматический ретикулум (Rogers, J. Biol. Chem. 260:3731-3738 (1985)).
В варианте осуществления донорная кассета полинуклеотида включает трансген. В некоторых вариантах осуществления в настоящей заявке предусмотрен трансген, кодирующий полипептид, включающий кассету экспрессии гена. Такой трансген может использоваться в любом из целого ряда применений для получения трансгенных растений. Конкретные примеры трансгена, включающего кассету экспрессии гена, представлены в настоящей заявке в иллюстративных целях и включают экспрессию гена, включающего ген признака, ген РНКи или репортерный ген/ген селективного маркера.
При конструировании гена для экспрессии в растениях предпочтение кодонов перспективного растения(й)-хозяина может быть определено, например, при использовании публично доступных баз данных последовательностей ДНК для поиска информации о распределении кодонов геномов растений или кодирующих белок областей различных растительных генов. После подбора оптимизированной (например, оптимизированной для растения) последовательности ДНК на бумаге или в электронной форме, молекулы химерной ДНК могут быть синтезированы в лаборатории с точным соответствием по последовательности подобранной последовательности. Такие синтетические молекулы нуклеиновых кислот могут быть клонированы и подвергнуты иным манипуляциям, как если бы они были получены из природных или нативных источников.
В варианте осуществления экспрессируемый трансген раскрыт в настоящей заявке. Кассета экспрессии гена может включать репортерный ген/ген селективного маркера, ген признака или ген РНКи. Примеры гена селективного маркера, гена признака и гена РНКи представлены ниже. Способы, раскрытые в настоящей заявке, обладают преимуществом, поскольку они предоставляют способ отбора транформантов зародышевой линии, который не зависит от определенной функции белкового продукта, или другой функции, трансгена.
Трансгены или кодирующая последовательность, которые придают устойчивость к вредителям или болезни
(A) Гены устойчивости к болезням растений. Защита растений часто активируется при специфичном взаимодействии между продуктом гена устойчивости к болезни (R) в растении и соответствующим продуктом гена авирулентности (Avr) в патогене. Сорт растения может быть трансформирован клонированным геном устойчивости с получением сконструированных растений, которые устойчивы к определенным штаммам патогенов. Примеры таких генов включают ген Cf-9 томата для устойчивости к Cladosporium fulvum (Jones et al., 1994 Science 266:789), ген Pto томата, который кодирует протеинкиназу, для устойчивости к Pseudomonas syringae pv. tomato (Martin et al., 1993 Science 262:1432) и ген RSSP2 Arabidopsis для устойчивости к Pseudomonas syringae (Mindrinos et al., 1994 Cell 78:1089).
(B) Белок Bacillus thuringiensis, его производное или синтетический полипептид, моделируемый на их основе, такой как нуклеотидная последовательность гена δ-эндотоксина Bt (Geiser et al., 1986 Gene 48:109) и растительный инсектицидный ген (VIP) (см., например, Estruch et al. (1996) Proc. Natl. Acad. Sci. 93:5389-94). Кроме того, молекулы ДНК, кодирующие гены δ-эндотоксина, могут быть приобретены в Американской коллекции типовых культур (American Type Culture Collection, Rockville, Md.) под номерами ATCC 40098, 67136, 31995 и 31998.
(C) Лектин, такой как нуклеотидные последовательности нескольких генов маннозосвязывающих лектинов Clivia miniata (Van Damme et al., 1994 Plant Molec. Biol. 24:825).
(D) Витаминсвязывающий белок, такой как авидин и гомологи авидина, которые могут применяться в качестве ларвицидов против насекомых-вредителей. См. патент США 5,659,026.
(E) Ингибитор фермента, например, ингибитор протеазы или ингибитор амилазы. Примеры таких генов включают ингибитор цистеинпротеиназы риса (Abe et al., 1987 J. Biol. Chem. 262:16793), ингибитор протеиназы табака I (Huub et al., 1993 Plant Molec. Biol. 21:985) и ингибитор α-амилазы (Sumitani et al., 1993 Biosci. Biotech. Biochem. 57:1243).
(F) Специфичный для насекомых гормон или феромон, такой как экдистероид и ювенильный гормон, их вариант, миметик на их основе или их антагонист или агонист, например, бакуловирусная экспрессия клонированной эстеразы ювенильного гормона, инактиватора ювенильного гормона (Hammock et al., 1990 Nature 344:458).
(G) Специфичный для насекомых пептид или нейропептид, который при экспрессии нарушает физиологию обрабатываемого вредителя (J. Biol. Chem. 269:9). Примеры таких генов включают рецептор диуретического гормона насекомых (Regan, 1994), аллостатин, идентифицированный в Diploptera punctata (Pratt, 1989), и специфичные для насекомых паралитические нейротоксины (патент США 5,266,361).
(H) Специфичный для насекомого токсин, вырабатываемый в природе у змеей, ос и т.д., такой как инсектотоксичный пептид скорпиона (Pang, 1992 Gene 116:165).
(I) Фермент, ответственный за избыточное накопление монотерпена, сесквитерпена, стероида, гидроксамовой кислоты, фенилпропаноидного производного или другой небелковой молекулы с инсектицидной активностью.
(J) Фермент, участвующий в модификации, в том числе посттрансляционной модификации, биологически активной молекулы; например, гликолитический фермент, протеолитический фермент, липолитический фермент, нуклеаза, циклаза, трансаминаза, эстераза, гидролаза, фосфатаза, киназа, фосфорилаза, полимераза, эластаза, хитиназа и глюканаза, природные или синтетические. Примеры таких генов включают ген callas (опубликованная заявка PCT WO93/02197), кодирующие хитиназу последовательности (которые могут быть получены, например, из ATCC под номерами 3999637 и 67152), хитиназу табачного бражника (Kramer et al., 1993 Insect Molec. Biol. 23:691) и ген полиубиквитина ubi4-2 петрушки (Kawalleck et al., 1993 Plant Molec. Biol. 21:673).
(K) Молекула, которая стимулирует передачу сигналов. Примеры таких молекул включают нуклеотидные последовательности кДНК клонов кальмодулина бобов мунг (Botella et al., 1994 Plant Molec. Biol. 24:757) и нуклеотидную последовательность кДНК клона кальмодулина кукурузы (Griess et al., 1994 Plant Physiol. 104:1467).
(L) Пептид с гидрофобным моментом. См. патенты США 5,659,026 и 5,607,914; в последнем описаны синтетические противомикробные пептиды, которые придают устойчивость к болезням.
(M) Мембранная пермеаза, формирователь каналов или блокатор каналов, такой как аналог цекропин-β литического пептида (Jaynes et al., 1993 Plant Sci. 89:43), который делает трансгенные растения табака устойчивыми к Pseudomonas solanacearum.
(N) Вирусно-инвазивный белок или сложный токсин, получаемый из него. Например, накопление вирусных белков оболочки в трансформированных растительных клетках придает устойчивость к вирусной инфекции и/или развитию болезни, вызываемой вирусом, из которого получен ген белка оболочки, а также родственными вирусами. Опосредованную белком оболочки устойчивость придавали трансформированным растениям против вируса мозаики люцерны, вируса мозаики огурца, вируса полосатости табака, вируса X картофеля, вируса Y картофеля, вируса гравировки табака, вируса погремковости табака и вируса табачной мозаики. См., например, Beachy et al. (1990) Ann. Rev. Phytopathol. 28:451.
(O) Специфичное для насекомых антитело или полученный из него иммунотоксин. Так например, антитело, направленное против важной метаболической функции в кишечнике насекомого, будет инактивировать соответствующий фермент, уничтожая насекомое. Например, в Taylor et al. (1994) Abstract #497, Seventh Int'l Symposium on Molecular Plant-Microbe Interactions, показана ферментативная инактивация в трансгенном табаке в результате продукции одноцепочечных фрагментов антитела.
(P) Вирусспецифичное антитело. См., например, Tavladoraki et al. (1993) Nature 266:469, где показано, что трансгенные растения, экспрессирующие рекомбинантные гены антител, защищены от вирусной атаки.
(Q) Ингибирующий развитие белок, вырабатываемый в природе патогеном или паразитом. Так например, грибковые эндо-α-1,4-D полигалактуроназы способствуют грибковой колонизации и высвобождению питательных веществ из растения в результате солюбилизации стенки растительных клеток гомо-α-1,4-D-галактуроназой (Lamb et al., 1992) Bio/Technology 10:1436. Клонирование и исследование гена, который кодирует эндополигалактуроназа-ингибирующий белок фасоли, описаны в Toubart et al. (1992 Plant J. 2:367).
(R) Ингибирующий развитие белок, вырабатываемый в природе растением, такой как рибосома-инактивирующий ген ячменя, который обеспечивает повышенную устойчивость к грибковой болезни (Longemann et al., 1992). Bio/Technology 10:3305.
(S) РНК интерференция, в которой молекула РНК используется для ингибирования экспрессии гена-мишени. Молекула РНК в одном примере является частично или полностью двухцепочечной, что вызывает реакцию сайленсинга, который приводит к расщепления дцРНК на малые интерферирующие РНК, которые затем включаются в направляющий комплекс, который разрушает гомологичные мРНК. См., например, Fire et al., патент США 6,506,559; Graham et al. 6,573,099.
Гены, которые придают устойчивость к гербициду
(A) Гены, кодирующие устойчивость или резистентность к гербициду, который ингибирует точку роста или меристему, такому как имидазалиноновый, сульфонанилидный или сульфонилмочевинный гербицид. Примеры генов в этой категории кодируют мутантный фермент ALS (Lee et al., 1988 EMBOJ. 7:1241), который также известен как фермент AHAS (Miki et al., 1990 Theor. Appl. Genet. 80:449).
(B) Один или более дополнительных генов, кодирующих устойчивость или резистентность к глифосату, придаваемую мутантными генами EPSP синтазы и aroA, или в результате метаболической инактивации такими генами, как GAT (глифосат-ацетилтрансфераза) или GOX (глифосатоксидаза), а также к другим фосфоновым соединениям, таким как глуфосинат (гены pat и bar; DSM-2), и арилоксифеноксипропионовым кислотам и циклогександионам (гены, кодирующие ингибитор ацетил-КоА-карбоксилазы). См., например, патент США 4,940,835, в котором раскрыта нуклеотидная последовательность формы EPSP, которая может придавать устойчивость к глифосату. Молекула ДНК, кодирующая мутантный ген aroA, может быть получена под номером ATCC 39256, и нуклеотидная последовательность мутантного гена раскрыта в патенте США 4,769,061. В европейской заявке на патент 0 333 033 и патенте США 4,975,374 раскрыты нуклеотидные последовательности генов глутаминсинтетазы, которые придают устойчивость к гербицидам, таким как L-фосфинотрицин. Нуклеотидная последовательность гена фосфинотрицинацетил-трансферазы приведена в европейской заявке 0 242 246. В De Greef et al. (1989) Bio/Technology 7:61 описано получение трансгенных растений, которые экспрессируют химерные bar гены, кодирующие активность фосфинотрицинацетилтрансферазы. Примеры генов, придающих устойчивость к арилоксифеноксипропионовым кислотам и циклогександионам, таким как сетоксидим и галоксифоп, гены Accl-S1, Accl-S2 и Accl-S3, описаны в Marshall et al. (1992) Theor. Appl. Genet. 83:435.
(C) Гены, кодирующие устойчивость или резистентность к гербициду, который замедляет фотосинтез, такому как триазин (гены psbA и gs+) и бензонитрил (ген нитрилазы). В Przibilla et al. (1991) Plant Cell 3:169 описано применение плазмид, кодирующих мутантные гены psbA, для трансформации Chlamydomonas. Нуклеотидные последовательности генов нитрилазы раскрыты в патенте США 4,810,648, и молекулы ДНК, содержащие эти гены, доступны под номерами ATCC 53435, 67441 и 67442. Клонирование и экспрессия ДНК, кодирующей глутатион-S-трансферазу, описаны в Hayes et al. (1992) Biochem. J. 285:173.
(D) Гены, кодирующие устойчивость или резистентность к гербициду, который связывается с гидроксифенилпируват-диоксигеназами (HPPD), ферментами, которые катализируют реакцию, в которой пара-гидроксифенилпируват (HPP) превращается в гомогентизат. Это включает гербициды, такие как изоксазолы (EP418175, EP470856, EP487352, EP527036, EP560482, EP682659, патент США 5,424,276), в частности изоксафлутол, который является селективным гербицидом для кукурузы, дикетонитрилы (EP496630, EP496631), в частности 2-циано-3-циклопропил-1-(2-SO2CH3-4-CF3-фенил)пропан-1,3-дион и 2-циано-3-циклопропил-1-(2-SO2CH3-4-2,3Cl2фенил)пропан-1,3-дион, трикетоны (EP625505, EP625508, патент США 5,506,195), в частности сулкотрион, и пиразолинаты. Ген, который производит избыток HPPD в растениях, может придавать резистентность или устойчивость к таким гербицидам, включая, например, гены, описанные в патентах США 6,268,549 и 6,245,968 и публикации заявки на патент США 20030066102.
(E) Гены, кодирующие устойчивость или резистентность к феноксиауксиновым гербицидам, таким как 2,4-дихлорфеноксиуксусная кислота (2,4-D), и которые могут также придавать устойчивость или резистентность к арилоксифеноксипропионатным (AOPP) гербицидам. Примеры таких генов включают ген фермента α-кетоглутарат-зависимой диоксигеназы (aad-1), описанный в патенте США 7,838,733.
(F) Гены, кодирующие устойчивость или резистентность к феноксиауксиновым гербицидам, таким как 2,4- дихлорфеноксиуксусная кислота (2,4-D), и которые могут также придавать устойчивость или резистентность к пиридилоксиауксиновым гербицидам, таким как флуроксипир или триклопир. Примеры таких генов включают ген фермента α-кетоглутарат-зависимой диоксигеназы (aad-12), описанный в WO 2007/053482 A2.
(G) Гены, кодирующие устойчивость или резистентность к дикамбе (см., например, патентную публикацию США 20030135879).
(H) Гены, обеспечивающие устойчивость или резистентность к гербицидам, которые ингибируют протопорфириногеноксидазу (PPO) (см. патент США 5,767,373).
(I) Гены, обеспечивающие устойчивость или резистентность к триазиновым гербицидам (таким как атразин) и гербицидам производным мочевины (такие как диурон), которые связываются с кор-белками реакционных центров фотосистемы II (PS II) (см. Brussian et al., (1989) EMBO J. 1989, 8(4): 1237-1245).
Гены, которые придают или способствуют приобретению ценного признака
(A) Модифицированный метаболизм жирных кислот, например, при трансформации кукурузы или Brassica антисмысловым геном стеароил-АПБ-десатуразы с увеличением содержания стеариновой кислоты в растении (Knultzon et al., 1992 Proc. Nat. Acad. Sci. USA 89:2624).
(B) Уменьшенное содержание фитата
(1) Введение кодирующего фитазу гена, такого как ген фитазы Aspergillus niger (Van Hartingsveldt et al., 1993 Gene 127:87), усиливает расщепление фитата, добавляя больше свободного фосфата в трансформированное растение.
2) Может быть введен ген, который уменьшает содержание фитата. В кукурузе это можно осуществить, например, путем клонирования и последующего повторного введения ДНК, ассоциированной с одним аллелем, который может быть ответственным за мутанты кукурузы, характеризующиеся низкими уровнями фитиновой кислоты (Raboy et al., 1990 Maydica 35:383).
(C) Модифицированный углеводный состав, получаемый, например, при трансформации растений геном, кодирующим фермент, который изменяет структуру разветвления крахмала. Примеры таких ферментов включают ген фруктозилтрансферазы Streptococcus mucus (Shiroza et al., 1988, J. Bacteol. 170:810), ген левансахаразы Bacuillus subtilis (Steinmetz et al., 1985 Mol. Gen. Genel. 200:220), α-амилазу Bacillus licheniformis (Pen et al., 1992 Bio/Technology 10:292), гены инвертазы томата (Elliot et al., 1993), ген амилазы ячменя (Sogaard et al., 1993 J. Biol. Chem. 268:22480) и крахмал-разветвляющий фермент II эндосперма кукурузы (Fisher et al., 1993 Plant Physiol. 102:10450).
В следующем варианте осуществления трансген включает репортерный ген. В различных вариантах осуществления репортерный ген выбран из группы, состоящей из гена yfp, гена gus, гена rfp, гена gfp, гена устойчивости к канамицину, гена aad-1, гена aad-12, гена pat и гена резистентности к глифосату. Репортерный или маркерный гены для отбора трансформированных клеток или тканей, или частей растения, или растений могут быть включены в трансформирующие векторы. Примеры селективных маркеров включают маркеры, которые придают устойчивость к антиметаболитам, таким как гербициды или антибиотики, например, дигидрофолатредуктазу, которая придает устойчивость к метотрексату (Reiss, Plant Physiol. (Life Sci. Adv.) 13:143-149, 1994; см. также Herrera Estrella et al., Nature 303:209-213, 1983; Meijer et al., Plant Mol. Biol. 16:807-820, 1991); неомицинфосфотрансферазу, которая придает устойчивость к аминогликозидам неомицину, канамицину и паромицину (Herrera-Estrella, EMBO J. 2:987-995, 1983 and Fraley et al. Proc. Natl. Acad. Sci USA 80:4803 (1983)); гигромицин-фосфотрансферазу, которая придает устойчивость к гигромицину (Marsh, Gene 32:481-485, 1984; см. также Waldron et al., Plant Mol. Biol. 5:103-108, 1985; Zhijian et al., Plant Science 108:219-227, 1995); trpB, который позволяет клеткам использовать индол вместо триптофана; hisD, который позволяет клеткам использовать гистинол вместо гистидина (Hartman, Proc. Natl. Acad. Sci., USA 85:8047, 1988); маннозо-6-фосфатизомеразу, которая позволяет клеткам использовать маннозу (WO 94/20627); орнитиндекарбоксилазу, которая придает устойчивость к ингибитору орнитиндекарбоксилазы, 2-(дифторметил)-DL-орнитину (DFMO; McConlogue, 1987, в: Current Communications in Molecular Biology, Cold Spring Harbor Laboratory ed.); и деаминазу из Aspergillus terreus, которая придает устойчивость к бластицидину C (Tamura, Biosci. Biotechnol. Biochem. 59:2336-2338, 1995).
Дополнительные селективные маркеры включают, например, мутантную ацетолактатсинтазу, которая придает устойчивость к имидазолинону или сульфонилмочевине (Lee et al., EMBO J. 7:1241-1248, 1988), мутантный psbA, который придает устойчивость к атразину (Smeda et al., Plant Physiol. 103:911-917, 1993), или мутантную протопорфириногеноксидазу (см. патент США 5,767,373), или другие маркеры, придающие устойчивость к гербициду, такому как глуфосинат. Примеры подходящих генов селективных маркеров включают, без ограничения перечисленными, гены, кодирующие устойчивость к хлорамфениколу (Herrera Estrella et al., EMBO J. 2:987-992, 1983); стрептомицину (Jones et al., Mol. Gen. Genet. 210:86-91, 1987); спектиномицину (Bretagne-Sagnard et al., Transgenic Res. 5:131-137, 1996); блеомицину (Hille et al., Plant Mol. Biol. 7:171-176, 1990); сульфонамиду (Guerineau et al., Plant Mol. Biol. 15:127-136, 1990); бромоксинилу (Stalker et al., Science 242:419-423, 1988); глифосату (Shaw et al., Science 233:478-481, 1986); фосфинотрицину (DeBlock et al., EMBO J. 6:2513-2518, 1987) и т.п.
Одним из вариантов выбора для применения селективного гена является ДНК, кодирующая устойчивость к глуфосинату, и в одном варианте осуществления может быть фосфинотрицинацетил-трансферазой (pat), оптимизированным для кукурузы геном pat или геном bar под контролем промотора вируса мозаики жилок маниоки. Эти гены придают устойчивость к биалафосу. См., Wohlleben et al., (1988) Gene 70: 25-37); Gordon-Kamm et al., Plant Cell 2:603, 1990; Uchimiya et al., BioTechnology 11:835, 1993; White et al., Nucl. Acids Res. 18:1062, 1990; Spencer et al., Theor. Appl. Genet. 79:625-631, 1990; и Anzai et al., Mol. Gen. Gen. 219:492, 1989. Вариантом гена pat является оптимизированный для кукурузы ген pat, описанный в патенте США 6,096,947.
Кроме того, могут использоваться маркеры, которые облегчают идентификацию растительной клетки, содержащей полинуклеотид, кодирующий маркер. Пригодные для подсчета или скрининга маркеры могут применяться, когда присутствие последовательности дает поддающийся измерению продукт и может давать продукт без разрушения растительной клетки. Примеры включают ген β-глюкуронидазы, или uidA (GUS), который кодирует фермент, для которого известны различные хромогенные субстраты (например, патенты США 5,268,463 и 5,599,670); хлорамфениколацетил-трансферазы (Jefferson et al. The EMBO Journal vol. 6 No. 13 pp. 3901-3907) и щелочной фосфатазы. В предпочтительном варианте осуществления используемый маркер является бета-каротином или провитамином A (Ye et al, Science 287:303-305 (2000)). Этот ген использовали для повышения пищевой ценности риса, но в данном случае эго использовали в качестве пригодного для скрининга маркера, при этом присутствие гена, связанного с целевым геном, определяется по наличию золотистого цвета. В отличие от ситуации, когда ген используют для повышения пищевой ценности растения, для применения в целях мечения требуется меньшее количество белка. Другие пригодные для скрининга маркеры включают гены антоцианинов/флавоноидов (для получения общих сведений см. Taylor and Briggs, The Plant Cell (1990)2:115-127), включающие, например, ген R-локуса, который кодирует продукт, который регулирует выработку антоцианиновых пигментов (красный цвет) в растительных тканях (Dellaporta et al., в Chromosome Structure and Function, Kluwer Academic Publishers, Appels and Gustafson eds., стр. 263-282 (1988)); гены, которые регулируют биосинтез флавоноидных пигментов, такие как ген C1 кукурузы (Kao et al., Plant Cell (1996) 8: 1171-1179; Scheffler et al. Mol. Gen. Genet. (1994) 242:40-48) и C2 кукурузы (Wienand et al., Mol. Gen. Genet. (1986) 203:202-207); ген B (Chandler et al., Plant Cell (1989) 1:1175-1183), ген p1 (Grotewold et al, Proc. Natl. Acad. Sci USA (1991) 88:4587-4591; Grotewold et al., Cell (1994) 76:543-553; Sidorenko et al., Plant Mol. Biol. (1999)39:11-19); гены локуса bronze (Ralston et al., Genetics (1988) 119:185-197; Nash et al., Plant Cell (1990) 2(11): 1039-1049) и прочие.
Другие примеры подходящих маркеров включают ген голубого флуоресцентного белка (CYP) (Bolte et al. (2004) J. Cell Science 117: 943-54 и Kato et al. (2002) Plant Physiol 129: 913-42), ген желтого флуоресцентного белка (PHIYFP™ (Evrogen); см. Bolte et al. (2004) J. Cell Science 117: 943-54); ген lux, который кодирует люциферазу, присутствие которой может быть обнаружено при использовании, например, рентгеночувствительной пленки, сцинтилляционного измерения, флуоресцентной спектрофотометрии, высокочувствительных видеокамер, камеры со счетчиком фотонов или многолуночной люминометрии (Teeri et al. (1989) EMBO J. 8:343); ген зеленого флуоресцентного белка (GFP) (Sheen et al., Plant J. (1995) 8(5):777-84); и DsRed2, когда растительные клетки, трансформированные таким маркерным геном, окрашены в красный цвет и, таким образом, позволяют выполнить их визуальный отбор (Dietrich et al. (2002) Biotechniques 2(2):286-293). Дополнительные примеры включают ген β-лактамазы (Sutcliffe, Proc. Nat'l. Acad. Sci. U.S.A. (1978) 75:3737), который кодирует фермент, для которого известны различные хромогенные субстраты (например, PADAC, хромогенный цефалоспорин); ген xylE (Zukowsky et al., Proc. Nat'l. Acad. Sci. U.S.A. (1983) 80:1101), который кодирует катехолдиоксигеназу, которая может превращать хромогенные катехолы; ген α-амилазы ((Ikuta et al., Biotech. (1990) 8:241) и ген тирозиназы (Katz et al., J. Gen. Microbiol. (1983) 129:2703), который кодирует фермент, способный окислять тирозин до ДОФЫ и дофахинона, который в свою очередь конденсируется с образованием легко обнаруживаемого соединения - меланина. Очевидно, что множество таких маркеров доступно и известно специалисту в данной области.
Термин "процент идентичности" (или "% идентичности"), как известно в уровне техники, является отношением между двумя или более полипептидными последовательностями или двумя или более полинуклеотидными последовательностями, которое определяют при сравнении таких последовательностей. В уровне техники "идентичность" также означает степень сходства последовательности между полипептидными или полинуклеотидными последовательностями, в зависимости от обстоятельств, которую определяют при сравнении цепей таких последовательностей. "Идентичность" и "подобие" могут быть с легкостью вычислены известными методами, включающими, без ограничения перечисленными, методы, раскрытые в: 1) Computational Molecular Biology (Lesk, A. M., Ed.) Oxford University: NY (1988); 2) Biocomputing: Informatics and Genome Projects (Smith, D. W., Ed.) Academic: NY (1993); 3) Computer Analysis of Sequence Data, Part I (Griffin, A. M., and Griffin, H. G., Eds.) Humania: NJ (1994); 4) Sequence Analysis in Molecular Biology (von Heinje, G., Ed.) Academic (1987); и 5) Sequence Analysis Primer (Gribskov, M. and Devereux, J., Eds.) Stockton: NY (1991).
Методики определения идентичности последовательностей нуклеиновых кислот и аминокислот известны в уровне техники. Как правило, такие методики включают определение нуклеотидной последовательности мРНК гена и/или определение аминокислотной последовательности, кодируемой таким образом, и сравнение этих последовательностей со второй нуклеотидной или аминокислотной последовательностью. Геномные последовательности также могут быть определены и сравнены таким образом. Как правило, идентичность относится к точному нуклеотид-нуклеотидному или аминокислота-аминокислотному соответствию двух полинуклеотидных или полипептидных последовательностей, соответственно. Две или больше последовательностей (полинуклеотидных или аминокислотных) можно сравнивать путем определения их процента идентичности. Процент идентичности двух последовательностей, нуклеотидных или аминокислотных последовательностей, является количеством точных соответствий между двумя выровненными последовательностями, деленным на длину более коротких последовательностей и умноженным на 100. См. статью Russell, R., and Barton, G., "Structural Features can be Unconserved in Proteins with Similar Folds", J. Mol. Biol. 244, 332-350 (1994), на стр. 337, которая полностью включена в настоящую заявку посредством отсылки.
Кроме того, методы определения идентичности и подобия закодированы в публично доступных компьютерных программах. Выравнивания и вычисления процента идентичности последовательностей могут быть выполнены, например, при использовании программы AlignX в пакете Vector NTI® (Invitrogen, Carlsbad, CA) или программы MegAlign™ в пакете вычислительных программ LASERGENE для биоинформатики (DNASTAR Inc., Madison, WI). Множественное выравнивание последовательностей производят при использовании "метода выравнивания Clustal", который охватывает несколько вариантов алгоритма, включающего "метод выравнивания Clustal V", соответствующий методу выравнивания, обозначенному Clustal V (раскрыт в Higgins and Sharp, CABIOS. 5:151-153 (1989); Higgins, D.G. et al., Comput. Appl. Biosci., 8:189-191 (1992)), и который можно найти в программе MegAlign™ из пакета вычислительных программ LASERGENE для биоинформатики (DNASTAR Inc.). Для множественных выравниваний значения по умолчанию являются следующими: GAP PENALTY=10 и GAP LENGTH PENALTY=10. Параметры по умолчанию для парных выравниваний и вычисления идентичности процента белковых последовательностей при использовании метода Clustal являются следующими: KTUPLE=1, GAP PENALTY=3, WINDOW=5 и DIAGONALS SAVED=5. Для нуклеиновых кислот эти параметры являются следующими: KTUPLE=2, GAP PENALTY=5, WINDOW=4 и DIAGONALS SAVED=4. После выравнивания последовательностей при использовании программы Clustal V можно получить значения "процента идентичности" при просмотре таблицы "расстояний последовательностей" в той же программе. Кроме того, доступен "метод выравнивания Clustal W", который соответствует методу выравнивания, обозначенному Clustal W (описан в Higgins and Sharp, CABIOS. 5:151-153 (1989); Higgins, D.G. et al., Comput. Appl. Biosci. 8:189-191(1992)), и который можно найти в программе MegAlign™ v6.1 из пакета вычислительных программ LASERGENE для биоинформатики (DNASTAR Inc.). Параметры по умолчанию для множественного выравнивания (GAP PENALTY=10, GAP LENGTH PENALTY=0.2, Delay Divergen Seqs(%)=30, DNA Transition Weight=0.5, Protein Weight Matrix=Gonnet Series, DNA Weight Matrix=IUB). После выравнивания последовательностей при использовании программы Clustal W можно получить значения "процента идентичности" при просмотре таблицы "расстояний последовательностей" в той же программе.
Специалисту в данной области хорошо известно, что множество уровней идентичности последовательности может применяться при идентификации полипептидов из других биологических видов, где такие полипептиды имеют такую же или подобную функцию или активность. Полезные примеры процентов идентичности включают, без ограничения перечисленными: 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95%, или же любое целочисленное процентное значение от 55% до 100% может применяться в описании вариантов осуществления настоящего описания, такое как 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99%. Подходящие фрагменты нуклеиновых кислот не только обладают вышеуказанной гомологией, но обычно кодируют полипептид, содержащий по меньшей мере 50 аминокислот, предпочтительно по меньшей мере 100 аминокислот, более предпочтительно по меньшей мере 150 аминокислот, еще более предпочтительно по меньшей мере 200 аминокислот и наиболее предпочтительно по меньшей мере 250 аминокислот.
Термин "программа для анализа последовательностей" относится к любому компьютерному алгоритму или программе, которые могут применяться для анализа нуклеотидных или аминокислотных последовательностей. "Программа для анализа последовательностей" может быть доступна коммерчески или разработана независимо. Типичная программа для анализа последовательностей будет включать, без ограничения перечисленным: 1) пакет программ GCG (Wisconsin Package Version 9.0, Genetics Computer Group (GCG), Madison, WI); 2) BLASTP, BLASTN, BLASTX (Altschul et al., J. Mol. Biol., 215:403-410 (1990)); 3) DNASTAR (DNASTAR, Inc. Madison, WI); 4) Sequencher (Gene Codes Corporation, Ann Arbor, MI); и 5) программу FASTA, включающую алгоритм Смита-Ватермана (W. R. Pearson, Comput. Methods Genome Res., [Proc. Int. Symp.] (1994), Meeting Date 1992, 111-20. Editor(s): Suhai, Sandor. Plenum: New York, NY)). В рамках настоящей заявки подразумевается, что в тех случаях, когда программа для анализа последовательности используется для анализа, результаты анализа будут основаны на "значениях по умолчанию" указанной программы, если не определено иное. При использовании в настоящем описании, "значения по умолчанию" будут означать любой набор значений или параметров, которые первоначально загружаются с программой при первом запуске.
При ссылке на методики гибридизации, вся или часть известной нуклеотидной последовательности могут использоваться в качестве зонда, который селективно гибридизуется с другими соответствующими нуклеотидными последовательностями, присутствующими в популяции клонированных фрагментов геномной ДНК или фрагментов кДНК (то есть геномные или кДНК библиотеки) из выбранного организма. Гибридизационные зонды могут быть фрагментами геномной ДНК, фрагментами плазмидной ДНК, фрагментами кДНК, фрагментами РНК, ПЦР-амплифицированными фрагментами ДНК, олигонуклеотидами или другими полинуклеотидами, и могут быть мечены детектируемой группой, такой как 32P, или любым другим детектируемым маркером. Таким образом, например, зонды для гибридизации могут быть получены путем мечения синтетических олигонуклеотидов, которые основаны на последовательностях ДНК вариантов осуществления настоящего описания. Способы получения зондов для гибридизации и для конструирования кДНК и геномных библиотек общеизвестны в уровне техники и раскрыты (Sambrook и другие, 1989).
Нуклеотидные зонды и праймеры вариантов осуществления настоящего описания гибридизуются в строгих условиях с целевой последовательностью ДНК. Любой стандартный метод гибридизации или амплификации нуклеиновых кислот может использоваться для идентификации присутствия ДНК из трансгенного объекта в образце. Молекулы нуклеиновой кислоты или ее фрагменты способны специфично гибридизоваться с другими молекулами нуклеиновых кислот при определенных обстоятельствах. При использовании в настоящем описании, две молекулы нуклеиновой кислоты, как говорят, способны специфично гибридизоваться друг с другом, если эти две молекулы способны образовывать антипараллельные, двухцепочечные структуры нуклеиновой кислоты. Молекула нуклеиновой кислоты, как говорят, "комплементарна" другой молекуле нуклеиновой кислоты, если две молекулы нуклеиновой кислоты демонстрируют полную комплементарность. При использовании в настоящем описании, молекулы, как говорят, демонстрируют "полную комплементарность", когда каждый нуклеотид одной из молекул комплементарен нуклеотиду другой молекулы. Молекулы, которые демонстрируют полную комплементарность, обычно гибридизуются друг с другом с достаточной стабильностью, чтобы они могли оставаться соединенными друг с другом в обычных условиях "высокой строгости". Обычные условия высокой строгости описаны в Sambrook et al., 1989.
Две молекулы, как говорят, демонстрируют "минимальную комплементарность", если они могут гибридизоваться друг с другом с достаточной стабильностью, чтобы они могли оставаться соединенными друг с другом, по меньшей мере, при обычных условиях "низкой строгости". Обычные условия низкой строгости описаны в Sambrook et al., 1989. Чтобы молекула нуклеиновой кислоты могла служить в качестве праймера или зонда, она должна демонстрировать минимальную комплементарность последовательности, чтобы она могла формировать стабильную двухцепочечную структуру при определенных используемых концентрациях растворителя и солей.
Факторы, которые влияют на строгость гибридизации, известны специалистам и включают, без ограничения перечисленными, температуру, pH, ионную силу и концентрацию органических растворителей, таких как, например, формамид и диметилсульфоксид. Как известно специалистам в данной области, строгость гибридизации увеличивается при более высоких температурах, более низкой ионной силе и более низких концентрациях растворителя.
Термин "строгое условие" или "строгие условия" функционально определен в отношении гибридизации нуклеотидного зонда с целевой нуклеиновой кислотой (то есть со специфической последовательностью целевой нуклеиновой кислоты) согласно определенной методике гибридизации, обсуждаемой в Sambrook et al., 1989, в 9.52-9.55. См. также, Sambrook et al., 1989, в 9.47-9.52 и 9.56-9.58.
Как правило, строгие условия будут такими условиями, при которых концентрация солей меньше чем приблизительно 1,5М иона Na+, обычно концентрация иона Na+ (или других солей) составляет приблизительно 0,01-1,0М при pH 7,0-8,3, и температура составляет по меньшей мере приблизительно 30°C в случае коротких зондов (например, 10-50 нуклеотидов) и по меньшей мере приблизительно 60°C в случае длинных зондов (например, больше 50 нуклеотидов). Строгие условия могут также быть достигнуты при добавлении дестабилизирующих агентов, таких как формамид. Примерные условия низкой строгости включают гибридизацию с буферным раствором, содержащим 30-35% формамида, 1,0М NaCl, 0,1% ДСН (додецилсульфат натрия), при 37°C, и промывку в 1X-2X SSC (20X SSC=3,0М NaCl/0,3М цитрата тринатрия) при 50-55°C. Примерные условия умеренной строгости включают гибридизацию в 40% формамида, 1,0М NaCl, 0,1% ДСН, при 37°C, и промывку в 0,5X-1X SSC при 55-60°C. Примерные условия высокой строгости включают гибридизацию в 50% формамида, 1,0М NaCl, 0,1% ДСН, при 37°C, и промывку в 0,1X SSC при 60-65°C.
Специфичность обычно является функцией постгибридизационных промывок, причем наиболее важными факторами являются ионная сила и температура последнего промывочного раствора. В случае ДНК-ДНК гибридов Тп может быть приближенно получена из уравнения Тп=81,5°C+16,6(logM)+0,41(%GC)-0,61(%форм.)-500/L, гдеМ является молярной концентрацией моновалентных катионов, %GC является процентом нуклеотидов гуанозина и цитозина в ДНК, %форм. является процентом формамида в гибридизационном растворе, и L является длиной гибрида в парах нуклеотидов (Meinkoth and Wahl, 1984). Тп является температурой (при определенной ионной силой и pH), при которой 50% комплементарной целевой последовательности гибридизуется с идеально совпадающим зондом. Тп снижается приблизительно на 1°C для каждого 1% некомплементарного спаривания; таким образом, Тп, условия гибридизации и/или промывки можно регулировать для гибридизации последовательностей требуемой идентичности. Например, если осуществляется поиск последовательности с 90% идентичностью, Тп может быть снижена на 10°C. Как правило, строгие условия выбирают так, чтобы температура была приблизительно на 5°C ниже, чем температура плавления (Тп) для определенной последовательности и ее комплементарной последовательности при определенной ионной силе и pH. Впрочем, при особо строгих условиях может использоваться гибридизация и/или промывка при температуре на 1, 2, 3 или 4°C ниже температуры плавления (Тп); при умеренно строгих условиях может использоваться гибридизация и/или промывка при температуре на 6, 7, 8, 9 или 10°C ниже температуры плавления (Тп); при условиях низкой строгости может использоваться гибридизация и/или промывка при температуре на 11-20°C ниже температуры плавления (Тп). При использовании уравнения, растворов для гибридизации и промывки, а также требуемой Тп, средним специалистам будет очевидно, что по существу описаны изменения строгости гибридизации и/или промывочных растворов. Если требуемая степень некомплементарного спаривания приводит к Тп меньше 45°C (водный раствор) или 32°C (раствор в формамиде), предпочтительно повысить концентрацию SSC так, чтобы можно было использовать более высокую температуру. Подробное руководство по гибридизации нуклеиновых кислот можно найти в Ausubel et al, Short Protocols in Molecular Biology, стр. 2-40, Third Edit. (1997) и Sambrook et al. (1989).
В другом варианте осуществления настоящего описания раскрыт способ направленной интеграции полинуклеотидной донорной кассеты в геном растительной клетки. В некоторых вариантах осуществления экспрессируется сайт-специфическая ДНК-связывающая нуклеаза, включающая по меньшей мере один ДНК-связывающий домен и по меньшей мере один нуклеазный домен, где по меньшей мере один ДНК-связывающий домен связывается с целевым участком в геноме растительной клетки. В других вариантах осуществления растительную клетку подвергают контакту с полинуклеотидной донорной кассетой. В других вариантах осуществления целевой участок в геноме растительной клетки расщепляется сайт-специфической ДНК-связывающей нуклеазой. В еще одном варианте осуществления полинуклеотидная донорная кассета интегрируется в целевой участок в геноме растительной клетки.
В варианте осуществления раскрыта направленная интеграция полинуклеотидной донорной кассеты в геном растительной клетки посредством направленного гомологией механизма репарации. В другом варианте осуществления раскрыта направленная интеграция полинуклеотидной донорной кассеты в геном растительной клетки посредством направленного негомологичным соединением концов механизма репарации.
Донорные молекулы, раскрытые в настоящей заявке, интегрируются в геном клетки посредством направленных, независимых от гомологии способов. Для такой направленной интеграции геном расщепляют в нужном положении (или положениях) с использованием нуклеазы, например, слитых друг с другом ДНК-связывающего домена (например, цинк-пальцевый связывающий домен или TAL эффекторный домен конструируют для связывания целевого участка в или вблизи заданного участка расщепления) и нуклеазного домена (например, расщепляющего домена или расщепляющего полудомена). В некоторых вариантах осуществления два слитых белка, каждый из которых включает ДНК-связывающий домен и расщепляющий полудомен, экспрессируются в клетке и связываются с целевыми участками, которые расположены таким образом, что функциональный расщепляющий домен воссоздается, и ДНК расщепляется вблизи целевых участков. В одном варианте осуществления расщепление происходит между целевыми участками двух ДНК-связывающих доменов. Один или оба ДНК-связывающих домена могут быть сконструированы. См., также, патент США 7,888,121; патентную публикацию США 20050064474 и международные патентные публикации WO05/084190, WO05/014791 и WO 03/080809.
Нуклеазы, как описано в настоящей заявке, могут быть введены в виде полипептидов и/или полинуклеотидов. Например, два полинуклеотида, каждый из которых включает последовательности, кодирующие один из вышеуказанных полипептидов, могут быть введены в клетку, и когда полипептиды экспрессируются, и каждый из них связывается со своей целевой последовательностью, расщепление происходит в или вблизи целевой последовательности. В альтернативе один полинуклеотид, включающий последовательности, кодирующие оба слитых полипептида, вводят в клетку. Полинуклеотиды могут представлять собой ДНК, РНК или их любые модифицированные формы или аналоги ДНК и/или РНК.
После введения двухцепочечного разрыва в целевой области трансген интегрируется в целевую область направленным способом посредством независимых от гомологии методов (например, негомологичного соединения концов (NHEJ)), после линеаризации двухцепочечной донорной молекулы, как описано в настоящей заявке. Двухцепочечный донор предпочтительно линеаризуется in vivo нуклеазой, например, одной или более одинаковыми или различными нуклеазами, которые используются для введения двухцепочечного разрыва в геном. Синхронизированное расщепление хромосомы и донора в клетке может ограничивать деградацию донорной ДНК (по сравнению с линеаризацией донорной молекулы до введения в клетку). Целевые участки нуклеазы, используемые для линеаризации донора, предпочтительно не прерывают последовательность(и) трансгена(ов).
Трансген может быть интегрирован в геном в направлении, предполагаемом при простом лигировании нуклеазных липких концов (обозначенном "прямая" или "AB" ориентация) или в другом направлении (обозначенном "обратная" или "BA" ориентация). В некоторых вариантах осуществления трансген интегрируется после точного лигирования липких концов хромосомы и донора. В других вариантах осуществления интеграция трансгена в BA или AB ориентации приводит к делеции нескольких нуклеотидов.
IV. Анализы для обнаружения сайт-специфической интеграции донорного полинуклеотида
В варианте осуществления реакция амплификации является количественной. В других вариантах осуществления реакция амплификации является детектируемой. В различных вариантах осуществления детектирование может включать визуализацию в агарозном или акриламидном геле, секвенирование ампликона или использование сигнатурного профиля, где сигнатурный профиль выбран из группы, состоящей из сигнатурного профиля температур плавления или флуоресценции.
Молекула нуклеиновой кислоты вариантов осуществления настоящего описания или ее сегменты могут применяться в качестве праймеров для ПЦР-амплификации. При проведении ПЦР-амплификации между праймером и матрицей может быть допущена некоторая степень некомплементарности. Таким образом, мутации, делеции и вставки (в особенности присоединение нуклеотидов на 5' или 3' концах) в представленных праймерах включены в объем настоящего описания. Мутации, вставки и делеции могут быть введены в данный праймер с помощью методов, известных среднему специалисту.
Другим примером детектирования является методика пиросеквенирования, описанная Winge (Innov. Pharma. Tech. 00:18-24, 2000). В этом методе создают олигонуклеотид, который перекрывает место соединения геномной ДНК и ДНК вставки. Олигонуклеотид гибридизуют с одноцепочечным продуктом ПЦР из целевой области (один праймер во вставленной последовательности и один во фланкирующей геномной последовательности) и инкубируют в присутствии ДНК-полимеразы, АТФ, сульфурилазы, люциферазы, апиразы, аденозин-5'-фосфосульфата и люциферина. Отдельно добавляют дНТФ, при этом введение приводит к световому сигналу, который измеряют. Световой сигнал указывает на присутствие вставки трансгена/фланкирующей последовательности в результате успешной амплификации, гибридизации, и одного или множества оснований (данная методика используется для первоначального скрининга, но не для обнаружения определенного гена, когда он известен).
Молекулярные маяки были описаны для применения в детектировании. Коротко, создают FRET-олигонуклеотидный зонд, который перекрывается с участком соединения фланкирующей геномной ДНК и ДНК вставки. Уникальная структура FRET-зонда приводит к тому, что он содержит вторичную структуру, которая удерживает флуоресцентную группу и группу тушения в непосредственной близости. FRET-зонд и ПЦР праймеры (один праймер в последовательности ДНК вставки и один праймер во фланкирующей геномной последовательности) подвергают циклам в присутствии термостабильной полимеразы и дНТФ. После успешной ПЦР амплификации гибридизация FRET-зонда(ов) с целевой последовательностью приводит к устранению вторичной структуры зонда и пространственному разделению флуоресцентной группы и группы тушения. Флуоресцентный сигнал указывает на присутствие фланкирующей геномной/трансгенной вставленной последовательности в результате успешной амплификации и гибридизации.
Анализ с гидролизом зондов, также известный как TAQMAN® (Life Technologies, Foster City, Calif.), представляет собой метод детектирования и количественного определения присутствия последовательности ДНК. Коротко, создают FRET-олигонуклеотидный зонд с одним олигонуклеотидом в трансгене и одним олигонуклеотидом во фланкирующей геномной последовательности для трансген-специфичного детектирования. FRET-зонд и ПЦР праймеры (один праймер в последовательности ДНК вставки и один праймер во фланкирующей геномной последовательности) подвергают циклам в присутствии термостабильной полимеразы и дНТФ. Гибридизация FRET-зонда приводит к отщеплению и освобождению флуоресцентной группы от группы тушения на FRET-зонде. Флуоресцентный сигнал указывает на присутствие фланкирующей/трансгенной вставленной последовательности в результате успешной амплификации и гибридизации.
Анализы KASPar представляют собой метод детектирования и количественного определения присутствия последовательности ДНК. Коротко, образец геномной ДНК, включающей направленный геномный локус, подвергают скринингу с использованием анализа на основе полимеразной цепной реакции (ПЦР), известного как система анализа KASPar®. В анализе KASPar®, используемом при практическом осуществлении настоящего описания, может использоваться смесь для ПЦР анализа KASPar®, которая содержит множество праймеров. Праймеры, используемые в смеси для ПЦР анализа, могут включить по меньшей мере один прямой праймер и по меньшей мере один обратный праймер. Прямой праймер содержит последовательность, соответствующую определенной области донорного ДНК полинуклеотида, а обратный праймер содержит последовательность, соответствующую определенной области геномной последовательности. Кроме того, праймеры, используемые в смеси для ПЦР анализа, могут включать по меньшей мере один прямой праймер и по меньшей мере один обратный праймер. Например, в смеси для ПЦР анализа KASPar® могут использоваться два прямых праймера, соответствующие двум различным аллелям, и один обратный праймер. Один из прямых праймеров содержит последовательность, соответствующую определенной области эндогенной геномной последовательности. Второй прямой праймер содержит последовательность, соответствующую определенной области донорного ДНК полинуклеотида. Обратный праймер содержит последовательность, соответствующую определенной области геномной последовательности. Такой анализ KASPar® для детектирования реакции амплификации является вариантом осуществления настоящего описания.
В некоторых вариантах осуществления флуоресцентный сигнал или флуоресцентный краситель выбраны из группы, состоящей из флуоресцентного красителя HEX, флуоресцентного красителя FAM, флуоресцентного красителя JOE, флуоресцентного красителя TET, флуоресцентного красителя Cy 3, флуоресцентного красителя Cy 3.5, флуоресцентного красителя Cy 5, флуоресцентного красителя Cy 5.5, флуоресцентного красителя Cy 7 и флуоресцентного красителя ROX.
В других вариантах осуществления реакцию амплификации проводят при использовании подходящих вторых флуоресцентных красителей ДНК, которые способны окрашивать клеточную ДНК в диапазоне концентраций, обнаруживаемом с помощью проточной цитометрии, и имеют флуоресцентный спектр испускания, который детектируют с помощью аплификатора для ПЦР в реальном времени. Средним специалистам в данной области будет очевидно, что известны и непрерывно разрабатываются другие красители для нуклеиновых кислот. Может использоваться любой подходящий краситель для нуклеиновой кислоты с подходящими спектрами возбуждения и испускания, такой как YO-PRO-1®, SYTOX Green®, SYBR Green I®, SYTO11®, SYTO12®, SYTO13®, BOBO®, YOYO® и TOTO®. в одном варианте осуществления вторым флуоресцентным красителем для ДНК является SYTO13®, используемый в концентрации меньше 10 мкМ, меньше 4 мкМ или меньше 2,7 мкМ.
Варианты осуществления настоящего описания далее иллюстрируются следующими Примерами. Следует понимать, что эти Примеры представлены лишь в качестве иллюстрации. На основе вышеуказанных вариантов осуществления и следующих Примеров специалист сумеет установить существенные характеристики настоящего описания и без отступления от его сущности и объема сможет провести различные изменения и модификации вариантов осуществления настоящего описания, чтобы адаптировать их к различным применениям и условиям. Таким образом, различные модификации вариантов осуществления настоящего описания, в дополнение к показанным и описанным в настоящей заявке, будут очевидны специалистам в данной области техники из предшествующего описания. Такие модификации также должны быть включены в объем прилагаемой формулы изобретения. Следующее далее представлено в качестве иллюстрации и не должно ограничивать объем изобретения.
ПРИМЕРЫ
Пример 1: Создание цинковых пальцев для связывания геномных локусов в Zea mays
Цинк-пальцевые белки, направленные против идентифицированных последовательностей ДНК геномных локусов-мишеней Zea mays, были созданы, как описано ранее. См., например, Urnov et al., (2005) Nature 435:646-551. Пример целевой последовательности и спирали распознавания показаны в Таблице 1 (конструкции областей спиралей распознавания) и Таблице 2 (целевые участки). В Таблице 2 нуклеотиды в целевом участке, которые контактируют с ZFP спиралями распознавания, указаны заглавными буквами, а нуклеотиды, которые не контактируют, указаны строчными буквами. Целевые участки цинк-пальцевой нуклеазы (ZFN) были сконструированы для всех 72 выбранных геномных локусов в Zea mays. Многочисленные конструкции ZFP были разработаны и проверены с целью идентификации пальцев, которые связываются с наибольшим уровнем эффективности в дрожжевой прокси-системе с целевыми участками 72 различных репрезентативных геномных локусов, которые были идентифицированы и выбраны в Zea mays. Специфические спирали распознавания ZFP (Таблица 1), которые связываются с наибольшим уровнем эффективности с последовательностями распознавания цинковых пальцев, использовались для таргетинга и интеграции донорной последовательности в геном Zea mays.
Конструкции цинковых пальцев для выбранных геномных локусов Zea mays
(N/A означает "не применимо").
pDAB
QSSHLTR
Целевой участок выбранных геномных локусов Zea mays.
ctACTCCGTATGCGAAGGCAcg
AGAGCAGGCGAG
Конструкции цинковых пальцев репрезентативных геномных локусов Zea mays были включены в векторы экспрессии цинковых пальцев, кодирующие белок, имеющий по меньшей мере один палец со структурой CCHC. См., патентную публикацию США 2008/0182332. В частности, последний палец в каждом белке содержал CCHC каркас спирали распознавания. Неканонические последовательности, кодирующие цинковые пальцы, были слиты с нуклеазным доменом рестриктазы типа IIS, FokI (аминокислоты 384-579 в последовательности из Wah et al., (1998) Proc. Natl. Acad. Sci. USA 95:10564-10569), через линкер из четырех аминокислот и сигналом ядерной локализации opaque-2, полученным из Zea mays, с получением цинк-пальцевых нуклеаз (ZFN). См., патент США 7,888,121. Цинковые пальцы для различных функциональных доменов были выбраны для применения in vivo. Из многочисленных ZFN, которые были разработаны, получены и протестированы на связывание с предполагаемым целевым участком генома, нуклеазы ZFN, описанные в Таблице 2 выше, были идентифицированы как обладающие in vivo активностью и охарактеризованы как способные к эффективному связыванию и расщеплению уникальных геномных полинуклеотидных целевых участков Zea mays in planta.
Сборка конструкции ZFN
Плазмидные векторы, содержащие экспрессионные конструкции гена ZFN, которые были идентифицированы, как описано ранее, были разработаны и закончены при использовании навыков и методик, общеизвестных в уровне техники (см., например, Ausubel или Maniatis). Каждая ZFN-кодирующая последовательность была слита с последовательностью, кодирующей сигнал ядерной локализации opaque-2 (Maddaloni et al., (1989) Nuc. Acids Res. 17:7532), который был расположен перед цинк-пальцевой нуклеазой. Неканонические последовательности, кодирующие цинк-пальцевые нуклеазы, были слиты с нуклеазным доменом рестриктазы типа IIS FokI (аминокислоты 384-579 последовательности из Wah et al. (1998) Proc. Natl. Acad. Sci. USA 95:10564-10569). Экспрессию слитых белков направлял сильный конститутивный промотор гена убиквитина Zea mays, (который включает 5'-нетранслируемую область (UTR) (Toki et al., (1992) Plant Physiology 100; 1503-07). Кассета экспрессии также включала 3'-UTR (включающую терминатор транскрипции и сайт полиаденилирования) из гена пероксидазы 5 (Per5) Zea mays (патентная публикация США 2004/0158887). Автогидролизующийся 2A, кодирующий нуклеотидную последовательность из вируса Thosea asigna (Szymczak et al., (2004) Nat Biotechnol. 22:760-760), добавляли между двумя слитыми белками цинк-пальцевых нуклеаз, которые клонировали в конструкцию.
Плазмидные векторы собирали при использовании технологии IN-FUSION™ Advantage (Clontech, Mountain View, CA). Эндонуклеазы рестрикции были получены от New England BioLabs (Ipswich, MA), и ДНК лигазу T4 (Invitrogen, Carlsbad, CA) использовали для лигирования ДНК. Получение плазмид выполняли при использовании набора NUCLEOSPIN® Plasmid Kit (Macherey-Nagel Inc., Bethlehem, PA) или Plasmid Midi Kit (Qiagen) в соответствии с инструкциями поставщиков. Фрагменты ДНК выделяли при использовании набора для выделения из геля QIAQUICK GEL EXTRACTION KIT™ (Qiagen) после электрофореза в агарозном геле с трис-ацетатным буфером. Колонии всех реакций лигирования подергали первичному скринингу путем рестрикции минипрепарата ДНК. Плазмидную ДНК отобранных клонов секвенировали с помощью поставщика коммерческих услуг секвенирования (Eurofins MWG Operon, Huntsville, AL). Данные последовательностей были собраны и проанализированы с использованием программы SEQUENCHER™ (Gene Codes Corp., Ann Arbor, MI).
Сборка универсальной донорной конструкции
Для обеспечения быстрого тестирования большого количества целевых локусов была разработана и создана новая, гибкая система универсальной донорной последовательности. Универсальная донорная полинуклеотидная последовательность была совместима с высокопроизводительными методами конструирования векторов и анализа. Универсальная донорная система состояла по меньшей мере из трех модульных доменов: невариабельный ZFN-связывающий домен, аналитический и обладающий заданными пользователем свойствами домен и простая плазмидная основа для масштабирования вектора. Невариабельная универсальная донорная полинуклеотидная последовательность была общей для всех доноров и позволяла применять схему с конечным набором анализов, которые могут использоваться на всех целевых участках Zea mays, обеспечивая, таким образом, единообразие при оценке таргетинга и снижение длительности аналитического цикла. Модульная природа этих доменов обеспечивала возможность высокопроизводительной донорной сборки. Кроме того, универсальная донорная полинуклеотидная последовательность обладает другими свойствами, направленными на упрощение последующего анализа и оптимизацию интерпретации результатов. Она содержала последовательность асимметричного сайта рестрикции, которая позволяет разрезать продукты ПЦР на фрагменты определенного размера. Последовательности, содержащие вторичные структуры, которые, как предполагали, будут проблемными при ПЦР амплификации, были удалены. Универсальная донорная полинуклеотидная последовательность имела небольщой размер (меньше 3,0 тпн). Наконец, универсальная донорная полинуклеотидная последовательность была построена на основе высококопийной плазмиды pUC19, которая позволяет накапливаться большому количеству анализируемой ДНК в течение определенного времени.
В качестве варианта осуществления пример плазмиды, включающей полинуклеотидную последовательность универсальной донорной кассеты, представлен в SEQ ID NO:132 и на Фигуре 1. В дополнительном варианте осуществления полинуклеотидная последовательность донорной кассеты представлена как: pDAB111846, SEQ ID NO:133, Фигура 2; pDAB117415, SEQ ID NO:134, Фигура 3; pDAB117416, SEQ ID NO:135, Фигура 4; pDAB117417, SEQ ID NO:136, Фигура 5; pDAB117419, SEQ ID NO:137, Фигура 6; pDAB117434 SEQ SEQ ID NO:138, Фигура 7; pDAB117418, SEQ ID NO:139, Фигура 8; pDAB117420, SEQ ID NO:140, Фигура 9; и pDAB117421, SEQ ID NO:141, Фигура 10. В другом варианте осуществления могут быть сконструированы дополнительные последовательности, включающие универсальную донорную полинуклеотидную последовательность с функционально экспрессирующейся кодирующей последовательностью или нефункциональные (беспромоторные) экспрессирующиеся кодирующие последовательности. Различные домены (невариабельный ZFN-связывающий домен, аналитический и обладающий заданными пользователем свойствами домен, и простая плазмидная основа), которые составляют универсальную донорную систему, сопровождаются примечаниями для конструкций, как описано выше, в Таблице 3.
Примечания к векторам универсальной донорной системы для идентификации невариабельных ZFN-связывающих доменов, аналитического и обладающего заданными пользователем свойствами домена, и плазмидной основы.
2339-2373 пн
288-322 пн
В другом варианте осуществления универсальная донорная полинуклеотидная последовательность представляет собой малую 2-3 тпн модульную донорную систему, предоставленную в виде плазмиды. Это - минимальный донор, включающий любое количество ZFN-связывающих участков, короткую 100-150 пн матричную область, обозначенную как "ДНК X" или "последовательность UZI" или "аналитический домен" (SEQ ID NO:142 и SEQ ID NO:143), которая несет сайты рестрикции, и последовательности ДНК для подбора праймеров (праймеры подбирают с Тп на 10°C больше, чем любые расчетные вторичные структуры) или кодирующие последовательности, и простую плазмидную основу (Фигура 11). В варианте осуществления разработан аналитический домен: содержащий процент пары оснований гуанина и цитозина от 40 до 60%; не содержащий повторяющиеся последовательности длиной больше 9 пн (например, 5'-gtatttcatgtatttcat-3'); не содержащий ряд идентичных пар оснований протяженностью больше 9 пн; и не содержащий вторичной структуры, где вторичная структура составляет меньше чем 18 ккал/моль свободной энергии при вычислении с помощью Markham, N. R. & Zuker, M. (2008) UNAFold: программа для фолдинга и гибридизации нуклеиновых кислот. В Keith, J. M., editor, Bioinformatics, Volume II. Structure, Function and Applications, number 453, в Methods in Molecular Biology, глава 1, страницы 3-31. Humana Press, Totowa, NJ. ISBN 978-1-60327-428-9. См., Таблица 4. Вся плазмида вставлена посредством NHEJ после введения двухцепочечного разрыва ДНК на подходящем ZFN-связывающем участке; ZFN-связывающие участки могут быть включены тандемно. Этот вариант осуществления универсальной донорной полинуклеотидной последовательности является наиболее подходящим для быстрого скрининга целевых участков и ZFN, при этом последовательности, которые сложно амплифицировать, в доноре минимизированы.
Анализ состава аналитического домена по δG свободной энергии, количеству 9 пн отрезков идентичных пар оснований, количеству повторяющихся последовательностей длиной больше 9 пн и проценту гуанина/цитозина.
последователь-ностей длиной больше 9 пн
В другом варианте осуществления универсальная донорная полинуклеотидная последовательность состоит по меньшей мере из четырех модулей и несет неполные ZFN-связывающие участки, плечи гомологии, ДНК X с приблизительно 100 пн аналитической частью или с кодирующими последовательностями. Данный вариант осуществления универсальной донорной полинуклеотидной последовательности подходит для проверки NHEJ-опосредованной вставки гена во множестве целевых участков полинуклеотида, с несколькими ZFN (Фигура 12).
Универсальная донорная полинуклеотидная последовательность может применяться со всеми направляющими молекулами с определенными ДНК-связывающими доменами, с двумя механизмами направленной донорной вставки (NHEJ/HDR). Таким образом, когда универсальную донорную полинуклеотидную последовательность вводят совместно с соответствующей экспрессионной конструкцией ZFN, донорный вектор и геном кукурузы разрезаются в одном специфическом положении, которое определяется при связывании с конкретной ZFN. После линеаризации донор может быть включен в геном посредством NHEJ или HDR. Различные аналитические особенности при создании вектора могут быть также применены для определения цинкового пальца, который максимально повышает эффективность доставки при направленной интеграции (Фигура 13).
Пример 2: Методики трансформации Zea mays
Перед доставкой в протопласты Zea mays c.v. Hi-II, плазмидную ДНК для каждой ZFN конструкции получали из культур E. coli при использовании PURE YIELD PLASMID MAXIPREP SYSTEM® (Promega Corporation, Madison, WI) или PLASMID MAXI KIT® (Qiagen, Valencia, CA) согласно инструкциям поставщиков.
Выделение протопластов
Суспензию клеток Zea mays c.v. Hi-II поддерживали согласно схеме в течение 3,5 дней, 4 мл осажденных клеток (PCV) собирали и переносили в стерильные конические пробирки объемом 50 мл (Fisher Scientific), содержащие 20 мл раствора фермента (0,6% PECTOLYASE™, 6% CELLULASE™ ("Onozuka" R10; Yakult Pharmaceuticals, Japan), 4 мМ MES (pH 5,7), 0,6М маннита, 15 мМ MgCl2). Культуры закрывали и оборачивали пленкой PARAFILM™ и помещали на шейкер (Thermo Scientific, Vari Mix Platform Rocker) на 10 скорости для инкубирования в течение 16-18 часов при комнатной температуре до получения протопластов. После инкубирования клетки исследовали с помощью микроскопа на предмет качества обработки ферментами. Обработанные ферментами клетки фильтровали через клеточный фильтр с отверстиями 100 мкм, промывали 10 мл среды W5 [2 мМ MES (pH 5,7), 205 мМ NaCl, 167 мМ CaCl2, 6,7 мМ KCl], после чего фильтровали через 70 мкМ и 40 мкМ клеточные фильтры. 100 мкм и 40 мкм фильтры промывали 10 мл среды W5. Отфильтрованные протопласты вместе с промытой средой собирали в центрифужную пробирку объемом 50 мл, при этом конечный объем составлял приблизительно 40 мл. Затем 8 мл "тяжелого градиентного раствора" [500 мМ сахарозы, 1 мМ CaCl2, 5 мМ MES (pH 6,0)] медленно добавляли под слой протопластов/раствора фермента, центрифугировали в центрифуге с бакет-ротором в течение 15 минут при 300-350 × g. После центрифугирования приблизительно 7-8 мл слоя протопластов отбирали, промывали 25 мл W5 и центрифугировали в течение 15 минут при 180-200 × g. Затем протопласты ресуспендировали в 10 мл раствора MMG [4 мМ MES (pH 5,7), 0,6М маннита, 15 мМ MgCl2]. Протопласты подсчитывали при использовании гемоцитометра или проточного цитометра и разбавляли до плотности 1,67 миллиона на мл, используя MMG.
Трансформация протопластов, полученных из суспензионной культуры Zea mays c.v. Hi-II, при использовании ПЭГ
Приблизительно 0,5 миллиона протопластов (300 мкл в растворе MMG) переносили в пробирки объемом 2 мл, смешивали с 40 мкл ДНК и инкубировали при комнатной температуре в течение 5-10 минут. Затем добавляли 300 мкл свежеприготовленного раствора ПЭГ (36% ПЭГ 4000, 0,3М маннита, 0,4M CaCl2) и инкубировали смесь при комнатной температуре в течение 15-20 минут при периодическом перемешивании с переворачиванием пробирок. После инкубирования медленно добавляли 1 мл промывки W5, клетки осторожно перемешивали и осаждали протопласты с помощью центрифугирования при 180-200 × g в течение 15 минут. Осадок ресуспендировали в 1 мл среды WI [4 мМ MES (pH 5,7), 0,6М маннита, 20 мМ KCl], пробирку оборачивали алюминиевой фольгой и оставляли для инкубирования при комнатной температуре на ночь, приблизительно на 16 часов.
Трансформация ZFN и донора
Для каждого выбранного геномного локуса протопласты Zea mays трансфицировали геном yfp для контроля экспрессии, одной ZFN, одним донором и смесью ZFN и донора в соотношении 1:10 (по весу). Общее количество ДНК для трансфекции 0,5 миллиона протопластов составило 80 мкг. Все обработки проводили в трех или шести повторах. Для контроля экспрессии гена yfp использовали pDAB8393 (Фигура 14), содержащий промотор убиквитина 1 Zea mays - кодирующую последовательность желтого флуоресцентного белка - 3'UTR Per5 Zea mays и промотор актина 1 риса - кодирующую последовательность pat - кассеты экспрессии 3'UTR гена липазы Zea mays. В типовом эксперименте таргетинга 4 мкг одной ZFN или с 36 мкг донора использовали для котрансфекции, при этом к каждой обработке добавляли 40 мкг конструкции с репортерным геном YFP. Включение соответствующих количеств экспрессионной плазмиды с геном yfp в качестве наполнителя позволяет исследовать качество трансфекции во множестве локусов и воспроизвести обработки в повторах. Кроме того, использование соответствующих количеств экспрессионных плазмид с геном yfp позволяет выполнить быстрый поиск и устранение любых технических проблем в быстром направленном анализе донорной вставки.
Пример 3: Расщепление геномных локусов в Zea mays с помощью цинк-пальцевой нуклеазы
Трансфицированные ZFN протопласты Zea mays c.v. Hi-II собирали через 24 часа после трансфекции центрифугированием при 1600 об/мин в 2 мл пробирках EPPENDORF™ и удаляли супернатант. Геномную ДНК выделяли из осажденных протопластов при использовании набора QIAGEN PLANT DNA EXTRACTION KIT™ (Qiagen, Valencia, CA). Выделенную ДНК ресуспендировали в 50 мкл воды и определяли концентрацию с помощью NANODROP® (Invitrogen, Grand Island, NY). Целостность ДНК оценивали при разгоне образцов на электрофорезе в 0,8% агарозном геле. Все образцы были нормализованы (20-25 нг/мкл) для ПЦР амплификации с целью получения ампликонов для секвенирования (Illumina, Inc., San Diego, CA). ПЦР-праймеры к штрихкоду для амплификации областей, включающих каждую тестируемую последовательность распознавания ZFN из обработанных и контрольных образцов, подбирали и приобретали в IDT (Coralville, IA, очищенные с помощью ВЭЖХ). Оптимальные условия амплификации определяли с помощью градиентной ПЦР при использовании 0,2 мкМ подходящих штрихкод праймеров ACCUPRIME PFX SUPERMIX™ (Invitrogen, Carlsbad, CA) и 100 нг матричной геномной ДНК в реакции объемом 23,5 мкл. Параметры циклов являлись следующими: начальная денатурация при 95°C (5 минут) с последующими 35 циклами денатурации (95°C, 15 сек), отжигом (55-72°C, 30 сек), элонгацией (68°C, 1 мин) и конечной достройкой (68°C, 7 мин). Продукты амплификации анализировали в 3,5% TAE агарозных гелях и определяли подходящую температуру отжига для каждой комбинации праймеров, которую затем использовали при амплификации ампликонов из контрольных и обработанных ZFN образцов, как описано выше. Все ампликоны очищали в 3,5% агарозных гелях, элюируемых водой, и концентрации определяли с помощью NANODROP™. Для секвенирования следующего поколения (Next Generation Sequencing) приблизительно 100 нг ПЦР ампликона из обработанных ZFN и соответствующих контрольных протопластов кукурузы объединяли в пулы и секвенировали с использованием Illumina Next Generation Sequencing (NGS).
Исследовали активность расщепления подходящими ZFN в каждом из выбранных геномных локусов Zea mays. Короткие ампликоны, содержащие участки расщепления ZFN, амплифицировали с геномной ДНК и подвергали Illumina NGS из обработанных ZFN и контрольных протопластов. Вызванный ZFN разрез или двухцепочечный разрыв ДНК устраняли посредством механизма клеточной репарации NHEJ со вставкой или делецией нуклеотидов (инсерции-делеции) на участке расщепления, при этом наличие инсерций-делеций на участке расщепления, таким образом, является показателем активности ZFN и определяется с помощью NGS. Активность расщепления целевых специфичных ZFN оценивали как количество последовательностей с инсерциями-делециями на один миллион последовательностей высокого качества при использовании программы для анализа NGS (патентная публикация 2012-0173,153, анализ данных последовательностей ДНК) (Фигура 15). Активности в 5-100-кратном диапазоне по сравнению с контролями наблюдали для выбранных геномных локусов-мишеней в Zea mays и дополнительно подтверждали с помощью выравнивания последовательностей, которые показали разнообразный футпринт инсерций-делеций на каждом участке расщепления ZFN. Эти данные указывают, что выбранные геномные локусы Zea mays поддаются расщеплению ZFN нуклеазами. Дифференциальная активность на каждой мишени отражает ее состояние хроматина и возможность ее расщепления, а также эффективность экспрессии каждой ZFN.
Пример 4: Быстрый направленный анализ интеграции полинуклеотидной донорной последовательности в геномных локусах Zea mays с помощью цинк-пальцевой нуклеазы
Проверку таргетинга универсальной донорной полинуклеотидной последовательности в выбранные геномные локусы-мишени Zea mays посредством донорной вставки, опосредованной негомологичным соединением концов (NHEJ), выполняли при использовании полупроизводительного способа быстрого направленного анализа на основе протопластов. Для каждого выбранного геномного локуса-мишени Zea mays тестировали от трех до шести схем с ZFN, при этом таргетинг оценивали при измерении опосредованного ZFN расщепления с помощью методов секвенирования следующего поколения (Фигура 15), а донорную вставку - с помощью соединенительной внутренней-внешней ПЦР (Фигура 16). Выбранные геномные локусы Zea mays, которые были положительными в обоих анализах, идентифицировали как локусы-мишени.
Быстрый направленный ZFN анализ донорной вставки
С целью определения, могут ли выбранные геномные локусы Zea mays являться мишенью для донорной вставки, конструкцию ZFN и универсальную конструкцию донорного полинуклеотида совместно вводили в протопласты кукурузы, которые инкубировали в течение 24 часов перед выделением геномной ДНК для анализа. Если экспрессируемая ZFN была способна разрезать целевой связывающий участок и в выбранных геномных локусах-мишенях Zea mays, и в доноре, линеаризованный донор встраивался в расщепленный целевой участок в геноме кукурузы посредством механизма негомологичного соединения концов (NHEJ). Подтверждение направленной интеграции в выбранные геномные локусы-мишени Zea mays выполняли на основе стратегии "внутренней-внешней" ПЦР, где "внешний" праймер распознает последовательность в нативных геномных локусах, а "внутренний" праймер связывается с последовательностью в донорной ДНК. Праймеры подбирают таким образом, что только в том случае, когда донорная ДНК встраивается в выбранные геномные локусы-мишени Zea mays, ПЦР анализ будет давать продукт амплификации ожидаемого размера. Анализ внутренней-внешней ПЦР выполняют на 5'- и на 3'-концах соединения вставки. Праймеры, используемые для анализа интегрированных донорных полинуклеотидных последовательностей, представлены в Таблице 5.
ZFN донорная вставка в целевые локусы с использованием гнездовой "внутренней-внешней" ПЦР
Все ПЦР амплификации проводили с использованием набора TAKARA EX TAQ HS™ (Clonetech, Mountain View, CA). Первую внутреннюю-внешнюю ПЦР проводили в конечном объеме реакции 20 мкл, которая содержала 1X буфер TAKARA EX TAQ HS™, 0,2 мМ дНТФ, 0,2 мкМ "внешнего" праймера (Таблица 5), 0,05 мкМ "внутреннего" праймера (подобранного к универсальной донорной кассете, описанной выше), 0,75 единицы полимеразы TAKARA EX TAQ HS™ и 10 нг выделенной ДНК протопластов кукурузы. Реакцию затем проводили при использовании программы ПЦР, которая состояла из следующего: 94°C в течение 2 мин, 20 циклов при 98°C в течение 12 сек и при 68°C в течение 2 мин, затем 72°C в течение 10 мин и выдерживание при 4°C. Полученные в результате продукты ПЦР разгоняли в агарозном геле с маркером 1KB PLUS DNA LADDER™ (Life Technologies, Grand Island, NY) для визуализации.
Гнездовую внутреннюю-внешнюю ПЦР проводили в конечном объеме реакции 20 мкл, которая содержала 1X буфер TAKARA EX TAQ HS™, 0,2 мм дНТФ, 0,2 мкМ "внешнего" праймера (Таблица 5), 0,1 мкМ "внутреннего" праймера (подобранного к универсальной донорной кассете, описанной выше, Таблица 6), 0,75 единицы полимеразы TAKARA EX TAQ HS™ и 1 мкл первого продукта ПЦР. Реакцию затем проводили при использовании программы ПЦР, которая состояла из из следующего: 94°C в течение 2 мин, 31 цикл при 98°C в течение 12 сек, 66°C в течение 30 сек и 68°C в течение 45 сек, затем 72°C в течение 10 мин и выдерживание при 4°C. Полученные в результате продукты ПЦР разгоняли в агарозном геле с маркером 1KB PLUS DNA LADDER™ (Life Technologies, Grand Island, NY) для визуализации.
Список всех "внешних" праймеров для гнездового внутреннего-внешнего ПЦР анализа оптимальных геномных локусов.
CGCCACAAATCTGAACCAGCA
CCACGATCGACATTGATCTGGCTA
GCGACATATCAGGCCAACAGG
GGGATATGTGTCCTACCGTATCAGG
CCAGCATACAGTTAGGGCCCA
GTTGCCTTGGTAGGTCCAGC
CGAAAACTCAGCATGCGGGAA
GAGCCATCAGTCCAACACTGC
ACAGGCGTACAGCAACACCA
GACCCTATGGTGTTGGATCCCA
CGGGAGCTAGGCAACAAATCG
TCTGACTAAACGGGTGGATGCTG
CGGATCAGTTGATTCGCTCACTTTCA
GCCGAAAAGCAGCAACTGGAA
GATTGCTACGCAGACCGCCTA
CACTATTCCTCCGGCATGCAG
TGACCTATTGATCGGTCGGCTC
TGCCTTGAATCTCAGGGATGCA
GCCGAAGCTAACTAGCGGACA
CATGGAGTAGCAGCTGTGCTG
GAAAAGCAGTCACCGGCTCTG
CCATGGACATGAATTCGGCACG
CTTTTGCACCACGGAGCAGAC
GCTAGCAAAACTTTGAAGCTCGCTC
GAGGTCCCTTACGGGTCATCG
ACCAGGTCTATCTTGCGCAGAC
AATAGCGTGGTCGGGTCCTAG
ACGAACGATCCAAGGTGCAGT
TAGAGACGAGGACTCTGGGCT
AAGTCCAACATGGGCACAACC
CCTCGTTAAGGGTGCAGGTTG
CCAAGTCAGCTTCTAAGCCATCAAAC
AACCCTAGACTTCTGCCTGGTG
GCTCACTTACGAGCAGATCCCA
GGTGCACGCATGTTCTCATGT
TGTTTACCGCAGCCATGCTTG
GTTGTATACGGCATCCATCCGCT
GAATGAAACTGGTGGTCTGCTCC
CCGACGAGGTACAAGTAGCAGG
CCCGTAGTCCAGATTCTTGTGGT
GTCGTTTGTTCGGAAGGGGAG
CGTAGTTGTCCGGCATGTCCT
TGTATCCCTTCGGTGAGCACG
TGAATCGACTCGCTGACAGGTG
Список всех "внутренних" праймеров для гнездового внутреннего-внешнего ПЦР анализа оптимальных геномных локусов.
CCACGATCGACATTGATCTGGCTA
GGGATATGTGTCCTACCGTATCAGG
GTTGCCTTGGTAGGTCCAGC
GAGCCATCAGTCCAACACTGC
Праймеры для активности расщепления ZFN.
TGGCACTAATCTCACCGGCT
AGTCTTAGAAGTACGCTACCGT
TACTTGGCTTCGGCGGCGA
GGGTGACTTTTACGCGTCTCG
GGTCACGACGCATGGCCTAA
AGGATGCATGGATCACCGTC
GCTCTGTTGTGCAGCCGTAC
CGTTGCAGATACCACAGTGTAC
GCTAGTAGCTGTTTACACGGCGTCT
AGGTCGAGACAACCAAGTAGAG
ACAGGACATCGAGCTTGCAT
CAGAAGAAAGGCATCAACTCATG
CTCTTTCACCTCTACTTTTACTTCAG
ATTGAACCGTTGTCAAAGCCA
CACAGCGTCAGGGCGGTAAC
GGCACGCACCTGTCACTGAC
GTACGCGCCCGGGAACTCCT
CCTGCGGCCCACGTGCATCT
Применение внутреннего-внешнего ПЦР анализа в системе таргетинга протопластов представляет особую сложность, поскольку большое количество плазмидной ДНК использовали для трансфекции, при этом большое количество плазмидной ДНК остается в системе таргетинга протопластов и впоследствии ее выделяют вместе с клеточной геномной ДНК. Остаточная плазмидная ДНК может уменьшить относительную концентрацию геномной ДНК и понизить общую чувствительность обнаружения, а также может быть существенной причиной неспецифичных, аберрантных реакций ПЦР. Вызванная ZFN и основанная на NHEJ донорная вставка обычно проходит в прямой или обратной ориентации. Внутренний-внешний ПЦР анализ ДНК в случае прямой ориентации вставки часто демонстрирует ложноположительные полосы, возможно обусловленные общими областями гомологии вокруг ZFN связывающего участка в мишени и доноре, что может приводить к связыванию с праймером и удлинению неинтегрированной донорной ДНК во время процесса амплификации. Ложноположительные сигналы не наблюдались в анализах, в которых исследовали продукты вставки в обратной ориентации, и поэтому все направленные анализы донорной интеграции проводили с исследованием обратной донорной вставки в быстром направленном анализе. Для дополнительного повышения специфичности и снижения фона также применяли стратегию гнездовой ПЦР. В стратегии гнездовой ПЦР использовали вторую реакцию ПЦР амплификации, в которой амплифицировали более короткую область в первом продукте амплификации первой реакции ПЦР. Использование неравных количеств "внутренних" и "внешних" праймеров оптимизировало соединительную ПЦР еще больше для быстрого направленного анализа в выбранных геномных локусах.
Результаты анализа внутренней-внешней ПЦР визуализировали в агарозном геле. Для всех выбранных геномных локусов Zea mays "обработки ZFN + донор" давали полосу близкого к ожидаемому размера на 5' и 3' концах. Контрольные обработки только ZFN или только донором были отрицательными по ПЦР, что указывает на то, что способ давал специфичную оценку донорной интеграции в целевом участке. Все обработки проводили в трех - шести повторах, и присутствие ожидаемого продукта ПЦР в нескольких повторах (≥2 на обоих концах) использовали для подтверждения таргетинга. Донорная вставка посредством NHEJ часто дает побочные продукты с более низкой интенсивностью, которые образуются в результате процессинга линеаризованных концов на целевых и/или донорных сайтах ZFN. Кроме того, наблюдали, что различные ZFN обеспечивали различные уровни эффективности при направленной интеграции, причем некоторые ZFN обеспечивали неизменно высокие уровни донорной интеграции, некоторые ZFN обеспечивали менее стабильные уровни донорной интеграции, и другие ZFN не обеспечивали интеграции. В целом, для каждого из выбранных геномных локусов-мишеней Zea mays, которые были исследованы, направленная интеграция была продемонстрирована в репрезентативных геномных локусах-мишенях Zea mays одной или более ZFN, что подтверждает, что каждый из этих локусов мог служить мишенью. Кроме того, каждый из выбранных геномных локусов-мишеней Zea mays подходит для точной генной трансформации. Проверку этих выбранных геномных локусов-мишеней Zea mays повторяли несколько раз с получением аналогичных результатов каждый раз, подтверждая таким образом воспроизводимость процесса проверки, который включает создание плазмиды и конструкции, трансформацию протопластов, обработку образца и анализ образца.
Выводы
Донорную плазмиду и одну из ZFN, предназначенную для специфичного расщепления выбранных геномных локусов-мишеней Zea mays, трансфицировали в протопласты Zea mays c.v. Hi-II и через 24 часа собирали клетки. Анализ геномной ДНК, выделенной из контрольных, обработанных ZFN и обработанных ZFN и донором протопластов, при использовании внутренней-внешней соединительной ПЦР показал наличие направленной вставки универсального донорного полинуклеотида в результате расщепления геномной ДНК под действием ZFN (Таблица 8). Эти исследования показывают, что универсальная донорная полинуклеотидная система может применяться для оценки таргетинга на эндогенных участках и для скрининга кандидатных ZFN. Наконец, быстрый направленный анализ на основе протопластов и новые универсальные донорные полинуклеотидные системы обеспечивают улучшенную систему для скрининга геномных мишеней и ZFN для работ в области точной геномной инженерии в растениях. Способы могут быть дополнены для оценки сайт-специфического расщепления и донорной вставки в геномных мишенях в любой представляющей интерес системе при использовании любой нуклеазы, которая вводит двухцепочечные или одноцепочечные разрывы ДНК.
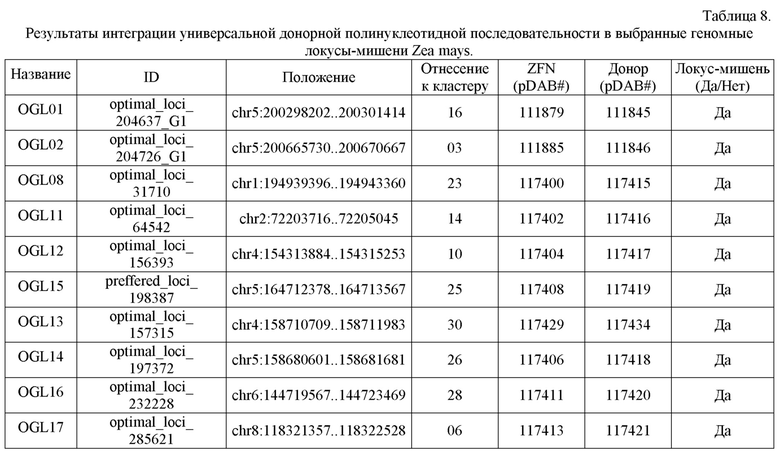
Пример 5: Получение и трансфекция протопластов кукурузы
Протопласты получали из суспензии клеток Zea mays c.v. Hi-II при инкубировании с ферментами, разрушающими клеточную стенку (целлюлаза, "Onozuka" R10 - Yakult Pharmaceuticals, Japan; и пектолаза, 320952 - MP Biomedicals, Santa Ana, CA), и очищали при использовании градиента сахарозы. Для трансфекции протопласты разбавляли до концентрации 1,67 миллиона/мл при использовании MMG (MES, pH 6,0, 0,6M маннита, 15 мМ MgCl2) и отбирали аликвоты 300 мкл протопластов (~500000) в стерильные пробирки объемом 2 мл, затем плазмидную ДНК (включающую кассету экспрессии трансгена YFP, кассету экспрессии трансгена ZFN, кассету экспрессии донорного полинуклеотидного трансгена, комбинированную кассету экспрессии ZFN/донорного полинуклеотидного трансгена) добавляли в общей концентрации 40 мкг в каждую 2 мл пробирку, осторожно перемешивали и инкубировали в течение 5-10 минут при комнатной температуре. Затем 300 мкл ПЭГ 4000 добавляли к раствору протопластов/ДНК и переворачивали смесь до полного перемешивания ПЭГ 4000 с раствором протопластов/ДНК. Затем смесь протопластов/ДНК/ПЭГ инкубировали при комнатной температуре в течение 15-20 минут. После инкубирования смесь протопластов/ДНК/ПЭГ промывали 1 мл W5 (2 мМ MES, pH 6,0, 205 мМ NaCl, 167 мМ CaCl2, 6,7 мМ KCl) и центрифугировали при 180-200 × g в течение 15 минут. После удаления супернатанта добавляли 1 мл среды WI (4 мМ MES, pH 6,0, 0,6М маннита, 20 мМ KCl) и ресуспендировали осадки протопластов клеток. Ресуспендированные осадки закрывали алюминиевой фольгой и оставляли на ночь. Эффективность трансфекции протопластов вычисляли при использовании проточного цитометра Quanta Flowcytometer™ производства Beckman-Coulter Inc (Brea, CA) и получали эффективность трансфекции в пределах 10-50%. Все обработки трансфекции выполняли в шести повторах.
Аналогичную методику трансфекции, как описанную ранее для полученных протопластов Zea mays c.v. Hi-II, применяли для выделения протопластов Zea mays c.v. B104. Протопласты получали из ювенильной ткани обвертки при нарезке обвертки вручную на тонкие (приблизительно 0,5 мм) полосы, а затем разрезая поперек. Нарезанную ткань перемещали в стерильную колбу Эрленмейера, содержащую 25 мл ферментного раствора, и помещали колбу в сушильную камеру на 15 минут. Затем колбы закрывали, накрывали алюминиевой фольгой и устанавливали в орбитальный шейкер на минимальной скорости при комнатной температуре.
Пример 6: Быстрый направленный анализ донорного полинуклеотида, интегрированного в сконструированный посадочный геномный участок
Донорная вставка в сконструированном локусе в кукурузе: анализ использовали, чтобы продемонстрировать вставку 5 тпн донора в целевой сконструированный посадочный участок 1 (ELP1) в геноме, как описано в заявке на патент США 2011/0191899. Донорную ДНК встраивали в геном линии протопластов Zea mays c.v. Hi-II (эта линия, "106685[1]-007", была получена в результате трансформации и интеграции pDAB106685) с помощью метода NHEJ интеграции. Донор интегрировался по сайтам связывания цинковых пальцев ZFN1 и ZFN3 (Фигура 18). Подход, используемый для NHEJ-опосредованной интеграции в геномной мишени ELP1, требовал, чтобы мишень ELP1 и донорные плазмиды содержали идентичные сайты ZFN (ZFN1 или ZFN3). Поскольку донорную полинуклеотидную последовательность и ZFN трансфицировали в протопласты клеток, ZFN разрезала геномную мишень ELP1 и донорную плазмидную ДНК с получением в результате идентичных концов. Полученные идентичные концы лигировали с помощью NHEJ-опосредованной репарации клеток, которая приводила к направленной вставке донорной плазмидной ДНК в геномную мишень ELP1. Таргетинг в геномную мишень ELP1 был продемонстрирован с двумя различными молярными отношениями ZFN-донор (1:1 и 1:10). Результаты донорной интеграции подтверждали при использовании анализа разрыва локуса и внутренней-внешней ПЦР, но не включали неравные концентрации ПЦР праймеров. Вставка донорной полинуклеотидной последовательности может проходить в двух ориентациях, при этом внутренняя-внешняя ПЦР была разработана для обнаружения обеих ориентаций.
Анализ разрыва: анализ разрыва представляет собой анализ с гидролизом зондов (аналогичный Taqman™), который позволяет определить, был ли изменен или перегруппирован связывающий участок ZFN последовательности геномной ДНК. Соответственно, проводят анализ интактности связывающего участка ZFN. ZFN опосредует донорную вставку или расщепление, которое впоследствии сопровождается NHEJ репарацией, приводящей к потере связывающих участков ZFN и снижению обнаруживаемого сигнала кПЦР (см. патентную публикацию США 2014/0173783, включенную в настоящую заявку посредством отсылки). Результаты ELP1 расщепления по сайтам ZFN1 и ZFN3 и направленная интеграция донорной последовательности по указанными сайтам представлены на Фигуре 19. Сайт ZFN1 анализировали с доставкой полинуклеотида ZFN и в сочетании с ZFN и донорным полинуклеотидом в соотношении 1:1 и 1:10. Результаты показали, что ZFN1 сайт ELP1 был прерван, что указывает на потенциальный таргетинг в этом сайте. Аналогичным образом, ZFN3 сайт ELP1 был прерван, что указывает на потенциальный таргетинг в этом сайте. Все обработки выполняли в 6 повторах для этого эксперимента, и данные представлены как средний результат.
Внутренний-внешний ПЦР анализ: Для подтверждения направленной донорной вставки по ZFN1 и ZFN3 в ELP1 внутреннюю-внешнюю ПЦР проводили на геномной ДНК, выделенной из образцов контрольных протопластов (например, протопластов, обработанных только ZFN полинуклеотидами или донорными полинуклеотидами), и образцов протопластов, обработанных ZFN и донорными полинуклеотидами. ПЦР праймеры подбирали для амплификации и обнаружения донорной вставки в любой ориентации. Результаты внутренней-внешней ПЦР показали наличие направленной донорной вставки по обоим сайтам ZFN1 и ZFN3 в ELP1 для всех протестированных образцов (например, отношения донора к ZFN 1:1 и 1:10). Сайты ZFN1 являлись мишенью четыре из шести раз, и сайты ZFN3 являлись мишенью три из шести раз. Донорные вставки в прямой и обратной ориентациях были обнаружены с помощью внутреннего-внешнего ПЦР анализа. Секвенирование материала ПЦР показало ожидаемые соединенные последовательности мишени-донора, а также соединения, где донор и/или мишень были процессированы перед лигированием (Фигура 20).
Пример 7: Быстрый направленный анализ донорного полинуклеотида, интегрированного в эндогенные локусы кукурузы
Геномный локус кукурузы объект DAS-59132 (называемый в настоящем описании E32), описанный в патентной публикации США 2014/0173783, включенной в настоящую заявку посредством отсылки, являлся мишенью для вставки донорного полинуклеотида. Донорный полинуклеотид длиной 5 тпн, который содержал трансген aad-1 (pDAB100651), направляли в эндогенный локус в кукурузе (E32) при использовании E32ZFN 6 (pDAB 105906). Сайт-специфическую интеграцию донорной полинуклеотидной последовательности в геном кукурузы подтверждали при помощи Быстрого направленного анализа с применением новых внутренних-внешних ПЦР анализов на 5' конце и 3' конце вставки донорного полинуклеотида (Фигура 21).
Применение Быстрого направленного анализа в качестве внутреннего-внешнего ПЦР анализа для системы трансфекции протопластов представляло особую сложность, поскольку система трансфекции протопластов является процессом транзиентной трансформации. Таким образом, большой избыток плазмидной ДНК, введенной в протопласты клеток, останется в системе и может быть выделен вместе с клеточной геномной ДНК. Введение больших количеств плазмидной ДНК не только уменьшает эффективную концентрацию геномной ДНК, что делает обнаружение геномного таргетинга сложным, но также приводит к неспецифичным реакциям ПЦР, которые дают ложноположительные сигналы.
При разработке внутреннего-внешнего ПЦР анализа Быстрого направленного анализа идентифицировали один основной источник ложноположительных сигналов в системе протопластов. Как было доказано во время этих исследований, донорная вставка на основе NHEJ может проходить в двух различных направлениях, донор может быть встроен в геном в прямой или обратной ориентации. Внутренняя-внешняя ПЦР амплификация и анализ вставки в прямой ориентации часто приводили к получению ампликонов с высокой интенсивностью сигналов, которые являлись ложноположительными. Напротив, внутренняя-внешняя ПЦР амплификация и анализ вставки в обратной ориентации не приводили к получению больших количеств ложноположительных ампликонов. Следует отметить, что донорный полинуклеотид и эндогенный локус E32 имеют одинаковые ZFN связывающие участки, которые могут вызывать перекрестную реакцию ПЦР (как показано на Фигуре 22). Ложноположительные сигналы, вероятно, являются побочным продуктом, который образуется в результате перекрестной реакции, вызванной репликацией матрицы, которая дает удлиненную амплифицированную цепь, которая включает ZFN связывающий участок. Полученная в результате амплифицированная цепь может затем связываться с ZFN связывающим участком эндогенных геномных последовательностей или с донорной полинуклеотидной последовательностью в следующем цикле ПЦР, что дает ложноположительную матрицу, которая амплифицируется реакцией ПЦР.
Асимметричная гнездовая внутренняя-внешняя (ANIO) ПЦР: Для дополнительного уменьшения неспецифичной ПЦР амплификации была разработана стратегия гнездовой внутренней-внешней ПЦР, которая позволяет использовать вторую внутреннюю-внешнюю ПЦР амплификацию для амплификации области в первом ампликоне внутренней-внешней ПЦР. Последующая ПЦР амплификация дополнительно увеличивала специфичность и обнаружение таргетинга и интеграции донора в геномном локусе. Во время разработки и осуществления гнездовой ПЦР реакции идентифицировали другое новое усовершенствование для уменьшения неспецифичной амплификации. Из-за присутствия больших количеств донорной плазмидной ДНК предполагали, что "внутренние" праймеры, которые связываются с донорной ДНК, могут в значительной степени способствовать появлению ложноположительных сигналов. При уменьшении концентрации "внутренних" праймеров по сравнению с концентрацией "внешних" праймеров, ложноположительные сигналы были существенно снижены. В итоге асимметричную гнездовую внутреннюю-внешнюю (ANIO) ПЦР использовали для демонстрации таргетинга донорного полинуклеотида в локус Zea mays E32 в протопластах клеток. Все ПЦР праймеры были подобраны на основе плазмиды положительного контроля, сконструированной для моделирования направленной вставки в локус E32 (Таблица 9).
Список праймеров для ANIO ПЦР показан в Таблице ниже.
В частности, первую внутреннюю-внешнюю ПЦР проводили в конечном объеме реакции 20 мкл, которые содержали 1X буфер TaKaRa Ex Taq HS™, 0,2 мМ дНТФ, 0,2 мкМ "внешнего" праймера, 0,05 мкМ "внутреннего" праймера, 0,75 единицы полимеразы TaKaRa Ex Taq HS™ и 10 нг выделенной ДНК протопластов кукурузы. Реакцию ПЦР проводили при использовании программы ПЦР, которая состояла из следующего: 94°C в течение 2 мин, 20 циклов при 98°C в течение 12 сек и 68°C в течение 2 мин, затем 72°C в течение 10 мин и выдерживание при 4°C.
Гнездовую (или вторую) внутреннюю-внешнюю ПЦР проводили в конечном объеме реакции 20 мкл, которые содержали 1X буфер TaKaRa Ex Taq HS™, 0,2 мМ дНТФ, 0,2 мкМ "внешнего" праймера, 0,1 мкМ "внутреннего" праймера, 0,75 единицы полимеразы TaKaRa Ex Taq HS™ и 1мкл первого ПЦР продукта. Реакцию проводили при использовании программы ПЦР, которая состояла из следующего: 94°C в течение 2 мин, 31 цикл при 98°C в течение 12 сек, 66°C в течение 30 сек и 68°C в течение 45 сек, затем 72°C в течение 10 мин и выдерживание при 4°C. Конечные продукты ПЦР разгоняли в агарозном геле с маркером 1Kb Plus DNA Ladder™ (Life Technologies, Grand Island, NY) для визуализации.
Быстрый направленный анализ обнаружил вставку донорного полинуклеотида в геномном локусе-мишени E32 в обратной ориентации. Из образцов, которые обработали комбинацией ZFN и донора, шесть из шести реакций привели к ампликонам ожидаемых размеров для 5' и для 3' концов (по сравнению с контролями, которые не показали сайт-специфической интеграции донорной полинуклеотидной последовательности). В отношении амплификаций 3' концов, на агарозном геле наблюдали небольшой шмер или лестницу. Это наблюдение, вероятно, обусловлено процессингом концов в разрывах ДНК, образующихся перед репарацией NHEJ. Кроме того, амплификацию неспецифического ампликона наблюдали в контрольных образцах, состоящих из "одного донора", при амплификации 3'-концов. Этот неспецифический ампликон имел меньшую молекулярную массу по сравнению с ожидаемым размером ампликона положительного контроля. Тем не менее, донорный полинуклеотид успешно интегрировался в целевой геномный локус E32, и Быстрый направленный анализ применили для эффективной идентификации и обнаружения сайт-специфических интегрантов.
Пример 8: Направленный анализ донорного полинуклеотида, интегрированного в эндогенные локусы сои
Разработанные ZFN трансформировали в протопласты сои, используя вышеописанную методику трансформации. Эффективность расщепления локуса FAD2 оценивали для различных ZFN с помощью анализа разрыва локуса, как описано в патентной публикации США 2014/0173783. Кроме того, опосредованную цинк-пальцевой нуклеазой интеграцию донорной последовательности в локусы FAD2 оценивали при использовании внутреннего-внешнего ПЦР анализа и секвенировали полученные ПЦР ампликоны, чтобы охарактеризовать донорную интеграцию в геном сои.
Эксперименты состояли из групп обработки, содержащих только донорный вектор, только вектор ZFN или комбинацию ZFN и донорного векторов (Таблица 10). Кроме того, эксперименты включали группы обработки отрицательного контроля из нетрансформированных клеток или клеток, трансформированных контрольным вектором pDAB7221 (Фигура 23), содержащим кассету экспрессии зеленого флуоресцентного белка под контролем промотора CsVMV и фланкированную 3'-UTR AtuORF24 в высококопийной плазмиде. Трансформированные образцы собирали приблизительно через 18-24 часа после трансфекции. Предварительные данные продемонстрировали высокую активность F2, ZFN, содержащейся в плазмиде, pDAB115601 и, следовательно, эту плазмиду ZFN использовали в качестве положительного контроля во всех последующих экспериментах.
Как подробно показано в Таблице 10, эксперименты трансформации содержали в общей сложности 80 мкг ДНК, при этом плазмиду pDAB7221 добавляли при необходимости, чтобы довести общее количество ДНК до 80 мкг. Отношение донорного вектора к ZFN-экспрессирующей плазмиде составляло приблизительно 10:1. Каждый эксперимент или обработка состояли из шести экспериментальных повторов, которые обрабатывали и анализированы независимо. Эксперименты по оценке ZFN проводили в двух наборах экспериментов.
Схема эксперимента. Плазмиды ZFN оценивали в двух наборах (F2 ZFN 1-3 и F2 ZFN 4-7). Донорные векторы, подходящие для плазмид ZFN, использовали в экспериментах таргетинга. Для каждой обработки выполняли шесть повторов.
Анализ таргетинга: образцы ДНК из экспериментов таргетинга анализировали при использовании анализа разрыва локуса для обнаружения модификаций в участках расщепления ZFN FAD2 и для оценки таргетинга NHEJ. Анализ кПЦР разработали для измерения интактных ZFN связывающих участков в мишенях FAD2. Опосредованная ZFN донорная вставка или расщепление, сопровождаемое NHEJ репарацией, приводит к потере ZFN связывающего участка и последующему снижению обнаруживаемого сигнала кПЦР. ZFN, которые обладают значительной расщепляющей активностью, обеспечивают получение ампликонов с пониженным сигналом по сравнению с обработкой только одним донором. Праймеры и зонды, используемые в анализе разрыва локуса, показаны в Таблице 11, а их относительные положения в локусах FAD2 показаны на Фигуре 24.
Обработка протопластов FAD2 2.3 ZFN2_WT ZFN (оба эксперимента) и FAD2 2.6 ZFN ZFN4_HF (один эксперимент) и F2 ZFN5_HF (оба эксперимента) в присутствии соответствующих донорных векторов приводила к статистически значимо более слабому сигналу по сравнению с сигналом, полученным от интактной последовательности (только донор).
Праймеры и зонды для прерывающей ПЦР
GTAATATGGGCTCAGAGGAATGGT
ATGGAGAAGAACATTGGAATTGC
CCATGGCCCGGTACCATCTGGTC
CACGAGTGTGGTCACCATGCCTT
TGAGTGTGACGAGAAGAGAAACAGCC
AGCAAGTACCAATGGGTTGATGATGTTGTG
TGCAAGCCACTACCACCCTTATGC
ZFN7
GGCAAAGTGTGTGTGCTGCAAATATG
ZFN7
CTAACCGTGAGAGGCTTCTGATCTATGTCTCTGA
TGAGTGTGATGAGAAGAGAAGCAGCC
AGCAAGTACCCATGGGTTGATGATGTTATG
CACGAGTGTGGTCACCATGCCTT
TTGGTTTGGCTGCTATGTGTTTATGG
TGTGGCATTGTAGAGAAGAGATGGTGAG
AGGGAGCTTTGGCAACTATGGACAGAGATTAT
AGCCTTCAATGTCTCTGGCAGACCCT
ZFN5
GGCATAGTGTGTGTGCTGCAGATATG
ZFN5
CAAATCGTGAGAGGCTTTTGATCTATGTCTCTGA
ZFN5
Локус-специфическая внутренняя-внешняя ПЦР: Для подтверждения направленной донорной вставки, ДНК из всех обработок подвергали локус-специфическому внутреннему-внешнему ПЦР анализу. Донорный вектор в экспериментах содержал связывающие участки для всех ZFN, которые тестировали на направленную интеграцию в локус FAD2. Cовместная доставка ZFN и донора в клетки сои приводила к расщеплению ZFN связывающих участков в мишени и в донорном векторе и к последующей интеграции донора в расщепленный локус FAD2 посредством механизма негомологичного соединения концов. Концы участка хромосомы FAD2 и линеаризованного донорного вектора, которые образовались при расщеплении ZFN, подвергаются обработке перед интеграцией в локус FAD2, и это может приводить к несовершенным продуктам соединения концов. Подтверждение направленной интеграции в мишень выполняли на основе стратегии "внутренней-внешней" ПЦР, где "внешний" праймер распознает последовательность в нативном геномном локусе, а "внутренний" праймер связывается с последовательностью в донорной ДНК. Внутренний-внешний ПЦР анализ проводили на 5'- и на 3'-концах соединения вставки.
Все протестированные ZFN продемонстрировали некоторое подтверждение таргетинга и интеграции донорного фрагмента в локус сои FAD2 по меньшей мере в одном эксперименте, как определили по продукту ПЦР в донорных и ZFN образцах. Результаты донорного интегрированного таргетинга с использованием следующих ZFN: F2 ZFN2_WT, F2 ZFN2_HF и F2 ZFN4_HF были воспроизводимыми, поскольку продукты ПЦР были получены по меньшей мере в 2 из 6 экспериментальных повторов на 5'- и на 3'-концах (Таблица 12).
Результаты NHEJ таргетинга в локус FAD2 в протопластах сои. Количество повторов, положительных во внутренней-внешней ПЦР в независимых экспериментах таргетинга, показано для экспериментов или обработок.
Секвенирование продуктов внутренней-внешней ПЦР: Два ампликона (ожидаемого размера) из каждого из экспериментов таргетинга с внутренней-внешней ПЦР, выполненных с pDAB1115620 и F2 ZFN2_WT или pDAB1115620 и F2 ZFN2_HF, клонировали в плазмиду. Полученную плазмиду секвенировали при использовании метода секвенирования Сэнгера. Последовательности выравнивали с референсной последовательностью, в которой одноцепочечные 4 пн концы, которые, как предполагалось, будут образовываться при расщеплении FokI, дублировали с получением всех возможных комбинаций концов. Десять уникальных структур последовательностей были обнаружены в 23 полученных клонированных последовательностях (Фигура 25). Все структуры последовательностей сохранили часть геномной референсной последовательности FAD2, расположенной между ZFN связывающими участками (GAAATTTC), но структуры последовательностей также имели делеции по сравнению с геномной референсной последовательностью FAD2. Последовательности 4WT1 и 4WT4 содержали делеции, которые распространялись на ZFN связывающий участок на 3' конце последовательности GAAATTTC. Две последовательности, 1HF4 и 6HF4, имели однонуклеотидные вставки. Наблюдаемые структуры последовательностей ДНК демонстрируют, что происходил таргетинг донорной ДНК в локус FAD2 сои.
Хотя аспекты настоящего изобретения были описаны в некоторых вариантах осуществления, они могут быть дополнительно изменены в рамках сущности и объема настоящего описания. Таким образом, предполагается, что настоящая заявка охватывает любые вариации, применения или адаптации вариантов осуществления изобретения при использовании его общих принципов. Кроме того, предполагается, что настоящая заявка охватывает такие отступления от настоящего описания как находящиеся в рамках известной или общепринятой практики в данной области техники, к которой относятся данные варианты осуществления и которые включены в рамки прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| УНИВЕРСАЛЬНАЯ ДОНОРНАЯ СИСТЕМА ДЛЯ НАПРАВЛЕННОГО ВОЗДЕЙСТВИЯ НА ГЕНЫ | 2014 |
|
RU2687369C2 |
| СКОНСТРУИРОВАННАЯ СПОСОБАМИ ИНЖЕНЕРИИ ПЛАТФОРМА ДЛЯ ВСТРАИВАНИЯ ТРАНСГЕНА (ETIP) ДЛЯ НАЦЕЛИВАНИЯ ГЕНОВ И СТЭКИНГА ПРИЗНАКОВ | 2013 |
|
RU2666916C2 |
| ОБОГАЩЕНИЕ АКТИВИРУЕМОЙ ФЛУОРЕСЦЕНЦИЕЙ СОРТИРОВКИ КЛЕТОК (FACS) ДЛЯ СОЗДАНИЯ РАСТЕНИЙ | 2013 |
|
RU2679510C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ОПОСРЕДОВАННОЙ НУКЛЕАЗОЙ НАПРАВЛЕННОЙ ИНТЕГРАЦИИ ТРАНСГЕНОВ | 2013 |
|
RU2650819C2 |
| ЛОКУСЫ ФУНКЦИОНАЛЬНОСТИ FAD2 И СООТВЕТСТВУЮЩИЕ СПЕЦИФИЧНЫЕ К УЧАСТКУ-МИШЕНИ СВЯЗЫВАЮЩИЕ БЕЛКИ, СПОСОБНЫЕ ИНДУЦИРОВАТЬ НАПРАВЛЕННЫЕ РАЗРЫВЫ | 2013 |
|
RU2656159C2 |
| ОПТИМАЛЬНЫЕ ЛОКУСЫ СОИ | 2014 |
|
RU2719150C2 |
| СПОСОБЫ ОБНАРУЖЕНИЯ ДНК ДЛЯ САЙТ-СПЕЦИФИЧЕСКОЙ НУКЛЕАЗНОЙ АКТИВНОСТИ | 2013 |
|
RU2678001C2 |
| ЛОКУСЫ FAD3 ДЛЯ ВЫПОЛНЕНИЯ ОПЕРАЦИЙ И СООТВЕТСТВУЮЩИЕ СВЯЗЫВАЮЩИЕСЯ СО СПЕЦИФИЧЕСКИМИ САЙТАМИ-МИШЕНЯМИ БЕЛКИ, СПОСОБНЫЕ К ВЫЗОВУ НАПРАВЛЕННЫХ РАЗРЫВОВ | 2013 |
|
RU2665811C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ВСТРАИВАНИЯ ЭКЗОГЕННОЙ ПОСЛЕДОВАТЕЛЬНОСТИ В ГЕНОМ РАСТЕНИЙ | 2014 |
|
RU2723130C2 |
| ФУНКЦИОНАЛЬНЫЕ ЛОКУСЫ FAD2 И СООТВЕТСТВУЮЩИЕ СПЕЦИФИЧНЫЕ ДЛЯ САЙТА-МИШЕНИ СВЯЗЫВАЮЩИЕСЯ БЕЛКИ, СПОСОБНЫЕ ИНДУЦИРОВАТЬ НАПРАВЛЕННЫЕ РАЗРЫВЫ | 2013 |
|
RU2656158C2 |























































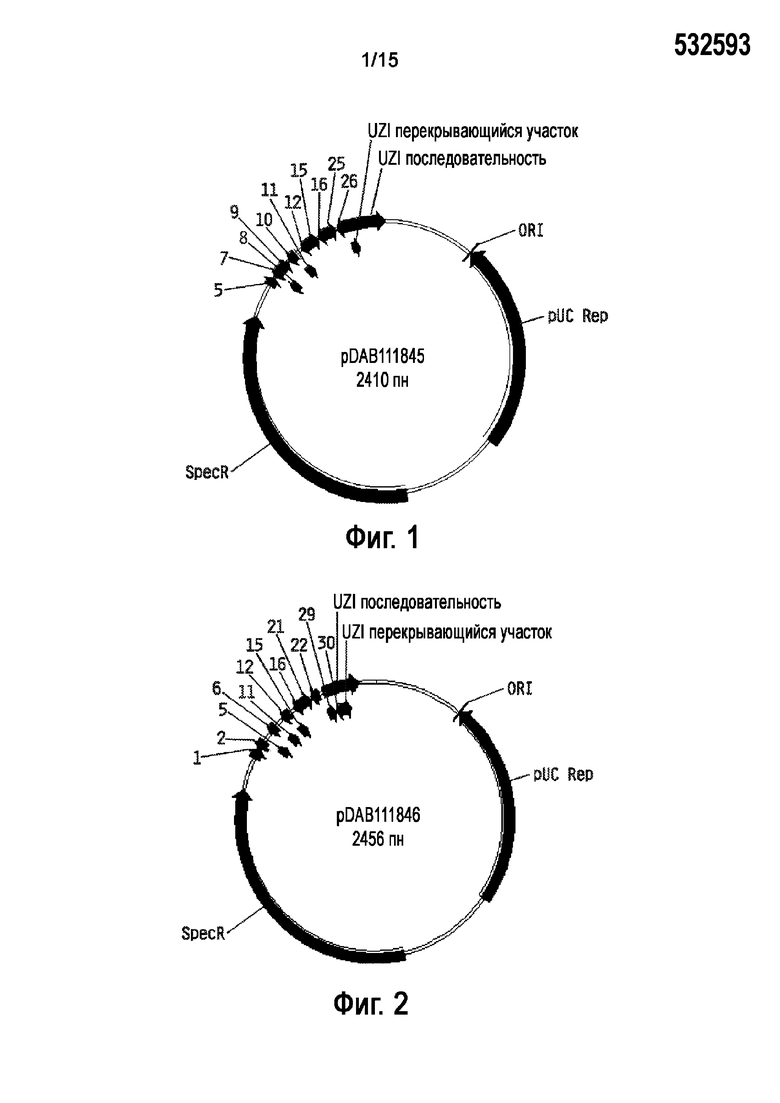
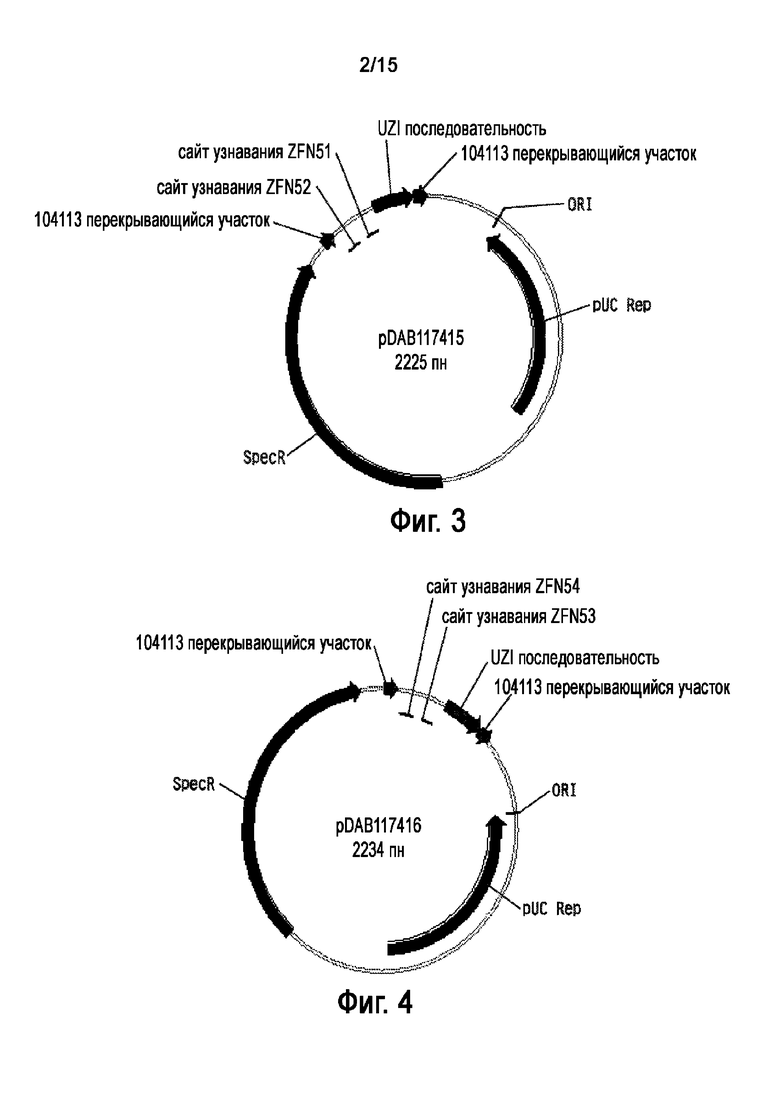
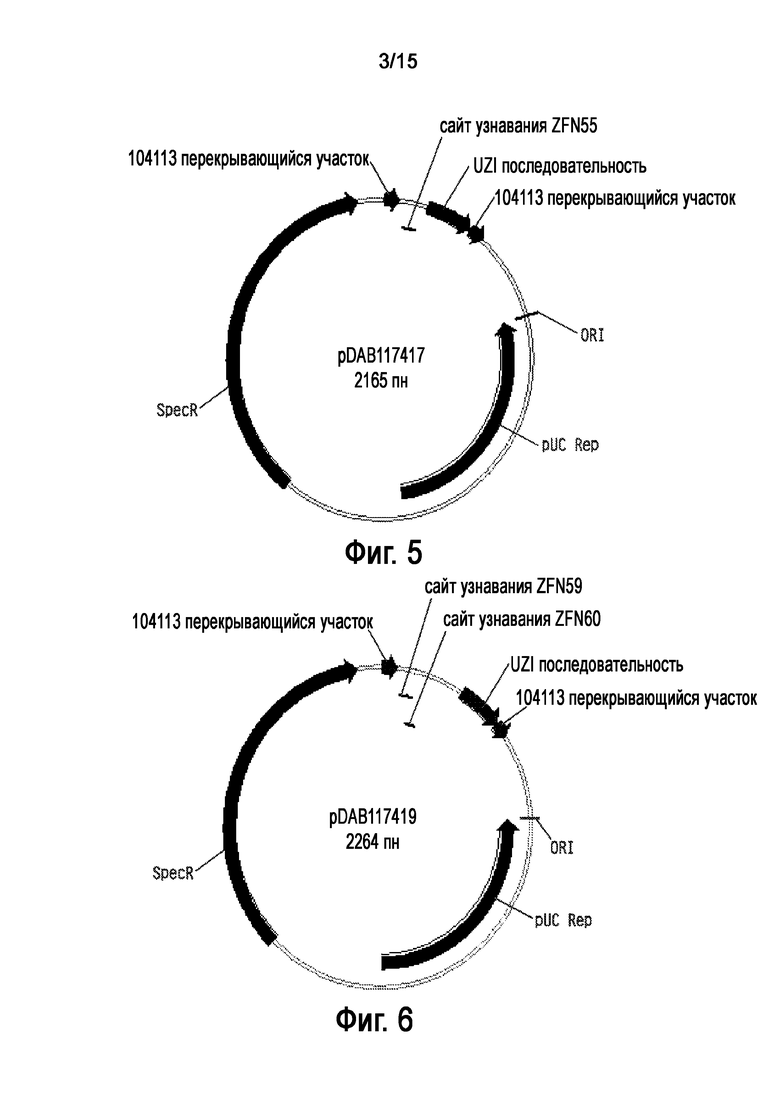
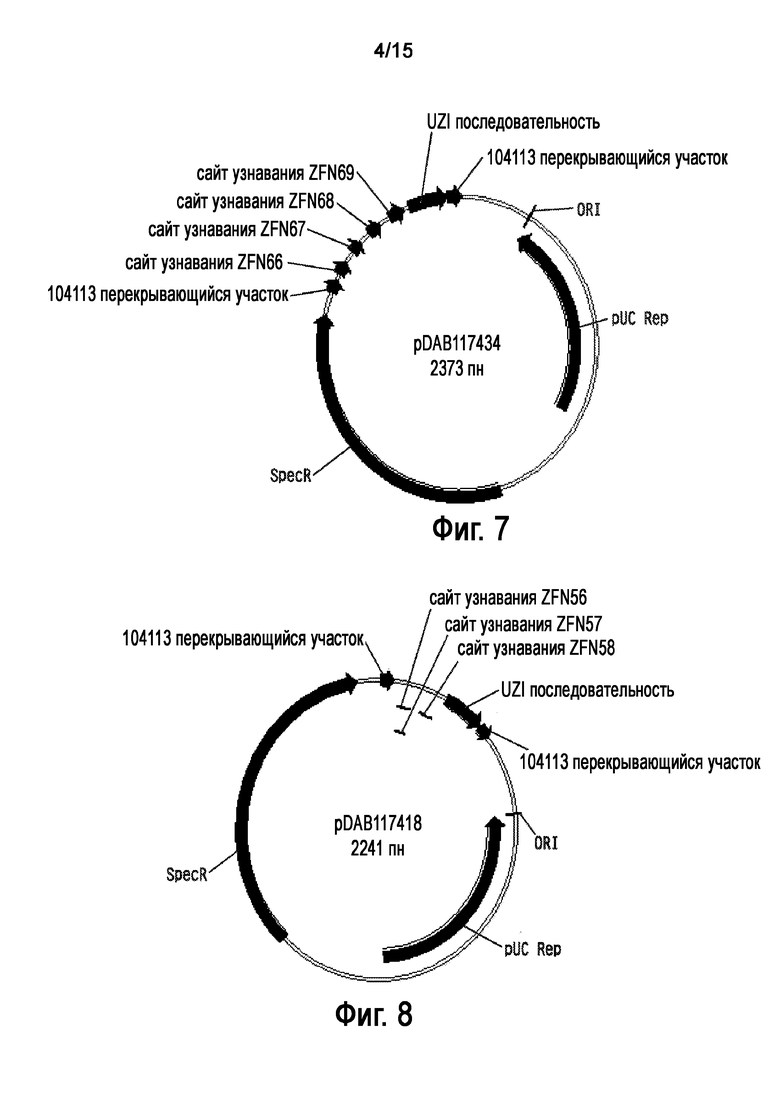
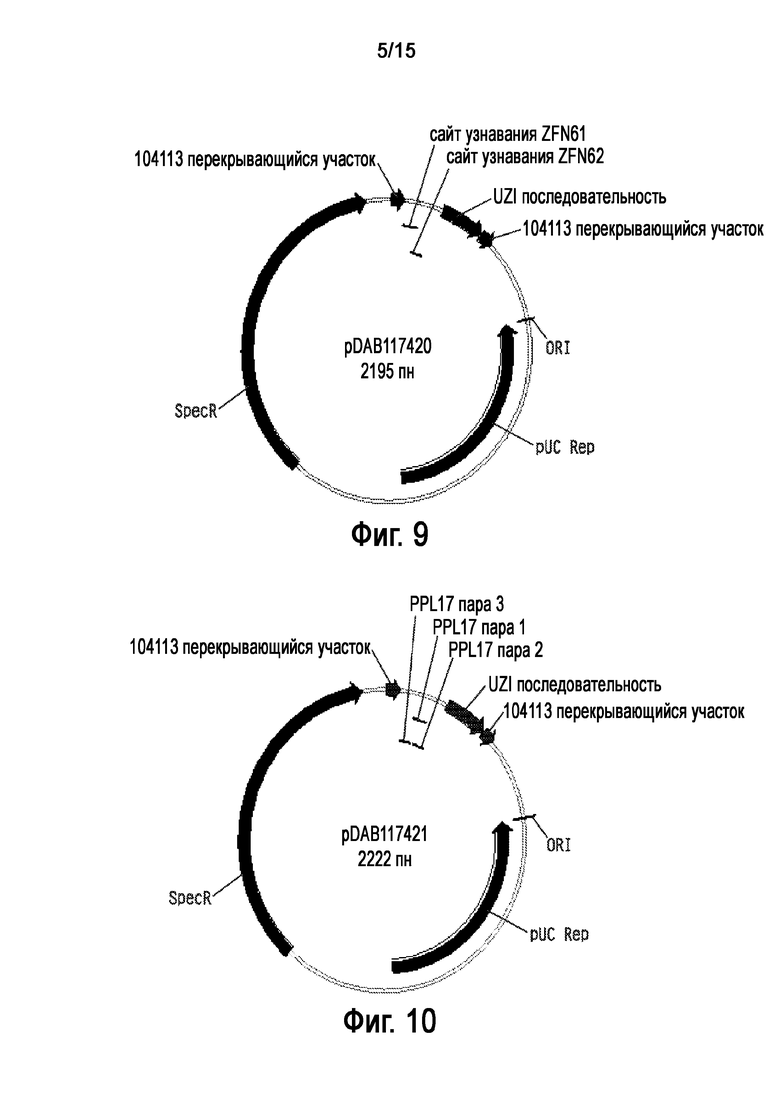
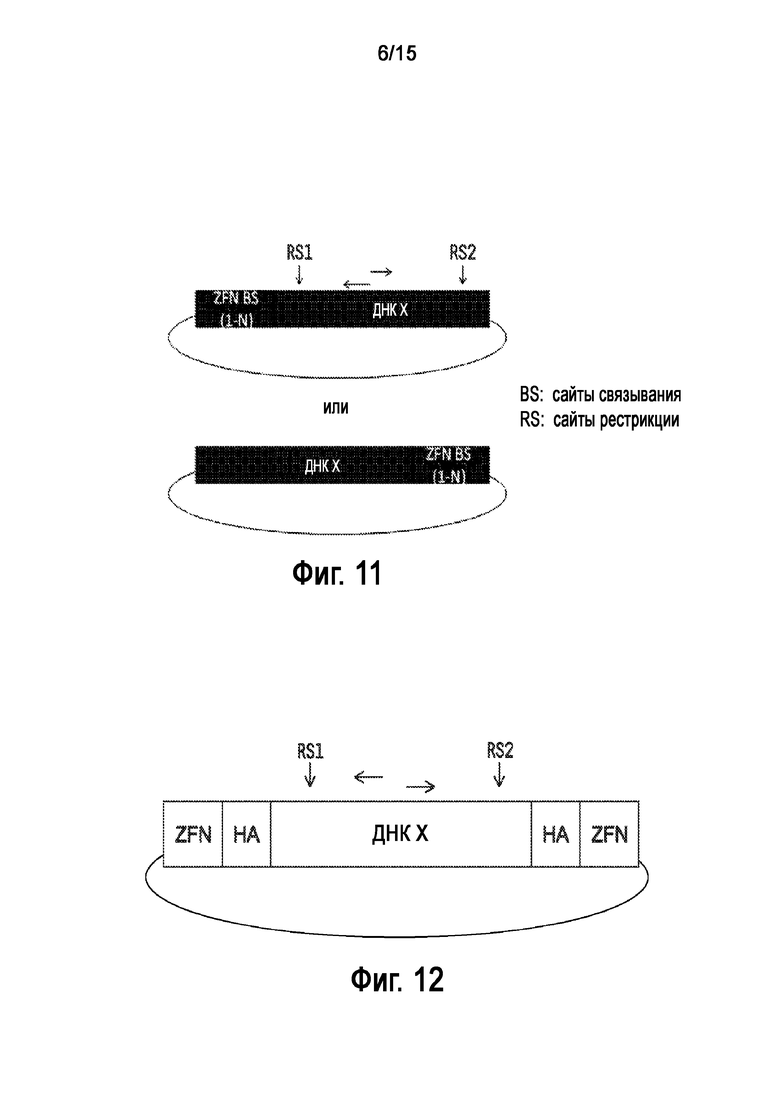
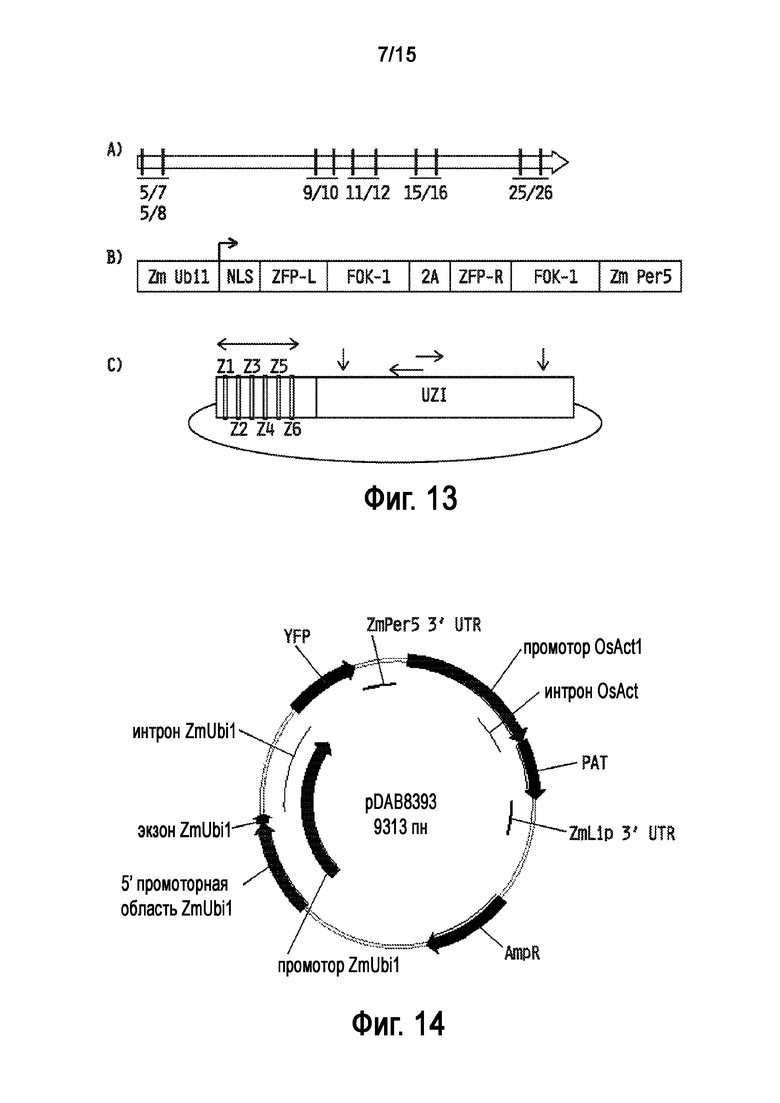

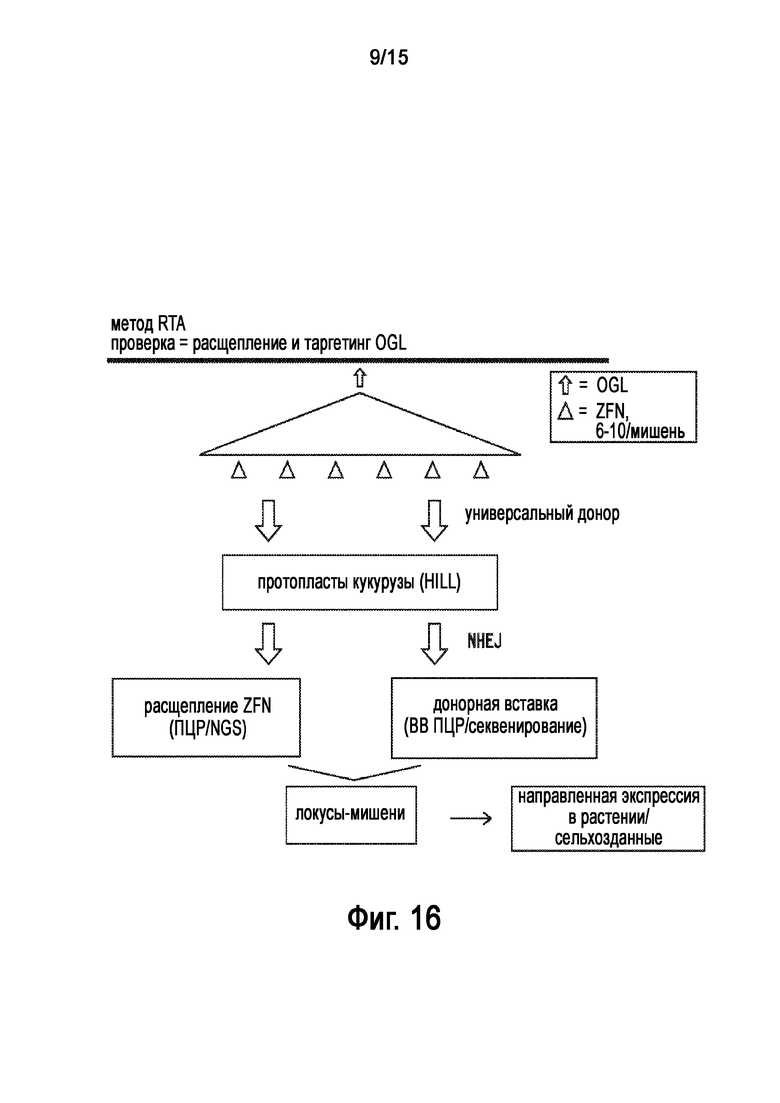

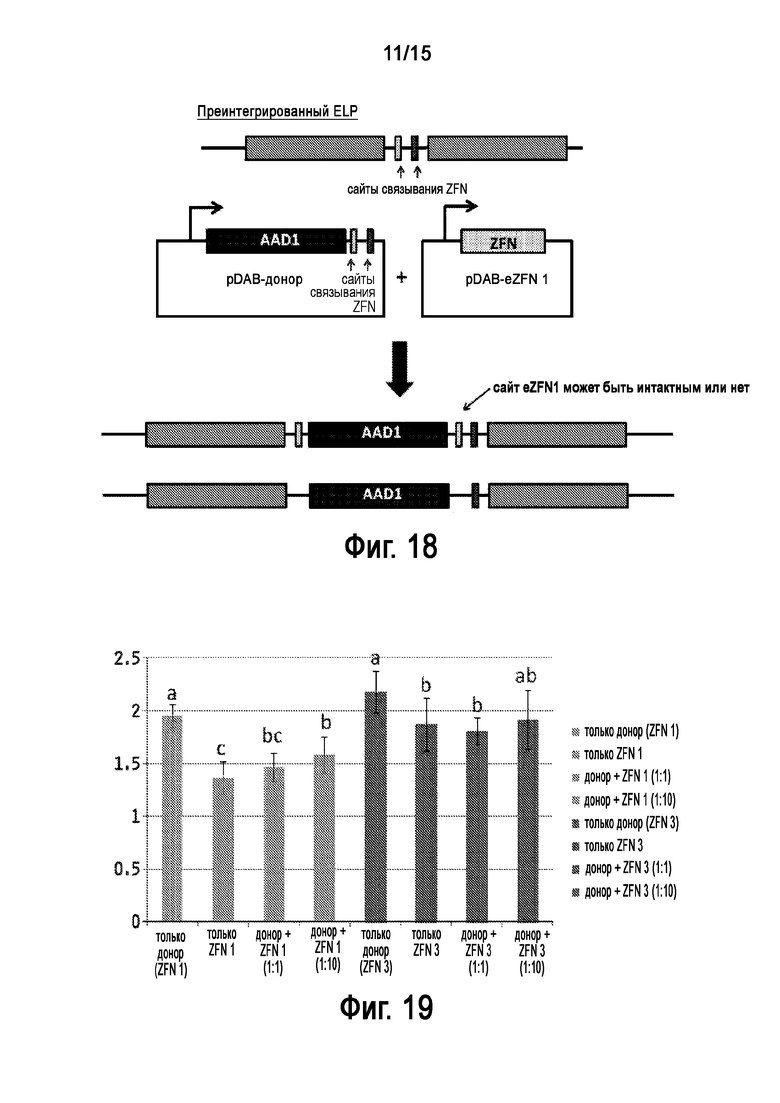
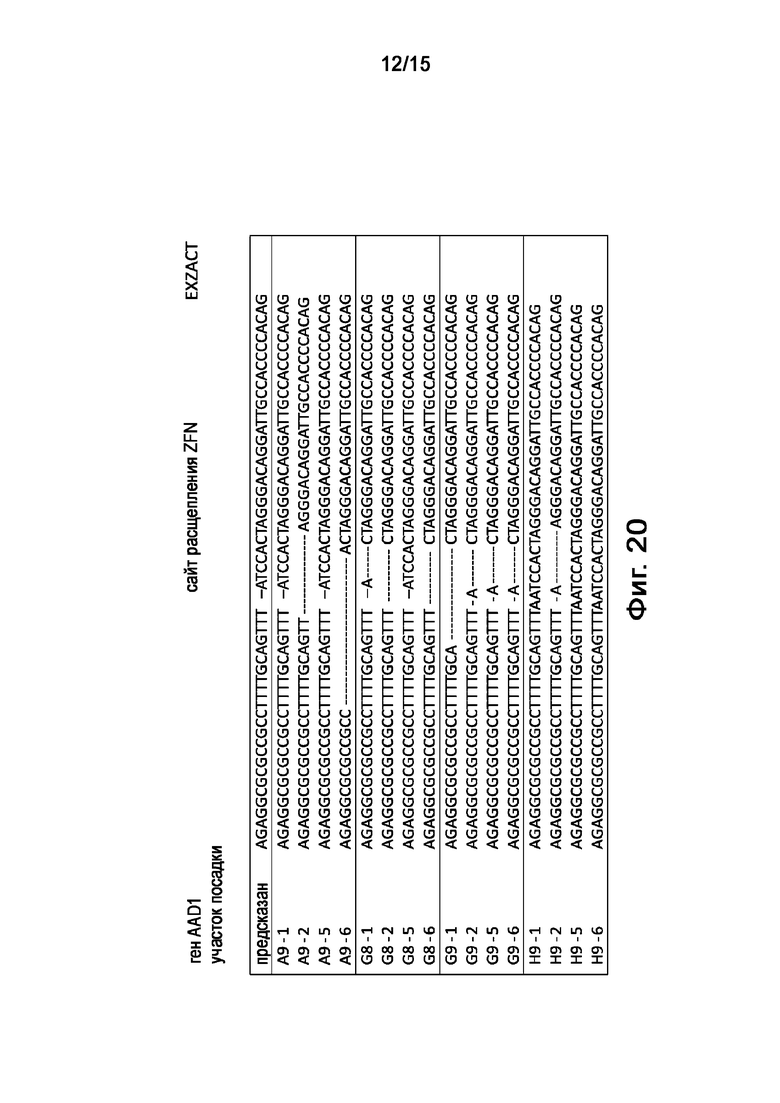
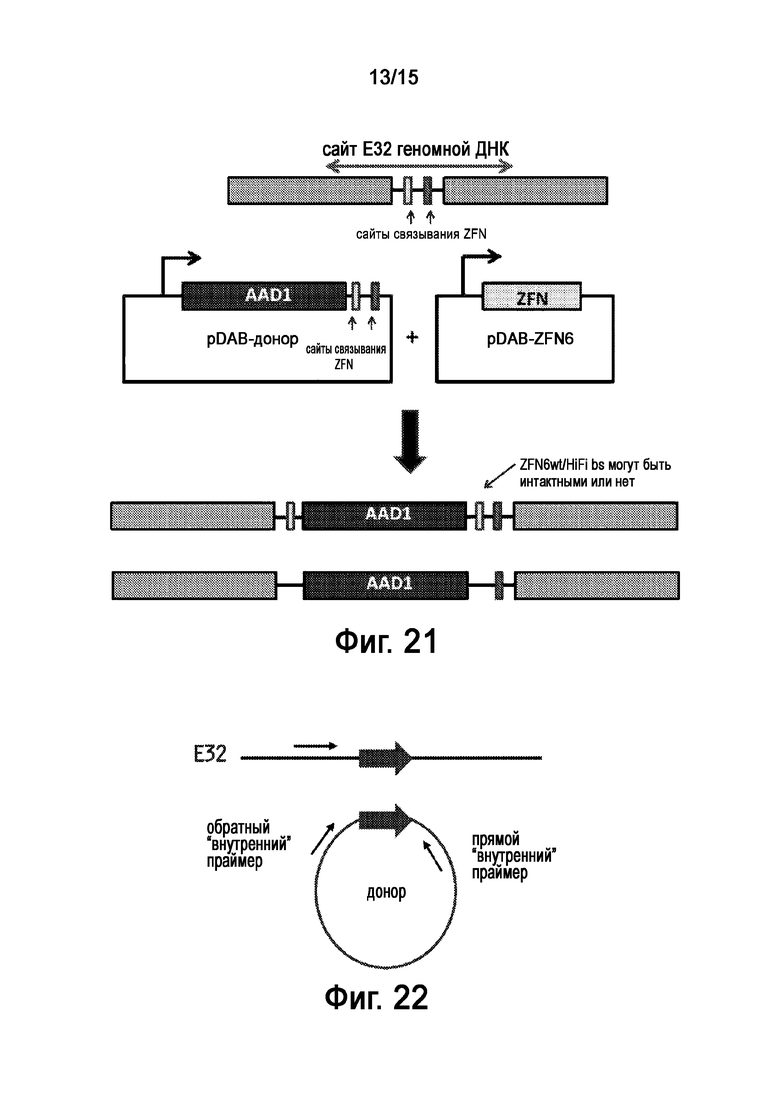
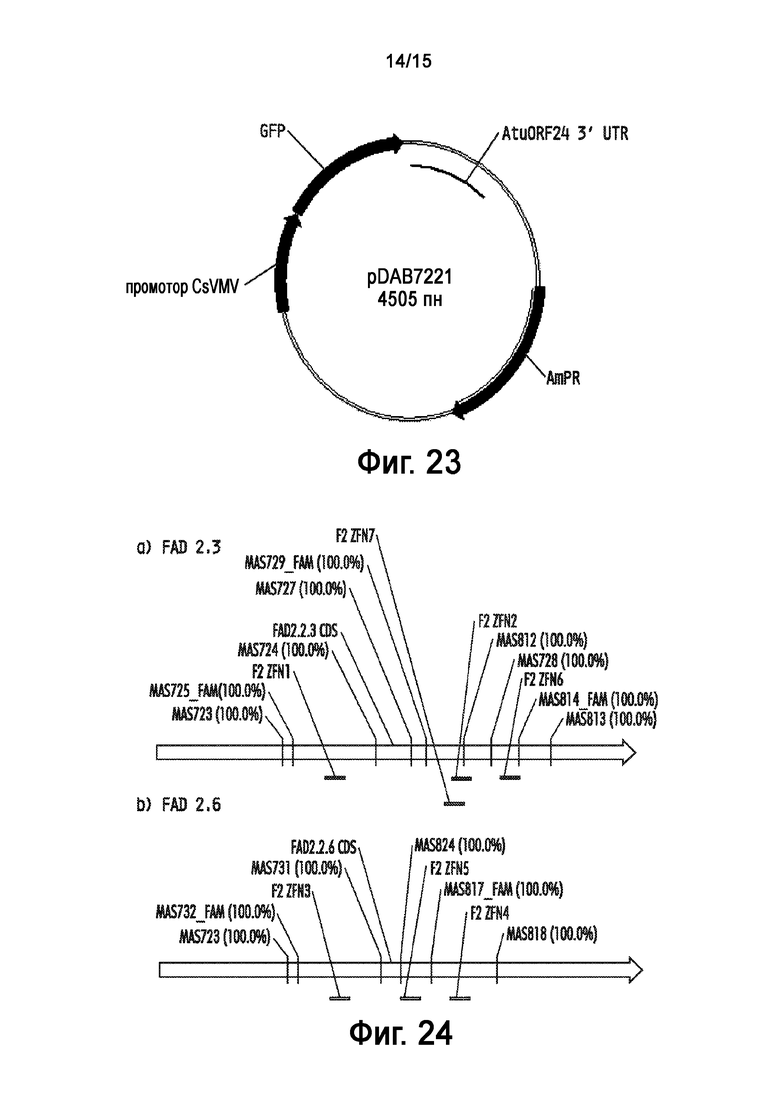
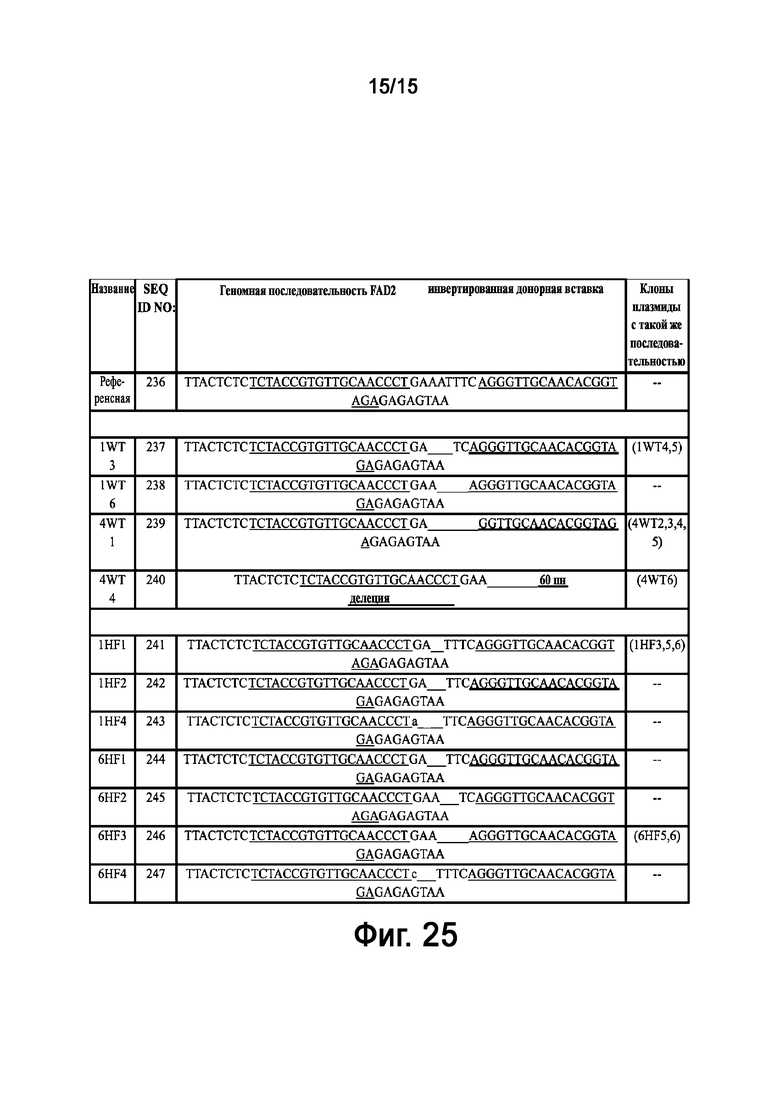
Изобретение относится к области биохимии, в частности к способу обнаружения присутствия сайт-специфической интеграции донорной полинуклеотидной последовательности в целевой участок генома клетки кукурузы или сои. Кроме того, раскрыт способ обнаружения присутствия сайт-специфической интеграции донорной полинуклеотидной последовательности в целевой участок генома трансфицированных растительных клеток кукурузы или сои. Изобретение позволяет устанавливать наличие сайт-специфической интеграции донорной полинуклеотидной последовательности в целевом участке генома с высокой эффективностью и достоверностью. 2 н. и 16 з.п. ф-лы, 12 табл., 26 ил., 8 пр.
1. Способ обнаружения присутствия сайт-специфической интеграции донорной полинуклеотидной последовательности в целевой участок генома клетки кукурузы или сои, где способ включает:
a. амплификацию геномной ДНК в первом раунде ПЦР с получением первого ампликона при использовании первого внешнего ПЦР-праймера, предназначенного для связывания с целевым участком геномной ДНК, и первого внутреннего ПЦР-праймера, предназначенного для связывания интегрированной донорной полинуклеотидной последовательности, где указанный первый внешний ПЦР-праймер и указанный первый внутренний ПЦР-праймер выбраны для амплификации только последовательностей донорных полинуклеотидов с обратной ориентацией, где обратная ориентация относится к ориентации исходного трансформирующего вектора;
b. амплификацию первого ампликона во втором раунде ПЦР с использованием праймеров, специфичных к последовательностям, расположенным в первом ампликоне, с получением второго ампликона; и,
c. обнаружение присутствия второго ампликона, где получение второго ампликона указывает на присутствие события сайт-специфической интеграции.
2. Способ по п.1, где целевой участок генома включает эндогенный или сконструированный целевой участок генома.
3. Способ по п.1, где первый внутренний ПЦР-праймер представлен в более низкой концентрации, чем первый внешний ПЦР-праймер.
4. Способ по п.1, где первый раунд ПЦР проводят при использовании относительной концентрации первого внешнего ПЦР-праймера к первому внутреннему ПЦР-праймеру приблизительно 4:1, 3:1 или 2:1.
5. Способ по п.1, где первый внутренний ПЦР-праймер включает концентрацию 0,05-0,09 мкМ, и первый внешний ПЦР-праймер включает концентрацию по меньшей мере 0,1 мкМ.
6. Способ по любому из пп.1-5, где второй раунд ПЦР включает второй внешний ПЦР-праймер, предназначенный для связывания с целевым участком геномной ДНК первого ампликона, и второй внутренний ПЦР-праймер, предназначенный для связывания интегрированной донорной полинуклеотидной последовательности первого ампликона.
7. Способ по п.6, где второй внутренний ПЦР-праймер представлен в более низкой концентрации, чем второй внешний ПЦР-праймер.
8. Способ по п.6, где второй раунд ПЦР проводят при использовании относительной концентрации второго внешнего ПЦР-праймера ко второму внутреннему ПЦР-праймеру приблизительно 4:1, 3:1 или 2:1.
9. Способ по п.6, где второй внутренний ПЦР-праймер включает концентрацию 0,05-0,1 мкМ, и второй внешний ПЦР-праймер включает концентрацию 0,2 мкМ.
10. Способ по п.1, где геномная ДНК, включающая сайт-специфическую интеграцию донорной полинуклеотидной последовательности в целевой участок генома, является растительной геномной ДНК.
11. Способ по п.10, где растительная геномная ДНК выделена из однодольного растения.
12. Способ по п.10, где растительная геномная ДНК выделена из двудольного растения.
13. Способ по п.10, где сайт-специфическую интеграцию донорной полинуклеотидной последовательности в целевой участок генома производят при расщеплении целевого участка геномной ДНК с помощью сайт-специфической нуклеазы.
14. Способ по п.13, где сайт-специфическая нуклеаза выбрана из группы, состоящей из цинк-пальцевой нуклеазы, нуклеазы CRISPR, нуклеазы TALEN и мегануклеазы.
15. Способ по п.13, где сайт-специфическая интеграция донорной полинуклеотидной последовательности в целевой участок генома проходит по механизму негомологичного соединения концов.
16. Способ по п.1, где этап обнаружения включает электрофорез второго ампликона в геле.
17. Способ по п.1, где этап обнаружения включает секвенирование второго ампликона.
18. Способ обнаружения присутствия сайт-специфической интеграции донорной полинуклеотидной последовательности в целевой участок генома трансфицированных растительных клеток кукурузы или сои, где указанный способ включает:
a. амплификацию геномной ДНК в первом раунде ПЦР с получением первого ампликона, где указанную ПЦР проводят при использовании первого внешнего ПЦР-праймера, предназначенного для связывания с целевым участком генома, и первого внутреннего ПЦР-праймера, предназначенного для связывания донорной полинуклеотидной последовательности, а также где указанный первый внутренний ПЦР-праймер представлен в более низкой концентрации, чем первый внешний ПЦР-праймер, где указанный первый внешний ПЦР-праймер и указанный первый внутренний ПЦР-праймер выбраны для амплификации только последовательностей донорных полинуклеотидов с обратной ориентацией, где обратная ориентация относится к ориентации исходного трансформирующего вектора;
b. амплификацию первого ампликона во втором раунде ПЦР с использованием второго внешнего ПЦР-праймера, предназначенного для связывания с целевым участком геномной ДНК указанного первого ампликона, и второго внутреннего ПЦР-праймера, предназначенного для связывания с интегрированной донорной полинуклеотидной последовательностью указанного первого ампликона; и
c. обнаружение присутствия второго ампликона, где получение второго ампликона указывает на присутствие события сайт-специфической интеграции.
| Колосоуборка | 1923 |
|
SU2009A1 |
| CARROLL D.: "A CRISPR Approach to Gene Targeting", MOLECULAR THERAPY, vol | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Металлический ключ для пчеловодов | 1924 |
|
SU1658A1 |
| ЛУТОВА Л | |||
| А., Биотехнология высших растений, Издательство С | |||
| - Петербургского университета, 2010, стр | |||
| Способ крашения тканей | 1922 |
|
SU62A1 |
Авторы
Даты
2018-10-02—Публикация
2014-09-03—Подача