Изобретение относится к применению производных в ряду 2,5-диарил-1,3,4-оксадиазолов в качестве люминесцентной метки в конфокальной и корреляционной микроскопии, а именно к 2-фенил-5-(3,4,5-триэтоксифенил)-1,3,4-оксадиазолу формулы I,
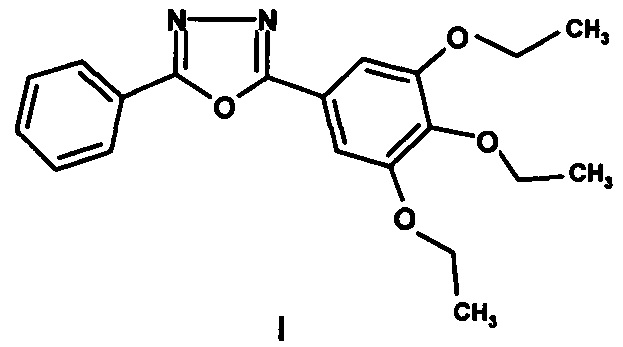
обладающему люминесцентной активностью в фиолетовой области видимого спектра, который может быть использован в качестве оптического отбеливателя (Красовицкий Б.М., Болотин Б.М. Органические люминофоры. М.: Химия. 336 с.), в виде активирующей добавки в жидких и пластмассовых сцинтилляционных детекторах (Birks J.B. The Theory and Practice uf Scintillation Counting. Pergamon Press: Oxford. 1967. 662 p.; Красовицкий Б.М., Григорьева В.И. // Хим. гетероцикл. соед. 1967. №7. С. 761-763.), электролюминесцентного материала для органических светоизлучающих диодов (OLEDs) (Михайлов И.Е., Душенко Г.А., Стариков Д.А., Михайлова О.И., Минкин В.И. // Вестник ЮНЦ. 2010. Т. 6. №4. С. 32-45), а также в дозиметрах ионизирующих излучений (Shorn C.F. // J. Chem. Phys. 1961. Vol. 34. №1. P. 240-246). Высокая поглощающая способность и большие квантовые выходы люминесценции соединения I открывают перспективу использования его и в качестве люминесцентной метки в конфокальной и корреляционной микроскопии для увеличения чувствительности и контрастности этих методов биоимиджинга (Zhao Q., Huang С, Li F. // Chem. Soc. Rev. 2011. Vol. 40. P. 2508-2524). Наличие полиароматической системы у данного соединения способствует образованию его нековалентных коньюгатов и супрамолекулярных комплексов включения с различными биомолекулами, например, с альбуминами, имеющими подходящий по размерам гидрофобный «карман» (Samari F., Hemmateenejad В., Shamsipur M., Rashidi M., Samouei H. // Inorg. Chem. 2012. Vol. 51. P. 3454-3464), а присутствие в оксадиазоле I трех этоксильных групп в 5-арильном фрагменте повышает его растворимость в физиологических средах, что может иметь большое значение при использовании его в качестве люминесцентной метки в биохимических исследованиях.
В ряду 2,5-диарил-1,3,4-оксадиазолов известны 2-фенил-5-(4-метокси(диметиламино)фенил-1,3,4-оксадиазолы (IIа, IIб) (Попова Н.А., Юшко Э.Г., Красовицкий Б.М., Минкин В.И., Любарская А.Э., Гольдберг М.Л. // Хим. гетероцикл. соед. 1983. №1. С. 26-32), 2-(2-гидроксифенил)-5-фенил-1,3,4-оксадиазол (IIв) (Doroshenko А.О., Posokhov Е.А., Verezubova А.А., Ptyagina L.M. // J. Phys. Org. Chem. 2000. Vol. 13. P. 253-265), 2-(2'-гидроксифенил)-5-(4''-нонилфенил)-1,3,4-оксадиазол (IIг) (Белдовская А.Д., Душенко Г.А., Викрищук Н.И., Попов Л.Д., Ревинский Ю.В., Михайлов И.Е., Минкин В.И. // ЖОХ. 2014. Т. 84. №1. С. 164-166), 2-[2-ацетил(бензоил)оксифенил]-5-(4-нонилфенил)-1,3,4-оксадиазолы (IIд, IIе), обладающие люминесцентной активностью, которая, тем не менее, остается недостаточно высокой.
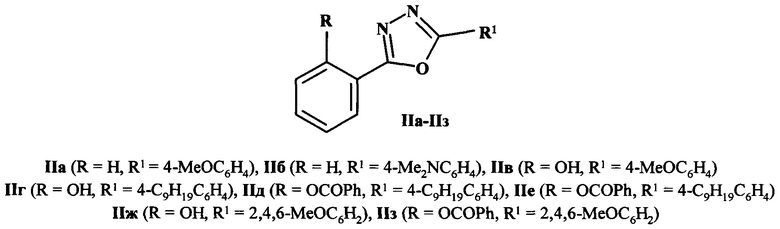
Наиболее близкими к соединению I по структуре являются 2-(2-гидрокси(бензоилокси)фенил-5-(3,4,5-триметоксифенил)-1,3,4-оксадиазолы (IIж, IIз) (Белдовская А.Д., Душенко Г.А., Викрищук Н.И., Попов Л.Д., Ревинский Ю.В., Михайлов И.Е., Минкин В.И. // ЖОрХ. 2013. Т. 49. Вып. 12. С. 1876-1878). Однако и их люминесцентная активность, что следует из данных, представленных в таблице, также остается недостаточно высокой и существенно ниже, чем у соединения I.
Техническим результатом изобретения является повышение люминесцентной активности в фиолетовой области видимого спектра соединений ряда 2,5-диарил-1,3,4-оксадиазолов при использовании их в качестве люминесцентной метки в конфокальной и корреляционной микроскопии для увеличения чувствительности и контрастности этих методов.
Технический результат достигается применением соединения формулы I в качестве люминесцентной метки в конфокальной и корреляционной микроскопии.
Изобретение удовлетворяет критерию изобретательского уровня, т.к. неизвестно применение 2-фенил-5-(3,4,5-триэтоксифенил)-1,3,4-оксадиазола в качестве люминесцентной метки в конфокальной и корреляционной микроскопии, а также в ряду 2,5-диарил-1,3,4-оксадиазолов неизвестно влияние заместителей в положениях 2,5 оксадиазольного цикла на проявление люминесцентной активности соединений данного ряда.
Способ получения соединения I заключается во взаимодействии 3,4,5-триэтоксибензоилхлорида IV, полученного действием на 3,4,5-триэтоксибензойную кислоту III тионилхлорида, с бензогидразидом V в сухом ацетонитриле с использованием триэтиламина в качестве основания, приводящим к образованию N'-бензоил-3,4,5-триэтоксибензогидразида VI, последующая циклизация которого кипячением с тионилхлоридом дает 2-фенил-5-(3,4,5-триэтоксифенил)-1,3,4-оксадиазол (I).

Ниже приведен пример получения соединений I.
N'-Бензоил-3,4,5-триэтоксибензогидразид (VI). К раствору 1.36 г (0.01 моль) бензогидразида (V) в 20 мл сухого ацетонитрила последовательно прибавляли 2 мл триэтиламина и 1.94 г (0.011 моль) хлорангидрида 3,4,5-триэтоксибензойной кислоты (IV) в 15 мл сухого ацетонитрила. Реакционную смесь оставляли на сутки при комнатной температуре, а затем кипятили 3 часа с обратным холодильником. Растворитель удаляли в вакууме, маслянистый остаток промывали водой (2×10 мл), сушили на воздухе и продукт выделяли колоночной хроматографией на силикагеле (0.063-0.200 мм, элюент - этилацетат/петролейный эфир (1:4)), собирая фракцию с Rƒ=0.50-0.55. После отгонки растворителя и перекристаллизации из изо-пропанола получили 1.77 г (выход 64%) N'-бензоил-3,4,5-триэтоксибензогидразида (VI). Бесцветные кристаллы, т. пл. 164-166°С. ИК спектр (KBr), v, см-1: 3220 уш. (NH); 2980-2885 (СН); 1685, 1654 (С=O); 1625, 1623 (С=С); 1603, 1580, 1579, 1488, 1483, 1328, 1316, 1231, 1129, 1104, 1030, 708, 689. Спектр ЯМР 1Н (CDCl3), δ, м.д.: 1.31 т (3Н, 4-СН3, J 7.5 Гц), 1.33 т (6Н, 3,5-(СН3)2, J 7.5 Гц), 3.96 кв (4Н, 3,5-(ОСН2)2, J 7.5 Гц), 4.06 кв (2Н, 4-ОСН2, J 7.5 Гц), 7.07 с (2Н, 2,6-HAr), 7.34 д.д (2Н, 3,5-HAr', J1 7.4 Гц, J2 7.5 Гц), 7.46 т (1Н, 4-HAr', J 7.5 Гц), 7.82 д (2Н, 2,6-HAr', J 7.5 Гц), 10.00 уш. с (1H, NH), 10.17 уш. с (1Н, NH). Спектр ЯМР 13Н (CDCl3), δ, м.д.: 14.80 (2С, 3,5-CCH3), 15.59 (С, 4-CCH3), 64.57 (2С, 3,5-ССН2), 68.85 (С, 4-ССН2), 105.98 (2С, 2,6-CAr), 125.92 (С, 1-CAr), 127.43 (2С, 3,5-CAr'), 128.45 (2С, 2,6-CAr'), 131.25 (С, 1-CAr') 132.15 (С, 4-CAr'), 141.26 (С, 4-CAr), 152.78 (2С, 3,5-CAr), 165.95 (С=O), 166.15 (С=O). Найдено, %: С 64.72; Н 6.31; N 7.48. C20H24N2O5. Вычислено, %: С 64.50; Н 6.50; N 7.52;
2-Фенил-5-(3,4,5-триэтоксифенил)-1,3,4-оксадиазол (I). Раствор 3.72 г (0.01 моль) N'-бензоил-3,4,5-триэтоксибензогидразида (VI) в 10 мл хлористого тионила кипятили с обратным холодильником на водяной бане в течение 5 часов. После отгонки тионилхлорида и охлаждения реакционной массы до комнатной температуры к ней добавили 50 г колотого льда. Выпавший осадок отфильтровали и продукт очищали колоночной хроматографией на силикагеле (0.063-0.200 мм, элюент - этилацетат/петролейный эфир (1:10)), собирая фракцию с Rƒ=0.60-0.65. После отгонки растворителя и перекристаллизации из изо-пропанола получили 1.59 г (выход 45%) 2-фенил-5-(3,4,5-триэтоксифенил)-1,3,4-оксадиазола (I). Бесцветные кристаллы, т.пл. 103-105°С. ИК спектр (KBr), v, см-1: 2979-2885 (СН); 1589-1556 (C=N, С=С); 1494, 1479, 1475, 1440, 1395, 1375, 1327, 1242, 1220, 1129, 1102, 1030, 725, 690. Спектр ЯМР 1Н (CDCl3), δ, м.д.: 1.36 т (3Н, 4-СН3, J 7.5 Гц), 1.45 т (6Н, 3,5-(СН3)2, J 7.5 Гц), 4.10 кв (2Н, 4-ОСН2, J 7.5 Гц), 4.12 кв (4Н, 3,5-(ОСН2)2, J 7.5 Гц), 7.31 с (2Н, 2,6-HAr), 7.50 т (1Н, 4-HAr', J 6.4 Гц), 7.51 д.д (2Н, 3,5-HAr', J1 6.4 Гц, J2 6.5 Гц), 8.06 д (2Н, 2,6-HAr', J 6.5 Гц), Спектр ЯМР 13Н (CDCl3), δ, м.д.: 14.73 (2С, 3,5-СН3), 15.62 (4-СН3), 65.02 (2С, 3,5-ССН2), 69.11 (С, 4-CCH2), 105.71 (2С, 2,6-CAr), 118.75 (С, 1-CAr') 123.95 (С, 4-CAr'), 125.92 (С, 1-CAr), 126.91 (2С, 3,5-CAr'), 129.04 (2С, 2,6-CAr'), 141.33 (С, 4-CAr), 153.45 (2С, 3,5-CAr), 164.41 (C=N), 164.67 (C=N). Найдено, %: С 67.79; Н 6.21; N 7.85. C20H22N2O4. Вычислено, %: С 67.68; Н 6.26; N 7.90;
Спектрально-абсорбционные и спектрально-люминесцентные характеристики соединений I и IIа-з получены в толуоле, октане, изо-октане, ацетонитриле и диметилсульфоксиде (ДМСО) при комнатной температуре по стандартным методикам. Электронные спектры поглощения регистрировали на спектрофотометре «Cary 100» (Varian). Спектры люминесценции были записаны на спектрофлуориметре Cary Eclipse. Квантовые выходы люминесценции были определены относительно ацетонитрильного раствора антрацена (Doroshenko А.О., Posokhov Е.А., Verezubova А.А., Ptyagina L.M. // J. Phys. Org. Chem. 2000. Vol. 13. P. 253-265). Использовавшиеся для измерений растворители были очищены и осушены по стандартным методикам (Гордон А., Форд Р. Спутник химика. М.: Мир. 1976. 536 с). ИК спектры снимали на спектрометре Varian Excalibur 3100 FT-IR в таблетках KBr.Спектры ЯМР 1Н (250.13 МГц) и 13С (62.90 МГц) записаны на приборе Bruker DPX-250 в CDCl3. В качестве внутреннего стандарта использовали сигналы остаточных протонов растворителя. Элементный анализ проведен на CHN-анализаторе KOVO. Хроматографирование проводили на колонках с наполнителем Silica gel 60 (0.063-0.200 мм) фирмы Merck. Температуры плавления определены на нагревательном столике Boetius.
Строение соединений I, IIа-з доказано элементным анализом, а также данными ИК-, ЯМР 1Н и 13С спектроскопии.
В таблице приведены спектры поглощения и люминесценции 2-фенил-5-(3,4,5-триэтоксифенил)-1,3,4-оксадиазола (I), а также его ближайших аналогов - соединений IIа-з.
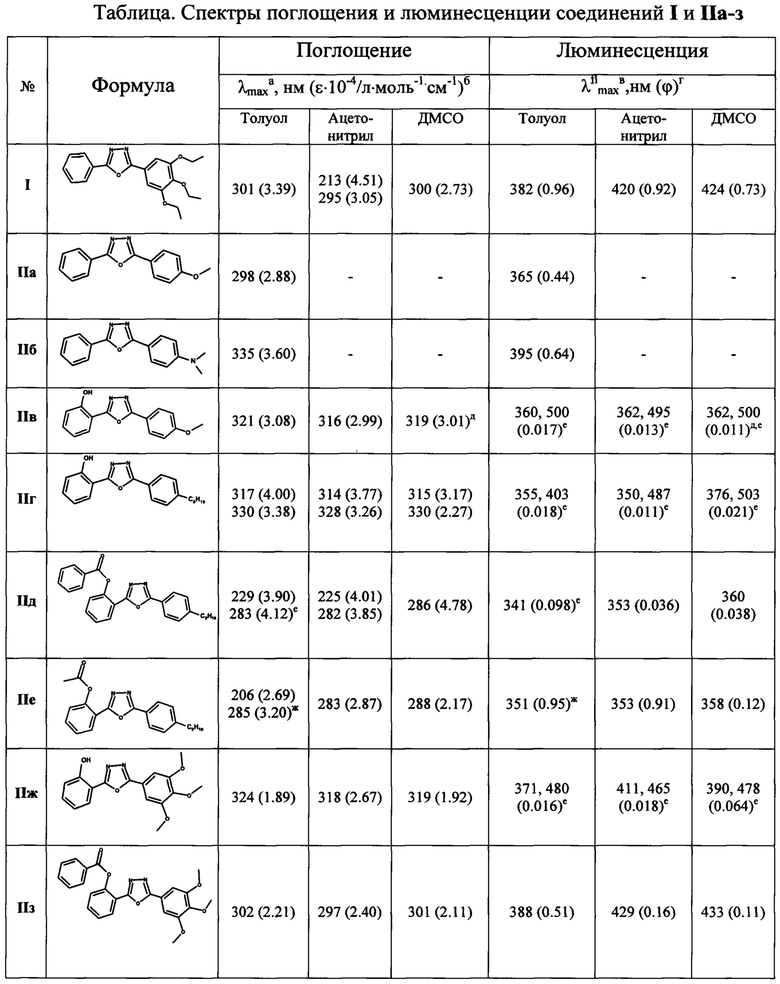
Примечание: a λmax - максимум длинноволновой полосы поглощения, б ε - значение молярной экстинкции, соответствующее данному максимуму, в λflmax - максимум полосы люминесценции, г ϕ - квантовый выход люминесценции (λвозб. 300 нм), д растворитель - октан, е суммарный квантовый выход люминесценции, ж растворитель - изо-октан.
Из таблицы видно, что соединение I обладает высокой поглощающей способностью ( ), бесцветно (λmax=295-301 нм) при дневном освещении и излучает в фиолетовой области видимого спектра (λflmax=382-424 нм) при облучении его ультрафиолетовым светом (λвозб. 300 нм), а его квантовая эффективность люминесценции (ϕ=0.73-0.96) существенно выше (1.5-70 раз), чем у его аналогов.
), бесцветно (λmax=295-301 нм) при дневном освещении и излучает в фиолетовой области видимого спектра (λflmax=382-424 нм) при облучении его ультрафиолетовым светом (λвозб. 300 нм), а его квантовая эффективность люминесценции (ϕ=0.73-0.96) существенно выше (1.5-70 раз), чем у его аналогов.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-(2-Алкоксифенил)-5-(3,4,5-триалкоксифенил)-1,3,4-оксадиазол, обладающий люминесцентными свойствами | 2018 |
|
RU2670829C1 |
| {2-[5-(3,4,5-ТРИМЕТОКСИФЕНИЛ)-1,3,4-ОКСАДИАЗОЛ-2-ИЛ]ФЕНИЛ} АЦЕТАТ С ЛЮМИНЕСЦЕНТНЫМИ СВОЙСТВАМИ | 2014 |
|
RU2568640C1 |
| Бис[2-(2-оксифенил)-5-(3,4,5-триметоксифенил)-1,3,4-оксадиазолил]бериллий(II) с люминесцентной активностью | 2015 |
|
RU2610527C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТИЛ-5-ЗАМЕЩЕННЫХ-1,3,4-ОКСАДИАЗОЛОВ | 2004 |
|
RU2317986C2 |
| ГИДРОКСАМОВЫЕ КИСЛОТЫ, СОДЕРЖАЩИЕ ЯДРА 1,2,4- И 1,3,4-ОКСАДИАЗОЛА В КАЧЕСТВЕ ПОТЕНЦИАТОРОВ ДЕЙСТВИЯ АНТИБИОТИКОВ | 2023 |
|
RU2830361C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1Н-БЕНЗО[F]ХРОМЕН-2-ИЛ(АРИЛ)КЕТОНОВ | 2015 |
|
RU2633368C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(1Н-БЕНЗОХРОМЕН-2-ИЛ)-2,2,2-ТРИФТОРЭТАНОНОВ | 2016 |
|
RU2662439C2 |
| ЦИНКОВЫЕ КОМПЛЕКСЫ 5-[2-ГИДРОКСИ(ТОЗИЛАМИНО)БЕНЗИЛИДЕНАМИНО]-2-(2-ТОЗИЛАМИНОФЕНИЛ)-1АЛКИЛБЕНЗИМИДАЗОЛОВ, ОБЛАДАЮЩИЕ ФОТОЛЮМИНЕСЦЕНТНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2532904C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ АРИЛ-ТИОГИДАНТОИНА, ИНГИБИТОРЫ АНДРОГЕНОВОГО РЕЦЕПТОРА, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2017 |
|
RU2708253C2 |
| РАЗВЕТВЛЕННЫЕ ОЛИГОАРИЛСИЛАНЫ С РЕАКЦИОННОСПОСОБНЫМИ КОНЦЕВЫМИ ГРУППАМИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2544863C2 |
Изобретение относится к применению 2-фенил-5-(3,4,5-триэтоксифенил)-1,3,4-оксадиазола в качестве люминесцентной метки в конфокальной и корреляционной микроскопии. Технический результат: повышение люминесцентной активности в фиолетовой области видимого спектра соединений ряда 2,5-диарил-1,3,4-оксадиазолов при использовании их в качестве люминесцентной метки в конфокальной и корреляционной микроскопии для увеличения чувствительности и контрастности этих методов. 1 табл.
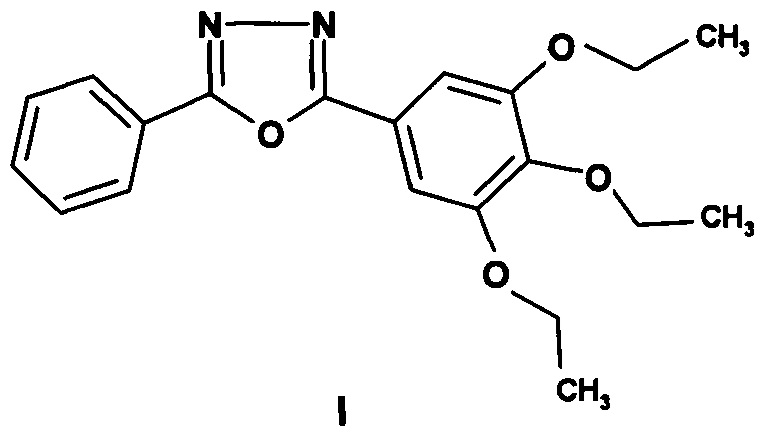
Применение 2-фенил-5-(3,4,5-триэтоксифенил)-1,3,4-оксадиазол формулы I

в качестве люминесцентной метки в конфокальной и корреляционной микроскопии.
| RU 2015117491 A, 27.11.2016 | |||
| {2-[5-(3,4,5-ТРИМЕТОКСИФЕНИЛ)-1,3,4-ОКСАДИАЗОЛ-2-ИЛ]ФЕНИЛ} АЦЕТАТ С ЛЮМИНЕСЦЕНТНЫМИ СВОЙСТВАМИ | 2014 |
|
RU2568640C1 |
| БЕЛДОВСКАЯ А.Д | |||
| и др | |||
| Журнал Органической Химии, т | |||
| Способ смешанной растительной и животной проклейки бумаги | 1922 |
|
SU49A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Электрическое клавишное шифровальное приспособление | 1924 |
|
SU1876A1 |
| WO 2009148452 A1, 10.12.2009. | |||
Авторы
Даты
2018-11-02—Публикация
2017-11-13—Подача