Изобретение относится к медицине, а именно фтизиатрии, и может быть использовано для лечения больных туберкулезом легких с множественной лекарственной устойчивостью возбудителя.
Современная эпидемиологическая ситуация по туберкулезу характеризуется высокой частотой множественной лекарственной устойчивости микобактерий туберкулеза (МЛУ МБТ) к антибактериальным препаратам и повышение эффективности химиотерапии туберкулеза легких с МЛУ МБТ является приоритетным направлением фтизиатрии во всем мире (Васильева И.А., 2015; ВОЗ, 2006).
Успех в лечении туберкулеза, вызванного возбудителем с множественной лекарственной устойчивостью, возможен только при длительной химиотерапии с одновременным назначением 6-8 антибактериальных и противотуберкулезных средств не менее 8 мес в период интенсивной фазы и 4-6 препаратов не менее 12 мес в фазе продолжения лечения (Приказ МЗ РФ №109 от 21.03.2003; Приказ МЗ РФ №951 от 29.12.2014). Однако при этом регистрируется высокая частота нежелательных проявлений и побочных реакций, препятствующих дальнейшему применению лекарственных средств и ведущих к исключению высокоэффективных препаратов из схемы химиотерапии (Ливчине Э., 2003; Малявина У.С., 2003; Черных Н.А., 2004; Шовкун Л.А., 2008). Несмотря на массивную антибактериальную терапию, 20-35% впервые выявленных больных туберкулезом с МЛУ остаются неизлеченными и переходят в контингент хронических больных с эпидемиологически опасной заразной формой туберкулеза (Сапожникова Н.В., 2003; Казенный Б.Я., 2004; Мишин В.Ю., 2009; Долгих С.А., 2012).
С целью снижения проявления побочных эффектов и улучшения переносимости антибактериальных препаратов (АБП) в комплексном лечении больных туберкулезом с МЛУ используются препараты для сопутствующей и патогенетической терапии: иммуностимулирующие, дезинтоксикационные, десенсибилизирующие, антигистаминные, противосудорожные, противорвотные, пробиотические, витаминные, седативные, нейролептические, антиксиолитические, антацидные препараты, антиоксиданты, антигипоксанты, гепатопротекторы, бронходилитаторы, антидепрессанты и др. Это создает чрезмерную медикаментозную нагрузку на организм пациента и повышает риск развития побочных реакций и нежелательных проявлений.
Многие исследователи убеждены, что только естественно природный путь воздействия на организм позволит снизить побочные действия синтезированных (химических) лекарственных средств (Виноградова Т.И., 1996; Беспалов В.Г., Некрасова В.Б., 2000; Орехов А.Н., 2003). Натуральные природные средства, в том числе биологически активные добавки, не являются фармацевтическими препаратами и относятся к группе безрецептурных пищевых и профилактических средств.
Известно достаточно много разнообразных средств на основе различных растительных экстрактов, применяемых в комплексном лечении туберкулеза.
Однако, большинство средств, оказывающие различные положительные действия на организм человека, в совокупности с ними не обладают доказанным антимикобактериальным действием в отношении возбудителя туберкулеза.
В последнее время вызывают интерес исследования по применению лишайника из рода кладонии, как перспективного биологически активного сырья. Обзор литературы по использованию лишайника в официальной и народной медицине показывает, что растение известно издавна как противотуберкулезное и общеукрепляющее средство, его применяли для лечения туберкулеза легких, коклюша, бронхита и других бронхолегочных заболеваний.
Известно средство для профилактики и лечения туберкулеза «Экстракт Cetraria islandica (L) Ach. Сухой, таблетированная форма» (Патент РФ 2321419), выполнено в виде таблетки с ядром и оболочкой, при этом ядро содержит сухой экстракт слоевищ лишайника с комплексом биологически активных веществ, извлеченных водно-этиловой смесью определенной концентрации. В качестве целевых добавок содержит лактозу, метилцеллюлозу, стеаратат кальция и другие ингредиенты, в том числе и для оболочки таблетки.
Также известен «Препарат Ислацет для профилактики и лечения туберкулеза и способ его получения» (Патент РФ №2203081), состоящий из спиртового и водного экстракта и содержащий экстрактивные вещества слоевища лишайника цетрарии исландской Cetraria islandica (L) Ach.
Однако, при использовании растительных препаратов в виде экстрактов основным недостатком является использование в технологии спирто-водных композиций, которые могут изменить эффект действующих веществ за счет этанола и также возможны нежелательные реакции со стороны организма пациентов (Машковский М.Д., 2001). Также неизвестно их действие при лечении туберкулеза с множественной лекарственной устойчивостью возбудителя заболевания.
Ранее в результате наших исследований доказано, что наиболее выраженным антибактериальным действием in vitro в отношении чувствительных и устойчивых к АБП штаммам МБТ и условно-патогенных микроорганизмов обладает экстракт, получаемый при помощи механохимической биотехнологии на стадии предэкстракционной обработки слоевищ лишайников (Патент РФ№2385159 «Способ получения препарата Ягель-М, обладающего противотуберкулезным действием»).
Развитие исследований позволило доказать, что, благодаря разработке оригинальной биотехнологии обработки лишайникового сырья, позволяющей непосредственно в твердой фазе, без участия любых растворителей расщеплять очень прочные лишайниковые β-полисахариды до β-олигосахаридов, обладающих свойством детоксикации внутренних сред организма (кровь, лимфа, межклеточные жидкости), получаемые механохимически активированные биопрепараты по способности детоксикации внутренних сред организма препараты, не имеют аналогов (Патент РФ №2477143 «Биологически активная добавка актопротекторного, адаптогенного действия из растительного сырья и способ его получения»). Таким образом, биологически активная добавка к пище «ЯГЕЛЬ ДЕТОКС», полученный в результате такой обработки, обладает свойствами, как стимулирующими выведение токсинов из организма и повышающими устойчивость организма к воздействию токсинов, так и антибактериальными, благодаря наличию лишайниковых кислот антибактериального действия.
Преимуществом препарата «ЯГЕЛЬ ДЕТОКС» по сравнению с аналогами, кроме доказанного антимикобактериального и детоксикационного действия, является и способ лекарственной формы, порошок, капсулированный в желатиновую капсулу, которая обеспечивает точный дозированный объем, является удобной формой для приема внутрь, быстро и безопасно растворяется в желудке.
Однако до настоящего времени, применение биопрепаратов, полученных путем механохимической активации слоевищ лишайников без участия растворителей, и обладающих одновременно антимикобактериальными и антитоксическими свойствами при массивной химиотерапии туберкулеза с множественной лекарственной устойчивостью не проводилось. Известно, что повышение эффективности лечения больных возможно лишь при адекватной и своевременной коррекции нарушений в обмене веществ, иммунной реактивности организма, антитоксической функции печени, антиоксидантной защиты и повышении биоактивности и биодоступности противотуберкулезных препаратов.
Таким комплексным средством для сопутствующей и патогенетической терапии при массивной химиотерапии туберкулеза с МЛУ МБТ может выступить препарат «ЯГЕЛЬ ДЕТОКС».
Целью предполагаемого изобретения является повышение эффективности лечения туберкулеза с множественной лекарственной устойчивостью путем применения «ЯГЕЛЬ ДЕТОКС» для снижения побочного токсического действия антибактериальных препаратов при массивной химиотерапии.
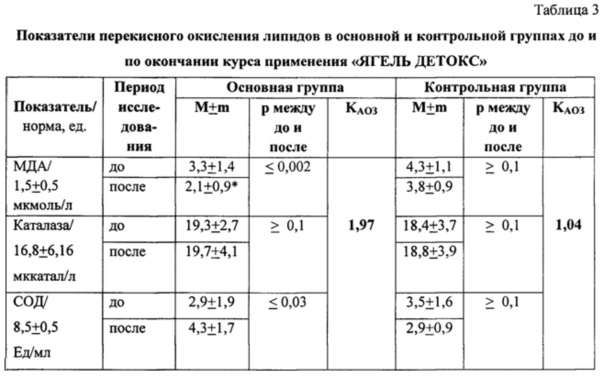
Поставленная цель достигается путем введения в комплексное лечение больных туберкулезом с МЛУ МБТ, на фоне схемы химиотерапии из 6-8 антибактериальных препаратов, средства БАД «ЯГЕЛЬ ДЕТОКС» (Свидетельство о государственной регистрации № RU.77.99.11.003.E.014127.09.12 от 27.09.2012 г.). Назначается через месяц после начала химиотерапии в соответствие с весом больного: до 60 кг веса больного по 1 капсуле, свыше 60 кг - по 2 капсулы. Прием проводится дважды в день: утром в 11 ч. и вечером в 20 ч., запить 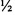 питьевой воды. Продолжительность курса 2 мес. По показаниям повторный курс проводится через 1 мес.
питьевой воды. Продолжительность курса 2 мес. По показаниям повторный курс проводится через 1 мес.
Для изучения эффективности препарата «ЯГЕЛЬ ДЕТОКС» проведено контролируемое слепое исследование, где в лечении 30 пациентов (основная группа) применяли БАД «ЯГЕЛЬ ДЕТОКС», а 20 пациентам (контрольная группа) применялось плацебо. У всех больных методом посева и абсолютных концентраций определена МЛУ МБТ. При лучевой диагностике у всех пациентов выявлены деструктивные изменения в легких. Контролируемая химиотерапия пациентам проводилась по IV режиму (Приказ МЗ РФ №109 от 21.03.2003; Приказ МЗ РФ №951 от 29.12.2014).
До и после завершения исследования проведены стандартные клинические, лабораторные и инструментальные методы исследования. Для более углубленного исследования проводились дополнительные биохимические исследования с определением показателей антиоксидантной защиты и перекисного окисления липидов. Для оценки иммунного статуса определяли показатели клеточного и гуморального иммунитета. Эти исследования проводились непосредственно до начала и по окончании курса приема «ЯГЕЛЬ ДЕТОКС».
Статистическая обработка биохимических и иммунологических показателей крови в группах наблюдения до и после применения «ЯГЕЛЬ ДЕТОКС» проведена с использованием коэффициента ранговой корреляции Спирмена. При сравнении качественных показателей с целью изучения сопоставимости, а также для сравнения эффективности лечения основной и контрольной групп больных использован критерий Хи-квадрат Пирсона.
Пациенты наблюдаемых групп сопоставимы по возрастно-половому и социальному составу, отмечаются умеренные признаки туберкулезной интоксикации (потеря в весе, слабость, потливость) и клинических проявлений (кашель, одышка, хрипы в легких, боли в груди), у большинства в клинической структуре преобладает инфильтративный туберкулез, сопровождающийся в половине случаев обильным бактериовыделением.
Все пациенты получали IV режим химиотерапии с учетом чувствительности к противотуберкулезным препаратам, в период интенсивной фазы в основном по схеме капреомицин/канамицин, фторхинолоны, пиразинамид, циклосерин/теризидон, протионамид/этионамид, аминосалициловая кислота не менее 8 мес.
С целью снижения побочных реакций и сопутствующей терапии с патогенетической направленностью через 1 мес химиотерапии больным назначили «ЯГЕЛЬ ДЕТОКС». Эффективность химиотерапии оценивали по критериям снижения симптомов интоксикации, клинических проявлений, прекращения бактериовыделения методом посева мокроты и закрытия полостей распада через 8 мес интенсивной фазы химиотерапии (табл. 1).
Через 8 мес химиотерапии у большинства больных обеих групп ликвидированы симптомы интоксикации и клинические проявления, при этом в основной группе они сохранились значительно реже. В основной группе прекращение бактериовыделения по данным посевов мокроты отмечалось у 26 (86,7%) пациентов, в контрольной группе - у 10 (50,0%) пациентов. По данным рентгено-томографических исследований в основной группе закрытие полостей распада отмечалось у 21 (70,0%) пациента, в контрольной группе - у 9 (45,0%) больных. Таким образом, различия в основной и контрольной группах по критериям прекращения бактериовыделения и закрытия полостей распада статистически достоверно значимы при p<0,01., применение «ЯГЕЛЬ ДЕТОКС» повышает эффективность лечения по данным критериям в 1,7 раз.
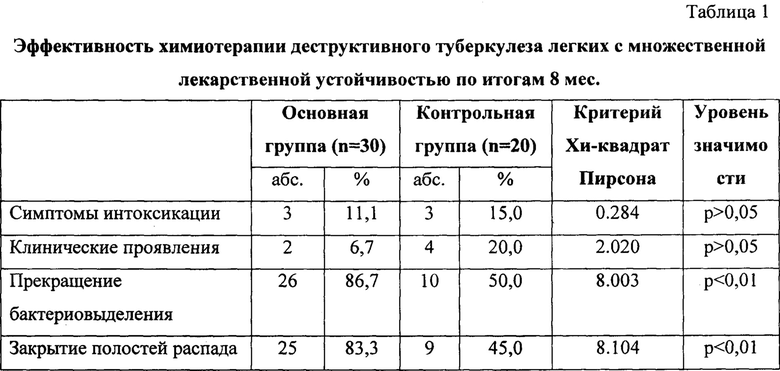
Эффективность применения «ЯГЕЛЬ ДЕТОКС» подтверждается показателями функционального состояния гепатобилиарной системы, перекисного окисления липидов и антиоксидантной системы, иммунного статуса (табл. 2-4).
Достоверные значения корреляции Спирмена после приема БАД между группами: *≤0,05; **≤0,01.
В группах до начала применения препарата отмечались незначительные изменения биохимических показателей, т.к. химиотерапия по IV режиму для больных с МЛУ МБТ была только назначена или проведена кратковременно. Через 2 мес после окончания курса приема «ЯГЕЛЬ ДЕТОКС» у больных наблюдаемых групп выявлены существенные различия: у больных основной группы показатели АЛТ и ACT, креатинина, тимоловой пробы в крови достоверно снизились по сравнению с исходными данными; в контрольной группе все отмеченные выше показатели имели тенденцию к росту, у части пациентов превышали нормальные значения, особенно отмечено повышение уровня общего билирубина и креатинина. При сравнении между группами отмечается существенное повышение альбумина и снижение билирубина у больных основной группы.
Таким образом, функциональное состояние гепатобилиарной системы у больных туберкулезом по основным данным биохимического исследования крови (уровень белка, аминотрансфераз, билирубина), несмотря на массивную химиотерапию антибактериальными препаратами в течение длительного времени, в т.ч. и с выраженными гепатотоксичными свойствами, при дополнительном приеме «ЯГЕЛЬ ДЕТОКС» не имело признаков к ухудшению, отмечена несомненная положительная динамика по сравнению с контрольной группой.
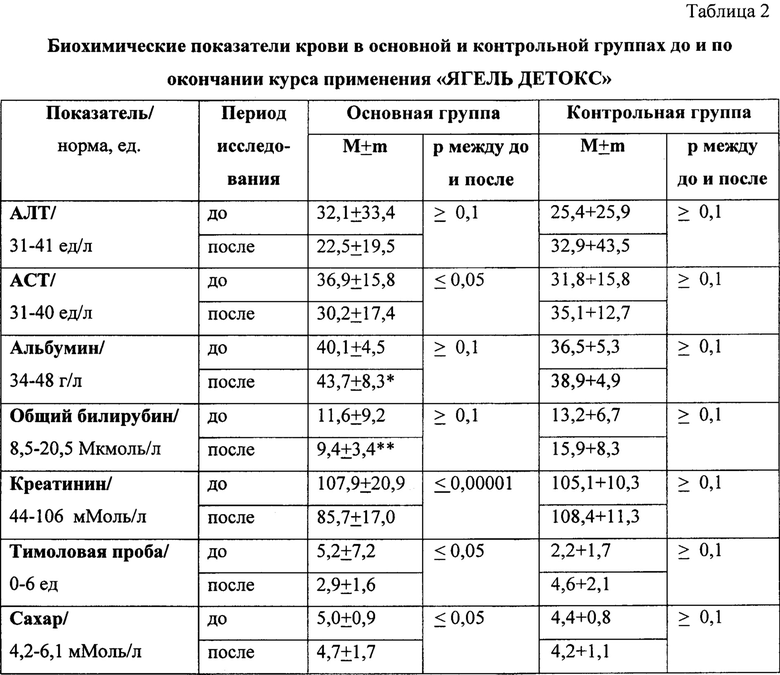
Результаты определения состояния перекисного окисления липидов (ПОЛ) на основе содержания малонового диальдегида (МДА), активности каталазы и супероксиддисмутазы (СОД) при туберкулезе легких показывают, что до начала применения БАД в комплексном лечении у больных обеих групп наблюдались высокие показатели МДА (см. табл. 3).
Достоверные значения корреляции Спирмена после приема БАД между группами: *≤0,0025.
Через 2 мес лечения, после окончания курса приема «ЯГЕЛЬ ДЕТОКС» у больных наблюдаемых групп выявлены существенные различия: у больных основной группы показатели МДА достоверно снизились по сравнению с исходными данными, показатели СОД достоверно повысились, в контрольной группе отмечалось несущественное снижение МДА и продолжающееся заметное снижение СОД. Наиболее ярким свидетельством изменения антиоксидантно-прооксидантного статуса является изменение коэффициента антиоксидантной защиты (КАОЗ) после курса приема «ЯГЕЛЬ ДЕТОКС» нормированного к соответствующим показателям до приема «ЯГЕЛЬ ДЕТОКС» - [(Каталаза)N+(СОД)N]/2(МДА)N (до приема «ЯГЕЛЬ ДЕТОКС» он в обеих группах был равен 1). Из табл. 3 видно, что в контрольной группе он практически не изменился (KАОЗ=1,04), а в основной группе увеличился до 1,97. То есть у больных основной группы, благодаря приему «ЯГЕЛЬ ДЕТОКС» клетки тканей организма оказались более защищенными от действия свободных радикалов в 1,9 раза.
Таким образом, применение «ЯГЕЛЬ ДЕТОКС» в комплексном лечении больных туберкулезом оказывает защитное действие на систему перекисного окисления липидов, что свидетельствует об угасании активности туберкулезного процесса.
При анализе показателей иммунного статуса больных отмечено, что процентные уровни Т-лимфоцитов периферической крови (CD3+) в контрольной и основной группах до начала применения препарата достоверно не отличались. Через 2 мес после окончания курса приема «ЯГЕЛЬ ДЕТОКС» у больных наблюдаемых групп выявлены существенные различия: в основной группе доли CD3+, CD4+ Т-лимфоцитов достоверно увеличились, тогда как доля CD8+ Т-лимфоцитов значимо уменьшилась. В контрольной группе заметных изменений не отмечено. Следовательно, применение «ЯГЕЛЬ ДЕТОКС» у пациентов основной группы оказало иммунопотенцирующее действие (см. табл. 4).
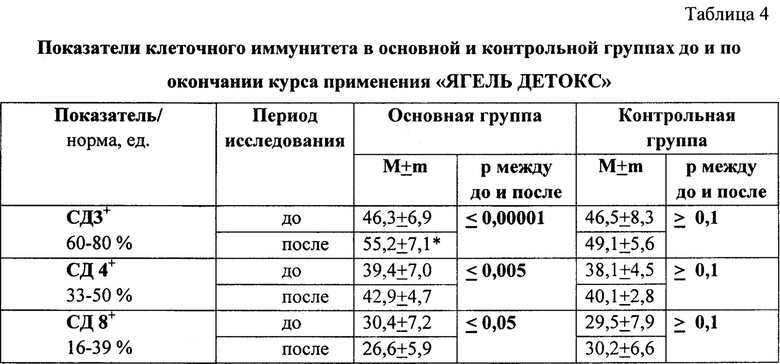
Достоверные значения корреляции Спирмена после приема БАД между группами: *≤0,01.
Положительные свойства «ЯГЕЛЬ ДЕТОКС», влияющие на снижение побочного действия антибактериальных препаратов подтверждаются клиническими примерами.
Клинический пример №1
Больная С., 32 лет, поступила на лечение в отделение легочного туберкулеза с диагнозом: Инфильтративный туберкулез верхней доли и S6 левого легкого в фазе распада и обсеменения, МБТ (+), МЛУ с устойчивостью к S Н R. На момент поступления жаловалась на слабость, потливость, повышение температуры тела до 37,5, кашель со слизисто-гнойной мокротой в течение 2-х недель. Аллергологический анамнез не отягощен. Алкоголь не злоупотребляет, курит умеренно. Работает, замужем, имеет двух детей. Считает себя больной в течение 2-х недель, когда повысилась температура тела до 37,2, появился кашель, при обращении в поликлинику сделан ФЛГ органов грудной клетки и в легких выявлены изменения. При микроскопии мокроты в большом количестве обнаружены КУМ. Взята на диспансерный учет по I (А) МБТ(+) группе и направлена на специализированное лечение в НПЦ «Фтизиатрия» стационарных условиях.
При поступлении состояние средней степени тяжести, рост 158 см., вес 58 кг., в легких выслушиваются сухие хрипы в верхнем отделе слева, живот мягкий, безболезненный, печень по краю реберной дуги. Сопутствующих заболеваний нет. На обзорной рентгенографии в 2х проекциях справа в S1, S2, слева S1+2, S6, S8 неоднородные затемнения, на фоне которых множественные очаговые изменения различной интенсивности, сливающиеся в инфильтраты с признаками деструкции. Бактериовыделение подтверждено методом микроскопии и посева, определена МЛУ МБТ с устойчивостью к стрептомицину (S) в 10γ, изониазиду (Н) в 1γ, рифампицину (R) 40γ. В OAК отмечается повышение СОЭ СОЭ-38 мм/ч. В биохимическом анализе крови особых изменений не отмечено, АЛТ - 26 U/л, АСТ - 48 U/л, билирубин общий - 14,4 ммоль/л, билирубин прямой - 2,9 ммоль/л, креатинин - 75 ммоль/л, тимоловая проба - 0,8 ед., сахар крови - 5,5 ммоль/л, общий белок - 68 г/л, альбумины - 37 г/л. По иммунограмме по сравнению с нормой отмечаются низкие показатели СД3 (44%) и СД4 (36%). Показатели перекисного окисления липидов: МДА - 4,2 мкмоль/л, каталаза - 20,3 мкмоль/л, СОД - 3,2 мкмоль/л.
В динамике через 1 мес после начала химиотерапии в биохимическом анализе крови отмечается повышение трансаминаз в 2,5 раза (АЛТ - 118 U/л, АСТ - 115 U/л). С целью улучшения переносимости химиотерапии и гепатопротекции назначен курс «ЯГЕЛЬ ДЕТОКС» в дозировке по 1 капсуле 2 раза в день в течение 2 мес.
Через 2 мес по окончании курса «ЯГЕЛЬ ДЕТОКС» клинико-рентгенологически отмечается улучшение самочувствия, повышение в весе до 3 кг, негативация мокроты методом микроскопии, рассасывание инфильтративных изменений и заметное уменьшение полости распада. Отмечается нормализация показателей крови - снижение СОЭ до 15 мм/ч; снижение АЛТ - 24 U/л и АСТ - 28 U/л; МДА снизилось до 1,79 мкмоль/л, содержание СОД повысилось до 6,54 мкмоль/л; показатели иммунограммы имеют тенденцию к повышению: СД3 - 53%, СД4 - 43%.
В результате 8 мес стационарного лечения получила полный курс интенсивной фазы химиотерапии по IV режиму (Z, Е, K, Fq, PAS/Cs) - 240 доз, отмечается стойкое прекращение бактериовыделения методом посева 5-кратно, закрытие полости распада. После курса «ЯГЕЛЬ ДЕТОКС» побочных эффектов на антибактериальные препараты не отмечено. Выписана с улучшением по месту жительства для прохождения фазы продолжения химиотерапии в амбулаторных условиях.
Клинический пример №2
Больной А., 19 лет, поступил на лечение в отделение легочного туберкулеза с диагнозом: инфильтративный туберкулез S1-S2 левого легкого фазе распада, МБТ (+) МЛУ, устойчивость к S Н R K Cap Eto. На момент поступления жалобы на общую слабость.
Анамнез жизни: состоял на учете у кардиолога по поводу врожденного порока сердца ДМПП, оперирован в подростковом возрасте. Отмечает частые ОРВИ, 4-5 раз в год, осложняющиеся бронхитами и трахеитами с обструктивным синдромом. Студент, холост, живет с родителями. Отмечает аллергические реакции на рыбу, морепродукты и некоторые лекарственные средства (названия не помнит). Не курит, алкоголь не злоупотребляет.
Больным себя не считает, выявлен при прохождении ежегодного медосмотра, где обнаружены изменения в легких, взят на диспансерный учет по I (А) МБТ(+) группе. Тубконтакт не известен, ФЛГ проходил ежегодно, направлен на специализированное лечение в НПЦ «Фтизиатрия» стационарных условиях.
При поступлении состояние средней степени тяжести, рост 162 см., вес 47 кг., телосложение гипостеническое, пониженного питания, подкожно-жировая клетчатка развита слабо. Лимфоузлы увеличены в подчелюстных группах до 1,0 см, безболезненны при пальпации. В легких дыхание проводится по всем полям, хрипов нет. Тоны сердца ритмичные, приглушены, ЧСС-86 в мин, АД - 100/60 мм рт.ст. Язык обложен белым налетом, влажный. Живот мягкий, чувствительный в эпигастрии. Печень по краю реберной дуги. Сопутствующие заболевания: состояние после устранения ДМПП; бронхиальная астма, аллергическая форма, стадия стойкой ремиссии; ВСД по смешанному типу; дискинезия желчевыводящих путей; полип желчного пузыря. По рентгенотомографическому исследованию в верхней доле левого легкого имеются множественные сливающиеся очагово-инфильтративные изменения, прослеживается полость распада с дорожкой к корню и очагами обсеменения в прикорневую зону и нижние отделы легкого. Бактериовыделение определено методом микроскопии и посева мокроты и смыва с бронхов при фибробронхоскопии, тест на лекарственную чувствительность определил МЛУ МБТ с устойчивостью к стрептомицину (S) в 10γ, изониазиду (Н) в 1γ, рифампицину (R) 40γ, канамицину (К) 30γ, этионамиду (Eto) 30γ, капреомицину (Сар) 30 γ. В общем анализе крови особых отклонений не выявлено, отмечается повышение СОЭ до 33 мм/ч. По биохимическому анализу крови особых изменений нет.
Через 1 мес после начала химиотерапии определено незначительное повышение трансаминаз и билирубинемия за счет повышения прямого билирубина (билирубин общий - 37,2 ммоль/л, прямой - 18 ммоль/л). По показателям иммунограммы отмечается снижение СД клеток: СД3 - 42%, СД4 - 28%, СД8 - 14%. Показатели перекисного окисления липидов повышены (МДА - 3,9 мкмоль/л), антиоксидантной защиты снижены (СОД - 2,5 мкмоль/л). С целью профилактики развития побочных реакций и патогенетической терапии назначен курс «ЯГЕЛЬ ДЕТОКС» по 1 капсуле 2 раза в день в течение 2 мес.
Через 2 мес лечения с назначением «ЯГЕЛЬ ДЕТОКС» отмечается снижение трансаминаз (ACT - 18 U/л, АЛТ - 24 U/л), билирубин приблизился к норме (Общий 21,5 мкмоль/л, прямой - 3,8 мкмоль/л), нормализация эозинофилов - 1% и снижение СОЭ до 6 мм/ч. Показатели иммунограммы повысились: СД3 - 65%, СД4 - 42%, СД8 - 22%. Показатели ПОЛ и АОС имеют тенденцию к нормализации. Рентгенологически отмечается некоторое рассасывание инфильтративных изменений, полость распада сохраняется. Отмечается снижение массивности бактериовыделения по микроскопии и посеву мокроты.
С учетом положительного эффекта через месяц химиотерапии курс «ЯГЕЛЬ ДЕТОКС» повторили по той же дозировке, 1 капе. 2 раза в день в течение 2 мес.
Через 8 мес химиотерапии с учетом формирования туберкулемы больному проведена резекция S1+2 левого легкого, послеоперационный период протекал удовлетворительно.
В результате комплексного лечения с приемом «ЯГЕЛЬ ДЕТОКС» больной успешно завершил интенсивную фазу химиотерапии, всего получил 305 доз IV режима (PAS, Z, Cs, Am, Fq), достигнуто стойкое прекращение бактериовыделения и ликвидация деструктивных изменений. Переносимость антибактериальных препаратов была удовлетворительной, несмотря на сопутствующие заболевания в виде дискинезии желчевыводящих путей с полипом желчного пузыря и отягощенного аллергологического анамнеза, возможные побочные реакции на антибактериальные препараты со стороны гепатобилиарной системы купированы назначением «ЯГЕЛЬ ДЕТОКС». Выписан с улучшением на дальнейшее лечение по фазе продолжения химиотерапии по месту жительства.
Таким образом, в результате применения «ЯГЕЛЬ ДЕТОКС» в качестве средства для лечения туберкулеза с множественной лекарственной устойчивостью, достигается прекращение бактериовыделения и закрытия полостей распада в 1,7 раз и снижение побочного токсического действия антибактериальных препаратов.
Изобретение относится к медицине, а именно к фтизиатрии, и может быть использовано для лечения туберкулеза с множественной лекарственной устойчивостью. Для этого в период интенсивной фазы химиотерапии больному дополнительно в течение двух месяцев назначают БАД «ЯГЕЛЬ ДЕТОКС» по 1 капсуле до 60 кг веса больного, свыше 60 кг по 2 капсулы два раза в день. Изобретение обеспечивает эффективное прекращение бактериовыделения и закрытие полостей распада, а также снижение побочного токсического действия антибактериальных препаратов. 4 табл., 2 пр.
Способ лечения туберкулеза с множественной лекарственной устойчивостью, отличающийся тем, что в период интенсивной фазы химиотерапии больному дополнительно в течение двух месяцев назначают БАД «ЯГЕЛЬ ДЕТОКС» по 1 капсуле до 60 кг веса больного, свыше 60 кг по 2 капсулы два раза в день.
| В.В | |||
| АНЬШАКОВА и др | |||
| Биоресурсный потенциал Северо-Восточных территорий России в создании инновационного производства эффективных препаратов лечебно-профилактического назначения// Экономика Востока России, 2015, выпуск 1, с.86-94 | |||
| СПОСОБ ЛЕЧЕНИЯ ИНФИЛЬТРАТИВНОГО ТУБЕРКУЛЕЗА ЛЕГКИХ, ВЫЗВАННОГО МНОЖЕСТВЕННО-ЛЕКАРСТВЕННОУСТОЙЧИВЫМИ И ВЫСОКОТОКСИЧНЫМИ ШТАММАМИ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА | 2009 |
|
RU2423129C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОАКТИВНОГО ТВЕРДОФАЗНОГО БИОПРЕПАРАТА АНТИБИОТИЧЕСКОГО ДЕЙСТВИЯ ЯГЕЛЬ ИЗ СЛОЕВИЩ ЛИШАЙНИКОВ | 2011 |
|
RU2467063C1 |
| MATA-ESPINOSA D.A | |||
| et al | |||
| Therapeutic effect of recombinant adenovirus encoding interferon-gamma in a murine model of progressive pulmonary tuberculosis // Mol Ther | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
Авторы
Даты
2018-11-28—Публикация
2017-05-22—Подача