Предложенное изобретение относится к генной терапии в регенеративной медицине и касается способов профилактики и лечения ишемического инсульта головного мозга с помощью средства, содержащего генетический материал - рекомбинантные гены человека, и может быть использовано для скорой неотложной помощи при наступлении ишемического инсульта головного мозга.
Проблема терапии острых нарушений мозгового кровообращения остается одной из актуальных в фундаментальной и практической медицине. В настоящее время качество и продолжительность жизни пациентов, перенесших инсульт, зависит от симптоматического лечения. Используемые лекарственные препараты могут лишь несколько замедлить течение болезни и неспособны остановить гибель нервных клеток, ведущую к инвалидности или смерти больного. В связи с этим, существует необходимость поиска новых методов лечения.
В последнее время активно проводятся клинические испытания новых генных, клеточных и генно-клеточных препаратов для стимулирования нейрорегенерации. Известно, что для терапии нейродегенеративных заболеваний во внимание принимаются ростовые и нейротрофические факторы, которые могут быть применены в качестве лекарственных препаратов. К ним относятся мозговой нейротрофический фактор (англ. Brain derived neurotrophic factor, BDNF), фактор роста нервов (англ. Nerve growth factor, NGF), глиальный нейротрофический фактор (англ. Glial derived neurotrophic factor, GDNF), инсулиноподобный фактор роста (англ. Insulinlike growth factor, IGF), основной фактор роста фибробластов (англ. Fibroblast growth factor 2, FGF2) и сосудистый эндотелиальный фактор роста (англ. Vascular endothelial growth factor, VEGF). Нейропротекторное действие этих факторов доказано в эксперименте in vitro и in vivo [Lunn J.S. et al. Stem cells: comprehensive treatments for amyotrophic lateral sclerosis in conjunction with growth factor delivery // Growth Factors. 2009. Vol. 27, №3. P. 133-140.]. При этом установлено, что комбинации нескольких нейротрофических факторов могут иметь более выраженный эффект на выживание нервных клеток. Клетки для клеточно-опосредованной генной терапии могут быть получены от больного (аутотрансплантация) или здорового человека (аллотрансплантация). Трансплантацию стволовых, прогениторных и дифференцированных клеток активно исследуют как способ доставки генов ростовых и нейротрофических факторов, сдерживающих гибель нейронов и стимулирующих нейрорегенерацию. Наиболее перспективны в этом смысле являются мононуклеарные клетки крови пуповины (МККП). Основанием для применения этих клеток является их пригодность как для алло-, так и для аутотрансплантации у человека, их низкая иммуногенность, доступность, простота получения и хранения [Liu Y. et al. An engineered transcription factor which activates VEGF-A enhances recovery after spinal cord injury. // Neurobiol. Dis. 2010. Vol. 37, №2. P. 384-393.].
Для лечения инсульта известны разные способы генной и клеточной терапии, эффективность которой доказана в многочисленных экспериментах на животных. Однако на сегодняшний день готовых, апробированных и эффективных препаратов, содержащих генетический материал, для сдерживания гибели нейронов при инсульте не существует.
Известные способы клеточной терапии инсульта
Способ клеточной терапии ишемического инсульта предполагает использование стволовых клеток различного генеза: индуцированные плюрипотентные клетки [Yuan М. et al. Effects of nucleus pulposus cell-derived acellular matrix on the differentiation of mesenchymal stem cells. // Biomaterials. 2013. Vol. 34, №16. P. 3948-3961.], нейрональные предшественники, полученные из ЭСК и крови пуповины [Zhu J. et al. Enhanced angiogenesis promoted by human umbilical mesenchymal stem cell transplantation in stroked mouse is Notch 1 signaling associated // Neuroscience. 2015. Vol. 290. P. 288-299.]. Положительный эффект у крыс с моделью ишемического инсульта установлен после внутривенной [Boltze J. et al. Determination of the Therapeutic Time Window for Human Umbilical Cord Blood Mononuclear Cell Transplantation following Experimental Stroke in Rats // Cell Transplant. 2012. Vol. 21, №6. P. 1199-1211.] или внутриартериальной [KarlupiaN. et al. Intraarterial transplantation of human umbilical cord blood mononuclear cells is more efficacious and safer compared with umbilical cord mesenchymal stromal cells in a rodent stroke model. // Stem Cell Res. Ther. 2014. Vol. 5, №2. P. 45.DOI 10.1186/scrt434] ксенотрансплантации МККП человека. В клинических испытаниях для трансплантации пациентам после инсульта преимущественно применяются аутологичные клетки, выделенные из красного костного мозга (мононуклеарные и мезенхимные стволовые клетки) или периферической крови (CD34+) [WangX.-L. et al. Umbilical cord blood cells regulate endogenous neural stem cell proliferation via hedgehog signaling in hypoxic ischemic neonatal rats. // Brain Res. 2013. Vol. 1518. P. 26-35.]. В России в НИИ Фундаментальной и клинической иммунологии были проведены клинические испытания клеточной терапии ишемического инсульта в восстановительном периоде с помощью интратекальной трансплантации фетальных клеток плода [Рабинович С.С. и др. Клеточная терапия мозгового инсульта // Клеточные технологии в биологии и медицине. 2005. №1. Ст.25-28.] и аутологичных макрофагов [Chernykh E.R. et al. Safety and Therapeutic Potential of M2 Macrophages in Stroke Treatment // Cell Transplant. 2016. Vol. 25, №8. P. 1461-1471.]. Особое внимание заслуживает тот факт, что, для терапии, как инсульта, так и других ишемических и нейродегенративных заболеваний, возможно применение аллогенных МККП без подбора донора на гистосовместимость, что является облигатным обстоятельством для замещения клеток реципиента на клетки донора в онкогематологии.
Известные способы генной терапии инсульта
Несмотря на то, что для лечения инсульта проводятся клинические испытания способа с применением аутологичных или аллогенных клеток различных типов [Jeong Н. et al. Efficacy and Safety of Stem Cell Therapies for Patients with Stroke: a Systematic Review and Single Arm Meta-Analysis // Int. J. Stem Cells. 2014. Vol. 7, №2. P. 63-69.], при этом нет ни одного способа, в котором используется прямая или клеточно-опосредованная генная терапия.
Эффективность генной терапии при инсульте доказана в многочисленных экспериментах в моделях на животных. Для доставки генов в мозг преимущественно применяются инъекции вирусных векторов в желудочки мозга или в зону инфаркта. Первым Российским лекарственным препаратом, содержащим генетический материал, является «Неоваскулоген». Препарат разработан ОАО «Институт стволовых клеток человека» на основе плазмидного вектора (pCMV) и рекомбинантного гена сосудистого эндотелиального фактора роста (VEGF165). Препарат предназначен для лечения ишемии нижних конечностей атеросклеротического генеза, продается в России с 2012 года. Также известен способ стимулирования регенерации спинного мозга путем введения в область повреждения плазмидного вектора pBud-VEGF-FGF2 (Патент РФ на изобретение №2459630). В настоящее время ООО «НТфарма» совместно с Научным центром неврологии проводят клинические испытания препарата «АдеВаск» для генной терапии бокового амиотрофического склероза [Zavalishin I.A. et al. Gene therapy of amyotrophic lateral sclerosis. // Bull. Exp. Biol. Med. 2008. Vol. 145, №4. P. 483-486.]. Препарат создан на основе двух аденовирусных векторов, несущих ген сосудистого эндотелиального фактора роста (VEGF) и ген ангиогенина (ANG). Способ предполагает введение комбинации аденовирусных векторов в скелетные мышцы пациента. Такой способ не позволяет проводить адресную доставку терапевтических генов в места нейродегенерации. Кроме того, инъекция аденовирусного вектора приведет к трансдукции разных других клеточных типов и в первую очередь мышечных, а повторные инъекции аденовирусного вектора могут вызывать сильную иммунологическую реакцию.
Список потенциальных молекул-нейропротекторов включает разные ростовые и нейротрофические факторы (BDNF, GDNF, VEGF), анти-апоптозные белки (Bcl-2, Bcl-XL), белки теплового шока (Hsp25, Hsp70), противовоспалительные молекулы (IL-1RA) [Rhim Т., Lee М. Targeted delivery of growth factors in ischemic stroke animal models // Expert Opin. DrugDeliv. 2016. Vol. 13, №5. P. 709-723.]. Для нас, из перечисленных, представляются наиболее перспективными сосудистый эндотелиальный фактор роста (VEGF), глиальный нейротрофический фактор (GDNF) и молекула адгезии нервных клеток (NCAM). Сосудистый эндотелиальный фактор роста (VEGF) обладает специфической митогенной активность в отношении эндотелиальных клеток [Ferrara N. et al. Molecular and Biological Properties of the Vascular Endothelial Growth Factor Family of Proteins // Endocr. Rev. 1992. Vol. 13, №1. P. 18-32.]. Однако, кроме ангиогенного действия VEGF также проявляет свойства типичного нейротрофического фактора. Он поддерживает выживание чувствительных [SondellM., LundborgG., KanjeM. Vascular endothelial growth factor has neurotrophic activity and stimulates axonal outgrowth, enhancing cell survival and Schwann cell proliferation in the peripheral nervous system. // J. Neurosci. 1999. Vol. 19, №14. P. 5731-5740.] и двигательных [Islamov R.R. et al. Induction of VEGF and its Flt-1 receptor after sciatic nerve crush injury. // Neuroreport. 2004. Vol. 15, №13. P. 2117-2121.] нейронов, стимулирует пролиферацию нейральных стволовых клеток, астроцитов [Rosenstein J.M. et al. Patterns of brain angiogenesis after vascular endothelial growth factor administration in vitro and in vivo. // Proc. Natl. Acad. Sci. U.S.A. 1998. Vol. 95, №12. P. 7086-7091.] и шванновских [Sondell M., Lundborg G., Kanje M. Vascular endothelial growth factor has neurotrophic activity and stimulates axonal outgrowth, enhancing cell survival and Schwann cell proliferation in the peripheral nervous system. // J. Neurosci. 1999. Vol. 19, №14. P. 5731-5740.] клеток. Глиальный нейротрофический фактор (GDNF) имеет выраженное нейропротекторное действие на нейроны головного и спинного мозга [Cheng Н., Wu J.-P., Tzeng S.-F. Neuroprotection of glial cell line-derived neurotrophic factor in damaged spinal cords following contusive injury. // J. Neurosci. Res. 2002. Vol.69, №3. P. 397-405.], стимулирует рост нервных отростков [Iannotti С.et al. Glial cell line-derived neurotrophic factor-enriched bridging transplants promote propriospinal axonal regeneration and enhance myelination after spinal cord injury. // Exp. Neurol. 2003. Vol. 183, №2. P. 379-393.]. Молекула адгезии нервных клеток NCAM экспрессируется на поверхности нейронов и клеток нейроглии. В ходе нейроонтогенеза и нейрорегенерации опосредуемые NCAM межклеточные взаимодействия обеспечивают выживание и миграцию нейронов, направленный рост нейритов и синаптогенез.
Известные способы клеточно-опосредованной генной терапии инсульта
Эффективность применения клеточной терапии для лечения инсульта в эксперименте с использованием нейрональных предшественников, полученных из эмбриональных стволовых [Mohamad О. et al. Vector-free and transgene-free human iPS cells differentiate into functional neurons and enhance functional recovery after ischemic stroke in mice. // PLoS One 2013. Vol. 8, №5. e64160. DOI 10.1371/journal.pone.0064160], индуцированных плюрипотентных клеток [Yuan M. et al. Effects of nucleus pulposus cell-derived acellular matrix on the differentiation of mesenchymal stem cells. // Biomaterials. 2013. Vol. 34, №16. P. 3948-3961.], мезенхимных стволовых клеток, выделенных из красного костного мозга [Не Q. et al. Transplantation of bone marrow-derived mesenchymal stem cells (BMSCs) improves brain ischemia-induced pulmonary injury in rats associated to TNF-α expression // Behav. Brain Funct. 2016. Vol. 12, №9.DOI 10.1186/s 12993-016-0093-0] или крови пуповины [Zhu H. et al. Phase III Clinical Trial Assessing Safety and Efficacy of Umbilical Cord Blood Mononuclear Cell Transplant Therapy of Chronic Complete Spinal Cord Injury. // Cell Transplant. 2016. Vol. 25, №11. P. 1925-1943.] предполагает применение этих клеток, как носителей терапевтических генов для доставки в мозг. Так, в эксперименте мезенхимные стволовые клетки применялись для доставки в мозг BDNF [NomuraT. et al. Infusion of brain-derived neurotrophic factor gene-modified human mesenchymal stem cells protects against injury in a cerebral ischemia model in adult rat. // Neuroscience. 2005. Vol. 136, №1. P. 161-169.], PIGF [Liu H. et al. Neuroprotection by P1GF gene-modified human mesenchymal stem cells after cerebral ischaemia. // Brain. 2006. Vol. 129, №10. P. 2734-2745.] и VEGF [Chen Y. et al. Regulation of naotai recipe on the expression of HIF-1α/VEGF signaling pathway in cerebral ischemia/reperfasion rats. // Chinese J. Integr. Tradit. West. Med. 2014. Vol. 34, №10. P. 1225-1230.]. Преимущество клеточно-опосредованной генной терапии над прямой обусловлено, тем, что кроме доставки терапевтического гена, клеточно-опосредованная терапия обеспечивает толерантность иммунной системы реципиента к вирусным антигенам, позволяет контролировать продукцию терапевтических молекул, а клеточные носители могут дифференцироваться в заданном направлении и быть источником биологически активных молекул, например, стимуляторов регенерации.
В способе [Suzuki К. et al. Highly efficient transient gene expression and gene targeting in primate embryonic stem cells with helper-dependent adenoviral vectors // Proc. Natl. Acad. Sci. 2008. Vol. 105, №37. P. 13781-13786.], чтобы избежать конфликт с вирусным носителем, доставку терапевтического гена осуществляли с помощью клеточного носителя. Терапевтический ген, кодирующий глиальный нейротрофический фактора роста (GDNF) для генетической модифиации мезенхимных стволовых клеток доставляется с помощью ретровирусного вектора. Существенным недостатком этого способа является интеграция вируса в геном трансплантируемых клеток, что может привести к мутациям и последующей опухолевой трансформацией генетически модифицированных клеток.
Известен способ получения генетически модифицированных клеток для лечения ишемических заболеваний сердца [Chen Н.К. et al. Combined cord blood stem cells and gene therapy enhances angiogenesis and improves cardiac performance in mouse after acute myocardial infarction // Eur. J. Clin. Invest. 2005. Vol. 35, №11. P. 677-686.]. Авторами для стимулирования ангиогенеза предложен способ получения лекарственного препарат на основе стволовых клеток пуповинной крови и двух векторов, кодирующих VEGF и Angiopoietin-1 на базе аденоассоциированного вируса. Важным недостатком препарата является интеграция вирусного вектора в геном стволовых клеток и последующая непредсказуемая дифференцировка стволовых клеток или их опухолевая трансформация. Кроме того, для приготовления эффективной лекарственной формы препарата по этому способу требуется большое количество стволовых клеток, что также усложняет процедуру получения генно-клеточного препарата.
Для лечения нейродегенеративных заболеваний с помощью генетически модифицированных МККП известны разные способы. Так для лечения разных случаев нейродегенерации известен способ трансплантации МККП путем инъекции в периферическую кровь реципиента [Bachstetter A.D. et al. Peripheral injection of human umbilical cord blood stimulates neurogenesis in the aged rat brain. // Neurosci. 2008. Vol. 9, №22. DOI 10.1186/1471-2202-9-22].
Известен способ генетической модификации МККП с помощью двухкассетного плазмидного вектора, кодирующего два терапевтических гена. Этот способ позволяет получать генетически модифицированные клетки, сверхэкспрессирующие два ростовых фактора VEGF и GDNF [патент РФ №2431669, МПК C12N 15/00 опубл. 20.10.2011, БИ №29]. Известен также способ стимулирования посттравматической регенерации спинного мозга с помощью генетически модифицированных МККП, трансдуцированных аденовирусом, несущим ген GDNF [патент РФ №2521225, МПК А61К 48/00, опубл. 27.06.2014, БИ №18]. В другой модификации этого способа двухкассетный плазмидный вектор содержит один терапевтический ген, кодирующий VEGF, и второй ген, кодирующий нейрональную молекулу адгезии L1 [Ризванов А.А. и др. Генно-клеточная терапия бокового амиотрофического склероза мононуклеарными клетками пуповинной крови человека, сверхэкспрессирующими гены нейронной молекулы адгезии L1cam и сосудистого эндотелиального фактора роста vegf. // Гены и Клетки. 2010. Vol. 5, №4. Р. 55-65.]. Предполагается, что нейрональная молекула адгезии повысит выживаемость, адресную миграцию и, следовательно, продолжительность терапевтического воздействия трансплантированных клеток. Однако, указанные способы с использованием плазмидного вектора, имеют серьезный недостаток. Плазмидный вектор имеет очень короткий срок экспрессионной активности. Кроме того, в указанных способах не изучена клиническая эффективность вышеуказанных лекарственных препаратов в терапии нейродегенеративных заболеваний. Поэтому прототип характеризуется недостаточной продукцией терапевтических молекул и неизвестной эффективностью действия при его применении.
Наиболее близким к заявленному изобретению является способ лечения бокового амиотрофического склероза (БАС) путем введения МККП, одновременно трансдуцированных аденовирусами, несущими гены VEGF, GDNF и NCAM. Установлено, что такой способ генно-клеточной терапии сдерживает развитие симптомов и продлевает жизнь у мышей с моделью БАС [Islamov R.R. et al. Tandem delivery of multiple therapeutic genes using umbilical cord blood cells improves symptomatic outcomes in ALS // Mol. Neurobiol., 2017. 54:4756-4763 DOI 10.1007/s12035-016-0017-x.].
Целью заявленного изобретения является средство для генно-клеточной терапии инсульта головного мозга, сдерживающее гибель нейронов в зоне ишемической полутени при инсульте головного мозга.
Способы генной терапии для инсульта головного мозга и средство для сдерживания гибели нейронов в зоне ишемического инсульта полутени при инсульте головного мозга в настоящее время не известны.
Поставленная цель достигается применением генетического материала, состоящего из гена сосудистого эндотелиального фактора роста VEGF, гена глиального нейротрофического фактора GDNF и гена нейрональной молекулы адгезии NCAM в качестве средства сдерживания гибели нейронов при ишемическом инсульте головного мозга и способом клеточно-опосредованной терапии ишемического инсульта средством сдерживания гибели нейронов при ишемическом инсульте головного мозга, в котором терапевтическую эффективную дозу средства сдерживания гибели нейронов непосредственно вводят путем интратекальной инъекции в течении 4-х часов после наступления ишемического инсульта головного мозга.
Таким образом, рекомбинантные репликативно-дефектные аденовирусы, содержащие фрагменты ДНК, кодирующие сосудистый эндотелиальный фактор роста изоформы 165 (VEGF 165), глиальный нейротрофический фактор GDNF и нейрональную молекулу адгезии 1 (англ. Neural cell adhesion molecule 1, NCAM1) используют для клеточно-опосредованной генной терапии. Комбинация терапевтических генов, кодирующих VEGF 165, GDNF и NCAM1 используется для сдерживания гибели нейронов при ишемическом инсульте головного мозга. Генетически модифицированные мононуклеарные клетки крови пуповины используются для доставки терапевтических генов в головной мозг.
Сущность предполагаемого изобретения иллюстрируется примером клеточно-опосредованной генной терапии ишемического инсульта головного мозга для сдерживания гибели нейронов в очаге нейродегенерации с помощью генетически модифицированных клеток (МККП+Ad5-VEGF165+Ad5-GDNF+Ad5-NCAM1) в модели ишемического инсульта головного мозга на крысах.
Пример клеточно-опосредованной генной терапии ишемического инсульта в моделях на крысах.
Первый этап. Получение генетически модифицированных МККП, сверхэкспрессирующих рекомбинантные гены VEGF165, GDNF и NCAM1 [препарат: МККП+Ad5-VEGF+GDNF+NCAM].
Аденовирусные векторы
Рекомбинантные репликативно-дефектные вирусные векторы созданы на основе аденовируса человека 5 серотипа (Ad5) в НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи (г.Москва), как было описано ранее [Povysheva T.V. et al. Post-spinal cord injury astrocyte-mediated functional recovery in rats after intraspinal injection of the recombinant adenoviral vectors Ad5-VEGF and Ad5-ANG // J Neurosurg Spine. 2017. Vol. 27, №1. p. 105-115.]. В настоящем исследовании были использованы Ad5, несущие гены VEGF 165 (Ad5-VEGF), GDNF (Ad5-GDNF) и NCAM1 (Ad5-NCAM).
Мононуклеарные клетки крови пуповины
Заготовку крови пуповины производили по инструкции Банка стволовых клеток КГМУ. Выделение мононуклеарных клеток крови пуповины (МККП) проводили в градиенте плотности фиколла по стандартной методике [Islamov R.R. et al. Symptomatic improvement, increased life-span and sustained cell homing in amyotrophic lateral sclerosis after transplantation of human umbilical cord blood cells genetically modified with adeno-viral vectors expressing a neuroprotective factor and a neur // Curr. GeneTher. 2015. Vol. 15, №3. P. 266-276.]. Сразу после выделения МККП высевали на 6 см культуральный планшет из расчета 2 млн. клеток/лунка и одновременно трансдуцировали тремя аденовирусными векторами в комбинации Ad5-VEGF+Ad5-GDNF+Ad5-NCAM в равном соотношении каждого вектора Ad5-VEGF (1/3), Ad5-GDNF (1/3), Ad5-NCAM (1/3), где MOI (multiplicity of infection - множественность инфицирования) был равен 10. Через 12 часов культивирования генетически модифицированные клетки (МККП+Ad5-VEGF+GDNF+NCAM) собирали и растворяли в стерильном физиологическом растворе из расчета 2×106 клеток в 20 мкл. Полученные генетически модифицированные МККП являются лекарственным препаратом, содержащим генетический материал для сдерживания гибели нейронов при ишемическом инсульте головного мозга. Второй этап. Способ клеточно-опосредованной генной терапии ишемического инсульта головного мозга для сдерживания гибели нейронов в очаге нейродегенерации в моделях на крысах
Операции на животных
Эксперименты выполнены с разрешения Локального этического комитета Казанского государственного медицинского университета (протокол №10, 2017 г). Половозрелые самцы крыс линии Wistar (250-300 г) приобретены в питомнике лабораторных животных «Пущино» (Пущино, Россия). Содержание и уход за животными производились в соответствии с международными правилами и нормами. Животные находились по одному в клетке в стандартных лабораторных условиях с соблюдением 12-ти часового цикла день/ночь и свободным доступом к пище и воде. Ишемический инсульт головного мозга вызывали методом дистальной окклюзии средней мозговой артерии [Lemarchant S. et al. Anti-inflammatory effects of ADAMTS-4 in a mouse model of ischemic stroke // Glia. 2016. Vol. 64, №9. P. 1492-507. doi: 10.1002/glia.23017.]. Кратко, глубокую анестезию вызывали путем внутрибрюшинного введения Золетила 100 (Virbac Sante Animale, Франция) 3 мг/кг и Ксилы (Interchemiewerken «De Adelaar» B.V», Нидерланды) 4.8 мг/кг. Температуру тела крысы во время операции поддерживали в пределах 37-38°С при помощи терморегулирующей панели. На первом этапе оперативного вмешательства для снижения кровотока в виллизиевом круге справа через вертикальный разрез по серединной линии шеи препарировали общую сонную артерию, которую лигировали с помощью шелковой хирургической нити (3.0), кожную рану ушивали лавсаном. На втором этапе операции слева производили продольный разрез кожи от угла глаза до наружного отверстия слухового прохода. Височную кость освобождали от прилегающей одноименной мышцы и с помощью твердосплавного бора №2 высверливали трепанационное отверстие в височной кости диаметром 10 мм. Под операционным микроскопом иссекали твердую мозговую оболочку, окклюзию средней мозговой артерии проводили с помощью термокоагулятора. После чего трепанационное отверстие укрывали височной мышцей, кожу ушивали лавсаном. Все операционные швы обрабатывали 2% раствором йода.
Через четыре часа после моделирования инсульта животным, находящихся в наркозе, производили ламинэктомию на уровне L4-L5 и интратекально вводили генно-клеточный препарат МККП+Ad5-VEGF+ GDNF+NCAM (2×106 клеток в 20 мкл 0.9% NaCl) (n=7). Животным из контрольной группы вводили 20 мкл 0.9% NaCl (n=6).
13
Третий этап. Оценка эффективности клеточно-опосредованной генной терапии инсульта
Идентификация МККП человека в головном мозге крысы и оценка способности генетически модифицированных МККП человека синтезировать рекомбинантные VEGF, GDNF и NCAM после интратекальной инъекции крысам с моделью ишемического инсульта головного мозга. Для идентификации VEGF, GDNF и NCAM в МККП было проведено двойное иммунофлуоресцентное окрашивание фронтальных срезов головного мозга крыс с помощью антител в комбинациях: (1) против ядерного АГ человека (HuAN) и (2) против одного из терапевтических генов VEGF, GDNF, или NCAM. Через 3 недели после интратекальной инъекции в очаге инсульта были обнаружены HuAN-позитивные клетки, экспрессирующие VEGF, GDNF и NCAM. Таким образом, через 3 недели после интратекальной инъекции МККП выявляются в зоне «полутени», где они не только сохраняют жизнеспособность, но и активно синтезируют терапевтические молекулы. Этот факт дает основание полагать, что генетически модифицированные МККП+Ad-VEGF+Ad-GDNF+Ad-NCAM за счет синергичной сверхпродукции терапевтических молекул VEGF и GDNF повышают жизнеспособность нервных клеток в очаге инсульта. Дополнительная трансдукция МККП аденовирусом, экспрессирующим NCAM, повышает выживаемость МККП после трансплантации и эффективность их адресной миграции в зону нейродегенерации.
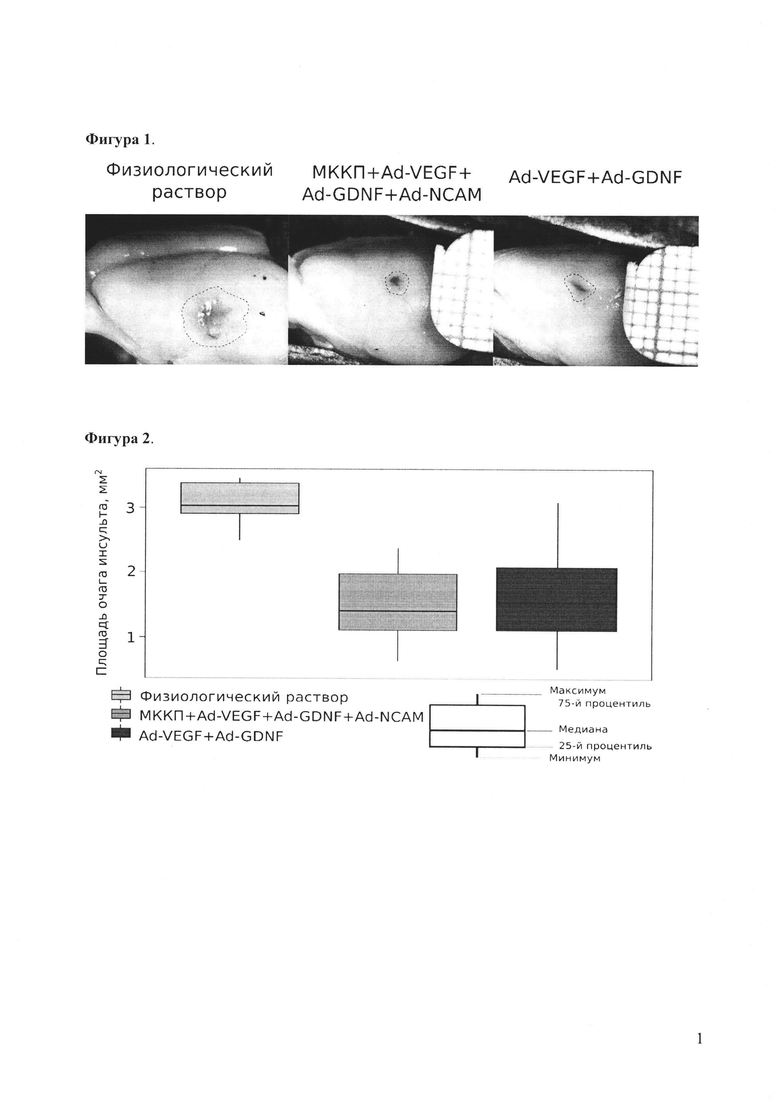
Эффективность сдерживания гибели нейронов при моделировании ишемического инсульта у крысы на фоне клеточно-опосредованной генной терапии. При сравнении площадей инфаркта головного мозга через 3 недели после моделирования инсульта у животных контрольной и терапевтических групп, выявлены статистически значимые различия. Следует обратить внимание на тот факт, что в группе животных, получивших интратекальную инъекцию генетически модифицированных клеток (МККП+Ad-VEGF+Ad-GDNF+Ad-NCAM) в течение 4 часов после моделирования ишемического инсульта головного мозга, медиана площади очага (1,41 [0,64];[2,38]) была на 53,3% ниже, чем в контрольной группе животных с инъекцией физиологического раствора (3,02 [2,48];[3,45]).
Площади очагов инсульта головного мозга через 3 недели после дистальной окклюзии средней мозговой артерии у животных, которым интратекально вводили физиологический раствор через 4 часа после моделирования инсульта (Физиологический раствор) и у животных, которым интратекально вводили генетически модифицированные клетки крови пуповины, экспрессирующих трансгены, кодирующие сосудистый эндотелиальный фактор роста (VEGF), глиальный нейротрофический фактор (GDNF) и нейрональную молекулу адгезии (NCAM), через 4 часа после моделирования инсульта (МККП+Ad-VEGF+Ad-GDNF+Ad-NCAM) представлены на Фигура 1 и Фигура 2.
Таким образом, Пример 1 свидетельствует что, генетически модифицированные МККП после интратекального введения с помощью церебро-спинальной жидкости (ЦСЖ) достигают головного мозга, где они мигрируют в область ишемической полутени и активно продуцируют рекомбинантные терапевтические молекулы, сдерживающие гибель нейронов. Эти результаты подтверждают возможность применения МККП как клеточных носителей терапевтических генов для клеточно-опосредованной генной терапии инсульта головного мозга.
Преимущество заявленного способа лечения ишемического инсульта с помощью интратекального введения генетически модифицированных клеток от известных в мире на дату подачи заявки заключается в использовании генетически модифицированных мононуклеарных клеток пуповинной крови человека, одновременно трансдуцированных тремя рекомбинантными аденовирусами, один из которых экспрессирует нейрональную молекулу адгезии, а два других нейротрофические факторы - молекулы, сдерживающие гибель нейронов. Применение такой комбинации рекомбинантных аденовирусов для модификации МККП является перспективным. Экспрессия нейрональной молекулы адгезии в трансплантированных клетках повышает их адресную миграцию в область ишемической полутени и жизнеспособность клеток-продуцентов терапевтических молекул, что в свою очередь обеспечивает секрецию терапевтических молекул сразу после трансплантации генетически модифицированных клеток и более продолжительное, а значит и более эффективное действие терапевтических молекул на нервные клетки. Лекарственный препарат генетически модифицированных клеток по способу используют в лечебных целях по конкретному назначению, например - путем интратекального введения пациенту с ишемическим инсультом головного мозга.
Приведенный пример осуществления предлагаемого способа не ограничивает применение иных, по сравнению с приведенным в примере, генных и клеточных компонентов. Использовать заявленный генно-клеточный лекарственный препарат рекомендуется также как способ лечения нейродегенеративных заболеваний, например, болезни Хантигтона, болезни Паркинсона, болезни Альцгеймера, бокового амиотрофического склероза, травматического повреждения спинного и головного мозга, так как заявленный препарат повышает жизнеспособность нервных клеток ЦНС.
Приведенный пример использования заявляемого изобретения показывают его полезность в практической медицине для лечения людей. Заявляемое изобретение способствует получению лекарственного препарата с лечебным свойством сдерживания гибели нервных клеток при ишемическом инсульте головного мозга.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ превентивной генной терапии для сдерживания гибели нейронов при ишемическом инсульте головного мозга | 2020 |
|
RU2748940C2 |
| Способ персонифицированной генной терапии при угрозе ишемического инсульта головного мозга | 2023 |
|
RU2808256C1 |
| Способ лечения травматического повреждения спинного мозга | 2021 |
|
RU2758760C1 |
| Способ изготовления средства для клеточно-опосредованной генной терапии и средство для клеточно-опосредованной генной терапии | 2019 |
|
RU2716013C2 |
| Фармацевтическая композиция и способ ее использования для терапии повреждений головного и спинного мозга | 2022 |
|
RU2784233C1 |
| СПОСОБ СТИМУЛИРОВАНИЯ РЕГЕНЕРАЦИИ СПИННОГО МОЗГА С ПОМОЩЬЮ ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫХ КЛЕТОК КРОВИ ПУПОВИНЫ ЧЕЛОВЕКА | 2013 |
|
RU2521225C2 |
| СПОСОБ СТИМУЛИРОВАНИЯ НЕЙРОГЕНЕРАЦИИ С ПОМОЩЬЮ ГЕНЕТИЧЕСКИХ КОНСТРУКЦИЙ | 2011 |
|
RU2459630C1 |
| Ноотропная композиция на основе полипептидных комплексов, выделенных из нейрональных прогениторных клеток в условиях теплового шока, и способ ее получения | 2019 |
|
RU2752906C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО ПРЕПАРАТА ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫХ КЛЕТОК | 2009 |
|
RU2431669C2 |
| Способ получения глиальных производных индуцированных плюрипотентных стволовых клеток с повышенной экспрессией BDNF для терапии ишемического инсульта | 2023 |
|
RU2829361C1 |
Изобретение относится к области медицины и предназначено для клеточно-опосредованной генной терапии ишемического инсульта. Терапевтическую эффективную дозу генетического материала, состоящего из гена сосудистого эндотелиального фактора роста VEGF, гена глиального нейротрофического фактора GDNF и гена нейрональной молекулы адгезии NCAM, непосредственно вводят путем интратекальной инъекции в течение 4-х часов после наступления ишемического инсульта головного мозга. Изобретение обеспечивает получение лекарственного препарата со свойством предупреждения и сдерживания гибели нейронов при ишемическом инсульте головного мозга. 2 ил., 1 пр.
Способ клеточно-опосредованной генной терапии ишемического инсульта средством сдерживания гибели нейронов при ишемическом инсульте головного мозга, заключающийся в том, что терапевтическую эффективную дозу средства сдерживания гибели нейронов, представляющего собой генетический материал, состоящий из гена сосудистого эндотелиального фактора роста VEGF, гена глиального нейротрофического фактора GDNF и гена нейрональной молекулы адгезии NCAM, непосредственно вводят путем интратекальной инъекции в течение 4-х часов после наступления ишемического инсульта головного мозга.
| ИСЛАМОВ Р.Р | |||
| и др | |||
| Исследование экспрессии рекомбинантных терапевтических генов в мононуклеарных клетках крови пуповины, трансдуцированных тремя аденовирусными векторами, кодирующими нейротрофические факторы GDNF и VEGF и молекулу нейрональной адгезии NCAM | |||
| Гены & клетки | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПРЕДОТВРАЩЕНИЯ ГИБЕЛИ НЕРВНЫХ КЛЕТОК, СПОСОБ ПРОФИЛАКТИКИ | 2001 |
|
RU2230060C2 |
| ISLAMOV R.R | |||
| et al | |||
| Tandem Delivery of Multiple Therapeutic Genes Using Umbilical Cord Blood Cells Improves Symptomatic Outcomes in ALS | |||
| Mol Neurobiol | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Токарный резец | 1924 |
|
SU2016A1 |
Авторы
Даты
2019-01-10—Публикация
2017-12-01—Подача