Впервые синтезированы новые химические соединения - олигопирокатехолаты меди Cu(II), кобальта Со(II), железа Fe(II), марганца Mn(II) и никеля Ni(II).
Одним из аспектов применения олигопирокатехолатов металлов переменной валентности может стать их применение в качестве катализаторов в реакциях окисления меркаптидной, меркаптановой и сульфидной серы, фенолов и т.д., в том числе, в условиях демеркаптанизации углеводородного сырья.
Аналогами олигопирокатехолатов переходных металлов по структуре являются их мономеры - катехолаты переходных металлов.
Аналогами олигопирокатехолатов переходных металлов по назначению являются - комплексы на основе ванадила VO(II) с олигопирокатехином (далее по тексту ОПК), о-хиноновые комплексы металлов II группы (Mg, Zn, Cd) и IV группы (Ge, Sn, Pb). Ниже описаны способы их получения.
Известны о-хиноновые комплексы металлов II группы (Mg, Zn, Cd), полученные прямым окислением амальгамированных металлов о-хиноном (3,6-ди-трет-бутил-о-хиноном) в среде различных растворителей. Также известны о-хиноновые комплексы металлов IV группы (Ge, Sn, Pb), при синтезе которых применялись три типа превращений: 1. прямое окисление металла о-хиноном; 2. обменные процессы с участием о-хиноновых производных щелочных металлов и галогенидов металлов IV группы;. 3. - окислительное присоединение о-хинона к хлоридам германия(II) и олова(II) [2-3]. Выход комплексов варьировался от 73,6% до 95%.
Известны также различные методы синтеза катехолатов: 1. окислительное присоединение соответствующего о-хинона (3,6-ди-трет-бутил-о-хинон) к трифенилсурьме (III); 2. обменная реакция катехолата таллия (I) и дихлорида трифенилсурьмы (V); 3. взаимодействие пирокатехина с дихлоридом трифенилсурьмы (V) в присутствии основания. Наиболее простым методом синтеза комплексов данного класса является окислительное присоединение о-бензохинона к производным сурьмы(III), не требующее в большинстве случаев отделения целевого продукта от побочных и протекающее с выходами, близкими к количественным. Перекристаллизация полученных катехолатов из полярных растворителей приводит к образованию шестикоординационных комплексов [4-5].
Наиболее близким по технической сущности и достигаемому результату является способ получения комплексов на основе ионов ванадила VO(II) с ОПК и пирокатехина (далее по тексту ПКХ), заключающийся в использовании водных растворов сульфата ванадила, ПКХ, ОПК и гидроксида калия (далее по тексту KOH).
ОПК синтезировали путем окислительной поликонденсации ПКХ в присутствии 30%-ного водного раствора Н2О2. Затем смешивали водные растворы ПКХ или ОПК и KOH при мольном соотношении 1:1 или 1:2. Далее раствор образовавшихся фенолятов смешивали с расчетным количеством водного раствора сульфата ванадила - VOSO4 [1].
Целью настоящего изобретения является разработка новых комплексных соединений олигомерной природы, а именно, олигопирокатехина (ОПК) с металлами переменной валентности (Cu, Со, Fe, Mn, Ni), которые могут быть представлены следующей структурой:
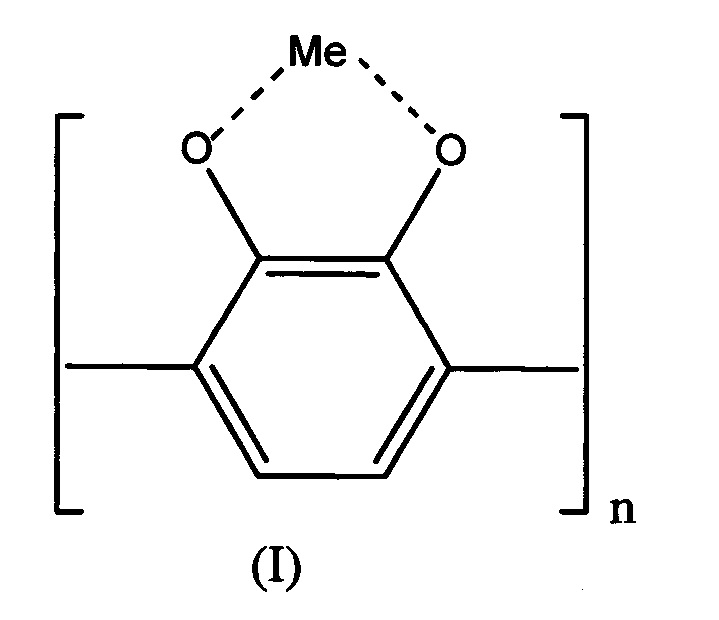
где Me - двухвалентный переходный металл, n=5÷15
Для синтеза вышеописанных соединений используется обменная реакция солей металлов: сульфата меди(II), нитрата кобальта(II), сульфата железа(II), сульфата марганца(II) и хлорида никеля(II) с олигокатехолатом натрия в водной среде.
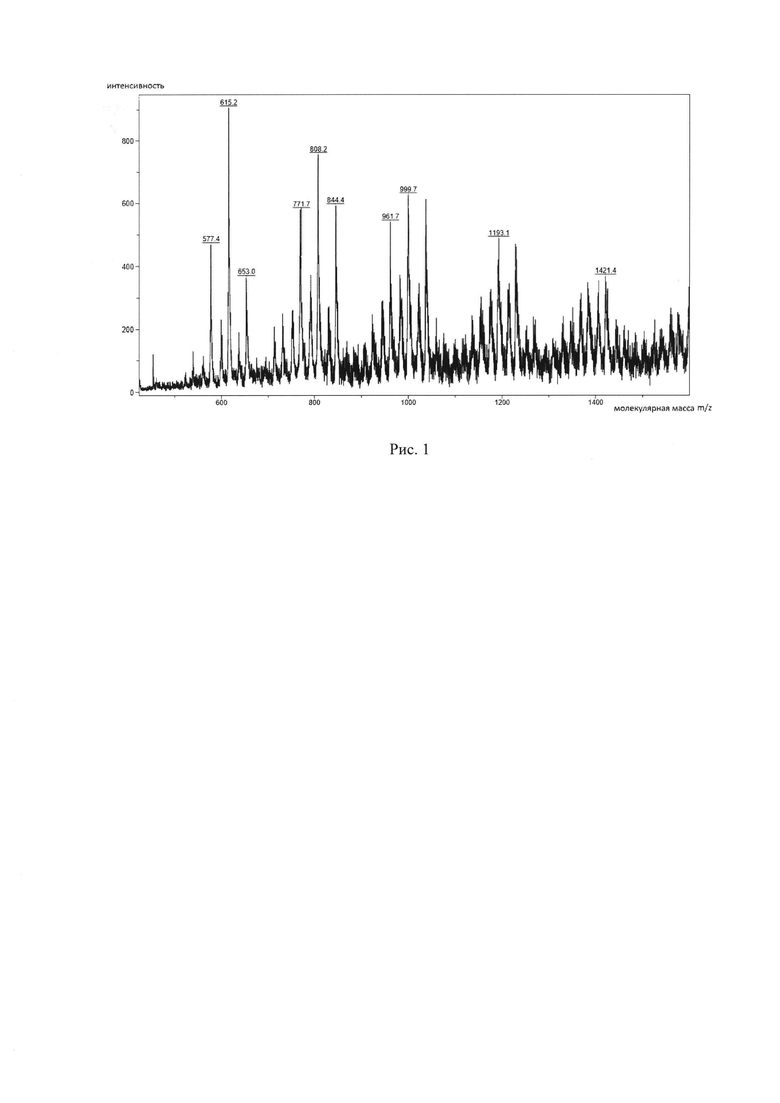
Олигопирокатехин (ОПК) синтезирован путем окислительной поликонденсации пирокатехина (ПКХ) в присутствии 3,3',5,5'-тетра-трет-бутил-4,4'-дифенохинона в водном растворе NaOH при 160°С по методу [6]. Молекулярная масса и количество звеньев в ОПК определены с использованием масс-спектрометрии MALDI TOF, на рис. 1 показано молекулярно-массовое распределение ОПК, которое варьируется от 577 до 1421, что соответствует количеству звеньев от 5 до 15.
Олигопирокатехолат натрия получен при растворении ОПК в водном растворе NaOH в мольном соотношении 1:1.
Пример 1.
Получение комплексов на основе олигопирокатехина и переходных металлов представляет собой двухстадийный процесс: первая стадия - синтез олигопирокатехолата натрия; вторая стадия - обменная реакция олигопирокатехолата натрия с хлоридами, нитратами и сульфатами металлов переменной валентности в водных растворах.
Для проведения первой реакции готовили водный раствор NaOH в цилиндрическом стаканчике объемом 200 мл: для этого 2,4 г (0,06 моль) NaOH квалификации ч.д.а. растворяли в 75 мл дистиллированной воды. Далее в полученный раствор добавляли ОПК массой 3,24 г (0,03 моль) и перемешивали на магнитной мешалке до его полного растворения с образованием при этом раствора черного цвета.
Концентрация исходных соединений для реакции между NaOH и ОПК выбрана в мольном соотношении 2:1, т.к. ОПК имеет две комлексообразующих гидроксильных группы.
Для проведения второй стадии синтеза готовили раствор кристаллогидрата CuSO4⋅5H2O: в реакторе растворяли 7,5 г (0,03 моль) CuSO4⋅5H2O в 75 мл дистиллированной воды. После полного растворения CuSO4 в воде, в реактор добавляли полученный на первой стадии синтеза черный раствор олигокатехолата натрия и реакционную смесь в течение 30 мин. перемешивали на магнитной мешалке. В ходе реакции образовался черный творожистый осадок олигопирокатехолата двухвалентной меди, который далее фильтровали и сушили.
Описанные реакции выражаются следующими химическими уравнениями:
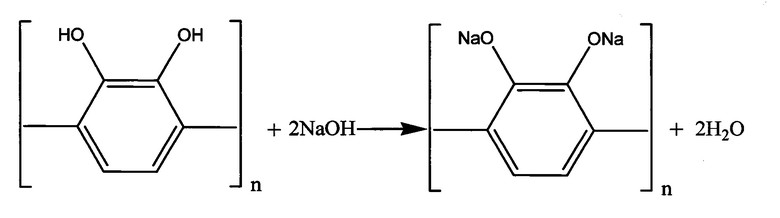
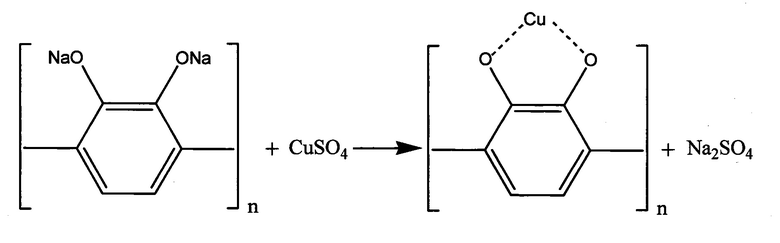
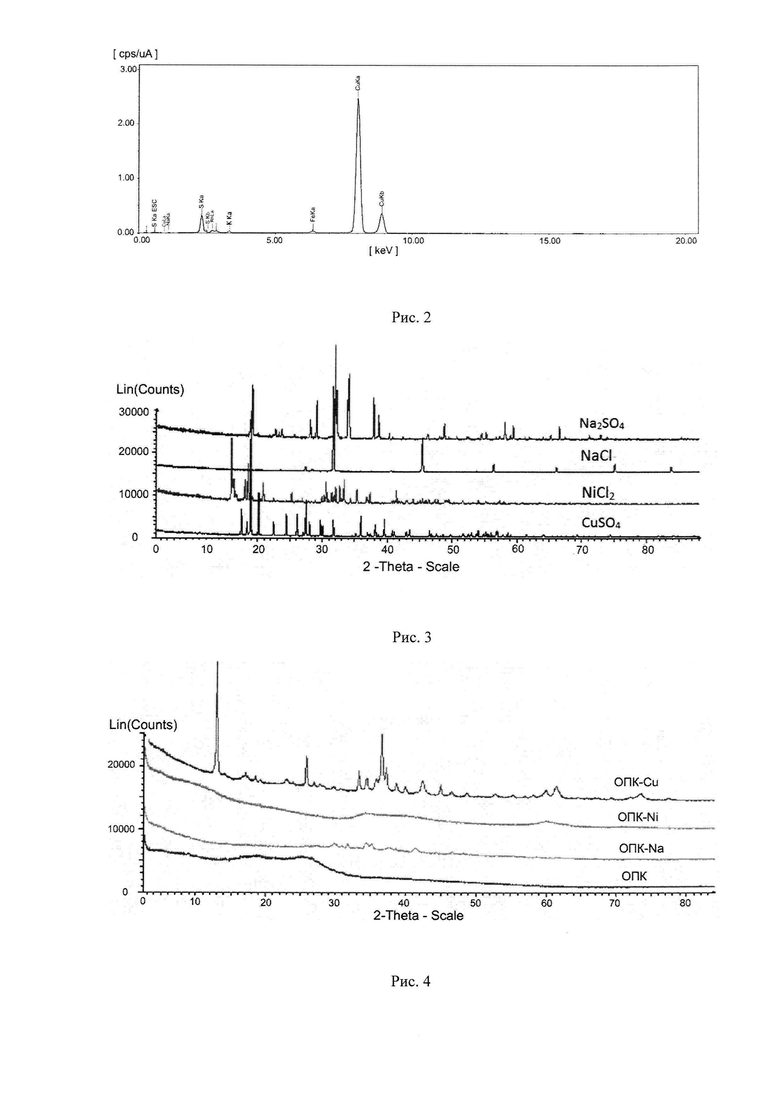
Данные рентгенофлуоресцентного анализа на содержание металла в образце, полученном по примеру 1, свидетельствуют о преимущественном замещении атомов натрия на атом меди (рис. 2). Количество меди в образце близко к 83% (остальные компоненты представлены преимущественно натрием (15%) и калием (2%).
Исследования всех последующих обменных реакций ОПК с солями других металлов (Со, Fe, Mn, Ni) проводились аналогично описанной методике, приведенной в примере 1.
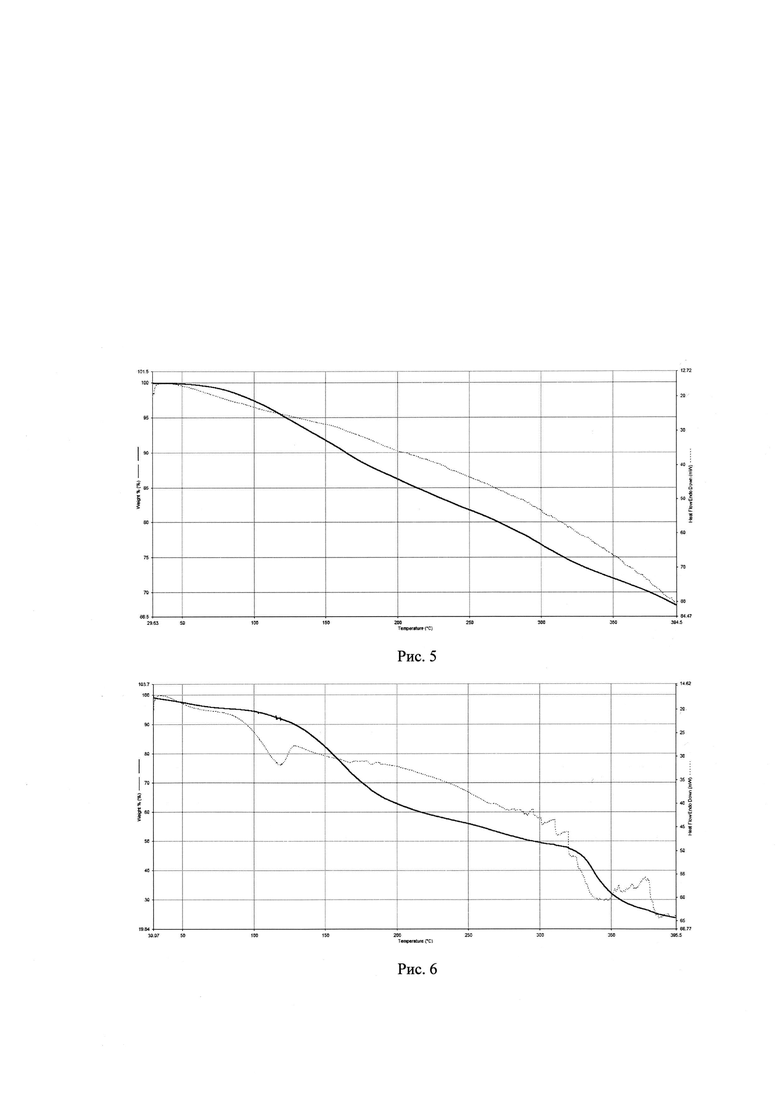
Рентгенодифракционный анализ образцов олигопирокатехина и его комплексов с натрием, никелем и медью был выполнен с использованием автоматического рентгеновского дифрактометра марки Bruker D8 Advance. Показано, что образец исходного олигопирокатехина является аморфным, его комплекс с никелем соответствует нанокристаллическому типу структурной организации вещества, а комплексы с натрием и медью характеризуются как частично кристаллические, причем комплекс олигопирокатехина с медью представляет собой в целом кристаллическую фазу с минимальной аморфной компонентой.
Сравнение полученных для олигомеров дифрактограмм с таковыми для исходных неорганических солей (рис. 3 и 4) свидетельствует об их отсутствии в полимерных образцах в индивидуальном виде (в виде механической примеси).
Дифрактограммы комплексов существенно отличаются и от таковой для индивидуального олигопирокатехина.
Таким образом, учитывая отсутствие в них исходных неорганических солей, полученные дифрактограммы можно считать доказательством образования гомогенных структур комплексных соединений на основе олигопирокатехина и соответствующих металлов с участием обоих компонентов.
Термогравиметрический анализ (ТГА) олигопирокатехолата меди представлен на рис. 5.
Все последующие синтезы с другими солями металлов (Примеры 2-5) проведены по аналогии с примером 1 в соответствии с вышеприведенными схемами реакций.
Пример 2
Синтез олигопирокатехолата кобальта проводили по примеру 1 с заменой кристаллогидрата CuSO4⋅5H2O на Со(NO3)2⋅6H2O массой 8,73 г (0,03 моль). ТГА анализ олигопирокатехолата кобальта представлен на рис. 6.
Пример 3
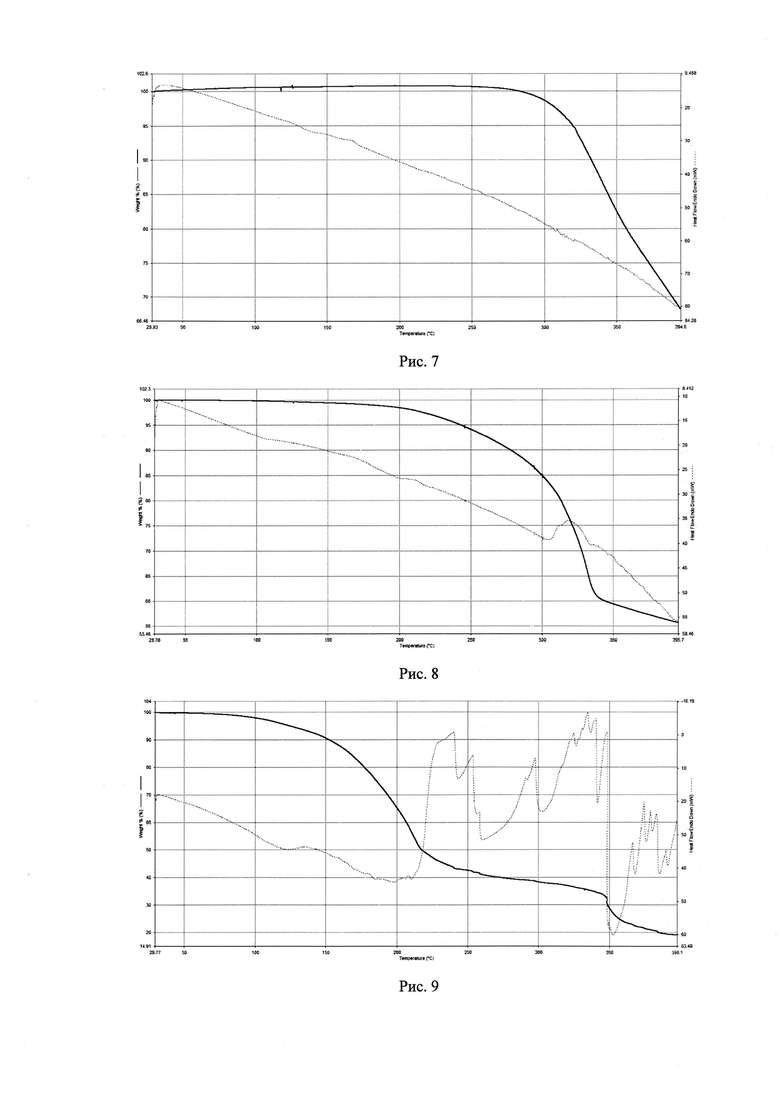
Синтез олигопирокатехолата железа вели по примеру 1 с заменой кристаллогидрата CuSO4⋅5H2O на FeSO4⋅7H2O массой 8,34 г (0,03 моль). ТГА анализ олигопирокатехолата железа представлен на рис. 7.
Пример 4
Синтез олигопирокатехолата марганца вели по примеру 1 с заменой кристаллогидрата CuSO4⋅5H2O на MnSO4⋅5H2O массой 7,23 г (0,03 моль). ТГА анализ олигопирокатехолата марганца представлен на рис. 8.
Пример 5
Синтез олигопирокатехолата никеля проводили по примеру 1 с заменой кристаллогидрата CuSO4⋅5H2O на NiCl2⋅6Н2О массой 7,14 г (0,03 моль). ТГА анализ олигопирокатехолата никеля представлен на рис. 9.
Преимуществами олигопирокатехалатов металлов являются: более высокая реакционная способность в виду наличия многих реакционно-способных центров, стабильность, нерастворимость в воде, что дает возможность их использования в водных средах в качестве каталитически активных компонентов гетерогенных катализаторов на полимерном носителе.
Приготовление гетерогенного катализатора на полимерной основе с использованием в качестве каталитически активных компонентов комплексных соединений на основе олигопирокатехина и переходных металлов (Cu, Со, Fe, Mn, Ni) демонстрируется примерами 6-10.
Для исследования влияния состава активных компонентов на эффективность катализатора в реакциях окисления меркаптидной и сульфидной серы могут быть использованы катализаторы на любом из полимерных носителей. В качестве такого носителя для испытаний был выбран ПЭНД, легче перерабатываемый в лабораторных условиях.
Пример 6.
Для приготовления испытуемого образца катализатора на основе олигопирокатехолата меди и ПЭНД рассчитанные количества порошкообразного комплексного соединения смешивают с полимером на обогреваемых лабораторных вальцах при температуре размягчения полимерного носителя (ПЭНД - при 140-160°С) до получения однородной катализаторной массы, из которой затем на прессе изготавливают пластину катализатора толщиной 1-2 мм. Полученную пластину нарезают на частицы размером 2-3 мм. Сокращенное название приготовленного катализатора 20% ОПК + Cu/ПЭНД.
Пример 7.
По примеру 6 с заменой олигопирокатехолата меди на олигопирокатехолат кобальта. Сокращенное название приготовленного катализатора 20% ОПК + Со/ПЭНД.
Пример 8.
По примеру 6 с заменой олигопирокатехолата меди на олигопирокатехолат железа. Сокращенное название приготовленного катализатора 20% ОПК + Fe/ПЭНД.
Пример 9.
По примеру 6 с заменой олигопирокатехолата меди на олигопирокатехолат марганца. Сокращенное название приготовленного катализатора 20% ОПК + Mn/ПЭНД.
Пример 10.
По примеру 6 с заменой олигопирокатехолата меди на олигопирокатехолат никеля. Сокращенное название приготовленного катализатора 20% ОПК + Ni/ПЭНД.
Пример 11.
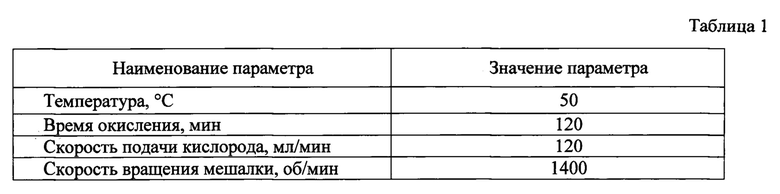
Условия проведения испытаний катализаторов в реакции окисления меркаптидной серы представлены в таблице 1. Масса катализатора 20% ОПК + Cu/ПЭНД - 5 г, объем 10%-ного раствора гидроксида натрия с пропилмеркаптидом натрия - 50 мл, исходная концентрация меркаптидной серы - 1,0 мас. %.
Пример 12.
По примеру 11 с заменой катализатора 20% ОПК + Cu/ПЭНД на 1% ОПК + Cu/ПЭНД.
Пример 13.
По примеру 11 с заменой катализатора 20% ОПК + Cu/ПЭНД на 20% ОПК + Ni/ПЭНД.
Пример 14.
По примеру 11 с заменой катализатора 20% ОПК + Cu/ПЭНД на 20% ОПК + Fe/ПЭНД.
Пример 15.
По примеру 11 с заменой катализатора 20% ОПК + Cu/ПЭНД на 20% ОПК + Со/ПЭНД.
Пример 16.
По примеру 11 с заменой катализатора 20% ОПК + Cu/ПЭНД на 20% ОПК + Mn/ПЭНД.
Для сравнения эффективности катализаторов были проведены испытания с известными в промышленности гетерогенными катализаторами КС-3 [7] - 20%-ый концентрат фталоцианина кобальта в ПЭНД - 20% РсСо/ПЭНД (пример 17) и КСМ-Х [8] на основе дихлорфталоцианина кобальта (ДХФцСо) состава: ДХФцСо - 10%, MnO2 - 5%, CuO - 5%, ПЭНД - 80% (пример 18).
Пример 17.
По примеру 11 с заменой катализатора 20% ОПК + Cu/ПЭНД на 20% РсСо/ПЭНД (КС-3)
Пример 18.
По примеру 11 с заменой катализатора 20% ОПК + Cu/ПЭНД на ДХФцСо - 10%, MnO2 - 5%, CuO - 5%, ПЭНД-80% (КСМ-Х)
Пример 19.
По примеру 11 без катализатора.
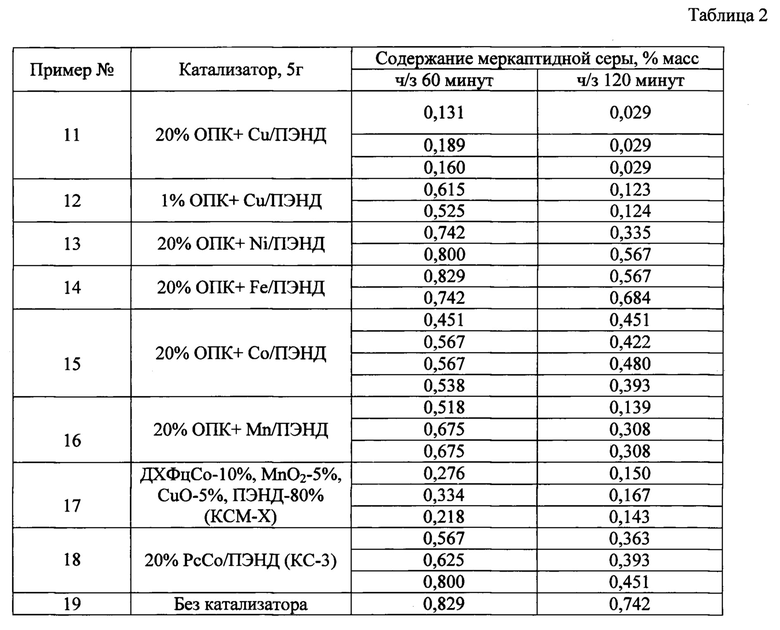
Об активности катализаторов судят по изменению остаточного содержания меркаптидной серы в щелочном растворе во времени потенциометрическим титрованием по ГОСТ 22985-90. Результаты испытаний по окислению меркаптидов в присутствии синтезированных катализаторов приведены в табл. 2. (примеры 11-19).
Из таблицы 2 видно, что катализатор 20% ОПК + Со/ПЭНД сравним с показателями для промышленного аналога КС-3, а катализатор 20% ОПК + Cu/ПЭНД превосходит по эффективности оба аналога: КС-3 и КСМ-Х. Эффективность использования синтезированных комплексных соединений на основе олигопирокатехина и переходных металлов (Cu, Со, Fe, Mn, Ni) в качестве катализатора окисления меркаптидов демонстрируется примерами 11-15.
Пример 20
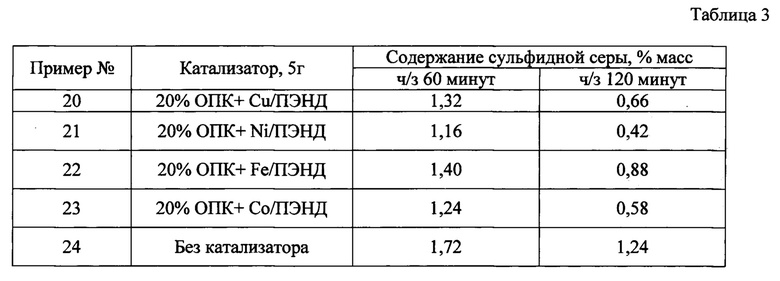
Условия проведения испытаний катализаторов в реакции окисления сульфида натрия представлены в таблице 1. Масса катализатора 20% ОПК + Cu/ПЭНД - 5 г, объем 2%-ного раствора гидроксида натрия с сульфидом натрия - 50 мл, исходная концентрация сульфидной серы - 2,0 мас. %.
Пример 21
По примеру 20 с заменой катализатора 20% ОПК + Cu/ПЭНД на 20% ОПК + Ni/ПЭНД.
Пример 22
По примеру 20 с заменой катализатора 20% ОПК + Cu/ПЭНД на 20% ОПК + Fe/ПЭНД.
Пример 23
По примеру 20 с заменой катализатора 20% ОПК + Cu/ПЭНД на 20% ОПК + Со/ПЭНД.
Пример 24
По примеру 20 без катализатора.
Об активности катализаторов судят по изменению остаточного содержания сульфидной серы в щелочном растворе во времени потенциометрическим титрованием по ГОСТ 22985-90. Результаты испытаний по окислению сульфида натрия в присутствии синтезированных катализаторов приведены в табл. 3. Эффективность использования синтезированных комплексных соединений на основе олигопирокатехина и переходных металлов (Cu, Со, Fe, Ni) в качестве катализатора окисления сульфида натрия демонстрируется примерами 20-23.
Источники информации
1. Б.А. Мамедов, А.И. Кокорин, А.В. Рагимов. Комплексообразование олигопирокатехина с ионами VO(II) в водных растворах // Высокомол. соед. Б. - 1991. - Т. 33. - №5. - С. 358-362.
2. Lado A.V.,  Piskunov A.V., Fukin G.K., Baranov E.V., Ikorskii V.N., Cherkasov V.K., Abakumov G.A. Oxidative addition of 3,6-di-tert-butyl-o-benzoquinoneand 4,6-di-tert-butyl-N(2,6-di-iso-propylphenyl)-o-iminobenzoquinone to SnCl2 // Inorg. Chim. Acta. - 2005. - V. 358. - N. 15. - P. 4443-4450.
Piskunov A.V., Fukin G.K., Baranov E.V., Ikorskii V.N., Cherkasov V.K., Abakumov G.A. Oxidative addition of 3,6-di-tert-butyl-o-benzoquinoneand 4,6-di-tert-butyl-N(2,6-di-iso-propylphenyl)-o-iminobenzoquinone to SnCl2 // Inorg. Chim. Acta. - 2005. - V. 358. - N. 15. - P. 4443-4450.
3. Piskunov A.V., Lado A.V., Fukin G.K., Baranov E.V., Abakumova L.G., Cherkasov V.K., Abakumov G.A. The reaction of 3,6-di-tert-butyl-o-benzoquinone with tin amalgam: synthesis and structure of tin catecholato complexes // Heteroatom Chem. - 2006. - V. 17. - N. 6. - P. 481-490.
4.  Antimony Complexes With o-Quinonato Ligands and Related 0,N-,0,N,0-,0,N,0,0-Ligands. Chapter 12 in book "Antimony: Characteristics, Compounds and Applications" (Eds. Manijeh Razeghi). // Nova Science Publishers. - 2012. - P. 267-302.
Antimony Complexes With o-Quinonato Ligands and Related 0,N-,0,N,0-,0,N,0,0-Ligands. Chapter 12 in book "Antimony: Characteristics, Compounds and Applications" (Eds. Manijeh Razeghi). // Nova Science Publishers. - 2012. - P. 267-302.
5. Piskunov А.У.,  The synthetic aspects in o-quinonato and o-iminoquinonato coordination chemistry of non-transition metals // Glob. J. Inorg. Chem. - 2011. - N. 2. - P. 110-149.
The synthetic aspects in o-quinonato and o-iminoquinonato coordination chemistry of non-transition metals // Glob. J. Inorg. Chem. - 2011. - N. 2. - P. 110-149.
6. Патент РФ 2552516.
7. AC 1041142.
8. Патент РФ 2529500.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР ДЛЯ ОКИСЛЕНИЯ СЕРНИСТЫХ СОЕДИНЕНИЙ | 2012 |
|
RU2529500C2 |
| СПОСОБ ДЕМЕРКАПТАНИЗАЦИИ УГЛЕВОДОРОДНОГО СЫРЬЯ | 2015 |
|
RU2603635C1 |
| СПОСОБ ОКИСЛЕНИЯ СУЛЬФИДА НАТРИЯ | 2020 |
|
RU2741546C1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ СУЛЬФИДНОЙ И/ИЛИ МЕРКАПТИДНОЙ СЕРЫ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2017 |
|
RU2659269C1 |
| СПОСОБ ОЧИСТКИ ВЫСОКОКИПЯЩИХ УГЛЕВОДОРОДНЫХ ФРАКЦИЙ ОТ МЕРКАПТАНОВ | 2019 |
|
RU2699020C1 |
| СПОСОБ РЕГЕНЕРАЦИИ АЛКАНОЛАМИНОВ ПРИ ОЧИСТКЕ УГЛЕВОДОРОДНЫХ ГАЗОВ ОТ СЕРОВОДОРОДА | 2018 |
|
RU2689572C1 |
| КАТАЛИЗАТОР ДЛЯ ЖИДКОФАЗНОГО ОКИСЛЕНИЯ СУЛЬФИДА НАТРИЯ | 2016 |
|
RU2644779C2 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ПОЛИХИНОНОВ И ЭТИЛЕНБИСФЕНОЛА | 2015 |
|
RU2647591C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИХИНОНОВ | 2014 |
|
RU2552516C1 |
| СПОСОБ РЕГЕНЕРАТИВНОЙ ОЧИСТКИ УГЛЕВОДОРОДНОГО СЫРЬЯ ОТ КИСЛЫХ ПРИМЕСЕЙ | 2018 |
|
RU2680522C1 |
Изобретение относится к новым химическим соединениям - олигопирокатехолатам металлов переменной валентности формулы (I),
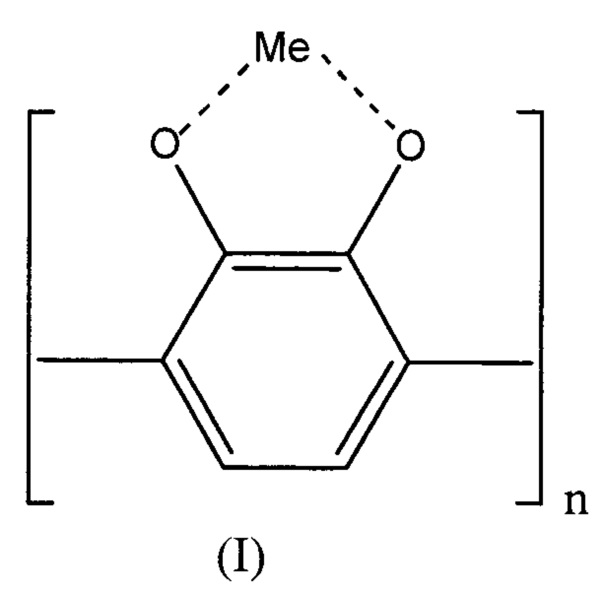
где Me - двухвалентный переходный металл в ряду Cu, Со, Fe, Mn, Ni, n=5÷15. Также предложен катализатор окисления сернистых соединений на полимерном носителе, содержащий олигопирокатехолат формулы (I). Предложенные новые соединения могут быть использованы в качестве эффективного катализатора окисления сернистых соединений. 2 н.п. ф-лы, 9 ил., 3 табл., 24 пр.
1. Новые химические соединения - олигопирокатехолаты металлов переменной валентности формулы (I),
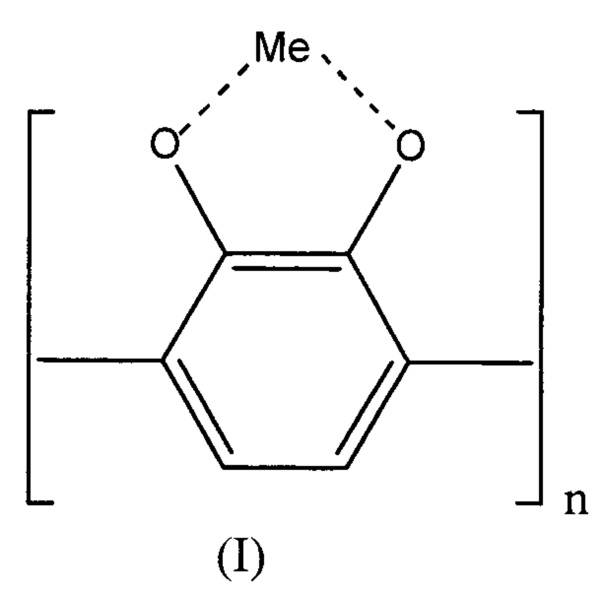
где Me - двухвалентный переходный металл в ряду Cu, Со, Fe, Mn, Ni, n=5÷15.
2. Катализатор окисления сернистых соединений на полимерном носителе из полиэтилена низкого давления (ПЭНД) или полипропилене, отличающийся тем, что в качестве водонерастворимого производного он содержит олигопирокатехолат металла переменной валентности по п. 1 в количестве, мас. %:
олигопирокатехолат по п. 1 - от 1,0 до 20,0;
ПЭНД или полипропилен - остальное.
| Мамедов Б.А | |||
| и др., Комплексообразование олигопирокатехина с ионами VO(II) в водных растворах, Высокомолекулярные соединения, 1991, т | |||
| Способ сопряжения брусьев в срубах | 1921 |
|
SU33A1 |
| Зажим для канатной тяги | 1919 |
|
SU358A1 |
| ZHIPING XU, Mechanics of metal-catecholate complexes: The roles of coordination state and metal types, Scientific Reports, 2013, v | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Пружинное репетирное ружье | 1924 |
|
SU2914A1 |
| КАТАЛИЗАТОР ДЛЯ ОКИСЛЕНИЯ СЕРНИСТЫХ СОЕДИНЕНИЙ | 2012 |
|
RU2529500C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИХИНОНОВ | 2014 |
|
RU2552516C1 |
| КАТАЛИЗАТОР ДЛЯ ОКИСЛЕНИЯ СЕРНИСТЫХ СОЕДИНЕНИЙ | 1996 |
|
RU2110324C1 |
Авторы
Даты
2019-01-16—Публикация
2017-11-22—Подача