Изобретение относится к области фармацевтики, а именно к новым физиологически активным веществам, новым частичным агонистам допаминовых D2/D3 рецепторов, активным компонентам для фармацевтических композиций, к фармацевтическим композициям и лекарственным средствам, содержащим метиламид 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты в качестве частичного агониста допаминовых D2/D3 рецепторов, который может применяться при лечении биполярного аффективного расстройства.
Биполярное расстройство - это психическое заболевание, характеризующееся частой сменой настроения, перепадами энергии, которые могут приводить к серьезным последствиям. Это хроническое заболевание влияет у взрослых людей на качество работы, у детей - на ухудшение учебы в школе, в крайних случаях, влечет за собой суицидальные наклонности. Биполярное аффективное расстройство присуще почти 1,5% населения.
Данное заболевание имеет два противоположных полюса нарушения эмоционального поведения, и патологические перепады настроения доходят до крайних пределов депрессивного или маниакального состояния, длясь иногда годами. Психическая нестабильность, резкая смена настроения - серьезные признаки биполярного расстройства. У больного происходит частая смена поведения: от симптомов мании, проявляющихся во взвинченности, эйфории, до тяжелой депрессии с явными признаками заторможенности. Между этими состояниями больной спокоен и здоров, ведет себя как человек с уравновешенной психикой. Мания может выражаться в чрезмерной возбужденности человека, переизбытком энергии, при которой он находится в эйфорическом состоянии, бездумно тратит деньги, решает «глобальные проблемы». У больного нарушается сон, замечается рассеянность, речь становится отрывистой, ускоренной, перебить его практически невозможно. Строгой очередности проявления этих фаз заболеваемости нет.
В основе данной патологии, как и в широком ряде других нейрологических и психических расстройств, отмечается изменение допаминергической функции, а сами допаминовые рецепторы являются мишенями для множества лекарственных препаратов. Поэтому главной проблемой в поиске препаратов для лечения биполярного расстройства, является не активность потенциального лекарства, а его специфичность.
Допаминовые рецепторы - класс трансмембранных метаботропных G-белок-связанных клеточных рецепторов, играющих важную роль в функционировании центральной нервной системы позвоночных. Основной эндогенный лиганд-агонист этих рецепторов - допамин. Допаминовые рецепторы участвуют в процессах мотивации, обучения, тонкой моторной координации, модулирования нейроэндокринных сигналов. Этот класс включает пять типов рецепторов: D1, D2, D3, D4 и D5. По структурным, биохимическим и фармакологическим характеристикам все эти рецепторы подразделяют на D1-подобные (D1, D5) и D2-подобные (D2, D3, D4).
К D2-подобным рецепторам относятся рецепторы D2, D3 и D4. Эти рецепторы связываются с G-белками семейства Gαi/o и поэтому ингибируют аденилатциклазу. В отличие от D1-подобных, рецепторы D2 и D3 присутствуют не только на постсинаптических мембранах клеток, чувствительных к допамину, но и на пресинаптических мембранах допаминергических нейронов, поэтому именно D2-подобные рецепторы являются на данный момент «мишенью выбора» для терапии биполярных расстройств.
Важным свойством, крайне желательным для терапевтических агентов биполярных расстройств, является их ЧАСТИЧНОЕ связывание с рецепторами - способность стабилизировать дофаминовую систему. Понятие «частичный агонист» подчеркивает, что эффект препарата зависит от первоначального состояния функциональной активности сети дофамина - такой препарат усиливает активность дофамина в тех областях мозга, где она снижена (мезокортикальные структуры), и понижает активность дофамина в тех структурах мозга, где она, напротив, усилена (мезолимбические структуры). В первом случае клинический эффект проявляется редукцией негативной, во втором - купированием позитивной симптоматики.
Среди агонистов/частичных агонистов допаминовых D2/D3 рецепторов известны различные классы соединений. В том числе, препараты из бензотиофендиазепинового ряда (Otsuka Pharmaceutical Co., Ltd. (JP)), 1,8-нафтиридиноны, разработанные Pfizer (US), а также арилпиперазины - Брекспипразол и Арипипразол (оба - Otsuka Pharmaceutical Co., Ltd. (JP)) и Карипразин (Gedeon Richter (HU)).
Именно последний препарат можно рассматривать в качестве ближайшего уровня техники (прототипа) представленного изобретения.
Было неожиданно обнаружено, что метиламид 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты - соединение формулы 1
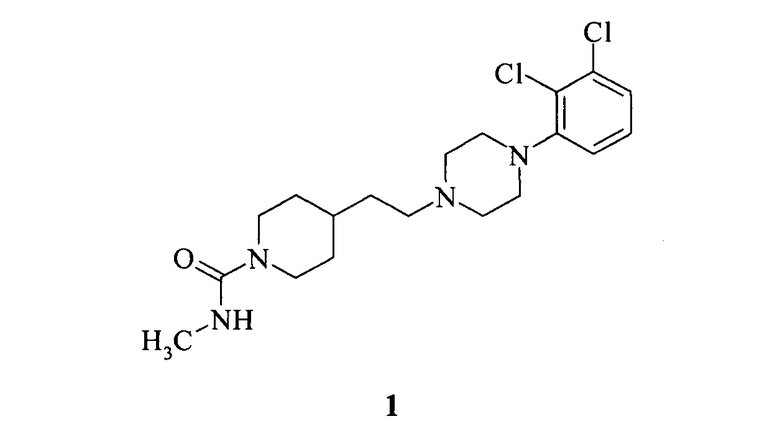
- является эффективным частичным агонистом допаминовых D2/D3 рецепторов и может быть использовано для разработки лекарственных средств для лечения биполярного расстройства.
Для заявленного соединения формулы 1 неожиданно наблюдали одинаковое его связывание соединения с D2S и D3 рецепторами, вовлеченными в механизм развития биполярного расстройства, в то время как для Карипразина, который можно рассматривать в качестве ближайшего аналога к заявленному соединению, связывание с D2S и D3 рецепторами отличается на два порядка. Это позволяет предположить более высокую активность соединения формулы 1 по сравнению с Карипразином.
Более того, получение соединения формулы 1 является более простым для специалиста, чем получение сравнимого соединения Карипразина, формула которого содержит сразу два центра асимметрии. Специалисту очевидна простота и доступность, а также дешевизна соединения формулы 1 по сравнению с его аналогом - Карипразином, при этом биологическая активность соединения формулы 1 не только не уступает известному аналогу, но и превосходит ее.
Ниже приведены определения терминов, которые использованы в описании этого изобретения.
«Агонисты» означают соединения, которые, связываясь с рецепторами определенного типа, активно способствуют передаче этими рецепторами свойственного им специфического сигнала и тем самым вызывают биологический ответ клетки.
«Активный компонент» (лекарственное вещество, лекарственная субстанция, drug-substance) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Действующее вещество» (лекарственное вещество, лекарственная субстанция, drug-substance) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного средства.
«Лекарственное комбинированное средство (препарат)» - комбинация нескольких лекарственных веществ для одновременного использования в виде таблеток, капсул, инъекций, мазей, ректальных суспензий и гелей и др. готовых форм, предназначенный для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего. Лекарственные вещества в одном комплекте могут быть представлены в виде различных готовых форм, предназначенных для введения в организм животного или человека различными способами, например перорально и ректально.
«Нейродегенеративное заболевание» означает специфическое состояние и заболевание, характеризующиеся повреждением и первичной гибелью популяций нервных клеток в определенных областях центральной нервной системы. Нейродегенеративные заболевания включают, но не ограничивают, болезни Альцгеймера и Паркинсона; болезнь (хорею) Хантингтона; рассеянный склероз; мозжечковую дегенерацию; амиотрофический латеральный склероз; деменцию с тельцами Леви; спинальную мускульную атрофию; периферическую нейропатию; губчатый энцефалит («коровье бешенство», Creutzfeld-Jakob Disease); СПИД-ассоциированную деменцию; мультиинфарктную деменцию; лобно-височную деменцию; лейкоэнцефалопатию (болезнь исчезающей белого вещества); хронические нейродегенеративные заболевания; инсульт; ишемическое, реперфузионное и гипоксическое повреждение мозга; эпилепсия; церебральная ишемия; глаукома; черепно-мозговая травма; синдром Дауна; энцефаломиелит; менингит; энцефалит; нейробластома; шизофрения; биполярное расстройство; депрессия. Кроме того, нейродегенеративные заболевания включают патологические состояния и расстройства, развивающиеся при гипоксии, злоупотреблении веществами, вызывающими зависимость, при воздействии нейротоксинов, инфекционных и онкологических заболеваниях головного мозга, а также нейрональные повреждения, ассоциированные с аутоиммунными и эндокринными заболеваниями; и прочие нейродегенеративные процессы.
«Рецепторы» (от латинского recipere - получать, узнавать) представляют собой биологические макромолекулы, расположенные на цитоплазматической мембране клетки или внутриклеточно, способные специфически взаимодействовать с ограниченным набором физиологически активных веществ (лигандов) и трансформировать сигнал об этом взаимодействии в определенный клеточный ответ.
«Сигнальный каскад» (сигнальная система, каскад передачи сигнала) означает совокупность взаимосвязанных последовательных и параллельных молекулярных процессов регуляции клеточного метаболизма внешними (первичными) сигналами, несущими в клетку информацию, что принципиально отличает их от других поступающих в клетку химических соединений, служащих для нее источником материи и энергии. Молекулярные механизмы передачи (трансдукции) внешних сигналов в клетку подразумевают не только передачу сигналов как таковую, но и весь комплекс событий, с ней сопряженных, в том числе усиление, ослабление и подавление (или выключение) сигналов.
«Фармацевтическая композиция» обозначает композицию, включающую в себя соединение общей формулы 1 и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых добавок, которые выбирают из группы состоящей из наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как, консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как, парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, алгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения. Фармацевтические композиции, как правило, получают с помощью стандартных процедур, предусматривающих смешение активного соединения с жидким или тонко измельченным твердым носителем. Для изготовления суппозиториев помимо активных компонентов используют также масло какао, сплавы его с парафином и гидрогенизированными жирами, растительные и животные гидрогенизированные жиры, твердый жир, ланоль, сплавы гидрогенизированных жиров с воском, твердым парафином и другие основы, разрешенные для медицинского применения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или приготовлены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные. (Подробное описание свойств таких солей дано в Berge S.M., et al., "Pharmaceutical Salts" J. Pharm. Sci. 1977, 66: 1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как, холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты - лизин, орнитин и аргинин.
«Фармацевтически приемлемые добавки» под фармацевтически приемлемыми добавками подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители.
«Частичный агонист» означает вещество, которое способно активировать рецептор, но с меньшим максимально возможным эффектом, чем природный агонист рецептора. Хотя они и являются агонистами, их фармакологический профиль, фактически, соответствует такому конкурентных антагонистов в присутствии полного агониста. В фармакологии используются для активации некоторого нужного процесса, но с предупреждением слишком активно его течения. Применение частичных агонистов в клинической практике способно предотвращать развитие адаптивных регуляторных механизмов ("привыкание") при его хроническом использовании.
Цель настоящего изобретения заключается в создании новых частичных агонистов допаминовых D2/D3 рецепторов как потенциальных препаратов для лечения биполярного расстройства.
Поставленная цель достигается метиламидом 4-{2-[4-(2,3-Дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты формулы 1.
Предметом настоящего изобретения является метиламид 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты формулы 1
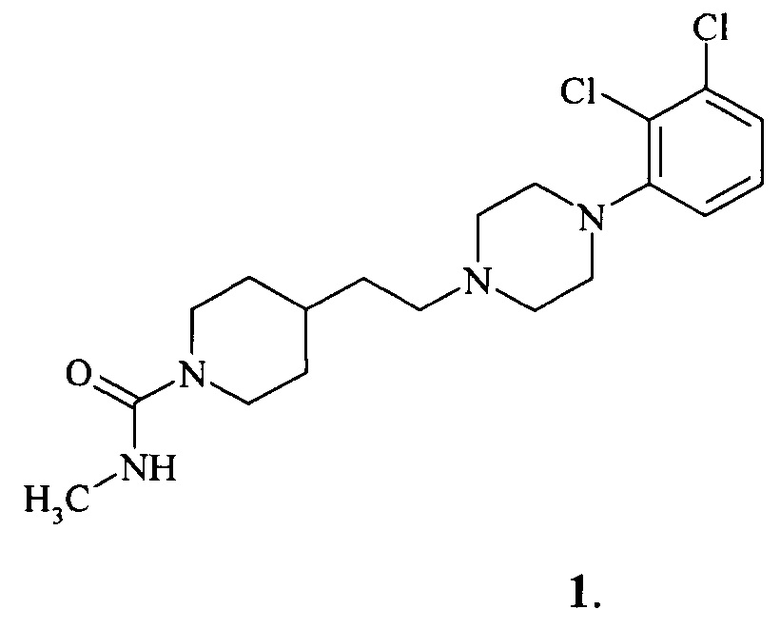
Соединение формулы 1 проявляет свойства частичного агониста допаминовых D2/D3 рецепторов.
Предметом данного изобретения также является способ получения метиламида 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты формулы 1 исходя из трет-бутил-4-(2-гидроксиэтил)пиперидин-1-карбоксилата 2 и гидрохлорида 1-(2,3-дихлорфенил)пиперазина 3 (схема 1). Первичный спирт 2 активируется превращением в эфир сульфокислоты 4, полученный алкилирующий агент 4 при кипячении в ацетонитриле реагирует с моно-арилзамещенным пиперазином 3. С образовавшегося в результате каплинга вос-эфира 5 удаляется защитная группа в кислых условиях с образованием замещенного пиперидина 6, и при охлаждении последнего до 0°С в ацетонитриле под воздействием N-метилкарбамоилхлорида в присутствии триэтиламина образуется структура 1.
Схема 1
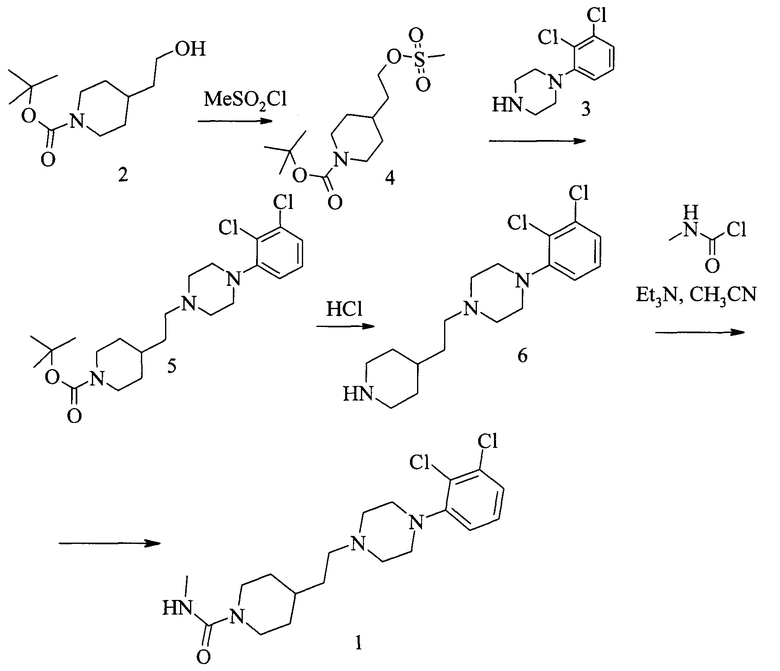
Более конкретно заявленный способ получения соединения формулы 1, включает следующие стадии:
A) взаимодействие трет-бутил-4-(2-гидроксиэтил)пиперидин-1-карбоксилата формулы 2 с метансульфонилхлоридом с образованием трет-бутил-4-[{(2-метилсульфонил)окси}этил]пиперидин-1-карбоксилата формулы 4;
B) взаимодействие полученного на стадии (А) эфира сульфокислоты формулы 4 с гидрохлоридом 1-(2,3-дихлорфенил)пиперазина с образованием трет-бутил-4-{2-[4-(2,3-дихлорфенил)пиперазин-1-ил]этил}пиперидин-1-карбоксилата формулы 5;
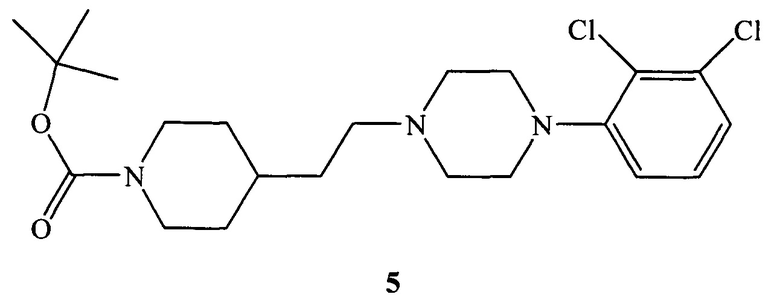
С) кипячение эфира формулы 5 в растворе соляной кислоты с получением 1-(2,3-дихлорфенил)-4-(2-пиперидин-4-илэтил)пиперазина формулы 6;
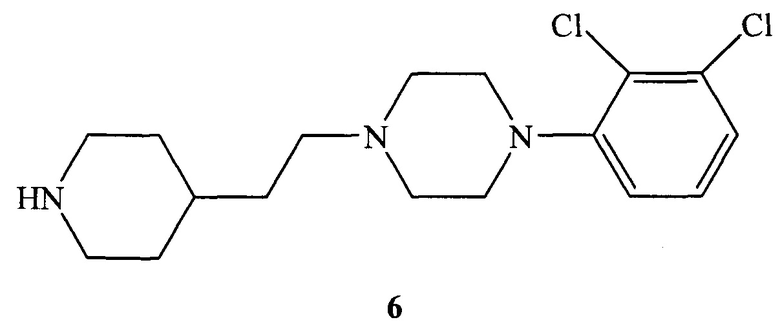
F) обработку замещенного пиперидина формулы 6 с помощью N-метилкарбамоилхлорида с получением соединения формулы 1.
Предпочтительный вариант способа получения предусматривает следующие этапы:
а) к смеси трет-бутил-4-(2-гидроксиэтил) пиперидин-1-карбоксилата и триэтиламина в хлористом метилене прибавляют при охлаждении метансульфонилхлорид, реакционную смесь промывают водой и концентрируют с образованием трет-бутил-4-[{(2-метилсульфонил)окси}этил]пиперидин-1-карбоксилата;
б) трет-бутил 4-{2-[(метилсульфонил)окси]этил}пиперидин-1-карбоксилат, гидрохлорид 1-(2,3-дихлорфенил)пиперазина и карбонат калия кипятят в ацетонитриле, выпавший по окончании реакции осадок отфильтровывают, промывают и высушивают с образованием трет-бутил-4-{2-[4-(2,3-дихлорфенил)пиперазин-1-ил]этил}пиперидин-1-карбоксилата в виде бежевых кристаллов;
в) трет-бутил-4-{2-[4-(2,3-дихлорфенил)пиперазин-1-ил]этил}пиперидин-1-карбоксилат растворют в водно-метанольном растворе соляной кислоты при кипении, по окончании реакции метанол отгоняют, а остаток при охлаждении льдом подщелачивают до рН=10. После длительного перемешивания отделяют осадок 1-(2,3-дихлорфенил)-4-(2-пиперидин-4-илэтил)пиперазина в виде бежевого порошка;
г) 1-(2,3-дихлорфенил)-4-(2-пиперидин-4-илэтил)пиперазин растворяют в ацетонитриле и в присутствии триэтиламина при охлаждении и перемешивании обрабатывают N-метилкарбамоилхлоридом, при этом выпавший осадок отфильтровывают, промывают, сушат, растворяют в этаноле и пропускают через слой целлита. Объединенные этанольные фильтраты слегка упаривают и наблюдают кристаллизацию продукта 4-{2-[4-(2,3-дихлорфенил)пиперазин-1-ил]этил}-N-метилпиперидин-1-карбоксамида в виде белого порошка, который отфильтровывают и сушат.
Конкретные режимы/условия осуществления способа получения могут быть подобраны специалистом экспериментальным путем.
Предметом настоящего изобретения является активный компонент, обладающий свойством частичного агониста допаминовых D2/D3 рецепторов, представляющий собой метиламид 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты формулы 1 в терапевтически эффективном количестве.
Предметом данного изобретения является фармацевтическая композиция, предназначенная для лечения биполярного расстройства, содержащая в эффективном количестве активный компонент, обладающий свойством частичного агониста допаминовых D2/D3 рецепторов.
Фармацевтическая композиция может быть выполнена в форме таблеток, капсул и инъекций, помещенных в фармацевтически приемлемую упаковку.
Фармацевтическая композиция может включать фармацевтически приемлемые добавки. Под фармацевтически приемлемыми добавками подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтически приемлемые добавки выбирают предпочтительно из крахмала картофельного и лактозы моногидрата. Крахмал картофельный может содержаться в количестве 30,5-32 мг, а лактозы моногидрат - в количестве около 67 мг.
Предпочтительно фармацевтическая композиция, для лечения биполярного расстройства содержит:
- от 1 до 2,5 вес. % соединения формулы 1,
- от 31 до 31,5 вес. % крахмала картофельного и
- от 66 до 68 вес. % лактозы моногидрата.
Фармацевтическая композиция наряду с активным компонентом по настоящему изобретению может включать и другие активные ингредиенты, при условии, что они не вызывают нежелательных эффектов, например, аллергических реакций.
При необходимости использования фармацевтических композиций по настоящему изобретению в клинической практике они могут смешиваться для изготовления различных форм, при этом они могут включать в свой состав традиционные фармацевтические носители; например, пероральные формы (такие как, таблетки, желатиновые капсулы, пилюли, растворы или суспензии); формы для инъекций (такие как, растворы или суспензии для инъекций, или сухой порошок для инъекций, который требует лишь добавления воды для инъекций перед использованием); местные формы (такие как, мази или растворы).
Носители, используемые в фармацевтических композициях по настоящему изобретению, представляют собой носители, которые применяются в сфере фармацевтики для получения распространенных форм, в том числе: в пероральных формах используются связующие вещества, смазывающие агенты, дезинтеграторы, растворители, разбавители, стабилизаторы, суспендирующие агенты, бесцветные агенты, корригенты вкуса; в формах для инъекций используются антисептические агенты, солюбилизаторы, стабилизаторы; в местных формах используются основы, разбавители, смазывающие агенты, антисептические агенты.
Новая фармацевтическая композиции может быть получена смешением с инертным наполнителем и/или растворителем активного компонента, представляющего собой,, соединение формулы 1.
Предметом данного изобретения является лекарственное средство, содержащее метиламид 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты формулы 1 в качестве активного компонента.
Лекарственные средства могут вводиться перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно, местно или ректально). Клиническая дозировка активного компонента (субстанции), фармацевтической композиции или лекарственного комбинированного средства, включающих фармацевтически эффективное количество активного компонента, у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента. Суточная доза активного компонента у взрослых обычно составляет 1-30 мг, предпочтительно 1-2,5 мг. Поэтому во время приготовления фармацевтических композиций по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 1-2,5 мг, предпочтительно - 1 мг активного компонента. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно - от одного до шести раз).
Предметом данного изобретения является способ лечения биполярного расстройства и связанных с ней нейродегенеративных заболеваний путем введения в эффективном количестве активного компонента, представляющего собой соединение формулы 1 или фармацевтической композиции, содержащей соединение формулы 1 в качестве активного компонента.
Предметом данного изобретения является применение соединения формулы 1 для получения лекарственного средства для лечения биполярного расстройства или для лечения других нейро-дегенеративных заболеваний.
Также заявленное изобретение относится к соединению формулы 1 для применения в способе лечения биполярного расстройства и/или других нейродегенеративных заболеваний.
Изобретение иллюстрируется следующими чертежами:
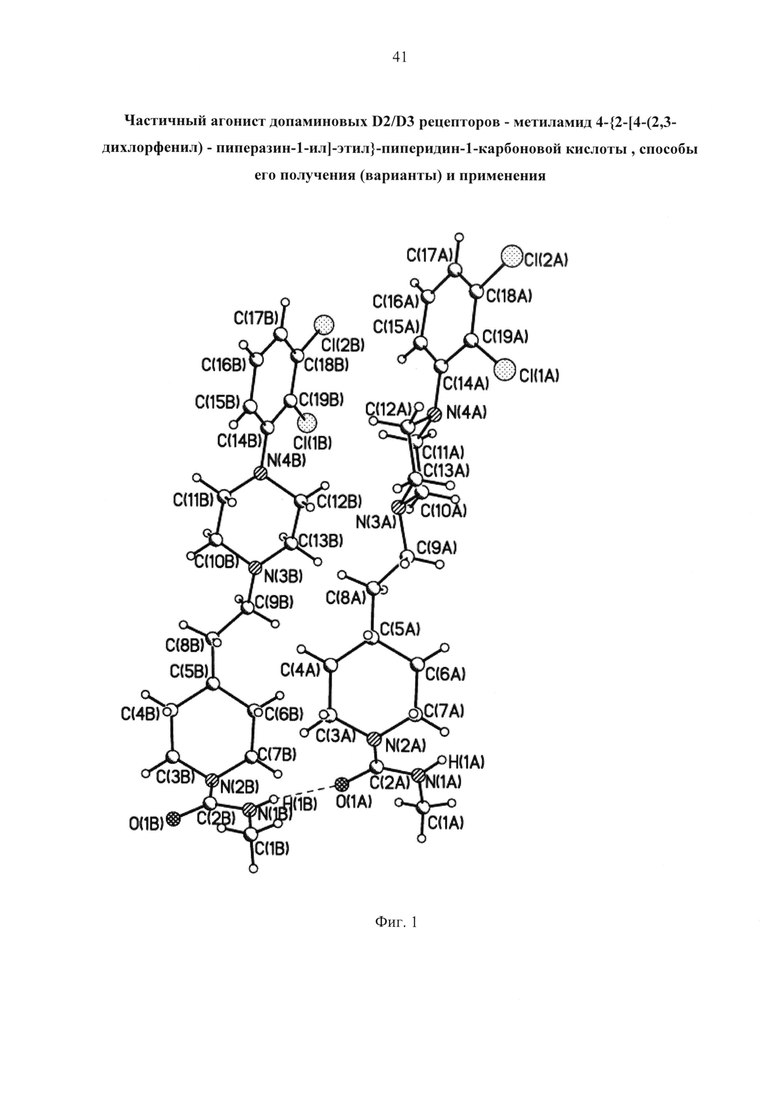
Фиг. 1. Система водородных связей в соединении формулы 1.
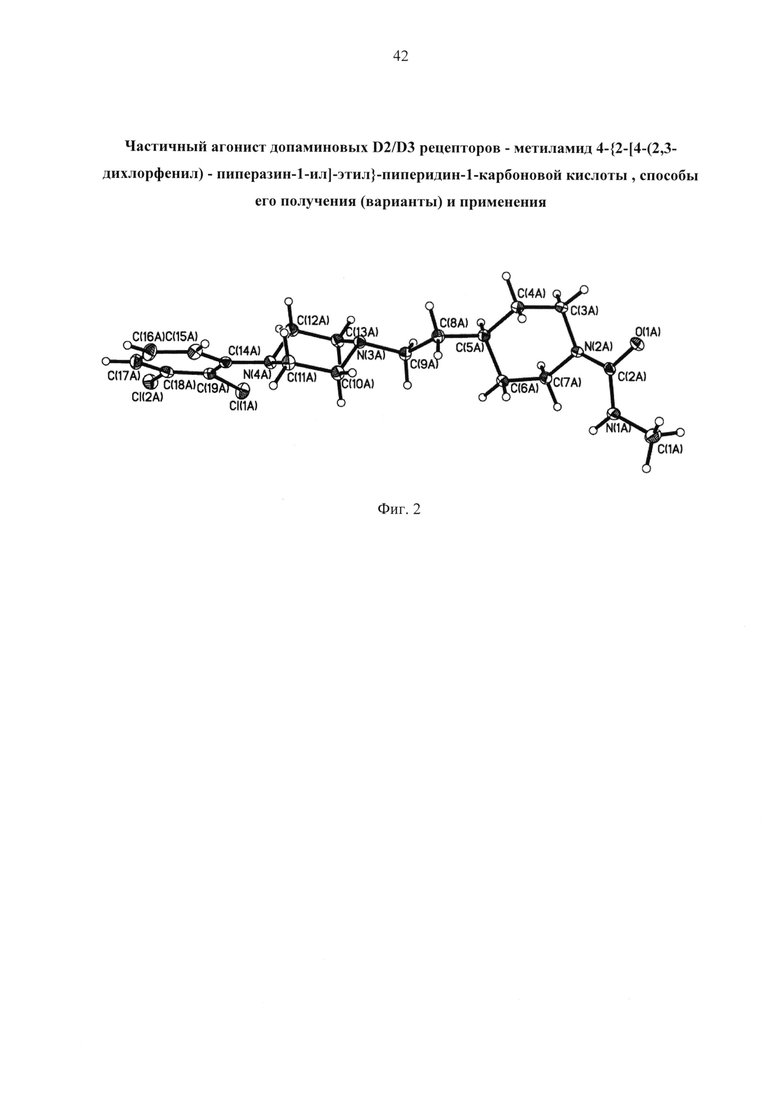
Фиг. 2. Общий вид молекулы соединения формулы 1 (элипсоиды тепловых колебаний приведены с вероятностью 50%). Представленные ниже примеры иллюстрируют, но не ограничивают изобретение.
Структуры полученных соединений подтверждались данными химического, хроматографического, рентгено-структурного и спектрального анализа.
Пример 1. Получение трет-бутил-4-[{(2-метилсульфонил)окси}этил]пиперидин-1-карбоксилата (4).
К смеси трет-бутил-4-(2-гидроксиэтил)пиперидин-1-карбоксилата (0.50 г, 2.18 ммоль) и триэтиламина (0.23 г, 2.29 ммоль) в хлористом метилене (100 мл), охлажденной до -10°С прибавляют по каплям метансульфонилхлорид (0.26 г, 2.29 ммоль), скорость прибавления должна быть такой, чтобы температура реакционной смеси не превышала -10°С. По окончании прибавления смесь перемешивают при комнатной температуре 1 час. Окончание прохождения реакции контролируют с помощью тонкослойной хроматографии (силикагель, гексан/этилацетат 2/1). Реакционную смесь промывают водой, органический слой сушат над сульфатом натрия (безводным). Растворитель упаривают в вакууме, остаток представляет собой технический трет-бутил-4-[{(2-метилсульфонил)окси}этил]пиперидин-1-карбоксилат. Выход составляет 92% (0.58 г).
Спектр ЯМР 1Н (400 МГц, ДСМО-д6, δ, м.д., J/Гц): 4,24 (т, 2Н, J=6,5 Гц), 3,90 (д, 2Н, J=12.0 Гц), 2,94 (с, 3Н), 2,78-2,61 (м, 2Н), 1.70-1.52 (м, 5Н), 1.38 (с, 9Н), 1.09-0.94 (м, 2Н).
ВЭЖХ-МС, [М+Н] 288.2.
Пример 2 Получение трет-бутил-4-{2-[4-(2,3-дихлорфенил)пиперазин-1-ил]этил}пиперидин-1-карбоксилата (5).
Смесь трет-бутил 4-{2-[(метилсульфонил)окси]этил}пиперидин-1-карбоксилата (0.50 г, 1.74 ммоль), гидрохлорида 1-(2,3-дихлорфенил)пиперазина (0.46 г, 1.74 ммоль) и карбоната калия (0.50 г, 3.62 ммоль) в ацетонитриле (250 мл) перемешивают при кипячении (81.6°С) в течение 72 часов. Полноту прохождения реакции контролируют методом ВЭЖХ. Реакционную смесь охлаждают, выпавший осадок отфильтровывают, промывают на фильтре последовательно водой, затем диэтиловым эфиром и сушат 6 ч при 100°С. Получают 0.50 г трет-бутил-4-{2-[4-(2,3-дихлорфенил)пиперазин-1-ил]этил}пиперидин-1-карбоксилата в виде бежевого кристаллического вещества, выход 65%.
Спектр ЯМР 1Н (400 МГц, ДМСО-д6, δ, м.д., J/Гц): 7.34-7.26 (м, 2Н), 7.14 (дд, 1Н, J1=2.6 Гц, J2=6.7 Гц), 3.92 (д, 2Н, J=12.5 Гц), 3.04-2.92 (м, 4Н), 2.78-2.61 (м, 2Н), 2.57-2.51 (м, 4Н), 2.37 (т, 2Н, J=7.0 Гц), 1.64 (д, 2Н, J=12.1 Гц), 1.53-1.41 (м, 3Н), 1.39 (с, 9Н), 1.07-0.92 (м, 2Н).
ВЭЖХ-МС, [М+Н] 443,4.
Пример 3. Получение 1-(2,3-дихлорфенил)-4-(2-пиперидин-4-ил)этил пиперазина (6).
К смеси метанола (10 мл), воды (10 мл) и концентрированной соляной кислоты (10 мл) прибавляют небольшими порциями трет-бутил-4-{2-[4-(2,3-дихлорфенил)пиперазин-1-ил]этил}пиперидин-1-карбоксилат (0.50 г, 1.13 ммоль). Затем реакционную смесь перемешивают при кипячении в течение 0.5 часов. Степень прохождения реакции контролируют методом ВЭЖХ. После окончания реакции метанол отгоняют при пониженном давлении, к остатку добавляют 10 г льда, затем подщелачивают 3М NaOH (16 мл) до рН=10. Продукт выпадает в виде светло-коричневого масла, которое через 15 мин начинает кристаллизоваться. Перемешивание продолжают 4 ч, осадок фильтруют, сушат на фильтре 12 ч. Получают 0.38 г (95%) 1-(2,3-дихлорфенил)-4-(2-пиперидин-4-илэтил)пиперазина в виде бежевого порошка.
Спектр ЯМР 1Н (400 МГц, ДМСО-д6, δ, м.д., J/Гц): 7.37-7.24 (м, 2Н), 7.21-7.08 (м, 1Н), 3.06-2.81 (м, 8Н), 2.45-2.28 (м, 6Н), 1.65-1.51 (м, 2Н), 1.44-1.27 (м, 3Н), 1.09-0.91 (м, 2Н).
ВЭЖХ-МС, [М+Н] 343,3.
Пример 4. Получение 4-(2-[4-(2,3-дихлорфенил)пиперазин-1-ил]этил-N-метилпиперидин-1-карбоксамида (1).
К смеси 1-(2,3-дихлорфенил)-4-(2-пиперидин-4-илэтил)пиперазина (0.38 г, 1.12 ммоль) и триэтиламина (0.12 г, 1.23 ммоль) в ацетонитриле (10 мл), охлажденной до 0°С, при перемешивании прибавляют по каплям N-метилкарбамоилхлорид (0.12 г, 1.23 ммоль) в ацетонитриле (5 мл), после чего реакционную смесь перемешивают при комнатной температуре 2 часа. Выпавший осадок отфильтровывают, промывают последовательно водой (20 мл), гексаном (20 мл), сушат на фильтре 1 час. Полученный осадок растворяют в 10 мл этанола и пропускают через слой целита (1 см), целит промывают 5 мл этанола. Объединенные этанольные фильтраты упаривают при пониженном давлении до объема 50 мл. Через 5 мин начинает кристаллизоваться продукт. Перемешивание продолжают еще 1 ч, выпавший осадок фильтруют, сушат при 70°С 24 часа. Получают 0.24 г (53%) 4-{2-[4-(2,3-дихлорфенил)пиперазин-1-ил]этил}-N-метилпиперидин-1-карбоксамида в виде белого порошка.
Спектр ЯМР 1Н (400 МГц, ДМСО-д6, δ, м.д., J/Гц): 7.33-7.27 (м, 2Н), 7.14 (дд, 1Н, J1=3.1 Гц, J2=6.7 Гц), 6.30 (дд, 1Н, J1=4.5 Гц, J2=8.8 Гц), 3.89 (д, 2Н, J=13.0 Гц), 3.01-2.94 (м, 4Н), 2.65-2.56 (м, 6Н), 2.54 (д, 3Н, J=4.3 Гц), 2.36 (т, 2Н, J=7.2 Гц), 1.62 (д, 2Н, J=11.9 Гц), 1.50-1.34 (м, 3Н), 1.05-0.92 (м, 2Н).
ВЭЖХ-МС, [М+Н] 399,2/403,4.
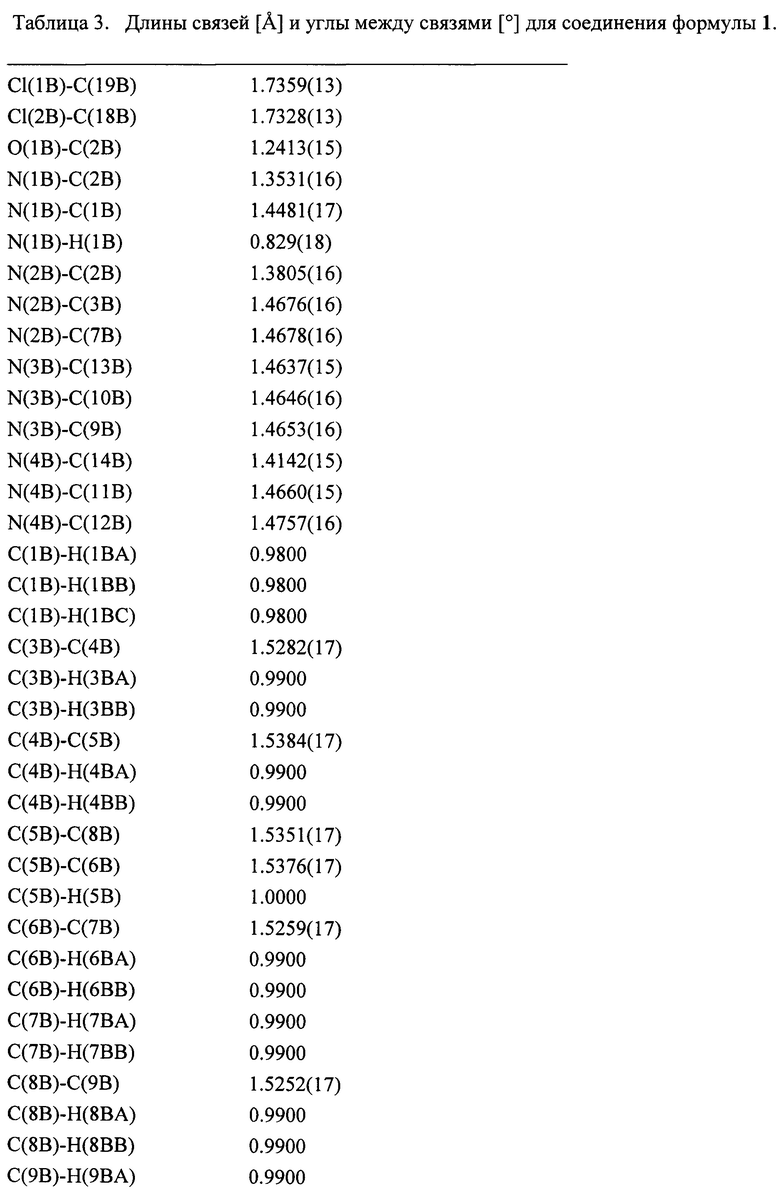
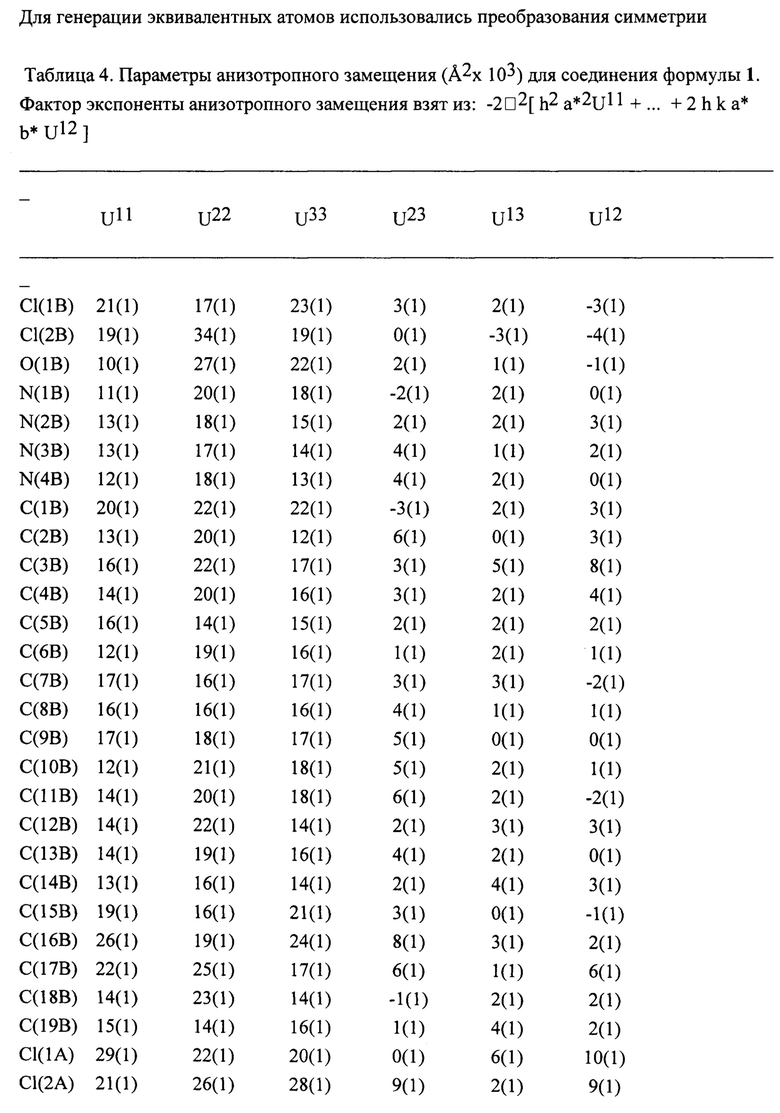
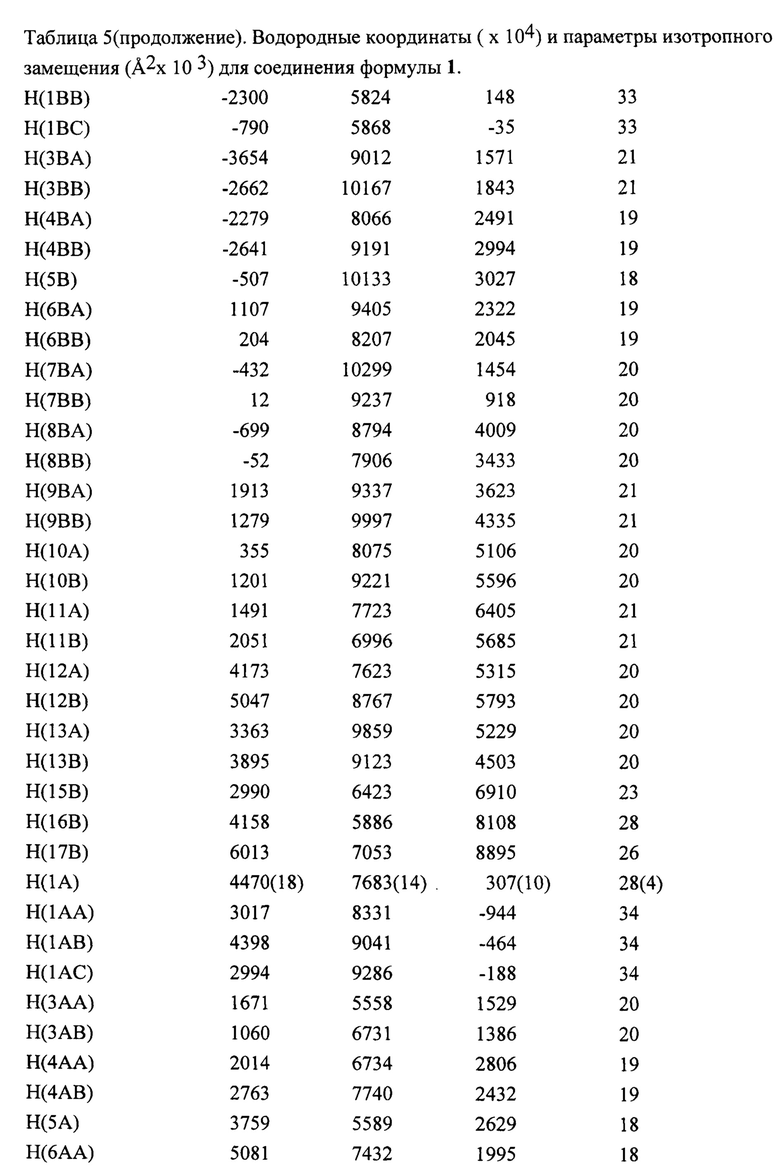
Пример 5. Рентгенодифракционное исследование соединения формулы 1
Рентгенодифракционное исследование соединения 1 провели на дифрактометре Bruker APEX II (MoKa-излучение, графитовый монохроматор, ω-сканирование. Структуры расшифрованы прямым методом и уточнены МНК в анизотропном полноматричном приближении по F2hkl. Атомы водорода рассчитаны геометрически и уточнены с наложением ограничений на длины связей С-Н и их изотропные параметры смещений. Основные кристаллографические данные и параметры уточнения представлены в табл. 1. Все расчеты проведены с использованием программ SHELXL1, SHELXT2 и OLEX-23. Общий вид молекулы показан на фиг. 1-2.
















Пример 6. Исследование активности in vitro.
Соединение формулы 1 протестировано на связывание с D2S (h) рецептором и D3 (h) рецептором в присутствии лигандов - [3H]7-OH-DPAT (1 нМ, Kd 0.68 нМ) и [3Н]-метилспиперон (0.3 нМ, Kd 0.085 нМ), соответственно, и ингибитора неспецифического связывания - бутакламола (10 мкМ) в диапазоне концентраций от 0,1 нМ до 1 мкМ в сравнении с Карипразином. Значения IC50 для соединения формулы 1 составили 6,2 и 7,2 нМ по отношению к рецепторам D2S и D3 соответственно, а для Карипразина - 110 и 3 нМ, соответственно. Таким образом, наблюдалось одинаковое связывание соединения формулы 1 с обоими типами рецепторов, вовлеченных в механизм развития биполярного расстройства, по порядку совпадающее с наименьшей ингибирующей концентрацией для Карипразина, в то время, как для Карипразина IC50 для двух типов рецепторов отличались на два порядка, что позволяет предположить более высокую активность соединения формулы 1 по сравнению с Карипразином.
Пример 7. Исследование антипсихотической активности соединения формулы 1 in vivo
Исследование проведено на моделях 1) апоморфин-индуцированной стереотипии (самцы крыс Sprague Dawley), 2) апоморфин-индуцированной гиперлокомоции (самцы мышей С57В1/6), 3) предстимульного торможения (ПСТ) акустического стартл-рефлекса (самцы мышей С57В1/6), 4) условного рефлекса пассивного избегания (самцы крыс Sprague Dawley) и 5) каталептогенных свойств (самцы крыс Sprague Dawley) в сравнении с типичным - Галоперидол - и атипичным - Оланзапин - антипсихотическими препаратами.
Результаты исследования
На модели апоморфин-индуцированной стереотипии у крыс было показано, что соединение 1 в дозах 0,3 и 3 мг/кг уменьшало степень выраженности стереотипии через 10 и 60 мин после введения апоморфина. В дозе 10 мг/кг соединение формулы 1 вызывало уменьшение степени выраженности и на протяжении всего периода наблюдения, удлинение периода развития и укорочение длительности стереотипии. Причем действие соединения формулы 1 в дозе 10 мг/кг на апоморфин-инудцированную стереотипию было сопоставимо с действием препарата оланзапин в дозе 10 мг/кг.
На модели апоморфин-индуцированной гиперактивности и гиперлокомоции было обнаружено, что соединение формулы 1 во всех изученных дозах (0,3, 1, 3 и 10 мг/кг), как и препараты олназапин в дозе 10 мг/кг и галоперидол в дозе 1 мг/кг, вызывали уменьшение показателей гиперлокомоции и гиперактивности.
В тесте горизонтального стержня на крысах были выявлены каталептогенные свойства соединения формулы 1 в дозах 5, 20 и 40 мг/кг.
В условном рефлексе пассивного избегания (УРПИ) нарушения процессов обучения и памяти после введения крысам соединения формулы 1 в дозах 0,3, 1, 3, 10 мг/кг не выявлено. Препараты сравнения оланзапин в дозе 10 мг/кг и галоперидол в дозе 5 мг/кг вызывали у крыс ухудшение запоминания, о чем свидетельствовало уменьшение латентного периода захода в темный отсек при тестировании через 22 ч после обучения.
Таким образом, в исследовании была показана антипсихотическая активность соединение формулы 1 в моделях in vivo, имитирующих позитивную симптоматику (аопомрфин-индуцированная гиперактивность у мышей и стереотипия у крыс. Также, были выявлены каталептогенные свойства, свидетельствующие об экстрапирамидном влиянии, характерном для типичных нейролептиков. При этом соединение формулы 1 в изученных дозах не оказывало ухудшающего воздействия на условно-рефлекторную память у крыс.
Изобретение относится к новому метиламиду 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты формулы 1, который обладает свойствами частичного агониста допаминовых D2/D3 рецепторов. Соединение может найти применение в качестве активного компонента для фармацевтической композиции и лекарственного средства для лечения психотического расстройства, например биполярного расстройства или некоторых нейродегенеративных заболеваний. Метиламид 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты соответствует формуле 1
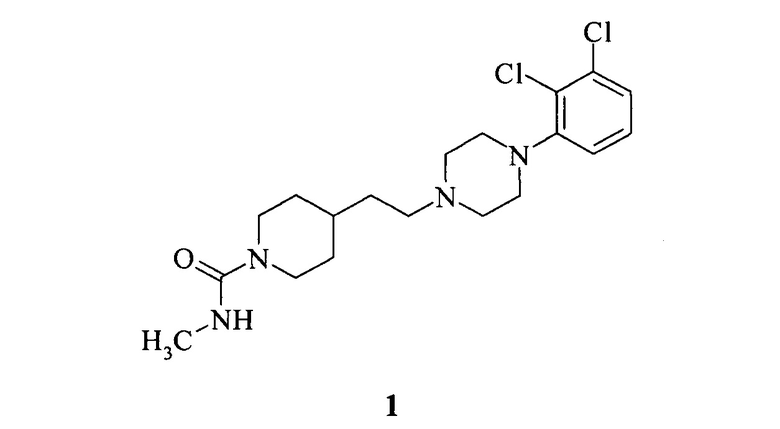
Фармацевтическая композиция может, например, содержать от 1 до 2,5 мас.% соединения I, от 31 до 31,5 мас.% крахмала картофельного и лактозы моногидрата – остальное. 3 н. и 7 з.п. ф-лы, 2 ил., 7 табл., 7 пр.
1. Метиламид 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты формулы 1
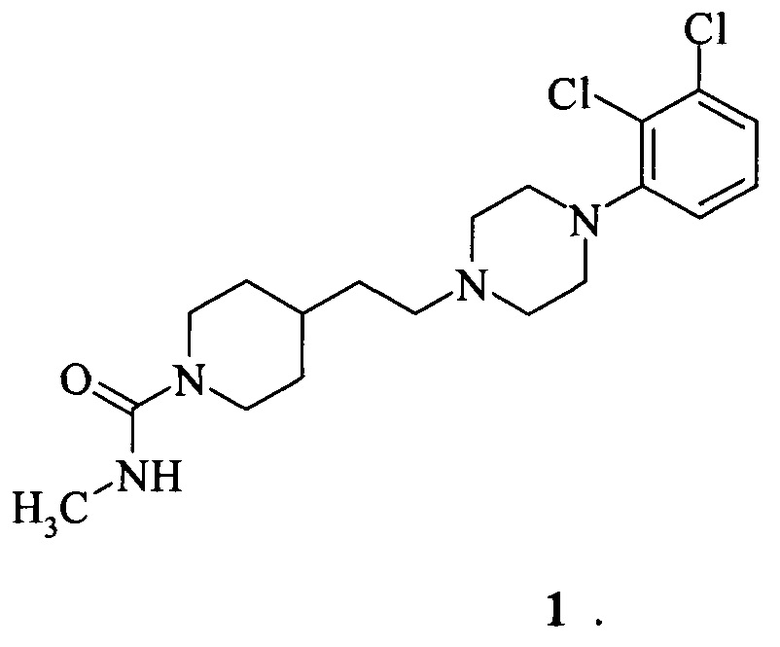
2. Метиламид 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты формулы 1 по п. 1, обладающий свойствами частичного агониста допаминовых D1/D2 рецепторов.
3. Метиламид 4-{2-[4-(2,3-дихлорфенил)-пиперазин-1-ил]-этил}-пиперидин-1-карбоновой кислоты формулы 1 по п. 1 или 2 в качестве активного компонента в эффективном количестве для получения лекарственного средства для лечения психотического расстройства.
4. Фармацевтическая композиция для лечения психотического расстройства, обладающая свойствами частичного агониста допаминовых D1/D2 рецепторов, содержащая в терапевтически эффективном количестве соединение формулы 1 по п. 1 и фармацевтически приемлемые добавки.
5. Фармацевтическая композиция по п. 4, в которой соединение формулы 1 содержится в количестве от 1 до 30 мг, предпочтительно от 1 до 2,5 мг.
6. Фармацевтическая композиция по п. 4, в которой фармацевтически приемлемые добавки выбирают из применяемых в сфере фармацевтики разбавителей, вспомогательных агентов и носителей.
7. Фармацевтическая композиция по п. 6, в которой фармацевтически приемлемые добавки выбирают из крахмала картофельного, лактозы моногидрата.
8. Фармацевтическая композиция по п. 7, отличающаяся тем, что содержит крахмал картофельный в количестве 30,5-32 мг, лактозы моногидрат в количестве 67 мг.
9. Фармацевтическая композиция по п. 4 для лечения психотического расстройства, содержащая:
- от 1 до 2,5 мас. % соединения формулы 1,
- от 31 до 31,5 мас. % крахмала картофельного,
- остальное лактозы моногидрата.
10. Способ лечения психотического расстройства посредством введения в терапевтически эффективном количестве соединения формулы 1 по п. 1 или фармацевтической композиции по любому из пп. 4-9 нуждающемуся в этом реципиенту.
| US 20100075979 A1, 25.03.2010 | |||
| ПРОИЗВОДНЫЕ 1-[М-КАРБОКСАМИДО(ГЕТЕРО)АРИЛ-МЕТИЛ]-ГЕТЕРОЦИКЛИЛ-КАРБОКСАМИДА | 2013 |
|
RU2644761C2 |
Авторы
Даты
2019-01-16—Публикация
2018-06-15—Подача