Изобретение относится к области органической химии, а именно к способу получения четвертичных аммониевых соединений метил дицианоацетата, которые могут быть использованы в качестве биологически активных соединений, оптических материалов и реагентов для органического синтеза.
где 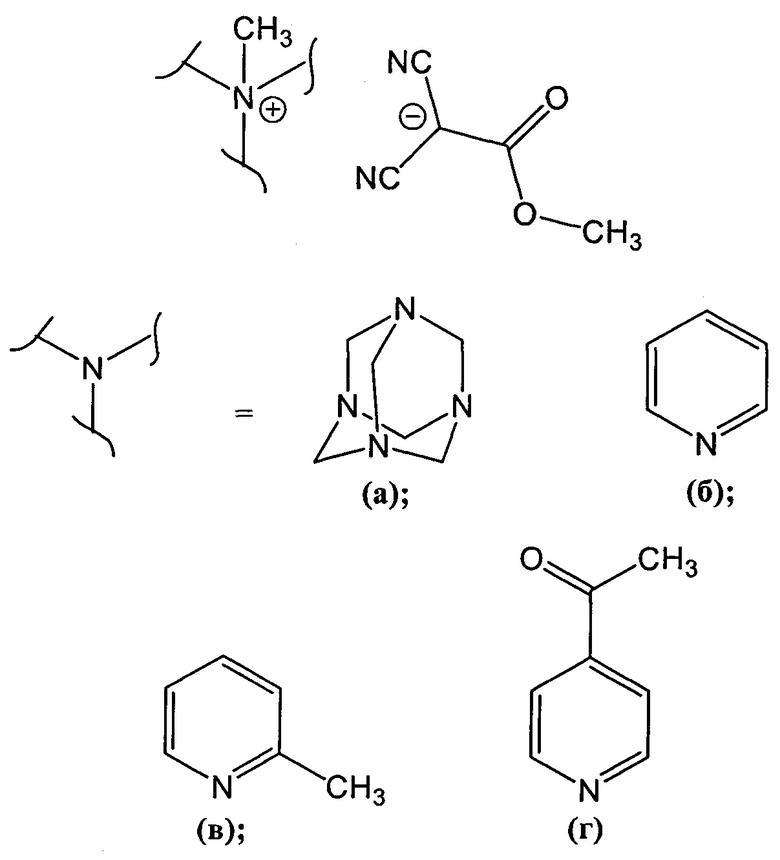
Четвертичные аммониевые соединения характеризуются широким спектром биологической активности, встречаются в природе и наиболее важные из них - холин, ацетилхолин, алкалоид тригонеллин. Четвертичные аммониевые соединения имеют выраженную антимикробную (Khunkitti W., Lloyd D., Furr J.R., Russell A.D. // J. Appl. Microbiol - 1996. - N.81. - P. 73-77.); (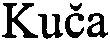 K., Kivala M., Dohnal V. // Journal of Applied Biomedicine - 2004. - N. 2. - P. 195-198) и антивирусную активность (Princt D.L., Prince H.N., Thraenhart O. // J. Clinic Microbiol. - 1993. - N. 31. - P. 3296-3304.).
K., Kivala M., Dohnal V. // Journal of Applied Biomedicine - 2004. - N. 2. - P. 195-198) и антивирусную активность (Princt D.L., Prince H.N., Thraenhart O. // J. Clinic Microbiol. - 1993. - N. 31. - P. 3296-3304.).
Практическое значение имеют противомикробные препараты цетилпиридиний хлорид (биосепт), бензалкония хлорид (герминол), цетавлон, гербицид паракват.
Соли N-метилпиридиния были использованы для получения органических красителей с электрооптическими (ЕО) и нелинейно-оптическими (NLO) свойствами. (Dumur F., Mayer C.R., Dumas E., Miomandre F., Frigoli M., and Secheresse F. // Org. Lett. - 2008. - Vol. 10. - No. 2. - P. 321-324.).
В работе (Neidlein R. and Sui Z. // HELVETICA CHIMICA ACTA - 1991. - Vol. 74. - P. 579-584) отмечено, что алкил дицианоацетаты оказались хорошими синтонами для синтеза гетероциклических соединений.
Известен способ получения солей четвертичных аммониевых соединений, включающий алкилирование третичных аминов на последней стадии, причем в большинстве подобных способов для протекания реакции требуется продолжительное время, нагревание, давление и постоянный контроль за процессом (RU 2414893; RU 2614412; RU 96122387).
Описан способ получения алифатических хлоридов четвертичного аммония из алифатических аминов взаимодействием с метилхлоридом и водным раствором гидроксида щелочного металла в низкокипящем растворителе под давлением. Побочный продукт реакции - хлорид натрия - необходимо постоянно удалять путем фильтрования (US 3813441, Process for the continuous preparation of quaternary ammonium compounds, 1974).
В патенте ЕР 0288857 (Verfahren zur Herstellung von  Ammoniumhalogeniden, 1988) описан способ кватернизации третичных аминов алкилгалогенидами в отсутствие растворителя при молярном соотношении в диапазоне от 1:3 до 1:8 при повышенном давлении (до 27,5 бар).
Ammoniumhalogeniden, 1988) описан способ кватернизации третичных аминов алкилгалогенидами в отсутствие растворителя при молярном соотношении в диапазоне от 1:3 до 1:8 при повышенном давлении (до 27,5 бар).
Известен способ получения четвертичных аммонийных соединений, N-бензил-N,N-диметилалкил-1-аммониум бромидов реакцией квартанизации N,N-диметилбензиламина алкилбромидами (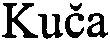 K., Kivala М., Dohnal V. // Journal of Applied Biomedicine. - 2004. - N.2. - P. 195-198). Однако, метод трудоемкий, так как проводится в абсолютном этаноле при кипячении реагентов в течение 28 ч. Продукты реакции очищали хромотографически.
K., Kivala М., Dohnal V. // Journal of Applied Biomedicine. - 2004. - N.2. - P. 195-198). Однако, метод трудоемкий, так как проводится в абсолютном этаноле при кипячении реагентов в течение 28 ч. Продукты реакции очищали хромотографически.
О метилировании аминов метанолом сообщено в работе (Dang Т.Т., Ramalingam В., Seayad А.М // ACS Catalysis. - 2015. - 5(7) - P. 4082-4088), но метод использует дорогостоящий и малодоступный рутениевый катализатор, нагревание до 100°С и не позволяет метилировать третичные амины.
Наиболее близким аналогом к настоящему изобретению является способ получения солей алкил дицианоацетата, заключающийся во взаимодействии малононитрила с алкилхлорформиатом в тетрагидрофуране и в медленном прибавлении к раствору при 30-40°С водного гидроксида калия (Patent ЕР 0010396 А1, 24,10,1980. Fungicidal and herbicidal compositions, certain cyanomethane and cyanoethene derivatives being active agents thereof, the preparation of these derivatives and methods for combating fungi and weeds // EP 0010396 A1. 1980. / Judson P.N., White C.R.H.).
Недостатками данного способа являются низкие выхода (40-58%), трудоемкость проведения процессов, невозможность получения органических производных четвертичных аммонийных соединений путем метилирования третичного атома азота.
Задачей заявленного изобретения является создание способа получения четвертичных аммониевых соединений метил дицианоацетата путем метилирования третичного атома азота в одну стадию в мягких условиях, с увеличенным выходом целевого продукта.
Техническим результатом заявляемого изобретения является получение неописанных в литературе четвертичных аммониевых соединений метил дицианоацетата.
Технический результат достигается тем, что способ получения четвертичных аммониевых соединений метил дицианоацетата общей формулы
где 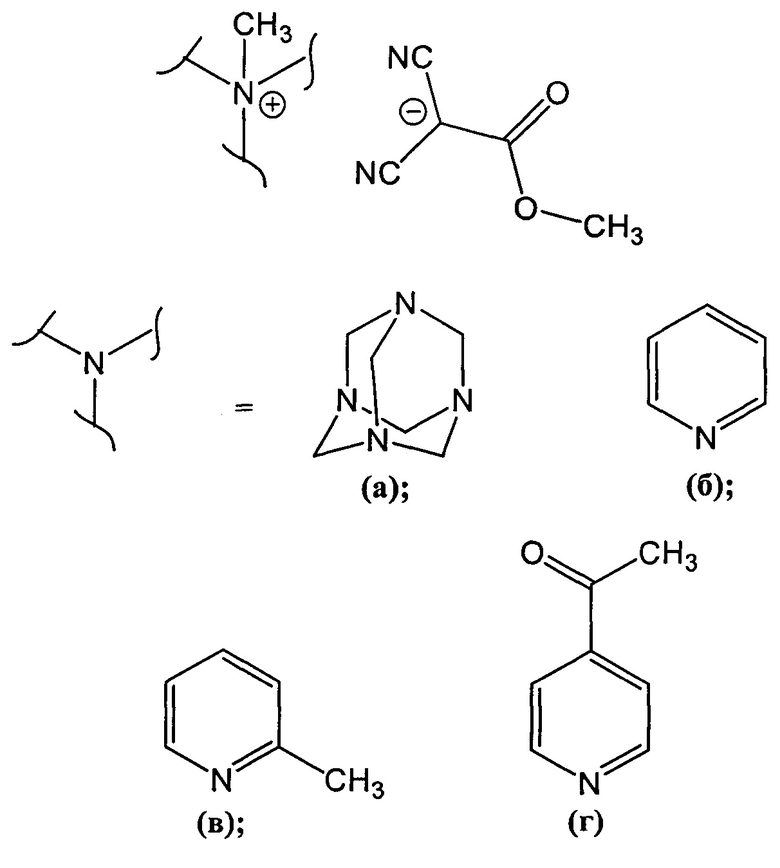
включает взаимодействие тетрацианоэтилена с третичными аминами в метаноле при комнатной температуре в течение 30-40 секунд.
При этом в способе в качестве третичного амина может использоваться уротропин или пиридин или 2-метилпиридин или 4-ацетилпиридин.
Такие условия позволяют получить N-метилзамещенные четвертичные аммониевые соединения метил дицианоацетата одностадийным методом, без побочных процессов и получением новых целевых продуктов с выходом 80-86%, неописанные в литературе.
Способ получения четвертичных аммониевых соединений метил дицианоацетата заключается в том, что раствору 2 ммоль третичного амина в 5-7 мл метанола добавили 2 ммоль (256 мг) тетрацианоэтилена растворенного в 5-7 мл метанола. Реакция протекает за 30-40 секунд. Смесь выдерживали при комнатной температуре в течении 30 мин, затем отгоняли под вакуумом метанол. Для более полной кристаллизации образующегося вещества остаток оставляли в открытом стакане при комнатной температуре в течении 24 ч. Кристаллическое вещество отфильтровывали, промывали смесью метанол-гексан (1:1).
Сущность изобретения заключается в том, что способ получения четвертичных аммониевых соединений метил дицианоацетата включает взаимодействие тетрацианоэтилена с третичными аминами в метаноле, с протекающими процессами N-метилирования и формирования метил дицианоацетатного фрагмента при комнатной температуре и в течение 30-40 секунд. Окончание взаимодействия контролируется ТСХ и качественной реакцией пробы реакционной массы на гидрохинон. Отсутствие синего окрашивания гидрохиноновой пробы свидетельствует о том, что тетрацианоэтилен в реакционной смеси отсутствует. Структуры четвертичных аммониевых соединений метил дицианоацетата определены методами ИК-, ЯМР 1Н, ЯМР 13С-спектроскопии.
Пример 1. Способ получения метил-1,3,5,7-тетраазаадамантан-1-иум 1,1-дициано-2-метокси-2-оксоэтан-1-ид.
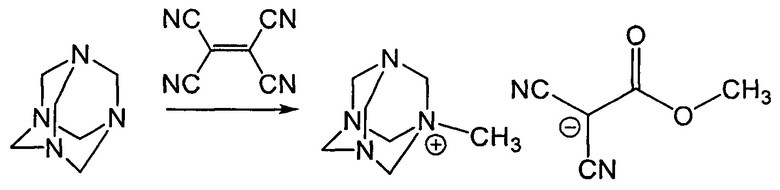
К раствору 2 ммоль (256 мг) тетрацианоэтилена в 5-7 мл метанола добавили 2 ммоль уротропина растворенного в 5-7 мл метанола. Реакция протекает за 30-40 секунд (контроль ТСХ; гидрохиноновая проба). Смесь выдерживали при комнатной температуре в течении 30 мин, затем отгоняли под вакуумом метанол. Для более полной кристаллизации образующегося вещества остаток оставляли в открытом стакане при комнатной температуре в течение 24 ч. Кристаллическое вещество отфильтровывали, промывали смесью метанол-гексан (1:1). Выход 86% (480 мг) светло-желтое вещество, т.пл. 167°С. ИК спектр, ν, см-1: 2184, 2161 (C≡N), 1790 (С=O), 1656 (С=С-O, таутомерная форма). Спектр ЯМР 1H, δ, м. д.: 4.57 (2Н, с, СН2), 3.59(3Н, с, СН3), 3.41 (2Н, с, СН2), 3.33 (3Н, с, СН3). Спектр ЯМР 13С, δC, м. д.: 170.8, 123.19, 122.7, 80.20, 70.58, 50.05, 43.12, 40.78. Найдено, %: С, 51.83; Н, 6,57; N, 30.08. C12H18N6O2. Вычислено, %: С, 51.79; Н, 6.52; N, 30.20.
Пример 2. Способ получения 1-метилпиридин-1-иум 1,1-дициано-2-метокси-2-оксоэтан-1-ида.
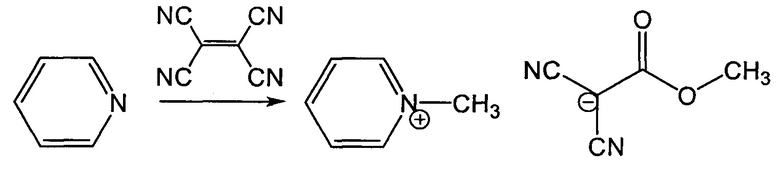
Способ осуществляли аналогично примеру 1, отличающемуся тем, что в качестве третичного амина использовали пиридин. Выход 81% (350 мг), светло-желтое вещество, т.пл. 51°С. ИК спектр, ν, см-1: 2195, 2165 (C≡N), 1723 (С=O), 1628 (С=C-O, таутомерная форма). Спектр ЯМР 1Н, δ, м. д.: 8.97-8.95 (1H, д, СН, J=6 Гц), 8.58-8.54 (1Н, т, СН, J=16 Гц), 8.13-8.09 (1Н, т, СН, J=14 Гц), 4.34 (3Н, с, СН3), 3.41 (3Н, с, СН3). Спектр ЯМР 13С, δC, м. д.: 170.18, 145.60, 145.10, 127.74, 127.71, 122.25, 121.85, 49.89, 47.99, 39.76. Найдено, %: С, 60.93; Н, 5.17; N, 19.48. C11H11N3O2. Вычислено, %: С, 60.82; Н, 5.10; N, 19.34.
Пример 3. Способ получения 1,2-диметилпиридин-1-иум 1,1-дициано-2-метокси-2-оксоэтан-1-ида.
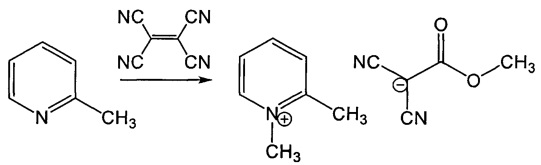
Способ осуществляли аналогично примеру 1, отличающемуся тем, что в качестве третичного амина использовали 2-метилпиридин. Выход 83% (380 мг), светло-желтое вещество, т.пл. 52°С. ИК спектр, ν, см-1: 2190, 2162 (С≡N, 1724 (С=O), 1641 (С=C-O, таутомерная форма). Спектр ЯМР 1Н, δ, м. д.: 8.95-8.92 (1Н, д, СН, J=6 Гц), 8.47-8.42 (1Н, т, СН, J=16 Гц), 8.04-8.00 (1Н, д, СН, J=8 Гц), 7.94-7.90 (1Н, т, СН, J=15 Гц), 4.21 (3Н, с, СН3), 3.41 (3Н, с, СН3), 2.76 (3Н, с, СН3). Спектр ЯМР 13С, δС, м. д.: 169.92, 155.89, 146.11, 145.03, 129.14, 125.24, 122.35, 121.92, 49.86, 45.47, 40.18, 19.92. Найдено, %: С, 61.46; Н, 5.68; N, 18.08. C12H13N3O2. Вычислено, %: С, 62.33; Н, 5.67; N, 18.17.
Пример 4. Способ получения 4-Ацетилпиридин-1-иум 1,1-дициано-2-метокси-2-оксоэтан-1-ида.
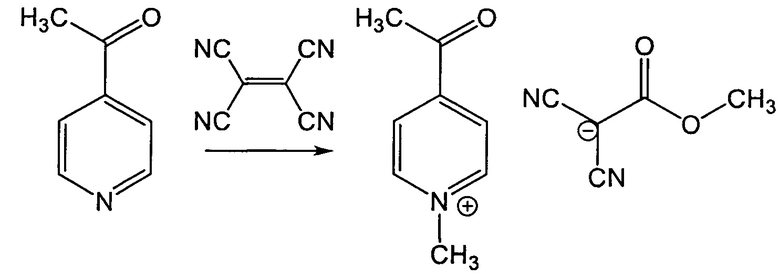
Способ осуществляли аналогично примеру 1, отличающемуся тем, что в качестве третичного амина использовали 4-ацетилпиридин. Выход 80% (415 мг), красное вещество, т.пл. 103°С. ИК спектр, ν, см-1: 2189, 2162 (C≡N), 1705 (С=O), 1642 (С=C-O, таутомерная форма). Спектр ЯМР 1H, δ, м. д.: 9.18-9.16 (1Н, д, СН, J=6 Гц), 8.46-8.45 (1Н, д, СН, J=6 Гц), 4.40 (3Н, с, СН3), 3.41 (3Н, с, СН3), 2.72 (3Н, с, СН3). Спектр ЯМР 13С, δС, м. д.: 195.87, 169.92, 149.75, 148.44, 147.11, 125.58, 122.14, 121.92, 49.86, 48.24, 40.17, 27.42. Найдено, %: С, 60.06; Н, 5.12; N, 16.33. C13H13N3O3. Вычислено, %: С, 60.23; Н, 5.05; N, 16.21.
Таким образом, предлагаемый способ позволяет получить четвертичные аммониевые соединения метил дицианоацетата, которые могут быть использованы в качестве биологически активных соединений, оптических материалов и в качестве реагентов для органического синтеза.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИБАКТЕРИАЛЬНЫЕ СРЕДСТВА НА ОСНОВЕ ЧЕТВЕРТИЧНЫХ АММОНИЕВЫХ СОЛЕЙ | 2014 |
|
RU2561281C1 |
| Четвертичные аммониевые соли на основе производных витамина В6 | 2015 |
|
RU2607522C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5,8,9,10-ТЕТРАГИДРОПИРИМИДО[4,5-d]АЗОЦИНОВ, ИМЕЮЩИХ В 4-М ПОЛОЖЕНИИ ТРИФЛАТНУЮ, ВТОРИЧНУЮ И ТРЕТИЧНУЮ АМИНОГРУППЫ | 2011 |
|
RU2478637C2 |
| Способ получения 2-ацил(ароил)-7-имино-6-оксабицикло[3.2.1]октан-1,8,8-трикарбонитрилов | 2017 |
|
RU2657250C1 |
| РЕАКЦИОННОСПОСОБНЫЕ ГЕТЕРОЦЕПНЫЕ ОЛИГОМЕРЫ НА ОСНОВЕ МЕТАКРИЛОВЫХ ПРОИЗВОДНЫХ, СОДЕРЖАЩИХ ГРУППЫ С ПОДВИЖНЫМ АТОМОМ ВОДОРОДА, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2228340C2 |
| НЕПРЕРЫВНЫЙ СПОСОБ АЛКИЛИРОВАНИЯ ЦИКЛИЧЕСКИХ ТРЕТИЧНЫХ АМИНОВ | 2012 |
|
RU2614412C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЗАМЕЩЕННЫХ 2-ОКСО-1,2-ДИГИДРОПИРИДИН-3,4-ДИКАРБОНИТРИЛОВ | 2015 |
|
RU2577526C1 |
| КРАУНСОДЕРЖАЩИЕ СТИРИЛОВЫЕ КРАСИТЕЛИ С АММОНИЙНОЙ ГРУППОЙ В N-ЗАМЕСТИТЕЛЕ ГЕТЕРОЦИКЛИЧЕСКОГО ОСТАТКА В КАЧЕСТВЕ ФОТО- И ТЕРМОЧУВСТВИТЕЛЬНЫХ СОЕДИНЕНИЙ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2278134C1 |
| Способ получения 7-имино-6-оксабицикло[3.2.1]окт-3-ен-1,8,8-трикарбонитрилов | 2017 |
|
RU2637941C1 |
| Четвертичные аммониевые соединения на основе производных пентаэритрита и пиридоксина, обладающие антибактериальной активностью | 2023 |
|
RU2811203C1 |
Изобретение относится к способу получения четвертичных аммониевых соединений и может быть применено в химической промышленности. Предложен способ получения метил дицианоацетата общей формулы
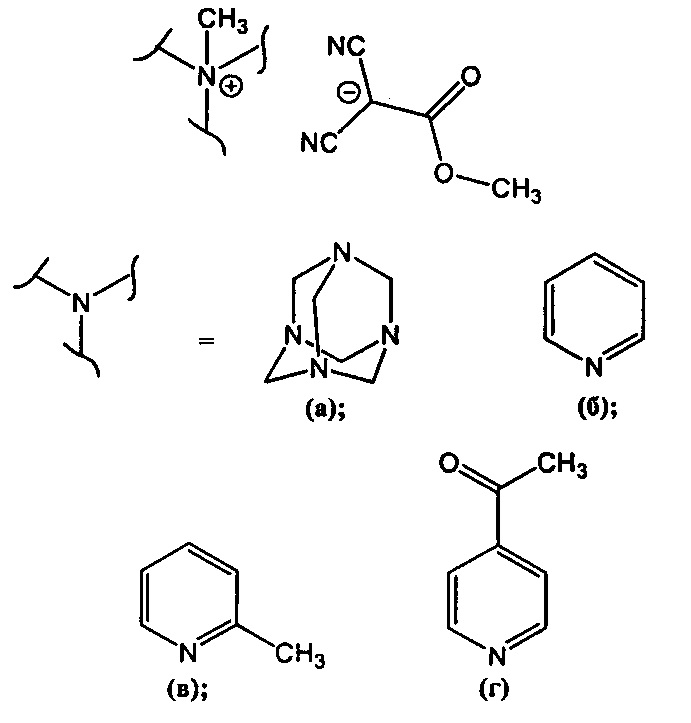 ,
,
включающий взаимодействие тетрацианоэтилена с третичными аминами в метаноле при комнатной температуре в течение 30-40 секунд. Технический результат - получение новых четвертичных аммониевых соединений метил дицианоацетата, которые могут быть использованы для получения биологически активных соединений, оптических материалов и в качестве реагентов для органического синтеза. 1 з.п. ф-лы, 4 пр.
1. Способ получения четвертичных аммониевых соединений метил дицианоацетата общей формулы
где 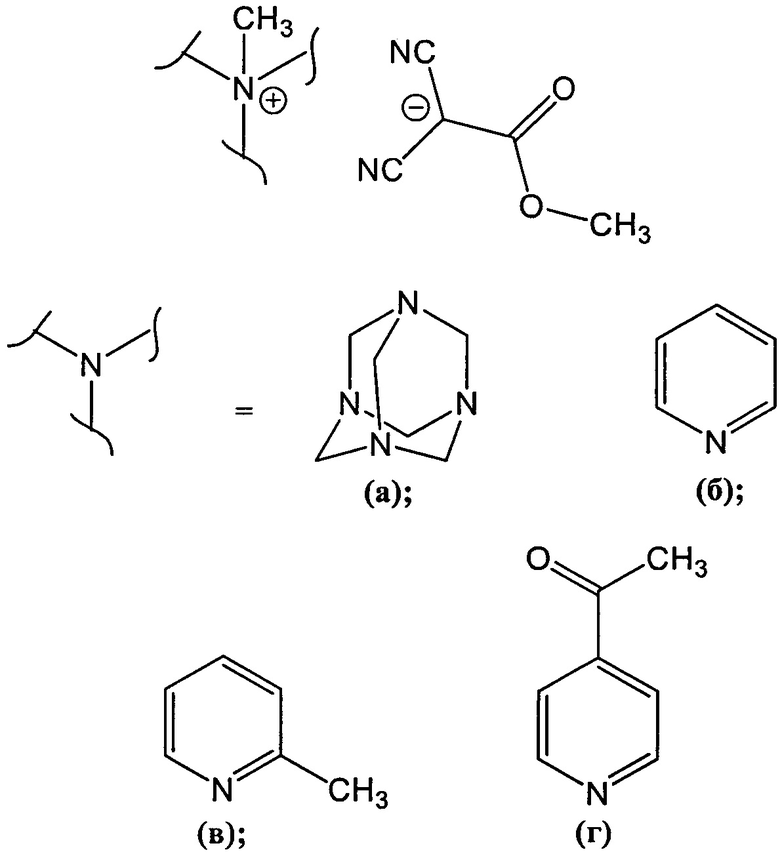
включающий взаимодействие тетрацианоэтилена с третичными аминами в метаноле при комнатной температуре в течение 30-40 секунд.
2. Способ по п. 1, отличающийся тем, что в качестве третичного амина используется уротропин, или пиридин, или 2-метилпиридин, или 4-ацетилпиридин.
| Жесткий трал против мин заграждения | 1928 |
|
SU10396A1 |
| US 4803011 A1, 07.02.1989 | |||
| US 3813441 A1, 28.05.1974 | |||
| ЧЕТВЕРТИЧНОЕ АММОНИЕВОЕ ПРОИЗВОДНОЕ НОВОКАИНА, ОБЛАДАЮЩЕЕ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2414893C1 |
| НЕПРЕРЫВНЫЙ СПОСОБ АЛКИЛИРОВАНИЯ ЦИКЛИЧЕСКИХ ТРЕТИЧНЫХ АМИНОВ | 2012 |
|
RU2614412C2 |
| RU 96122387 A, 27.12.1998. | |||
Авторы
Даты
2019-01-16—Публикация
2018-07-30—Подача