Настоящее изобретение относится к новому способу промышленного синтеза 7-метокси-1-нафталин-1-карбальдегида и к его применению в промышленном производстве агомелатина, или N-[2-(7-метокси-1-нафтил)этил]ацетамида.
Более конкретно, настоящее изобретение относится к способу промышленного синтеза соединения формулы (I):
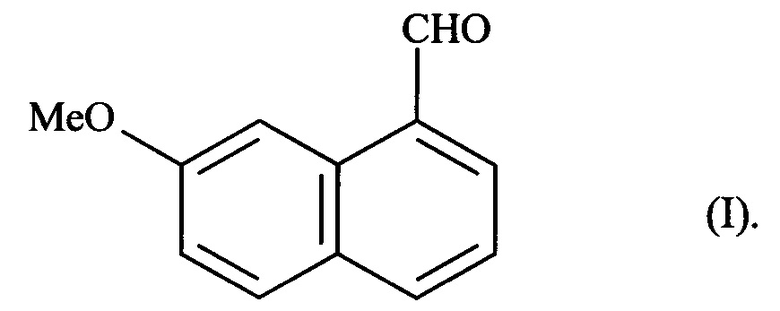
Соединение формулы (I), полученное согласно способу изобретения является полезным в синтезах агомелатина, или N-[2-(7-метокси-1-нафтил)этил]ацетамида, формулы (II):
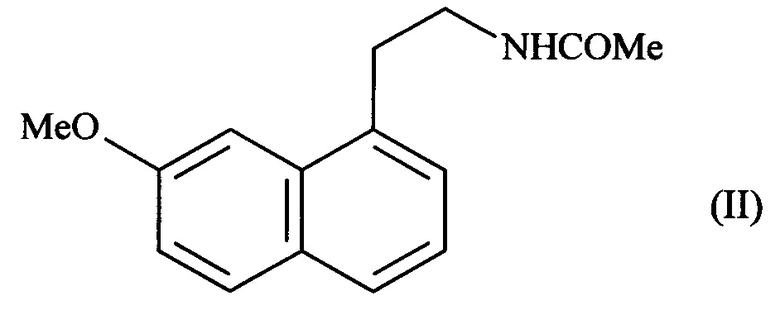
Агомелатин, или N-[2-(7-метокси-1-нафтил)этил]ацетамид, обладает ценными фармакологическими свойствами.
Он, по факту, имеет двойную характеристику, будучи, с одной стороны, агонистом рецепторов мелатонергетической системы и, с другой стороны, антагонистом рецептора 5-HT2C. Эти свойства обеспечивают активность в центральной нервной системе и, более конкретно, в лечении большой депрессии, сезонного аффективного расстройства, нарушений сна, патологий сердечнососудистой системы, патологий органов пищеварения, бессонницы и усталости через нарушение суточного ритма организма, нарушении аппетита и ожирении.
Агомелатин, его получение и его применение в лечении описано в описаниях Европейских патентов ЕР 0 447 285 и ЕР 1 564 202.
Принимая во внимание фармацевтическое значение этого соединения, важно иметь возможность получать его способом эффективного синтеза, который является ликвидным в промышленном масштабе и который дает в результате агомелатин с хорошим выходом и с отличной чистотой, начиная с экономичных и легко получаемых исходных материалов.
Описание к патенту ЕР 0 447 285 описывает получение агомелатина в восемь стадий, начиная с 7-метокси-1-тетралона. Тем не менее, быстро обнаружились трудности в осуществлении такого способа, при переходе на промышленный масштаб.
В литературе описано получение 7-метокси-нафталин-1-карбальдегида в 5 стадий, начиная с 8-амино-нафталин-2-ола (Kandagatla et al., Tetrahedron Lett. 2012, 53, 7125-7127). Получение 7-метокси-нафталин-1-карбальдегида в 4 стадии, начиная с 7-метокси-тетралона, также было описано (Garipati et al., Bioorg. Med. Chem. Lett. 1997, 7, 1421-1426). 7-Метокси-1-тетралон и 8-амино-нафталин-2-ол являются, тем не менее, дорогими исходными материалами, и, следовательно, все еще продолжается поиск новых путей синтеза, конкретно, начиная с менее дорогих реагентов.
Заявитель продолжил свои исследования и развил новый промышленный синтез, который соответствуя требованиям воспроизводимости и не требуя трудоемкой очистки, дает агомелатин с чистотой, которая совместима с его применением в качестве фармацевтического активного действующего вещества, начиная с менее дорогого и более легко получаемого исходного материала.
Более конкретно, Заявитель в данный момент развил новый промышленный способ синтеза, позволяющий получать 7-метокси-нафталин-1-карбальдегид в соответствии с требованиями воспроизводимости, не требуя трудоемкой очистки, применяя 7-метокси-нафталин-2-ол в качестве исходного материала. Этот новый исходный материал имеет преимущества, будучи простым и легко получаемым в больших количествах при малой стоимости. 7-Метокси-нафталин-2-ол также имеет преимущества, имея в своей структуре систему нафталинового кольца, которая не допускает включения стадии ароматизации в синтезах - стадии, которая всегда является проблематичной с промышленной точки зрения.
Более конкретно, настоящее изобретение относится к способу промышленного синтеза соединения формулы (I):
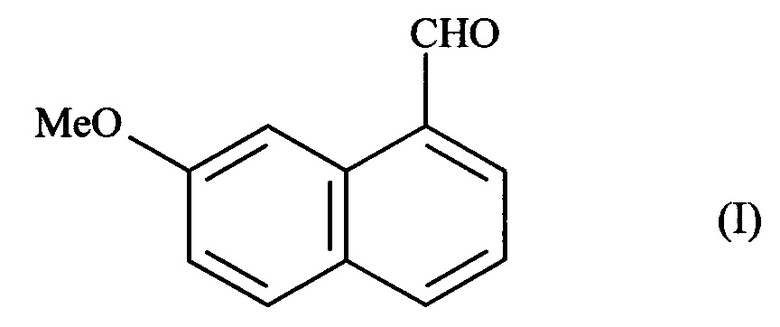
который отличается тем, что 7-метокси-нафталин-2-ол формулы (III):
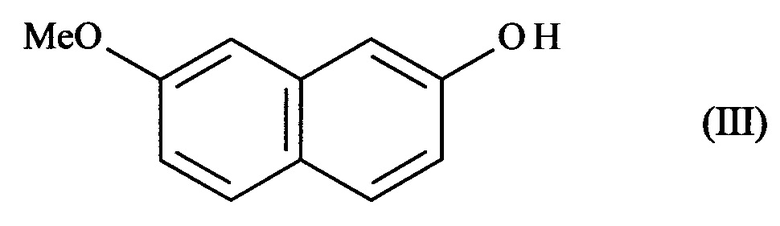
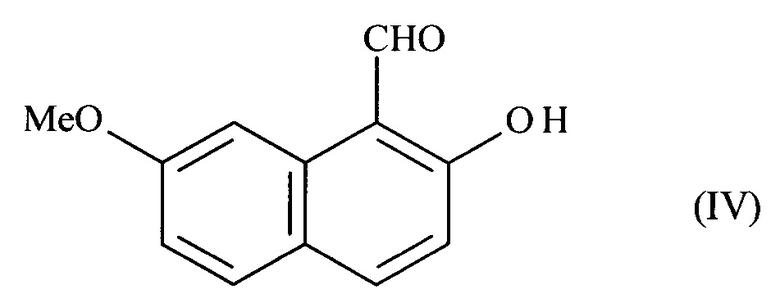
применяют для реакции, реакции формилирования, выполняемой в положении 1 соединения формулы (III), чтобы получить соединение формулы (IV):
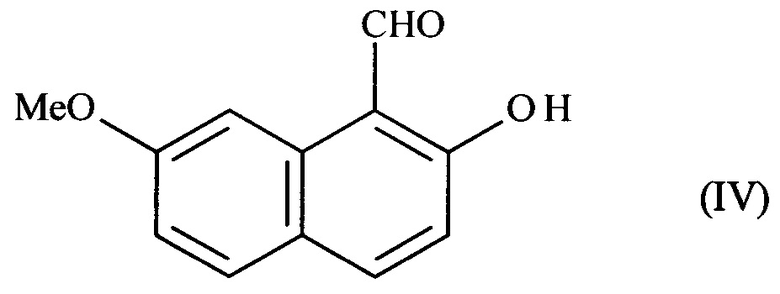
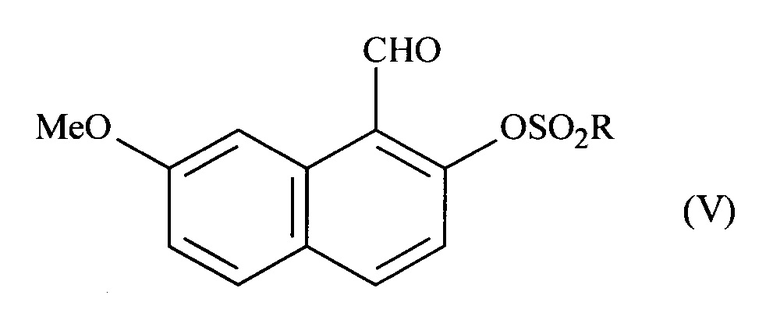
где соединение формулы (IV) подвергают реакции сульфонилирования, чтобы получить соединение формулы (V):
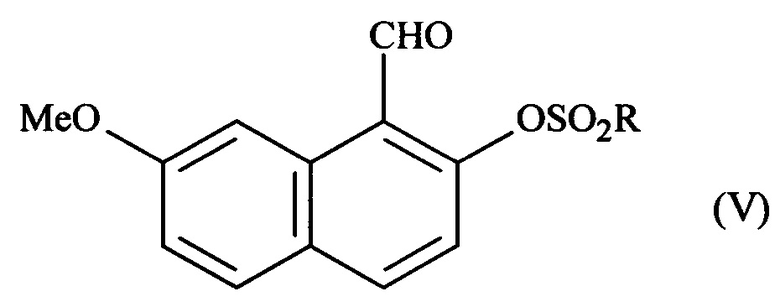
где R означает -СН3, -(СН2)2-СН3, -CF3 или толильную группу;
где соединение формулы (V) подвергают реакции дезоксигенирования в присутствии переходного металла и восстановителя, чтобы получить соединение формулы (I), которое выделяют в форме твердого вещества.
Соединение формулы (III) является коммерчески доступным или легко получаемым специалистом в данной области техники, применяя химические реакции, которые являются общепринятыми или описаны в литературе.
R предпочтительно означает -СН3 или толильную группу.
В способе согласно изобретению, преобразование соединения формулы (III) в соединение формулы (IV) включает действие этилортоформиата в присутствии анилин с последующим гидролизом полученного промежуточного иминового соединения.
В способе согласно изобретению, преобразование соединения формулы (IV) в соединение формулы (V) включает стадию сульфонилирования выполняемую с помощью действия сульфонил хлорида, ангидрида сульфокислоты или сульфонимида. В предпочтительном варианте осуществления, эту стадию сульфонилирования проводят с помощью действия сульфонил хлорида и, конкретно, тозил хлорида или мезил хлорида.
В способе согласно изобретению, преобразование соединения формулы (V) в соединение формулы (I) включает стадию дезоксигенирования в присутствии переходного металла и восстановителя.
Предпочтительно, переходной металл представляет собой никель, палладий или платину. Переходной металл может быть или в форме соли или в форме простого вещества. Предпочтительно, соль переходного металла является солью никеля или солью палладия, более предпочтительно солью палладия.
Преимущественно, восстановителем является или гидрид, такой как боргидрид натрия или алюмогидрид лития; или аминоборан, такой как диметиламин боран; или алкоксисилан, такой как диметоксиметилсилан; или алкилсилан, такой как триэтилсилан; или щелочноземельный металл, такой как магний; или водород. Предпочтительно, восстановитель представляет собой водород, который применяют прямо в его газообразной форме или непрямо, полученный разложением формиата аммония. Восстановителем предпочтительно является водород, полученный разложением формиата аммония.
В соответствии с другим предпочтительным вариантом осуществления, преобразование соединения формулы (V) в соединение формулы (I) включает стадию дезоксигенирования в присутствии никеля, конкретно соли никеля, и гидрида, предпочтительно боргидрида натрия.
В соответствии с другим предпочтительным вариантом осуществления, преобразование соединения формулы (V) в соединение формулы (I) включает стадию дезоксигенирования в присутствии палладия и водорода.
В соответствии с другим предпочтительным вариантом осуществления, преобразование соединения формулы (V) в соединение формулы (I) включает стадию дезоксигенирования в присутствии палладия и щелочноземельного металла, предпочтительно магния.
Преимущественно, реакцию превращения соединения формулы (V) в соединение формулы (I) проводят в диметилформамиде, диоксане, тетрагидрофуране и толуоле, и более предпочтительно диметилформамиде.
Предпочтительно, реакцию превращения соединение формулы (V) в соединение формулы (I) проводят между 25°С и 110°С, более конкретно между 40°С и 95°С.
В соответствии с другим предпочтительным вариантом осуществления, преобразование соединения формулы (V) в соединение формулы (I) включает стадию дезоксигенирования в присутствии переходного металла, восстановителя и лиганда.
Лиганд может быть или фосфиновым лигандом или диаминокарбеновым лигандом, более предпочтительно фосфиновым лигандом и, более конкретно, 1,3-бис(дифенилфосфино)пропаном или (9,9-диметил-9H-ксантан-4,5-диил)бис(дифенилфосфином).
Вариант, который является преимущественным для способа промышленного синтеза, включает преобразование соединения формулы (IV), выполняемое, чтобы непосредственно сформировать соединение формулы (I), указанную реакцию сульфонилирования и указанную реакцию дезоксигенирования в присутствии переходного металла, выполняют в виде "однореакторной" методики.
Этот способ является конкретно преимущественным по следующему ряду причин:
- он делает возможным получить соединение формулы (I) в промышленном масштабе с хорошими выходами, начиная с простого и недорогого исходного материала;
- он делает возможным избежать реакции ароматизации, потому что в исходном веществе присутствует система нафталинового кольца;
- он делает возможным получить агомелатин, начиная с 7-метокси-нафталин-2-ол в уменьшенном числе стадий.
Соединения формулы (V), полученные согласно способу изобретения, являются новыми и полезными в качестве промежуточных соединений в синтезах агомелатина и соединения формулы (I).
Предпочтительными соединениями формулы (V) являются следующие:
- 1-формил-7-метоксинафталин-2-ил 4-метилбензолсульфонат;
- 1-формил-7-метоксинафталин-2-ил метансульфонат.
Полученное соединение формулы (I) настоящего документа последовательно подвергают сериям общепринятых химических реакций (например: восстановление альдегида до первичного спирта, цианирование, восстановление и ацетилирование полученного первичного амина), чтобы получить агомелатин формулы (II).
Примеры, далее, ниже, иллюстрируют изобретение, но не ограничивают его каким-либо образом.
Для того чтобы должным образом согласовать пути реакции, синтезированные промежуточные соединения систематически изолировали и обнаруживали. Тем не менее, возможно существенно оптимизировать методики, ограничивая число изолированных промежуточных соединений.
Структуры описанных соединений подтверждали обычными спектроскопическими методиками: протонный ЯМР (s = синглет; d = дублет; dd = двойной дублет); углеродный ЯМР (s = синглет; d = дублет; q = квадруплет).
ПРИМЕР 1: 7-метоксинафталин-1-карбальдегид
Стадия А: 2-гидрокси-7-метоксинафталин-1-карбалъдегид
7-Метокси-нафталин-2-ол (3.5 г; 20.11 ммоль), этилортоформиат (3.51 мл; 21.12 ммоль) и анилин (1.83 мл; 20.11 ммоль) вводят в сосуд, снащенный холодильником. После перемешивания в течение 20 часов кипения с обратным холодильником и охлаждения, твердую фазу измельчают в 2М этанольном растворе соляной кислоты (20 мл). После перемешивания в течение 30 минут при 60°С и охлаждения, твердую фазу собирают фильтрованием и затем промывают водой и высушивают азеотропной перегонкой с этанолом и применяют непосредственно без какой-либо другой очистки (2.95 г; 73%).
1Н ЯМР-спектроскопический анализ (CDCl3, δ в млн.д.) 13.17 (s, 1Н); 10.74 (s, 1Н); 7.88 (d, J=9.1 Гц, 1Н); 7.69 (d, J=8.9 Гц, 1Н); 7.65 (d, J=2.4 Гц, 1Н); 7.07 (dd, J=8.9 и 2.4 Гц, 1Н); 6.97 (d, J=9.1 Гц, 1Н); 3.95 (s, 3Н).
Стадия В: 1-формил-7-метоксинафталин-2-ил 4-метилбензолсулъфонат
К раствору продукта, вышеуказанной Стадии А, (1 г; 4.95 ммоль) в дихлорметане (20 мл) добавляют триэтиламин (826 мкл; 5.94 ммоль) и тозил хлорид (0.99 г; 5.2 ммоль). После перемешивания в течение 24 часов, растворитель испаряют и затем остаток поглощают смесью вода/этилацетат. Органическую фазу промывают разбавленным раствором соляной кислоты, воды и солевого раствора и затем высушивают над сульфатом натрия и фильтруют. Испарение растворителей приводит к неочищенному продукту, который очищают перекристаллизацией из горячего этилацетата, чтобы получить титульный продукт (1.132 г; 65%).
Точка плавления: 147-148°С.
1Н ЯМР-спектроскопический анализ (CDCl3, δ в млн.д.) 10.41 (s, 1Н); 8.68 (d, J=2.6 Гц, 1Н); 7.95 (d, J=8.9 Гц, 1Н); 7.74 (d, J=8.2 Гц, 2Н); 7.72 (d, J=8.9 Гц, 1H); 7.33 (d, J=8.2 Гц, 2H); 7.19 (dd, J=8.9 и 2.6 Гц, 1H); 7.15 (d, J=8.9 Гц, 1H); 3.93 (s, 3H); 2.45 (s, 3H).
13С ЯМР-спектроскопический анализ (CDCl3, δ в млн.д.) 190.3 (d); 161.5 (s); 154.3 (s); 146.4 (s); 136.4 (d); 132.8 (s); 131.5 (s); 130.3 (2 x d); 129.9 (d); 128.6 (2 x d); 127.8 (s); 121.5 (s); 120.1 (d); 118.6 (d); 104.1 (d); 55.6 (q); 21.9 (q).
Стадия С: 7-метоксинафталин-1-карбальдегид
Продукт вышеуказанной Стадии В (356 мг; 1 ммоль), ацетат палладия (4.5 мг; 0.02 ммоль), 1,3-бис(дифенилфосфино)пропан (8.2 мг; 0.02 ммоль), диметилформамид (2 мл), триэтиламин (556 мкл; 4 ммоль) и муравьиную кислоту (150 мкл; 4 ммоль) вводят в сосуд, помещенный в сушильный шкаф и очищенный аргоном. Сосуд помещают в баню, нагреваемую до 90°С в течение 1.5 часа. После охлаждения, смесь разбавляют этилацетатом и органическую фазу промывают 1М водным раствором соляной кислоты и солевым раствором, высушивают над сульфатом натрия и фильтруют. После испарения растворителя, неочищенный продукт очищают фильтрацией над нейтральным оксидом алюминия, чтобы получить титульный продукт (139 мг; 15%).
Точка плавления: 65-67°С.
1Н ЯМР-спектроскопический анализ (CDCl3, 300.13 МГц, δ в млн.д.) 10.29 (s, 1Н); 8.75 (d, J=2.6 Гц, 1H); 7.99 (d, J=8.1 Гц, 1Н); 7.9 (d, J=7.1 Гц, 1Н); 7.77 (d, J=8.9 Гц, 1Н); 7.45 (dd, J=8.1 и 7.1 Гц, 1Н); 7.23 (dd, J=8.9 и 2.6 Гц, 1Н); 3.98 (s, 3Н).
13C ЯМР-спектроскопический анализ (CDCl3, 75.5 МГц, δ в млн.д.) 194.1 (d); 160.7 (s); 138.3 (d); 135.1 (d); 132.2 (s); 130.2 (s); 129.9 (d); 129.3 (s); 122.5 (d); 119.8 (d); 103.6 (d); 55.6 (q).
ПРИМЕР 2: 7-метоксинафталин-1-карбальдегид
Стадия А: 1-формил-7-метоксинафталин-2-ил метансульфонат
К раствору соединения, полученного на Стадии А Примера 1 (300 мг; 1.485 ммоль), в дихлорметане (5 мл) добавляют триэтиламин (250 мкл; 1.782 ммоль) и мезил хлорид (120 мкл). После перемешивания в течение одного часа, растворитель испаряют, и остаток поглощают смесью этилацетат/вода. Органическую фракцию промывают дважды водой и затем солевым раствором, высушивают над сульфатом натрия и фильтруют. Испарение растворителя приводит к чистому титульному продукту (416 мг; 95%) без необходимости для очистки.
1Н ЯМР-спектроскопический анализ (CDCl3, δ в млн.д.) 10.74 (s, 1Н); 8.72 (d, J=2.4 Гц, 1H); 8.03 (d, J=8.9 Гц, 1H); 7.75 (d, J=8.9 Гц, 1H); 7.36 (d, J=8.9 Гц, 1H); 7.22 (dd, J=8.9 и 2.4 Гц, 1H); 3.97 (s, 3H); 3.32 (s, 3H).
13C ЯМР-спектроскопический анализ (CDCl3, δ в млн.д.) 190.4 (d); 161.6 (s); 153.2 (s); 136.8 (d); 133.1 (s); 130.0 (d); 128.0 (s); 121.6 (s); 120.3 (d); 118.2 (d); 104.0 (d); 55.7 (q); 38.5 (q).
Стадия В: 7-метоксинафталин-1-карбальдегид
Титульный продукт (84%) получают согласно способу, описанному в Стадии С Примера 1, начиная с продукта вышеуказанной Стадии А и со времени реакции 4 часа при 90°С вместо 1.5 часа.
Точка плавления: 65-67°С.
1Н ЯМР-спектроскопический анализ (CDCl3, 300.13 МГц, δ в млн.д.) 10.29 (s, 1Н); 8.75 (d, J=2.6 Гц, 1Н); 7.99 (d, J=8.1 Гц, 1Н); 7.9 (d, J=7.1 Гц, 1H); 7.77 (d, J=8.9 Гц, 1Н); 7.45 (dd, J=8.1 и 7.1 Гц, 1H); 7.23 (dd, J=8.9 и 2.6 Гц, 1Н); 3.98 (s, 3Н).
13C ЯМР-спектроскопический анализ (CDCl3, 75.5 МГц, δ в млн.д.) 194.1 (d); 160.7 (s); 138.3 (d); 135.1 (d); 132.2 (s); 130.2 (s); 129.9 (d); 129.3 (s); 122.5 (d); 119.8 (d); 103.6 (d); 55.6 (q).
ПРИМЕР 3: 7-метоксинафталин-1-карбальдегид
Гидрид натрия (60%; 17 мг; 0.415 ммоль) добавляют, несколькими порциями, к раствору 7-метокси-нафталин-2-ола (70 мг; 0.35 ммоль) в обезвоженном диметилформамиде (1 мл), в сосуд, очищенный аргоном. После перемешивания в течение 30 минут при температуре окружающей среды, затем, несколькими порциями, добавляют тозил хлорид (190.5 мг; 0.36 ммоль). После перемешивания в течение 4 часов при температуре окружающей среды добавляют 1,3-бис(дифенилфосфино)пропан (7.1 мг; 0.017 ммоль), ацетат палладия (3.9 мг; 0.073 ммоль), триэтиламин (192 мкл; 1.38 ммоль) и муравьиную кислоту (150 мкл; 4 ммоль) и реакционную смесь нагревают при 90°С в течение 1.5 часа. После охлаждения, смесь перегоняют с этилацетатом и органическую фазу промывают 1М водным раствором соляной кислоты и затем солевым раствором, высушивают над сульфатом натрия и фильтруют. После испарения растворителя, неочищенный продукт фильтруют над нейтральным оксидом алюминия (элюент: этилацетат), чтобы получить титульный продукт (61.6 мг; 95%).
Точка плавления: 65-67°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ СПОСОБ СИНТЕЗА АГОМЕЛАТИНА | 2014 |
|
RU2683279C1 |
| НОВЫЙ СПОСОБ СИНТЕЗА АГОМЕЛАТИНА | 2012 |
|
RU2550812C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ НАФТАЛИН-2-ИЛ-ПИРАЗОЛ-3-ОНА, ИСПОЛЬЗУЕМЫХ В СИНТЕЗЕ ИНГИБИТОРОВ СИГМА РЕЦЕПТОРА | 2009 |
|
RU2509763C2 |
| СПОСОБ СИНТЕЗА(Z)-3-[2-БУТОКСИ-3'-(3-ГЕПТИЛ-1-МЕТИЛУРЕИДО)БИФЕНИЛ-4-ИЛ]-2-МЕТОКСИАКРИЛОВОЙ КИСЛОТЫ | 2008 |
|
RU2478614C2 |
| ПРОИЗВОДНЫЕ 3-КАРБОКСИПРОПИЛ-АМИНОТЕТРАЛИНА И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ АНТАГОНИСТОВ MU-ОПИОИДНОГО РЕЦЕПТОРА | 2008 |
|
RU2482107C2 |
| ПРОИЗВОДНЫЕ 2-ГИДРОКСИЭТИЛ-1Н-ХИНОЛИН-2-ОНА И ИХ АЗАИЗОСТЕРИЧЕСКИЕ АНАЛОГИ С АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2540862C2 |
| АНТИБИОТИЧЕСКИЕ ПРОИЗВОДНЫЕ 2-ОКСО-ОКСАЗОЛИДИН-3, 5-ДИИЛА | 2012 |
|
RU2616609C2 |
| СИНТЕЗ ГАЛИХОНДРИНОВ | 2018 |
|
RU2794176C2 |
| СПОСОБ СИНТЕЗА | 2011 |
|
RU2572554C2 |
| ПРОИЗВОДНЫЕ ХРОМОНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2010 |
|
RU2545214C2 |
Настоящее изобретение относится к способу синтеза соединения формулы (I) – промежуточного соединения для получения агомелатина, обладающего ценными фармакологическими свойствами. Способ заключается в том, что 7-метокси-нафталин-2-ол формулы (III) взаимодействует с этилортоформиатом в присутствии анилина с последующим гидролизом полученного промежуточного иминового соединения с получением соединения формулы (IV), затем соединение формулы (IV) подвергают реакции сульфонилирования, чтобы получить соединение формулы (V), где R означает -СН3 или толильную группу, и полученное соединение формулы (V) подвергают реакции дезоксигенирования в присутствии переходного металла и восстановителя, чтобы получить соединение формулы (I), которое выделяют в форме твердого вещества. Предлагаемый способ позволяет получить целевой продукт в соответствии с требованиями воспроизводимости, без использования трудоемкой очистки. Также настоящее изобретение относится к способу синтеза агомелатина, к соединению формулы (V), где R означает -СН3 или толильную группу, а также к применению соединения формулы (V) и соединения формулы (III) в синтезе соединения формулы (I). 5 н. и 17 з.п. ф-лы, 3 пр.
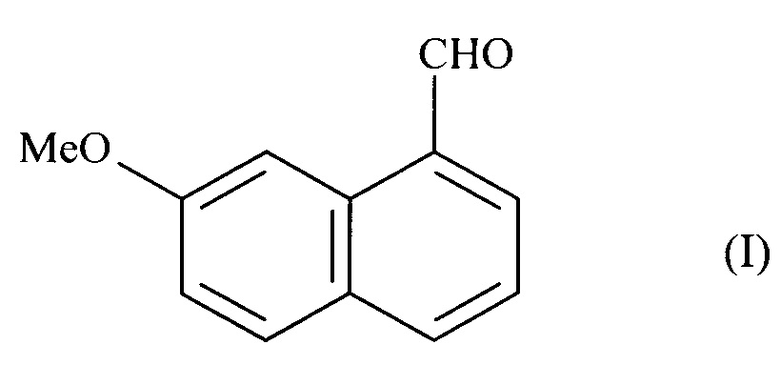
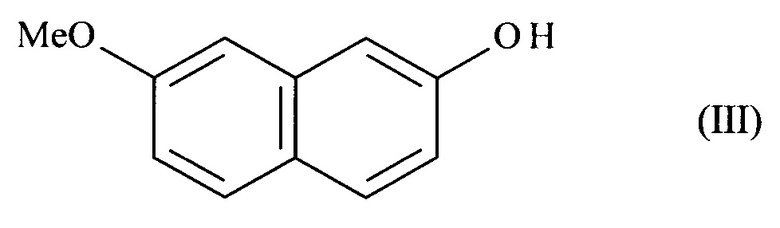
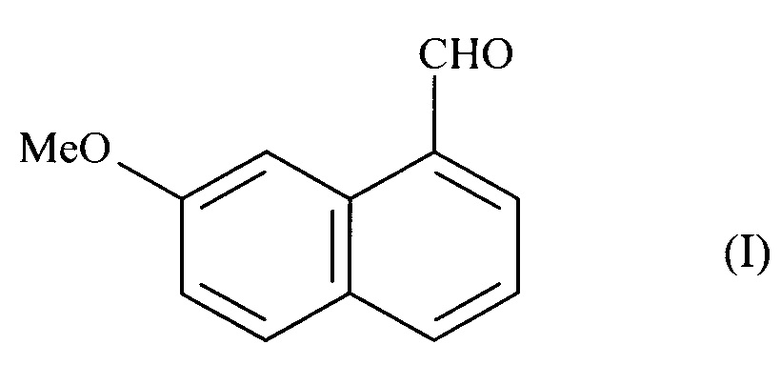
1. Способ промышленного синтеза соединения формулы (I):
который отличается тем, что 7-метокси-нафталин-2-ол формулы (III):
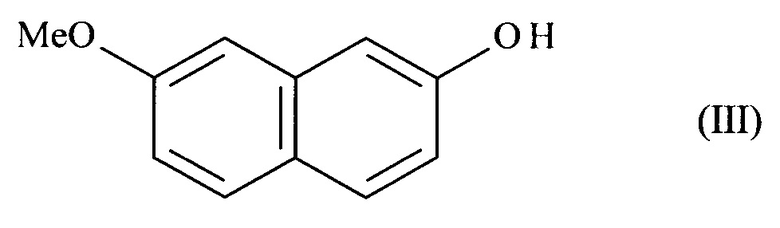
взаимодействует с этилортоформиатом в присутствии анилина с последующим гидролизом полученного промежуточного иминового соединения с получением соединения формулы (IV):
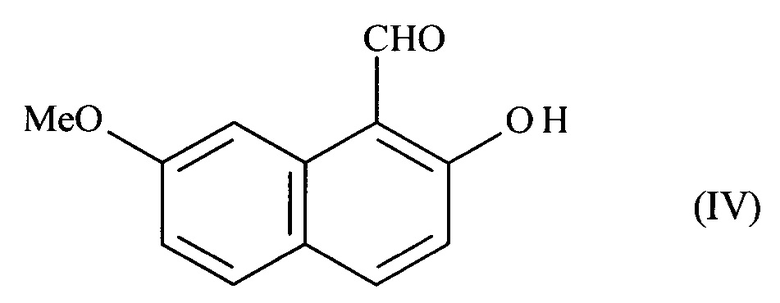
где соединение формулы (IV) подвергают реакции сульфонилирования, чтобы получить соединение формулы (V):
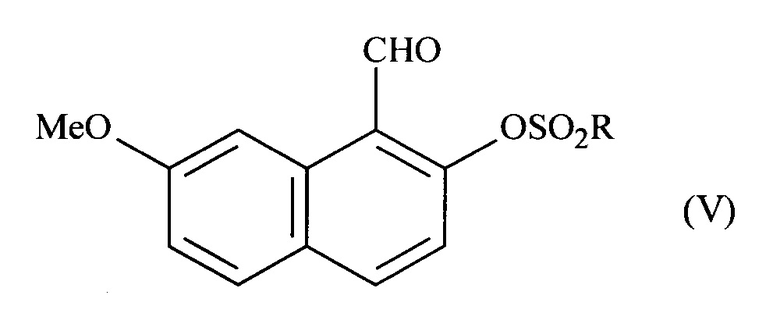
где R означает -СН3 или толильную группу;
где соединение формулы (V) подвергают реакции дезоксигенирования в присутствии переходного металла и восстановителя, чтобы получить соединение формулы (I), которое выделяют в форме твердого вещества.
2. Способ промышленного синтеза соединения формулы (I) по п. 1, который отличается тем, что R означает -СН3 или толильную группу.
3. Способ промышленного синтеза соединения формулы (I) по п. 1, который отличается тем, что преобразование соединения формулы (IV) в соединение формулы (V) проводят с помощью действия сульфонил хлорида, ангидрида сульфокислоты или сульфонимида.
4. Способ промышленного синтеза соединения формулы (I) по п. 3, который отличается тем, что преобразование соединения формулы (IV) в соединение формулы (V) проводят с помощью действия сульфонил хлорида.
5. Способ промышленного синтеза соединения формулы (I) по п. 1, который отличается тем, что в преобразовании соединения формулы (V) в соединение формулы (I) переходной металл представляет собой никель, палладий или платину.
6. Способ промышленного синтеза соединения формулы (I) по п. 1, который отличается тем, что в преобразовании соединения формулы (V) в соединение формулы (I) переходной металл представляет собой соль палладия.
7. Способ промышленного синтеза соединения формулы (I) по п. 1, который отличается тем, что преобразование соединения формулы (V) в соединение формулы (I) проводят в диметилформамиде, диоксане, тетрагидрофуране или толуоле.
8. Способ промышленного синтеза соединения формулы (I) по п. 7, который отличается тем, что преобразование соединения формулы (V) в соединение формулы (I) проводят в диметилформамиде.
9. Способ промышленного синтеза соединения формулы (I) по п. 1, который отличается тем, что преобразование соединения формулы (V) в соединение формулы (I) проводят между 25°С и 110°С.
10. Способ промышленного синтеза соединения формулы (I) по п. 9, который отличается тем, что преобразование соединения формулы (V) в соединение формулы (I) проводят между 40°С и 95°С.
11. Способ промышленного синтеза соединения формулы (I) по п. 1, который отличается тем, что в преобразовании соединения формулы (V) в соединение формулы (I) восстановитель представляет собой водород.
12. Способ промышленного синтеза соединения формулы (I) по п. 11, который отличается тем, что водород получают разложением формиата аммония.
13. Способ промышленного синтеза соединения формулы (I) по п. 1, который отличается тем, что преобразование соединения формулы (V) в соединение формулы (I) проводят в присутствии палладия и водорода.
14. Способ промышленного синтеза соединения формулы (I) по п. 1, который отличается тем, что преобразование соединения формулы (V) в соединение формулы (I) проводят в присутствии (9,9-диметил-9H-ксантан-4,5-диил)бис(дифенилфосфина) или 1,3-бис(дифенилфосфино)пропана.
15. Способ синтеза агомелатина, начиная с соединения формулы (V), который отличается тем, что соединение формулы (V) получают путем способа синтеза по любому из пп. 1-4.
16. Соединение формулы (V):
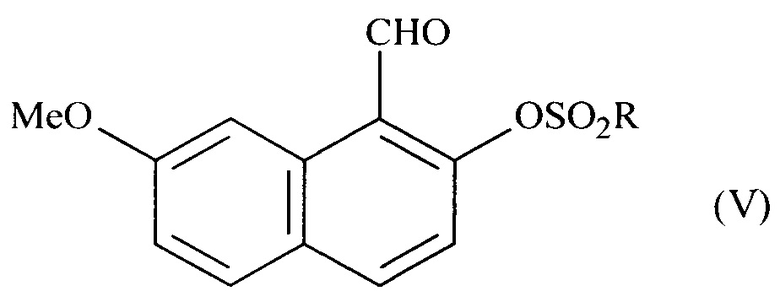
где R означает -СН3 или толильную группу;
для применения в качестве промежуточного соединения в синтезе соединения формулы (I) по п. 1.
17. Соединение формулы (V) по п. 16 для применения в качестве промежуточного соединения в синтезе агомелатина формулы (II) по п. 15:
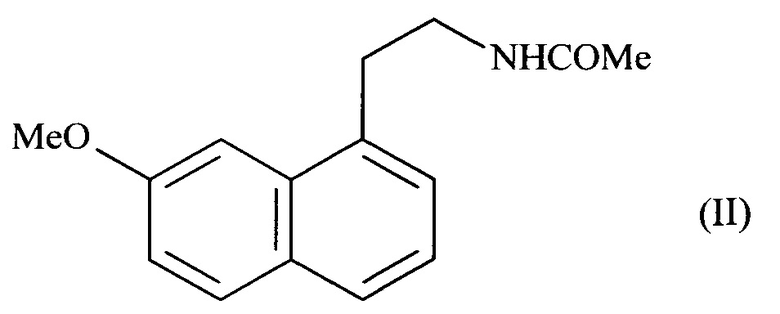
18. Соединение формулы (V) по п. 16 или 17, которое выбирают из следующих соединений:
- 1-формил-7-метоксинафталин-2-ил 4-метилбензолсульфонат;
- 1-формил-7-метоксинафталин-2-ил метансульфонат.
19. Применение соединения формулы (V):
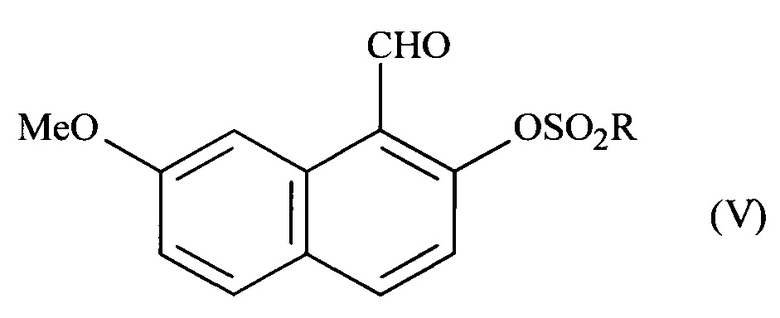
где R означает -СН3 или толильную группу;
в синтезе соединения формулы (I) по п. 1.
20. Применение соединения формулы (V) по п. 19 в синтезе агомелатина формулы (II) по п. 15:
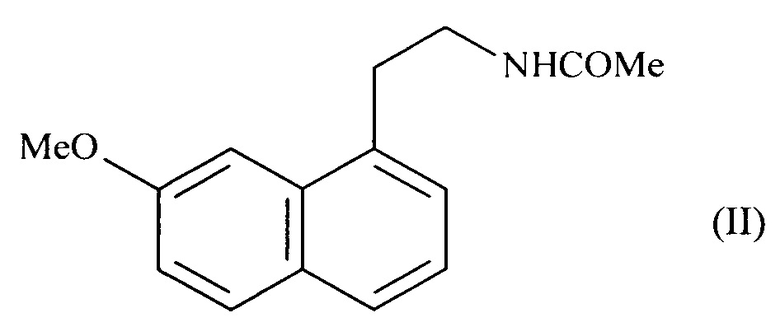
21. Применение соединения формулы (III)
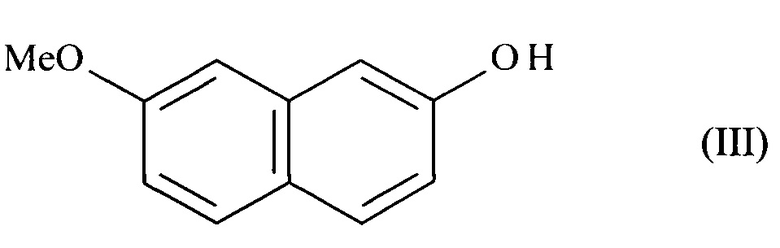
в синтезе соединения формулы (I) по п. 1.
22. Применение соединения формулы (III) по п. 21 в синтезе агомелатина формулы (II) по п. 15:
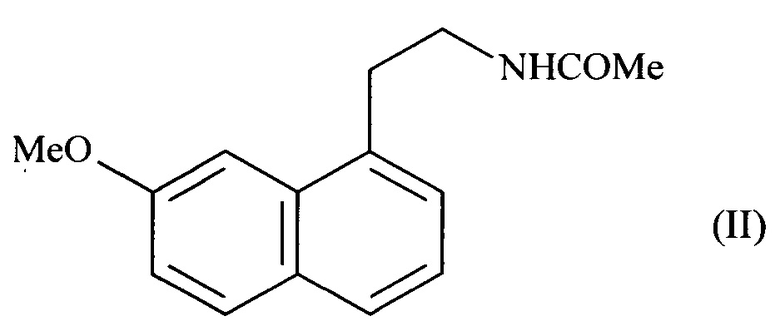
| Garigipati R.S | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Bioorganic & Medicinal Chemistry Letters, 1997, 7(11), 1421-1426 | |||
| FR 2918369 A1, 09.01.2009 | |||
| Kandagatla B | |||
| et al | |||
| A facile synthesis of melatonergic antidepressant agomelatine | |||
| Tetrahedron Letters, 2012, 53, 7125-7127 | |||
| СПОСОБ ПОЛУЧЕНИЯ СЕРНИСТЫХ КУБОВЫХ КРАСИТЕЛЕЙ | 1927 |
|
SU7787A1 |
Авторы
Даты
2019-02-19—Публикация
2014-12-04—Подача