ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к антисмысловому олигомеру, который вызывает пропуск экзона 55, 45, 50 или 44 в гене дистрофина человека, а также к фармацевтической композиции, включающей этот олигомер.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Мышечная дистрофия Дюшена (DMD) представляет собой наиболее распространенную форму наследственной прогрессирующей мышечной дистрофии, которая поражает примерно одного из 3500 новорожденных мальчиков. Хотя двигательные функции в младенчестве и детстве редко отличаются от здоровых людей, мышечная слабость у детей наблюдается, начиная примерно с 4-5-летнего возраста. Затем мышечная слабость прогрессирует вплоть до потери способности к передвижению в возрасте примерно 12 лет от роду и смерти из-за сердечной или дыхательной недостаточности в возрасте от 20 до 30 лет. Таким образом, DMD является тяжелым расстройством. В настоящее время не существует эффективных способов лечения DMD, и очень желательна разработка новых терапевтических агентов.
Известно, что причиной DMD является мутация в гене дистрофина. Ген дистрофина локализован на X хромосоме, представляя собой ген огромного размера, состоящий из 2,2 миллионов пар нуклеотидов. ДНК претерпевает транскрипцию в предшественников мРНК, после чего в результате сплайсинга происходит удаление интронов с образованием мРНК, в которой объединено 79 экзонов. Затем осуществляется трансляция этой мРНК с образованием аминокислотной последовательности из 3685 остатков, в результате чего формируется белок дистрофин. Дистрофин связан с поддержанием стабильности мембран мышечных клеток и необходим для того, чтобы сделать мышечные клетки менее хрупкими. Ген дистрофина у пациентов с DMD содержит мутацию, вследствие чего дистрофин, который функционирует в мышечных клетках, экспрессируется в недостаточной степени. Таким образом, в организме пациентов с DMD не поддерживается нормальная структура мышечных клеток, что приводит к значительному поступлению ионов кальция в мышечные клетки. Затем в качестве реакции на этот процесс появляется воспаление, которое способствует фиброзу, из-за которого затрудняется регенерация мышечных клеток.
Мышечная дистрофия Беккера (BMD) также вызвана мутацией в гене дистрофина. Симптомы этого заболевания включают мышечную слабость, сопровождающуюся атрофией мышц, но, как правило, мышечная слабость является умеренной и прогрессирует медленно по сравнению с DMD. Во многих случаях BMD начинается в зрелом возрасте. Считается, что причина различия клинических симптомов DMD и BMD заключается в том, прерывается ли мутацией рамка считывания, кодирующая аминокислоты, при трансляции мРНК дистрофина в соответствующий белок (непатентный документ 1). Более конкретно, при DMD имеются мутационные сдвиги рамки считывания аминокислот, вследствие чего прекращается экспрессия функционального дистрофина, тогда как при BMD вырабатывается дистрофин, который является функциональным, хотя и не полностью, поскольку сохраняется рамка считывания аминокислот, хотя часть экзонов пропущена из-за мутации.
Ожидается, что пропуск экзонов может являться способом лечения DMD. Этот способ включает модификацию сплайсинга для восстановления рамки считывания аминокислот мРНК дистрофина и стимулирование экспрессии дистрофина с частично восстановленными функциональными свойствами (непатентный документ 2). При этом часть аминокислотной последовательности, которая соответствует пропущенному экзону, будет потеряна. По этой причине дистрофин, который экспрессируется при описанном способе лечения, становится короче нормального, но, поскольку рамка считывания аминокислот сохраняется, у полученного белка частично остается способность стабилизировать мышечные клетки. Таким образом ожидается, что пропуск экзона приведет к DMD, с симптомами, аналогичными более мягким симптомам BMD. Подход, связанный с пропуском экзона, прошел тестирование на животных, в котором использовались мыши или собаки, и в настоящее время проходит клинические испытания на пациентах из числа людей с DMD.
Пропуск экзона можно вызвать нацеленным связыванием антисмысловых нуклеиновых кислот по любому 5' или 3' сайту сплайсинга, по обоим указанным сайтам, либо по внутренним участкам экзона. Экзон будет включен в мРНК, только если оба его сайта сплайсинга распознаны комплексом сплайсингосомы. Таким образом, пропуск экзона может быть вызван направленным взаимодействием сайтов сплайсинга с антисмысловыми нуклеиновыми кислотами. Кроме того, связывание SR белка с экзонным энхансером сплайсинга (ESE) считается необходимым для того, чтобы экзон был распознан механизмом сплайсинга. Соответственно, пропуск экзона можно вызвать направленным взаимодействием с ESE.
Поскольку мутации гена дистрофина могут быть различными у разных пациентов с DMD, необходимо разрабатывать антисмысловые нуклеиновые кислоты, исходя из участка или типа соответствующей мутации гена. В прошлом, антисмысловые нуклеиновые кислоты, которые вызывают пропуск экзона, для всех 79 экзонов производились Steve Wilton, et al., University of Western Australia (непатентный документ 3), и антисмысловые нуклеиновые кислоты, которые вызывают пропуск экзона для 39 экзонов, производились Annemieke Aartsma-Rus et al., Netherlands (непатентный документ 4).
Считается, что примерно 20% всех пациентов с DMD можно лечить посредством пропуска 55-го, 45-го, 50-го и 44-го экзонов (далее по тексту именуемых экзон 55, экзон 45, экзон 50 и экзон 44, соответственно). В последние годы несколько исследовательских организаций сообщали об исследованиях, в которых мишенями для пропуска являлись экзоны 55, 45, 50 или 44 гена дистрофина (патентные документы 1-8). Однако до сих пор не разработана достаточно эффективная методика пропуска экзонов 55, 45, 50 или 44.
Патентный документ 1: Международная публикация WO 2006/000057
Патентный документ 2: Международная публикация WO 2004/048570.
Патентный документ 3: Опубликованная нерассмотренная патентная заявка США US 2010/0168212.
Патентный документ 4: Международная публикация WO 2010/048586.
Патентный документ 5: Международная публикация WO 2004/083446.
Патентный документ 6: Международная публикация WO 2010/050801.
Патентный документ 7: Международная публикация WO 2009/139630.
Непатентный документ 1: Monaco A.P. et al., Genomics 1988; 2: p.90-95.
Непатентный документ 2: Matsuo M., Brain Dev 1996; 18: p.167-172.
Непатентный документ 3: Wilton S.D., et al., Molecular Therapy 2997: 15: p.1288-96.
Непатентный документ 4: Annemieke Aartsma-Rus et al. (2002) Neuromuscular Disorders 12: S71-S77.
Непатентный документ 5: Linda J. Popplewell et al., (2010) Neuromuscular Disorders, vol.20, no.2, p.102-10.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
В описанных выше обстоятельствах, желательно разработать антисмысловые олигомеры, которые эффективно вызывают пропуск экзона 55, экзона 45, экзона 50 или экзона 44 в гене дистрофина, а также средства для лечения мышечной дистрофии, включающие эти олигомеры.
В результате подробных исследований структуры гена дистрофина, авторы настоящего изобретения обнаружили, что пропуск экзона 55 в гене дистрофина можно с высокой эффективностью вызвать действием антисмысловых олигомеров, которые нацелены на последовательность, состоящую из примерно 1-го - 21-го, 11-го - 31-го и 14-го - 34-го нуклеотидов, считая от 5'-конца экзона 55 в предшественнике мРНК (далее по тексту именуемого "пре-мРНК").
Кроме того, авторы настоящего изобретения обнаружили, что пропуск экзона 45 в гене дистрофина можно с высокой эффективностью вызвать действием антисмысловых олигомеров, которые нацелены на последовательность, состоящую из примерно 1-го - 25-го и 6-го - 30-го нуклеотидов, считая от 5'-конца экзона 45 в пре-мРНК.
Далее, авторы настоящего изобретения обнаружили, что пропуск экзона 50 в гене дистрофина можно с высокой эффективностью вызвать действием антисмысловых олигомеров, которые нацелены на последовательность, состоящую из примерно 107-го - 127-го нуклеотидов, считая от 5'-конца экзона 50 в пре-мРНК.
Наконец, авторы настоящего изобретения установили, что пропуск экзона 44 в гене дистрофина можно с высокой эффективностью вызвать действием антисмысловых олигомеров, которые нацелены на последовательность, состоящую из примерно 11-го - 32-го и 26-го - 47-го нуклеотидов, считая от 5'-конца экзона 44 в пре-мРНК.
Исходя из этих данных, авторы завершили работу над настоящим изобретением.
Таким образом, в настоящем изобретении разработаны:
1. Антисмысловой олигомер, который вызывает пропуск 55-го экзона в гене дистрофина человека, состоящий из нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей, состоящих из -2-го - 19-го, -2-го - 20-го, -2-го - 21-го, -2-го - 22-го, -2-го - 23-го, -1-го - 19-го, -1-го - 20-го, -1-го - 21-го, -1-го - 22-го, -1-го - 23-го, 1-го - 19-го, 1-го - 20-го, 1-го - 21-го, 1-го - 22-го, 1-го - 23-го, 2-го - 19-го, 2-го - 20-го, 2-го - 21-го, 2-го - 22-го, 2-го -23-го, 3-го - 19-го, 3-го - 20-го, 3-го - 21-го, 3-го - 22-го, 3-го - 23-го, 9-го - 29-го, 9-го - 30-го, 9-го - 31-го, 9-го - 32-го, 9-го - 33-го, 10-го - 29-го, 10-го - 30-го, 10-го - 31-го, 10-го - 32-го, 10-го - 33-го, 11-го - 29-го, 11-го - 30-го, 11-го - 31-го, 11-го - 32-го, 11-го - 33-го, 12-го - 29-го, 12-го - 30-го, 12-го - 31-го, 12-го - 32-го, 12-го - 33-го, 13-го - 29-го, 13-го - 30-го, 13-го - 31-го, 13-го - 32-го, 13-го - 33-го, 12-го - 34-го, 12-го - 35-го, 12-го - 36-го, 13-го - 34-го, 13-го - 35-го, 13-го - 36-го, 14-го - 32-го, 14-го - 33-го, 14-го - 34-го, 14-го - 35-го, 14-го - 36-го, 15-го - 32-го, 15-го - 33-го, 15-го - 34-го, 15-го - 35-го, 15-го - 36-го, 16-го - 32-го, 16-го - 33-го, 16-го - 34-го, 16-го - 35-го или 16-го - 36-го нуклеотидов, считая от 5'-конца 55-го экзона гена дистрофина человека.
2. Антисмысловой олигомер, который вызывает пропуск 45-го экзона в гене дистрофина человека, состоящий из нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей, состоящих из -3-го - 19-го, -3-го - 20-го, -3-го - 21-го, -3-го - 22-го, -3-го - 23-го, -2-го - 19-го, -2-го - 20-го, -2-го - 21-го, -2-го - 22-го, -2-го - 23-го, -1-го - 19-го, -1-го - 20-го, -1-го - 21-го, -1-го - 22-го, -1-го - 23-го, 1-го - 19-го, 1-го - 20-го, 1-го - 21-го, 1-го - 22-го, 1-го - 23-го, 2-го - 19-го, 2-го - 20-го, 2-го - 21-го, 2-го - 22-го, 2-го - 23-го, -2-го - 24-го, -2-го - 25-го, -2-го - 26-го, -2-го - 27-го, -1-го - 24-го, -1-го - 25-го, -1-го - 26-го, -1-го - 27-го, 1-го - 24-го, 1-го - 25-го, 1-го - 26-го, 1-го - 27-го, 2-го - 24-го, 2-го - 25-го, 2-го - 26-го, 2-го - 27-го, 3-го - 23-го, 3-го - 24-го, 3-го - 25-го, 3-го - 26-го, 3-го - 27-го, 4-го - 28-го, 4-го - 29-го, 4-го - 30-го, 4-го - 31-го, 4-го - 32-го, 5-го - 28-го, 5-го - 29-го, 5-го - 30-го, 5-го - 31-го, 5-го - 32-го, 6-го - 28-го, 6-го - 29-го, 6-го - 30-го, 6-го - 31-го, 6-го - 32-го, 7-го - 28-го, 7-го - 29-го, 7-го - 30-го, 7-го - 31-го, 7-го - 32-го, 8-го - 28-го, 8-го - 29-го, 8-го - 30-го, 8-го - 31-го или 8-го - 32-го нуклеотидов, считая от 5'-конца 45-го экзона гена дистрофина человека.
3. Антисмысловой олигомер, который вызывает пропуск 50-го экзона в гене дистрофина человека, состоящий из нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей, состоящих из 105-го - 125-го, 105-го - 126-го, 105-го - 127-го, 105-го - 128-го, 105-го - 129-го, 106-го - 125-го, 106-го - 126-го, 106-го - 127-го, 106-го - 128-го, 106-го - 129-го, 107-го - 125-го, 107-го - 126-го, 107-го - 127-го, 107-го - 128-го, 107-го - 129-го, 108-го - 125-го, 108-го - 126-го, 108-го - 127-го, 108-го - 128-го, 108-го - 129-го, 109-го - 125-го, 109-го - 126-го, 109-го - 127-го, 109-го - 128-го или 109-го - 129-го нуклеотидов, считая от 5'-конца 50-го экзона гена дистрофина человека.
4. Антисмысловой олигомер, который вызывает пропуск 44-го экзона в гене дистрофина человека, состоящий из нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей, состоящих из 9-го - 30-го, 9-го - 31-го, 9-го - 32-го, 9-го - 33-го, 9-го - 34-го, 10-го - 30-го, 10-го - 31-го, 10-го - 32-го, 10-го - 33-го, 10-го - 34-го, 11-го - 30-го, 11-го - 31-го, 11-го - 32-го, 11-го - 33-го, 11-го - 34-го, 12-го - 30-го, 12-го - 31-го, 12-го - 32-го, 12-го - 33-го, 12-го - 34-го, 13-го - 30-го, 13-го - 31-го, 13-го - 32-го, 13-го - 33-го, 13-го - 34-го, 24-го - 45-го, 24-го - 46-го, 24-го - 47-го, 24-го - 48-го, 24-го - 49-го, 25-го - 45-го, 25-го - 46-го, 25-го - 47-го, 25-го - 48-го, 25-го - 49-го, 26-го - 45-го, 26-го - 46-го, 26-го - 47-го, 26-го - 48-го, 26-го - 49-го, 27-го - 45-го, 27-го - 46-го, 27-го - 47-го, 27-го - 48-го, 27-го - 49-го, 28-го - 45-го, 28-го - 46-го, 28-го - 47-го, 28-го - 48-го, 28-го - 49-го, 29-го - 45-го, 29-го - 46-го, 29-го - 47-го, 29-го - 48-го или 29-го - 49-го нуклеотидов, считая от 5'-конца 44-го экзона гена дистрофина человека.
5. Антисмысловой олигомер по п.1, который состоит из последовательности, комплементарной нуклеотидной последовательности, состоящей из 1-го - 21-го, 11-го - 31-го или 14-го - 34-го нуклеотидов, считая от 5'-конца 55-го экзона гена дистрофина человека.
6. Антисмысловой олигомер по п.1, состоящий из нуклеотидной последовательности, представленной любой последовательностью, выбранной из группы, состоящей из 170-го - 190-го, 160-го - 180-го и 157-го - 177-го нуклеотидов последовательности SEQ ID NO:5.
7. Антисмысловой олигомер по п.2, который состоит из последовательности, комплементарной нуклеотидной последовательности, состоящей из -2-го - 19-го, 1-го - 21-го, 1-го - 25-го или 6-го - 30-го нуклеотидов, считая от 5'-конца 45-го экзона гена дистрофина человека.
8. Антисмысловой олигомер по п.2, состоящий из нуклеотидной последовательности, представленной любой последовательностью, выбранной из группы, состоящей из 158-го - 178-го, 156-го - 176-го, 152-го - 176-го и 147-го - 171-го нуклеотидов последовательности SEQ ID NO:6.
9. Антисмысловой олигомер по п.3, который состоит из последовательности, комплементарной нуклеотидной последовательности, состоящей из 106-го - 126-го или 107-го - 127-го нуклеотидов, считая от 5'-конца 50-го экзона гена дистрофина человека.
10. Антисмысловой олигомер по п.3, состоящий из нуклеотидной последовательности, представленной любой последовательностью, выбранной из группы, состоящей из 4-го - 24-го и 3-го - 23-го нуклеотидов последовательности SEQ ID NO:7.
11. Антисмысловой олигомер по п.4, который состоит из последовательности, комплементарной нуклеотидной последовательности, состоящей из 11-го - 32-го, 25-го - 45-го, 26-го - 46-го, 26-го - 47-го или 27-го - 47-го нуклеотидов, считая от 5'-конца 44-го экзона гена дистрофина человека.
12. Антисмысловой олигомер по п.4, состоящий из нуклеотидной последовательности, представленной любой последовательностью, выбранной из группы, состоящей из 117-го - 138-го, 104-го - 124-го, 103-го - 123-го, 102-го - 123-го и 102-го - 122-го нуклеотидов последовательности SEQ ID NO:8.
13. Антисмысловой олигомер по любому из пп.1-12, который представляет собой олигонуклеотид.
14. Антисмысловой олигомер по п.13, где остаток сахара и/или область связывания с остатком фосфорной кислоты по меньшей мере одного нуклеотида, входящего в олигонуклеотид, подверглись модификации.
15. Антисмысловой олигомер по п.14, где остаток сахара по меньшей мере одного нуклеотида, входящего в олигонуклеотид, представляет собой рибозу, в которой группа 2'-OH замещена любым фрагментом, выбранным из группы, состоящей из OR, R, R'OR, SH, SR, NH2, NHR, NR2, N3, CN, F, Cl, Br и I (где R представляет собой алкил или арил, и R' представляет собой алкилен).
16. Антисмысловой олигомер по п.14 или 15, где область связывания с остатком фосфорной кислоты по меньшей мере одного нуклеотида, входящего в олигонуклеотид, представляет собой любой фрагмент, выбранный из группы, состоящей из фосфортиоатной связи, фосфордитиоатной связи, алкилфосфонатной связи, фосфорамидатной связи и боранфосфатной связи.
17. Антисмысловой олигомер по любому из пп.1-12, который представляет собой морфолино-олигомер.
18. Антисмысловой олигомер по п.17, который представляет собой фосфордиамидатный морфолино-олигомер.
19. Антисмысловой олигомер по п.17 или 18, где 5'-конец представляет собой любую из групп приведенных ниже химических формул (1)-(3):

20. Фармацевтическая композиция для лечения мышечной дистрофии, включающая в качестве действующего ингредиента антисмысловой олигомер по любому из пп.1-19 или его фармацевтически приемлемую соль или гидрат.
Антисмысловой олигомер по настоящему изобретению может с высокой эффективностью вызывать пропуск экзона 55, экзона 45, экзона 50 или экзона 44 в гене дистрофина человека. Кроме того, путем введения фармацевтической композиции по настоящему изобретению можно эффективно облегчать синдромы мышечной дистрофии Дюшена. Далее, поскольку антисмысловой олигомер по настоящему изобретению нацелен только на экзонные последовательности пациентов, эти целевые последовательности остаются неизменными у различных индивидуумов, по сравнению со случаями, когда целевые последовательности расположены в интронах. Таким образом, антисмысловой олигомер по настоящему изобретению позволяет добиваться отличной эффективности пропуска экзонов независимо от индивидуальной изменчивости (различий между пациентами). Более того, антисмысловой олигомер по настоящему изобретению имеет небольшую длину, равную 20 парам оснований или около того, и для него существует меньшая вероятность наличия мутаций, возникающих из-за индивидуальных различий (различий между пациентами), например SNP (однонуклеотидного полиморфизма), в целевых последовательностях, по сравнению с известными антисмысловыми олигомерами для лечения DMD, длина которых составляет 25 пар оснований или около того. Эта особенность также помогает антисмысловому олигомеру по настоящему изобретению достигать отличной эффективности пропуска экзонов, независимо от индивидуальной изменчивости (различий между пациентами). Кроме того, антисмысловой олигомер по настоящему изобретению вызывает меньше побочных эффектов, которые появляются из-за индукции цитокинов и т.п., поскольку антисмысловые олигомеры с более короткими цепями в целом имеют меньшую склонность вызывать реакцию иммунной системы.
Наконец, поскольку антисмысловой олигомер по настоящему изобретению является довольно коротким, стоимость его производства является относительно невысокой.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг.1 показана эффективность пропуска экзона 45 в гене дистрофина человека под действием 2'-OMe-S-РНК олигомера в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.2 показана эффективность пропуска экзона 45 в гене дистрофина человека под действием 2'-OMe-S-РНК олигомера в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.3 показана эффективность пропуска экзона 45 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.4 показана эффективность пропуска экзона 45 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.5 показана эффективность пропуска экзона 45 в гене дистрофина человека под действием PMO в клетках, в которых ген MyoD человека индуцирован в фибробласты, взятые у человека, больного DMD (клетки GM05017), чтобы вызвать их дифференцировку с образованием мышечных клеток.
На фиг.6 показана эффективность пропуска экзона 55 в гене дистрофина человека под действием 2'-OMe-S-РНК олигомера в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.7 показана эффективность пропуска экзона 55 в гене дистрофина человека под действием 2'-OMe-S-РНК олигомера в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.8 показана эффективность пропуска экзона 55 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.9 показана эффективность пропуска экзона 44 в гене дистрофина человека под действием 2'-OMe-S-РНК олигомера в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.10 показана эффективность пропуска экзона 44 в гене дистрофина человека под действием 2'-OMe-S-РНК олигомера в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.11 показана эффективность пропуска экзона 44 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.12 показана эффективность пропуска экзона 44 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.13 показана эффективность пропуска экзона 50 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.14 показана эффективность пропуска экзона 45 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.15 показана эффективность пропуска экзона 45 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.16 показана эффективность пропуска экзона 55 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.17 показана эффективность пропуска экзона 55 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.18 показана эффективность пропуска экзона 44 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.19 показана эффективность пропуска экзона 50 в гене дистрофина человека под действием PMO в клетках линии рабдомиосаркомы человека (клетках RD).
На фиг.20 показана эффективность пропуска экзона 44 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с делецией экзона 45 (клетки GM05112).
На фиг.21 показан эффект (Вестерн Блоттинг) пропуска экзона 44 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с делецией экзона 45 (клетки GM05112).
На фиг.22 показан эффект (RT-PCR) пропуска экзона 50 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с делецией экзона 45 (клетки GM05112).
На фиг.23 показана эффективность пропуска экзона 50 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с делецией экзона 45 (клетки GM05112).
На фиг.24 показан эффект (RT-PCR) пропуска экзона 55 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с делецией экзона 45 (клетки GM05112).
На фиг.25 показана эффективность пропуска экзона 55 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с делецией экзона 45 (клетки GM05112).
На фиг.26 показан эффект (RT-PCR) пропуска экзона 50 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с дупликацией экзонов 8-9 (клетки 11-0627).
На фиг.27 показана эффективность пропуска экзона 50 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с дупликацией экзонов 8-9 (клетки 11-0627).
На фиг.28 показан эффект (RT-PCR) пропуска экзона 50 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с делецией экзонов 51-55 (клетки GM04364).
На фиг.29 показана эффективность пропуска экзона 50 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с делецией экзонов 51-55 (клетки GM04364).
На фиг.30 показан эффект (RT-PCR) пропуска экзона 55 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с делецией экзона 54 (клетки 04-035).
На фиг.31 показана эффективность пропуска экзона 55 в гене дистрофина человека под действием PMO в фибробластах человека, больного DMD, с делецией экзона 54 (клетки 04-035).
НАИЛУЧШИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Далее по тексту приведено подробное описание настоящего изобретения. Имеется в виду, что описанные ниже варианты осуществления представлены только в качестве примеров для описания изобретения, но изобретение не ограничено только приведенными ниже вариантами. Настоящее изобретение можно реализовать различными путями, не отступая от сути изобретения.
Все упомянутые в настоящем описании публикации, опубликованные патентные заявки, патенты и другие патентные документы включены в описание в полном объеме посредством ссылок. В настоящее описание посредством ссылки включено содержание описания и иллюстративного материала патентной заявки Японии № 2011-288040, поданной 28 декабря 2011 года, и патентной заявки Японии № 2012-043092, поданной 29 февраля 2012 года, на основании которых осуществляется притязание на приоритет.
Далее по тексту приведено подробное описание настоящего изобретения. Имеется в виду, что описанные ниже варианты осуществления представлены только в качестве примеров для описания изобретения, но изобретение не ограничено только приведенными ниже вариантами. Настоящее изобретение можно реализовать различными путями, не отступая от сути изобретения.
Не вдаваясь в конкретные детали, амино-конец аминокислотной последовательности отображается с левой стороны, а карбокси-конец - с правой, и 5'-конец нуклеотидной последовательности отображается с левой стороны, а 3'-конец - с правой.
1. Антисмысловой олигомер
Настоящее изобретение относится к антисмысловому олигомеру (далее по тексту именуемому "олигомер, способствующий пропуску экзона 55 по настоящему изобретению"), который вызывает пропуск экзона 55 в гене дистрофина человека, состоящему из нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей (далее по тексту также именуемых "целевыми последовательностями экзона 55"), состоящих из -2-го - 19-го, -2-го - 20-го, -2-го - 21-го, -2-го - 22-го, -2-го - 23-го, -1-го - 19-го, -1-го - 20-го, -1-го - 21-го, -1-го - 22-го, -1-го - 23-го, 1-го - 19-го, 1-го - 20-го, 1-го - 21-го, 1-го - 22-го, 1-го - 23-го, 2-го - 19-го, 2-го - 20-го, 2-го - 21-го, 2-го - 22-го, 2-го - 23-го, 3-го - 19-го, 3-го - 20-го, 3-го - 21-го, 3-го - 22-го, 3-го - 23-го, 9-го - 29-го, 9-го - 30-го, 9-го - 31-го, 9-го - 32-го, 9-го - 33-го, 10-го - 29-го, 10-го - 30-го, 10-го - 31-го, 10-го - 32-го, 10-го - 33-го, 11-го - 29-го, 11-го - 30-го, 11-го - 31-го, 11-го - 32-го, 11-го - 33-го, 12-го - 29-го, 12-го - 30-го, 12-го - 31-го, 12-го - 32-го, 12-го - 33-го, 13-го - 29-го, 13-го - 30-го, 13-го - 31-го, 13-го - 32-го, 13-го - 33-го, 12-го - 34-го, 12-го - 35-го, 12-го - 36-го, 13-го - 34-го, 13-го - 35-го, 13-го - 36-го, 14-го - 32-го, 14-го - 33-го, 14-го - 34-го, 14-го - 35-го, 14-го - 36-го, 15-го - 32-го, 15-го - 33-го, 15-го - 34-го, 15-го - 35-го, 15-го - 36-го, 16-го - 32-го, 16-го - 33-го, 16-го - 34-го, 16-го - 35-го или 16-го - 36-го нуклеотидов, считая от 5'-конца 55-го экзона гена дистрофина человека.
Кроме того, настоящее изобретение относится к антисмысловому олигомеру (далее по тексту именуемому "олигомер, способствующий пропуску экзона 45 по настоящему изобретению"), который вызывает пропуск экзона 45 в гене дистрофина человека, состоящему из нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей (далее по тексту также именуемых "целевыми последовательностями экзона 45"), состоящих из -3-го - 19-го, -3-го - 20-го, -3-го - 21-го, -3-го - 22-го, -3-го - 23-го, -2-го - 19-го, -2-го - 20-го, -2-го - 21-го, -2-го - 22-го, -2-го - 23-го, -1-го - 19-го, -1-го - 20-го, -1-го - 21-го, -1-го - 22-го, -1-го - 23-го, 1-го - 19-го, 1-го - 20-го, 1-го - 21-го, 1-го - 22-го, 1-го - 23-го, 2-го - 19-го, 2-го - 20-го, 2-го - 21-го, 2-го - 22-го, 2-го - 23-го, -2-го - 24-го, -2-го - 25-го, -2-го - 26-го, -2-го - 27-го, -1-го - 24-го, -1-го - 25-го, -1-го - 26-го, -1-го - 27-го, 1-го - 24-го, 1-го - 25-го, 1-го - 26-го, 1-го - 27-го, 2-го - 24-го, 2-го - 25-го, 2-го - 26-го, 2-го - 27-го, 3-го - 23-го, 3-го - 24-го, 3-го - 25-го, 3-го - 26-го, 3-го - 27-го, 4-го - 28-го, 4-го - 29-го, 4-го - 30-го, 4-го - 31-го, 4-го - 32-го, 5-го - 28-го, 5-го - 29-го, 5-го - 30-го, 5-го - 31-го, 5-го - 32-го, 6-го - 28-го, 6-го - 29-го, 6-го - 30-го, 6-го - 31-го, 6-го - 32-го, 7-го - 28-го, 7-го - 29-го, 7-го - 30-го, 7-го - 31-го, 7-го - 32-го, 8-го - 28-го, 8-го - 29-го, 8-го - 30-го, 8-го - 31-го или 8-го - 32-го нуклеотидов, считая от 5'-конца 45-го экзона гена дистрофина человека.
Далее, настоящее изобретение относится к антисмысловому олигомеру (далее по тексту именуемому "олигомер, способствующий пропуску экзона 50 по настоящему изобретению"), который вызывает пропуск экзона 50 в гене дистрофина человека, состоящему из нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей (далее по тексту также именуемых "целевыми последовательностями экзона 50"), состоящих из 105-го - 125-го, 105-го - 126-го, 105-го - 127-го, 105-го - 128-го, 105-го - 129-го, 106-го - 125-го, 106-го - 126-го, 106-го - 127-го, 106-го - 128-го, 106-го - 129-го, 107-го - 125-го, 107-го - 126-го, 107-го - 127-го, 107-го - 128-го, 107-го - 129-го, 108-го - 125-го, 108-го - 126-го, 108-го - 127-го, 108-го - 128-го, 108-го - 129-го, 109-го - 125-го, 109-го - 126-го, 109-го - 127-го, 109-го - 128-го или 109-го - 129-го нуклеотидов, считая от 5'-конца 50-го экзона гена дистрофина человека.
Помимо этого, настоящее изобретение относится к антисмысловому олигомеру (далее по тексту именуемому "олигомер, способствующий пропуску экзона 44 по настоящему изобретению"), который вызывает пропуск экзона 44 в гене дистрофина человека, состоящему из нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей (далее по тексту также именуемых "целевыми последовательностями экзона 44"), состоящих из 9-го - 30-го, 9-го - 31-го, 9-го - 32-го, 9-го - 33-го, 9-го - 34-го, 10-го - 30-го, 10-го - 31-го, 10-го - 32-го, 10-го - 33-го, 10-го - 34-го, 11-го - 30-го, 11-го - 31-го, 11-го - 32-го, 11-го - 33-го, 11-го - 34-го, 12-го - 30-го, 12-го - 31-го, 12-го - 32-го, 12-го - 33-го, 12-го - 34-го, 13-го - 30-го, 13-го - 31-го, 13-го - 32-го, 13-го - 33-го, 13-го - 34-го, 24-го - 45-го, 24-го - 46-го, 24-го - 47-го, 24-го - 48-го, 24-го - 49-го, 25-го - 45-го, 25-го - 46-го, 25-го - 47-го, 25-го - 48-го, 25-го - 49-го, 26-го - 45-го, 26-го - 46-го, 26-го - 47-го, 26-го - 48-го, 26-го - 49-го, 27-го - 45-го, 27-го - 46-го, 27-го - 47-го, 27-го - 48-го, 27-го - 49-го, 28-го - 45-го, 28-го - 46-го, 28-го - 47-го, 28-го - 48-го, 28-го - 49-го, 29-го - 45-го, 29-го - 46-го, 29-го - 47-го, 29-го - 48-го или 29-го - 49-го нуклеотидов, считая от 5'-конца 44-го экзона гена дистрофина человека.
Далее по тексту олигомеры, способствующие пропуску экзонов 55, 45, 50 и 44, могут совместно именоваться "олигомерами по настоящему изобретению".
Экзоны 55, 45, 50 и 44 в гене дистрофина человека
Имеется в виду, что в настоящем изобретении термин "ген" означает геномный хромосомный ген, а также включает кДНК, предшественника мРНК и РНК. Предпочтительно "ген" означает предшественника мРНК, т.е. пре-мРНК.
В геноме человека ген дистрофина человека локализован в локусе Xp21.2. Ген дистрофина человека имеет размер 3,0 Mbp и является самым крупным геном среди известных человеческих генов. Однако размер кодирующих областей гена дистрофина человека составляет только 14 Kb, разделенных на 79 экзонов, находящихся в гене дистрофина человека (Roberts, RG, et al., Genomics, 16: 536-538 (1993)). Пре-мРНК, которая является транскриптом гена дистрофина человека, подвергается сплайсингу с образованием зрелой мРНК размером 14 Kb. Известна нуклеотидная последовательность гена дистрофина человека дикого типа (учетный номер GeneBank NM_004006).
Нуклеотидная последовательность, состоящая из -2-го - 190-го нуклеотидов, считая от 5'-конца экзона 55 в гене дистрофина человека, дикого типа представлена последовательностью SEQ ID NO:1. Нуклеотидная последовательность, состоящая из -3-го - 176-го нуклеотидов, считая от 5'-конца экзона 45 в гене дистрофина человека, дикого типа представлена последовательностью SEQ ID NO:2. Нуклеотидная последовательность, состоящая из 1-го - 109-го нуклеотидов, считая от 5'-конца экзона 50, и 1-го - 20-го нуклеотидов, считая от 5'-конца интрона 50, в гене дистрофина человека, дикого типа представлена последовательностью SEQ ID NO:3.
Нуклеотидная последовательность, состоящая из 1-го - 148-го нуклеотидов, считая от 5'-конца экзона 44 в гене дистрофина человека, дикого типа представлена последовательностью SEQ ID NO:4.
Олигомер по настоящему изобретению предназначен для того, чтобы вызывать пропуск экзона 55, 45, 50 или 44 в гене дистрофина человека, тем самым превращая белок, закодированный геном дистрофина DMD-типа, в дистрофин BMD-типа. Соответственно, экзоны 55, 45, 50 и 44 в гене дистрофина, которые являются мишенями пропуска экзонов под действием олигомера по настоящему изобретению, включают как последовательности дикого типа, так и мутантные последовательности.
Конкретно, мутанты экзонов 55, 45, 50 и 44 гена дистрофина человека представляют собой полинуклеотиды, определенные ниже по тексту в пунктах (a) или (b):
(a) полинуклеотид, который в жестких условиях гибридизуется с полинуклеотидом, состоящим из последовательности нуклеотидов, комплементарной последовательности SEQ ID NO:1 (или последовательности, состоящей из 3-го - 192-го нуклеотидов последовательности SEQ ID NO:1), SEQ ID NO:2 (или последовательности, состоящей из 4-го - 179-го нуклеотидов последовательности SEQ ID NO:2), SEQ ID NO:3 (или последовательности, состоящей из 1-го - 109-го нуклеотидов последовательности SEQ ID NO:3) или SEQ ID NO:4;
(b) полинуклеотид, состоящий из последовательности нуклеотидов, обладающей по меньшей мере 90% гомологией с последовательностью SEQ ID NO:1 (или последовательностью, состоящей из 3-го - 192-го нуклеотидов последовательности SEQ ID NO:1), SEQ ID NO:2 (или последовательностью, состоящей из 4-го - 179-го нуклеотидов последовательности SEQ ID NO:2), SEQ ID NO:3 (или последовательностью, состоящей из 1-го - 109-го нуклеотидов последовательности SEQ ID NO:3) или SEQ ID NO:4.
В настоящей заявке термин "полинуклеотид" предназначен для обозначения ДНК или РНК.
В настоящей заявке термин "полинуклеотид, который гибридизуется в жестких условиях" относится, например, к полинуклеотиду, полученному гибридизацией колоний, гибридизацией бляшек, Саузерн-гибридизацией или подобными способами, с использованием в качестве зонда части полинуклеотида или целого полинуклеотида, состоящего из последовательности нуклеотидов, комплементарной последовательности SEQ ID NO:1 (или последовательности, состоящей из 3-го - 192-го нуклеотидов последовательности SEQ ID NO:1), SEQ ID NO:2 (или последовательности, состоящей из 4-го - 179-го нуклеотидов последовательности SEQ ID NO:2), SEQ ID NO:3 (или последовательности, состоящей из 1-го - 109-го нуклеотидов последовательности SEQ ID NO:3) или SEQ ID NO:4. Подходящие методики гибридизации включают методики, описанные, например, в "Sambrook & Russell, Molecular Cloning: A Laboratory Manual Vol.3, Cold Spring Harbor, Laboratory Press 2001", "Ausubel, Current Protocols in Molecular Biology, John Wiley & Sons 1987-1997" и т.д.
В настоящей заявке термин "комплементарная нуклеотидная последовательность" не ограничен только нуклеотидными последовательностями, которые образуют пары Уотсона-Крика с целевыми нуклеотидными последовательностями, но предназначен также для указания на нуклеотидные последовательности, которые образуют неоднозначные пары оснований. В настоящей заявке термин "пара Уотсона-Крика" относится к паре нуклеиновых оснований, в которой водородные связи образованы между аденином-тимином, аденином-урацилом или гуанином-цитозином, и термин "неоднозначные пары оснований" относится к парам нуклеиновых оснований, в которых водородные связи образуются между гуанином-урацилом, инозином-урацилом, инозином-аденином или инозином-цитозином. В настоящей заявке термин "комплементарная нуклеотидная последовательность" относится не только к нуклеотидной последовательности, которая на 100% комплементарна целевой нуклеотидной последовательности, но и к комплементарной нуклеотидной последовательности, которая может содержать, например, от 1 до 3 или от 1 до 2, или один нуклеотид, не комплементарный целевой нуклеотидной последовательности.
В настоящей заявке термин "жесткие условия" может относится к любому уровню жесткости, т.е. условиям низкой жесткости, условиям умеренной жесткости или условиям высокой жесткости. Термин "условия низкой жесткости" относится, например, к следующим условиям 5×SSC, 5× раствор Денхардта, 0,5% SDS, 50% формамид при 32°C. Термин "условия умеренной жесткости" относится, например, к следующим условиям 5×SSC, 5× раствор Денхардта, 0,5% SDS, 50% формамид при 42°C или 5×SSC, 1% SDS, 50 мМ Tris-HCl (pH 7,5), 50% формамид при 42°C. Термин "условия высокой жесткости" относится, например, к следующим условиям 5×SSC, 5× раствор Денхардта, 0,5% SDS, 50% формамид при 50°C или 0,2×SSC, 0,1% SDS при 65°C. Ожидается, что в этих условиях полинуклеотиды с более высокой степенью гомологичности будут более эффективно взаимодействовать при более высоких температурах, хотя жесткость условий гибридизации определяется многими факторами, в том числе температурой, концентрацией зонда, длиной зонда, ионной силой, временем, концентрацией солей и прочими, и специалист в данной области техники может приблизительно подобрать перечисленные факторы для достижения аналогичной жесткости условий.
Если для гибридизации применяются коммерчески доступные наборы, можно использовать, например, Alkphos Direct Labelling and Detection System (GE Healthcare). В этом случае, согласно приложенному к набору протоколу, после культивирования с меченым зондом в течение ночи, мембрану промывают первичным буфером для промывания, содержащим 0,1% (масса/объем) SDS при 55°C, выявляя гибридизованные полинуклеотиды. В качестве альтернативы, если зонд мечен дигоксигенином (DIG) с использованием коммерчески доступного реагента (например, PCR Labelling Mix (Roche Diagnostics) и т.д.) при получении зонда на основе всей или части последовательности, комплементарной нуклеотидной последовательности SEQ ID NO:1 (или последовательности, состоящей из 3-го - 192-го нуклеотидов последовательности SEQ ID NO:1), SEQ ID NO:2 (или последовательности, состоящей из 4-го - 179-го нуклеотидов последовательности SEQ ID NO:2), SEQ ID NO:3 (или последовательности, состоящей из 1-го - 109-го нуклеотидов последовательности SEQ ID NO:3) или SEQ ID NO:4, гибридизацию можно обнаружить с помощью набора DIG Nucleic Acid Detection Kit (Roche Diagnostics).
Помимо описанных выше полинуклеотидов, другие полинуклеотиды, которые могут участвовать в гибридизации, включают полинуклеотиды, имеющие степень идентичности 90% или более, 91% или более, 92% или более, 93% или более, 94% или более, 95% или более, 96% или более, 97% или более, 98% или более, 99% или более, 99,1% или более, 99,2% или более, 99,3% или более, 99,4% или более, 99,5% или более, 99,6% или более, 99,7% или более, 99,8% или более, 99,9% или более с полинуклеотидом, имеющим последовательность SEQ ID NO:1 (или последовательность, состоящую из 3-го - 192-го нуклеотидов последовательности SEQ ID NO:1), SEQ ID NO:2 (или последовательность, состоящую из 4-го - 179-го нуклеотидов последовательности SEQ ID NO:2), SEQ ID NO:3 (или последовательность, состоящую из 1-го - 109-го нуклеотидов последовательности SEQ ID NO:3) или SEQ ID NO:4, вычисленную с помощью программы для поиска гомологии BLAST с использованием параметров по умолчанию.
Идентичность нуклеотидных последовательностей можно определить с использованием алгоритма BLAST (Basic Local Alignment Search Tool - Средство поиска на основе локальных выравниваний), разработанного Karlin и Altschul (Proc.Natl.Acad.Sci. USA 872264-2268, 1990; Proc.Natl.Acad.Sci USA 90:5873, 1993). На основе алгоритма BLAST были разработаны программы BLASTN и BLASTX (Altschul SF, et al.: J.Mol.Biol.215: 403, 1990). При исследовании нуклеотидной последовательности с использованием BLASTN используются, например, следующие параметры сумма=100 и длина слова=12. При использовании программ BLAST и Gapped BLAST применяются параметры по умолчанию каждой из программ.
Последовательность, комплементарная нуклеотидной последовательности, состоящей из -2-го - 190-го нуклеотидов, считая от 5'-конца экзона 55, представлена последовательностью SEQ ID NO:5. В данном случае последовательность, состоящая из -2 - -1 нуклеотидов, считая с 5'-конца экзона 55 (нуклеотидная последовательность, состоящая из 1-го и 2-го нуклеотидов SEQ ID NO:1), представляет собой нуклеотидную последовательность, состоящую из 2 нуклеотидов, находящихся в направлении 5'-3' от самого 3'-конца интрона 54, который находится между экзоном 54 и экзоном 55. Более конкретно, нуклеотидная последовательность экзона 55 представляет собой последовательность, состоящую из 3-го - 192-го нуклеотидов SEQ ID NO:1, и последовательность, комплементарная экзону 55, представляет собой последовательность, состоящую из 1-го - 190-го нуклеотидов SEQ ID NO:5.
В данном случае последовательность, комплементарная нуклеотидной последовательности, состоящей из -2-го - 19-го, -2-го - 20-го, -2-го - 21-го, -2-го - 22-го, -2-го - 23-го, -1-го - 19-го, -1-го - 20-го, -1-го - 21-го, -1-го - 22-го, -1-го - 23-го, 1-го - 19-го, 1-го - 20-го, 1-го - 21-го, 1-го - 22-го, 1-го - 23-го, 2-го - 19-го, 2-го - 20-го, 2-го - 21-го, 2-го - 22-го, 2-го - 23-го, 3-го - 19-го, 3-го - 20-го, 3-го - 21-го, 3-го - 22-го, 3-го - 23-го, 9-го - 29-го, 9-го - 30-го, 9-го - 31-го, 9-го - 32-го, 9-го - 33-го, 10-го - 29-го, 10-го - 30-го, 10-го - 31-го, 10-го - 32-го, 10-го - 33-го, 11-го - 29-го, 11-го - 30-го, 11-го - 31-го, 11-го - 32-го, 11-го - 33-го, 12-го - 29-го, 12-го - 30-го, 12-го - 31-го, 12-го - 32-го, 12-го - 33-го, 13-го - 29-го, 13-го - 30-го, 13-го - 31-го, 13-го - 32-го, 13-го - 33-го, 12-го - 34-го, 12-го - 35-го, 12-го - 36-го, 13-го - 34-го, 13-го - 35-го, 13-го - 36-го, 14-го - 32-го, 14-го - 33-го, 14-го - 34-го, 14-го - 35-го, 14-го - 36-го, 15-го - 32-го, 15-го - 33-го, 15-го - 34-го, 15-го - 35-го, 15-го - 36-го, 16-го - 32-го, 16-го - 33-го, 16-го - 34-го, 16-го - 35-го или 16-го - 36-го нуклеотидов, считая от 5'-конца 55-го экзона гена дистрофина человека, соответственно идентична нуклеотидной последовательности, состоящей из 172-го - 192-го, 171-го - 192-го, 170-го - 192-го, 169-го - 192-го, 168-го - 192-го, 172-го - 191-го, 171-го - 191-го, 170-го - 191-го, 169-го - 191-го, 168-го - 191-го, 172-го - 190-го, 171-го - 190-го, 170-го - 190-го, 169-го - 190-го, 168-го - 190-го, 172-го - 189-го, 171-го - 189-го, 170-го - 189-го, 169-го - 189-го, 168-го - 189-го, 172-го - 188-го, 171-го - 188-го, 170-го - 188-го, 169-го - 188-го, 168-го - 188-го, 162-го - 182-го, 161-го - 182-го, 160-го - 182-го, 159-го - 182-го, 158-го - 182-го, 162-го - 181-го, 161-го - 181-го, 160-го - 181-го, 159-го - 181-го, 158-го - 181-го, 162-го - 180-го, 161-го - 180-го, 160-го - 180-го, 159-го - 180-го, 158-го - 180-го, 162-го - 179-го, 161-го - 179-го, 160-го - 179-го, 159-го - 179-го, 158-го - 179-го, 162-го - 178-го, 161-го - 178-го, 160-го - 178-го, 159-го - 178-го, 158-го - 178-го, 157-го - 179-го, 156-го - 179-го, 155-го - 179-го, 157-го - 178-го, 156-го - 178-го, 155-го - 178-го, 159-го - 177-го, 158-го - 177-го, 157-го - 177-го, 156-го - 177-го, 155-го - 177-го, 159-го - 176-го, 158-го - 176-го, 157-го - 176-го, 156-го - 176-го, 155-го - 176-го, 159-го - 175-го, 158-го - 175-го, 157-го - 175-го, 156-го - 175-го или 155-го - 175-го нуклеотидов SEQ ID NO:5.
Последовательность, комплементарная нуклеотидной последовательности, состоящей из -3-го - 176-го нуклеотидов, считая от 5'-конца экзона 45, представлена последовательностью SEQ ID NO:6. В данном случае последовательность, состоящая из -3 - -1 нуклеотидов, считая с 5'-конца экзона 45 (нуклеотидная последовательность, состоящая из 1-го - 3-го нуклеотидов SEQ ID NO:2), представляет собой нуклеотидную последовательность, состоящую из 3 нуклеотидов, находящихся в направлении 5'-3' от самого 3'-конца интрона 44, который находится между экзоном 44 и экзоном 45. Более конкретно, нуклеотидная последовательность экзона 45 представляет собой последовательность, состоящую из 4-го - 179-го нуклеотидов SEQ ID NO:2, и последовательность, комплементарная экзону 45, представляет собой последовательность, состоящую из 1-го - 176-го нуклеотидов SEQ ID NO:6.
В данном случае последовательность, комплементарная нуклеотидной последовательности, состоящей из -3-го - 19-го, -3-го - 20-го, -3-го - 21-го, -3-го - 22-го, -3-го - 23-го, -2-го - 19-го, -2-го - 20-го, -2-го - 21-го, -2-го - 22-го, -2-го - 23-го, -1-го - 19-го, -1-го - 20-го, -1-го - 21-го, -1-го - 22-го, -1-го - 23-го, 1-го - 19-го, 1-го - 20-го, 1-го - 21-го, 1-го - 22-го, 1-го - 23-го, 2-го - 19-го, 2-го - 20-го, 2-го - 21-го, 2-го - 22-го, 2-го - 23-го, -2-го - 24-го, -2-го - 25-го, -2-го - 26-го, -2-го - 27-го, -1-го - 24-го, -1-го - 25-го, -1-го - 26-го, -1-го - 27-го, 1-го - 24-го, 1-го - 25-го, 1-го - 26-го, 1-го - 27-го, 2-го - 24-го, 2-го - 25-го, 2-го - 26-го, 2-го - 27-го, 3-го - 23-го, 3-го - 24-го, 3-го - 25-го, 3-го - 26-го, 3-го - 27-го, 4-го - 28-го, 4-го - 29-го, 4-го - 30-го, 4-го - 31-го, 4-го - 32-го, 5-го - 28-го, 5-го - 29-го, 5-го - 30-го, 5-го - 31-го, 5-го - 32-го, 6-го - 28-го, 6-го - 29-го, 6-го - 30-го, 6-го - 31-го, 6-го - 32-го, 7-го - 28-го, 7-го - 29-го, 7-го - 30-го, 7-го - 31-го, 7-го - 32-го, 8-го - 28-го, 8-го - 29-го, 8-го - 30-го, 8-го - 31-го или 8-го - 32-го нуклеотидов, считая от 5'-конца 45-го экзона гена дистрофина человека, соответственно идентична нуклеотидной последовательности, состоящей из 158-го - 179-го, 157-го - 179-го, 156-го - 179-го, 155-го - 179-го, 154-го - 179-го, 158-го - 178-го, 157-го - 178-го, 156-го - 178-го, 155-го - 178-го, 154-го - 178-го, 158-го - 177-го, 157-го - 177-го, 156-го - 177-го, 155-го - 177-го, 154-го - 177-го, 158-го - 176-го, 157-го - 176-го, 156-го - 176-го, 155-го - 176-го, 154-го - 176-го, 158-го - 175-го, 157-го - 175-го, 156-го - 175-го, 155-го - 175-го, 154-го - 175-го, 153-го - 178-го, 152-го - 178-го, 151-го - 178-го, 150-го - 178-го, 153-го - 177-го, 152-го - 177-го, 151-го - 177-го, 150-го - 177-го, 153-го - 176-го, 152-го - 176-го, 151-го - 176-го, 150-го - 176-го, 153-го - 175-го, 152-го - 175-го, 151-го - 175-го, 150-го - 175-го, 154-го - 174-го, 153-го - 174-го, 152-го - 174-го, 151-го - 174-го, 150-го - 174-го, 149-го - 173-го, 148-го - 173-го, 147-го - 173-го, 146-го - 173-го, 147-го - 173-го, 149-го - 172-го, 148-го - 172-го, 147-го - 172-го, 146-го - 172-го, 145-го - 172-го, 149-го - 171-го, 148-го - 171-го, 147-го - 171-го, 146-го - 171-го, 145-го - 171-го, 149-го - 170-го, 148-го - 170-го, 147-го - 170-го, 146-го - 170-го, 145-го - 170-го, 149-го - 169-го, 148-го - 169-го, 147-го - 169-го, 146-го - 169-го или 145-го - 169-го нуклеотидов SEQ ID NO:6.
Последовательность, комплементарная нуклеотидной последовательности, состоящей из 1-го - 109-го нуклеотидов, считая от 5'-конца экзона 50, и 1-го - 20-го нуклеотидов, считая от 5'-конца интрона 50, представлена последовательностью SEQ ID NO:7. В данном случае последовательность, состоящая из 1-20 нуклеотидов, считая с 5'-конца интрона 50 (нуклеотидная последовательность, состоящая из 110-го - 129-го нуклеотидов SEQ ID NO:3), представляет собой нуклеотидную последовательность, состоящую из 20 нуклеотидов, находящихся в направлении 3'-5' от самого 5'-конца интрона 50, который находится между экзоном 50 и экзоном 51. Более конкретно, нуклеотидная последовательность экзона 50 представляет собой последовательность, состоящую из 1-го - 109-го нуклеотидов SEQ ID NO:3, и последовательность, комплементарная экзону 50, представляет собой последовательность, состоящую из 21-го - 129-го нуклеотидов SEQ ID NO:7.
В данном случае последовательность, комплементарная нуклеотидной последовательности, состоящей из 105-го - 125-го, 105-го - 126-го, 105-го - 127-го, 105-го - 128-го, 105-го - 129-го, 106-го - 125-го, 106-го - 126-го, 106-го - 127-го, 106-го - 128-го, 106-го - 129-го, 107-го - 125-го, 107-го - 126-го, 107-го - 127-го, 107-го - 128-го, 107-го - 129-го, 108-го - 125-го, 108-го - 126-го, 108-го - 127-го, 108-го - 128-го, 108-го - 129-го, 109-го - 125-го, 109-го - 126-го, 109-го - 127-го, 109-го - 128-го или 109-го - 129-го нуклеотидов, считая от 5'-конца 50-го экзона гена дистрофина человека, соответственно идентична нуклеотидной последовательности, состоящей из 5-го - 25-го, 4-го - 25-го, 3-го - 25-го, 2-го - 25-го, 1-го - 25-го, 5-го - 24-го, 4-го - 24-го, 3-го - 24-го, 2-го - 24-го, 1-го - 24-го, 5-го - 23-го, 4-го - 23-го, 3-го - 23-го, 2-го - 23-го, 1-го - 23-го, 5-го - 22-го, 4-го - 22-го, 3-го - 22-го, 2-го - 22-го, 1-го - 22-го, 5-го - 21-го, 4-го - 21-го, 3-го - 21-го, 2-го - 21-го или 1-го - 21-го нуклеотидов SEQ ID NO:7.
Последовательность, комплементарная нуклеотидной последовательности, состоящей из 1-го - 148-го нуклеотидов, считая от 5'-конца экзона 44, представлена последовательностью SEQ ID NO:8.
В данном случае последовательность, комплементарная нуклеотидной последовательности, состоящей из 9-го - 30-го, 9-го - 31-го, 9-го - 32-го, 9-го - 33-го, 9-го - 34-го, 10-го - 30-го, 10-го - 31-го, 10-го - 32-го, 10-го - 33-го, 10-го - 34-го, 11-го - 30-го, 11-го - 31-го, 11-го - 32-го, 11-го - 33-го, 11-го - 34-го, 12-го - 30-го, 12-го - 31-го, 12-го - 32-го, 12-го - 33-го, 12-го - 34-го, 13-го - 30-го, 13-го - 31-го, 13-го - 32-го, 13-го - 33-го, 13-го - 34-го, 24-го - 45-го, 24-го - 46-го, 24-го - 47-го, 24-го - 48-го, 24-го - 49-го, 25-го - 45-го, 25-го - 46-го, 25-го - 47-го, 25-го - 48-го, 25-го - 49-го, 26-го - 45-го, 26-го - 46-го, 26-го - 47-го, 26-го - 48-го, 26-го - 49-го, 27-го - 45-го, 27-го - 46-го, 27-го - 47-го, 27-го - 48-го, 27-го - 49-го, 28-го - 45-го, 28-го - 46-го, 28-го - 47-го, 28-го - 48-го, 28-го - 49-го, 29-го - 45-го, 29-го - 46-го, 29-го - 47-го, 29-го - 48-го или 29-го - 49-го нуклеотидов, считая от 5'-конца 44-го экзона гена дистрофина человека, соответственно идентична нуклеотидной последовательности, состоящей из 119-го - 140-го, 118-го - 140-го, 117-го - 140-го, 116-го - 140-го, 115-го - 140-го, 119-го - 139-го, 118-го - 139-го, 117-го - 139-го, 116-го - 139-го, 115-го - 139-го, 119-го - 138-го, 118-го - 138-го, 117-го - 138-го, 116-го - 138-го, 115-го - 138-го, 119-го - 137-го, 118-го - 137-го, 117-го - 137-го, 116-го - 137-го, 115-го - 137-го, 119-го - 136-го, 118-го - 136-го, 117-го - 136-го, 116-го - 136-го, 115-го - 136-го, 104-го - 125-го, 103-го - 125-го, 102-го - 125-го, 101-го - 125-го, 100-го - 125-го, 104-го - 124-го, 103-го - 124-го, 102-го - 124-го, 101-го - 124-го, 100-го - 124-го, 104-го - 123-го, 103-го - 123-го, 102-го - 123-го, 101-го - 123-го, 100-го - 123-го, 104-го - 122-го, 103-го - 122-го, 102-го - 122-го, 101-го - 122-го, 100-го - 122-го, 104-го - 121-го, 103-го - 121-го, 102-го - 121-го, 101-го - 121-го, 100-го - 121-го, 104-го - 120-го, 103-го - 120-го, 102-го - 120-го, 101-го - 120-го или 100-го - 120-го нуклеотидов SEQ ID NO:8.
Взаимосвязь между положением нуклеотидной последовательности относительно 5'-конца 55-го, 45-го, 50-го и 44-го экзонов, и положением соответствующего участка в нуклеотидных последовательностях SEQ ID NO:5-8 представлена в приведенных ниже таблицах.
Предпочтительно, чтобы олигомер, способствующий пропуску экзона 55 по настоящему изобретению, состоял из последовательности, комплементарной любой из нуклеотидных последовательностей, состоящих из 1-го - 21-го, 11-го - 31-го или 14-го - 34-го нуклеотидов, считая от 5'-конца 55-го экзона гена дистрофина человека (например, любой из последовательностей, состоящих из 170-го - 190-го, 160-го - 180-го или 157-го - 177-го нуклеотидов последовательности SEQ ID NO:5).
Предпочтительно, чтобы олигомер, способствующий пропуску экзона 45 по настоящему изобретению, состоял из последовательности, комплементарной любой из нуклеотидных последовательностей, состоящих из -2-го - 19-го, 1-го - 21-го, 1-го - 25-го или 6-го - 30-го нуклеотидов, считая от 5'-конца 45-го экзона гена дистрофина человека (например, любой из последовательностей, состоящих из 158-го - 178-го, 156-го - 176-го, 152-го - 176-го или 147-го - 171-го нуклеотидов последовательности SEQ ID NO:6).
Предпочтительно, чтобы олигомер, способствующий пропуску экзона 50 по настоящему изобретению, состоял из последовательности, комплементарной любой из нуклеотидных последовательностей, состоящих из 106-го - 126-го или 107-го - 127-го нуклеотидов, считая от 5'-конца 50-го экзона гена дистрофина человека (например, любой из последовательностей, состоящих из 4-го - 24-го или 3-го - 23-го нуклеотидов последовательности SEQ ID NO:7).
Предпочтительно, чтобы олигомер, способствующий пропуску экзона 44 по настоящему изобретению, состоял из последовательности, комплементарной любой из нуклеотидных последовательностей, состоящих из 11-го - 32-го, 25-го - 45-го, 26-го - 46-го, 26-го - 47-го или 27-го - 47-го нуклеотидов, считая от 5'-конца 44-го экзона гена дистрофина человека (например, любой из последовательностей, состоящих из 117-го - 138-го, 104-го - 124-го, 103-го - 123-го, 102-го - 123-го или 102-го - 122-го нуклеотидов последовательности SEQ ID NO:8).
Термин "вызывать пропуск 55-го экзона в гене дистрофина человека" служит для обозначения того, что в результате связывания олигомера по настоящему изобретению с сайтом, соответствующим экзону 55 транскрипта (например, пре-мРНК) гена дистрофина человека, например, нуклеотидная последовательность, соответствующая 5'-концу экзона 56 оказывается сшитой с 3' стороной нуклеотидной последовательности, соответствующей 3'-концу экзона 53 у пациентов с DMD с делецией экзона 54 после сплайсирования транскрипта, что приводит к образованию зрелой мРНК, которая свободна от сдвига рамки считывания кодонов.
Термин "вызывать пропуск 45-го экзона в гене дистрофина человека" служит для обозначения того, что в результате связывания олигомера по настоящему изобретению с сайтом, соответствующим экзону 45 транскрипта (например, пре-мРНК) гена дистрофина человека, например, нуклеотидная последовательность соответствующая 5'-концу экзона 46 оказывается сшитой с 3' стороной нуклеотидной последовательности, соответствующей 3'-концу экзона 43 у пациентов с DMD с делецией экзона 44 после сплайсирования транскрипта, что приводит к образованию зрелой мРНК, которая свободна от сдвига рамки считывания кодонов.
Термин "вызывать пропуск 50-го экзона в гене дистрофина человека" служит для обозначения того, что в результате связывания олигомера по настоящему изобретению с сайтом, соответствующим экзону 50 транскрипта (например, пре-мРНК) гена дистрофина человека, например, нуклеотидная последовательность соответствующая 5'-концу экзона 52 оказывается сшитой с 3' стороной нуклеотидной последовательности, соответствующей 3'-концу экзона 49, у пациентов с DMD с делецией экзона 51 после сплайсирования транскрипта, что приводит к образованию зрелой мРНК, которая свободна от сдвига рамки считывания кодонов.
Термин "вызывать пропуск 44-го экзона в гене дистрофина человека" служит для обозначения того, что в результате связывания олигомера по настоящему изобретению с сайтом, соответствующим экзону 44 транскрипта (например, пре-мРНК) гена дистрофина человека, например, нуклеотидная последовательность соответствующая 5'-концу экзона 46 оказывается сшитой с 3' стороной нуклеотидной последовательности, соответствующей 3'-концу экзона 43 у пациентов с DMD, с делецией экзона 45 после сплайсирования транскрипта, что приводит к образованию зрелой мРНК, которая свободна от сдвига рамки считывания кодонов.
Соответственно, не требуется, чтобы олигомер по настоящему изобретению имел нуклеотидную последовательность, которая на 100% комплементарна каждой из целевых последовательностей, если этот олигомер вызывает пропуск экзона 55, 45, 50 или 44 в гене дистрофина человека. Олигомер по настоящему изобретению может включать, например, 1-3, 1 или 2, или один нуклеотид, не комплементарный целевой последовательности.
В данном случае имеется в виду, что термин "связывание" означает, что, когда олигомер по настоящему изобретению смешивают с транскриптом гена дистрофина человека, обе молекулы гибридизуются в физиологических условиях с образованием двухцепочечной структуры. Термин "в физиологических условиях" относится к комбинации условий, которые имитируют среду живого организма, с точки зрения pH, солевого состава и температуры. Эти условия включают, например, температуру от 25 до 40°C, предпочтительно, 37°C, значения pH от 5 до 8, предпочтительно pH 7,4, и 150 мМ концентрацию хлорида натрия.
Подтвердить, действительно ли осуществляется пропуск экзона 55, 45, 50 или 44 в гене дистрофина человека, можно путем введения олигомера по настоящему изобретению в клетку, экспрессирующую дистрофин (например, клетки рабдомиосаркомы человека), амплификации области, окружающей экзон 55, 45, 50 или 44 мРНК гена дистрофина человека, с помощью RT-PCR (полимеразной цепной реакции с обратной транскрипцией) по отношению к целой РНК клетки, экспрессирующей дистрофин, и осуществления "вложенной" PCR или секвенирования продукта, амплифицированного PCR.
Эффективность пропуска можно определить следующим образом. Из тестовых клеток изолируют мРНК, образовавшуюся из гена дистрофина человека; измеряют уровень полинуклеотидов полосы "A", в которой пропущен экзон 55, 45, 50 или 44, и уровень полинуклетоидов полосы "B", в которой экзон 55, 45, 50 или 44 не пропущен. Используя результаты измерений "A" и "B", вычисляют эффективность пропуска, используя следующую формулу:
Эффективность пропуска (%) = A/(A+B)×100
Олигомер по настоящему изобретению включает, например, олигонуклеотид, морфолино-олигомер или пептидную нуклеиновую кислоту (PNA) длиной от 18 до 28 нуклеотидов. Предпочтительно, эта длина составляет от 15 до 30 нуклеотидов, или от 20 до 25 нуклеотидов и предпочтительными являются морфолино-олигомеры.
Описанный выше олигонуклеотид (далее по тексту именуемый "олигонуклеотидом по настоящему изобретению") представляет собой олигомер по настоящему изобретению, состоящий из нуклеотидов, которые являются его структурными единицами. Такие нуклеотиды могут представлять собой любые молекулы из числа рибонуклеотидов, дезоксирибонуклеотидов и модифицированных нуклеотидов.
Термин "модифицированные нуклеотиды" относится к нуклеотидам, имеющим полностью или частично модифицированные нуклеиновые основания, фрагменты сахаров и/или области связывания с остатками фосфорной кислоты, которые являются составными частями рибонуклеотида или дезоксирибонуклеотида.
Нуклеиновые основания включают, например, аденин, гуанин, гипоксантин, цитозин, тимин, урацил и продукты их модификации. Примеры таким модифицированных нуклеиновых оснований включают, не ограничиваясь перечисленными, псевдоурацил, 3-метилурацил, дигидроурацил, 5-алкилцитозины (например, 5-метилцитозин), 5-алкилурацилы (например, 5-этилурацил), 5-галогенурацилы (5-бромурацил), 6-азапиримидин, 6-алкилпиримидины (6-метилурацил), 2-тиоурацил, 4-тиоурацил, 4-ацетилцитозин, 5-(карбоксигидроксиметил)урацил, 5'-карбоксиметиламинометил-2-тиоурацил, 5-карбоксиметиламинометилурацил, 1-метиладенин, 1-метилгипоксантин, 2,2-диметилгуанин, 3-метилцитозин, 2-метиладенин, 2-метилгуанин, N6-метиладенин, 7-метилгуанин, 5-метоксиаминометил-2-тиоурацил, 5-метиламинометилурацил, 5-метилкарбонилметилурацил, 5-метилоксиурацил, 5-метил-2-тиоурацил, 2-метилтио-N6-изопентениладенин, урацил-5-оксиуксусную кислоту, 2-тиоцитозин, пурин, 2,6-диаминопурин, 2-аминопурин, изогуанин, индол, имидазол, ксантин и т.д.
Модификации фрагмента сахара могут включать, например, модификации по положению 2' рибозы, а также модификации по другим положениям остатка сахара. Модификации по положению 2' рибозы включают замещение 2'-OH-группы рибозы фрагментами OR, R, R'OR, SH, SR, NH2, NHR, NR2, N3, CN, F, Cl, Br или I, где R означает алкил или арил, и R' означает алкилен.
Модификации по другим положениям остатка сахара включают, например, замену атома O в положении 4' рибозы или дезоксирибозы атомом S, формирование мостика между положениями 2' и 4' сахара, с образованием, например, LNA (Locked Nucleic acid - запертой нуклеиновой кислоты) или ENA (нуклеиновых кислот с 2'-O, 4'-C-этиленовым мостиком), но не ограничиваясь только этим.
Модификации области связывания с остатком фосфорной кислоты включают, например, замену фосфодиэфирной связи фосфортиоатной связью, фосфордитиоатной связью, алкилфосфонатной связью, фосфорамидатной связью или боранофосфатной связью (Enya et al: Bioorganic & Medicinal Chemistry, 2008, 18, 9154-9160) (сравните, например, повторную внутреннюю публикацию в Японии заявок PCT №№ 2006/129594 и 2006/038608).
Алкил предпочтительно представляет собой линейный или разветвленный алкил, включающий от 1 до 6 атомов углерода. Конкретные примеры алкилов включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, трет-пентил, н-гексил и изогексил. Алкил необязательно может быть замещенным. Примерами подходящих заместителей являются галоген, алкокси, циано и нитро. Алкил может быть замещен 1-3 заместителями.
Циклоалкил предпочтительно является циклоалкилом, содержащим от 5 до 12 атомов углерода. Конкретные примеры циклоалкилов включают циклопентил, циклогексил, циклогептил, циклооктил, циклодецил и циклододецил.
Галогены включают фтор, хлор, бром и йод.
Алкоксигруппа является линейной или разветвленной алкоксигруппой, содержащей от 1 до 6 атомов углерода, например, метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, н-пентилокси, изопентилокси, н-гексилокси, изогексилокси и т.д. Среди алкоксигрупп предпочтительными являются группы, содержащие 1-3 атома углерода.
Арил предпочтительно является арилом, содержащим от 6 до 10 атомов углерода. Конкретные примеры арилов включают фенил, α-нафтил и β-нафтил. Предпочтительным среди арилов является фенил. Арил необязательно может быть замещенным. Примерами подходящих заместителей являются алкил, галоген, алкокси, циано и нитро. Арил может быть замещен 1-3 заместителями из приведенного перечня.
Алкилен предпочтительно является линейным или разветвленным алкиленом, содержащим от 1 до 6 атомов углерода. Конкретные примеры алкиленов включают метилен, этилен, триметилен, тетраметилен, пентаметилен, гексаметилен, 2-(этил)триметилен и 1-(метил)тетраметилен.
Ацилы включают линейные или разветвленные алканоилы или ароилы. Примеры алканоилов включают формил, ацетил, 2-метилацетил, 2,2-диметилацетил, пропионил, бутирил, изобутирил, пентаноил, 2,2-диметилпропионил, гексаноил и т.д. Примеры ароилов включают бензоил, толуоил и нафтоил. Ароил необязательно может быть замещен по доступным положениям, причем заместители могут являться алкилами.
Предпочтительно, олигонуклеотид по настоящему изобретению является олигомером по настоящему изобретению, содержащим структурные фрагменты, представленные приведенной ниже общей формулой, где группа -OH в положении 2' остатка рибозы замещена метоксигруппой, и область связывания с остатком фосфорной кислоты включает фосфортиоатную связь:
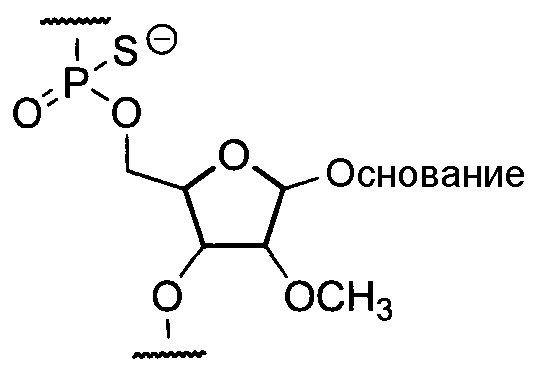
где "основание" означает нуклеиновое основание.
Олигонуклеотид по настоящему изобретению можно без труда синтезировать с помощью различных автоматических приборов для синтеза (например, AKTA oligopilot plus 10/100 (GE Healthcare)). В качестве альтернативы, синтез можно также поручить сторонней организации (например, Promega Inc., или Takara Co.) и т.п.
Морфолино-олигомер по настоящему изобретению представляет собой олигомер по настоящему изобретению, включающий структурную единицу приведенной ниже общей формулы
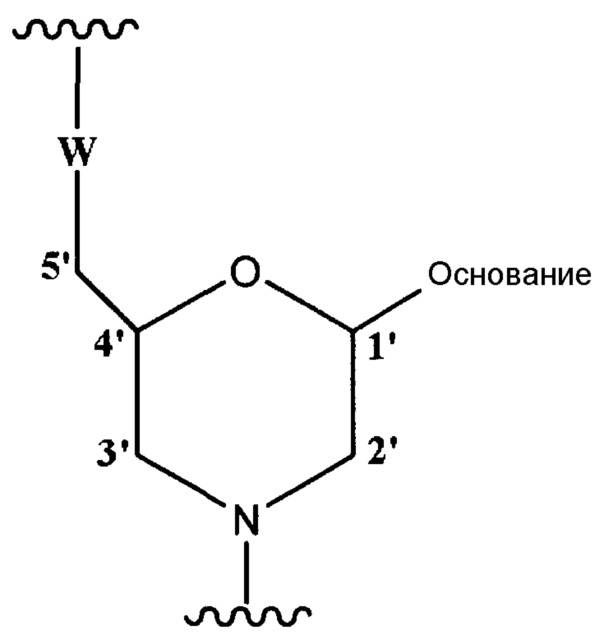
где "основание" имеет указанное выше значение, и W означает группу, представленную одной из приведенных ниже формул:
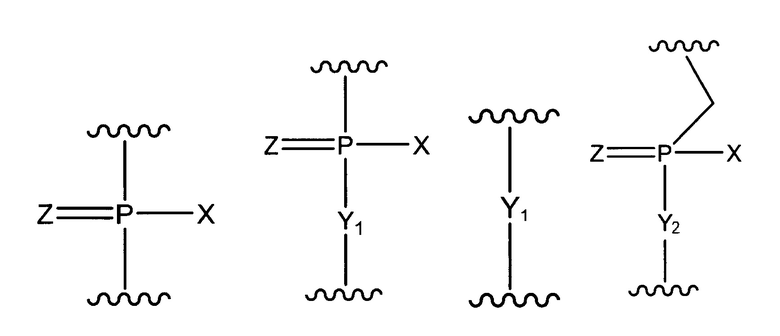
где
X представляет собой -CH2R1, -O-CH2R1, -S-CH2R1, -NR2R3 или F;
R1 представляет собой H или алкил;
каждый из R2 и R3, которые могут быть одинаковыми или различными, представляет собой H, алкил, циклоалкил или арил;
Y1 представляет собой O, S, CH2 или NR1;
Y2 представляет собой O, S или NR1;
Z представляет собой O или S.
Предпочтительно, морфолино-олигомер представляет собой олигомер, включающий структурное звено приведенной ниже общей формулы (фосфордиамидатный морфолино-олигомер (далее по тексту именуемый "PMO")).
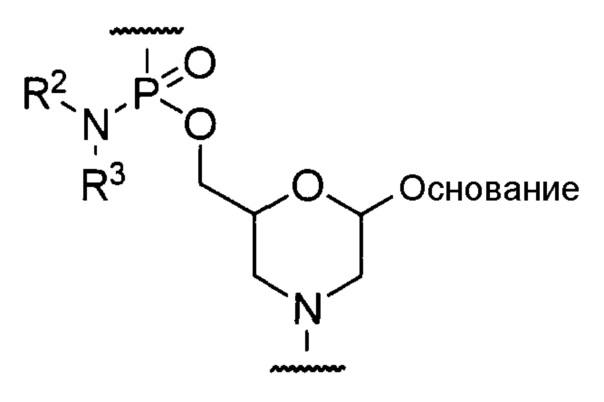
где "основание", R2 и R3 соответствуют данным выше определениям.
Морфолино-олигомер можно получить по методикам, изложенным, например, в WO 1991/009033 или WO 2009/064471. В частности, PMO можно получить по методике, описанной в WO 2009/064471, или показанным ниже способом.
Способ получения PMO
Одним из вариантов осуществления PMO является, например, соединение приведенной ниже общей формулы (I) (далее по тексту PMO (I)).
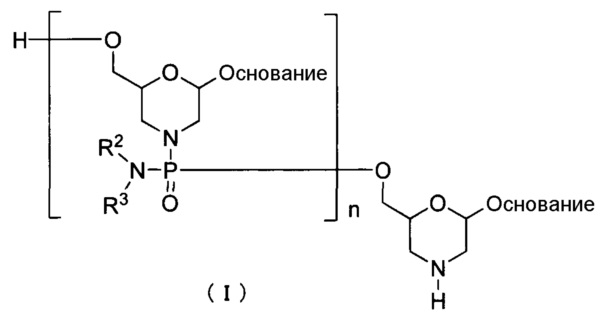
где "основание", R2 и R3 соответствуют данным выше определениям; и n означает целое число от 1 до 99, предпочтительно от 18 до 28.
PMO (I) можно получать по известным методикам, например, осуществляя методику, состоящую из следующих стадий.
Соединения и реагенты, которые применяются в показанных ниже стадиях, не ограничены конкретными рамками, если они традиционно применяются для получения PMO.
Кроме того, эти стадии можно проводить по методикам, которые реализуются в жидкой фазе или в твердой фазе (осуществляя синтез вручную или с помощью коммерчески доступных автоматических приборах для твердофазного синтеза). При получении PMO по твердофазной методике, желательно использовать автоматические синтезаторы, ввиду простоты проведения процедур и точности синтеза.
(1) Стадия A
Соединение приведенной ниже общей формулы (II) (далее по тексту именуемое соединением (II)) вводят в реакцию с кислотой, получая соединение приведенной ниже общей формулы (III) (далее по тексту именуемое соединение (III)):

где n, R2 и R3 соответствуют данным выше определениям;
каждый из фрагментов Bp независимо представляет собой нуклеиновое основание, которое необязательно может быть защищено;
T представляет собой тритил, монометокситритил или диметокситритил; и
L представляет собой водород, ацил или группу приведенной ниже общей формулы (IV) (далее по тексту именуемую группой (IV)).

"Нуклеиновое основание", обозначенное символом Bp, представляет собой такое же нуклеиновое основание, которое обозначено "основание", при условии, что амино- или гидроксигруппа в нуклеиновом основании, обозначенном символом Bp, может быть защищенной.
На защитные фрагменты для аминогруппы не накладывается конкретных ограничений, если эти группы применяются в качестве защитных групп для нуклеиновых кислот. Конкретные примеры таких групп включают бензоил, 4-метоксибензоил, ацетил, пропионил, бутирил, изобутирил, фенилацетил, феноксиацетил, 4-трет-бутилфеноксиацетил, 4-изопропилфеноксиацетил и (диметиламино)метилен. Конкретные примеры защитных групп для гидроксигруппы включают 2-цианоэтил, 4-нитрофенэтил, фенилсульфонилэтил, метилсульфонилэтил, а также триметилсилилэтил и фенил, который может быть замещен 1-5 электроноакцепторными группами по любым доступным положениям, дифенилкарбамоил, диметилкарбамоил, диэтилкарбамоил, метилфенилкарбамоил, 1-пирролидинилкарбамоил, морфолинокарбамоил, 4-(трет-бутилкарбокси)бензил, 4-[(диметиламино)карбокси]бензил и 4-(фенилкарбокси)бензил (сравните, например, WO 2009/064471).
На "твердый носитель" не накладывается конкретных ограничений, если он является носителем, подходящим для проведения твердофазных реакций нуклеиновых кислот. Желательно, чтобы этот твердый носитель имел следующие свойства: например, (1) обладал незначительной растворимостью в реагентах, которые могут применяться для синтеза морфолино-производных нуклеиновых кислот (например, дихлорметане, ацетонитриле, тетразоле, N-метилимидазоле, пиридине, уксусном ангидриде, лутидине, трифторуксусной кислоте); (ii) обладал химической устойчивостью по отношению к реагентам, применимым для синтеза морфолино-производных нуклеиновых кислот; (iii) мог подвергаться химическим модификациям; (iv) носитель можно было насытить желаемыми морфолино-производными нуклеиновых кислот; (v) обладал достаточной прочностью, чтобы выдерживать высокое давление при обработке; и (vi) обладал равномерным диапазоном и распределением диаметров частиц. Конкретно могут применяться набухающий полистирол (например, аминометил полистрирольная смола, сшитая 1% дибензилидена (200-400 меш) (2,4-3,0 ммоль/г) (производства Tokyo Chemical Industry), аминометилированная полистрирольная смола·HCl [дибензилиден 1%, 100-200 меш] (производства Peptide Institute, Inc.)), не набухающий полистрирол (например, Primer Support (производства GE Healthcare)), полистрирол, к которому прикреплены цепи ПЭГ (например, NH2·ПЭГ (производства Watanabe Chemical Co.), полимерная смола TentaGel), стекло с порами регулируемого размера (стекло с порами регулируемого размера; CPG) (производства, например, CPG), пористое стекло, полученное с применением оксалила (сравните, например, Alul et al., Nucleic Acids Research, Vol. 19, 1527 (1991)), подложка TentaGel - подложка на основе модифицированного аминополиэтиленгликоля (сравните, например, Wright et al., Tetrahedron Letters, Vol.34, 3373 (1993)) и пористый полистирол/дивинилбензол.
Подходящий "линкер" представляет собой известный линкер, традиционно применяемый для связывания нуклеиновых кислот или морфолино-производных нуклеиновых кислот. Примеры линкеров включают 3-аминопропил, сукцинил, 2,2'-диэтанолсульфонил и алкиламиногруппу с длинной цепью (LCAA).
Описываемую стадию осуществляют путем взаимодействия соединения (II) с кислотой.
"Кислота", которая может применяться на данной стадии, включает, например, трифторуксусную кислоту, дихлоруксусную кислоту и трихлоруксусную кислоту. Подходящее количество применяемой кислоты находится в диапазоне, например, от 0,1 мольного эквивалента до 1000 мольных эквивалентов на 1 моль соединения (II), предпочтительно, в диапазоне от 1 мольного эквивалента до 100 мольных эквивалентов на 1 моль соединения (II).
В комбинации с описанной выше кислотой на данной стадии можно применять органический амин. На применяемый органический амин не налагается конкретных ограничений, и в число таких аминов входит, например, триэтиламин. Подходящее количество применяемого органического амина находится в диапазоне, например, от 0,01 мольного эквивалента до 10 мольных эквивалентов и, предпочтительно, в диапазоне от 0,1 мольного эквивалента до 2 мольных эквивалентов на 1 моль кислоты.
Если на данной стадии применяется соль или смесь кислоты и органического амина, эта соль или смесь включает, например, соль или смесь трифторуксусной кислоты и триэтиламина и, более конкретно, смесь 1 эквивалента триэтиламина и 2 эквивалентов трифторуксуной кислоты.
Кислоту, которая может применяться на данной стадии, можно также разбавлять подходящим растворителем до концентрации 0,1-30%. На растворитель не налагается конкретных ограничений, если он не принимает участия в реакции, и в число таких растворителей входят, например, дихлорметан, ацетонитрил, спирты (этанол, изопропанол, трифторэтанол и т.д.), вода или их смеси.
Температура проведения описанной выше реакции предпочтительно находится в диапазоне, например, от 10°C до 50°C, более предпочтительно, в диапазоне от 20°C до 40°C и, наиболее предпочтительно, в диапазоне от 25°C до 35°C.
Время проведения реакции можно менять в зависимости от применяемой кислоты и температуры проведения реакции, и подходящее время, как правило, находится в диапазоне от 0,1 минуты до 24 часов и, предпочтительно, в диапазоне от 1 минуты до 5 часов.
После завершения описанной стадии, при необходимости, можно добавить основание для нейтрализации оставшейся в реакционной смеси кислоты. На упомянутое "основание" не налагается конкретных ограничений, и эти основания включают, например, диизопропиламин. Основание может также разбавлять подходящим растворителем до концентрации 0,1% (объем/объем) до 30% (объем/объем).
На растворитель, применяемый на этой стадии, не налагается конкретных ограничений, если он не влияет на ход реакции, и подходящие растворители включают дихлорметан, ацетонитрил, спирт (этанол, изопропанол, трифторэтанол и т.д.), воду и их смеси. Температура проведения реакции предпочтительно находится в диапазоне, например, от 10°C до 50°C, более предпочтительно, в диапазоне от 20°C до 40°C и, наиболее предпочтительно, в диапазоне от 25°C до 35°C.
Время проведения реакции можно менять в зависимости от применяемого основания и температуры проведения реакции, и подходящее время, как правило, находится в диапазоне от 0,1 минуты до 24 часов и, предпочтительно, в диапазоне от 1 минуты до 5 часов.
Соединение приведенной ниже общей формулы (IIa) (далее по тексту соединение (IIa)), входящее в число соединений формулы (II), где n означает 1, и L представляет собой группу (IV), можно получить по следующей методике.

где Bp, T, линкер и твердый носитель соответствуют данным выше определениям.
Стадия 1:
Соединение приведенной ниже общей формулы (V) вводят во взаимодействие с ацилирующим агентом, получая соединение приведенной ниже общей формулы (VI) (далее по тексту именуемое соединением (VI)).

где Bp, T и линкер соответствуют данным выше определениям; и R4 представляет собой гидрокси, галоген или амино.
Эту стадию можно осуществлять по известным методикам введения линкеров, используя соединение (V) в качестве исходного вещества.
В частности, соединение приведенной ниже общей формулы (VIa) можно получать, осуществляя реакцию, известную, как этерификация, используя соединение (V) и янтарный ангидрид.
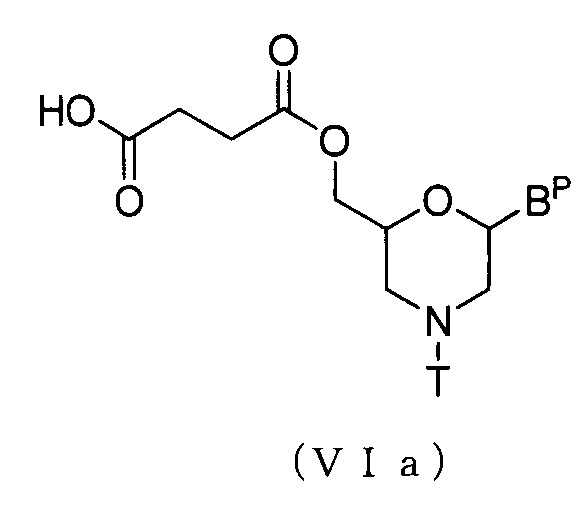
где Bp и T соответствуют данным выше определениям.
Стадия 2:
Соединение (VI) вводят во взаимодействие с твердым носителем с использованием конденсирующего агента, получая соединение (IIa).
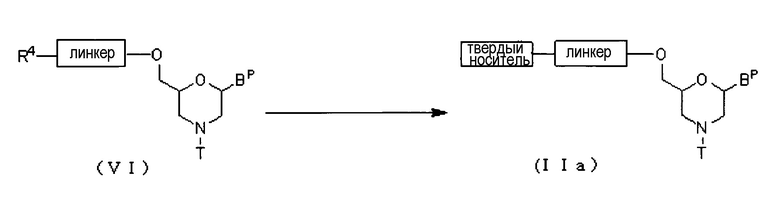
где Bp, R4, T, линкер и твердый носитель соответствуют данным выше определениям.
Эту стадию можно проводить, используя соединение (VI) и твердый носитель в соответствии со способом, известным, как реакция конденсации.
Соединение приведенной ниже общей формулы (IIa2), которое относится к числу соединений формулы (II), где n означает 2-99, и L представляет собой группу общей формулы (IV), можно получать с использованием соединения (IIa) в качестве исходного вещества и повторяя стадию A и стадию B способа получения PMO, описанного в заявке, желаемое число раз.
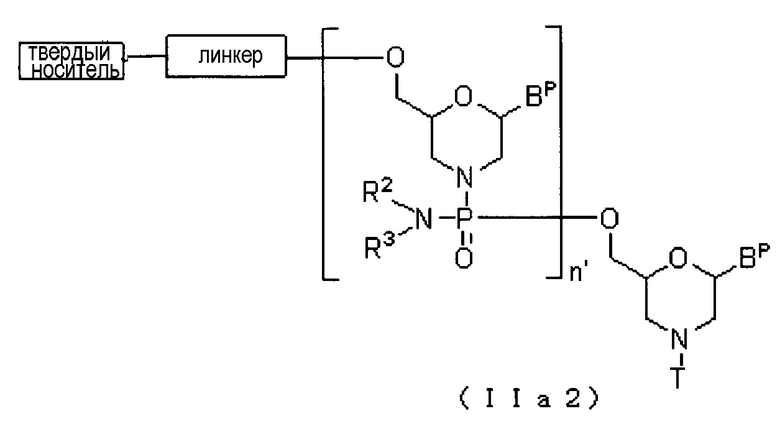
где Bp, R2, T, линкер и твердый носитель соответствуют данным выше определениям; и
n' означает число от 1 до 98.
Соединение приведенной ниже общей формулы (IIb), которое относится к числу соединений формулы (II), где n означает 1, и L означает водород, можно получить по методике, описанной, например, в WO 1991/009033
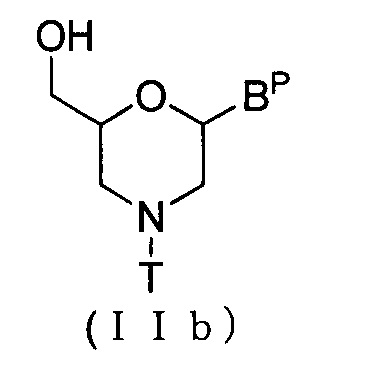
где Bp и T соответствуют данным выше определениям.
Соединение приведенной ниже общей формулы (IIb2), которое относится к числу соединений формулы (II), где n означает 2-99, и L представляет собой водород, можно получать с использованием соединения (IIb) в качестве исходного вещества и повторяя стадию A и стадию B способа получения PMO, описанного в заявке, желаемое число раз.

где Bp, n', R2, R3 и T соответствуют данным выше определениям.
Соединение приведенной ниже общей формулы (IIc), которое относится к числу соединений формулы (II), где n означает 1, и L означает ацил, можно получить по методике, известной, как реакция ацилирования, используя соединение (IIb).

где Bp и T соответствуют данным выше определениям; и R5 означает ацил.
Соединение приведенной ниже общей формулы (IIc2), которое относится к числу соединений формулы (II), где n означает 2-99, и L представляет собой ацил, можно получать с использованием соединения (IIc) в качестве исходного вещества и повторяя стадию A и стадию B способа получения PMO, описанного в заявке, желаемое число раз.
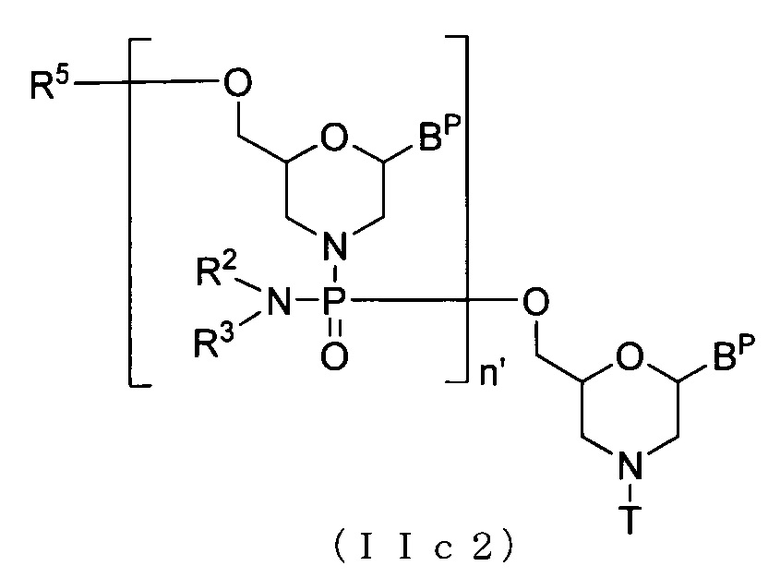
где Bp, n', R2, R3, R5 и T соответствуют данным выше определениям.
(2) Стадия B
Соединение (III) вводят во взаимодействие с мономерным морфолиновым соединением в присутствии основания, получая соединение приведенной ниже общей формулы (VII) (далее по тексту именуемое соединением (VII):
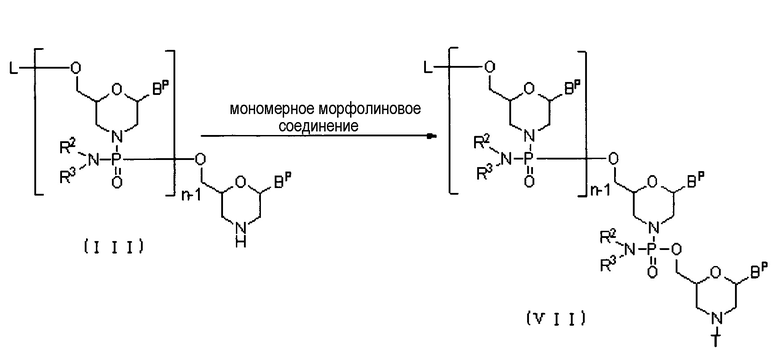
где Bp, L, n, R2, R3 и T соответствуют данным выше определениям.
Эту стадию синтеза можно осуществлять, вводя во взаимодействие соединение (III) с мономерным морфолиновым соединением в присутствии основания.
Мономерное морфолиновое соединение включает, например, соединения, представленные приведенной ниже общей формулой (VIII):
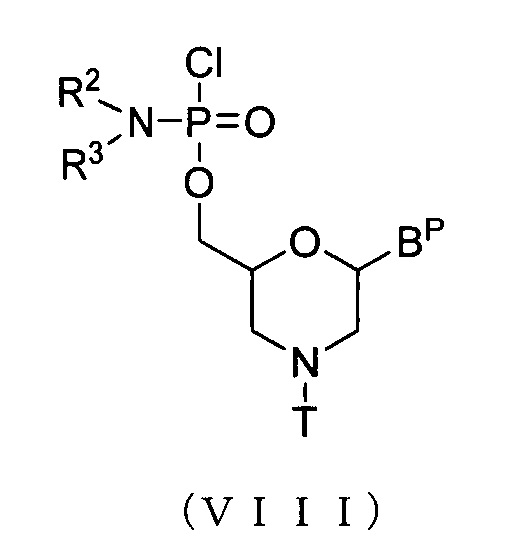
где Bp, R2, R3 и T соответствуют данным выше определениям.
Основания, которые могут применяться на данной стадии, включают, например, диизопропиламин, триэтиламин и N-этилморфолин. Подходящее для проведения реакции количество основания находится в диапазоне от 1 мольного эквивалента до 1000 мольных эквивалентов на моль соединения (III), предпочтительно, от 10 мольных эквивалентов до 100 мольных эквивалентов на 1 моль соединения (III).
Мономерное морфолиновое соединение и основание, которое можно применять на этой стадии, можно также разбавлять подходящим растворителем до концентрации 0,1-30%. На выбор растворителя не налагается конкретных ограничений, если он не участвует в реакции, и в число подходящих растворителей входят, например, N,N-диметилимидазолидон, N-метилпиперидон, ДМФА, дихлорметан, ацетонитрил, тетрагидрофуран или их смеси.
Температура проведения реакции предпочтительно находится в диапазоне, например, от 0°C до 100°C и, более предпочтительно, в диапазоне от 10°C до 50°C.
Время проведения реакции можно менять в зависимости от применяемого основания и температуры проведения реакции, и подходящее время, как правило, находится в диапазоне от 1 минуты до 48 часов и, предпочтительно, в диапазоне от 30 минут до 24 часов.
Кроме того, после завершения этой стадии, при необходимости, можно добавлять ацилирующий агент. "Ацилирующие агенты" включают, например, уксусный ангидрид, ацетилхлорид и феноксиуксусный ангидрид. Ацилирующий агент можно также разбавлять подходящим растворителем до концентрации от 0,1% до 30%. Выбор растворителя не ограничен конкретными рамками, если он не принимает участия в реакции, и подходящие растворители включают, например, дихлорметан, ацетонитрил, спирт(ы) (этанол, изопропанол, трифторэтанол и т.д.), воду или их смеси.
Если это необходимо, в комбинации с ацилирующим агентом можно также применять основание, например, пиридин, лутидин, коллидин, триэтиламин, диизопропилэтиламин, N-этилморфолин и т.д. Подходящее количество ацилирующего агента находится в диапазоне от 0,1 мольного эквивалента до 10000 мольных эквивалентов и, предпочтительно, в диапазоне от 1 мольного эквивалента до 1000 мольных эквивалентов. Подходящее количество основания находится в диапазоне от, например, 0,1 мольного эквивалента до 100 мольных эквивалентов и, предпочтительно, в диапазоне от 1 мольного эквивалента до 10 мольных эквивалентов на 1 моль ацилирующего агента.
Температура проведения этой реакции предпочтительно находится в диапазоне от 10°C до 50°C, более предпочтительно, в диапазоне от 10°C до 50°C, еще более предпочтительно, в диапазоне от 20°C до 40°C, и, наиболее предпочтительно, в диапазоне от 25°C до 35°C. Время проведения реакции можно менять в зависимости от применяемого ацилирующего агента и температуры проведения реакции, и подходящее время, как правило, находится в диапазоне от 0,1 минуты до 24 часов и, предпочтительно, в диапазоне от 1 минуты до 5 часов.
(3) Стадия C
В соединении (VII), полученном на стадии B, удаляют защитную группу, используя реагент для снятия защиты, и получают соединение общей формулы (IX).

где "основание", Bp, L, n, R2, R3 и T соответствуют данным выше определениям.
Эту стадию можно проводить, осуществляя взаимодействие соединения (VII) с реагентом для снятия защиты.
"Реагенты для снятия защиты" включают, например, концентрированный раствор аммиака в воде и метиламин. Реагенты для снятия защиты, используемые на данной стадии, можно также разбавлять подходящими растворителями, например, водой, метанолом, этанолом, изопропиловым спиртом, ацетонитрилом, тетрагидрофураном, ДМФА, N,N-диметилимидазолидоном, N-метилпиперидоном или смесью этих растворителей. Среди перечисленных растворителей предпочтительным является этанол. Подходящее количество применяемого реагента для снятия защиты находится, например, в диапазоне от 1 мольного эквивалента до 100000 мольных эквивалентов и, предпочтительно, в диапазоне от 10 мольных эквивалентов до 1000 мольных эквивалентов на 1 моль соединения (VII).
Подходящая температура проведения реакции находится в диапазоне от 15°C до 75°C, предпочтительно, в диапазоне от 40°C до 70°C и, более предпочтительно, в диапазоне от 50°C до 60°C. Время проведения реакции снятия защиты можно менять в зависимости от типа соединения (VII), температуры проведения реакции и т.п., и подходящее время, как правило, находится в диапазоне от 10 минут до 30 часов, предпочтительно, в диапазоне от 30 минут до 24 часов и, более предпочтительно, в диапазоне от 5 часов до 20 часов.
(4) Стадия D
PMO (I) получают взаимодействием соединения (IX), полученного на стадии C, с кислотой:
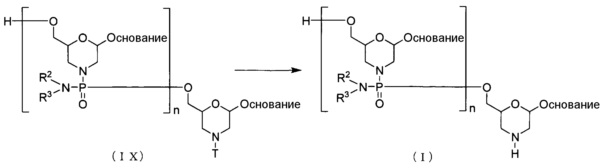
где "основание", n, R2, R3 и T соответствуют данным выше определениям.
Эту стадию можно осуществлять путем добавления кислоты к соединению (IX).
"Кислоты", которые можно применять на этой стадии, включают, например, трихлоруксусную кислоту, дихлоруксусную кислоту, уксусную кислоту, фосфорную кислоту, хлористоводородную кислоту и т.д. Подходящими для применения являются кислоты, которые позволяют получить значение pH раствора в диапазоне от 0,1 до 4,0 и, более предпочтительно, в диапазоне от 1,0 до 3,0. Выбор растворителя не ограничен конкретными рамками, если он не участвует в реакции, и в число подходящих растворителей входят, например, ацетонитрил, вода или смесь этих растворителей.
Подходящая температура проведения реакции находится в диапазоне от 10°C до 50°C, предпочтительно, в диапазоне от 20°C до 40°C и, более предпочтительно, в диапазоне от 25°C до 35°C. Время проведения реакции снятия защиты можно менять в зависимости от типа соединения (IX), температуры проведения реакции и т.п., и подходящее время находится в диапазоне от 0,1 минуты до 5 часов, предпочтительно, от 1 минуты до 1 часа и, более предпочтительно, в диапазоне от 1 минуты до 30 минут.
PMO (I) можно получать, осуществляя разделение и очистку реакционной смеси, полученной на данной стадии, обычными способами, такими как экстракция, концентрирование, нейтрализация, фильтрование, центрифугирование, перекристаллизация, колоночная хроматография на обращенной фазе C8-C18, катионообменная колоночная хроматография, анионообменная колоночная хроматография, гель-фильтрационная колоночная хроматография, высокоэффективная жидкостная хроматография, диализ, ультрафильтрация и т.д., индивидуально или в виде комбинации. Таким образом можно изолировать и очистить желаемый PMO (I) (сравните, например, WO 1991/09033).
При очистке PMO (I) хроматографией на обращенной фазе, в качестве элюирующего растворителя можно применять, например, смесь 20 мМ буфера триэтиламин/ацетат и ацетонитрила.
При очистке PMO (I) ионообменной хроматографией в качестве элюирующего растворителя можно применять, например, смесь 1% раствора соли в воде и 10 мМ водный раствор гидроксида натрия.
Пептидная нуклеиновая кислота представляет собой олигомер по настоящему изобретению, включающий в качестве структурного звена группу приведенной ниже общей формулы:

где "основание" соответствует данному выше определению.
Пептидные нуклеиновые кислоты можно получать по методикам, изложенным в следующих литературных источниках

В олигомере по настоящему изобретению 5'-конец может иметь любую из приведенных ниже химических структур (1)-(3), и предпочтительно представляет собой структуру (3) -OH.
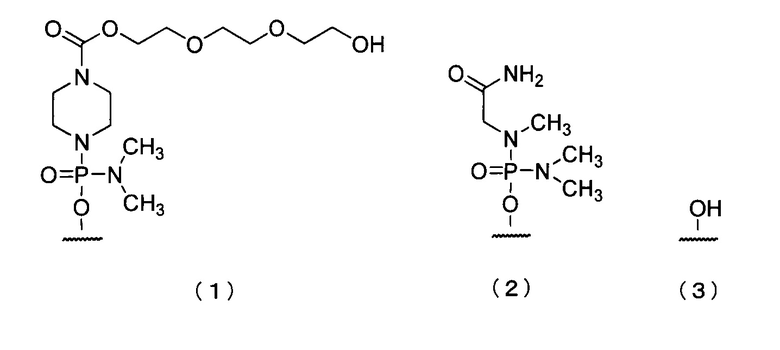
Далее по тексту группы, представленные формулами (1), (2) и (3), именуются "группа (1)", "группа (2)" и группа (3), соответственно.
2. Фармацевтическая композиция
Олигомер по настоящему изобретению вызывает пропуск экзона 55, 45, 50 и 44 с более высокой эффективностью по сравнению с антисмысловыми олигомерами известного уровня техники. Поэтому ожидается, что при введении пациентам с DMD фармацевтической композиции, включающей олигомер по настоящему изобретению, с высокой эффективностью можно облегчить состояние мышечной дистрофии. Например, если применяется фармацевтическая композиция, включающая олигомер по настоящему изобретению, того же терапевтического эффекта можно добиться даже меньшей дозой, чем в случае олигомеров известного уровня техники. Соответственно, при этом можно ослабить побочные эффекты и добиться определенного экономического эффекта.
В другом варианте осуществления настоящее изобретение относится к фармацевтической композиции для лечения мышечной дистрофии, включающей в качестве действующего ингредиента олигомер по настоящему изобретению, его фармацевтически приемлемую соль или гидрат (далее по тексту "композиции по настоящему изобретению").
Примеры фармацевтически приемлемой соли олигомера по настоящему изобретению, входящей в композицию по настоящему изобретению, являются соли щелочных металлов, например, соли натрия, калия и лития; щелочноземельных металлов, например, соли кальция и магния; соли таких металлов, как алюминий, железо, цинк, медь, никель, кобальт и т.д.; соли аммония; соли органических аминов, например, соли трет-октиламина, дибензиламина, морфолина, глюкозамина, алкиловых эфиров фенилглицина, этлендиамина, N-метилглюкамина, гуанидина, диэтиламина, триэтиламина, дициклогексиламина, N,N'-дибензилэтилендиамина, хлорпрокаина, прокаина, диэтаноламина, N-бензилфенэтиламина, пиперазина, тетраметиламмония, трис(гидроксиметил)аминометана; гидрогалогениды, например, гидрофториды, гидрохлориды, гидробромиды и гидройодиды; соли неорганических кислот, например, нитраты, перхлораты, сульфаты, фосфаты и т.д.; низшие алкансульфонаты, например, метансульфонаты, трифторметансульфонаты и этансульфонаты; арилсульфонаты, например, бензолсульфонаты и п-толуолсульфонаты; соли органических кислот, например, ацетаты, малаты, фумараты, сукцинаты, цитраты, тартраты, оксалаты, малеаты и т.д.; а также соли аминокислот, например, соли глицина, лизина, аргинина, орнитина, глутаминовой кислоты и аспарагиновой кислоты. Эти соли можно получать известными способами. В качестве альтернативы, олигомер по настоящему изобретению, входящий в композицию по настоящему изобретению, может иметь форму гидрата.
Путь введения композиции по настоящему изобретению не ограничен конкретными рамками, если он подходит для введения с фармацевтической точки зрения, и этот путь можно выбрать в зависимости от способа лечения. С точки зрения легкости доставки в мышечную ткань, предпочтительным является внутривенное введение, внутриартериальное введение, внутримышечное введение, подкожное введение, пероральное введение, введение в соответствующую ткань, трансдермальное введение и т.д. Дозированная форма, которая подходит для соединения по настоящему изобретению, также не ограничена конкретными рамками, и подходящие формы включают, например, различные составы для инъекций, пероральные средства, капли, составы для ингаляции, мази, лосьоны и т.д.
В случае введения олигомера по настоящему изобретению пациентам с мышечной дистрофией, композиция по настоящему изобретению предпочтительно содержит носитель, который способствует доставке олигомера в мышечную ткань. Выбор такого носителя не ограничен конкретными рамками, если он является фармацевтически приемлемым, и примеры подходящих носителей включают катионные носители, например, катионные липосомы, катионные полимеры и т.д. или носители, в которых используются оболочка вируса. Катионными липосомами являются, например, липосомы, основными компонентами которых являются 2-O-(2-диэтиламиноэтил)карбамоил-1,3-O-диолеоилглицерин и фосфолипиды (далее по тексту именуемые "липосомами A"), Oligofectamine (зарегистрированная торговая марка) (производства Invitrogen Corp.), Lipofectin (зарегистрированная торговая марка) (производства Invitrogen Corp.), Lipofectamin (зарегистрированная торговая марка) (производства Invitrogen Corp.), Lipofectamin 2000 (зарегистрированная торговая марка) (производства Invitrogen Corp.), DMRIE-C (зарегистрированная торговая марка) (производства Invitrogen Corp.), GeneSilencer (зарегистрированная торговая марка) (производства Gene Therapy Systems), TransMessenger (зарегистрированная торговая марка) (производства QIAGEN, Inc.), TransIT TKO (зарегистрированная торговая марка) (производства Mirus) и Nucleofector II (Lonza). Среди перечисленных носителей предпочтительными являются липосомы A. Примерами катионных полимеров являются JetSI (зарегистрированная торговая марка) (производства Qbiogene, Inc.) и Jet-PEI (зарегистрированная торговая марка) (полиэтиленимин, производства Qbiogene, Inc.). Примером носителя, в котором применяются оболочки вирусов, является GenomeOne (зарегистрированная торговая марка) (HVJ-E липосомы, производства Ishihara Sangyo). В качестве альтернативы могут применяться также медицинские устройства, описанные в патенте Японии № 2924179, и катионные носители, описанные в повторных внутренних публикациях японских PCT №№ 2006/129594 и 2008/096690.
Концентрация олигомера по настоящему изобретению, содержащегося в композиции по настоящему изобретению, может меняться в зависимости от вида носителя и других факторов, и подходящая концентрация находится в диапазоне от 0,1 нМ до 100 мкМ, предпочтительно в диапазоне от 1 нМ до 10 мкМ, и более предпочтительно в диапазоне от 10 нМ до 1 мкМ. Отношение массы олигомера по настоящему изобретению, входящего в композицию по настоящему изобретению, и массы носителя (носитель/олигомер по настоящему изобретению) может меняться в зависимости от свойств олигомера, типа носителя и т.д., и подходящее отношение находится в диапазоне от 0,1 до 100, предпочтительно, в диапазоне от 1 до 50 и, более предпочтительно, в диапазоне от 10 до 20.
Помимо олигомера по настоящему изобретению и описанного выше носителя, в композицию по настоящему изобретению необязательно можно включать фармацевтически приемлемые добавки. Примерами таких добавок являются эмульгирующие средства (например, жирные кислоты, включающие 6-22 атомов углерода, и их фармацевтически приемлемые соли, альбумин и декстран), стабилизаторы (например, холестерин и фосфатидиновую кислоту), агенты для придания изотоничности (например, хлорид натрия, глюкозу, мальтозу, лактозу, сахарозу, трегалозу) и средства для регулирования pH (например, хлористоводородную кислоту, серную кислоту, фосфорную кислоту, уксусную кислоту, гидроксид натрия, гидроксид калия и триэтаноламин). Можно применять одну или несколько из перечисленных добавок. Содержание упомянутых добавок в композиции по настоящему изобретению может составлять 90 масс.% или менее, предпочтительно, 70 масс.% или менее и, более предпочтительно, 50 масс.% или менее.
Композицию по настоящему изобретению можно получать добавлением олигомера по настоящему изобретению к дисперсии носителя с достаточным перемешиванием полученной смеси. Добавки можно вводить на подходящем этапе, либо до, либо после добавления олигомера по настоящему изобретению. Водный растворитель, который может применяться при добавлении олигомера по настоящему изобретению, не ограничен конкретными рамками, если он является фармацевтически приемлемым, и примерами таких растворителей являются вода для инъекций или дистиллированная вода для инъекций, жидкие электролиты, например, солевой физиологический раствор и т.д. и жидкие растворы сахаров, например, раствор глюкозы, раствор мальтозы и т.д. Специалист в данной области техники способен надлежащим образом подобрать условия смешивания, такие как pH среды и температуру.
Композиция по настоящему изобретению можно получить, например, в жидкой форме или в форме лиофилизированного препарата. Лиофилизированный препарат можно получать лиофилизацией композиции по настоящему изобретению, имеющей жидкую форму, с применением стандартных способов. Лиофилизацию можно осуществлять, например, путем стерилизации композиции по настоящему изобретению в жидкой форме подходящими способами, разделения композиции на аликвоты в подходящие сосуды, предварительного замораживания в течение 2 часов при температуре примерно от -40°C до -20°C, первичного высушивания при температуре от 0 до -10°C при пониженном давлении и вторичного высушивания при температуре от примерно 15 до 25°C при пониженном давлении. Как правило, лиофилизированные препараты композиций по настоящему изобретению можно получать, заменяя воздух в сосуде на газообразный азот и затем плотно закрывая сосуд.
Лиофилизированный препарат композиции по настоящему изобретению, как правило, можно применять после восстановления, которое осуществляют добавлением необязательного подходящего растворителя (жидкости для восстановления) и повторным растворением препарата. Упомянутые жидкости для восстановления включают воду для инъекций, физиологический солевой раствор и другие жидкости, применяемые при инфузиях. Объем жидкости для восстановления может меняться в зависимости от намеченной цели и т.д., этот объем не ограничен конкретными рамками и обычно в 0,5-2 раза превышает объем до лиофилизации или не превосходит 500 мл.
Желательно регулировать дозу вводимой композиции по настоящему изобретению, принимая во внимание такие факторы, как тип и дозированная форма олигомера по настоящему изобретению; состояние пациента, в том числе возраст, массу тела и т.д.; путь введения; а также характеристики и продолжительность заболевания. Дневная доза для одного пациента, выраженная в виде количества олигомера по настоящему изобретению, обычно находится в диапазоне от 0,1 мг до 10 г и, предпочтительно, от 1 мг до 1 г. Это количество может меняться по обстоятельствам, в зависимости от целевого заболевания, пути введения и молекулярной мишени. Таким образом, в некоторых случаях может оказаться достаточной доза ниже указанного диапазона и, наоборот, может потребоваться доза, превышающая указанный диапазон. Композиции по настоящему изобретению можно вводить от одного до нескольких раз ежедневно, или через промежутки от одного дня до нескольких дней.
В еще одном варианте осуществления композиция по настоящему изобретению представляет собой фармацевтическую композицию, включающую вектор, способный экспрессировать олигонуклеотид по настоящему изобретению и описанный выше носитель. Этот вектор экспрессии может являться вектором, способным экспрессировать большое количество олигонуклеотидов по настоящему изобретению. Такая композиция может включать фармацевтически приемлемые добавки, как и в случае композиции по настоящему изобретению, содержащей олигомер по настоящему изобретению. Концентрация вектора экспрессии, содержащегося в композиции, может меняться в зависимости от типа носителя и т.д. и подходящая концентрация находится в диапазоне от 0,1 нМ до 100 мкМ, предпочтительно, в диапазоне от 1 нМ до 10 мкМ и, более предпочтительно, в диапазоне от 10 нМ до 1 мкМ. Отношение массы содержащегося в композиции вектора экспрессии и массы носителя (носитель/вектор экспрессии) может меняться в зависимости от свойств вектора экспрессии, типа носителя и т.д. и подходящее значение находится в диапазоне от 0,1 до 100, предпочтительно в диапазоне от 1 до 50 и более предпочтительно в диапазоне от 10 до 20. Содержание носителя в композиции такое же, как и в случае композиции по настоящему изобретению, включающей олигомер по настоящему изобретению, и способ получения композиции также совпадает со способом получения композиции, включающей олигомер по настоящему изобретению.
ПРИМЕРЫ
Ниже по тексту настоящее изобретение будет описано более подробно с помощью примеров и тестовых примеров, но не следует считать, что изобретение ограничено этими примерами.
Справочный пример 1:
4-{[(2S,6R)-6-(4-бензамидо-2-оксопиримидин-1-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановая кислота, адсорбированная на аминополистирольную смолу
Стадия 1: получение 4-{[(2S,6R)-6-(4-бензамидо-2-оксопиримидин-1(2H)-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановой кислоты
В атмосфере аргона суспендировали 3,44 г N-{1-[(2R,6S)-6-(гидроксиметил)-4-тритилморфолин-2-ил]-2-оксо-1,2-дигидропиримидин-4-ил}бензамида и 1,1 г 4-диметиламинопиридина (4-DMAP) в 50 мл дихлорметана, добавляли к суспензии 0,90 г янтарного ангидрида и затем перемешивали при комнатной температуре в течение 3 часов. К реакционной смеси добавляли 10 мл метанола и концентрировали смесь при пониженном давлении. Остаток экстрагировали этилацетатом и 0,5 М водным раствором дигидрофосфата калия. Полученный органический слой последовательно промывали 0,5 М водным раствором дигидрофосфата калия, водой и насыщенным раствором соли в указанном порядке. Полученный органический слой высушивали над сульфатом натрия и концентрировали при пониженном давлении, получая 4,0 г продукта.
Стадия 2: получение 4-{[(2S,6R)-6-(4-бензамидо-2-оксопиримидин-1-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановой кислоты, адсорбированной на аминополистирольную смолу
Растворяли 4,0 г 4-{[(2S,6R)-6-(4-бензамидо-2-оксопиримидин-1(2H)-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановой кислоты в 200 мл пиридина (обезвоженного) и затем добавляли к раствору 0,73 г DMAP и 11,5 г гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида. Затем к смеси добавляли 25,0 г аминополистирольной смолы Primer support 200 amino (производства GE Healthcare Japan Co., Ltd., 17-5214-97) и 8,5 мл триэтиламина, после чего встряхивали при комнатной температуре в течение 4 дней. По окончании реакции отделяли смолу фильтрованием. Полученную смолу последовательно промывали пиридином, метанолом и дихлорметаном в указанном порядке и высушивали при пониженном давлении. К полученной смоле добавляли 200 мл тетрагидрофурана (обезвоженного), 15 мл уксусного ангидрида и 15 мл 2,6-лутидина, и встряхивали смесь при комнатной температуре в течение 2 часов. Смолу отделяли фильтрованием, последовательно промывали пиридином, метанолом и дихлорметаном в указанном порядке и высушивали при пониженном давлении, получая 26,7 г продукта.
Количество продукта, адсорбированного на смолу, определяли по количеству молей тритила на грамм смолы по данным измерения поглощения в УФ диапазоне на волне 409 нм с использованием известной методики. Количество действующего вещества, адсорбированного на смолу, составляло 192,2 мкмоль/г.
Условия проведения УФ-измерений:
Прибор: U-2910 (Hitachi, Ltd.)
Растворитель: метансульфоновая кислота
Длина волны: 265 нм
Длина волны: 26
Справочный пример 2:
4-[[(2S,6R)-6-[6-(2-цианоэтокси)-2-[(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановая кислота, адсорбированная на аминополистирольную смолу
Стадия 1: получение N2-(феноксиацетил)гуанозина
Гуанозин (100 г) высушивали при 80°C при пониженном давлении в течение 24 часов. Затем к нему добавляли 500 мл пиридина (безводного) и 500 мл дихлорметана (безводного), к полученной смеси по каплям в атмосфере аргона при температуре 0°C добавляли 401 мл хлортриметилсилана, после чего перемешивали при комнатной температуре в течение 3 часов. Смесь вновь охлаждали льдом и по каплям добавляли к ней 66,3 г феноксиацетилхлорида. Смесь перемешивали в течение еще 3 часов, охлаждая льдом. К реакционному раствору добавляли 500 мл метанола и перемешивали смесь при комнатной температуре в течение ночи. Затем удаляли растворитель отгонкой при пониженном давлении. К остатку добавляли 500 мл метанола и концентрировали при пониженном давлении, и эту стадию повторяли 3 раза. К остатку добавляли 4 л воды и перемешивали смесь в течение часа, охлаждая льдом. Образовавшийся осадок отделяли фильтрованием, последовательно промывали водой и холодным метанолом, и затем высушивали, получая 150,2 г целевого соединения (выход 102%) (сравните: Org.Lett.(2004), vol.6, No.15, 2555-2557).
Стадия 2: п-толуолсульфонат N9-{[(2R,6S)-6-(гидроксиметил)-4-морфолин-2-ил]-6-оксо-6,9-дигидро-1H-пурин-2-ил}-2-феноксиацетамида
В 480 мл метанола суспендировали 30 г соединения, полученного на стадии 1, и к этой суспензии при охлаждении льдом добавляли 130 мл 2 н. хлористоводородной кислоты. Затем к смеси последовательно добавляли 56,8 г тетрагидрата тетрабората аммония и 16,2 г перйодата натрия в указанном порядке и перемешивали смесь при комнатной температуре в течение 3 часов. Реакционную смесь охлаждали льдом и отделяли нерастворимые вещества фильтрованием, после чего промывали 100 мл метанола. Фильтрат и промывную жидкость объединяли и охлаждали смесь льдом. К смеси добавляли 11,52 г 2-пиколинборана. После перемешивания в течение 20 минут, к смеси медленно добавляли 54,6 г моногидрата п-толуолсульфоновой кислоты и затем перемешивали при 4°C в течение ночи. Образовавшийся осадок отделяли фильтрованием, промывали 500 мл холодного метанола и высушивали, получая 17,7 г целевого соединения (выход 43,3%). Регистрировали 1H-ЯМР спектр осадка (1H, c), 7,55 (2H, м), 7,35 (2H, м), 7,10 (2H, д, J=7,82 Гц), 7,00 (3H, м), 5,95 (1H, дд, J=10,64, 2,42 Гц), 4,85 (2H, с), 4,00 (1H, м), 3,90-3,60 (2H, м), 3,50-3,20 (5H, м), 2,90 (1H, м), 2,25 (3H, с).
Стадия 3: получение N9-{(2R,6S)-6-гидроксиметил-4-тритилморфолин-2-ил}-N2-(феноксиацетил)гуанина
Соединение, полученное на стадии 2 (2,0 г), суспендировали в дихлорметане (30 мл) и к суспензии при охлаждении льдом добавляли триэтиламин (13,9 г) и тритилхлорид (18,3 г). Полученную смесь перемешивали при комнатной температуре в течение часа. Реакционную смесь промывали насыщенным водным раствором бикарбоната натрия и затем водой. Органический слой отделяли, высушивали над сульфатом натрия и концентрировали при пониженном давлении. К остатку добавляли смесь 0,2 М буферный раствор цитрата натрия (pH 3)/метанол (1:4 (объем/объем), 40 мл) и перемешивали смесь. Затем добавляли воду (40 мл) и перемешивали суспензию в течение часа при охлаждении льдом. Осадок отделяли фильтрованием, промывали холодным метанолом и высушивали, получая 1,84 г целевого соединения (выход 82,0%).
Стадия 4: получение N9-[(2R,6S)-6-{(трет-бутилдиметилсилилокси)метил}-4-тритилморфолин-2-ил]-N2-(феноксиацетил)гуанина
Соединение, полученное на стадии 3 (38,3 г), растворяли в дихлорметане (300 мл) и к раствору при охлаждении льдом добавляли имидазол (4,64 г) и трет-бутилдиметилсилил хлорид (9,47 г) в указанном порядке. Реакционный раствор перемешивали при комнатной температуре в течение часа. Реакционный раствор промывали 0,2 М буферным раствором цитрата натрия (pH 3) и затем насыщенным раствором соли. Органический слой отделяли, высушивали над сульфатом магния и концентрировали при пониженном давлении, получая 44,1 г неочищенного целевого соединения.
Стадия 5: получение N9-[(2R,6S)-6-{(трет-бутилдиметилсилилокси)метил}-4-тритилморфолин-2-ил]-N2-(феноксиацетил)-O6-триизопропилбензолсульфонил гуанина
Соединение, полученное на стадии 4 (44,1 г), растворяли в дихлорметане (300 мл) и при охлаждении льдом добавляли 4-диметиламинопиридин (0,64 г), триэтиламин (29,2 мл) и триизопропилбензолсульфонилхлорид (19,0 г). Реакционный раствор перемешивали при комнатной температуре в течение часа. Реакционный раствор промывали 1 М водным раствором дигидрофосфата натрия. Органический слой отделяли, высушивали над сульфатом магния и концентрировали при пониженном давлении, получая 60,5 г неочищенного целевого соединения.
Стадия 6: получение N9-[(2R,6S)-6-{(трет-бутилдиметилсилилокси)метил}-4-тритилморфолин-2-ил]-N2-(феноксиацетил)-O6-(2-цианоэтил)гуанина
Соединение, полученное на стадии 5 (60,5 г), растворяли в дихлорметане (300 мл) и к этому раствору при охлаждении льдом добавляли N-метилпирролидин (54,5 мл). Реакционный раствор перемешивали в течение часа при охлаждении льдом. Затем к раствору добавляли этиленцианогидрин (37,2 г) и 1,8-диазабицикло[5.4.0]ундец-7-ен (11,96 г), и раствор перемешивали при охлаждении льдом в течение 2 часов. Реакционный раствор промывали 1 М раствором дигидрофосфата натрия и затем водой. Органический слой отделяли, высушивали над сульфатом магния и концентрировали при пониженном давлении, получая 72,4 г неочищенного целевого соединения.
Стадия 7: получение N9-[(2R,6S)-6-гидроксиметил-4-тритилморфолин-2-ил]-N2-(феноксиацетил)-O6-(2-цианоэтил)гуанина
Соединение, полученное на стадии 6 (72,4 г), растворяли в дихлорметане (300 мл), и к этому раствору добавляли тригидрофторид триэтиламина (21,1 г). Реакционный раствор перемешивали при комнатной температуре в течение 17 часов. Реакционный раствор выливали в холодный насыщенный водный раствор бикарбоната натрия, нейтрализуя реакционный раствор. Затем слой дихлорметана отделяли, высушивали над сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (прибор PSQ100B (производства FUJI SILYSIA CHEMICAL LTD) этот же прибор будет применяться в дальнейшем), получая 14,3 г целевого соединения (выход, начиная со стадии 4: 39,2%).
Стадия 8: получение 4-[[(2S,6S)-6-[6-(2-цианоэтокси)-2-(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановой кислоты, адсорбированной на аминополистирольную смолу
Указанное в заголовке соединение получали способом, аналогичным способу справочного примера 1, за исключением того, что на данной стадии использовали N9-[(2R,6S)-6-гидроксиметил-4-тритилморфолин-2-ил]-N2-(феноксиацетил)-O6-(2-цианоэтил)гуанин вместо N-{1-[(2R,6S)-6-(гидроксиметил)-4-тритилморфолин-2-ил]-2-оксо-1,2-дигидропиримидин-4-ил}бензамида, использованного на стадии 1 справочного примера 1.
Справочный пример 3
4-{[(2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановая кислота, адсорбированная на аминополистирольную смолу
Указанное в заголовке соединение получали способом, аналогичным способу справочного примера 1, за исключением того, что использовали 1-[(2R,6S)-6-(гидроксиметил)-4-тритилморфолин-2-ил]-5-метилпиримидин-2,4-(1H,2H)-дион вместо N-{1-[(2R,6S)-6-(гидроксиметил)-4-тритилморфолин-2-ил]-2-оксо-1,2-дигидропиримидин-4-ил}бензамида, который использовали на стадии 1 справочного примера 1.
Справочный пример 4
4-{[(2S,6R)-6-(6-бензамидпурин-9-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановая кислота, адсорбированная на аминополистрирольную смолу
Указанное в заголовке соединение получали способом, аналогичным способу справочного примера 1, за исключением того, что использовали N-{9-[(2R,6S)-6-(гидроксиметил)-4-тритилморфолин-2-ил]пурин-6-ил}бензамид вместо N-{1-[(2R,6S)-6-(гидроксиметил)-4-тритилморфолин-2-ил]-2-оксо-1,2-дигидропиримидин-4-ил}бензамида, который использовали на стадии 1 справочного примера 1.
Справочный пример 5
1,12-диоксо-1-(4-тритилпиперазин-1-ил)-2,5,8,11-тетраокса-15-пентадекановая кислота, адсорбированная на аминополистирольную смолу
Указанное в заголовке соединение получали способом, аналогичным способу справочного примера 1, за исключением того, что использовали 2-[2-(2-гидроксиэтокси)этокси]этил-4-тритилпиперазин-1-карбоновую кислоту (соединение, описанное в WO 2009/064471) вместо N-{1-[(2R,6S)-6-(гидроксиметил)-4-тритилморфолин-2-ил]-2-оксо-1,2-дигидропиримидин-4-ил}бензамида, который использовали на стадии 1 справочного примера 1.
ЭКЗОН 45
В соответствии с описанием приведенных ниже примеров 1-8 и справочного примера 1, синтезировали различные типы PMO, обозначенные как PMO №№ 1-6 и 8-10 в таблице 5. Полученные PMO растворяли в воде для инъекций (производства Otsuka Pharmaceutical Factory, Inc.). PMO № 7 приобретали у Gene Tools, LLC.
Пример 1: PMO № 1
0,2 г 4-{[(2S,6R)-6-(4-бензамид-2-оксопиримидин-1(2H)-ил)-4-тритилморфолин-2-ил]метокси}-4-оксибутановую кислоту, адсорбированную на аминополистрирольную смолу (справочный пример 1) (26 мкмоль), помещали в колонку с фильтрующим наконечником. Затем запускали показанный ниже цикл синтеза, используя аппарат для синтеза нуклеиновых кислот (AKTA Oligopilot 10 plus). На каждом цикле реакций сочетания добавляли желаемое мономерное морфолино-соединение, получая нуклеотидную последовательность данного примера.
В качестве деблокирующего раствора применялся дихлорметан, содержащий 3% (масса/объем) трифторуксусной кислоты. В качестве нейтрализующего и промывочного раствора использовался раствор, полученный растворением N,N-диизопропилэтиламина до концентрации 10% (объем/объем) и тетрагидрофурана до концентрации 5% (объем/объем) в дихлорметане, содержащем 35% (объем/объем) ацетонитрила. В качестве раствора для реакции сочетания A использовали раствор, полученный растворением морфолинового мономерного соединения в тетрагидрофуране, до концентрации 0,10 М. В качестве раствора для реакции сочетания B использовали раствор, полученный растворением N,N-диизопропилэтиламина до концентрации 20% (объем/объем) и тетрагидрофурана до концентрации 10% (объем/объем) в ацетонитриле. В качестве кэппирующего раствора использовали раствор, полученный растворением 20% (объем/объем) уксусного ангидрида и 30% (объем/объем) 2,6-лутидина в ацетонитриле.
Аминополистрирольную смолу с адсорбированным PMO, синтезированным по описанной выше методике, извлекали из реакционного сосуда и высушивали при комнатной температуре в течение по меньшей мере 2 часов при пониженном давлении. Высушенный PMO, адсорбированный на аминополистирольной смоле, помещали в реакционный сосуд и добавляли 5 мл 28% раствора аммиака в смеси вода/этанол (1/4). Полученную смесь перемешивали при 55°C в течение 15 часов. Аминополистрирольную смолу отделяли фильтрованием и промывали 1 мл смеси вода-этанол (1/4). Полученный фильтрат концентрировали при пониженном давлении. Полученный остаток растворяли в 10 мл смеси 20 мМ уксусная кислота-триэтиламиновый буфер (TEAA буфер) и 10 мл ацетонитрила (4/1) и фильтровали через мембранный фильтр. Полученный фильтрат очищали ВЭЖХ на обращенной фазе. При этом использовались следующие условия.
1 CV=14 мл)
Каждую фракцию анализировали, выделяли целевой продукт и концентрировали при пониженном давлении. К концентрированному остатку добавляли 0,5 мл 2 М водного раствора фосфорной кислоты и перемешивали смесь в течение 15 минут. Затем добавляли 2 мл 2 М раствора гидроксида натрия, подщелачивая раствор, после чего фильтровали через мембранный фильтр (0,45 мкм).
Полученный водный раствор, содержащий целевой продукт, очищали на колонке с анионообменной смолой. При этом использовались следующие условия.
1 CV=8,5 мл)
1 М водный раствор хлорида натрия
Каждую фракцию анализировали (с помощью ВЭЖХ), и получали целевой продукт в виде водного раствора. К полученному водному раствору для нейтрализации добавляли 0,1 М фосфатный буфер (pH 6,0). Затем из полученной смеси удаляли минеральные компоненты ВЭЖХ на обращенной фазе в описанных ниже условиях.
1 CV=4 мл)
Выделяли целевой продукт и смесь концентрировали при пониженном давлении. Полученный остаток растворяли в воде. Полученный раствор подвергали лиофилизации, получая 1,5 мг целевого соединения в виде белого твердого вещества, напоминающего вату.
ESI-TOF-МС (ионизация электрораспылением времяпролетная масс-спектроскопия) вычислено: 6877,8; найдено: 6877,4.
Пример 2: PMO № 3
Соединение данного примера получали в соответствии с методикой примера 1
ESI-TOF-МС вычислено: 6862,8; найдено: 6862,5.
Пример 3: PMO № 2
Соединение данного примера получали в соответствии с методикой примера 1
ESI-TOF-МС вычислено: 6862,8; найдено: 6862,3.
Пример 4: PMO № 4
Соединение данного примера получали в соответствии с методикой примера 1, за исключением того, что в качестве исходного вещества использовали 4-[[(2S,6R)-6-[6-(2-цианоэтокси)-2-[(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 2).
ESI-TOF-МС вычислено: 6902,8; найдено: 6902,3.
Пример 5: PMO № 5
Соединение данного примера получали в соответствии с методикой примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6902,8; найдено: 6902,4.
Пример 6: PMO № 8
Соединение данного примера получали в соответствии с методикой примера 1
ESI-TOF-МС вычислено: 6547,5; найдено: 6547,2.
Пример 7: PMO № 9
Соединение данного примера получали в соответствии с методикой примера 1
ESI-TOF-МС вычислено: 6547,5; найдено: 6547,2.
Пример 8: PMO № 10
Соединение данного примера получали в соответствии с методикой примера 1, за исключением того, что в качестве исходного вещества использовали 1,12-диоксо-1-(4-тритилпиперазин-1-ил)-2,5,8,11-тетраокса-15-пентадекановую кислоту, нанесенную на аминополистирольную смолу (справочный пример 5).
ESI-TOF-МС вычислено: 7214,1; найдено: 7213,7.
Сравнительный пример 1: PMO № 6
Указанное в заголовке соединение получали в соответствии с методикой примера 1.
ESI-TOF-МС вычислено: 8193,9; найдено: 8195,3.
Тестовый пример 1: исследование in vitro
Проводили эксперименты с использованием антисмысловых олигомеров, имеющих структуру 2'-O-метоксифосфортиоатов (2'-OMe-S-РНК), представленные последовательностями SEQ ID NO:19 - SEQ ID NO:35. Различные антисмысловые олигомеры, применяемые для этого анализа, приобретали у Japan Bio Services. Ниже приведены последовательности этих антисмысловых олигомеров.
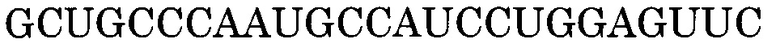
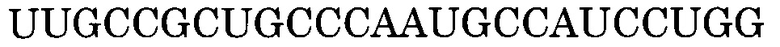
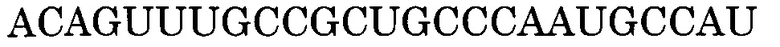
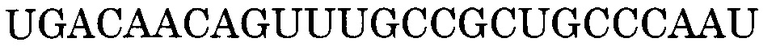
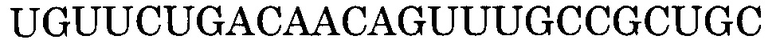

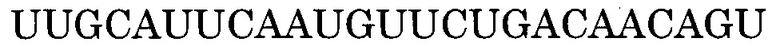

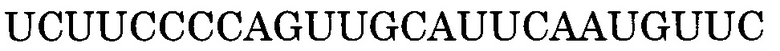

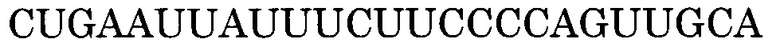
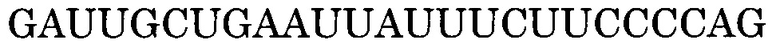
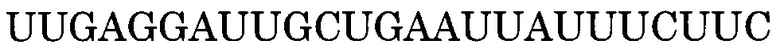
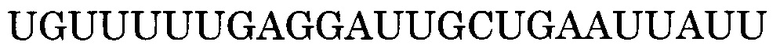

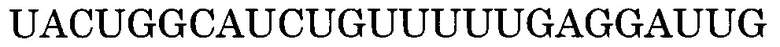

Клетки RD (клеточная линия рабдомиосаркомы человека) помещали в лунки 12-луночных планшетов в количестве 1×105 клеток на лунку и культивировали в 1 мл минимальной питательной среды Игла (EMEM) (производства Sigma, Inc., далее по тексту имеется в виду та же среда), содержащей 10% эмбриональной сыворотки телят (FCS) (производства Invitrogen Corp.) при 37°C и 5% CO2 в течение ночи. Готовили комплексы различных антисмысловых олигомеров (Japan Bio Services) (0,3 или 1 мкМ) для пропуска экзона 45 и Lipofectamine 2000 (производства Invitrogen Corp.) и 100 мкл комплексов добавляли к клеткам RD, заменяя 0,9 мл среды, добиваясь конечной концентрации 30 или 100 нМ.
По окончании добавления клетки культивировали в течение ночи. Клетки дважды промывали PBS (производства Nissui, далее по тексту имеется в виду этот же продукт) и затем добавляли к клеткам 250 мкл ISOGEN (производства Nippon Gene). Препараты оставляли стоять при комнатной температуре в течение нескольких минут для лизиса клеток и собирали лизаты в пробирки Эппендорфа. Осуществляли полное извлечение РНК, согласно протоколу, приложенному к ISOGEN. Общую концентрацию извлеченного РНК определяли с использованием NanoDrop ND-1000 (производства LMS).
Осуществляли RT-PCR с 400 нг экстрагированной РНК, используя набор QIAGEN OneStep RT-PCR. Реакционный раствор готовили в соответствии с протоколом, приложенным к набору. В качестве термоциклера использовали PTC-100 (производства MJ Research). Применяли следующую программу для проведения RT-PCR.
50°C, 30 минут: обратная транскрипция
94°C, 15 минут: термическая денатурация
[94°C, 30 секунд; 60°C, 30 секунд; 72°C, 1 мин]×35 циклов; PCR-амплификация
72°C 10 мин:
Нуклеотидные последовательности прямого праймера и обратного праймера, применяемых для RT-PCR, приведены ниже.
Прямой праймер: 5'-GCTCAGGTCGGATTGACATT-3' (SEQ ID NO:36)
Обратный праймер: 5'-GGGCAACTCTTCCACCAGTA-3' (SEQ ID NO:37)
Продукт реакции, т.е. 1 мкл реакционной смеси PCR, полученной, как описано выше, подвергали анализу с использованием прибора Bioanalyzer (производства Agilent Technologies, Inc.). Измеряли уровень полинуклеотида "A", соответствующий полосе с пропуском экзона 45, и уровень полинуклеотида "B", соответствующий полосе без пропуска экзона 45. Исходя из измеренных значений "A" и "B", определяли эффективность пропуска экзона по следующей формуле:
Эффективность пропуска(%)=A/(A+B)×100
Результаты эксперимента
Результаты экспериментов показаны на фиг.1 и 2. Эти эксперименты показали, что если антисмысловые олигомеры соответствуют 1-у - 25-у или 6-у - 30-у нуклеотидам, считая от 5'-конца экзона 45 в гене дистрофина человека, пропуск экзона 45 мог происходить с большей эффективностью, чем в случае антисмысловых олигомеров, соответствующих 7-у - 31-у нуклеотидам, считая от 5'-конца экзона 45.
Тестовый пример 2: исследование in vitro
Используя набор Amaxa Cell Line Nucleofector Kit L на основе Nucleofector II (Lonza), трансфецировали 3,5×105 клетки RD (клеточная линия рабдомиосаркомы человека) 1, 3 или 10 мкМ олигомерами PMO №№ 1-5 и 8-10 по настоящему изобретению и антисмысловыми олигомерами PMO №№ 6 и 7. Использовали программу T-030.
После трансфекции клетки культивировали в течение 3 дней в 2 мл минимальной питательной среды Игла (EMEM) (производства Sigma, далее по тексту подразумевается такой же препарат), содержащей 10% сыворотку эмбрионов телят (FCS) (производства Invitrogen) при 37°C и 5% CO2. Клетки дважды промывали PBS (производства Nissui, далее по тексту подразумевается такой же препарат) и к клеткам добавляли 500 мкл ISOGEN (производства Nippone Gene). Клеточные препараты оставляли стоять при комнатной температуре в течение нескольких минут для лизиса клеток и собирали лизаты в пробирки Эппендорфа. Осуществляли полное извлечение РНК, согласно протоколу, приложенному к ISOGEN. Общую концентрацию извлеченного РНК определяли с использованием NanoDrop ND-1000 (производства LMS).
Осуществляли RT-PCR с 400 нг изолированной РНК, используя набор QIAGEN OneStep RT-PCR (производства QIAGEN). Реакционный раствор готовили в соответствии с протоколом, приложенным к набору. В качестве термоциклера использовали PTC-100 (производства MJ Research). Применяли следующую программу для проведения RT-PCR.
50°C, 30 минут: обратная транскрипция
94°C, 15 минут: термическая денатурация
[94°C, 30 секунд; 60°C, 30 секунд; 72°C, 1 мин]×35 циклов; PCR-амплификация
72°C 10 мин:
Нуклеотидные последовательности прямого праймера и обратного праймера, применяемых для RT-PCR, приведены ниже.
Прямой праймер: 5'-GCTCAGGTCGGATTGACATT-3' (SEQ ID NO:36)
Обратный праймер: 5'-GGGCAACTCTTCCACCAGTA-3' (SEQ ID NO:37)
Продукт реакции, т.е. 1 мкл реакционной смеси PCR, полученной, как описано выше, подвергали анализу с использованием прибора Bioanalyzer (производства Agilent Technologies, Inc.).
Измеряли уровень полинуклеотида "A", соответствующий полосе с пропуском экзона 45, и уровень полинуклеотида "B", соответствующий полосе без пропуска экзона 45. Исходя из измеренных значений "A" и "B", определяли эффективность пропуска экзона по следующей формуле:
Эффективность пропуска(%)=A/(A+B)×100
Результаты эксперимента
Результаты показаны на фиг. 3, 4, 14 и 15. Эти эксперименты показали, что олигомеры PMO №№ 1 и 3 по настоящему изобретению вызывали пропуск экзона 45 в клетках RD с эффективностью, эквивалентной эффективности антисмыслового олигомера PMO № 6 (фиг. 3, 4). Кроме того, эксперименты показали, что олигомеры PMO №№ 1, 2 и 3 по настоящему изобретению вызывают пропуск экзона с более высокой эффективностью, чем антисмысловой олигомер PMO № 7 (фиг.14). Помимо этого, эксперименты показали, что олигомер PMO № 3 вызывал пропуск экзона 45 с более высокой эффективностью, чем антисмысловой олигомер PMO № 10, концевая структура которого отличается от структуры PMO № 3 (фиг.15).
Тестовый пример 3: исследование in vitro с использованием фибробластов человека
Ген человека myoD (SEQ ID NO:38) вводили в клетки GM05017 (человеческие фибробласты, полученные у пациента с DMD, Coriell Institute for Medical Research), используя ретровирусный вектор коэкспрессии ZsGreen1.
После инкубирования в течение 4-5 дней, ZsGreen-положительные фибробласты, трансформированные геном MyoD, собирали с помощью FACS и помещали в лунки 12-луночного планшета в количестве 5×104/см2. В качестве ростовой среды использовали 1 мл среды Игла, модифицированной Дульбекко: питательная смесь F-12 (DMEM F-12) (Invitrogen Corp.), содержащей 10% FCS и 1% пенициллин/стрептомицин (P/S) (Sigma-Aldrich, Inc.).
Через 24 часа среду заменяли средой для дифференцировки (DMEM/F-12, содержащей 2% лошадиной сыворотки (Invitrogen Corp.), 1% P/S and ITS Liquid Media Supplement (Sigma, Inc.)). Среду меняли каждый 2-3 дня и продолжали инкубирование в течение 12-14 дней для дифференцировки в мышечные трубочки.
Затем среду для дифференцировки заменяли средой для дифференцировки, содержащей 6 мкМ Endo-Porter (Gene Tools) и добавляли к смеси морфолино-олигомер до конечной концентрации 10 мкМ. После инкубирования в течение 48 часов из клеток полностью извлекали РНК, используя TRIzol (производства Invitrogen Corp.). Проводили RT-PCR с 50 нг изолированной РНК, используя набор QIAGEN OneStep RT-PCR. Реакционный раствор готовили согласно протоколу, приложенному к набору. В качестве термоциклера использовали iCycler (производства Bio-Rad). Использовали следующую программу RT-PCR:
50°C, 30 минут: обратная транскрипция
94°C, 15 минут: термическая денатурация
[94°C, 1 мин; 60°C, 1 мин; 72°C, 1 мин]×35 циклов; PCR-амплификация
72°C 7 мин: термическая инактивация полимеразы
Использовали праймеры hDMD44F и hDMD46R.
hDMD44F: 5'-CCTGAGAATTGGGAACATGC-3' (SEQ ID NO:39)
hDMD46R: 5'-TTGCTGCTCTTTTCCAGGTT-3' (SEQ ID NO:40)
Продукты описанной выше RT-PCR разделяли электрофорезом на 2% агарозном геле и полученные гелевые изображения фиксировали с помощью GeneFlash (Syngene). Используя Image J (производства National Institutes of Health) измеряли уровень полинуклеотидов "A", соответствующий полосе с пропуском экзона 45, и уровень полинуклеотидов "B", соответствующий полосе без пропуска экзона 45. Исходя из измеренных значений "A" и "B", определяли эффективность пропуска по следующей формуле:
Эффективность пропуска(%)=A/(A+B)×100
Результаты экспериментов
Результаты экспериментов показаны на фиг.5. Эксперименты показали, что олигомер PMO № 3 по настоящему изобретению вызывал пропуск экзона 45 в клетках GM05017 с высокой эффективностью.
ЭКЗОН 55
В соответствии с описанием приведенных ниже примеров 9-19, синтезировали различные типы PMO обозначенные в таблице 11, как PMO №№ 11-14 и 16-22. Полученные PMO растворяли в воде для инъекций (производства Otsuka Pharmaceutical Factory, Inc.). PMO № 15 приобретали у Gene Tools, LLC.
Пример 9: PMO № 11
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-{[(2S,6R)-6-(6-бензамидопурин-9-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 4).
ESI-TOF-МС вычислено: 6807,8; найдено: 6807,0.
Пример 10: PMO № 12
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6822,8; найдено: 6822,5.
Пример 11: PMO № 13
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6837,8; найдено: 6837,3.
Пример 12: PMO № 14
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-[[(2S,6R)-6-(6-бензамидопурин-9-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 4).
ESI-TOF-МС вычислено: 6861,8; найдено: 6861,4.
Пример 13: PMO № 16
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6812,8; найдено: 6812,7.
Пример 14: PMO № 17
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-[[(2S,6R)-6-[6-(2-цианоэтокси)-2-[(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 2).
ESI-TOF-МС вычислено: 6852,8; найдено: 6852,7.
Пример 15: PMO № 18
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-[[(2S,6R)-6-[6-(2-цианоэтокси)-2-[(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 2).
ESI-TOF-МС вычислено: 6901,8; найдено: 6901,5.
Пример 16: PMO № 19
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6901,8; найдено: 6901,7.
Пример 17: PMO № 20
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-[[(2S,6R)-6-[6-(2-цианоэтокси)-2-[(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 2).
ESI-TOF-МС вычислено: 6522,5; найдено: 6522,0.
Пример 18: PMO № 21
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-{[(2S,6R)-6-(6-бензамидопурин-9-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 4).
ESI-TOF-МС вычислено: 6546,5; найдено: 6546,0.
Пример 19: PMO № 22
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 1,12-диоксо-1-(4-тритилпиперазин-1-ил)-2,5,8,11-тетраокса-15-пентадекановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 5).
ESI-TOF-МС вычислено: 7213,1; найдено: 7212,5.
Тестовый пример 4: исследование in vitro
Проводили эксперименты с использованием антисмысловых олигомеров, имеющих структуру 2'-O-метоксифосфортиоатов (2'-OMe-S-РНК), представленные последовательностями SEQ ID NO:49 - SEQ ID NO:68. Различные антисмысловые олигомеры, применяемые для этого анализа, приобретали у Japan Bio Services. Ниже приведены последовательности этих антисмысловых олигомеров.

Эксперименты проводили, используя условия и методики, аналогичные использованным при исследовании экзона 45 (тестовый пример 1) за исключением того, что при проведении RT-PCR применяли приведенные ниже праймеры
Прямой праймер: 5'-CATGGAAGGAGGGTCCCTAT-3' (SEQ ID NO:69)
Обратный праймер: 5'-CTGCCGGCTTAATTCATCAT-3' (SEQ ID NO:70)
Результаты эксперимента
Результаты экспериментов показаны на фиг.6 и 7. Эти эксперименты показали, что если антисмысловые олигомеры соответствуют 1-у - 21-у или 11-у - 31-у нуклеотидам, считая от 5'-конца экзона 55 в гене дистрофина человека, пропуск экзона 55 для этих антисмысловых олигомеров мог происходить с большей эффективностью, чем в случае антисмысловых олигомеров, соответствующих 104-у - 123-у нуклеотидам, считая от 5'-конца экзона 55.
Тестовый пример 5: исследование in vitro
Проводили эксперименты в соответствии с условиями и методикой, описанными выше для экзона 45 (тестовый пример 2), за исключением того, RT-PCR проводили с использованием приведенных ниже праймеров:
Прямой праймер: 5'-CATGGAAGGAGGGTCCCTAT-3' (SEQ ID NO:69)
Обратный праймер: 5'-CTGCCGGCTTAATTCATCAT-3' (SEQ ID NO:70)
Результаты экспериментов
Результаты показаны на фиг. 8, 16 и 17. Проведенные эксперименты показали, что в клетках RD все олигомеры PMO №№ 12, 13 и 14 (H55_8-12 (OH), H55_11-31 (OH) и H55_14-34 (OH)) по настоящему изобретению с высокой эффективностью вызывают пропуск экзона 55. Аналогично, было обнаружено, что олигомеры PMO №№ 14, 16, 17, 18 и 19 (H55_14-34 (OH), H55_12-32 (OH), H55_13-33 (OH), H55_15-35 (OH) и H55_16-36 (OH)) по настоящему изобретению вызывают пропуск экзона 55 в клетках RD с заметно более высокой эффективностью, чем антисмысловой олигомер PMO № 15 (H55_139-156 (GT)) (фиг.16). Олигомер PMO № 14 по настоящему изобретению и олигомер PMO № 21 (H55_15-34 (OH)), который на одно основание короче, чем олигомер PMO № 14, как было установлено, вызывают пропуск экзона 55 с одинаковой эффективностью (фиг.17). Кроме того, проведенные эксперименты показали, что олигомер PMO № 14 по настоящему изобретению вызывает пропуск экзона 55 с такой же эффективностью, как и олигомер PMO № 22 (H55_14-34 (TEG)), концевая структура которого отличается от концевой структуры олигомера PMO № 14 (фиг.17).
ЭКЗОН 44
В соответствии с описанием приведенных ниже примеров 20-29, синтезировали различные типы PMO обозначенные в приведенной ниже таблице 13, как PMO №№ 23-29 и 31-33. Полученные PMO растворяли в воде для инъекций (производства Otsuka Pharmaceutical Factory, Inc.). PMO № 30 приобретали у Gene Tools, LLC.
Пример 20: PMO № 23
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3)
ESI-TOF-МС вычислено: 6918,9; найдено: 6918,3.
Пример 21: PMO № 24
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6903,9; найдено: 6904,2.
Пример 22: PMO № 25
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-{[(2S,6R)-6-(6-бензамидопурин-9-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 4).
ESI-TOF-МС вычислено: 6912,9; найдено: 6912,4.
Пример 23: PMO № 26
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6903,9; найдено: 6904,2.
Пример 24: PMO № 27
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-{[(2S,6R)-6-(6-бензамидопурин-9-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 4).
ESI-TOF-МС вычислено: 6927,9; найдено: 6927,4.
Пример 25: PMO № 28
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6942,9; найдено: 6942,3.
Пример 26: PMO № 29
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6917,9; найдено: 6918,3.
Пример 27: PMO № 31
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-{[(2S,6R)-6-(6-бензамидопурин-9-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 4).
ESI-TOF-МС вычислено: 6573,6; найдено: 6572,4.
Пример 28: PMO № 32
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6588,6; найдено: 6588,3.
Пример 29: PMO № 33
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 1,12-диоксо-1-(4-тритилпиперазин-1-ил)-2,5,8,11-тетраокса-15-пентадекановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 5).
ESI-TOF-МС вычислено: 7255,2; найдено: 7254,7.
Тестовый пример 6: исследование in vitro
Проводили эксперименты с использованием антисмысловых олигомеров, имеющих структуру 2'-O-метоксифосфортиоатов (2'-OMe-S-РНК), представленных последовательностями SEQ ID NO:82 - SEQ ID NO:95 и SEQ ID NO:109 - SEQ ID NO:118. Различные антисмысловые олигомеры, применяемые для этого анализа, приобретали у Japan Bio Services. Ниже приведены последовательности этих антисмысловых олигомеров.
Эксперименты проводили, используя условия и методики, аналогичные использованным при исследовании экзона 45 (тестовый пример 1).
Результаты эксперимента
Результаты экспериментов показаны на фиг. 9 и 10. Эти эксперименты показали, что если антисмысловые олигомеры соответствуют 11-у - 32-у или 26-у - 47-у нуклеотидам, считая от 5'-конца экзона 44 в гене дистрофина человека, пропуск экзона 44 для этих антисмысловых олигомеров мог происходить с той же эффективностью, как и в случае антисмысловых олигомеров, соответствующих 62-у - 81-у нуклеотидам, считая от 5'-конца экзона 44.
Тестовый пример 7: исследование in vitro
Проводили эксперименты в соответствии с условиями и методикой, описанными выше для экзона 45 (тестовый пример 2).
Результаты экспериментов
Результаты представлены на фиг. 11, 12 и 18. Проведенные эксперименты показали, что в клетках RD олигомеры PMO №№ 24 и 26 (H44_25-45 (OH) и H44_27-47 (OH)) по настоящему изобретению вызывают пропуск экзона 44 с той же эффективностью, что и антисмысловой олигомер PMO № 30 (H44_10-39 (OH)) (фиг.11, 12). Олигомер PMO № 26 по настоящему изобретению и олигомер PMO № 31 (H44_27-46 (OH)), который на одно основание короче, чем олигомер PMO № 26, как было установлено, вызывают пропуск экзона 44 с одинаковой эффективностью (фиг.18). Кроме того, было обнаружено, что олигомер PMO № 26 по настоящему изобретению вызывает пропуск экзона 44 с такой же эффективностью, как и олигомер PMO № 33 (H44_27-47 (TEG)), который имеет концевую структуру, отличную от олигомера PMO № 26 (фиг.18).
ЭКЗОН 50
В соответствии с описанием приведенных ниже примеров 30-39, синтезировали различные типы PMO обозначенные в таблице 15, как PMO №№ 34-38 и 41-45. Полученные PMO растворяли в воде для инъекций (производства Otsuka Pharmaceutical Factory, Inc.). PMO №№ 39 и 40 приобретали у Gene Tools, LLC.
Пример 30: PMO № 34
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-{[(2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6861,8; найдено: 6861,8.
Пример 31: PMO № 35
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-{[(2S,6R)-6-(6-бензамидопурин-9-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 4).
ESI-TOF-МС вычислено: 6885,8; найдено: 6885,9.
Пример 32: PMO № 36
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-[[(2S,6R)-6-[6-(2-цианоэтокси)-2-[(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 2).
ESI-TOF-МС вычислено: 6925,9; найдено: 6925,9.
Пример 33: PMO № 37
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-[[(2S,6R)-6-[6-(2-цианоэтокси)-2-[(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 2).
ESI-TOF-МС вычислено: 6950,9; найдено: 6950,9.
Пример 34: PMO № 38
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-[[(2S,6R)-6-[6-(2-цианоэтокси)-2-[(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 2).
ESI-TOF-МС вычислено: 6990,9; найдено: 6991,0.
Пример 35: PMO № 41
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-[[(2S,6R)-6-[6-(2-цианоэтокси)-2-[(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 2).
ESI-TOF-МС вычислено: 6635,6; найдено: 6635,0.
Пример 36: PMO № 42
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-[[(2S,6R)-6-[6-(2-цианоэтокси)-2-[(2-феноксиацетил)амино]пурин-9-ил]-4-тритилморфолин-2-ил]метокси]-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 2).
ESI-TOF-МС вычислено: 6635,6; найдено: 6634,9.
Пример 37: PMO № 43
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-(((2S,6R)-6-(5-метил-2,4-диоксо-3,4-дигидропиримидин-1(2H)-ил)-4-тритилморфолин-2-ил)метокси)-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 3).
ESI-TOF-МС вычислено: 6965,9; найдено: 6965,2.
Пример 38: PMO № 44
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 4-{[(2S,6R)-6-(6-бензамидопурин-9-ил)-4-тритилморфолин-2-ил]метокси}-4-оксобутановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 4).
ESI-TOF-МС вычислено: 6949,9; найдено: 6949,2.
Пример 39: PMO № 45
Указанное в заголовке соединение получали по методике примера 1, за исключением того, что в качестве исходного вещества использовали 1,12-диоксо-1-(4-тритилпиперазин-1-ил)-2,5,8,11-тетраокса-15-пентадекановую кислоту, адсорбированную на аминополистирольную смолу (справочный пример 5).
ESI-TOF-МС вычислено: 7342,2; найдено: 7341,6.
Тестовый пример 8: исследование in vitro
Эксперименты проводили, используя условия и методики, аналогичные использованным при исследовании экзона 45 (тестовый пример 2) за исключением того, что при проведении RT-PCR применяли приведенные ниже праймеры в концентрациях 0,1, 0,3 или 1 мкМ.
Прямой праймер: 5'-AACAACCGGATGTGGAAGAG-3' (SEQ ID NO:103)
Обратный праймер: 5'-TTGGAGATGGCAGTTTCCTT-3' (SEQ ID NO:104)
Результаты эксперимента
Результаты экспериментов показаны на фиг.13 и 19. Эти эксперименты показали, что в клетках RD олигомер PMO № 38 (H50_107-127 (OH)) по настоящему изобретению вызывал пропуск экзона 50 с более высокой эффективностью, чем антисмысловые олигомеры PMO № 39 или 40 (H50_90-114 (GT), H50_103-127 (GT)). Кроме того, эксперименты показали, что олигомер PMO № 38 вызывал пропуск экзона 50 с более высокой эффективностью, чем олигомер PMO № 45 (H50_107-127 (TEG)), концевая структура которого отличается от олигомера PMO № 28 (фиг.19).
Тестовый пример 9: исследование пропуска экзона 44 in vitro с использованием фибробластов человека
Активность при инициировании пропуска экзона 44 определяли с использованием клеток GM05112 (человеческие фибробласты, полученные у пациента с DMD, с делецией экзона 45 Coriell Institute for Medical Research). В качестве ростовой среды использовали среду Игла, модифицированную Дульбекко: питательная смесь F-12 (DMEM/F-12) (Invitrogen Corp.), содержащую 10% FCS и 1% пенициллин/стрептомицин (P/S) (Sigma-Aldrich, Inc.), и клетки культивировали при 37°C и 5% CO2.
Клетки культивировали в колбе T225, причем к 35 мл ростовой среды добавляли 2,5 мл ретровируса (вектор коэкспрессии ZsGreen1), вызывающего экспрессию человеческого MyoD (SEQ ID NO: 38), и Полибрен (Sigma-Aldrich, Inc.) до конечной концентрации 8 мкг/мл. После инкубирования при 32°C в течение 2 дней, среду заменяли на свежую ростовую среду и продолжали инкубирование при 37°C в течение 3 дней.
ZsGreen1-положительные фибробласты, трансформированные геном MyoD, собирали с помощью сортировщика клеток BD FACS Aria Cell Sorter (BD Bioscience) и помещали в покрытые коллагеном лунки 24-луночного планшета в количестве 9×104/см2. На следующий день среду заменяли средой для дифференцировки (DMEM/F-12, содержащей 2% лошадиной сыворотки (Invitrogen Corp.), 1% P/S и добавку ITS Liquid Media Supplement (Sigma, Inc.)). Среду меняли каждый 2-3 дня и продолжали инкубирование для дифференцировки в мышечные трубочки.
На 7-й день после замены среды на среду для дифференцировки, среду заменяли средой для дифференцировки, содержащей Endo-Porter (Gene Tools) в конечной концентрации 6 мкМ и олигомеры PMO № 26 и 31 в конечной концентрации 1, 3, 10 мкМ. После инкубирования клеток в течение 7 дней, клетки собирали и полностью извлекали РНК, используя RNeasy Mini Kit (QIAGEN).
Проводили RT-PCR с 50 нг изолированной РНК, используя набор QIAGEN OneStep RT-PCR. Реакционный раствор готовили согласно протоколу, приложенному к набору. В качестве термоциклера использовали iCycler (производства Bio-Rad). Использовали следующую программу RT-PCR:
50°C, 30 мин: обратная транскрипция
95°C, 15 мин: термическая денатурация
[94°C, 1 мин; 60°C, 1 мин; 72°C, 1 мин]×35 циклов; PCR-амплификация
72°C 7 мин: реакция достройки цепи
Нуклеотидные последовательности прямого праймера и обратного праймера, которые использовали для реакции RT-PCR, приведены ниже:
Прямой праймер: 5'-GCTCAGGTCGGATTGACATT-3' (SEQ ID NO:36)
Обратный праймер: 5'-GGGCAACTCTTCCACCAGTA-3' (SEQ ID NO:37)
Продукты описанной выше RT-PCR разделяли электрофорезом на 2% агарозном геле и полученные гелевые изображения регистрировали с помощью анализатора изображений ImageQuant LAS 4000 mini (производства FUJI Film). Используя программное обеспечение, входящее в комплект прибора, измеряли уровень полинуклеотидов "A", соответствующий полосе с пропуском экзона 44, и уровень полинуклеотидов "B", соответствующий полосе без пропуска экзона 44. Исходя из измеренных значений "A" и "B", определяли эффективность пропуска по следующей формуле:
Эффективность пропуска(%)=A/(A+B)×100
Результаты экспериментов
Результаты экспериментов показаны на фиг.20. Эксперименты показали, что олигомеры PMO № 26 и 31 по настоящему изобретению вызывали пропуск экзона 44 в клетках GM05112 с высокой эффективностью.
Тестовый пример 10
Получали фибробласты, трансформированные геном MyoD, используя клетки GM05112, согласно методике тестового примера 9 и осуществляли их дифференцировку в мышечные трубочки. Затем среду для дифференцировки заменяли средой для дифференцировки, содержащей Endo-Porter (Gene Tools) в итоговой концентрации 6 мкМ, и на 6-й день после замены среды на среду для дифференцировки, добавляли к клеткам олигомеры PMO №№ 26 и 31 до конечной концентрации 10 мкМ. После инкубирования в течении 14 дней, клетки собирали скребком, используя буфер для лизиса клеток RIPA (производства Pierce), содержащий смесь ингибиторов протеазы Complete Mini (производства Roche). Клеточный лизат извлекали из клеток путем разрушения клеточных оболочек ультразвуковым прибором Bioruptor UCD-250 (Tosho Denki) и собирали супернатант после центрифугирования. Количественное определение концентрации белка осуществляли с использованием аналитического набора Pierce BCA (Pierce). Определяли поглощение на длине волны 544 нм, используя прибор для считывания планшетов Thermo Appliskan Type 2001 (Thermo Electron).
3 мкг клеточных лизатов подвергали электрофорезу в акриламидном геле NuPAGE Novex Tris-Acetate Gel 3-8% (производства Invitrogen) и переносили на мембрану Immobilon-P (производства Millipore), используя полусухой блоттер. Мембраны с перенесенными препаратами промывали PBS (PBST), содержащим 0,1% Tween20 и блокировали PBST, содержащим 5% блокирующего агента Amersham ECL Prime Blocking (GE Healthcare) в холодильнике в течение ночи. После промывания мембран PBST, их инкубировали с раствором антитела против дистрофина (производства NCL-Dys1, Novokastra), разбавленным в 50 раз составом Can Get Signal1 (производства TOYBO), при комнатной температуре в течение 1 часа. После промывания PBST, мембраны инкубировали в растворе козьего антимышиного IgG антитела, конъюгированного с пероксидазой (170-6516, Bio-Rad), разбавленным в 2500 раз составом Can Get Signal1 (производства TOYBO) при комнатной температуре в течение 10 минут. После промывания PBST, мембраны окрашивали с помощью системы детектирования ECL Plus Western Blotting Detection System (GE Healthcare). Хемолюминисценцию белка дистрофина с пропущенными экзонами 44-45 определяли с помощью анализатора люминисцентных изображений ImageQuant LAS 4000 mini (FUJI Film).
Результаты эксперимента
Результаты вестерн-блоттинга показаны на фиг.21. На фиг.21 стрелка указывает на полосу дистрофина, экспрессия которого подтверждена. Этот эксперимент показал, что олигомеры PMO № 26 и 31 по настоящему изобретению вызывают экспрессию белка дистрофина в клетках GM05112.
Тестовый пример 11: исследование пропуска экзона 50, in vitro анализ с использованием человеческих фибробластов
Получали фибробласты, трансформированные геном MyoD, используя клетки GM05112, и осуществляли дифференцировку в мышечные трубочки согласно методике тестового примера 9.
Затем среду для дифференцировки заменяли средой для дифференцировки, содержащей 6 мкМ Endo-Porter (Gene Tools), и на 12-й день после замены среды на среду для дифференцировки, добавляли олигомер PMO №№ 38 до конечной концентрации 0,1, 0,3, 1, 3, 10 мкМ. После инкубирования в течение 2 дней собирали клетки. РНК полностью извлекали из клеток, проводили RT-PCR и определяли эффективность пропуска по методике тестового примера 9, за исключением того, что для RT-PCR использовали приведенные ниже нуклеотидные последовательности прямого праймера и обратного праймера.
Прямой праймер: 5'-AACAACCGGATGTGGAAGAG-3' (SEQ ID NO:103)
Обратный праймер: 5'-TTGGAGATGGCAGTTTCCTT-3' (SEQ ID NO:104)
Результаты эксперимента
Результаты RT-PCR показаны на фиг.22 и данные по эффективности пропуска экзона 50 приведены на фиг.23. Проведенные эксперименты показали, что в клетках GM05112 олигомер PMO № 38 по настоящему изобретению вызывал пропуск экзона 50 с высокой эффективностью, и значение EC50 составляло 1,3 мкМ.
Тестовый пример 12
Эксперименты по пропуску экзона проводили в условиях и по методике тестового примера 11, за исключением того, что использовали клетки 11-0627 (фибробласты, отобранные у пациента с DMD с дупликацией экзонов 8-9, National Center of Neurology and Psychiatry neuromuscular disorder research repository) и олигомер PMO № 38 добавляли до конечной концентрации 0,1, 1, 10 мкМ.
Результаты экспериментов
Результаты RT-PCR показаны на фиг.26 и эффективность пропуска представлена на фиг.27. Проведенные эксперименты показали, что в клетках 11-0627 олигомер PMO № 38 по настоящему изобретению вызывал пропуск экзона 50 с высокой эффективностью.
Тестовый пример 13: получение лентивируса pLVX-MyoD-ZsGreen1
pLVZ-puro (8120 о.п., Clontech) линеаризовали удалением 1164 о.п. нуклеотидов, которые локализованы от сайта XhoI на сайте множественного клонирования (с положения 2816) до сайта (в положении 3890), который соседствует с 3'-концом кодирующей области гена устойчивости к пуромицину, получая линеаризованный вектор. Затем к этому гену последовательно присоединяли нуклеотидную последовательность (2272 о.п.), которая кодирует человеческий ген MyoD, последовательность IRES, ген ZsGreen 1, получая линеаризованный вектор и затем получали лентивирусный вектор экспрессии pLVX-MyoDZsGreen1 (9210 о.п.).
Клетки Lenti-X 293T помещали на 10 см тарелки, покрытые коллагеном, согласно протоколу, приложенному к системе Lenti-X HTX Packaging System (Clontech). Лентивирусный вектор экспрессии и упаковывающий вектор трансфецировали в фибробласты за три дня до инфицирования. Через четыре часа, среду заменяли и инкубировали клетки в течение трех дней без замены среды. За день до инфицирования, собирали культуральный супернатант в качестве вирусного раствора (примерно 9 мл на 10-см тарелку). Культуральный супернатант фильтровали через клеточный фильтр (40 мкм) и центрифугировали при 500×g в течение 10 мин. Супернатант концентрировали согласно протоколу, приложенному к Lenti-X Concentrator (Clontech) и затем растворяли в среде DMEM/F12 до одной десятой концентрации собранного культурального супернатанта. Этот раствор использовали в качестве вирусного раствора.
Инфицирование фибробластов вирусами
Клетки GMO04364 (фибробласты, полученные у пациента с DMD, с делецией экзонов 51-55, Coriell Institute for Medical Research) помещали в 24-луночные планшеты с коллагеновым покрытием в количестве 3×104 клеток/лунку в день инфицирования. В день инфицирования, в каждую лунку добавляли 400 мкл среды для дифференцировки, 100 мкл вирусного раствора и полибрен до конечной концентрации 8 мкг/мл. Через день после инфицирования среду, содержащую вирус, заменяли на 500 мкл среды для дифференцировки. Среду для дифференцировки заменяли каждые 2 или 3 дня и клетки инкубировали в течение 12 дней, чтобы вызвать дифференцировку в мышечные трубочки.
На 12-й день после замены среды на среду для дифференцировки, среду заменяли на среду для дифференцировки, содержащую Endo-Porter (Gene Tools) в итоговой концентрации 6 мкМ, и добавляли в лунки олигомер PMO № 38 до конечной концентрации 0,1, 0,3 1, 3, 10 мкМ. После инкубирования в течение 2 дней клетки собирали. Эффективность пропуска определяли по методике тестового примера 11, за исключением того, что для проведения RT-PCR использовали показанные ниже нуклеотидные последовательности прямого праймера и обратного праймера.
Прямой праймер: 5'-AACAACCGGATGTGGAAGAG-3' (SEQ ID NO:103)
Обратный праймер: 5'-CTGCCGGCTTAATTCATCAT-3' (SEQ ID NO:70)
Результаты эксперимента
Результаты RT-PCR показаны на фиг.28, и данные по эффективности пропуска приведены на фиг.29. Проведенные эксперименты показали, что в клетках GM04364 олигомер PMO № 38 по настоящему изобретению вызывал пропуск экзона 50 с высокой эффективностью.
Исследование пропуска экзона 55
Тестовый пример 14: анализ in vitro с использованием фибробластов человека
Эксперимент проводили с использованием условий и по методике тестового примера 11, за исключением того, что использовали олигомеры PMO №№ 14 и 21, и при проведении RT-PCR использовали приведенные ниже праймеры.
Прямой праймер: 5'-CATGGAAGGAGGGTCCCTAT-3' (SEQ ID NO:69)
Обратный праймер: 5'-CTGCCGGCTTAATTCATCAT-3' (SEQ ID NO:70)
Результаты эксперимента
Результаты RT-PCR показаны на фиг.24 и данные по эффективности пропуска приведены на фиг.25. Проведенные эксперименты показали, что в клетках GM05112 олигомеры PMO № 14 и 21 по настоящему изобретению вызывали пропуск экзона 55 с высокой эффективностью и значения EC50 составляли 3,5 мкМ и 7,5 мкМ, соответственно.
Тестовый пример 15
Эксперимент проводили с использованием условий и по методике тестового примера 13, за исключением того, что использовали клетки 04-035 (клетки, отобранные у пациента с DMD с одиночной делецией экзона 54, National Center of Neurology and Psychiatry neuromuscular disorder research resource repository), добавляли олигомеры PMO № 14 и 21 до конечной концентрации 0,1, 1 и 10 мкМ и RT-PCR проводили с использованием приведенных ниже праймеров.
Прямой праймер: 5'-CATGGAAGGAGGGTCCCTAT-3' (SEQ ID NO:69)
Обратный праймер: 5'-CTGCCGGCTTAATTCATCAT-3' (SEQ ID NO:70)
Результаты эксперимента
Результаты RT-PCR показаны на фиг.30, и данные по эффективности пропуска приведены на фиг.31. Проведенные эксперименты показали, что в клетках пациентов с DMD с одиночной делецией экзона 54, олигомеры PMO № 14 и 21 по настоящему изобретению вызывали пропуск экзона 55 с высокой эффективностью.
Промышленная применимость
Результаты экспериментов, описанных в тестовых примерах, демонстрируют, что олигомеры по настоящему изобретению с очень высокой эффективностью вызывали пропуск экзонов, как в клетках RD, так и в клетках, отобранных у пациентов с DMD.
Таким образом, олигомеры по настоящему изобретению исключительно хорошо подходят для лечения DMD.
Список последовательностей в виде текста в свободной форме
SEQ ID NO: 9: синтетическая нуклеиновая кислота
SEQ ID NO: 10: синтетическая нуклеиновая кислота
SEQ ID NO: 11: синтетическая нуклеиновая кислота
SEQ ID NO: 12: синтетическая нуклеиновая кислота
SEQ ID NO: 13: синтетическая нуклеиновая кислота
SEQ ID NO: 14: синтетическая нуклеиновая кислота
SEQ ID NO: 15: синтетическая нуклеиновая кислота
SEQ ID NO: 16: синтетическая нуклеиновая кислота
SEQ ID NO: 17: синтетическая нуклеиновая кислота
SEQ ID NO: 18: синтетическая нуклеиновая кислота
SEQ ID NO: 19: синтетическая нуклеиновая кислота
SEQ ID NO: 20: синтетическая нуклеиновая кислота
SEQ ID NO: 21: синтетическая нуклеиновая кислота
SEQ ID NO: 22: синтетическая нуклеиновая кислота
SEQ ID NO: 23: синтетическая нуклеиновая кислота
SEQ ID NO: 24: синтетическая нуклеиновая кислота
SEQ ID NO: 25: синтетическая нуклеиновая кислота
SEQ ID NO: 26: синтетическая нуклеиновая кислота
SEQ ID NO: 27: синтетическая нуклеиновая кислота
SEQ ID NO: 28: синтетическая нуклеиновая кислота
SEQ ID NO: 29: синтетическая нуклеиновая кислота
SEQ ID NO: 30: синтетическая нуклеиновая кислота
SEQ ID NO: 31: синтетическая нуклеиновая кислота
SEQ ID NO: 32: синтетическая нуклеиновая кислота
SEQ ID NO: 33: синтетическая нуклеиновая кислота
SEQ ID NO: 34: синтетическая нуклеиновая кислота
SEQ ID NO: 35: синтетическая нуклеиновая кислота
SEQ ID NO: 36: синтетическая нуклеиновая кислота
SEQ ID NO: 37: синтетическая нуклеиновая кислота
SEQ ID NO: 38: синтетическая нуклеиновая кислота
SEQ ID NO: 39: синтетическая нуклеиновая кислота
SEQ ID NO: 40: синтетическая нуклеиновая кислота
SEQ ID NO: 41: синтетическая нуклеиновая кислота
SEQ ID NO: 42: синтетическая нуклеиновая кислота
SEQ ID NO: 43: синтетическая нуклеиновая кислота
SEQ ID NO: 45: синтетическая нуклеиновая кислота
SEQ ID NO: 46: синтетическая нуклеиновая кислота
SEQ ID NO: 47: синтетическая нуклеиновая кислота
SEQ ID NO: 48: синтетическая нуклеиновая кислота
SEQ ID NO: 49: синтетическая нуклеиновая кислота
SEQ ID NO: 50: синтетическая нуклеиновая кислота
SEQ ID NO: 51: синтетическая нуклеиновая кислота
SEQ ID NO: 52: синтетическая нуклеиновая кислота
SEQ ID NO: 53: синтетическая нуклеиновая кислота
SEQ ID NO: 54: синтетическая нуклеиновая кислота
SEQ ID NO: 55: синтетическая нуклеиновая кислота
SEQ ID NO: 56: синтетическая нуклеиновая кислота
SEQ ID NO: 57: синтетическая нуклеиновая кислота
SEQ ID NO: 58: синтетическая нуклеиновая кислота
SEQ ID NO: 59: синтетическая нуклеиновая кислота
SEQ ID NO: 60: синтетическая нуклеиновая кислота
SEQ ID NO: 61: синтетическая нуклеиновая кислота
SEQ ID NO: 62: синтетическая нуклеиновая кислота
SEQ ID NO: 63: синтетическая нуклеиновая кислота
SEQ ID NO: 64: синтетическая нуклеиновая кислота
SEQ ID NO: 65: синтетическая нуклеиновая кислота
SEQ ID NO: 66: синтетическая нуклеиновая кислота
SEQ ID NO: 67: синтетическая нуклеиновая кислота
SEQ ID NO: 68: синтетическая нуклеиновая кислота
SEQ ID NO: 69: синтетическая нуклеиновая кислота
SEQ ID NO: 70: синтетическая нуклеиновая кислота
SEQ ID NO: 71: синтетическая нуклеиновая кислота
SEQ ID NO: 72: синтетическая нуклеиновая кислота
SEQ ID NO: 73: синтетическая нуклеиновая кислота
SEQ ID NO: 74: синтетическая нуклеиновая кислота
SEQ ID NO: 75: синтетическая нуклеиновая кислота
SEQ ID NO: 76: синтетическая нуклеиновая кислота
SEQ ID NO: 77: синтетическая нуклеиновая кислота
SEQ ID NO: 78: синтетическая нуклеиновая кислота
SEQ ID NO: 79: синтетическая нуклеиновая кислота
SEQ ID NO: 80: синтетическая нуклеиновая кислота
SEQ ID NO: 81: синтетическая нуклеиновая кислота
SEQ ID NO: 82: синтетическая нуклеиновая кислота
SEQ ID NO: 83: синтетическая нуклеиновая кислота
SEQ ID NO: 84: синтетическая нуклеиновая кислота
SEQ ID NO: 85: синтетическая нуклеиновая кислота
SEQ ID NO: 86: синтетическая нуклеиновая кислота
SEQ ID NO: 87: синтетическая нуклеиновая кислота
SEQ ID NO: 88: синтетическая нуклеиновая кислота
SEQ ID NO: 89: синтетическая нуклеиновая кислота
SEQ ID NO: 90: синтетическая нуклеиновая кислота
SEQ ID NO: 91: синтетическая нуклеиновая кислота
SEQ ID NO: 92: синтетическая нуклеиновая кислота
SEQ ID NO: 93: синтетическая нуклеиновая кислота
SEQ ID NO: 94: синтетическая нуклеиновая кислота
SEQ ID NO: 95: синтетическая нуклеиновая кислота
SEQ ID NO: 96: синтетическая нуклеиновая кислота
SEQ ID NO: 97: синтетическая нуклеиновая кислота
SEQ ID NO: 98: синтетическая нуклеиновая кислота
SEQ ID NO: 99: синтетическая нуклеиновая кислота
SEQ ID NO: 100: синтетическая нуклеиновая кислота
SEQ ID NO: 101: синтетическая нуклеиновая кислота
SEQ ID NO: 102: синтетическая нуклеиновая кислота
SEQ ID NO: 103: синтетическая нуклеиновая кислота
SEQ ID NO: 104: синтетическая нуклеиновая кислота
SEQ ID NO: 105: синтетическая нуклеиновая кислота
SEQ ID NO: 106: синтетическая нуклеиновая кислота
SEQ ID NO: 107: синтетическая нуклеиновая кислота
SEQ ID NO: 108: синтетическая нуклеиновая кислота
SEQ ID NO: 109: синтетическая нуклеиновая кислота
SEQ ID NO: 110: синтетическая нуклеиновая кислота
SEQ ID NO: 111: синтетическая нуклеиновая кислота
SEQ ID NO: 112: синтетическая нуклеиновая кислота
SEQ ID NO: 113: синтетическая нуклеиновая кислота
SEQ ID NO: 114: синтетическая нуклеиновая кислота
SEQ ID NO: 115: синтетическая нуклеиновая кислота
SEQ ID NO: 116: синтетическая нуклеиновая кислота
SEQ ID NO: 117: синтетическая нуклеиновая кислота
SEQ ID NO: 118: синтетическая нуклеиновая кислота
SEQ ID NO: 119: синтетическая нуклеиновая кислота
SEQ ID NO: 120: синтетическая нуклеиновая кислота
SEQ ID NO: 121: синтетическая нуклеиновая кислота
SEQ ID NO: 122: синтетическая нуклеиновая кислота
Список последовательностей (см. в конце описания)
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2012 |
|
RU2619184C2 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2012 |
|
RU2651468C1 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2015 |
|
RU2695430C2 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2015 |
|
RU2825834C2 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2011 |
|
RU2567664C2 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2015 |
|
RU2730681C2 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2015 |
|
RU2702424C2 |
| АНТИСМЫСЛОВАЯ НУКЛЕИНОВАЯ КИСЛОТА | 2016 |
|
RU2724554C2 |
| ИНГИБИТОР СИГНАЛА МИОСТАТИНА | 2019 |
|
RU2820270C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИСМЫСЛОВОЙ ОЛИГОНУКЛЕОТИД, И ЕЕ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ МЫШЕЧНОЙ ДИСТРОФИИ ДЮШЕННА | 2019 |
|
RU2799442C2 |

























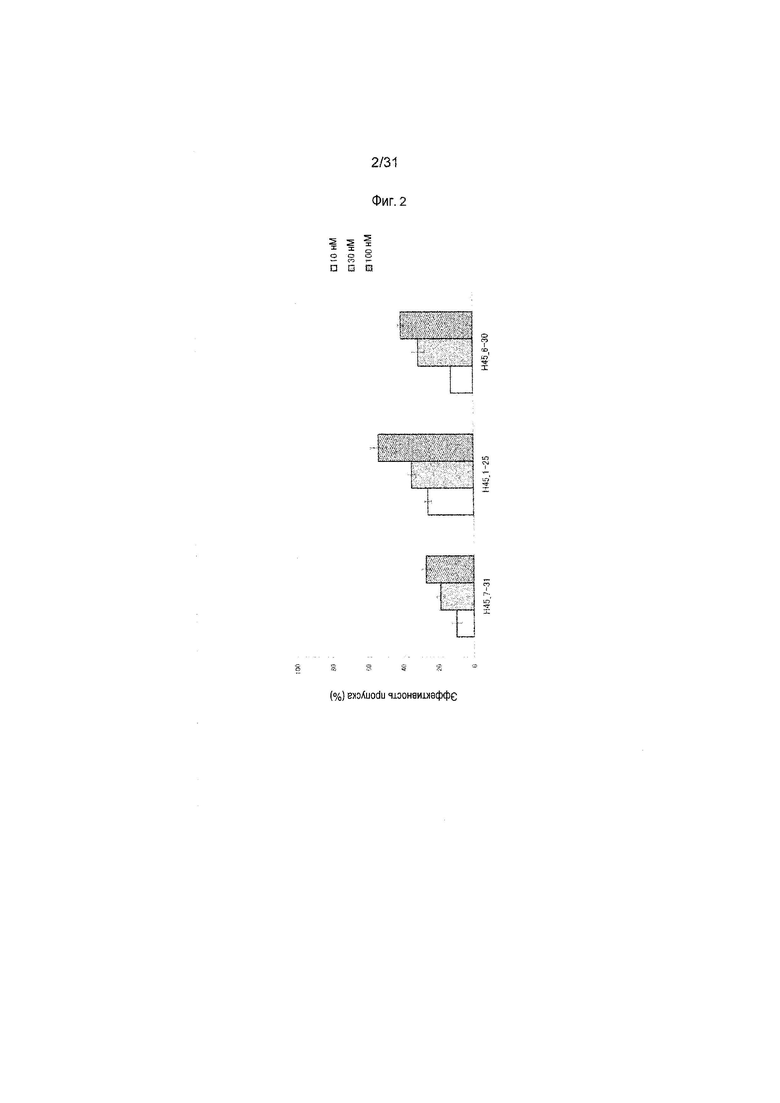

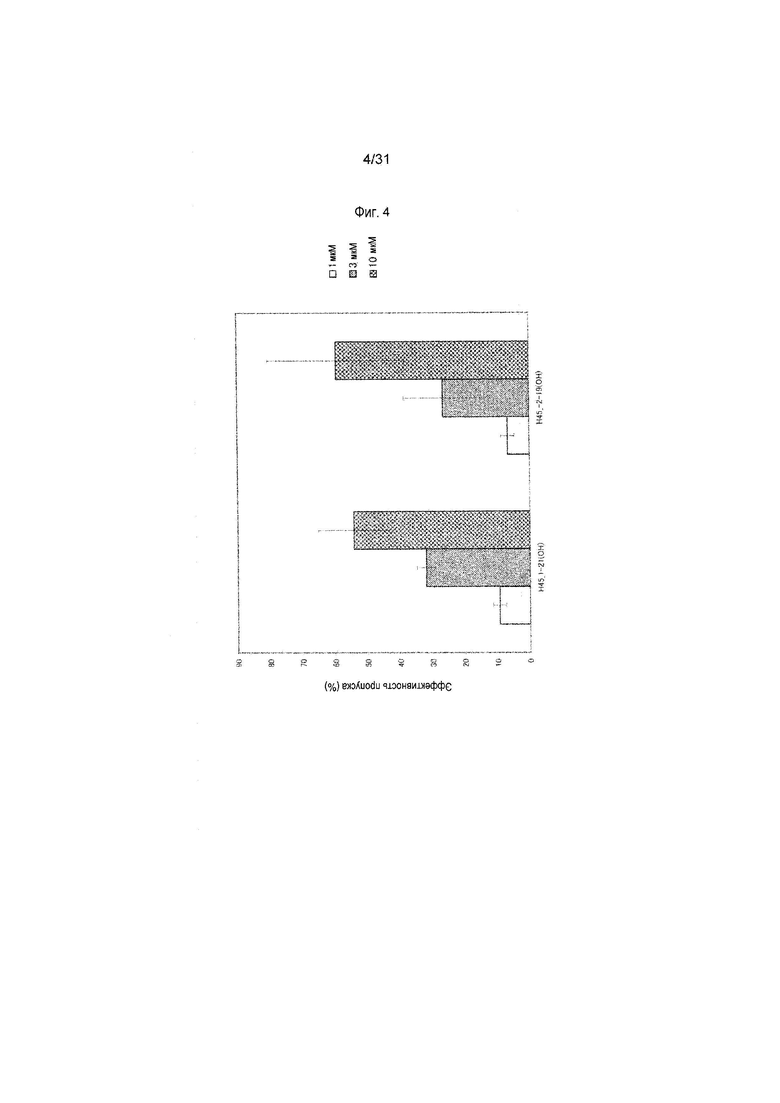


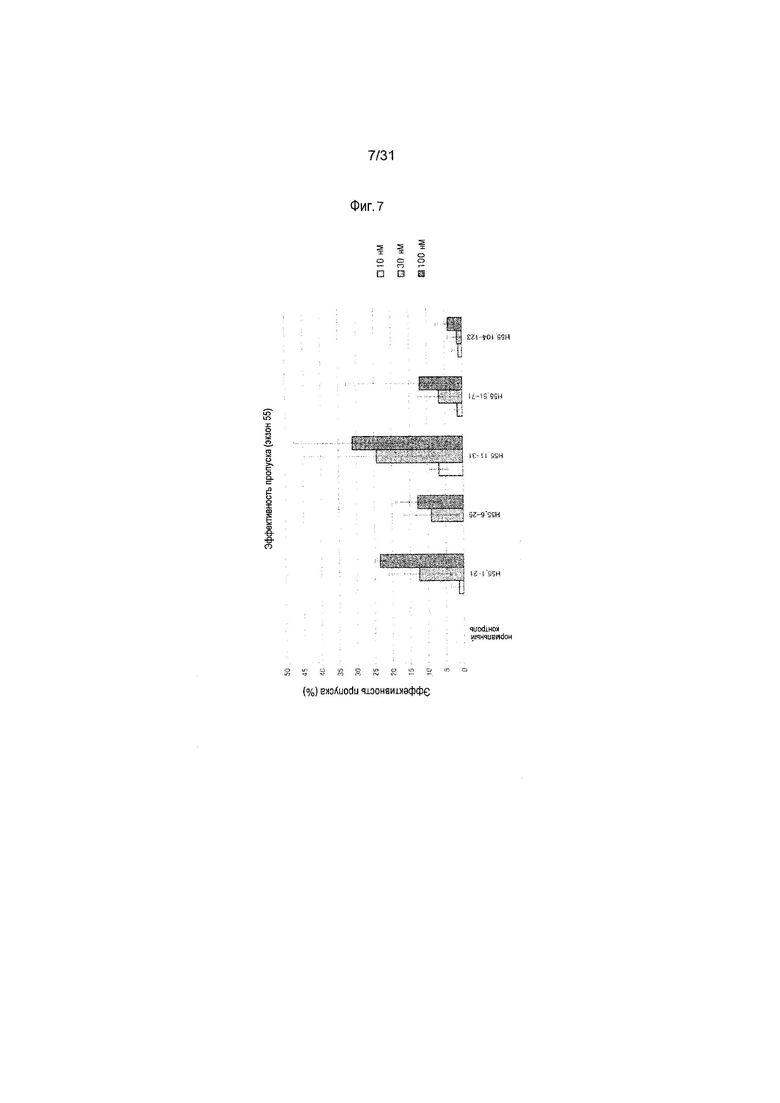




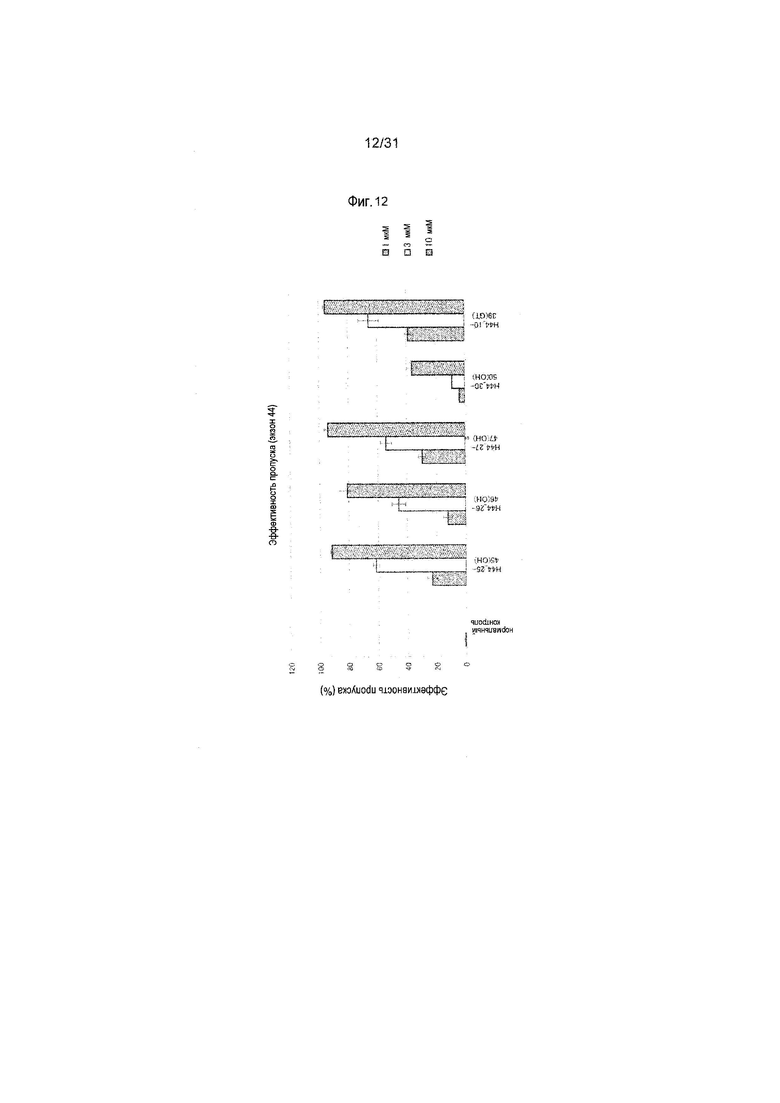


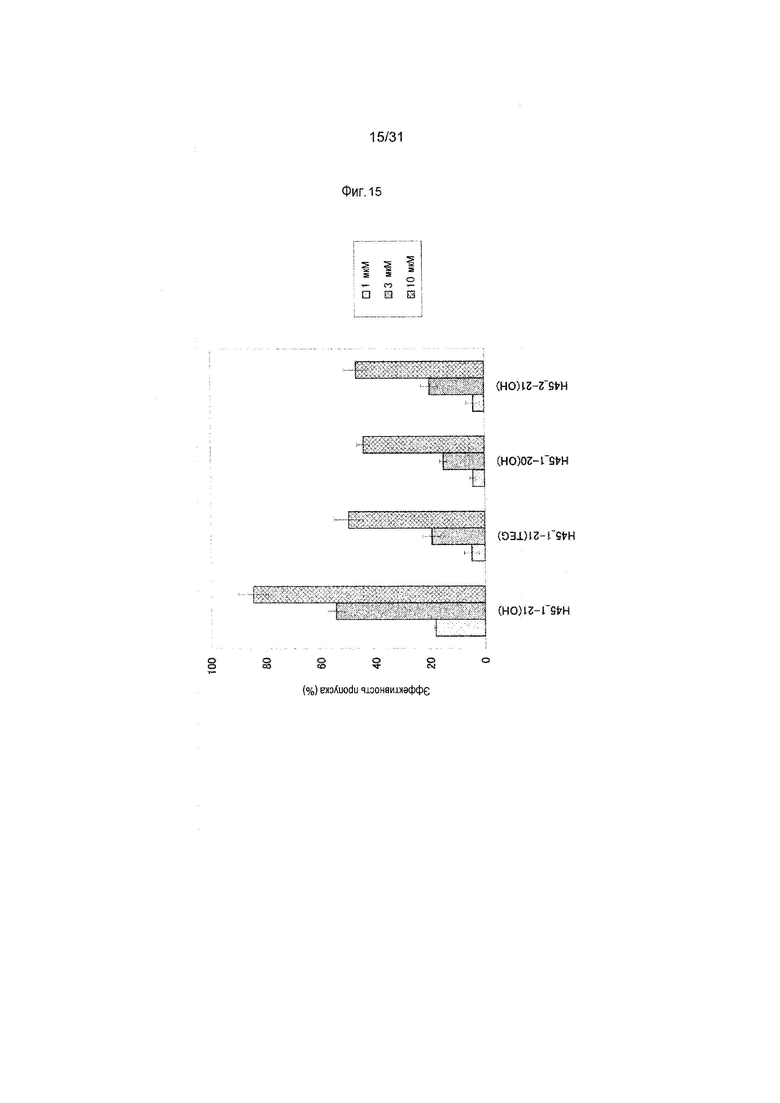












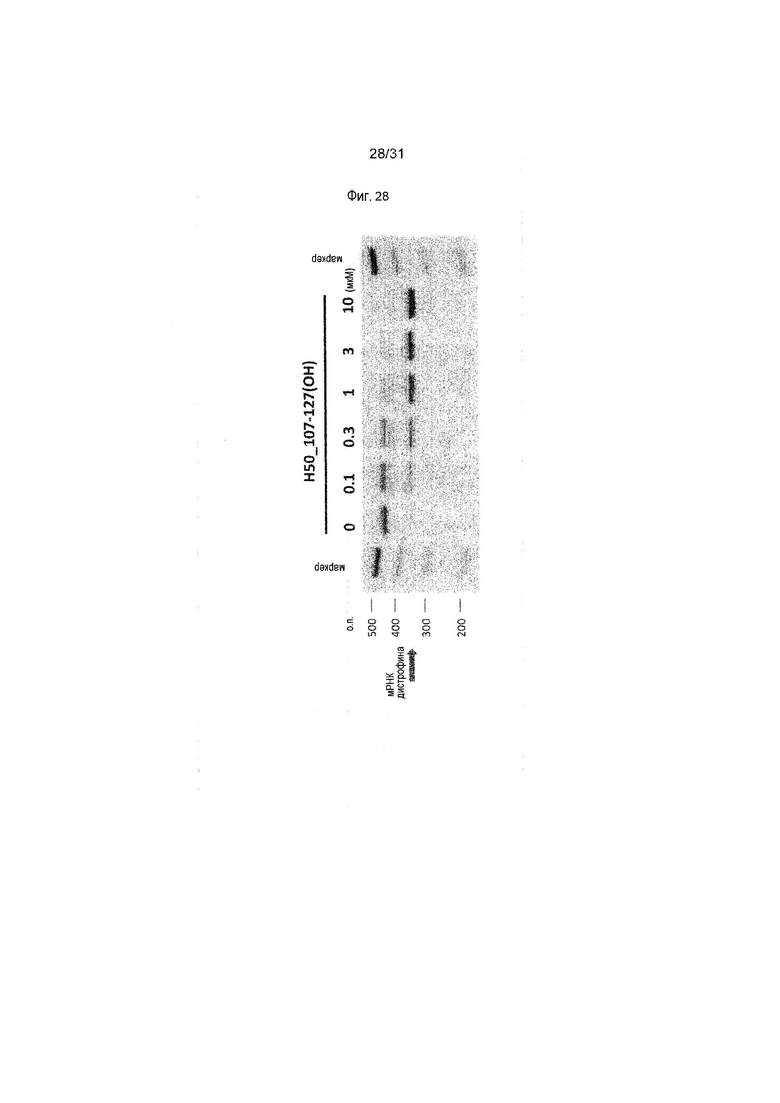
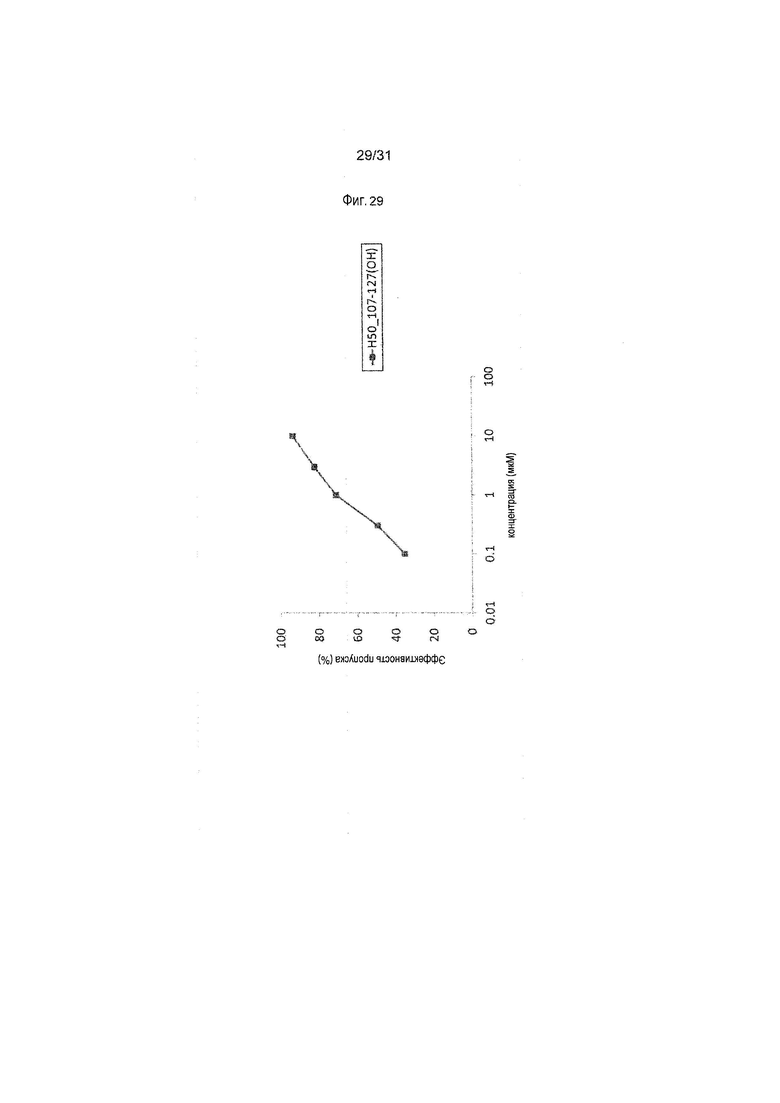
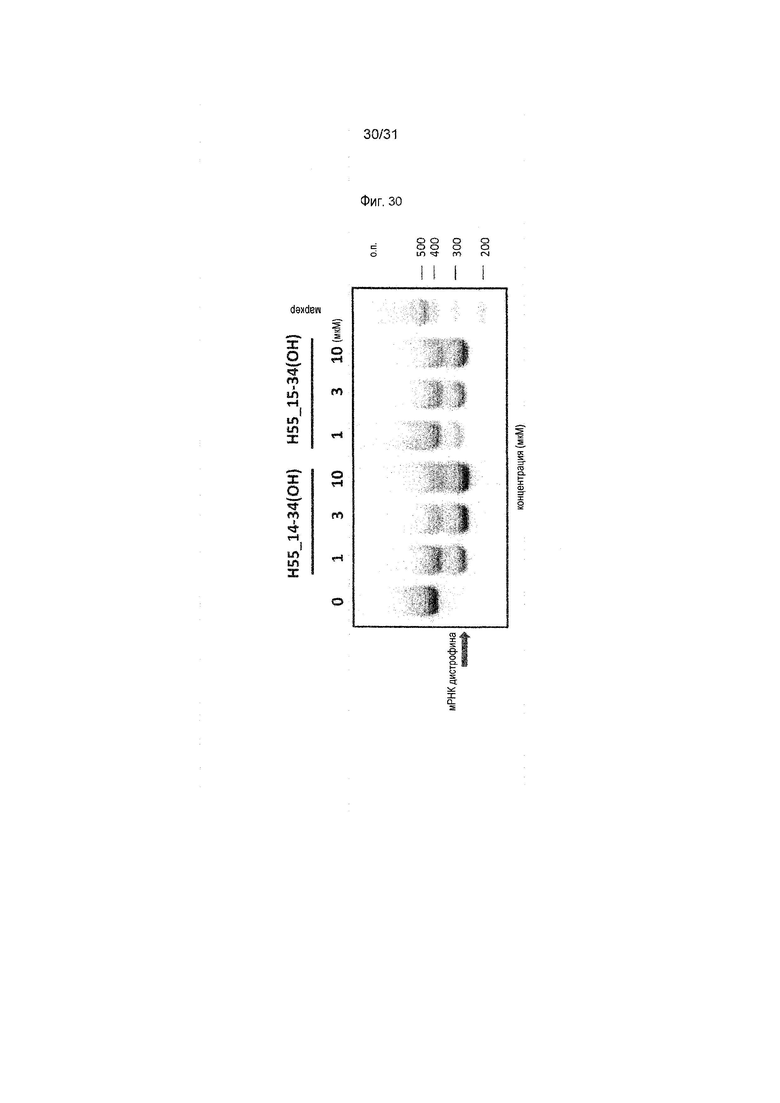

Изобретение относится к биотехнологии. Описан антисмысловой олигомер, который вызывает пропуск 55-го экзона в гене дистрофина человека, состоящий из нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей, состоящих из 10 - 31-го, 10 - 32-го, 11 - 31-го, 11 - 32-го, 13 - 34-го, 13 - 35-го, 13 - 36-го, 14 - 35-го, 14 - 36-го, 15-го – 35-го, 15-го – 36-го, 16 - 34-го, 16 - 35-го или 16 - 36-го нуклеотидов, считая от 5'-конца 55-го экзона гена дистрофина человека. Представлена фармацевтическая композиция, содержащая указанный олигомер. 2 н. и 8 з.п. ф-лы, 31 ил., 15 табл., 39 пр.
1. Антисмысловой олигомер, который вызывает пропуск 55-го экзона в гене дистрофина человека, состоящий из нуклеотидной последовательности, комплементарной любой из нуклеотидных последовательностей, состоящих из 10 - 31-го, 10 - 32-го, 11 - 31-го, 11 - 32-го, 13 - 34-го, 13 - 35-го, 13 - 36-го, 14 - 35-го, 14 - 36-го, 15 – 35-го, 15 – 36-го, 16 - 34-го, 16 - 35-го или 16 - 36-го нуклеотидов, считая от 5'-конца 55-го экзона гена дистрофина человека.
2. Антисмысловой олигомер по п. 1, состоящий из нуклеотидной последовательности, представленной любой из последовательностей, выбранных из группы, состоящей из 160 – 181-го, 159 – 181-го, 160 – 180-го, 159 – 180-го, 157 – 178-го, 156 – 178-го, 155 – 178-го, 156 – 177-го, 155 – 177-го, 156 – 176-го, 155 – 176-го, 157 – 175-го, 156 – 175-го и 155 – 175-го нуклеотидов SEQ ID NO: 5.
3. Антисмысловой олигомер по п. 1 или 2, который представляет собой олигонуклеотид.
4. Антисмысловой олигомер по п. 3, в котором модифицирован остаток сахара и/или область связывания с остатком фосфорной кислоты по меньшей мере одного нуклеотида, являющегося структурным звеном олигонуклеотида.
5. Антисмысловой олигомер по п. 4, где остаток сахара по меньшей мере одного нуклеотида, являющегося структурным звеном олигонуклеотида, представляет собой остаток рибозы, в котором группа 2'-OH заменена на любой фрагмент, выбранный из группы, состоящей из OR, R, R'OR, SH, SR, NH2, NHR, NR2, N3, CN, F, Cl, Br и I (где R означает алкил или арил и R' означает алкилен).
6. Антисмысловой олигомер по п. 4 или 5, где область связывания с остатком фосфорной кислоты по меньшей мере одного нуклеотида, являющегося структурным звеном олигонуклеотида, представляет собой любой фрагмент, выбранный из группы, состоящей из фосфортиоатной связи, фосфордитиоатной связи, алкилфосфонатной связи, фосфорамидатной связи и боранофосфатной связи.
7. Антисмысловой олигомер по п. 1 или 2, который представляет собой морфолино-олигомер.
8. Антисмысловой олигомер по п. 7, который представляет собой фосфордиамидатный морфолино-олигомер.
9. Антисмысловой олигомер по п. 7 или 8, в котором 5'-концевой фрагмент представляет собой любую из групп приведенных ниже химических формул (1)-(3):
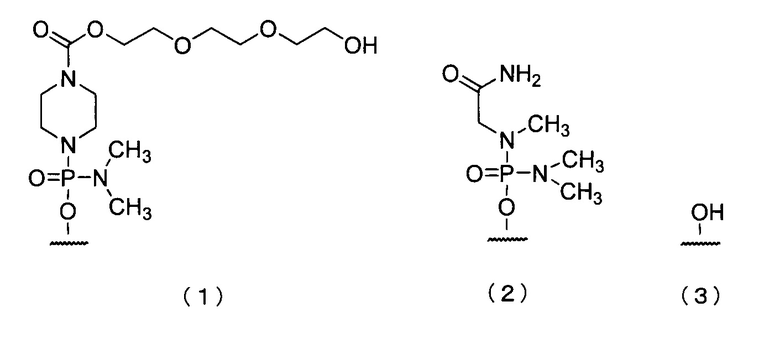
10. Фармацевтическая композиция для лечения мышечной дистрофии, включающая в качестве действующего ингредиента антисмысловой олигомер по любому из пп. 1-9 или его фармацевтически приемлемую соль или гидрат.
| US 7807816 B2 (UNIVERSITY OF WESTERN AUSTRALIA) 05.10.2010 | |||
| ДЕФЕКТНЫЙ РЕКОМБИНАНТНЫЙ АДЕНОВИРУСНЫЙ ВЕКТОР (ВАРИАНТЫ) | 1994 |
|
RU2219241C2 |
Авторы
Даты
2019-03-06—Публикация
2018-03-21—Подача