Уровень техники
Способы лечения рака на основе антител обладают потенциалом к более высокой специфичности и меньшей совокупности побочных эффектов, чем традиционные лекарства. В основе этого лежит точное различение антителами нормальных и неопластических клеток и то, что их механизм действия основан на менее токсичных иммунологических противоопухолевых механизмах, таких как активация комплемента и мобилизация цитотоксических иммунных клеток.
Мишени для терапии на основе антител должны обладать особыми свойствами, которые лежат в основе правильного различения нормальных и неопластических клеток. Очевидно, для разработки эффективных и безопасных лечебных антител будет идеальной такая мишень, которая ограничивается исключительно раковыми клетками и совсем не обнаруживается на нормальных тканях. С другой стороны, основанием для терапевтического индекса и уменьшения побочных эффектов может служить высокий уровень суперэкспрессии на примере рецептора фактора роста эпидермиса человека 2-го типа (HER-2), который в результате амплификации гена является хорошей мишенью для антитела трастузумаб (Herceptin).
Другие мишени для антител, которые либо уже одобрены, либо находятся в клинической разработке для терапии опухолей, обладают особыми свойствами, которые не основываются на количественной суперэкспрессии молекул мишени на опухолевых клетках. В случает антител к протеогликану MUC-1, эпитоп из пептидного повтора на остове мишени недостаточно гликозилирован в опухолевых клетках, поэтому он изменен по сравнению с нормой. В случает антител к CD20 (ритуксимаб), CD52 (Campath-1H) и CD22 (эпратузумаб) антитела-мишени имеют сравнимые уровни экспрессии в раковых клетках и нормальных лимфоцитах. При этом устранение нормальных клеток антителами допустима, так как отрицательные по отношению к мишени стволовые клетки восстанавливают нормальный репертуар лимфоцитов. Другими примерами различной доступности мишеней антител являются онкофетальный антиген (СЕА) и карбоангидраза IX (СА9). Оба антигена экспрессируются в нормальном эпителии толстой кишки и почек, соответственно. Однако интроскопия с помощью радиоактивно меченых антител хорошо отличает опухолевые и нормальные ткани, а цитотоксические антитела хорошо переносятся. Это скорее всего обусловлено ограниченной экспрессией СА9 и СЕА со стороны просвета нормальной ткани эпителия, куда антитела типа IgG не имеют доступа. К той же категории относится и антиген молекул адгезии клеток эпителия (Ер-САМ). Как гомотипическая молекула клеточной адгезии для эпителиальных клеток, она локализуется в межклеточном пространстве. Интересно, что хотя высокоаффинные антитела к Ер-САМ очень токсичны, но антитела с промежуточной аффинностью хорошо переносятся. Это предполагает доступность мишени Ер-САМ на нормальных клетках, но также свидетельствует о том, что кинетика связывания антител может открыть терапевтическое окно.
Одна из возможностей состоит в том, что для антительных подходов могут оказаться привлекательными и другие специфичные к эпителиальным клеткам белки, участвующие в межклеточной адгезии, так как они едва ли доступны антителам в хорошо структурированном эпителии, но могут стать доступными на опухолевых клетках. Поэтому мы проанализировали белки, участвующие в организации архитектуры эпителиальных тканей, на предмет их пригодности в качестве мишеней для лечебных антител. Наше внимание особенно привлек белок клаудин-18.
Молекула клаудина-18 (CLD18) (номера доступа в Genbank: сплайс-вариант 1 (CLD18A1): NP_057453, NM_016369, и сплайс-вариант 2 (CLD18A2): NM_001002026, NP_001002026)) представляет собой интегральный трансмембранный белок с молекулярным весом примерно 27,9/27,72 кД. Клаудины являются интегральными мембранными белками, локализованными в плотных контактах (tight junctions) эпителия и эндотелия. Плотные контакты образуют сеть переплетенных нитей внутримембранных частиц между соседними клетками. Наиболее заметными компонентами в плотных контактах являются трансмембранные белки окклюдин и клаудины. Благодаря своим свойствам сильной межклеточной адгезии они образуют первичный барьер, предотвращающий и контролирующий парацеллюлярный транспорт растворимых веществ и ограничивающий латеральную диффузию мембранных липидов и белков для поддержания клеточной полярности. Белки, образующие плотные контакты, решающим образом участвуют в организации архитектуры эпителиальных тканей. Мы предположили, что такие белки едва ли доступны антителам в хорошо структурированном эпителии, но могут стать доступными на опухолевых клетках.
CLD18 является тетраспанином и поэтому содержит 4 гидрофобных участка. Мы получили данные, свидетельствующие о том, что CLD18 проявляет несколько различных конформаций, которые могут быть избирательно атакованы антителами. Одна из конформаций (конформация-1 CLD18) предполагает, что все 4 гидрофобных участка служат в качестве обычных трансмембранных доменов (ТМ), причем образуются 2 внеклеточные петли (петля 1, окруженная гидрофобным участком 1 и гидрофобным участком 2, и петля 2, окруженная гидрофобными участками 3 и 4), как это описано для подавляющего большинства представителей семейства клаудинов. Вторая конформация (конформация-2 CLD18) предполагает, как это описано для РМР22, другого представителя семейства тетраспанинов (Taylor et al., J. Neurosc. Res. 62:15-27, 2000), что второй и третий гидрофобные домены не полностью пересекают плазматическую мембрану с тем, что участок (петля D3), находящийся между первым и четвертым трансмембранным доменом, является внеклеточным. Третья конформация (конформация-3 CLD18) предполагает наличие большого внеклеточного домена с двумя внутренними гидрофобными участками, окруженными первым и четвертым трансмембранными участками, которые служат в качестве обычных трансмембранных доменов. Благодаря наличию классического сайта N-гликозилирования в петле D3, варианты топологии клаудина-18 - топология-2 CLD18 и топология-3 CLD18 - содержат дополнительный внеклеточный сайт N-гликозилирования.
Еще один уровень сложности в молекулу CLD18 вносит наличие двух разных сплайс-вариантов, которые описаны у мышей и у человека (Niimi, Mol. Cell. Biol. 21:7380-90, 2001). Сплайс-варианты CLD18A1 и CLD18A2 отличаются по первым 21 N-концевым аминокислотам, составляющим первый ТМ и петлю 1, тогда как первичная последовательность белка на С-конце идентична.
CLD18A1 избирательно экспрессируется в нормальном эпителии легких и желудка, тогда как CLD18A2 экспрессируется только в клетках желудка (Niimi, Mol. Cell. Biol. 21:7380-90, 2001). Наиболее важно то, что CLD18A2 приурочен к дифференцированным короткоживущим клеткам эпителия желудка, но отсутствует в районе стволовых клеток желудка. Используя чувствительный метод ОТ-ПЦР, мы показали, что оба варианта совсем не обнаруживаются в других нормальных органах человека, но сильно экспрессируются при некоторых типах рака, включая рак желудка, пищевода, поджелудочной железы и легких, а также линии раковых клеток человека. Экспрессия наиболее заметна у подтипов аденокарциномы этих заболеваний.
Молекулярный вес белка отличается в некоторых опухолях и соседней нормальной ткани. Белок с большим молекулярным весом, наблюдавшийся в здоровой ткани, можно довести до того же молекулярного веса, что наблюдается при раке, путем обработки лизатов тканей дегликозилирующим соединением PNGase F. Это говорит о том, что CLD18 менее гликозилирован при раке, чем в нормальной ткани. Это структурное отличие, вероятно, вызывает изменение эпитопа. Классический мотив N-гликозилирования находится в положении а.к. 116 в домене петли D3 этой молекулы.
Термины "CLD18" и "вариант CLD18" согласно изобретению должны охватывать: (i) сплайс-варианты CLD18, (ii) варианты по N-гликозилированию CLD18, (iii) варианты по конформаций CLD18, (iv) свободные и гомотипически/гетеротипически ассоциированные варианты CLD18, локализованные в межклеточных плотных контактах, и (v) варианты CLD18 раковых и нераковых клеток.
Молекулярные и функциональные характеристики CLD18 делают эту молекулу очень интересной мишенью для антительной терапии рака. В частности, это (i) отсутствие CLD18 в подавляющем большинстве подверженных токсичности нормальных тканей, (ii) приуроченность экспрессии варианта CLD18A2 к восполнимой популяции клеток типа дифференцированных клеток желудка, которые можно восполнить за счет лишенных мишени стволовых клеток желудка, (iii) данные о возможных отличиях по гликозилированию между нормальными и неопластическими клетками, и (iv) наличие различных конформационных топологий. Более того, роль CLD18 в качестве белка плотных контактов может дополнительно способствовать и хорошему терапевтическому индексу. Поскольку раковые клетки экспрессируют клаудины, но часто не образуют классических плотных контактов путем гомотипической и гетеротипической ассоциации клаудинов, как это происходит в нормальной ткани эпителия, то раковые клетки могут содержать значительный пул свободного клаудина, который поддается связыванию с внеклеточными антителами и иммунотерапии. Возможно, что у клаудина эпитопы для связывания в здоровом эпителии экранированы внутри плотных контактах от доступа таких антител.
Кроме того, высокий уровень экспрессии в плазматических мембранах, наблюдавшийся согласно изобретению не только в первичных опухолях, но и в метастазах от экспрессирующих CLD18A2 первичных опухолей, в частности опухолей желудка, делают специфичные к CLD18A2 антитела ценным инструментом для предотвращения, лечения и/или диагностики раковых метастазов, в частности метастазов от опухолей желудка, как-то метастазов лимфатических узлов, перитонеальных метастазов и опухолей Крукенберга.
Целью настоящего изобретения является получение антител, применимых для терапии таких заболеваний, при которых экспрессируется CLD18, как-то раковых заболеваний. Описанные в нем антитела также обладают полезностью в диагностике таких заболеваний.
Раскрытие изобретения
Настоящим изобретением в целом предусмотрены антитела, применимые в качестве лечебных средств для лечения и/или предотвращения заболеваний, связанных с клетками, экспрессирующими CLD18, включая такие раковые заболевания, как рак желудка, рак пищевода, рак поджелудочной железы, рак легких типа немелкоклеточного рака легких (NSCLC), рак яичников, рак толстой кишки, рак печени, рак головы и шеи, рак желчного пузыря и их метастазы, в частности метастазы от рака желудка, как-то опухоли Крукенберга, перитонеальные метастазы и метастазы лимфатических узлов.
В одном аспекте изобретение касается антител, обладающих способностью к связыванию с CLD18. Предпочтительно антитела обладают способностью к связыванию с CLD18, экспрессированным на поверхности клеток, и предпочтительно связываются с одним или несколькими эпитопами, расположенными во внеклеточных участках CLD18, предпочтительно в первом внеклеточном домене (положения аминокислот 29-70 у CLD18). Предпочтительно антитела по изобретению связываются с одним или несколькими пептидами, выбранными из группы, состоящей из SEQ ID NO: 151, 153, 155, 156 и 157. Предпочтительно антитела связываются с раковыми клетками, в частности клетками тех видов рака, что приведены выше, и предпочтительно практически не связываются с нераковыми клетками. Предпочтительно связывание данных антител с клетками, экспрессирующими CLD18, как-то раковыми клетками, вызывает гибель клеток, экспрессирующих CLD18. Предпочтительно антитела связываются с CLD18A1 и CLD18A2, более предпочтительно они связываются с CLD18A2, но не связываются с CLD18A1. Предпочтительно антитела по изобретению связываются с и проявляют специфичность к петле-1 или петле-2 в конформаций-1 CLD. В других предпочтительных воплощениях антитела по изобретению связываются с и проявляют специфичность к петле D3 в конформации-2 CLD, в частности, связываются на или около потенциального сайта N-гликозилирования в положении 116 на петле D3. В других воплощениях антитела по изобретению проявляют специфичность к негликозилированной форме потенциального сайта N-гликозилирования в положении 116 на петле D3.
Предпочтительно в связывании антител по изобретению с CLD18A2 участвует одна или несколько аминокислот, выбранных из группы, состоящей из Ala в положении 42, Asn в положении 45 и Glu в положении 56 у CLD18A2 (SEQ ID NO: 2). Предпочтительно антитела по изобретению не связываются с такими вариантами CLD18A2 или их фрагментами, у которых одна или несколько аминокислот, а предпочтительно все аминокислоты в этих положениях заменены другими аминокислотами, в частности теми аминокислотами, которые находятся в соответствующих положениях у CLD18A1 (SEQ ID NO: 8) (Ala42Ser, Asn45Gln и Glu56Gln).
Гибель клеток предпочтительно вызывается антителами по изобретению при связывании антител с CLD18, экспрессированным данными клетками, более предпочтительно при связывании антител с CLD18A2, экспрессированным данными клетками. В одном воплощении связывание антител по изобретению с CLD18A1, экспрессированным данными клетками, не вызывает гибели данных клеток. Такая гибель клеток может использоваться в терапии, как описано в настоящем изобретении. В частности, гибель клеток может использоваться для лечения или предотвращения рака, в частности раковых метастазов и метастазирования раковых клеток.
Клетки, экспрессирующие CLD18, предпочтительно являются раковыми клетками, в частности, они выбираются из группы, состоящей из опухолевых клеток рака желудка, пищевода, поджелудочной железы, легких, яичников, толстой кишки, печени, головы и шеи и желчного пузыря.
Предпочтительно антитела по изобретению вызывают гибель клеток, индуцируя лизис по механизму обусловленной комплементом цитотоксичности (CDC), лизис по механизму антителозависимой клеточной цитотоксичности (ADCC), апоптоз, гомотопическую адгезию и/или фагоцитоз, предпочтительно вызывая лизис по механизму CDC и/или ADCC.
В одном воплощении антитела по изобретению не вызывают лизиса клеток по механизму CDC.
Предпочтительно лизис клеток по механизму ADCC происходит в присутствии эффекторных клеток, которые в предпочтительных воплощениях выбираются из группы, состоящей из моноцитов, мононуклеаров, NK-клеток и PMN, а фагоцитоз осуществляется макрофагами.
Антитела по изобретению могут представляет собой моноклональные, химерные, гуманизированные или антитела человека либо фрагменты антител и выбираются из группы, состоящей из антител типа IgG1, IgG2, предпочтительно IgG2a и IgG2b, IgG3, IgG4, IgM, IgA1, IgA2, секреторных IgA, IgD и IgE.
В соответствии со всеми аспектами изобретения, CLD18 предпочтительно означает CLD18 человека, предпочтительно CLD18A2 человека, причем CLD18A2 предпочтительно имеет аминокислотную последовательность согласно SEQ ID NO: 2, а CLD18A1 предпочтительно имеет аминокислотную последовательность согласно SEQ ID NO: 8.
В особенно предпочтительных воплощениях антитела по изобретению связываются с нативными эпитопами CLD18, находящимися на поверхности живых клеток. В других предпочтительных воплощениях антитела по изобретению специфичны к раковым клеткам, предпочтительно клеткам рака желудка.
В некоторых воплощениях изобретения CLD18 экспрессируется на поверхности клеток.
Антитела по изобретению могут быть получены способом, включающим стадию иммунизации животного белком или пептидом, включающим аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 2, 4, 6, 16, 18, 20, 21-23, 26-31, 151, 153 и 155-157, либо его иммуногенным фрагментом или производным, либо нуклеиновой кислотой или клетками-хозяевами, экспрессирующими данный белок или пептид либо его иммуногенный фрагмент или производное. Предпочтительно антитела по изобретению специфичны к вышеуказанным белкам, пептидам либо их иммуногенным фрагментам или производным. В связи с белками или пептидами, используемыми при иммунизации, производное означает такой вариант данного белка или пептида, который имеет такие же или близкие иммуногенные свойства, как и белкок или пептид, из которого он происходит. В частности, производное белка или пептида при использовании при иммунизации для получения антител, в частности моноклональных антител, дает антитела с такой же специфичностью, как и антитела, полученные при использовании этого белка или пептида при иммунизации. Например, такое производное может включать делецию, замену или вставку одной или нескольких аминокислот. В частности, оно может включать добавление одной или нескольких аминокислот типа цистеина на N-конец или С-конец или на оба конца либо замену остатков цистеина остатками серина. Данные, представленные в настоящем изобретении, раскрывают те аминокислоты в CLD18, которые не являются критическими для связывания с антителами. Соответственно, белки и пептиды CLD, их иммуногенные фрагменты или производные, описанные в настоящем изобретении, используемые для иммунизации, могут содержать одну или несколько замен аминокислот в тех положениях, которые не являются критическими для связывания с антителами.
В особенно предпочтительном воплощении антитела по изобретению вырабатываются клоном, имеющим номер доступа DSM АСС2737 (182-D1106-055), DSM АСС2738 (182-D1106-056), DSM АСС2739 (182-D1106-057), DSM АСС2740 (182-D1106-058), DSM АСС2741 (182-D1106-059), DSM АСС2742 (182-D1106-062), DSM АСС2743 (182-D1106-067), DSM АСС2745 (182-D758-035), DSM АСС2746 (182-D758-036), DSM АСС2747 (182-D758-040), DSM АСС2748 (182-D1106-061), DSM АСС2808 (182-D1106-279), DSM АСС2809 (182-D1106-294) или DSM АСС2810 (182-D1106-362).
В одном воплощении антитела по изобретению конъюгированы с таким лечебным средством, как токсин, радиоизотоп, лекарственный препарат или цитотоксический агент.
В другом аспекте изобретение касается гибридом, способных вырабатывать антитела по изобретению. Предпочтительными гибридомами являются те, которые имеют номер доступа DSM АСС2737 (182-D1106-055), DSM АСС2738 (182-D1106-056), DSM ACC2739 (182-D1106-057), DSM ACC2740 (182-D1106-058), DSM ACC2741 (182-D1106-059), DSM ACC2742 (182-D1106-062), DSM ACC2743 (182-D1106-067), DSM ACC2745 (182-D758-035), DSM ACC2746 (182-D758-036), DSM ACC2747 (182-D758-040), DSM ACC2748 (182-D1106-061), DSM ACC2808 (182-D1106-279), DSM ACC2809 (182-D1106-294) или DSM ACC2810 (182-D1106-362).
Антитела по изобретению обозначаются по названию антитела, напр., 182-D758-035, и/или по названию клона, вырабатывающего это антитело, напр., 26D12.
Изобретение также касается фармацевтических композиций, содержащих антитела по изобретению и/или их конъюгаты с лечебными средствами, а также фармацевтически приемлемые носители.
В следующем аспекте изобретение касается способа ингибирования роста и/или уничтожения клеток, экспрессирующих CLD18, предпочтительно CLD18A2, который включает контактирование клеток с эффективным количеством антитела по изобретению и/или его конъюгата с лечебным средством. CLD18 предпочтительно экспрессируется на поверхности данных клеток.
В следующем аспекте изобретение касается способа лечения или предотвращения заболеваний с участием клеток, экспрессирующих CLD18, предпочтительно CLD18A2, который включает введение субъекту антител по изобретению, их конъюгатов с лечебным средством или фармацевтических композиций, содержащих антитела по изобретению или их конъюгаты с лечебными средствами. Предпочтительно заболевания представляют собой раковые заболевания, которые в предпочтительных воплощениях выбираются из группы, состоящей из рака желудка, рака пищевода, рака поджелудочной железы, рака легких, рака яичников, рака толстой кишки, рака печени, рака головы и шеи, рака желчного пузыря и их метастазов. CLD18 предпочтительно экспрессируется на поверхности данных клеток.
Предпочтительно антитела по изобретению обладают способностью к различению вариантов CLD18, экспрессирующихся различными типами клеток, включая раковые клетки и нераковые клетки. В особенно предпочтительном воплощении антитела по изобретению обладают способностью к связыванию с CLD18A2, но не связываются с CLD18A1 или же связываются с CLD18A1 с меньшей специфичностью по сравнению со специфичностью связывания с CLD18A2.
Термин "связывание" по изобретению предпочтительно относится к специфическому связыванию. "Специфическое связывание" означает, что агент типа антитела связывается с мишенью типа эпитопа, к которому он специфичен, сильнее, чем с другой мишенью. Агент связывается с одной мишенью сильнее, чем с другой мишенью, если он связывается с первой мишенью с меньшей константой диссоциации (KD), чем константа диссоциации для второй мишени. Предпочтительно константа диссоциации (KD) для мишени, с которой агент связывается специфически, более чем в 10 раз, предпочтительно более чем в 20 раз, более предпочтительно более чем в 50 раз, еще более предпочтительно более чем в 100 раз, 200 раз, 500 раз или 1000 раз меньше, чем константа диссоциации (KD) для мишени, с которой агент не связывается специфически.
Предпочтительно у антител по изобретению константа диссоциации для CLD18, предпочтительно для CLD18A2, составляет 10-6 М или меньше, предпочтительно 10-7 М или меньше, предпочтительно 10-8 М или меньше либо предпочтительно 10-9 М или меньше. Предпочтительно у антител по изобретению константа диссоциации для CLD18, предпочтительно для CLD18A2, находится в пределах от 10-8 М до 10-9 М.
Антитела по изобретению вызывают гибель клеток, экспрессирующих CLD18, предпочтительно CLD18A2, при связывании с CLD18, предпочтительно экспрессирующегося на поверхности данных клеток. В одном воплощении антитела по изобретению индуцируют обусловленную комплементом цитотоксичность (CDC), напр., вызывают лизис по механизму CDC у 20-40+ клеток, предпочтительно у 40-50% клеток, более предпочтительно у более чем 50% клеток, экспрессирующих CLD18. Такие антитела в настоящем изобретении представлены следующими антителами: 37Н8, 38G5, 38Н3, 39F11, 61С2, 26В5, 26D12, 28D10, 163Е12, 175D10, 45С1, 125Е1, ch-163E12 и ch-175D10. Вместо или вместе с индуцированием CDC, антитела по изобретению могут индуцировать антителозависимую клеточную цитотоксичность (ADCC) в отношении клеток, экспрессирующих CLD18, в присутствии эффекторных клеток (напр., моноцитов, мононуклеаров, NK-клеток и PMN). Такие антитела в настоящем изобретении представлены следующими антителами: 37G11, 37Н8, 38G5, 38Н3, 39F11, 43А11, 61С2, 26В5, 26D12, 28D10, 42Е12, 163Е12, 175D10, 45С1 и 125Е1. Антитела по изобретению могут обладать способностью индуцировать апоптоз клеток, экспрессирующих CLD18, индуцировать гомотипическую адгезию клеток, экспрессирующих CLD18, и/или индуцировать фагоцитоз клеток, экспрессирующих CLD18, в присутствии макрофагов. Антитела по изобретению могут обладать одним или несколькими из вышеописанных функциональных свойств. Предпочтительно антитела по изобретению индуцируют лизис клеток, экспрессирующих CLD18, по механизму CDC и по механизму ADCC, а более предпочтительно они индуцируют лизис клеток, экспрессирующих CLD18, по механизму ADCC, но не индуцируют лизиса данных клеток по механизму CDC. Примеры клеток-мишеней для антител по изобретению включают раковые клетки, экспрессирующие CLD18, предпочтительно CLD18A2, как-то опухолеродные раковые клетки желудка, поджелудочной железы, пищевода и легких. В особенно предпочтительном воплощении гибель клеток, вызванная антителами по изобретению, специфична по отношению к CLD18A2, т.е. антитела по изобретению вызывают гибель клеток, предпочтительно лизис клеток, экспрессирующих CLD18A2, по механизму CDC и/или ADCC, однако они не вызывают гибели клеток, экспрессирующих CLD18A1, но не экспрессирующих CLD18A2. Вышеописанные антитела могут применяться для уничтожения опухолевых клеток при лечении или профилактике рака, как-то рака желудка, рака пищевода, рака поджелудочной железы, рака легких, рака яичников, рака толстой кишки, рака печени, рака головы и шеи, рака желчного пузыря и/или их метастазов.
Антитела по изобретению можно отнести к различным классам по их свойствам связывания и по их способности опосредовать эффекторные функции на клетках, экспрессирующих CLD18. Антитела по изобретению можно классифицировать по:
- свойствам связывания с клетками, экспрессирующими либо CLD18A1, либо CLD18A2, и/или опосредованию эффекторных функций на клетках, экспрессирующих либо CLD18A1, либо CLD18A2 (различение сплайс-вариантов CLD18),
- свойствам связывания с клетками, экспрессирующими либо гликозилированные, либо негликозилированные варианты CLD18, и/или опосредованию эффекторных функций на клетках, экспрессирующих либо гликозилированные, либо негликозилированные варианты CLD18 (различение вариантов CLD18 с N-гликозилированием или без него),
- свойствам связывания либо с раковыми клетками, либо с нормальными типами клеток, и/или опосредованию эффекторных функций либо на раковых клетках, либо на нормальных типах клеток (различение вариантов CLD18, экспрессируемых раковыми клетками или нормальными нераковыми клетками),
- свойствам связывания с эпитопами CLD18, экранируемыми при образовании плотных контактов,
- способности индуцировать образование агрегатов CLD18 на живых клетках, и
- способности к связыванию с другими вариантами CLD18, чем у человека, в особенности с вариантами CLD18 у мышей, крыс, кроликов и приматов.
Антитела по изобретению могут иметь одно или несколько из следующих свойств, которые приводятся на конкретных примерах описанных в нем антител (24Н5, 26В5, 26D12, 28D10, 37G11, 37Н8, 38G5, 38Н3, 39F11, 41С6, 42Е12, 43А11, 44Е10, 47D12, 61С2, 75В8, 85А3, 9Е8, 19В9, 45С1, 125Е1, 163Е12, 166Е2, 175D10, ch-43A11, ch-45C1, ch-125E1, ch-163E12, ch-166E2, ch-175D10):
a) связывание как с CLD18A2, так и с CLD18A1 (напр., 26D12, 28D10, 37Н8, 38H3, 39F11, 61C2, 41C6)
b) связывание с CLD18A2, но не с CLD18A1 (напр., 26В5, 37G11, 38G5, 42Е12, and 43А11, 45С1, 125Е1, 163Е12, 166Е2, 175D10, ch-43A11, ch-45C1, ch-125E1, ch-163E12, ch-166E2, ch-175D10)
c) связывание с CLD18, естественным образом экспрессирующимся раковыми клетками, но не с CLD18, естественным образом экспрессирующимся нераковыми клетками или тканями, как-то клетками желудка и легких (напр., 26В5, 75В8, 24Н5, 39F11, 45С1, 125Е1, 163Е12, 166Е2, 175D10)
d) опосредование по механизму CDC гибели клеток, экспрессирующих CLD18A2, но не клеток, экспрессирующих CLD18A1 (напр., 26D12, 28D10, 37Н8, 39F11, 163Е12, ch-125Е1, ch-163E12, ch-175D10)
e) опосредование по механизму ADCC гибели клеток, экспрессирующих CLD18 (напр., 26В5, 37G11, 37Н8, 38G5, 38Н3, 39F11, 43А11, 47D12, 61С2, ch-163E12, ch-175D10)
f) опосредование по механизму ADCC, но не по механизму CDC гибели клеток, экспрессирующих CLD18 (напр., 37G11, 42Е12, 43А11)
g) опосредование и по механизму ADCC, и по механизму CDC гибели клеток, экспрессирующих CLD18A2 (напр., 37Н8, 38Н3, 39F11, ch-163E12, ch-175D10).
Как изложено в настоящем изобретении, антитела по изобретению также охватывают молекулы, которые:
a) связываются с дифференцированными клетками нормального желудка, но не со стволовыми клетками желудка (напр., 39F11)
b) не связываются с нормальной тканью желудка, а также других нормальных органов, а только с раковыми клетками (напр., 26В5)
c) связываются с эпитопом, охватывающим негликозилированный Asn в положении 116 у CLD18
d) связываются и с CLD18 человека, и с CLD18 мыши, что дает возможность проводить тщательные доклинические исследования по токсичности на мышах.
Антитела по изобретению могут происходить из различных видов, в том числе мыши, крысы, кролика, морской свинки и человека. Антитела по изобретению также включают химерные молекулы, в которых константная область антитела из одного вида, предпочтительно человека, сочетается с антигенсвязывающим сайтом из другого вида. Кроме того, антитела по изобретению включают и гуманизированные молекулы, в которых антигенсвязывающие сайты антител из другого вида, чем человек, сочетаются с константными и каркасными областями антител человека.
Антитела по изобретению включают поликлональные и моноклональные антитела и включают антитела типа IgG2a (напр., IgG2a, κ, λ), IgG2b (напр., IgG2b, κ, λ), IgG3 (напр., IgG3, κ, λ) и IgM. Однако изобретение охватывает и другие изотипы антител, включая антитела типа IgG1, IgA1, IgA2, секреторного IgA, IgD и IgE. Антитела могут представлять собой целые антитела либо их антитенсвязывающие фрагменты, включая, к примеру, фрагменты Fab, F(ab')2, Fv, одноцепочечные Fv-фрагменты и биспецифичные антитела. Кроме того, антигенсвязывающие фрагменты включают слитые белки связывающих доменов иммуноглобулина, содержащие: (i) полипептид связывающего домена (как-то вариабельной области тяжелой цепи или вариабельной области легкой цепи), слитый с полипептидом шарнирного участка иммуноглобулина, (ii) константную область CH3 тяжелой цепи иммуноглобулина, слитую с константной областью CH2. Такие слитые белки связывающих доменов иммуноглобулина более подробно раскрыты в US 2003/0118592 and US 2003/0133939.
Антитела настоящего изобретения предпочтительно диссоциируют от CLD18 со значением равновесной константы диссоциации (KD) примерно 1-100 нМ или меньше. Предпочтительно антитела по изобретению не дают перекрестной реакции с родственными антигенами поверхности клеток и поэтому не ингибируют их функционирование.
В предпочтительных воплощениях антитела настоящего изобретения могут характеризоваться одним или несколькими из следующих свойств:
a) специфичностью к CLD18, в частности специфичностью к CLD18A2;
b) сродством связывания с CLD18, в частности CLD18A2, составляющим около 100 нМ или меньше, предпочтительно 5-10 нМ или меньше, более предпочтительно 1-3 нМ или меньше;
c) способностью опосредовать высокий уровень CDC на CD55/59-отрицательных либо CD55/59-положительных клетках;
d) способностью ингибировать рост клеток, экспрессирующих CLD18;
e) способностью индуцировать апоптоз клеток, экспрессирующих CLD18;
f) способностью индуцировать гомотипическую адгезию клеток, экспрессирующих CLD18;
g) способностью индуцировать ADCC на клетках, экспрессирующих CLD18, в присутствии эффекторных клеток;
h) способностью продлевать жизнь у субъектов с раковыми клетками, экспрессирующими CLD18;
i) способностью устранять клетки, экспрессирующие CLD18;
j) способностью устранять клетки, экспрессирующие CLD18 на низком уровне;
k) способностью вызывать агрегацию CLD18 на поверхности живых клеток.
Антитела настоящего изобретения против CLD18 можно подвергать дериватизации, присоединять к или экспрессировать вместе с другими специфичностями связывания. В предпочтительном воплощении изобретения предусмотрены биспецифичные или мультиспецифичные молекулы, содержащие по меньшей мере одну первую специфичность связывания с CLD18 (напр., антитело к CLD18 или его аналог) и вторую специфичность связывания с эффекторными клетками, как-то специфичность связывания с Fc-рецептором (напр., Fcγ-рецептором, как-то FcγRI или иным Fc-рецептором) либо с Т-клеточным рецептором, напр., CD3.
Соответственно, настоящее изобретение включает биспецифичные и мультиспецифичные молекулы, которые связываются и с CLD18, и с Fc-рецептором либо Т-клеточным рецептором, напр., CD3. Примерами Fc-рецепторов являются IgG-рецепторы, Fcγ-рецепторы (FcγR), как-то FcγRI (CD64), FcγRII (CD32) и FcγRIII (CD16). Мишенями могут служить и другие Fc-рецепторы, как-то IgA-рецепторы (напр., FcαRI). Fc-рецепторы предпочтительно находятся на поверхности эффекторных клеток, напр., моноцитов, макрофагов или активированных мононуклеаров. В предпочтительном воплощении биспецифичные и мультиспецифичные молекулы связываются с Fc-рецептором по сайту, который отличается от сайта связывания иммуноглобулина (напр., IgG or IgA) у Fc-рецептора. Следовательно, связывание биспецифичных и мультиспецифичных молекул не будет блокироваться физиологическими уровнями иммуноглобулинов.
В следующем аспекте антитела против CLD18 по изобретению подвергаются дериватизации, присоединяются к или экспрессируются вместе с другой функциональной молекулой, напр., другим пептидом или белком (напр., Fab'-фрагментом). Например, антитело по изобретению можно функционально соединить (напр., путем химического конъюгирования, генетического слияния, нековалентной ассоциации или иным способом) с одной или несколькими разновидностями молекул, как-то с другим антителом (напр., для получения биспецифичных или мультиспецифичных антител), цитотоксином, клеточным лигандом или антигеном (напр., для получения иммуноконъюгата, как-то иммунотоксина). Антитела настоящего изобретения можно присоединять к другим лечебным молекулам, напр., радиоизотопам, противораковым препаратам из небольших молекул, рекомбинантным цитокинам или хемокинам. Соответственно, настоящее изобретение охватывает широкий спектр конъюгатов антител, биспецифичных и мультиспецифичных молекул и слитых белков, которые все связываются с экспрессирующими CLD18 клетками и могут применяться для доставки других молекул к таким клеткам.
В следующем аспекте изобретением также предусмотрены связывающие CLD18 белки, происходящие из доменов не иммуноглобулинов, в частности, одноцепочечные белки. Такие связывающие белки и способы их получения описаны, к примеру, в Binz et al. (2005) Nature Biotechnology 23 (10): 1257-1268, включенном в настоящее изобретение путем ссылки. Следует иметь в виду, что изложенные в настоящем изобретении положения в отношении иммуноглобулинов или происходящих из иммуноглобулинов связывающих молекул, соответственно, также применимы к связывающим молекулам, происходящим из доменов не иммуноглобулинов. В частности, с помощью таких связывающих молекул, происходящих из доменов не иммуноглобулинов, можно блокировать CLD18 у клеток, экспрессирующих данную мишень, и тем самым осуществить терапевтические эффекты, изложенные в настоящем изобретении в отношении антител по изобретению, в частности ингибировать пролиферацию раковых клеток. Необязательно таким неиммуноглобулиновым связывающим молекулам можно придать эффекторные функции антител, напр., путем слияния с областью Fc антител.
В следующем аспекте изобретением предусмотрены композиции, напр., фармацевтические и диагностические композиции/наборы, включающие фармацевтически приемлемый носитель вместе с одним или с комбинацией антител по изобретению. В предпочтительном воплощении композиция включает комбинацию антител, связывающихся с разными эпитопами или обладающими различными функциональными характеристиками, как-то индуцирование CDC и/или ADCC и индуцирование апоптоза. В этом воплощении изобретения антитела могут применяться в комбинации, напр., в виде фармацевтической композиции, содержащей два или несколько моноклональных антител к CLD18. Например, в одной терапии можно объединить антитела к CLD18, обладающие различными, но дополняющими друг друга активностями для достижения требуемого терапевтического эффекта. В предпочтительном воплощении композиция включает антитело к CLD18, вызывающее CDC, в сочетании с другим антителом к CLD18, вызывающим апоптоз. В другом воплощении композиция включает антитело к CLD18, очень эффективно вызывающее гибель клеток мишени в присутствии эффекторных клеток, в сочетании с другим антителом к CLD18, ингибирующим рост клеток, экспрессирующих CLD18.
Настоящее изобретение также включает одновременное или последовательное введение двух или нескольких антител к CLD18 по изобретению, при котором по меньшей мере одно из данных антител является химерным антителом к CLD18, а по меньшей мере одно другое антитело является антителом человека к CLD18, причем эти антитела связываются с одними и теми же либо различными эпитопами CLD18. Предпочтительно сначала вводится химерное антитело к CLD18 по изобретению, а затем вводится антитело человека к CLD18 по изобретению, при этом антитело человека к CLD18 предпочтительно вводится в течение длительного периода времени, т.е. в качестве поддерживающей терапии.
Антитела, иммуноконъюгаты, биспецифичные и мультиспецифичные молекулы и композиции настоящего изобретения могут применяться в целом ряде способов ингибирования роста клеток, экспрессирующих CLD18, в частности CLD18A2, и/или избирательного уничтожения клеток, экспрессирующих CLD18, в частности CLD18A2, путем контактирования клеток с эффективным количеством антитела, иммуноконъюгата, биспецифичной/мультиспецифичной молекулы или композиции с тем, чтобы рост клеток ингибировался и/или клетки погибали. В одном воплощении способ включает уничтожение клеток, экспрессирующих CLD18, необязательно в присутствии эффекторных клеток, например, по механизму CDC, апоптоза, ADCC, фагоцитоза или комбинации двух или нескольких из этих механизмов. Экспрессирующие CLD18 клетки, которые можно ингибировать или уничтожить с помощью антител по изобретению, включают раковые клетки, как-то опухолеродные клетки желудка, поджелудочной железы, пищевода, легких, яичников, толстой кишки, печени, головы и шеи, желчного пузыря.
Соответственно, антитела настоящего изобретения могут применяться для лечения и/или предотвращения целого ряда заболеваний с участием клеток, экспрессирующих CLD18, путем введения антител пациентам, страдающим такими заболеваниями. Примеры заболеваний, которые можно лечить (напр., облегчить) или предотвращать, включают и опухолеродные заболевания. Примеры опухолеродных заболеваний, которые можно лечить и/или предотвращать, включают рак желудка, рак поджелудочной железы, рак пищевода, рак легких, рак яичников, рак толстой кишки, рак печени, рак головы и шеи, рак желчного пузыря и их метастазы.
В предпочтительном воплощении изобретения субъект, которому вводятся антитела, дополнительно подвергается лечению химиотерапевтическим средством, облучением или средством, модулирующим, напр., усиливающим или тормозящим экспрессию и/или активность Fc-рецептора, напр., Fcγ-рецептора, как-то цитокином. Типичные цитокины для введения при лечении включают колониестимулирующий фактор гранулоцитов (G-CSF), колониестимулирующий фактор гранулоцитов/макрофагов (GM-CSF), γ-интерферон (IFN-γ) и фактор некроза опухолей (TNF). Типичные терапевтические средства включают, среди прочего, такие антинеопластические средства, как доксорубицин, цисплатин, тааксотер, 5-фторурацил, метотрексат, гемзитабин и циклофосфамид.
В следующем аспекте изобретение касается способа иммунизации для иммунизирования таких животных (но не человека), как мыши, с помощью CLD18 человека или его пептидного фрагмента, предпочтительно CLD18A2 или его пептидного фрагмента, для получения антител. Предпочтительными пептидами для иммунизации являются пептиды, выбираемые из группы, состоящей из SEQ ID NO: 2, 4, 6, 16, 18, 20-23, 26-31, 151, 153 и 155-157, или пептиды, содержащие данные последовательности. Соответственно, в предпочтительном воплощении антитела по изобретению получают при иммунизации с помощью пептидов, выбираемых из группы, состоящей из SEQ ID NO: 2, 4, 6, 16, 18, 20-23, 26-31, 151, 153 и 155-157, или с помощью пептидов, содержащих данные последовательности. Аналогичным образом антитела к CLD18 могут вырабатываться у трансгенного животного (но не человека), как-то у трансгенной мыши. Трансгенное животное может представлять собой трансгенную мышь с геномом, содержащим трансген тяжелой цепи и трансген легкой цепи, кодирующие все антитело или его часть.
Животных дикого типа, как и трансгенных животных, можно иммунизировать очищенным или обогащенным препаратом антигена CLD18 и/или нуклеиновой кислотой и/или клетками, экспрессирующими CLD18 или его пептидный фрагмент. Предпочтительно животное способно вырабатывать множественные изотипы моноклональных антител человека к CLD18 (напр., IgG, IgA и/или IgM), подвергаясь рекомбинации V-D-J и переключению изотипа. Переключение изотипа может происходить, напр., по механизму классического или не классического переключения изотипа.
Соответственно, в следующем аспекте изобретением предусмотрены выделенные из животного В-клетки, как описано выше. Выделенные В-клетки можно затем сделать "бессмертными" путем слияния с иммортализоваными клетками, получая источник (напр., гибридому) антител по изобретению. Такие гибридомы (т.е. вырабатывающие антитела по изобретению) также охвачены рамками изобретения.
Как изложено в настоящем изобретении, антитела по изобретению могут быть получены непосредственно из гибридом, экспрессирующих эти антитела, либо они могут быть клонированы и экспрессированы рекомбинантным путем в клетках-хозяевах (напр., клетках СНО или лимфоцитарных клетках). Другими примерами клеток-хозяев являются микроорганизмы, как-то Е. coli, и грибы, как-то дрожжи. С другой стороны, они могут быть получены рекомбинантным путем в трансгенных животных или растениях.
Предпочтительными клетками гибридом для получения антител по изобретению являются клетки с установленной последовательностью или депонированные в DSMZ (Mascheroder Weg 1b, 31824 Braunschweig, Германия; новый адрес: Inhoffenstr. 7В, 31824 Braunschweig, Германия), имеющие следующие обозначения и номера доступа:
a. 182-D1106-055, № доступа DSM АСС2737, депонированы 19 октября 2005 г.
b. 182-D1106-056, № доступа DSM АСС2738, депонированы 19 октября 2005 г.
c. 182-D1106-057, № доступа DSM АСС2739, депонированы 19 октября 2005 г.
d. 182-D1106-058, № доступа DSM АСС2740, депонированы 19 октября 2005 г.
e. 182-D1106-059, № доступа DSM АСС2741, депонированы 19 октября 2005 г.
f. 182-D1106-062, № доступа DSM АСС2742, депонированы 19 октября 2005 г.
g. 182-D1106-067, № доступа DSM АСС2743, депонированы 19 октября 2005 г.
h. 182-D758-035, № доступа DSM АСС2745, депонированы 17 ноября 2005 г.
i. 182-D758-036, № доступа DSM АСС2746, депонированы 17 ноября 2005 г.
j. 182-D758-040, № доступа DSM АСС2747, депонированы 17 ноября 2005 г.
k. 182-D1106-061, № доступа DSM АСС2748, депонированы 17 ноября 2005 г.
l. 182-D1106-279, № доступа DSM АСС2808, депонированы 26 октября 2006 г.
m. 182-D1106-294, № доступа DSM АСС2809, депонированы 26 октября 2006 г.
n. 182-D1106-362, № доступа DSM АСС2810, депонированы 26 октября 2006 г.
Предпочтительными антителами по изобретению являются антитела, полученные и получаемые из вышеописанных гибридом, т.е. 37G11 в случае 182-D1106-055, 37Н8 в случае 182-D1106-056, 38G5 в случае 182-D1106-057, 38Н3 в случае 182-D1106-058, 39F11 в случае 182-D1106-059, 43А11 в случае 182-D1106-062, 61С2 в случае 182-D1106-067, 26В5 в случае 182-D758-035, 26D12 в случае 182-D758-036, 28D10 в случае 182-D758-040, 42Е12 в случае 182-D1106-061, 125Е1 в случае 182-D1106-279, 163Е12 в случае 182-D1106-294 и 175D10 в случае 182-D1106-362; а также их химерные и гуманизированные формы.
В предпочтительных воплощениях антитела, в частности химерные формы антител по изобретению, включают антитела, содержащие константную область тяжелой цепи (CH), включающую аминокислотную последовательность, происходящую из константной области тяжелой цепи человека, как-то аминокислотную последовательность, представленную SEQ ID NO: 46 или 150 либо ее фрагментом. В других предпочтительных воплощениях антитела, в частности химерные формы антител по изобретению, включают антитела, содержащие константную область легкой цепи (CL), включающую аминокислотную последовательность, происходящую из константной области легкой цепи человека, как-то аминокислотную последовательность, представленную SEQ ID NO: 41 или 148 либо ее фрагментом. В особенно предпочтительном воплощении антитела, в частности химерные формы антител по изобретению, включают антитела, содержащие область CH, включающую аминокислотную последовательность, происходящую из CH человека, как-то аминокислотную последовательность, представленную SEQ ID NO: 46 или 150 либо ее фрагментом, а также содержащие область CL, включающую аминокислотную последовательность, происходящую из CL человека, как-то аминокислотную последовательность, представленную SEQ ID NO: 41 или 148 либо ее фрагментом.
Область CH, включающая аминокислотную последовательность, представленную SEQ ID NO: 46, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 45. Область CH, включающая аминокислотную последовательность, представленную SEQ ID NO: 150, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 149. Область CL, включающая аминокислотную последовательность, представленную SEQ ID NO: 41, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 40. Область CL, включающая аминокислотную последовательность, представленную SEQ ID NO: 148, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 147.
В некоторых предпочтительных воплощениях химерные формы антител включают антитела, содержащие тяжелую цепь, включающую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 115, 116, 117, 118, 119, 120 и их фрагментов, и/или содержащие легкую цепь, включающую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 121, 122, 123, 124, 125, 126, 127, 128, 129 и их фрагментов.
В некоторых предпочтительных воплощениях химерные формы антител включают антитела, содержащие комбинацию из тяжелых цепей и легких цепей, выбранную из следующих возможностей от (i) до (ix):
(i) тяжелая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 115 или ее фрагментом, а легкая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 122 или ее фрагментом;
(ii) тяжелая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 116 или ее фрагментом, а легкая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 121 или ее фрагментом;
(iii) тяжелая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 117 или ее фрагментом, а легкая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 123 или ее фрагментом;
(iv) тяжелая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 119 или ее фрагментом, а легкая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 126 или ее фрагментом;
(v) тяжелая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 118 или ее фрагментом, а легкая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 125 или ее фрагментом;
(vi) тяжелая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 120 или ее фрагментом, а легкая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 124 или ее фрагментом;
(vii) тяжелая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 120 или ее фрагментом, а легкая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 127 или ее фрагментом;
(viii) тяжелая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 120 или ее фрагментом, а легкая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 128 или ее фрагментом;
(ix) тяжелая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 120 или ее фрагментом, а легкая цепь включает аминокислотную последовательность, представленную SEQ ID NO: 129 или ее фрагментом.
"Фрагмент" или "фрагмент аминокислотной последовательности", как приведено выше, относится к части последовательности антитела, т.е. такой последовательности, которая представляет собой последовательность антитела, укороченную на N- и/или С-конце, причем если она заменяет данную последовательность антитела в антителе, то она сохраняет связывание данного антитела с CLD18 и предпочтительно функции данного антитела, как описано в настоящем изобретении, напр., лизис по механизму CDC или по механизму ADCC. Предпочтительно фрагмент аминокислотной последовательности содержит по меньшей мере 90, 95, 96, 97, 98 или 99% аминокислотных остатков данной аминокислотной последовательности. Предпочтительно к такой последовательности относится фрагмент аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128 и 129, у которой удалены 17, 18, 19, 20, 21, 22 или 23 аминокислоты из N-конца. Фрагменты аминокислотных последовательностей, описанные в настоящем изобретении, могут кодироваться соответствующими фрагментами последовательностей нуклеиновых кислот, кодирующих данные аминокислотные последовательности.
Тяжелая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 115, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 100. Тяжелая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 116, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 101. Тяжелая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 117, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 102. Тяжелая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 119, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 104. Тяжелая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 118, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 103. Тяжелая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 120, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 105.
Легкая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 122, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 107. Легкая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 121, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 106. Легкая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 123, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 108. Легкая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 126, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 111. Легкая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 125, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 110. Легкая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 124, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 109. Легкая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 127, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 112. Легкая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 128, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 113. Легкая цепь, включающая аминокислотную последовательность, представленную SEQ ID NO: 129, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 114.
В предпочтительном воплощении антитело по изобретению содержит вариабельную область тяжелой цепи (VH), включающую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 132, 133, 134, 135, 136, 137 и их фрагментов.
В предпочтительном воплощении антитело по изобретению содержит вариабельную область легкой цепи (VL), включающую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO 138, 139, 140, 141, 142, 143, 144, 145, 146 и их фрагментов.
В некоторых предпочтительных воплощениях антитело по изобретению содержит комбинацию из вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL), выбранную из следующих возможностей от (i) до (ix):
(i) область VH включает аминокислотную последовательность, представленную SEQ ID NO: 132 или ее фрагментом, а область VL включает аминокислотную последовательность, представленную SEQ ID NO: 139 или ее фрагментом;
(ii) область VH включает аминокислотную последовательность, представленную SEQ ID NO: 133 или ее фрагментом, а область VL включает аминокислотную последовательность, представленную SEQ ID NO: 138 или ее фрагментом;
(iii) область VH включает аминокислотную последовательность, представленную SEQ ID NO: 134 или ее фрагментом, а область VL включает аминокислотную последовательность, представленную SEQ ID NO: 140 или ее фрагментом;
(iv) область VH включает аминокислотную последовательность, представленную SEQ ID NO: 136 или ее фрагментом, а область VL включает аминокислотную последовательность, представленную SEQ ID NO: 143 или ее фрагментом;
(у) область VH включает аминокислотную последовательность, представленную SEQ ID NO: 135 или ее фрагментом, а область VL включает аминокислотную последовательность, представленную SEQ ID NO: 142 или ее фрагментом;
(vi) область VH включает аминокислотную последовательность, представленную SEQ ID NO: 137 или ее фрагментом, а область VL включает аминокислотную последовательность, представленную SEQ ID NO: 141 или ее фрагментом;
(vii) область VH включает аминокислотную последовательность, представленную SEQ ID NO: 137 или ее фрагментом, а область VL включает аминокислотную последовательность, представленную SEQ ID NO: 144 или ее фрагментом;
(viii) область VH включает аминокислотную последовательность, представленную SEQ ID NO: 137 или ее фрагментом, а область VL включает аминокислотную последовательность, представленную SEQ ID NO: 145 или ее фрагментом;
(ix) область VH включает аминокислотную последовательность, представленную SEQ ID NO: 137 или ее фрагментом, а область VL включает аминокислотную последовательность, представленную SEQ ID NO: 146 или ее фрагментом.
Область VH, включающая аминокислотную последовательность, представленную SEQ ID NO: 132, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 55. Область VH, включающая аминокислотную последовательность, представленную SEQ ID NO: 133, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 56. Область VH, включающая аминокислотную последовательность, представленную SEQ ID NO: 134, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 57. Область VH, включающая аминокислотную последовательность, представленную SEQ ID NO: 136, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 59. Область VH, включающая аминокислотную последовательность, представленную SEQ ID NO: 135, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 58. Область VH, включающая аминокислотную последовательность, предста вленную SEQ ID NO: 137, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 60.
Область VL, включающая аминокислотную последовательность, представленную SEQ ID NO: 139, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 62. Область VL, включающая аминокислотную последовательность, представленную SEQ ID NO: 138, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 61. Область VL, включающая аминокислотную последовательность, представленную SEQ ID NO: 140, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 63. Область VL, включающая аминокислотную последовательность, представленную SEQ ID NO: 143, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 66. Область VL, включающая аминокислотную последовательность, представленную SEQ ID NO: 142, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 65. Область VL, включающая аминокислотную последовательность, представленную SEQ ID NO: 141, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 64. Область VL, включающая аминокислотную последовательность, представленную SEQ ID NO: 144, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 67. Область VL, включающая аминокислотную последовательность, представленную SEQ ID NO: 145, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 68. Область VL, включающая аминокислотную последовательность, представленную SEQ ID NO: 146, может кодироваться нуклеиновой кислотой, включающей нуклеотидную последовательность, представленную SEQ ID NO: 69.
В предпочтительном воплощении антитело по изобретению включает область VH, содержащую набор гипервариабельных участков CDR1, CDR2 и CDR3, выбранных из следующих воплощений от (i) до (vi):
(i) CDR1: положения 45-52 в SEQ ID NO: 115, CDR2: положения 70-77 в SEQ ID NO: 115, CDR3: положения 116-125 в SEQ ID NO: 115;
(ii) CDR1: положения 45-52 в SEQ ID NO: 116, CDR2: положения 70-77 в SEQ ID NO: 116, CDR3: положения 116-126 в SEQ ID NO: 116;
(iii) CDR1: положения 45-52 в SEQ ID NO: 117, CDR2: положения 70-77 в SEQ ID NO: 117, CDR3: положения 116-124 в SEQ ID NO: 117;
(iv) CDR1: положения 45-52 в SEQ ID NO: 118, CDR2: положения 70-77 в SEQ ID NO: 118, CDR3: положения 116-126 в SEQ ID NO: 118;
(v) CDR1: положения 44-51 в SEQ ID NO: 119, CDR2: положения 69-76 в SEQ ID NO: 119, CDR3: положения 115-125 в SEQ ID NO: 119;
(vi) CDR1: положения 45-53 в SEQ ID NO: 120, CDR2: положения 71-78 в SEQ ID NO: 120, CDR3: положения 117-128 в SEQ ID NO: 120.
В предпочтительном воплощении антитело по изобретению включает область VL, содержащую набор гипервариабельных участков CDR1, CDR2 и CDR3, выбранных из следующих воплощений от (i) до (ix):
(i) CDR1: положения 47-58 в SEQ ID NO: 121, CDR2: положения 76-78 в SEQ ID NO: 121, CDR3: положения 115-123 в SEQ ID NO: 121;
(ii) CDR1: положения 49-53 в SEQ ID NO: 122, CDR2: положения 71-73 в SEQ ID NO: 122, CDR3: положения 110-118 в SEQ ID NO: 122;
(iii) CDR1: положения 47-52 в SEQ ID NO: 123, CDR2: положения 70-72 в SEQ ID NO: 123, CDR3: положения 109-117 в SEQ ID NO: 123;
(iv) CDR1: положения 47-58 в SEQ ID NO: 124, CDR2: положения 76-78 в SEQ ID NO: 124, CDR3: положения 115-123 в SEQ ID NO: 124;
(v) CDR1: положения 47-58 в SEQ ID NO: 125, CDR2: положения 76-78 в SEQ ID NO: 125, CDR3: положения 115-123 в SEQ ID NO: 125;
(vi) CDR1: положения 47-58 в SEQ ID NO: 126, CDR2: положения 76-78 в SEQ ID NO: 126, CDR3: положения 115-122 в SEQ ID NO: 126;
(vii) CDR1: положения 47-58 в SEQ ID NO: 127, CDR2: положения 76-78 в SEQ ID NO: 127, CDR3: положения 115-123 в SEQ ID NO: 127;
(viii) CDR1: положения 47-58 в SEQ ID NO: 128, CDR2: положения 76-78 в SEQ ID NO: 128, CDR3: положения 115-123 в SEQ ID NO: 128;
(ix) CDR1: положения 47-52 в SEQ ID NO: 129, CDR2: положения 70-72 в SEQ ID NO: 129, CDR3: положения 109-117 в SEQ ID NO: 129.
В предпочтительном воплощении антитело по изобретению включает комбинацию областей VH и VL, каждая из которых содержит набор гипервариабельных участков CDR1, CDR2 и CDR3, выбранных из следующих воплощений от (i) до (ix):
(i) VH: CDR1: положения 45-52 в SEQ ID NO: 115, CDR2: положения 70-77 в SEQ ID NO: 115, CDR3: положения 116-125 в SEQ ID NO: 115, VL: CDR1: положения 49-53 в SEQ ID NO: 122, CDR2: положения 71-73 в SEQ ID NO: 122, CDR3: положения 110-118 в SEQ ID NO: 122;
(ii) VH: CDR1: положения 45-52 в SEQ ID NO: 116, CDR2: положения 70-77 в SEQ ID NO: 116, CDR3: положения 116-126 в SEQ ID NO: 116, VL: CDR1: положения 47-58 в SEQ ID NO: 121, CDR2: положения 76-78 в SEQ ID NO: 121, CDR3: положения 115-123 в SEQ ID NO: 121;
(iii) VH: CDR1: положения 45-52 в SEQ ID NO: 117, CDR2: положения 70-77 в SEQ ID NO: 117, CDR3: положения 116-124 в SEQ ID NO: 117, VL: CDR1: положения 47-52 в SEQ ID NO: 123, CDR2: положения 70-72 в SEQ ID NO: 123, CDR3: положения 109-117 в SEQ ID NO: 123;
(iv) VH: CDR1: положения 44-51 в SEQ ID NO: 119, CDR2: положения 69-76 в SEQ ID NO: 119, CDR3: положения 115-125 в SEQ ID NO: 119, VL: CDR1: положения 47-58 в SEQ ID NO: 126, CDR2: положения 76-78 в SEQ ID NO: 126, CDR3: положения 115-122 в SEQ ID NO: 126;
(v) VH: CDR1: положения 45-52 в SEQ ID NO: 118, CDR2: положения 70-77 в SEQ ID NO: 118, CDR3: положения 116-126 в SEQ ID NO: 118, VL: CDR1: положения 47-58 в SEQ ID NO: 125, CDR2: положения 76-78 в SEQ ID NO: 125, CDR3: положения 115-123 в SEQ ID NO: 125;
(vi) VH: CDR1: положения 45-53 в SEQ ID NO: 120, CDR2: положения 71-78 в SEQ ID NO: 120, CDR3: положения 117-128 в SEQ ID NO: 120, VL: CDR1: положения 47-58 в SEQ ID NO: 124, CDR2: положения 76-78 в SEQ ID NO: 124, CDR3: положения 115-123 в SEQ ID NO: 124;
(vii) VH: CDR1: положения 45-53 в SEQ ID NO: 120, CDR2: положения 71-78 в SEQ ID NO: 120, CDR3: положения 117-128 в SEQ ID NO: 120, VL: CDR1: положения 47-58 в SEQ ID NO: 127, CDR2: положения 76-78 в SEQ ID NO: 127, СОЮ: положения 115-123 в SEQ ID NO: 127;
(viii) VH: CDR1: положения 45-53 в SEQ ID NO: 120, CDR2: положения 71-78 в SEQ ID NO: 120, CDR3: положения 117-128 в SEQ ID NO: 120, VL: CDR1: положения 47-58 в SEQ ID NO: 128, CDR2: положения 76-78 в SEQ ID NO: 128, CDR3: положения 115-123 в SEQ ID NO: 128;
(ix) VH: CDR1: положения 45-53 в SEQ ID NO: 120, CDR2: положения 71-78 в SEQ ID NO: 120, СDR3: положения 117-128 в SEQ ID NO: 120, VL: CDR1: положения 47-52 в SEQ ID NO: 129, CDR2: положения 70-72 в SEQ ID NO: 129, СDRP: положения 109-117 в SEQ ID NO: 129.
В других предпочтительных воплощениях антитело по изобретению предпочтительно включает один или несколько гипервариабельных участков (CDR), предпочтительно по меньшей мере участок CDR3 вариабельной области тяжелой цепи (VH) и/или вариабельной области легкой цепи (VL) моноклонального антитела против CLD18, предпочтительно описанного в настоящем изобретении, которое предпочтительно содержит один или несколько гипервариабельных участков (CDR), предпочтительно по меньшей мере участок CDR3 вариабельной области тяжелой цепи (VH) и/или вариабельной области легкой цепи (VL), описанных в настоящем изобретении. В одном воплощении настоящего изобретения данные один или несколько гипервариабельных участков (CDR) выбираются из описанного в настоящем изобретении набора гипервариабельных участков CDR1, CDR2 и CDR3. В особенно предпочтительном воплощении антитело по изобретению предпочтительно включает гипервариабельные участки CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи (VH) и/или вариабельной области легкой цепи (VL) моноклонального антитела против CLD18, предпочтительно описанного в настоящем изобретении, которое предпочтительно содержит гипервариабельные участки CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи (VH) и/или вариабельной области легкой цепи (VL), описанные в настоящем изобретении.
В одном воплощении антитело по изобретению, включающее один или несколько участков CDR, набор участков CDR или комбинацию наборов CDR, как описано в настоящем изобретении, содержит данные CDR вместе с разделяющими их каркасными участками. Предпочтительно эта часть должна включать по меньшей мере 50% одного из или обоих 1-го и 4-го каркасных участков, причем эти 50% должны составлять 50% с С-конца 1-го каркасного участка и 50% с N-конца 4-го каркасного участка. Конструирование антител настоящего изобретения методами рекомбинантной ДНК может привести к введению на N- и С-концы вариабельных областей остатков, кодируемых линкерами, вставленными для облегчения клонирования или других рабочих операций, включая введение линкеров для соединения вариабельных областей по изобретению с другими белковыми последовательностями, в том числе тяжелыми цепями иммуноглобулина, другими вариабельными доменами (напр., при получении диател) или белковыми метками.
В одном воплощении антитело по изобретению, включающее один или несколько участков CDR, набор участков CDR или комбинацию наборов CDR, как описано в настоящем изобретении, содержит данные CDR в каркасе антител человека.
Упоминание в настоящем изобретении антитела, содержащего в отношении своей тяжелой цепи определенную цепь либо определенный участок или последовательность, предпочтительно относится к такой ситуации, когда все тяжелые цепи данного антитела содержат данную определенную цепь, участок или последовательность. Соответственно, это касается и легкой цепи антитела.
Настоящее изобретение также касается нуклеиновых кислот, содержащих гены или последовательности нуклеотидов, кодирующие антитела или их части, напр., цепи антител, как описано в настоящем изобретении. Нуклеиновые кислоты могут содержаться в векторе, напр., плазмидном, космидном, вирусном, бактериофаговом или ином векторе, обычно используемом, напр., в генетической инженерии. Вектор может содержать и другие гены, как-то маркерные гены, способствующие селекции вектора в подходящих клетках-хозяевах в соответствующих условиях. Кроме того, вектор может содержать контролирующие экспрессию элементы, способствующие надлежащей экспрессии кодирующей области в подходящем хозяине. Такие контрольные элементы известны специалистам, причем они могут включать промотор, кассету сплайсинга и кодон инициации трансляции.
Предпочтительно нуклеиновая кислота по изобретению функционально соединяется с вышеприведенными контролирующими экспрессию последовательностями, способствующими экспрессии в эукариотических или прокариотических клетках. Контрольные элементы, обеспечивающие экспрессию в эукариотических или прокариотических клетках, хорошо известны специалистам.
Способы конструирования молекул нуклеиновых кислот по изобретению, конструирования векторов, содержащие такие молекулы нуклеиновых кислот, введения векторов в правильно выбранные клетки-хозяева, инициирования или осуществления экспрессии хорошо известны в этой области.
Следующий аспект настоящего изобретения касается клеток-хозяев, содержащих нуклеиновую кислоту или вектор, как изложено в настоящем изобретении.
Другие особенности и преимущества настоящего изобретения станут понятными из нижеследующего подробного описания и формулы изобретения.
Краткое описание фигур
На фиг. 1 представлен иммунофлуоресцентный анализ клеток НЕК293, трансфицированных CLD18A2, конъюгированным с зеленым флуорохромом, и обработанных сывороткой мыши после иммунизации с помощью ДНК согласно SEQ ID NO: 15, слитой с эпитопом клеток-хелперов.
На фиг. 2 представлен анализ методом вестерн-гибридизации клеток HEK293, трансфицированных CLD18A2-myc (SEQ ID NO: 3), и нетрансфицированных клеток HEK293 с помощью моноклонального антитела мыши 9Е11 к c-myc (Serotec, CRL МСА2200).
На фиг. 3 представлен иммунофлуоресцентный анализ клеток СНО, трансфицированных CLD18A2, с помощью поликлональных антител кролика к CLD18 (Zymed, CRL 38-8000).
На фиг. 4А и В представлено связывание супернатантов гибридом 24Н5 и 85A3 с клетками HEK293, временно трансфицированными CLD18A2 человека с флуоресцентным маркером при определении методом проточной цитометрии. На фиг. 4С представлено связывание супернатантов гибридом 45С1, 125Е1, 163Е12, 166Е2 и 175D10 с клетками HEK293, устойчиво трансфицированными CLD18A2 человека и контрастно окрашенными пропидия иодидом.
На фиг. 5 представлено связывание супернатантов гибридом 24Н5 (А), 9Е8 (В), 26В5 (С) и 19В9 (D) с клетками HEK293, временно трансфицированными флуоресцентным маркером и либо CLD18A2 человека, либо CLD18A2-Myc или CLD18A2-HA, при анализе методом проточной цитометрии.
На фиг. 6А и В представлено связывание супернатантов гибридом 37Н8, 43АН, 45С1 и 163Е12 с клетками HEK293, устойчиво трансфицированными CLD18A2 человека или CLD18A1 человека, при определении методом проточной цитометрии.
На фиг. 7 представлен иммунофлуоресцентный анализ специфичного к изоформе CLD18A2 моноклонального антитела 37G11 по окрашиванию клеток HEK293, трансфицированных CLD18A2 (А, С) и CLD18A1 (В, D), соответственно, в нативном состоянии (А, В) и при фиксации параформальдегидом (С, D).
На фиг. 8 представлен иммунофлуоресцентный анализ моноклонального антитела 26В5 к CLD18 по окрашиванию клеток НЕК293, трансфицированных CLD18A2 (А, С) и CLD18A1 (В, D), соответственно, в нативном состоянии (А, В) и при фиксации параформальдегидом (С, D).
На фиг. 9 представлен анализ клеточных линий методом ОТ-ПЦР. Анализ с помощью специфичных к CLD18A2 праймеров четко показал экспрессию у 4/5 из исследованных линий клеток.
На фиг. 10 представлен иммунофлуоресцентный анализ клеток DAN-G (субклон F2) с помощью поликлональных антител кролика к CLD18 (Zymed, CRL 38-8000).
На фиг. 11 представлен иммунофлуоресцентный анализ клеток KATO-III (субклон 3В9 4D5) с помощью поликлональных антител кролика к CLD18 (Zymed, CRL 38-8000).
На фиг. 12А представлен иммунофлуоресцентный анализ клеток SNU-16 (субклон G5) с помощью поликлональных антител кролика к CLD18 (Zymed, CRL 38-8000). На фиг. 12В представлен иммунофлуоресцентный анализ клеток KATO-III с помощью моноклональных антител по изобретению.
На фиг. 13 представлена поверхностная экспрессия CLD18 на клетках KATO-III и NUGC-4 при анализе по окрашиванию клеток моноклональными антителами 61С2 и 163Е12 с последующим анализом методом проточной цитометрии.
На фиг. 14 представлено выравнивание белков CLD18A1 человека (NP_057453), CLD18A2 человека (NP_001002026), CLD18A1 мыши (NP_062789) и CLD18A2 мыши (AAL15636).
На фиг. 15А и В представлено связывание супернатантов гибридом 38G5, 38Н3, 37G11, 45С1 и 163Е12, соответственно, с клетками HEK293, временно трансфицированными флуоресцентным маркером и либо CLD18A1 мыши, либо CLD18A2 мыши, при анализе методом проточной цитометрии.
На фиг. 16 представлен иммуногистохимический анализ с помощью поликлонального антитела р105. Иммуногистохимическое окрашивание на группе нормальных тканей (желудка, легких, костного мозга и простаты) подтверждает специфичность к ткани желудка (А). Экспрессия также проявлялась в карциномах желудка (верхний ряд) и карциномах легких (В). CLD18A2 экспрессируют только дифференцированные клетки, но не стволовые клетки (С).
На фиг. 17 представлен иммуногистохимический анализ с помощью моноклонального антитела 39F11D7. (А) Специфическая экспрессия белка обнаружена в нормальной слизистой желудка, тогда как все другие исследованные нормальные ткани дали отрицательные результаты. (В) Сильная экспрессия CLD18A2 обнаружена в карциномах желудка и легких.
На фиг. 18 представлен иммуногистохимический анализ с помощью моноклональных антител 26В5 (A), 175D10 (В), 43А11 (С), 163Е12 (D) и 45С1 (Е). Все антитела давали сильное окрашивание ксенотрансплантатов HEK293-CLD18A2 и образцов рака желудка, но не контрольных ложно-трансфицированных ксенотрансплантатов HEK293.
На фиг. 19 представлена сравнительная диаграмма процента мертвых клеток после индукции CDC антителами 85А3, 28D10, 24Н5 или 26D12 на клетках HEK293, устойчиво трансфицированных CLD18A2 человека, при анализе методом проточной цитометрии.
На фиг. 20 представлена сравнительная диаграмма процента специфического лизиса клеток после индукции CDC антителами 24Н5, 26D12, 28D10, 37G11, 37Н8, 38G5, 38Н3, 39F11, 41С6, 42Е12, 43А11, 44Е10, 47D12 или 61С2 на адгерентных клетках СНО, устойчиво трансфицированных CLD18A2 человека или CLD18A1 человека, при определении по измерению флуоресценции.
На фиг. 21 представлена зависимая от концентрации индукция CDC антителами 75В8 (A), 28D10 (В) или 37Н8 (С) на клетках СНО, устойчиво трансфицированных CLD18A2 человека, при определении по измерению флуоресценции.
На фиг. 22 представлен лизис клеток HEK293-CLD18A2 антителами 26В5, 37Н8, 38G5, 47D12 и 61С2, соответственно, в присутствии мононуклеаров (MNC).
На фиг. 23 представлен лизис клеток HEK293-CLD18A1 антителами 26В5, 37Н8, 38G5, 47D12 и 61С2, соответственно, в присутствии мононуклеаров (MNC).
На фиг. 24 представлено ингибирование роста опухолей антителами изобретения на модели раннего лечения ксенотрансплантатов с клетками HEK293-CLD18A2.
На фиг. 25А и В представлено продление срока жизни антителами изобретения на двух моделях раннего лечения ксенотрансплантатов с клетками HEK293-CLD18A2.
На фиг. 26 представлено продление срока жизни антителами изобретения на модели позднего лечения ксенотрансплантатов с клетками HEK293-CLD18A2.
На фиг. 27А представлено ингибирование роста опухолей антителами изобретения на модели раннего лечения ксенотрансплантатов. На фиг. 27В представлено продление срока жизни антителами изобретения на модели раннего лечения ксенотрансплантатов. Использовали клетки DAN-G, экспрессирующие эндогенный CLD18A2.
На фиг. 28 представлена экспрессия мРНК CLD18A2 в тканях мыши. Исследования методом ОТ-ПЦР с помощью специфичных к CLD18A2 праймеров показали отсутствие значительной экспрессии во всех исследованных нормальных тканях, за исключением желудка. Подвергали анализу следующие ткани: 1 - тонкий кишечник, 2 - селезенка, 3 - кожа, 4 - желудок, 5 - легкие, 6 - поджелудочная железа, 7 - лимфатические узлы, 8 - тимус, 9 - отрицательный контроль.
На фиг. 29 представлена экспрессия CLD18 в нормальном желудке. Иммуногистохимический анализ желудка мыши с помощью специфичных к CLD18 антител показал консервативный профиль экспрессии. В то время, как в поверхностном эпителии и более глубоких криптах CLD18 экспрессируется на поверхности клеток, центральная область шейки дает отрицательную реакцию на CLD18.
На фиг. 30 представлено окрашивание гематоксилином и эозином тканей желудка мыши. Представлены общий вид (А) и детальный вид (В) желудка обработанной\37G11 мыши в сравнении с контрольной мышью (С и D), получавшей только PBS.
На фиг. 31А и В представлена проточная цитометрия окрашивания с помощью антител по изобретению (43А11, 125Е1, 163Е12, 166Е2 и 175D10) клеток HEK293, устойчиво трансфицированных CLD18A1 и CLD18A2, соответственно, а также эндогенно экспрессирующих клеток KATO-III.
На фиг. 32 представлена CDC на экспрессирующих CLD18A2 клетках, вызванная химерными антителами изобретения.
На фиг. 33 представлена ADCC на клетках KATO-III, вызванная химерными антителами изобретения.
На фиг. 34 представлено продление срока жизни при обработке химерными антителами ch-175D10 и ch-163E12 на модели раннего лечения ксенотрансплантатов.
На фиг. 35 представлено продление срока жизни при обработке химерными антителами ch-175D10 и ch-163E12 на модели позднего лечения ксенотрансплантатов.
На фиг. 36 представлены опыты по картированию эпитопов с помощью антител ch-175D10 и ch163E12. Анализировали аминокислотную последовательность первого внеклеточного домена CLD18A2 без модификаций (верхний ряд, нет замены Cys-Ser) или с заменой цистеина на серии (нижний ряд, есть замена Cys-Ser).
На фиг. 37 представлены три различные модели укладки белка для первого внеклеточного домена CLD18A2.
На фиг. 38А, В и С представлено связывание ch-175D10, ch-163E12 и ch-125E1 с клетками HEK293, временно трансфицированными флуоресцентным маркером и либо CLD18A1/CLD18A2 мыши, либо CLD18A1/CLD18A2 человека, при анализе методом проточной цитометрии. Анализировали только трансфицированные клетки, а мертвые клетки исключали из анализа по окрашиванию с помощью PI.
На фиг. 39 представлен высокий уровень экспрессии CLD18A2 на плазматических мембранах в первичных опухолях желудка и метастазах рака желудка. Неизбирательные образцы первичного рака желудка и метастазов рака желудка (опухолей Крукенберга и лимфатических узлов) окрашивали с помощью специфичной к GC182 антисыворотки кролика. Иммуногистохимию, а также оценку интенсивности окрашивания (нет, слабая =1, средняя =2, сильная =3) и доли раковых клеток, проявляющих окрашивание плазматической мембраны (0-100%), выполняли профессиональные патологоанатомы. Каждый кружочек представляет независимый образец опухоли. Наблюдалось статистически значимое повышение интенсивности окраски в метастазах (р=0,034, точный критерий Фишера).
Осуществление изобретения
Описанные в настоящем изобретении антитела могут представлять собой выделенные моноклональные антитела, специфически связывающиеся с каким-нибудь эпитопом на CLD18, предпочтительно с эпитопом, расположенным во внеклеточных доменах CLD18, в частности первом внеклеточном домене. Выделенные моноклональные антитела, охваченные настоящим изобретением, включают антитела типа IgA, IgG1-4, IgE, IgM и IgD. В одном воплощении антитела представляют собой антитела типа IgG1, более предпочтительно IgG1 изотипа каппа или лямбда. В другом воплощении антитела представляют собой антитела типа IgG3, более предпочтительно IgG3 изотипа каппа или лямбда. В следующем воплощении антитела представляют собой антитела типа IgG4, более предпочтительно IgG4 изотипа каппа или лямбда. В следующем воплощении антитела представляют собой антитела типа IgA1 или IgA2. В следующем воплощении антитела представляют собой антитела типа IgM.
В одном воплощении изобретение касается антител, специфически связывающихся с клетками, экспрессирующими CLD18, которые предпочтительно (i) связываются с клетками, экспрессирующими CLD18A2, и (ii) не связываются с клетками, экспрессирующими CLD18A1, но не экспрессирующими CLD18A2. Антитела по изобретению предпочтительно (i) вызывают гибель клеток, экспрессирующих CLD18A2, но не вызывают гибели клеток, экспрессирующих CLD18A1, но не экспрессирующих CLD18A2.
В другом воплощении изобретение касается антител, которые (i) связываются с раковыми клетками, экспрессирующими CLD18, (ii) не связываются с экспрессирующими CLD18 клетками нормальной слизистой желудка и/или (iii) не связываются с экспрессирующими CLD18 клетками нераковой ткани легких.
Изобретение также охватывает антитела, которые (i) вызывают гибель раковых клеток, экспрессирующих CLD18, (ii) не вызывают гибели экспрессирующих CLD18 клеток нормальной слизистой желудка и/или (iii) не вызывают гибели экспрессирующих CLD18 клеток нераковой ткани легких.
В предпочтительных воплощениях антитела по изобретению (i) связываются с таким эпитопом на CLD18A2, которого нет на CLD18A1, предпочтительно SEQ ID NO: 21, 22 и 23, (ii) связываются с эпитопом, расположенным на петле 1 CLD18A2, предпочтительно SEQ ID NO: 28, (iii) связываются с эпитопом, расположенным на петле 2 CLD18A2, предпочтительно SEQ ID NO: 30, (iv) связываются с эпитопом, расположенным на петле D3 CLD18A2, предпочтительно SEQ ID NO: 31, (v) связываются с эпитопом, охватывающим петлю 1 CLD18A2 и петлю D3 CLD18A2, (vi) связываются с негликозилированным эпитопом, расположенным на петле D3 CLD18A2, предпочтительно SEQ ID NO: 29, или (vii) связываются с эпитопом, присутствующим в CLD18 человека и мыши (SEQ ID NO: 2, SEQ ID NO: 8 и SEQ ID NO: 35, SEQ ID NO: 37, соответственно).
В особенно предпочтительных воплощениях антитела по изобретению связываются с таким эпитопом на CLD18A2, которого нет на CLD18A1.
Антитела по изобретению включают полностью антитела человека. Такие антитела могут быть получены у трансгенного животного (кроме человека), напр., трансгенной мыши, способной вырабатывать множественные изотипы моноклональных антител человека к CLD18, подвергаясь рекомбинации V-D-J и переключению изотипа. Таким трансгенным животным может быть и трансгенный кролик, предназначенный для вырабатывания поликлональных антител, как это изложено в US 2003/0017534.
Связывание антител по изобретению с антигеном CLD18 может вызывать гибель клеток, экспрессирующих CLD18 (напр., раковых клеток), напр., путем активации системы комплемента. Гибель клеток, экспрессирующих CLD18, может происходить по одному или нескольким из следующих механизмов: обусловленной комплементом цитотоксичности (CDC) для клеток, экспрессирующих CLD18; апоптоза клеток, экспрессирующих CLD18; фагоцитоза эффекторными клетками экспрессирующих CLD18 клеток; или антителозависимой клеточной цитотоксичности (ADCC) эффекторными клетками экспрессирующих CLD18 клеток.
Для того, чтобы настоящее изобретение стало более понятным, сначала определим некоторые термины. Дополнительные определения приводятся по всему описанию.
Определение терминов
Термин "CLD18" относится к клаудину-18 и включает любые варианты, в том числе CLD18A1 и CLD18A2, конформаций, изоформы и видовые гомологи CLD18, которые естественным образом экспрессируются клетками либо экспрессируются клетками, трансфицированными геном CLD18. Предпочтительно "CLD18" относится к CLD18 человека, в особенности CLD18A2 человека и/или CLD18A1 человека, более предпочтительно CLD18A2 человека. CLD18A2 человека предпочтительно означает: (i) нуклеиновую кислоту, включающую нуклеотидную последовательность, кодирующую аминокислотную последовательность SEQ ID NO: 2, как-то нуклеиновую кислоту, включающую нуклеотидную последовательность SEQ ID NO: 1, либо (ii) белок, включающий аминокислотную последовательность SEQ ID NO: 2, и включает любые варианты, конформаций, изоформы и видовые гомологи CLD18A2, которые естественным образом экспрессируются клетками либо экспрессируются клетками, трансфицированными геном CLD18A2. CLD18A1 человека предпочтительно означает: (i) нуклеиновую кислоту, включающую нуклеотидную последовательность, кодирующую аминокислотную последовательность SEQ ID NO: 8, как-то нуклеиновую кислоту, включающую нуклеотидную последовательность SEQ ID NO: 7, либо (ii) белок, включающий аминокислотную последовательность SEQ ID NO: 8, и включает любые варианты, конформаций, изоформы и видовые гомологи CLD18A2, которые естественным образом экспрессируются клетками либо экспрессируются клетками, трансфицированными геном CLD18A1.
"Варианты CLD18" также включают формы CLD18, состоящие в основном из внеклеточного домена или эктодомена CLD18. "Внеклеточный домен" или "эктодомен" CLD18 относится к такой форме полипептида CLD18, которая в основном лишена трансмембранных и цитоплазматических доменов. Следует иметь в виду, что любые трансмембранные домены, идентифицированные у полипептидов CLD18 настоящего изобретения, идентифицируются согласно критериям, которые обычно применяются в этой области для идентификации гидрофобных доменов этого типа. Точные границы трансмембранного домена могут варьироваться, но скорее всего не более чем на 5 аминокислот на том или другом конце домена, первоначально идентифицированного в настоящем изобретении. Поэтому необязательно внеклеточный домен полипептида CLD18 может содержать по 5 или меньше аминокислот с каждой стороны границы трансмембранного домена/внеклеточного домена, идентифицированного в примерах или описании, причем такие полипептиды, вместе с соответствующим сигнальным пептидом или без него, а также кодирующие их нуклеиновые кислоты, предусмотрены настоящим изобретением.
Термин "вариант CLD18" охватывает: (i) сплайс-варианты CLD18, (ii) прошедшие посттрансляционные модификации варианты CLD18, предпочтительно включающие варианты в различном состоянии N-гликозилирования, (iii) конформационные варианты CLD18, предпочтительно включающие конформацию-1 CLD18, конформацию-2 CLD18 и конформацию-3 CLD18, (iv) свободные и гомотипически/гетеротипически ассоциированные варианты CLD18, локализованные в межклеточных платных контактах, и (v) раковые и нераковые варианты CLD18.
Термин "островок" относится к богатым сфинголипидами и холестерином микродоменам, локализованным в районе наружного монослоя плазматических мембран клеток. Способность некоторых белков к ассоциации в таких доменах и их способность к образованию "агрегатов" или "фокальных агрегатов" может повлиять на функцию белка. Например, при транслокации молекул CLD18 в такие структуры, после связывания с антителами настоящего изобретения, создается высокая плотность комплексов антиген CLD18-антитело в плазматической мембране. Такая высокая плотность комплексов антиген CLD18-антитело может способствовать эффективной активации системы комплемента при CDC.
Термины "конформация" и "топология" описывают, каким образом интегральная мембранная молекула располагается в клеточной мембране, в частности, какие ее участки являются внеклеточными и поэтому подходят для антител. Например, CLD18 может существовать в трех разных конформациях, которые больше всего зависят от того, что в нем преобладает - гомомеры или гетеромеры и от того, будет он встроен в супрамолекулярные структуры плотных контактов или "свободен". Эти различные состояния приводят к образованию различных эпитопов, подходящих для антител.
Согласно изобретению, термин "заболевание" относится к любому патологическому состоянию, в том числе раку, в частности тем формам рака, которые описаны в настоящем изобретении. Любая ссылка в нем на рак или определенные формы рака также включает их раковые метастазы.
Под "опухолью" понимается аномальная группа клеток или ткань, которая растет путем быстрой, неконтролируемой пролиферации клеток и продолжает расти после того, как исчезает раздражитель, вызвавший новый рост. Опухоли проявляют частичное или полное отсутствие структурной организации и функциональной координации с нормальной тканью и обычно образуют отдельную массу ткани, которая может быть доброкачественной либо злокачественной.
Под "метастазами" понимается диссеминация раковых клеток из своего первоначального места в другую часть организма. Образование метастазов является очень сложным процессом и зависит от отделения злокачественных клеток от первичной опухоли, инвазии внеклеточного матрикса, проникновения через базальные мембраны эндотелия с выходом в полости и сосуды организма, а затем, после переноса их через кровь, инфильтрации органов-мишеней. Наконец, развитие новой опухоли на месте мишени зависит от ангиогенеза. Метастазирование опухолей зачастую происходит даже после удаления первичной опухоли, так как клетки или компоненты опухолей могут остаться и приобрести метастатический потенциал. В одном воплощении термин "метастазы" по изобретению относится к "отдаленным метастазам", что означает метастазы, удаленные от первичной опухоли и системы местных лимфатических узлов. В одном воплощении термин "метастазы" по изобретению относится к метастазам лимфатических узлов. Одна особенная форма метастазов, которая подлежит лечению с помощью антител изобретения, представляет собой метастазы, происходящие из рака желудка как первичного очага. В предпочтительных воплощениях такие метастазы рака желудка представляют собой опухоли Крукенберга, перитонеальные метастазы и/или метастазы лимфатических узлов.
Опухоль Крукенберга - это редкая метастатическая опухоль яичников, составляющая от 1% до 2% всех опухолей яичников. Прогноз при опухолях Крукенберга все еще очень плохой, и пока что нет общепринятого способа лечения опухолей Крукенберга. Опухоль Крукенберга представляет собой метастатическую перстневидноклеточную аденокарциному яичников. Первичным очагом в большинстве случаев (70%) опухолей Крукенберга является желудок. Менее распространенными первичными очагами являются карциномы толстой кишки, аппендикса и молочной железы (главным образом инвазивная лобулярная карцинома). Описаны и редкие случаи опухолей Крукенберга, происходящих из карцином желчного пузыря, желчных путей, поджелудочной железы, тонкого кишечника, фатерова соска, шейки матки и мочевого пузыря/урахуса. Интервал между диагнозом первичной карциномы и последующим обнаружением поражения яичников обычно составляет 6 месяцев или меньше, но известны и более длительные промежутки. Во многих случаях первичная опухоль бывает очень маленькой и может остаться не замеченной. В анамнезе предшествующая карцинома желудка или иного органа выявляется лишь в 20-30% случаев.
Опухоль Крукенберга является примером избирательного распространения рака, чаще всего по оси желудок-яичники. Исторически эта ось диссеминации опухолей привлекала внимание многих патологов, особенно когда обнаружилось, что неоплазмы желудка избирательно дают метастазы в яичники без поражения других тканей. Долгое время пути метастазирования карциномы желудка в яичники оставались загадкой, но сейчас уже ясно, что наиболее вероятным путем распространения метастазов является ретроградный лимфатический путь.
Женщины с опухолями Крукенберга необычайно молоды для пациентов с метастатическими карциномами, так как им обычно за сорок, в среднем их возраст составляет 45 лет. Такой ранний возраст частично может быть связан с повышенной частотой перстневидноклеточной карциномы желудка у молодых женщин. Наиболее распространенные симптомы обычно связаны с поражением яичников, самыми частыми из них являются боль в животе и растяжение (в основном из-за обычно двусторонней и зачастую большой массы яичников). У остальных пациентов имеются неспецифические желудочно-кишечные симптомы либо нет симптомов. Кроме того, опухоли Крукенберга, как сообщалось, связаны с вирилизацией в результате продукции гормонов в строме яичников. В 50% случаев имеются асциты и обычно выявляются злокачественные клетки.
Опухоли Крукенберга являются двусторонними в более чем 80% известных случаев. Яичники обычно асимметрически увеличены и имеют шишковатые контуры. На срезах они желтого или белого цвета, обычно твердые, хотя иногда кистозные. Немаловажно то, что капсулярная поверхность яичников с опухолями Крукенберга обычно гладкая и свободна от спаек или перитонеальных отложений. Примечательно, что другие метастатические опухоли в яичниках часто связаны с поверхностными имплантатами. Этим может объясняться то, что макроскопическая морфология опухолей Крукенберга может обманчиво выглядеть как первичная опухоль яичников. Однако двусторонность опухолей Крукенберга свидетельствует об их метастатической природе.
У больных с опухолями Крукенберга общий показатель смертности весьма высокий. Большинство больных умирают в течение 2 лет (медиана выживаемости равна 14 мес.). В нескольких исследованиях показано, что прогноз бывает плохим, если первичная опухоль будет идентифицирована после обнаружения метастазов в яичниках, причем прогноз ухудшается, если первичная опухоль остается скрытой.
В литературе пока еще четко не установлена оптимальная стратегия лечения опухолей Крукенберга. Нет адекватного ответа на вопрос о том, стоит ли проводить хирургическое удаление. Химиотерапия или радиотерапия не оказывает значительного влияния на прогноз у больных с опухолями Крукенберга.
Термин "лечение заболевания" включает излечение, сокращение продолжительности, улучшение, предотвращение, замедление или торможение прогрессирования или ухудшения либо предотвращение или отсрочку возникновения заболевания или его симптомов.
Согласно изобретению, "образец" может представляет собой любой образец, применимый по настоящему изобретению, в частности биологический образец, как-то образец ткани, включая жидкие среды организма, и/или клеточный образец, причем он может быть получен стандартным способом, как-то методом тканевой биопсии, в том числе уколом, и взятием проб крови, бронхиальной жидкости, слюны, мочи, кала или иной жидкой среды организма. Согласно изобретению, термин "биологический образец" охватывает и порции биологических образцов.
Термин "антитело" относится к гликопротеинам, содержащим по меньшей мере две тяжелые (Н) цепи и две легкие (L) цепи, соединенные друг с другом дисульфидными связями, или к их антигенсвязывающей части. Термин "антитело" охватывает и все рекомбинантные формы антител, в частности антител, описанных в настоящем изобретении, напр., антитела, экспрессируемые в прокариотах, негликозилированные антитела, а также любые антигенсвязывающие фрагменты и производные антител, как описано ниже. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (сокращенно VH) и константной области тяжелой цепи. Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращенно VL) и константной области легкой цепи. Области VH и VL дополнительно подразделяются на гипервариабельные участки, именуемые участками, определяющими комплементарность (CDR), которые перемежаются с более консервативными участками, именуемыми каркасными участками (FR). Каждая область VH и VL состоит из трех CDRs и четырех FRs, которые располагаются в следующем порядке от N-конца к С-концу: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелых и легких цепей содержат связывающий домен, который взаимодействует с антигеном. Константные области антител могут опосредовать связывание иммуноглобулина с тканями или факторами организма, в том числе с различными клетками иммунной системы (напр., эффекторными клетками) и первым компонентом (C1q) классической системы комплемента.
Термин "гуманизированное антитело" относится к молекулам, содержащим антигенсвязывающий центр, который в основном происходит из иммуноглобулина другого вида, чем человек, тогда как остальная структура молекулы иммуноглобулина основана на структуре и/или последовательности иммуноглобулина человека. Антигенсвязывающий центр может содержать либо полные вариабельные домены, слитые с константными доменами, либо только гипервариабельные участки (CDR), пришитые к соответствующим каркасным участкам в вариабельных доменах. Антигенсвязывающие центры могут быть дикого типа либо модифицированы путем замены одной или нескольких аминокислот, напр., модифицированы так, чтобы они стали более похожими на иммуноглобулины человека. У некоторых форм гуманизированных антител сохраняются все последовательности CDR (напр., у гуманизированного антитела мыши, в котором содержатся все шесть CDR из антител мыши). У других форм содержится одно или несколько CDR, видоизмененных по отношению к исходному антителу.
Термин "химерное антитело" относится к таким антителам, у которых одна часть каждой из аминокислотных последовательностей тяжелых и легких цепей гомологична соответствующим последовательностям в антителах из определенного вида либо принадлежащих к определенному классу, тогда как остальная часть цепи гомологична соответствующим последовательностям в других антителах. Как правило, вариабельные области легких и тяжелых цепей копируют вариабельные области антител из одного вида млекопитающих, тогда как константные участки гомологичны последовательностям антител из другого вида. Одним из явных преимуществ таких химерных форм является то, что вариабельная область может быть легко получена из уже известных источников с помощью вполне доступных В-клеток или гибридом из других организмов, чем человек, в сочетании с константными участками, полученными, к примеру, из препаратов клеток человека. При том, что вариабельная область дает преимущество в легкости получения, а специфичность не зависит от источника, принадлежащая человеку константная область с меньшей вероятностью вызовет иммунный ответ у человека при введении антител, чем константная область из другого источника, чем человек. Впрочем, данное определение не ограничивается этим конкретным примером.
Термин "антигенсвязывающая часть" антитела (или просто "связывающая часть") в настоящем изобретении относится к одному или нескольким фрагментам антитела, сохраняющим способность к специфическому связыванию с антигеном. Было показано, что антигенсвязывающая функция антител может выполняться фрагментами целого антитела. Примеры связывающих фрагментов, охваченных термином "антигенсвязывающая часть" антитела, включают: (i) Fab-фрагменты - одновалентные фрагменты, состоящие из доменов VL, VH, CL и CH; (ii) F(ab')2-фрагменты - двухвалентные фрагменты, содержащие два Fab-фрагмента, соединенные дисульфидным мостиком на шарнирном участке; (iii) Fd-фрагменты, состоящие из доменов VH и CH; (iv) Fv-фрагменты, состоящие из доменов VL и VH одной ветви антитела; (v) dAb-фрагменты (Ward et al., (1989) Nature 341: 544-546), которые состоят из домена VH; (vi) выделенные участки комплементарности (CDR); и (vii) комбинации из двух или нескольких выделенных CDRs, которые необязательно могут соединяться синтетическим линкером. Кроме того, хотя два домена Fv-фрагмента, VL и VH, кодируются отдельными генами, их можно соединить, используя рекомбинантные методы, синтетическим линкером, позволяющим вырабатывать их в виде единой белковой цепи, в которой области VL и VH спарены с образованием одновалентных молекул, известных как одноцепочечные Fv (scFv); напр., см. Bird et al. (1988) Science 242: 423-426; и Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85: 5879-5883). Такие одноцепочечные антитела тоже охватываются термином "антигенсвязывающая часть" антитела. Другим примером являются слитые белки связывающих доменов иммуноглобулина, включающие: (i) полипептид связывающего домена, слитый с полипептидом шарнирного участка иммуноглобулина, (ii) константную область CH2 тяжелой цепи иммуноглобулина, слитую с шарнирным участком, и (iii) константную область CH3 тяжелой цепи иммуноглобулина, слитую с константной областью CH2. Полипептид связывающего домена может представлять собой вариабельную область тяжелой цепи или вариабельную область легкой цепи. Слитые белки связывающих доменов иммуноглобулина более подробно изложены в US 2003/0118592 и US 2003/0133939. Такие фрагменты антител получают стандартными методами, известными специалистам в этой области, причем фрагменты подвергают скринингу на пригодность таким же образом, как и интактные антитела.
Термин "эпитоп" обозначает белковую детерминанту, способную связываться с антителом, при этом "связывание" предпочтительно относится к специфическому связыванию. Эпитопы обычно состоят из химических активных поверхностных группировок таких молекул, как аминокислоты, или боковых цепей Сахаров, причем обычно они обладают специфическими характеристиками трехмерной структуры и специфическими характеристиками заряда. Конформационные и неконформационные эпитопы отличаются между собой тем, что связывание с первыми из них исчезает в присутствии денатурирующих растворителей.
Термин "дискретный эпитоп" обозначает конформационный эпитоп на белковом антигене, который образуется по меньшей мере из двух отдельных участков первичной последовательности белка.
Термин "биспецифичная молекула" служит для обозначения любого агента, напр., белка, пептида либо белкового или пептидного комплекса, обладающего двумя различными специфичностями связывания. Например, молекула может связываться или взаимодействовать с (а) антигеном клеточной поверхности и (b) Fc-рецептором на поверхности эффекторной клетки. Термин "мультиспецифичная молекула" или "гетероспецифичная молекула" служит для обозначения любого агента, напр., белка, пептида либо белкового или пептидного комплекса, обладающего более чем двумя различными специфичностями связывания. Например, молекула может связываться или взаимодействовать с (а) антигеном клеточной поверхности, (b) Fc-рецептором на поверхности эффекторной клетки и (c) по меньшей мере еще с одним компонентом. Соответственно, изобретение включает биспецифичные, триспецифичные, тетраспецифичные и другие мультиспецифичные молекулы, направленные на CLD18 и на другие мишени, как-то Fc-рецепторы на эффекторных клетках. Термин "биспецифичные антитела" также включает диатела. Диатела представляют собой двухвалентные, биспецифичные антитела, в которых домены VH и VL экспрессируются на одной полипептидной цепи, но с помощью такого линкера, который оказывается слишком коротким для спаривания между двумя доменами на одной и той же цепи, тем самым вынуждая домены спариваться с комплементарными доменами другой цепи и создавая два антигенсвязывающих центра (напр., см. Holliger P. et al. (1993) Proc. Natl. Acad. Sci. USA 90: 6444-6448; Poljak R.J. et al. (1994) Structure 2: 1121-1123).
Изобретение также включает производные описанных в нем антител. Термин "производные антител" относится к любым модифицированным формам антител, напр., конъюгатам антител с другим агентом или антителом. В настоящем изобретении антитело "происходит из" определенной зародышевой последовательности, если оно выделено из системы при иммунизации животного или при скрининге библиотеки генов иммуноглобулинов, при этом выделенное антитело по аминокислотной последовательности по меньшей мере на 90%, более предпочтительно на 95%, еще более предпочтительно на 96, 97, 98 или 99% идентично аминокислотной последовательности, кодируемой гаметным геном иммуноглобулина. Как правило, антитело, происходящее из определенной зародышевой последовательности, должно проявлять не более 10 отличий по аминокислотам, более предпочтительно не более 5 и еще более предпочтительно не более 4, 3, 2 или 1 отличия по аминокислотам от аминокислотной последовательности, кодируемой гаметным геном иммуноглобулина.
В настоящем изобретении термин "гетероантитела" относится к двум или нескольким антителам, их производным или соединенным вместе антигенсвязывающим участкам, из которых по меньшей мере два обладают различными специфичностями. К этим различным специфичностям относятся специфичность связывания с Fc-рецептором на эффекторных клетках и специфичность связывания с антигеном или эпитопом на клетках мишени, напр., опухолевых клетках.
Описанные антитела могут представлять собой антитела человека. Термин "антитела человека" в настоящем изобретении служит для обозначения таких антител, у которых вариабельные и константные области происходят из зародышевых последовательностей иммуноглобулинов человека. Антитела человека по изобретению могут содержать остатки аминокислот, не кодируемых зародышевыми последовательностями иммуноглобулинов человека (напр., мутации, введенные методом случайного или направленного мутагенеза in vitro либо при соматических мутациях in vivo).
Термин "моноклональные антитела" в настоящем изобретении относится к препаратам молекул антител одинакового молекулярного состава. Моноклональные антитела проявляют единую специфичность связывания и сродство к определенному эпитопу. В одном воплощении моноклональные антитела вырабатываются гибридомой, включающей В-клетки, полученные из животного кроме человека, напр., мыши, слитые с 'бессмертными' клетками.
Термин "рекомбинантные антитела" в настоящем изобретении охватывает все антитела, полученные, экспрессированные, созданные или выделенные рекомбинантным способом, как-то: (а) антитела, выделенные из животного (напр., мыши), трансгенного или трансхромосомного в отношении генов иммуноглобулинов, или из гибридомы, полученной из него; (b) антитела, выделенные из клеток-хозяев, трансформированных для экспрессирования этого антитела, напр., из трансфектомы; (c) антитела, выделенные из рекомбинантной комбинаторной библиотеки антител; и (d) антитела, полученные, экспрессированные, созданные или выделенные любым иным способом, включающим сплайсинг последовательностей генов иммуноглобулинов с другими последовательностями ДНК.
Термин "трансфектома" в настоящем изобретении охватывает рекомбинантные клетки эукариотического хозяина, экспрессирующие антитела, как-то клетки СНО, клетки NS/0, клетки HEK293, клетки HEK293T, клетки растений или грибов, включая дрожжевые клетки.
В настоящем изобретении "гетерологичные антитела" определяются по отношению к трансгенному организму, вырабатывающему такие антитела. Этот термин относится к таким антителам, у которых аминокислотная последовательность или кодирующая их последовательность нуклеиновой кислоты соответствует той, что находится у организма, не являющегося трансгенным организмом, и обычно происходит из другого вида, чем трансгенный организм.
В настоящем изобретении "гетерогибридные антитела" означают такие антитела, у которых легкие и тяжелый цепи происходят из различных организмов. Например, антитела, у которых тяжелая цепь человека связана с легкой цепью мыши, являются гетерогибридными антителами.
Описанные антитела предпочтительно являются выделенными. "Выделенные антитела" в настоящем изобретении означают такие антитела, которые практически свободны от других антител, обладающих иной антигенной специфичностью (напр., выделенные антитела, специфически связывающиеся с CLD18, практически свободны от антител, специфически связывающихся с другими антигенами, чем CLD18). Однако выделенные антитела, специфически связывающиеся с эпитопом, изоформой или вариантом CLD18 человека, могут обладать перекрестной реактивностью к другим родственным антигенам, напр., из другого вида (напр., видовым гомологам CLD18). Более того, выделенные антитела могут быть практически свободными от других клеточных материалов и/или химических веществ. В одном воплощении изобретения комбинация "выделенных" моноклональных антител означает, что эти антитела имеют различные специфичности и объединены в хорошо определенной композиции.
Согласно изобретению, термин "связывание" предпочтительно относится к "специфическому связыванию". В настоящем изобретении "специфическое связывание" относится к связыванию антител с заданным антигеном. Как правило, антитело связывается со сродством, соответствующим значению KD в 1×10-7 М или меньше, а с заданным антигеном оно связывается со сродством, соответствующим значению KD, как минимум на два порядка меньшему, чем его сродство при связывании с неспецифическим антигеном (напр., BSA, казеином), другим, чем заданный антиген или близкородственный антиген.
Термин "KD" (М) в настоящем изобретении служит для обозначения равновесной константы диссоциации для определенного взаимодействия антитело-антиген.
В настоящем изобретении "изотип" означает класс антитела (напр., IgM или IgG1), кодируемого генами константной области тяжелой цепи.
В настоящем изобретении "переключение изотипа" относится к явлению, при котором класс, то есть изотип антитела, меняется из одного класса Ig на один из других классов Ig.
Термин "встречающийся в природе" при его применении в отношении объекта означает то, что объект может встречаться в природе. Например, последовательность полипептида или полинуклеотида у организма (включая вирусы), которая может быть выделена из природного источника и не подвергалась преднамеренной модификации, является встречающейся в природе (природной).
Термин "перестроенный" в настоящем изобретении обозначает такой локус тяжелой цепи или легкой иммуноглобулина, в котором V-сегмент непосредственно соседствует с D-J или J-сегментом в конформаций, кодирующей практически полный домен VH или VL, соответственно. Перестроенный локус гена иммуноглобулина (антитела) можно идентифицировать при сравнении с гаметной ДНК, при этом перестроенный локус будет содержать по меньшей мере один подвергшийся рекомбинации элемент гомологии в виде гептамера/нонамера.
Термин "неперестроенный" или "в гаметной конфигурации" при его применении в отношении V-сегмента означает такую конфигурацию, в которой V-сегмент не подвергается рекомбинации с тем, чтобы оказаться в непосредственном соседстве с D- или J-сегментом.
Термин "молекула нуклеиновой кислоты" в настоящем изобретении служит для обозначения молекул ДНК и молекул РНК. Молекула нуклеиновой кислоты может быть одноцепочечной или двухцепочечной, но предпочтительно она представляет собой двухцепочечную ДНК.
Молекулы нуклеиновых кислот, описанные в настоящем изобретении, предпочтительно были выделены. Термин "выделенная нуклеиновая кислота" по изобретению означает, что эта нуклеиновая кислота была: (i) амплифицирована in vitro, к примеру, методом полимеразной цепной реакции (ПЦР); (ii) получена рекомбинантным образом при клонировании; (iii) очищена, к примеру, путем расщепления и фракционирования методом гель-электрофореза; или (iv) синтезирована, к примеру, путем химического синтеза. Выделенная нуклеиновая кислота есть такая нуклеиновая кислота, которая доступна для обработки методами рекомбинантной ДНК.
Нуклеиновой кислоты по изобретению могут присутствовать сами по себе или в комбинации с другими нуклеиновыми кислотами, которые могут быть гомологичными или гетерологичными. В предпочтительных воплощениях нуклеиновая кислота функционально соединена с контролирующими экспрессию последовательностями, которые могут быть гомологичными или гетерологичными относительно данной нуклеиновой кислоты. Термин "гомологичная" означает то, что нуклеиновая кислота естественным образом функционально соединена с контролирующей экспрессию последовательностью, а термин "гетерологичная" означает то, что нуклеиновая кислота не соединена функционально с контролирующей экспрессию последовательностью естественным образом.
Нуклеиновая кислота, как-то нуклеиновая кислота, экспрессирующая РНК и/или белок или пептид, и контролирующая экспрессию последовательность "функционально" соединяются друг с другом, если они ковалентно соединяются друг с другом таким образом, что экспрессия или транскрипция данной нуклеиновой кислоты находится под контролем или под влиянием данной контролирующей экспрессию последовательности. Если нуклеиновая кислота будет транслироваться в функциональный белок, то при функциональном соединении контролирующей экспрессию последовательности с кодирующей последовательностью индукция данной контролирующей экспрессию последовательности приведет к транскрипции данной нуклеиновой кислоты без сдвига рамки считывания в кодирующей последовательности или потери способности данной кодирующей последовательности к транслированию в требуемый белок или пептид.
Термин "контролирующая экспрессию последовательность" согласно изобретению включает промоторы, сайты рибосомного связывания, энхансеры и другие контрольные элементы, регулирующие транскрипцию гена или трансляцию мРНК. В предпочтительных воплощениях изобретения контролирующие экспрессию последовательности могут быть регулируемыми. Точная структура контролирующих экспрессию последовательностей может варьировать в зависимости от вида или типа клеток, но в общем она включает 5'-нетранскрибируемые и 5'- и 3'-нетранслируемые последовательности, которые участвуют в запуске транскрипции и трансляции, соответственно, такие как рамка TATA, последовательность кэппинга, последовательность СААТ и др. Более определенно 5'-нетранскрибируемые контролирующие экспрессию последовательности содержат участок промотора, который включает последовательность промотора для транскрипционного контроля функционально связанной нуклеиновой кислоты. Контролирующие экспрессию последовательности также могут включать последовательности энхансеров или вышележащие последовательности активаторов.
Согласно изобретению, термин "промотор" или "участок промотора" относится к последовательности нуклеиновой кислоты, находящейся впереди (5') от экспрессируемой последовательности нуклеиновой кислоты и контролирующей экспрессию этой последовательности, составляя сайт распознавания и связывания РНК-полимеразы. "Участок промотора" может включать дополнительные сайты распознавания и связывания других факторов, участвующих в регуляции транскрипции гена. Промотор может контролировать транскрипцию прокариотического или эукариотического гена. Кроме того, промотор может быть "индуцибельным" и запускать транскрипцию в ответ на индуцирующего агента, либо он может быть "конститутивным", если транскрипция не контролируется индуцирующим агентом. Ген, находящийся под контролем индуцибельного промотора, не экспрессируется или экспрессируется лишь в небольшой степени, если индуцирующий агент отсутствует. В присутствии индуцирующего агента происходит запуск гена или повышение уровня транскрипции. Обычно это опосредуется связыванием специфического фактора транскрипции.
К предпочтительным промоторам по изобретению относятся промоторы для SP6, полимеразы Т3 и Т7, РНК-промотор U6 человека, промотор CMV и их искусственные гибридные промоторы (напр., CMV), одна или несколько частей которых слиты с одной или несколькими частями промоторов генов других клеточных белков, таких, напр., как GAPDH (глицеральдегид-3-фосфатдегидрогеназа) человека, и включают или не включают дополнительные интроны.
Согласно изобретению, термин "экспрессия" применяется в самом общем значении и включает продукцию РНК либо РНК и белка/пептида. Он также охватывает частичную экспрессию нуклеиновых кислот. Кроме того, экспрессия может осуществляться кратковременным или устойчивым образом.
В предпочтительном воплощении молекула нуклеиновой кислоты по изобретению находится в векторе, если нужно, то вместе с промотором, контролирующим экспрессию данной нуклеиновой кислоты. Термин "вектор" применяется в самом общем значении и включает любые промежуточные носители для нуклеиновой кислоты, которые дают возможность, к примеру, ввести данную нуклеиновую кислоту в прокариотические и/или эукариотические клетки и, если нужно, встроить в геном. Вектора этого типа предпочтительно реплицируются и/или экспрессируются в клетках. Вектора включают плазмиды, фагемиды, бактериофаги или вирусные геномы. Термин "плазмида" в настоящем изобретении в общем относится к конструкции из внехромосомного генетического материала, обычно кольцевого дуплекса ДНК, который может реплицироваться независимо от хромосомной ДНК.
В качестве вектора для экспрессии антител может использоваться такой тип вектора, у которого тяжелая цепь и легкая цепь антитела находятся в разных векторах, либо такой тип вектора, у которого тяжелая цепь и легкая цепь находятся в одном и том же векторе.
Изложенные здесь положения относительно определенных последовательностей нуклеиновых кислот и аминокислотных последовательностей, напр., приведенных в перечне последовательностей, следует понимать так, что они касаются и модификаций данных конкретных последовательностей, дающих последовательности, функционально эквивалентные данным конкретным последовательностям, напр., аминокислотные последовательности, проявляющие свойства, идентичные или близкие свойствам этих конкретных аминокислотных последовательностей, и последовательности нуклеиновых кислот, кодирующих аминокислотные последовательности, проявляющие свойства, идентичные или близкие свойствам аминокислотных последовательностей, кодируемых этими конкретными последовательностями нуклеиновых кислот. Одним из важных свойств является сохранность связывания антител со своими мишенями или эффекторных функций антител. Предпочтительно, если последовательность, модифицированная по отношению к определенной последовательности, заменяет эту конкретную последовательность в антителе, то при этом сохраняется связывание данного антитела с CLD18 и предпочтительно функции данного антитела, описанные в настоящем изобретении, напр., лизис по механизму CDC или лизис по механизму ADCC.
Специалистам должно быть известно, что в особенности последовательности CDR, гипервариабельных и вариабельных участков можно модифицировать без потери ими способности к связыванию с CLD18. Например, участки CDR должны быть либо идентичны, либо сильно гомологичны участкам антител, приведенных в настоящем изобретении. Под "сильно гомологичными" подразумевается то, что в участках CDR можно делать от 1 до 5, предпочтительно от 1 до 4, как-то от 1 до 3 либо 1 или 2 замены. Кроме того, гипервариабельные и вариабельные участки можно модифицировать таким образом, чтобы они проявляли существенную гомологию к участкам антител, конкретно приведенных в настоящем изобретении.
Следует иметь в виду, что определенные нуклеиновые кислоты, описанные в настоящем изобретении, также включают нуклеиновые кислоты, модифицированные с целью оптимизации употребления кодонов в определенных клетках или организме хозяина. Отличия по употребительности кодонов между организмами могут приводить к различным проблемам в отношении экспрессии гетерологичных генов. Оптимизация кодонов путем замены одного или нескольких нуклеотидов в исходной последовательности может привести к оптимизации экспрессии нуклеиновой кислоты, в частности к оптимизации эффективности трансляции в гомологичном или гетерологичном хозяине, в котором должна экспрессироваться данная нуклеиновая кислота. Например, если нуклеиновые кислоты, полученные из человека и кодирующие константные области или каркасные участки антител, будут использоваться по настоящему изобретению, напр., для получения химерных или гуманизированных антител, то будет предпочтительней модифицировать данные нуклеиновые кислоты с целью оптимизации употребления кодонов, особенно если данные нуклеиновые кислоты, необязательно слитые с гетерологичными нуклеиновыми кислотами, как-то нуклеиновыми кислотами, полученными из других организмов, как описано в настоящем изобретении, будут экспрессироваться в клетках от другого организма, а не человека, как-то мыши или хомячка. Например, последовательности нуклеиновых кислот, кодирующих константные области легких и тяжелых цепей человека, как-то согласно SEQ ID NO: 40 и 45, соответственно, можно модифицировать так, чтобы они включали замену одного или нескольких, предпочтительно по меньшей мере 1, 2, 3, 4, 5, 10, 15, 20 и предпочтительно вплоть до 10, 15, 20, 25, 30, 50, 70 или 100 и больше нуклеотидов, приводящих к оптимизации употребления кодонов, но не к изменению аминокислотной последовательности. Такие замены нуклеотидов предпочтительно касаются замены нуклеотидов в SEQ ID NO: 40 и 45, соответственно, из числа замен, приведенных в нижеследующих выравниваниях SEQ ID NO: 40 и 45, соответственно, со своими модифицированными копиями, и не вызывающих изменения кодируемой аминокислотной последовательности, либо они касаются соответствующих замен по соответствующим положениям в других последовательностях нуклеиновых кислот, кодирующих константные области легких и тяжелых цепей человека, соответственно. Предпочтительно в последовательностях нуклеиновых кислот, кодирующих константные области легких и тяжелых цепей человека, соответственно, производятся все замены, приведенные в нижеследующих выравниваниях SEQ ID NO: 40 и 45, соответственно, со своими модифицированными копиями, и не вызывающие изменения кодируемой аминокислотной последовательности.
Выравнивание SEQ ID NO: 40 и SEQ ID NO: 147:

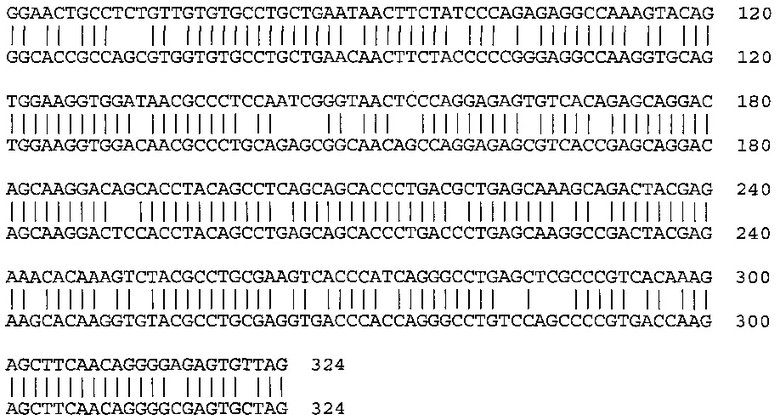
Выравнивание SEQ ID NO: 45 и SEQ ID NO: 149:


Кроме того, по настоящему изобретению может понадобиться модифицировать описанные в нем аминокислотные последовательности, в частности константных участков тяжелой цепи человека, чтобы адаптировать эти последовательности к нужному аллотипу, напр., аллотипу, распространенному в европейской расе. Такие модификации предпочтительно выбираются из группы, состоящей из следующих замен аминокислот в SEQ ID NO: 46 или по соответствующим положениям в других константных участках тяжелой цепи человека: K93R, D235E и L237M. Предпочтительно все эти модификации входят в аминокислотные последовательности константных участков тяжелой цепи человека.
В соответствии с изобретением, термин "соответствующие положения" относится к таким остаткам нуклеотидов или аминокислот, которые при выравнивании последовательностей двух нуклеиновых кислот или белков совмещаются друг с другом.
Предпочтительно степень идентичности между последовательностью определенной нуклеиновой кислоты, описанной в настоящем изобретении, и последовательностью нуклеиновой кислоты, модифицированной по отношению к или являющейся вариантом данной конкретной нуклеиновой кислоты, составляет по меньшей мере 70%, предпочтительно по меньшей мере 75%, более предпочтительно по меньшей мере 80%, еще более предпочтительно по меньшей мере 90% и наиболее предпочтительно по меньшей мере 95, 96, 97, 98 или 99%. Касательно вариантов нуклеиновых кислот CLD18, степень идентичности предпочтительно приводится для участка из по меньшей мере 300, по меньшей мере 400, по меньшей мере 450, по меньшей мере 500, по меньшей мере 550, по меньшей мере 600, по меньшей мере 650, по меньшей мере 700, по меньшей мере 750 или по меньшей мере 780 нуклеотидов. В предпочтительных воплощениях степень идентичности приводится для всего протяжения эталонной последовательности нуклеиновой кислоты, как-то последовательности нуклеиновой кислоты, приведенной в перечне последовательностей. Предпочтительно эти две последовательности способны гибридизоваться и образовывать устойчивый дуплекс друг с другом, причем гибридизация предпочтительно проводится в условиях, способствующих специфической гибридизации между полинуклеотидами (строгих условиях). Строгие условия описаны, к примеру, в Molecular Cloning: A Laboratory Manual, J. Sambrook et al., Editors, 2nd Edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York, 1989; или Current Protocols in Molecular Biology, F.M. Ausubel et al., Editors, John Wiley & Sons, Inc., New York; и означают, к примеру, гибридизацию при 65°С в буфере для гибридизации (3,5×SSC, 0,02% фиколла, 0,02% поливинилпирролидона, 0,02% бычьего сывороточного альбумина, 2,5 мМ NaH2PO4 pH 7, 0,5% SDS, 2 мМ EDTA). SSC означает 0,15 М хлорид натрия/0,15 М цитрат натрия, pH 7. После гибридизации мембрану, на которую была перенесена ДНК, промывают, например, в 2×SSC при комнатной температуре, а затем в 0,1-0,5×SSC/0,1×SDS при температуре вплоть до 68°С.
Предпочтительно степень сходства, предпочтительно идентичности между определенной аминокислотной последовательностью, описанной в настоящем изобретении, и аминокислотной последовательностью, модифицированной по отношению к или являющейся вариантом данной конкретной аминокислотной последовательности, составляет по меньшей мере 70%, предпочтительно по меньшей мере 80%, еще более предпочтительно по меньшей мере 90% и наиболее предпочтительно по меньшей мере 95, 96, 97, 98 или 99%. Касательно вариантов полипептида CLD18, степень сходства или идентичности приводится предпочтительно для участка из по меньшей мере 100, по меньшей мере 120, по меньшей мере 140, по меньшей мере 160, по меньшей мере 180, по меньшей мере 200, по меньшей мере 220, по меньшей мере 240, по меньшей мере 250 или 260 аминокислот. В предпочтительных воплощениях степень сходства или идентичности приводится для всего протяжения эталонной аминокислотной последовательности, как-то аминокислотной последовательности, приведенной в перечне последовательностей.
Все вышеописанные модифицированные последовательности или варианты последовательностей входят в рамки настоящего изобретения.
"Сходство последовательностей" означает процент таких аминокислот, которые либо идентичны, либо представляют консервативные замены аминокислот. "Идентичность последовательностей" между двумя последовательностями полипептидов или нуклеиновых кислот означает процент таких аминокислот или нуклеотидов, которые идентичны между этими последовательностями.
"Идентичность в процентах" получается после наилучшего выравнивания, причем эти проценты чисто статистические, а различия между двумя последовательностями распределяются случайным образом и по всей длине. Сравнение последовательностей между двумя нуклеотидными или аминокислотными последовательностями обычно осуществляется путем сравнения этих последовательностей после оптимального их выравнивания, причем сравнение проводится по сегментам или по "окнам сравнения" с тем, чтобы идентифицировать и сравнить локальные участки сходства последовательностей. Оптимальное выравнивание последовательностей для сравнения может быть получено, помимо сравнения вручную, при помощи алгоритма локальной гомологии Smith and Waterman, 1981, Ads App. Math. 2, 482, при помощи алгоритма локальной гомологии Neddleman and Wunsch, 1970, J. Mol. Biol. 48, 443, при помощи метода поиска сходства Pearson and Lipman, 1988, Proc. Natl Acad. Sci. USA 85, 2444, или при помощи компьютерных программ, использующих эти алгоритмы (GAP, BESTFIT, FASTA, BLAST Р, BLAST N и TFASTA в комплекте программ Wisconsin Genetics Software Package, Genetics Computer Group, 575 Science Drive, Madison, Wis.).
Идентичность в процентах рассчитывают путем определения числа идентичных положений между двумя сравниваемыми последовательностями, деления этого числа на общее число сравниваемых положений и умножения результата на 100, получая при этом степень идентичности между этими двумя последовательностями в процентах.
"Консервативные замены" могут производиться, к примеру, на основе сходства по полярности, заряду, растворимости, гидрофобности, гидрофильности и/или амфипатической природе рассматриваемых остатков. Например, (а) неполярные (гидрофобные) аминокислоты включают аланин, лейцин, изолейцин, валин, пролин, фенилаланин, триптофан и метионин; (b) полярные нейтральные аминокислоты включают глицин, серии, треонин, цистеин, тирозин, аспарагин и глютамин; (c) положительно заряженные (основные) аминокислоты включают аргинин, лизин и гистидин; и (d) отрицательно заряженные (кислые) аминокислоты включают аспарагиновую кислоту и глютаминовую кислоту. Как правило, замены производятся внутри групп (a)-(d). Кроме того, глицин и пролин можно заменять друг на друга на основе их способности разрушать α-спирали. Некоторые предпочтительные замены могут производиться внутри следующих групп: (i) S и Т; (ii) Р и G; и (iii) А, V, L и I. Исходя из известного генетического кода и методов рекомбинантной и синтетической ДНК, квалифицированный специалист может легко сконструировать ДНК, кодирующую варианты с консервативными заменами аминокислот.
Настоящее изобретение включает антитела, у которых проводились изменения в области Fc для того, чтобы изменить функциональные или фармакокинетические свойства этих антител. Такие изменения могут привести к снижению или повышению связывания C1q и механизма CDC либо связывания FcγR и механизма ADCC. Например, можно произвести замены одного или нескольких аминокислотных остатков константной области тяжелой цепи, что приведет к изменению эффекторной функции при сохранении способности к связыванию с антигеном по сравнению с модифицированным антителом, см. US 5,624,821 и US 5,648,260.
Время полужизни антител in vivo можно улучшить путем модификации эпитопа спасательного рецептора константного домена Ig или Ig-подобного константного домена таким образом, чтобы молекула не содержала интактного домена CH2 или интактной Fc-области Ig, см. US 6,121,022 и US 6,194,551. К тому же время полужизни in vivo можно повысить с помощью мутаций в области Fc, напр., путем замены лейцина на треонин в положении 252, замены серина на треонин в положении254 или замены фенилаланина на треонин в положении 254 256, см. US 6,277,375.
Кроме того, можно модифицировать профиль гликозилирования антител с тем, чтобы изменить эффекторную функцию антител. Например, можно экспрессировать антитела в трансфектоме, не способной к добавлению звена фукозы, которое в норме присоединяется к Asn в положении 297 области Fc с тем, чтобы усилить сродство Fc-области к Fc-рецепторам, что в свою очередь приведет к повышению ADCC антител в присутствии NK-клеток, см. Shield et al. (2002) JBC, 277: 26733. Кроме того, можно провести модификацию галактозилирования с тем, чтобы модифицировать CDC.
С другой стороны, в следующем воплощении можно ввести мутации случайным образом по всей или по части кодирующей последовательности антител к CLD18, как-то методом насыщающего мутагенеза, а затем провести скрининг модифицированных антител к CLD18 на наличие активности связывания.
Термин "рекомбинантные клетки-хозяева" (или просто "клетки-хозяева") в настоящем изобретении служит для обозначения клеток, в которые был введен рекомбинантный экспрессионный вектор. Следует иметь в виду, что такие термины относятся не только к определенным клеткам субъекта, но и к потомству таких клеток. Поскольку в последующих поколениях могут произойти некоторые модификации либо вследствие мутаций, либо вследствие влияния окружающей среды, то такое потомство на самом деле может оказаться не идентичным исходным клеткам, но оно все-таки охватывается рамками термина "клетки-хозяева" в настоящем изобретении. Рекомбинантные клетки-хозяева включают, к примеру, такие трансфектомы, как клетки СНО, клетки NS/0 и лимфоцитарные клетки.
В настоящем изобретении термин "субъект" включает и человека, и животных. Термин "животное, а не человек" включает всех позвоночных, напр., млекопитающих и не млекопитающих, как-то приматов (кроме человека), овец, собак, коров, кур, амфибий, рептилий и т.д.
Термин "трансгенное животное" относится к таким животным, в геноме которых содержится один или несколько трансгенов, предпочтительно трансгенов тяжелой и/или легкой цепи (встроенных либо не встроенных в природную геномную ДНК животного), и которые предпочтительно способны экспрессировать эти трансгены. Например, трансгенная мышь может содержать трансген легкой цепи человека и либо трансген тяжелой цепи человека, либо трансхромосому тяжелой цепи человека, так что эта мышь будет вырабатывать антитела человека против CLD18 при иммунизации антигеном CLD18 и/или клетками, экспрессирующими CLD18. Трансген тяжелой цепи человека может быть встроен в хромосомную ДНК мыши, как в случае трансгенных мышей, напр., мышей HuMAb, как-то мышей НСо7 или HCol2, или же трансген тяжелой цепи человека может находиться вне хромосом, как в случае трансхромосомных мышей, напр., мышей KM, как описано в WO 02/43478. Такие трансгенные и трансхромосомные мыши могут обладать способностью вырабатывать множественные изотипы моноклональных антител человека к CLD18 (напр., IgG, IgA и/или IgE), подвергаясь рекомбинации V-D-J и переключению изотипа.
"Снижать" или "ингибировать" в настоящем изобретении означает способность вызывать общее снижение уровня, предпочтительно на 5% или больше, на 10% или больше, на 20% или больше, более предпочтительно на 50% или больше, наиболее предпочтительно на 75% или больше, напр., уровня пролиферации клеток.
Механизмы действия mAb
Хотя далее представлены соображения касательно механизма, лежащего в основе терапевтической эффективности антител по изобретению, это никоим образом не следует рассматривать как ограничение изобретения.
Антитела, описанные в настоящем изобретении, предпочтительно взаимодействуют с компонентами иммунной системы, предпочтительно по механизму ADCC или CDC. Антитела по изобретению также можно использовать для доставки полезных веществ (напр., радиоизотопов, препаратов или токсинов), чтобы непосредственно уничтожить опухолевые клетки, либо использовать синергетическим образом вместе с традиционными средствами химиотерапии, воздействуя на опухоли через комплементарные механизмы действия, которые могут включать противоопухолевые иммунные ответы, которые могли быть нарушены вследствие цитотоксических побочных эффектов средств химиотерапии на Т-лимфоциты. Однако антитела по изобретению также могут оказывать эффект просто путем связывания с CLD18 на клеточной поверхности, тем самым, напр., блокируя пролиферацию клеток.
Антителозависимая клеточная цитотоксичность (ADCC)
ADCC означает способность эффекторных клеток вызывать гибель других клеток, описанных в настоящем изобретении, в частности лимфоцитов, для чего предпочтительно нужно, чтобы клетки мишени были маркированы антителом.
ADCC преимущественно происходит тогда, когда антитела связываются с антигенами на раковых клетках, а Fc-домены антител занимают Fc-рецепторы (FcR) на поверхности иммунных эффекторных клеток. Идентифицировано несколько семейств Fc-рецепторов, а специфические популяции клеток характерным образом экспрессируют определенные Fc-рецепторы. ADCC можно рассматривать как механизм, который в различной степени непосредственно вызывает немедленное разрушение опухолей, что ведет к презентации антигена и индуцирует направленные на опухоли Т-клеточные ответы. Предпочтительно индукция ADCC in vivo должна вызывать направленные на опухоли Т-клеточные ответы и реакции собственных антител организма.
Обусловленная комплементом цитотоксичность (CDC)
Другим способом гибели клеток является CDC, которую могут вызывать антитела. Наиболее эффективным изотипом для активации комплемента является IgM. IgG1 и IgG3 также очень эффективно вызывают CDC через классический путь активации комплемента. Предпочтительно в этом каскаде образование комплексов антиген-антитело приводит к разблокированию множественных C1q-связывающих центров, находящихся в непосредственной близости на доменах CH2 взаимодействующих молекул антител, как-то молекул IgG (C1q является одним из трех субкомпонентов комплемента С1). Предпочтительно эти разблокированные C1q-связывающие центры преобразуют прежнее низкоаффинное взаимодействие C1q-IgG во взаимодействие с высокой авидностью, которое запускает каскад событий, затрагивающих ряд других белков комплемента, и ведет к протеолитическому высвобождению вызывающих хемотаксис/активацию эффекторных клеток веществ С3а и С5а. Предпочтительно каскад комплемента оканчивается образованием атакующего мембрану комплекса, который создает поры в клеточной мембране, способствующие свободному прохождению воды и растворимых веществ в клетку и из клетки.
Получение антител
Антитела по изобретению могут быть получены различными методами, включая стандартную методологию моноклональных антител, напр., стандартным методом соматической гибридизации клеток Kohler and Milstein, Nature 256: 495 (1975). Хотя методы соматической гибридизации клеток и предпочтительны, однако в принципе можно воспользоваться и другими методами получения моноклональных антител, напр., вирусной или онкогенной трансформации В-лимфоцитов или методами фагового дисплея с использованием библиотек генов антител.
Предпочтительной системой на животных для получения гибридом, секретирующих моноклональные антитела, является система на мышах. Получение гибридом у мышей является очень хорошо разработанным методом. Методики иммунизации и методы выделения иммунизированных спленоцитов для слияния хорошо известны в этой области. Также известны партнеры для слияния (напр., клетки миеломы мышей) и методики слияния.
Другими предпочтительными системами на животных для получения гибридом, секретирующих моноклональные антитела, являются системы на крысах и на кроликах (напр., описанные в Spieker-Polet et al., Proc. Natl. Acad. Sci. USA 92: 9348 (1995); также см. Rossi et al., Am. J. Clin. Pathol. 124: 295 (2005)).
В следующем предпочтительном воплощении моноклональные антитела человека против CLD18 могут быть получены с помощью трансгенных или трансхромосомных мышей, несущих части иммунной системы человека, а не мыши. К этим трансгенным и трансхромосомным мышам относятся мыши, известные как мыши HuMAb и мыши KM, соответственно, которые собирательно именуются здесь "трансгенными мышами". Получение антител человека у таких трансгенных мышей может осуществляться, как описано подробно для CD20 в WO 2004 035607.
Еще одна стратегия получения моноклональных антител заключается в прямом выделении кодирующих антитела генов из лимфоцитов, вырабатывающих антитела определенного плана, напр., см. Babcock et al. (1996) A novel strategy for generating monoclonal antibodies from single, isolated lymphocytes producing antibodies of defined strategy. Подробнее о рекомбинантной инженерии антител также см. Welschof and Kraus, Recombinant antibodies for cancer therapy ISBN-0-89603-918-8; и Benny K.C. Lo, Antibody Engineering ISBN 1-58829-092-1.
Иммунизация
Для получения антител к CLD18 можно иммунизировать мышей с помощью конъюгированных с носителями пептидов, полученных из последовательности CLD18, обогащенного препарата экспрессируемого рекомбинантным способом антигена CLD18 или его фрагментов и/или клеток, экспрессирующих CLD18, как описано. В качестве альтернативы мышей можно иммунизировать с помощью ДНК, кодирующей полный CLD18 человека (напр., SEQ ID NO: 1), или ее фрагментами, в частности согласно SEQ ID NO: 15, 17 и 19. В том случае, если иммунизация с помощью очищенного или обогащенного препарата антигена CLD18 не даст антител, мышей можно иммунизировать с помощью клеток, экспрессирующих CLD18, напр., клеточной линии, чтобы вызвать иммунные ответы.
Иммунный ответ можно отслеживать по мере выполнения иммунизации с помощью образцов плазмы и сыворотки, взятых из хвостовой вены, или ретроорбитальных проб крови. Мышей с достаточным титром иммуноглобулинов против CLD18 можно использовать для слияния. Мышам можно сделать повторную иммунизацию (бустер) с помощью клеток, экспрессирующих CLD18, за 3 дня до забоя и извлечения селезенки, чтобы повысить скорость секреции специфических антител гибридомой.
Получение гибридом, вырабатывающих моноклональные антитела
Для получения гибридом, вырабатывающих моноклональные антитела к CLD18, можно выделить спленоциты и клетки лимфатических узлов из иммунизированных мышей и слить с подходящей "бессмертной" линией клеток типа линии клеток миеломы мыши. Затем полученные гибридомы можно подвергнуть скринингу на выработку специфичных к антигену антител. Затем индивидуальные лунки можно подвергнуть скринингу методом ELISA на наличие секретирующих антитела гибридом. Методом иммунофлуоресценции и анализа FACS с использованием экспрессирующих CLD18 клеток можно идентифицировать антитела, обладающие специфичностью к CLD18. Секретирующие антитела гибридомы можно засеять на чашки, снова подвергнуть скринингу и, если они окажутся положительными на моноклональные антитела к CLD18, субклонировать методом предельного разбавления. Устойчивые субклоны можно затем культивировать in vitro для получения антител в культуральной среде для изучения.
Получение трансфектом, вырабатывающих моноклональные антитела
Антитела по изобретению также можно получить в трансфектоме клеток-хозяев, например, используя сочетание методов рекомбинантной ДНК и трансфекции генов, как это хорошо известно в данной области (Morrison S. (1985) Science 229: 1202).
Например, в одном воплощении гены, представляющие интерес, напр., гены антител, можно лигировать в такой экспрессионный вектор, как плазмида для экспрессии в эукариотах типа той, что используется в системе экспрессии генов GS, раскрытой в WO 87/04462, WO 89/01036 и ЕР 338841, или других системах экспрессии, хорошо известных в этой области. Очищенную плазмиду с клонированными генами антител можно ввести в эукариотические клетки-хозяева, как-то клетки СНО, клетки NS/0, клетки HEK293T или клетки HEK293 либо в другие эукариотические клетки типа растительных клеток, грибков или дрожжевых клеток. Для введения этих генов можно использовать описанные методы, как-то методы электропорации, с помощью липофектина, липофектамина и др. После введения этих генов антител в клетки-хозяева можно идентифицировать и подвергнуть отбору клетки, экспрессирующие антитела. Эти клетки представляют собой трансфектомы, которые можно затем амплифицировать по уровню экспрессии и размножить для продукции антител. Из супернатантов культур и/или клеток можно выделить и очистить рекомбинантные антитела.
В качестве альтернативы клонированные гены антител можно экспрессировать в других системах экспрессии, включающих прокариотические клетки, как-то микроорганизмы, напр., Е. coli. Кроме того, антитела можно получать в трансгенных животных (кроме человека), как-то в молоке овец или кроликов либо в куриных яйцах, или в трансгенных растениях, напр., см. Verma R. et al. (1998) J. Immunol. Meth. 216: 165-181; Pollock et al. (1999) J. Immunol. Meth. 231: 147-157; и Fischer R. et al. (1999) Biol. Chem. 380: 825-839.
Использование частичных последовательностей антител для экспрессирования интактных антител (т.е. гуманизация и химеризация)
а) Химеризация
Моноклональные антитела мыши можно использовать в качестве терапевтических антител на людях, если пометить их токсинами или радиоактивными изотопами. Немеченые антитела мыши сильно иммуногенны для человека при неоднократном применении, что ведет к уменьшению терапевтического эффекта. В основном иммуногенность опосредуется константными областями тяжелой цепи. Иммуногенность антител мыши у человека можно уменьшить или полностью устранить, если соответствующие антитела подвергнуть химеризации или гуманизации. Химерные антитела - это такие антитела, различные части которых происходят из разных видовживотных, как-то такие, у которых вариабельная область происходит из антител мыши, а константная область из иммуноглобулина человека. Химеризация антител осуществляется путем соединения вариабельных участков тяжелой и легкой цепи антитела мыши с константными участками тяжелой и легкой цепи человека (напр., как описано в Kraus et al., in Methods in Molecular Biology series, Recombinant antibodies for cancer therapy ISBN-0-89603-918-8). В одном предпочтительном воплощении химерные антитела получают путем соединения константной области каппа легкой цепи человека с вариабельной областью легкой цепи мыши. В другом предпочтительном воплощении химерные антитела получают путем соединения константной области лямбда легкой цепи человека с вариабельной областью легкой цепи мыши. Предпочтительные константные области тяжелой цепи для получения химерных антител принадлежат к IgG1, IgG3 или IgG4. Другие предпочтительные константные области тяжелой цепи для получения химерных антител принадлежат к IgG2, IgA, IgD и IgM.
b) Гуманизация
Антитела взаимодействуют с антигенами мишени преимущественно через аминокислотные остатки, находящиеся на шести участках гипервариабельности (CDR) тяжелой и легкой цепи. По этой причине аминокислотные последовательности в пределах CDRs отличаются большим разнообразием между индивидуальными антителами, чем последовательности вне участков CDR. Поскольку последовательности CDR ответственны за большинство взаимодействий антитело-антиген, то можно экспрессировать рекомбинантные антитела, воспроизводящие свойства определенных природных антител, путем конструирования экспрессионных векторов, включающих последовательности CDR из конкретного природного антитела, пришитые к каркасным последовательностям из другого антитела с другими свойствами (напр., см. Riechmann L. et al. (1998) Nature 332: 323-327; Jones P. et al. (1986) Nature 321: 522-525; и Queen C. et al. (1989) Proc. Natl. Acad. Sci. USA 86: 10029-10033). Такие каркасные последовательности могут быть получены из публичных баз данных по ДНК, содержащих зародышевые последовательности генов антител. Зародышевые последовательности отличаются от зрелых последовательностей генов антител тем, что они не содержат полностью собранных генов вариабельных областей, которые образуются путем соединения участков V-(D)-J при созревании В-клеток. Зародышевые последовательности генов также отличаются от последовательностей высокоаффинных антител из вторичного репертуара индивидуума равномерно по всей вариабельной области. Например, соматические мутации сравнительно редко встречаются в N-концевой части каркасного участка 1 и в С-концевой части каркасного участка 4. Кроме того, многие соматические мутации существенно не меняют свойства связывания антител. По этой причине вовсе не обязательно иметь полную последовательность ДНК определенного антитела для того, чтобы воссоздать интактное рекомбинантное антитело со свойствами связывания, близкими свойствам исходного антитела (см. WO 99/45962). Как правило, для этого достаточно иметь частичные последовательности тяжелых и легких цепей, охватывающие участки CDR. Частичные последовательности используются для того, чтобы определить, какие гаметные сегменты генов вариабельных и соединительных участков внесли вклад в гены прошедших рекомбинацию вариабельных участков. Затем зародышевые последовательности используются для заполнения недостающих частей вариабельных участков. Лидерные последовательности тяжелых и легких цепей отщепляются при созревании белка и не вносят вклад в свойства окончательного антитела. Для добавления недостающих последовательностей клонированные последовательности ДНК можно соединить с синтетическими олигонуклеотидами путем лигирования или ПЦР-амплификации. С другой стороны, можно синтезировать всю вариабельную область в виде набора коротких, перекрывающихся олигонуклеотидов и соединить их методом ПЦР-амплификации, получая полностью синтетический клон вариабельной области. Такой способ имеет определенные преимущества, такие, как устранение или включение определенных сайтов рестрикции или оптимизация определенных кодонов.
Для разработки перекрывающегося набора синтетических олигонуклеотидов используются нуклеотидные последовательности транскриптов тяжелых и легких цепей, чтобы получить синтетические V-последовательности с такими же возможностями кодирования аминокислот, как у природных последовательностей. Последовательности синтетических тяжелых и каппа-цепей могут отличаться от природных последовательностей трояким образом: перемежаются цепочки повторяющихся оснований нуклеотидов для облегчения синтеза олигонуклеотидов и ПЦР-амплификации; вставлены оптимальные сайты инициации трансляции согласно правилам Козака (Kozak, 1991, J. Biol. Chem. 266: 19867-19870); и встроены сайты HindIII впереди от сайтов инициации трансляции.
В отношении вариабельных областей тяжелых и легких цепей оптимизированные последовательности соответствующей кодирующей и некодирующей нити разбивают на участки по 30-50 нуклеотидов примерно посередине соответствующего некодирующего олигонуклеотида. Таким образом для каждой цепи из олигонуклеотидов можно собрать перекрывающиеся наборы двойных спиралей, охватывающие сегменты из 150-400 нуклеотидов. Все они затем используются в качестве матриц для получения продуктов ПЦР-амплификации из 150-400 нуклеотидов. Как правило, один набор олигонуклеотидов вариабельной области разбивают на два комплекта, которые по отдельности подвергают амплификации, получая два перекрывающиеся продукта ПЦР. Затем эти перекрывающиеся продукты соединяют методом ПЦР-амплификации, получая целую вариабельную область. При ПЦР-амплификации может понадобиться включить перекрывающийся фрагмент константной области тяжелой или легкой цепи, чтобы получить фрагменты, которые можно легко клонировать в конструкции для экспрессирующего вектора.
Реконструированные химеризованные или гуманизованные вариабельные области тяжелых и легких цепей затем соединяют с клонированными последовательностями промотора, лидера, инициации трансляции, константной области, 3'-нетранслируемого участка, полиаденилирования и терминации транскрипции, получая конструкции для экспрессирующего вектора. Экспрессирующие тяжелые и легкие цепи конструкции можно объединить в одном векторе, ввести методом котрансфекции, последовательной трансфекции или раздельной трансфекции в клетки-хозяева, которые затем подвергнуть слиянию для получения клеток-хозяев, экспрессирующих обе цепи. Плазмиды для конструирования экспрессионных векторов для IgGκ человека описаны ниже. Плазмиды конструировали таким образом, чтобы можно было использовать ПЦР-амплифицированные последовательности кДНК V-областей тяжелой цепи и легкой цепи каппа для воссоздания целых минигенов тяжелой и легкой цепи. Эти плазмиды можно использовать для экспрессирования полностью человеческих либо химерных антител типа IgG1κ или IgG4κ. Можно сконструировать аналогичные плазмиды для экспрессии других изотипов тяжелой цепи либо для экспрессии антител, содержащих легкие цепи лямбда.
Итак, в следующем аспекте изобретения структурные особенности антител против CLD18 по изобретению используются для создания близких по структуре гуманизированных антител против CLD18, сохраняющих по меньшей мере одно функциональное свойство антител по изобретению, как-то связывание с CLD18. В частности, можно соединить рекомбинантным способом один или несколько участков CDR моноклональных антител мыши с известными каркасными участками и участками CDR человека, получая другие, созданные рекомбинантным способом, гуманизированные антитела по изобретению против CLD18.
Связывание с клетками, экспрессирующими антиген
Способность антител к связыванию с CLD18 можно определить стандартными методами анализа связывания типа тех, что изложены в примерах (напр., методами ELISA, вестерн-гибридизации, иммунофлуоресценции и проточной цитометрии).
Изучение связывания антител
Для очистки антител против CLD18 можно культивировать отобранные гибридомы во вращающихся колбах на 2 л для продукции моноклональных антител. С другой стороны, можно получить антитела против CLD18 в диализных биореакторах. Супернатанты можно профильтровать и, при необходимости, сконцентрировать перед аффинной хроматографией на сефарозе с белком G или сефарозе с белком А. Элюированный IgG можно проверить на чистоту методом гель-электрофореза или высокоэффективной жидкостной хроматографии. Буферный раствор можно заменить на PBS, а концентрацию определить по OD280, используя коэффициент экстинкции 1,43. Моноклональные антитела можно разделить на порции и хранить при -80°С.
Чтобы убедиться, что отобранные моноклональные антитела против CLD18 связываются с уникальными эпитопами, можно использовать направленный мутагенез по одному сайту или множественным сайтам.
Определение изотипа
Для определения изотипа очищенных антител можно провести анализ на изотип методом ELISA с помощью различных коммерческих наборов (напр., Zymed, Roche Diagnostics). Лунки микропланшета покрывают антителами против Ig мыши. После блокирования планшет обрабатывают моноклональными антителами или очищенными препаратами контрольных изотипов, при комнатной температуре в течение 2 часов. Затем лунки обрабатывают IgG1, IgG2a, IgG2b или IgG3 мыши либо специфичными к IgA или IgM мыши зондами, конъюгированными с пероксидазой. После отмывки планшет проявляют с помощью субстрата ABTS (1 мг/мл) и анализируют по OD при 405-650 нм. В качестве альтернативы можно использовать набор для определения изотипа моноклональных антител мыши IsoStrip Mouse Monoclonal Antibody Isotyping Kit (Roche, кат. №1493027), как описано производителем.
Анализ методом проточной цитометрии
Для того, чтобы установить наличие антител против CLD18 в сыворотке иммунизированных мышей или связывание моноклональных антител с живыми клетками, экспрессирующими CLD18, можно использовать проточную цитометрию. Клетки линии, экспрессирующей CLD18 естественным образом или после трансфекции, и отрицательные контроли, не экспрессирующие CLD18 (выращенные при стандартных условиях культивирования), смешивают с моноклональными антителами при различных концентрациях в супернатантах гибридом или в PBS, содержащем 1% FBS, и инкубируют при 4°С в течение 30 мин. После отмывки меченные АРС или Alexa647 антитела против IgG могут связываться со связавшимися с CLD18 моноклональными антителами в тех же условиях, что и при окрашивании первичных антител. Образцы анализируют методом проточной цитометрии на приборе FACS при параметрах освещения и бокового светорассеяния, выделяющих одиночные живые клетки. Для того, чтобы отличить специфичные к CLD18 моноклональные антитела от специфических связывающих молекул при однократном измерении, можно использовать метод котрансфекции. Клетки, временно трансфицированные плазмидами, кодирующими CLD18 и флуоресцентный маркер, окрашивают, как описано выше. Трансфицированные клетки можно детектировать на другом канале флуоресценции, чем окрашенные антителами клетки. Поскольку большинство трансфицированных клеток экспрессирует оба трансгена, то специфичные к CLD18 моноклональные антитела преимущественно связываются с клетками, экспрессирующими флуоресцентный маркер, тогда как неспецифические антитела в сравнимой степени связываются с нетрансфицированными клетками. Наряду с или вместо метода проточной цитометрии можно использовать альтернативный метод флуоресцентной микроскопии. Клетки можно окрашивать точно так же, как описано выше, и исследовать методом флуоресцентной микроскопии.
Белки плотных контактов подвергаются интернализации, если клетки перестают контактировать с соседними клетками, в частности адгерентными клетками, напр., при отделении клеток. Экспрессию CLD18 на клеточной поверхности можно оптимизировать путем: а) подбора условий культивирования, напр., культивировать при более высокой плотности клеток стандартизированным образом, используя мягкие способы отделения (напр., 2 мМ EDTA/PBS или аккутазу) при комнатной температуре и добавляя ингибиторы эндоцитоза (напр., азид натрия) или активаторы транскрипции или трансляции CLD18; и b) отбора и клонирования клеток, поддерживающих высокий уровень CLD18 на клеточной поверхности, напр., отбора с помощью антибиотиков в отношении трансфицированных клеток, иммуномагнитной сортировки клеток или методом FACS и клонирования методом предельного разведения.
Иммунофлуоресцентная микроскопия
Для того, чтобы установить наличие антител против CLD18 в сыворотке иммунизированных мышей или связывание моноклональных антител с живыми клетками, экспрессирующими CLD18, можно использовать метод иммунофлуоресцентной микроскопии. Например, клетки линии, экспрессирующей CLD18 спонтанно или после трансфекции, и отрицательные контроли, не экспрессирующие CLD18, культивируют на камерных предметных стеклах при стандартных условиях культивирования в среде DMEM/F12 с добавлением 10% телячьей сыворотки (FCS), 2 мМ L-глутамина, 100 МЕ/мл пенициллина и 100 мкг/мл стрептомицина. Затем клетки фиксируют метанолом или параформальдегидом или оставляют без обработки. Затем клетки можно обработать моноклональными антителами против CLD18 в течение 30 мин при 25°С. После отмывки клетки обрабатывают меченным Alexa555 вторичным антителом против IgG мыши (Molecular Probes) при тех же условиях. После этого клетки можно исследовать методом флуоресцентной микроскопии.
Общий уровень CLD18 можно наблюдать в клетках, фиксированных метанолом или параформальдегидом и пермеабилизованных с помощью Triton Х-100. В живых клетках и непермеабилизованных, фиксированных параформальдегидом клетках можно исследовать поверхностную локализацию CLD18. Кроме того, приуроченность CLD18 к плотным контактам можно анализировать при совместном окрашивании маркерами плотных контактов типа ZO-1. Кроме того, можно исследовать эффекты связывания антител и локализацию CLD18 на клеточной мембране.
Вестерн-гибридизация
IgG против CLD18 можно дополнительно тестировать на реактивность с антигеном CLD18 методом вестерн-гибридизации. Вкратце, получают экстракты из клеток, экспрессирующих CLD18, и соответствующих отрицательных контролей, и подвергают электрофорезу в полиакриламидном геле с додецилсульфатом натрия (SDS). После электрофореза разделенные антигены переносят на нитроцеллюлозные мембраны, блокируют и обрабатывают исследуемыми моноклональными антителами. Связывание IgG можно детектировать с помощью конъюгата антител к IgG мыши с пероксидазой и проявить с помощью субстрата ECL.
Иммуногистохимия
IgGs мыши против CLD18 можно дополнительно тестировать на реактивность с антигеном CLD18 методом иммуногистохимии хорошо известным специалистам способом, напр., используя фиксированные параформальдегидом или ацетоном срезы замороженных тканей либо срезы залитых парафином тканей, фиксированных параформальдегидом, из нераковых тканей или образцов раковых тканей, взятых у пациентов во время плановых хирургических операций или у мышей, несущих ксенотрансплантаты опухолей, инокулированных клетками линий, экспрессирующих CLD18 спонтанно (напр., DAN-G, SNU-16 или KATO-III) или после трансфекции (напр., HEK293). Для иммуноокрашивания проводится инкубация антител, реагирующих с CLD18, с последующей обработкой конъюгированными с пероксидазой хрена козьими антителами против Ig мыши или кролика (DAKO) согласно инструкциям поставщика.
Активность антител in vitro - фагоцитоз и гибель клеток
Помимо специфического связывания с CLD18, антитела против CLD18 можно тестировать на способность их опосредовать фагоцитоз и гибель клеток, экспрессирующих CLD18. Тестирование активности моноклональных антител in vitro обеспечивает начальный скрининг перед тестированием на моделях in vivo.
Антителозависимая клеточная цитотоксичность
Вкратце, полиморфноядерные клетки (PMNs), NK-клетки, моноциты, мононуклеары или другие эффекторные клетки от здоровых доноров можно очистить методом центрифугирования в градиенте фиколла Hypaque, а затем лизировать загрязняющие эритроциты. Промытые эффекторные клетки можно суспендировать в среде RPMI с добавлением 10% инактивированной нагреванием телячьей сыворотки либо 5% инактивированной нагреванием сыворотки человека и смешать с меченными 51Cr клетками мишени, экспрессирующими CLD18, при различных пропорциях эффекторных клеток и клеток мишени. В качестве альтернативы клетки мишени можно пометить усиливающим флуоресценцию лигандом (BATDA). Сильно флуоресцирующий хелат европия с усиливающим лигандом, который выделяется из мертвых клеток, измеряют на флуориметре. После этого добавленный краситель Lucifer желтый может окисляться только жизнеспособными клетками. Затем добавляют очищенные IgGs против CLD18 в различных концентрациях. В качестве отрицательного контроля можно использовать посторонние IgG человека. Определение проводится от 4 до 20 часов при 37°С в зависимости от типа используемых эффекторных клеток. Образцы анализируют на цитолиз по измерению выделения 51Cr или по наличию хелата EuTDA в супернатанте культуры. В качестве альтернативы можно измерять люминесценцию, возникающую при окислении красителя Lucifer желтый, в качестве меры жизнеспособных клеток.
Моноклональные антитела против CLD18 также можно тестировать в различных комбинациях, чтобы установить, будет ли усиливаться цитолиз в присутствии нескольких моноклональных антител.
Обусловленная комплементом цитотоксичность (CDC)
Моноклональные антитела против CLD18 можно тестировать на способность вызывать CDC, используя целый ряд известных методов. Например, сыворотку для комплемента получают из крови способом, известным специалистам. Для определения активности CDC у mAbs можно использовать различные способы. Например, можно измерять высвобождение 51Cr или измерять повышение мембранной проницаемости по исключению пропидия иодида (PI). Вкратце, клетки мишени промывают и инкубируют 5×105/мл при различных концентрациях mAb в течение 10-30 мин при комнатной температуре или при 37°С. Затем добавляют сыворотку или плазму до конечной концентрации 20% об. и инкубируют клетки при 37°С в течение 20-30 мин. Все клетки из каждого образца вносят в раствор PI в пробирке для FACS. Смесь анализируют сразу же методом проточной цитометрии на приборе FACSArray.
В альтернативном методе определяют индукцию CDC на адгерентных клетках. В одном воплощении этого метода клетки высеивают в плоскодонные лунки планшета для тканевой культуры за 24 ч до определения при плотности 3×104/лунку. На следующий день среду удаляют, а клетки инкубируют с антителами в тройных пробах. Контрольные клетки инкубируют с чистой средой или со средой, содержащей 0,2% сапонина, для определения фонового лизиса и максимального лизиса, соответственно. После инкубации в течение 20 мин при комнатной температуре удаляют супернатант, а к клеткам добавляют 20% об. плазмы или сыворотки человека в DMEM (подогретой до 37°С) и инкубируют еще 20 мин при 37°С. Все клетки из каждого образца вносят в раствор пропидия иодида (10 мкг/мл). Затем супернатанты заменяют на PBS, содержащий 2,5 мкг/мл этидия бромида, и измеряют испускаемую при 600 нм флуоресценцию при возбуждении при 520 нм на приборе Тесал Safire. Специфический лизис в процентах рассчитывают следующим образом: специфический лизис в % = (флуоресценция образца - флуоресценция фона)/(флуоресценция при максимальном лизисе - флуоресценция фона)×100.
Ингибирование пролиферации клеток моноклональными антителами
Для тестирования на способность вызывать апоптоз моноклональные антитела против CLD18 можно инкубировать, к примеру, с CLD18-положительными раковыми клетками, напр., SNU-16, DAN-G, KATO-III, либо с раковыми клетками, трансфицированными CLD18, при 37°С примерно в течение 20 часов. Клетки собирают, промывают буфером для связывания Annexin-V (BD Biosciences) и инкубируют с Annexin-V, конъюгированным с FITC или АРС (BD Biosciences) в течение 15 мин в темноте. Все клетки из каждого образца вносят в раствор PI (10 мкг/мл в PBS) в пробирке для FACS и сразу же анализируют методом проточной цитометрии (см. выше). В качестве альтернативы можно определять общее ингибирование пролиферации клеток моноклональными антителами с помощью коммерческого набора. Набор DELFIA Cell Proliferation Kit (Perkin-Elmer, кат. № AD0200) представляет собой неизотопный набор для иммуноанализа по измерению включения 5-бром-2'-дезоксиуридина (BrdU) при синтезе ДНК в пролиферирующих клетках на микропланшетах. Включение BrdU детектируют с помощью меченных европием моноклональных антител. Для детектирования антител клетки фиксируют и денатурируют ДНК с помощью раствора Fix. Несвязавшиеся антитела отмывают и добавляют индуктор DELFIA, вызывающий диссоциацию ионов европия из меченных антител в раствор, где они образуют сильно флуоресцирующие хелаты с компонентами индуктора DELFIA. Флуоресценция, измеряемая методом флуориметрии с разрешением во времени при детектировании, пропорциональна синтезу ДНК в клетках из каждой лунки.
Доклинические исследования
Моноклональные антитела, связывающиеся с CLD18, также можно тестировать на модели in vivo (напр., на иммунодефицитных мышах, несущих ксенотрансплантаты опухолей, инокулированных с помощью клеток экспрессирующих CLD18 линий, напр., DAN-G, SNU-16 или KATO-III, либо после трансфекции, напр., HEK293), чтобы установить эффективность контролирования ими роста экспрессирующих CLD18 раковых клеток.
Исследования in vivo на иммунодефицитных мышах или других животных после ксенотрансплантации экспрессирующих CLD18 раковых клеток можно проводить с использованием антител по изобретению. Антитела можно вводить свободным от опухолей мышам с последующей инъекцией раковых клеток, чтобы измерить эффекты антител по предотвращению образования опухолей или опухолевых симптомов. Антитела можно вводить и несущим опухоли мышам, чтобы определить терапевтическую эффективность соответствующих антител по уменьшению роста опухолей, метастазов или опухолевых симптомов. Применение антител можно комбинировать с применением других веществ, как-то цитостатических препаратов, ингибиторов факторов роста, блокаторов клеточного цикла, ингибиторов ангиогенеза или других антител, чтобы определить синергическую эффективность и возможную токсичность комбинаций. Для анализа токсических побочных эффектов, вызванных антителами изобретения, можно инокулировать животных антителами или контрольными реагентами и тщательно исследовать на наличие симптомов, вероятно связанных с терапией антителами к CLD18. Возможные побочные эффекты применения in vivo антител к CLD18 в частности включают токсичность на экспрессирующих CLD18 тканях, включая желудок и легкие. Для предсказания возможных побочных эффектов, вызванных применением моноклональных антител к CLD18 на людях, особенно полезны антитела, распознающие CLD18 у человека и у других видов, напр., мышей.
Картирование эпитопов
Картирование эпитопов, распознаваемых антителами изобретения, может проводиться так, как описано подробно в "Epitope Mapping Protocols (Methods in Molecular Biology) by Glenn E. Morris ISBN-089603-375-9; и в "Epitope Mapping: A Practical Approach", Practical Approach Series, 248 by Olwyn M.R. Westwood, Frank C. Hay.
I. Биспецифичные/мультиспецифичные молекулы, связывающиеся с CLD18
В следующем воплощении изобретения антитела к CLD18 могут быть подвергнуты функционализации или присоединены к другой функциональной молекуле, напр., к другому пептиду или белку (напр., Fab'-фрагменту) для создания биспецифичной или мультиспецифичной молекулы, связывающейся со множественными центрами связывания или эпитопами мишени. Например, антитела по изобретению могут быть функционально соединены (напр., при помощи химической конъюгации, генетического слияния, нековалентной ассоциации или иным способом) с одной или несколькими другими связывающими молекулами, как-то другим антителом, пептидом или связывающим аналогом.
Соответственно, настоящее изобретение включает биспецифичные и мультиспецифичные молекулы, содержащие по меньшей мере одну первую специфичность связывания для CLD18 и вторую специфичность связывания для второго эпитопа-мишени. В предпочтительном воплощении изобретения вторым эпитопом-мишенью является Fc-рецептор, напр., FcγRI (CD64) человека или Fcα-рецептор (CD89) человека, либо Т-клеточный рецептор, напр., CD3. Таким образом, изобретение включает биспецифичные и мультиспецифичные молекулы, способные связываться и с эффекторными клетками, экспрессирующими FcγR, FcαR или FcεR (напр., моноцитами, макрофагами или полиморфноядерными клетками (PMN)), и с клетками, экспрессирующими CLD18. Эти биспецифичные и мультиспецифичные молекулы могут доставлять экспрессирующие CLD18 клетки к эффекторным клеткам и запускать такие опосредованные Fc-рецепторами активности эффекторных клеток, как фагоцитоз экспрессирующих CLD18 клеток, антителозависимая клеточная цитотоксичность (ADCC), выделение цитокинов или вырабатывание аниона супероксида.
Биспецифичные и мультиспецифичные молекулы изобретения могут дополнительно включать и третью специфичность связывания, в дополнение к специфичности связывания для Fc и специфичности связывания для CLD18. В одном воплощении третья специфичность связывания составляет участок против фактора усиления (EF), напр., молекулы, связывающейся с поверхностным белком, участвующим в цитотоксической активности, и тем самым усиливающей иммунный ответ против клеток мишени. "Участок против фактора усиления" может представлять собой антитело, функциональный фрагмент антитела или лиганд, связывающийся с данной молекулой, напр., антигеном или рецептором, и тем самым вызывающий усиление эффекта связывающих детерминант на Fc-рецептор или антиген клеток мишени. "Участок против фактора усиления" может связываться с Fc-рецептором или антигеном клеток мишени. С другой стороны, участок против фактора усиления может связываться с объектом, который отличается от того объекта, с которым связываются первая и вторая специфичности связывания. Например, участок против фактора усиления может связываться с цитотоксическими Т-клетками (напр., через CD2, CD3, CD8, CD28, CD4, CD40, ICAM-1) или иными иммунными клетками, что приведет к усилению иммунного ответа против клеток мишени.
В одном воплощении биспецифичные и мультиспецифичные молекулы изобретения включают в качестве связывающей специфичности по меньшей мере одно антитело, в том числе, напр., Fab, Fab', F(ab')2, Fv или одноцепочечный Fv-фрагмент. Антитело также может представлять собой димер легкой цепи или тяжелой цепи либо какой-нибудь минимальный фрагмент, как-то Fv или одноцепочечную конструкцию, как описано в Ladner et al., US 4,946,778. Антитело также может представлять собой слитый со связывающим доменом иммуноглобулина белок, как изложено в US 2003/0118592 и US 2003/0133939.
В одном воплощении биспецифичные и мультиспецифичные молекулы изобретения включают связывающую специфичность для FcγR или FcαR, находящихся на поверхности эффекторных клеток, и вторую связывающую специфичность для антигена клеток мишени, напр., CLD18.
В одном воплощении специфичность связывания с Fc-рецептором обеспечивается моноклональным антителом, связывание которого не блокируется иммуноглобулином G (IgG) человека. В настоящем изобретении термин "рецептор IgG" относится к любому из 8 генов γ-цепи, локализованных на хромосоме 1. Эти гены в целом кодируют 12 трансмембранных или растворимых изоформ рецептора, которые входят в 3 класса Fcγ-рецепторов: FcγRI (CD64), FcγRII (CD32) и FcγRIII (CD16). В одном предпочтительном воплощении Fcγ-рецептор представляет собой высокоаффинный FcγRI человека.
Получение и характеристика этих предпочтительных моноклональных антител описаны Fanger et al. в WO 88/00052 и в US 4,954,617. Эти антитела связываются с эпитопом FcγRI, FcγRII или FcγRIII по сайту, который отличается от Fcγ-связывающего сайта рецептора, поэтому их связывание практически не блокируется при физиологическом уровне IgG. Специфичные к FcγRI антитела, применимые в настоящем изобретении - mAb 22, mAb 32, mAb 44, mAb 62 и mAb 197. В других воплощениях антитело к Fcγ-рецептору представляет собой гуманизованную форму моноклонального антитела 22 (Н22). Получение и характеристика антитела Н22 описаны в Graziano R.F. et al. (1995) J. Immunol. 155(10): 4996-5002; и WO 94/10332. Продуцирующая антитело H22 линия клеток депонирована в Американской коллекции типовых культур 4 ноября 1992 г. под названием HA022CL1 и имеет номер доступа CRL 11177.
В следующих предпочтительных воплощениях специфичность связывания с Fc-рецептором обеспечивается антителом, связывающимся с рецептором IgA человека, напр., Fcα-рецептором (FcαRI (CD89)), связывание которого предпочтительно не блокируется иммуноглобулином A (IgA) человека. Термин "рецептор IgA" служит для обозначения генного продукта одного α-гена (FcαRI), локализованного на хромосоме 19. Известно, что этот ген кодирует несколько подвергающихся альтернативному сплайсингу трансмембранных изоформ от 55 до 110 кДа. FcαRI (CD89) экспрессируется конститутивно на моноцитах/макрофагах, эозинофильных и нейтрофильных гранулоцитах, но не на клетках, не относящихся к популяциям эффекторных клеток. FcαRI обладает умеренным сродством к IgA1 и IgA2, которое повышается под воздействием таких цитокинов, как G-CSF или GM-CSF (Morton Н.С. et al. (1996) Critical Reviews in Immunology 16: 423-440). Были описаны 4 специфичные к FcαRI моноклональные антитела, обозначенные как A3, А59, А62 и А77, которые связываются с FcαRI за пределами домена связывания лигандов IgA (Monteiro R.C. et al. (1992) J. Immunol. 148: 1764).
FcαRI и FcγRI являются предпочтительными пусковыми рецепторами для применения в изобретении, так как они: (1) экспрессируются главным образом на иммунных эффекторных клетках, напр., моноцитах, PMN, макрофагах и дендритных клетках; (2) экспрессируются на высоком уровне (напр., 5000-100000 на клетку); (3) являются медиаторами цитотоксической активности (напр., ADCC, фагоцитоза); (4) опосредуют усиление презентации направляемых к ним антигенов, включая аутоантигены.
В другом воплощении биспецифичная молекула состоит из двух моноклональных антител по изобретению, обладающих комплементарными функциональными активностями, как-то одно антитело преимущественно работает, индуцируя CDC, а другое преимущественно работает, индуцируя апоптоз.
"Специфичное к эффекторным клеткам антитело" в настоящем изобретении означает такое антитело или функциональный фрагмент антитела, которое связывается с Fc-рецептором эффекторных клеток. Предпочтительные антитела для применения в настоящем изобретении связываются с Fc-рецептором эффекторных клеток по сайту, с которым не связывается эндогенный иммуноглобулин.
В настоящем изобретении термин "эффекторные клетки" относится к таким иммунным клеткам, которые участвуют в эффекторной фазе иммунного ответа, в противоположность распознавательной и активационной фазам иммунного ответа. Примеры иммунных клеток включают клетки миелоидного или лимфоидного происхождения, напр., лимфоциты (напр., В-клетки и Т-клетки, в том числе цитолитические Т-клетки (CTLs)), клетки-киллеры, нормальные клетки-киллеры, макрофаги, моноциты, эозинофилы, нейтрофилы, полиморфноядерные клетки, гранулоциты, тучные клетки и базофилы. Некоторые эффекторные клетки экспрессируют определенные Fc-рецепторы и выполняют специфические иммунные функции. В предпочтительных воплощениях эффекторные клетки способны индуцировать антителозависимую клеточную цитотоксичность (ADCC), напр., нейтрофилы способны индуцировать ADCC. Например, моноциты, макрофаги, экспрессирующие FcR, участвуют в специфическом уничтожении клеток мишени и презентации антигенов другим компонентам иммунной системы либо в связывании клеток, презентирующих антигены. В других воплощениях эффекторные клетки могут подвергать фагоцитозу антиген мишени, клетки мишени или микроорганизмы. Экспрессия определенного FcR на эффекторных клетках может регулироваться такими гуморальными факторами, как цитокины. Например, оказалось, что экспрессия FcγRI усиливается под действием у-интерферона (IFN-γ). Такое усиление экспрессии повышает цитотоксическую активность несущих FcγRI клеток против мишеней. Эффекторные клетки могут подвергать фагоцитозу или лизировать антиген мишени или клетки мишени.
"Клетки-мишени" означают любые нежелательные клетки у субъекта (напр., человека или животного), которые могут служить мишенью для антител изобретения. В предпочтительных воплощениях клетками мишени являются клетки, экспрессирующие или суперэкспрессирующие CLD18. Клетки, экспрессирующие CLD18, как правило, включают раковые клетки.
Биспецифичные и мультиспецифичные молекулы настоящего изобретения могут быть получены химическими методами (напр., см. D.M. Kranz et al. (1981) Proc. Natl. Acad. Sci. USA 78: 5807), "полидомными" методами (см. US 4,474,893 на Reading) или методами рекомбинантной ДНК.
В частности, биспецифичные и мультиспецифичные молекулы настоящего изобретения могут быть получены путем конъюгирования входящих в их состав специфичностей связывания, напр., специфичностей связывания с FcR и CLD18, используя известные методы. Например, каждая специфичность связывания биспецифичной или мультиспецифичной молекулы может быть создана отдельно, а затем конъюгирована с другими. Если специфичности связывания представлены белками или пептидами, то для ковалентного конъюгирования можно использовать целый ряд конъюгирующих или сшивающий реагентов. Примеры сшивающих реагентов включают белок А, карбодиимид, N-сукцинимидил-S-ацетилтиоацетат (SATA), 5,5'-дитиобис(2-нитробензойную кислоту) (DTNB), о-фенилендималеимид (oPDM), N-сукцинимидил-3-(2-пиридилтио)пропионат (SPDP) и сульфосукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (сульфо-SMCC) (напр., см. Karpovsky et al. (1984) J. Exp. Med. 160: 1686; Liu MA et al. (1985) Proc. Natl. Acad. Sci. USA 82: 8648). Другие методы включают методы, описанные в работах Paulus (Behring Ins. Mitt. (1985) No. 78, 118-132); Brennan et al. (Science (1985) 229: 81-83); и Glennie et al. (J. Immunol. (1987) 139: 2367-2375). Предпочтительными конъюгирующими реагентами являются SATA и сульфо-SMCC, которые доступны от Pierce Chemical Co. (Rockford, IL).
Если специфичности связывания представлены антителами, то их можно конъюгировать через сульфгидрильные связи С-концевых шарнирных участков двух тяжелых цепей. В особенно предпочтительном воплощении шарнирные участки подвергают модификации с тем, чтобы они перед конъюгированием содержали нечетное количество сульфгидрильных остатков, предпочтительно один.
С другой стороны, специфичности связывания могут кодироваться в одном и том же векторе и экспрессироваться и проходить сборку в одних и тех же клетках-хозяевах. Такой метод особенно полезен, если биспецифичная или мультиспецифичная молекула представляет собой слитый белок типа mAb×mAb, mAb×Fab, Fab×F(ab')2 или лиганд×Fba. Биспецифичная или мультиспецифичная молекула по изобретению, напр., биспецифичная молекула, может представлять собой одноцепочечную молекулу, как-то одноцепочечное биспецифичное антитело, при этом одноцепочечная биспецифичная молекула содержит одно одноцепочечное антитело и детерминанту связывания или же одноцепочечная биспецифичная молекула содержит две детерминанты связывания. Биспецифичные и мультиспецифичные молекулы также могут представлять собой одноцепочечные молекулы либо могут содержать по меньшей мере две одноцепочечные молекулы. Методы получения би- и мультиспецифичных молекул описаны, к примеру, в US 5,260,203; US 5,455,030; US 4,881,175; US 5,132,405; US 5,091,513; US 5,476,786; US 5,013,653; US 5,258,498; и US 5,482,858.
Связывание биспецифичных и мультиспецифичных молекул со своими специфическими мишенями можно подтвердить методом ферментного иммуносорбционного анализа (ELISA), радиоиммуноанализа (RIA), методом FACS, биологическим методом (напр., по ингибированию роста) или методом вестерн-гибридизации. Каждый из этих методов выявляет присутствие представляющих интерес комплексов белок-антитело при помощи меченого реагента (напр., антитела), специфичного для данного комплекса. Например, комплексы FcR-антитело можно детектировать, напр., с помощью соединенного с ферментом антитела или фрагмента антитела, распознающего и специфически связывающегося с комплексами антитело-FcR. С другой стороны, можно детектировать комплексы, используя любой из ряда других методов иммуноанализа. Например, антитело может быть помечено радиоактивной меткой и использовано в методе радиоиммуноанализа (RIA) (к примеру, см. Weintraub, В., Principles of Radioimmunoassays, Seventh Training Course on Radioligand Assay Techniques, The Endocrine Society, March, 1986). Радиоактивный изотоп можно детектировать такими способами, как с помощью γ-счетчика или сцинтилляционного счетчика либо методом ауторадиографии.
II. Иммуноконъюгаты
В следующем аспекте настоящего изобретения представлены антитела к CLD18, конъюгированные с лечебной молекулой или средством, как-то цитотоксином, лекарственным препаратом (напр., иммунодепрессантом) или радиоизотопом. Такие конъюгаты в настоящем изобретении именуются "иммуноконъюгатами". Иммуноконъюгаты, включающие один или несколько цитотоксинов, именуются "иммунотоксинами". К цитотоксинам или цитотоксическим средствам относятся любые средства, которые губительны для клеток, в частности, убивают их. Примеры таковых включают таксол, цитохалазин В, грамицидин D, этидия бромид, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрацендион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол и пуромицин, а также их аналоги и гомологи.
К подходящим лечебным средствам для получения иммуноконъюгатов по изобретению относятся и антиметаболиты (напр., метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин, флударабин, 5-фторурацил, декарбазин), алкилирующие вещества (напр., мехлорэтамин, тиоэпа, хлорамбуцил, мелфалан, кармустин (BSNU) и ломустин (CCNU), циклофосфамид, бусульфан, дибромманнит, стрептозотоцин, митомицин С, цис-дихлордиаминоплатина (II) (DDP), цисплатин), антрациклины (напр., даунорубицин (ранее дауномицин) и доксорубицин)), антибиотики (напр., дактиномицин (ранее актиномицин), блеомицин, митрамицин и антрамицин (АМС)) и антимитотические вещества (напр., винкристин и винбластин). В предпочтительном воплощении лечебное средство представляет собой цитотоксическое вещество или радиотоксическое вещество. В другом воплощении лечебное средство представляет собой иммунодепрессант. В следующем воплощении лечебное средство представляет собой GM-CSF. В предпочтительном воплощении лечебное средство представляет собой доксорубицин, цисплатин, блеомицин, кармустин, хлорамбуцил, циклофосфамид или рицин А.
Антитела настоящего изобретения могут быть конъюгированы и с радиоизотопом, напр., иодом-131, иттрием-90 или индием-111, для получения цитотоксических радиофармпрепаратов для лечения связанных с CLD18 заболеваний, как-то рака. Конъюгаты антител по изобретению могут применяться для модифицирования определенной биологической реакции, а лекарственная молекула не обязательно должна ограничиваться средствами химиотерапии. Например, лекарственная молекула может представлять собой белок или полипептид, обладающий требуемой биологической активностью. К таким белкам можно отнести, к примеру, энзиматически активные токсины или их активные фрагменты, такие как абрин, рицин А, экзотоксин Pseudomonas или дифтерийный токсин; такие белки, как фактор некроза опухолей или γ-интерферон; либо модификаторы биологических ответов, такие, к примеру, как лимфокины, интерлейкин-1 (IL-1), интерлейкин-2 (IL-2), интерлейкин-6 (IL-6), колониестимулирующий фактор гранулоцитов/макрофагов (GM-CSF), колониестимулирующий фактор гранулоцитов (G-CSF) и другие факторы роста.
Методы конъюгирования таких лечебных молекул хорошо известны, напр., см. Arnon et al., "Monoclonal Antibodies for Immunotargeting of Drugs in Cancer Therapy", in Monoclonal Antibodies and Cancer Therapy, Reisfeld et al. (eds.), pp. 243-56 (Alan R. Liss, Inc. 1985); Hellstrom et al., "Antibodies for Drug Delivery", in Controlled Drug Delivery (2nd Ed.), Robinson et al. (eds.), pp. 623-53 (Marcel Dekker, Inc. 1987); Thorpe, "Antibody Carriers of Cytotoxic Agents in Cancer Therapy: A Review", in Monoclonal Antibodies '84: Biological and Clinical Applications, Pinchera et al. (eds.), pp. 475-506 (1985); "Analysis, Results, and Future Prospective of the Therapeutic Use of Radiolabeled Antibody in Cancer Therapy", in Monoclonal Antibodies for Cancer Detection and Therapy, Baldwin et al. (eds.), pp. 303-16 (Academic Press 1985); и Thorpe et al., "The Preparation and Cytotoxic Properties of Antibody-Toxin Conjugates", Immunol. Rev., 62: 119-58 (1982).
В следующем воплощении антитела по изобретению присоединяют к линкеру-хелатору, напр., тиуксетану, что позволяет конъюгировать антитело с радиоизотопом.
III. Фармацевтические композиции
В следующем аспекте настоящего изобретения представлены композиции, напр., фармацевтические композиции, содержащие одно или несколько антител настоящего изобретения. Фармацевтические композиции могут быть составлены с фармацевтически приемлемыми носителями или разбавителями, а также с любыми другими известными вспомогательными веществами и наполнителями в соответствии со стандартными методами типа тех, что изложены в Remington: The Science and Practice of Pharmacy, 19th Edition, Gennaro, Ed., Mack Publishing Co., Easton, PA, 1995. В одном воплощении композиции включают комбинации из нескольких (двух и больше) выделенных антител по изобретению, действующих по различным механизмам, напр., одно антитело, которое преимущественно действует, индуцируя CDC, в комбинации с другим антителом, которое преимущественно действует, индуцируя апоптоз.
Фармацевтические композиции изобретения также могут применяться при комбинированной терапии, т.е. в сочетании с другими агентами. Например, комбинированная терапия может включать композицию настоящего изобретения вместе с по меньшей мере одним противовоспалительным средством или по меньшей мере одним иммунодепрессантом. В одном воплощении такие терапевтические средства включают одно или несколько противовоспалительных средств, как-то стероидных препаратов или NSAID (нестероидных противовоспалительных препаратов). Предпочтительными средствами являются, к примеру, аспирин и другие салицилаты, такие ингибиторы Сох-2, как рофекоксиб (Vioxx) и целекоксиб (Celebrex), такие NSAID, как ибупрофен (Motrin, Advil), фенопрофен (Nalfon), напроксен (Naprosyn), сулиндак (Clinoril), диклофенак (Voltaren), пироксикам (Feldene), кетопрофен (Orudis), дифлунисал (Dolobid), набуметон (Relafen), этодолак (Lodine), оксапрозин (Daypro) и индометацин (Indocin).
В другом воплощении такие терапевтические средства включают средства, вызывающие истощение или функциональную инактивацию регуляторных Т-клеток, как-то циклофосфамид в низких дозах, антитела против CTLA4, антитела против IL2 или рецептора IL2.
В следующем воплощении такие терапевтические средства включают одно или несколько средств химиотерапии, как-то производные таксола, таксотер, гемцитабин, 5-фторурацил, доксорубицин (Adriamycin), цисплатин (Platinol), циклофосфамид (Cytoxan, Procytox, Neosar). В другом воплощении антитела настоящего изобретения могут применяться в комбинации с такими средствами химиотерапии, которые предпочтительно проявляют терапевтическую эффективность на пациентах, страдающих раком желудка, пищевода, поджелудочной железы и легких.
В следующем воплощении антитела по изобретению могут применяться в сочетании с радиотерапией и/или пересадкой аутологических стволовых клеток или костного мозга.
В следующем воплощении антитела по изобретению могут применяться в сочетании с одним или несколькими антителами из числа антител против CD25, антител против ЕРСАМ, антител против EGFR, против Her2/neu и против CD40.
В следующем воплощении антитела по изобретению могут применяться в сочетании с антителом против C3b(i) для того, чтобы усилить активацию комплемента.
В настоящем изобретении "фармацевтически приемлемый носитель" включает всевозможные растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые средства, изотонические и замедляющие всасывание средства и др., которые являются физиологически совместимыми. Предпочтительно носитель подходит для внутривенного, внутримышечного, подкожного, парентерального, интраспинального или эпидермального применения (напр., инъекции или инфузии). В зависимости от способа применения активное соединение, т.е. антитело, биспецифичная или мультиспецифичная молекула, может быть покрыто каким-то материалом, защищающим это соединение от действия кислот и других природных условий, которые могут его инактивировать.
"Фармацевтически приемлемая соль" означает такую соль, которая сохраняет желательную биологическую активность исходного соединения и не оказывает каких-либо нежелательных токсикологических эффектов (напр., см. Berge S.М. et al. (1977) J. Pharm. Sci. 66: 1-19).
Примеры таких солей включают кислотноаддитивные соли и основноаддитивные соли. Кислотноаддитивные соли включают соли, образованные с нетоксичными неорганическими кислотами, такими как соляная, азотная, фосфорная, серная, бромистоводородная, йодистоводородная кислота, фосфористая кислота и др., а также с нетоксичными органическими кислотами, такими как алифатические моно- и дикарбоновые кислоты, фенилзамещенные алкановые кислоты, гидроксиалкановые кислоты, ароматические кислоты, алифатические и ароматические сульфоновые кислоты и др. Основноаддитивные соли включают соли, образованные с щелочноземельными металлами, такими как натрий, калий, магний, кальций и др., а также с нетоксичными органическими аминами, такими как N,N'-дибензил-этилендиамин, N-метилглюкамин, хлорпрокаин, холин, диэтаноламин, этилендиамин, прокаин и др.
Композиции настоящего изобретения могут применяться целым рядом способов, известных в этой области. Специалистам должно быть известно, что способ и/или режим применения зависит от требуемых результатов. Активные соединения могут быть приготовлены вместе с носителями, которые должны защищать соединения от быстрого выделения, как-то лекарственные формы с контролируемым высвобождением, включая импланты, трансдермальные пластыри и микроинкапсулированные системы доставки. Можно использовать такие биоразрушимые, биосовместимые полимеры, как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полимолочная кислота. Методы приготовления таких лекарственных форм широко известны специалистам в этой области, напр., см. Sustained and Controlled Release Drug Delivery Systems, J.R. Robinson, ed., Marcel Dekker, Inc., New York, 1978.
Для введения соединений по изобретению при некоторых способах применения может потребоваться покрытие соединения или совместное введение его с материалом, предотвращающим его инактивацию. Например, соединения можно вводить субъекту в соответствующем носителе, к примеру, липосомах или разбавителе. Липосомы включают эмульсии CGF типа "вода-масло-вода", а также стандартные липосомы (Strejan et al. (1984) J. Neuroimmunol. 7: 27).
Фармацевтически приемлемые носители включают стерильные водные растворы или дисперсии и стерильные порошки для приготовления ex temporo стерильных растворов или дисперсий для инъекций. Применение таких сред и веществ для фармацевтически активных субстанций известно в данной области. За исключением тех случаев, когда какая-то стандартная среда или вещество несовместимы с активным соединением, предусматривается их применение в фармацевтических композициях изобретения. В композиции также можно включать вспомогательные активные соединения.
Терапевтические композиции, как правило, должны быть стерильными и стабильными в условиях производства и хранения. Композиции могут быть составлены в виде раствора, микроэмульсии, липосом или иной упорядоченной структуры, подходящей для высокой концентрации лекарственного вещества. Носитель может представлять собой растворитель или дисперсионную среду, содержащую, к примеру, воду, этанол, полиоли (как-то глицерин, пропиленгликоль, полиэтиленгликоль и др.) и их подходящие смеси. Надлежащая текучесть может поддерживаться, к примеру, с помощью таких покровных материалов, как лецитин, соблюдением требуемого размера частиц в случае дисперсий и с помощью поверхностно-активных веществ. Во многих случаях предпочтительно в композиции нужно включать вещества, поддерживающие изотоничность, например, сахара, такие полиспирты, как маннит, сорбит, либо хлорид натрия. Можно вызвать замедленное всасывание композиций для инъекций добавлением в композицию веществ, замедляющих всасывание, например, солей моностеарата и желатина.
Стерильные растворы для инъекций могут быть получены включением активного соединения в требуемом количестве в надлежащий растворитель с одним или с комбинацией ингредиентов, перечисленных выше, как потребуется, с последующей стерилизацией микрофильтрованием.
В общем случае дисперсии получают включением активного соединения в стерильный носитель, содержащий щелочную дисперсионную среду и другие нужные ингредиенты из числа перечисленных выше. В случае стерильных порошков для приготовления стерильных растворов для инъекций предпочтительными способами получения являются вакуумная сушка и замораживание-высушивание (лиофилизация), которые дают порошок активного ингредиента вместе с любым другим требуемым ингредиентом из предварительно стерилизованного фильтрованием раствора.
Схемы дозировки подбирают таким образом, чтобы обеспечить оптимальную требуемую реакцию (напр., терапевтическую реакцию). Например, можно вводить дозы одним болюсом, несколькими дробными дозами за какое-то время или же можно снижать либо повышать дозу пропорционально в соответствии с требованиями терапевтической ситуации. Особенно предпочтительно составление парентеральных композиций в виде стандартных лекарственных форм для удобства введения и единообразия дозировки. Стандартная лекарственная форма в настоящем изобретении означает физически дискретные единицы, пригодные в качестве однократных доз для подлежащих лечению субъектов, при этом каждая единица содержит заданное количество активного соединения, рассчитанное на оказание требуемого терапевтического эффекта вместе с конкретным фармацевтическим носителем. Технические условия на стандартные лекарственные формы по изобретению диктуются и прямо зависят от: (а) уникальных характеристик активного соединения и заданного конкретного терапевтического эффекта, и (b) ограничений, существующих в области составления рецептур таких активных соединений для лечения отдельных лиц.
Примеры фармацевтически приемлемых антиоксидантов включают: (1) водорастворимые антиоксиданты, такие как аскорбиновая кислота, цистеина гидрохлорид, бисульфат натрия, метабисульфит натрия, сульфит натрия и др.; (2) жирорастворимые антиоксиданты, такие как аскорбилпальмитат, бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), лецитин, пропилгаллат, α-токоферол и др.; и (3) хелаторы металлов, такие как лимонная кислота, этилендиаминтетрауксусная кислота (ЭДТА), сорбит, винная кислота, фосфорная кислота и др.
Что касается терапевтических композиций, то они включают лекарственные формы настоящего изобретения, подходящие для перорального, интраназального, местного (в том числе трансбуккального и подъязычного), интраректального, интравагинального и/или парентерального применения. Лекарственные формы для удобства могут быть представлены в стандартной лекарственной форме и могут быть получены любыми способами, известными в области фармации. Количество активного ингредиента, которое можно сочетать с материалом носителя для получения стандартной лекарственной формы, будет варьировать в зависимости от подлежащего лечению субъекта и конкретного способа применения. Количество активного ингредиента, которое можно сочетать с материалом носителя для получения стандартной лекарственной формы, в общем должно быть таким, чтобы композиция оказывала терапевтический эффект.
В общем случае это количество из 100% составляет от 0,01% до 99% активного ингредиента, предпочтительно от 0,1% до 70%, наиболее предпочтительно от 1% до 30%.
Составы настоящего изобретения, которые подходят для интравагинального применения, включают маточные кольца, тампоны, кремы, гели, пасты, пенистые или аэрозольные формы, содержащие такие носители, которые в этой области считаются подходящими. Лекарственные формы для местного или трансдермального введения соединений настоящего изобретения включают порошки, аэрозоли, мази, пасты, кремы, лосьоны, гели, растворы, пасты и средства для ингаляции. Активное соединение можно смешивать в стерильных условиях с фармацевтически приемлемым носителем и с такими консервантами, буферами или вытеснителями, которые могут потребоваться.
Выражения "парентеральное введение" и "вводится парентерально" в настоящем изобретении означают другие способы применения, чем энтеральное и местное введение, обычно с помощью инъекции, и охватывают внутривенные, внутримышечные, внутриартериальные, интратекальные, внутрисуставные, подглазничные, внутрисердечные, интрадермальные, внутрибрюшинные, транстрахеальные, подкожные, субкутикулярные, внутрисуставные, субкапсулярные, субарахноидные, интраспинальные, эпидуральные и внутригрудинные инъекции и вливания.
Примеры подходящих водных и неводных носителей, которые можно использовать в фармацевтических композициях изобретения, включают воду, этанол, полиоли (как-то глицерин, пропиленгликоль, полиэтиленгликоль и др.) и их подходящие смеси, растительные масла, как-то оливковое масло, и такие пригодные для инъекций органические эфиры, как этилолеат. Надлежащая текучесть может поддерживаться, к примеру, с помощью таких покровных материалов, как лецитин, соблюдением требуемого размера частиц в случае дисперсий и с помощью поверхностно-активных веществ.
Эти композиции также могут содержать вспомогательные вещества, как-то консерванты, смачивающие вещества, эмульгирующие вещества и диспергирующие вещества. Защита от присутствия микроорганизмов может обеспечиваться как мероприятиями по стерилизации, так и добавлением различных антибактериальных и противогрибковых средств, к примеру, парабена, хлорбутанола, фенола, сорбиновой кислоты и др. Также может потребоваться включение в композиции таких веществ, поддерживающих изотоничность, как сахара, хлорид натрия и др. Кроме того, можно вызвать замедленное всасывание фармацевтических форм для инъекций добавлением таких веществ, замедляющих всасывание, как моностеарат алюминия и желатин.
В одном воплощении моноклональные антитела по изобретению вводятся в кристаллическом виде путем подкожной инъекции, см. Yang et al. (2003) PNAS, 100(12): 6934-6939. Когда соединения настоящего изобретения вводятся людям и животным в виде фармацевтических препаратов, то они могут вводиться сами по себе или в виде фармацевтической композиции, содержащей, к примеру, от 0,01 до 99,5% (более предпочтительно от 0,1 до 90%) активного соединения в сочетании с фармацевтически приемлемым носителем.
Независимо от выбранного способа применения, соединения настоящего изобретения, которые могут применяться в подходящей гидратированной форме, и/или фармацевтические композиции настоящего изобретения заключаются в фармацевтически приемлемые лекарственные формы стандартными методами, известными специалистам в этой области.
Фактический уровень дозы активных ингредиентов в фармацевтических композициях настоящего изобретения можно варьировать с тем, чтобы получить такое количество активного ингредиента, которое будет эффективным для достижения требуемой терапевтической реакции для определенного пациента, композиции и способа применения, но не будет токсичным для пациента. Выбираемый уровень дозы зависит от ряда фармакокинетических факторов, включая активность конкретной композиции настоящего изобретения, способа применения, времени введения, скорости выведения конкретного соединения, продолжительности лечения, других лекарств, соединений и/или материалов, используемых в сочетании с конкретными композициями, возраста, пола, веса, заболевания, общего состояния здоровья и истории болезни подвергающегося лечению пациента и других факторов, хорошо известных в области медицины.
Рядовой врач или ветеринар легко может установить и предписать эффективное количество требуемой фармацевтической композиции. Например, врач или ветеринар может начать дозировку соединения по изобретению, используемого в фармацевтической композиции, с меньших доз, чем это нужно для достижения требуемого терапевтического эффекта, и постепенно повышать дозировку, пока не будет достигнут требуемый эффект. В общем, подходящая суточная доза композиции по изобретению должна составлять такое количество соединения, которое представляет собой наименьшую дозу, эффективно дающую терапевтический эффект. Такая эффективная доза в общем зависит от факторов, описанных выше. Предпочтительно введение осуществляется внутривенно, внутримышечно или подкожно, предпочтительно в ближайшее к мишени место. При желании эффективная суточная доза терапевтической композиции может вводиться в виде 2, 3, 4, 5, 6 и больше дробных доз, вводимых по отдельности через соответствующие интервалы в течение суток, необязательно в виде стандартных лекарственных форм. Хотя соединения настоящего изобретения можно вводить и сами по себе, однако предпочтительно они вводятся в виде лекарственной формы (фармацевтической композиции).
В одном воплощении антитела по изобретению вводятся вливанием, предпочтительно медленным непрерывным вливанием в течение длительного времени, как-то более 24 часов, чтобы уменьшить токсические побочные эффекты. Введение также может осуществляться непрерывным вливанием в течение от 2 до 24 часов, как-то от 2 до 12 часов. Такая схема может быть повторена один или несколько раз, как потребуется, например, через 6 месяцев или 12 месяцев. Дозировка может быть установлена или скорректирована путем измерения количества циркулирующих антител к CLD18 после введения в биологическом образце с помощью антиидиотипических антител, мишенью которых являются антитела к CLD18.
В следующем воплощении антитела вводятся в виде поддерживающей терапии, как-то, напр., раз в неделю на протяжении 6 месяцев или больше.
В следующем воплощении антитела по изобретению могут вводиться по схеме, включающей одно вливание антител к CLD18 с последующим вливанием антител к CLD18, конъюгированных с радиоизотопом. Такая схема может быть повторена, напр., через 7-9 дней.
Терапевтические композиции могут вводиться с помощью медицинских приспособлений, известных в этой области. Например, в одном воплощении терапевтическая композиция изобретения может вводиться с помощью безыгольного шприца-инъектора типа тех, что приведены в US 5,399,163; US 5,383,851; US 5,312,335; US 5,064,413; US 4,941,880; US 4,790,824; или US 4,596,556. Примеры хорошо известных имплантов и модулей, применимых в настоящем изобретении, включают те, что описаны в: US 4,487,603, в котором раскрыт имплантируемый микроинфузионный насос для дозирования медикаментов с контролируемой скоростью; US 4,486,194, в котором раскрыто терапевтическое устройство для введения медикаментов через кожу; US 4,447,233, в котором раскрыт медицинский инфузионный насос для введения медикаментов с точной скоростью вливания; US 4,447,224, в котором раскрыт имплантируемый инфузионный аппарат с вариабельным потоком для непрерывно введения лекарств; US 4,439,196, в котором раскрыта осмотическая система введения лекарств с многоячейными отсеками; и US 4,475,196, в котором раскрыта осмотическая система введения лекарств.
Специалистам известно много таких имплантов, систем и модулей введения. В некоторых воплощениях антитела по изобретению могут быть составлены таким образом, чтобы обеспечить надлежащее распределение in vivo. Например, гематоэнцефалический барьер (ВВВ) не пропускает многие сильно гидрофильные соединения. Для того, чтобы терапевтические соединения изобретения проходили через ВВВ (если нужно), они могут быть заключены, к примеру, в липосомы. Насчет способов изготовления липосом см., напр., US 4,522,811; US 5,374,548 и US 5,399,331. Липосомы могут содержать одну или несколько молекул, которые избирательно транспортируются в определенные клетки или органы и при этом усиливают прицельную доставку лекарств (напр., см. V.V. Ranade (1989) J. Clin. Pharmacol. 29: 685). Примеры наводящих молекул включают фолат или биотин (напр., см. US 5,416,016 на Low et al.); маннозиды (Umezawa et al. (1988) Biochem. Biophys. Res. Commun. 153: 1038); антитела (P.G. Bloeman et al. (1995) FEBS Lett. 357: 140; M. Owais et al. (1995) Antimicrob. Agents Chemother. 39: 180); и рецептор белка A сурфактанта (Briscoe et al. (1995) Am. J. Physiol. 1233: 134).
В одном воплощении изобретения терапевтические соединения по изобретению заключаются в липосомы. В более предпочтительном воплощении липосомы включают наводящую молекулу. В наиболее предпочтительном воплощении терапевтические соединения в липосомах вводятся при инъекции болюсом в место, ближайшее к нужной зоне, напр., на место опухоли. Композиция должна быть жидкой в такой степени, чтобы ее можно было легко вводить шприцем. Она должна быть стабильной в условиях производства и хранения и защищена от заражающего действия таких микроорганизмов, как бактерии и грибки.
В следующем воплощении антитела по изобретению могут быть составлены так, чтобы предотвратить или уменьшить их транспорт через плаценту. Это можно сделать методами, известными в данной области, напр., ПЭГилированием антител или использованием F(ab')2-фрагментов. Дополнительно можно привести работы: Cunniningham-Rundles С, Zhuo Z, Griffith В, Keenan J. (1992) Biological activities of polyethylene-glycol immunoglobulin conjugates. Resistance to enzymatic degradation. J. Immunol. Methods, 152: 177-190; и Landor M. (1995) Maternal-fetal transfer of immunoglobulins, Ann. Allergy Asthma Immunol. 74: 279-283.
"Терапевтически эффективная дозировка" для лечения опухолей может быть измерена по объективным реакциям опухоли, которые могут быть полными либо частичными. Полная реакция (CR) определяется как отсутствие клинических, радиологических или иных признаков болезни. Частичная реакция (PR) означает уменьшение совокупного размера опухоли более чем на 50%. Медиана времени до прогрессирования является мерой, характеризующей продолжительность объективной реакции опухоли.
"Терапевтически эффективная дозировка" для лечения опухолей также может быть измерена по способности стабилизировать прогрессирование болезни. Способность соединения к торможению рака может быть оценена на животных в модельной системе, прогнозирующей его эффективность на опухолях человека. С другой стороны, это свойство композиции может быть оценено при исследовании способности соединения ингибировать рост клеток или апоптоз методами in vitro, известными специалистам. Терапевтически эффективное количество лекарственного соединения может вызывать уменьшение размера опухолей либо иным образом облегчать симптомы у субъекта. Рядовой специалист в этой области сможет определить такое количество, исходя из таких факторов, как габариты субъекта, тяжесть симптомов у субъекта и конкретная композиция или выбранный способ применения.
Композиция должна быть стерильной и жидкой в такой степени, чтобы ее можно было легко вводить шприцем. Наряду с водой, носитель может представлять собой изотонический буферный солевой раствор, этанол, полиоль (например, глицерин, пропиленгликоль, полиэтиленгликоль и др.) и их подходящие смеси. Надлежащая текучесть может поддерживаться, к примеру, с помощью таких покровных материалов, как лецитин, соблюдением требуемого размера частиц в случае дисперсий и с помощью поверхностно-активных веществ. Во многих случаях предпочтительно в композиции нужно включать вещества, поддерживающие изотоничность, например, сахара, такие полиспирты, как маннит или сорбит, и хлорид натрия. Можно вызвать замедленное всасывание композиций для инъекций добавлением в композицию веществ, замедляющих всасывание, например, моностеарата алюминия или желатина.
Если активное соединение надлежащим образом защищено, как описано выше, то его можно вводить перорально, например, с инертным разбавителем или усваиваемым съедобным носителем.
IV. Применения и способы изобретения
Антитела (включая иммуноконъюгаты, биспецифичные/мультиспецифичные, композиции и другие производные, описанные в настоящем изобретении) настоящего изобретения обладают разнообразными терапевтическими свойствами, включая лечение заболеваний с участием клеток, экспрессирующих CLD18. Например, антитела можно вводить клеткам в культуре, напр., in vitro или ex vivo, либо людям-субъектам, напр., in vivo, для лечения или предотвращения ряда заболеваний типа тех, что описаны в настоящем изобретении. В настоящем изобретении термин "субъект" служит для обозначения человека и других животных, реагирующих на антитела против CLD18. Предпочтительными субъектами являются люди, страдающие такими заболеваниями, которые можно корригировать или облегчить путем уничтожения больных клеток, в частности клеток, отличающихся изменением профиля экспрессии CLD18 в сравнении с нормальными клетками.
Терапевтический эффект в способах лечения, приведенных в настоящем изобретении, предпочтительно достигается через функциональные свойства антител по изобретению для уничтожения клеток, напр., индуцируя лизис по механизму обусловленной комплементом цитотоксичности (CDC), лизис по механизму антителозависимой клеточной цитотоксичности (ADCC), апоптоз, гомотипическую адгезию и/или фагоцитоз, предпочтительно индуцируя лизис по механизму CDC и/или ADCC.
Например, в одном воплощении антитела настоящего изобретения могут применяться для лечения субъектов с опухолеродными заболеваниями, напр., заболеваниями, отличающимися наличием раковых клеток, экспрессирующих CLD18, в том числе, к примеру, рака желудка. Примеры опухолеродных заболеваний, которые можно лечить и/или предотвращать, охватывают все раковые заболевания, экспрессирующие CLD18, включая рак желудка, рак пищевода, рак поджелудочной железы, рак легких, рак яичников, рак молочной железы, рак толстой кишки, рак печени, рак желчного пузыря и рак головы и шеи. Эти раковые заболевания могут находиться на ранней, промежуточной или поздней стадии, напр., метастазирования.
Описанные фармацевтические композиции и способы лечения по изобретению могут применяться и для иммунизации или вакцинации для профилактики описанных в нем заболеваний.
В другом воплощении антитела по изобретению могут применяться для выявления уровня CLD18 или определенных форм CLD18 либо уровня клеток, содержащих CLD18 на поверхности своих мембран, при этом уровень может быть связан с определенными заболеваниями или симптомами заболеваний типа тех, что описаны выше. С другой стороны, антитела могут применяться для удаления или воздействия на функции экспрессирующих CLD18 клеток, чтобы показать, что эти клетки являются важными медиаторами заболевания. Это достигается путем обработки образца и контрольного образца антителами к CLD18 в условиях, способствующих образованию комплекса между антителом и CLD18. Образовавшиеся комплексы между антителами и CLD18 выявляют и сравнивают их в образце и контрольном образце, т.е. стандартном образце.
Антитела по изобретению можно сначала протестировать на активность связывания в связи терапевтическим или диагностическим применением in vitro. Например, антитела можно протестировать методом проточной цитометрии, как описано в настоящем изобретении.
Кроме того, можно определить активность антител в запуске по меньшей мере одной эффекторной активности эффекторных клеток, включая ингибирование роста и/или уничтожение клеток, экспрессирующих CLD18. Например, можно определить способность антител к запуску CDC и/или апоптоза. Методики анализа CDC, гомотипической адгезии, молекулярной агрегации или апоптоза описаны в настоящем изобретении.
Антитела по изобретению могут применяться для того, чтобы вызвать in vivo или in vitro одну или несколько из следующих биологических активностей: ингибировать рост и/или дифференцировку клеток, экспрессирующих CLD18; уничтожать клетки, экспрессирующие CLD18; опосредовать фагоцитоз или ADCC у экспрессирующих CLD18 клеток в присутствии эффекторных клеток; опосредовать CDC у экспрессирующих CLD18 клеток в присутствии комплемента; опосредовать апоптоз клеток, экспрессирующих CLD18; индуцировать гомотипическую адгезию; и/или индуцировать транслокацию в липидные островки при связывании с CLD18.
В предпочтительном воплощении антитела применяются in vivo или in vitro для лечения, профилактики или диагностики целого ряда связанных с CLD18 заболеваний. Примеры связанных с CLD18 заболеваний включают, среди прочего, такие раковые заболевания, как рак желудка, рак поджелудочной железы, рак пищевода, рак легких и другие разновидности рака, перечисленные выше.
CLD18A2 также экспрессируется в дифференцированных нормальных клетках желудка. Возможные вызванные антителами клинические побочные эффекты при гибели этих клеток можно уменьшить или устранить путем параллельного применения таких защищающих желудок препаратов, как антациды, или таких ингибиторов протонного насоса желудка, как омепразол и родственные ему препараты.
Подходящие способы применения композиций антител по изобретению in vivo и in vitro хорошо известны и могут быть выбраны рядовым специалистом.
Как описано выше, антитела против CLD18 по изобретению можно вводить совместно с одним или несколькими другими терапевтическими средствами, напр., цитотоксическим средством, радиотоксическим средством, антиангиогенным средством или иммунодепрессантом, чтобы уменьшить возникновение иммунных ответов против антител изобретения. Антитело можно присоединить к агенту (в виде иммунокомплекса) или вводить отдельно от агента. В последнем случае (раздельное введение) антитела можно вводить до, после или вместе с агентом либо вводить совместно с другими известными способами терапии, как-то противораковой терапии, напр., облучением. Такие терапевтические средства включают, среди прочего, антинеопластические средства типа тех, что перечислены выше. Совместное введение антител к CLD18 настоящего изобретения со средствами химиотерапии обеспечивает два противораковые средства, работающие по различным механизмам, оказывающим цитотоксический эффект на опухолевые клетки. Такое совместное введение может решить проблемы, связанные с возникновением устойчивости к лекарственным препаратам или с изменением антигенности опухолевых клеток, вследствие чего они перестают реагировать на антитела.
В другом предпочтительном воплощении изобретения субъект, которому вводятся антитела, дополнительно получает антиангиогенное средство, включая антитела к VEGF или VEGFR и одно или несколько химических соединений, ингибирующих ангиогенез. Предварительная обработка или параллельное применение этих препаратов может улучшить проникновение антител в большие опухоли.
В следующем предпочтительном воплощении изобретения субъект, которому вводятся антитела, дополнительно получает соединение, ингибирующее передачу сигнала от рецептора фактора роста, включая антитела, связывающиеся с рецептором EGFR, а также химические соединения, ингибирующие передачу сигналов, запускаемых рецепторами EGFR, Her1 или Her2/neu.
Специфичные к мишени эффекторные клетки, напр., эффекторные клетки, связанные с композициями (напр. антителами, мультиспецифичными и биспецифичными молекулами) по изобретению, также могут применяться в качестве терапевтических средств. Эффекторные клетки для воздействия на мишень могут представлять собой лейкоциты человека, как-то макрофаги, нейтрофилы или моноциты. Другие клетки включают эозинофилы, нормальные клетки-киллеры и другие клетки, несущие рецепторы IgG или IgA. При желании эффекторные клетки можно получить у подлежащего лечению пациента. Специфичные к мишени эффекторные клетки можно вводить в виде суспензии клеток в физиологически приемлемом растворе. Количество вводимых клеток может составлять от 108 до 109, но оно будет зависеть от цели терапии. В общем, это количество должно быть достаточным для достижения локализации на клетках мишени, напр., на опухолевых клетках, экспрессирующих CLD18, и уничтожения клеток, напр., путем фагоцитоза. Способы применения также могут быть разными.
Терапия с помощью специфичных к мишени эффекторных клеток может проводиться в сочетании с другими методами удаления намеченных клеток. Например, противоопухолевая терапия с помощью композиций изобретения и/или эффекторных клеток, заряженных этими композициями, может применяться в сочетании с химиотерапией. Кроме того, может применяться комбинированная терапия для того, чтобы направить две разные цитотоксические эффекторные популяции на удаление раковых клеток. Например, можно использовать антитела к CLD18, соединенные с антителами к Fc-RI или CD3, вместе со специфичными агентами связывания рецепторов IgG или IgA.
Биспецифичные и мультиспецифичные молекулы по изобретению также могут применяться для модулирования уровня FcγR или FcαR на эффекторных клетках, как-то путем кэппинга и удаления рецепторов на поверхности клеток. Для этой цели также можно использовать смеси антител к Fc-рецепторам.
Композиции (напр. антитела, мультиспецифичные и биспецифичные молекулы и иммуноконъюгаты) по изобретению, обладающие сайтами связывания комплемента, к примеру, те части IgG1, -2, или -3 либо IgM, которые связываются с комплементом, также могут применяться в присутствии комплемента. В одном воплощении обработка ex vivo популяции клеток, составляющей клетки мишени, связывающим агентом по изобретению и соответствующими эффекторными клетками, может дополняться добавлением комплемента или сыворотки, содержащей комплемент. При связывании белков комплемента может улучшиться фагоцитоз клеток мишени, покрытых связьшающим агентом изобретения. В другом воплощении клетки мишени, покрытые композициями изобретения, также могут быть лизированы комплементом. В еще одном воплощении композиции изобретения не активируют комплемент.
Композиции изобретения также могут вводиться вместе с комплементом. Соответственно, в рамки изобретения входят композиции, содержащие антитела, мультиспецифичные или биспецифичные молекулы и сыворотку или комплемент. Такие композиции дают преимущество в том, что комплемент находится в тесном соседстве с антителами, мультиспецифичными или биспецифичными молекулами.
С другой стороны, антитела, мультиспецифичные или биспецифичные молекулы изобретения и комплемент или сыворотка могут вводиться раздельно. Связывание композиций настоящего изобретения с клетками мишени может вызвать транслокацию комплекса антиген CLD18-антитело в липидные островки клеточной мембраны. Такая транслокация создает высокую плотность комплексов антиген-антитело, которые могут эффективно активировать и/или усиливать CDC.
Также в рамки изобретения входят наборы, содержащие композиции антител по изобретению (напр., антитела и иммуноконъюгаты) и инструкции по применению. Набор может дополнительно содержать один или несколько дополнительных реагентов, как-то иммунодепрессант, цитотоксическое средство или радиотоксическое средство либо одно или несколько дополнительных антител по изобретению (напр., антител, обладающих комплементарной активностью).
Соответственно, пациентам, получающим композиции антител по изобретению, можно дополнительно вводить (до, одновременно с или после введения антител по изобретению) другое терапевтическое средство, как-то цитотоксическое или радиотоксическое средство, которое усиливает или увеличивает терапевтический эффект антител по изобретению.
В других воплощениях субъект может дополнительно получать средство, которое модулирует, напр., усиливает или ингибирует активность Fcγ- или Fcα-рецепторов, к примеру, при обработке субъекта цитокином. Предпочтительными цитокинами являются колониестимулирующий фактор гранулоцитов (G-CSF), колониестимулирующий фактор гранулоцитов/макрофагов (GM-CSF), γ-интерферон (IFN-γ) и фактор некроза опухолей (TNF). Другие важные средства для повышения терапевтической эффективности антител и фармацевтических композиций, описанных в настоящем изобретении, - это β-глюканы, которые представляют собой гомополисахариды из разветвленных глюкозных звеньев и вырабатываются многими растениями и микроорганизмами, например, бактериями, водорослями, грибами, дрожжами и зерновыми. Также можно использовать фрагменты β-глюканов, вырабатываемых организмами. Предпочтительно β-глюкан является полимером β(1,3)-глюкозы, в котором по крайней мере некоторые глюкозные звенья остова, напр., 3-6% глюкозных звеньев остова имеют ответвления типа β(1,6)-глюкозы.
В предпочтительном воплощении изобретения предусмотрены способы детектирования присутствия антигена CLD18 в образцах или измерения количества антигена CLD18, которые включают контактирование образца и контрольного образца с антителом, специфически связывающимся с CLD18, в условиях, способствующих образованию комплекса между антителом или его частью и CLD18. Затем детектируют образование комплекса, при этом отличия по образованию комплекса между образцом по сравнению с контрольным образцом указывают на присутствие антигена CLD18 в образце.
В следующем воплощении изобретения предусмотрен способ детектирования присутствия или определения количества экспрессирующих CLD18 клеток in vivo или in vitro. Способ включает: (i) введение субъекту композиции по изобретению, конъюгированной с детектируемым маркером; (ii) подвергание субъекта средству детектирования данного детектируемого маркера для идентификации зон, содержащих экспрессирующие CLD18 клетки.
Вышеописанные способы применимы, в частности, для диагностики связанных с CLD18 заболеваний и/или локализации таких связанных с CLD18 заболеваний, как раковые заболевания. Предпочтительно более высокое содержание CLD18, предпочтительно CLD18-A2, в образце, чем содержание CLD18, предпочтительно CLD18-А2, в контрольном образце, указывает на наличие связанного с CLD18 заболевания у субъекта, в частности человека, у которого был взят образец.
В следующем воплощении иммуноконъюгаты по изобретению могут применяться для доставки соединений (напр., терапевтических средств, меток, цитотоксинов, радиотоксинов, иммунодепрессантов и т.п.) к клеткам, на поверхности которых экспрессирован CLD18, путем присоединения таких соединений к антителам. При этом изобретением также предусмотрены способы локализации ex vivo или in vitro клеток, экспрессирующих CLD18, как-то циркулирующих раковых клеток.
Далее настоящее изобретение раскрывается на следующих примерах, которые не следует воспринимать как ограничивающие рамки изобретения.
ПРИМЕРЫ
Пример 1. Получение антител мыши против CLD18
а. Иммунизация
Мышей Balb/c или C57/BL6 иммунизировали с помощью эукариотических экспрессионных векторов, кодирующих фрагменты CLD18 человека (SEQ ID NO: 15, 16; 17, 18). Вводили 50 мкг или 25 мкг плазмидной ДНК в четырехглавую мышцу (внутримышечно, i.m.) в 1-й и 10-й день для получения моноклональных антител набора 1 либо в 1-й и 9-й, 1-й и 11-й или 1-й, 16-й и 36-й день для получения моноклональных антител набора 2 в присутствии адъювантов, например, CpG (подробности см. в таблице 1b). CpG, равно как и клетки, трансфицированные только CLD18A2 (SEQ ID NO: 1) либо вместе с другой РНК, кодирующей растворимый CD40L мыши, вводили внутримышечно, a PEI-Man вводили внутримышечно либо внутрибрюшинно. Наличие антител против CLD18 человека в сыворотке мышей отслеживали методом иммунофлуоресцентной микроскопии между 16 и 43 днем в зависимости от конкретной методики иммунизации. Иммунофлуоресценцию определяли на клетках HEK293, временно трансфицированных нуклеиновой кислотой, кодирующей слитую конструкцию, содержащую CLD18A2 человека (SEQ ID NO: 1, 2) и флуоресцентный белок-репортер. Мышам с заметными иммунными ответами (фиг. 1) делали повторную иммунизацию (бустер) за 3 дня до спленэктомии для получения моноклональных антител набора 1 либо за 3 дня, за 3 и 2 дня или же за 4, 3 и 2 дня до спленэктомии для получения моноклональных антител набора 2 путем внутрибрюшинного введения 5×107 либо 1×108 клеток HEK293, временно трансфицированных нуклеиновой кислотой, кодирующей CLD18A2 человека (SEQ ID NO: 1, 2) (подробности см. в таблице 1b). Методики иммунизации для соответствующих моноклональных антител приведены в таблице 1а.
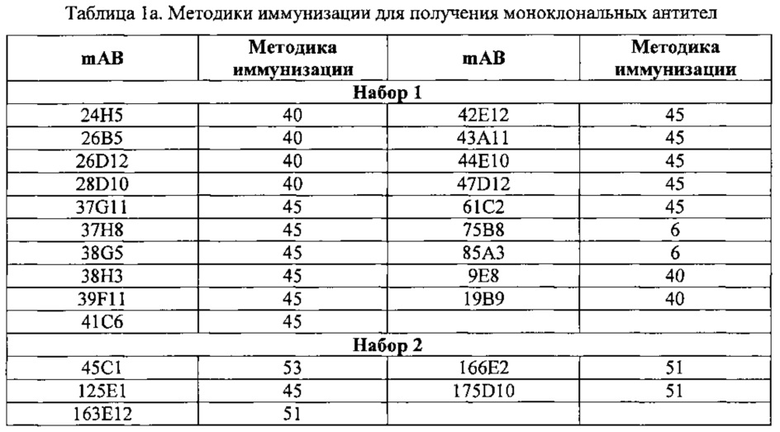
* Конкретные методики иммунизации см. в таблице 1b
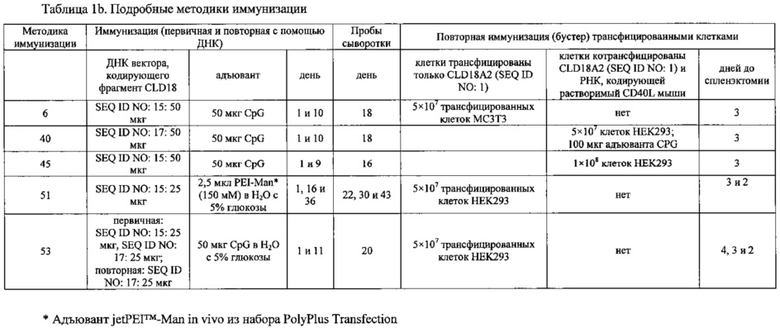
b. Получение гибридом, вырабатывающих моноклональные антитела человека к CLD18
Выделяли спленоциты мыши и сливали с линией клеток миеломы мыши по стандартным методикам. Затем полученные гибридомы подвергали скринингу на вырабатывание специфичных к CLD18 иммуноглобулинов, используя клетки HEK293, трансфицированные нуклеиновой кислотой, кодирующей CLD18 человека, методом анализа FACS.
Одноклеточные суспензии селезеночных лимфоцитов из иммунизированных мышей сливали с клетками несекретирующей миеломы мыши P3X63Ag8U.1 (АТСС, CRL 1597) в соотношении 2:1 с помощью 50% PEG (Roche Diagnostics, CRL 738641). Клетки высеивали примерно при 3×104 клеток на лунку в плоскодонных микропланшетах, а затем инкубировали около 2 недель в селективной среде, содержащей 10% телячьей сыворотки, 2% слитой гибридомы и клонирующую добавку (HFCS, Roche Diagnostics, CRL 1363735) плюс 10 мМ HEPES, 0,055 мМ 2-меркаптоэтанол, 50 мкг/мл гентамицина и 1×HAT (Sigma, CRL Н0262). Через 10-14 дней индивидуальные лунки проверяли методом проточной цитометрии на моноклональные антитела к CLD18. Секретирующие антитела гибрид ома снова высеивали, проверяли еще раз и, если они опять давали положительную реакцию на моноклональные антитела к CLD18, субклонировали методом предельного разведения. Затем устойчивые субклоны культивировали in vitro для получения небольших количеств антител в культуральной среде для изучения. Отбирали по меньшей мере один клон от каждой гибридомы, который сохранял реактивность исходных клеток (методом FACS). Для каждого клона создавали банк клеток в 9 пузырьках и хранили в жидком азоте.
c. Отбор моноклональных антител, связывающихся с CLD18
Для определения изотипа антител проводили анализ методом ELISA. Для определения подкласса Ig у идентифицированных реагирующих с CLD18 моноклональных антител использовали набор для антител мыши Mouse monoAB ID Kit (Zymed, CRL 90-6550) либо IsoStrip Mouse Monoclonal Antibody Isotyping Kit (Roche, кат. % 1493027).
Было получено 19 линий клеток гибридом, обозначенных как набор 1: 6 от слияния клеток мыши C57/BL6, иммунизированной с помощью CLD18A2-LoopD3 (SEQ ID NO: 17, 18), и 13 от слияния клеток мыши Balb/c, иммунизированной с помощью CLD18A2-LoopD1 (SEQ ID NO: 15, 16), которые экспрессируют следующие антитела: 24Н5, 26В5, 26D12, 28D10, 37G11, 37Н8, 38G5, 38Н3, 39F11, 41С6, 42Е12, 43А11, 44Е10, 47D12, 61С2, 75В8, 85А3, 9Е8, 19В9.
24Н5: моноклональное κ-антитело мыши типа IgG2b, 182-D758-034
26В5: моноклональное κ-антитело мыши типа IgG2a, 182-D758-035, DSM АСС2745
26D12: моноклональное κ-антитело мыши типа IgG3, 182-D758-036, DSM АСС2746
28D10: моноклональное κ-антитело мыши типа IgG3, 182-D758-040, DSM АСС2747
37G11: моноклональное κ-антитело мыши типа IgG2a, 182-D1106-055, DSM АСС2737
37Н8: моноклональное κ-антитело мыши типа IgG3, 182-D1106-056, DSM АСС2738
38G5: моноклональное κ-антитело мыши типа IgG3, 182-D1106-057, DSM АСС2739
38Н3: моноклональное κ-антитело мыши типа IgG3, 182-D1106-058, DSM АСС2740
39F11: моноклональное κ-антитело типа IgG3, 182-D1106-059, DSM АСС2741
41С6: моноклональное κ-антитело мыши типа IgG2a, 182-D1106-060
42Е12: моноклональное κ-антитело мыши типа IgG2a, 182-D1106-061, DSM АСС2748
43A11: моноклональное κ-антитело мыши типа IgG2a, 182-D1106-062, DSM АСС2742
44Е10: моноклональное κ-антитело мыши типа IgG3, 182-D1106-063
47D12: моноклональное κ-антитело мыши типа IgG3, 182-D1106-064
61С2: моноклональное κ-антитело мыши типа IgG2b, 182-D1106-067, DSM АСС2743
75В8: моноклональное κ-антитело мыши типа IgM, 182-D756-001
85A3: моноклональное κ-антитело мыши типа IgM, 182-D756-002
9Е8: моноклональное κ-антитело мыши типа IgM, 182-D758-011
19В9: моноклональное κ-антитело мыши типа IgM, 182-D758-024
Было получено 5 линий клеток гибридом, обозначенных как набор 2:1 от слияния клеток мыши Balb/c, иммунизированной с помощью CLD18A2-LoopD3 (SEQ ID NO: 17, 18) и CLD18A2-LoopD1 (SEQ ID NO: 15, 16), и 4 от слияния клеток мыши Balb/c, иммунизированной с помощью CLD18A2-LoopD1 (SEQ ID NO: 15, 16), которые экспрессируют следующие антитела: 45С1, 125Е1, 163Е12, 166Е2, 175D10.
45С1: моноклональное κ-антитело мыши типа IgG2a, 182-D758-187
125Е1: моноклональное κ-антитело мыши типа IgG2a, 182-D1106-279, DSM АСС2808
163Е12: моноклональное κ-антитело мыши типа IgG3, 182-D1106-294, DSM АСС2809
166Е2: моноклональное κ-антитело мыши типа IgG3, 182-D1106-308
175D10:моноклональное κ-антитело мыши типа IgG1, 182-D1106-362, DSM АСС2810
Пример 2. Получение моноклональных антител
Получение и очистка моноклональных антител, реагирующих с CLD 18
Для получения антител в масштабе нескольких мг для функционального исследования клетки гибридом высеивали в диализные биореакторы (CELLine CL1000, Integra, Chur, СН) при 2×106 клеток/мл. Содержащий антитела супернатант собирали раз в неделю. Моноклональные антитела мыши очищали с помощью геля Melon Gel (Pierce, Rockford, USA) и концентрировали путем осаждения сульфатом аммония либо очищали с помощью белка А методом FPLC. Концентрацию и степень очистки антител определяли методом BCA-Assay и проверяли чистоту методом гель-электрофореза с додецилсульфатом натрия и окрашивания Кумасси.
Пример 3. Характеристики связывания моноклональных антител
a. Контроль качества трансфектантов в WB, IF 3
Для получения клеток, экспрессирующих CLD18A2, клетки HEK293 или СНО трансфицировали нуклеиновыми кислотами, кодирующими CLD18A2 (SEQ ID NO: 1, 2) или CLD18A2-myc (SEQ ID NO: 3, 4).
Клетки HEK293 трансфицировали с помощью CLDN18A2-myc (SEQ ID NO: 3, 4) либо оставляли нетрансфицированными. Через 24 после трансфекции клетки собирали, лизировали и подвергали гель-электрофорезу с додецилсульфатом натрия. Гель подвергали блоттингу и прокрашивали с помощью антитела мыши против myc. После инкубации с меченным пероксидазой антителом против мыши блот проявляли с помощью реагента ECL и отображали на приборе для визуализации LAS-3000 (Fuji). Полоса с ожидаемым молекулярным весом CLD18-myc наблюдалась только в трансфицированных клетках, но не в отрицательном контроле (фиг. 2).
Клетки СНО трансфицировали с помощью CLD18A2 (SEQ ID NO: 1, 2) и культивировали на камерных предметных стеклах в течение 24 ч. Клетки фиксировали метанолом и окрашивали с помощью поликлонального антитела кролика против CLD18 при 1 мкг/мл в течение 60 мин при 25°С. После отмывки клетки окрашивали с помощью меченных А1еха488 козьих антител против IgG кролика (Molecular Probes) и исследовали методом флуоресцентной микроскопии. На фиг. 3 представлены трансфицированные клетки СНО, экспрессирующие CLD18 на клеточной мембране, а также нетрансфицированные клетки.
Эти гетерологически экспрессирующие CLD18 клетки использовали при нижеследующих анализах для проверки специфичности связывания антител.
b. Отбор моноклональных антител, связывающихся с CLD18 - первичный скрининг методом проточной цитометрии
Клетки HEK293 трансфицировали совместно экспрессионными векторами, кодирующими CLD18A2 человека (SEQ ID NO: 1, 2) и флуоресцентный белок-репортер за 40 ч до анализа или же использовали клетки HEK293, устойчиво экспрессирующие CLD18A2 человека (HEK293-CLD18A2), и делали контрастное окрашивание пропидия иодидом (PI). После отделения клеток с помощью 2 мМ EDTA/PBS клетки отмывали полной средой культивирования и высеивали примерно при 1-5×105 клеток на лунку в микропланшеты с U-образным дном. Клетки инкубировали в течение 30 мин при 4°С с супернатантом гибридомы с последующей отмывкой два раза раствором 1% инактивированной нагреванием FBS/PBS и заключительной инкубацией с конъюгированным с АРС или Alexa647 вторичным антителом против IgG мыши. После двукратной отмывки котрансфицированные клетки фиксировали с помощью CellFLX (BD Biosciences). Связывание определяли методом проточной цитометрии на приборе BD FACSArray. Строили график экспрессии флуоресцентного маркера по горизонтальной оси против связывания антител по вертикальной оси. Все антитела мыши: 24Н5, 26В5, 26D12, 28D10, 37G11, 37Н8, 38G5, 38Н3, 39F11, 41С6, 42Е12, 43А11, 44Е10, 47D12, 61С2, 75В8, 85А3, 9Е8, 19В9, 45С1, 125Е1, 163Е12, 166Е2 и 175D10 проявляли специфическое связывание с поверхностью экспрессирующих флуоресцентный маркер клеток (фиг. 4, клетки в Q2), что видно на примере супернатантов гибридом, содержащих моноклональные антитела 24Н5 (фиг. 4А, клетки в Q2), 85А3 (фиг. 4В), 175D10, 125Е1, 163Е12, 166Е2 и 45С1 (фиг. 4С, клетки в Q1).
c. Сравнение связывания антител с CLD18A2, меченным Myc или HA
Характеристики связывания идентифицированных моноклональных антител, специфичных к CLD18, изучали более подробно. При этом анализировали связывание антител с мутантами CLD18A2, созданным путем вставки эпитопных меток. CLD18A2-НА (SEQ ID NO: 6) содержит эпитопную метку НА в петле 1 CLD18A2, a CLD18A2-Myc (SEQ ID NO: 4) содержит эпитопную метку Myc, вставленную в петлю 2 CLD18A2. Поскольку вставка этих меток вызывает разрушение эпитопов, то идентифицированные моноклональные антитела можно разбить на группы в соответствии с потерей связывания с одним из мутантов. Клетки HEK293, временно котрансфицированные флуоресцентным маркером и CLD18A2 человека либо флуоресцентным маркером и CLD18A2-HA либо флуоресцентным маркером и CLD18A2-Myc, инкубировали с супернатантами гибридом, содержащих моноклональные антитела, специфичные к CLD18, в течение 30 мин при 4°С, с последующей инкубацией с конъюгированным с Alexa647 вторичным антителом против IgG мыши. Перед проведением анализа на приборе BD FACSArray клетки фиксировали с помощью CellFIX. Как видно на примере 24Н5, 9Е8, 26В5 и 19В9 на фиг. 5, моноклональные антитела по своим характеристикам связывания разбиваются на 4 различные группы: (i) антитела, которые связываются с немодифицированным CLD18A2, равно как и с CLD18A2-HA и CLD18A2-Myc, напр., 24Н5 (фиг. 5A); (ii) антитела, которые не связываются с CLD18A2-HA, напр., 9Е8 (фиг. 5В); (iii) антитела, которые не связываются с CLD18A2-Myc, напр., 26В5 (фиг. 5С); и (iv) антитела, которые не связываются ни с CLD18A2-HA, ни с CLD18A2-Myc, напр., 19В9 (фиг. 5D).
d. Сравнение связывания антител с трансфектантами CLD18A1 и CLD18A2 человека методом проточной цитометрии
Анализировали специфичность связывания идентифицированных моноклональных антител с изоформами CLD18 методом проточной цитометрии. Клетки HEK293, устойчиво экспрессирующие CLD18A2 человека (HEK293-CLD18A2), и клетки HEK293, устойчиво экспрессирующие CLD18A1 человека (SEQ ID NO: 7, 8) (HEK293-CLD18A1), инкубировали в течение 30 мин при 4°C с супернатантами гибридом, содержащих моноклональные антитела, с последующей инкубацией с конъюгированным с Alexa647 вторичным антителом против IgG мыши и фиксированием клеток или же без фиксирования, но с контрастным окрашиванием с помощью PI. Связывание определяли методом проточной цитометрии на приборе BD FACSArray. На фиг. 6 представлены примеры для двух групп моноклональных антител, идентифицированных из числа 24Н5, 26В5, 26D12, 28D10, 37G11, 37Н8, 38G5, 38Н3, 39F11, 41С6, 42Е12, 43А11, 44Е10, 47D12, 61С2, 75В8, 85А3, 9Е8, 19В9, 45С1, 125Е1, 163Е12, 166Е2, 175D10: (i) моноклональные антитела 43A11, 45С1 и 163Е12 специфически связываются с CLD18A2 человека, но не с CLD18A1 человека (фиг. 6А, В); и (ii) моноклональное антитело 37Н8 связывается с обеими изоформами CLD18 человека (фиг. 6А).
e. Сравнение связывания антител с трансфектантами CLD18A1 и CLD18A2 человека методом иммунофлуоресцентной микроскопии
Клетки HEK293 временно трансфицировали экспрессионным вектором, кодирующим слитый белок CLD18A1 (SEQ ID NO: 8) или CLD18A2 (SEQ ID NO: 2) с флуоресцентным репортером и культивировали на Chamber Slides. Клетки окрашивали без фиксации либо после фиксации параформальдегидом с помощью супернатантов культур, содержащих моноклональные антитела, в течение 30 мин при 37°С. После отмывки клетки окрашивали с помощью меченных Alexa555 антител против Ig мыши (Molecular Probes). Связывание антител определяли методом флуоресцентной микроскопии. Как видно из фиг. 7, антитело 37G11 специфически реагирует с CLD18A2 (фиг. 7А), но не с CLD18A1 (фиг. 7В). Напротив, антитело 26В5 реагирует и с CLD18A2, и с CLD18A1 (фиг. 8).
У антител 24Н5, 26В5, 26D12, 28D10, 37G11, 37Н8, 38G5, 38Н3, 39F11, 41С6, 42Е12, 43А11, 44Е10, 47D12, 61С2, 75В8, 85А3, 9Е8, 19В9 наблюдалось четкое отличие между окрашиванием живых клеток и фиксированных параформальдегидом клеток. Антитела давали однородное окрашивание мембран у фиксированных клеток (фиг. 7С, 8С, 8D). В противоположность этому инкубация живых клеток с этими антителами ведет к образованию белковых агрегатов, проявляющихся в виде пятнистого окрашивания (фиг. (Fig. 7A, 8A, 8B). Это означает, что все антитела связываются с нативными эпитопами, находящимися на поверхности живых клеток.
f. Определение эндогенно экспрессирующих линий клеток
Для скрининга клеточных линий на экспрессирование CLD18A2 методом ОТ-ПЦР использовали специфичную к гену CLD18A2 пару праймеров (SEQ ID NO: 11, 12). Как оказалось, линии клеток карциномы желудка человека NCI-SNU-16 (АТСС CRL-5974), NUGC-4 (JCRB0834) и KATO-III (АТСС НТВ-103) и линия клеток аденокарциномы поджелудочной железы человека DAN-G (DSMZ АСС249) проявляют хорошую эндогенную экспрессию CLD18 (фиг. 9). Экспрессия подтвердилась на уровне белка при окрашивании с помощью поликлональной сыворотки кролика против CLD18.
g. Окрашивание эндогенно экспрессирующих линий клеток специфичными к CLD18 антителами и иммунофлуоресцентный анализ
Клетки DAN-G, SNU-16, NUGC-4 и KATO-III культивировали на Chamber Slides при стандартных условиях. Клетки не фиксировали либо фиксировали метанолом и окрашивали с помощью соответствующих антител. У антител 24Н5, 26В5, 26D12, 28D10, 37G11, 37Н8, 38G5, 38Н3, 39F11, 41С6, 42Е12, 43А11, 44Е10, 47D12, 61С2, 75В8, 85А3, 9Е8, 19В9 наблюдалось окрашивание поверхности клеток, как видно из фиг. 10, 11 и 12А. У антител 45С1, 125Е1, 163Е12, 166Е2 и 175D10 отмечалось распознавание нативных эпитопов и наблюдалось окрашивание поверхности клеток на нефиксированных клетках, как видно из фиг. 12В. Подгруппы антител проявляли однородное окрашивание клеточной мембраны либо преимущественно на границе между клетками, либо на свободных частях мембраны, не примыкающих к другим клеткам. Другие антитела окрашивали отдельные очаги и агрегаты на клеточной мембране, в целом показывая, что соответствующие антитела связываются с разными эпитопами, включая эпитопы, которые маскируются при гомотипической или гетеротипической ассоциации CLD18, а также эпитопы, доступные в сформированных плотных контактах.
h. Окрашивание эндогенно экспрессирующих линий клеток по данным проточной цитометрии
Анализировали поверхностную экспрессию конститутивно экспрессируемого CLD18A2 на живых клетках KATO-III и NUGC-4 методом проточной цитометрии. Это представлено на примере клеток KATO-III и NUGC-4, окрашенных с помощью моноклональных антител 61С2 или 163Е12 с последующей инкубацией с конъюгированным с Alexa647 вторичным антителом против IgG мыши и фиксацией клеток либо без фиксации. Связывание определяли методом проточной цитометрии на приборе BD FACSArray. На фиг. 6 видно сильное связывание 61С2 по меньшей мере с 70,3% клеток KATO-III и связывание 163Е12 с CLD18A2 на клетках KATO-III и NUGC-4.
i. Сопоставление последовательностей CLD18A1 и CLD18A2 мыши и человека
CLD18A2 человека (NP_001002026) и CLD18A1 человека (NP_057453) при сравнении последовательностей отличаются по N-концевой части, а варианты CLD18 мыши (NP_062789 и AAL15636) проявляют высокую гомологичность и сайты вариации последовательностей между молекулами (см. фиг. 14).
j. Реактивность антител с CLD18A1 мыши и CLD18A2 мыши при анализе методом проточной цитометрии
Анализировали связывание идентифицированных моноклональных антител с CLD18A2 и CLD18A1 мыши методом проточной цитометрии. Клетки HEK293, временно котрансфицированные флуоресцентным маркером и CLD18A2 мыши (SEQ ID NO: 33, 35) или флуоресцентным маркером и CLD18A1 мыши (SEQ ID NO: 36, 37), инкубировали с супернатантами гибридом, содержащих специфичные к CLD18 человека моноклональные антитела 38G5, 38Н3, 37G11, 45С1 и 163Е12, соответственно, в течение 30 мин при 4°С, с последующей инкубацией с конъюгированным с Alexa647 вторичным антителом против IgG мыши и фиксированием клеток. Связывание определяли методом проточной цитометрии на приборе BD FACSArray. На фиг. 15 представлено 3 различных профиля связывания: 38G5 и 45С1 не связываются ни с одной изоформой CLD18 мыши; 37G11, и 163Е12 связываются с CLD18A2 мыши, но не с CLD18A1 мыши; а 38Н3 связывается с CLD18A1 и CLD18A2 мыши. Эти антитела являются ценными инструментами для определения возможной токсичности моноклональных антител к CLD18 при доклинических исследованиях.
В целом эти данные показывают, что моноклональные антитела по изобретению 24Н5, 26В5, 26D12, 28D10, 37G11, 37Н8, 38G5, 38Н3, 39F11, 41С6, 42Е12, 43А11, 44Е10, 47D12, 61С2, 75В8, 85А3, 9Е8, 19В9, 45С1, 125Е1, 163Е12, 166Е2 и 175D10 против CLD18 представляют разнообразие характеристик связывания с различными эпитопами и топологиями CLD18 человека.
Комбинация различных свойств, описанных в примерах 3b, c, d, e, g, h и j, может использоваться для классификации моноклональных антител на различные классы.
Пример 4. Иммуногистохимия (IHC)
Для иммуногистохимического изучения экспрессии CLD18A2 использовали специфичное к эпитопу CLD18A2 антитело, полученное при иммунизации пептидом SEQ ID NO: 21. Для анализа экспрессии и локализации белка использовали заключенные в парафин срезы тканей из обширной панели нормальных и опухолевых тканей. За исключением желудка, никакой существенной экспрессии в нормальных тканях других органов не обнаружено (см. таблицу 2, фиг. 16А). Напротив, методом иммуногистохимии установлена экспрессия CLD18A2 при различных видах рака, включая рак желудка и рак легких (фиг. 16В).
Интересно, что экспрессия белка CLD18A2 в слизистой желудка ограничивалась терминально дифференцированными клетками эпителия в области основания и ямки желудка. Напротив, клетки слизистой желудка в области шейки, в частности стволовые клетки желудка в области перехвата, которые восполняют всю слизистую, не экспрессируют CLD18A2 (фиг. 16С).
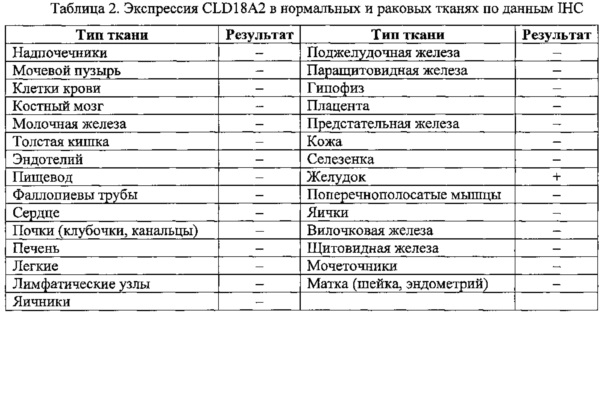
Для иммуногистохимического исследования специфической экспрессии CLD18A2 использовали моноклональное антитело 39F11. Как видно из фиг. 17А, не обнаружено никакой существенной реактивности во всех исследованных нормальных тканях, за исключением желудка (фиг. 17А), тогда как карциномы желудка и карциномы легких давали сильную положительную реакцию (фиг. 17В).
Другая группа антител по изобретению проявляет специфический раковый профиль окрашивания, проявляя связывание при раке желудка, но не реагируя с нормальной тканью желудка. Такой профиль окрашивания представлен на фиг. 18А у моноклонального антитела 26В5.
Метод иммуногистохимии использовали для анализа специфичности антител 175D10 (фиг. 18В), 43А11 (фиг. 18С), 163Е12 (фиг. 18D) и 45С1 (фиг. 18Е) на срезах, полученных из раковых линий клеток HEK293. Для получения твердых опухолей мышам прививали раковые линии клеток HEK293, устойчиво экспрессирующих CLD18A2 (HEK293-CLD18A2) или CLD18A1 (HEK293-CLD18A1) человека либо трансфицированных контрольной экспрессирующей плазмидой, содержащей только ген устойчивости к антибиотику для отбора (HEK293-mock). В подвергнутых холостой трансфекции ксенотрансплантатах HEK293 экспрессия не обнаруживалась. Напротив, сильное и однородное окрашивание мембран наблюдалось в ксенотрансплантатах HEK293-CLD18A2 и в образцах карциномы желудка.
Пример 5. Комплемент-зависимая цитотоксичность (CDC)
a. CDC у моноклональных антител из набора 1 методом проточной цитометрии
Плазму для обусловленного комплементом лизиса получали из крови, взятой у здоровых добровольцев в герметичные пробирки S-Monovette-EDTA (Sarstedt,  , Германия), которые затем центрифугировали при 600 g в течение 20 мин. Плазму собирали и хранили при -20°С.
, Германия), которые затем центрифугировали при 600 g в течение 20 мин. Плазму собирали и хранили при -20°С.
В первой серии экспериментов анализировали супернатанты гибридом на их способность вызывать комплемент-зависимую цитотоксичность (CDC) против клеток HEK293, устойчиво экспрессирующих CLD18A2 человека (HEK293-CLD18A2). Клетки инкубировали с супернатантами гибридом, содержащих моноклональные антитела 85А3, 28D10, 24Н5 или 26D12, соответственно, в течение 20 мин при комнатной температуре. После центрифугирования (5 мин при 450 g) супернатант удаляли, а к клеткам добавляли 20% плазмы человека в среде DMEM (подогретой до 37°С) и инкубировали еще 20 мин при 37°С. После этого определяли лизис клеток методом FACS по окрашиванию их пропидия иодидом (PI), который добавляли до конечной концентрации 2,5 мкг/мл. Для проточной цитометрии использовали проточный цитометр BD FACSArray (BD Biosciences, Mountain View, С А). Для анализа накапливали по меньшей мере 10000 событий, при этом обломки клеток исключали путем регулирования порога прямого бокового рассеяния света (FCS). Содержание лизированных клеток (PI-положительных) в процентах представлено на фиг. 19. Моноклональные антитела 85А3, 28D10 и 26D12 вызывали лизис у 33,5, 38,2 и 39,2%, соответственно, клеток HEK293-CLD18A2, тогда как обусловленная 24Н5 CDC составила только 19,3%.
b. CDC у моноклональных антител из набора 1
Во второй серии экспериментов анализировали специфичность моноклональных антител при индукции ими CDC на экспрессирующих CLD18A2 клетках. Для этого набор антител, специфически связывающихся с CLD18A2 человека либо также связывающихся с CLD18A1 человека, тестировали на индуцирование CDC против клеток СНО, устойчиво трансфицированных CLD18A2 человека (CHO-CLD18A2) или CLD18A1 человека (СНО-CLD18A1). Клетки CHO-CLD18A2 и CHO-CLD18A1 высеивали за 24 ч до определения при плотности в 3×104 клеток на лунку в плоскодонных микропланшетах для тканевой культуры. На следующий день культуральную среду удаляли, а клетки инкубировали в тройных пробах с доведенными до концентрации 10 мкг/мл супернатантами гибридом, содержащих моноклональные антитела 24Н5, 26D12, 28D10, 37G11, 37Н8, 38G5, 38Н3, 39F11, 41С6, 42Е12, 43А11, 44Е10, 47D12 и 61С2, соответственно. Контрольные клетки инкубировали с чистой средой или со средой, содержащей 0,2% сапонина, для определения фонового лизиса и максимального лизиса, соответственно. После инкубации в течение 20 мин при комнатной температуре супернатант удаляли, а к клеткам добавляют 20% плазмы человека в DMEM (подогретой до 37°С) и инкубировали еще 20 мин при 37°С. Затем супернатанты заменяли на PBS, содержащий 2,5 мкг/мл этидия бромида, и измеряли испускаемую флуоресценцию при возбуждении при 520 нм на приборе Tecan Safire. Специфический лизис в процентах рассчитывали следующим образом: специфический лизис в % = (флуоресценция образца - флуоресценция фона)/(флуоресценция при максимальном лизисе - флуоресценция фона)×100. Из фиг. 20 видно, что моноклональные антитела 26D12, 28D10, 37Н8, 38Н3 и 39F11 опосредуют высокую, моноклональное антитело 38G5 опосредует среднюю, моноклональные антитела 41С6 и 61С2 опосредуют низкую, а моноклональные антитела 24Н5, 37G11, 42Е12, 43А11, 44Е10 и 47D12 вообще не опосредуют CDC против клеток CHO-CLD18A2. Напротив, некоторые из антител способны индуцировать CDC против клеток CHO-CLDA1, хотя 26D12, 28D10, 37Н8, 38Н3, 39F11, 41С6, 47D12 и 61С2 еще и связываются с CLD18A1, как установлено методами проточной цитометрии и иммунофлуоресценции.
c. Титрование моноклональных антител и CDC с помощью моноклональных антител из набора 1
Для измерения способности антител против CLD18 индуцировать CDC при низких концентрациях проводили эксперимент, в котором подвергали титрованию три различных антитела. Клетки CHO-CLD18A2, растущие в микропланшетах, инкубировали при различных концентрациях 75В8 (100, 30, 10, 3 и 1 мкг/мл), 37Н8 (10, 3,3 и 1 мкг/мл) и 28D10 (10, 1 и 0,1 мкг/мл), соответственно, в течение 20 мин при комнатной температуре. Супернатант удаляли, а к клеткам добавляют 20% плазмы человека в DMEM (подогретой до 37°С) и инкубировали еще 20 мин при 37°С. Перед анализом на приборе Tecan Safire супернатанты заменяли на PBS, содержащий 2,5 мкг/мл этидия бромида. На фиг. 21А-С представлен специфический лизис в процентах в зависимости от концентрации антител. Моноклональное антитело 75В8 вызывает лизис у 31,0% клеток CHO-CLD18A2 при 10 мкг/мл, который падает до 6,2% при 1 мкг/мл (фиг. 21А), тогда как моноклональные антитела 28D10 и 37Н8 все еще вызывают специфический лизис на 39% и 26,5% при 1 мкг/мл (фиг. 21В, С), соответственно.
d. CDC у моноклональных антител из набора 2 по данным проточной цитометрии
Сыворотку для обусловленного комплементом лизиса получали из крови, взятой у здоровых добровольцев в герметичные пробирки Serum-Monovette (Sarstedt,  , Германия), которые затем центрифугировали при 600 g в течение 20 мин. Сыворотку собирали и хранили при -20°С. Контрольную сыворотку перед хранением инактивировали нагреванием при 56°С в течение 30 мин.
, Германия), которые затем центрифугировали при 600 g в течение 20 мин. Сыворотку собирали и хранили при -20°С. Контрольную сыворотку перед хранением инактивировали нагреванием при 56°С в течение 30 мин.
Анализировали супернатанты гибридом на их способность вызывать комплементзависимую цитотоксичность (CDC) против клеток KATO-III, эндогенно экспрессирующих CLD18A2 человека. Клетки инкубировали с неочищенными или очищенными супернатантами гибридом, содержащих моноклональные антитела 45С1, 125Е1, 163Е12, 166Е2 и 175D10, соответственно, в течение 30 мин при 37°С. К клеткам добавляли 20% сыворотки человека в среде RPMI и инкубировали еще 30 мин при 37°С. После этого определяли лизис клеток методом FACS по окрашиванию их пропидия иодидом (PI), который добавляли до конечной концентрации 2,5 мкг/мл. Для проточной цитометрии использовали проточный цитометр BD FACSArray (BD Biosciences, Mountain View, CA). Для анализа накапливали по меньшей мере 10000 событий, при этом обломки клеток исключали путем регулирования порога прямого бокового рассеяния света (FSC/SSC). Специфический лизис рассчитывали по следующей формуле: специфический лизис = (% PI-положительных клеток в образце - % PI-положительных клеток в образце с инактивированной нагреванием сывороткой). Наблюдался хороший лизис по механизму CDC, в частности у 163Е12.
Пример 6. Антителозависимая клеточная цитотоксичность (ADCC)
Анализировали супернатанты гибридом на их способность вызывать антителозависимую клеточную цитотоксичность (ADCC) против клеток HEK293, устойчиво экспрессирующих CLD18A2 человека (HEK293-CLD18A2) или CLD18A1 человека (HEK293-CLD18A1).
a. Обогащение мононуклеаров периферической крови человека. Кровь человека от здоровых доноров разбавляли вдвое фосфатным буфером (PBS) и наслаивали клетки крови на фиколл (Lymphocyte Separation Medium 1,077 г/мл, РАА Laboratories, кат. № J15-004). Мононуклеары периферической крови (MNCs) собирали на границе фаз, промывали и ресуспендировали в культуральной среде RPMI 1640 с добавлением 10% инактивированной нагреванием телячьей сыворотки, 2 мМ L-глутамина.
b. Постановка ADCC. Клетки мишени метили усиливающим флуоресценцию лигандом (BADTA, набор DELFIA для определения цитотоксичности фирмы Perkin Elmer, реагенты для цитотоксичности EuTDA, кат. № AD0116) в течение 30 мин. После тщательной отмывки средой RPMI-10 с добавлением 10 мМ пробенецида (Sigma, кат. № Р8761), 10-20 мМ HEPES и 10% инактивированной нагреванием телячьей сыворотки клетки доводили до 1×105 клеток/мл. Меченные клетки мишени, эффекторные клетки (MNCs) и супернатанты, содержащие моноклональные антитела, доведенные до концентрации 10 мкг/мл, вносили в кругло донные лунки микропланшета. Для выделенных эффекторных клеток соотношение эффектор/мишень (Е:Т) составляло 100:1 (данные для 50:1 и 25:1 не приводятся). После инкубации (2 часа, 37°С) определение останавливали центрифугированием и измеряли высвобождение флуоресцентного лиганда в двойных пробах по сигналам европия на флуориметре с разрешением во времени. Клеточную цитотоксичность в процентах рассчитывали по следующей формуле: специфический лизис в % = (сигнал при экспериментальном высвобождении - сигнал при спонтанном высвобождении)/(сигнал при максимальном высвобождении - сигнал при спонтанном высвобождении)×100, причем максимальное высвобождение флуоресцентного лиганда определяли при добавлении Triton Х-100 (конечная концентрация 0,25%) к клеткам мишени, а спонтанное высвобождение измеряли в отсутствие антител и эффекторных клеток. Из фиг. 22 видно, что моноклональные антитела 26В5, 37Н8, 38G5, 47D12 и 61С2 вызывают ADCC против клеток HEK293-CLD18A2. Напротив, эти антитела не вызывают существенной или вызывают лишь низкий уровень цитотоксичности на содержащих CLD18A1 мишенях, что свидетельствует о CLD18A2-специфичной ADCC (фиг. 23).
Пример 7. Ингибирование пролиферации
Очищенные моноклональные антитела мыши анализировали на их способность ингибировать рост клеток KATO-III, эндогенно экспрессирующих CLD18A2 человека.
По 1×104 клеток мишени, эндогенно экспрессирующих CLD18A2 (KATO-III), культивировали в присутствии примерно 10 мкг моноклональных антител.
Набор DELFIA Cell Proliferation Kit (Perkin-Elmer, кат. № AD0200) представляет собой неизотопный набор для иммуноанализа по измерению включения 5-бром-2-дезоксиуридина (BrdU) при синтезе ДНК в пролиферирующих клетках на микропланшетах. Включение BrdU детектируют с помощью меченных европием моноклональных антител. Для детектирования антител клетки фиксируют и денатурируют ДНК с помощью раствора Fix. Несвязавшиеся антитела отмывают и добавляют индуктор DELFIA, вызывающий диссоциацию ионов европия из меченных антител в раствор, где они образуют сильно флуоресцирующие хелаты с компонентами индуктора DELFIA. Флуоресценция, измеряемая методом флуориметрии с разрешением во времени при детектировании, пропорциональна синтезу ДНК в клетках из каждой лунки.
Сильное ингибирование пролиферации наблюдалось в присутствии антител 125Е1, 163Е12, 45С1, 37G11, 37Н8, 28D10 и 166Е2, соответственно. Умеренное ингибирование пролиферации наблюдалось в присутствии мышиных антител 43А11, 175D10, 42Е12, 26D12, 61С2 и 38Н3, соответственно.
Пример 8. Эффективность на терапевтических моделях ксенотрансплантатов мыши
Исследовали терапевтический потенциал идентифицированных моноклональных антител, специфически связывающихся с CLD18A2, на терапевтических моделях ксенотрансплантатов.
a. Раннее лечение сильно экспрессирующих CLD18A2 опухолей у мышей
Мышам SCID инокулировали подкожно 1×107 клеток HEK293, устойчиво экспрессирующих CLD18A2 человека (HEK293-CLD18A2). Уровень экспрессии CLD18A2 человека в клетках HEK293-CLD18A2 был сравним с уровнем экспрессии при первичном раке желудка у больных. Каждая группа экспериментального лечения включала 10 мышей (количество мышей на группу n=10). Лечение мышей начинали через 3 дня после прививки опухоли. Мышам вводили внутривенно по 200 мкг очищенных супернатантов гибридом, представляющих мышиные моноклональные антитела 26В5, 26D12, 28D10, 37G11, 37Н8, 38G5, 39F11, 42Е12, 43А11, 38Н3 или 61С2, раз в неделю на протяжении 4 недель. В качестве альтернативы мышам вводили по 200 мкг очищенных супернатантов гибридом, содержащих мышиные моноклональные антитела 45С1, 125Е1, 163Е12, 166Е2 или 175D10, два раза в неделю на протяжении 6 недель, чередуя внутривенное и внутрибрюшинное введение. Рост опухолей у обработанных мышей отмечали два раза в неделю (объем опухоли = длина × ширина × ширина, деленная на 2, в мм3). Мышей забивали, если опухоль достигала объема 500 мм3 или в случае тяжелого состояния. На фиг. 24 видно хорошее ингибирование роста опухолевых клеток HEK293-CLD18A2 антителами по изобретению. На фиг. 25А и 25В видно продление срока жизни при лечении антителами по изобретению на модели раннего лечения ксенотрансплантатов с использованием клеток HEK293-CLD18A2.
b. Позднее лечение запущенных сильно экспрессирующих CLD18A2 опухолей у мышей
Та же самая модель опухолей-ксенотрансплантатов на основе клеток HEK293-CLD18A2 была спланирована как методика позднего начала терапии в противоположность раннему лечению, описанному выше. На 27-й день после инокуляции раковых клеток мышей разбивали случайным образом на опытные группы, включающие по 5-6 мышей, и начинали лечение с помощью 200 мкг очищенных супернатантов гибридом, содержащих мышиные моноклональные антитела 43А11, 163Е12 и 175D10, соответственно. Антитела вводили два раза в неделю на протяжении 6 недель, чередуя внутривенное и внутрибрюшинное введение. Также и на этой модели оказалось, что антитела по изобретению ингибируют рост опухолей. У некоторых антител это приводило к продлению срока жизни (фиг. 26).
c. Раннее лечение опухолей, экспрессирующих CLD18A2 на низком уровне
Мышам SCID инокулировали подкожно 2×105 клеток раковой линии DAN-G, линии клеток инфильтрующей аденокарциномы поджелудочной железы человека, которая конститутивно экспрессирует белок CLD18A2 на низком уровне. Лечение мышей (10 на группу) начинали через 3 дня после прививки опухолей. Мышам вводили по 200 мкг очищенных супернатантов гибридом, содержащих мышиные моноклональные антитела 45С1, 125Е1, 163Е12, 166Е2 или 175D10, два раза в неделю на протяжении 6 недель, чередуя внутривенное и внутрибрюшинное введение. Вследствие агрессивного и быстрого роста опухолей раковой линии клеток поджелудочной железы DAN-G in vivo у мышей развивалась раковая кахексия и они погибали в течение нескольких дней. Несмотря на то, что из-за этого окно для измерения терапевтических эффектов оказалось узким, ингибирование роста опухолей и продление срока жизни под действием антител по изобретению наблюдалось и на этой модели (фиг. 27А и 27В).
d. Антитела по изобретению не вызывают побочных эффектов у мышей
Использовали специфичную к CLD18A2 мыши пару праймеров (s: СТА CCA AGG GCT ATG GCG ТТС, as: GCA CCG AAG GTG ТАС CTG GTC), чтобы методом ОТ-ПЦР амплифицировать кДНК, полученную из обширной панели нормальных тканей мыши (см. фиг. 28).
Экспрессия CLD18A2 мыши не обнаруживалась ни в одной нормальной ткани, за исключением желудка (см. фиг. 28). Кроме того, использовали специфичное к CLD18A2 антитело, дающее перекрестную реакцию с CLD18A2 человека и мыши, для иммуногистологического анализа экспрессии CLD18A2 в большой группе нормальных тканей мыши (см. таблицу 3). За исключением нормальной ткани желудка, все исследованные нормальные ткани не проявляли экспрессии CLD18A2. Так же, как это наблюдалось в случае CLD18A2 человека, у его мышиного аналога тоже оказалось, что в то время, как клетки поверхностного эпителия и более глубоких крипт экспрессируют CLD18A2 на своей поверхности, центральная область шейки дает отрицательную реакцию на CLD18A2 (см. фиг. 29А-С). В целом тканевое распределение CLD18A2 оказалось одинаковым у людей и мышей.
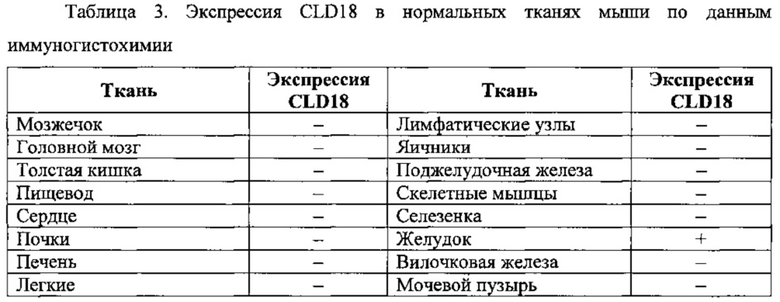
Далее исследовали возможные побочные эффекты у антител 125Е1, 163Е12, 166Е2 и 175D10 на мышах. Ранее было показано методом FACS, что все эти антитела реагируют с CLD18A2 мыши так же, как и с белком человека.
У мышей не наблюдалось никаких видимых побочных эффектов во время и после обработки этими антителами, как и не наблюдалось никаких гистоморфологических коррелятов токсичности в слизистой желудка у получавших антитела мышей в сравнении с необработанными (получавшими PBS) мышами (см. фиг. 30).
e. Раннее лечение сильно экспрессирующих CLD18A2 опухолей у мышей с помощью химерных моноклональных антител
Аналогично примеру 8, но с использованием химерных моноклональных антител, исследовали раннее лечение сильно экспрессирующих CLD18A2 опухолей у мышей антителами по изобретению. Вкратце, мышам SCID инокулировали подкожно 1×107 клеток HEK293, устойчиво экспрессирующих CLD18A2 человека на высоком уровне (HEK293-CLD18A2). Каждая группа экспериментального лечения включала 10 мышей. Лечение мышей начинали через 3 дня после прививки опухоли. Мышам вводили по 200 мкг очищенных супернатантов культур клеток HEK293T, подвергнутых временной трансфекции для получения химерных моноклональных антител ch-163E12 или ch-175D10 (см. ниже, пример 9), два раза в неделю на протяжении 6 недель, чередуя внутривенное и внутрибрюшинное введение. Наблюдалось хорошее ингибирование роста опухолевых клеток HEK293-CLD18A2 химерными антителами по изобретению. На фиг. 34 видно продление срока жизни при лечении химерными антителами по изобретению на модели раннего лечения ксенотрансплантатов с использованием клеток HEK293-CLD18A2.
f. Позднее лечение запущенных сильно экспрессирующих CLD18A2 опухолей у мышей с помощью химерных моноклональных антител
Та же самая модель опухолей-ксенотрансплантатов на основе клеток HEK293-CLD18A2, что описана выше, была спланирована как методика позднего начала терапии в противоположность раннему лечению, описанному выше. На 8-й день после инокуляции раковых клеток мышей разбивали случайным образом на опытные группы, включающие по 9 мышей, и начинали лечение с помощью 200 мкг очищенных супернатантов культур клеток HEK293T, подвергнутых временной трансфекции для получения химерных моноклональных антител ch-163E12 или ch-175D10 (см. ниже, пример 9). Антитела вводили два раза в неделю на протяжении 6 недель, чередуя внутривенное и внутрибрюшинное введение. Также и на этой модели оказалось, что химерные антитела по изобретению ингибируют рост опухолей. У некоторых химерных антител это приводило к продлению срока жизни (фиг. 26).
Пример 9. Химеризация антител
а. Получение химерных моноклональных антител мышь/человек
Тотальную РНК и затем одноцепочечную кДНК получали из мононуклеаров периферической крови человека (РВМС) и из ткани селезенки человека стандартными методами, известными специалистам в этой области, например, с помощью набора RNeasy Midi Kit (Qiagen) и обратной транскриптазы Superscript II (Invitrogen).
Константную область легкой κ-цепи человека амплифицировали из кДНК РВМС методом ПЦР. Смысловой олигомер (SEQ ID NO: 38) вводит рестрикционный сайт BamHI на 5'-конец константной области и изменяет первоначальную последовательность нуклеотидов 5'-CGAACT-3', кодирующую первые две аминокислоты (Arg-Thr) константной области, на 5'-CGTACG-3', создавая рестрикционный сайт BsiWI без изменения аминокислотной последовательности. Антисмысловой олигомер (SEQ ID NO: 39) включает стоп-кодон и вводит рестрикционный сайт NotI на 3'-конец амплифицированной константной области. И продукт ПЦР, и стандартный экспрессионный вектор (например, pcDNA3.1(+), Invitrogen) последовательно инкубировали с рестрикционными ферментами BamHI и NotI. Вектор дополнительно обрабатывали щелочной фосфатазой из кишечника теленка, чтобы предотвратить повторное замыкание кольца. Наконец, константную область лигировали в вектор, так что теперь возможно любое предстоящее слияние вариабельной области перед константной областью через рестрикционный сайт HindIII (5'-AAGCTT-3') из оставшегося от вектора сайта множественного клонирования и через рестрикционный сайт BsiWI (5'-CGTACG-3'), созданный с помощью продукта ПЦР. Последовательность константной области легкой κ-цепи человека, вставленной в вектор, приведена как SEQ ID NO: 40, а аминокислотная последовательность константной области каппа приведена как SEQ ID NO: 41.
Константную область тяжелой γ1-цепи человека амплифицировали из кДНК селезенки методом ПЦР. 5'-Фосфорилированный смысловой олигомер (SEQ ID NO: 42) садится на природный рестрикционный сайт ApaI, расположенный на 11 нуклеотидов ниже от начала константной области, и вводит рестрикционный сайт HindIII на 5'-конец амплифицированной части константной области. 5'-Фосфорилированный антисмысловой олигомер (SEQ ID NO: 43) включает стоп-кодон и вводит рестрикционный сайт NotI на 3'-конец амплифицированной константной области. Полученный при этом продукт ПЦР имеет тупые концы и 5'-фосфорилирован. Амплифицированная константная область гамма относится к подклассу IgGl, что подтверждено методом ПЦР с различительным антисмысловым олигомером (SEQ ID NO: 44) и секвенированием. Стандартный экспрессионный вектор (например, pcDNA3.1(+)/Hygro, Invitrogen) с устойчивостью к другому антибиотику (к примеру, гигромицину), чем у вектора для экспрессирования легкой цепи (к примеру, неомицину), инкубировали с рестрикционным ферментом PmeI для полного удаления сайта множественного клонирования, оставляя тупые концы. Вектор дополнительно обрабатывали щелочной фосфатазой из кишечника теленка, чтобы предотвратить повторное замыкание кольца. Наконец, константную область лигировали в вектор, так что теперь возможно любое предстоящее слияние вариабельной области перед константной областью через рестрикционный сайт HindIII (5'-AAGCTT-3') и через рестрикционный сайт ApaI (5'-GGGCCC-3'), оба созданные с помощью продукта ПЦР. Правильность ориентации константной области в векторе, т.е. подгонки под предшествующий ей промотор вектора, проверяли секвенированием. Из-за расположения рестрикционного сайта ApaI любая амплификация вариабельной области с этой целью должна включать первые 11 нуклеотидов из последовательности константной области гамма-1 человека в дополнение к последовательности сайта ApaI. Последовательность полученной при амплификации константной области тяжелой γ1-цепи человека, вставленной в вектор, приведена как SEQ ID NO: 45, а аминокислотная последовательность экспрессируемой константной области гамма-1 человека приведена как SEQ ID NO: 46.
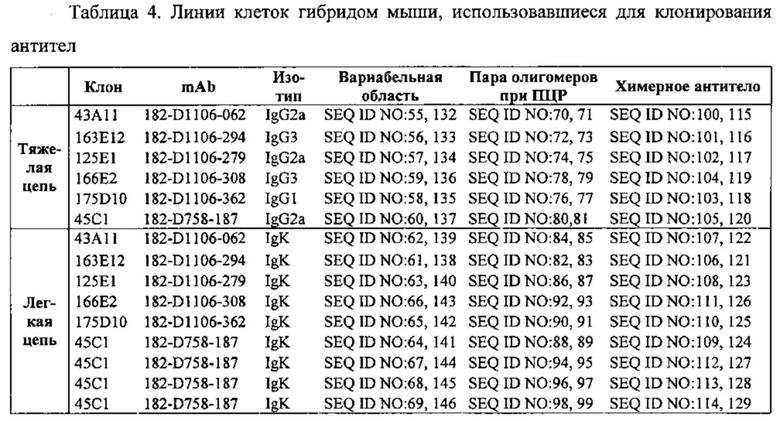
Химерным моноклональным антителам давали наименования, соответствующие их мышиным прототипам с добавлением префикса "ch-", напр., ch-43A11, ch-163E12, ch-125Е1, ch-166E2, ch-175D10, ch-45C1.
Амплификацию вариабельных областей легкой и тяжелой цепей мыши проводили в соответствии с методом "выступающей ПЦР", описанным в Matz et al. (Nucleic Acids Research, 1999, Vol. 27, No.6). Для этого выделяли тотальную РНК из моноклональных линий клеток гибридом (см. таблицу 4) стандартными методами, известными специалистам в этой области, например, с помощью набора RNeasy Mini Kit (Qiagen). Одноцепочечную кДНК получали в соответствии с методом "переключения матрицы", также описанным в Matz et al. (Nucleic Acids Research, 1999, Vol. 27, No.6, 1558). Наряду с олигомером (dT)30 (SEQ ID NO: 47), он включает гибридный олигомер ДНК/РНК, служащий в качестве 5'-адаптора для переключения матрицы во время полимеризации нити кДНК. У этого олигомера-адаптора последние 3 нуклеотида являются рибонуклеотидами, а не дезоксирибонуклеотидами. Для последующей реакции "выступающей ПЦР" использовали антисмысловой олигомер, подогнанный к константной области мышиной κ-цепи или к константной области подкласса 1, 2а или 3 γ-цепи (SEQ ID NO: 49-52, соответственно). Перед этим моноклональные антитела мыши подкласса IgG, вырабатываемые линиями клеток гибридом, подвергали иммунологическому анализу с помощью набора IsoStrip (см. Пример 1), и в соответствии с этим выбирали надлежащий антисмысловой олигомер (см. табл. 4). В качестве смыслового олигомера при "выступающей ПЦР" служила смесь праймеров, содержащая два олигомера, приведенных в SEQ ID NO: 53 и 54. Некоторые линии клеток гибридом экспрессировали более чем одну тяжелую или легкую цепь (помимо цепей, экспрессируемых линией клеток миеломы, использовавшейся для создания гибридом). В таблице 4 приведены номера SEQ ID клонированных и просеквенированных вариабельных областей цепей мышиных антител (SEQ ID NO: 55-69 и SEQ ID NO: 132-146) и клонированных и просеквенированных полноразмерных цепей химерных антител (SEQ ID NO: 100-129).
После этого идентифицированные вариабельные области мыши амплифицировали методом ПЦР, исключая область 5'-UTR и 3'-концевую константную область мыши, добавляя на концы рестрикционные сайты, способствующие субклонированию в заготовленные экспрессионные вектора, несущие константные области человека. Кроме того, смысловые олигомеры обеспечивали консенсусную последовательность Козака (5'-GCCGCCACC-3' или 5'-AGCCACC-3'), а антисмысловые олигомеры для вариабельных областей тяжелой цепи включали первые 11 нуклеотидов константной области гамма-1 человека наряду с рестрикционным сайтом ApaI (см. таблицу 4, SEQ ID NO: 70-99). Вариабельные области легкой к-цепи клонировали с помощью рестрикционных ферментов HindIII и BsiWI, а для вариабельных областей тяжелой γ-цепи требовались рестрикционные ферменты HindIII и ApaI. Вариабельная область тяжелой γ-цепи моноклонального антитела 45С1 содержала внутренний рестрикционный сайт HindIII, но вместо него использовали совместимый фермент BsaI (см. SEQ ID NO: 80). Нуклеотидные последовательности получаемых химерных антител представлены SEQ ID NO: 100-114 (см. таблицу 4), а аминокислотные последовательности соответствующих экспрессируемых химерных антител представлены SEQ ID NO: 115-129 (см. таблицу 4).
b. Создание и получение химерных антител против CLD18
Создавали линии клеток млекопитающих, вырабатывающие химерные антитела со специфичностью к CLD18. Клеточные линии происходили из клеток HEK293T (АТСС CRL-11268). За день до трансфекции 2,5×107 клеток высеивали на чашки диаметром 14,5 см и культивировали в 20 мл полной среды, или же 1×107 клеток высеивали на чашки диаметром 10 см и культивировали в 10 мл полной среды, или же 0,6×106 клеток высеивали в лунки 12-луночного планшета и культивировали в 2-3 мл полной среды (полная среда: среда DMEM:F12 с добавлением 10% FBS без антибиотиков). Рекомендуемая плотность клеток во время трансфекции должна составлять 90% конфлуэнтности. Непосредственно перед трансфекцией среду заменяли свежей средой. Клетки HEK293T трансфицировали с помощью реагентов для трансфекции, напр., Lipofectamine 2000 (Invitrogen, 11668-019) или же Polyethylenimine (Sigma-Aldrich, 408727). Для трансфекции клеток HEK293T использовали ДНК в общем количестве от 110 мкг до 296 мкг на чашку диаметром 14,5 см, а соотношение трансфекционного реагента к ДНК составляло 1:2,5 и 1:12 для Lipofectamine 2000 и PEI, соответственно. Через 24 ч после трансфекции среду заменяли подходящей средой GMP, напр., Х-Vivo 15 (Cambrex), либо средой заданного химического состава типа Pro293a (Cambrex) без сыворотки. Трансфицированные клетки HEK293T, вырабатывающие химерные моноклональные антитела против CLD18, культивировали еще 96 ч. Выделяли неочищенные супернатанты, стерилизовали фильтрованием и очищали на сефарозе с белком А. Концентрацию антител определяли методом ВСА, а чистоту проверяли методом гель-электрофореза с додецилсульфатом и окрашивания Кумасси.
c. Характеристики связывания химерных моноклональных антител
Специфичность связывания с CLD18A2 у клонированных и созданных химерных моноклональных антител анализировали методом проточной цитометрии, как описано в примере 3. Живые клетки HEK293, устойчиво экспрессирующие CLD18A2 человека (HEK293-CLD18A2), и клетки HEK293, устойчиво экспрессирующие CLD18A1 (SEQ ID NO: 7, 8) человека (HEK293-CLD18A1), инкубировали 30 мин при 4°C с очищенными супернатантами культур клеток HEK293T, содержащими химерные моноклональные антитела, после чего инкубировали с конъюгированным с АРС вторичным антителом - F(ab')2-фрагментом козьего Fcγ против IgG человека и контрастно окрашивали с помощью PI. Связывание определяли методом проточной цитометрии на приборе BD FACSArray.
Аналогичным образом анализировали методом проточной цитометрии раковые линии клеток человека, эндогенно экспрессирующие CLD18A2, например, клетки KATO-III и NUGC-4.
На фиг. 31А и В представлен анализ методом проточной цитометрии химерных антител ch-43A11, ch-125E1, ch-163E12, ch-166E2 и ch-175D10. Все они проявляют распознавание нативного эпитопа и проявляют специфическое и сильное связывание с клетками, экспрессирующими CLD18A2, но не CLD18A1.
d. Комплемент-зависимая цитотоксичность (CDC)
Сыворотку для обусловленного комплементом лизиса получали из крови, взятой у здоровых добровольцев в герметичные пробирки Serum-Monovette (Sarstedt, 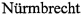 , Германия), которые затем центрифугировали при 600 g в течение 20 мин. Сыворотку собирали и хранили при -20°С. Контрольную сыворотку перед хранением инактивировали нагреванием при 56°С в течение 30 мин.
, Германия), которые затем центрифугировали при 600 g в течение 20 мин. Сыворотку собирали и хранили при -20°С. Контрольную сыворотку перед хранением инактивировали нагреванием при 56°С в течение 30 мин.
Очищенные на сефарозе с белком А химерные антитела настоящего изобретения анализировали на их способность вызывать комплемент-зависимую цитотоксичность (CDC) против клеток KATO-III, эндогенно экспрессирующих CLD18A2 человека, а также устойчиво трансфицированных клеток CHO-CLD18A2. Клетки инкубировали с моноклональными антителами ch-163E12, ch-166E2 и ch-175D10, соответственно, при конечной концентрации от 2,5 мкг/мл до 35 мкг/мл в течение 30 мин при 37°С. К клеткам добавляли 20% сыворотки человека в среде RPMI и инкубировали еще 30 мин при 37°С. После этого дифференцировали мертвые клетки от живых по окрашиванию их пропидия иодидом (PI) в конечной концентрации 2,5 мкг/мл и определяли степень обусловленного антителами лизиса клеток методом проточной цитометрии. Для метода проточной цитометрии использовали проточный питометр BD FACSArray (BD Biosciences, Mountain View, CA). Для анализа накапливали по меньшей мере 10000 событий, при этом обломки клеток исключали путем регулирования порога прямого бокового рассеяния света (FSC/SSC). Специфический лизис рассчитывали по следующей формуле: специфический лизис = (% PI-положительных клеток в образце - % PI-положительных клеток в образце с инактивированной нагреванием сывороткой). У нескольких антител был продемонстрирован специфический лизис по механизму CDC. На клетках CHO-CLD18A2 все три антитела хорошо вызывали CDC (фиг. 32). На клетках KATO-III антитела ch-163Е12 и ch-175D10 хорошо индуцировали CDC.
e. Антителозависимая клеточная цитотоксичность (ADCC)
Очищенные методом FPLC химерные антитела по изобретению анализировали на их способность вызывать антителозависимую клеточную цитотоксичность (ADCC) против клеток KATO-III, эндогенно экспрессирующих CLD18A2 человека.
Кровь человека от здоровых доноров разбавляли вдвое фосфатным буфером (PBS) и наслаивали клетки крови на фиколл (1,077 г/мл, Pharmacia). После центрифугирования мононуклеары периферической крови (РВМС) собирали на границе фаз, промывали и ресуспендировали в культуральной среде X-Vivo-15 с добавлением 5% инактивированной нагреванием человеческой сыворотки.
За 15 ч до анализа клетки KATO-III трансфицировали люциферазой и высеивали при 5×104 клеток на лунку в белый микропланшет.
Для анализа добавляли эффекторные клетки (РВМС, полученные как описано выше) при соотношении эффектор/мишень (Е:Т) 20:1 и очищенные методом FPLC химерные антитела и инкубировали 2-3 часа при 37°С, 5% СО2. Конечная концентрация антител в лунках составляла 50 мкг/мл. После преинкубации в течение 2-3 ч добавляли люцифер желтый (BD Biosciences, San Jose, USA) при 1 мг/мл. Люминесценцию, возникающую при окислении люцифера желтого люциферазой жизнеспособных клеток, измеряли непрерывно вплоть до 6 ч на считывающем устройстве для микропланшетов (Infinite200, Tecan, Швейцария). Клеточную цитотоксичность в процентах рассчитывали по следующей формуле: специфический лизис в % = 100 - ((люминесценция образца - спонтанная люминесценция)/(максимальная люминесценция - спонтанная люминесценция)×100), причем спонтанную люминесценцию определяли при добавлении Triton Х-100 (конечная концентрация 0,2%) к клеткам мишени, а максимальный сигнал измеряли в отсутствие антител.
Этим методом было показано, что моноклональные антитела ch-163E12 и ch-175D10 вызывают сильную ADCC на клетках KATO-III (фиг. 33).
f. Ингибирование пролиферации
Очищенные методом FPLC химерные антитела по изобретению анализировали на их способность ингибировать рост клеток KATO-III, эндогенно экспрессирующих CLD18A2 человека.
Клетки мишени (KATO-III) культивировали в присутствии соответствующих химерных антител (см. ингибирование пролиферации антителами мыши, пример 7). Показано, что очищенные методом FPLC химерные антитела ch-163E12 и ch-166E2 ингибируют пролиферацию клеток.
Пример 10. Отбор антител в качестве кандидатов для клинической разработки
Идеальные клинические разработки могут охватывать широкий круг терапевтических и диагностических применений (также см. раздел IV - Применения и способы изобретения). Изобретением предусмотрены антитела против CLD18A2. Показано, что предусмотренные изобретением антитела обладают широким кругом свойств касательно специфичности, способности вызывать CDC и ADCC и ингибировать пролиферацию клеток, экспрессирующих CLD18, в частности раковых клеток. Кроме того, было показано, что химеризация антител может привести к приобретению дополнительных Fc-зависимых эффекторных функций, которых нет у исходных мышиных молекул. Например, в настоящем изобретении показано, что антитело 175D10 с IgG1 мыши не вызывает комплемент-зависимой цитотоксичности (см. Пример 5), тогда как ch-175D10 с IgG1 человека вызывает специфический лизис конститутивно экспрессирующих CLD18 раковых клеток (см. таблицу 5 и таблицу 6).
Предусмотренные настоящим изобретением антитела можно отнести к различным классам в соответствии с их свойствами связывания и способностью опосредовать эффекторные функции на клетках, экспрессирующих CLD18. Из предусмотренных настоящим изобретением антител можно отобрать кандидатов для клинической разработки на основании их функциональных характеристик. Общий обзор свойств отобранных мышиных и химерных антител по изобретению представлен в таблице 5 и таблице 6, соответственно.
Кандидаты для клинической разработки по изобретению могут обладать одним или несколькими из следующих свойств:
a) связывание с CLD18A2 человека, но не с CLD18A1 человека (напр., 43А11, 45С1, 125Е1, 163Е12, 166Е2 и 175D10, и ch-43A11, ch-45C1, ch-125E1, ch-163E12, ch-166E2 и ch-175D10). См. примеры на фиг. 6А и 6В.
b) связывание с CLD18A2 мыши, но не с CLD18A1 мыши (напр., 125Е1, 163Е12, 166Е2 и 175D10). См. примеры на фиг. 15А и 15В.
c) связывание с CLD18, естественным образом экспрессирующимся в раковых клетках (напр., (e.g. 45С1, 43А11, 125Е1, 163Е12, 166Е2 и 175D10, и ch-45C1, ch-43A11, ch-125E1, ch-163E12, ch-166E2 и ch-175D10). См. примеры на фиг. 13.
d) связывание с CLD18 в зонах межклеточных контактов (напр., 45С1, 43А11, 125Е1, 163Е12, 166Е2 и 175D10). См. примеры на фиг. 12А и 12В.
e) опосредование вызванной CDC гибели клеток, экспрессирующих CLD18 (напр., 45С1, 125Е1, 163Е12, 166Е2 и 175D10, и ch-163E12 и ch-175D10). См. примеры на фиг. 32.
f) опосредование вызванной ADCC гибели клеток, экспрессирующих CLD18 (напр., ch-163E12 и ch-175D10). См. примеры на фиг. 33.
g) ингибирование пролиферации клеток, экспрессирующих CLD18 (напр., 45С1, 125Е1, 163Е12, 166Е2 и 175D10, и ch-163E12 и ch-166E2).
h) ингибирование роста опухолей на модели ксенотрансплантатов с клетками, экспрессирующими CLD18 (напр., 43А11, 125Е1, 163Е12, 166Е2 и 175D10). См. примеры на фиг. 24.
i) продление срока жизни на модели ксенотрансплантатов с клетками, экспрессирующими CLD18 (напр., 43А11, 125Е1, 163Е12, 166Е2 и 175D10). См. примеры на фиг. 25В.
Обзор типичных свойств для отбора кандидатов для разработки
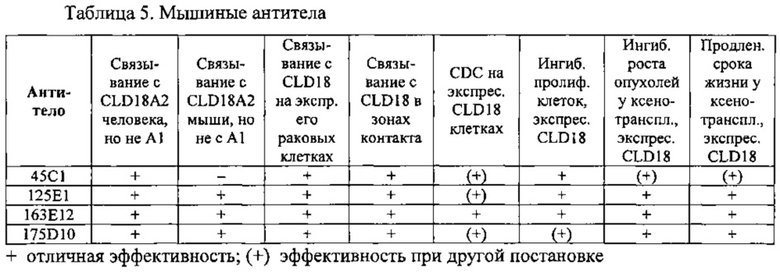
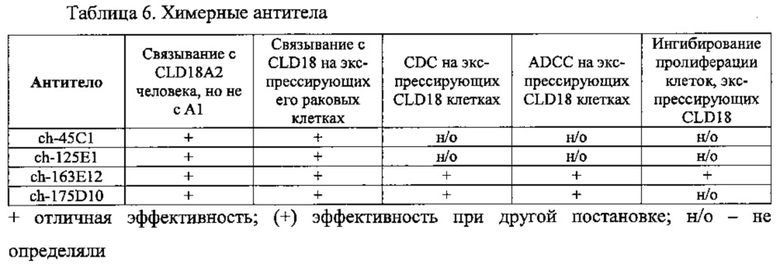
Пример 11. Анализ эпитопов
Картирование эпитопов, распознаваемых антителами изобретения, может проводиться так, как описано подробно в "Epitope Mapping Protocols (Methods in Molecular Biology) by Glenn E. Morris ISBN-089603-375-9; и в "Epitope Mapping: A Practical Approach", Practical Approach Series, 248 by Olwyn M.R. Westwood, Frank C. Hay.
Вкратце, для картирования эпитопов можно создать подборку пептидов из синтетических перекрывающихся пептидов (полученных методом SPOT-синтеза), происходящих из аминокислотной последовательности антигена. Мембрану с пептидной картой отмывают с помощью TBS, блокируют смесью 10% молоко/Tween 20-TBS и инкубируют с антителами изобретения, конъюгированными с пероксидазой, в течение ночи при 4°С, разбавляют смесью 5% молоко/Tween 20-TBS, а затем отмывают Tween20-TBS и TBS, проявляют, напр., с помощью ECL Lumi-Light (Roche) и детектируют на Lumi Imager.
a. Молекулярный анализ эпитопов
Первый внеклеточный домен (ECD1) CLD18 человека проявляет высокую степень гомологии между двумя изоформами, причем различия между ними заключаются только в 8 положениях аминокислотной последовательности.
Были отобраны моноклональные антитела, которые избирательно распознают только специфичную для желудка изоформу CLD18A2 (см. пример 1). Для того, чтобы определить критические аминокислоты из тех, по которым отличаются две изоформы, в белках CLD18 делали аминокислотные замены путем замены аминокислот у одной изоформы аминокислотами, находящимися в соответствующих положениях у другой изоформы. Конкретно, было создано 8 вариантов, у каждого из которых в домене ECD1 CLD18A2 одна из восьми аминокислот, отличающихся от аминокислотной последовательности CLD18A1, была заменена аминокислотой, находящейся в соответствующем положении у CLD18A1. Были созданы 3 варианта, у каждого из которых 2 аминокислоты были заменены аминокислотами, находящимися в соответствующих положениях у CLD18A1: вторая и третья, третья и четвертая, четвертая и пятая аминокислоты из тех 8 аминокислот. Было создано 11 соответствующих конструкций и для другой изоформы - CLD18A1, путем замены соответствующих аминокислот у CLD18A1 аминокислотами, находящимися у CLD18A2.
Измененные белки CLD18 создавали путем мутагенеза нуклеиновой кислоты, кодирующей соответствующую изоформу CLD18, и клонирования мутантных нуклеиновых кислот в стандартный экспрессирующий вектор.
Снижение связывания исследуемых антител с полученными вариантами CLD18A2 и повышение связывания с полученными вариантами CLD18A1 наблюдали методом проточной цитометрии. При анализе также включали немодифицированные CLD18A1 и CLD18A2 дикого типа.
Для этого клетки HEK293 временно трансфицировали нуклеиновыми кислотами, кодирующими CLD18A1 или CLD18A2 дикого типа либо их мутантные варианты, получая клетки, экспрессирующие CLD18A1 или CLD18A2 человека. Трансфектантов инкубировали с исследуемыми антителами изобретения и анализировали характеристики связывания методом проточной цитометрии.
Моноклональное антитело мыши 44E4D3F11 (182-D1106-179, IgG2a, κ) распознает и CLD18A1, и CLD18A2 на поверхности клеток. Антитело ch-175D10 проявляло сильное специфическое связывание с CLD18A2 дикого типа (см. таблицу 7). Антитело ch-175D10 не связывается с вариантами CLD18A2 3, 4 и 6, содержащими следующие замены аминокислот: вариант 3: A42S; вариант 4: N45Q; вариант 6: E56Q. Также не наблюдалось связывания с двойными вариантами CLD18A2, содержащими по меньшей мере одну из одинарных замен аминокислот вариантов 3 и 4.
b. Картирование эпитопов методом пептидного сканирования
Для того, чтобы идентифицировать и картировать эпитоп, распознаваемый антителами изобретения, создавали подборку пептидов (peptide scan) из синтетических перекрывающихся пептидов (полученных методом SPOT-синтеза), происходящих из аминокислотной последовательности первого внеклеточного домена CLD18A2. Все последовательности антигена синтезировали на фирме Jerini AG, Berlin, Германия, в виде линейных 15-мерных пептидов (с перекрыванием 11 аминокислот), а затем тестировали на связывание с антителами изобретения. Кроме того, все цистеины линейных пептидов заменяли на серии с тем, чтобы избежать образования дисульфидных связей между пептидами. Химерные моноклональные антитела по изобретению конъюгировали с пероксидазой согласно инструкциям изготовителя (Pierce, набор EZ-Link Plus Activated Peroxidase Kit) и инкубировали с подборкой пептидов. Специфическое распознавание эпитопа CLD18A2 наблюдали по люминесценции. В таблице 8 представлена интенсивность связывания химерных моноклональных антител ch-175D10 и ch-163E12 с синтетическими пептидами, происходящими из аминокислотной последовательности первого внеклеточного домена CLD18A2.

Оба антитела ch-175D10 и ch-163E12 распознают дискретный (конформационный) эпитоп по меньшей мере с двумя центрами связывания, свидетельствуя, что ключевые аминокислотные остатки распределены по двум или нескольким участкам связывания, которые разделены в первичной структуре белка. После свертывания эти связывающие участки соединяются на поверхности белка с образованием составного эпитопа. Сильное связывание антитела ch-175D10 с пептидами 1 и 7 без замены цистеина, но слабое связывание с пептидом 7, содержащим серины вместо двух цистеинов, свидетельствует о центральной роли цистеинов для распознавания эпитопа и, вероятно, свертывании белка (фиг. 36). Наши данные предполагают три различные модели свертывания белка для первого внеклеточного домена CLD18A2, содержащего эпитоп для обеих химерных антител (фиг. 37). В первой модели, приведенной на фиг. 37, представлен линейный пептид 7, содержащий оба цистеина, во второй модели приведена внутримолекулярная дисульфидная связь, приводящая к образованию петли, а в третьей модели приведены два цистеина, образующие две межмолекулярные дисульфидные связи.
Пример 12. Определение аффинности антител
Для определения констант связывания по методу Скэтчарда можно протитровать связывание антител изобретения с CLD18A2 человека на клетках HEK293, устойчиво экспрессирующих CLD18A2, методом проточной цитометрии. Человеческие или химерные антитела по изобретению можно детектировать методом "сэндвич"-ELISA с неконъюгированными антителами мыши против IgG человека и конъюгированными с FITC козьими антителами против IgG мыши. Каждая стадия инкубации антител проводится в течение 30 мин при 4°С с последующими 2 отмывками буфером для FACS. Мышиные антитела по изобретению детектируют непосредственно с помощью вторичного козьего антитела против мыши, конъюгированного с FITC. Для количественного определения связавшихся антител по изобретению может потребоваться детектирование методом "сэндвича" с использованием вторичных и третичных антител с помощью набора QIFIKIT (DAKO, Glostrup, Дания). С помощью этого набора количество связавшихся антител определяется методом проточной цитометрии согласно инструкциям изготовителя. Должна получиться строго линейная зависимость между средней интенсивностью флуоресценции и связанным IgG. Данные анализируют построением графиков Скэтчарда и определяют KD непосредственно из кривых связывания. Константы диссоциации можно рассчитать согласно Krause et al., Behring Inst. Mitt. 87: 56-67, 1990; и Nauendorf et al., Int J Cancer 100:101-120, 2002.
В соответствии с изобретением, константы диссоциации для антител изобретения определяли по связыванию методом проточной цитометрии, используя клетки HEK293-CLD18A2, устойчиво экспрессирующие CLD18A2. Анализ данных по связыванию с клетками методом Скэтчарда дал константы диссоциации в интервале от 10-8 М до 10-9 М для мышиных и химерных антител 175D10 и 163Е12. Константы диссоциации рассчитывали согласно Krause et al., Behring Inst. Mitt. 87: 56-67, 1990; и Nauendorf et al., Int J Cancer 100:101-120, 2002.
Пример 13. Ортологическая перекрестная реактивность
Связывание с CLD18A2 и CLD18A1 анализировали методом проточной цитометрии. Клетки HEK293, временно котрансфицированные флуоресцентным маркером и CLD18A2 мыши (SEQ ID NO: 33, 35) или флуоресцентным маркером и CLD18A1 мыши (SEQ ID NO: 36, 37) либо флуоресцентным маркером и CLD18A2 человека (SEQ ID NO: 1, 2) или флуоресцентным маркером и CLD18A1 человека (SEQ ID NO: 7, 8) инкубировали с ch-175D10, ch-163E12 и ch-125E1 в течение 30 мин при 4°С, после чего инкубировали с конъюгированным с аллофикоцианином вторичным антителом против IgG человека (30 мин, 4°С).
На фиг. 38 представлен профиль связывания для антител ch-175D10, ch-163E12 и ch-125E1. Эти антитела являются ценными инструментами для определения потенциальной токсичности моноклональных антител к CLD18 в доклинических исследованиях, как это описано в Примере 3j для их мышиных прототипов.
Пример 14. CLD18A2 проявляет высокую экспрессию на плазматической мембране в первичных опухолях желудка и метастазах рака желудка
Неизбирательные образцы первичного рака желудка и метастазов рака желудка (опухолей Крукенберга и лимфатических узлов) окрашивали с помощью специфичной к GC182 антисыворотки кролика. Иммуногистохимию, а также оценку интенсивности окрашивания (нет, слабая =1, средняя =2, сильная =3) и доли раковых клеток, проявляющих окрашивание плазматической мембраны (0-100%), выполняли профессиональные патологоанатомы; см. фиг. 39. На фиг. 39 каждый кружочек представляет независимый образец опухоли. Наблюдалось статистически значимое повышение интенсивности окраски в метастазах (р=0,034, точный критерий Фишера).
| название | год | авторы | номер документа |
|---|---|---|---|
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ КЛАУДИНА-18 ДЛЯ ЛЕЧЕНИЯ РАКА | 2008 |
|
RU2571923C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ С ИСПОЛЬЗОВАНИЕМ АНТИТЕЛ К КЛАУДИНУ 18.2 ДЛЯ ЛЕЧЕНИЯ РАКА | 2013 |
|
RU2789478C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ С ИСПОЛЬЗОВАНИЕМ АНТИТЕЛ К КЛАУДИНУ 18.2 ДЛЯ ЛЕЧЕНИЯ РАКА | 2013 |
|
RU2662066C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ С ИСПОЛЬЗОВАНИЕМ АНТИТЕЛ К КЛАУДИНУ 18.2 ДЛЯ ЛЕЧЕНИЯ РАКА | 2013 |
|
RU2665321C2 |
| АНТИТЕЛО ПРОТИВ КЛАУДИНА 18А2 И ЕГО ПРИМЕНЕНИЕ | 2017 |
|
RU2793445C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ С ИСПОЛЬЗОВАНИЕМ АНТИТЕЛ ПРОТИВ КЛАУДИНА 18.2 ДЛЯ ЛЕЧЕНИЯ РАКА | 2014 |
|
RU2699549C2 |
| КОНЪЮГАТЫ ЛЕКАРСТВЕННЫХ СРЕДСТВ, СОДЕРЖАЩИЕ АНТИТЕЛА ПРОТИВ КЛАУДИНА 18.2 | 2016 |
|
RU2841168C2 |
| АНТИТЕЛА ПРОТИВ АЛЬФА5-БЕТА 1 И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2528736C2 |
| ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ РАКА, ВКЛЮЧАЮЩАЯ АНТИТЕЛА ПРОТИВ КЛАУДИНА 18.2 | 2014 |
|
RU2678700C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ АНТИТЕЛО К ФОСФОЛИПАЗЕ D4 | 2014 |
|
RU2709741C2 |



















































































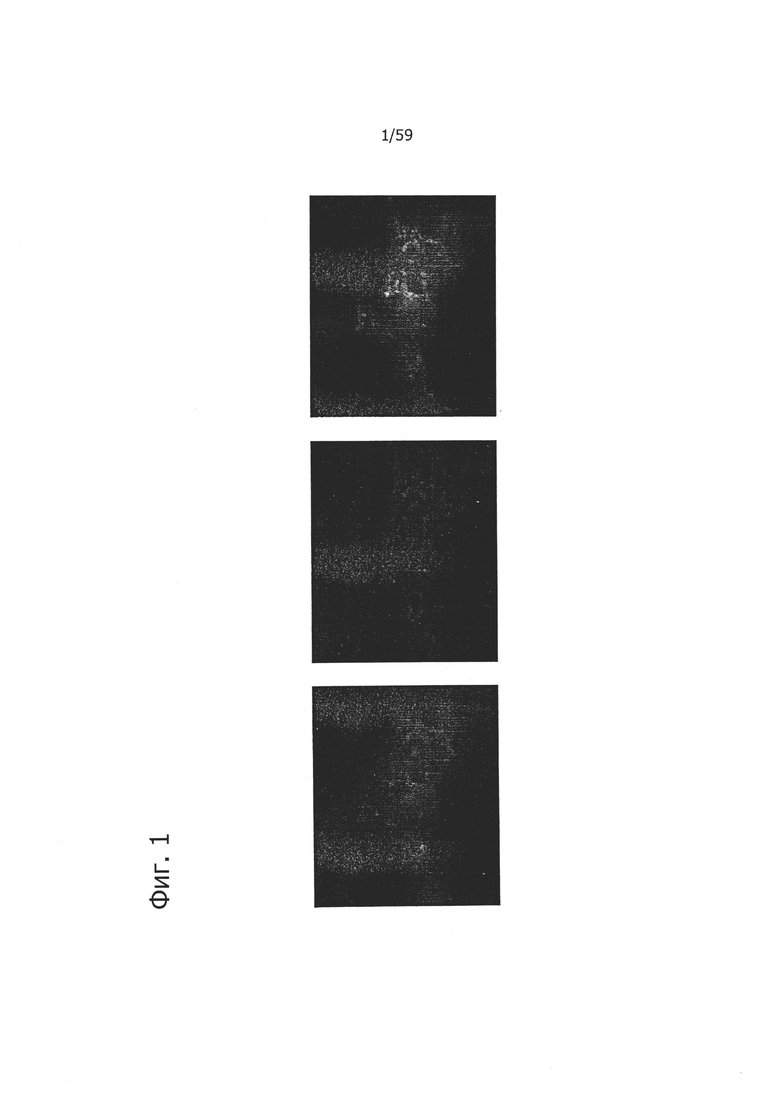
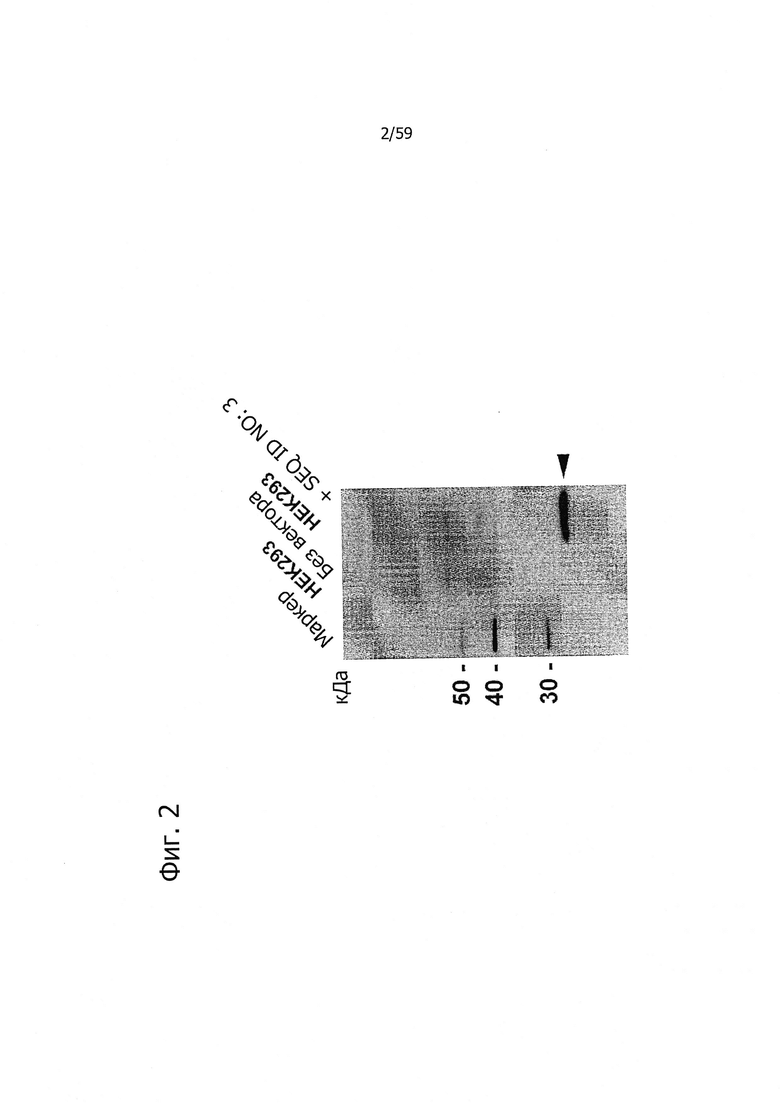


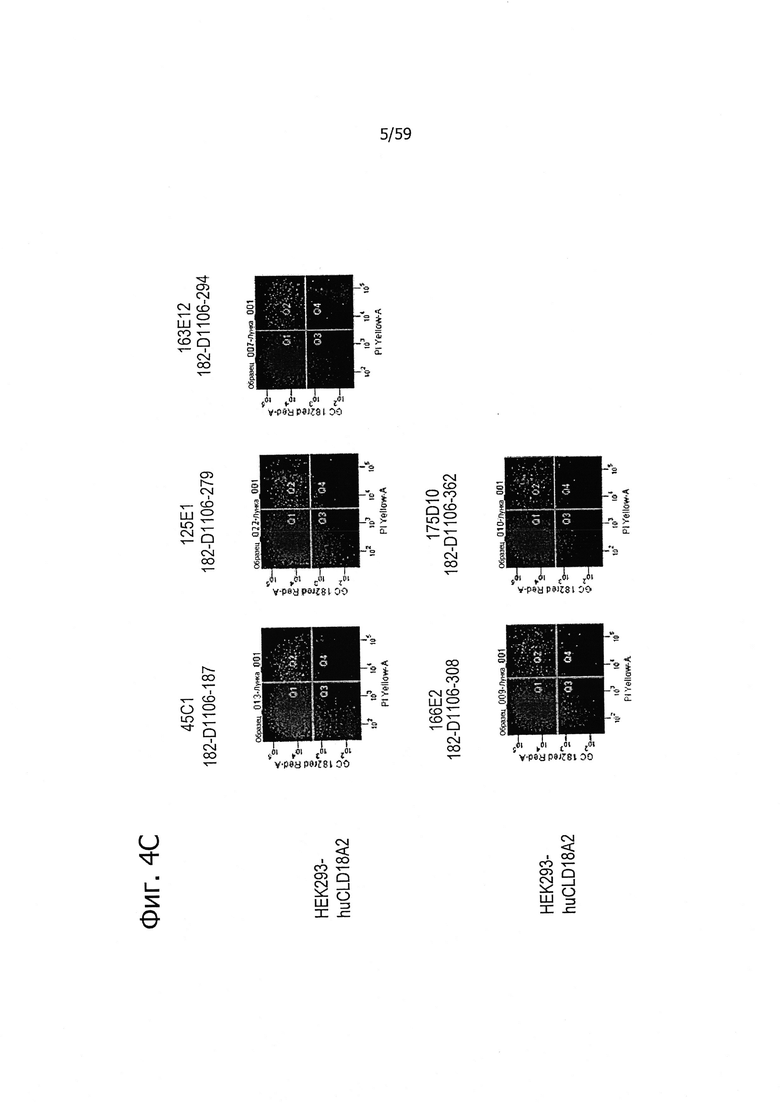
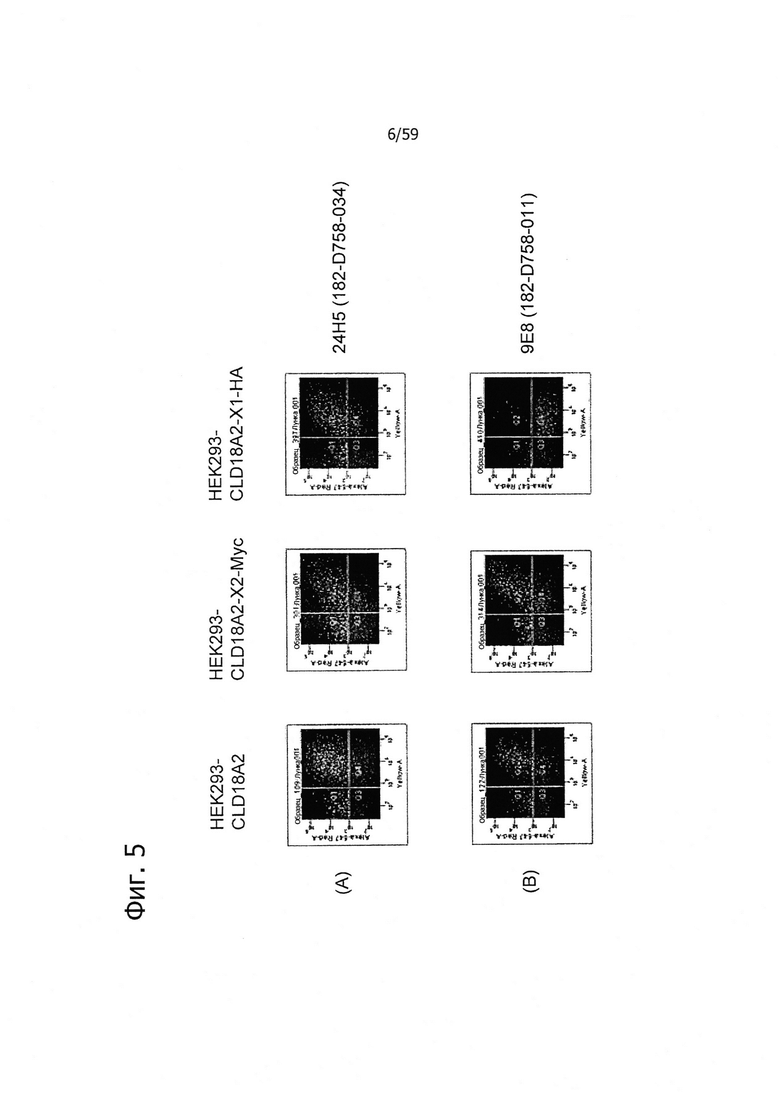
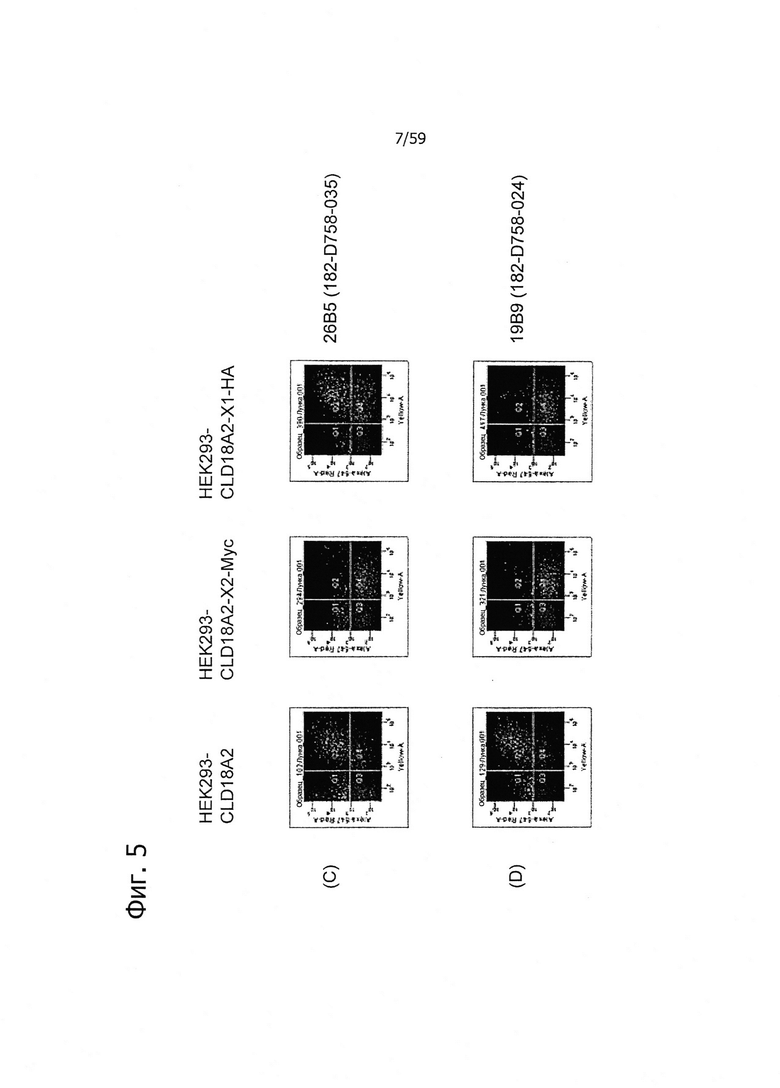
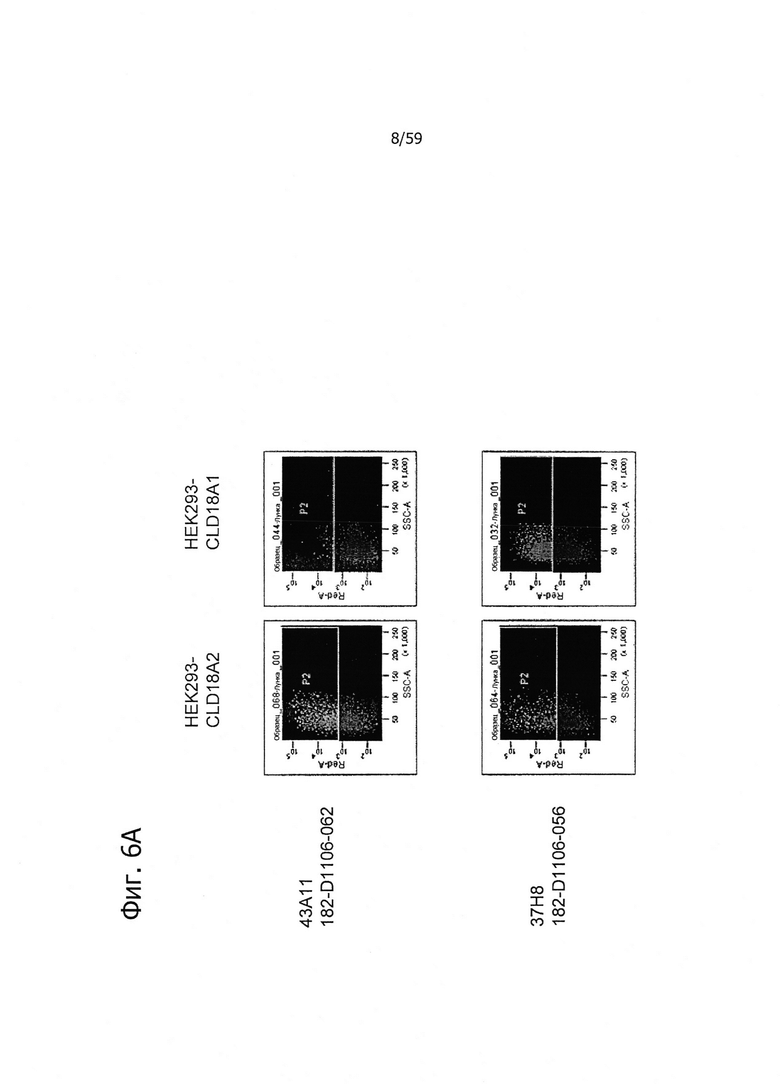




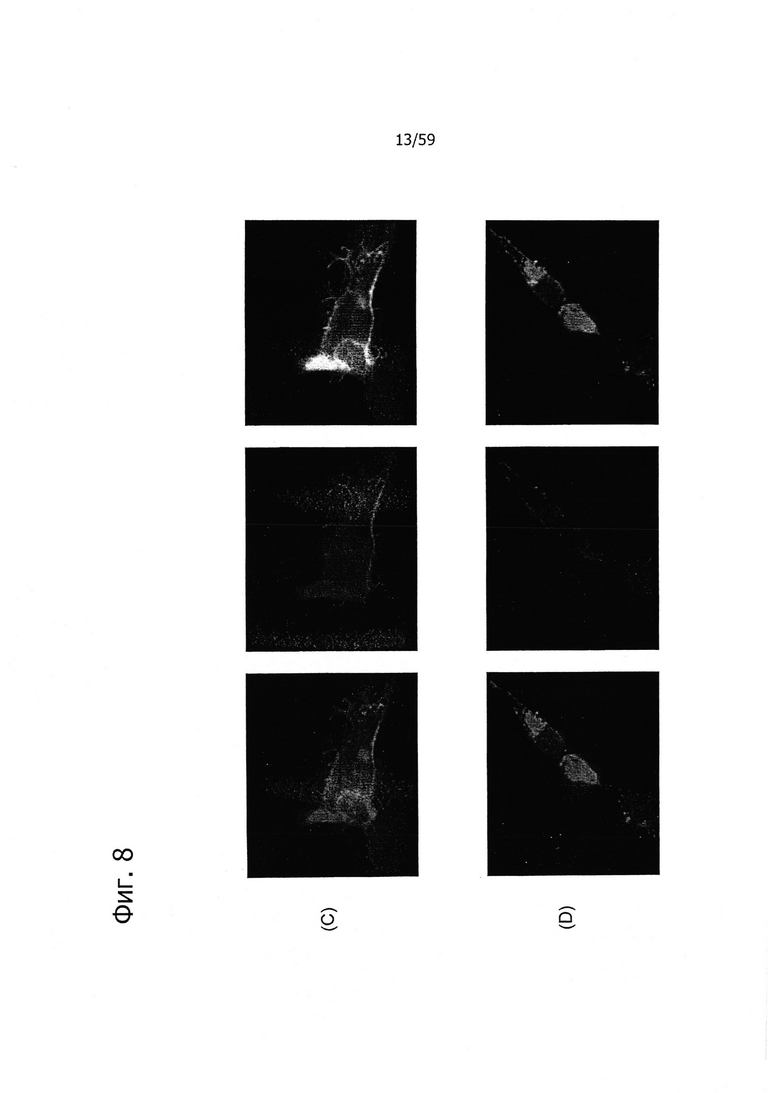
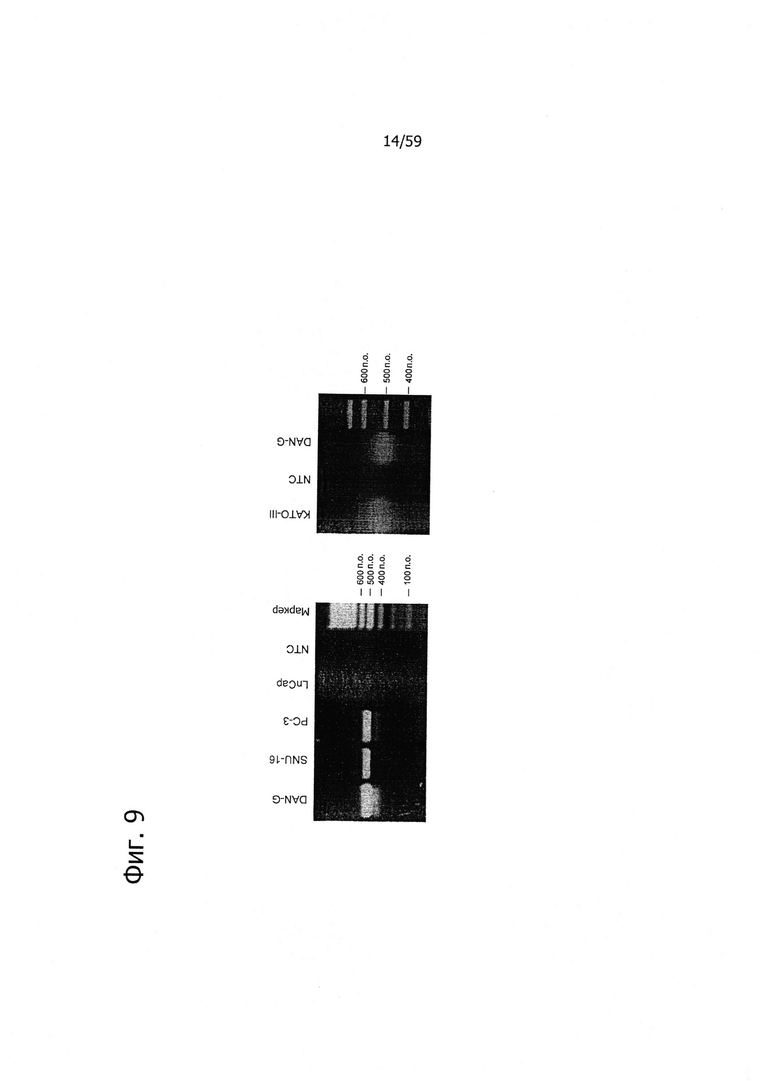



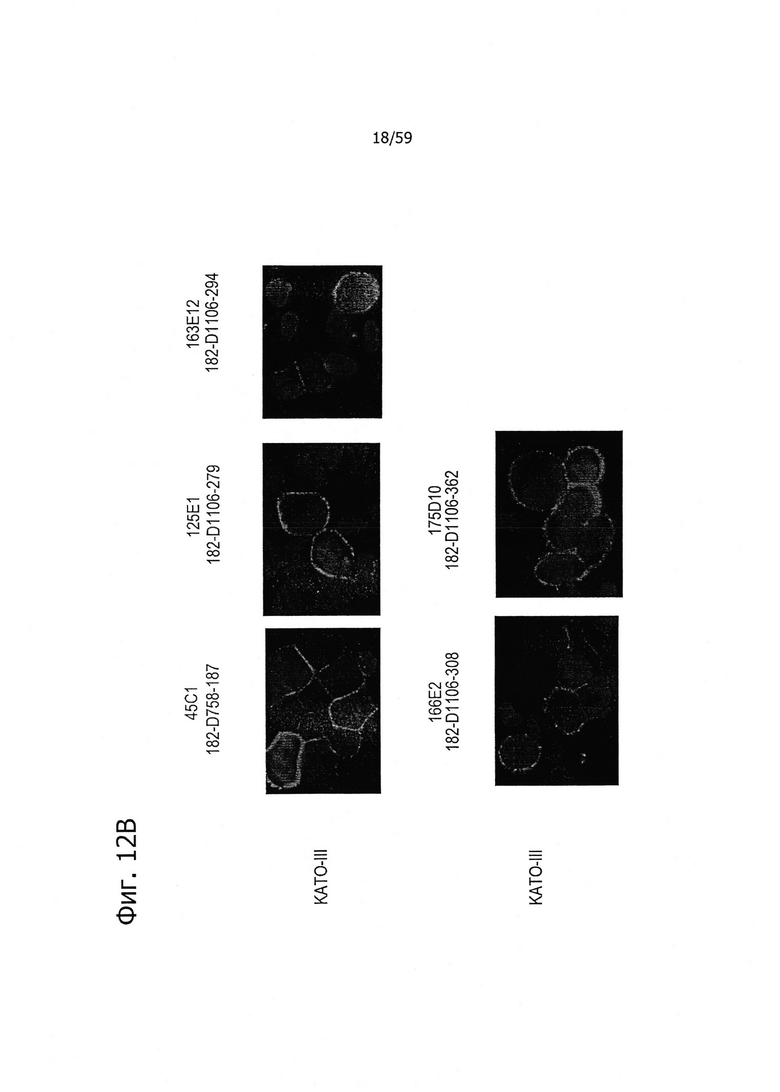


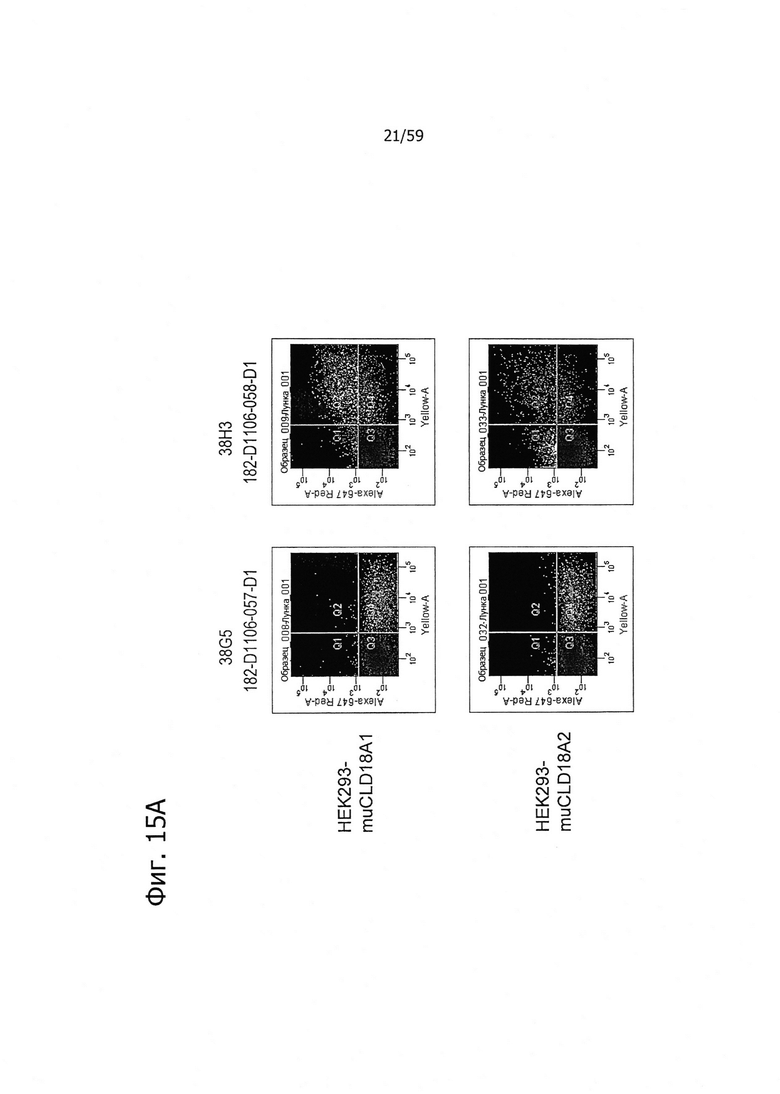

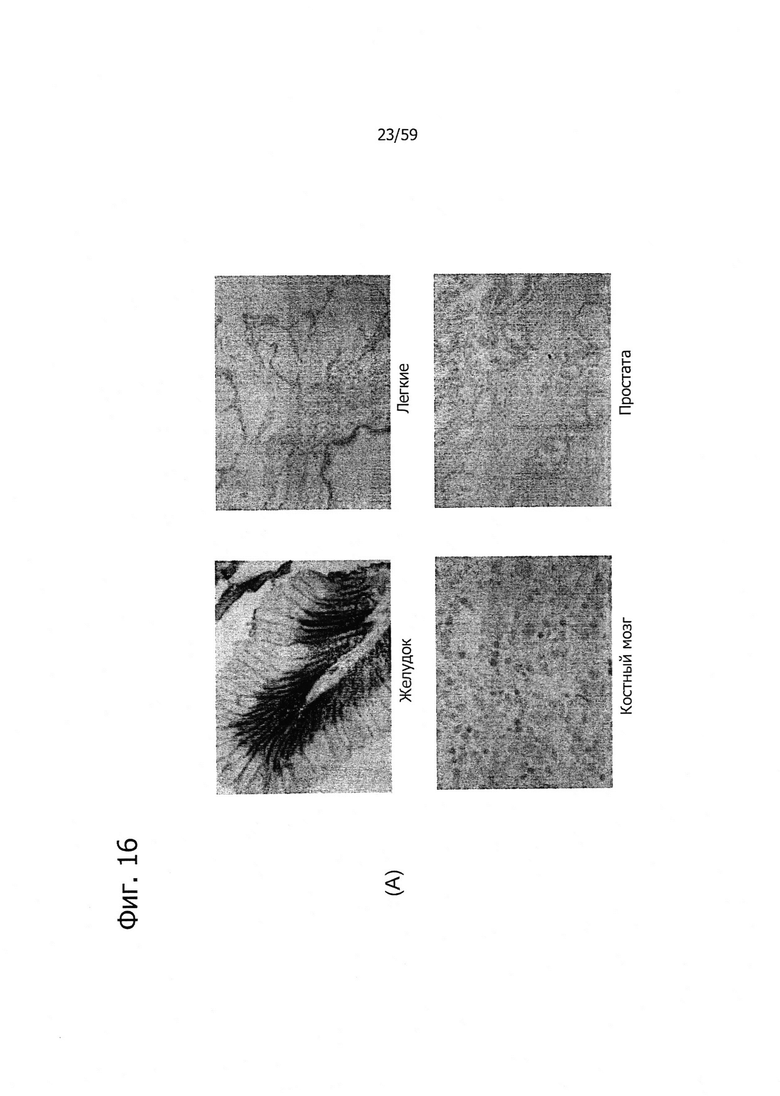
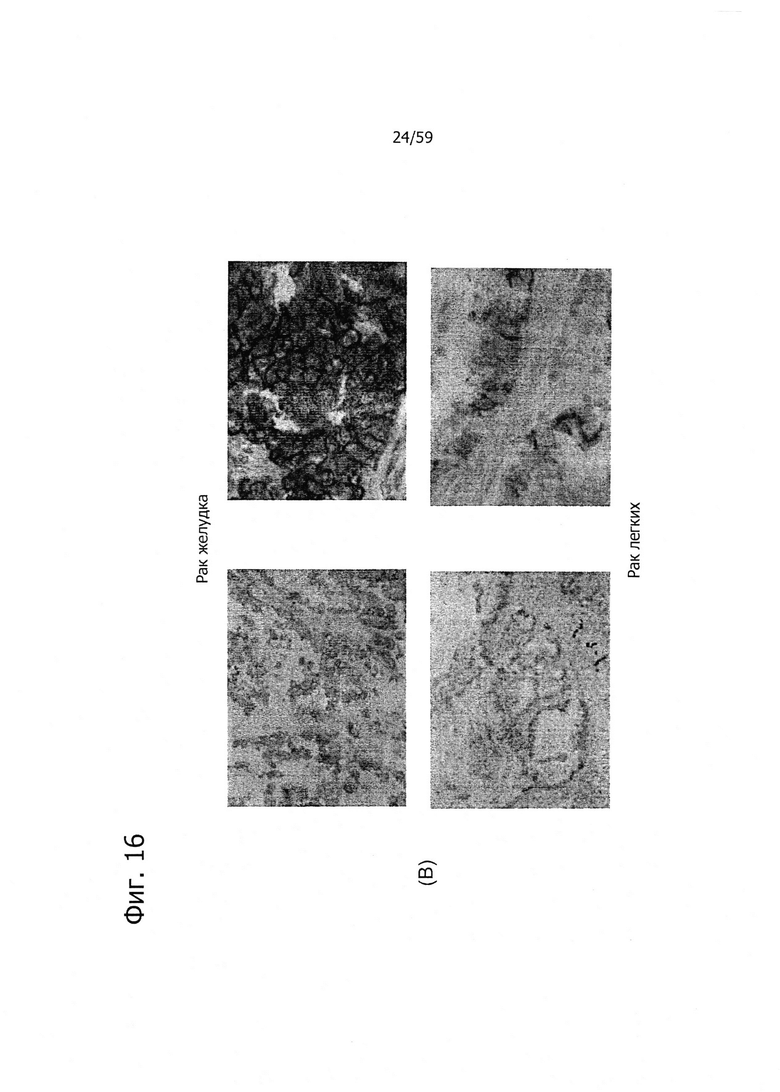



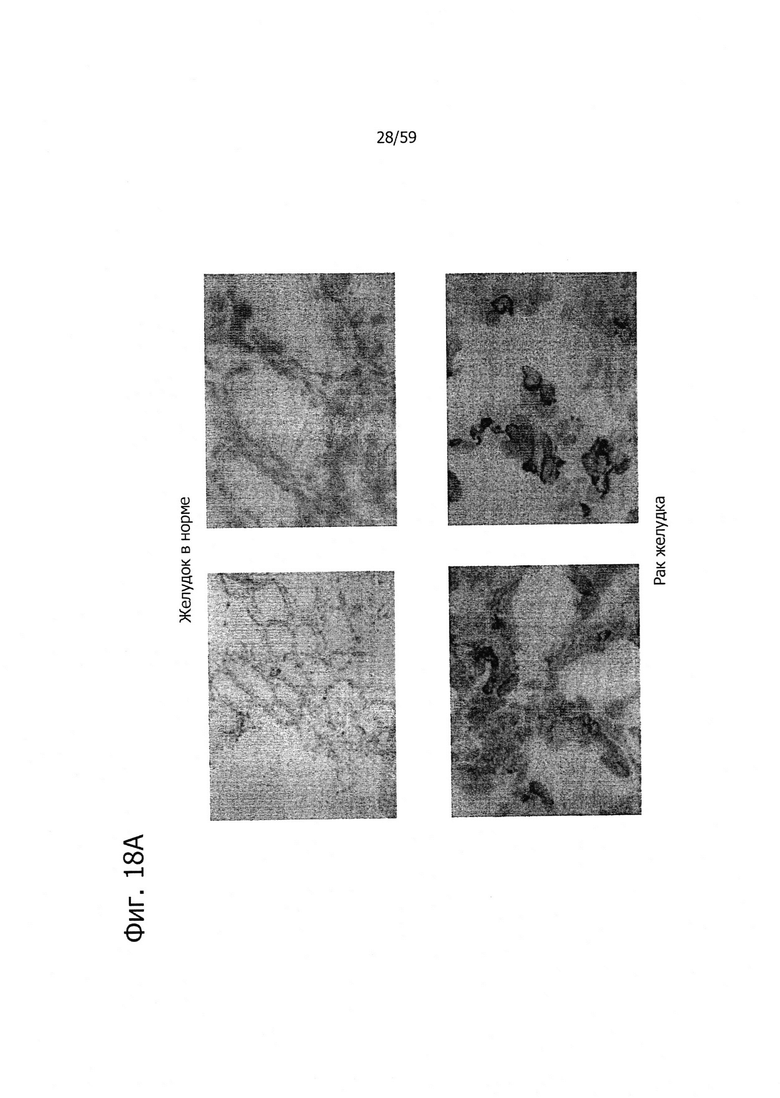




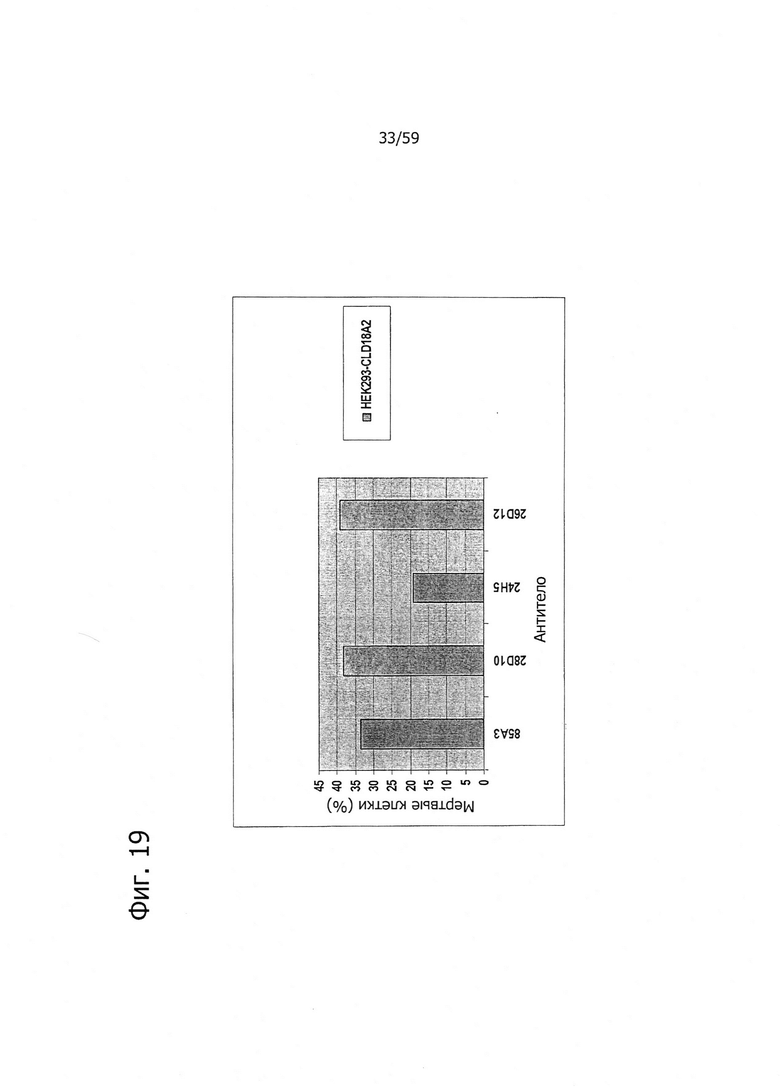
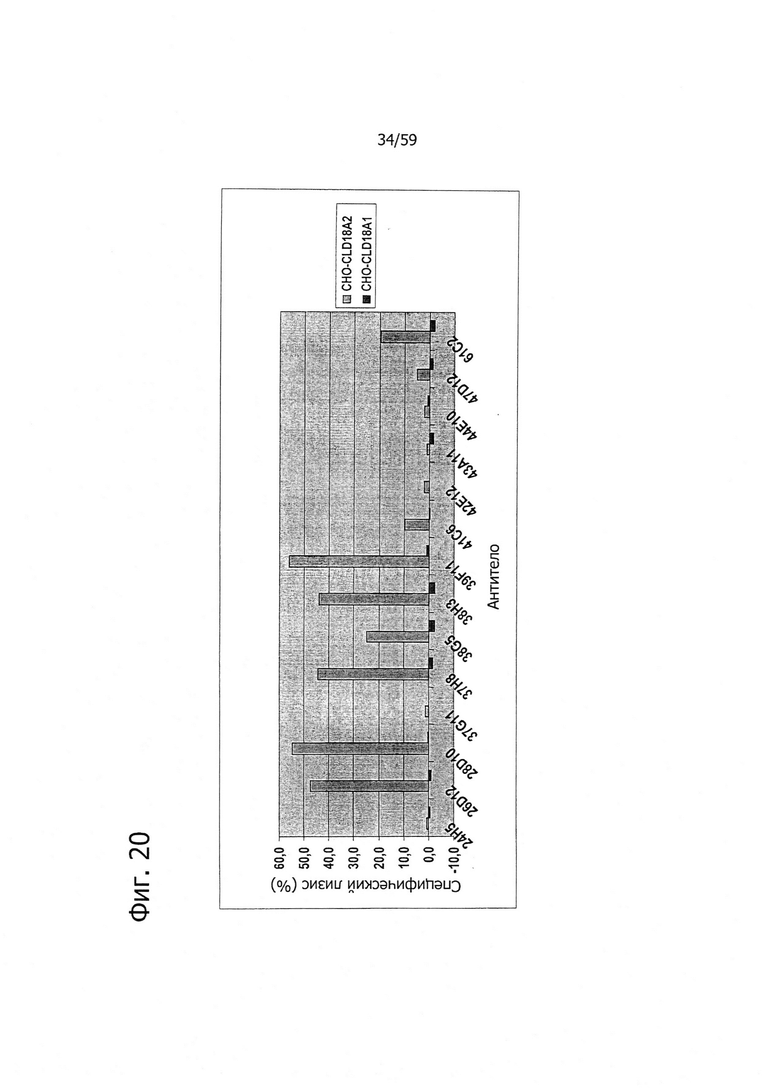
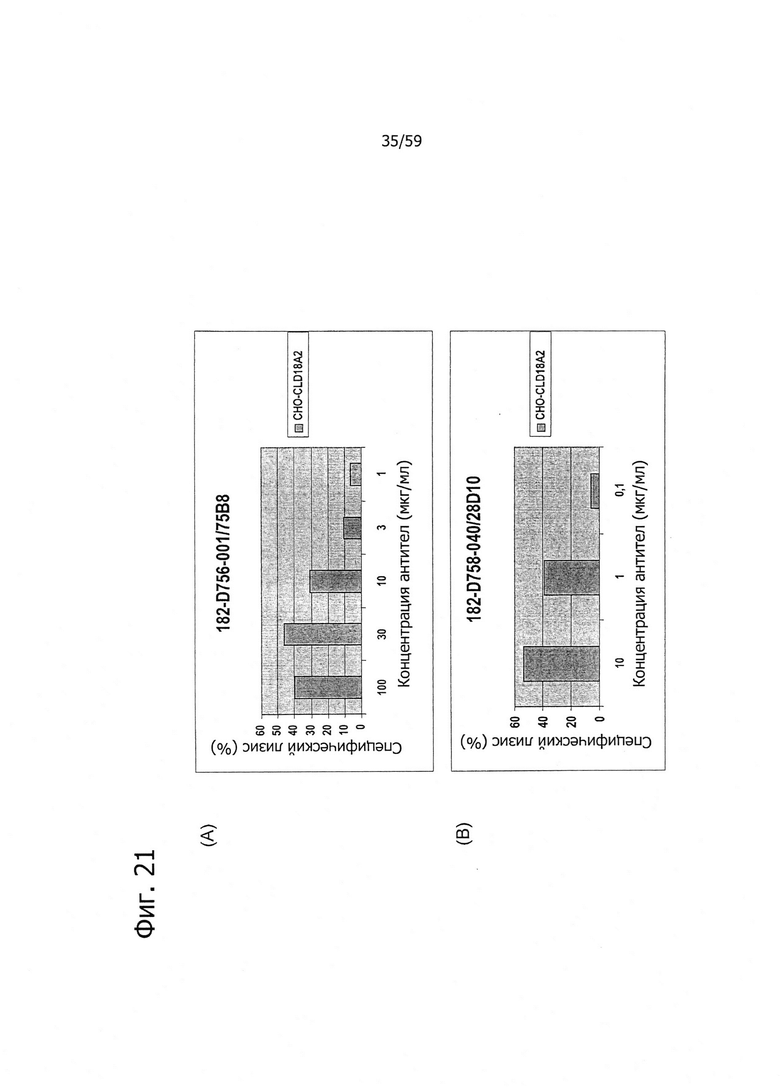

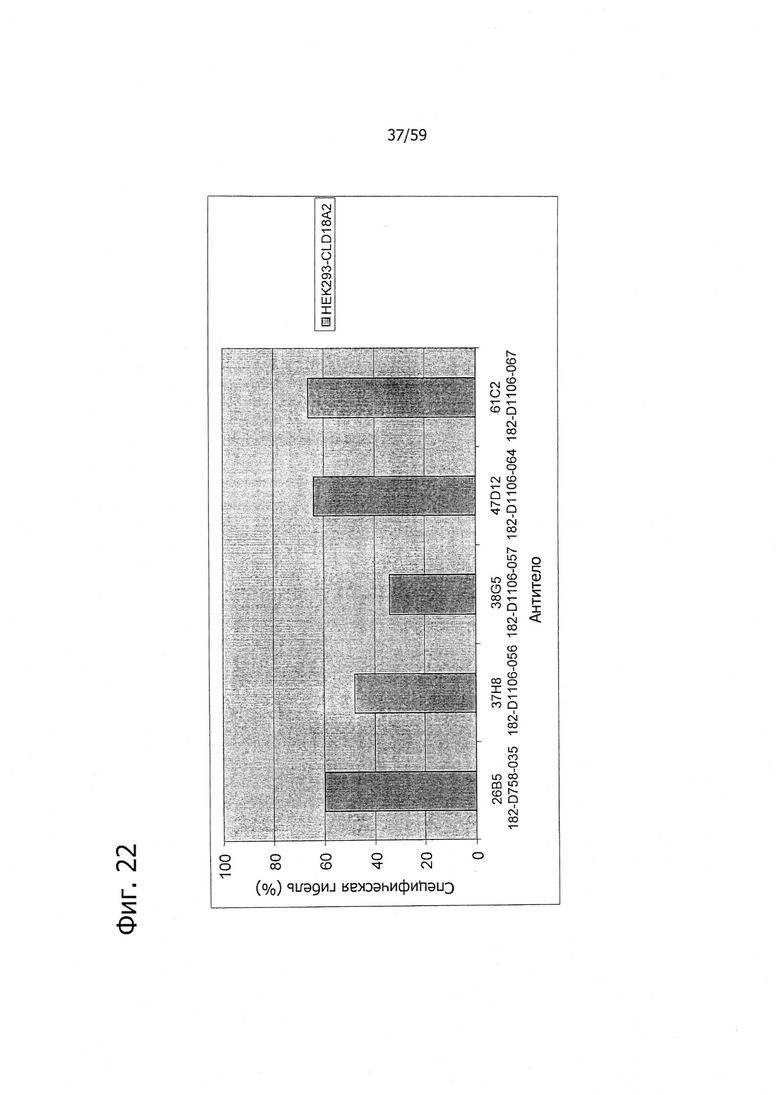
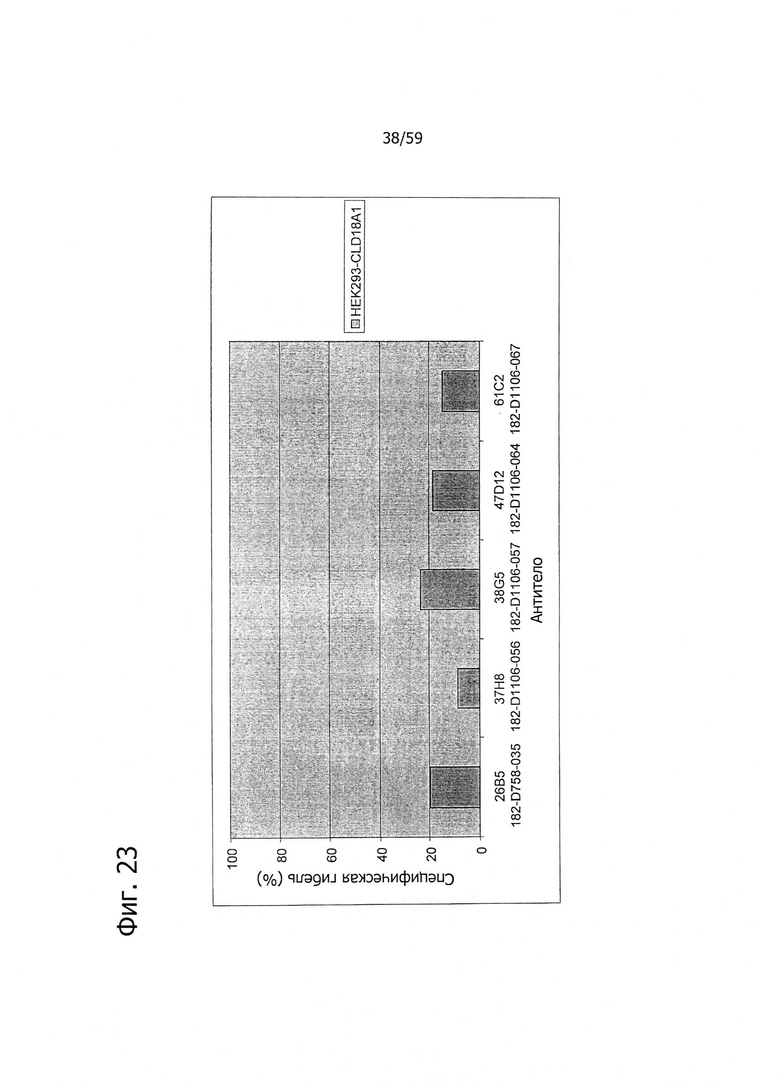
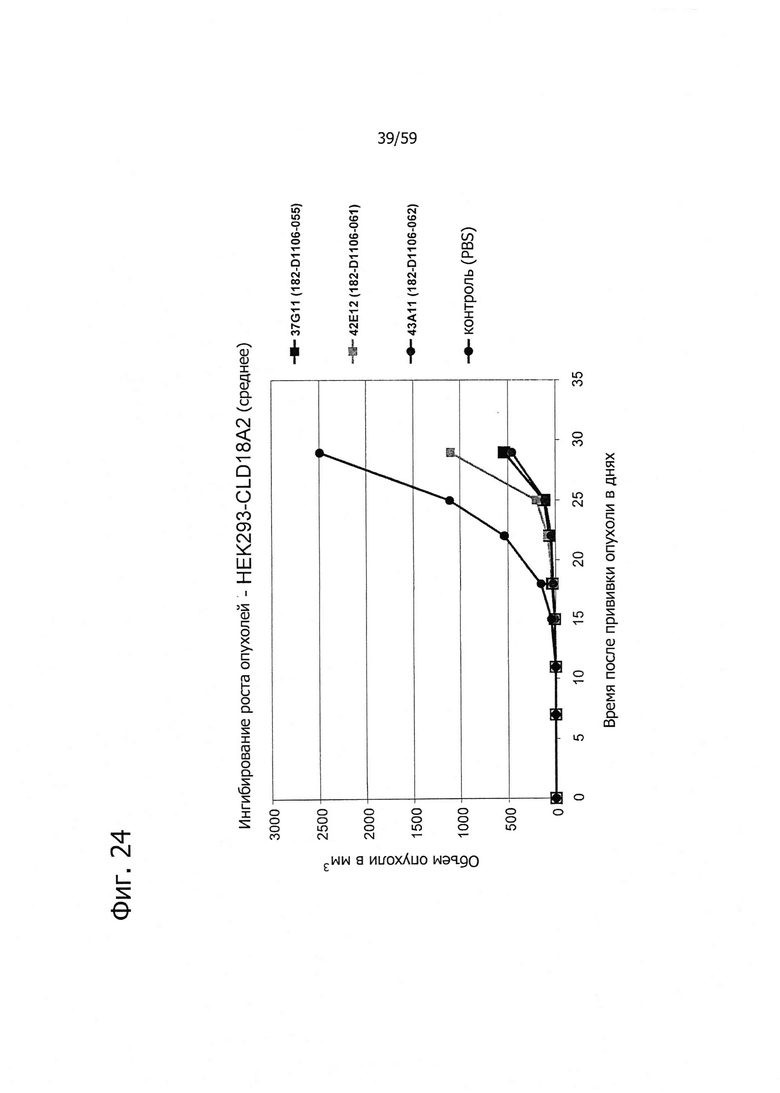
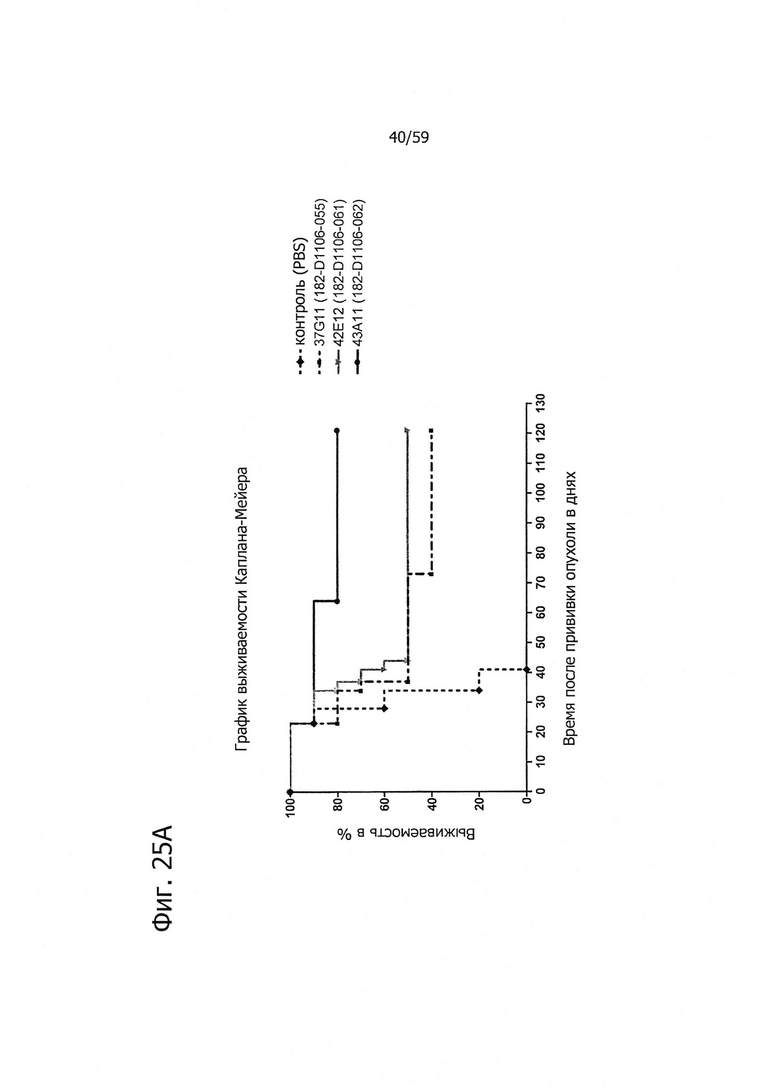
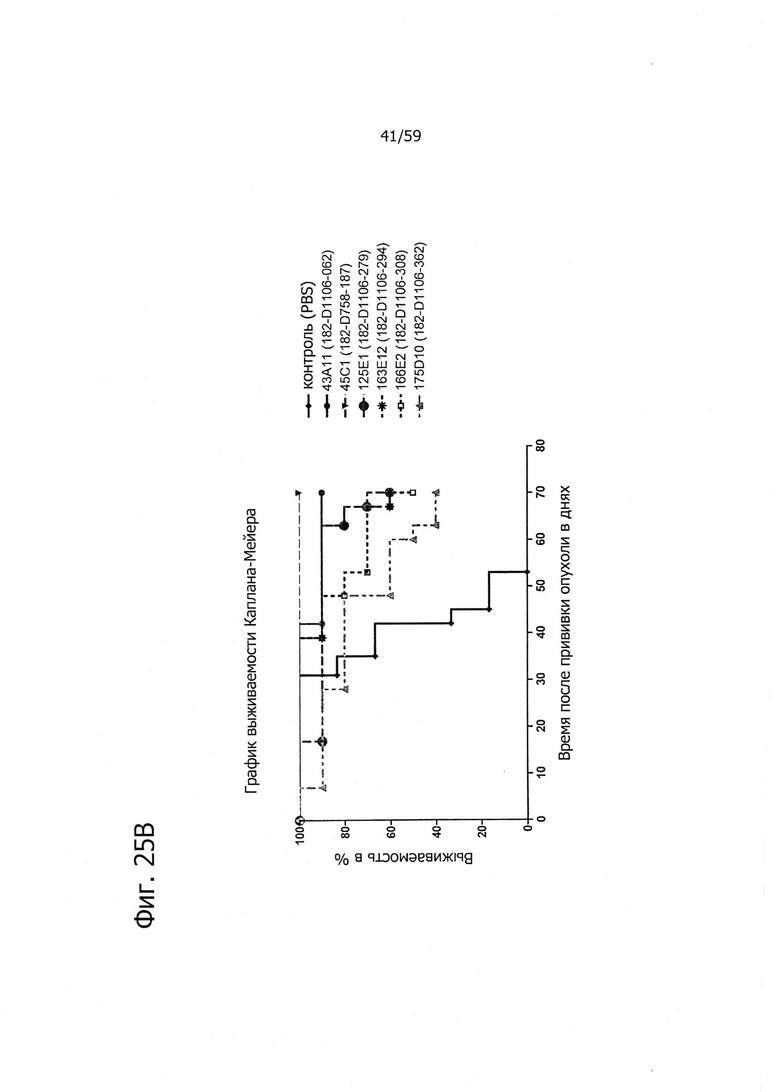
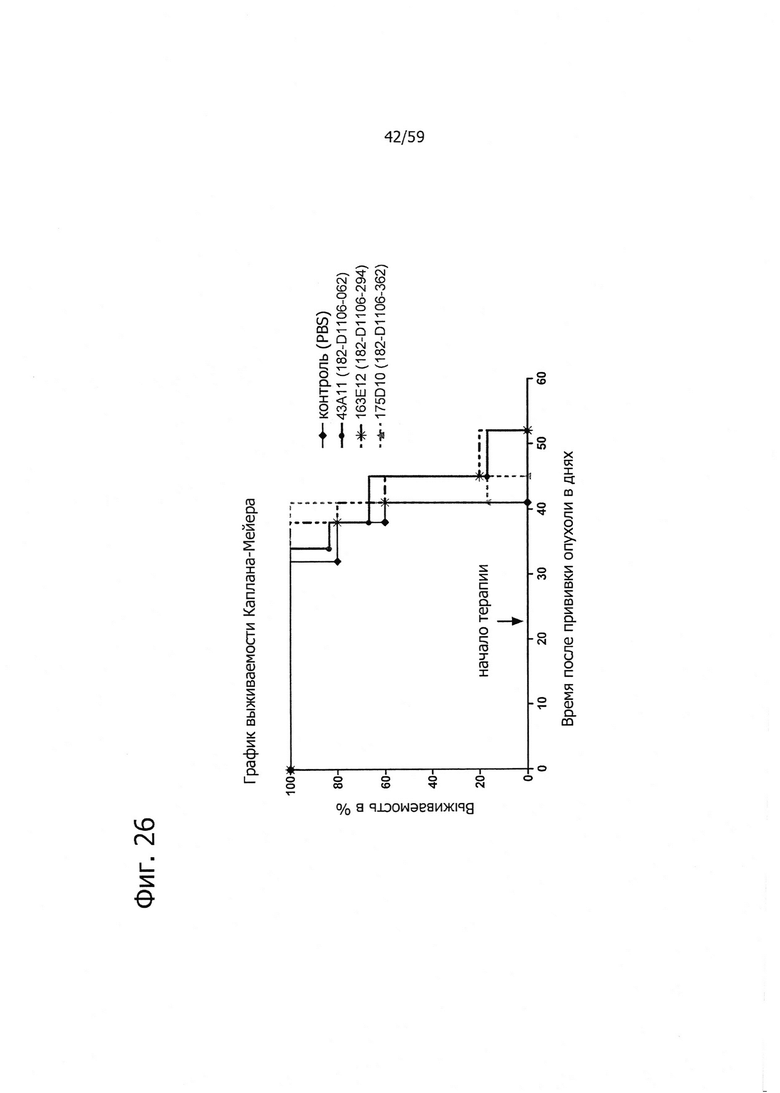
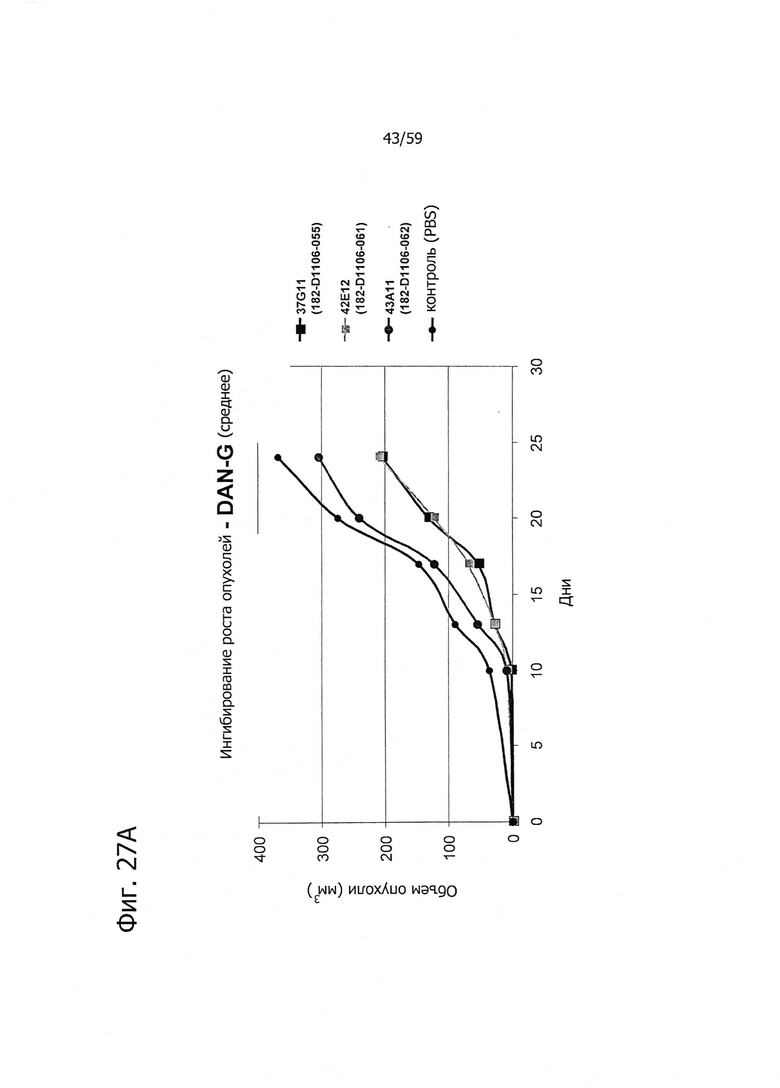
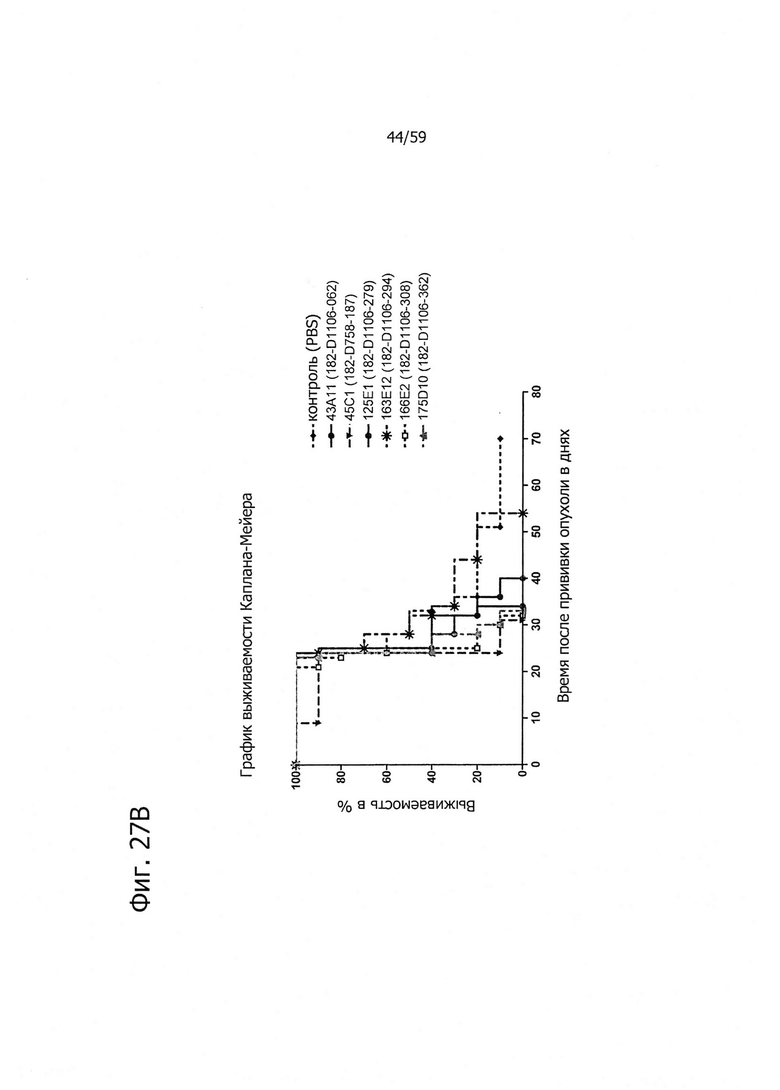






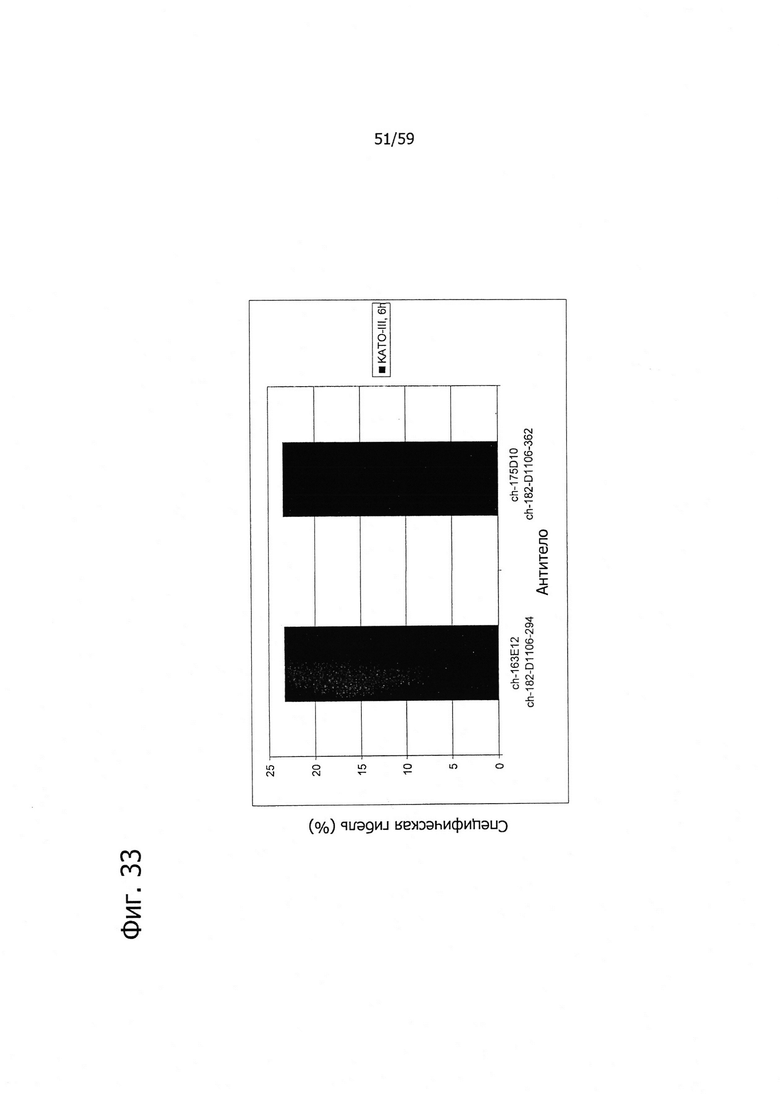
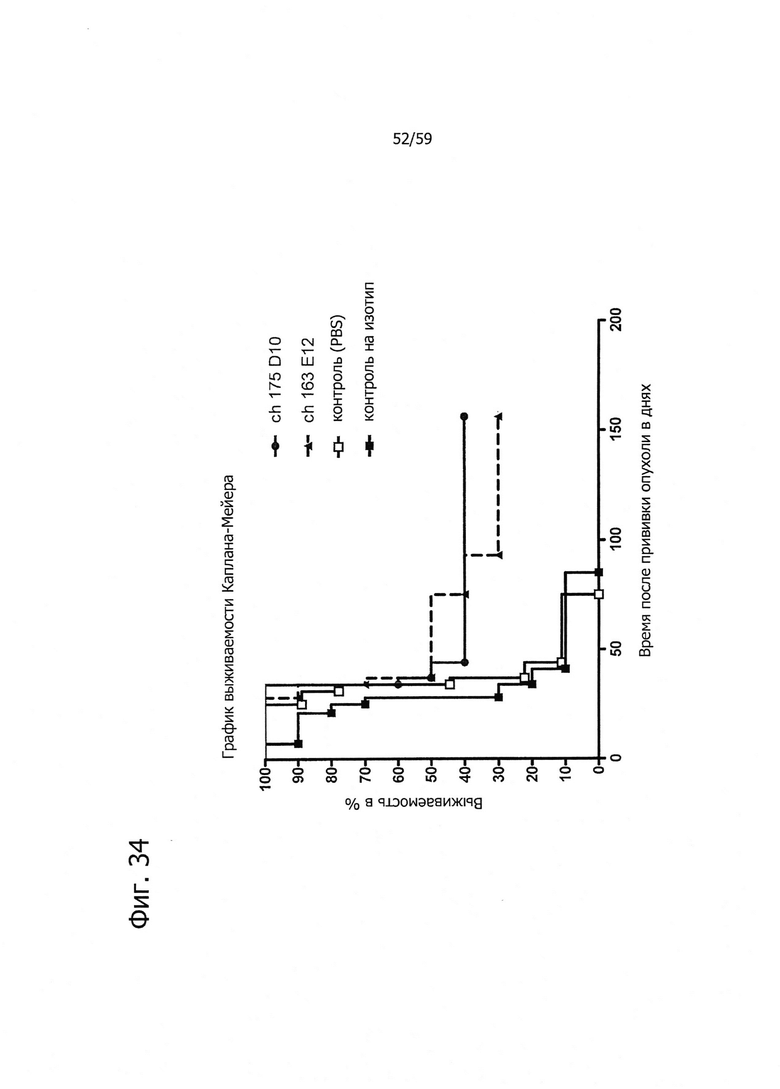
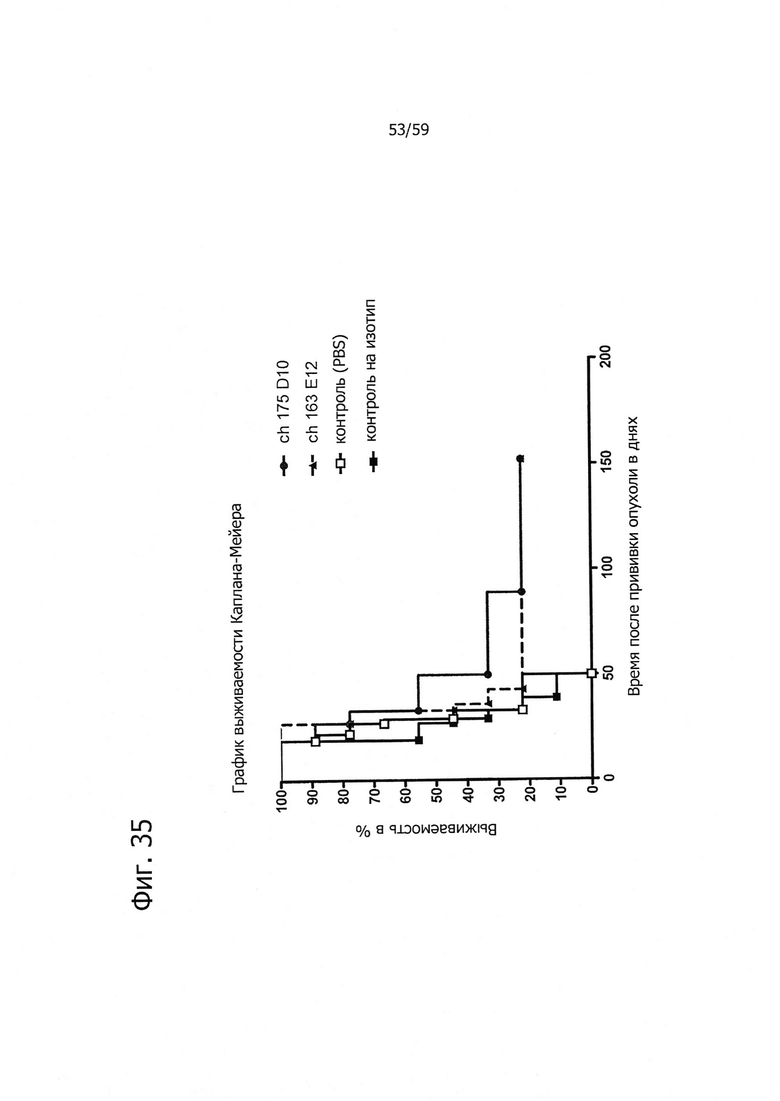
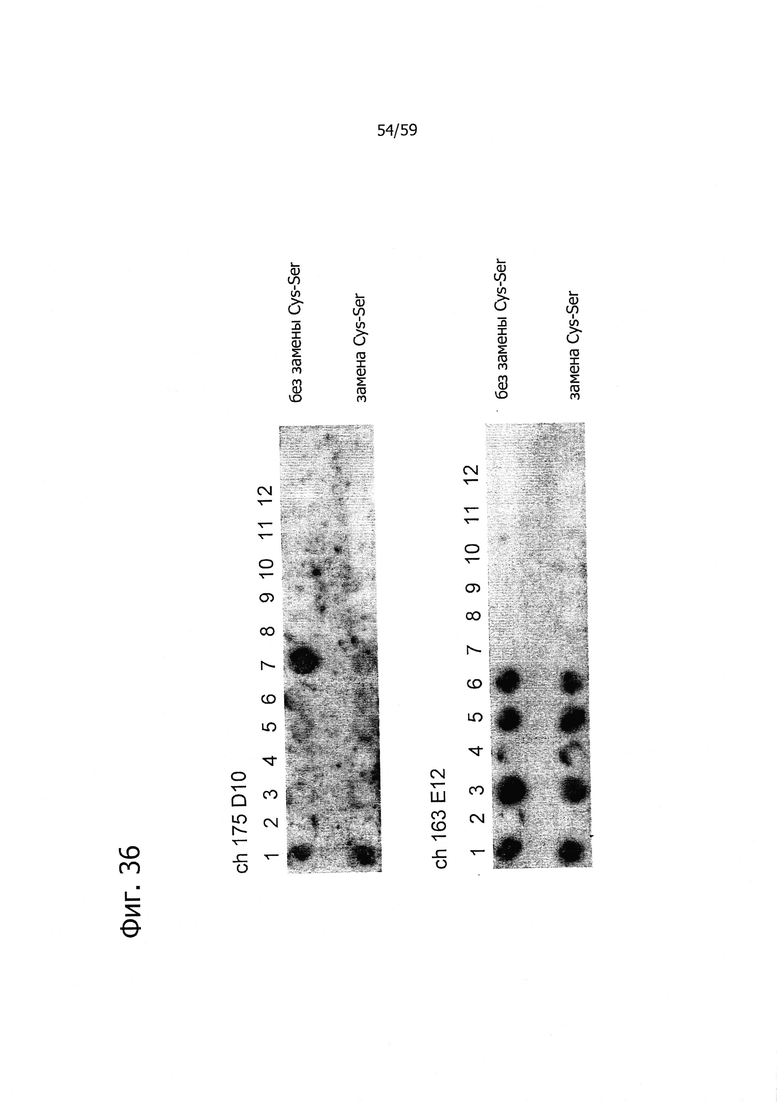

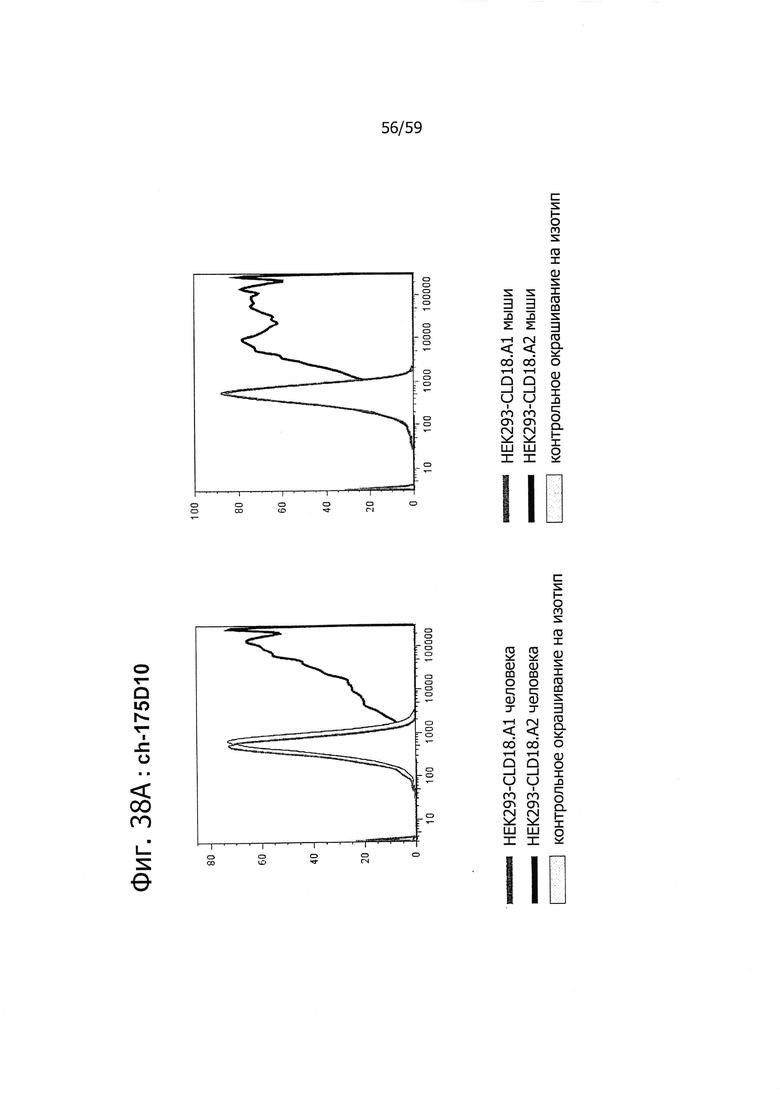
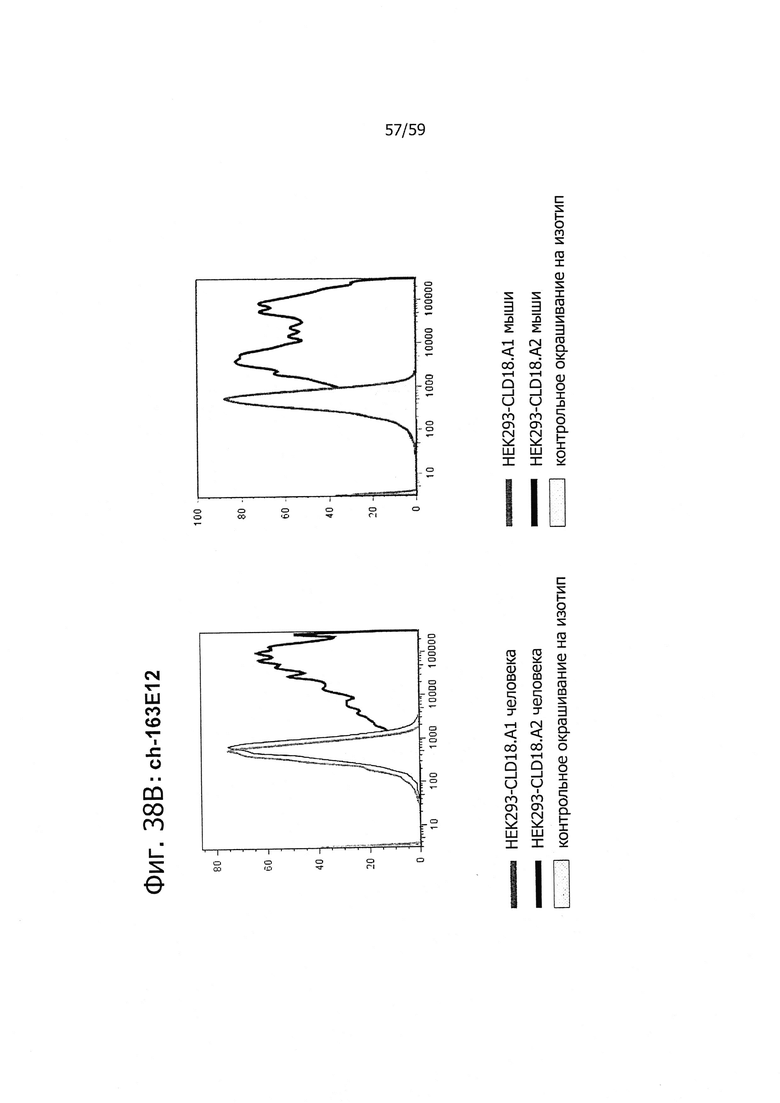


Настоящее изобретение относится к биотехнологии и медицине, в частности к применению антитела, связывающегося с клаудином для получения медикамента для лечения или профилактики раковых метастазов в лимфатических узлах. 2 н. и 48 з.п. ф-лы, 39 ил., 8 табл., 14 пр.
1. Применение антитела, связывающегося с CLD18A2 и опосредующего уничтожение и/или ингибирование пролиферации клеток, экспрессирующих CLD18A2, где указанное уничтожение клеток и/или ингибирование пролиферации вызывается связыванием указанного антитела с CLD18A2 экспрессируемым данными клетками, для получения медикамента для лечения или профилактики раковых метастазов в лимфатических узлах, где антитело связывается с эпитопом, расположенным на петле D1 CLD18A2, содержащей аминокислотную последовательность SEQ ID NO: 28, или на петле D3 CLD18A2, содержащей аминокислотную последовательность SEQ ID NO: 29.
2. Применение по п. 1, где указанное антитело связывается с CLD18A1 и CLD18A2.
3. Применение по п. 1, где указанное антитело связывается с CLD18A2, но не с CLD18A1.
4. Применение по п. 1, где уничтожение клеток вызывается связыванием указанного антитела с CLD18A2, экспрессируемым данными клетками.
5. Применение по п. 1, где уничтожение клеток и/или ингибирование пролиферации не вызывается связыванием указанного антитела с CLD18A1, экспрессируемым данными клетками.
6. Применение по п. 1, где указанное антитело опосредует уничтожение клеток, индуцируя лизис по механизму комплемент-зависимой цитотоксичности (CDC), лизис по механизму антителозависимой клеточной цитотоксичности (ADCC), апоптоз, гомотипическую адгезию и/или фагоцитоз.
7. Применение по п. 1, где указанное антитело опосредует уничтожение клеток, индуцируя лизис по механизму CDC и/или лизис по механизму ADCC.
8. Применение по п. 1, где указанное антитело не вызывает лизиса клеток по механизму CDC.
9. Применение по п. 6, где лизис по механизму ADCC происходит в присутствии эффекторных клеток, выбранных из группы, состоящей из моноцитов, мононуклеаров, NK-клеток и PMN.
10. Применение по п. 6, где указанный фагоцитоз осуществляется макрофагами.
11. Применение по п. 1, где указанное антитело представляет собой моноклональное, химерное или гуманизованное антитело либо антиген-связывающий фрагмент антитела.
12. Применение по п. 1, где указанное антитело выбрано из группы, состоящей из антител IgG1, IgG2, предпочтительно IgG2a и IgG2b, IgG3, IgG4, IgM, IgA1, IgA2, секреторного IgA, и IgE.
13. Применение по п. 2, где CLD18A2 имеет аминокислотную последовательность согласно SEQ ID NO: 2.
14. Применение по п. 2, где CLD18A1 имеет аминокислотную последовательность согласно SEQ ID NO: 8.
15. Применение по п. 1, где указанное антитело связывается с нативными эпитопами CLD18, находящегося на поверхности живых клеток.
16. Применение по п. 1, где указанное антитело получают способом, включающим стадию иммунизации животного белком или пептидом, включающим аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 2, 4, 6, 16, 18, 20-23, 27-29, 31, 151, 153 и 155-157, либо нуклеиновой кислотой или клетками-хозяевами, экспрессирующими данный белок или пептид.
17. Применение по п. 1, где указанное антитело вырабатывается клоном, депонированным под номером доступа DSM АСС2737, DSM АСС2738, DSM АСС2739, DSM АСС2740, DSM АСС2741, DSM АСС2742, DSM АСС2743, DSM АСС2745, DSM АСС2746, DSM АСС2747, DSM АСС2748, DSM АСС2808, DSM АСС2809 или DSM АСС2810.
18. Применение по п. 1, где указанные метастазы являются метастазами рака желудка.
19. Применение антитела для получения медикамента для лечения или профилактики раковых метастазов в лимфатических узлах, где указанное антитело содержит один или несколько определяющих комплементарность участков (CDR), предпочтительно по меньшей мере CDR3 вариабельной области тяжелой цепи (VH) и/или вариабельной области легкой цепи (VL) антитела, которое содержит комбинацию VH или VL, каждый из которых содержит набор определяющих комплементарность участков CDR1, CDR2 и CDR3, выбранных из следующих от (i) до (ix):
(i) VH: CDR1: положения 45-52 SEQ ID NO: 115, CDR2: положения 70-77 SEQ ID NO: 115, CDR3: положения 116-125 SEQ ID NO: 115, VL: CDR1: положения 49-53 SEQ ID NO: 122, CDR2: положения 71-73 SEQ ID NO: 122, CDR3: положения 110-118 SEQ ID NO: 122,
(ii) VH: CDR1: положения 45-52 SEQ ID NO: 116, CDR2: положения 70-77 SEQ ID NO: 116, CDR3: положения 116-126 SEQ ID NO: 116, VL: CDR1: положения 47-58 SEQ ID NO: 121, CDR2: положения 76-78 SEQ ID NO: 121, CDR3: положения 115-123 SEQ ID NO: 121,
(iii) VH: CDR1: положения 45-52 SEQ ID NO: 117, CDR2: положения 70-77 SEQ ID NO: 117, CDR3: положения 116-124 SEQ ID NO: 117, VL: CDR1: положения 47-52 SEQ ID NO: 123, CDR2: положения 70-72 SEQ ID NO: 123, CDR3: положения 109-117 SEQ ID NO: 123,
(iv) VH: CDR1: положения 44-51 SEQ ID NO: 119, CDR2: положения 69-76 SEQ ID NO: 119, CDR3: положения 115-125 SEQ ID NO: 119, VL: CDR1: положения 47-58 SEQ ID NO: 126, CDR2: положения 76-78 SEQ ID NO: 126, CDR3: положения 115-122 SEQ ID NO: 126,
(v) VH: CDR1: положения 45-52 SEQ ID NO: 118, CDR2: положения 70-77 SEQ ID NO: 118, CDR3: положения 116-126 SEQ ID NO: 118, VL: CDR1: положения 47-58 SEQ ID NO: 125, CDR2: положения 76-78 SEQ ID NO: 125, CDR3: положения 115-123 SEQ ID NO: 125,
(vi) VH: CDR1: положения 45-53 SEQ ID NO: 120, CDR2: положения 71-78 SEQ ID NO: 120, CDR3: положения 117-128 SEQ ID NO: 120, VL: CDR1: положения 47-58 SEQ ID NO: 124, CDR2: положения 76-78 SEQ ID NO: 124, CDR3: положения 115-123 SEQ ID NO: 124,
(vii) VH: CDR1: положения 45-53 SEQ ID NO: 120, CDR2: положения 71-78 SEQ ID NO: 120, CDR3: положения 117-128 SEQ ID NO: 120, VL: CDR1: положения 47-58 SEQ ID NO: 127, CDR2: положения 76-78 SEQ ID NO: 127, CDR3: положения 115-123 SEQ ID NO: 127,
(viii) VH: CDR1: положения 45-53 SEQ ID NO: 120, CDR2: положения 71-78 SEQ ID NO: 120, CDR3: положения 117-128 SEQ ID NO: 120, VL: CDR1: положения 47-58 SEQ ID NO: 128, CDR2: положения 76-78 SEQ ID NO: 128, CDR3: положения 115-123 SEQ ID NO: 128, и
(ix) VH: CDR1: положения 45-53 SEQ ID NO: 120, CDR2: положения 71-78 SEQ ID NO: 120, CDR3: положения 117-128 SEQ ID NO: 120, VL: CDR1: положения 47-52 SEQ ID NO: 129, CDR2: положения 70-72 SEQ ID NO: 129, CDR3: положения 109-117 SEQ ID NO: 129.
20. Применение по п. 19, где указанное антитело содержит VH, содержащий набор определяющих комплементарность участков CDR1, CDR2 и CDR3, выбранных из следующих от (i) до (vi):
(i) CDR1: положения 45-52 SEQ ID NO: 115, CDR2: положения 70-77 SEQ ID NO: 115, CDR3: положения 116-125 SEQ ID NO: 115,
(ii) CDR1: положения 45-52 SEQ ID NO: 116, CDR2: положения 70-77 SEQ ID NO: 116, CDR3: положения 116-126 SEQ ID NO: 116,
(iii) CDR1: положения 45-52 SEQ ID NO: 117, CDR2: положения 70-77 SEQ ID NO: 117, CDR3: положения 116-124 SEQ ID NO: 117,
(iv) CDR1: положения 45-52 SEQ ID NO: 118, CDR2: положения 70-77 SEQ ID NO: 118, CDR3: положения 116-126 SEQ ID NO: 118,
(v) CDR1: положения 44-51 SEQ ID NO: 119, CDR2: положения 69-76 SEQ ID NO: 119, CDR3: положения 115-125 SEQ ID NO: 119, и
(vi) CDR1: положения 45-53 SEQ ID NO: 120, CDR2: положения 71-78 SEQ ID NO: 120, CDR3: положения 117-128 SEQ ID NO: 120.
21. Применение по п. 19, где указанное антитело содержит VL, содержащий набор определяющих комплементарность участков CDR1, CDR2 и CDR3, выбранных из следующих от (i) до (ix):
(i) CDR1: положения 47-58 SEQ ID NO: 121, CDR2: положения 76-78 SEQ ID NO: 121, CDR3: положения 115-123 SEQ ID NO: 121,
(ii) CDR1: положения 49-53 SEQ ID NO: 122, CDR2: положения 71-73 SEQ ID NO: 122, CDR3: положения 110-118 SEQ ID NO: 122,
(iii) CDR1: положения 47-52 SEQ ID NO: 123, CDR2: положения 70-72 SEQ ID NO: 123, CDR3: положения 109-117 SEQ ID NO: 123,
(iv) CDR1: положения 47-58 SEQ ID NO: 124, CDR2: положения 76-78 SEQ ID NO: 124, CDR3: положения 115-123 SEQ ID NO: 124,
(v) CDR1: положения 47-58 SEQ ID NO: 125, CDR2: положения 76-78 SEQ ID NO: 125, CDR3: положения 115-123 SEQ ID NO: 125,
(vi) CDR1: положения 47-58 SEQ ID NO: 126, CDR2: положения 76-78 SEQ ID NO: 126, CDR3: положения 115-122 SEQ ID NO: 126,
(vii) CDR1: положения 47-58 SEQ ID NO: 127, CDR2: положения 76-78 SEQ ID NO: 127, CDR3: положения 115-123 SEQ ID NO: 127,
(viii) CDR1: положения 47-58 SEQ ID NO: 128, CDR2: положения 76-78 SEQ ID NO: 128, CDR3: положения 115-123 SEQ ID NO: 128, и
(ix) CDR1: положения 47-52 SEQ ID NO: 129, CDR2: положения 70-72 SEQ ID NO: 129, CDR3: положения 109-117 SEQ ID NO: 129.
22. Применение по п. 20, где указанное антитело содержит VL, содержащий набор определяющих комплементарность участков CDR1, CDR2 и CDR3, выбранных из следующих от (i) до (ix):
(i) CDR1: положения 47-58 SEQ ID NO: 121, CDR2: положения 76-78 SEQ ID NO: 121, CDR3: положения 115-123 SEQ ID NO: 121,
(ii) CDR1: положения 49-53 SEQ ID NO: 122, CDR2: положения 71-73 SEQ ID NO: 122, CDR3: положения 110-118 SEQ ID NO: 122,
(iii) CDR1: положения 47-52 SEQ ID NO: 123, CDR2: положения 70-72 SEQ ID NO: 123, CDR3: положения 109-117 SEQ ID NO: 123,
(iv) CDR1: положения 47-58 SEQ ID NO: 124, CDR2: положения 76-78 SEQ ID NO: 124, CDR3: положения 115-123 SEQ ID NO: 124,
(v) CDR1: положения 47-58 SEQ ID NO: 125, CDR2: положения 76-78 SEQ ID NO: 125, CDR3: положения 115-123 SEQ ID NO: 125,
(vi) CDR1: положения 47-58 SEQ ID NO: 126, CDR2: положения 76-78 SEQ ID NO: 126, CDR3: положения 115-122 SEQ ID NO: 126,
(vii) CDR1: положения 47-58 SEQ ID NO: 127, CDR2: положения 76-78 SEQ ID NO: 127, CDR3: положения 115-123 SEQ ID NO: 127,
(viii) CDR1: положения 47-58 SEQ ID NO: 128, CDR2: положения 76-78 SEQ ID NO: 128, CDR3: положения 115-123 SEQ ID NO: 128, и
(ix) CDR1: положения 47-52 SEQ ID NO: 129, CDR2: положения 70-72 SEQ ID NO: 129, CDR3: положения 109-117 SEQ ID NO: 129.
23. Применение по любому из пп. 19-22, где указанное антитело содержит комбинацию VH и VL, каждый из которых содержит набор определяющих комплементарность участков CDR1, CDR2 и CDR3, выбранных из следующих от (i) до (ix):
(i) VH: CDR1: положения 45-52 SEQ ID NO: 115, CDR2: положения 70-77 SEQ ID NO: 115, CDR3: положения 116-125 SEQ ID NO: 115, VL: CDR1: положения 49-53 SEQ ID NO: 122, CDR2: положения 71-73 SEQ ID NO: 122, CDR3: положения 110-118 SEQ ID NO: 122,
(ii) VH: CDR1: положения 45-52 SEQ ID NO: 116, CDR2: положения 70-77 SEQ ID NO: 116, CDR3: положения 116-126 SEQ ID NO: 116, VL: CDR1: положения 47-58 SEQ ID NO: 121, CDR2: положения 76-78 SEQ ID NO: 121, CDR3: положения 115-123 SEQ ID NO: 121,
(iii) VH: CDR1: положения 45-52 SEQ ID NO: 117, CDR2: положения 70-77 SEQ ID NO: 117, CDR3: положения 116-124 SEQ ID NO: 117, VL: CDR1: положения 47-52 SEQ ID NO: 123, CDR2: положения 70-72 SEQ ID NO: 123, CDR3: положения 109-117 SEQ ID NO: 123,
(iv) VH: CDR1: положения 44-51 SEQ ID NO: 119, CDR2: положения 69-76 SEQ ID NO: 119, CDR3: положения 115-125 SEQ ID NO: 119, VL: CDR1: положения 47-58 SEQ ID NO: 126, CDR2: положения 76-78 SEQ ID NO: 126, CDR3: положения 115-122 SEQ ID NO: 126,
(v) VH: CDR1: положения 45-52 SEQ ID NO: 118, CDR2: положения 70-77 SEQ ID NO: 118, CDR3: положения 116-126 SEQ ID NO: 118, VL: CDR1: положения 47-58 SEQ ID NO: 125, CDR2: положения 76-78 SEQ ID NO: 125, CDR3: положения 115-123 SEQ ID NO: 125,
(vi) VH: CDR1: положения 45-53 SEQ ID NO: 120, CDR2: положения 71-78 SEQ ID NO: 120, CDR3: положения 117-128 SEQ ID NO: 120, VL: CDR1: положения 47-58 SEQ ID NO: 124, CDR2: положения 76-78 SEQ ID NO: 124, CDR3: положения 115-123 SEQ ID NO: 124,
(vii) VH: CDR1: положения 45-53 SEQ ID NO: 120, CDR2: положения 71-78 SEQ ID NO: 120, CDR3: положения 117-128 SEQ ID NO: 120, VL: CDR1: положения 47-58 SEQ ID NO: 127, CDR2: положения 76-78 SEQ ID NO: 127, CDR3: положения 115-123 SEQ ID NO: 127,
(viii) VH: CDR1: положения 45-53 SEQ ID NO: 120, CDR2: положения 71-78 SEQ ID NO: 120, CDR3: положения 117-128 SEQ ID NO: 120, VL: CDR1: положения 47-58 SEQ ID NO: 128, CDR2: положения 76-78 SEQ ID NO: 128, CDR3: положения 115-123 SEQ ID NO: 128, и
(ix) VH: CDR1: положения 45-53 SEQ ID NO: 120, CDR2: положения 71-78 SEQ ID NO: 120, CDR3: положения 117-128 SEQ ID NO: 120, VL: CDR1: положения 47-52 SEQ ID NO: 129, CDR2: положения 70-72 SEQ ID NO: 129, CDR3: положения 109-117 SEQ ID NO: 129.
24. Применение по любому из пп. 19-22, где указанное антитело содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 132, 133, 134, 135, 136 и 137.
25. Применение по п. 23, где указанное антитело содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 132, 133, 134, 135, 136 и 137.
26. Применение по любому из пп. 19-22, где указанное антитело содержит вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 138, 139, 140, 141, 142, 143, 144, 145 и 146.
27. Применение по п. 23, где указанное антитело содержит вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 138, 139, 140, 141, 142, 143, 144, 145 и 146.
28. Применение по п. 24, где указанное антитело содержит вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 138, 139, 140, 141, 142, 143, 144, 145 и 146.
29. Применение по любому из пп. 19-22, где указанное антитело содержит комбинацию вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL), выбранную из следующих вариантов от (i) до (ix):
(i) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 132, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 139,
(ii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 133, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 138,
(iii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 134, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 140,
(iv) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 136, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 143,
(v) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 135, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 142,
(vi) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 141,
(vii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 144,
(viii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 145, и
(ix) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 146.
30. Применение по п. 23, где указанное антитело содержит комбинацию вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL), выбранную из следующих вариантов от (i) до (ix):
(i) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 132, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 139,
(ii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 133, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 138,
(iii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 134, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 140,
(iv) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 136, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 143,
(v) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 135, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 142,
(vi) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 141,
(vii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 144,
(viii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 145, и
(ix) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 146.
31. Применение по п. 24, где указанное антитело содержит комбинацию вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL), выбранную из следующих вариантов от (i) до (ix):
(i) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 132, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 139,
(ii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 133, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 138,
(iii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 134, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 140,
(iv) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 136, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 143,
(v) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 135, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 142,
(vi) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 141,
(vii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 144,
(viii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 145, и
(ix) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 146.
32. Применение по п. 26, где указанное антитело содержит комбинацию вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL), выбранную из следующих вариантов от (i) до (ix):
(i) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 132, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 139,
(ii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 133, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 138,
(iii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 134, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 140,
(iv) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 136, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 143,
(v) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 135, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 142,
(vi) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 141,
(vii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 144,
(viii) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 145, и
(ix) VH содержит аминокислотную последовательность, представленную SEQ ID NO: 137, и VL содержит аминокислотную последовательность, представленную SEQ ID NO: 146.
33. Применение по любому из пп. 19-22, где указанное антитело содержит
(i) тяжелую цепь, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 115, 116, 117, 118, 119 и 120, и/или
(ii) легкую цепь, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 121, 122, 123, 124, 125, 126, 127, 128 и 129.
34. Применение по п. 23, где указанное антитело содержит
(i) тяжелую цепь, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 115, 116, 117, 118, 119 и 120, и/или
(ii) легкую цепь, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 121, 122, 123, 124, 125, 126, 127, 128 и 129.
35. Применение по п. 24, где указанное антитело содержит
(i) тяжелую цепь, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 115, 116, 117, 118, 119 и 120, и/или
(ii) легкую цепь, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 121, 122, 123, 124, 125, 126, 127, 128 и 129.
36. Применение по п. 26, где указанное антитело содержит
(i) тяжелую цепь, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 115, 116, 117, 118, 119 и 120, и/или
(ii) легкую цепь, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 121, 122, 123, 124, 125, 126, 127, 128 и 129.
37. Применение по п. 29, где указанное антитело содержит
(i) тяжелую цепь, содержащую аминокислотную последовательность, выбранную из группы включающей SEQ ID NO: 115, 116, 117, 118, 119 и 120, и/или
(ii) легкую цепь, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 121, 122, 123, 124, 125, 126, 127, 128 и 129.
38. Применение по любому из пп. 19-22, где указанное антитело содержит комбинацию тяжелых цепей и легких цепей (VL), выбранную из следующих вариантов от (i) до (ix):
(i) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 115, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 122,
(ii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 116, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 121,
(iii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 117, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 123,
(iv) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 119, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 126,
(v) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 118, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 125,
(vi) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 124,
(vii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 127,
(viii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 128, и
(ix) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 129.
39. Применение по п. 23, где указанное антитело содержит комбинацию тяжелых цепей и легких цепей (VL), выбранную из следующих вариантов от (i) до (ix):
(i) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 115, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 122,
(ii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 116, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 121,
(iii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 117, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 123,
(iv) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 119, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 126,
(v) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 118, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 125,
(vi) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ IDNO: 124,
(vii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 127,
(viii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 128, и
(ix) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 129.
40. Применение по п.24, где указанное антитело содержит комбинацию тяжелых цепей и легких цепей (VL), выбранную из следующих вариантов от (i) до (ix):
(i) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 115, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 122,
(ii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 116, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 121,
(iii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 117, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 123,
(iv) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 119, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 126,
(v) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 118, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 125,
(vi) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 124,
(vii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 127,
(viii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 128, и
(ix) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 129.
41. Применение по п. 26, где указанное антитело содержит комбинацию тяжелых цепей и легких цепей (VL), выбранную из следующих вариантов от (i) до (ix):
(i) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 115, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 122,
(ii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 116, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 121,
(iii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 117, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 123,
(iv) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 119, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 126,
(v) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 118, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 125,
(vi) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 124,
(vii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 127,
(viii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 128, и
(ix) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 129.
42. Применение по п. 29, где указанное антитело содержит комбинацию тяжелых цепей и легких цепей (VL), выбранную из следующих вариантов от (i) до (ix):
(i) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 115, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 122,
(ii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 116, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 121,
(iii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 117, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 123,
(iv) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 119, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 126,
(v) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 118, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 125,
(vi) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 124,
(vii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 127,
(viii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 128, и
(ix) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 129.
43. Применение по п. 33, где указанное антитело содержит комбинацию тяжелых цепей и легких цепей (VL), выбранную из следующих вариантов от (i) до (ix):
(i) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 115, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 122,
(ii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 116, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 121,
(iii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 117, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 123,
(iv) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 119, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 126,
(v) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 118, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 125,
(vi) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 124,
(vii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 127,
(viii) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 128, и
(ix) тяжелая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 120, и легкая цепь содержит аминокислотную последовательность, представленную SEQ ID NO: 129.
44. Применение по любому из пп. 19-22, где указанные метастазы являются метастазами рака желудка.
45. Применение по п. 23, где указанные метастазы являются метастазами рака желудка.
46. Применение по п. 24, где указанные метастазы являются метастазами рака желудка.
47. Применение по п. 26, где указанные метастазы являются метастазами рака желудка.
48. Применение по п. 29, где указанные метастазы являются метастазами рака желудка.
49. Применение по п. 33, где указанные метастазы являются метастазами рака желудка.
50. Применение по п. 38, где указанные метастазы являются метастазами рака желудка.
| TOMOAKI NIIMI et.al., claudin-18, a Novel Downstream Target Gene for the T/EBP/NKX2.1 Homeodomain Transcription Factor, Encodes Lung- and Stomach-Specific Isoforms through Alternative Splicing., 2001 Nov; 21(21): 7380-7390. | |||
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ IL-1БЕТА | 2001 |
|
RU2286351C2 |
Авторы
Даты
2019-03-18—Публикация
2008-05-27—Подача