Изобретение относится к медицине, а именно к фтизиатрии, и может быть использовано для лабораторного определения микобактерий туберкулеза, относящихся к генотипу Beijing В0-кластер.
Возбудитель туберкулеза человека - Mycobacterium tuberculosis имеет клональную структуру популяции, внутри вида М. tuberculosis выделяют отдельные генетические семейства, которые могли сформироваться в различных географических регионах. Со временем, некоторые генотипы возбудителя распространились по всему миру [Sola С.et al., 2001; Gagneux S. et al., 2006]. Примером такого генотипа M. tuberculosis является генетическое семейство (генотип) Beijing, вероятно возникшее в северном Китае [van Soolingen D. et al. 1995]. Штаммы M. tuberculosis, принадлежащие к этому семейству, выделяют в различных странах, в том числе и в России (40-60% больных туберкулезом) [Нарвская О.В. и соавт., 1999; Bifani P. et al., 2002; Drobniewski F., et al. 2005; Mokrousov I., 2015; Luo T. et al., 2015]. Молекулярное типирование штаммов M. tuberculosis, циркулирующих в России с середины 1990-х годов, выявило не только преобладание штаммов Beijing, но и широкое распространение варианта с характерным профилем IS6110-RFLP Beijing В0 (Нарвская О.В., 2003). Особенностью профиля Beijing В0 является наличие двух дополнительных фрагментов в верхней части профиля размером 7,1 тпн и 9,2 тпн (Фиг. 1). Этот профиль М. tuberculosis был впервые выявлен в российских штаммах в середине 1990-х годов [Marttila Н. et al., 1997; Нарвская О.В. и соавт., 1999; Portaels F. et al., 1999]. Эти штаммы широко циркулируют на территории постсоветского пространства и доминируют в США и Западной Европе среди мультирезистентных штаммов, выделенных от иммигрантов из бывшего СССР [Сох Н. et al., 2005; Kubica Т. et al., 2004; Ghebremichael S. et al., 2010]. Профиль В0 и сходные с ним профили гибридизации IS6110-RFLP определяют как В0-кластер [Mokrousov I. et al., 2008]. Компьютерное моделирование эволюции 17 полиморфных локусов VNTR с использованием Байесовой статистики показало существенно более быстрый (в 10.6 раза) рост субпопуляции ВО в сравнении с популяцией Beijing в целом [Мокроусов И.В., 2009].
Известен метод определения штаммов Beijing В0-кластера, основанный на гибридизационном анализе полиморфизма длин фрагментов рестрикции ДНК, содержащих инсерционный элемент IS6110 (метод IS6110-RFLP) с последующим сравнением с референтным профилем для этого штамма [Нарвская О.В., 2003]. Метод IS6110-RFLP ограничен трудоемкостью выполнения анализа, требующего выделения большого количества ДНК. Таким образом, разработка быстрого и простого способа детекции эпидемиологически и клинически значимого варианта М. tuberculosis Beijing В0-кластер является актуальной задачей программы контроля туберкулеза в России и мире.
Проведенный нами анализ полного генома штамма Mycobacterium tuberculosis NZ_CP012090.1 (номер доступа в GenBank), относящегося к В0-кластеру, позволил картировать известные фрагменты его профиля IS6110-RFLP в определенных локусах генома, ограниченных сайтами рестрикции PvuII. В частности, мы установили, что элемент IS6110 в позициях 2755667-2757021 обратно ориентирован и расположен внутри фрагмента рестрикции Pvull длиной 9162 пн. Это соответствует одному из двух крупных фрагментов гибридизации (9,2 тпн), характерных для профиля В0. Данная вставка IS6110 соответствует позициям 2982598/9 в полном геноме лабораторного штамма H37Rv, в интактном участке между генами Rv2664 и Rv2665 (GenBank NC 000962.3). Данный участок является интактным и во всех других полных геномах штаммов М. tuberculosis различных генотипов, депонированных в GenBank, за исключением вышеупомянутого штамма NZ_CP012090.1 (Фиг. 2).
Задачей предлагаемого изобретения является разработка способа быстрой и надежной детекции микобактерий туберкулеза генотипа Beijing В0-кластер.
Задача реализуется за счет того, что определяют вставку элемента IS6110 в локусе генома Rv2664-Rv2665 с помощью ПЦР в формате реального времени с использованием олигонуклеотидных праймеров BZF  BZR
BZR 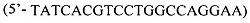 и BZRi
и BZRi  и флуоресцентно-меченых зондов PBZ
и флуоресцентно-меченых зондов PBZ 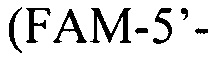
 и nPBZ
и nPBZ  , с оценкой результатов ПЦР между 15-35 циклами путем регистрации сигнала флуоресценции по FAM-каналу с длиной волны 510 нм и при экспоненциальном его накоплении судят о принадлежности штамма М. tuberculosis к Beijing В0-кластеру, а при регистрации сигнала флуоресценции по контрольному НЕХ-каналу с длиной волны 555 нм судят о принадлежности штамма к другому генотипу М. tuberculosis.
, с оценкой результатов ПЦР между 15-35 циклами путем регистрации сигнала флуоресценции по FAM-каналу с длиной волны 510 нм и при экспоненциальном его накоплении судят о принадлежности штамма М. tuberculosis к Beijing В0-кластеру, а при регистрации сигнала флуоресценции по контрольному НЕХ-каналу с длиной волны 555 нм судят о принадлежности штамма к другому генотипу М. tuberculosis.
Мультиплексная ПЦР основана на использовании сконструированных нами: (1) трех праймеров - двух внешних (по отношению к специфической вставке IS6110 в геноме В0, фланкирующих ее и выступающих в качестве прямого и обратного) и одного внутреннего (расположенного внутри IS6110 и действующего как обратный праймер) и (2) двух флуоресцентно-меченых зондов для выявления наличия или отсутствия специфической вставки IS6110 в определенной позиции в межгенном участке Rv2664-Rv2665. Преимущества предлагаемого способа:
1. быстрота (меньше одного дня от момента выделения ДНК);
2. простая и однозначная интерпретация результатов;
3. возможность быстрого анализа больших коллекций штаммов М. tuberculosis для оценки их принадлежности к кластеру Beijing В0 с диагностической целью и при популяционных исследованиях.
Изобретение поясняется чертежами, где Фиг. 1 - Примеры профилей IS6110-RFLP микобактерий туберкулеза (генотип Beijing В0 отмечен звездочкой, профили Beijing В0-кластера - серый фон). Фиг. 2 - Схема ПЦР (не в масштабе). Крупная стрелка показывает ориентацию элемента IS6110, короткие стрелки - позиции праймеров и зондов в геномах референс-штаммов В0 и H37Rv. Фиг. 3 - накопление сигнала флуоресценции: (а) по специфическому (FAM) каналу детекции, на М. tuberculosis Beijing В0-кластер и (б) контрольному (HEX) каналу детекции, на штамм другого генотипа М. tuberculosis. Вода служит отрицательным контрольным образцом.
Способ осуществляется следующим образом. Выделение ДНК из культуры М. tuberculosis, выращенной на среде Левенштейна-Йенсена, проводят по van Embden et al. [1993]: суспендируют 1 стандартную бактериологическую петлю культуры в 400 мкл буфера ТЕ х1 и инкубируют 20 мин при 85°C. Дальнейшую обработку проводят с использованием лизоцима, протеиназы К, додецилсульфата натрия и цетилтриметиламмонийбромида. Полученный клеточный лизат обрабатывают смесью фенол-хлороформ-изоамиловый спирт (25:24:1), центрифугируют, осаждают изопропанолом, промывают 70% этанолом, осадок высушивают и растворяют в 30-50 мкл ТЕ x1.
Были использованы следующие сконструированные нами праймеры и зонды для ПЦР в реальном времени (Фиг. 2) для проведения реакции ПЦР и детекции флуоресценции по двум каналам в одной пробирке одновременно: праймеры BZF 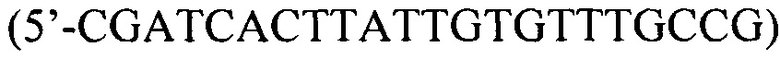 , BZR
, BZR  и BZRi
и BZRi 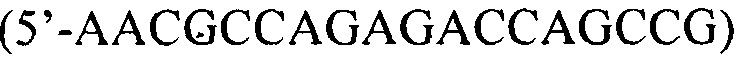 и флуоресцентно-меченые зондов PBZ
и флуоресцентно-меченые зондов PBZ 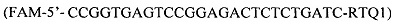 и nPBZ
и nPBZ  .
.
Для детекции генотипа Beijing В0-кластер служили праймеры BZF и BZRi и зонд PBZ (Фиг. 2). Детекцию сигнала проводили по FAM-каналу детекции (длина волны 510 нм) (Фиг. 3а).
Для детекции штамма любого другого генотипа М. tuberculosis служили праймеры BZF, BZR и зонд nPBZ (Фиг. 2); детекцию сигнала проводили по НЕХ-каналу (длина волны 555 нм) (Фиг. 3б).
Очищенная ДНК (0.1-0.5 мкл) добавляется к смеси ПЦР (конечный объем 30 мкл) содержащей 1,5 mM MgCl2, 1 U Taq ДНК полимеразы для ПЦР в реальном времени в режиме «горячего старта», 200 μМ каждого из дНТФ, праймеры (по 5 пмоль), зонды (по 2 пмоль). ПЦР проводили в термоциклере Rotorgene6000 (Corbette Research) в следующих условиях: 95°C, 10 мин; далее 40 циклов 94°C, 15 с; 60°C, 40 с. Считывание сигнала флуоресценции - при 60°C по каналам 510 и 555 нм.
Оценка результатов.
Полученные данные - кривые накопления флуоресцентного сигнала между 15-35 циклом по двум каналам - анализируют с помощью программного обеспечения прибора, используемого для проведения ПЦР в формате реального времени. По каналу FAM (длина волны 510 нм) - регистрируется накопление продукта амплификации фрагмента ДНК, специфического для генотипа М. tuberculosis Beijing В0-кластер (Фиг. 3а), по каналу HEX (длина волны 555 нм) - фрагмента ДНК, специфического для любого другого генотипа М. tuberculosis (Фиг. 3б).
При отсутствии сигнала флуоресценции по обоим каналам (510 и 555 нм) делается вывод о недостаточном количестве и/или качестве ДНК или ингибировании реакции ПЦР и невозможности какого-либо вывода о наличии или отсутствии ДНК штамма Beijing В0 в образце.
Обязательная амплификация одного или другого продукта ПЦР является контролем качества: при отсутствии сигнала судят о деградированной ДНК или ингибировании реакции, при наличии сигнала по обоим каналам делают вывод о микс-образце (контаминация на каком-либо из этапов исследования или выделение двух штаммов от одного больного).
Пример 1. Анализ ДНК клинических изолятов М. tuberculosis из коллекции лаборатории молекулярной микробиологии ФБУН НИИЭМ им. Пастера.
Способ был апробирован на представительной и ранее охарактеризованной методами сполиготипирования и IS6110-RFLP типирования коллекции ДНК штаммов М. tuberculosis различных генотипов, выделенных от больных из России, Вьетнама и Китая. При этом все штаммы генотипа Beijing были генотипированы методом IS6110-RFLP для точного выявления штаммов В0-кластера. Штаммы других генотипов представляли различные генетические семейства (LAM, Haarlem, Т, Ural, Manu, X, EAI), установленные на основе результатов сполиготипирования и дополнительного анализа других генетических маркеров для отдельных семейств (однонуклеотидные или делеционные полиморфизмы).
Всего предлагаемым способом ПЦР в формате реального времени было проанализировано 204 штамма из Санкт-Петербурга и Пскова (из них 136 штаммов генотипа Beijing), 57 штаммов из Китая (из них 45 штаммов генотипа Beijing), 59 штаммов из Вьетнама (из них 37 штаммов генотипа Beijing). В результате, специфический участок генома, характерный для штамма с профилем IS6110-RFLP В0, был выявлен только у штаммов кластера В0 (n=35), что подтверждает наличие у них специфической инсерции IS6110 в Rv2664-Rv2665, характерной для этого геноварианта М. tuberculosis.
В то же время, у российских штаммов других вариантов генотипа Beijing, не относящихся к кластеру В0, и штаммов других генетических семейств, а также всех штаммов из Вьетнама и Китая был выявлен фрагмент, соответствующий данному участку генома, не содержащему инсерцию IS6110. Таким образом, специфичность и чувствительность данного способа выявления штаммов кластера В0 генотипа Beijing составили 100% для изученной коллекции штаммов.
Пример 2. Анализ коллекции ДНК изолятов М. tuberculosis, выделенных от больных туберкулезным спондилитом.
Всего было проверено 107 образцов ДНК, выделенных от больных туберкулезным спондилитом, находившихся на лечении в Санкт-Петербургском НИИ фтизиопульмонологии в 2009-2012 годах. Все образцы ДНК М. tuberculosis были охарактеризованы методами сполиготипирования и IS110-RFLP типирования. Штаммы генотипа Beijing (n=80) были генотипированы методом IS6110-RFLP для выявления штаммов В0-кластера. Штаммы других генотипов представляли различные генетические семейства, установленные методом сполиготипирования, а именно, Т (n=12), Ural (n=7), LAM (n=3), Manu (n=2), Haarlem (n=1), S (n=1). Далее ДНК всех штаммов была протестирована предлагаемым способом ПЦР в формате реального времени для выявления штаммов Beijing В0-кластера. В результате проведения ПЦР было установлено, что 30 изолятов относились к Beijing В0-кластеру, что полностью соответствовало результатам IS6110-RFLP анализа.
Литература
1. Мокроусов И.В., дис. д-ра биол. наук. СПб., 2009.
2. Нарвская О.В., дис. д-ра мед. наук. С.-Петербург, 2003
3. Bifani P. et al. Trends Microbiol. 2002, 10: 45-52.
4. Cox H. et al. Respir. Res. 2005, 6: 134.
5. Drobniewski F. et al. JAMA 2005, 293: 2726-2731.
6. Gagneux S. et al. Proc. Natl. Acad. Sci. USA. 2006, 103: 2869-2873.
7. Ghebremichael S. et al. PLoS One, 2010, 5: e10893.
8. Kubica T.et al. Int. J. Tuberc. Lung Dis. 2004, 8: 1107-1113.
9. Luo T. et al., PNAS. 2015, 112: 8136-8141.
10. Marttila H. et al. Antimicrob. Agents Chemother. 1997, 42: 2443-2445.
11. Mokrousov I. Tuberculosis (Edinb). 2015; 95: S167-176.
12. Mokrousov I. et al. J Clin Microbiol. 2008, 46: 3576-3584.
13. Sola С.et al. J. Mol. Evol. 2001, 53: 680-689.
14. Portaels F. et al. Int. J. Tuberc. Lung Dis. 1999, 3: 582-588.
15. van Soolingen D. et al. J. Clin. Microbiol. 1995, 33: 3234-3238.
16. van Embden J. et al. J. Clin. Microbiol. 31: 406-409.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫЯВЛЕНИЯ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА ГЕНОТИПА ВЕIJING В РЕЖИМЕ РЕАЛЬНОГО ВРЕМЕНИ | 2011 |
|
RU2528866C2 |
| Способ детекции филогенетических сублиний генотипа Beijing Mycobacterium tuberculosis в формате реального времени | 2020 |
|
RU2743365C1 |
| СПОСОБ ВЫЯВЛЕНИЯ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА ГЕНОТИПА BEIJING | 2008 |
|
RU2405836C2 |
| Способ детекции изолятов Mycobacterium tuberculosis Beijing 94-32-кластера в формате реального времени | 2017 |
|
RU2689800C1 |
| Способ детекции генотипа Mycobacterium tuberculosis Beijing 1071-32-кластер в формате реального времени | 2021 |
|
RU2768021C1 |
| Способ выявления микобактерий туберкулеза Центрально-Азиатского эпидемического кластера генотипа Beijing | 2019 |
|
RU2735415C1 |
| СПОСОБ ОБНАРУЖЕНИЯ МИКОБАКТЕРИЙ ТУБЕРКУЛЁЗА ГЕНЕТИЧЕСКОГО КЛАСТЕРА Beijing B0/W148 | 2013 |
|
RU2551764C2 |
| Способ детекции генотипа Mycobacterium tuberculosis Beijing 14717-15-кластер методом полимеразной цепной реакции в формате реального времени | 2023 |
|
RU2839699C2 |
| Способ детекции штаммов Mycobacterium bovis BCG в формате реального времени | 2018 |
|
RU2689801C1 |
| Способ детекции генотипа Mycobacterium tuberculosis Beijing 14717-15-кластер | 2022 |
|
RU2812351C1 |
Изобретение относится к биотехнологии. Предложен способ быстрой и надежной детекции микобактерий туберкулеза генотипа Beijing В0-кластер. Поставленная задача достигается выявлением специфического для микобактерий туберкулеза генотипа Beijing В0-кластер участка ДНК (вставки элемента IS6110 в локусе генома Rv2664-Rv2665), амплифицированного методом ПЦР в формате реального времени. Анализ результатов проводится путем выявления продукта ПЦР в формате реального времени с использованием специфического флуоресцентного зонда. По каналу FAM регистрируется накопление продукта амплификации фрагмента ДНК, специфического для Beijing В0-кластер, по каналу HEX-фрагмента ДНК, специфического для штамма любого другого генотипа М. tuberculosis. При наличии в образце ДНК штамма Beijing В0-кластер, между 15-35 циклами ПЦР происходит экспоненциальный рост сигнала флуоресценции по каналу детекции FAM и при этом отсутствует сигнал флуоресценции по контрольному каналу детекции HEX. 3 ил., 2 пр.
Способ определения микобактерий туберкулеза генотипа Beijing В0-кластер путем проведения лабораторных исследований, отличающийся тем, что выявляют наличие вставки элемента IS6110 в локусе генома Rv2664-Rv2665 с помощью ПЦР в формате реального времени с использованием олигонуклеотидных праймеров BZF (5'-CGATCACTTATTGTGTTTGCCG), BZR (5'-TATCACGTCCTGGCCAGGAA) и BZRi (5'-AACGCCAGAGACCAGCCG) и флуоресцентно-меченых зондов PBZ (FAM-5'-CCGGTGAGTCCGGAGACTCTCTGATC-RTQ1) и nPBZ (R6G-5'-GGCGATGGGCTTGATTCCTCTGA-BHQ2), с оценкой результатов ПЦР между 15-35 циклами путем регистрации сигнала флуоресценции по FAM-каналу с длиной волны 510 нм и при экспоненциальном его накоплении судят о принадлежности штамма М. tuberculosis к Beijing В0-кластеру, а при регистрации сигнала флуоресценции по контрольному НЕХ-каналу с длиной волны 555 нм судят о принадлежности штамма к другому генотипу М. tuberculosis.
| СПОСОБ ОБНАРУЖЕНИЯ МИКОБАКТЕРИЙ ТУБЕРКУЛЁЗА ГЕНЕТИЧЕСКОГО КЛАСТЕРА Beijing B0/W148 | 2013 |
|
RU2551764C2 |
| СПОСОБ ПОЛУЧЕНИЯ АНТГЕЛЬМИНТНЫХ СРЕДСТВ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ С ФАСЦИОЛОЦИДНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ЭКЦИСТИРОВАННЫХ ЛИЧИНОК Fasciola hepatica | 2014 |
|
RU2576831C2 |
| WO 2012031752 A2, 15.03.2012. | |||
Авторы
Даты
2019-04-05—Публикация
2017-06-30—Подача