Изобретение относится к медицинской вирусологии и может быть использовано в здравоохранении для профилактики заболеваемости среди взрослых и детей, вызванной вирусом гриппа птиц подтипа A(H7N9) с пандемическим потенциалом. Аттенуированный штамм А/17/Гонконг/2017/75108 (H7N9) {Ortomyxoviridae, род Influenzavirus А) является резервным штаммом для живой гриппозной интраназальной вакцины в случае распространения в человеческой популяции вируса гриппа подтипа A(H7N9).
Впервые случаи заражения людей новым вирусом гриппа птиц подтипа азиатского A(H7N9) были зарегистрированы в начале 2013 г. во время первой волны эпидемии, однако в процессе эволюции в 2016 во время пятой эпидемической волны произошло разделение циркулирующих вирусов A(H7N9) на 2 антигенно разные линии: линия дельты реки Чжуцзян и линия дельты реки Янцзы. Опасность данных вирусов заключается в том, что они вызывают тяжелые респираторные заболевания у млекопитающих, и при этом являются низкопатогенными для птиц, что способствует их персистенции в популяции птиц. Кроме того, вирусы A(H7N9) характеризуются наличием в геноме множественных маркеров адаптации к клеткам млекопитающих, что создает предпосылки для возникновения новой пандемии A(H7N9) [Kile J.С. et al. Update: Increase in Human Infections with Novel Asian Lineage Avian Influenza A(H7N9) Viruses During the Fifth Epidemic - China, October 1, 2016-August 7, 2017. MMWR Morb Mortal Wkly Rep. 2017. Vol. 66. №35. P. 928-932. https://www.cdc.gov/mmwr/volumes/66/wr/mm6635a2.htm]. Для того, чтобы избежать разрушительных последствий новой пандемии, необходимо иметь в наличии вакцинные штаммы A(H7N9) для своевременной вакцинации наиболее уязвимых групп населения.
В результате появления в циркуляции антигенно новой линии дельты реки Янцзы представителем которой является штамм вируса гриппа А/Гонконг/125/2017 (H7N9), известный вакцинный штамм А/17/Ануи/2013/61 (H7N9) - прототип [Патент РФ №2563351 от 20.09.2015. - опубл. БИ 2015. - №26] - утратил антигенную актуальность и вследствие этого не может вызвать защитную реакцию в случае возникновения пандемической ситуации, вызванной широким распространением А/Гонконг/125/2017 - подобных штаммов вируса гриппа H7N9, к которым у населения нет иммунитета.
Задачей, на решение которой направлено заявляемое изобретение, является получение антигенно актуального вакцинного штамма для взрослых и для детей на основе холодоадаптированного донора аттенуации А/Ленинград/134/17/57 (H2N2) и нового потенциально-пандемического вируса А/Гонконг/125/2017 (H7N9).
Применяемые в настоящее время штаммы для живых гриппозных вакцин получают методом генетической реассортации эпидемически актуальных вирусов с холодоадаптированными штаммами - донорами аттенуации [Александрова Г.И. Применение метода генетической рекомбинации для получения вакцинных штаммов вируса гриппа // Вопр. Вирусол - 1977 - №4, - С. 387-395].
Донор аттенуации А/Ленинград/134/17/57 (H2N2) - холодоадаптированный (са) и температурочувствительный (ts) штамм вируса гриппа - разрешен для получения безвредных живых интраназальных вакцин для взрослых и детей [Александрова Г.И. Новое в эпидемиологии и профилактике вирусных инфекций. Л., 1968. - С. 66-83].
Цель реассортации - получить штамм с вакцинной формулой генома 6:2. Гены, кодирующие поверхностные белки вируса гриппа гемагглютинин (НА) и нейраминидазу (NA), наследуются от антигенно актуального циркулирующего штамма, а шесть генов, кодирующих внутренние и неструктурные белки (РВ2, РВ1, PA, NP, М, NS), от безвредного донора аттенуации.
Получение вакцинного штамма. Вакцинный штамм А/17/Гонконг/2017/75108 (H7N9) получен методом генетической реассортации потенциально-пандемического вируса гриппа птиц подтипа A(H7N9) с донором аттенуации А/Ленинград/134/17/57 (H2N2) путем одновременного инфицирования развивающихся куриных эмбрионов (РКЭ) смесью родительских вирусов в эквивалентных инфекционных дозах, с последующей селекцией клонов с заданными свойствами при пониженной до 26°С температуре инкубации в присутствии овечьей антисыворотки к донору аттенуации. Клоны дополнительно очищены тремя последовательными клонированиями методом предельных разведений в присутствии антисыворотки к донору аттенуации при пониженной (26°С) и оптимальной (32°С) температурах инкубации. Чистый клон проверен по фенотипическим характеристикам (ts-и са-фенотип) и по формуле генома на соответствие вакцинному штамму.
Антигенная характеристика вакцинного штамма.
Изучение антигенных свойств вакцинного штамма А/17/Гонконг/2017/75108 (H7N9) показало, что:
- ответственный за антигенную специфичность поверхностный белок вакцинного штамма - гемагглютинин (НА) - в РТГА с гомологичной сывороткой антигенно идентичен потенциально-пандемическому вирусу А/Гонконг/125/2017 (H7N9), поскольку показатели взаимодействия реассортанта А/17/Гонконг/2017/75108 (H7N9) и родительского штамма А/Гонконг/125/2017 (H7N9) с крысиной антисывороткой, полученной к вирусу А/Гонконг/125/2017 (H7N9), полностью совпадали (табл. 1), что так же подтверждено полногеномным секвенированием.
- второй ответственный за антигенную специфичность поверхностный белок вакцинного штамма - нейраминидаза (NA) - проверен методом частичного секвенирования, а также полногеномным секвенированием и идентичен вирусу А/Гонконг/125/2017 (H7N9).

Для анализа состава генома полученных реассортантов использовали частичное секвенирование ДНК копий генов [Matyushenko V. et. al. Genotyping assay for differentiation of wild-type and vaccine viruses in subjects immunized with live attenuated influenza vaccine. PLoS One. 2017. Vol. 12 №7. P.e0180497. doi: 10.1371/journal.pone.0180497].
Формула генома 6:2 соответствует требованиям, предъявляемым к штаммам живой гриппозной вакцины: гены, кодирующие поверхностные белки гемагглютинин (НА) и нейраминидазу (NA) принадлежат потенциально-пандемическому вирусу родительскому вирусу А/Гонконг/125/2017 (H7N9), а гены, кодирующие внутренние белки (РВ2, РВ1, PA, NP, М, NS), принадлежат донору аттенуации А/Ленинград/134/17/57 (H2N2). Результаты анализа всех генов вакцинного штамма А/17/Гонконг/2017/75108 (H7N9) представлены в табл. 2.
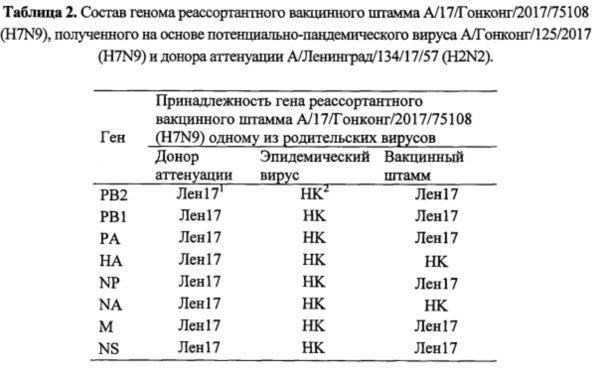
1Лен17 - ген принадлежит донору аттенуации А/Ленинград/134/17/57 (H2N2);
2 HK - ген принадлежит эпидемическому вирусу А/Гонконг/125/2017 (H7N9)
Данные, полученные при первичном отборе вакцинного кандидата, были подтверждены полным секвенированием его генома и показали, что вакцинный штамм А/17/Гонконг/2017/7510 (H7N9) унаследовал все 6 генов, кодирующих внутренние и неструктурные белки, от донора аттенуации А/Ленинград/134/17/57 (H2N2) (табл. 2).
Все кодирующие нуклеотидные и аминокислотные замены, охарактеризованные для донора аттенуации А/Ленинград/134/17/57 (H2N2) как ответственные за его аттенуацию (табл. 3), присутствуют во внутренних генах реассортантного штамма А/17/Гонконг/2017/75108 (H7N9). Таким образом, полное секвенирование генома вакцинного штамма А/17/Гонконг/2017/75108 (H7N9) показало, что он унаследовал от донора А/Ленинград/134/17/47 полный набор аттенуирующих мутаций.
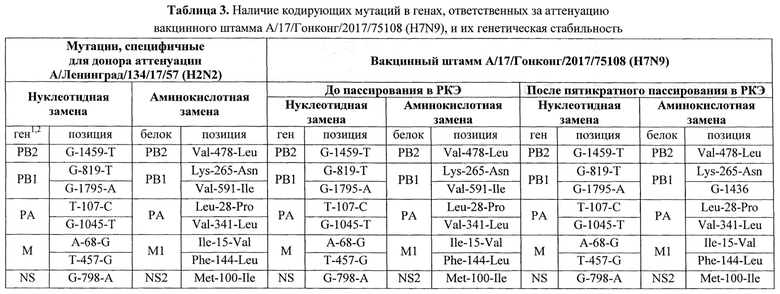
1в сравнении с «диким» предшественником донора аттенуации: А/Ленинград/134/57 (H2N2);
2ген NP донора аттенуации А/Ленинград/134/17/57 (H2N2) не содержит аттенуирующих мутаций.
Генетическую стабильность кодирующих мутаций вакцинного штамма А/17/Гонконг/2017/75108 (H7N9) изучали сравнением сохранности кодирующих мутаций до и после пятикратного пассирования вакцинного штамма в куриных эмбрионах с использованием метода частичного секвенирования. Показано, что нуклеотидная последовательность вакцинного штамма А/17/Гонконг/2017/75108 (H7N9) до и после его пятикратного пассирования, осталась неизменной, доказательством чего служат результаты секвенирования, приведенные в табл. 3.
Оценку фенотипических свойств вакцинного штамма А/17/Гонконг/2017/75108 (H7N9), проводили путем его параллельного титрования в РКЭ при разных температурах. Вакцинный штамм А/17/Гонконг/2017/75108 (H7N9), в развивающихся куриных эмбрионах обладает выраженным температурочувствительным и холодоадаптированным фенотипом, идентичным фенотипу донора аттенуации А/Ленинград/134/17/57 (H2N2). Установлено, что вакцинный вирус является температурочувствительным (ts фенотип) - его инфекционная активность при температуре 40°С составила ≤0,7 lg ЭИД50/мл, и холодоадаптированным (са фенотип) - инфекционная активность при пониженной до 26°С температуре инкубации достигала 7,7 lg ЭИД50/мл, что свидетельствует о его безвредности для человека, поскольку по этим показателям он идентичен донору аттенуации А/Ленинград/134/17/57 (H2N2). Пятикратное пассирование вакцинного штамма не изменило его фенотипических свойств. Результаты фенотипического анализа представлены в табл. 4.

Безвредность для мышей. Доклинические исследования острой токсичности вакцинного штамма А/17/Гонконг/2017/75108 (H7N9) проводили на белых беспородных мышах в соответствии с Методическими рекомендациями по доклиническим испытаниям новых иммунобиологических препаратов [Методические рекомендации «Доклинические испытания эффективности и безопасности новых иммунобиологических лекарственных препаратов». М.: 2010. 39 с.] и с «Правилами надлежащей лабораторной практики» [Правила надлежащей лабораторной практики. Приказ Минздрава РФ №199н от 01.04. 2016. https://rg.ru/2016/09/02/minzdrav-prikaz199-site-dok.html]
Мышам вводили однократно одну человеческую дозу, соответствующую 0.5 мл, вакцинного вируса внутрибрюшинно в дозе 7.0 lg ЭИД50/мл. Животным контрольной группы вводили внутрибрюшинно физиологический раствор. Ежедневно в течение всего исследования (10 дней) проводился контроль общего состояния каждого животного.
Данные физиологического исследования (подвижность, поведенческие реакции, кинетика массы тела) показали, что внутрибрюшинное введение вакцинного штамма не вызывало гибели экспериментальных животных (табл. 5) и не приводило к изменению их внешнего вида, поведения, не отражалось на потреблении ими пищи и воды, что свидетельствует о безвредности вакцинного препарата.

1ВШ - вакцинный штамм А/17/Гонконг/2017/75108 (H7N9).
Безвредность и иммуногенность на хорьках.
Доклининческие исследования безвредности и иммуногенности вакцинного штамма А/17/Гонконг/2017/75108 (H7N9) также были проведены на хорьках, поскольку эта модель животных наиболее точно воспроизводит гриппозную инфекцию человека без предварительной адаптации (симптоматику, течение инфекции, распространение вируса в организме и индукцию иммунного ответа) [Langlois I. Viral diseases of ferrets. Vet Clin North Am Exot Anim Pract. 2005. Vol. 8. №1. Р. 139-160].
Данные исследования проводили в соответствии с Методическими рекомендациями по доклиническим испытаниям новых иммунобиологических препаратов [Методические рекомендации «Доклинические испытания эффективности и безопасности новых иммунобиологических лекарственных препаратов». М.: 2010. 39 с.], с «Правилами надлежащей лабораторной практики» [Правила надлежащей лабораторной практики. Приказ Минздрава РФ №199н от 01.04. 2016. https://rg.ru/2016/09/02/minzdrav-prikaz199-site-dok.html] и с Санитарно-эпидемиологическими правилами СП 2.2.1.3218-14 "Санитарно-эпидемиологические требования к устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев)" (утв. постановлением Главного государственного санитарного врача РФ №51 от 29.08. 2014).
Хорькам интраназально вводили по 0,5 мл в каждый носовой ход вакцинный вирус в дозе 7.0 lg ЭИД50/мл. Животным контрольной группы вводили интраназально физиологический раствор. Ежедневно в течение всего исследования проводился контроль общего состояния каждого животного.
Физиологическое исследование (подвижность, поведенческие реакции, кинетика массы тела и т.д.) вакцинированных хорьков показало, что иммунизация не вызывала гибель экспериментальных животных, каких-либо побочных эффектов и не приводила к физиологическим изменениям (изменение внешнего вида, поведения, потребления пищи и воды и т.д.).
Репродукцию вируса в верхних дыхательных путях оценивали на 1, 3 и 5 сутки после вакцинации, в легких - на 3 сутки. Пробы носовых смывов и легочной ткани анализировали на наличие вакцинного вируса путем их титрования в эмбриональных куриных яйцах. Анализ показал, что вакцинный штамм являлся аттенуированным для хорьков, поскольку размножался только в тканях верхних дыхательных путей, но не в легких (табл. 6).
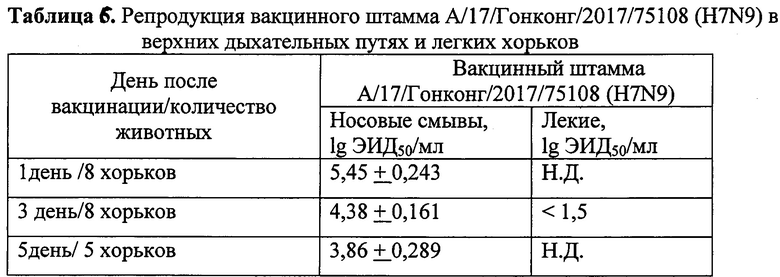
Н.Д. - не делали
Иммуногенность вакцинного штамма оценивали путем определения титров сывороточных антигемагглютинирующих антител через 4 недели после иммунизации.
Вакцинный реассортант А/17/Гонконг/2017/75108 (H7N9) был иммуногенным для хорьков: среднегеометрический титр антител в реакции торможения гемагглютинации с гомологичным антигеном и 1%-ными эритроцитами лошади превышал 200 гемагглютинирующих единиц
Полученные выше данные в эксперименте на хорьках свидетельствуют о безвредности и иммуногенности вакцинного штамма А/17/Гонконг/2017/75108 (H7N9).
Заключение
В результате проведенных доклинических исследований установлено, что заявляемый вакцинный штамм живой гриппозной вакцины А/17/Гонконг/2017/75108 (H7N9) характеризуется сочетанием полезных признаков, необходимых вакцинному штамму живой гриппозной вакцины: антигенной специфичностью эпидемического вируса А/Гонконг/4801/2014 (H3N2), структурой генома 6:2, оптимальной для реассортантных вакцинных штаммов, а также характерной для донора аттенуации температурочувствительностью и холодоадаптированностью, безвредностью, что коррелирует с аттенуацией для человека, а также обладает иммуногенностью для лабораторных животных.
Образец паспорта на вакцинный штамм А/17/Гонконг/2017/75108 (H7N9) прилагается.
Таким образом, вакцинный штамм А/17/Гонконг/2017/75108 (H7N9) по основным биологическим свойствам, изученным в доклинических экспериментах in vitro и in vivo, соответствует требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей (ФСП: ЛСР-002340/09-250309 изм. №2) на Ультрагривак® - вакцину для профилактики птичьего гриппа [живая].
Полученный штамм А/17/Гонконг/2017/75108 (H7N9) депонирован 18.01.2018 года в Государственную коллекцию вирусов ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России, Институт вирусологии им. Д.И. Ивановского (Россия RU, 123098, город Москва, улица Гамалеи, 16) под №2860 и имеет характеристики, представленные в образце паспорта штамма.
ХАРАКТЕРИСТИКА ШТАММА
Инфекционная активность штамма А/17/Гонконг/2017/75108 (H7N9) при репродукции в развивающихся куриных эмбрионах при 32°С в течение 48 часов - 8.7 lg ЭИД50/мл. Гемагглютинирующая активность - 1:256.
Штамм проявляет генетическую стабильность фенотипических признаков после 5 пассажей на куриных эмбрионах (при использовании больших заражающих доз).
Полезным свойством вакцинного штамма вируса гриппа А/17/Гонконг/2017/75108 (H7N9) является его пригодность для наработки живой гриппозной вакцины. Предлагаемый по изобретению вакцинный штамм вируса гриппа А/17/Гонконг/2017/75108 (H7N9) может быть использован для профилактики пандемического гриппа как у взрослых, так и у детей с трехлетнего возраста.
ПАСПОРТ ВАКЦИННОГО ШТАММА
1 Название штамма: А/17/Гонконг/2017/75108 (H7N9)
2 ИЭМ идентификационный №: НК 32/74/75/10/8
3 Серия: №1
4 Сероподтип: H7N9
5 Метод подготовки: классическая реассортация в куриных эмбрионах
6 Родительские вирусы
6.1 Эпидемический вирус: А/Гонконг /125/2017 (H7N9); CDC ID #3000687670
6.2 Донор аттенуации: А/Ленинград/134/17/57 (H2N2)
7 Число пассажей в процессе Е8 (Е7/Е1) скрещивание, два селективных пассажа,
реассортации: один слепой пассаж, три клонирования предельными
разведениями и одно накопление
8 Состав генома: Гены РВ2, РВ1, PA, NP, М и NS от донора аттенуации, НА
и NA - от эпидемического вируса (формула генома 6:2)
9 Характеристика штамма до лиофильной сушки
9.1 Оптимальные условия репродукции: 32°С, 48 часов
9.2 Гемагглютинирующая активность: 1:256 с 1.0% куриными эритроцитами
9.3 Инфекционная активность при оптимальной температуре 32°С: 8,7 lg ЭИД50/мл
9.4 ts маркер (температурочувствительность репродукции; инфекционная активность при температуре 40°С): ≤0,7 lg ЭИД50/мл (ts фенотип)
9.5 са маркер (холодоустойчивость репродукции; инфекционная активность при температуре 26°С): 7,7 lg ЭИД50/мл [са фенотип)
10 Характеристика штамма после лиофильной сушки
10.1 Дата лиофилизации: 03.08.2017 г.
10.2 Объем материала в ампуле: 0.5 мл
10.3 Инфекционная активность при оптимальной температуре 32°С: 8,7 lg ЭИД50/мл
10.4 Гемагглютинирующая активность: 1:128 с 1,0% куриными эритроцитами
11 Антигенная специфичность
11.1 Гемагглютинин: идентичен эпидемическому вирусу А/Гонконг/125/2017 (H7N9) по данным секвенирования и РТГА
11.2 Нейраминидаза: идентична эпидемическому вирусу А/Гонконг/125/2017 (H7N9) по данным секвенирования
12 Токсикологическое
исследование т vivo (острая
токсичность): не токсичен после внутрибрюшинного введения мышам
13 Контроль стерильности: стерилен (22.09.2017)
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ ВИРУСА ГРИППА А/17/Ануи/2013/61 (H7N9) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ИНТРАНАЗАЛЬНОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2013 |
|
RU2563351C2 |
| Реассортантный штамм вируса гриппа А/17/Гонконг/2019/2573 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2783894C1 |
| ШТАММ ВИРУСА ГРИППА ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ И ИНАКТИВИРОВАННОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2011 |
|
RU2464309C1 |
| Вакцинный штамм вируса гриппа А/17/ГОНКОНГ/2014/8296 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2016 |
|
RU2606019C1 |
| Вакцинный штамм вируса гриппа А/17/Южная Африка/2013/01 (H1N1)pdm09 для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2016 |
|
RU2627188C1 |
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА А/17/СИНГАПУР/2016/3571 (H3N2) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2018 |
|
RU2683500C1 |
| Вакцинный штамм вируса гриппа А/17/СЛОВЕНИЯ/2015/1121 (H1N1)pdm09 для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2724706C1 |
| Вакцинный штамм вируса гриппа А/17/Швейцария/2017/51 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2715674C1 |
| Реассортантный вакцинный штамм вируса гриппа А/17/Тасмания/2020/151 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2023 |
|
RU2825672C1 |
| Вакцинный штамм вируса гриппа А/17/КАНЗАС/2017/631 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2732610C1 |
Изобретение относится к области биотехнологии. Изобретение представляет собой штамм вируса гриппа А/17/Гонконг/2017/75108 (H7N9), депонированный в Государственную коллекцию вирусов ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России, Институт вирусологии им. Д.И.Ивановского под №2860. Заявленный штамм используется для производства живой интраназальной гриппозной вакцины для взрослых и для детей. 6 табл.
Штамм вируса гриппа А/17/Гонгонг/2017/75108 (H7N9), депонированный в Государственную коллекцию вирусов Института вирусологии им. Д.И. Ивановского ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России под №2860, используемый для производства живой интраназальной гриппозной вакцины для взрослых и для детей.
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА А/17/БРИСБЕН/07/1 (H3N2) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2010 |
|
RU2416640C1 |
| ЛАРИОНОВА Н.В | |||
| Возбудитель гриппа: изменчивость в природе и эксперименте, автореферат диссертации, Санкт-Петербург, 2017. | |||
Авторы
Даты
2019-04-16—Публикация
2018-06-08—Подача