Изобретение относится к медицинской вирусологии и может быть использовано в здравоохранении для профилактики заболеваемости гриппом среди взрослых и детей с помощью живой гриппозной интраназальной вакцины из штамма А/17/Гонконг/2019/2573 (H3N2) вируса гриппа А, семейства Orthomyxoviridae, рода Influenzavirus А.
В феврале 2020 ВОЗ (Всемирная организация здравоохранения) дала рекомендации по замене A/H3N2 компонента в составе противогриппозных вакцин для Северного полушария на 2020-2021 эпидемический сезон на А/Гонконг/2671/2019 (H3N2)-подобные вирусы [WHO. Recommended composition of influenza virus vaccines for use in the 2020 - 2021 northern hemisphere influenza season. 28 February 2020. https://wvvw.whoint/publications/m/item/recommended-composition-of-infiuenza-virus-vaccines-for-use-in-the-2020-2021-northern-hemisphere-influenza-season], затем в сентябре 2020 данный вирус был рекомендован в качестве A/H3N2 компонента в составе противогриппозных вакцин и для Южного полушария на эпидемический сезон 2021 [WHO. Recommended composition of influenza virus vaccines for use in the 2021 southern hemisphere influenza season. 25 September 2020. https://www.who.int/publications/m/item/recommended-composition-of-influenza-virus-vaccines-for-use-in-the-2021-southern-hemisphere-influenza-season].
В результате появления в циркуляции нового эпидемического штамма вируса гриппа А/Гонконг/2671/2019 (H3N2), известный вакцинный штамм А/17/Канзас/2017/631 (H3N2) - прототип [Степанова Е.А., Крутикова Е.В., Баженова Е.А., Ларионова Н.В., Киселева И.В., Котомина Т.С., Исакова-Сивак И.Н., Руденко Л.Г. Вакцинный штамм вируса гриппа А/17/Канзас/2017/631 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей. Патент РФ №2732610 от 20.09.2020 - Опубл. БИ 2020. - №27] - утратил антигенную актуальность и вследствие этого не может вызвать защитную реакцию во время эпидемии, вызванной А/Гонконг/2671/2019-подобными штаммами вируса гриппа.
Задачей, на решение которой направлено заявляемое изобретение, является получение антигенно актуального вакцинного штамма для взрослых и для детей на основе холодоадаптированного донора аттенуации А/Ленинград/134/17/57 (H2N2) и нового эпидемического вируса А/Гонконг/2671/2019 (H3N2).
Применяемые в настоящее время штаммы для живых гриппозных вакцин получают методом генетической реассортации эпидемически актуальных вирусов с холодоадаптированными, безвредными для человека штаммами - донорами аттенуации [Александрова Г.И. Применение метода генетической рекомбинации для получения вакцинных штаммов вируса гриппа // Вопр. Вирусол - 1977.- №4,- С. 387-395.].
Донор аттенуации А/Ленинград/134/17/57 (H2N2) - холодоадапти-рованный (са) и температурочувствительный (ts) штамм вируса гриппа -разрешен для получения живых интраназальных вакцин для взрослых и детей [Александрова Г.И. Новое в эпидемиологии и профилактике вирусных инфекций. Л. Д968. - С. 66-83].
Цель реассортации - получить штамм с вакцинной формулой генома 6:2 - два гена, кодирующих поверхностные белки вируса гриппа гемагглютинин (НА) и нейраминидазу (NA), наследуются от антигенно актуального циркулирующего эпидемического штамма, а шесть генов, кодирующих внутренние и неструктурные белки (РВ2, РВ1, PA, NP, М, NS) -от донора аттенуации.
Получение вакцинного штамма.
Вакцинный штамм А/17/Гонконг/2019/2573 (H3N2) получен методом генетической реассортации эпидемического вируса А/Гонконг/2671/2019 (H3N2) с донором аттенуации А/Ленинград/134/17/57 (H2N2) путем одновременного инфицирования развивающихся куриных эмбрионов (РКЭ) смесью родительских вирусов в эквивалентных инфекционных дозах, с последующей селекцией при пониженной до 26°С температуре инкубации в присутствии кроличьей антисыворотки к донору аттенуации. Клоны дополнительно очищены тремя последовательными клонированием методом предельных разведений в присутствии антисыворотки к донору при пониженной (26°С) и оптимальной (32°С) температурах инкубации. Выбранный чистый клон проверен по фенотипическим характеристикам {ts- и ca-фенотип) и по формуле генома на соответствие вакцинному штамму.
Антигенная характеристика вакцинного штамма.
Изучение антигенных свойств вакцинного штамма А/17/Гонконг/2019/2573 (H3N2) показало, что ответственный за антигенную специфичность поверхностный белок вакцинного штамма - гемагглютинин (НА) - в перекрестной РТГА с гомологичной сывороткой антигенно идентичен эпидемическому вирусу А/Гонконг/2671/2019 (H3N2), поскольку показатели взаимодействия реассортанта А/17/Гонконг/2019/2573 (H3N2) и родительского штамма А/Гонконг/2671/2019 (H3N2) с крысиными антисыворотками, полученными к эпидемическому вирусу А/Гонконг/2671/2019 (H3N2) и к вакцинному реассортанту А/17/Гонконг/2019/2573 (H3N2), полностью совпадали (табл. 1).
Второй ответственный за антигенную специфичность поверхностный белок вакцинного штамма - нейраминидаза (NA) - проверен методом частичного и полногеномного секвенирования, подтвердившими его идентичность эпидемическому родительскому вирусу
А/Гонконг/2671/2019 (H3N2).

Для анализа состава генома полученных реассортантов использовали частичное секвенирование ДНК копий генов [Isakova-Sivak I. et. al. Development and pre-clinical evaluation of two LAIV strains against potentially pandemic H2N2 influenza virus. PLoS One. 2014. Vol. 9. №7. P. e102339].
Результаты анализа всех генов вакцинного штамма А/17/Гонконг/2019/2573 (H3N2) представлены в табл.2. Установлено, что формула генома вакцинного штамма А/17/Гонконг/2019/2573 (H3N2) - 6:2, что соответствует требованиям, предъявляемым к штаммам живой гриппозной вакцины: гены, кодирующие поверхностные белки гемагглютинин (НА) и нейраминидазу (NA) принадлежат эпидемическому родительскому вирусу А/Гонконг/2671/2019 (H3N2), гены, кодирующие внутренние белки (РВ2, РВ1, PA, NP, М, NS), унаследованы от донора аттенуации А/Ленинград/134/17/57 (H2N2).
Данные, полученные при отборе вакцинного кандидата, были подтверждены полным секвенированием его генома и показали, что вакцинный штамм А/17/Гонконг/2019/2573 (H3N2) унаследовал все 6 генов, кодирующих внутренние и неструктурные белки, от донора аттенуации А/Ленинград/134/17/57 (H2N2) (табл. 2).

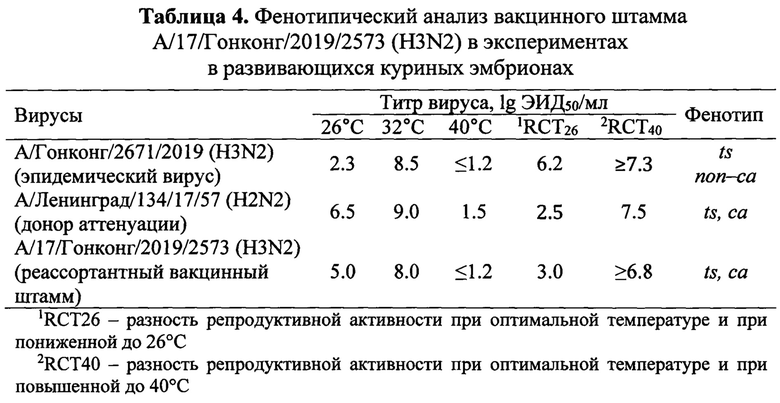
Генетическую стабильность кодирующих мутаций вакцинного штамма А/17/Гонконг/2019/2573 (H3N2) изучали сравнением сохранности кодирующих мутаций до и после пятикратного пассирования вакцинного штамма, подготовленного на основе донора аттенуации А/Ленинград/134/17/57, в куриных эмбрионах с использованием метода пиросеквенирования. Для данного анализа были разработаны специфические праймеры, позволяющие оценивать наличие данных мутаций с использованием пиросеквенатора PyroMark Q24. Праймеры разработаны с использованием компьютерной программы PSQ Assay Design. На фиг.1 приведен пример пирограммы, полученной для фрагмента гена РА, содержащего аттенуирующую мутацию в позиции 1045 у донора аттенуации А/Ленинград/134/17/57 (H2N2). Аттенуирующая замена G-1045-T, приводит к замене Val-341-Leu. Чтение нуклеотидов происходит с комплементарной цепи. Присутствие замены характеризуется отсутствием пика в четвертой позиции и увеличенным пиком в третьей позиции. В результате пиросеквенирования вируса А/Ленинград/134/57 (H2N2) - эпидемического предшественника донора аттенуации, не обладающего аттенуирующей мутацией, пики в третьей (А) и четвертой (С) позициях одинаковой высоты (фиг. 1, фрагмент А). Наличие аттенуирующей мутации С→А характеризуется пиком увеличенной высоты в третьей позиции (А) и отсутствием пика в четвертой позиции (С), что можно увидеть на пирограмме, полученной для донора аттенуации А/Ленинград/134/17/57 (H2N2) (фиг. 1, фрагмент Б), а также на пирограмме, полученной для гена РА вакцинного штамма А/17/Гонконг/2019/2573 (H3N2) (фиг. 1, фрагмент В).
В таблице 3 приведены результаты пиросеквенирования всех фрагментов генов вакцинного штамма А/17/Гонконг/2019/2573 (H3N2), содержащих аттенуирующие мутации, соответствующие донору аттенуации А/Ленинград/134/17/57 (H2N2), до и после пятикратного пассирования в развивающихся куриных эмбрионах. Все кодирующие нуклеотидные замены, охарактеризованные для донора аттенуации А/Ленинград/134/17/57 (H2N2) как ответственные за его аттенуацию (табл.3), присутствуют во внутренних генах реассортантного штамма А/17/Гонконг/2019/2573 (H3N2) и не утрачиваются в процессе пассирования.
Таким образом, анализ генома вакцинного штамма А/17/Гонконг/2019/2573 (H3N2) показал генетическую стабильность его аттенуирующих мутаций.

Оценку фенотипических свойств реассортантного штамма А/17/Гонконг/2019/2573 (H3N2), проводили путем его параллельного титрования в РКЭ при разных температурах. Вакцинный штамм А/17/Гонконг/2019/2573 (H3N2) в развивающихся куриных эмбрионах обладает выраженным температурочувствительным и холодоадаптиро-ванным фенотипом, идентичным фенотипу донора аттенуации А/Ленинград/134/17/57 (H2N2). Установлено, что вакцинный вирус является температурочувствительным (ts фенотип) - его инфекционная активность при температуре 40°С составила ≤1.2 log10 ЭИД50/мл, и холодоадаптированным (са фенотип) - инфекционная активность при пониженной до 26°С температуре инкубации достигала 5.0 log10 ЭИД50/мл, что свидетельствует о его безвредности для человека, поскольку по этим показателям он идентичен донору аттенуации А/Ленинград/134/17/57 (H2N2). Результаты фенотипического анализа представлены в таблице 4.
Безвредность для мышей. Доклинические исследования острой токсичности вакцинного штамма А/17/Гонконг/2019/2573 (H3N2) проводили на белых беспородных мышах в соответствии с Руководством по проведению доклинических исследований лекарственных средств [Руководство по проведению доклинических исследований лекарственных средств (Иммунобиологические лекарственные препараты); Часть вторая. - М.: Гриф и К, 2012. - 536 с] и с «Правилами надлежащей лабораторной практики» [Правила надлежащей лабораторной практик. Приказ Минздрава РФ №199н от 01.04.2016. https://rg.ru/2016/09/02/minzdrav-prikaz199-site-dok.html]
Мышам вводили однократно внутрибрюшинно одну человеческую дозу, соответствующую 0.5 мл вакцинного вируса в дозе 7.0 lg ЭИД50/мл. Животным контрольной группы вводили внутрибрюшинно физиологический раствор. Ежедневно в течение всего исследования (7 дней) проводился контроль общего состояния каждого животного.
Данные физиологического исследования (подвижность, поведенческие реакции, кинетика массы тела) показали, что внутрибрюшинное введение вакцинного штамма не вызывало гибели экспериментальных животных (табл. 4) и не приводило к изменению их внешнего вида, поведения, не отражалось на потреблении ими пищи и воды, что свидетельствует о безвредности вакцинного препарата.

В результате проведенных доклинических исследований установлено, что заявляемый вакцинный штамм живой гриппозной вакцины А/17/Гонконг/2019/2573 (H3N2) характеризуется сочетанием полезных признаков, необходимых вакцинному штамму: антигенной специфичностью актуального эпидемического вируса А/Гонконг/2671/2019 (H3N2), структурой генома 6:2, оптимальной для реассортантных вакцинных штаммов, а также характерной для донора аттенуации температуро-чувствительностью и холодоадаптированностью и безвредностью для лабораторных животных, что коррелирует с аттенуацией для человека.
Таким образом, вакцинный штамм А/17/Гонконг/2019/2573 (H3N2) по основным биологическим свойствам, изученным в доклинических экспериментах in vitro и in vivo, соответствует требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей (ФСП: Р N003224/01-270313) на Ультравак®, вакцину гриппозную аллантоисную живую для интраназального применения для взрослых и для детей.
Полученный штамм А/17/Гонконг/2019/2573 (H3N2) депонирован 11.11.2020 года в Государственную коллекцию вирусов ФГБУ «ФНИЦЭМ им. Н.Ф. Гамалеи Минздрава России Институт вирусологии им. Д.И. Ивановского под №2962 и имеет характеристики, представленные в образце паспорта штамма.
ХАРАКТЕРИСТИКА ШТАММА
Инфекционная активность штамма А/17/Гонконг/2019/2573 (H3N2) при репродукции в развивающихся куриных эмбрионах при 32°С в течение 48 часов - 8.0 log10 ЭИД50/мл. Гемагглютинирующая активность - 1:256.
Штамм проявляет генетическую стабильность фенотипических признаков после 5 пассажей на куриных эмбрионах (при использовании больших заражающих доз).
Полезным свойством вакцинного штамма вируса гриппа А/17/Гонконг/2019/2573 (H3N2) является его пригодность для наработки живой гриппозной вакцины. Предлагаемый по изобретению вакцинный штамм вируса гриппа А/17/Гонконг/2019/2573 (H3N2) может быть использован для профилактики гриппа как у взрослых, так и у детей с трехлетнего возраста.

| название | год | авторы | номер документа |
|---|---|---|---|
| Реассортантный вакцинный штамм вируса гриппа А/17/Тасмания/2020/151 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2023 |
|
RU2825672C1 |
| Реассортантный вакцинный штамм вируса гриппа А/17/Мичиган/2020/484 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2023 |
|
RU2825583C1 |
| Реассортантный вакцинный штамм вируса гриппа А/17/Дарвин/2021/410 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2023 |
|
RU2825673C1 |
| Вакцинный штамм вируса гриппа А/17/БРИСБЕН/2018/3610 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2734897C1 |
| Вакцинный штамм вируса гриппа А/17/КАНЗАС/2017/631 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2732610C1 |
| Вакцинный штамм вируса гриппа А/17/ГОНКОНГ/2014/8296 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2016 |
|
RU2606019C1 |
| Реассортантный штамм вируса гриппа А/17/Ньюкасл/2018/22 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2783887C1 |
| Вакцинный штамм вируса гриппа А/17/БРИСБЕН/2017/7178 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2711101C1 |
| Реассортантный штамм вируса гриппа А/17/Виктория/2019/276 (H1N1) pdm09 для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2783878C1 |
| Вакцинный штамм вируса гриппа А/17/Швейцария/2017/51 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2715674C1 |
Изобретение относится к медицинской вирусологии. Предложен вакцинный штамм А/17/Гонконг/2019/2573 (H3N2) - реассортант, полученный путем скрещивания эпидемического вируса А/Гонконг/2671/2019 (H3N2) с холодоадаптированным температурочувствительным вирусом А/Ленинград/134/17/57 (H2N2) - донором аттенуации, безвредным для людей. Предложенный штамм может быть использован для производства живой гриппозной интраназальной вакцины для взрослых и для детей. 1 ил., 5 табл.
Реассортантный штамм вируса гриппа А/17/Гонконг/2019/2573 (H3N2), депонированный в Государственную коллекцию вирусов Института вирусологии им. Д.И. Ивановского ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России под №2962, для производства живой гриппозной интраназальной вакцины для взрослых и для детей.
| Вакцинный штамм вируса гриппа А/17/КАНЗАС/2017/631 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2732610C1 |
| Вакцинный штамм вируса гриппа А/17/ГОНКОНГ/2014/8296 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2016 |
|
RU2606019C1 |
| КИСЕЛЕВА И.В | |||
| И ДР | |||
| Особенности реассортации современных штаммов вируса гриппа с донорами аттенуации живой гриппозной вакцины | |||
| Вопросы вирусологии, 2013, Т | |||
| Способ окисления боковых цепей ароматических углеводородов и их производных в кислоты и альдегиды | 1921 |
|
SU58A1 |
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
| Найдено онлайн: https://www.elibrary.ru/download/elibrary_20502174_27123238.pdf Дата обращения 07.10.2022 | |||
| GROHSKOPF | |||
Авторы
Даты
2022-11-21—Публикация
2022-04-15—Подача