Изобретение относится к области медицины, а именно, к онкологической гинекологии, и представляет собой способ диагностики серозного рака яичников (РЯ) высокой степени злокачественности (high grade) с помощью анализа содержания липидов в сыворотке крови методом высоко эффективной хроматографии масс-спектрометрии (ВЭЖХ МС). Изобретение может быть использовано для диагностики РЯ в качестве дополнения или замены имеющихся методов в ходе лабораторного анализа сыворотки крови.
В то время, как популяционный скрининг экономически не выгоден, выявление более ранних стадий (I-II стадии по международной классификации Международной федерации гинекологов и акушеров - FIGO, International Federation of Obstetrics and Gynaecology) заболевания ассоциировано с улучшением исходов, однако, сопряжено с существенными сложностями в связи с асимптомным или малосимптомным течением, в связи с чем рак яичников диагностируется на поздних стадиях, выживаемость при которых не превышает 44%, что практически в 2 раза ниже по сравнению с 90% пятилетней выживаемостью после радикального лечения заболевания, выявленного на ранней стадии [1], [2]. Вопрос по проблеме остается открытым и требует усилий по изучению диагностики заболевания, особенном посредством неинвазивных методов, - в связи с чем акцент многих исследований сделан на жидкостной биопсии при образованиях яичников.
По данным интерактивной платформы GLOBOCAN и Центра контроля и профилактики заболеваний США, РЯ занимает седьмое место в структуре заболеваемости ЗНО в мире, восьмое место - в структуре смертей, обусловленных онкологическими заболеваниями у женщин, и второе место - в структуре смертей, обусловленных ЗНО репродуктивных органов, уступая первенство раку шейки матки [2], [3], [4]. Смертность от ЗНО яичников в США и Российской Федерации занимает первое место, опережая опухоли остальных органов репродуктивной системы за исключением молочной железы [5], [6]. Возраст 80-90% заболевших составляет 20-65 лет [7]. Благодаря достижениям последних 30 лет в области онкологии (внедрение скрининговых программ, внедрение инновационных подходов в хирургии, внедрение новых лекарственных средств., и др.) при многих ЗНО наблюдается повышение пятилетней выживаемости на 20% [3], [5]. Однако данная тенденция наименее заметна для опухолей яичников, что связано с отсутствием эффективных мер, направленных на выявление РЯ на ранних стадиях, - в 75% случаев диагноз устанавливается на III-IV стадиях заболевания [7-9].
Таким образом, на сегодняшний день очевидна необходимость разработки новых более точных методов диагностики, поскольку прогноз значительно более благоприятен при выявлении заболевания на более ранней стадии.
Одним из самых перспективных подходов для диагностики данного онкологического заболевания на сегодняшний день является метаболомный анализ, осуществляемый методами масс-спектрометрии. Метаболомный подход включает комбинированное использование хроматографических, спектрометрических и спектроскопических методов анализа образцов совместно со статистической и биоинформатической обработкой экспериментальных данных. Анализ и интерпретация данных предполагают методы создания мультипараметрических классификационных моделей для проверки диагностической точности выявленных биомаркеров [10]. Ряд липидов обладают опухоль-инициирующей активностью, в связи с чем был введен термин «онколипид» [11]. Было показано, что высокое содержание разнообразных онколипидов в микроокружении опухоли отображает их способность инициировать и поддерживать процессы инвазии [11-13]. К сожалению, на сегодняшний день отсутствуют адекватные способы высокоточной ранней и предоперационной диагностики РЯ (I-II стадии по классификации Международной федерации гинекологов и акушеров - FIGO), поэтому очевидна необходимость разработки неинвазивных и объективных методов диагностики.
Вследствие недостаточной информативности какого-либо одного биомаркера, необходимо рассматривать возможность выявления набора веществ, отличающих одно состояние пациента от другого. Масс-спектрометрические подходы для определения изменений липидома крови характеризуются малыми временами и относительной простотой приготовления образцов, а также высокой информативностью получаемых результатов. Регистрируемые в процессе эксперимента характеристические масс-спектры, называемые также "отпечатки пальцев" (fingerprints), позволяют создать классификационную модель для отнесения данного образца сыворотки или плазмы крови к группе нормы или патологии. Внедрение предлагаемого метода в практическое здравоохранение позволит создать персонифицированные алгоритмы обследования и ведения пациенток с раком яичников.
В качестве прототипа предлагаемого метода использован способ, описанный в исследованиях М. Hilvo и соавт. Авторами было установлено повышение уровня гидроксибутиратов (2,4-дигидроксибутира, 3,4-дигидроксибутират) в сыворотке крови пациентов с раком яичников высокой степени злокачественности по сравнению с образцами группы контроля, а также предположено прогностическое значение данного потенциального маркера [14], [15]. Ограничением данного и многих других проведенных исследований является преобладание в структуре исследуемых пациентов с III-IV стадиями, что сужает спектр возможностей настоящего метода диагностики.
М.F. Buas и соавт. провели исследование «случай-контроль», в процессе которого проанализировали по 50 образцов плазмы крови пациентов, подвергшихся оперативному лечению по поводу объемного образования яичников серозного гистотипа (рака или доброкачественной опухоли (группа контроля)). Образцы были исследованы с помощью ВЭЖХ МС. Было обнаружено, что 34 метаболита из 372 обнаруженных статистически значимо отличались в группах. Авторы пришли к выводу, что выявленные отличия метаболического профиля могут способствовать повышению точности дифференциальной диагностики доброкачественных и злокачественных заболеваний яичников [16]. После исключения образцов плазмы пациентов, у которых не был исследован маркер СА-125, в исследовании осталось лишь 84 образца (рак яичника, 44; доброкачественные опухоли в группе контроля, 40). В исследование были включены только женщины постменопаузального возраста, что следует отнести к важному ограничению дизайна рассматриваемого исследования. Помимо этого, использование крови пациентов с наличием доброкачественного объемного образования яичников в качестве группы контроля не исключает «химеризм» липидного профиля, который может быть характерен для каждого заболевания [17]. В связи с чем более информативные и точные данные могут быть получены при сравнении с исследуемой группой пациентов, при скрининго-диагностическом обследовании которых не получено данных об объемных образованиях яичников («здоровые добровольцы»).
Также принципиальной особенностью, которую следует учитывать при планировании исследования, посвященного разработке метода, направленного на выявление серозного РЯ высокой степени злокачественности, является этапность исследования, которая заключается в возможности выявить группу пациентов с злокачественным процессом, радикально отличимую от пациентов группы контроля, состоящей из обследованных с исключенной патологией, затем, вторым этапом, необходимо провести внутригрупповое сравнение (I-II по сравнению с прогрессирующими III-IV), чтобы различить пациентов с более ранними стадиями I-II и пациентов группы контроля. Данная последовательность позволяет дифференцировать более ранние стадии заболевания от нормы и прогрессирующих стадий серозного РЯ высокой степени злокачественности.
Задачей, решаемой изобретением, является диагностика I-II стадий серозного рака яичников высокой степени злокачественности по липидному профилю сыворотки крови посредством ВЭЖХ МС в результате последовательного применения двух моделей, построенных на основании метода логистической регрессии для вычисления переменной отклика (у'): на первом этапе с учетом уровней 3 липидов рассчитывается переменная отклика y'1 (при значении 0<y'1<0.7 делают заключение о том, что пациент относится к группе контроля, при значении 0.7≤у'1<1 диагностируется серозный рак яичника), на втором этапе при помощи подстановки уровней 2 липидов рассчитывается переменная отклика у'2 (при значении 0.6≤<у'2<1 делают заключение о наличии у пациента распространенного серозного РЯ III-IV стадий, при значениях 0<у'2<0.6 - I-II стадий заболевания), позволяющая выявить пациентов с ранними стадиями серозного рака яичников.
Поставленная задача решается предлагаемым способом, заключающимся в подготовке экстракта липидов образцов сыворотки крови пациентов с известным гистологическим диагнозом модифицированным посредством метода Фолча; разделении полученных экстрактов с помощью обращенно-фазовой жидкостной хроматографии и получении масс-спектров высокого разрешения методом ионизации электрораспылением (ИЭР) в режиме положительных ионов на коммерческом масс-спектрометре с разрешением более 10000 и точностью определения массы не хуже, чем 5-10 ppm; идентификации липидов в соответствии с их точными массами и МС/МС спектрами; отборе статистически значимых липидов, дифференцирующих образцы крови наблюдаемых группы контроля и пациентов с серозным раком яичников с использованием непараметрического теста Манна-Уитни (при величине p-value ≤ 0,05 различие принимали за статистически значимое); в выборе липидов, имеющих статистически значимые различия уровней в образцах крови пациентов с серозным РЯ I-II стадий и пациентов с серозным РЯ III-IV стадий; выборе липидов при помощи информационного критерия Акаике (ИКА) для построения моделей для двухэтапного анализа, первая из которых дифференцирует образцы крови наблюдаемых группы контроля и пациентов с серозным раком яичников, вторая - образцы крови пациентов с I-II и III-IV стадиями заболевания; удалении переменных (липидов), не удовлетворяющих условию статистически значимого неравенства их коэффициентов нулю (граница значимости равенства нулю α=0,05); вычислении на основании ROC-анализа граничного значения переменной отклика; вычислении значений переменных отклика для классификации новых образцов и отнесения образцов к группе контроля или рака яичников на первом этапе (y'1) и к группе РЯ I-II стадий или РЯ III-IV стадий на втором (у'2).
Отбор статистически значимых липидов, дифференцирующих образцы крови наблюдаемых группы контроля и пациентов с серозным раком яичников с использованием непараметрического теста Манна-Уитни. Вычисление вероятности равенства уровней липидов осуществлялось в следующей последовательности действий.
Для каждого липида вычисляют критерий Манна-Уитни по формуле:
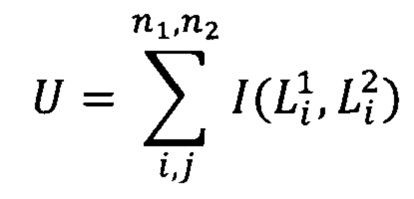
где n1 и n2 - размеры выборок 1 и 2, i, j - порядковые номера образцов в выборках 1 и 2, I1i и I2i - площади пиков из выборки 1 и 2. F - функция, возвращающая 1 в случае I1i и I2i больше I2i, - 1 - в случае 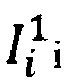 меньше
меньше 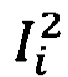 , 0 - в случае равенства.
, 0 - в случае равенства.
Вычисляют нормированный критерий Манна-Уитни:
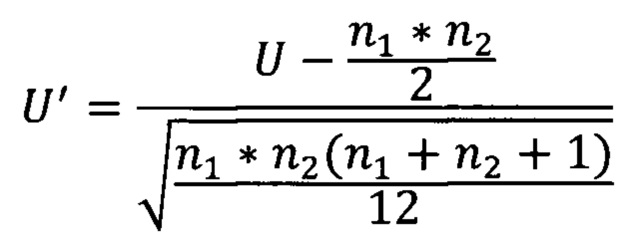
Вычисляют вероятность равенства нулю:
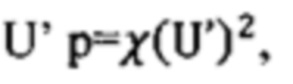
где χ(U')2 - распределение квадрата независимой стандартной нормальной случайной величины.
При вероятности равенства нулю липид относят к статистически значимым (р<0,05).
Выбор липидов в финальные модели для разделения образцов группы контроля и группы с серозным РЯ и для разделения группы с серозным РЯ I-II стадий и серозным РЯ III-IV стадий осуществлялся выбором по одному из соединений, приводящих к минимизации ИКА [18] на каждой итерации отбора переменных по алгоритму, содержащем в себе этапы расчета ИКА (шаг 1), выбора максимального ИКА (шаг 2) и сравнения старого и нового ИКА (шаг 3).
Шаг 1. Произвольно выбирают переменную из набора переменных, сформированного на основе теста Манна-Уитни. Далее следует этап расчета ИКА.
1) Строят лог-функция правдоподобия:
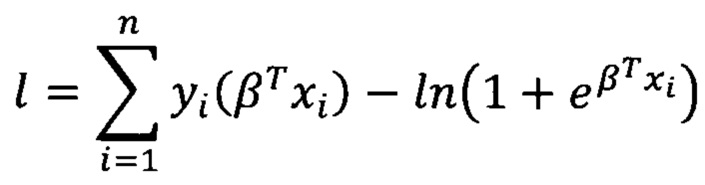
где yi - переменная отклика, принимающая значения 0 или 1, xi - объединенный вектор единицы и независимых переменных, β - объединенный вектор свободного члена и коэффициентов при переменных.
2) Выполняют дифференцирование функции по β, получают уравнение:

3) Рассчитывают вторую производную:
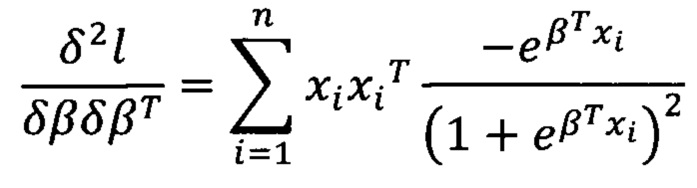
4) На основе метода Ньютона-Рафсона рассчитывают вектор β:
βk+1=βk-(XTWX)-1XT(y-р),
где k - номер итерации, X - матрица единичного вектора и независимых переменных, W - диагональная матрица с элементами 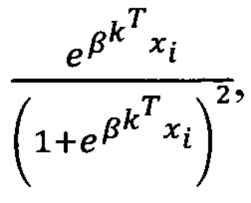 у - вектор переменной отклика и р - вектор вероятности
у - вектор переменной отклика и р - вектор вероятности 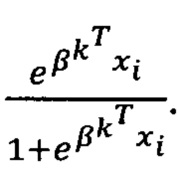 Вычисление βk происходит, пока
Вычисление βk происходит, пока 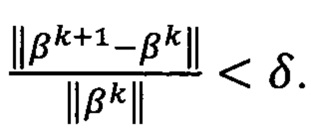 Относительная разница модулей векторов между итерациями от нуля δ=0,01.
Относительная разница модулей векторов между итерациями от нуля δ=0,01.
5) Подставляют вычисленные значения в лог-функцию правдоподобия из п. 1).
6) Рассчитывают информационный критерий по формуле:
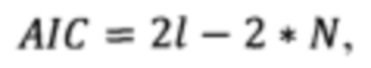
где AIC - информационный критерий Акаике, N - число независимых переменных, задействованных в регрессиях.
Шаг 2. Повторяют шаг 1 для всех m переменных.
Шаг 3. Выбирают переменную, для которой рассчитанное значение AIC будет максимальным (шаг 2). Обозначим это значение как AIC.
Шаг 4. Выполняют 1 и 2 шаги для комбинации «выбранная ранее переменная + каждая из оставшихся переменных».
Шаг 5. Сравнивают AIC со значением AIC (шаг 3).
Шаг 6. Если AIC из п. 5 больше AIC, повторяют Этапы 1-3, имея в качестве постоянных переменных переменные, отобранные ранее, и обозначив как AIC значение из п. 5., если AIC из п. 5 меньше AIC, п. 7.
Шаг 7. Переменные, при которых было получено AIC и рассчитанные для них коэффициенты, используют дальше.
Проверку переменных с удалением не удовлетворяющих условию статистически значимого неравенства их коэффициентов нулю выполняют следующим образом:
1. с использованием выбранных ранее переменных строится лог-функция правдоподобия:
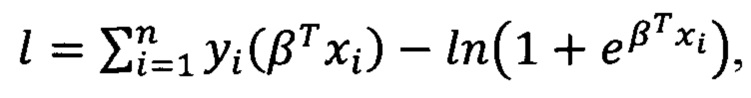 где yi - переменная отклика, принимающая значения 0 или 1, xi - объединенный вектор единицы и независимых переменных, β - объединенный вектор свободного члена и коэффициентов при переменных;
где yi - переменная отклика, принимающая значения 0 или 1, xi - объединенный вектор единицы и независимых переменных, β - объединенный вектор свободного члена и коэффициентов при переменных;
2. выполняют дифференцирование функции по β, получая уравнения:

3. рассчитывают вторую производную:
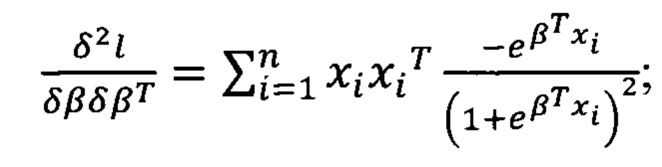
4. рассчитывают вектор β на основе метода Ньютона-Рафсона:
βk+1=βk-(xTWX)-1XT(y-р);
где k - номер итерации, X - матрица единичного вектора и независимых переменных, W - диагональная матрица с элементами 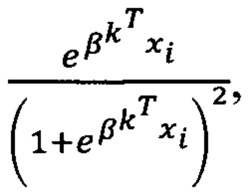 у - вектор переменной отклика и р - вектор вероятности
у - вектор переменной отклика и р - вектор вероятности 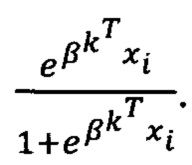 Вычисление βk происходит, пока
Вычисление βk происходит, пока 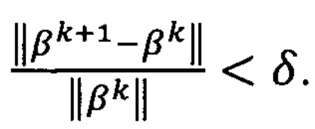 Относительная разница модулей векторов между итерациями от нуля δ=0,01.
Относительная разница модулей векторов между итерациями от нуля δ=0,01.
5. подставляют вычисленные значения β в матрицу 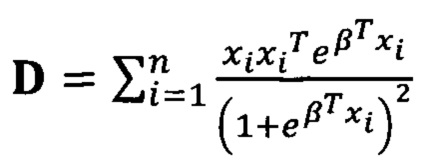 и вычисляют значения стандартной ошибки для коэффициента
и вычисляют значения стандартной ошибки для коэффициента 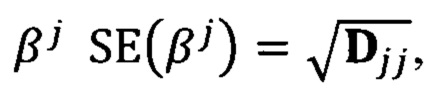 где j - порядковый номер коэффициента в векторе β;
где j - порядковый номер коэффициента в векторе β;
6. вычисляют вероятность равенства нулю коэффициента 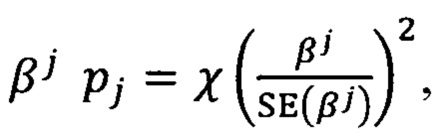 где χ(U')2 - распределение квадрата независимой стандартной нормальной случайной величины: если существует pi>α, где α - некая критическая величина и i>0, то переменная, соответствующая pi, исключается из задействованного набора переменных и действия 1-6 повторяются (граница значимости равенства нулю α=0,05).
где χ(U')2 - распределение квадрата независимой стандартной нормальной случайной величины: если существует pi>α, где α - некая критическая величина и i>0, то переменная, соответствующая pi, исключается из задействованного набора переменных и действия 1-6 повторяются (граница значимости равенства нулю α=0,05).
Граничные значения переменной отклика вычисляют на основании ROC-анализа результатов перекрестного контроля, выполненного с использованием разбиения данных «тренировка» / «тест» 70/30 с 100-кратным повтором. В качестве граничного значения переменной отклика у' используется значение, при котором максимизируется сумма значений чувствительности и специфичности.
Для классификации образцов вычисляют значение у' с использованием формулы:
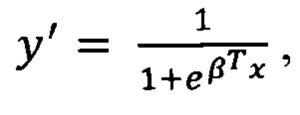
где у' - переменная отклика, Р - вектор коэффициентов, вычисленный ранее, х - вектор формата (интенсивность липидов-маркеров). Данное уравнение было использовано для расчета переменной отклика у'1 на первом этапе и у'2 на втором этапе.
Итоговую классификация выполняют по результатам сравнения y'1 и у'2 с их граничными значением у' для данной модели.
Способ был реализован на масс-спектрометре Maxis Impact qTOF (Bruker Daltonics, Бремен, Германия), который имеет типичный для современных масс-спектрометров входной интерфейс для работы с источниками ионизации при атмосферном давлении, в частности электроспрейного источника ИЭР. Экстракты липидов получали модифицированным методом Фолча: к 40 мкл образца добавляется 480 мкл смеси хлороформ-метанол 2:1, об/об; смесь инкубируется 10 мин, добавляется 150 мкл воды, центрифугируется при 13000 g при комнатной температуре; органический нижний слой, содержащий липиды, высушивается в потоке азота и растворяется в смеси ацетонитрил-2-пропанол, 1:1, об/об. Для стабильного электрораспыления липидного экстракта образца устанавливали оптимальные параметры, которые зависят от модели прибора. В случае масс-спектрометра Maxis Impact использовались следующие параметры: напряжение на капилляре 4.1 кВ, давление распыляющего газа 0.7 бар, скорость потока осушающего газа 6 л/мин, температура осушающего газа 200°С; на высокоэффективном жидкостном хроматографе Dionex UltiMate 3000 (Thermo Scientific, Гермеринг, Германия, колонка Zorbax XDB-C18 (250 × 0.5 мм, 5 мкм; Agilent, США) поддерживалась температура 50°С, скорость потока 35 мкл/мин. Для хроматографического разделения в качестве растворителя А используется вода/ацетонитрил (40/60, о/о) с 0,1% муравьиной кислоты и 10 ммоль/k формиата аммония, в качестве растворителя В используется изопропанол / ацетонитрил/вода (90/8/2, о/о/о) с 0,1% муравьиной кислоты и 10 ммоль/Л формиата аммония. Доля растворителя В меняется по закону линейного градиента от 30 до 95% (о/о) в течение 25 минут. Сигнал записывается в течение 31 минуты: 3 минуты при 30% В, в течение 25 минут линейного изменения доли В и 3 минуты при 95% В. Масс-спектры регистрируются с частотой 2 Гц, то есть 360 спектров за 3 минуты. Диапазон масс m/z 400-1000. Тандемная МС проводится методом результат-зависимого анализа - DDA - со следующими параметрами: три наиболее интенсивных пика выбираются после полного сканирования всего диапазона масс и подвергаются фрагментации посредством столкновительной диссоциации с энергией 35 эВ, время исключения иона из анализа составило 1 минуту. Полученные масс-спектрометрические данные подверглись предобработке и последующей статистической обработке согласно последовательности действий вышеописанного способа. Статистическую обработку полученных экспериментальных данных проводили с помощью скриптов, написанных на языке R в RStudio [19], [20]. В результате для первого этапа отнесения пациентов к группе контроля или к группе больных раком яичников была разработана формула расчета переменной отклика y'1 на основании отобранных липидов SM d16:1/14:0, PC 12:0_18:1 и PC 18:2_20:3 (номенклатура липидов соответствует LipidMaps [21]):
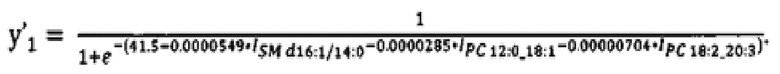
Для определения среди пациентов больных раком яичником стадии прогрессирования заболевания (I-II или III-IV) была разработана формула расчета переменной отклика у'2 на основании отобранных липидов PC Р-16:0/18:1 и PC Р- 16:0/18:2:
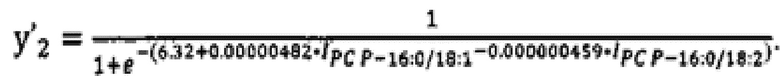
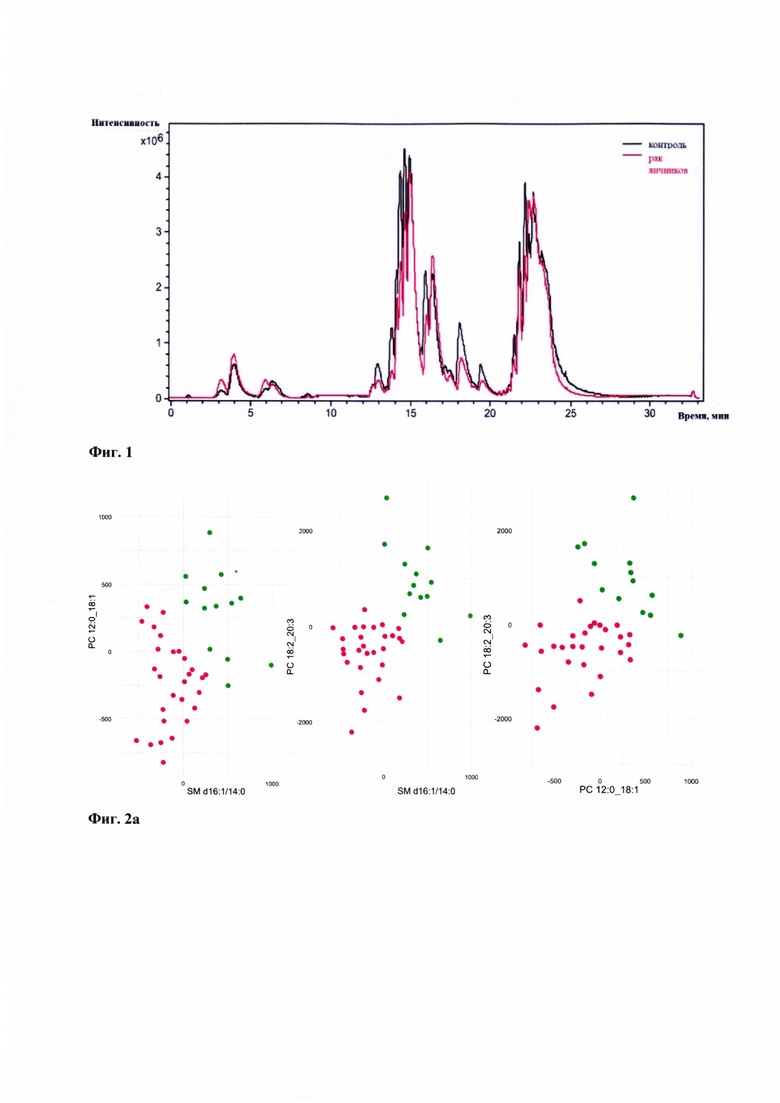
На Фиг. 1 приведены примеры хроматограмм по выбранному иону (липидов- маркеров) для экстракта липидов сыворотки крови в режиме положительных ионов. Красная кривая на Фиг. 1а соответствует образцу от пациента с подтвержденным РЯ, зеленая - образцу группы контроля. Красная кривая на Фиг. 16 соответствует образцу от пациента с РЯ III- IV стадии, черная - образцу от пациента с РЯ I-II.
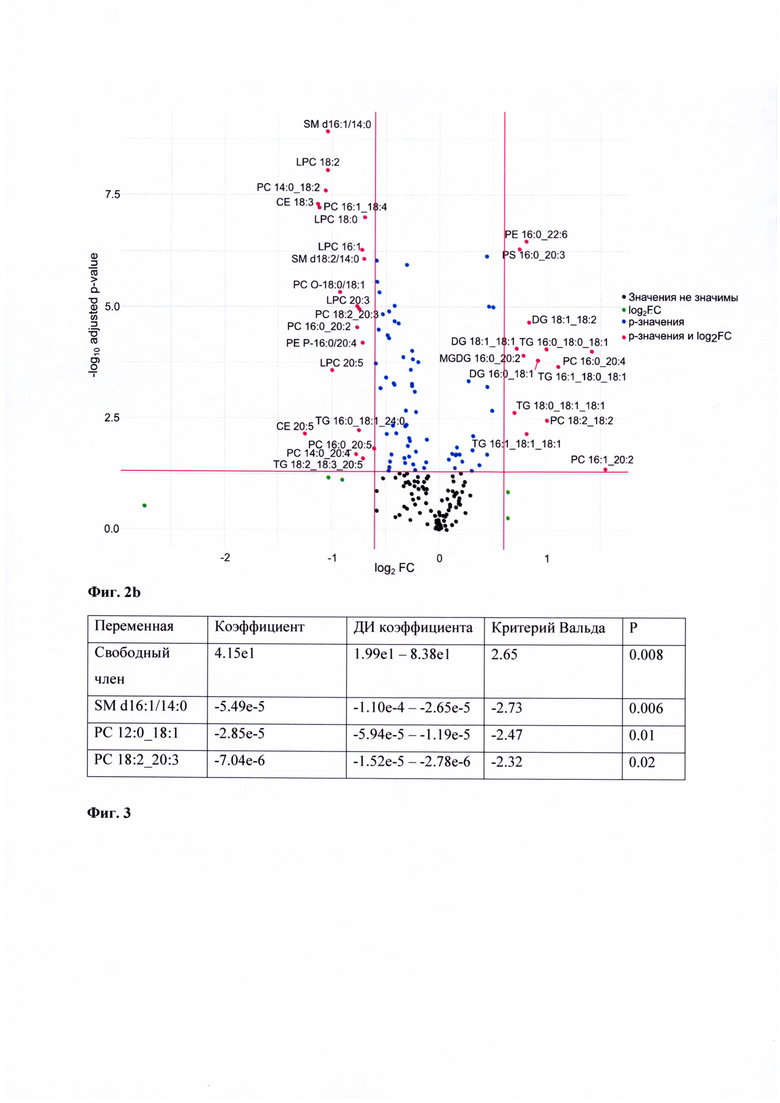
На Фиг. 2а приведены диаграммы рассеяния для липидов, использованных для дифференциации образцов крови наблюдаемых группы контроля (зеленые точки, n=13) и пациентов с серозным РЯ высокой степени злокачественности I-IV стадии (красные точки, n=28) посредством логистической регрессии. Созданная статистическая модель на основе логистической регрессии для дифференциальной диагностики образцов сыворотки крови пациентов группы контроля от пациентов с злокачественным серозным новообразованием яичников характеризуется точностью (Фиг. 3), определенной с использованием перекрестного контроля с разбитием данных в отношении тренировочные / тестовые данные 70/30 и 100 повторениями, и являющейся равной 99%. Это свидетельствует о хорошей прогнозирующей способности метода и позволяет предложить предлагаемую модель для отнесения анализируемых образцов к той или иной клинической подгруппе.
Чувствительность и специфичность данной модели на основе логистической регрессии, достигают 100% и 99% соответственно.
На Фиг. 2b представлен график рассеяния для большого массива данных (вулканная диаграмма), построенный по результатам сравнения уровней липидов образцах сыворотки крови пациентов группы контроля и исследуемой группы (РЯ I-IV стадии). Из 345 идентифицированных липидов статистически значимую разницу имеют 99 липидов, 67 из которых снижены, 32 - повышены при РЯ. На основании математической точечной диаграммы был проведен анализ наличия корреляции между двумя переменными (отрицательным логарифмом второй степени показателя статистической достоверности и логарифмом второй степени). На декартовой плоскости данной диаграммы рассеяния в виде паттернов представлены липиды образцов сыворотки крови пациентов исследуемых групп.
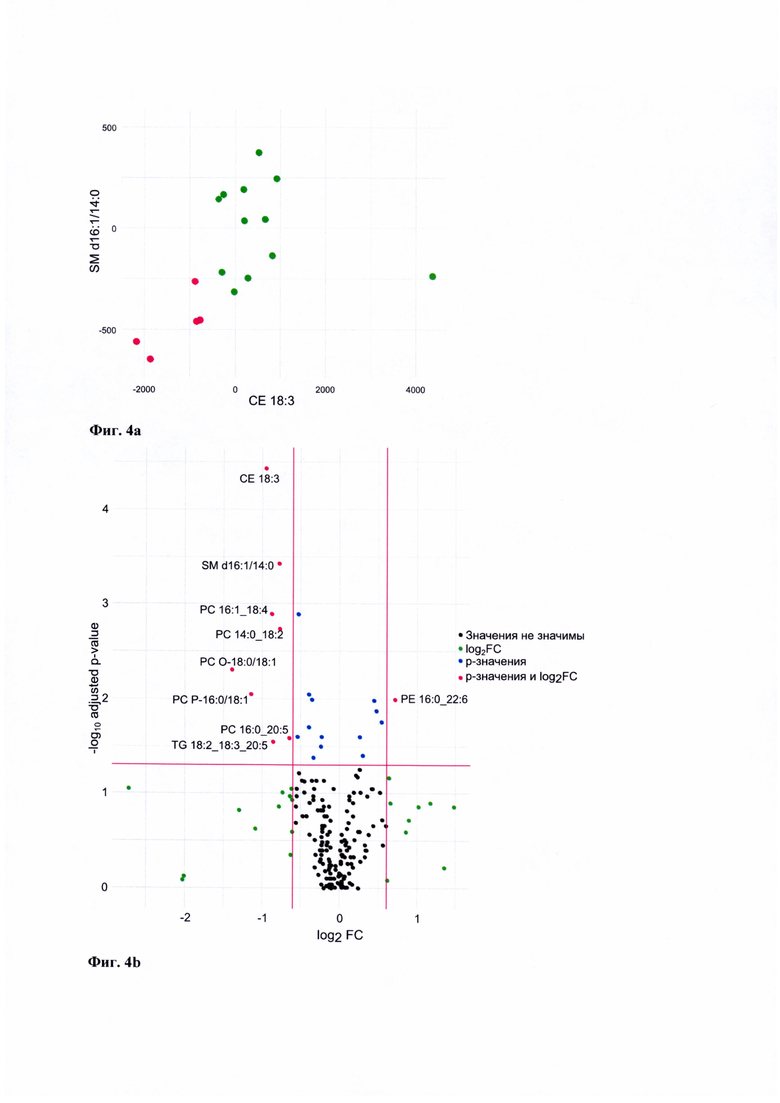
На Фиг. 4а приведены диаграммы рассеяния для липидов, использованных для дифференцирования образцов крови пациентов группы контроля, n=13, и пациентов с I-II стадиями РЯ, n=5. Точность модели на основе логистической регрессии (Фиг. 5) составила 98%, то есть, ее можно использовать для отнесения анализируемых образцов к той или иной клинической подгруппе.
Как продемонстрировано на Фиг. 4b, различия между сывороткой на ранних стадиях и сывороткой из контрольных групп менее выражены и в основном характеризуются липидами из класса фосфатидилходинов. Уровни 8 липидов образцов сыворотки пациентов при ранних стадиях статистически значимо снижены более чем в 1,5 раза по сравнению с уровнем липидов сыворотки крови пациентов группы контроля, уровень 1 липида повышен при РЯ.
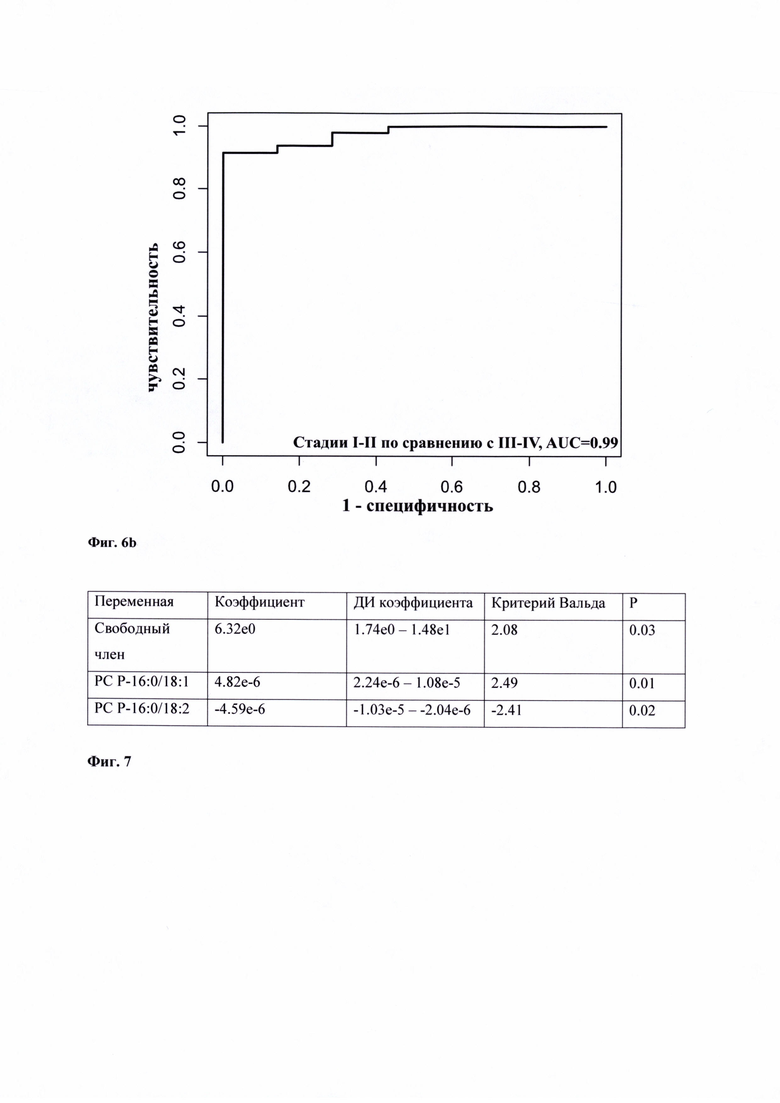
На Фиг. 6а приведены диаграммы рассеяния для липидов, использованных для дифференцирования образцов крови из группы рак яичников I-II стадии (красные точки) и III-IV стадии (синие точки). На основе результатов валидации построенной модели (Фиг. 7) была построена ROC-кривая (Фиг. 6b): чувствительность и специфичность достигли 97% и 100%, соответственно.
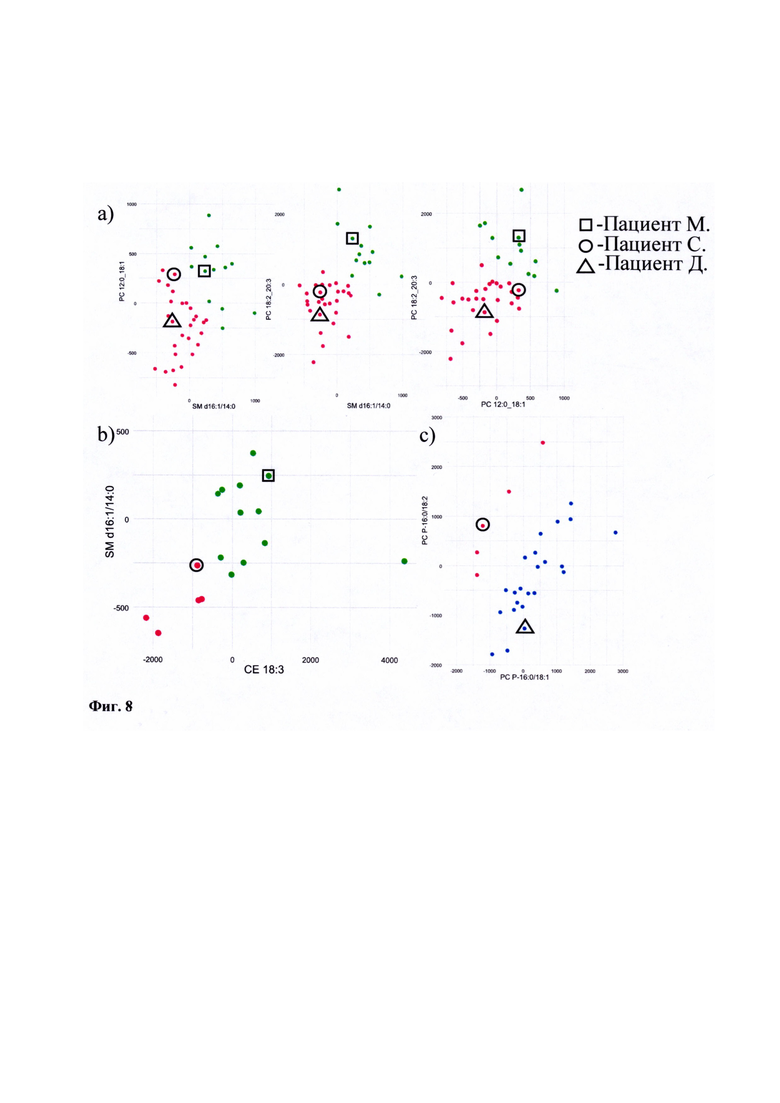
В качестве иллюстрации применения метода приведены диаграммы рассеяния (Фиг. 8) с уточнением расположения образцов крови пациентов исследуемых групп (I-II, III-IV стадии РЯ, группа контроля), клиническое описание которых приведено ниже.
Пациент Д., 36 лет 26.03.2020 обратилась на консультацию к врачу-акушеру-гинекологу, онкологу НМИЦ АГП им. В.И. Кулакова с данными ультразвукового исследования (УЗИ) органов малого таза, выполненного по месту жительства. По результатам УЗИ органов малого таза: объемное образование правого яичника, кистозно-солидное образование левого яичника неясного происхождения, образования брюшной полости неясного происхождения (в брюшной полости слева на уровне пупка определяются три округлых образования 9.1 см, 4.4 см, 3.4 см). Рекомендовано после дообследования хирургическое лечение в плановом порядке. Выявлено повышение онкомаркеров (СА 125 до 7080 (норма - до 35) Ед/мл, НЕ 4 до 545 (норма - до 70) пмоль/л). По данным компьютерной томографии (КТ) органов грудной клетки, выявлены множественные очаги в легких (предположительно метастатического генеза). 24.04.2020 выполнено оперативное лечение в объеме: лапароскопия, биопсия опухоли (данные исследования представлены на Фиг. 8). Пациент Д. направлена на консультацию к химиотерапевту. Учитывая распространенность заболевания, данные морфологии, клинико-инструментальные и лабораторные методы - у пациентки рак яичников IVB стадии T3cNxM1 (печень, легкие). Показано проведение лекарственного лечения по схеме: «Паклитаксел 175 мг/м2, Карбоплатин AUC 6 в/в, кап, 1 раз в 21 день, Бевацизумаб 7,5 мг в/в, кап, 1 раз в 21 день, в объеме 3-х курсов», далее проведение контрольного исследования и определение дальнейшей тактики лечения. По данным иммуногистохимического исследования (ИГХ) материалов опухоли пациента Д. (группа I-II стадий заболевания) с антителом anti-WT1 (клон 6F-H2, CellMarque), ядерная диффузная позитивная реакция, с антителом anti-PAX8 (клон MRQ-50, CellMarque), - ядерная диффузная позитивная реакция, с антителом anti-p53 (клон DO-7, Ventana), - негативная реакция (mutant type), с антителом anti-p16 (клон Е6Н4, Ventana), яркая диффузная позитивная реакция, с антителом anti-Estrogen Receptor (ER) (клон SP1, Ventana), - ядерная фокальная позитивная реакция. Данная иммунофенотипическая картина соответствует серозной карциноме яичников высокой степени злокачественности. Заключение (диагноз): в присланном материале карцинома высокой степени злокачественности. При применении разработанной первой модели на основе логистической регрессии к липидному профилю сыворотки крови пациента Д в соответствии с шагом (5) было получено значение y'1=0.99, что позволяет в соответствии с шагом (6) отнести пациента Д. к группе с наличием злокачественного серозного новообразования яичников, поэтому необходимо применение второй из полученных моделей на основе логистической регрессии, которая дает значение у'2=0.95, что свидетельствует о принадлежности пациента Д. к группе серозного РЯ III-IV стадий.
Пациент С., 47 лет, обратилась с жалобами на наличие объемного образования правого яичника. 27.11.2019 получила оперативное лечение в плановом порядке в объеме: гистерорезектоскопия, раздельное диагностическое выскабливание цервикального канала и полости матки, лапароскопическая резекция правого яичника. Заключение срочного интраоперационного гистологического исследования ткани опухоли: узел серозной низкодифференцированной карциномы. Рекомендовано проведение ИГХ-исследования. Диагноз: рак яичников IA стадии, T1aNxMo. Состояние после нерадикального хирургического лечения от 27.11.2019. Пациент С. повторно госпитализирована в Центр для выполнения радикального лечения. По данным ИГХ материалов опухоли пациента С. (группа III-IV стадий заболевания) с антителом anti-WT1 (клон 6F-H2, CellMarque), ядерная диффузная позитивная реакция, с антителом anti-p53 (клон DO-7, Ventana), ядерная яркая диффузная позитивная реакция (mutant type), с антителом anti-PAX8 (клон MRQ-50, CellMarque), ядерная диффузная позитивная реакция, с антителом anti-Ki-67 (клон 30-9, Ventana), Ki-67=95%, высокий уровень пролиферативной активности опухолевых клеток по сравнению с серозной карциномой яичника низкой степени злокачественности. Заключение: серозная карцинома правого яичника высокой степени злокачественности. Применение первой модели на основе логистической регрессии в соответствии с шагом (5) дает значение y'1=0.99, что позволяет в соответствии с шагом (6) отнести пациента С. к группе с наличием злокачественного серозного новообразования яичников, поэтому необходимо применение второй из полученных моделей на основе логистической регрессии, которая дает значение у'2=0.14, что свидетельствует о принадлежности пациента С.к группе серозного РЯ I-II стадий.
Пациент М., 36 лет, была включена в группу контроля данного исследования в связи с соответствием критериям включения. По данным опроса, анкетирования, УЗИ органов малого таза у пациента не было получено данных о наличии острых или хронических воспалительных процессов, объемных новообразований органов малого таза, указания на прием медикаментов на момент исследования, а также в анамнезе в течение 6 и более месяцев. Уровень онкомаркера СА 125 составил 10 Ед/мл, НЕ 4-12 пмоль/л. По данным УЗИ органов малого таза пациента группы контроля М.: матка 55×48×37 мм, не увеличена, в положении anteflexion, изоэхогенная, однородная. М-эхо не расширено (до 0.5 см), не уплотнено, соответствует пролиферативной фазе менструального цикла. Шейка матки - до 1.3×2.4 см, без особенностей. Цервикальный канал не расширен. Правый яичник размерами 31×20×16 мм, объем 5.0 см3, контуры четкие, ровные, изоэхогенный, неоднородной мелкофолликулярной структуры (количество фолликулов - 8, максимальным размером до 7 мм). Левый яичник размерами 32×19×12 мм, объем 5.0 см3, контуры четкие, ровные, изоэхогенный, неоднородной мелкофолликулярной структуры (количество фолликулов - 8, максимальным размером до 8 мм). В заднем своде свободная жидкость не визуализируется. Вены малого таза не расширены, до 3.0 мм. Заключение: патологии органов малого таза не выявлено. Применение первой модели на основе логистической регрессии в соответствии с шагом (5) дает значение y'1=0.01, что в соответствии с шагом (6) позволяет отнести пациента М. к группе контроля.
Таким образом, на диаграммах рассеяния (Фиг. 8), показано, что метод масс-спектрометрического определения липидома крови позволяет дифференцировать пациентов по стадиям опухолевого процесса в пределах одного гистологического типа заболевания.
Возможность реализации и воспроизводимости предлагаемого метода с получением заявленного технического результата проиллюстрирована нижеследующими примерами выявления пациентов с серозным РЯ высокой степени злокачественности, а также дифференцировки более ранних стадий от более прогрессивных на основании идентификации возможных маркерных липидов (разработанной панели) сыворотки крови.
В качестве ПРИМЕРА 1, демонстрирующего воспроизводимость метода получения масс-спектров образцов крови пациентов, на Фиг. 1 приведен пример хроматограммы полного ионного тока положительных ионов липидов, полученной при ВЭЖХ МС анализе липидных экстрактов сыворотки крови пациента группы контроля и пациента с гистологически подтвержденным раком яичника. На хроматограмме наблюдаются группы пиков, соответствующие лизофосфолипидам, моно- и диглицеридам (времена удерживания 0-10 минут); фосфолипидам (времена удерживания 10-20 минут); триглицеридам (времена удерживания более 20 минут). Обнаруживается воспроизводимая разница в распределении относительной интенсивности пиков. Относительное стандартное отклонение интенсивности пика составляет менее 5% для одного образца сыворотки крови.
В качестве ПРИМЕРА 2, демонстрирующего возможности работы метода для выявления пациентов со злокачественным серозным новообразованием яичников приведена диаграмма рассеяния для группы контроля (зеленые точки) и группы «рак яичников I-IV стадий по FIGO» (красные точки) (Фиг. 2а, 2b). Данные результаты получены в рамках обсервационного исследования «случай-контроль», проведенного на базе ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России. Объект исследования: группа 1 (основная) - 28 пациентов с гистологически верифицированным серозным раком яичников I-IV стадий, у которых до оперативного вмешательства был выполнен забор сыворотки крови, группа 2 (контроль) - 13 условно здоровых женщин, наличие патологии у которых было исключено при клиническом обследовании (клинический анализ крови, ультразвуковое исследование (УЗИ) органов малого таза). Группы были сопоставимы по индексу массы тела. Диагноз рака яичников клинически был предположен при повышении маркеров крови (СА 125>35 ЕД/мл, НЕ 4>70 пмоль/л в репродуктивном возрасте; >140 пмоль/л в постменопаузе) в составе алгоритмов Risk of Ovarian Malignancy Algorithm (ROMA; ROMA 1 для пременопаузы, ROMA 2 для постменопаузы), при выявлении объемного образования органов малого таза по данным УЗИ (или МРТ), при наличии симптомов заболевания, данных анамнеза и гинекологического осмотра, а также интраоперационно (при лапароскопии или лапаротомии) на основании осмотра и пальпации яичников и органов-мишеней. Патоморфологическая экспертиза фрагментов опухолевой ткани выполнялась в срочном и плановом порядке.
Критерии включения пациентов в группы исследования:
1. гистологически верифицированный рак яичников I-IV стадий.
2. Возраст пациентов от 18 до 50 лет.
3. Информированное согласие на участие в исследовании.
Критерии невключения: первично-множественный опухолевый процесс (n=9), эндометриоидная, светлоклеточная, герминогенная, гепатоидная, муцинозная и доброкачественная опухоли (n=10), рак маточной трубы или брюшины (n=3), наличие BRCA-мутации (n=2), опухоли низкой степени злокачественности (low grade; n=2), сопутствующая патология (сахарный диабет, острый воспалительный процесс на момент забора крови, хронический панкреатит, заболевания печени, n=3), беременность на момент забора крови (n=1).
На основании уровней липидов, удовлетворяющих условию статистической значимости согласно тесту Манна-Уитни и минимизации при помощи применения ИКА, выполнено построение первой модели на основе логистической регрессии согласно действиям алгоритма (Фиг 3).
Уровни липидов-маркеров подставляют в модели на основе логистической регрессии (SM d16:1/14:0, PC 12:0_18:1, PC 18:2_20:3 для первой модели), для которых рассчитывают переменную отклика (y'1) по формуле:
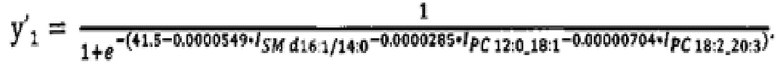
Уровень маркерных липидов статистически значимо ниже в сыворотке пациентов, имеющих серозный РЯ (Фиг. 2а, 2b).
Вычисленная y'1 позволила дифференцировать пациентов группы контроля (0 < y'1 < 0.7) от пациентов с серозным РЯ I-IV стадий (0.7 < y'1 < 1). Чувствительность и специфичность модели, вычисленные с использованием ROC-анализа, достигли 100% и 99%, соответственно. Это демонстрирует высокую точность дифференцировки пациентов без новообразований и пациентов с раком яичника I-IV стадии.
В качестве ПРИМЕРА 3, демонстрирующего возможности диагностики серозного РЯ высокой степени злокачественности на более ранних стадиях было проведено сравнение липидного профиля образцов сыворотки крови пациентов групп контроля (n=13) и пациентов с I-II стадиями серозного РЯ (n=5). Используя критерии включения и невключения, а также методы, аналогичные представленным в ПРИМЕРЕ 2, были получены следующие данные (Фиг. 4а, 4b).
На основании 2 маркерных липидов (SM 616:1/14:0, СЕ 18:3) сыворотки крови 18 пациентов, определенных предложенным способом, построена дополнительная модель на основе логистической регрессии, имеющей формулу:
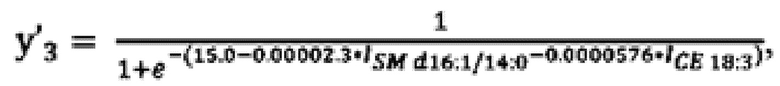
позволившая провести классификацию образцов из анализируемых клинических групп (Фиг. 5).
Вышеизложенное свидетельствует о том, что, на основании данных, полученных с помощью масс-спектрометрии (визуальное представление модели, липидный профиль из единиц, отличие которых в группах является статистически значимым), можно с высокой точностью различить липидный профиль здорового человека и пациентов при наличии злокачественной опухоли на I-II стадиях заболевания, лечение которых сопровождается более благоприятным прогнозом, однако выявление которых с помощью имеющихся методов диагностики сопряжено с существенными трудностями.
В качестве ПРИМЕРА 4, демонстрирующего возможности дифференциальной диагностики различных стадий серозного РЯ высокой степени злокачественности в группах более ранних (I-II стадии; n=5) и прогрессирующих стадий (III-IY; n=23), проведено сравнение липидного профиля образцов сыворотки крови пациентов указанных групп. Используя критерии включения и невключения, а также методы, аналогичные представленным в ПРИМЕРАХ 2 и 3, были получены следующие данные (Фиг. 6а, 6b).
Приведено сравнение информативности предлагаемого метода дифференциации образцов сыворотки крови пациентов при более ранних и более прогрессирующих стадиях РЯ на основе глубокого исследования липидома сыворотки с помощью жидкостной хроматографии с масс-спектрометрической детекцией. Сравнение проведено на материалах, полученных от 28 пациентов отделения инновационной онкологии и гинекологии ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России.
На основании липидного профиля сыворотки крови 28 пациентов с использованием предложенного способа была построена вторая модель на основе логистической регрессии, использующая в качестве маркеров 2 липида (PC Р-16:0/18:1 и PC Р-16:0/18:2) и вычислены границы переменной отклика для классификации образцов (Фиг. 7) по формуле:
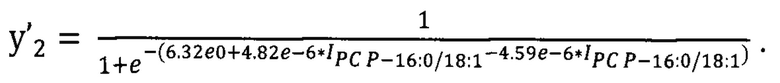
Список литературы
1. Amoroso M.R. et al. Stress-Adaptive Response in Ovarian Cancer Drug Resistance: Role of TRAP1 in Oxidative Metabolism-Driven Inflammation // Advances in Protein Chemistry and Structural Biology. 1st ed. Elsevier Inc., 2017. Vol. 108. 163-198 p.
2. Каприн А.Д. Состояние онкологической помощи населению России в 2019 году. А.Д. Каприн, В.В. Старинский, А.О. Шахзадова. 2020. С. 239 с.
3. Ueland FR L.A. Serum biomarkers for evaluation of an adnexal mass for epithelial carcinoma of the ovary, fallopian tube, or peritoneum // UpToDate. 2016. P. 1-13.
4. Li J. et al. Distinct plasma lipids profiles of recurrent ovarian cancer by liquid chromatography-mass spectrometry. 2017. Vol. 8, №29. P. 46834-46845.
5. Tomao F. et al. Fertility preservation in ovarian tumours // Ecancermedicalscience. 2018. Vol. 12. P. 1-14.
6. Ashraf M.A., Dasari P. Outcome of fertility-preserving surgery for ovarian malignancy in young women Case Report. 2018. P. 51-54.
7. Warren L.A. et al. Analysis of menstrual effluent: Diagnostic potential for endometriosis // Mol. Med. Molecular Medicine, 2018. Vol. 24, №1. P. 1-12.
8. Cragun J.M. Screening for ovarian cancer // Cancer Control. 2011. Vol. 18, №1. P. 16-21.
9. Grossman D.C. et al. Screening for ovarian cancer US preventive services task force recommendation statement // JAMA - J. Am. Med. Assoc. 2018. Vol. 319, №6. P. 588-594.
10. Madsen R., Lundstedt Т., Trygg J. Chemometrics in metabolomics-A review in human disease diagnosis. Anal Chim Act 2010; 659: 23-33.doi: 10.1016/j.aca.2009.11.042.
11. Ray U. et al. Gene regulatory networking reveals the molecular cue to lysophosphatidic acid-induced metabolic adaptations in ovarian cancer cells // Mol. Oncol. 2017. Vol. 11, №5. P. 491-516.
12 Xu Y. Lysophospholipid signaling in the epithelial ovarian cancer tumor microenvironment // Cancers (Basel). 2018. Vol. 10, №7.
13. Hiramatsu K., Serada S., Enomoto Т., et al. LSR antibody therapy inhibits ovarian epithelial tumor growth by inhibiting lipid uptake. Cancer Research. 2018. Vol. 78. №2. P. 516-527.
14. Hilvo M. et al. Accumulated metabolites of hydroxybutyric acid serve as diagnostic and prognostic biomarkers of ovarian high-grade serous carcinomas. Cancer Res. 2016. Vol. 76, №4. P. 796-804.
15. Braicu E.I. et al. High-grade ovarian serous carcinoma patients exhibit profound alterations in lipid metabolism. 2017. Vol. 8, №61. P. 102912-102922.
16. Buas M.F. et al. Identification of novel candidate plasma metabolite biomarkers for distinguishing serous ovarian carcinoma and benign serous ovarian tumors // Gynecol. Oncol. Elsevier B.V., 2016. Vol. 140, №1. P. 138-144.
17. Ghahremanfard F. et al. The valuable role of measuring serum lipid profile in cancer progression // Oman Med. J. 2015. Vol. 30, №5. P. 353-357.
18. Hirotugu Akaike. A new look at the statistical model identification. IEEE Trans. Automat. Control. 19(6), 716-723 (1974).
19. R CoreTeam (2018). R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. URL https://www.R-project.org.
20. RStudio Team (2016). RStudio: Integrated Development for R. RStudio, Inc., Boston, MA URL http://www.rstudio.com.
21. Sud M, Fahy E, Cotter D, Brown A, Dennis EA, Glass CK, Merrill AH Jr, Murphy RC, Raetz CR, Russell DW, Subramaniam S. LMSD: LIPID MAPS structure database. Nucleic Acids Res. 2007 Jan; 35(Database issue):D527-32. doi: 10.1093/nar/gk1838. Epub 2006 Nov 10. PMID: 17098933; PMCID: PMC1669719.
Фиг.1. Хроматограммы по выбранному иону липидов-маркеров, а) определения рака яичника относительно контрольной группы, б) определения рака яичника III-IV стадии относительно I-II стадии. Пики соответствующих ионов липидов-маркеров подписаны. Фиг. 2а. Диаграммы рассеяния для парето-нормированных площадей пиков липидов- маркеров для образцов групп: «Контроль» (зеленые точки) и «Рак яичников, I-IV стадии» (красные точки).
Фиг. 2b. Вулканная диаграмма (график рассеяния для большого массива данных), построенная по результатам сравнения уровней липидов в образцах сыворотки крови пациентов групп контроля и исследуемой группы («Рак яичников, I-IV стадии»).
Фиг. 3. Параметры логистической регрессии, задействованной в классификационной модели «Контроль» / «Серозный рак яичников, I-IV стадии»
Фиг. 4а. Диаграммы рассеяния для парето-нормированных площадей пиков липидов-маркеров для образцов групп: для образцов групп «Контроль» (зеленые точки) и «Рак яичников, I-II стадии» (красные точки).
Фиг. 4b. Вулканная диаграмма (график рассеяния для большого массива данных), построенная по результатам сравнения уровней (содержания, площадь хроматографического пика под кривой) липидов образцов крови наблюдаемых группы контроля и пациентов с диагнозом «Рак яичников, I-II стадии».
Фиг. 5. Параметры логистической регрессии, задействованной в классификационной модели «Контроль» / «Серозный рак яичников, I-II стадии»
Фиг. 6а. Диаграммы рассеяния для парето-нормированных площадей пиков липидов- маркеров для образцов групп: «Рак яичников, I-II стадии» (красные точки) и «Рак яичников, III-IV стадии» (синие точки).
Фиг. 6b. ROC-кривая модели, построенной на основе результатов логистической регрессии анализа уровней липидов в крови в группах «Рак яичников, I-II стадии» (красные точки) и «Рак яичников, III-IV стадии» (синие точки).
Фиг. 7. Параметры логистической регрессии, задействованной в классификационной модели «Серозный рак яичников, I-II стадии» / «Серозный рак яичников, III-IV стадии» Фиг. 8. Топическое расположение на графиках счетов пациентов Д. (36 лет, диагноз: «Рак яичников, IVB стадия, T3cNxM1 (метастатическое поражение печени и легких)»), С. (47 лет, диагноз «Рак яичников, IA стадия, T1aNxMo. Состояние после нерадикального хирургического лечения от 27.11.2019»), М. (46 лет, наблюдаемый группы контроля) на диаграммах рассеяния в пространстве парето-нормированных липидов-маркеров.
Сравнение образцов:
a) Пациенты Д., С., М. на графиках счетов для образцов групп «Контроль» (зеленые точки) и «Рак яичников, I-IV стадии» (красные точки).
b) Пациенты М. и С. для образцов групп «Контроль» (зеленые точки) и «Рак яичников, I-II стадии» (красные точки).
c) Пациенты С. и Д. для образцов групп «Рак яичников, I-II стадии» (красные точки) и «Рак яичников, III-IV стадии» (синие точки).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ неинвазивной диагностики эндометриоза по липидному профилю сухих капель менструальной крови | 2024 |
|
RU2829265C1 |
| Способ оценки первичного ответа на проводимую комбинированную химиотерапию спорадического рака яичников III и IV стадий | 2021 |
|
RU2769543C2 |
| Способ прогнозирования степени вероятности возможности выполнения оптимальной циторедуктивной операции у больных с диссеминированными формами рака яичников | 2017 |
|
RU2637399C1 |
| Способ дифференциальной диагностики рака яичников, кистозных образований яичника и рака тела матки | 2024 |
|
RU2836527C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ДЕФИЦИТА ЖЕЛЕЗА У БОЛЬНЫХ РАКОМ ЯИЧНИКОВ | 2023 |
|
RU2800104C2 |
| Способ определения эффективности химиотерапии препаратами платины при раке яичников III-IV стадии | 2020 |
|
RU2738167C1 |
| Способ дифференциальной диагностики доброкачественных и злокачественных новообразований яичников | 2018 |
|
RU2686180C1 |
| Способ прогнозирования эффективности неоадъювантной химиотерапии у больных с диссеминированными формами рака яичников | 2017 |
|
RU2637410C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВИРОВАНИЯ СЕРОЗНОЙ КАРЦИНОМЫ ЯИЧНИКОВ | 2020 |
|
RU2749361C1 |
| СПОСОБ ОБРАБОТКИ ХРОМАТО-МАСС-СПЕКТРОМЕТРИЧЕСКИХ ДАННЫХ ДЛЯ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ПОИСКА ДИАГНОСТИЧЕСКИХ МАРКЕРОВ ПРИ ПРОВЕДЕНИИ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ | 2021 |
|
RU2803128C2 |

Изобретение относится к медицине, а именно к онкологической гинекологии, и может быть использовано для диагностики серозного рака яичников высокой степени злокачественности по липидному профилю сыворотки крови, полученному методом высокоэффективной жидкостной хроматографии с масс-спектрометрической детекцией. Первым этапом на основании липидов SM d16:1/14:0, PC 12:0_18:1, PC 18:2_20:3 рассчитывают переменную отклика y'1:
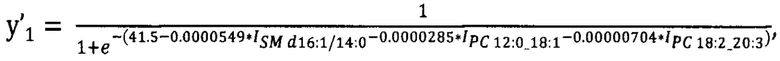 где
где 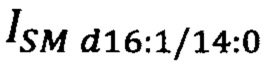 - площадь пиков липидов-маркеров SM d16:1/14:0 на хроматограмме образца крови пациента, у.е.;
- площадь пиков липидов-маркеров SM d16:1/14:0 на хроматограмме образца крови пациента, у.е.; 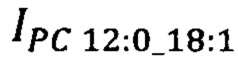 - площадь пиков липидов-маркеров PC 12:0_18:1 на хроматограмме образца крови пациента, у.е.;
- площадь пиков липидов-маркеров PC 12:0_18:1 на хроматограмме образца крови пациента, у.е.; 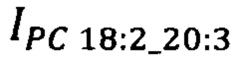 - площадь пиков липидов-маркеров PC 18:2_20:3 на хроматограмме образца крови пациента, у.е. При значении 0.7 ≤ y'1 ≤ 1 приходят к заключению о принадлежности пациента к группе больных раком яичников. При значении 0 < y'1 < 0.7 - к группе контроля. Вторым этапом на основании липидов PC Р-16:0/18:1 и PC Р-16:0/18:2 рассчитывают переменную отклика у'2:
- площадь пиков липидов-маркеров PC 18:2_20:3 на хроматограмме образца крови пациента, у.е. При значении 0.7 ≤ y'1 ≤ 1 приходят к заключению о принадлежности пациента к группе больных раком яичников. При значении 0 < y'1 < 0.7 - к группе контроля. Вторым этапом на основании липидов PC Р-16:0/18:1 и PC Р-16:0/18:2 рассчитывают переменную отклика у'2:
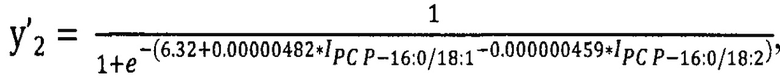 где
где 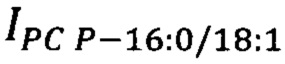 - площадь пиков липидов-маркеров PC Р-16:0/18:1 на хроматограмме образца крови пациента, у.е.;
- площадь пиков липидов-маркеров PC Р-16:0/18:1 на хроматограмме образца крови пациента, у.е.; 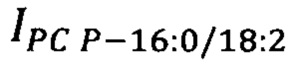 - площадь пиков липидов-маркеров PC Р-16:0/18:2 на хроматограмме образца крови пациента, у.е. При значении 0.6 ≤ у'2 < 1 приходят к заключению о наличии серозного РЯ III-IV стадий. При значении 0 < у'2 < 0.6 - о наличии серозного рака яичников I-II стадий. Способ обеспечивает возможность повышения диагностической точности выявления эпителиального серозного рака яичников высокой степени злокачественности на ранних стадиях (I-II стадии) за счет определения липидного профиля сыворотки крови посредством высокоэффективной жидкостной хроматографии с масс-спектрометрической детекцией, позволяющих идентифицировать возможные маркерные молекулы, характерные для патологических состояний при ранних стадиях онкологического процесса; последовательного применения двух моделей, построенных на основании метода логистической регрессии для вычисления переменной отклика, позволяющей выявить пациентов с ранними стадиями серозного рака яичников. 8 ил., 4 пр.
- площадь пиков липидов-маркеров PC Р-16:0/18:2 на хроматограмме образца крови пациента, у.е. При значении 0.6 ≤ у'2 < 1 приходят к заключению о наличии серозного РЯ III-IV стадий. При значении 0 < у'2 < 0.6 - о наличии серозного рака яичников I-II стадий. Способ обеспечивает возможность повышения диагностической точности выявления эпителиального серозного рака яичников высокой степени злокачественности на ранних стадиях (I-II стадии) за счет определения липидного профиля сыворотки крови посредством высокоэффективной жидкостной хроматографии с масс-спектрометрической детекцией, позволяющих идентифицировать возможные маркерные молекулы, характерные для патологических состояний при ранних стадиях онкологического процесса; последовательного применения двух моделей, построенных на основании метода логистической регрессии для вычисления переменной отклика, позволяющей выявить пациентов с ранними стадиями серозного рака яичников. 8 ил., 4 пр.
Способ диагностики серозного рака яичников высокой степени злокачественности по липидному профилю сыворотки крови, полученному методом высокоэффективной жидкостной хроматографии с масс-спектрометрической детекцией, отличается тем, что первым этапом на основании липидов SM d16:1/14:0, PC 12:0_18:1, PC 18:2_20:3 рассчитывают переменную отклика y'1:
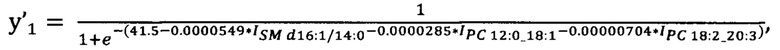
где 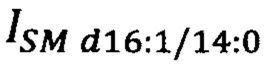 - площадь пиков липидов-маркеров SM d16:1/14:0 на хроматограмме образца крови пациента, у.е.;
- площадь пиков липидов-маркеров SM d16:1/14:0 на хроматограмме образца крови пациента, у.е.;
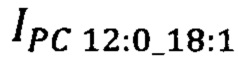 - площадь пиков липидов-маркеров PC 12:0_18:1 на хроматограмме образца крови пациента, у.е.;
- площадь пиков липидов-маркеров PC 12:0_18:1 на хроматограмме образца крови пациента, у.е.;
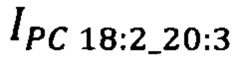 - площадь пиков липидов-маркеров PC 18:2_20:3 на хроматограмме образца крови пациента, у.е.;
- площадь пиков липидов-маркеров PC 18:2_20:3 на хроматограмме образца крови пациента, у.е.;
при значении 0.7 ≤ y'1 ≤ 1 приходят к заключению о принадлежности пациента к группе больных раком яичников, при значении 0 < y'1 < 0.7 - к группе контроля;
вторым этапом на основании липидов PC Р-16:0/18:1 и PC Р-16:0/18:2 рассчитывают переменную отклика у'2:
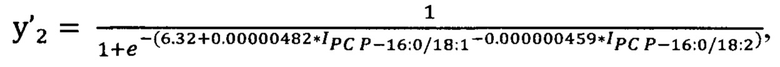
где 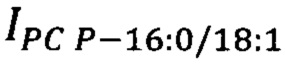 - площадь пиков липидов-маркеров PC Р-16:0/18:1 на хроматограмме образца крови пациента, у.е.;
- площадь пиков липидов-маркеров PC Р-16:0/18:1 на хроматограмме образца крови пациента, у.е.;
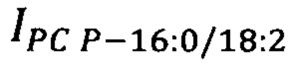 - площадь пиков липидов-маркеров PC Р-16:0/18:2 на хроматограмме образца крови пациента, у.е.;
- площадь пиков липидов-маркеров PC Р-16:0/18:2 на хроматограмме образца крови пациента, у.е.;
при значении 0.6 ≤ у'2 < 1 приходят к заключению о наличии серозного РЯ III-IV стадий, при значении 0 < у'2 < 0.6 - о наличии серозного рака яичников I-II стадий.
| NIEMI R.J | |||
| et al | |||
| Ovarian tumours of different histologic type and clinical stage induce similar changes in lipid metabolism | |||
| Br J Cancer | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Способ для диагностирования рака яичников на основе набора генов длинных некодирующих РНК | 2021 |
|
RU2779550C1 |
| СПОСОБ ДИАГНОСТИКИ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ И РАКА ЯИЧНИКОВ | 2017 |
|
RU2696114C2 |
| СПОСОБ ДИАГНОСТИКИ ПРОГРЕССИРУЮЩИХ ФОРМ РАКА ЯИЧНИКОВ | 2013 |
|
RU2536272C1 |
| US 20150293104 A1, 15.10.2015 | |||
| KR 1020110068695 A, 22.06.2011 | |||
| IUROVA M.V | |||
| et al | |||
| Lipid Alterations in | |||
Авторы
Даты
2023-11-14—Публикация
2022-12-09—Подача