Изобретение относится к области медицины, в частности к нейрохирургии, и может быть использовано для лечения больных с хирургической патологией позвоночника и неврально-сосудистых структур позвоночного канала.
Чрескожные видеоэндоскопические операции на позвоночнике относятся к разряду операций, выполняемых в искусственно созданных малых полостях (в данном случае - эпидуральном пространстве). Одной из существенных особенностей этих операций является поэтапное формирование рабочего пространства, имеющего небольшие размеры. При этом, всегда присутствует проблема создания и поддержания на протяжении всей операции качественного изображения, позволяющего полноценно визуализировать и манипулировать в зоне хирургического интереса.
Известен способ чрескожного видеоэндоскопического вмешательства на позвоночнике в жидкой среде. Во всех современных руководствах по чрескожной видеоэндоскопии позвоночника дается описание именно этого способа [Kim D.H. Endoscopic spine procedures / D.H. Kim, G. Choi, S.H. Lee - New York: Thieme Medical Publishers, Inc., 2011. - 279 p.; Lewandrowski K.U. Endoscopic spinal surgery / K.-U. Lewandrowski, S-H. Lee, M. Iprenburg - London: JP Medical Ltd., 2013 - 162 р.]. В качестве жидкости большинством авторов используется физиологический (0,9%) раствор хлорида натрия, подача которого в операционное пространство осуществляется через ирригационный канал эндоскопа, а отток - через аспирационный канал. Эндоскоп также содержит рабочий канал для введения инструментов. Подача физиологического раствора осуществляется посредством насосной или гравитационной систем, обеспечивающих поддержание определенного уровня давления. Давление подаваемой жидкости в насосной системе регулируется изменением объема в единицу времени, а в гравитационных системах - высотой уровня жидкости.
К преимуществам методики чрескожной видеоэндоскопии позвоночника в жидкой среде относят:
- хорошую визуализацию анатомических структур позвоночного канала вследствие прозрачности среды физиологического раствора;
- возможность манипуляций хирургическими инструментами в искусственно увеличенном пространстве между эндоскопом и тканями;
- возможность диссекции анатомических структур за счет умеренного проникновения жидкости в пространства между тканями;
- возможность гемостаза посредством регуляции давления и температуры подаваемой жидкости [Schubert М. Endoscopic transforaminal nucleotomy with foraminoplasty for lumbar disk herniation / M. Schubert, T. Hoogland // Operative Orthopadie und Traumatologic - 2005. - T. 17. - №. 6. - C. 641-661; Lewandrowski K.U. Pre-operative planning for endoscopic lumbar foraminal decompression-A prospective study / K.U. Lewandrowski // European Musculoskeletal Review. - 2008. - T. 3. - №. 1. - C. 46-51].
Однако, несмотря на вышеизложенные преимущества, у способа чрескожной видеоэндоскопии в жидкой среде имеются следующие недостатки:
- при превышении давления и объема вводимой жидкости, возможно ее распространение за пределы операционного поля - по эпидуральному пространству, субдуральному пространству (в случае повреждения твердой мозговой оболочки), в плевральную полость (при выполнении вмешательства на грудном отделе позвоночника). В литературе известны случаи осложнений, связанных с воздействием давления и объема вводимой жидкости при подобных операциях. В частности, при повышении давления вводимого в эпидуральное пространство физиологического раствора у больных во время чрескожной видеоэндоскопической операции на поясничном отделе позвоночника отмечались боль в шее, головная боль, что коррелировало с увеличением давления в эпидуральном пространстве шейного отдела. По мнению авторов, судорожный синдром, отмеченный в 0,025% случаях чрескожной эндоскопической поясничной дискэктомии, был обусловлен внутричерепной гипертензией вследствие перемещения ликвора из конечной цистерны в краниальном направлении по мере заполнения эпидурального пространства физиологическим раствором и сдавлением дурального мешка [Choi G. et al. Risk of developing seizure after percutaneous endoscopic lumbar discectomy // Clinical Spine Surgery. - 2011. - T. 24. - №. 2. - C. 83-92.; Gupta R.S. et al. Technique of percutaneous transforaminal endoscopic discectomy for the treatment of lumbar disc herniation // Open Journal of Orthopedics. - 2015. - T. 5. - №. 7. - C. 208-216];
- в условиях непрерывной ирригации физиологического раствора возникает сложность верификации ликвореи - истечения спинномозговой жидкости через дефекты твердой мозговой оболочки, а также отсутствует возможность пластики таких дефектов. В литературе имеются единичные рекомендации производить в таких случаях скарификацию замыкательной пластинки позвонка до губчатого вещества, с помощью крови образовавшимся вследствие этой манипуляции [Schubert М. Endoscopic transforaminal nucleotomy with foraminoplasty for lumbar disk herniation / M. Schubert, T. Hoogland // Operative Orthopadie und Traumatologie. - 2005. - T. 17. - №. 6. - C. 641-661];
- непрерывная ирригация является препятствием к использованию противоспаечных компонентов при ревизионных вмешательствах по поводу эпидурального фиброза;
- поток жидкости в зоне вмешательства не позволяет эффективно использовать химические средства гемостаза (окисленная целлюлоза, фибрин-тромбиновые композиции и пр.).
Прототипами предлагаемого способа являются видеоэндоскопические операции в искусственно созданных малых полостях других анатомических областей, проводимые в условиях воздушной среды:
1.1) Способ эндоскопичекой диссекции перфорантных вен в переднем миофасциальном ложе голени, выполняемый с инсуфляцией углекислого газа [Сушков С.А., Кухтенков П.А., Павлов А.Г. Применение троакарной технологии эндоскопической диссекции перфорантных вен // Новости хирургии. - 2007. - Т. 15. - № 3; Сушков С.А., Павлов А.Г., Кухтенков П.А. Эндоскопическая субфасциальная диссекция перфорантных вен в переднем миофасциальном ложе голени // Новости хирургии. - 2009. - Т. 17. - №3].
Данный способ предполагает создание первичной операционной полости тупым путем: при помощи пальца или физиологического раствора глубокую фасцию отделяют от прилежащих мышечных структур в дистальном направлении на протяжении нескольких сантиметров. После подготовки первичного операционного пространства, вводят троакары, накладывают герметизирующие швы на кожу и подкожную клетчатку. В последующем осуществляется инсуфляция углекислого газа со скоростью не менее 5 л/мин, что позволяет поддерживать давление в субфасциальном пространстве голени до 25-30 мм рт.ст.
В результате под давлением газа формируется полость достаточная для манипуляций.
Указанный способ имеет ряд недостатков для того, чтобы рассмотреть возможность его применения в хирургии позвоночника:
- при работе с газом возникает целый ряд проблем связанных с герметизацией доступа и инструментального канала эндоскопа;
- происходит быстрое запотевание оптики;
- периодически возникает задымление операционного поля при коагуляции сосудов и тканей;
- распространение газа под большим давлением по эпидуральному, а в некоторых случаях, и субдуральному пространствам позвоночника, неминуемо приведет к развитию эмфиземы, пневмоцефалии, внутричерепной гипертензии, сдавлению газом невральных структур позвоночного канала;
- высокоскоростная подача газа под давлением до 25 мм. рт.ст., чревата развитием газовой эмболии. Последнее осложнение может развиться, если во время операции на фоне напряженной газовой среды происходит ранение вены и газ попадает в сосудистое русло через зияющий дефект. Хотя газовая эмболия, имеющая клиническое значение, встречается редко, ее возникновение может привести к смерти пациента. В лапароскопической хирургии это крайне тяжелое осложнение наблюдается с частотой 1-2 случая на 10000 операций. При этом истинная частота клинически скрытой газовой эмболии неизвестна [Федоров И.В., Сигал Е.И., Одинцов В.В. Эндоскопическая хирургия. - М.: ГЭОТАР, 1998. - 352 с.].
2) Известен безгазовый способ эндоскопической субфасциальной диссекции перфорантных вен голени [Славин Д.А. и др. Безгазовая эндоскопическая субфасциальная диссекция перфорантных вен // Эндоскопическая хирургия. - 2007. - Т. 13. - № 1. - С. 142-142].
При этом способе операционное поле формируется препаровочными тубусами операционного эндоскопа, имеющими больший диаметр или препаровочную булавовидную оливу на дистальном конце.
При этом в поле зрения оказывается лишь небольшой участок субфасциального пространства в зоне диссекции, что создает определенные трудности при ориентации и выделении перфорантных вен. Наибольшие трудности возникают даже при незначительном кровотечении. Малый объем операционного поля быстро заполняется кровью, что приводит к практически полной потери ориентации, необходимости гемостаза методом пальцевого прижатия через кожу и существенно увеличивает продолжительность операции. Обеспечение «сухого» операционного поля в субфасциальном пространстве, достигается наложением на нижнюю треть бедра стерильной манжеты Лофквиста, предварительно накаченной воздухом до давления в 150 мм рт.ст. В результате перемещения надутой манжеты от стопы к бедру происходит опорожнение венозной системы от крови. Обязательная ее фиксация специальным клином на бедре сопровождается прекращением кровообращения в конечности. Аспирация продуктов горения из вновь созданной полости при коагуляции, через инсуффляционный канал тубуса, является эффективным способом сохранения хорошей видимости на протяжении всей операции.
Недостатками этого способа, ограничивающими его применение в чрескожной видеоэндоскопической хирургии позвоночника, являются:
- невозможность обеспечить надежный гемостаз в области позвоночного канала методом временного прекращения магистрального кровоснабжения в зоне операции или временным пальцевым прижатием оливы невозможно осуществить в эпидуральном пространстве позвоночника ввиду угрозы компрессионного воздействия на неврально-сосудистые структуры.
3) Известен способ эндоскопического лечения синдрома карпального канала [Wong K.С. et al. Carpal tunnel release // Bone & Joint Journal. - 2003. - T. 85. - № 6. - C. 863-868]. Данный способ также можно отнести к видам видеоэндоскопических вмешательств в искусственно созданных малых полостях организма.
Способ заключается в выполнении одного или двух (в зависимости от методики) разрезов длиной 1 см. на внутренней стороне запястья. Через разрезы под связку вводится расширяющий зонд эндоскопа и устанавливается камера, позволяющая визуализировать срединный нерв среди сухожилий. Проводится полное или частичное рассечение поперечной связки, устраняющее ущемление нерва. Операция выполняется под жгутом на плече, для того чтобы избежать даже минимального кровотечения. Это позволяет увидеть все структуры в проекции карпального канала.
К недостаткам, ограничивающим использование данного способа в хирургии позвоночника, можно отнести:
- пространством для манипуляций, при эндоскопических вмешательствах на карпальном канале, является полость расширяющей канюли, а структуры подлежащие визуализации, и на которые направлено хирургическое воздействие, располагаются в боковом отверстии этой канюли, имеющем овальную форму, тогда как при хирургическом вмешательстве на структурах позвоночного канала операционная полость расположена за пределами канала рабочей канюли со стороны ее дистального конца;
- отчетливая визуализация в воздушной среде достигается отсутствием кровотечения из операционной раны за счет временного пережатия магистральных сосудов жгутом, что невозможно выполнить при вмешательствах на структурах области позвоночного канала.
В основу изобретения положена задача создания способа чрескожного видеоэндоскопического вмешательства на позвоночнике, который позволяет повысить эффективность этого вида операций, расширить возможности хирургической техники и условий для осуществления ликворо- и гемостаза, а также снизить риски, связанные с воздействием на неврально-сосудистые структуры позвоночного канала избыточного давления/объема жидкости или газа, не снижая при этом качества изображения передаваемого на монитор.
Решение поставленной задачи обеспечивается тем, что в способе чрескожного видеоэндоскопического вмешательства на структурах позвоночного канала, включающем использование воздуха в качестве среды для эндоскопии, проводят двухэтапное вмешательство со сменой сред для эндоскопии, на первом этапе которого после введения в эпидуральное пространство рабочей канюли с эндоскопом выполняют диссекцию неврально-сосудистых структур в условиях ирригации физиологическим раствором хлорида натрия; после создания операционного пространства для манипуляций прекращают ирригацию физиологического раствора и заполняют операционное пространство воздухом, поступающим извне через ирригационный и манипуляционный каналы эндоскопа по градиенту - в область низкого давления вследствие эффекта разрежения, достигаемого непрерывным откачиванием воздуха из эпидурального пространства через аспирационный канал эндоскопа.
Технический результат изобретения состоит в повышении эффективности чрескожных видеоэндоскопических вмешательств на структурах позвоночного канала путем использования в качестве среды для эндоскопии воздуха, попадающего в эпидуральное пространство по градиенту - в область низкого давления, при этом поддержание операционной полости в объеме достаточном для оптимальной визуализации и выполнения хирургических манипуляций, достигается благодаря жесткости костно-связочного аппарата образующего стенки позвоночного канала, что обеспечивает:
- постоянную эвакуацию крови из операционной полости при имеющемся кровотечении;
- аспирацию дыма, образующегося при диатермической коагуляции сосудов и тканей;
- качественную визуализацию неврально-сосудистых структур позвоночного канала;
- выполнение необходимых хирургических манипуляций.
Этот результат достигается тем, что проводят двухэтапное вмешательство со сменой сред для эндоскопии, на первом этапе которого после введения в эпидуральное пространство рабочей канюли с эндоскопом выполняют диссекцию неврально-сосудистых структур в условиях ирригации физиологическим раствором хлорида натрия; после создания первичного операционного пространства для манипуляций прекращают подачу физиологического раствора, и заполняют операционное пространство воздухом, поступающим туда через ирригационный и манипуляционный каналы эндоскопа по градиенту - в область низкого давления, вследствие эффекта разрежения, на дистальном конце эндоскопа, достигаемого непрерывным откачиванием воздуха из эпидурального пространства через аспирационный канал эндоскопа.
Данный способ, не изменяя качества передаваемого изображения на экран монитора, позволяет:
- предотвратить осложнения связанные с воздействием избыточного давления жидкости или газа на невральные структуры позвоночного канала благодаря сохраняющемуся эффекту разрежения в области вмешательства, что предотвращает распространение воздуха по эпидуральному пространству;
- своевременно диагностировать ликворею и оценить ее интенсивность путем прямой визуализации, в случаях интраоперационного повреждения твердой и паутинной оболочек спинного мозга;
- герметизировать дефект твердой мозговой оболочки жидкими клеевыми компонентами;
- заполнить эпидуральное пространство противорубцовыми гидрогелевыми компонентами в оптимальной концентрации;
- осуществить гемостаз биполярной коагуляцией сосудов и химическими средствами, с использованием твердых и жидких имплантатов (фибрин-тромбиновые смеси, препараты окисленной целлюлозы);
- в условиях временного прекращения аспирации воздуха и остановки воздушного потока осуществлять контроль эффективности гемостаза и ликворостаза, визуализировать истинное взаимоотношение анатомических структур позвоночного канала.
Терапевтический эффект получают в раннем и позднем послеоперационном периодах за счет использования дополнительных хирургических опций по профилактике развития внутричерепной гипертензии, послеоперационных гематом, гипотензионного синдрома, связанного с ликвореей, а также болевых синдромов вызванных развитием эпидурального рубцового фиброза.
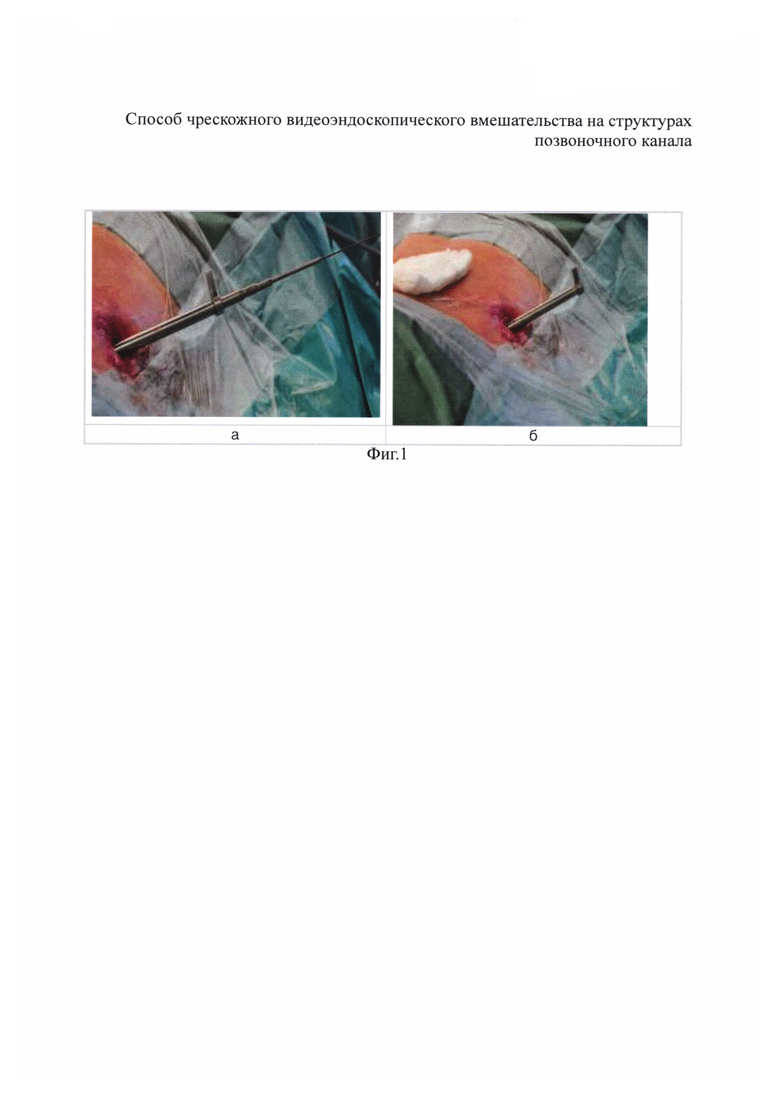
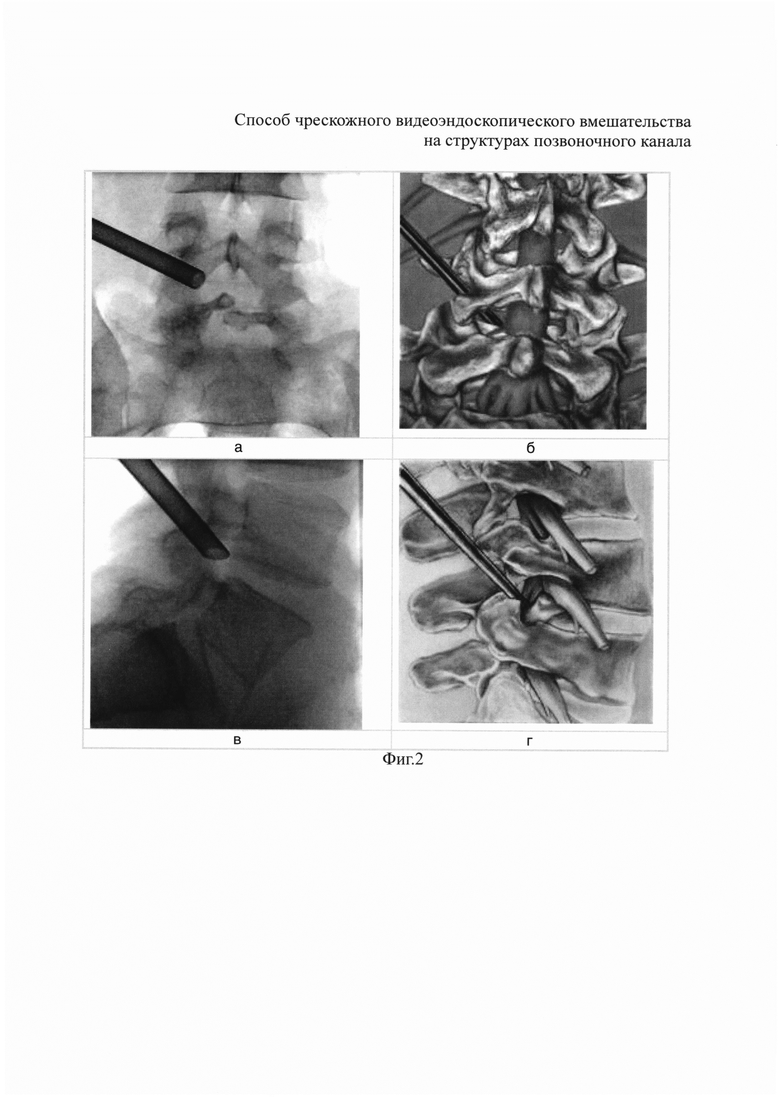
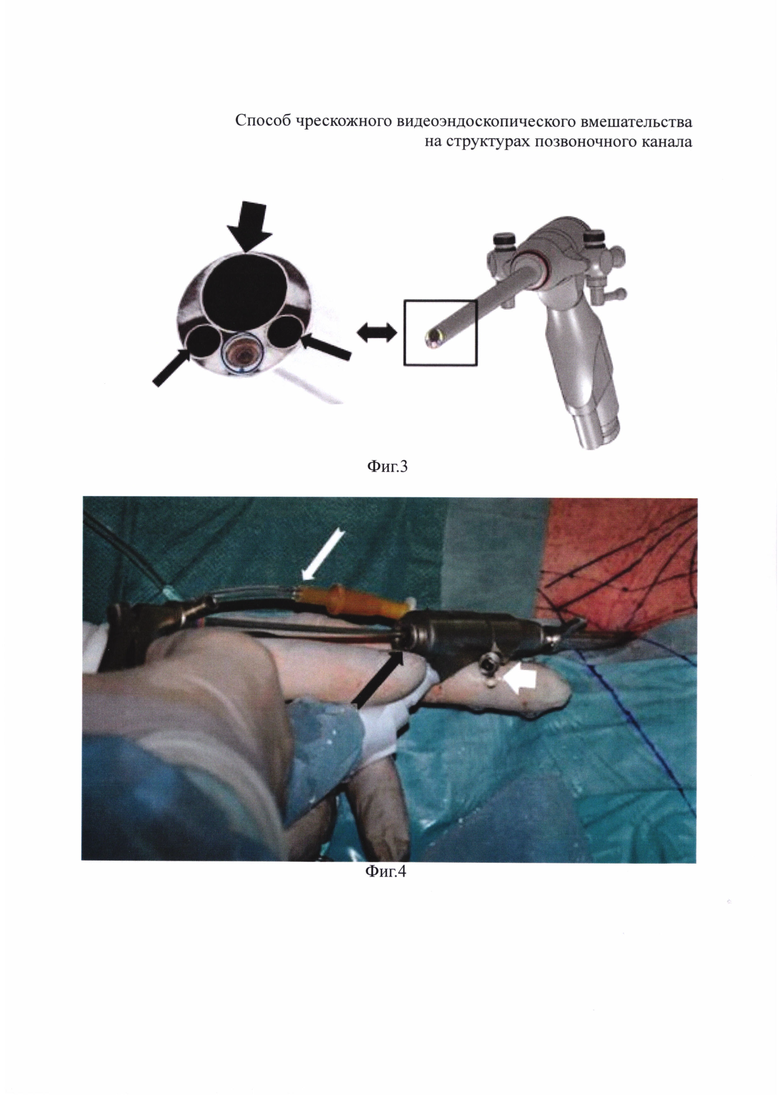
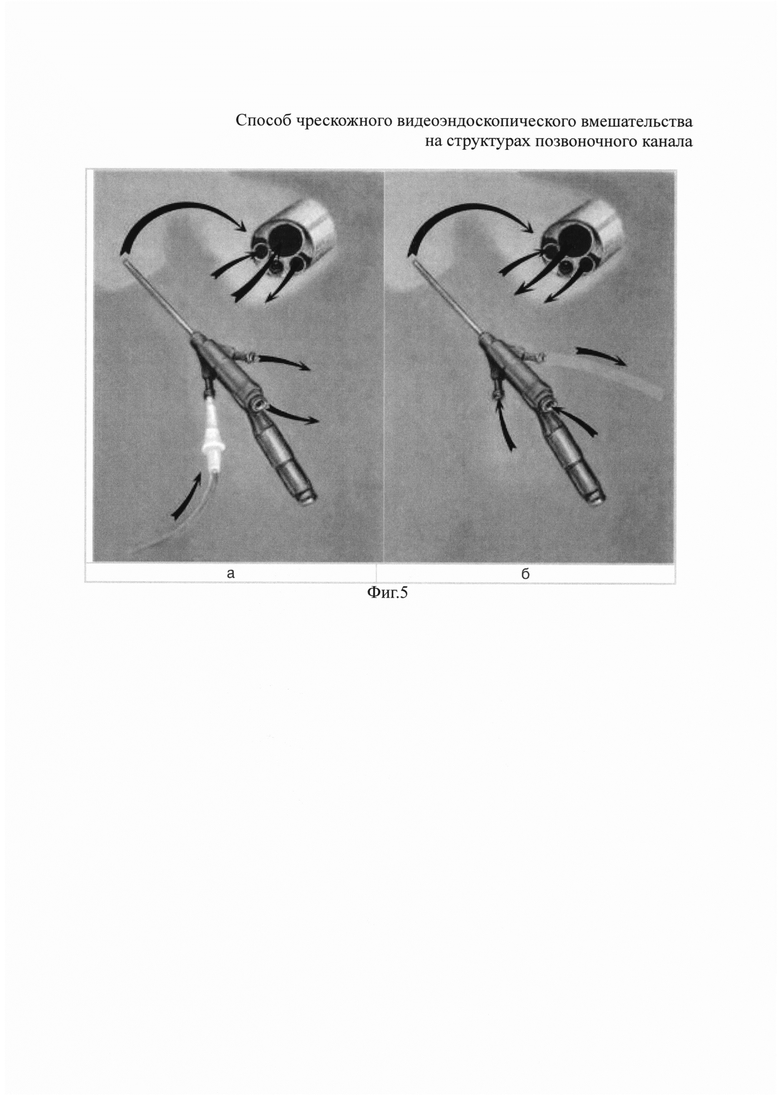
На фиг. 1 показаны этапы операционного доступа: а - рабочая канюля установлена по проводникам и канюлям увеличивающегося диаметра; б - завершения доступа: извлечены проводники и канюли, оставлена рабочая канюля диаметром 7,5 мм, через которую будет установлен эндоскоп. На фиг. 2 показано положение рабочей канюли установленной трансфораминальным доступом в рентгеновском и схематичном изображениях: а - прямая рентгеновская проекция поясничного отдела позвоночника; б - поясничный отдел позвоночника - вид сзади; в - боковая рентгеновская проекция поясничного отдела позвоночника; г - поясничный отдел позвоночника - вид сбоку. На фиг. 3 представлена схема, поясняющая строение эндоскопа: прямоугольником указана дистальная часть эндоскопа; слева - та же часть эндоскопа в увеличении (стрелками обозначены каналы эндоскопа: большой - манипуляционный, маленькими - ирригационный и аспирационный). На фиг. 4 показан общий вид эндоскопа, установленного через рабочую канюлю: белой узкой стрелкой указана трубка подсоединенная к ирригационному каналу для подачи физиологического раствора; черной стрелкой указано наружное отверстие манипуляционного канала с введенным в него инструментом; белой широкой стрелкой указано наружное отверстие аспирационного канала, через который осуществляется пассивный отток физиологического раствора из операционной полости. На фиг. 5 схематически отображены этапы хирургического вмешательства: а - на первом этапе создание первичной операционной полости достигается подачей физиологического раствора хлорида натрия по ирригационному каналу (стрелками указано движение физиологического раствора на уровне проксимальной и дистальной частей эндоскопа); б - на втором этапе через ирригационный и манипуляционный каналы в операционную полость поступает воздух благодаря эффекту разрежения, создаваемому посредством постоянного откачивания воздуха электрическим отсосом через систему трубок и аспирационный канал эндоскопа (стрелками указано движение воздуха на уровне проксимальной и дистальной частей эндоскопа). На фиг. 6 показано видеоэндоскопическое изображение позвоночного канала поясничного отдела в жидкой среде через эндоскоп, установленный интраламинарным доступом: стрелкой указан дефект твердой мозговой оболочки (а, б) - под разными углами зрения. На фиг. 7 показано видеоэндоскопическое изображение позвоночного канала поясничного отдела в воздушной среде низкого давления посредством того же эндоскопа, что и на фиг. 6: стрелкой указан дефект твердой мозговой оболочки (а, б) - под разными углами зрения. На фиг. 8 показано изображение с видеомонитора сразу после активной аспирации ликвора путем приближения дистальной части эндоскопа к месту дефекта твердой мозговой оболочки (а), и через несколько секунд после (б): быстрое накопление прозрачной жидкости в операционной полости - свидетельствуют об истечении цереброспинальной жидкости; тонкой стрелкой указан участок твердой мозговой оболочки с дефектом не закрытые ликвором; толстой стрелкой указана та же область скрытая под слоем жидкости. На фиг. 9 приведено фотоизображение в жидкой (а) и воздушной (б) средах идентичным эндоскопом. Цифрами обозначено: 1 - нервный корешок, 2 - пространство между нервным корешком и межпозвонковым диском, образовавшееся после удаления грыжи и рассечения спаек эпидурального пространства, 3 - межпозвонковый диск. Незначительное скопление крови в эпидуральном пространстве при эндоскопии в воздушной среде (б) связано с временным прекращением откачивания воздуха с целью оценки качества гемостаза и последующего введения гидрогелевого имплантата. На фиг. 10 показаны этапы введения гидрогелевого противорубцового имплантата: а - этап установки дистального конца катетера через манипуляционный канал эндоскопа в пространство между корешком и межпозвонковым диском (белая стрелка); 1 - нервный корешок; 2 - межпозвонковый диск; б - этап введения гидрогелевого имплантата: отчетливое изменение условий визуализации через среду геля повышенной вязкости (б); черной стрелкой указано замедленное прохождение воздушного пузыря через гель.
Способ осуществляют следующим образом. Чрескожное видеоэндоскопическое вмешательство на структурах позвоночного канала выполняют под местной или общей анестезией. Доступ в позвоночный канал осуществляют через разрез кожи длиной менее 1 см, при этом используют специальные иглы, проводники и несколько канюль увеличивающегося диаметра. Доступ завершают установкой дистального конца рабочей канюли, диаметром 7,5 мм в эпидуральном пространстве позвоночника (фиг. 1, фиг. 2). Через рабочую канюлю вводят эндоскоп, содержащий три канала: ирригационный, аспирационный и манипуляционный. (фиг. 3).
В условиях ирригации физиологического раствора хлорида натрия через ирригационный канал выполняют диссекцию неврально-сосудистых структур с использованием инструментов и за счет умеренного проникновения раствора между тканями (фиг. 4).
После создания операционного пространства внутри позвоночного канала прекращают подачу физиологического раствора, отключая при этом трубку для подачи раствора от павильона ирригационного канала эндоскопа. К павильону аспирационного канала подключают трубку, соединенную с электрическим отсосом. Непрерывной работой электрического отсоса (с разрежением не более 0,2 атм) обеспечивается эффект разрежения, распространяющийся с аспирационного канала на эпидуральное пространство, и затем на пространства манипуляционного и ирригационного каналов эндоскопа. При этом вначале из эпидурального пространства происходит эвакуация оставшегося объема физиологического раствора, а затем операционное пространство заполняется воздухом, поступающим туда извне через ирригационный и манипуляционный каналы эндоскопа по градиенту - в область низкого давления. Дальнейшие манипуляции осуществляют в воздушной среде с пониженным давлением за счет сохраняющегося эффекта разрежения в области вмешательства, что предотвращает распространение воздуха по эпидуральному пространству. При этом объем операционной полости является достаточным для отчетливой визуализации структур и выполнения необходимых манипуляций (фиг. 5).
КЛИНИЧЕСКИЕ ПРИМЕРЫ
1. Пациент С., 67 лет. Диагноз: рецидивная срединно-боковая грыжа межпозвонкового диска LIV-LV, эпидуральный фиброз; левосторонний L5 корешковый синдром.
Оперативное пособие (26.01.2017 г.): чрескожный интраламинарный эндоскопический менгигорадикулолиз на уровне LIV-LV позвонков, микрохирургическое удаление грыжи межпозвонкового диска LIV-LV из интерламинарного доступа декомпрессия невральных структур.
Во время операции при выполнении этапа менингорадикулолиза была нарушена целостность твердой мозговой оболочки.
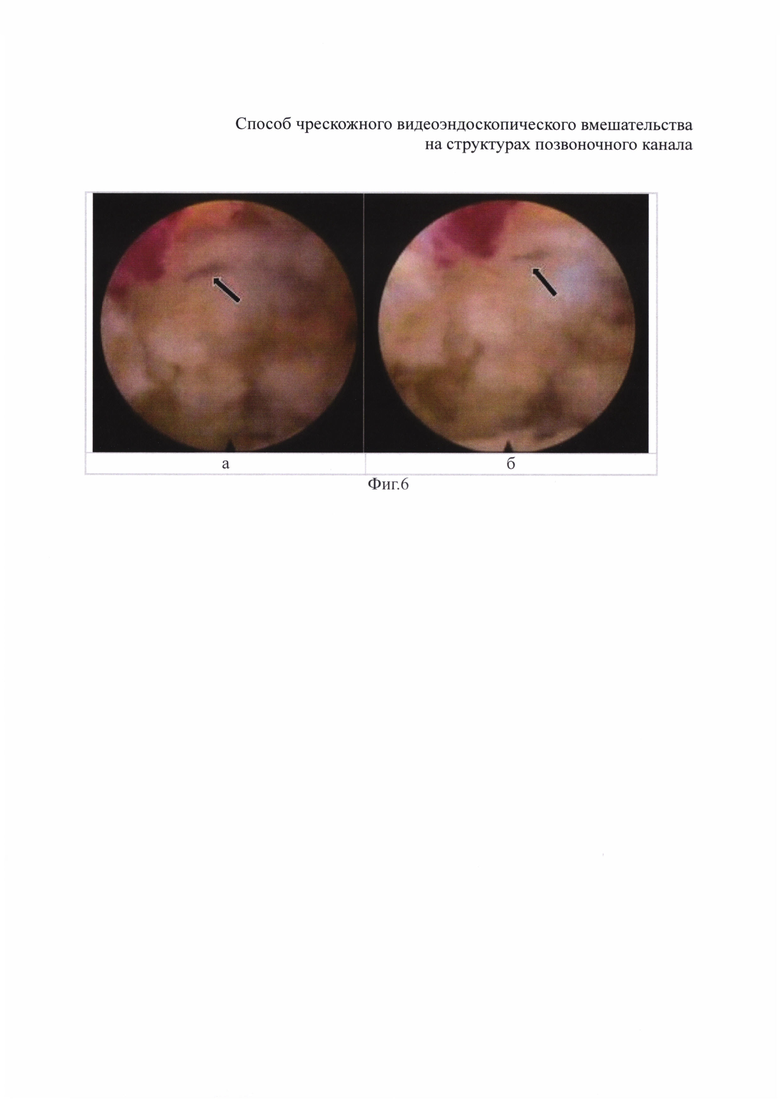
На фиг. 6 и 7 отображено видеоэндоскопическое изображение дефекта твердой мозговой оболочки и ликвореи в жидкой и воздушной средах (при помощи однотипного эндоскопа).
Видеоэндоскопия в жидкой среде позволяет обнаружить дефект твердой мозговой оболочки, однако при этом установить факт истечения цереброспинальной жидкости не представляется возможным. На видео и фотоизображениях, полученных при эндоскопии в жидкой среде, явно изменяются естественные взаимоотношения анатомических структур позвоночного канала. В частности, на фиг. 6 дуральный мешок вдавлен за счет разницы давления ликвора, которое снижено из-за ликвореи, и давления физиологического раствора.
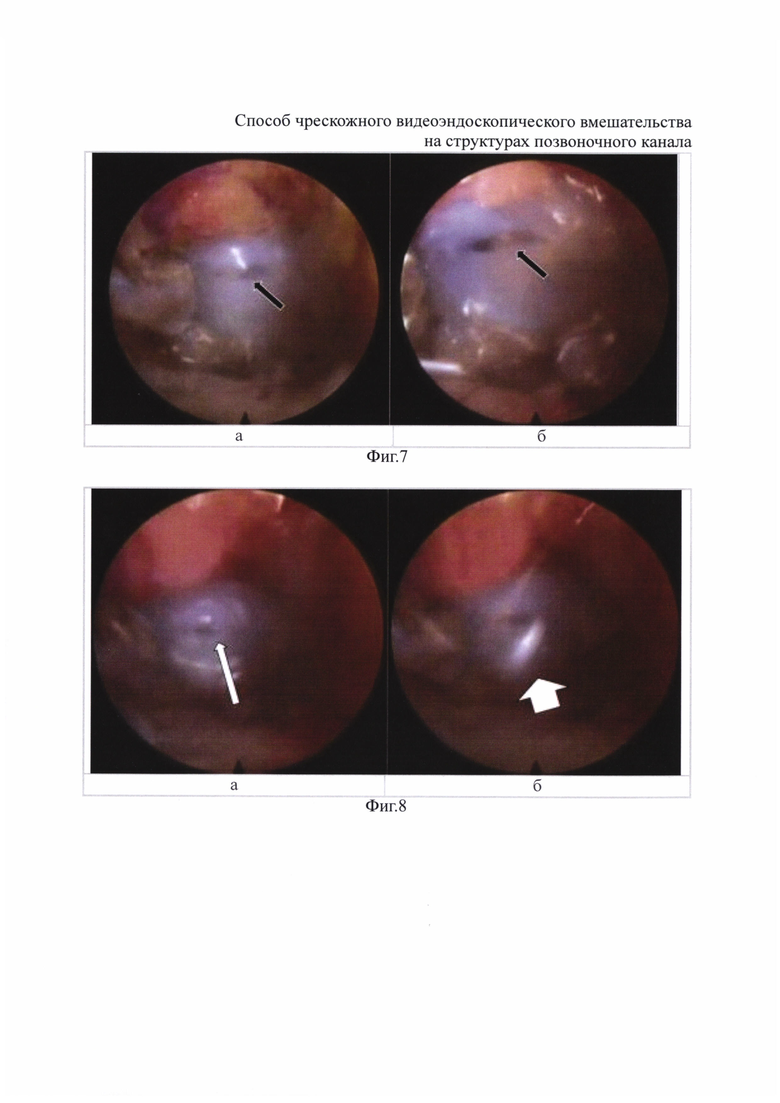
При изменении видеоэндоскопии в жидкой среде на воздушную среду пониженного давления, изображения анатомических структур значительно изменяются (фиг. 7).
В сравнении с визуализацией в жидкой среде, эндоскопия в воздушном потоке низкого давления позволяет отчетливее определить дефект твердой мозговой оболочки, за счет большей прозрачности воздушной среды и принятия дуральным мешком естественной (сферической) формы. Также, указанный способ эндоскопии обеспечивает более четкую визуальную дифференцировку тканей - по цвету и контурам. Опалесцирующая поверхность при визуализации в воздушном потоке низкого давления свидетельствует об истечении ликвора через дефект мозговых оболочек, что еще более отчетливо отмечается при передаче видеоизображения. Истечение цереброспинальной жидкости, помимо прямой визуализации видеоизображения, может быть оценено во временном интервале (фиг. 8).
Данный способ эндоскопии позволил выполнить пластику дефекта твердой мозговой оболочки при помощи клеевых композиций, введенных через катетер, помещенный в операционную полость через манипуляционный канал. В раннем послеоперационном периоде явления наружной ликвореи и ликворной гипотензии отсутствовали, что позволило активизировать пациента на следующие сутки после операции.
2. Пациент Г., 38 лет. Диагноз: дегенеративно-дистрофическое заболевание поясничного отдела позвоночника; рецидивная срединно-боковая грыжа межпозвонкового диска LV-SI, эпидуральный фиброз; левосторонний S1 корешковый болевой синдром; люмбалгия.
Оперативное пособие (21.12.2016 г.): чрескожное эндоскопическое удаление рецидивной грыжи межпозвонкового диска LV-SI из интерламинарного доступа, менингорадикулолиз, декомпрессия невральных структур.
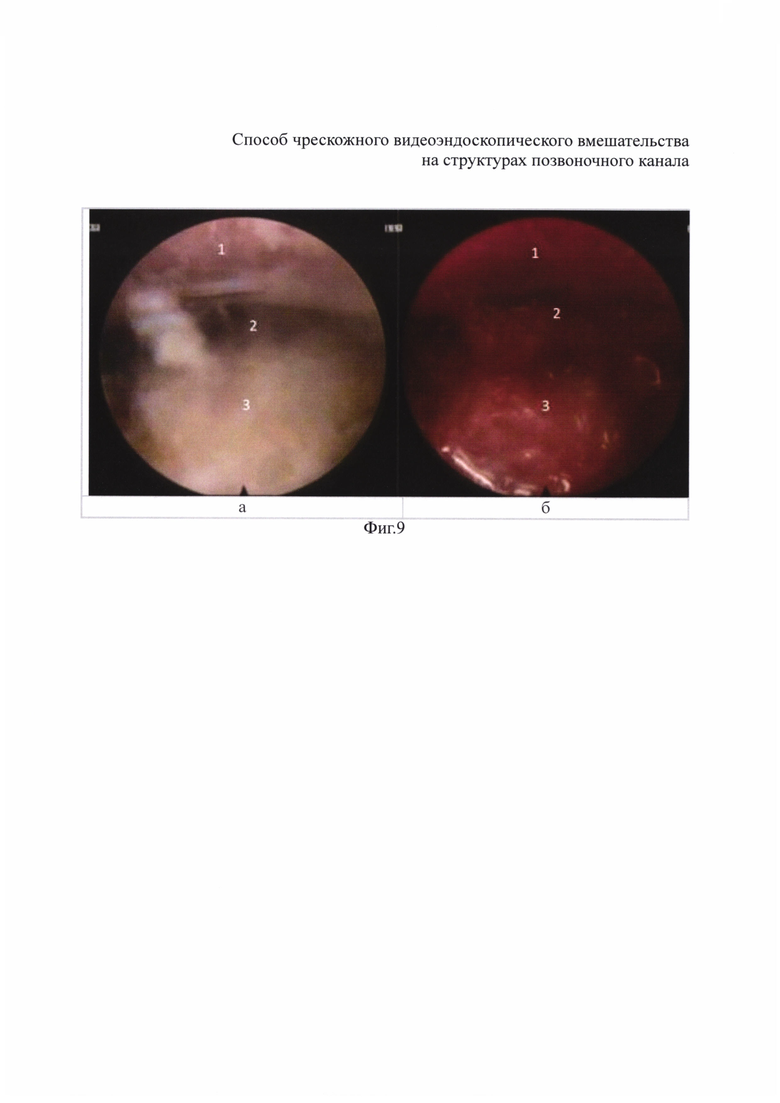
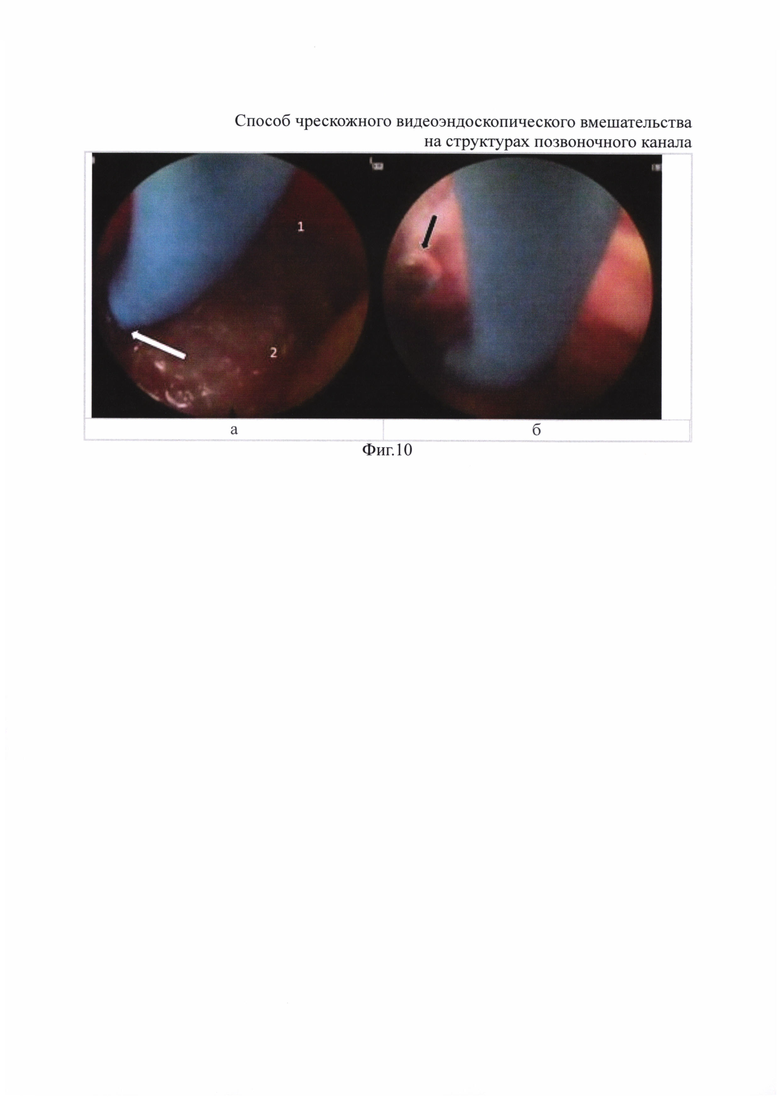
Во время операции, после выполнения этапа менингорадикулолиза, для профилактики повторного формирования эпидурального фиброза было осуществлено введение противорубцового гидрогелевого компонента в эпидуральное пространство способом эндоскопии в воздушной среде.
На интраоперационных фиг. 9 и 10, сделанных при видеоэндоскопическом вмешательстве, отображены этапы смены сред эндоскопии и введения гидрогелевого компонента в эпидуральное пространство позвоночника, также даны пояснения.
В раннем послеоперационном периоде у пациента отмечен полный регресс корешкового синдрома.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВО ДЛЯ ЧРЕСКОЖНОГО УДАЛЕНИЯ ГРЫЖ МЕЖПОЗВОНКОВЫХ ДИСКОВ ШЕЙНОГО ОТДЕЛА ПОЗВОНОЧНИКА С ЭНДОСКОПИЧЕСКОЙ АССИСТЕНЦИЕЙ | 2022 |
|
RU2790945C1 |
| УСТРОЙСТВО ДЛЯ ЧРЕСКОЖНОГО УДАЛЕНИЯ ГРЫЖ МЕЖПОЗВОНКОВЫХ ДИСКОВ ШЕЙНОГО ОТДЕЛА ПОЗВОНОЧНИКА С ЭНДОСКОПИЧЕСКОЙ АССИСТЕНЦИЕЙ | 2020 |
|
RU2759406C1 |
| СПОСОБ ПЕРКУТАННОЙ ПОЯСНИЧНОЙ ФОРАМИНОТОМИИ | 2018 |
|
RU2688733C1 |
| СПОСОБ ПРОФИЛАКТИКИ ЭПИДУРАЛЬНОГО ФИБРОЗА ПРИ РЕВИЗИОННОЙ БИПОРТАЛЬНОЙ ЭНДОСКОПИЧЕСКОЙ ДИСКЭКТОМИИ | 2024 |
|
RU2828821C1 |
| Способ эндоскопической хирургической обработки огнестрельных слепых ранений | 2023 |
|
RU2813954C1 |
| СПОСОБ БИПОРТАЛЬНОЙ ЭНДОСКОПИЧЕСКОЙ СЕКВЕСТРЭКТОМИИ | 2023 |
|
RU2823787C1 |
| СПОСОБ МИКРОХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГРЫЖИ ПОЯСНИЧНОГО ОТДЕЛА ПОЗВОНОЧНИКА | 2011 |
|
RU2474396C1 |
| СПОСОБ ЛЕЧЕНИЯ СПИНАЛЬНЫХ АРАХНОИДИТОВ И АРАХНОИДАЛЬНЫХ КИСТ | 2013 |
|
RU2536715C1 |
| Способ пьезоэлектрической ультразвуковой диссекции костных тканей для формирования носослезного соустья при эндоназальной дакриоцисториностомии | 2022 |
|
RU2802237C1 |
| СПОСОБ ПРОФИЛАКТИКИ РАЗВИТИЯ ПОСЛЕОПЕРАЦИОННОГО РУБЦОВО-СПАЕЧНОГО ПРОЦЕССА ПРИ ХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВАХ НА ПОЯСНИЧНЫХ МЕЖПОЗВОНКОВЫХ ДИСКАХ | 2017 |
|
RU2683735C2 |
Изобретение относится к медицине, а именно к нейрохирургии, и может быть использовано для лечения больных с хирургической патологией позвоночника и неврально-сосудистых структур позвоночного канала. Способ чрескожного видеоэндоскопического вмешательства на структурах позвоночного канала проводят путем двухэтапного вмешательства со сменой сред для эндоскопии. На первом этапе, после введения в эпидуральное пространство рабочей канюли с эндоскопом, выполняют диссекцию неврально-сосудистых структур в условиях ирригации физиологическим раствором хлорида натрия. После создания операционного пространства для манипуляций прекращают ирригацию физиологического раствора. Заполняют операционное пространство воздухом, поступающим извне через ирригационный и манипуляционный каналы эндоскопа по градиенту - в область низкого давления вследствие эффекта разрежения, достигаемого непрерывным откачиванием воздуха из эпидурального пространства через аспирационный канал эндоскопа. Способ обеспечивает уменьшение рисков, связанных с воздействием на неврально-сосудистые структуры позвоночного канала избыточного давления/объема жидкости или газа, не снижая при этом качества изображения за счет того, что смена сред для эндоскопии происходит по градиенту в область низкого давления. 10 ил., 2 пр.
Способ чрескожного видеоэндоскопического вмешательства на структурах позвоночного канала, включающий использование воздуха в качестве среды для эндоскопии, отличающийся тем, что проводят двухэтапное вмешательство со сменой сред для эндоскопии, на первом этапе которого после введения в эпидуральное пространство рабочей канюли с эндоскопом выполняют диссекцию неврально-сосудистых структур в условиях ирригации физиологическим раствором хлорида натрия; после создания операционного пространства для манипуляций прекращают ирригацию физиологического раствора и заполняют операционное пространство воздухом, поступающим извне через ирригационный и манипуляционный каналы эндоскопа по градиенту - в область низкого давления вследствие эффекта разрежения, достигаемого непрерывным откачиванием воздуха из эпидурального пространства через аспирационный канал эндоскопа.
| Сушков С.А | |||
| и др | |||
| Эндоскопическая субфасциальная диссекция перфорантных вен в переднем миофасциальном ложе голени | |||
| Новости хирургии, 2009, Т | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Переносная печь-плита | 1920 |
|
SU184A1 |
| СПОСОБ ДЕКОМПРЕССИИ СПИННОГО МОЗГА ПРИ ПЕРЕЛОМАХ ГРУДНЫХ И ПОЯСНИЧНЫХ ПОЗВОНКОВ | 2011 |
|
RU2467716C1 |
| СПОСОБ МОБИЛИЗАЦИИ ПОЯСНИЧНОГО ОТДЕЛА ПОЗВОНОЧНИКА С ФОРМИРОВАНИЕМ ПЕРЕДНЕГО СПОНДИЛОДЕЗА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2011 |
|
RU2483687C1 |
| СПОСОБ ОПОЗНАВАНИЯ ИЗОБРАЖЕНИИ ПЛОСКИХ ГЕОМЕТРИЧЕСКИХ ФИГУР | 0 |
|
SU179099A1 |
| Кравцов М | |||
| Н | |||
| и др | |||
| Чрескожная видеоэндоскопическая задняя цервикальная фораминотомия и дискэктомия при латеральных грыжах межпозвонковых дисков (обзор литературы и результаты собственных исследований) | |||
| Гений Ортопедии, 2018, т | |||
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
| Русская печь | 1919 |
|
SU240A1 |
| Yang J.S | |||
| et al | |||
| Anterior or posterior approach of full-endoscopic cervical discectomy for cervical intervertebral disc herniation? A comparative cohort study | |||
| Spine, 2014, vol | |||
| Машина для изготовления проволочных гвоздей | 1922 |
|
SU39A1 |
| Тормозная велосипедная втулка | 1923 |
|
SU1743A1 |
| Fessler R.G | |||
| et al | |||
| Minimally invasive cervical microendoscopic foraminotomy: an initial clinical experience., Neurosurgery, 2002, Vol | |||
| Способ запрессовки не выдержавших гидравлической пробы отливок | 1923 |
|
SU51A1 |
| Пишущая машина | 1922 |
|
SU37A1 |
Авторы
Даты
2019-05-21—Публикация
2017-05-10—Подача