ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к терапевтическим способам, вариантам применения и композициям для лечения заболеваний и состояний, связанных с нарушениями лимфатической системы, в частности, лимфедемы.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Лимфедема является хроническим, приводящим к потере трудоспособности и обезображивающим состоянием локализованного застоя лимфатической жидкости и прогрессирующего отека, которое вызвано дисфункциональным состоянием лимфатической системы. Это пожизненное состояние, серьезно влияющее на качество жизни примерно 140 миллионов пациентов во всем мире.
Первичная лимфедема, редкое наследственное заболевание, как правило, возникает в результате аномального развития лимфатических сосудов. Симптомы первичной лимфедемы могут возникать при рождении или позже на протяжении жизни.
Приобретенная или вторичная лимфедема возникает в результате повреждения лимфатической системы. В западных странах она чаще всего возникает в результате диссекции лимфатических узлов, хирургической операции и/или радиотерапии, когда повреждение лимфатической системы возникает в процессе лечения рака, в частности, рака молочной железы. По оценкам, в США примерно 110000 пациентов с раком молочной железы страдают лимфедемой вследствие диссекции и/или облучения подмышечных лимфатических узлов, и каждый год примерно у 15000 новых пациентов развивается связанная с раком молочной железы лимфедема.
Терапевтический лимфангиогенез, регенерация лимфатических сосудов, является привлекательным подходом к лечению лимфедемы. Несмотря на недавний прорыв в области знаний о молекулярных механизмах, обусловливающих лимфангиогенез, точные морфогенетические механизмы первичного лимфангиогенеза остаются не до конца понятными.
Фактор роста эндотелия сосудов C (VEGF-C) является основным фактором лимфангиогенеза в период эмбрионального развития и в различных лимфангиогенных процессах у взрослых (Alitalo, 2011, Nature Medicine 17: 1371-1380). VEGF-C действует путем активации VEGFR-3 и - в его протеолитически процессированной зрелой форме - также VEGFR-2. Делеция гена Vegfc у мышей приводит к нарушению развития лимфатической системы из-за неспособности новых дифференцированных лимфатических эндотелиальных клеток мигрировать из центральных вен к участкам, где образуются первые лимфатические структуры (Karkkainen et al., 2003, Nature Immunology 5: 74-80; Hägerling et al., 2013, EMBO J 32: 629-644). Данный фенотип мог быть спасен за счет использования рекомбинантного VEGF-C (Karkkainen et al., 2003, там же). Для спасения использовали «зрелую» рекомбинантную форму VEGF-C, лишенную N- и C-концевых пропептидов. В клетках, секретирующих эндогенный VEGF-C, эти пропептиды должны быть протеолитически отщеплены от центрального домена гомологии VEGF (VHD), чтобы VEGF-C достиг своего полного сигнального потенциала (Joukov et al., 1997, EMBO J 16: 3898-3911). VEGF-C может в значительной степени активировать основной ангиогенный рецептор VEGFR-2, только если оба пропептида отщеплены (Joukov et al., 1997, там же), и, таким образом, зрелый VEGF-C также стимулирует ангиогенез.
Показано, что мутации в рецепторе VEGF-C VEGFR-3 приводят к развитию наследственной лимфедемы, известной как болезнь Милроя (Karkkainen et al., 2000, Nature Genetics 25: 153-159). С другой стороны, синдром лимфангиэктазии-лимфедемы Хеннекама связан с мутациями в гене коллаген- и кальций-связывающие домены EGF-содержащего белка 1 (CCBE1) (Alders et al., 2009, Nature Genetics 41: 1272-1274), но неясно, каким образом мутант CCBE1 вызывает лимфатический фенотип. В любом случае, предположение о генетическом взаимодействии CCBE1 и VEGF-C возникло благодаря фенотипу двойных гетерозиготных CCBE1+/-;VEGF-C+/- мышей (Hägerling et al., 2013, там же).
Хотя было высказано предположение, что CCBE1 увеличивает про-лимфангиогенную активность VEGF-C в анализе микрокармана роговицы (Bos et al., 2011, Circulation Research 109: 486-491), его истинная роль в лимфангиогенезе оставалась неясной. Одна из причин заключается в том, что, поскольку продуцирование нативного полноразмерного CCBE1 было невозможно, белок CCBE1, используемый в экспериментах, был искусственным укороченным белком CCBE1, слитым с Fc-доменом IgG человека.
Несмотря на значительный прогресс, достигнутый в последние годы в выявлении молекул, специфически экспрессируемых на лимфатических сосудах, для лимфедемы не существует радикального лечения. Поскольку современная практика включает только паллиативное лечение, существует потребность в усовершенствованных методах лечения лимфедемы.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном аспекте настоящее изобретение относится к сочетанию полноразмерного CCBE1 и VEGF-C для использования в лечении лимфедемы.
В другом аспекте настоящее изобретение относится к способу лечения лимфедемы путем введения пациенту, который нуждается в этом, сочетания полноразмерного CCBE1 и VEGF-C одновременно, раздельно или последовательно.
В некоторых вариантах осуществления вышеуказанных аспектов сочетание включает CCBE1 в форме полипептида, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 1, аминокислоты 35-406 из SEQ ID NO: 1 или аминокислотную последовательность, имеющую по меньшей мере 80% идентичности аминокислотной последовательности с ними.
В некоторых других вариантах осуществления сочетание включает CCBE1 в форме полинуклеотида, содержащего нуклеотидную последовательность, приведенную в SEQ ID NO: 2, нуклеотиды 71-1291 из SEQ ID NO: 2 или нуклеотидную последовательность, имеющую по меньшей мере 80% идентичности нуклеотидной последовательности с ними.
В некоторых других вариантах осуществления сочетание включает VEGF-C в форме полипептида, содержащего аминокислотную последовательность, выбранную из группы, состоящей из аминокислот 32-419 из SEQ ID NO: 3; аминокислот 32-227, ковалентно связанных с аминокислотами 228-419 из SEQ ID NO: 3; аминокислот 112-227 из SEQ ID NO: 3; аминокислот 103-227 из SEQ ID NO: 3, а также аминокислотной последовательности, имеющей по меньшей мере 80% идентичности аминокислотной последовательности с ними.
В некоторых других вариантах осуществления сочетание включает VEGF-C в форме полинуклеотида, содержащего нуклеотидную последовательность, выбранную из группы, состоящей из нуклеотидов 524-1687 из SEQ ID NO: 4; нуклеотидов 737-1687 из SEQ ID NO: 4; нуклеотидов 764-1687 из SEQ ID NO: 4; нуклеотидов 737-1111 из SEQ ID NO: 4; нуклеотидов 764-1111 из SEQ ID NO: 4, а также нуклеотидной последовательности, имеющей по меньшей мере 80% идентичности нуклеотидной последовательности с ними.
Следующий аспект настоящего изобретения относится к фармацевтической композиции, содержащей сочетание полноразмерного CCBE1 и VEGF-C из любого из вариантов осуществления, описанных выше.
Другие аспекты, конкретные варианты осуществления, цели, подробности и преимущества изобретения изложены в следующих далее чертежах, подробном описании и примерах.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Далее изобретение описано более подробно путем изложения предпочтительных вариантов осуществления со ссылкой на прилагаемые чертежи, в которых
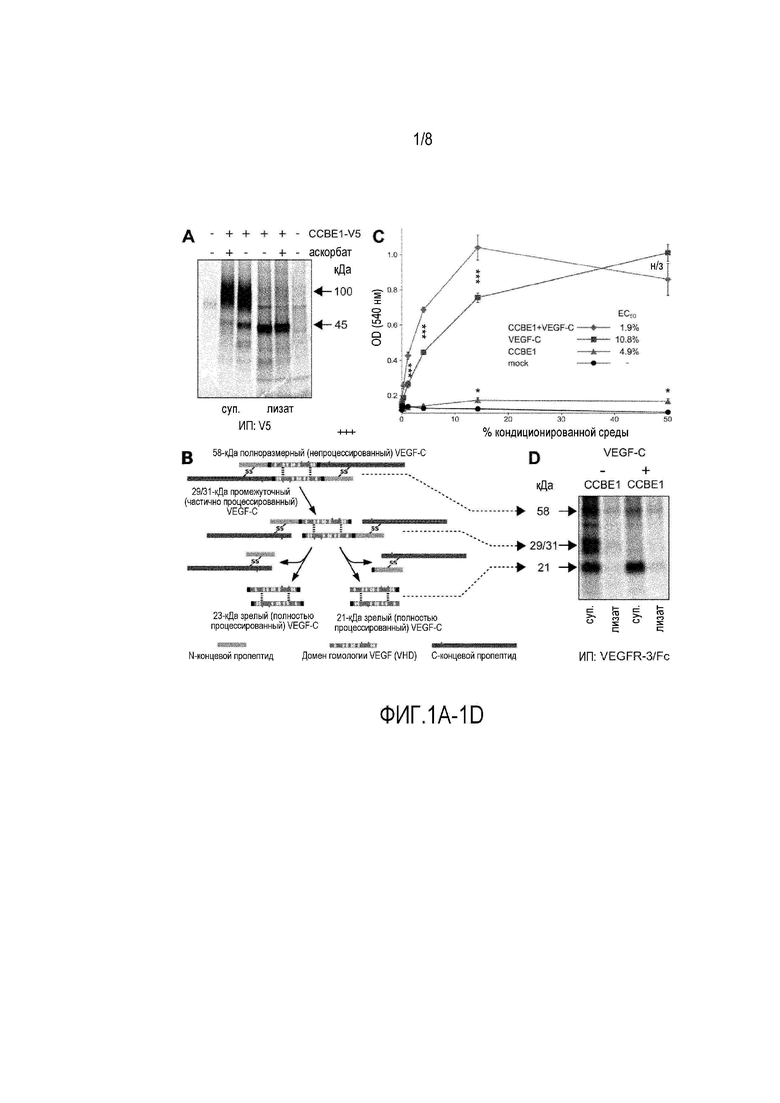
Фигура 1 демонстрирует, что коэкспрессия с CCBE1 увеличивает протеолитический процессинг VEGF-C до зрелого, полностью активного VEGF-C. Клетки 293T трансфицировали только CCBE1 (фигура 1A) или VEGF-C+/-CCBE1 (фигура 1D), инкубировали с радиоактивными аминокислотами и супернатанты среды (суп) и клеточные лизаты анализировали путем преципитации с антителом V5 (ИП:V5) и растворимым рецептором VEGF-C (VEGFR-3/Fc), с последующей авторадиографией. Следует отметить, что обнаружен как внутри-, так и внеклеточный CCBE1, и секреция CCBE1, в отличие от коллагенов, не зависит от добавления аскорбата в среду для культивирования клеток. На фигуре 1B приведено схематическое изображение биосинтеза и процессинга VEGF-C. Показана схематическая структура предшественника VEGF-C и различные процессированные формы (Karpanen & Alitalo, 2008, Annual Review of Pathology: Mechanisms of Disease 3: 367-397). Стрелки указывают на соответствующие полосы в панели D. Фигура 1D демонстрирует, что преципитаты VEGF-C с VEGFR-3/Fc содержат нерасщепленный, частично расщепленный и расщепленный VEGF-C. Коэкспрессия с CCBE1 уменьшает количество нерасщепленного VEGF-C и увеличивает количество активированного VEGF-C. На фигуре 1C показано, что супернатанты культур, экспрессирующих как CCBE1, так и VEGF-C, имеют более высокую активность в стимулировании роста клеток Ba/F3-VEGFR-3/EpoR, чем супернатанты культур, экспрессирующих только VEGF-C. Статистически значимое различие с P<0,05 отмечено * и с P<0,001 отмечено ***, н/з указывает, что различия не являются статистически значимыми; n=4.
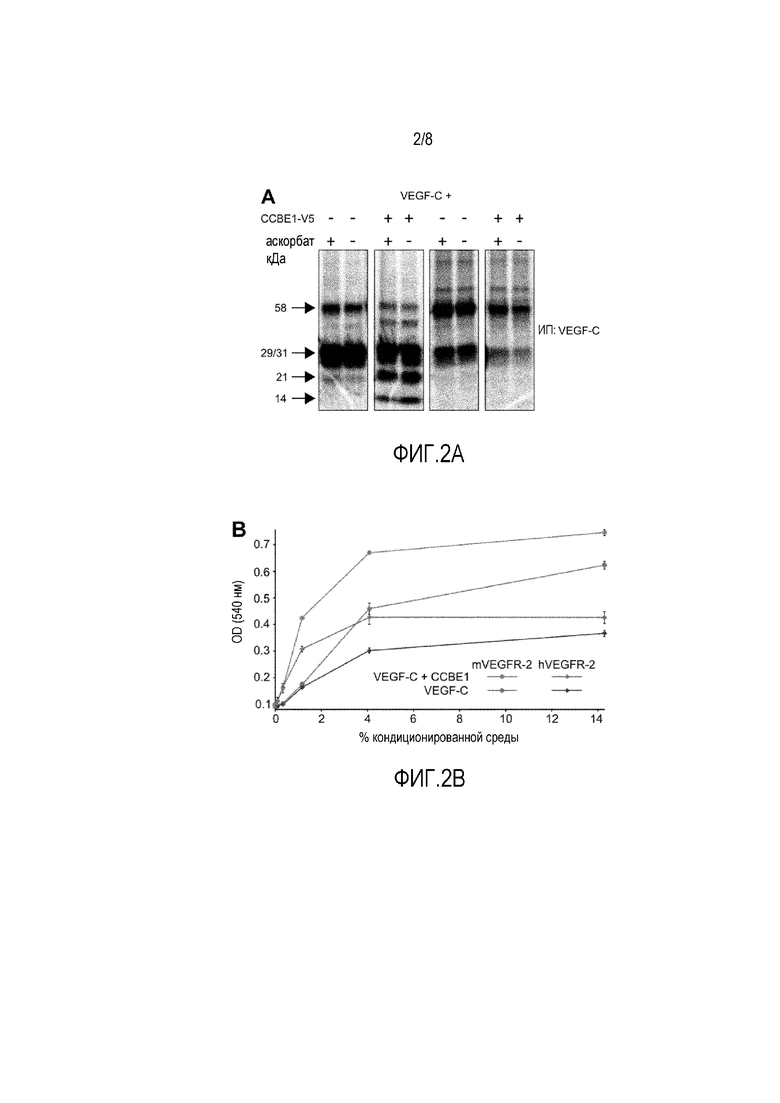
Фигура 2 демонстрирует, что CCBE1 способствует секреции VEGF-C. На фигуре 2A показана иммунопреципитация VEGF-C из супернатантов и лизатов клеток, трансфицированных VEGF-C с и без CCBE1, как указано. Значения молекулярной массы слева показывают подвижность основных форм VEGF-C. Следует отметить, что в супернатанте количество зрелой 21-кДа формы VEGF-C возрастает (8-кратно) и количество нерасщепленного VEGF-C и 29/31-кДа полипептида снижается (на 74% и 51%, соответственно) при котрансфекции с CCBE1 (сравните дорожки 1, 2 и 3, 4). 14-кДа фрагмент, возникающий в результате N-концевого расщепления VEGF-C, обнаружен только в супернатантах котрансфицированных клеток. Котрансфекция с CCBE1 способствует секреции VEGF-C, поскольку количество внутриклеточных полипептидов VEGF-C снижается на 80% в клеточных лизатах CCBE1-котрансфицированных клеток (сравните дорожки 5, 6 и 7, 8). Фигура 2B демонстрирует, что кондиционированная среда от культур, экспрессирующих как CCBE1, так и VEGF-C, имеет более высокую активность стимулирования роста клеток Ba/F3, экспрессирующих мышиные (м) или человеческие (ч) химеры VEGFR-2/EpoR, чем супернатанты от культур, экспрессирующих только VEGF-C.
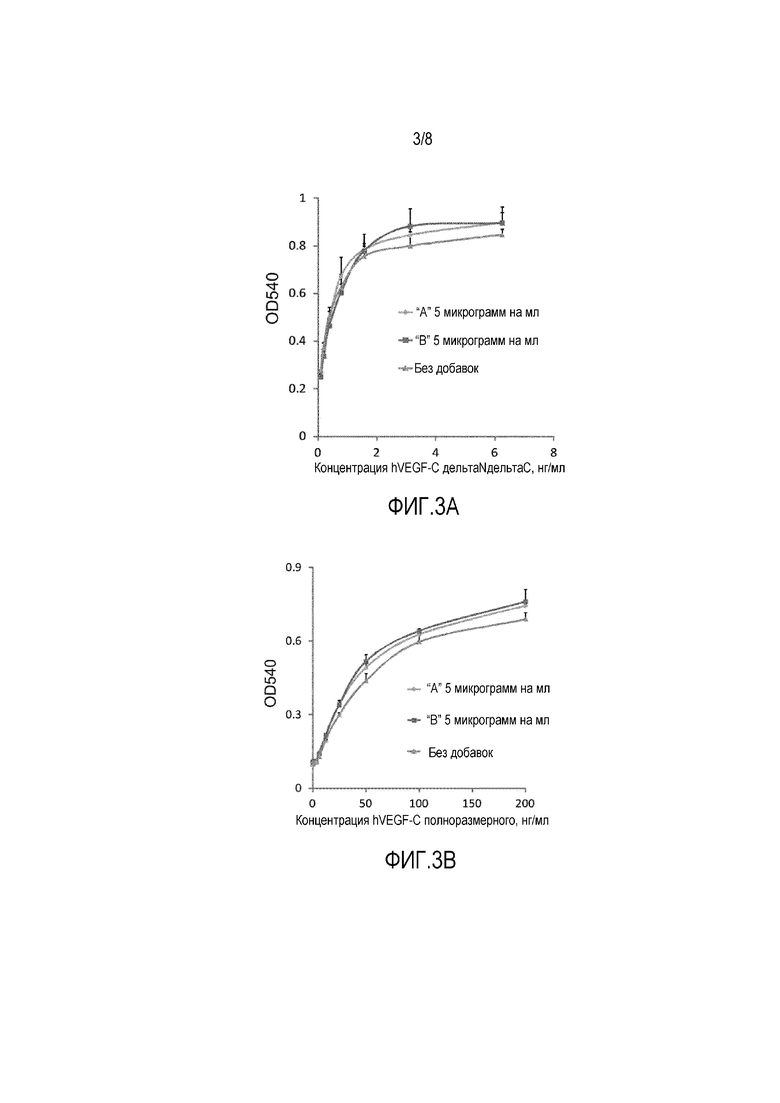
Фигура 3 демонстрирует, что укороченный на домен коллагена слитый с Fc CCBE1 не влияет на стимулирующую VEGFR-3 активность VEGF-C. Клетки чVEGFR-3/EpoR-Ba/F3 стимулировали VEGF-CΔNΔC человека (зрелый VEGF-C; фигура 3A) или полноразмерным VEGF-C (предшественник VEGF-C; фигура 3B) в возрастающих концентрациях в присутствии постоянной дозы (5 мкг/мл) укороченного CCBE1-Fc («A») или белка отрицательного контроля, состоящего только из Fc-части («B»). Клетки инкубировали в условиях стимуляции в общей сложности в течение 3 дней. По окончании этого периода к культурам клеток добавляли тиазолил синий тетразолий бромид (MTT, Sigma-Aldrich) и количество живых клеток в каждой культуре (прямой показатель клеточной пролиферации) подсчитывали путем измерения оптической плотности OD540 (желтый MTT восстанавливается митохондриальными ферментами живых клеток, с образованием темно-синего материала).
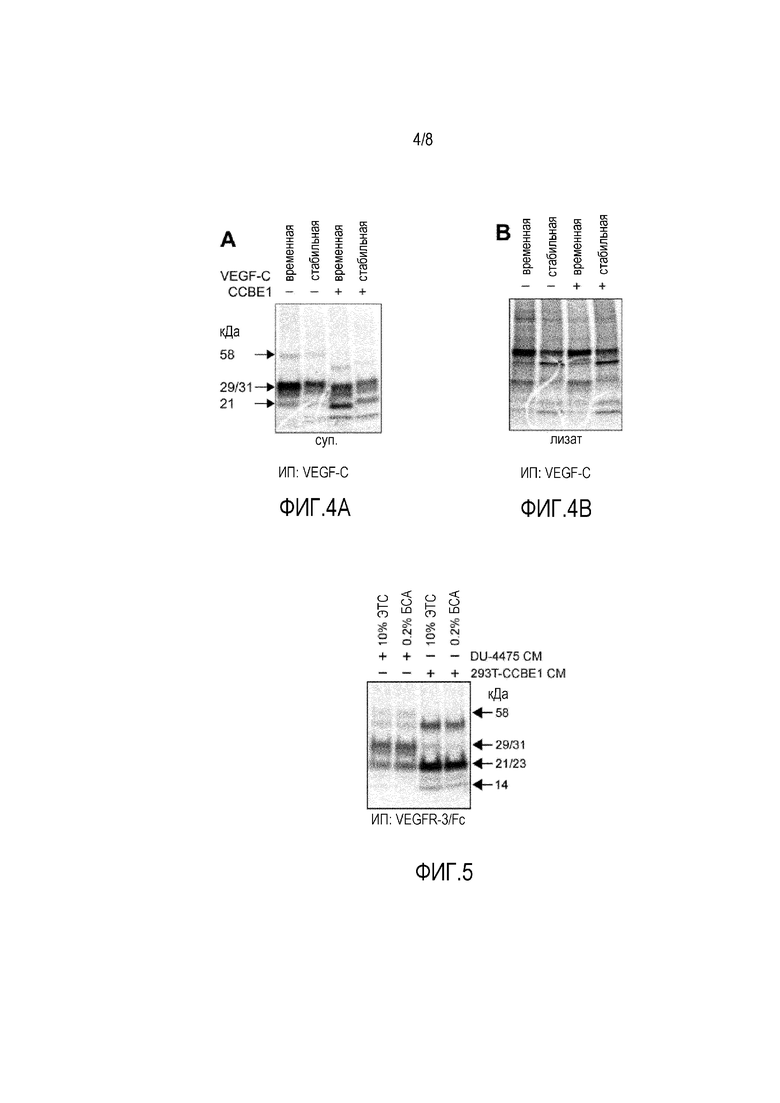
Фигура 4 демонстрирует, что расщепление VEGF-C возрастает в клетках, экспрессирующих CCBE1 in trans. Отдельные клеточные популяции трансфицировали VEGF-C или CCBE1 и затем смешивали на период метаболического мечения, как указано. Следует отметить, что при ко(трансфекции) с CCBE1 количество зрелого VEGF-C (21-кДа) возрастает и количество полноразмерного (58-кДа) или частично расщепленного (29/31-кДа) VEGF-C в супернатанте уменьшается (фигура 4A), тогда как количество в клеточных лизатах остается без изменения (фигура 4B). Следует также отметить небольшую разницу в миграции VEGF-C между стабильно и временно трансфицированными клетками, возникающую вследствие различных паттернов гликозилирования VEGF-C, продуцируемого стабильно трансфицированными клетками 293S GnTI (Chaudhary et al, 2012, Nature Protocols 7: 453-466).
Фигура 5 демонстрирует, что усиливающая расщепление VEGF-C активность CCBE1 секретируется в среду, то есть, является растворимым компонентом кондиционированного супернатанта CCBE1-продуцирующих клеток 293T. Это свидетельствует о том, что активность не ограничена областью клеточной поверхности или внеклеточного матрикса, но может быть введена терапевтически, например, в виде растворимого белка. Более того, усиливающая расщепление активность не ингибируется или существенно не ингибируется при добавлении 10% ЭТС. Однако не все формы CCBE1 усиливают расщепление VEGF-C. Например, CCBE1, продуцируемый DU-4475, не усиливает расщепление VEGF-C.
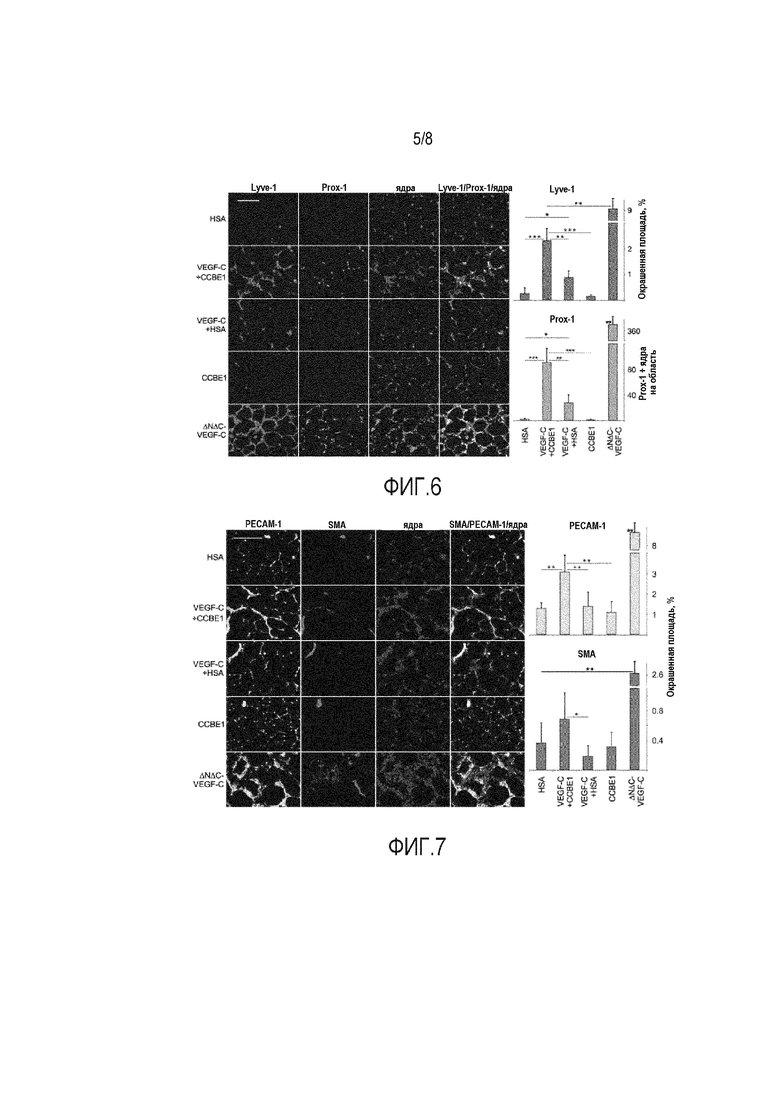
Фигура 6 демонстрирует, что CCBE1 усиливает лимфангиогенез in vivo. Иммуноокрашивание мышиной передней большеберцовой мышцы, трансдуцированной AAV9, кодирующим указанные факторы, с окрашиванием на указанные антигены. Следует отметить, что полноразмерный VEGF-C сам по себе индуцирует лишь умеренный лимфангиогенный ответ, однако его котрансдукция с CCBE1 приводит к сильному ответу, о чем свидетельствует окрашивание лимфатических сосудов на LYVE-1 и Prox-1. В качестве положительного контроля использовали AAV9, кодирующий ΔNΔC-VEGF-C (эквивалент полностью процессированного зрелого VEGF-C). Ответ на сывороточный альбумин был сопоставим с ответом на одиночный CCBE1. Статистически значимое различие с P<0,05 отмечено *, с P<0,01 отмечено ** и с P<0,001 отмечено ***, н/з указывает, что различия не являются статистически значимыми; n ≥5.
Фигура 7 демонстрирует, что котрансдукция CCBE1 с VEGF-C стимулирует ангиогенез. Иммуногистохимическое окрашивание на эндотелиальные (PECAM-1) и гладкомышечные клеточные (SMA) маркеры в передней большеберцовой мышце. Количественная оценка окрашенных областей показана справа. Статистически значимое различие с P<0,05 отмечено *, с P<0,01 отмечено ** и с P<0,001 отмечено ***, n ≥5.
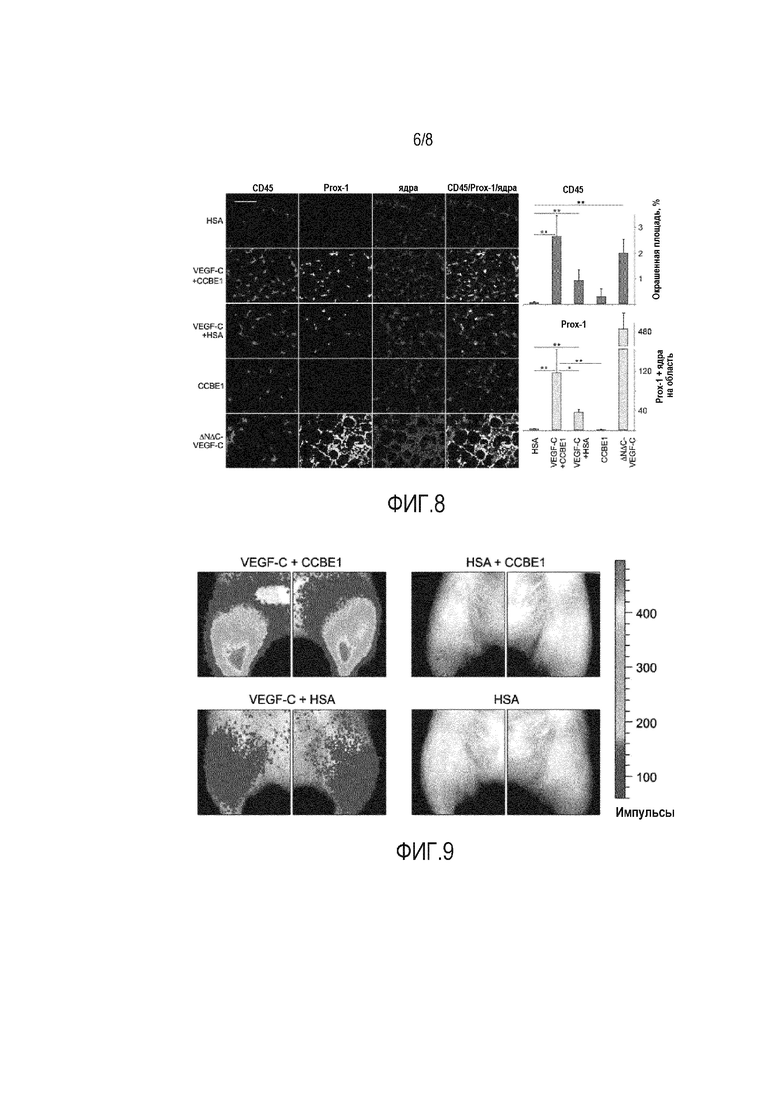
Фигура 8 иллюстрирует рекрутинг CD45+ лейкоцитов в результате котрансдукции CCBE1/VEGF-C. Фактор транскрипции Prox1 использовали в качестве маркера для лимфатических эндотелиальных клеток. Анализ выполняли, как указано на фигуре 7.
Фигура 9 демонстрирует сигналы репортера VEGFR-3-люцифераза у мышей, инъецированных указанными векторами AAV9 в переднюю большеберцовую мышцу. Следует отметить, что котрансдукция VEGF-C и CCBE1 приводит к сильному люциферазному сигналу, свидетельствующему о масштабном ответе в виде лимфангиогенеза, в то время как полноразмерный VEGF-C и CCBE1 приводили лишь к незначительной люциферазной активности.
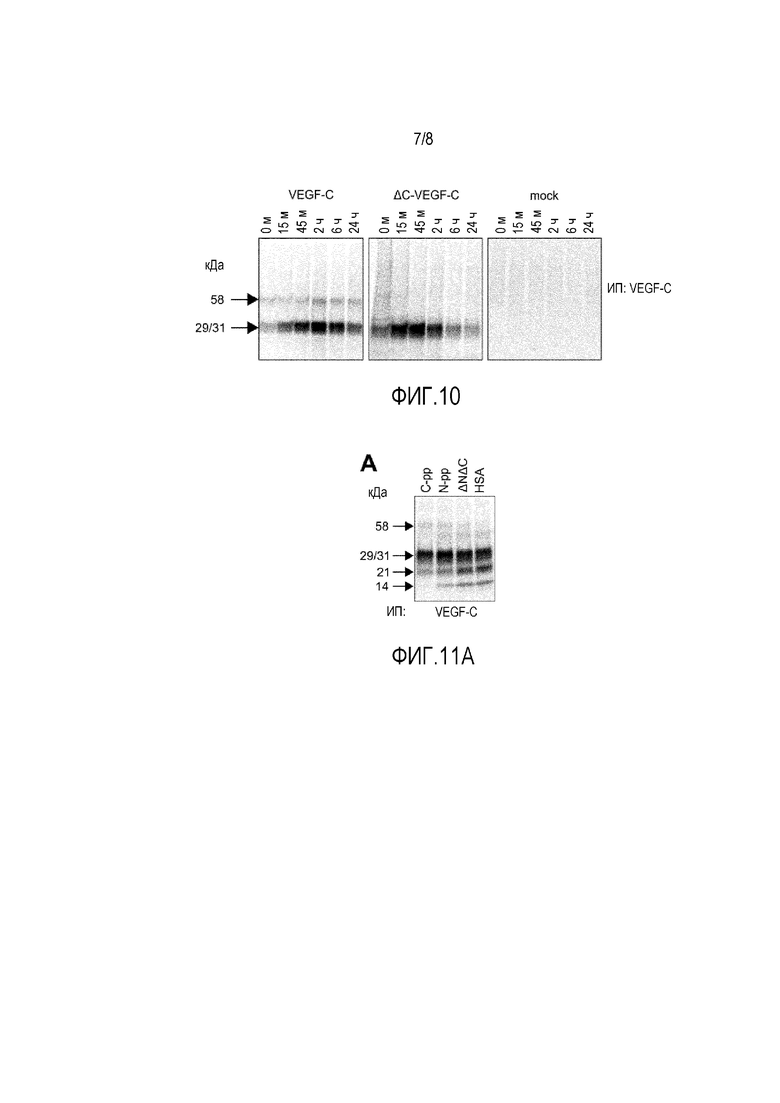
Фигура 10 демонстрирует, что в анализе вытеснения метки пик секреции VEGF-C дикого типа имеет место через 2 часа, тогда как пик для мутанта VEGF-C без C-концевого пропептида (ΔC-VEGF-C) имеет место уже в период от 15 до 45 минут.
Фигура 11 демонстрирует эффект N- и C-концевых пропептидов VEGF-C на процессинг фактора роста. Следует отметить, что количества как зрелой 21-кДа формы VEGF-C, так и 14-кДа N-концевого пропептида снижаются за счет конкуренции с C- и N-концевыми пропептидами (фигура 11A). Фигура 11B иллюстрирует протеолитический процессинг VEGF-D и химеры VEGF-D/VEGF-C (CDC) в присутствии или в отсутствие котрансфекции с CCBE1. C-пп, C-концевой пропептид; N-пп, N-концевой пропептид; ЧСА, человеческий сывороточный альбумин; ΔNΔC, укороченные с C- и N-конца формы VEGF-C в сравнении со зрелым VEGF-C.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Изобретение основано на том открытии, что полноразмерный коллаген- и кальций-связывающие EGF домены-содержащий белок 1 (CCBE1) стимулирует секрецию фактора роста эндотелия сосудов C (VEGF-C) и протеолитическое расщепление большего по размеру неактивного предшественника VEGF-C, что приводит к полной активации VEGF-C, ведущей к усиленной сигнализации рецепторов VEGF-C VEGFR-3 и VEGFR-2, лимфангиогенезу и ангиогенезу in vivo. Таким образом, настоящее изобретение относится терапевтическому инструменту, сочетанию CCBE1 и VEGF-C, для модулирования лимфангиогенеза и ангиогенеза при различных заболеваниях, связанных с дисфункциональной лимфатической системой, таких как лимфедема.
Терапевтическое применение CCBE1 и VEGF-C можно реализовывать различными способами. Например, можно осуществлять совместно введение CCBE1 и VEGF-C методами генной терапии, белковой терапии или при помощи любого нужного их сочетания. Иными словами, путь и способ введения CCBE1 и VEGF-C можно выбирать независимо. Кроме того, совместное введение CCBE1 и VEGF-C может быть одновременным, раздельным или последовательным.
Используемый в настоящем документе термин «или» является инклюзивным оператором «или» и эквивалентен термину «и/или», если из контекста явно не следует иное. Кроме того, во всем тексте описания единственное число существительных включает и их множественное число.
Используемый в настоящем документе термин «генная терапия» означает перенос полинуклеотида CCBE1 или VEGF-C в выбранные целевые клетки или ткани таким образом, который делает возможной их экспрессию в терапевтически эффективном количестве. В соответствии с настоящим изобретением генную терапию можно использовать для замены дефектного гена или добавки генного продукта, который не продуцируется в терапевтически эффективном количестве или в терапевтически полезное время у млекопитающего, в частности, человека, с нарушенной лимфатической системой.
Используемый в настоящем документе термин «белковая терапия» означает введение полипептида CCBE1 или VEGF-C в терапевтически эффективном количестве млекопитающему, в частности, человеку, с нарушенной лимфатической системой, которому необходима терапия. В настоящем документе термины «полипептид» и «белок» используют взаимозаменяемо для обозначения полимеров аминокислот любой длины.
Используемый в настоящем документе термин «терапевтически эффективное количество» означает количество CCBE1 или VEGF-C, при котором вредные эффекты нарушенной лимфатической системы, как минимум, ослабляются.
Используемый в настоящем документе термин «CCBE1» означает полноразмерный полипептид CCBE1 или полинуклеотид, кодирующий указанный полноразмерный CCBE1, если четко не указано иное. Предпочтительно, CCBE1 представляет собой CCBE1 млекопитающего, предпочтительно человека. В некоторых вариантах осуществления полноразмерный полипептид CCBE1 содержит аминокислотную последовательность, приведенную в SEQ ID NO: 1, предпочтительно без сигнального пептида. Предположительно, сигнальный пептид человеческого CCBE1 состоит из аминокислот 1-34 последовательности SEQ ID NO: 1, однако при продуцировании в клетках млекопитающих сигнальный пептид автоматически отщепляется надлежащим образом. Стоит отметить, что полипептид CCBE1, CCBE1Δколлаген-Fc, описанный Bos et al. в Clinical Research 2011, 109: 486-491, представляет собой укороченный полипептид CCBE1, продуцируемый с кДНК, кодирующей аминокислоты 1-191 в SEQ ID NO: 1 и Fc-часть IgG1 человека. Такой укороченный CCBE1 состоит из EGF и кальций-связывающих доменов EGF CCBE1, слитых с Fc-доменом IgG человека, однако лишен домена коллагеновых повторов.
Для специалиста в данной области понятно, что полипептид CCBE1, используемый по настоящему изобретению, может отличаться от полипептида, приведенного в SEQ ID NO: 1, при условии, что он сохраняет свою биологическую активность. Иллюстративным способом определения того, сохраняет ли вариант CCBE1 свою биологическую активность, является определение его способности расщеплять полноразмерный VEGF-C. Это можно выполнять, например, инкубируя клетки, экспрессирующие полноразмерный VEGF-C, с тестируемым вариантом CCBE1 и делая вывод о том, что вариант CCBE1 сохраняет свою биологическую активность, если расщепление VEGF-C увеличивается. Указанное расщепление VEGF-C можно определять, например, путем метаболического мечения и специфичной для белка преципитации, такой как иммунопреципитация, используя методы, хорошо известные в данной области. При желании, CCBE1, имеющий аминокислотную последовательность, приведенную в SEQ ID NO: 1, можно использовать в качестве положительного контроля.
В некоторых вариантах осуществления полипептид CCBE1 содержит аминокислотную последовательность, которая является консервативным вариантом последовательности SEQ ID NO: 1. Применительно к полипептидам термин «консервативный вариант последовательности» означает модификации аминокислотной последовательности, возникающие в результате замен аминокислот аналогичными аминокислотами, хорошо известными в данной области (например, аминокислотами аналогичного размера и с аналогичными свойствами заряда), которые существенно не изменяют биологические свойства конкретного полипептида. То же относится к делециям и добавлениям аминокислот. В некоторых других вариантах осуществления полипептид CCBE1 содержит аминокислотную последовательность, которая по меньшей мере на 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или более идентична аминокислотной последовательности, приведенной в SEQ ID NO: 1.
При использовании в настоящем документе % идентичности между двумя последовательностями является функцией от числа идентичных положений, общих для последовательностей (то есть, % идентичности = количеству идентичных положений/общее количество положений × 100), с учетом количества делеций и длины каждой делеции, которые необходимо вносить для оптимального выравнивания двух последовательностей. Сравнение последовательностей и определение процента идентичности между двумя последовательностями можно выполнять с использованием математических алгоритмов, известных в данной области. Это относится как к аминокислотным, так и к нуклеотидным последовательностям.
Используемый в настоящем документе термин «полинуклеотид CCBE1» означает любой полинуклеотид, такой как одноцепочечная или двухцепочечная ДНК или РНК, содержащий нуклеотидную последовательность, кодирующую полипептид CCBE1. В некоторых вариантах осуществления полинуклеотид CCBE1 содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 2, с 5’- и 3’ нетранслируемыми областями (UTR) или консервативный вариант этой последовательности. В некоторых предпочтительных вариантах осуществления полинуклеотид CCBE1 содержит кодирующую последовательность (CDS) для полноразмерного CCBE1, то есть, нуклеотиды 71-1291 в SEQ ID NO: 2, или консервативный вариант этой последовательности.
Применительно к полинуклеотидам термин «консервативный вариант последовательности» означает модификации нуклеотидной последовательности, которые существенно не изменяют биологические свойства закодированного полипептида. Консервативные варианты нуклеотидной последовательности включают варианты, возникающие вследствие вырожденности генетического кода и в результате молчащих мутаций. То же относится к заменам, делециям и добавлениям нуклеотидов. Таким образом, для любого полипептида CCBE1 существует несколько кодирующих CCBE1 полинуклеотидных последовательностей, любую из которых можно использовать терапевтически в соответствии с настоящим изобретением. В некоторых других вариантах осуществления полинуклеотид CCBE1 может быть по меньшей мере на 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или более идентичен нуклеотидной последовательности, приведенной в SEQ ID NO: 2, при условии, что он кодирует полипептид CCBE1, который сохраняет свою биологическую активность.
Используемый в настоящем документе термин «полипептид VEGF-C» означает любую известную форму VEGF-C, включая препро-VEGF-C, частично процессированный VEGF-C и полностью процессированный зрелый VEGF-C. В процессе биосинтеза полноразмерная форма VEGF-C (58-кДа) сначала подвергается протеолитическому расщеплению в C-концевой части, что приводит к образованию 29/31-кДа промежуточной формы, удерживаемой вместе дисульфидными связями, и последующему расщеплению в двух альтернативных сайтах в N-концевой части, что приводит к образованию зрелой, полностью активной 21-кДа или 23-кДа формы VEGF-C. Известно, что этот процесс является неэффективным, поскольку большинство белка VEGF-C не активируется. Однако различие в лимфангиогенном потенциале между зрелой и 29/31-кДа промежуточной формами является существенным (Anisimov et al., 2009, Circulation Research 104: 1302-1312).
В некоторых вариантах осуществления полипептид VEGF-C, предназначенный для терапевтического использования в соответствии с настоящим изобретением, представляет собой полноразмерную, или препро, форму VEGF-C. В некоторых других неограничивающих вариантах осуществления полипептид препро-VEGF-C лишен сигнальной последовательности и, таким образом, может содержать аминокислоты 32-419 из последовательности, приведенной в SEQ ID NO: 3, например. Специалист в данной области понимает, что существуют альтернативные сайты расщепления для сигнальных пептидаз и что другие протеазы могут осуществлять процессинг N-конца VEGF-C, не оказывая влияние на его активность. Следовательно, полипептид VEGF-C может отличаться от полипептида, содержащего или состоящего из аминокислот 32-419 последовательности SEQ ID NO: 3.
Альтернативно или дополнительно, полипептид VEGF-C может находиться в форме частично процессированного VEGF-C, например, такого, который содержит аминокислоты 32-227, ковалентно связанные с аминокислотами 228-419 аминокислотной последовательности, приведенной в SEQ ID NO: 3. Опять-таки, из-за альтернативных сайтов расщепления для сигнальных пептидаз и других протеаз частично процессированный полипептид VEGF-C может иметь аминокислотный состав, отличающийся от такового из неограничивающего примера, описанного выше, без отклонения от сущности настоящего изобретения и вариантов его осуществления.
В некоторых других вариантах осуществления полипептид VEGF-C, который предназначен для введения субъекту, страдающему от нарушенного лимфангиогенеза, находится в своей полностью процессированной, или зрелой, форме, такой, которая содержит аминокислоты 112-227 или 103-227 из аминокислотной последовательности, приведенной в SEQ ID NO: 3. Кроме того, полипептид VEGF-C может находиться в любой другой природной или сконструированной форме. При желании, различные формы полипептида VEGF-C можно использовать в любом сочетании. Предпочтительно, полипептид VEGF-C является полипептидом VEGF-C млекопитающего, более предпочтительно, человека.
Также подразумевают, что любой из полипептидов VEGF-C, описанных в настоящем документе, может отличаться по своей аминокислотной последовательности при условии, что они сохраняют свою биологическую активность, в частности, их способность связывать и активировать VEGFR-2 и/или VEGFR-3. В некоторых вариантах осуществления полипептид VEGF-C может представлять собой консервативный вариант последовательности любого полипептида VEGF-C, описанного в настоящем документе, или он может содержать аминокислотную последовательность, которая по меньшей мере на 85%, 90%, 95%, 96%, 97%, 98%, 99% или более идентична аминокислотной последовательности, приведенной в SEQ ID NO: 3, или любой ее биологически активный фрагмент.
Используемый в настоящем документе термин «полинуклеотид VEGF-C» означает любой полинуклеотид, такой как одноцепочечная или двухцепочечная ДНК или РНК, содержащий нуклеотидную последовательность, кодирующую любой полипептид VEGF-C. Например, полинуклеотид VEGF-C может кодировать полноразмерный VEGF-C и содержать или состоять из нуклеотидов 524-1687 нуклеотидной последовательности, приведенной в SEQ ID NO: 4. В некоторых других вариантах осуществления полинуклеотид VEGF-C может кодировать промежуточные формы VEGF-C и содержать или состоять из нуклеотидов либо 737-1687, либо 764-1687 нуклеотидной последовательности, приведенной в SEQ ID NO: 4. В некоторых других вариантах осуществления полинуклеотид VEGF-C может кодировать зрелые формы VEGF-C и содержать или состоять из нуклеотидов либо 737-1111, либо 764-1111 нуклеотидной последовательности, приведенной в SEQ ID NO: 4. Ни один из приведенных выше вариантов осуществления не содержит последовательности, кодирующие сигнальный пептид или стоп-кодон, однако другие варианты осуществления могут содержать такие последовательности. В некоторых других вариантах осуществления C-конец зрелых форм может быть укорочен без потери способности к активации рецептора.
Также подразумевают консервативные варианты последовательности указанных нуклеотидных последовательностей. Соответственно, для любого конкретного полипептида VEGF-C существует несколько кодирующих VEGF-C полинуклеотидных последовательностей, каждую из которых можно использовать терапевтически, как описано в настоящем документе.
В некоторых других вариантах осуществления полинуклеотид VEGF-C может содержать нуклеотидную последовательность, которая по меньшей мере на 85%, 90%, 95%, 96%, 97%, 98%, 99% или более идентична нуклеотидным последовательностям VEGF-C, описанным выше, при условии, что она кодирует полипептид VEGF-C, сохраняющий свою биологическую активность, в частности, способность связывать и активировать VEGFR-2 и VEGFR-3.
Предпочтительно, любой полинуклеотид CCBE1 или VEGF-C, описанный в настоящем документе, содержит дополнительный N-концевой нуклеотидный фрагмент, кодирующий секреторный сигнальный пептид, функционально связанный с полинуклеотидной последовательностью. Секреторный сигнальный пептид, как правило, состоит из примерно 5-30 аминокислот, направляет транспорт полипептида за пределы клетки через эндоплазматический ретикулум и отщепляется от секретированного полипептида. Соответствующие последовательности сигнального пептида включают те, которые являются естественными для CCBE1 или VEGF-C, те, которые получены из других секретируемых белков, таких как CD33, Ig каппа или IL-3, а также синтетические сигнальные последовательности.
Полинуклеотид CCBE1 или VEGF-C также может содержать соответствующую последовательность промотора и/или энхансера для экспрессии в целевых клетках, при этом указанная последовательность расположена выше и функционально связана с кодирующей последовательностью. При желании, промотор может быть индуцируемым промотором или специфичным для клеточного типа промотором, например, специфичным для эндотелиальных клеток промотором. Соответствующие последовательности промотора и/или энхансера легкодоступны в данной области и включают, но не ограничиваются ими, EF1, CMV и CAG.
Кроме того, любой полинуклеотид CCBE1 или VEGF-C, описанный в настоящем документе, может содержать соответствующую последовательность полиаденилирования, расположенную ниже и функционально связанную с кодирующей последовательностью.
Для генной терапии «голые» полинуклеотиды CCBE1 или VEGF-C, описанные выше, можно использовать в форме рекомбинантной ДНК, плазмид или вирусных векторов. Доставку «голых» полинуклеотидов можно осуществлять любым методом, который физически или химически пермеабилизирует клеточную мембрану. Такие методы известны в данной области и включают, но не ограничиваются ими, электропорацию, бомбардировку покрытыми генами частицами, сонопорацию, магнитофекцию, липофекцию, опосредуемую липосомами доставку нуклеиновой кислоты, а также любое их сочетание.
В некоторых других вариантах осуществления полинуклеотиды CCBE1 или VEGF-C могут быть встроены в вирусный вектор под соответствующими последовательностями контроля экспрессии. Подходящие вирусные векторы для такой генной терапии включают, но не ограничиваются ими, ретровирусные векторы, такие как лентивирусные векторы, аденоассоциированные вирусные векторы и аденовирусные векторы. Предпочтительно, вирусный вектор представляет собой дефектный по репликации вирусный вектор, то есть, вектор, который неспособен реплицироваться в организме субъекта-млекопитающего. Неограничивающим предпочтительным примером такого дефектного по репликации вектора является дефектный по репликации аденовирус. Соответствующие вирусные векторы легкодоступны в данной области.
Доставку терапевтических полинуклеотидов CCBE1 или VEGF-C в организм субъекта-млекопитающего, предпочтительно субъекта-человека, можно осуществлять различными способами, хорошо известными в данной области. Например, вирусные векторы, содержащие кодирующие CCBE1 или VEGF-C полинуклеотиды, можно вводить непосредственно в организм субъекта, подлежащего лечению, например, путем инъекции в целевые ткани, имеющие аномальные лимфатические сосуды. Такая доставка приводит к экспрессии полипептидов in vivo и, вследствие этого, часто называется in vivo генной терапией. Альтернативно или дополнительно, доставку настоящих терапевтических полипептидов можно осуществлять ex vivo с использованием вирусных векторов или «голых» полипептидов. Ex vivo генная терапия означает, что целевые клетки, предпочтительно полученные от субъекта, подлежащего лечению, трансфицируют (или трансдуцируют вирусами с) настоящими полинуклеотидами ex vivo, а затем вводят субъекту с терапевтическими целями. Неограничивающие примеры соответствующих целевых клеток для ex vivo генной терапии включают эндотелиальные клетки, предшественники эндотелиальных клеток, гладкомышечные клетки, лейкоциты и особенно стволовые клетки различных видов.
В генной терапии экспрессия CCBE1 или VEGF-C может быть либо стабильной, либо временной. Временная экспрессия часто является предпочтительной. Специалист в данной области знает, когда и как применять стабильную или временную генную терапию.
Количества и схемы для терапевтического введения CCBE1 и VEGF-C по настоящему изобретению могут легко определять специалисты в области лечения заболеваний или состояний, связанных с нарушениями лимфатической сосудистой системы. Как правило, дозировка CCBE1 или VEGF-C для лечения будет варьироваться в зависимости от таких факторов, как: возраст, пол и общее состояние здоровья пациента, подлежащего лечению; вид сопутствующего лечения, при наличии; частота лечения и характер ожидаемого эффекта; степень поражения ткани; продолжительность симптомов и другие переменные, которые будут учитываться каждым отдельным врачом. Например, если для доставки генов используют вирусные векторы, вектор, как правило, вводят, необязательно, в фармацевтически приемлемом носителе в количестве от 107 до 1013 вирусных частиц, предпочтительно, в количестве по меньшей мере 109 вирусных частиц. С другой стороны, если используют белковую терапию, типичная доза находится в диапазоне от 0,01 до 20 мг/кг, более предпочтительно в диапазоне от 0,1 до 10 мг/кг, наиболее предпочтительно 0,5-5 мг/кг. Нужную дозу можно вводить в виде одной или более доз с соответствующими интервалами для достижения желаемых результатов. Типичная неограничивающая суточная доза может варьироваться от примерно 50 мг/сутки до примерно 300 мг/сутки.
Для белковой терапии CCBE1 или VEGF-C можно получать стандартными рекомбинантными методами. Нужный полинуклеотид можно клонировать в соответствующий экспрессионный вектор и экспрессировать в совместимом хозяине с использованием методов, хорошо известных в данной области. Примеры подходящих хозяев включают, но не ограничиваются ими, бактерии (такие как E. coli), дрожжи (такие как S. cerevisiae), клетки насекомых (такие как клетки SF9) и, предпочтительно, линии клеток млекопитающих. Можно использовать маркеры экспрессии, такие как His-метки, эпитопы гемагглютинина (HA-метки) или эпитопы глутатион-S-трансферазы (GST-метки), для облегчения очистки CCBE1 или VEGF-C. Если используют маркеры экспрессии, их следует отщеплять до введения субъекту, который нуждается в этом.
Как указано выше, настоящие терапевтические способы и варианты применения относятся к лечению заболеваний и состояний, связанных с нарушениями лимфатической сосудистой системы. Неограничивающие примеры таких заболеваний и состояний включают лимфедему, например, первичную лимфедему (например, синдром Милроя, лимфедему Мейджа и позднюю лимфедему), вторичную лимфедему и липедему.
Используемый в настоящем документе термин «лечение» или «терапия» означает совместное введение CCBE1 и VEGF-C субъекту-млекопитающему, предпочтительно человеку, с целью, которая включает не только полное излечение, но также профилактику, ослабление или облегчение заболеваний или симптомов, связанных с нарушениями лимфатической системы. Терапевтический эффект совместного введения CCBE1 и VEGF-C можно оценивать путем контролирования симптомов, таких как отек, боль, дискомфорт, тяжесть или плотность пораженной ткани.
Настоящее изобретение относится не только к терапевтическим способам и вариантам применения для лечения заболеваний и состояний, связанных с нарушениями лимфатической сосудистой системы, но также и к фармацевтическим композициям, предназначенным для использования в указанных способах и терапевтических вариантах применения. Такие фармацевтические композиции содержат CCBE1 и VEGF-C, либо отдельно, либо в сочетании, и любую фармацевтически приемлемую среду, такую как фармацевтически приемлемый растворитель, разбавитель, адъювант, эксципиент или носитель. Например, фармацевтически приемлемая среда может представлять собой стерильный неводный носитель, такой как пропиленгликоль, полиэтиленгликоль или инъекционный органический сложный эфир. Соответствующие водные носители включают, но не ограничиваются ими, воду, солевой раствор, фосфатно-солевой буфер и раствор декстрозы Рингера.
Можно использовать различные пути введения для доставки эффективной дозы в нужную зону действия, как хорошо известно в данной области. Таким образом, подходящие пути введения включают, но не ограничиваются ими, парентеральную доставку (например, внутривенную инъекцию), энтеральную доставку (например, пероральное введение), местное введение, топическое введение (например, кожное или чрескожное), как известно специалисту в данной области.
Фармацевтическая композиция может быть предоставлена в концентрированном виде или в виде порошка, который может быть восстановлен в нужный момент. В случае лиофилизации, предпочтительно использовать определенные криопротекторы, включая полимеры (повидоны, полиэтиленгликоль, декстран), сахара (сахарозу, глюкозу, лактозу), аминокислоты (глицин, аргинин, глютаминовую кислоту) и альбумин. Если в упаковку добавляют раствор для восстановления, он может состоять, например, из стерильной воды, раствора хлорида натрия, либо растворов декстрозы или глюкозы.
Средства и способы для формулирования настоящих фармацевтических препаратов известны специалистам в данной области, и препараты могут быть изготовлены известными методами, например, путем обычного смешивания, гранулирования, растворения, лиофилизации или аналогичных процедур.
Любые из вариантов осуществления и признаков, описанных выше, можно применять независимо к CCBE1 и VEGF-C и можно использовать в любом нужном сочетании. Таким образом, либо один, либо оба из CCBE1 и VEGF-C могут быть доставлены методами генной терапии или белковой терапии. Также подразумевают, что CCBE1 или VEGF-C могут быть введены с использованием методов как генной терапии, так и белковой терапии.
Для специалиста в данной области будет очевидно, что по мере развития технологий патентоспособную концепцию можно реализовывать различными путями. Изобретение и его варианты осуществления не ограничиваются примерами, описанными ниже, но могут варьироваться в пределах объема формулы изобретения.
ПРИМЕРЫ
Материалы и методы
Клонирование. Гены, экспрессируемые с помощью рекомбинантного аденоассоциированного вирусного (rAAV9) вектора, клонировали в плазмиду psubCAG-WPRE (Paterna et al., 2000, Gene Therapy 7: 1304-1311), которая является производной от плазмиды psubCMV-WPRE, в которой промотор CMV был заменен сложным промотором CAG, состоящим из промотора куриного β-актина, энхансера цитомегаловируса и интрона β-актина (Okabe et al., 1997, FEBS Letters 407: 313-319). Клонирование полноразмерного мVEGF-C, ΔNΔC-мVEGF-C и ЧСА в AAV-вектор (psubCAG-WPRE) описано ранее (Anisimov et al., 2009, там же). мCCBE1, слитый с V5-меткой (мCCBE1-V5), клонировали следующим образом: последовательность ДНК, кодирующую частичный CCBE1 (CDS; Genebank № BC152322, Image clone ID 40140631), клонировали в виде SacI/XbaI фрагмента в pVK1 (полученный из pUC19 вектор (Anisimov et al., 2007, Molecular Breeding 19: 241-253)). Пропущенные нуклеотиды амплифицировали из мРНК бурой жировой ткани с праймерами 5'-GCCGCTAGCGCCACCATGGTGCCGCCGCCT-3' (SEQ ID NO: 5) и 5'-GGAGCTTGGGCACAAATGTC-3' (SEQ ID NO: 6) и вышеуказанный CDS дополняли путем вставки NheI/SacI фрагмента, получая вектор pVK1-CCBE1. ПЦР-амплифицированную V5-метку (полученную с праймерами 5'-ACCAGGAGCACCAGGAAGAC-3' (SEQ ID NO: 7) и 5'-GCCTCTAGAACGCGTCTAGGTGCTGTCCAGGCCCAGCAGAGGGTTAGGGATAGGCTTGCCTGGA TAAAAATTTCTTGGGG-3' (SEQ ID NO: 8)) добавляли к CDS в виде Eco81I/XbaI фрагмента. Из полученного вектора полный CDS вырезали в виде MluI фрагмента и клонировали в psubCAG-WPRE.
Для in vitro исследований конструировали идентичный вектор, в котором мышиный CDS CCBE1 заменяли человеческим CDS CCBE1 (Genebank № NM_133459), и для исследований совместной иммунопреципитации StrepIII-метку (Junttila et al., 2005, PROTEOMICS 5: 1199-1203) вставляли сразу после CDS CCBE1. Конструкты для экспрессии VEGF-C и ΔC-VEGF-C в клетках млекопитающих описаны ранее (Joukov et al., 1997, там же). Химерный экспрессионный конструкт VEGF-C/VEGF-D (CDC) собирали методом ПЦР с перекрывающимися праймерами в вектор pMosaic (Jeltsch et al., 2006, J. Biol. Chem. 281: 12187-12195). Вставка содержала последовательности, кодирующие аминокислотные остатки Phe32-Ala111 и Ser228-Ser419 из VEGF-C человека и промежуточные остатки Thr92-Arg206 из VEGF-D человека.
Конструкты для экспрессии рекомбинантного белка в клетках S2 были включены в вектор pMT-Ex (модифицированная версия pMT-BiP-V5His-C (Kärpänen et al., 2006, The FASEB Journal 20: 1462-1472)) и содержали последовательности, кодирующие аминокислотные остатки Phe32-Ala111 для N-концевого пропептида, Ser228-Ser419 для C-концевого пропептида и Thr112-Arg227 для ΔNΔC формы VEGF-C, за которыми следовали последовательности, кодирующие гексагистидиновую метку.
Получение rAAV. Вирусы rAAV9 получали методом трехплазмидной трансфекции и очищали ультрацентрифугированием с использованием прерывистого градиента йодиксанола, как описано (Anisimov et al., 2009, там же). Для получения серотипа AAV9 авторы изобретения использовали определяющую серотип хелперную плазмиду p5E18-VP2/9 вместо p5E18-VP2/8 (Michelfelder et al., 2011, PLoS ONE 6: e23101).
Экспрессия и очистка белка. Клетки S2 трансфицировали с использованием Effectene (Qiagen, Venlo, The Netherlands). Стабильные клеточные пулы отбирали в течение 3 недель с помощью 400 мкг/мл гигромицина, начиная отбор через 2 дня после трансфекции. Для продуцирования белка клетки адаптировали к суспензионному культивированию и индуцировали в течение 4-5 дней 1 мМ CuSO4. После связывания скорректированного по pH кондиционированного супернатанта в емкости с Ni2+NTA-сефарозой, Ni2+NTA-сефарозу вносили в колонку, промывали 20 мМ имидазолом и элюировали ступенчатым градиентом 250 мМ имидазола. Затем белок разделяли по размеру на колонке с Superdex 200, используя PBS в качестве протекающего буфера.
Культура клеток. Клетки 293T, 293S GnTI- и NIH-3T3 выращивали в среде D-MEM с 10% ЭТС. Клетки PC-3 выращивали в среде Хэма F-12 с 10% ЭТС, клетки DU-4475 выращивали в среде RPMI 1640 с 20% ЭТС и клетки S2 выращивали в среде HyClone SFX-Insect (Thermo-Scientific, Rockford, IL) или Insect-Xpress (Lonza Group, Basel, Switzerland).
Трансфекции, метаболическое мечение и анализ белка. Клетки 293T и 293S GnTI- (ко)трансфицировали экспрессионными конструктами, кодирующими указанные белки. Через 24 часа после трансфекции клетки метаболически метили [35S]-цистеином/[35S]-метионином (PerkinElmer, Waltham, MA) и через 48 часов собирали кондиционированную клеточную культуральную среду и клеточные лизаты. Для экспериментов по краткосрочному мечению сбор проводили уже через 24 часа. Альтернативно, чтобы получить немеченый белок для вестерн-блоттинга, культуральную среду клеток заменяли на DMEM с 0,2% БСА, и супернатант и клеточные лизаты собирали через 48 часов.
Перед иммунопреципитацией образцы, необязательно, предварительно осветляли с помощью протеин A-сефарозы (поликлональные антитела и антисыворотка кролика) или протеин G-сефарозы (моноклональные антитела). Для иммунопреципитации использовали анти-VEGF-C антисыворотку (Baluk et al., 2005, J. Clin. Invest. 115: 247-257), анти-V5 антитело (Invitrogen, Carlsbad, CA, № 46-0705), анти-чCCBE1 антитело (Atlas Antibodies AB, Stockholm, Sweden, № HPA041374), анти-VEGF-D антитело VD1 (Achen et al., 2000, Eur. J. Biochem. 267: 2505-2515) или химерный белок VEGFR-3/IgGFc (Mäkinen et al., 2001, Nature Medicine 7: 199-205).
Образцы промывали и подвергали электрофорезу в 4-20% SDS-ПААГ. Для авторадиографии гели высушивали и экспонировали с пластинами phosphoimager или рентгеновской пленкой. Для иммунодетекции белки переносили на нитроцеллюлозу. Специфические сигналы обнаруживали с помощью анти-VEGF-C антисыворотки, анти-V5 антитела или анти-чCCBE1 антитела в сочетании с ECL. Количественные результаты авторадиографии и вестерн-блоттинга получали на основании показаний лазерного сканирования или сканирования рентгеновской пленки с использованием программы ImageJ (NIH, Bethesda, MD).
Анализы Ba/F3-VEGFR/EpoR. Биологические анализы Ba/F3-чVEGFR-3/EpoR (Achen et al., 2000, там же) и Ba/F3-мVEGFR-2/EpoR (Stacker et al., 1999b) выполняли с кондиционированной клеточной культуральной средой, в целом как описано (Mäkinen et al., 2001, там же). Линию клеток Ba/F3-чVEGFR-2/EpoR получали аналогично тому, как получали описанные выше линии клеток; однако использовали pCI-neo вместо pEF-BOS. Соединительными аминокислотными последовательностями химеры были ...FFIIEGAQEKTNLEGS (конец VEGFR-2 части) - (начало мEpoR части) LILTLSLILVLISLLLTVLALLSHRRTLQQKIWPGIPSPESEFE... (SEQ ID NOs: 9 и 10, соответственно) Этот химерный конструкт вводили электропорацией с использованием одного импульса 30 мс 1400 В (устройство для трансфекции Neon, Invitrogen) в клетки Ba/F3. Клетки выращивали в среде, содержащей 2 нг/мл мIL-3, в течение 36 часов, после чего их разделяли и начинали селекцию продолжительностью три недели с помощью 1,2 мг/мл G418. Клетки поддерживали при субоптимальной концентрации мIL-3 (0,4 нг/мл) и оптимальных концентрациях VEGF-A и VEGF-C (200 и 300 нг/мл, соответственно).
Вытеснение метки. Клетки 293T трансфицировали и выращивали в течение 36 часов на 6-см чашках почти до конфлюэнтности. Клетки оставляли голодать на 30 минут в met-/cys-дефицитной среде D-MEM с 5% диализованной ЭТС, после чего клетки метаболически метили в течение 2 часов [35S]-цистеином/[35S]-метионином. Затем клетки промывали теплым PBS и добавляли 5 мл среды для вытеснения (D-MEM, 10% ЭТС + 2 мМ холодного L-метионина + 2 мМ холодного L-цистеина). В указанные моменты времени чашки помещали на лед и среду отбирали для анализа.
Конкуренция VEGF-C пропептидов в расщеплении VEGF-C. Очищенные белки с гистидиновой меткой включали в среду для мечения VEGF-C/CCBE1-котрансфицированных клеток 293T в концентрации 25 мкг/мл. Среда для мечения была кондиционирована через 30-72 часов после трансфекции, освобождена от меченых гистидином белков с помощью Ni2+NTA-сефарозы, и VEGF-C был иммунопреципитирован, разделен в ПААГ и визуализирован экспонированием с рентгеновской пленкой. Ингибирование N-концевого расщепления VEGF-C количественно определяли путем подсчета 14-кДа N-концевого продукта расщепления на основании показаний лазерного сканирования.
Анализ совместной иммунопреципитации strep-меченого CCBE1. Клетки 293T трансфицировали конструктами либо CCBE1-strepIII, либо полноразмерного VEGF-C. Кондиционированную среду использовали в преципитации с Strep-Tactin (Qiagen) либо отдельно, либо в виде смеси CCBE1 и полноразмерного VEGF-C. Смешанную среду инкубировали в течение 10 минут при комнатной температуре перед тем, как начать преципитацию. Преципитаты анализировали с использованием анти-CCBE1 антитела и анти-VEGF-C антисыворотки после SDS-ПААГ и вестерн-блоттинга. Вносили 25 мкл кондиционированной среды с полноразмерным VEGF-C, которая служила в качестве положительного контроля.
Эксперименты in vivo. В передние большеберцовые мышцы самцов мышей FVB/N инъекцией вводили смешанные 1:1 растворы rAAV9, кодирующих м(мышиный)CCBE1-V5, полноразмерный мVEGF-C или ЧСА. Одиночные векторы AAV9-ЧСА и AAV9-ΔNΔC-мVEGF-C использовали в качестве отрицательного и положительного контролей, соответственно. Общая концентрация векторных частиц в одной инъекционной дозе составляла 6×1010. Через три недели после трансдукции мышей умерщвляли передозировкой CO2. Передние большеберцовые мышцы изолировали, погружали в O.C.T. (Sakura Finetek Europe, Alphen aan den Rijn, The Netherlands), делали срезы (толщиной 10 мкм) и окрашивали на маркеры лимфатических (LYVE-1, Prox-1) и кровеносных сосудов (PECAM-1), а также маркеры гладкомышечных клеток/перицитов (актин гладких мышц, SMA) и лейкоцитов (CD45), с последующей обработкой Alexa-конъюгированными вторичными антителами (Molecular Probes, Invitrogen). Флуоресцентные изображения получали на микроскопе Axioplan 2 (Carl Zeiss AG, Oberkochen, Germany); характеристики: 10x NA=0,3 WD 5,6 и 20x NA=0,5 WD 2,0; использовали камеру Zeiss AxioCam-FIRm ПЗС с градацией серого цвета 14 бит; для сбора данных использовали программное обеспечение Zeiss AxioVision 4.6. Количественное определение окрашенных областей выполняли с использованием программы ImageJ. Положительные по Prox-1 ядра подсчитывали вручную. Обнаружение люциферазной активности в случае EGFP/Luc Vegfr3EGFP/Luc мышей выполняли, как описано ранее (Martinez-Corral et al., 2012, PNAS 109: 6223-6228). Национальный совет по проведению экспериментов на животных Провинциального государственного управления Южной Финляндии одобрил все эксперименты на животных, проводимые в данном исследовании.
Статистический анализ. Значимость различий определяли с использованием однофакторного дисперсионного анализа. В случае предполагаемых равных дисперсий в качестве апостериорного анализа использовали критерий Тьюки. В случае предполагаемых неравных дисперсий в качестве апостериорного анализа использовали критерий Геймса-Хоуэлла. Величину EC50 в анализах Ba/F3 рассчитывали с использованием логистической регрессии. Планки погрешностей на фигурах указывают стандартное отклонение.
Результаты
CCBE1 увеличивает процессинг и секрецию VEGF-C, что приводит к повышению активации VEGFR-3. CCBE1 был обнаружен в виде белка с молекулярной массой 40-55 кДа как в клеточных лизатах, так и в кондиционированной среде клеток 293T, трансфицированных экспрессионным вектором CCBE1 (фигура 1A). Часть CCBE1 из супернатанта мигрировала в виде диффузной гликозилированной полосы, соответствующей предполагаемому димеру CCBE1. Трансфицированный VEGF-C экспрессировался в виде нерасщепленного 58-кДа предшественника, процессированной с C-конца 29/31-кДа и полностью процессированной 21-кДа зрелой формы (фигура 1D, дорожка 1). Однако если VEGF-C и CCBE1 были котрансфицированы, количества нерасщепленного VEGF-C и 29/31-кДа полипептида резко снижались, и зрелый, полностью активированный VEGF-C становился основной формой (фигура 1D, сравните дорожки 1 и 3). Эти результаты свидетельствуют о том, что CCBE1 ускоряет как N-концевой, так и C-концевой протеолитический процессинг VEGF-C.
Чтобы иметь возможность проанализировать эффект контрансфекции с CCBE1 на внутриклеточные формы VEGF-C, авторы изобретения использовали более короткий период мечения. Котрансфекция с CCBE1 способствовала секреции VEGF-C, поскольку внутриклеточное количество снижалось на 80% в лизатах котрансфицированных клеток (фигура 2A, сравните дорожки 5, 6 и 7, 8).
Кондиционированная среда от котрансфицированных CCBE1/VEGF-C культур стимулировала рост и выживание клеток Ba/F3-VEGFR-3/EpoR и Ba/F3-VEGFR-2/EpoR лучше, чем супернатант от клеток, трансфицированных только VEGF-C, в то время как отдельно CCBE1 проявлял очень небольшую активность. Это подтверждало, что повышенная секреция и расщепление приводили к повышенным уровням активного белка VEGF-C в культурах (фигура 1C и фигура 2B). Следует отметить, что супернатанты от клеток, экспрессирующих только CCBE1, также способствовали небольшому увеличению выживаемости клеток Ba/F3-VEGFR-3/EpoR, вероятно, вследствие увеличения процессинга и активации эндогенного VEGF-C, производимого клетками.
Укороченный CCBE1 не увеличивает стимулированную VEGF-C активность VEGFR-3. CCBE1 укорачивали, как описано Bos et al. (2011, там же), то есть, таким образом, что коллаген-связывающий домен был удален и остаток молекулы CCBE1 был слит с Fc-доменом IgG человека для лучшей стабильности белка. Укороченный CCEB1 очищали до гомогенного состояния и тестировали в разработанной in vitro системе совместно с очищенным полноразмерным или зрелым белком VEGF-C. Авторы изобретения проводили эксперимент следующим образом. Клетки чVEGFR-3/EpoR-Ba/F3 стимулировали VEGF-CΔNΔC человека (зрелый VEGF-C) (фигура 3A) или полноразмерным VEGF-C (предшественник VEGF-C) (фигура 3B) в возрастающих концентрациях в присутствии постоянной дозы (5 мкг/мл) укороченного CCBE1-Fc или белка отрицательного контроля, который представлял собой Fc-часть. Клетки инкубировали в условиях стимуляции в общей сложности в течение 3 дней. По окончании этого периода к клеточным культурам добавляли тиазолил синий тетразолий бромид (MTT, Sigma-Aldrich) и количество живых клеток в каждой культуре (прямой показатель клеточной пролиферации) подсчитывали путем измерения оптической плотности OD540 (желтый MTT восстанавливается митохондриальными ферментами живых клеток, с образованием темно-синего материала). Результаты отчетливо свидетельствовали, что укороченный CCBE1 не способен усиливать стимулирующую FGFR-3 активность VEGF-C.
CCBE1 способен увеличивать процессинг VEGF-C in trans. При развитии мышиного эмбриона и данио CCBE1 экспрессируется рядом с развивающимися лимфатическими структурами, но не самим эндотелием (Hogan et al., 2009, Nature Genetics 41: 396-398). Вследствие этого, авторы изобретения намеревались определить, может ли продуцирование CCBE1 in trans другими клетками также увеличивать процессинг VEGF-C. Они трансфицировали отдельные культуры клеток 293T VEGF-C или CCBE1 и смешивали клеточные популяции через 24 часа после трансфекции. Альтернативно, они смешивали CCBE1-трансфицированные клетки с клетками, стабильно экспрессирующими VEGF-C. Как и в экспериментах по котрансфекции, CCBE1 повышал эффективность внеклеточного процессинга VEGF-C (фигура 4A). Напротив, внутриклеточный процессинг и секреция VEGF-C не изменялись, когда соседние клетки продуцировали избыток CCBE1 (фигура 4B).
CCBE1 повышает лимфангиогенную активность VEGF-C in vivo. Для изучения того, усиливает ли CCBE1 лимфангиогенез in vivo, авторы изобретения трансдуцировали передние большеберцовые мышцы мыши отдельно аденоассоциированными вирусными (AAV) векторами, экспрессирующими CCBE1 (AAV9-CCBE1), совместно с вектором AAV9-VEGF-C в соотношении 1:1 или вектором AAV9-человеческий сывороточный альбумин (ЧСА) в качестве отрицательного контроля. AAV9, кодирующий активированную форму VEGF-C (ΔNΔC-VEGF-C), использовали в качестве положительного контроля для имитации полностью протеолитически процессированной (зрелой) формы VEGF-C.
Через две недели после трансдукции AAV скелетные мышцы анализировали иммуногистохимическими методами с использованием маркеров для эндотелиальных клеток (PECAM-1), лимфатических эндотелиальных клеток (LYVE-1, Prox1) и лейкоцитов (CD45). В этом анализе как полноразмерный VEGF-C, так и ΔNΔC-VEGF-C стимулировали лимфангиогенез, хотя последний («зрелая» форма) вызывал значительно более сильный ответ при той же дозе вируса, в то время как только ΔNΔC-VEGF-C стимулировал ангиогенез (фигура 6 и фигура 7, нижний ряд). Это свидетельствовало о том, что протеолитический процессинг полноразмерного VEGF-C был неэффективен в трансдуцированной AAV9 мышце.
Однако когда полноразмерный VEGF-C котрансдуцировали с CCBE1, лимфангиогенез значительно увеличивался, как видно по окрашиванию на LYVE-1 и Prox-1 (фигура 6). Авторы изобретения также наблюдали значительно более выраженный ангиогенез (фигура 7), указывающий на то, что CCBE1 увеличивает протеолитический процессинг VEGF-C также и in vivo. Возросшее количество CD45+ лейкоцитов наблюдали после котрансдукции полноразмерного VEGF-C/CCBE1 (фигура 8), это свидетельствовало о том, что активация VEGF-C увеличивает также рекрутинг лейкоцитов через VEGFR-3.
Для подтверждения этих результатов авторы изобретения использовали AAV9-трансдуцированных гетерозиготных мышей Vegfr3EGFP/Luc (Martinez-Corral et al., 2012, там же) для контролирования лимфангиогенеза путем оптической биолюминисцентной визуализации in vivo. Они обнаружили сильные люциферазные сигналы у мышей, котрансдуцированных AAV, кодирующими VEGF-C и CCBE1, в то время как более слабые сигналы были обнаружены у мышей, трансдуцированных только VEGF-C или CCBE1, и никаких биолюминесцентных сигналов не было у мышей, трансдуцированных ЧСА (фигура 9).
Пропептиды VEGF-C вовлечены в опосредованный CCBE1 протеолиз. Попытки авторов изобретения продемонстрировать физическое взаимодействие VEGF-C и CCBE1 были безуспешными. Вследствие этого, они предположили, что взаимодействие CCBE1-VEGF-C является слабым, недолговременным и, возможно, непрямым. Авторы изобретения пытались идентифицировать структурный элемент в VEGF-C, ответственный за опосредованные CCBE1 ускоренные секрецию и расщепление. Когда они сравнили кинетику секреции VEGF-C дикого типа и мутанта VEGF-C, лишенного его C-концевого пропептида, в эксперименте по вытеснению метки, меченый мутант VEGF-C достигал своего пика секреции уже в период от 15 до 45 минут, в то время как VEGF-C дикого типа достигал своего пика секреции только через два часа (фигура 10). Это свидетельствовало о том, что C-концевой пропептид регулирует эффективность секреции. Авторы изобретения пытались ингибировать CCBE1-усиленный процессинг VEGF-C путем добавления очищенного N-концевого или C-концевого пропептида VEGF-C или VHD в высоких концентрациях. Ингибирование процессинга VEGF-C примерно на 79% наблюдали в случае C-концевого пропептида и ингибирование примерно на 43% наблюдали в случае N-концевого пропептида, в то время как VHD или контроль БСА не изменяли соотношение протеолитических фрагментов, продуцируемых трансфицированными клетками (фигура 11A), подтверждая, что пропептиды VEGF-C вовлечены в опосредованное CCBE1 расщепление. Хотя VEGF-D очень сходен с VEGF-C по структуре и протеолитическому процессингу (Leppänen et al., 2011, Blood 117: 1507-1515; Stacker et al., 1999a, J. Biol. Chem. 274: 32127-32136), котрансфекция с CCBE1 не ускоряла протеолитический процессинг человеческого полноразмерного VEGF-D или химерного фактора, в котором VHD VEGF-D фланкирован N- и C-концевыми пропептидами VEGF-C (фигура 11B, дорожки 3-6).

Группа изобретений относится к медицине и может быть использована для лечения лимфедемы. Для этого вводят комбинацию полноразмерного CCBE1 и VEGF-C, где CCBE1 и VEGF-C находятся в форме полипептида или полинуклеотида. Также предложены фармацевтическая композиция и способ лечения лимфедемы. Группа изобретений обеспечивает лечение лимфедемы путем усиления полноразмерным CCBE1 лимфангиогенного ответа VEGF-C. 3 н. и 2 з.п. ф-лы, 11 ил.
1. Комбинация полноразмерного CCBE1 и VEGF-C для лечения лимфедемы, где CCBE1 находится
(а) в форме полипептида, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 1, аминокислоты 35-406, приведенные в SEQ ID NO: 1, или аминокислотную последовательность, имеющую по меньшей мере 80% идентичности аминокислотной последовательности с ними, или
(b) в форме полинуклеотида, содержащего нуклеотидную последовательность, приведенную в SEQ ID NO: 2, или нуклеотидную последовательность, имеющую по меньшей мере 80% идентичности нуклеотидной последовательности с ней, и
где VEGF-C находится
(с) в форме полипептида, содержащего аминокислотную последовательность, выбранную из группы, состоящей из аминокислот 32-419 из SEQ ID NO: 3; аминокислот 32-227, ковалентно связанных с аминокислотами 228-419 из SEQ ID NO: 3; аминокислот 112-227 из SEQ ID NO: 3 и аминокислот 103-227 из SEQ ID NO: 3; а также аминокислотной последовательности, имеющей по меньшей мере 80% идентичности аминокислотной последовательности с ними, или
(d) в форме полинуклеотида, содержащего нуклеотидную последовательность, выбранную из группы, состоящей из нуклеотидов 524-1687 из SEQ ID NO: 4; нуклеотидов 737-1687 из SEQ ID NO: 4; нуклеотидов 764-1687 из SEQ ID NO: 4; нуклеотидов 737-1111 из SEQ ID NO: 4; нуклеотидов 764-1111 из SEQ ID NO: 4, а также нуклеотидной последовательности, имеющей по меньшей мере 80% идентичности нуклеотидной последовательности с ними.
2. Комбинация по п. 1, где лимфедему выбирают из группы, состоящей из первичной лимфедемы, синдрома Милроя, лимфедемы Мейджа, поздней лимфедемы, вторичной лимфедемы и липедемы.
3. Фармацевтическая композиция для лечения лимфедемы, содержащая комбинацию по п. 1 и фармацевтически приемлемый носитель.
4. Способ лечения лимфедемы путем введения пациенту, который нуждается в этом, комбинации полноразмерного CCBE1 и VEGF-C одновременно, раздельно или последовательно, где CCBE1 находится
(а) в форме полипептида, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 1, аминокислоты 35-406, приведенные в SEQ ID NO: 1, или аминокислотную последовательность, имеющую по меньшей мере 80% идентичности аминокислотной последовательности с ними или
(b) в форме полинуклеотида, содержащего нуклеотидную последовательность, приведенную в SEQ ID NO: 2, или нуклеотидную последовательность, имеющую по меньшей мере 80% идентичности нуклеотидной последовательности с ней, и
где VEGF-C находится
(с) в форме полипептида, содержащего аминокислотную последовательность, выбранную из группы, состоящей из аминокислот 32-419 из SEQ ID NO: 3; аминокислот 32-227, ковалентно связанных с аминокислотами 228-419 из SEQ ID NO: 3; аминокислот 112-227 из SEQ ID NO: 3, аминокислот 103-227 из SEQ ID NO: 3; а также аминокислотной последовательности, имеющей по меньшей мере 80% идентичности аминокислотной последовательности с ними, или
(d) в форме полинуклеотида, содержащего нуклеотидную последовательность, выбранную из группы, состоящей из нуклеотидов 524-1687 из SEQ ID NO: 4; нуклеотидов 737-1687 из SEQ ID NO: 4; нуклеотидов 764-1687 из SEQ ID NO: 4; нуклеотидов 737-1111 из SEQ ID NO: 4; нуклеотидов 764-1111 из SEQ ID NO: 4, а также нуклеотидной последовательности, имеющей по меньшей мере 80% идентичности нуклеотидной последовательности с ними.
5. Способ по п. 4, где лимфедему выбирают из группы, состоящей из первичной лимфедемы, синдрома Милроя, лимфедемы Мейджа, поздней лимфедемы, вторичной лимфедемы и липедемы.
| WO 2010056123 A1, 20.05.2010 | |||
| US 2007110744 A1, 17.05.2007 | |||
| RU 2010114041 A, 20.10.2011 | |||
| BOS FL et al., CCBE1 is essential for mammalian lymphatic vascular development and enhances the lymphangiogenic effect of vascular endothelial growth factor-C in vivo,Circ Res | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
Авторы
Даты
2019-06-11—Публикация
2014-08-13—Подача