Изобретение относится к техническим средствам электрохимических производств, а именно, к электродам для электрохимических процессов и технологии их получения, и может найти применение при изготовлении электродов, необходимых при проведении различных промышленных процессов, в медицине и сельском хозяйстве, а также в научно-исследовательской работе для мониторинга рН природных и техногенных вод, для определения содержания в растворах сильных и слабых кислот и оснований.
В частности, от значения рН зависят скорость и механизм многих химических реакций, протекающих в водной среде, а наиболее точным, быстрым и распространенным методом его определения в настоящее время является потенциометрический метод.
Известен стеклянный электрод для потенциометрических измерений (а.с. СССР №759943, опубл. 1980.08.30), содержащий стеклянный изолирующий корпус, индикаторную мембрану из ионопроводящего стекла, металлический токоотвод и переходный материал между стеклом мембраны и токоотводом, при этом в качестве переходного материала использовано стекло преимущественно с электронным характером проводимости, содержащее в своем составе тот же оксид щелочного металла, что и оксид ион-чувствительной мембраны, причем токоотвод непосредственно контактирует со стеклом, обладающим электронной проводимостью, либо приведен с ним в контакт с помощью другого материала с электронной проводимостью. Стеклянный электрод обладает высокой селективностью и чувствительностью, однако он является хрупким, не способным к деформации без разрушения, требует особых условий хранения и специальной подготовки перед измерениями. Его устройство не предполагает возможности миниатюризации и выполнения в плоской форме, что затрудняет его использование при анализе малых объемов жидкости или вязких и твердых веществ, необходимого в медицине, пищевой промышленности, при анализе биохимических и биологических процессов.
Альтернативой стеклянным электродам в качестве рН-сенсоров являются различные металлические и металлооксидные электроды, в том числе сурьмяные, висмутовые, из нержавеющей стали, а также смешанные системы типа RuO2-TiO2, Ti/Co3O4/PbO2/(SnO2+Sb2O3), Ti/PbO2/Sb2O3, Ti/TiO2/SnO2(Sb) и целый ряд других.
Известен металлооксидный электрод (RU 2487198, опубл. 2013.07.10), представляющий собой основу из титана или его сплава с покрытием из оксидов титана, на которое нанесены наночастицы платины в количестве, не превышающем 0.01 г/м2. Способ его получения включает формирование на основе из титана или его сплава покрытия из оксидов титана методом плазменно-электролитического оксидирования (ПЭО) с последующим нанесением на сформированную пористую поверхность наночастиц платины и их агломератов посредством пропитки упомянутой поверхности платинохлористоводородной кислотой с ее последующим термическим разложением.
Известный электрод не обеспечивает достаточно высоких показателей по аналитическим характеристикам, в том числе по величине аналитического сигнала при кислотно-основном титровании и крутизне электродной функции зависимости Е-рН.
Задачей изобретения является создание электрода металлооксидного типа сложного оксидного состава с высокой рН чувствительностью, получаемого простым и технологичным способом.
Технический результат изобретения заключается в увеличении рН чувствительности получаемого электрода, повышении технологичности и упрощении способа его получения.
Указанный технический результат достигают металлооксидным электродом для потенциометрических измерений, содержащим титановую основу с покрытием из оксидов титана, сформированным методом плазменно-электролитического оксидирования, который, в отличие от известного, во внешнем слое покрытия дополнительно содержит до 1 ат. % сурьмы в виде оксидов Sb2O3 и Sb2O5.
Указанный технический результат достигают также способом изготовления металлооксидного электрода для потенциометрических измерений методом плазменно-электролитического оксидирования (ПЭО) титана в гальваностатическом режиме, в котором, в отличие от известного, ПЭО осуществляют при эффективной плотности тока i=0.10-0.20 А/см2 в течение 10-20 минут из электролита, содержащего Sb2O3⋅3H2O и NaOH при следующем содержании компонентов, М:
В результате протекающей в водных растворах реакции между оксидом сурьмы (III) и гидроксидом натрия образуются гидрооксокомплексы сурьмы Na[Sb(OH)4] и Na3[Sb(OH)6] согласно уравнениям реакций:
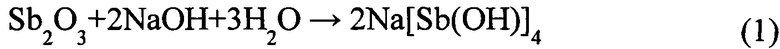
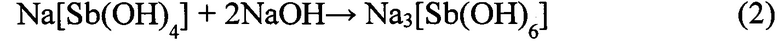
Отрицательно заряженные Sb-содержащие ионные частицы, попадая в прианодное пространство, под действием электрических разрядов в ходе ПЭО встраиваются в растущий на анодно поляризованном титане оксидный слой TiO2.
Таким образом, предлагаемый способ обеспечивает получение модифицированного оксидами сурьмы металлооксидного электрода в одну стадию, в то время как известный электрод получают в три последовательные стадии: 1) плазменно-электролитическое оксидирование титана, 2) пропитка в растворе платинохлористоводородной кислоты и 3) отжиг, которые требуют затрат времени, энергозатрат и применения своего оборудования для каждой стадии.
Сформированное покрытие имеет двухслойное строение. В каналах, присутствующих во внешнем слое покрытия из оксида титана, видны участки нижележащего пронизанного порами покрытия. Наличие в электролите оксида сурьмы обеспечивает более плотное заполнение внешнего слоя, образованного четко выраженными гранулами, при этом площадь каналов уменьшается, количество их увеличивается (на фиг. 1 показаны СЭМ изображения поверхности электродов: а - Ti/TiO2; б - Ti/TiO2, SbOx).
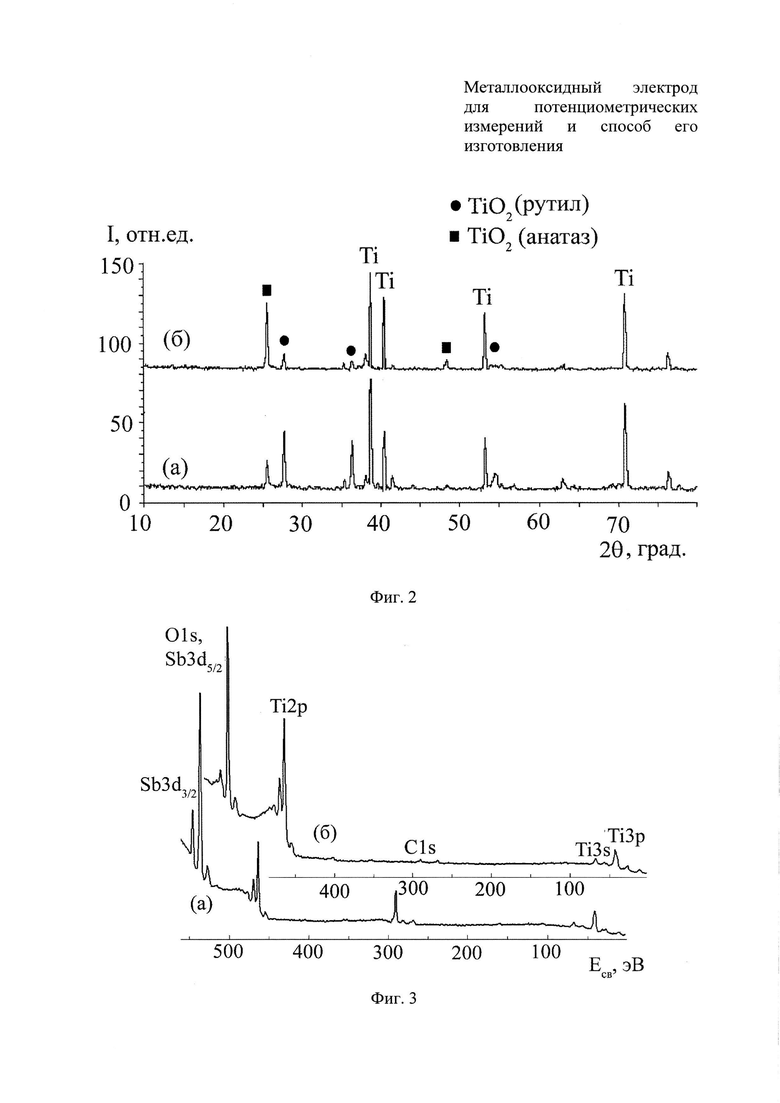
Рентгенограммы сформированных покрытий свидетельствуют о том, что наличие в электролите анионных гидрооксокомплексов сурьмы и встраивание сурьмы в состав растущего слоя TiO2 приводят к стабилизации его анатазной модификации (фиг. 2: а - Ti/TiO2; б - Ti/TiO2, SbOx). Определение элементного состава поверхности оксидных покрытий с помощью рентгеновской фотоэлектронной спектроскопии (РФЭС) показывает, что в составе внешних слоев (толщиной около 3 нм) содержание сурьмы составляет от 3 до 4 ат. % при среднем значении ее содержания в покрытии примерно 1 ат. %. Анализ РФЭ спектров (фиг. 3) свидетельствует о том, что сурьма во внешних слоях образцов находится в окисленном состоянии, в виде Sb2O3 и Sb2O5. Кроме того, РФЭС анализ позволяет установить наличие во внешнем слое покрытия кислорода, который присутствует в составе диоксида титана и в виде кислорода гидроксильного/карбонильного ряда, а также значительное количество углерода, основная часть (4/5) которого - алифатические формы (С-С, С-Н), около 1/5 - окисленные.
После стравливания поверхностного слоя толщиной 3-5 нм у обнажившегося слоя, в сравнении с исходным, наблюдается увеличение доли окисленных форм титана, уменьшение количества сурьмы, которая при этом находится в двух различных состояниях: окисленном и «металлическом», а также существенно меньшее количество углерода.
Потенциометрическое исследование поведения предлагаемого электрода в сравнении с известным проводили в интервале рН 2÷10.
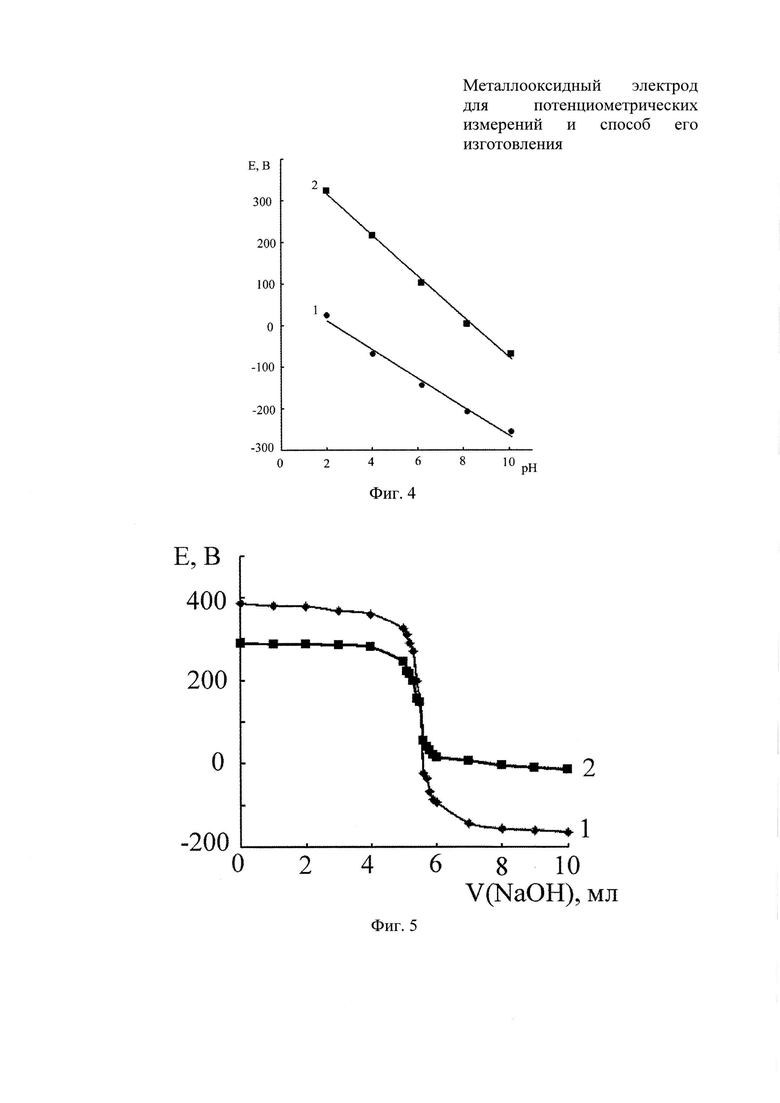
Электродные функции E=ƒ(pH) электродов на основе титана со смешанным оксидным покрытием, описываются уравнением Е=а-bpH и являются линейными во всем исследуемом диапазоне рН (фиг. 4).
В таблице 1 приведены параметры уравнения E=a-bpH и значения скачков потенциала ΔЕ/ΔV (мВ/мл) при потенциометрическом кислотно-основном титровании 0.1М раствора HCl 0.1М раствором NaOH (n=5; Р=0.95).
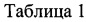
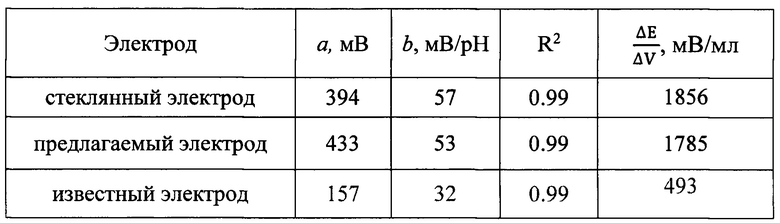
Значение коэффициента b в уравнении Е=а-b(рН) для электродов, полученных предлагаемым способом, в большей степени приближается к Нернстовскому: 53 мВ/рН (в сравнении с 32 для известного и 45 мВ/рН для электрода Ti/TiO2).
Таким образом, наличие сурьмы в заявленном количестве в составе покрытия из TiO2 приводит к увеличению рН чувствительности формируемых электродов, что объясняется тем, что электродная реакция протекает не только с участием оксида титана, но и оксида сурьмы. Кроме того, увеличение рН чувствительности может происходить в связи с преобладанием в модифицированном оксидом сурьмы покрытии анатазной модификации титана, а также за счет более развитой поверхности тонкого наружного слоя.
Величина коэффициента а в уравнении Е=а-b(рН), которая в основном зависит от состояния поверхности электрода и природы оксидов, в результате введения сурьмы в состав оксидных слоев увеличивается, что свидетельствует о повышении термодинамической устойчивости формируемых электродов.
Примеры конкретного осуществления изобретения
Электроды изготавливали из листового титана марки ВТ1-0 в виде пластинок размером 2.0×2.0 см. Для снятия поверхностного слоя металла и стандартизации поверхности образцы химически полировали в смеси концентрированных кислот HF:HNO3=1:3 при 60-80°С в течение 2-3 с.
Оксидные покрытия на титане формировали методом плазменно-электролитического оксидирования (ПЭО) в гальваностатическом режиме при эффективной плотности тока i=0.05-0.20A/см2 в течение 10-20 минут. Источник тока - тиристорный преобразователь типа ТЕР4-100/46ОН с импульсной однополярной формой тока. В качестве катода использовали трубчатый змеевик из нержавеющей стали марки Х18Н9Т, охлаждаемый водопроводной водой. Оксидированные образцы промывали водой и сушили на воздухе при комнатной температуре.
При изучении рН чувствительности электродов использовали буферные растворы с известными значениями рН. Поведение электродов в потенциометрическом кислотно-основном титровании изучали на примере титрования 0.1М раствора HCl с использованием 0.1М раствора NaOH. В качестве электрода сравнения использовали хлоридсеребряный электрод ЭВЛ-1-М-1.
Фазовый состав образцов определяли методом рентгенофазового анализа (РФА) на дифрактометре D8 ADVANCE (Германия) в Cuka-излучении по стандартной методике.
Данные по морфологии, элементному составу поверхности получали с помощью сканирующего электронного микроскопа Hitachi S-5500 (Япония) с системой энергодисперсионного рентгеноспектрального микроанализа. Глубина анализируемого слоя составляла ~1 мкм.
Для определения элементного состава поверхности оксидных покрытий использовали рентгеновскую фотоэлектронную спектроскопию (РФЭС). Измерение спектров осуществляли на сверхвысоковакуумной установке фирмы Specs (Германия) с 150-мм электростатическим полусферическим анализатором. Глубина анализируемого поверхностного слоя составляла около 3 нм. Для удаления верхнего слоя применяли ионное травление.
Пример 1
С помощью электрода, сформированного в электролите, содержащем 0.01М Sb2O3⋅3H2O и 0.05М NaOH, при эффективной плотности тока 0.10 А/см2 в течение 20 мин, осуществляли кислотно-основное титрование 0,1 М раствора HCl с применением 0.1М раствора NaOH. Интегральные кривые вышеупомянутого титрования приведены на фиг. 5 с электродами: 1 - Ti/TiO2,SbOx; 2 - прототип.
Приведенные на графике кривые характеризуются ярко выраженными скачками потенциала в точке эквивалентности.
Пример 2
Титрование осуществляли с помощью электрода, сформированного в электролите, содержащем 0,01М Sb2O3⋅3H2O и 0,05М NaOH, при эффективной плотности тока 0.20 А/см2 в течение 10 мин.
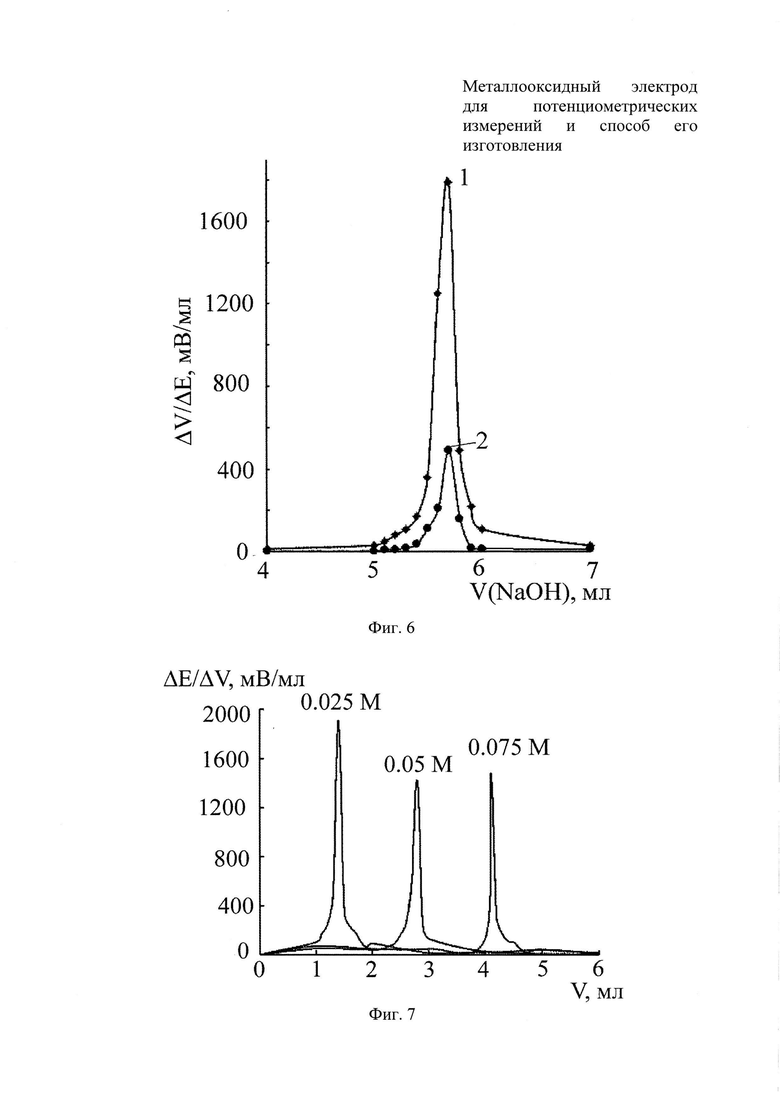
На фиг. 6 представлены дифференциальные кривые кислотно-основного титрования 0.1 М раствора HCl 0.1 М раствором NaOH с электродами: 1 - Ti/TiO2,SbOx; 2 - прототип.
Пример 3
Электрод, содержащий только TiO2, электроды, изготовленные по примеру 1 [I], по примеру 2 [II], и электрод по прототипу использовали для количественного определения сильной соляной кислоты. Сравнительные результаты приведены в таблице 2.
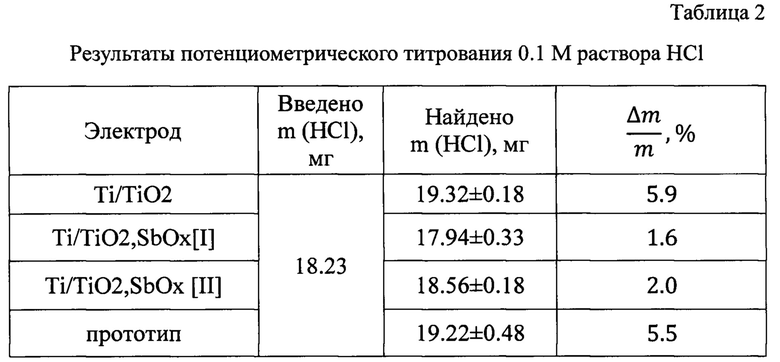
Относительная ошибка 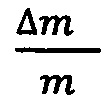 определения сильной кислоты с использованием оксидного (Ti/TiO2) электрода достигает 5.9%, известного - 5.5%, тогда как использование предлагаемого электрода позволяет повысить точность анализа и снизить ошибку до значения ~2%.
определения сильной кислоты с использованием оксидного (Ti/TiO2) электрода достигает 5.9%, известного - 5.5%, тогда как использование предлагаемого электрода позволяет повысить точность анализа и снизить ошибку до значения ~2%.
Пример 4
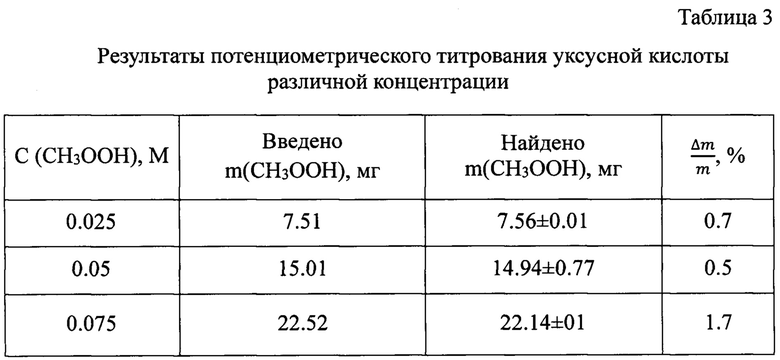
Электрод, изготовленный по примеру 2, использовали в качестве индикаторного для потенциометрического титрования водных растворов 0.025 М, 0.05 М и 0.075 М слабой уксусной кислоты.
Дифференциальные кривые титрования, приведенные на фиг. 7, имеют типичный для потенциометрического титрования вид с максимумом в точке эквивалентности.
Значения массы титруемой уксусной кислоты, определенные по результатам титрования, приведены в таблице 3.
Относительная погрешность при определении содержания слабой кислоты предлагаемым электродом также не превышает 2%, что дает возможность успешно применять его и для титрования слабых кислот.
| название | год | авторы | номер документа |
|---|---|---|---|
| МЕТАЛЛОКСИДНЫЙ ЭЛЕКТРОД, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2012 |
|
RU2487198C1 |
| ЭЛЕКТРОД И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2005 |
|
RU2288973C1 |
| ОСТЕОСИНТЕЗ С НАНОСЕРЕБРОМ | 2010 |
|
RU2557938C2 |
| СПОСОБ ПОЛУЧЕНИЯ НА ТИТАНОВОЙ ПОДЛОЖКЕ ОКСИДНОГО ПОКРЫТИЯ, СОДЕРЖАЩЕГО МАНГАНИТ СОСТАВА LaCaMnO (0≤х≤0,4) | 2023 |
|
RU2819473C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГРАДИЕНТНОГО КАТАЛИТИЧЕСКОГО ПОКРЫТИЯ | 2011 |
|
RU2490372C2 |
| Способ получения тонких слоев титаната висмута | 2016 |
|
RU2614916C1 |
| СПОСОБ ФОРМИРОВАНИЯ ОБЪЕМНО-ПОРИСТОГО СЛОЯ МЕТАЛЛА С ОТКРЫТОЙ ПОРИСТОСТЬЮ НА ЭЛЕКТРОПРОВОДНОЙ ПОДЛОЖКЕ | 1999 |
|
RU2150533C1 |
| ЛЮМИНЕСЦЕНТНОЕ ПОКРЫТИЕ НА ОКСИДИРОВАННОМ ТИТАНЕ НА ОСНОВЕ СОЕДИНЕНИЙ ЕВРОПИЯ(II, III) | 2022 |
|
RU2788775C1 |
| ЭЛЕКТРОЛИТ ДЛЯ ФОРМИРОВАНИЯ ПОКРЫТИЙ НА ВЕНТИЛЬНЫХ МЕТАЛЛАХ | 1992 |
|
RU2046156C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИТИЧЕСКИ АКТИВНЫХ КОМПОЗИТНЫХ СЛОЕВ НА СПЛАВЕ АЛЮМИНИЯ | 2014 |
|
RU2571099C1 |

Изобретение относится к металлооксидному электроду для потенциометрических измерений, содержащему титановую основу с покрытием из оксидов титана, сформированным методом плазменно-электролитического оксидирования. Электрод характеризуется тем, что внешний слой покрытия толщиной 1 мкм дополнительно содержит до 1 ат.% сурьмы в виде оксидов Sb2O3 и Sb2O5. Также изобретение относится к способу изготовления электрода. Технический результат - увеличение рН чувствительности электрода при одновременном повышении технологичности и упрощении способа его получения. 2 н.п. ф-лы, 7 ил., 3 табл., 4 пр.
1. Металлооксидный электрод для потенциометрических измерений, содержащий титановую основу с покрытием из оксидов титана, сформированным методом плазменно-электролитического оксидирования, отличающийся тем, что внешний слой покрытия толщиной 1 мкм дополнительно содержит до 1 ат.% сурьмы в виде оксидов Sb2O3 и Sb2O5.
2. Способ изготовления металлооксидного электрода для потенциометрических измерений по п. 1 методом плазменно-электролитического оксидирования титановой основы в гальваностатическом режиме, отличающийся тем, что ПЭО осуществляют при эффективной плотности тока i=0,10-0,20 А/см2 в течение 10-20 минут из электролита, содержащего Sb2O3⋅3Н2О и NaOH при следующем содержании компонентов, М:
| МЕТАЛЛОКСИДНЫЙ ЭЛЕКТРОД, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2012 |
|
RU2487198C1 |
| CN 201247218 Y, 27.05.2009 | |||
| СПОСОБ ИЗГОТОВЛЕНИЯ ТРУБ С ПОКРЫТИЕМ | 2006 |
|
RU2373053C2 |
Авторы
Даты
2019-06-17—Публикация
2018-07-20—Подача