Предшествующий уровень техники
Болезнь Альцгеймера (AD; от англ. "Alzheimer's disease") представляет собой нейродегенеративное расстройство центральной нервной системы и является ведущей причиной прогрессирующей деменции у пожилого населения. Ее клиническими симптомами являются ухудшение памяти, познавательной способности, временной и пространственной ориентации, суждения и мышления, а также тяжелые эмоциональные нарушения. В настоящее время нет доступных способов лечения, которые могут предупреждать это заболевание или его прогрессирование, либо вызывать стабильную реверсию его клинических симптомов. AD стала значительной проблемой здравоохранения во всех обществах с высокой средней продолжительностью жизни, а также значительным экономическим бременем для их систем здравоохранения.
AD характеризуется двумя основными патологиями центральной нервной системы (ЦНС): возникновением амилоидных бляшек и нейрофибриллярных клубков (Hardy et al., The amyloid hypothesis of Alzheimer's disease: progress and problems on the road to therapeutics, Science. 2002 Jul 19; 297(5580):353-6, Selkoe, Cell biology of the amyloid beta-protein precursor and the mechanism of Alzheimer's disease, Annu Rev Cell Biol. 1994; 10:373-403). Эти обе патологии также обычно наблюдают у пациентов с синдромом Дауна (трисомией 21), у которых также развиваются AD-подобные симптомы в раннем возрасте. Нейрофибриллярные клубки представляют собой внутриклеточные агрегаты ассоциированного с микротрубочками белка tau (МАРТ; от англ. "microtubule-associated protein tau"). Амилоидные бляшки возникают во внеклеточном пространстве, их основными компонентами являются Аβ-пептиды. Последние представляют собой группу протеолитических фрагментов, образованных от белка-предшественника β-амилоида (АРР; от англ. "β-amyloid precursor protein") в результате серии стадий протеолитического расщепления. Идентифицировано несколько форм АРР, из которых наиболее распространенными являются белки длиной 695, 751 и 770 аминокислот. Все они имеют происхождение от одного гена в результате дифференциального сплайсинга. Аβ-пептиды образованы из одного и того же домена АРР, но отличаются их N- и С-концами, где основные виды молекул имеют длину 40 и 42 аминокислоты. Существует несколько линий доказательств, которые убедительно свидетельствуют о том, что Аβ-пептиды являются существенными молекулами в патогенезе AD: 1) амилоидные бляшки, образованные из Аβ-пептидов, составляют неизменную часть патологии AD; 2) Аβ-пептиды токсичны для нейронов; 3) при семейной болезни Альцгеймера (FAD; от англ. "Familial Alzheimer's Disease") мутации в генах этого заболевания АРР, PSN1, PSN2 приводят к повышенным уровням Аβ-пептидов и раннему амилоидозу головного мозга; 4) у трансгенных мышей, которые экспрессируют такие гены FAD, развивается патология, которая имеет много сходств с заболеванием у человека. Аβ-пептиды продуцируются из АРР посредством последовательного действия двух протеолитических ферментов, называемых β- и γ-секретазой. β-Секретаза сначала отщепляет примерно 28 аминокислот во внеклеточном домене АРР снаружи от трансмембранного домена (ТМ; от англ. "transmembrane domain") с образованием С-концевого фрагмента АРР, содержащего ТМ и цитоплазматический домен (CTFβ). CTFβ является субстратом для γ-секретазы, которая расщепляет в нескольких соседних положениях внутри ТМ с образованием Аβ пептидов и цитоплазматического фрагмента. γ-Секретаза представляет собой комплекс, состоящий по меньшей мере 4 различных белков, и ее каталитической субъединицей весьма вероятно является белок пресенилин (PSEN1, PSEN2). β-Секретаза (ВАСЕ1, Asp2; ВАСЕ обозначает β-сайт АРР-расщепляющего фермента) представляет собой аспартилпротеазу, которая заякорена в мембране посредством трансмембранного домена (Vassar et al., Beta-secretase cleavage of Alzheimer's amyloid precursor protein by the transmembrane aspartic protease BACE, Science. 1999 Oct 22; 286(5440):735). Она экспрессируется во многих тканях организма человека, но ее уровень особенно высок в ЦНС. Генетическое разрушение гена ВАСЕ1 у мышей четко показало, что его активность существенна для процессинга АРР, который приводит к образованию Аβ-пептидов, в отсутствие ВАСЕ1 Аβ-пептиды не продуцируются (Luo et al., Mice deficient in BACE1, the Alzheimer's beta-secretase, have normal phenotype and abolished beta-amyloid generation, Nat Neurosci. 2001 Mar; 4(3):231-2, Roberds et al., BACE knockout mice are healthy despite lacking the primary beta-secretase activity in brain: implications for Alzheimer's disease therapeutics, Hum Mol Genet. 2001 Jun 1; 10(12):1317-24). Мыши, у которых генно-инженерным путем получена экспрессия гена АРР человека, и у которых образуются обширные амилоидные бляшки и патологии, подобные болезни Альцгеймера, при старении, этого не происходит, когда активность β-секретазы снижена в результате генетического разрушения одного из аллелей ВАСЕ1 (McConlogue et al., Partial reduction of BACE1 has dramatic effects on Alzheimer plaque and synaptic pathology in APP Transgenic Mice. J Biol Chem. 2007 Sep 7; 282(36):26326). Следовательно, предполагают, что ингибиторы активности ВАСЕ1 могут быть полезными агентами для терапевтического вмешательства в болезнь Альцгеймера (AD).
В WO 2011044181 описаны диоксиды иминотиадиазина и в WO 2011044184 описаны пентафторсульфуриминогетероциклы в качестве ингибиторов ВАСЕ1.
Кроме того, образование, или образование и осаждение β-амилоидных пептидов в, на или вокруг неврологической ткани (например, в головном мозге) ингибируется соединениями настоящего изобретения, то есть путем ингибирования продуцирования Аβ из АРР или фрагмента АРР.
Настоящее изобретение относится к новым соединениям формулы I, их получению, к лекарственным средствам на основе соединения в соответствии с изобретением и к их получению, а также к применению соединений формулы I для контроля или профилактики заболеваний, таких как болезнь Альцгеймера.
Область изобретения
Настоящее изобретение относится к триазабициклам, обладающим свойствами ингибиторов ВАСЕ1, к их получению, фармацевтическим композициям, содержащим их, и к их применению в качестве терапевтически активных веществ.
Сущность изобретения
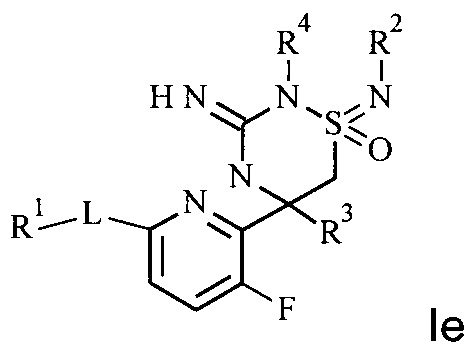
Настоящее изобретение относится к соединению формулы I,
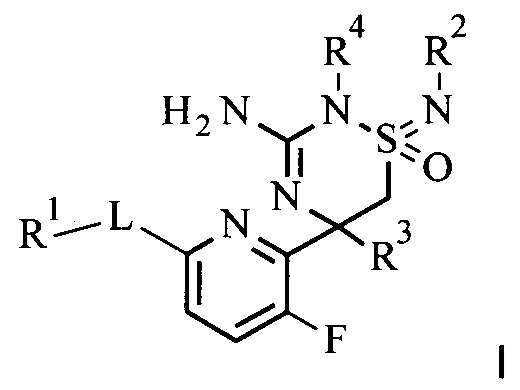
в котором заместители и переменные являются такими, как описано ниже и в формуле изобретения, либо к его фармацевтически приемлемой соли.
Соединения согласно настоящему изобретению обладают активностью ингибирования Asp2 (β-секретазы, ВАСЕ1 или мемапсина-2) и, следовательно, их можно применять при терапевтическом и/или профилактическом лечении заболеваний и расстройств, характеризующихся повышенными уровнями β-амилоида и/или олигомеров β-амилоида и/или β-амилоидных бляшек и дополнительных отложений, в частности, болезни Альцгеймера.
Подробное описание изобретения
Настоящее изобретение предлагает соединения формулы I и их фармацевтически приемлемые соли, получение этих соединений, содержащие их лекарственные средства и их получение, а также применение указанных соединений в терапевтическом и/или профилактическом лечении заболеваний и расстройств, связанном с ингибированием активности ВАСЕ1, таких как болезнь Альцгеймера. Кроме того, настоящие соединения ингибируют образование или образование и отложение β-амилоидных бляшек в неврологической ткани (например, в головном мозге) или вокруг нее посредством ингибирования продуцирования Аβ из АРР или фрагмента АРР.
Приведенные ниже определения общих терминов, используемых в настоящем описании, применяют независимо от того, встречаются ли обсуждаемые термины отдельно или в сочетании с другими группами.
Если не указано иное, приведенные ниже термины, используемые в данной заявке, включая описание и формулу изобретения, имеют приведенные ниже определения. Необходимо отметить, что, как используют в описании и прилагаемой формуле изобретения, формы единственного числа включают формы множественного числа, если контекстом явным образом не продиктовано иное.
Термин "C1-6-алкил", отдельно или в комбинации с другими группами, означает углеводородный радикал, который может быть линейным или разветвленным, с одиночным или множественным разветвлением, где алкильная группа, как правило, включает от 1 до 6 атомов углерода, например, метил (Me), этил (Et), пропил, изопропил (i-пропил), н-бутил, i-бутил (изобутил), 2-бутил (втор-бутил), t-бутил (трет-бутил), изопентил, 2-этилпропил (2-метилпропил), 1,2-диметилпропил и тому подобное. Конкретный "С1-6-алкил" представляет собой "С1-3-алкил". Особые группы представляют собой метил и этил. Наиболее конкретная группа представляет собой метил.
Термин "галоген-С1-6-алкил" или "С1-6-алкилгалоген", отдельно или в комбинации с другими группами, относится к C1-6-алкилу, как определено в данной работе, замещенному одним или несколькими атомами галогена, в частности, 1-5 атомами галогена, более конкретно 1-3 атомами галогена. Конкретным галогеном является фтор. Конкретный "галоген-С1-6-алкил" представляет собой фтор-С1-6-алкил и конкретный "галоген-С1-3-алкил" представляет собой фтор-С1-3-алкил. Примерами являются трифторметил, дифторметил, фторметил и т.п. Конкретная группа представляет собой фторметил.
Термин "циано", отдельно или в комбинации с другими группами, означает N≡C-(NC-).
Термин "галоген", отдельно или в комбинации с другими группами, означает атом хлора (Cl), йода (I), фтора (F) и брома (Br). Конкретный "галоген" представляет собой Cl, I и F. Конкретная группа представляет собой F.
Термин "гетероарил", отдельно или в комбинации с другими группами, относится к ароматической карбоциклической группе, имеющей одно 4-8-членное кольцо, в частности, 5-8-членное, или несколько конденсированных колец, включающих от 6 до 14, в частности, от 6 до 10, кольцевых атомов, и содержащих 1, 2 или 3 гетероатома, индивидуально выбранных из N, О и S, в частности, 1Н или 2N, причем, в этой группе по меньшей мере одно гетероциклическое кольцо является ароматическим. Примеры "гетероарила" включают бензофурил, бензоимидазолил, 1Н-бензимидазолил, бензооксазинил, бензоксазолил, бензотиазинил, бензотиазолил, бензотиенил, бензотриазолил, фурил, имидазолил, индазолил, 1Н-индазолил, индолил, изохинолинил, изотиазолил, изоксазолил, оксазолил, пиразинил, пиразолил (пиразил), 1Н-пиразолил, пиразоло[1,5-а]пиридинил, пиридазинил, пиридинил (пиридил), пиримидинил (пиримидил), пирролил, хинолинил, тетразолил, тиазолил, тиенил, триазолил, 6,7-дигидро-5Н-[1]пиридинил и т.п. Конкретными "гетероарильными" группами являются пиридил и пиразинил.
Термин "арил" означает одновалентную ароматическую карбоциклическую моно- или бициклическую кольцевую систему, содержащую от 6 до 10 кольцевых атомов углерода. Примеры арильных групп включают фенил и нафтил. Конкретным арилом является фенил.
Термин "фармацевтически приемлемые соли" относится к солям, которые пригодны для применения в контакте с тканями людей и животных. Примерами подходящих солей с неорганическими и органическими кислотами являются, но не ограничены ими, соли со следующими кислотами: уксусной кислотой, лимонной кислотой, муравьиной кислотой, фумаровой кислотой, соляной кислотой, молочной кислотой, малеиновой кислотой, яблочной кислотой, метансульфоновой кислотой, азотной кислотой, фосфорной кислотой, пара-толуолсульфоновой кислотой, янтарной кислотой, серной кислотой, винной кислотой, трифторуксусной кислотой и тому подобное. Конкретными являются следующие кислоты: муравьиная кислота, трифторуксусная кислота и соляная кислота. Конкретной кислотой является соляная кислота.
Термины "фармацевтически приемлемый носитель" и "фармацевтически приемлемое вспомогательное вещество" относятся к носителям и вспомогательным веществам, таким как разбавители или эксципиенты, совместимые с другими ингредиентами композиции.
Термин "фармацевтическая композиция" включает продукт, содержащий указанные ингредиенты в предопределенных количествах или пропорциях, а также любой продукт, который является, прямо или косвенно, результатом объединения указанных ингредиентов в указанных количествах. В частности, этот термин включает продукт, содержащий один или более активных ингредиентов, и необязательный носитель, включающий инертные ингредиенты, а также любой продукт, который является, прямо или косвенно, результатом объединения, комплексообразования или агрегации любых двух или более ингредиентов, либо диссоциации одного или более ингредиентов, либо других типов реакций или взаимодействий одного или более ингредиентов.
Термин "ингибитор" означает соединение, которое конкурирует с, уменьшает или предотвращает связывание определенного лиганда с определенным рецептором или которое уменьшает или предотвращает ингибирование функции определенного белка.
Термин "половинная максимальная ингибиторная концентрация" (IC50) означает концентрацию конкретного соединения, необходимую для получения 50% ингибирования биологического процесса in vitro. Значения IC50 можно логарифмически преобразовать в значения pIC50 (-log IC50), в которых более высокие значения указывают на экспоненциально более высокую эффективность. Значение IC50 не является абсолютной величиной, а зависит от экспериментальных условий, например, от используемых концентраций. Значение IC50 можно преобразовать в абсолютную константу ингибирования (Ki), используя уравнение Ченга-Прусоффа (Biochem. Pharmacol. (1973) 22:3099). Термин "константа ингибирования" (Ki) означает абсолютное сродство связывания конкретного ингибитора с рецептором. Ее измеряют, используя анализы конкурентного связывания, и она равна концентрации, при которой конкретный ингибитор занимал бы 50% рецепторов, если отсутствует конкурирующий лиганд (например, радиолиганд). Значения Ki можно логарифмически преобразовать в значения pKi (-log Ki), в которых более высокие значения указывают на экспоненциально более высокую эффективность.
"Терапевтически эффективное количество" означает количество соединения, которое при введении субъекту для лечения болезненного состояния, является достаточным, чтобы осуществить такое лечение болезненного состояния. "Терапевтически эффективное количество" варьирует в зависимости от соединения, болезненного состояния, подлежащего лечению, тяжести заболевания, подлежащего лечению, возраста и относительного состояния здоровья субъекта, пути и формы введения, мнения лечащего врача или ветеринара и от других факторов.
Термин "как определено в данной работе" и "как раскрыто в данной работе" при отнесении к переменной включает посредством ссылки, как широкое определение этой переменной, так и конкретные, более конкретные и наиболее конкретные определения, если они есть.
Термины "обработка", "приведение в контакт" и "взаимодействие" при отнесении к химической реакции означают добавление или смешивание двух или более реагентов в соответствующих условиях с получением указанного и/или желаемого продукта. Понятно, что реакция, которая дает указанный и/или желаемый продукт, может необязательно являться прямым результатом объединения двух реагентов, которые были первоначально добавлены, то есть может существовать одно или более промежуточных соединений, которые образуются в смеси, что, в конце концов, приводит к образованию указанного и/или желаемого продукта.
Термин "ароматический" означает обычную идею ароматичности, как это определено в литературе, в частности, в IUPAC - Сборнике химической терминологии, 2-е изд., A.D. McNaught & A. Wilkinson (Eds). Blackwell Scientific Publications, Oxford (1997).
Термин "фармацевтически приемлемый эксципиент" означает любой ингредиент, не обладающий терапевтической активностью и являющийся нетоксичным, такой как дезинтеграторы, связующие вещества, наполнители, растворители, буферы, агенты тоничности, стабилизаторы, антиоксиданты, поверхностно-активные вещества или лубриканты, используемые в приготовлении фармацевтических продуктов.
В любом случае, когда в химической структуре присутствует хиральный атом углерода, подразумевают, что все стереоизомеры, связанные с этим хиральным атомом углерода, охвачены данной структурой, как чистые стереоизомеры, так и их смеси.
Изобретение также относится к фармацевтическим композициям, способам их применения и к способам получения указанных выше соединений.
Все отдельные варианты осуществления изобретения могут быть объединены.
Один вариант осуществления изобретения относится к соединению формулы I,

где
R1 выбран из группы, состоящей из
i) Н,
ii) арила,
iii) арила, замещенного 1-3 заместителями, индивидуально выбранными из циано, галогена, С1-6-алкила, галоген-С1-6-алкила и, -О-С1-6-алкила, -O-С2-6-алкинила, -О-С1-6-алкилгалогена
iv) гетероарила, и
v) гетероарила, замещенного 1-3 заместителями, индивидуально выбранными из циано, галогена C1-6-алкила, галоген-С1-6-алкила, -О-С1-6-алкила, -O-С2-6-алкинила и -O-C1-6-алкилгалогена;
R2 выбран из группы, состоящей из
i) C1-6-алкила, и
ii) галоген-С1-6-алкила;
R3 выбран из группы, состоящей из
i) С1-6-алкила, и
ii) галоген-С1-6-алкила;
R4 выбран из группы, состоящей из
i) С1-6-алкила, и
ii) галоген-С1-6-алкила;
L выбран из группы, состоящей из
i) отсутствия, и
ii) -NH-C(=O)-;
или к его фармацевтически приемлемым солям.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, которое имеет формулу Ia, где L, R1, R2, R3 и R4 являются такими, как раскрыто в данной работе
 .
.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, которое имеет формулу Ia, где L, R1, R2, R3 и R4 являются такими, как раскрыто в данной работе
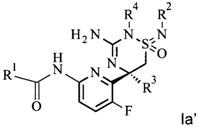 .
.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R1 представляет собой гетероарил, замещенный 1-2 заместителями, индивидуально выбранными из циано, галогена, C1-6-алкила, галоген-С1-6-алкила, -О-С1-6-алкила, -O-С2-6-алкинила и -О-С1-6-алкилгалогена.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R1 представляет собой пиридил или пиразинил, замещенный 1-2 заместителями, индивидуально выбранными из циано, метила, метокси, фторметокси, трифторэтокси, бут-2-инокси и проп-2-инокси.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R1 представляет собой 5-циано-3-хлорпиридил, 5-циано-3-метилпиридил, 5-цианопиридил, 5-фтор-3-метилпиридил, 5-(фторметокси)пиридил, 5-бут-2-иноксипиразинил, 5-метоксипиразинил, 5-(2,2,2-трифторэтокси)пиридил, 5-проп-2-иноксипиридил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R1 представляет собой 5-циано-3-метилпиридил, 5-цианопиридил, 5-фтор-3-метилпиридил, 5-(фторметокси)пиридил, 5-бут-2-иноксипиразинил, 5-метоксипиразинил, 5-(2,2,2-трифторэтокси)пиридил, 5-проп-2-иноксипиридил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R2 представляет собой галоген-C1-6-алкил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R2 представляет собой 2,2,2-трифторэтил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R2 представляет собой С1-6-алкил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R2 представляет собой метил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R3 представляет собой С1-6-алкил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R3 представляет собой метил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R4 представляет собой C1-6-алкил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R4 представляет собой метил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R4 представляет собой галоген-С1-6-алкил.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, где R4 представляет собой -CH2CF3.
Определенный вариант осуществления изобретения относится к промежуточному соединению формулы I', где R2, R3 и R4 являются такими, как раскрыто в данной работе
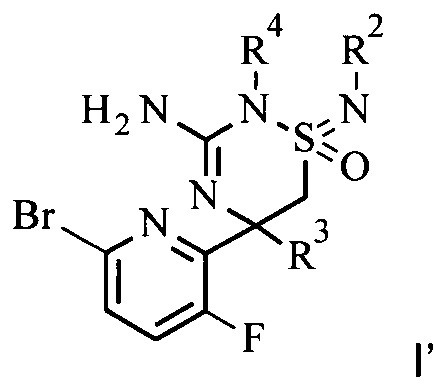 .
.
Определенный вариант осуществления изобретения относится к промежуточному соединению формулы А12, где R1, R2, R3 и R4 являются такими, как раскрыто в данной работе
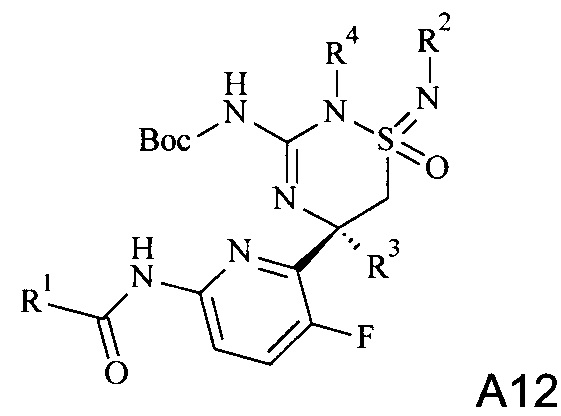 .
.
Определенный вариант осуществления изобретения относится к промежуточному соединению формулы II, где R2, R3 и R4 являются такими, как раскрыто в данной работе, и Ar представляет собой арил или гетероарил, как раскрыто в данной работе.
 .
.
Определенный вариант осуществления изобретения относится к соединению формулы I'', где R2, R3 и R4 являются такими, как раскрыто в данной работе
 .
.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, которое выбрано из группы, состоящей из
(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина;2,2,2-трифторуксусной кислоты,
(1R,5R)-5-[3-фтор-6-(1H-пиразол-5-ил)пиридин-2-ил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
(1R,5R)-5-[6-(5-хлортиофен-2-ил)-3-фторпиридин-2-ил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
(1S,5R)-5-(6-бром-3-фторпиридин-2-ил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина;2,2,2-трифторуксусной кислоты,
(5R)-5-(6-бром-3-фторпиридин-2-ил)-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-3-амина;2,2,2-трифторуксусной кислоты,
N-(6-((5R)-3-амино-5-метил-1-(метилимино)-1-оксидо-2-(2,2,2-трифторэтил)-5,6-дигидро-2Н-1,2,4-тиадиазин-5-ил)-5-фторпиридин-2-ил)-3-хлор-5-цианопиколинамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-цианопиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-фтор-3-метилпиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-(фторметокси)пиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-бут-2-иноксипиразин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-метоксипиразин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-(2,2,2-трифторэтокси)пиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-проп-2-иноксипиридин-2-карбоксамида,
N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида,
N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида,
N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-фтор-3-метилпиридин-2-карбоксамида и
N-[6-[3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида, или их фармацевтически приемлемых солей.
Определенный вариант осуществления изобретения относится к соли 2,2,2-трифторуксусной кислоты соединения формулы I, как раскрыто в данной работе, которая выбрана из группы, состоящей из
(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина;2,2,2-трифторуксусной кислоты,
(1R,5R)-5-[3-фтор-6-(1Н-пиразол-5-ил)пиридин-2-ил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
(1R,5R)-5-[6-(5-хлортиофен-2-ил)-3-фторпиридин-2-ил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
(1S,5R)-5-(6-бром-3-фторпиридин-2-ил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина;2,2,2-трифторуксусной кислоты,
(5R)-5-(6-бром-3-фторпиридин-2-ил)-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-3-амина;2,2,2-трифторуксусной кислоты,
N-(6-((5R)-3-амино-5-метил-1-(метилимино)-1-оксидо-2-(2,2,2-трифторэтил)-5,6-дигидро-2Н-1,2,4-тиадиазин-5-ил)-5-фторпиридин-2-ил)-3-хлор-5-цианопиколинамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-цианопиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-фтор-3-метилпиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-(фторметокси)пиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-бут-2-иноксипиразин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-метоксипиразин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-(2,2,2-трифторэтокси)пиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-проп-2-иноксипиридин-2-карбоксамида,
N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида,
N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида,
N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-фтор-3-метилпиридин-2-карбоксамида, и
N-[6-[3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида.
Определенный вариант осуществления изобретения относится к соединению формулы I, как раскрыто в данной работе, которое выбрано из группы, состоящей из
(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
(1S,5R)-5-(6-бром-3-фторпиридин-2-ил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-цианопиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-фтор-3-метилпиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-(фторметокси)пиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-бут-2-иноксипиразин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-метоксипиразин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-(2,2,2-трифторэтокси)пиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-проп-2-иноксипиридин-2-карбоксамида,
(1R,5R)-5-[3-фтор-6-(1H-пиразол-5-ил)пиридин-2-ил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина, и
(1R,5R)-5-[6-(5-хлортиофен-2-ил)-3-фторпиридин-2-ил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
или их фармацевтически приемлемых солей.
Определенный вариант осуществления изобретения относится к способу, включающему взаимодействие соединения формулы XI' с соединением формулы XII' с получением соединения формулы I.
 ,
,
где R1, R2, R3 и R4 являются такими, как определено в данной работе.
Определенный вариант осуществления изобретения относится к способу, включающему взаимодействие соединения формулы А10 с получением соединения формулы II.

где R2, R3 и R4 являются такими, как определено в данной работе, и Ar представляет собой арил или гетероарил, как раскрыто в данной работе.
Определенный вариант осуществления изобретения предлагает соединение формулы I, как раскрыто в данной работе, полученное способом, как раскрыто в данной работе.
Определенный вариант осуществления изобретения предлагает соединение формулы I, как раскрыто в данной работе, для применения в качестве терапевтически активного вещества.
Определенный вариант осуществления изобретения предлагает соединение формулы I, как раскрыто в данной работе, для применения в качестве ингибитора активности ВАСЕ1.
Определенный вариант осуществления изобретения предлагает соединение формулы I, как раскрыто в данной работе, для применения в качестве терапевтически активного вещества для терапевтического и/или профилактического лечения заболеваний и расстройств, характеризующихся повышенными уровнями β-амилоида и/или олигомеров β-амилоида и/или β-амилоидных бляшек и дополнительных отложений, или болезни Альцгеймера.
Определенный вариант осуществления изобретения предлагает соединение формулы I, как раскрыто в данной работе, для применения в качестве терапевтически активного вещества для терапевтического и/или профилактического лечения болезни Альцгеймера.
Определенный вариант осуществления изобретения предлагает фармацевтическую композицию, содержащую соединение формулы I, как раскрыто в данной работе, и фармацевтически приемлемый носитель и/или фармацевтически приемлемое вспомогательное вещество.
Определенный вариант осуществления изобретения предлагает применение соединения формулы I, как раскрыто в данной работе, для изготовления лекарственного средства для применения в ингибировании активности ВАСЕ1.
Определенный вариант осуществления изобретения предлагает применение соединения формулы I, как раскрыто в данной работе, для изготовления лекарственного средства для терапевтического и/или профилактического лечения заболеваний и расстройств, характеризующихся повышенными уровнями β-амилоида и/или олигомеров β-амилоида и/или β-амилоидных бляшек и дополнительных отложений, или болезни Альцгеймера.
Определенный вариант осуществления изобретения предлагает применение соединения формулы I, как раскрыто в данной работе, для изготовления лекарственного средства для терапевтического и/или профилактического лечения болезни Альцгеймера.
Определенный вариант осуществления изобретения предлагает применение соединения формулы I, как раскрыто в данной работе, для изготовления лекарственного средства для терапевтического и/или профилактического лечения болезни Альцгеймера.
Определенный вариант осуществления изобретения предлагает соединение формулы I, как раскрыто в данной работе, для применения в ингибировании активности ВАСЕ1.
Определенный вариант осуществления изобретения предлагает соединение формулы I, как раскрыто в данной работе, для применения в терапевтическом и/или профилактическом лечении заболеваний и расстройств, характеризующихся повышенными уровнями β-амилоида и/или олигомеров β-амилоида и/или β-амилоидных бляшек и дополнительных отложений, или болезни Альцгеймера.
Определенный вариант осуществления изобретения предлагает соединение формулы I, как раскрыто в данной работе, для применения в терапевтическом и/или профилактическом лечении болезни Альцгеймера.
Определенный вариант осуществления изобретения предлагает способ для применения в ингибировании активности ВАСЕ1, в частности, в терапевтическом и/или профилактическом лечении заболеваний и расстройств, характеризующихся повышенными уровнями β-амилоида и/или олигомеров β-амилоида и/или β-амилоидных бляшек и дополнительных отложений, или болезни Альцгеймера, включающий введение соединения формулы I, как раскрыто в данной работе, человеку или животному.
Определенный вариант осуществления изобретения предлагает способ для применения в терапевтическом и/или профилактическом лечении болезни Альцгеймера, включающий введение соединения формулы I, как раскрыто в данной работе, человеку или животному.
Кроме того, изобретение включает все оптические изомеры, то есть диастереоизомеры, диастереомерные смеси, рацемические смеси, все их соответствующие энантиомеры и/или таутомеры, а также их сольваты соединений формулы I.
Специалистам в данной области техники понятно, что соединения формулы I могут существовать в таутомерной форме
 .
.
Все таутомерные формы включены в объем настоящего изобретения.
Соединения, имеющие формулу I, могут содержать один или более асимметрических центров, и, следовательно, могут существовать в виде рацематов, рацемических смесей, отдельных энантиомеров, диастереомерных смесей и индивидуальных диастереомеров. Дополнительные асимметрические центры могут присутствовать в зависимости от природы различных заместителей на молекуле. Каждый такой асимметрический центр независимо образует два оптических изомера, и подразумевают, что все возможные оптические изомеры и диастереомеры в виде смесей и в виде чистых или частично очищенных соединений включены в данное изобретение. Подразумевают, что настоящее изобретение включает все такие изомерные формы этих соединений. Независимые синтезы этих диастереомеров или их хроматографические разделения могут быть достигнуты, как известно в данной области техники, путем соответствующей модификации методологии, раскрытой в настоящей работе. Их абсолютная стереохимия может быть определена с помощью рентгенокристаллографии кристаллических продуктов или кристаллических промежуточных соединений, которые являются дериватизированными, при необходимости, реагентом, содержащим асимметрический центр, имеющий известную абсолютную конфигурацию. При желании рацемические смеси соединений могут быть разделены таким образом, чтобы выделить индивидуальные энантиомеры. Это разделение можно осуществить способами, хорошо известными в данной области техники, такими как конденсация рацемической смеси соединений с энантиомерно чистым соединением с образованием диастереомерной смеси с последующим разделением индивидуальных диастереомеров стандартными способами, такими как фракционная кристаллизация или хроматография.
В тех формах осуществления, в которых предложены оптически чистые энантиомеры, оптически чистый энантиомер означает, что соединение содержит более 90% желаемого изомера по массе, в частности, более 95% желаемого изомера по массе, или более конкретно более 99% желаемого изомера по массе, причем, данный процент по массе основан на суммарной массе изомера (изомеров) соединения. Хирально чистые или хирально обогащенные соединения могут быть получены путем стереоселективного синтеза или путем разделения энантиомеров. Разделение энантиомеров может быть выполнено на конечном продукте или альтернативно на подходящем промежуточном соединении.
Соединения, имеющие формулу I, могут быть получены в соответствии со способами синтеза, например, как проиллюстрировано на схеме 1. Получение соединений формулы I по настоящему изобретению может быть осуществлено с помощью последовательных или конвергентных способов синтеза. Синтезы соединений по изобретению показаны на следующей схеме 1. Навыки, необходимые для проведения реакции и очистки полученных продуктов, известны специалистам в данной области техники. Заместители и индексы, используемые в нижеследующем описании способов, имеют значения, приведенные в данной работе, если не указано иное.
Более подробно соединения формулы I в соответствии с настоящим изобретением могут быть получены способами и методиками, приведенными ниже. Некоторые типичные методики получения соединений формулы I показаны на схеме 1.
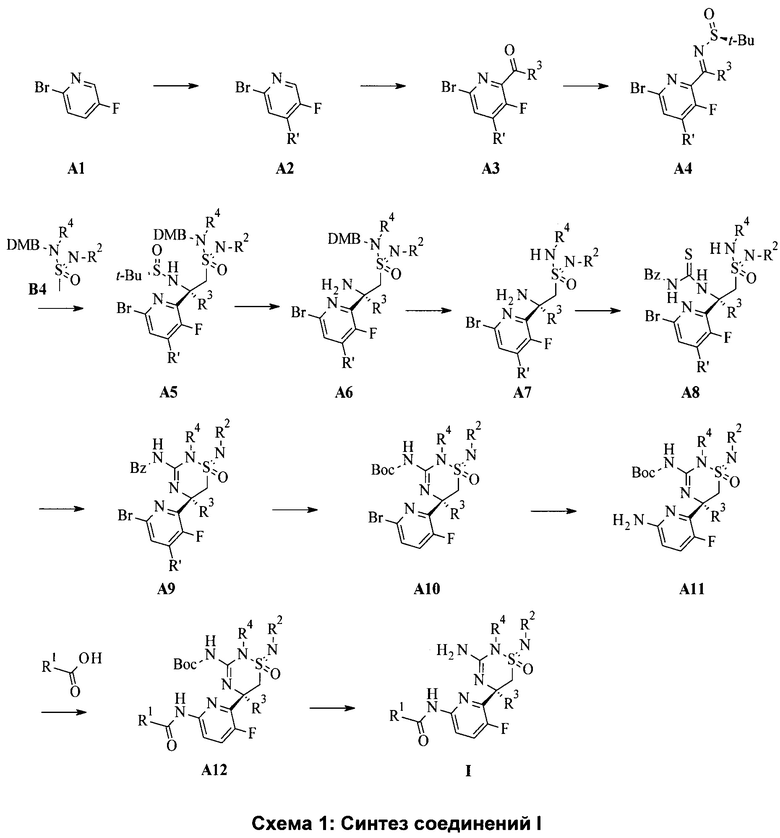
Некоммерческие арилкетоны общей формулы A3 могут быть синтезированы из силилзащищенного пиридина А2, полученного из пиридина А1, путем реакции с сильным основанием, например, с LDA и алкилхлорсиланом, предпочтительно с триэтилхлорсиланом, в инертном апротонном растворителе, таком как тетрагидрофуран или диэтиловый эфир. Затем защищенный пиридин А2 можно подвергнуть снова взаимодействию с сильным основанием, например, LDA и амидом, например ацетамидом, для R3 представляющим собой Me, предпочтительно N,N-диметилацетамидом, в инертном апротонном растворителе, таком как тетрагидрофуран или диэтиловый эфир, с получением желаемого арилкетона A3.
Сульфинилимины формулы А4 могут быть получены по аналогии с документом Т.Р. Tang & J.A. Ellman, J. Org. Chem. 1999, 64, 12, путем конденсации арилкетона формулы В3 и сульфинамида, например, алкилсульфинамида, наиболее конкретно (R)-(+)-трет-бутилсульфинамида или (S)-трет-бутилсульфинамида, в присутствии кислоты Льюиса, такой как, например, алкоксид титана(IV), более конкретно, этоксид титана(IV), в растворителе, таком как эфир, например, диэтиловый эфир, или, более конкретно, тетрагидрофуран.
Преобразование сульфинилиминов А4 в сульфонамиды-сульфонимидамиды формулы А5 протекает стереоселективно посредством хиральной направляющей группы, как описано в статье Tang & Ellman. Сульфинилимины А4 можно подвергать взаимодействию в реакции присоединения с литий-сульфонимидамидами, полученными из сульфонимидамида формулы В4 и основания, такого как н-бутиллитий, гексаметилдисилазид лития или LDA, в растворителе, таком как простой эфир, например диэтиловый эфир, или, в частности, тетрагидрофуран, при низких температурах, предпочтительно -78°С.
Гидролиз хиральной направляющей группы и 2,4-диметоксибензильной группы (DMB) сульфонамидов-сульфонимидамидов формулы А5 с получением аминосульфонимидамидов формулы А7 может быть осуществлен первой обработкой минеральной кислотой, например серной кислотой или, в частности, соляной кислотой, в растворителе, таком как простой эфир, например, диэтиловый эфир, тетрагидрофуран или, более конкретно, 1,4-диоксан, с получением А6, и второй обработкой сильной органической кислотой, например трифторуксусной кислотой, где обе стадии предпочтительно проводят при температуре окружающей среды с получением А7.
Реакция аминосульфонимидамидов формулы А7 с изотиоцианатом, таким как бензоилизотиоцианат в растворителях, таких как этилацетат, тетрагидрофуран или ацетонитрил, при температурах между 0°С и 80°С, предпочтительно 23°С, приводит к получению тиомочевиносульфонимидамидов формулы А8.
Тиомочевиносульфонимидамиды формулы А8 можно циклизовать с получением N-бензоилированных амидинсульфонимидамидов формулы А9 путем дегидратации посредством реакции с карбодиимидом, таким как, например, дициклогексилкарбодиимид, диизопропилкарбодиимид или N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорид (EDC⋅HCl), предпочтительно EDC⋅HCl, в растворителях, таких как этилацетат, тетрагидрофуран или ацетонитрил, предпочтительно ацетонитрил, при температурах между 23°С и 100°С, предпочтительно 80°С.
Превращение сульфонимидамидов формулы А9, где R' представляет собой SiEt3, в десилилированные сульфонимидамиды формулы А10 можно осуществить с помощью тетрабутиламмония фторида или предпочтительно фторида натрия в присутствии кислоты, например уксусной кислоты, в эфире или амиде, предпочтительно в смеси ТГФ (тетрагидрофурана) и диметилформамида, при температуре от комнатной до повышенной, в частности, от 23 до 40°С.
Замена защитных групп от N-бензоилированных амидинсульфонимидамидов формулы А9 до N-трет-бутоксикарбонилированных амидинсульфонимидамидов формулы А10 может быть достигнута в двухстадийном способе сначала путем реакции с ди-трет-бутилдикарбонатом (Boc2O) в присутствии аминового основания, такого как триэтиламин или N-этил-N,N-диизопропиламин, в растворителе, таком как дихлорметан, тетрагидрофуран или ацетонитрил, при температурах между 0°С и 40°С, предпочтительно 23°С, с получением дважды ацилированных амидинсульфонимидамидов формулы А18, и затем путем селективного удаления бензоильной группы путем реакции дважды ацилированных амидинсульфонимидамидов с аминонуклеофилом, таким как, например, диэтиламин, диметиламин или аммиак, предпочтительно аммиак, в растворителе, таком как дихлорметан или тетрагидрофуран, предпочтительно тетрагидрофуран, при температурах между 0°С и 40°С, предпочтительно 23°С.
Превращение бромной группы в формуле А10 в аминогруппу в формуле А11 можно выполнить путем реакции с азидом, в частности, азидом натрия и галогенидом меди (I), в частности иодидом меди (I) в присутствии L-аскорбата и алкил-1,2-диамина, в частности транс-N,N'-диметилциклогексан-1,2-диамина, в протонном растворителе, таком как спирт, в частности этанол, и вода при повышенной температуре предпочтительно приблизительно 70°С.
Конденсацию ароматического амина А11 с карбоновыми кислотами (R1-CO2H) с получением амидов формулы А12 можно осуществить с ТЗР в апротонном растворителе, таком как EtOAc, при температуре окружающей среды; или альтернативно, карбоновые кислоты (R1-CO2H) можно активировать с использованием реагентов, таких как оксалилхлорид или 1-хлор-N,N,2-триметил-1-пропениламин (реагент Госеза, CAS-no. 26189-59-3), в хлорированном растворителе, таком как дихлорметан, при 0°C с последующей реакцией с ароматическим амином А11 в присутствии аминового основания, такого как триэтиламин или диизопропилэтиламин, при температуре от 0°С до температуры окружающей среды.
Отщепление защитных трет-бутоксикарбонильных групп в соединениях формулы А12 с получением соединений общей формулы I можно осуществить с использованием кислоты, такой как трифторуксусная кислота, в инертном растворителе, таком как дихлорметан, при температурах между 0°С и температурой окружающей среды.
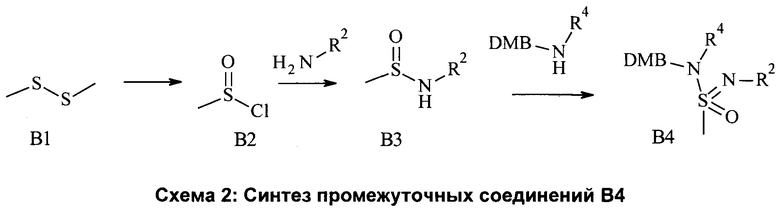
Метансульфинилхлорид формулы В2 можно получить путем обработки коммерчески доступного диметилдисульфида формулы В1 сульфурилхлоридом и уксусной кислотой при температурах между -30°С и 35°С, как описано Youn, Joo-Hack; Herrmann, Rudolf в Tempahedron Letters 1986, 27(13), 1493-1494. Сырой метансульфинилхлорид формулы B2 можно очистить путем дистилляции или использовать непосредственно на следующей стадии с получением сульфинамидов формулы В3, что достигается путем простой реакции с избытком амина R2-NH2 или смесей амина R2-NH2 с аминовым основанием, таким как триэтиламин или N-этил-N,N-диизопропиламин, в растворителе, таком как дихлорметан или тетрагидрофуран, при температурах от -78°С и с нагреванием до 0°С или 23°С.
Сульфонимидамиды формулы В4 можно получить из сульфинамидов формулы В3 путем реакции с хлорирующим реагентом, таким как N-хлорсукцинамид или трет-бутилгипохлорит, предпочтительно трет-бутилгипохлорит, в инертном растворителе, таком как ацетонитрил, тетрагидрофуран или дихлорметан, предпочтительно дихлорметан, при температурах от -78°С и с нагреванием до 0°С, с получением промежуточного соединения сульфонимидоилхлорида с последующей реакцией с избытком амина R4-NHDMB или смесей амина R4-NHDMB с аминовым основанием, таким как триэтиламин или N-этил-N,N-диизопропиламин, при температурах от -78°С и с нагреванием до 0°С или 23°С. Амины R4-NHDMB обычно получают путем восстановительного аминирования амина R4-NH2 2,4-диметоксибензальдегидом способами, известными специалистам.

Превращение бром-производного А10 в арилированные соединения формулы II может быть достигнуто путем реакции А10 с бороновой кислотой или соответствующими ее сложными эфирами, такими как пинаколовый эфир, в присутствии основания, такого как карбонат цезия, карбонат натрия, фосфат натрия, ацетат натрия, и палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий или комплекс 2'-(диметиламино)-2-бифенилпалладия(II) хлорида и динорборнилфосфина, при повышенной температуре в микроволновой печи от 80 до 120°С в смеси растворителей диоксан/вода или ацетонитрил/вода. В этих условиях Вос-защитную группу отщепляют термически, чтобы прямо получить соединения формулы II.
Соответствующие фармацевтически приемлемые соли с кислотами могут быть получены стандартными способами, известными специалистам в данной области техники, например, путем растворения соединения, имеющего формулу I, в подходящем растворителе, таком как, например, диоксан или тетрагидрофуран, и добавления соответствующего количества соответствующей кислоты. Продукты могут быть обычно выделены путем фильтрования или путем хроматографии. Преобразование соединения, имеющего формулу I, в фармацевтически приемлемую соль с основанием может быть выполнено путем обработки такого соединения таким основанием. Одним из возможных способов образования такой соли является, например, добавление 1/n эквивалентов основной соли, такой как, например, М(ОН)n, в которой М - катион металла или аммония и n - число анионов гидроксида, к раствору соединения в подходящем растворителе (например, в этаноле, в смеси этанол-вода, в смеси тетрагидрофуран-вода) и удаление растворителя путем выпаривания или лиофилизации. Конкретными солями являются гидрохлорид, формиат и трифторацетат. Особой является трифторацетат.
Если их получение не описано в примерах, соединения, имеющие формулу I, а также все промежуточные продукты могут быть получены аналогичными способами или способами, раскрытыми в данной работе. Исходные вещества имеются в продаже, известны в данной области техники или могут быть получены способами, известными в данной области техники, или по аналогии с ними.
Понятно, что соединения, имеющие общую формулу I, по данному изобретению могут быть дериватизированы по функциональным группам с получением производных, способных к обратному преобразованию в исходное соединение in vivo.
Фармакологические тесты
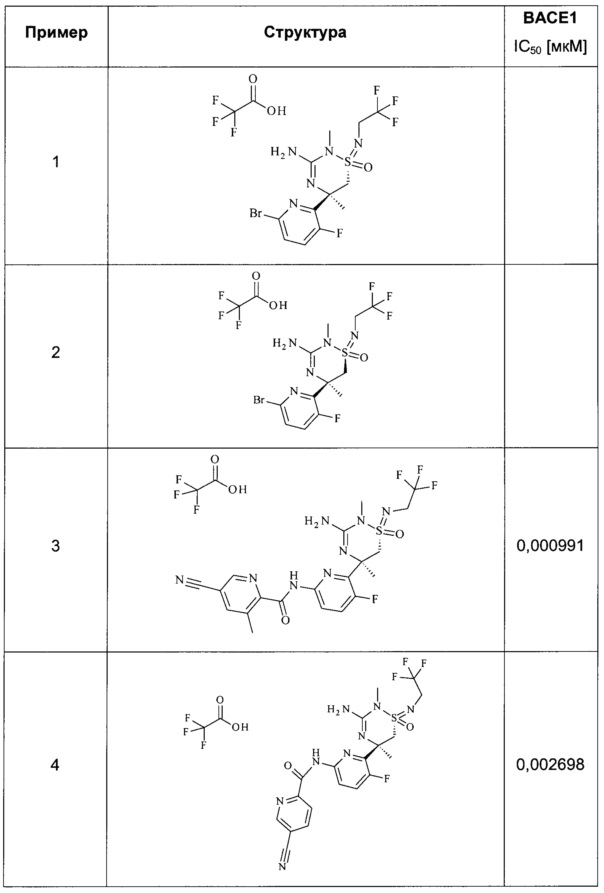
Соединения, имеющие формулу I, и их фармацевтически приемлемые соли обладают ценными фармакологическими свойствами. Обнаружено, что соединения по настоящему изобретению связаны с ингибированием активности ВАСЕ1. Эти соединения были исследованы в соответствии с тестом, приведенным в данной работе ниже.
Клеточный анализ снижения Аβ:
Можно использовать анализ AlphaLISA Аβ 40. Клетки HEK293 АРР высевали в 96-луночные микротитрационные планшеты в среде для клеточных культур (Iscove, с добавлением 10% (об/об) фетальной бычьей сыворотки (ФБС), пенициллина/стрептомицина) примерно до 80% конфлюентности, и соединения добавляли в 3x концентрации в 1/3 объема культуральной среды (конечную концентрацию диметилсульфоксида (ДМСО) поддерживали при 1% об/об). После 18-20 ч инкубации при 37°С и 5% CO2 в увлажненном термостате супернатант культуры собирали для определения концентраций Аβ 40 с использованием набора Perkin-Elmer Human Amyloid beta 1-40 (высокой специфичности) (№ по каталогу AL275C).
В планшете White Optiplate-384 фирмы Perkin-Elmer (№ по каталогу 6007290) 2 мкл супернатантов культур объединяли с 2 мкл 10-кратной смеси акцепторных гранул AlphaLISA анти-hAβ с биотинилированным антителом анти-Аβ 1-40 (50 мкг/мл/5 нМ). После 1-часовой инкубации при комнатной температуре добавляли 16 мкл 1,25-кратного препарата донорных гранул стрептавидина (СА) (25 мкг/мл) и инкубировали в течение 30 минут в темноте. Затем регистрировали испускание света при 615 нм, используя считывающее устройство EnVision-Alpha. Уровни Аβ 40 в супернатантах культуры вычисляли в виде процента от максимального сигнала (клетки, обработанные 1% ДМСО без ингибитора). Значения IC50 вычисляли, используя программу Excel XLfit.



Фармацевтические композиции
Соединения, имеющие формулу I, и их фармацевтически приемлемые соли можно применять в качестве терапевтически активных веществ, например, в форме фармацевтических препаратов. Фармацевтические препараты можно вводить перорально, например, в форме таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Введение можно, однако, также осуществлять ректально, например, в форме суппозиториев, или парентерально, например, в форме инъекционных растворов.
Соединения, имеющие формулу I, и их фармацевтически приемлемые соли можно обрабатывать фармацевтически инертными, неорганическими или органическими носителями, предназначенными для получения фармацевтических препаратов. Лактозу, кукурузный крахмал или его производные, тальк, стеариновые кислоты или их соли и тому подобное можно использовать, например, в качестве таких носителей для таблеток, таблеток с покрытием, драже и твердых желатиновых капсул. Подходящими носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и тому подобное. Тем не менее, в зависимости от природы активного вещества в случае мягких желатиновых капсул носители обычно не требуются. Подходящими носителями для получения растворов и сиропов являются, например, вода, полиолы, глицерин, растительное масло и тому подобное. Подходящими носителями для суппозиториев являются, например, натуральные или отвержденные масла, воски, жиры, полужидкие или жидкие полиолы и тому подобное.
Фармацевтические препараты могут, кроме того, содержать фармацевтически приемлемые вспомогательные вещества, такие как консерванты, солюбилизаторы, стабилизаторы, увлажняющие агенты, эмульгаторы, подсластители, красители, корригенты, соли для варьирования осмотического давления, буферы, маскирующие агенты или антиоксиданты. Эти препараты могут также содержать другие терапевтически ценные вещества.
Лекарственные средства, содержащие соединение, имеющее формулу I, или его фармацевтически приемлемую соль и терапевтически инертный носитель, также являются объектом настоящего изобретения, а также способ их получения, включающий приведение одного или более соединений, имеющих формулу I, и/или их фармацевтически приемлемых солей и, если желательно, одного или более других терапевтически ценных веществ в форму лекарственного препарата для введения вместе с одним или большим числом терапевтически инертных носителей.
Дозировка может варьировать в широких пределах и, конечно, ее следует регулировать по индивидуальным потребностям в каждом конкретном случае. В случае перорального введения доза для взрослых может варьировать от приблизительно 0,01 мг до приблизительно 1000 мг в сутки соединения, имеющего общую формулу I, или соответствующего количества его фармацевтически приемлемой соли. Суточную дозу можно вводить в виде однократной дозы или в разделенных дозах и, кроме того, верхний предел может быть также превышен, если обнаружены показания к этому.
Приведенные ниже примеры иллюстрируют настоящее изобретение без его ограничения, но служат исключительно как репрезентативные. Фармацевтические препараты обычно содержат примерно 1-500 мг, в частности, 1-100 мг соединения, имеющего формулу I. Примерами композиций в соответствии с изобретением являются следующие композиции:
Пример А
Таблетки, имеющие приведенную ниже композицию, готовят обычным способом:

Способ получения
1. Смешивают ингредиенты 1, 2, 3 и 4 и гранулируют с дистиллированной водой.
2. Высушивают гранулы при 50°С.
3. Пропускают гранулы через подходящее оборудование для измельчения.
4. Добавляют ингредиент 5 и смешивают в течение трех минут; прессуют на подходящем прессе.
Пример В-1
Готовят капсулы, имеющие приведенную ниже композицию:


Способ получения
1. Смешивают ингредиенты 1, 2 и 3 в подходящем смесителе в течение 30 минут.
2. Добавляют ингредиенты 4 и 5 и смешивают в течение 3 минут.
3. Заполняют в подходящую капсулу.
Соединение формулы I, лактозу и кукурузный крахмал сначала смешивают в смесителе, а затем в измельчающем аппарате. Смесь возвращают в смеситель; добавляют к ней тальк и тщательно смешивают. Смесь заполняют с помощью аппарата в подходящие капсулы, например, в твердые желатиновые капсулы.
Пример В-2
Готовят мягкие желатиновые капсулы, имеющие приведенную ниже композицию:



Способ получения
Соединение формулы I растворяют в теплом расплаве других ингредиентов, и смесь заполняют в мягкие желатиновые капсулы подходящего размера. Заполненные мягкие желатиновые капсулы обрабатывают в соответствии с обычными методами.
Пример С
Готовят суппозитории, имеющие приведенную ниже композицию:

Способ получения
Суппозиторную массу плавят в стеклянном или стальном сосуде, тщательно смешивают и охлаждают до 45°С. После этого к ней добавляют тонкоизмельченное соединение, имеющее формулу I, и перемешивают до тех пор, пока оно полностью не диспергируется. Смесь заливают в формы для суппозиториев подходящего размера, оставляют до охлаждения; затем суппозитории извлекают из форм и упаковывают индивидуально в вощеную бумагу или металлическую фольгу.
Пример D
Готовят инъекционные растворы, имеющие приведенную ниже композицию:

Способ получения
Соединение формулы I растворяют в смеси полиэтиленгликоля 400 и воды для инъекций (части). Доводят pH до 5,0 уксусной кислотой. Объем доводят до 1,0 мл добавлением остального количества воды. Раствор фильтруют, заполняют во флаконы, используя подходящий допустимый избыток, и стерилизуют.
Пример Е
Готовят пакеты-саше, имеющие приведенную ниже композицию:

Способ получения
Соединение формулы I смешивают с лактозой, микрокристаллической целлюлозой и натриевой солью карбоксиметилцеллюлозы и гранулируют со смесью поливинилпирролидона в воде. Гранулят смешивают со стеаратом магния, добавляют добавки корригентов и заполняют в пакеты-саше.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Приведенные ниже примеры предложены для иллюстрации изобретения. Их не следует рассматривать как ограничивающие объем изобретения, но исключительно в качестве репрезентативных примеров.
Общая часть
Сокращения
Boc - трет-Бутоксикарбонил, DMB - 3,3-диметил-1-бутенил, DCM - дихлорметан, EDC⋅HCl - N-(3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорид, EtOAc - этилацетат, HCl - хлористый водород, ВЭЖХ - высокоэффективная жидкостная хроматография, LDA - литийдиизопропиламид, МС - масс-спектр, ТГФ - тетрагидрофуран и Т3Р - 2,4,6-трипропил-1,3,5,2,4,6-триоксатрифосфоринан-2,4,6-триоксид.
ЯМР: спектры 1Н ЯМР записывали на спектрометре Bruker АС-300 при 25°C с ТМС (тетраметилсиланом) или остаточным 1Н данных дейтерированных растворителей в качестве внутренних стандартов.
МС: Масс-спектры (МС) измеряли методом положительного или отрицательного ионного распыления (ISP или ISN) на Perkin-Elmer SCIEX API 300, либо методом электронного удара (EI, 70 эВ) на спектрометре Finnigan MAT SSQ 7000.
Данные ЖХ-МС (ESI, положительные или отрицательные ионы) регистрировали в системах Waters UPLC-MS, оборудованных Waters Acquity, автосэмплером СТС PAL и одиночным квадрупольным масс-спектрометром Waters SQD с использованием ионизационных мод ES (положительных и/или отрицательных). Разделение достигали на колонке Zorbax Eclipse Plus С18 1,7 мкм 2,1×30 мм при 50°С; А - 0,01% муравьиная кислота в воде, В - ацетонитрил при потоке 1; градиент: 0 мин 3% В, 0,2 мин 3% В, 2 мин 97% В, 1,7 мин 97% В, 2,0 мин 97% В. Объем инъекции составлял 2 мкл. МС (ESI, положительный или отрицательный ион): FIA (анализ впрыскивания потока)-МС регистрировали на масс-спектрометре AppliedBiosystem API150. Введение образца выполняли с помощью автосэмплера СТС PAL и насоса Shimadzu LC-10ADVP. Образцы непосредственно вводили в источник ESI масс-спектрометра с потоком 50 мкл/мин смеси ацетонитрила и 10 мМ ацетата аммония (1:1) без колонки. Объем инъекции составлял 2 мкл.
Синтез соединений Примеров
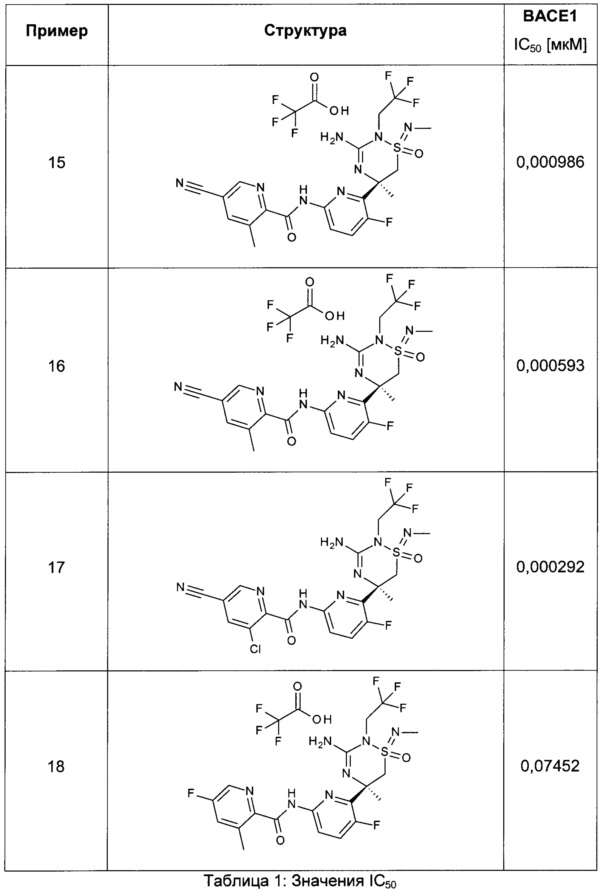
Пример 1: Соль 2,2,2-трифторуксусной кислоты и (1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина
а) N-(2,2,2-трифторэтил)метансульфинамид

К раствору 2,2,2-трифторэтиламина (3,02 г, 2,41 мл, 30,4 ммоль, экв: 3) в диэтиловом эфире (40 мл) добавляли по каплям при -78°С раствор метансульфинхлорида (1,0 г, 10,1 ммоль, экв: 1,00)(CAS 676-85-7) в диэтиловом эфире (5 мл). После полного добавления образовывался белый осадок. Реакционную смесь оставляли нагреваться до 0°С и перемешивали при этой температуре в течение 2 ч. Через 2 ч перемешивания при комнатной температуре реакция была завершена. Белый осадок отфильтровывали и полученный фильтрат выпаривали при 30°С с получением N-(2,2,2-трифторэтил)метансульфинамида в виде бесцветной жидкости (1,52 г; 93%). МС: m/z составляет 162,0 [М+Н]+
b) 1-(2,4-диметоксифенил)-N-метил-N-[S-метил-N-(2,2,2-трифторэтил)-сульфонимидоил]метанамин
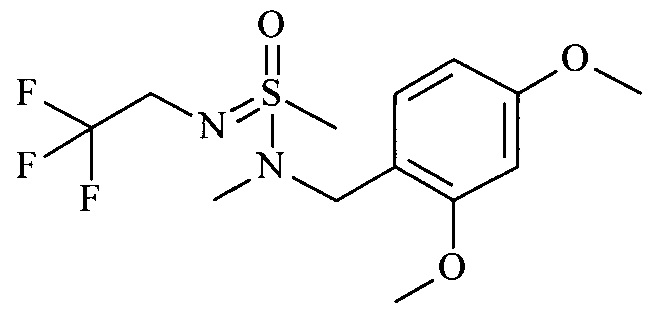
Предупреждение: t-BuOCl является светочувствительным (работать в темноте) и бурно реагирует с резиной, не использовать резиновую прокладку!
К перемешиваемому раствору N-(2,2,2-трифторэтил)метансульфинамида (1,5 г, 9,31 ммоль, экв: 1,00) в сухом тетрагидрофуране (ТГФ) (50 мл) при -78°С быстро добавляли трет-бутилгипохлорит (1,06 г, 1,11 мл, 9,77 ммоль, экв: 1,05) и смесь перемешивали при -78°С в течение 10 мин. К реакционной смеси добавляли по каплям 1-(2,4-диметоксифенил)-N-метилметанамин (2,02 г, 11,2 ммоль, экв: 1,2) (CAS 102503-23-1) в ТГФ (10 мл) при -78°С, затем триэтиламин (1,88 г, 2,59 мл, 18,6 ммоль, экв: 2,0), и перемешивали при -78°С в течение 10 мин. Охлаждающую баню заменяли на ледяную баню и смесь перемешивали при 0°С в течение 1 ч, затем при 22°С в течение 30 мин. Добавляли насыщенный водный раствор бикарбоната натрия (NaHCO3) и перемешивали при комнатной температуре в течение 10 мин. После этого смесь осторожно выливали в 1Н водный раствор HCl, разбавляли этилацетатом и фазы разделяли. Органический слой промывали солевым раствором, сушили над сульфатом натрия (Na2SO4), фильтровали и выпаривали досуха. Сырой материал очищали флэш-хроматографией (силикагель, 40 г, от 25% до 60% этилацетата (EtOAc) в гептане) с получением указанного в заголовке соединения в виде белого твердого вещества (2,56 г; 80,8%). МС (ESI): m/z составляет 341,2 [М+Н]+
с) (S,Е)-N-(1-(6-Бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)этилиден)-2-метилпропан-2-сульфинамид
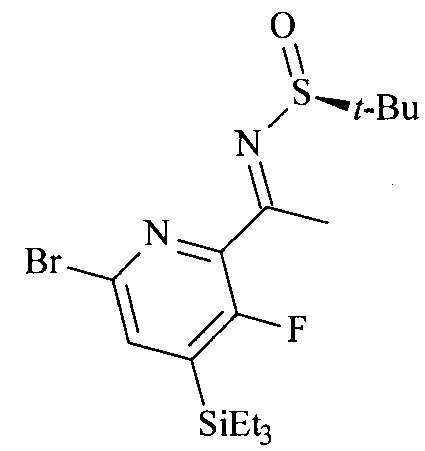
К раствору 1-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)этанона, полученного согласно Badiger, S. et al., межд. патентная публикация WO 2012095469 А1, (8,13 г) в ТГФ (59 мл) добавляли последовательно при 22°С (S)-(-)-трет-бутилсульфинамид (3,26 г) и титан(IV)этоксид (11,2 г) и раствор перемешивали при 60°С в течение 6 ч. Смесь охлаждали до 22°С, обрабатывали солевым раствором, суспензию перемешивали в течение 10 мин и фильтровали через дикалит. Слои разделяли, водный слой экстрагировали этилацетатом, объединенные органические слои промывали водой, сушили и выпаривали. Остаток очищали флэш-хроматографией (SiO2, н-гептан/EtOAc, 5:1) с получением указанного в заголовке соединения (7,5 г, 70%) в виде желтого масла. МС (ESI): m/z составляет 435,3, 437,3 [М+Н]+.
d) N-[(1R)-1-(6-бром-3-фтор-4-триэтилсилил-2-пиридил)-2-[S-[(2,4-диметоксифенил)метил-метил-амино]-N-(2,2,2-трифторэтил)сульфонимидоил]-1-метил-этил]-2-метил-пропан-2-сульфинамид
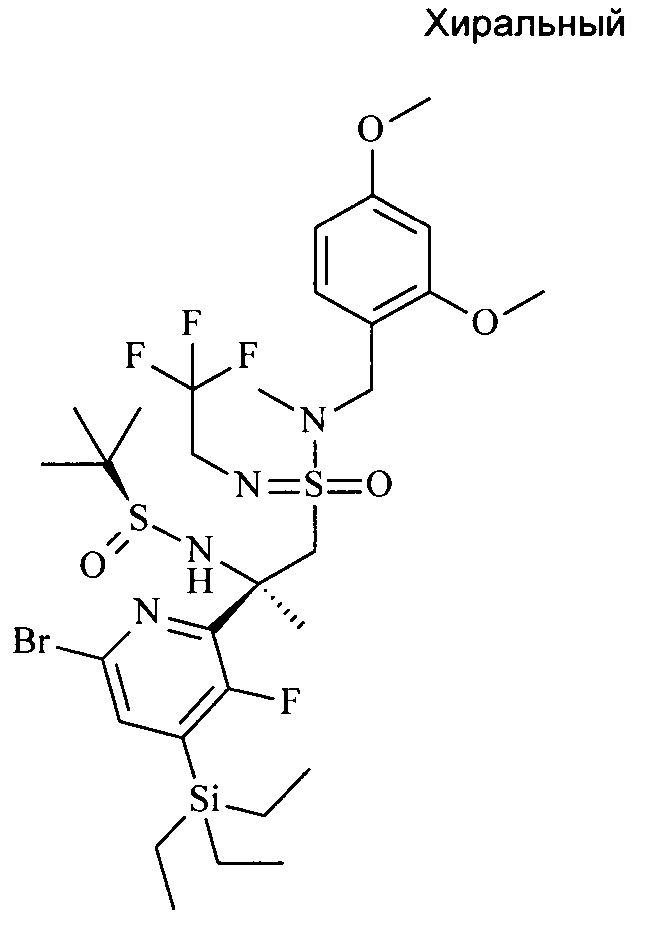
К раствору 1-(2,4-диметоксифенил)-N-метил-N-[S-метил-N-(2,2,2-трифторэтил)-сульфонимидоил]метанамина (пример 1b) (7,97 г, 23,4 ммоль, экв: 1,4) в ТГФ (100 мл) при -78°С добавляли n-BuLi (1,6М в гексане) (20,7 мл, 33,1 ммоль, экв: 1,98) по каплям. Прозрачный раствор перемешивали при -78°С/-40°С в течение 2,5 ч (Реакционную смесь через 1 ч оставляли до -40°С, перемешивали при этой температуре в течение 0,5 ч и затем при -78°С в течение оставшегося времени). Раствор (S,Е)-N-(1-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)этилиден)-2-метилпропан-2-сульфинамида (пример 1с) (7,28 г, 16,7 ммоль, экв: 1,00) в ТГФ (50 мл) добавляли по каплям таким образом, чтобы температура оставалась между -78°С и -73°С. Реакционную смесь перемешивали при -78°С в течение 3 ч, затем гасили при -78°С водным насыщенным раствором хлорида аммония (NH4Cl) (80 мл) и водой (100 мл), затем экстрагировали AcOEt (3×500 мл). Объединенные органические экстракты промывали солевым раствором, сушили над Na2SO4, фильтровали и выпаривали с получением коричневатого масла. Сырой материал очищали флэш-хроматографией (силикагель, 120 г, от 10% до 50% EtOAc в гептане) с получением указанного в заголовке соединения в виде бесцветного вязкого масла (2,14 г; 17%). МС (ESI): m/z=[М+Н]+. 1Н ЯМР (300 МГц, хлороформ-d) 0,77-1,05 (m, 15 Н) 1,16-1,32 (m, 9 Н) 1,92 (s, 3 Н) 2,78 (s, 3 Н) 3,22-3,71 (m, 2 Н) 3,82 (6 Н) 3,92 (d, J=14,33 Гц, 1 Н) 4,14 (d, J=14,13 Гц, 1 Н) 4,24-4,29 (d, 1 Н) 4,39-4,44 (d, 1 Н) 5,81 (s, 1 Н) 6,51 (m, 2 Н) 6,45-6,51 (m, 2 Н) 7,15-7,23 (m, 1 Н) 7,30-7,44 (m, 1 Н) 7,38 (d, 1 Н).
е) (2R)-2-(6-бром-3-фтор-4-триэтилсилил-2-пиридил)-1-[S-[(2,4-диметоксифенил)метил-метил-амино]-N-(2,2,2-трифторэтил)сульфонимидоил]propan-2-амин

К перемешиваемому раствору примера 1d) (2,1 г, 2,71 ммоль, экв: 1,00) в ТГФ (20 мл) добавляли раствор HCl (37% в water) (1,33 г, 1,11 мл, 13,5 ммоль, экв: 5) при 25°С и перемешивали в течение 2 ч. Сырую смесь выпаривали и остаток экстрагировали смесью AcOEt (250 мл)/насыщенный водный раствор NaHCO3 (100 мл), водный слой снова экстрагировали EtOAc (3×100 мл). Органические слои объединяли, промывали насыщенным водным раствором NaCl (1×100 мл), сушили над сульфатом натрия (MgSO4) и концентрировали в вакууме с получением указанного в заголовке соединения в виде бесцветного вязкого масла (1,75 г; 96%). МС (ESI): m/z составляет 673,2 [М+Н]+.
f) (2R)-2-(6-бром-3-фтор-4-триэтилсилил-2-пиридил)-1-[S-(метиламино)-N-(2,2,2-трифторэтил)сульфонимидоил]пропан-2-амин
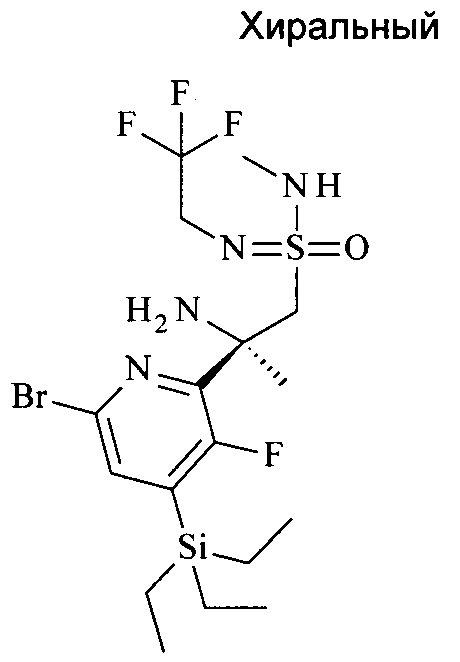
К перемешиваемому раствору примера 1е) (1,75 г, 2,61 ммоль, экв: 1,00) в дихлорметане (10 мл) добавляли при 25°С TFA (14,9 г, 10,0 мл, 130 ммоль, экв: 50). Смесь перемешивали в течение 1 ч. После добавления трифторуксусной кислоты (TFA) и перемешивания в течение приблизительно 15 мин образовывался ярко-розовый раствор. Реакционную смесь доводили ледяным водным раствором 10% Na2CO3 (80 мл) до pH равен 8-9, экстрагировали дихлорметаном (250 мл), водный слой снова экстрагировали дихлорметаном (3×100 мл). Органические слои объединяли, промывали солевым раствором (1×100 мл), сушили над MgSO4 и концентрировали в вакууме с получением светло-желтого воскообразного твердого вещества (1,4 г; 100%). МС (ESI): m/z составляет 523,1 [М+Н]+.
g) N-[[(1R)-1-(6-бром-3-фтор-4-триэтилсилил-2-пиридил)-1-метил-2-[S-(метиламино)-N-(2,2,2-трифторэтил)сульфонимидоил]этил]карбамотиоил]-бензамид


В круглодонной колбе на 10 мл объединяли (2R)-2-амино-2-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)-N-метил-N'-(2,2,2-трифторэтил)пропан-1-сульфонимидамид (пример 1f), 0,205 г, 393 мкмоль, экв: 1,00) с ТГФ (2,4 мл) с получением светло-желтой разбавленной суспензии. Добавляли бензоилизотиоцианат (70,6 мг, 58,1 мкл, 432 мкмоль, экв: 1,1) и темно-желтую суспензию перемешивали при комнатной температуре в течение 1,5 ч. Реакционную смесь разбавляли метанолом (МеОН) (1 мл) и полученный осадок отфильтровывали, полученный фильтрат выпаривали. Сырой материал последовательно очищали флэш-хроматографией (силикагель, 12 г, 0% до 40% EtOAc в н-гептане) с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (214 мг; 79%). МС (ESI): m/z составляет 682,3 [М+Н]+.
h) N-[(1R,5R)-5-(6-бром-3-фтор-4-триэтилсилил-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]бензамид и N-[(1S,5R)-5-(6-бром-3-фтор-4-триэтилсилил-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]бензамид

К раствору N-((2R)-2-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)-1-(N-метил-N'-(2,2,2-трифторэтил)сульфамимидоил)пропан-2-илкарбамотиоил)-бензамида (пример 1g), 0,210 г, 307 мкмоль, экв: 1,00) в ацетонитриле (2,9 мл) добавляли при комнатной температуре N-1-((этилимино)метилен)-N,N-диметилпропан-1,3-диамин (EDC) (71,4 мг, 81,4 мкл, 460 мкмоль, экв: 1,5) и перемешивали при 80°С в течение 1,5 ч. Светло-желтый раствор выпаривали. Сырой материал очищали флэш-хроматографией (силикагель, 12 г, от 0% до 40% EtOAc в н-гептане) с получением указанных в заголовке соединений в виде бесцветных аморфных твердых веществ в виде смеси диастереомеров (80 мг; 40%; N-[(1R,5R)-5-(6-бром-3-фтор-4-триэтилсилил-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]бензамид и 102 мг; 51% N-[(1S,5R)-5-(6-бром-3-фтор-4-триэтилсилил-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]бензамид). МС (ESI): m/z составляет 652,2 [М+Н]+.
i) N-[(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]бензамид
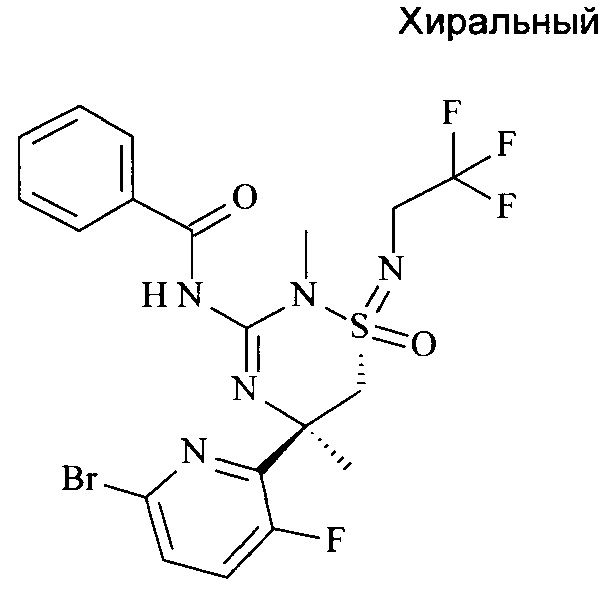
К раствору N-[(1R,5R)-5-(6-бром-3-фтор-4-триэтилсилил-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]бензамида (пример 1h), 0,08 г, 123 мкмоль, экв: 1,00) в сухом ТГФ (0,8 мл) и DMF (0,8 мл) добавляли при комнатной температуре уксусную кислоту (14,8 мг, 14,1 мкл, 246 мкмоль, экв: 2) и фторид натрия (14,3 мг, 246 мкмоль, экв: 2) и полученную белую суспензию перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь выпаривали, остаток экстрагировали смесью AcOEt (20 мл)/водный насыщенный раствор NaHCO3 (5 мл). Водный слой снова экстрагировали EtOAc (3×15 мл). Органические слои объединяли, промывали насыщ. NaCl (1×5 мл), сушили над Na2SO4 и концентрировали в вакууме с получением указанного в заголовке соединения в виде белого твердого вещества (0,06 г; 91%). МС (ESI): m/z составляет 538,1 [М+Н]+.
j) трет-бутил N-[(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]карбамат
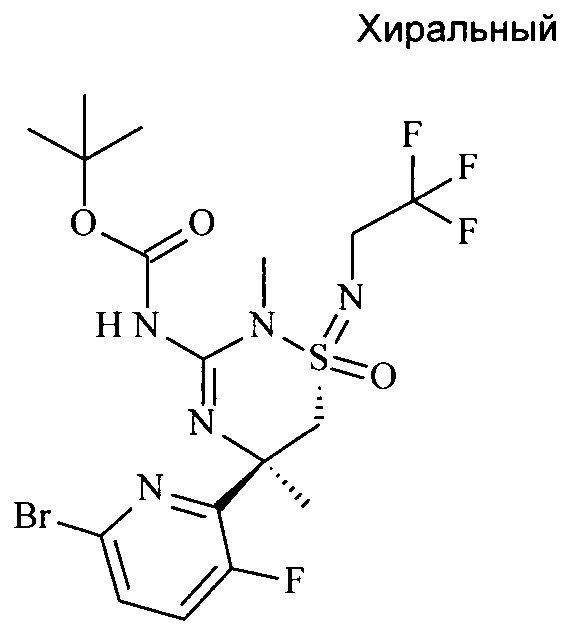
1) К перемешиваемому раствору N-[(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]бензамида (пример 1i), 0,060 г, 112 мкмоль, экв: 1,00) в ТГФ (800 мкл) добавляли при комнатной температуре триэтиламин (24,9 мг, 34,3 мкл, 246 мкмоль, экв: 2,2) и 4-(диметиламино)-пиридинил (DMAP) (2,73 мг, 22,4 мкмоль, экв: 0,2), затем добавляли Boc2O (53,7 мг, 246 мкмоль, экв: 2,2). Реакционную смесь перемешивали в течение 3 ч. Темно-желтую сырую реакционную смесь выпаривали досуха.
Остаток растворяли в метаноле (500 мкл) и добавляли аммиак (7Н в МеОН) (799 мкл, 5,59 ммоль, экв: 50) при комнатной температуре. Полученный светло-коричневый раствор перемешивали в течение 15 мин. Реакционную смесь выпаривали и последовательно очищали флэш-хроматографией (силикагель, 4 г, от 0% до 30% EtOAc в н-гептане) с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (0,043 г; 72%). МС (ESI): m/z составляет 534,1 [М+Н]+.
k) Соль (1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина и 2,2,2-трифторуксусной кислоты
К перемешиваемому раствору трет-бутил-N-[(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]карбамата (пример 1j); 0,002 г, 3,76 мкмоль, экв: 1,00) в дихлорметане (60 мкл) добавляли при комнатной температуре TFA (85,7 мг, 57,9 мкл, 751 мкмоль, экв: 200) и перемешивали в течение 2 ч. Реакционную смесь концентрировали в вакууме с получением указанного в заголовке соединения в виде аморфного, бесцветного твердого вещества (2,18 мг; 106%). МС (ESI): m/z составляет 434,1 [М+Н]+.
Пример 2: Соль (1S,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина и 2,2,2-трифторуксусной кислоты
Соединение Примера 2 получали из N-[(1S,5R)-5-(6-бром-3-фтор-4-триэтилсилил-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]бензамида (пример 1h) аналогично способам, описанным в примерах 1i-k) с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (3,32 мг; 100%). МС (ESI): m/z составляет 434,1 [М+Н]+.
Пример 3: Соль N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фтор-2-пиридил]-5-циано-3-метил-пиридин-2-карбоксамида и 2,2,2-трифторуксусной кислоты
трет-Бутил N-[(1R,5R)-5-(6-амино-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]карбамат
В круглодонной колбе на 10 мл соединение примера 1k) (0,075 г, 141 мкмоль, экв: 1,00) объединяли с диоксаном (350 мкл) и водой (100 мкл) с получением бесцветного раствора. К этому раствору добавляли при 25°С азид натрия (73,3 мг, 1,13 ммоль, экв: 8), иодид меди (I) (10,7 мг, 56,4 мкмоль, экв: 0,4), аскорбат натрия (11,2 мг, 56,4 мкмоль, экв: 0,4), затем транс-N,N'-диметилциклогексан-1,2-диамин (12,0 мг, 13,3 мкл, 84,5 мкмоль, экв: 0,6). Темно-зеленую реакционную смесь нагревали до 70°С и перемешивали в течение 45 мин. Реакционную смесь гасили водным насыщенным раствором NaHCO3 и экстрагировали 3 раза AcOEt (2 мл). Органический слой объединяли и промывали солевым раствором, сушили над Na2SO4 и концентрировали в вакууме. Сырой материал очищали флэш-хроматографией (силикагель, 4 г, от 5% до 40% EtOAc в н-гептане) с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (51 мг; 77%). МС (ESI): m/z составляет 469,2 [М+Н]+.

а) трет-Бутил N-[(1R,5R)-5-[6-[(5-циано-3-метил-пиридин-2-карбонил)амино]-3-фтор-2-пиридил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]карбамат
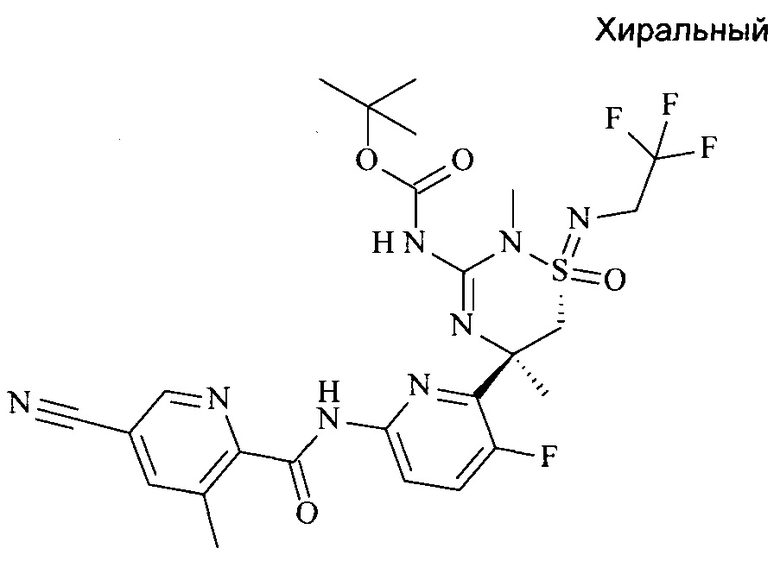
К суспензии 5-циано-3-метилпиколиновой кислоты (1,33 мг, 8,2 мкмоль, экв: 1,2) в дихлорметане (100 мкл) добавляли при 0°С 1-хлор-N,N-2-триметилпроп-1-ен-1-амин (1,14 мг, 1,13 мкл, 8,54 мкмоль, экв: 1,25) и полученную бесцветную суспензию перемешивали при 0°С 20 мин. Раствор трет-бутил-N-[(1R,5R)-5-(6-амино-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]карбамата (3,2 мг, 6,83 мкмоль, экв: 1,00) в дихлорметане (146 мкл) добавляли к указанной реакционной смеси при 0°С и полученный желтый раствор перемешивали при комнатной температуре в течение 60 мин. Реакционную смесь концентрировали в вакууме. Остаток очищали флэш-хроматографией (4 г силикагеля, изократично 40% AcOEt в н-гептане) с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (3,8 мг; 91%). МС (ESI): m/z составляет 613,2 [М+Н]+.
b) Соль N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фтор-2-пиридил]-5-циано-3-метил-пиридин-2-карбоксамида и 2,2,2-трифтор-уксусной кислоты
К перемешиваемому раствору трет-бутил-N-[(1R,5R)-5-(6-амино-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]карбамата (3,8 мг, 6,2 мкмоль, экв: 1,00) в дихлорметане (70 мкл) добавляли при комнатной температуре TFA (106 мг, 71,7 мкл, 930 мкмоль, экв: 150) и перемешивали в течение 30 мин. Реакционную смесь концентрировали в вакууме с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (4,05 мг; 100%). МС (ESI): m/z составляет 513,2 [М+Н]+.
Пример 4: Соль N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фтор-2-пиридил]-5-циано-пиридин-2-карбоксамида и 2,2,2-трифторуксусной кислоты
Соединение Примера 4 получали аналогично способам, описанным для примера 3, используя в качестве исходного вещества 5-цианопиколиновую кислоту, с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (11,8 мг; 100%). МС (ESI): m/z составляет 499,2 [М+Н]+.
Пример 5: Соль N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-фтор-3-метилпиридин-2-карбоксамида и 2,2,2-трифторуксусной кислоты
Соединение Примера 5 получали аналогично способам, описанным для примера 3, используя в качестве исходного вещества 5-фтор-2-метилпиколиновую кислоту, с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (16,6 мг; 100%). МС (ESI): m/z составляет 506,3 [М+Н]+.
Пример 6: Соль N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-(фторметокси)пиридин-2-карбоксамида и 2,2,2-трифторуксусной кислоты
Соединение Примера 6 получали аналогично способам, описанным для примера 3, используя в качестве исходного вещества 5-(фторметокси)пиридин-2-карбоновую кислоту, с получением указанного в заголовке соединения в виде светло-коричневого аморфного твердого вещества (16,6 мг; 100%). МС (ESI): m/z составляет 522,2 [М+Н]+.
Пример 7: Соль N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-бут-2-иноксипиразин-2-карбоксамида и 2,2,2-трифторуксусной кислоты
Соединение Примера 7 получали аналогично способам, описанным для примера 3, используя в качестве исходного вещества 5-бут-2-иноксипиразин-2-карбоновую кислоту, с получением указанного в заголовке соединения в виде светло-коричневого аморфного твердого вещества (11,9 мг; 100%). МС (ESI): m/z составляет 543,2 [М+Н]+.
Пример 8: Соль N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-метоксипиразин-2-карбоксамида и 2,2,2-трифторуксусной кислоты
Соединение Примера 8 получали аналогично способам, описанным для примера 3, используя в качестве исходного вещества 5-метоксипиразин-2-карбоновую кислоту, с получением указанного в заголовке соединения в виде светло-коричневого аморфного твердого вещества (13,1 мг; 100%). МС (ESI): m/z составляет 505,2 [М+Н]+.
Пример 9: Соль N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-(2,2,2-трифторэтокси)пиридин-2-карбоксамида и 2,2,2-трифторуксусной кислоты
Соединение Примера 9 получали аналогично способам, описанным для примера 3, используя в качестве исходного вещества 5-(2,2,2-трифторэтокси)пиридин-2-карбоновую кислоту, с получением указанного в заголовке соединения в виде светло-коричневого аморфного твердого вещества (3,92 мг; 95%). МС (ESI): m/z составляет 572,1 [М+Н]+.
Пример 10: Соль N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-проп-2-иноксипиридин-2-карбоксамида и 2,2,2-трифторуксусной кислоты
Соединение Примера 10 получали аналогично способам, описанным для примера 3, используя в качестве исходного вещества 5-проп-2-иноксипиридин-2-карбоновую кислоту, с получением указанного в заголовке соединения в виде светло-коричневого аморфного твердого вещества (31 мг; 100%). МС (ESI): m/z составляет 528,2 [М+Н]+.
Пример 11: (1R,5R)-5-[3-фтор-6-(1Н-пиразол-5-ил)пиридин-2-ил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амин
В микроволновой (MW) пробирке объединяли трет-бутил-N-[(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]карбамат (пример 1j) (30 мг, 56,4 мкмоль, экв: 1,00) с ацетонитрилом (340 мкл) и водой (340 мкл) с получением бесцветного раствора. Добавляли ацетат натрия (16,6 мг, 169 мкмоль, экв: 3,00) и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол (13,1 мг, 67,6 мкмоль, экв: 1,2) с получением суспензии и затем добавляли в атмосфере азота тетракис(трифенилфосфин)палладий (0) (6,51 мг, 5,64 мкмоль, экв: 0,1). MW-пробирку закрывали и нагревали в микроволновой печи при 140°С в течение 20 мин. Реакционную смесь очищали препаративной ВЭЖХ с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (5,14 мг; 22%). МС (ESI): m/z составляет 420,2 [М+Н]+.
Пример 12: (1R,5R)-5-[6-(5-хлортиофен-2-ил)-3-фторпиридин-2-ил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амин
В микроволновой пробирке объединяли трет-бутил-N-[(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-ил]карбамат (пример 1j) (30 мг, 56,4 мкмоль, экв: 1,00) с диоксаном (340 мкл) и водой (340 мкл) с получением бесцветного раствора. Добавляли тринатрийфосфат (35,9 мг, 169 мкмоль, экв: 3) и 5-хлортиофен-2-илбороновую кислоту (11,0 мг, 67,6 мкмоль, экв: 1,2) с получением суспензии и затем в атмосфере азота - комплекс 2'-(диметиламино)-2-бифенилпалладия(II) хлорида и динорборнилфосфина (3,16 мг, 5,64 мкмоль, экв: 0,1). MW-пробирку закрывали и нагревали в микроволновой печи при 120°С в течение 300 мин. Сырую реакционную смесь очищали препаративной ВЭЖХ с получением указанного в заголовке соединения в виде светло-желтого твердого вещества (8,39 мг; 32%). МС (ESI): m/z составляет 570,1 [М+Н]+.
Пример 13: N-[6-[3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида;2,2,2-трифторуксусная кислота
а) N-[(2,4-диметоксифенил)метил]-N-(N,S-диметилсульфонимидоил)-2,2,2-трифтор-этанамин

К перемешиваемому раствору метансульфиновой кислоты метиламида (CAS 18649-17-7) (2,4 г, 25,806 ммоль) в ТГФ (30 мл) при 0°С tBuOCl (4,3 мл, 38,71 ммоль) добавляли по каплям в темноте и перемешивали реакционную смесь в течение 2 ч при той же температуре. К этой смеси добавляли (2,4-диметокси-бензил)-(2,2,2-трифтор-этил)-амин (CAS 1016734-11-4) (8,3 г, 33,548 ммоль) и Cs2CO3 (18,2 г, 51,613 ммоль) соответственно и перемешивали раствор в течение 16 ч при 25°С. Реакцию гасили водой и экстрагировали дихлорметаном (3 раза). Объединенные органические слои промывали солевым раствором, сушили над безводным Na2SO4, выпаривали при пониженном давлении с получением сырого продукта, который очищали колоночной хроматографией на силикагеле с использованием 0-25% EtOAc-гексан в качестве элюирующего агента с получением N-[(2,4-диметоксифенил)метил]-N-(N,S-диметилсульфонимидоил)-2,2,2-трифтор-этанамина в виде бесцветной жидкости (2 г, 22,8%). m/z составляет 341,2 [М+Н]+.
b) N-[2-(6-бром-3-фтор-4-триэтилсилилпиридин-2-ил)-1-[S-[(2,4-диметоксифенил)метил-(2,2,2-трифторэтил)амино]-N-метилсульфонимидоил]пропан-2-ил]-2-метилпропан-2-сульфинамид; смесь диастереомеров

К раствору N-(2,4-диметоксибензил)-N'-метил-N-(2,2,2-трифторэтил)-метансульфонимидамида (2,08 г, 6,11 ммоль, экв: 1,4) в ТГФ (24 мл) при -78°С добавляли н-бутиллитий (1,6Н в гексане) (5,4 мл, 8,64 ммоль, экв: 1,98) по каплям. Прозрачный раствор перемешивали при -78°С/-40°С в течение 2,5 ч (Реакционную смесь оставляли нагреваться в течение 1 часа до -40°С, перемешивали при этой температуре в течение 0,5 ч и затем при -78°С в течение оставшегося времени). Раствор (S,Z)-N-(1-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)этилиден)-2-метилпропан-2-сульфинамида (1,9 г, 4,36 ммоль, экв: 1) в ТГФ (10 мл) добавляли по каплям (так, чтобы температура оставалась между -78°С и -73°С). Реакционную смесь перемешивали при -78°С в течение 3 ч, затем гасили при -78°С 20 мл насыщенного водного раствора NH4Cl и 30 мл воды, затем экстрагировали AcOEt (3×150 мл). Объединенные органические экстракты промывали солевым раствором, сушили над Na2SO4, фильтровали и выпаривали с получением коричневатого масла. Сырой материал очищали флэш-хроматографией (силикагель, 80 г, от 10% до 50% EtOAc в гептане) дважды с получением указанного в заголовке соединения «вещества А» (68 мг; 2%) и указанного в заголовке соединения «вещества В» (236 мг; 7%). m/z составляет 777,199 [М+Н]+.
«Вещество А»: 1Н ЯМР (300 МГц, хлороформ-d) δ ppm 0,82-1,01 (m, 17 Н) 0,83-0,84 (m, 1 Н) 1,31-1,33 (m, 1 Н) 1,35 (s, 9 Н) 1,85 (s, 3 Н) 2,47 (s, 3 Н) 3,80 (s, 1 Н) 3,82 (s, 3 Н) 3,83 (s, 3 Н) 4,44 (s, 2 Н) 6,45-6,48 (m, 2 Н) 6,45-6,48 (m, 1 Н) 6,46-6,51 (m, 2 Н) 7,22 (d, J=8,07 Гц, 1 Н) 7,30 (d, J=2,62 Гц, 1 Н) 7,36 (s, 1 Н)
«Вещество В»: 1Н ЯМР (300 МГц, хлороформ-d) δ ppm 0,83-0,97 (m, 15 Н) 0,84-0,98 (m, 15 Н) 1,18-1,30 (m, 11 Н) 1,23-1,23 (m, 1 Н) 1,23-1,23 (m, 1 Н) 1,23-1,24 (m, 2 Н) 2,52-2,58 (m, 3 Н) 3,11 (d, J=13,72 Гц, 1 Н) 3,65-3,76 (m, 1 Н) 3,78-3,83 (m, 6 Н) 3,86-3,98 (m, 1 Н) 4,35-4,43 (m, 1 Н) 4,45-4,57 (m, 1 Н) 6,44-6,49 (m, 2 Н) 6,56-6,57 (m, 1 Н) 6,58 (s, 1 Н) 7,22 (d, J=8,07 Гц, 1 Н) 7,33 (d, J=2,62 Гц, 1 Н)
с) 2-Амино-2-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)-N'-метил-N-(2,2,2-трифторэтил)пропан-1-сульфонимидамид
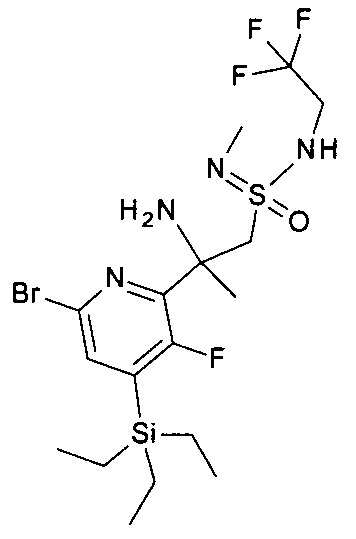
К перемешиваемому раствору 2-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)-N-(2,4-диметоксибензил)-2-((S)-1,1-диметилэтилсульфинамидо)-N'-метил-N-(2,2,2-трифторэтил)пропан-1-сульфонимидамида (0,1 г, 129 мкмоль, экв: 1) в ТГФ (0,5 мл) добавляли HCl (37% в воде) (63,5 мг, 52,9 мкл, 644 мкмоль, экв: 5) при комнатной температуре и перемешивали в течение 1 ч. Сырую смесь выпаривали и остаток экстрагировали 10 мл AcOEt/3 мл насыщенного водного раствора NaHCO3, водный слой снова экстрагировали EtOAc (3×10 мл). Органические слои объединяли, промывали насыщенным водным раствором NaCl (1×3 мл), сушили над MgSO4 и концентрировали в вакууме с получением указанного в заголовке соединения в виде светло-желтой смолы (88 мг сырой). m/z составляет 523,2 [М+Н]+.
d) N-[[2-(6-Бром-3-фтор-4-триэтилсилилпиридин-2-ил)-1-[N-метил-S-(2,2,2-трифторэтиламино)сульфонимидоил]пропан-2-ил]карбамотиоил]бензамид

В колбе на 10 мл объединяли 2-амино-2-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)-N'-метил-N-(2,2,2-трифторэтил)пропан-1-сульфонимидамид (0,067 г, 128 мкмоль, экв: 1) с ТГФ (800 мкл) с получением светло-желтого раствора. Добавляли бензоилизотиоцианат (23,1 мг, 19 мкл, 141 мкмоль, экв: 1,1) и желтый раствор перемешивали при 25°С в течение 1,5 ч. Реакционную смесь выпаривали. Сырой материал очищали последовательно флэш-хроматографией (силикагель, 4 г, 10% до 40% EtOAc в гептан) с получением указанного в заголовке соединения в виде светло-желтого аморфного твердого вещества (44 мг; 50%). m/z составляет 684,3 [М+Н]+.
е) N-[(1R)-5-(6-6ром-3-фтор-4-триэтилсилилпиридин-2-ил)-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-3-ил]бензамид и N-[(1S)-5-(6-бром-3-фтор-4-триэтилсилилпиридин-2-ил)-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-3-ил]бензамид (смесь диастереомеров)
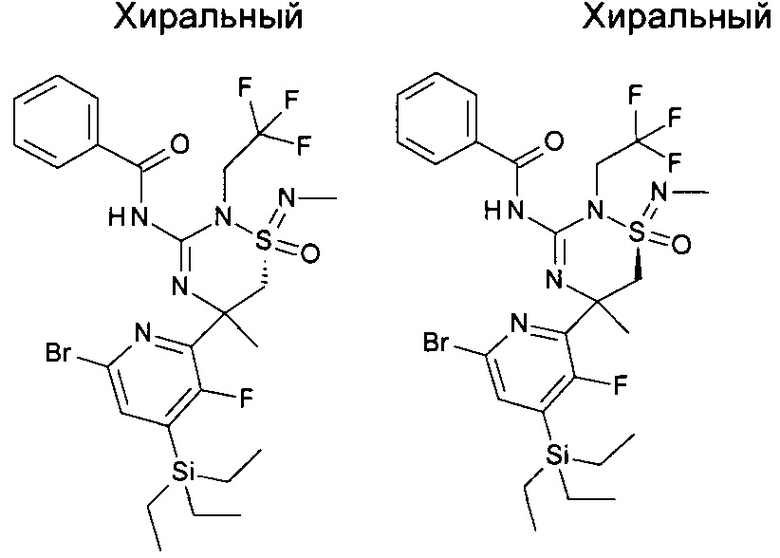
К раствору N-[[2-(6-Бром-3-фтор-4-триэтилсилилпиридин-2-ил)-1-[N-метил-S-(2,2,2-трифторэтиламино)сульфонимидоил]пропан-2-ил]карбамотиоил]бензамида в ацетонитриле (0,7 мл) добавляли при комнатной температуре N-1-((этилимино)метилен)-N3,N3-диметилпропан-1,3-диамин (14,3 мг, 16,3 мкл, 92 мкмоль, экв: 1,5) и смесь перемешивали при 80°С в течение 1,5 ч. Светло-желтый раствор выпаривали. Сырой материал очищали флэш-хроматографией (силикагель, 4g, 0% до 40% EtOAc в гептане) с получением указанных в заголовке соединений в виде бесцветного аморфного твердого вещества (22 мг; 55% и 10 мг; 25%). m/z составляет 653,4 [М+Н]+.
f) N-[5-(6-бром-3-фторпиридин-2-ил)-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-3-ил]бензамид
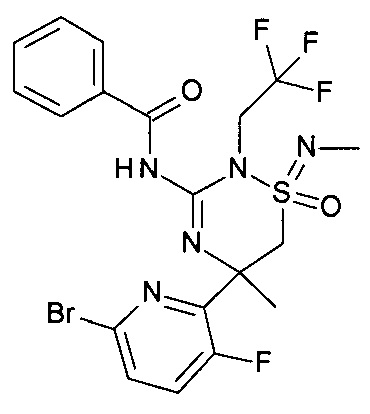
К раствору N-(5-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)-5-метил-1-(метилимино)-1-оксидо-2-(2,2,2-трифторэтил)-5,6-дигидро-2Н-1,2,4-тиадиазин-3-ил)бензамида (0,180 г, 277 мкмоль, экв: 1) в сухом ТГФ (1,8 мл) и DMF (1,8 мл) добавляли при 25°С уксусную кислоту (33,2 мг, 31,6 мкл, 553 мкмоль, экв: 2) и фторид натрия (32,1 мг, 553 мкмоль, экв: 2) и полученную белую суспензию перемешивали при 25°С в течение 1 ч. Реакционную смесь выпаривали, остаток экстрагировали 7 мл AcOEt/3 мл водного насыщенного раствора NaHCO3. Водный слой снова экстрагировали EtOAc (3×5 мл). Органические слои объединяли, промывали насыщ. NaCl (1×5 мл), сушили над Na2SO4 и концентрировали в вакууме с получением указанного в заголовке соединения в виде белого твердого вещества (72 мг; 49%). m/z составляет 538,2 [М+Н]+.
g) трет-бутил-N-[5-(6-бром-3-фторпиридин-2-ил)-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-3-ил]карбамат
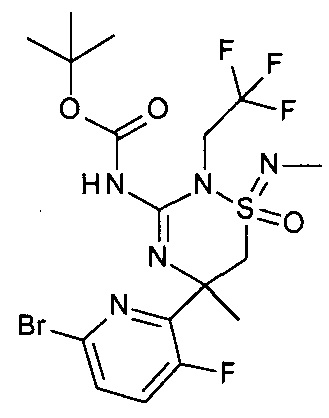
К перемешиваемому раствору N-(5-(6-бром-3-фторпиридин-2-ил)-5-метил-1-(метилимино)-1-оксидо-2-(2,2,2-трифторэтил)-5,6-дигидро-2Н-1,2,4-тиадиазин-3-ил)бензамида (0,085 г, 158 мкмоль, экв: 1) в ТГФ (1,0 мл) добавляли при 25°С триэтиламин (35,3 мг, 48,6 мкл, 349 мкмоль, экв: 2,2) и DMAP (19,4 мг, 158 мкмоль, экв: 1), затем добавляли ди-трет-бутил-дикарбонат (76,1 мг, 349 мкмоль, экв: 2,2). Реакционную смесь перемешивали в течение 6 ч. Добавляли дополнительный ди-трет-бутил-дикарбонат (34,6 мг, 158 мкмоль, экв: 1), DMAP (3,87 мг, 31,7 мкмоль, экв: 0,2), триэтиламин (16 мг, 22,1 мкл, 158 мкмоль, экв: 1) к реакционной смеси и перемешивали в течение еще 1 ч. Темно-желтую сырую реакционную смесь выпаривали досуха. Остаток растворяли в МеОН (1,0 мл) и добавляли аммиак (7Н в МеОН) (1,13 мл, 7,92 ммоль, экв: 50) при 25°С. Полученный коричневатый раствор перемешивали в течение 25 мин. Реакционную смесь выпаривали и последовательно очищали флэш-хроматографией (силикагель, 4 г, от 0% до 30% EtOAc в гептане) с получением указанного в заголовке соединения в виде бесцветной пены (42 мг; 50%). m/z составляет 534,2 [М+Н]+.
h) трет-Бутил-N-[5-(6-амино-3-фторпиридин-2-ил)-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-3-ил]карбамат

В круглодонной колбе на 10 мл объединяли трет-бутил-(5-(6-бром-3-фторпиридин-2-ил)-5-метил-1-(метилимино)-1-оксидо-2-(2,2,2-трифторэтил)-5,6-дигидро-2Н-1,2,4-тиадиазин-3-ил)карбамат (0,045 г, 84,5 мкмоль, экв: 1) с диоксаном (225 мкл) и водой (90 мкл) с получением бесцветного раствора. К этому раствору добавляли при 25°С азид натрия (44 мг, 676 мкмоль, экв: 8), иодид меди (I) (6,44 мг, 33,8 мкмоль, экв: 0,4), аскорбат натрия (6,7 мг, 33,8 мкмоль, экв: 0,4), затем транс-N,N-диметилциклогексан-1,2-диамин (12 мг, 13,3 мкл, 84,5 мкмоль, экв: 1). Темно-зеленую реакционную смесь нагревали до 70°С и перемешивали в течение 70 мин. Реакционную смесь гасили водным насыщенным раствором NaHCO3 и экстрагировали 3 раза AcOEt. Органические слои объединяли и промывали насыщенным водным раствором NaCl, сушили над Na2SO4 и концентрировали в вакууме. Сырой материал очищали флэш-хроматографией (силикагель, 4 г, от 5% до 40% EtOAc в гептане) с получением указанного в заголовке соединения в виде аморфного твердого вещества (15 мг; 38%). m/z составляет 469,3 [М+Н]+.
i) трет-бутил-N-[5-[6-[(5-циано-3-метилпиридин-2-карбонил)амино]-3-фторпиридин-2-ил]-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-3-ил]карбамат

К суспензии 5-циано-3-метилпиколиновой кислоты (7,89 мг, 48,7 мкмоль, экв: 1,2) в дихлорметане (0,6 мл) добавляли при 0°С 1-хлор-N,N,2-триметилпроп-1-ен-1-амин (реагент Госеза (Ghosez)) (6,77 мг, 6,71 мкл, 50,7 мкмоль, экв: 1,25) и полученный бесцветный раствор перемешивали при 0°С в течение 15 мин. Раствор трет-бутил-(5-(6-амино-3-фторпиридин-2-ил)-5-метил-1-(метилимино)-1-оксидо-2-(2,2,2-трифторэтил)-5,6-дигидро-2Н-1,2,4-тиадиазин-3-ил)карбамата (0,019 г, 40,6 мкмоль, экв: 1) в дихлорметане (800 мкл) добавляли к указанной реакционной смеси при 0°С и полученный желтый раствор оставляли нагреваться до комнатной температуры и перемешивали в течение 60 мин. Реакционную смесь концентрировали в вакууме. Остаток очищали флэш-хроматографией (силикагель, 4 г, изократично 40% AcOEt в н-гептане) с получением указанного в заголовке соединения в виде белого твердого вещества (8,8 мг; 35%). m/z составляет 513,3 [М+Н-Вос]+.
j) N-[6-[3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамид;2,2,2-трифторуксусная кислота
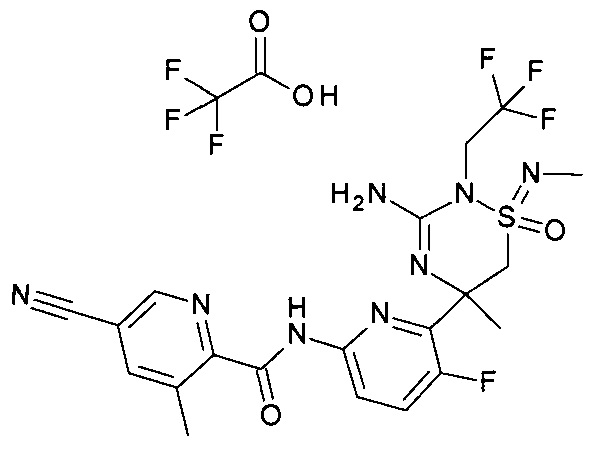
К перемешиваемому раствору трет-бутил-(5-(6-(5-циано-3-метилпиколинамидо)-3-фторпиридин-2-ил)-5-метил-1-(метилимино)-1-оксидо-2-(2,2,2-трифторэтил)-5,6-дигидро-2Н-1,2,4-тиадиазин-3-ил)карбамата (8,8 мг, 14,4 мкмоль, экв: 1) в дихлорметане (110 мкл) добавляли при 25°С TFA (164 мг, 111 мкл, 1,44 ммоль, экв: 100) и перемешивали в течение 30 мин. Реакционную смесь концентрировали в вакууме с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (8,43 мг; 94%). m/z составляет 513,3 [M+H-TFA]+.
Пример 14: (5R)-5-(6-бром-3-фторпиридин-2-ил)-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-3-амин;2,2,2-трифторуксусная кислота
Соединение Примера 14 получали аналогично способам, описанным для примера 13а)-13g) и 13j), используя в качестве исходного вещества (R,Z)-N-(1-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)этилиден)-2-метилпропан-2-сульфинамид с получением указанного в заголовке соединения в виде светло-желтого аморфного твердого вещества. m/z составляет 434,1 [M+H-TFA]+.
Пример 15: N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамид;2,2,2-трифторуксусная кислота ([1 Эпимер][Вещество В])
Указанное в заголовке соединение получали аналогично способам, описанным для примера 13a)-13j), используя в качестве исходного вещества (R,Z)-N-(1-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)этилиден)-2-метилпропан-2-сульфинамид. m/z составляет 434,1 [M+H-TFA]+.
Пример 16: N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамид;2,2,2-трифторуксусная кислота ([1 Эпимер][Вещество С])
Указанное в заголовке соединение получали аналогично способам, описанным для примера 13a)-13j), используя в качестве исходного вещества (R,Z)-N-(1-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)этилиден)-2-метилпропан-2-сульфинамид. m/z составляет 434,1 [M+H-TFA]+.
Пример 17: N-(6-((5R)-3-амино-5-метил-1-(метилимино)-1-оксидо-2-(2,2,2-трифторэтил)-5,6-дигидро-2Н-1,2,4-тиадиазин-5-ил)-5-фторпиридин-2-ил)-3-хлор-5-цианопиколинамид ([1 Эпимер][Вещество С])
Указанное в заголовке соединение получали аналогично способам, описанным для примера 13a)-13j), используя в качестве исходного вещества (R,Z)-N-(1-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)этилиден)-2-метилпропан-2-сульфинамид. m/z составляет 533,1/531,2 [М+Н]+. Cl-Изотопы.
Пример 18: N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-фтор-3-метилпиридин-2-карбоксамид;2,2,2-трифторуксусная кислота ([1 Эпимер][Вещество С])
Указанное в заголовке соединение получали аналогично способам, описанным для примера 13a)-13j), используя в качестве исходного вещества (R,Z)-N-(1-(6-бром-3-фтор-4-(триэтилсилил)пиридин-2-ил)этилиден)-2-метилпропан-2-сульфинамид. m/z составляет 506,2 [M+H-TFA]+.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ БЕТА-СЕКРЕТАЗЫ | 2016 |
|
RU2712272C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ АЗЕТИДИНА | 2013 |
|
RU2629114C2 |
| БЕНЗОКСАЗЕПИНОВЫЕ ИНГИБИТОРЫ PI3K И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2600927C2 |
| БИЦИКЛИЧЕСКИЕ ЛАКТАМЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2827714C1 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ, ПРИМЕНЯЕМЫЕ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, СВЯЗАННЫХ С NTRK | 2016 |
|
RU2744974C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРРОЛИДИНА | 2017 |
|
RU2736498C1 |
| 2,5,6,7-ТЕТРАГИДРО-[1,4]ОКСАЗЕПИН-3-ИЛАМИНЫ ИЛИ 2,3,6,7-ТЕТРАГИДРО-[1,4]ОКСАЗЕПИН-5-ИЛАМИНЫ | 2011 |
|
RU2570796C2 |
| ЗАМЕЩЕННЫЕ ТИОФЕНКАРБОКСАМИДЫ И АНАЛОГИ В КАЧЕСТВЕ АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2019 |
|
RU2799335C2 |
| БИЦИКЛИЧЕСКИЕ КЕТОНЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2797922C2 |
| ИНГИБИТОРЫ МУТАЦИИ HER2 | 2022 |
|
RU2834124C2 |
Изобретение относится к соединению формулы Ia', где R1 представляет собой пиридил или пиразинил, замещенный 1-2 заместителями, индивидуально выбранными из циано, метила, метокси, фторметокси, трифторэтокси, бут-2-инокси и проп-2-инокси; R2 представляет собой 2,2,2-трифторэтил или метил; R3 представляет собой метил; R4 представляет собой метил или -CH2CF3; к или его фармацевтически приемлемой соли, а также к промежуточному соединению формулы I'. Описана также фармацевтическая композиция, ингибирующая ВАСЕ1, на основе соединения формулы Ia'. Технический результат – получены новые соединения и фармацевтические композиции на их основе, которые могут найти применение в медицине для терапевтического и/или профилактического лечения болезни Альцгеймера. 7 н. и 3 з.п. ф-лы, 8 табл., 18 пр.
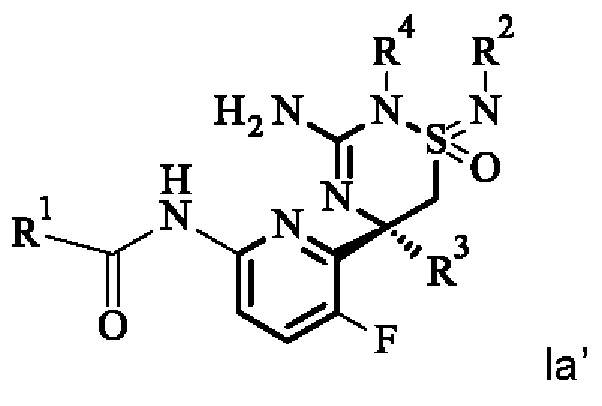 ,
,
1. Соединение формулы Ia'
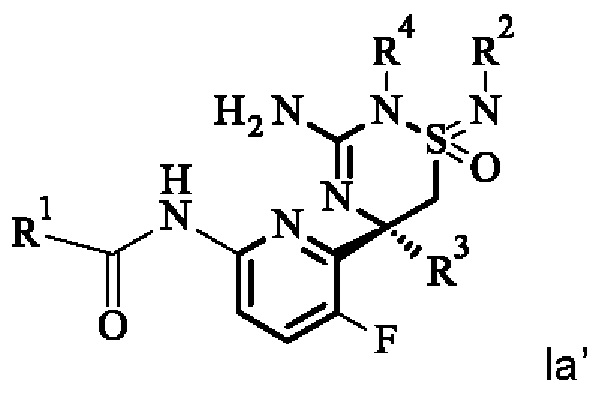
где
R1 представляет собой пиридил или пиразинил, замещенный 1-2 заместителями, индивидуально выбранными из циано, метила, метокси, фторметокси, трифторэтокси, бут-2-инокси и проп-2-инокси;
R2 представляет собой 2,2,2-трифторэтил или метил;
R3 представляет собой метил;
R4 представляет собой метил или -CH2CF3;
или его фармацевтически приемлемые соли.
2. Соединение формулы Ia' по п. 1, где R1 представляет собой 5-циано-3-хлорпиридил, 5-циано-3-метилпиридил, 5-циано-пиридил, 5-фтор-3-метилпиридил, 5-(фторметокси)пиридил, 5-бут-2-иноксипиразинил, 5-метоксипиразинил, 5-(2,2,2-трифторэтокси)пиридил, 5-проп-2-иноксипиридил.
3. Соединение формулы Ia' по п. 1 или 2, где R1 представляет собой 5-циано-3-метилпиридил, 5-циано-пиридил, 5-фтор-3-метилпиридил, 5-(фторметокси)пиридил, 5-бут-2-иноксипиразинил, 5-метоксипиразинил, 5-(2,2,2-трифторэтокси)пиридил, 5-проп-2-иноксипиридил.
4. Промежуточное соединение формулы I', где R2, R3 и R4 являются такими, как описано в п. 1

5. Соединение, выбранное из группы, состоящей из:
(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина;2,2,2-трифторуксусной кислоты,
(1R,5R)-5-[3-фтор-6-(1Н-пиразол-5-ил)пиридин-2-ил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
(1R,5R)-5-[6-(5-хлортиофен-2-ил)-3-фторпиридин-2-ил]-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
(1S,5R)-5-(6-бром-3-фторпиридин-2-ил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина;2,2,2-трифторуксусной кислоты,
(5R)-5-(6-бром-3-фторпиридин-2-ил)-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-3-амина;2,2,2-трифторуксусной кислоты,
N-(6-((5R)-3-амино-5-метил-1-(метилимино)-1-оксидо-2-(2,2,2-трифторэтил)-5,6-дигидро-2Н-1,2,4-тиадиазин-5-ил)-5-фторпиридин-2-ил)-3-хлор-5-цианопиколинамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-цианопиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-фтор-3-метилпиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-(фторметокси)пиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-бут-2-иноксипиразин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-метоксипиразин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-(2,2,2-трифторэтокси)пиридин-2-карбоксамида,
N-[6-[(1R,5R)-3-амино-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-проп-2-иноксипиридин-2-карбоксамида,
N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида,
N-[6-[(5R)-3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-фтор-3-метилпиридин-2-карбоксамида и
N-[6-[3-амино-5-метил-1-метилимино-1-оксо-2-(2,2,2-трифторэтил)-6H-1,2,4-тиадиазин-5-ил]-5-фторпиридин-2-ил]-5-циано-3-метилпиридин-2-карбоксамида, или их фармацевтически приемлемых солей.
6. Соединение, выбранное из группы, состоящей из:
(1R,5R)-5-(6-бром-3-фтор-2-пиридил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
(1S,5R)-5-(6-бром-3-фторпиридин-2-ил)-2,5-диметил-1-оксо-1-(2,2,2-трифторэтилимино)-6Н-1,2,4-тиадиазин-3-амина,
или их фармацевтически приемлемых солей.
7. Соединение формулы Ia' по любому из пп. 1-3 для применения в качестве терапевтически активного вещества для терапевтического и/или профилактического лечения болезни Альцгеймера.
8. Применение соединения формулы Ia' по любому из пп. 1-3 для изготовления лекарственного средства для терапевтического и/или профилактического лечения болезни Альцгеймера.
9. Способ терапевтического и/или профилактического лечения болезни Альцгеймера путем предоставления соединения формулы Ia' по любому из пп. 1-3.
10. Фармацевтическая композиция, ингибирующая активность BACE1, содержащая эффективное количество соединения, описанного в любом из пп. 1-3, и фармацевтически приемлемый носитель.
| WO 2011044181 A1, 14.04.2011 | |||
| WO 2011044184 A1, 14.04.2011 | |||
| 3-АЛКОКСИКАРБОНИЛ-ТИАДИАЗИНОНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1996 |
|
RU2162087C2 |
Авторы
Даты
2019-06-21—Публикация
2015-08-12—Подача