Изобретение относится к соединениям, выбранным из группы, включающей:
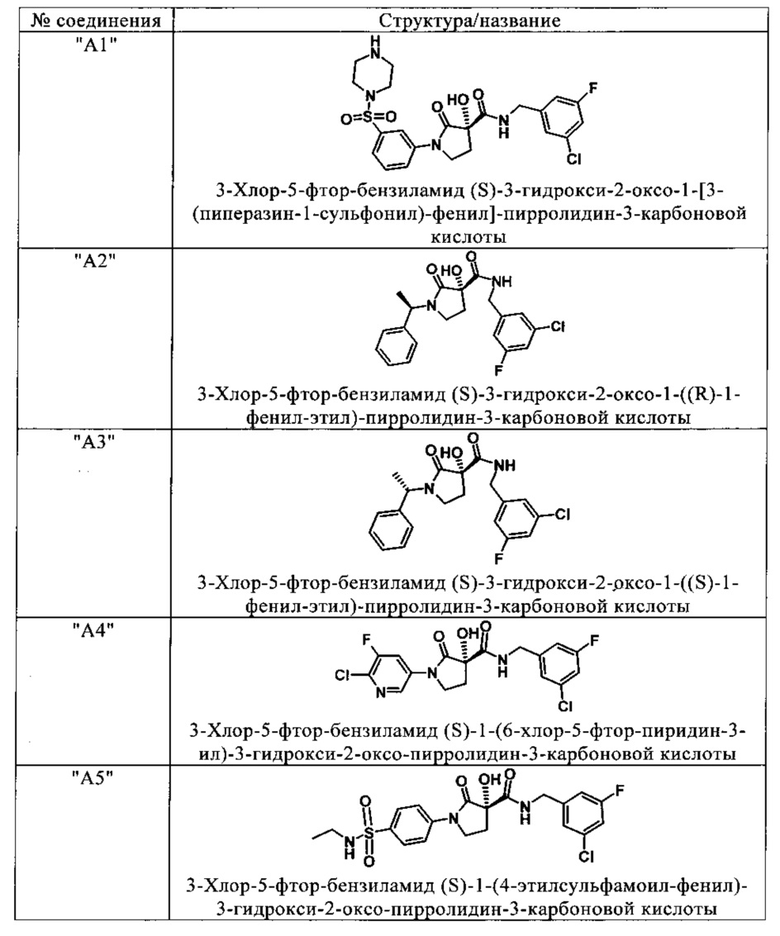
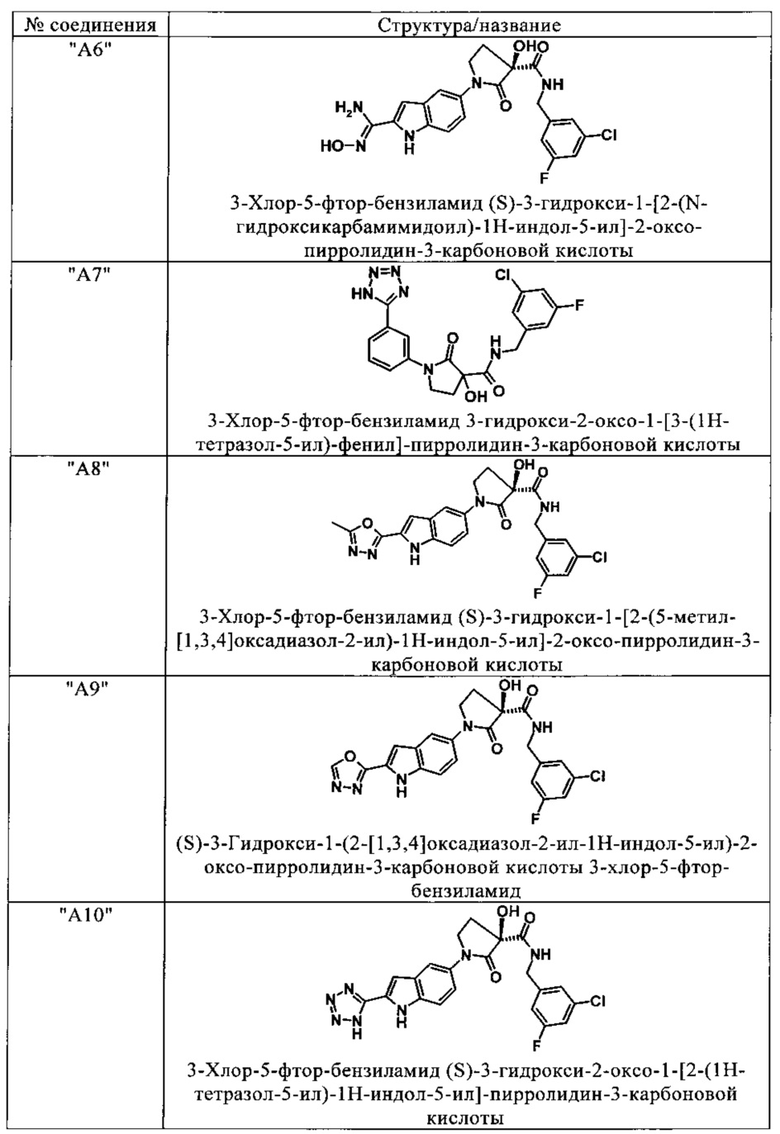
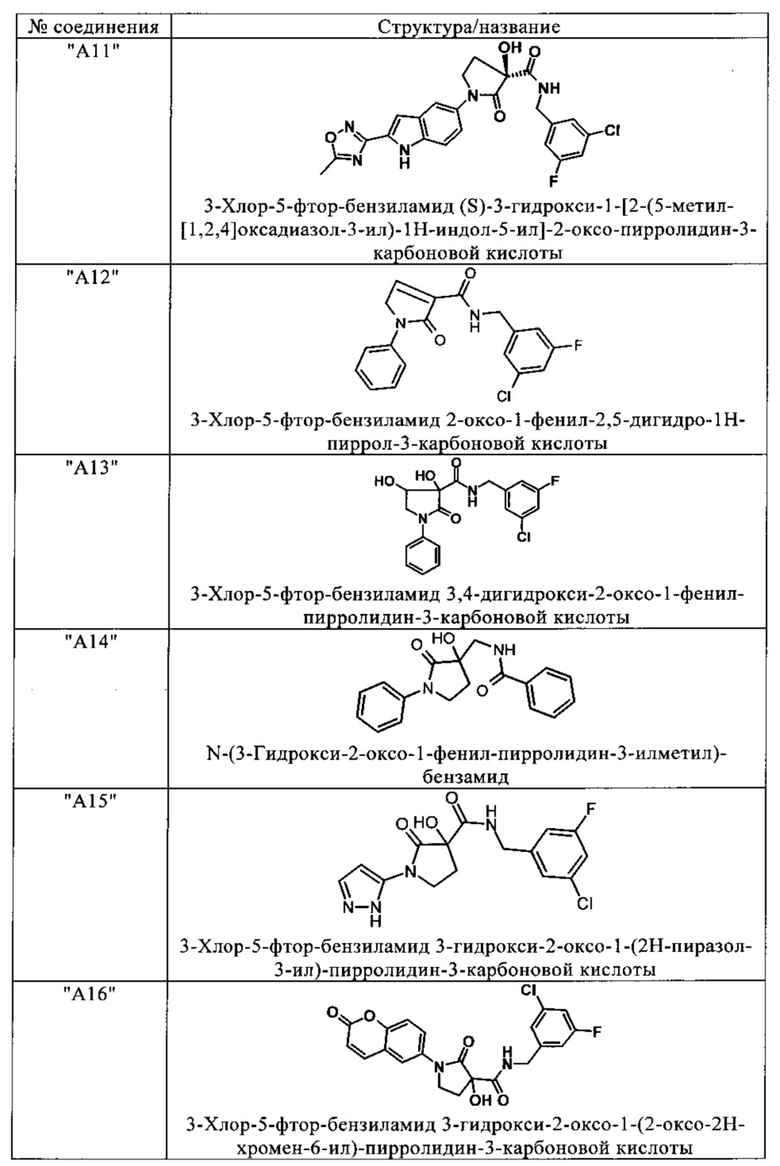


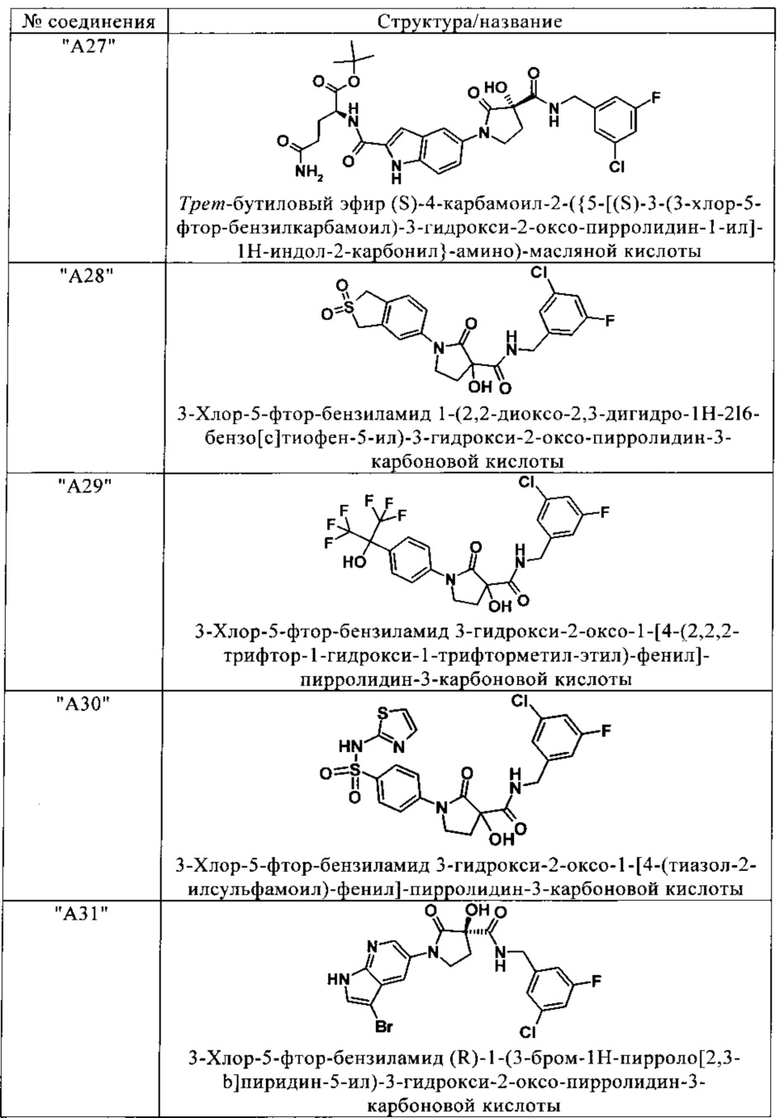

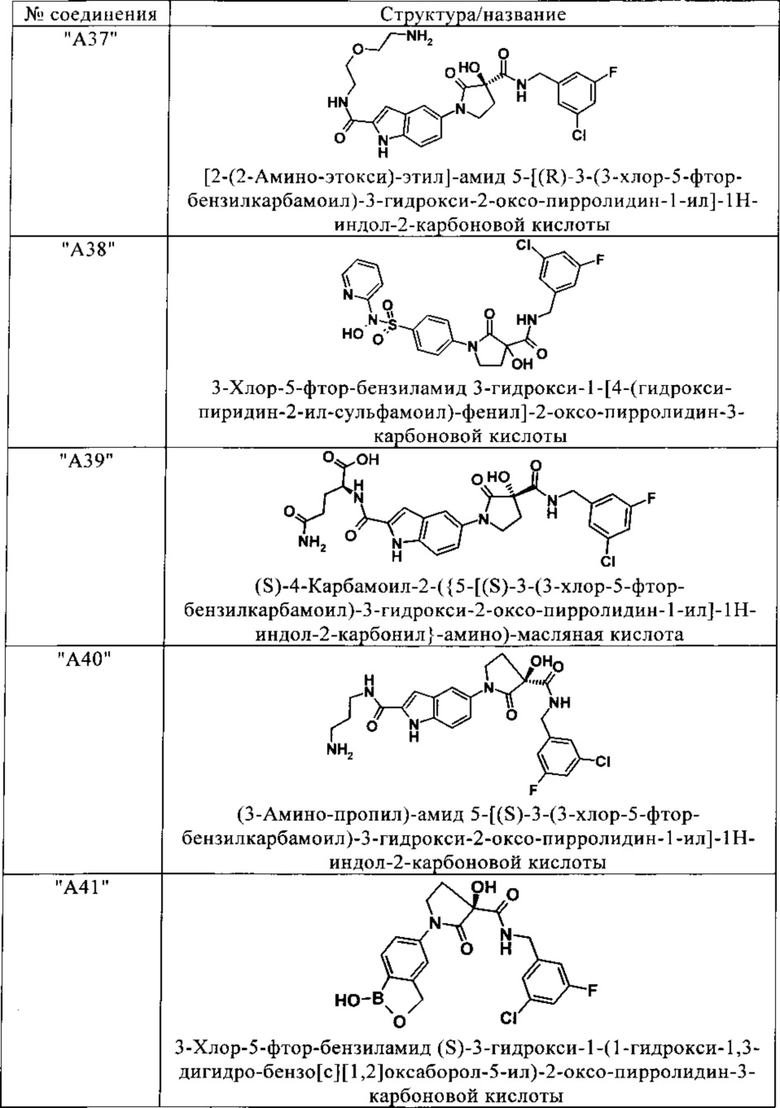
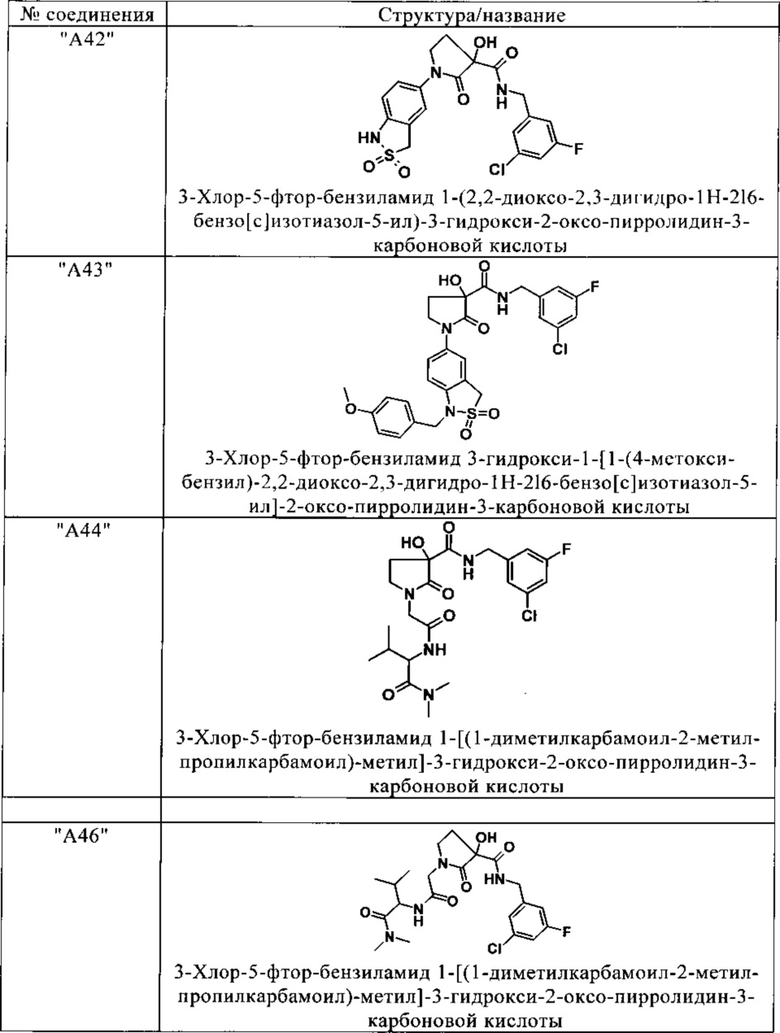
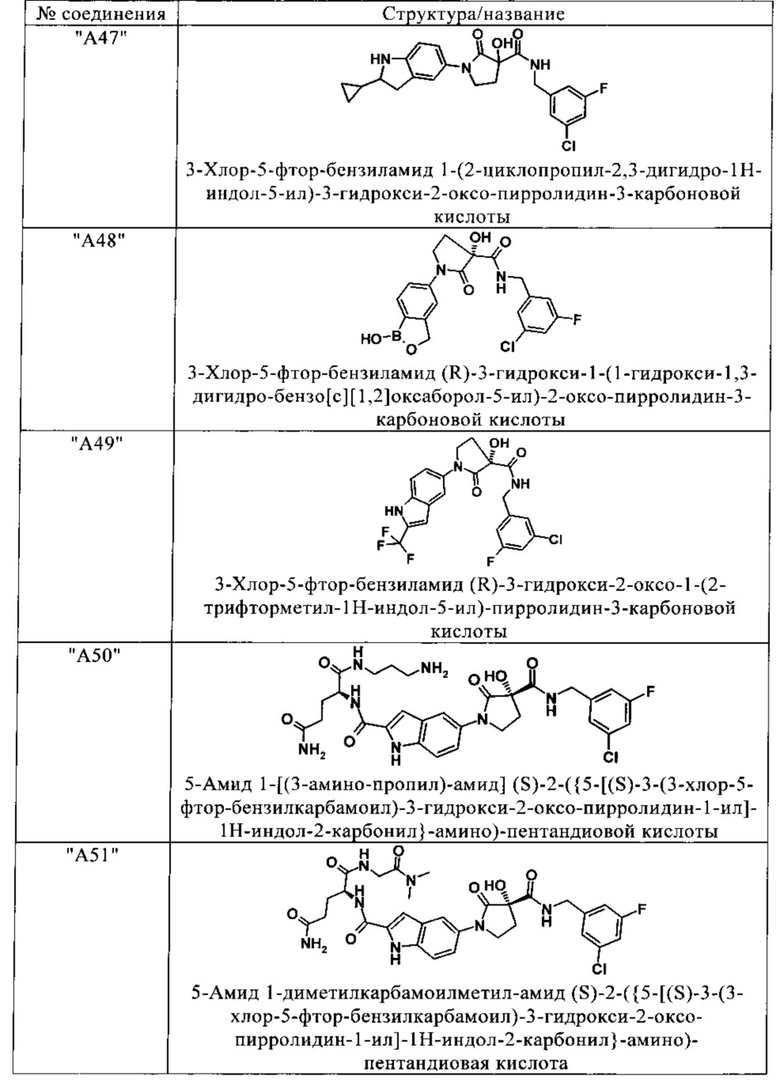
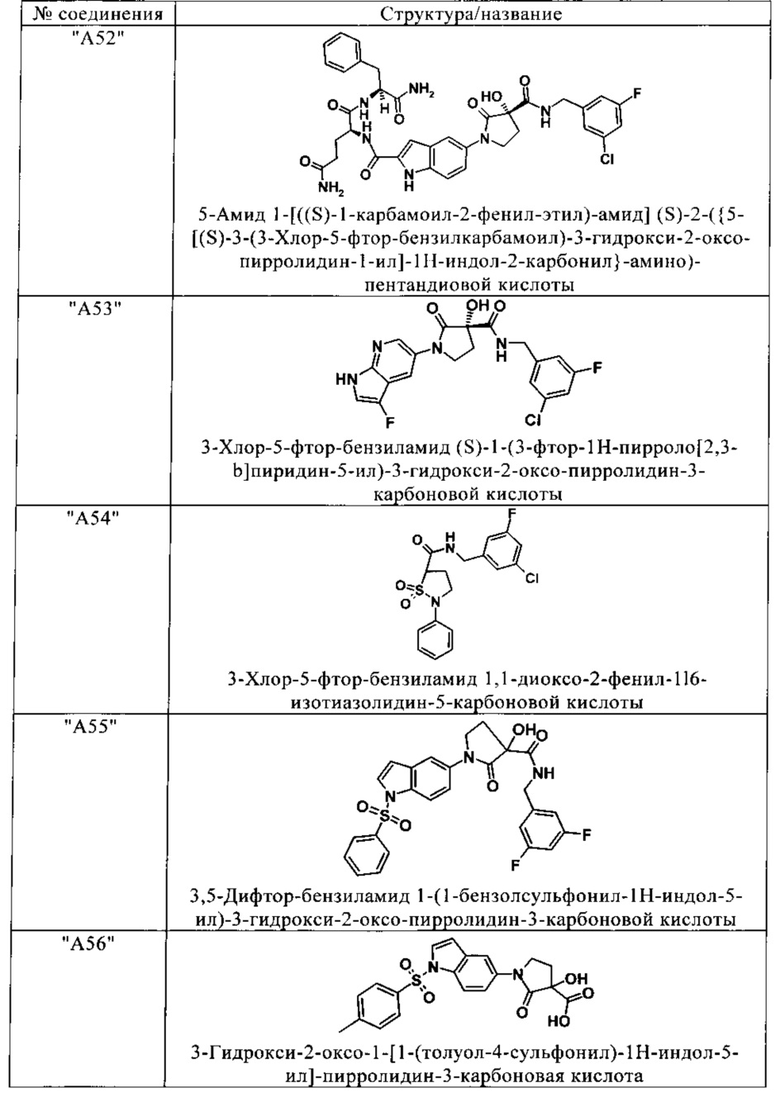
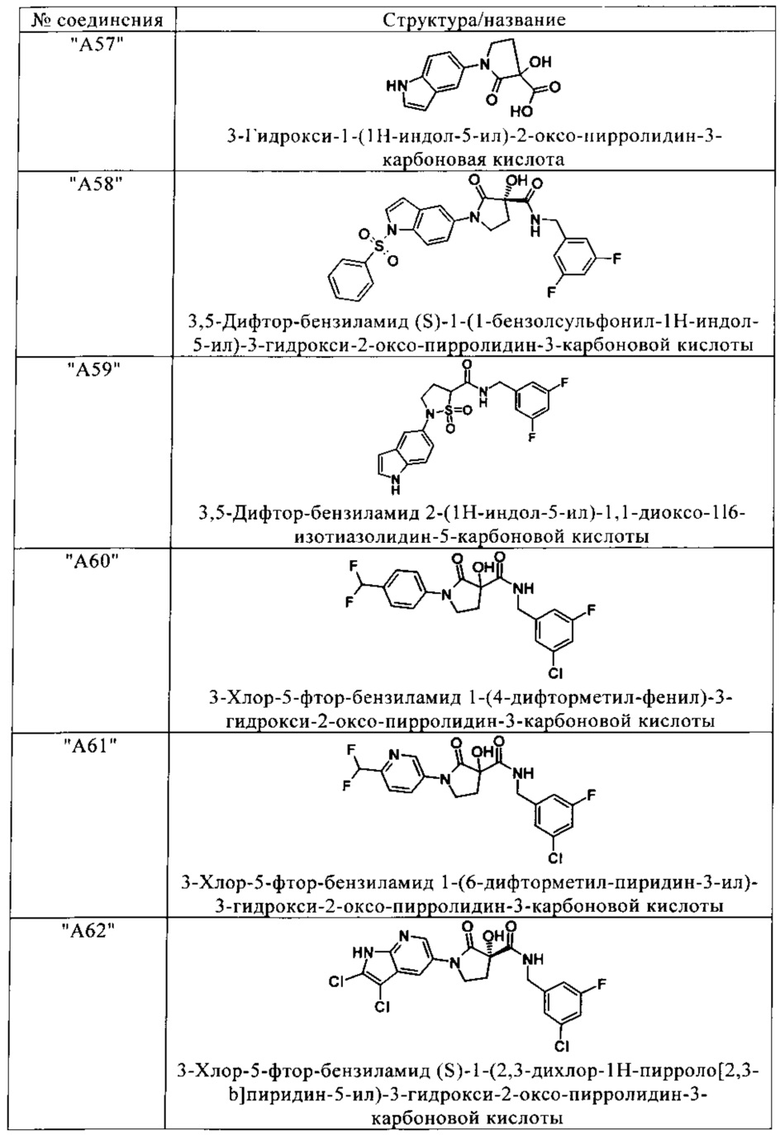
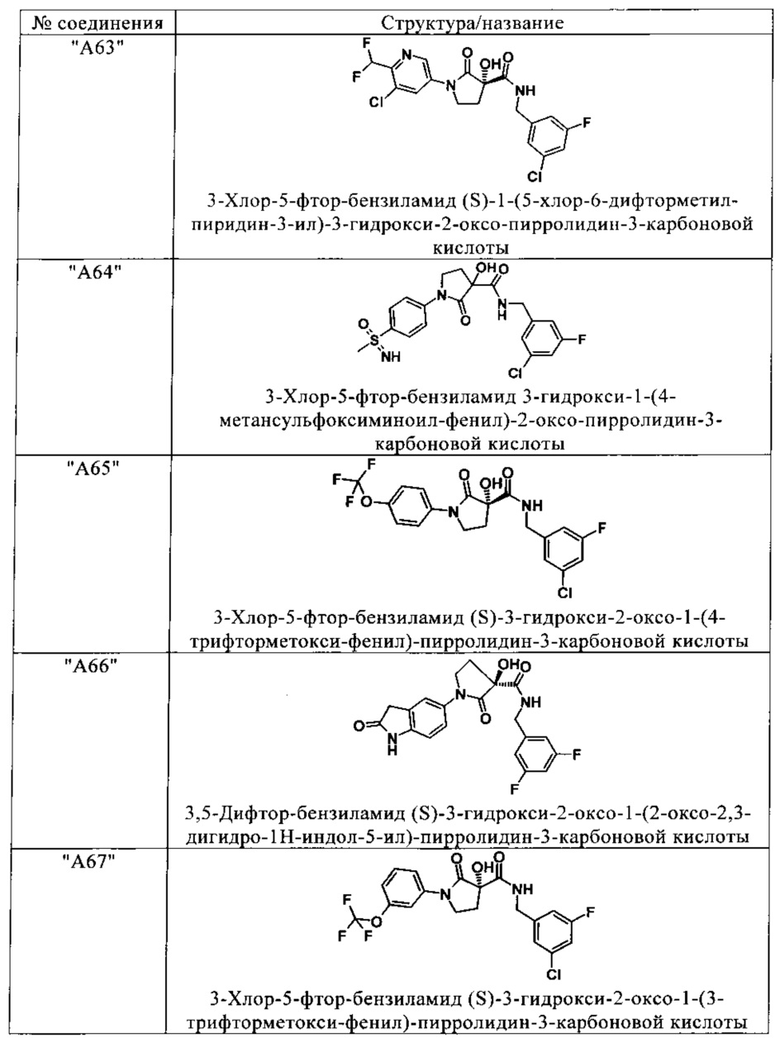
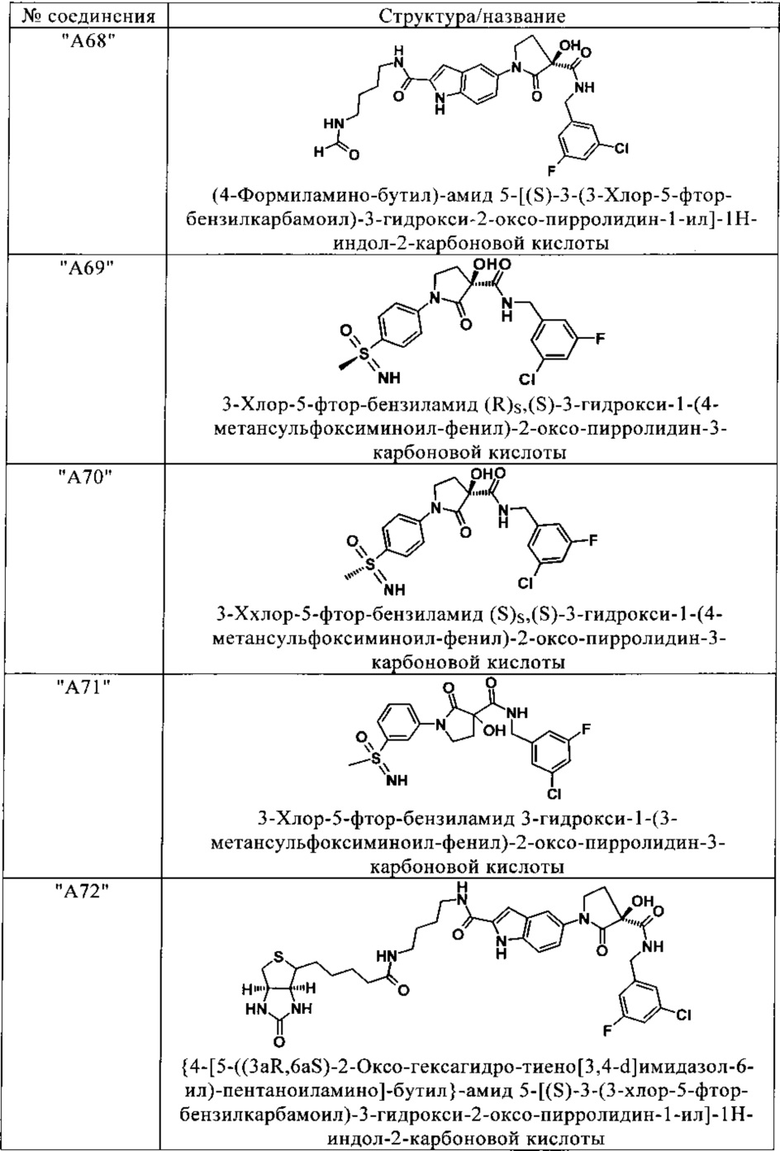
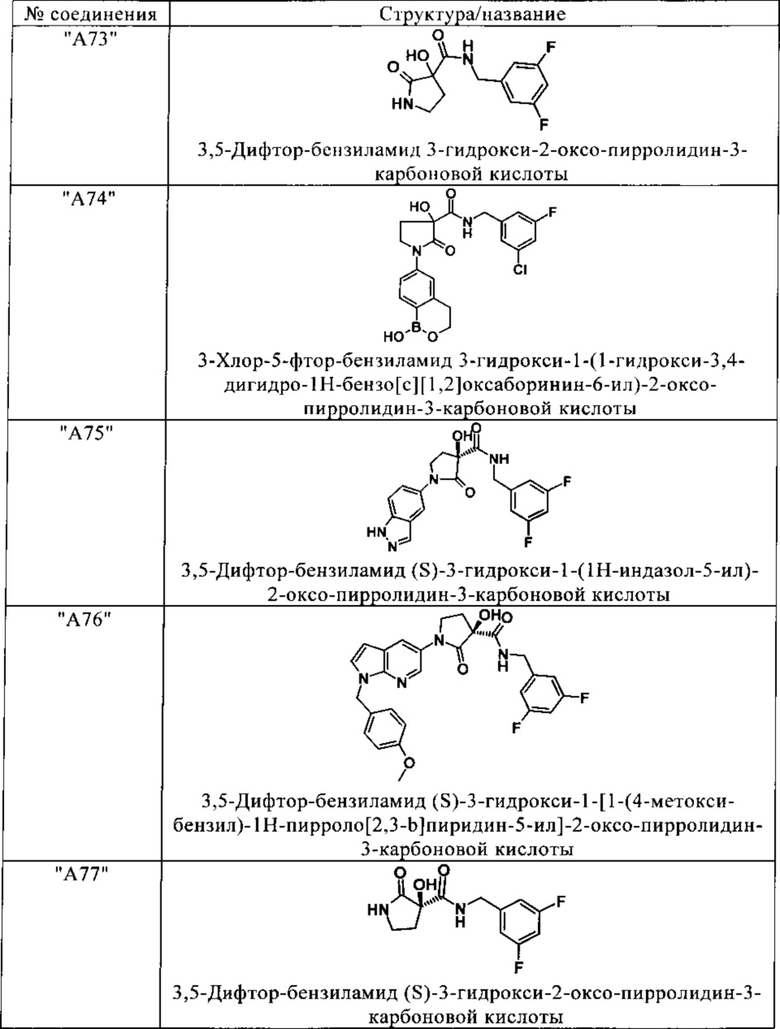
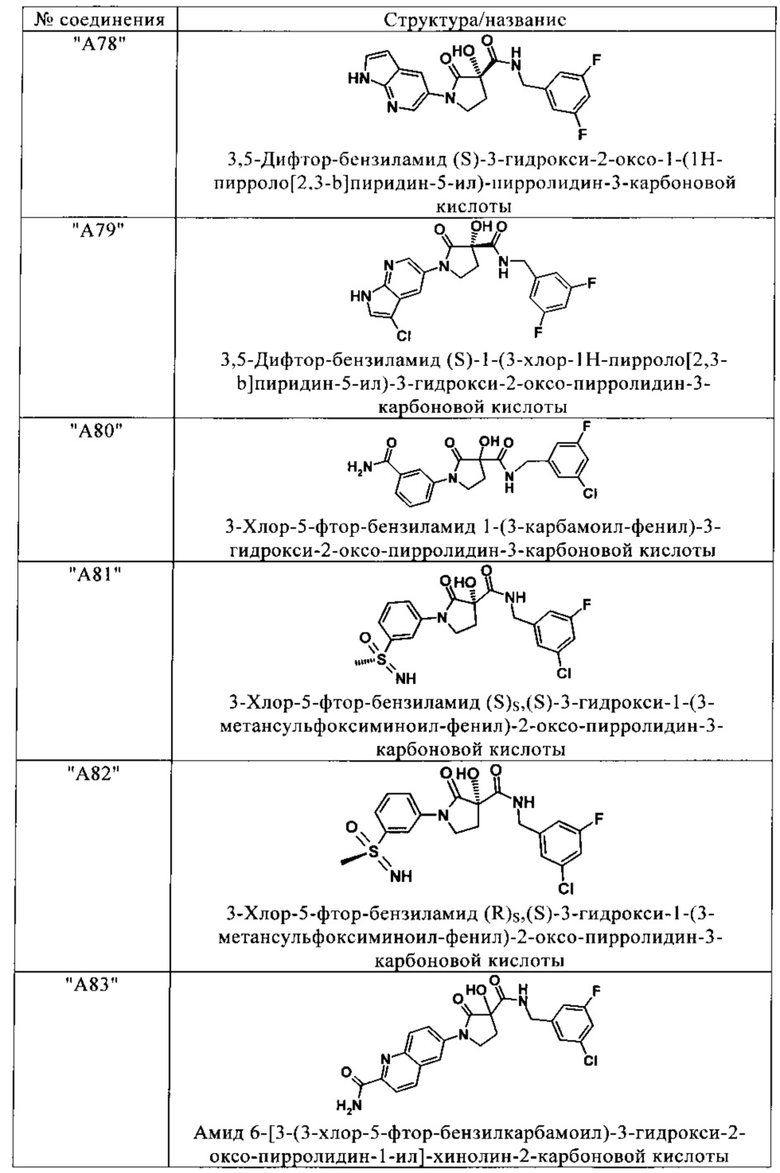
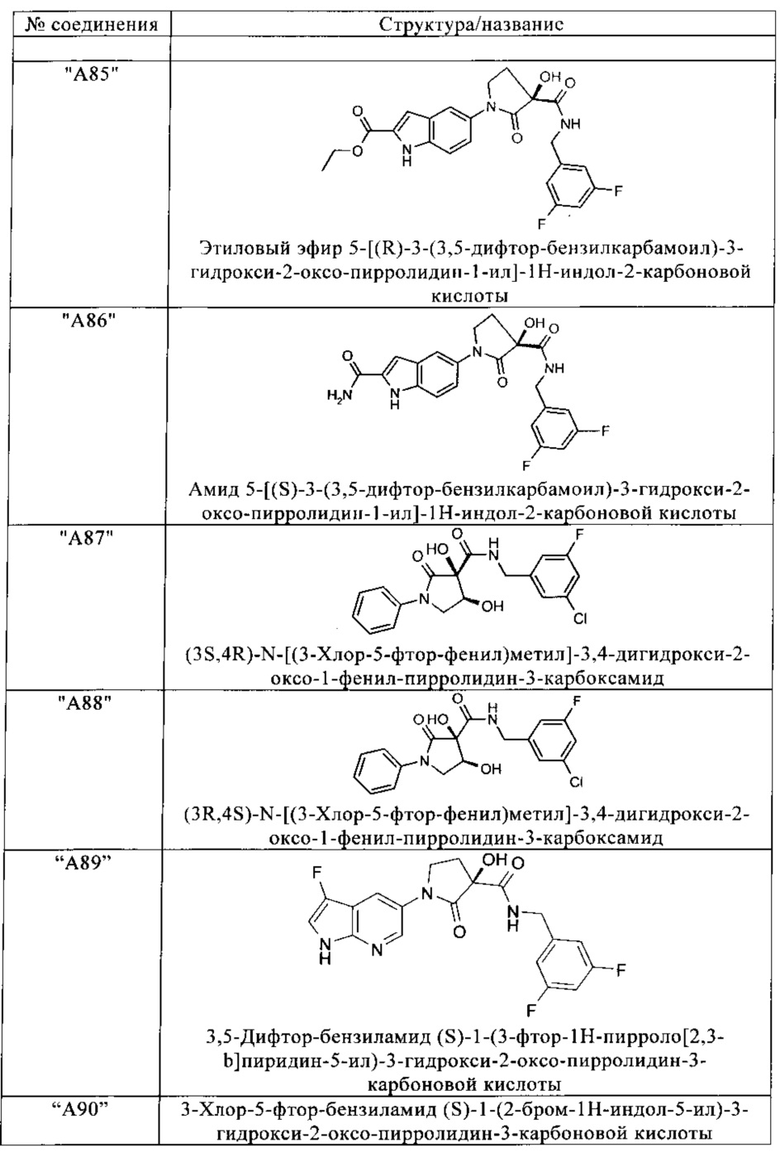
 и их фармацевтически применимые соли, таутомеры и стереоизомеры, включая их смеси во всех отношениях.
и их фармацевтически применимые соли, таутомеры и стереоизомеры, включая их смеси во всех отношениях.
В основе изобретения лежала задача найти новые соединения, обладающие ценными свойствами, в частности такие, которые можно использовать для получения лекарственных средств.
Было обнаружено, что соединения в соответствии с изобретением и их соли обладают весьма ценными фармакологическими свойствами, а также хорошей переносимостью.
В частности, они проявляют регулирующее, модулирующее и/или ингибирующее действие на металлопротеазы, предпочтительно на метионинаминопептидазу (MetAP), в особенности на подтип MetAP-2.
Их можно применять в качестве лекарственных средств против злокачественного новообразования, а также в качестве лекарственных средств, которые положительно влияют на жировой обмен, но и в качестве лекарственных средств против воспаления.
Другие гидроксил-замещенные пирролидиноны известны из:
WO 2011/004608 (ингибиторы MetAP2) и WO 2013/149704 (ингибиторы MetAP2);
Zeitschrift fur Naturforschung, В: Chemical Sciences (1994), 49(11), 1586-95; Analytica Chimica Acta (1987), 202, 167-74;
Journal of Electroanalytical Chemistry and Interfacial Electrochemistry (1988), 239(1-2), 161-73;
Zeitschrift fur Naturfor. Part B: Anorg. Chem. Org. Chem (1978), 33B(12), 1540-6;
J. Chem. Soc. (1965), (Oct.), 5556-62; J. Chem. Soc. (1965), (Oct.), 5551-6.
В WO 01/79157 описаны замещенные гидразиды и N-алкоксиамиды, обладающие активностью, ингибирующей MetAP-2 и могут быть использованы для ингибирования антиогенеза, в частности для лечения заболеваний, таких как, например, рак, развитие которого зависит от ангиогенеза.
В WO 02/081415 описаны ингибиторы MetAP-2, которые можно применять для лечения рака, гемангиома, пролиферативная ретинопатия, ревматоидный артрит, атеросклеротическая неоваскуляризация, псориаз, глазная неоваскуляризация и ожирение.
В WO 2008/011114 описаны соединения в качестве ингибиторов ангиогенеза и ингибиторов MetAP-2, которые можно применять для лечения лимфоидной лейкемии и лимфомы.
Действие соединений в соответствии с изобретением против рака в частности заключается в х действии против ангиогенеза. Ингибирование ангиогенеза оказалось целесообразным при более чем 70 заболеваниях, таких как, например, рак яичников (F. Spinella et al. J. Cardiovasc. Pharmacol. 2004, 44, SI40), рак груди (A. Morabito et al. Crit. Rev. Oncol./Hematol. 2004, 49, 91), рак предстательной железы (В. Nicholson et al. Рак Metastas. Rev. 2001, 20, 297), диабетическая слепота, псориаз и дегенерация желтого пятна (Е. Ng et al. Can. J. Ophthalmol. 2005, 23, 3706).
Протеазы регулируют множество различных клеточных процессов, в частности, модуляцию пептидов и белков, в особенности, преобразование белков, созревание белков и процессинг сигнальных пептидов, разрушение аномальных белков и деактивацию/активацию регуляторных белков. В частности, аминоконцевая модификация формирующихся полипептидов представляет собой наиболее частую модуляцию. Аминопротеазы представляют собой металлопротеазы, которые отщепляют аминокислоты от незащищенного N-конца пептидов или белков, которые могут быть осуществлены либо способом котрансляции или посттрансляции.
Метионинаминопептидаза (MetAP) отщепляет концевой метионин образующихся пептидов, в частности если предпоследняя аминокислота является малой и незаряженной (например, Gly, Ala, Ser, Thr, Val, Pro или Cys).
Во многих механизмах заболевания ангиогенеза является либо причинным в центре заболевания или оказывает ухудшающее воздействие на прогрессирование заболевания. В случаях злокачественных новообразований, например, ангиогенез приводит к увеличению опухоли в размерах и способен проникать в другие
органы. Другие заболевания, при которых ангиогенез играет важную роль, представляют собой псориаз, артроз, артериосклероз и глазные заболевания, такие как диабетическая ретинопатия, возрастная дегенерация желтого пятна, покраснение радужной оболочки или неоваскулярная глаукома, кроме того, при воспалениях. Таким образом, соединения, которые лежат в основе настоящего изобретения, содержат эти соединения композиции, а также описанные способы могут быть использованы для лечения этих заболеваний.
Соответственно, соединения в соответствии с изобретением или их фармацевтически приемлемую соль вводят для лечения рака, включая солидные карциномы, такие как, например, карциномы (легких, поджелудочной железы, щитовидной железы, мочевого пузыря или толстой кишки), миелоидных заболеваний (например, миелоидной лейкемии) или аденом (например, ворсинчатая аденома толстой кишки).
Помимо этого, опухоли включают моноцитарный лейкоз, карциному головного мозга, мочеполовой, лимфатической системы, желудка, гортани и легких, включая аденокарциному легкого и мелкоклеточный рак легкого, поджелудочной железы и/или рак молочной железы.
Поэтому настоящее изобретение относится к соединениям в соответствии с изобретением в качестве лекарственных средств и/или лекарственных активных соединений в лечении и/или профилактики указанных заболеваний и к применению соединений в соответствии с изобретением для приготовления фармацевтического средства для лечения и/или профилактики указанных заболеваний и к способу лечения указанных заболеваний, который включает введение одного или нескольких соединений в соответствии с изобретением пациенту, нуждающемуся в таком введении.
Может быть доказано, что соединения в соответствии с изобретением обладают антиканцерогенным действием. Соединения в соответствии с изобретением вводят пациенту, имеющему заболевание, например, для ингибирования роста опухоли, чтобы уменьшить воспаление, связанное с лимфопролиферативным заболеванием, для ингибирования отторжения трансплантата или неврологического повреждения в результате восстановления ткани, и т.д. Данные соединения пригодны для профилактических или терапевтических целей. Используемое в настоящей заявке, понятие "лечение" применяют как относящееся как к предупреждению заболеваний, так и к лечению существовавших ранее состояний. Предупреждения пролиферации/жизнеспособности достигают посредством введения соединений в соответствии с изобретением до развития явной болезни, например, для предупреждения роста опухоли. Альтернативно, соединения применяют для лечения текущих заболеваний путем стабилизации или улучшения клинических симптомов пациента.
Реципиент или пациент может относиться к любому из видов млекопитающих, например, к видам приматов, в частности, к людям; грызунам, включая мышей, крыс и хомяков; кроликам, лошадям, коровам, собакам, кошкам и т.д. Животные модели представляют интерес для экспериментальных исследований, обеспечивая модель для лечения болезней человека.
Восприимчивость конкретной клетки к лечению соединениями в соответствии с изобретением может быть определена с помощью испытания in vitro. Типично, клеточную культуру инкубируют с соединением в соответствии с изобретением в различных концентрациях в течение периода времени, которого достаточно для того, чтобы активные агенты смогли вызвать клеточную смерть или ингибировать клеточную пролиферацию, жизнеспособность или миграцию клеток, обычно приблизительно от одного часа до одной недели. Тестирование in vitro может быть осуществлено с применением культивируемых клеток из образца биопсии. Затем определяют количество клеток, оставшихся после обработки.
Доза варьирует в зависимости от конкретного применяемого соединения, конкретного заболевания, состояния пациента и т.д. Обычно терапевтическая доза является достаточной для того, чтобы значительно уменьшить численность нежелательной клеточной популяции в целевой ткани наряду с поддержанием жизнеспособности пациента. Как правило, лечение продолжается до наступления значительного снижения, например, снижения, которое составляет, по меньшей мере, 50% клеточной нагрузки, и может продолжаться, по сути, до полного отсутствия обнаружения нежелательных клеток в организме.
Было обнаружено, что соединения в соответствии с изобретением вызывают специфическое ингибирование MetAP-2. Соединения в соответствии с изобретением предпочтительно проявляют выгодную биологическую активность, которая может быть обнаружена в описанных тестах, например, в настоящей заявке. В этих тестах, соединения в соответствии с изобретением проявляют и вызывают ингибирующий эффект, который, как правило, подтверждается документально значениями IC50 в приемлемом диапазоне, предпочтительно в микромолярном диапазоне и более предпочтительно в наномолярном диапазоне.
К тому же, соединения в соответствии с изобретением можно применять для достижения аддитивных или синергетических эффектов в некоторых существующих химиотерапиях рака и лучевых терапиях и/или чтобы восстановить эффективность некоторых существующих химиотерапий рака и лучевых терапий.
Соединения в соответствии с изобретением также можно применять для лечения ожирения. У Henri R. Lijnen et al. in Obesity, том 18 № 12, 2241-2246 (2010) описано применение фумагиллина, ингибитора Met-AP2, для уменьшения жировой ткани.
Применение ингибиторов Met-AP2 (соединений типа фумагиллина) для лечения ожирения также описано в WO 2011/085201 А1.
Соединения в соответствии с изобретением можно также применять для лечения малярии. У X. Chem et al. in Chemistry & Biology, том 16, 193-202 (2009) описано применение фумагиллина, ингибитора Met-AP2, для лечения малярии.
Соединения в соответствии с изобретением можно также применять для лечения доброкачественной гипертрофии предстательной железы.
Применение ингибиторов Met-AP2 (соединений типа фумагиллина) для лечения доброкачественной гипертрофии предстательной железы описано в WO 2011/085198 А1.
Под соединениями в соответствии с изобретением также следует понимать гидраты и сольваты этих соединений, кроме того фармацевтически приемлемые производные.
Изобретение также относится к оптически активным формам (стереоизомерам), солям, энантиомерам, рацематам, диастереомерам и гидратам, и сольватам этих соединений. Термин сольваты соединений следует понимать как аддукции молекул инертного растворителя на соединениях, которые образуются вследствие силы их взаимного притяжения. Сольватами являются, например, моно- или дигидраты или алкоксиды.
Под термином фармацевтически приемлемые производные следует понимать, например, соли соединений в соответствии с изобретением, а также так называемые пролекарства соединений.
Термин производные пролекарств следует понимать как соединения в соответствии с изобретением, которые были модифицированы посредством, например, алкильных или ацильных групп, Сахаров или олигопептидов и которые быстро расщепляются в организме, образуя эффективные соединения в соответствии с изобретением.
К ним также относят способные к биологическому разложению полимерные производные соединений в соответствии с изобретением, как описано, например, в Int. J. Pharm. 115, 61-67 (1995).
Выражение "эффективное количество" означает количество лекарственного средства или фармацевтического активного соединения, которое вызывает в ткани, системе, животном или человеке биологическую или лекарственную ответную реакцию, которую стремится или желает получить, например, исследователь или лечащий врач.
Кроме того, выражение "терапевтически эффективное количество" означает то количество, которое, имеет следующие последствия по сравнению с соответствующим субъектом, который не получал этого количества:
улучшенное лечение, излечение, предотвращение или устранение заболевания, синдрома, состояния, жалобы, расстройства или побочных эффектов, а также уменьшение прогрессирования заболевания, состояния или расстройства.
Выражение "терапевтически эффективное количество" также охватывает количества, которые эффективны для повышения нормальной физиологической функции.
Изобретение также относится к применению смесей соединений в соответствии с изобретением, например, смесей из двух диастереомеров, например, в соотношении 1:1, 1:2, 1:3, 1:4, 1:5, 1:10, 1:100 или 1:1000.
В особенности предпочтительны смеси стереоизомерных соединений.
Предпочтительные соединения в соответствии с изобретением выбирают из группы, включающей:
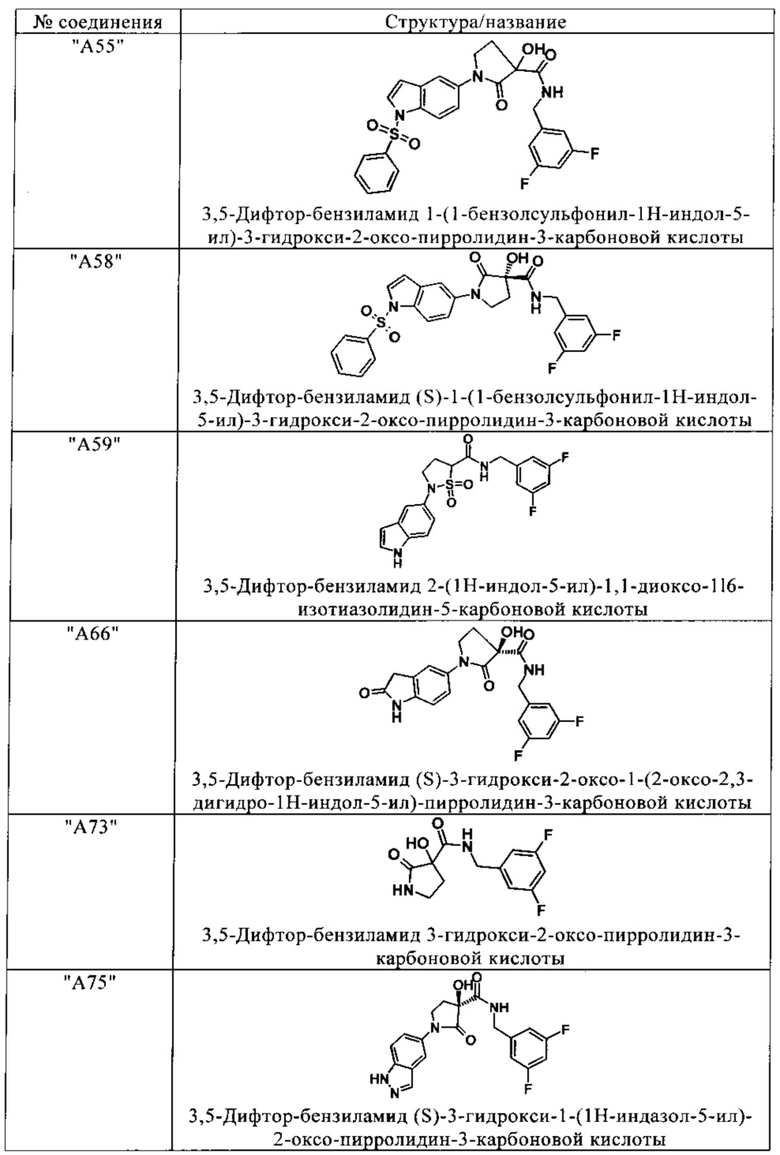
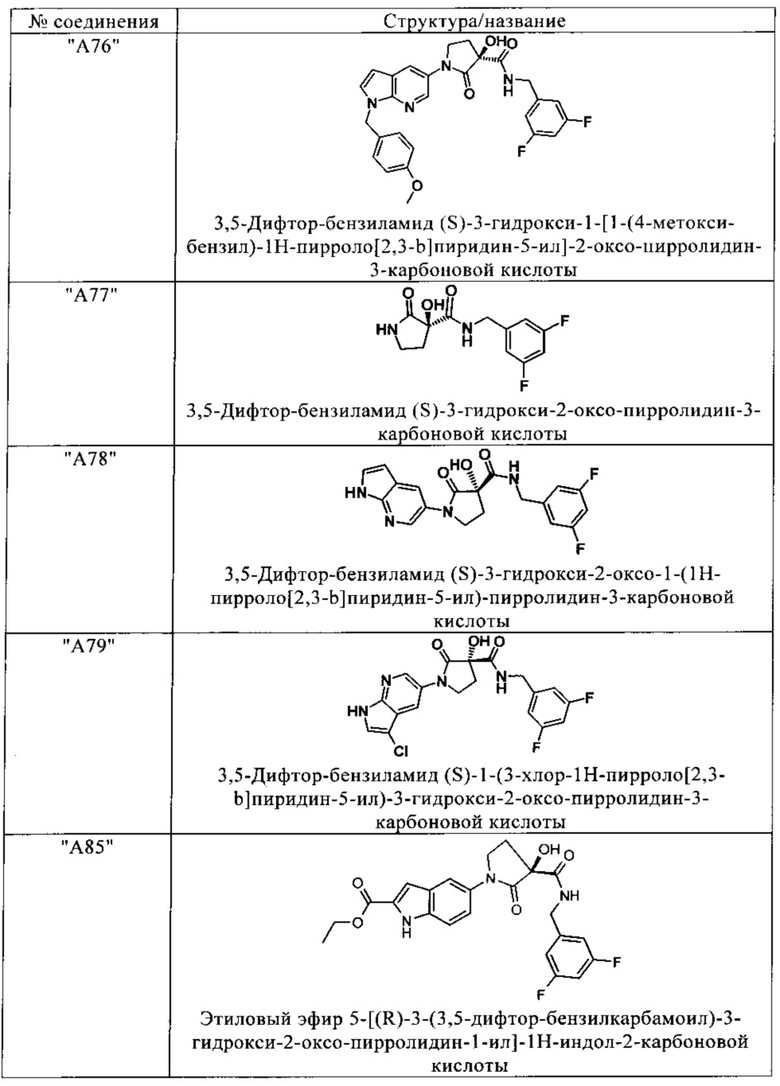
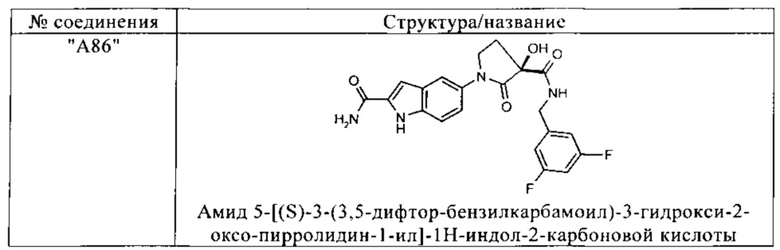
и их фармацевтически применимые соли, таутомеры и стереоизомеры, включая их смеси во всех отношениях.
Сверх того, предпочтительные соединения в соответствии с изобретением выбирают из группы, включающей:
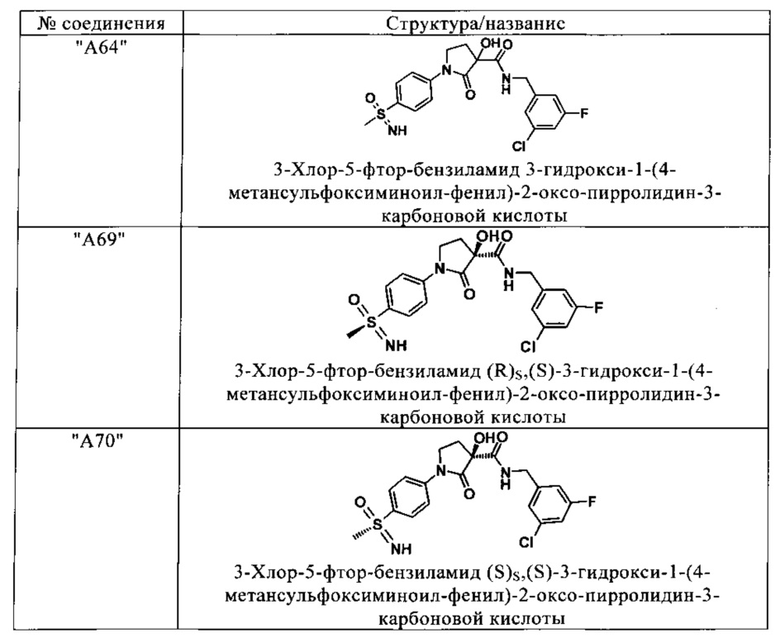
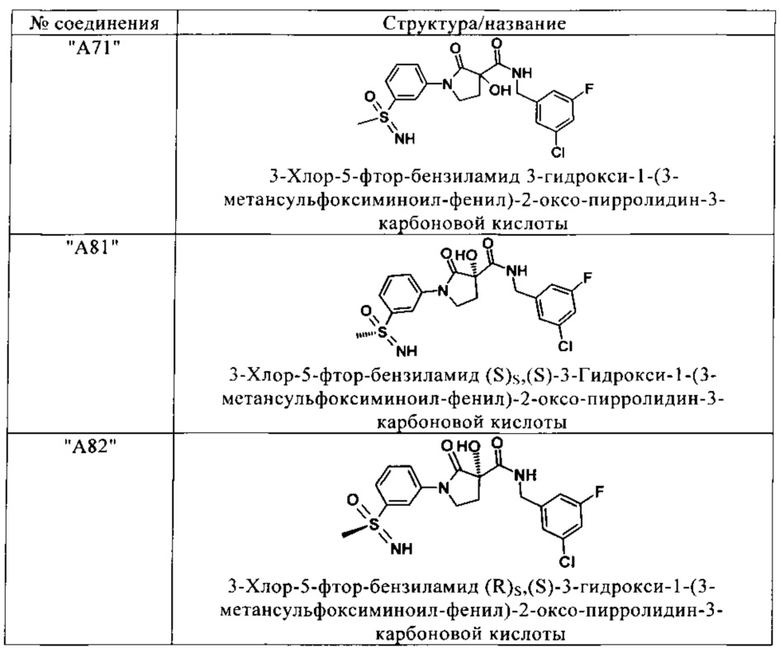
и их фармацевтически применимые соли, таутомеры и стереоизомеры, включая их смеси во всех отношениях.
Преимущественно предпочтительными являются "А75", "А78" и "А79" и их фармацевтически применимые соли, таутомеры и стереоизомеры, включая их смеси во всех отношениях.
Соединения в соответствии с изобретением и их соли получают, как описано для соединений формулы I в WO 2011/004608 и WO 2013/149704.
Получение соединений в соответствии с изобретением осуществляют аналогично соединениям формулы I как описано в WO 2011/004608 и их фармацевтически применимым солям, таутомерам и стереоизомерам, отличающееся тем, что
а) соединение формулы II
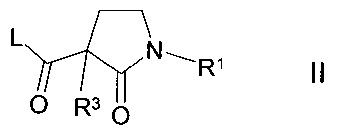
в которой R1 и R3 имеют значения, указанные в п. 1 заявки WO 2011/004608, и L означает CI, Br, I или свободно или реакционноспособно функционально модифицированную ОН группу,
взаимодействует с соединением формулы III
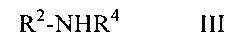
в которой R2 и R4 имеют значения, указанные в п. 1 заявки WO 2011/004608, или
б) для получения соединений формулы I заявки WO 2011/004608, в которых R3 означает ОН,
соединение формулы IV

в которой R1, R2 и R4 имеют значения, указанные в п. 1 заявки WO 2011/004608, окисляется, или
в) радикал R3 превращается в другой радикал R3 посредством замещения ОН группы атомом галогена, или замещения атома галогена посредством N3,
и/или основание или кислота формулы I превращается в одну из его солей.
К тому же соединения в соответствии с изобретением, а также исходные вещества для их получения получают по существу известными способами, как описано в литературных источниках (например, в стандартных работах, таких как Houben-Weyl, Methoden der organischen Chemie [Способы органической химии], Georg-Thieme-Verlag, Штутгарт), чтобы быть точным в условиях реакции, которые известны и пригодны для указанных реакций. В данном контексте также могут
основания, такого как DIPEA, триэтиламин, диметиланилин, пиридин или хинолин.
Также может быть благоприятным добавление гидроксида, карбоната или бикарбоната щелочного или щелочноземельного металла или другой соли слабой кислоты и щелочных или щелочноземельных металлов, предпочтительно калия, натрия, кальция или цезия.
В зависимости от используемых условий, время реакции составляет от нескольких минут до 14 дней, температура реакции составляет от -15° до 150°, обычно от 40° до 130°, в особенности предпочтительно от 60° до 110°С.
Пригодными инертными растворителями являются, например, углеводороды, такие как гексан, петролейный эфир, бензол, толуол или ксилол; хлорированные углеводороды, такие как трихлорэтилен, 1,2-дихлорэтан, четыреххлористый углерод, хлороформ или дихлорметан; спирты, такие как метанол, этанол, изопропанол, н-пропанол, н-бутанол или трет-бутанол; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран (ТГФ) или диоксан; гликолевые эфиры, такие как монометиловый или моноэтиловый эфир этиленгликоля, диметиловый эфир этиленгликоля (диглим); кетоны, такие как ацетон или бутанон; амиды, такие как ацетамид, диметилацетамид или диметилформамид (ДМФА); нитрилы, такие как ацетонитрил; сульфоксиды, такие как диметилсульфоксид (ДМСО); сероуглерод; карбоновые кислоты, такие как муравьиная кислота или уксусная кислота; нитросоединения, такие как нитрометан или нитробензол; сложные эфиры, такие как этилацетат, или смеси вышеуказанных растворителей.
Особое предпочтение отдают гликолевым эфирам, таким как монометиловый эфир этиленгликоля, ТГФ, дихлорметан и/или ДМФА.
Помимо этого соединения формулы I предпочтительно могут быть получены окислением соединений формулы IV.
Окисление предпочтительно осуществляют, используя mpem-бутилгидропероксид.
В зависимости от используемых условий, время реакции составляет от нескольких минут до 14 дней, температура реакции составляет от -15° до 150°, обычно от 40° до 130°, в особенности предпочтительно от 60° до 110°С.
Растворитель предпочтительно представляет собой воду, при этом также может быть благоприятным добавление гидроксида, карбоната или бикарбоната щелочного или щелочноземельного металла или другой соли слабой кислоты и щелочных или щелочноземельных металлов, предпочтительно калия, натрия, кальция или цезия.
Фармацевтические соли и другие формы
Указанные соединения в соответствии с изобретением можно применять в своей конечной, не солевой форме. С другой стороны, настоящее изобретение также охватывает применение таких соединений в форме их фармацевтически приемлемых солей, которые могут быть получены с помощью разнообразных органических и неорганических кислот и оснований в соответствии со способами, хорошо известными в данной области техники. Фармацевтически приемлемые солевые формы соединений в соответствии с изобретением получают, главным образом, с применением традиционных способов. Если соединение в соответствии с изобретением содержит карбоксильную группу, то его приемлемая соль может быть образована с помощью реакции соединения с приемлемым основанием для получения соответствующей соли присоединения основания. Такими основаниями являются, например, гидроксиды щелочных металлов, включая гидроксид калия, гидроксид натрия и гидроксид лития; гидроксиды щелочноземельных металлов, такие, как гидроксид бария и гидроксид кальция; алкоксиды щелочных металлов, например, этилат калия и пропилат натрия; а также различные органические основания, такие, как пиперидин, диэтаноламин и N-метилглутамин. Сюда также включены соли алюминия соединений в соответствии с изобретением. В случае некоторых соединений в соответствии с изобретением соли присоединения кислоты могут быть образованы путем обработки указанных соединений фармацевтически приемлемыми органическими и неорганическими кислотами, например, гидрогалогенидами, такими, как хлористый водород, бромистый водород или йодистый водород; другими минеральными кислотами, и их соответствующими солями, такими как сульфат, нитрат или фосфат и т.п., и алкил- и моноарилсульфонатами, такими, как этансульфонат, толуолсульфонат и бензолсульфонат, и другими органическими кислотами и их соответствующими солями, такими, как ацетат, трифторацетат, тартрат, малеат, сукцинат, цитрат, бензоат, салицилат, аскорбат и т.п. Соответственно, фармацевтически приемлемые соли присоединения кислоты соединений формулы I включают следующие, но не ограничиваются только ними: ацетат, адипат, альгинат, аргинат, аспартат, бензоат, бензолсульфонат (безилат), бисульфат, бисульфит, бромид, бутират, камфорат, камфорсульфонат, каприлат, хлорид, хлорбензоат, цитрат, циклопентанпропионат, диглюконат, дигидрофосфат, динитробензоат, додецилсульфат, этансульфонат, фумарат, формиат, галактерат (из муциновой кислоты), галактуронат, глюкогептаноат, глюконат, глутамат, глицерофосфат, гемисукцинат, гемисульфат, гептаноат, гексаноат, гиппурат, гидрохлорид, гидробромид, гидройодид, 2-гидроксиэтансульфонат, йодид, изетионат, изобутират, лактат, лактобионат, малат, малеат, малонат, манделат, метафосфат, метансульфонат, метилбензоат, моногидрофосфат, 2-нафталинсульфонат, никотинат, нитрат, оксалат, олеат, пальмоат, пектинат, персульфат, фенилацетат, 3-фенилпропионат, фосфат, фосфонат, фталат.
Кроме того, основные соли соединений в соответствии с изобретением включают, но не ограничиваются только ними, соли алюминия, аммония, кальция, меди, железа(III), железа(II), лития, магния, марганца(III), марганца(II), калия, натрия и цинка. Среди перечисленных выше солей предпочтение отдают солям аммония; солям щелочных металлов - натрия и калия; и солям щелочноземельных металлов - кальция и магния. Соли соединений в соответствии с изобретением, которые получают из фармацевтически приемлемых органических нетоксических оснований, включают, но не ограничиваются только ними, соли первичных, вторичных и третичных аминов, замещенных аминов, также включая природные замещенные амины, циклические амины и основные ионообменные смолы, например, аргинин, бетаин, кофеин, хлорпрокаин, холин, N,N'-дибензилэтилендиамин (бензатин), дициклогексиламин, диэтаноламин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лидокаин, лизин, меглюмин, N-метил-D-глюкамин, морфолин, пиперазин, пиперидин, полиаминные смолы, прокаин, пурины, теобромин, триэтаноламин, триэтиламин, триметиламин, трипропиламин и трис-(гидроксиметил)метиламин (трометамин).
Соединения в соответствии с настоящим изобретением, которые включают основные азотсодержащие группы, могут быть кватернизированы с помощью таких агентов, как (С1-С4)-алкилгалогениды, например, метил-, этил-, изопропил-и трет-бутилхлорид, бромид и йодид; ди-(С1-С4)-алкилсульфаты, например, диметил-, диэтил- и диамилсульфат; (С10-С18)-алкилгалогениды, например, децил-, додецил-, лаурил-, миристил- и стеарилхлорид, бромид и йодид; и арил-(С1-С4)-алкилгалогениды, например, бензилхлорид и фенэтилбромид. При использовании таких солей можно получить как растворимые в воде, так и растворимые в масле соединения в соответствии с изобретением.
Предпочтительные указанные выше фармацевтические соли включают, но не ограничиваются только ними, ацетат, трифторацетат, безилат, цитрат, фумарат, глюконат, гемисукцинат, гиппурат, гидрохлорид, гидробромид, изетионат, манделат, меглюмин, нитрат, олеат, фосфонат, пивалат, фосфат натрия, стеарат, сульфат, сульфосалицилат, тартрат, тиомалат, тозилат и трометамин.
Соли присоединения кислот основных соединений в соответствии с изобретением получают путем введения в контакт формы свободных оснований с достаточным количеством целевой кислоты с получением соли традиционным способом. Свободное основание может быть регенерировано путем введения в контакт солевой формы с основанием и выделения свободного основания традиционным способом. Формы свободного основания в некоторой степени отличаются от своих соответствующих солевых форм определенными физическими свойствами, такими, как растворимость в полярных растворителях; тем не менее, для целей настоящего изобретения во всем остальном соли являются эквивалентными своим соответствующим формам свободных оснований.
Как уже было указано, фармацевтически приемлемые соли присоединения основания соединений в соответствии с изобретением образованы с металлами или аминами, такими как щелочные металлы и щелочноземельные металлы или органические амины. Предпочтительные металлы представляют собой натрий, калий, магний и кальций. Предпочтительные органические амины представляют собой N,N'-дибензилэтилендиамин, хлорпрокаин, холин, диэтаноламин, этилендиамин, N-метил-D-глюкамин и прокаин.
Соли присоединения основания кислотных соединений в соответствии с изобретением получают путем введения в контакт формы свободной кислоты с достаточным количеством целевого основания для получения соли традиционным способом. Форма свободной кислоты может быть регенерирована путем введения в контакт солевой формы с кислотой и выделения формы свободной кислоты обычным способом. Формы свободной кислоты в некоторой степени отличаются от своих соответствующих солевых форм определенными физическими свойствами, такими как растворимость в полярных растворителях, тем не менее, для целей настоящего изобретения во всем остальном соли являются эквивалентными своим соответствующим формам свободных кислот.
Если соединение в соответствии с изобретением содержит более, чем одну группу, которая способна к образованию фармацевтически приемлемых солей этого типа, то изобретение также охватывает составные соли. Примеры типичных составных солевых форм включают, но не ограничиваются только ними, битартрат, диацетат, дифумарат, димеглюмин, дифосфат, динатрий и тригидрохлорид.
В свете описанного выше можно понять, что выражение "фармацевтически приемлемая соль" в контексте данной заявки предназначено для обозначения активного компонента, который включает соединение в соответствии с изобретением в форме одной из его солей, особенно в том случае, если указанная солевая форма придает указанному активному соединению улучшенные фармакокинетические свойства по сравнению со свободной формой указанного активного соединения или любой другой солевой формой указанного активного соединения, которые использовались ранее. Фармацевтически приемлемая солевая форма активного компонента изначально может также придавать указанному активному соединению желаемое фармакокинетическое свойство, которым он ранее не обладал, а также может даже оказывать положительное влияние на фармакодинамику данного активного компонента в отношении его терапевтической эффективности в организме.
Кроме того, изобретение относится к лекарственным средствам, содержащим по меньшей мере одно соединение в соответствии с изобретением и/или его фармацевтически приемлемые производные, сольваты и стереоизомеры, включая их смеси во всех соотношениях, и необязательно наполнители и/или вспомогательные вещества.
Фармацевтические составы можно вводить в виде дозированных единиц, которые содержат заранее установленное количество активного соединения на дозированную единицу. Такая единица может включать, например, от 0,5 мг до 1 г, предпочтительно от 1 мг до 700 мг, более предпочтительно от 5 мг до 100 мг, соединения в соответствии с изобретением, в зависимости от состояния, подвергаемого лечению, способа введения и возраста, массы тела и состояния пациента, или фармацевтические составы можно вводить в виде дозированных единиц, которые содержат заранее установленное количество активного соединения на дозированную единицу. Предпочтительными составами дозированных единиц являются те, которые содержат суточную дозу или часть суточной дозы, как указано выше, или соответствующую ей порцию активного соединения. Кроме того, фармацевтические составы этого типа могут быть получены способом, который хорошо известен в области фармацевтики.
Фармацевтические составы могут быть приспособлены для введения при помощи любого приемлемого способа, например, путем перорального (включая буккальное или подъязычное), ректального, назального, местного (включая буккальное, подъязычное или трансдермальное), вагинального или парентерального (включая подкожное, внутримышечное, внутривенное или внутрикожное) введения. Такие составы могут быть приготовлены с помощью любого способа, известного в области фармацевтики, например, путем объединения активного соединения с наполнителем(ями) или вспомогательным(ыми) веществом(ами).
Фармацевтические составы, предназначенные для перорального введения, можно вводить в виде отдельных единиц, таких как, например, капсулы или таблетки; порошки или гранулы; растворы или суспензии в водных или неводных жидкостях; съедобных пен или пенящихся пищевых продуктов; или жидких эмульсий масло-в-воде или жидких эмульсий вода-в-масле.
Так, например, в случае перорального введения в виде таблетки или капсулы, активный ингредиент может быть объединен с пероральным, нетоксичным и фармацевтически приемлемым инертным наполнителем, таким как, например, этанол, глицерин, вода и т.п. Порошки получают путем измельчения соединения до необходимого малого размера и смешивания его с фармацевтическим наполнителем, измельченным аналогичным способом, таким как, например, пищевой углевод, такой как, например, крахмал или маннит.
Равным образом могут присутствовать ароматизатор, консервант, диспергирующее вещество и краситель.
Капсулы получают путем приготовления порошковой смеси, как описано выше, и заполнения нею формованных желатиновых капсул. Перед заполнением капсул к порошковой смеси можно добавлять придающие скользкость и смазывающие вещества, такие как, например, высокодисперсная кремниевая кислота, тальк, стеарат магния, стеарат кальция или полиэтиленгликоль в твердой форме. Для улучшения доступности лекарственного средства, заключенного в капсулу, также можно добавлять дезинтегрирующее вещество или солюбилизатор, такой как, например, агар-агар, карбонат кальция или карбонат натрия.
Кроме того, при желании или необходимости в смесь также можно добавлять пригодные связующие вещества, смазывающие вещества, дезинтеграторы, а также красители. Пригодные связующие включают крахмал, желатин, природные сахара, такие как, например, глюкоза или бета-лактоза, подсластители, полученные из кукурузы, природные и синтетические смолы, такие как, например, аравийская камедь, трагакантовая камедь или альгинат натрия, карбоксиметилцеллюлоза, полиэтиленгликоль, воски и т.п. Смазывающие вещества, которые можно применять в таких дозированных формах, включают олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п. Дезинтеграторы включают, но не ограничиваются только ними, крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и т.п. Таблетки получают, например, путем приготовления порошковой смеси, гранулирования или сухого прессования смеси, добавления смазывающего вещества и дезинтегратора и прессования полученной смеси в таблетки. Порошковую смесь готовят путем смешивания соединения, измельченного приемлемым образом, с разбавителем или основанием, как описано выше, и необязательно со связующим веществом, таким как, например, карбоксиметилцеллюлоза, альгинат, желатин или поливинилпирролидон, замедлителем растворения, таким как, например, парафин, усилителем абсорбции, таким как, например, четвертичная соль, и/или абсорбентом, таким как, например, бентонит, каолин или фосфат дикальция. Порошковую смесь можно гранулировать посредством ее смачивания связующим веществом, таким как, например, сироп, крахмальная паста, слизь акации или растворы целлюлозы или полимерных веществ и прессования ее через сито. В качестве альтернативы грануляции, порошковую смесь можно пропускать через таблетировочную машину, получая куски неправильной формы, которые распадаются, образуя гранулы. Гранулы могут быть смазаны посредством добавления стеариновой кислоты, стеарата, талька или минерального масла, чтобы предотвратить прилипание к таблетировочной литейной форме. После этого смазанную смесь спрессовывают, получая таблетки. Соединения в соответствии с изобретением также можно объединять с сыпучим инертным наполнителем и затем подвергать прямому прессованию, получая таблетки без осуществления стадий грануляции или сухого прессования. Таблетки также можно покрывать прозрачным или непроницаемым защитным слоем, состоящим из шеллакового герметизирующего слоя, слоя сахара или полимерного вещества и глянцевого слоя воска. К этим покрытиям также можно добавлять красители для возможности различения между разными дозированными единицами.
Жидкости для перорального введения, такие как, например, раствор, сиропы и эликсиры, могут быть приготовлены в виде дозированных единиц таким образом, чтобы они содержали заранее установленное количество соединения. Сиропы могут быть получены путем растворения соединения в водном растворе с пригодным ароматизатором, тогда как эликсиры готовят с применением нетоксичного спиртового наполнителя. Суспензии могут быть приготовлены путем диспергирования соединения в нетоксичном наполнителе. Также можно добавлять солюбилизаторы и эмульгаторы, такие как, например, этоксилированные изостеариловые спирты и полиоксиэтиленовые эфиры сорбита, консерванты, ароматические добавки, такие как, например, масло перечной мяты, или натуральные заменители сахара или сахарин, или другие искусственные подсластители и т.п.
При желании составы для перорального введения в виде дозированных единиц могут быть инкапсулированы в микрокапсулы. Также состав может быть приготовлен таким образом, чтобы пролонгировать или замедлить высвобождение, например, путем применения покрытий или введения вещества в виде частиц в полимеры, воск и т.п.
Соединения в соответствии с изобретением и соли, их сольваты и физиологически функциональные производные также можно вводить в виде липосомных систем доставки, таких как, например, небольшие однослойные пузырьки, большие однослойные пузырьки и многослойные пузырьки. Липосомы могут быть образованы с помощью различных фосфолипидов, таких как, например, холестерин, стеариламин или фосфатидилхолины.
Соединения в соответствии с изобретением и соли, их сольваты и физиологически функциональные производные могут быть также доставлены путем применения моноклональных антител в качестве индивидуальных носителей, к которым присоединены молекулы соединения. Соединения также могут быть соединены с растворимыми полимерами в качестве прицельных носителей лекарственных средств. Такими полимерами могут являться поливинилпирролидон, сополимер пирана, полигидроксипропилметакриламидофенол, полигидроксиэтиласпартамидофенол или полиэтиленоксидполилизин, замещенный пальмитоиловыми радикалами. Кроме того, соединения можно связывать с биоразлагаемыми полимерами, которые пригодны для обеспечения контролируемого высвобождения лекарственного средства, например полимолочной кислотой, поли-эпсилон-капролактоном, полигидроксимасляной кислотой, полиортоэфирами, полиацеталями, полидигидроксипиранами, полицианоакрилатами и перекрестно-сшитыми или амфипатическими блок-сополимерами гидрогелей.
Фармацевтические составы, предназначенные для трансдермального введения, можно вводить в виде независимых пластырей для пролонгированного, тесного контакта с эпидермисом реципиента. Таким образом, например, активное соединение может быть доставлено из пластыря путем ионтофореза, как в общих чертах описано в Pharmaceutical Research, 3(6), 318 (1986).
Фармацевтические соединения, предназначенные для местного введения, могут быть приготовлены в виде мазей, кремов, суспензий, лосьонов, порошков, растворов, паст, гелей, спреев, аэрозолей или масел.
Для лечения глаз или других наружных тканей, например рта и кожи, предпочтительно применяют составы в виде мази или крема для местного нанесения. Для приготовления состава в виде мази, активное соединение можно применять с парафиновым или смешиваемым с водой мазевым основанием. Альтернативно, для получения крема активное соединение может быть приготовлено с основой для крема типа масло-в-воде или основой вода-в-масле.
Фармацевтические составы, предназначенные для местного применения для глаз, включают глазные капли, в которых активное соединение растворено или суспендировано в приемлемом носителе, предпочтительно в водном растворителе.
Фармацевтические составы, предназначенные для местного введения в полость рта, включают леденцы, пастилки и жидкости для полоскания рта.
Фармацевтические составы, предназначенные для ректального введения, можно вводить в виде суппозиториев или клизм.
Фармацевтические составы, предназначенные для назального введения, в которых носитель представляет собой твердое вещество, включают крупнозернистый порошок, имеющий размер частичек, например, в пределах 20-500 микрон, который вводят путем вдыхания, то есть путем быстрого вдоха через нос из контейнера, содержащего порошок, который придерживают возле носа. Пригодные составы для введения в виде назального спрея или носовых капель с жидкостью в качестве носителя включают растворы активного вещества в воде или в масле.
Фармацевтические составы, предназначенные для введения путем ингаляции, включают тонкоизмельченные частички в виде тонкого порошка или аэрозоля, которые могут быть получены с помощью различных диспергирующих устройств под давлением при помощи аэрозолей, распылителей или инсуффляторов.
Фармацевтические составы, предназначенные для вагинального введения, можно вводить в виде маточных колец, тампонов, кремов, гелей, паст, пен или составов для распыления.
Фармацевтические составы, предназначенные для парентерального введения, включают водные или неводные стерильные растворы для инъекций, содержащие антиоксиданты, буферы, бактериостатические вещества и растворенные вещества, с помощью которых состав поддерживается изотоническим по отношению к крови реципиента, которого лечат; и водные или неводные стерильные суспензии, которые могут содержать суспензионную среду и загустители. Составы могут быть введены с помощью емкостей для однократного или многократного введения, например, запечатанных ампул и флаконов, и их можно хранить в лиофилизированном состоянии, при этом непосредственно перед введением необходимо только добавить стерильную жидкость-носитель, например, воду для инъекций. Растворы и суспензии для инъекций, приготовленные согласно рецептуре, могут быть приготовлены из стерильных порошков, гранул и таблеток.
Само собой разумеется, что дополнительно к предпочтительным описанным выше компонентам, составы также могут содержать другие вещества, которые используют в данной области техники для конкретных типов составов; например, составы, пригодные для перорального введения, могут содержать ароматизаторы.
Терапевтически эффективное количество соединения в соответствии с изобретением зависит от многих факторов, включая, например, возраст и вес животного, определенное состояние, которое необходимо лечить, и его тяжесть, природу лекарственного средства и способ введения, и в конечном счете оно может быть определено лечащим врачом или ветеринаром. Тем не менее, эффективное количество соединения в соответствии с изобретением, как правило, находится в пределах от 0,1 до 100 мг/кг веса тела реципиента (млекопитающего) в сутки и предпочтительно обычно находится в пределах от 1 до 10 мг/кг массы тела в сутки. Таким образом, фактическое суточное количество для взрослого млекопитающего весом 70 кг обычно может составлять от 70 до 700 мг, причем это количество можно вводить в виде отдельной дозы один раз в сутки или обычно в виде ряда отдельных доз (таких как, например, два, три, четыре, пять или шесть раз) в сутки, так что общая суточная доза является такой же самой. Эффективное количество его соли, сольвата или физиологически функционального производного может быть определено в виде части эффективного количества соединения в соответствии с изобретением как такового. Также можно предположить, что аналогичные дозы пригодны для лечения других состояний, описанных выше.
Кроме того, изобретение относится к лекарственным средствам, содержащим по меньшей мере одно соединение в соответствии с изобретением и/или его фармацевтически приемлемые соли и стереоизомеры, включая их смеси во всех соотношениях, и по меньшей мере одно другое активное соединение лекарственного средства.
Изобретение также относится к комплекту (набору), состоящему из отдельных упаковок
(а) эффективного количества соединения в соответствии с изобретением и/или его фармацевтически приемлемых солей и стереоизомеров, включая их смеси во всех соотношениях,
и
(б) эффективного количества другого активного соединения лекарственного средства.
Комплект содержит в себе пригодные емкости, такие как коробки, отдельные бутылочки, пакеты или ампулы. Комплект может включать, например, отдельные ампулы, каждая из которых содержит эффективное количество соединения в соответствии с изобретением и/или его фармацевтически приемлемых солей и стереоизомеров, включая их смеси во всех соотношениях,
и эффективное количество другого активного соединения лекарственного средства в растворенной или лиофилизированной форме.
Изобретение относится к соединениям в соответствии с изобретением, и их фармацевтически применимым солям, таутомерам и стереоизомерам, включая их смеси во всех отношениях, для применения в лечении опухолевых новообразований, метастаз опухолей, пролиферативных заболеваний мезангиальных клеток, гемангиомы, пролиферативной ретинопатии, ревматоидного артрита, атеросклеротической неоваскуляризации, псориаза, глазной неоваскуляризации, остеопороза, диабетов и ожирения, лимфолейкоза, лимфомы, малярии и гипертрофии предстательной железы.
Применение
Данные соединения пригодны в качестве фармацевтических активных соединений для млекопитающих, в особенности для людей, при лечении и контроле течения заболеваний. Эти заболевания включают пролиферацию опухолевых клеток, патологическую неоваскуляризацию (или ангиогенез), которая ускоряет рост солидных опухолей, неоваскуляризацию в глазу (диабетическая ретинопатия, возрастная дегенерация желтого пятна и т.п.) и воспаление (псориаз, ревматоидный артрит и т.п.), и пролиферативные заболевания мезангиальных клеток.
Настоящее изобретение включает применение соединений в соответствии с изобретением и/или их физиологически приемлемых солей и сольватов для получения лекарственного средства для лечения или предотвращения опухолевых новообразований, опухолевых заболеваний и/или метастаз опухолей. Опухолевое заболевание преимущественно выбирают из группы новообразование чешуйчатого эпителия, мочевого пузыря, желудка, почек, головы и шеи, пищевода, шейки матки, щитовидной железы, кишечника, печени, головного мозга, предстательной железы, мочеполовых путей, лимфатической системы, желудка, гортани, легкого, кожи, моноцитарный лейкоз, аденокарцинома легкого, немелкоклеточная карцинома легких, рак поджелудочной железы, глиобластома, рак молочной железы, острая миелоцитарная лейкемия, хроническая миелоцитарная лейкемия, острый лимфобластный лейкоз, хронический лимфолейкоз, лимфома Ходжкина, неходжкинская лимфома.
Равным образом включено применение соединений в соответствии с изобретением и/или их физиологически приемлемых солей и сольватов для получения лекарственного средства для лечения остеопороза, диабетов и ожирение.
Равным образом включено применение соединений в соответствии с изобретением и/или их физиологически приемлемых солей и сольватов для получения лекарственного средства для лечения или предотвращения заболевания, в которое вовлечен ангиогенез.
Заболевание такого типа, в которое вовлечен ангиогенез, представляет собой заболевание глаз, такое как васкуляризация сетчатки, диабетическая ретинопатия, возрастная дегенерация желтого пятна и т.п.
Ангиогенное заболевание преимущественно выбирают из группы:
диабетическая ретинопатия, артрит, рак, псориаз, саркома Капоши, гемангиома, миокардиальный ангиогенез, неоваскуляризация атеросклеротической бляшки, ангиогенные болезни глаз, хориоидальную неоваскуляризацию, ретролентальная фиброплазия, дегенерация желтого пятна, отторжение трансплантата роговицы, покраснение радужной оболочки, неоваскулярная глаукома, синдром Ослера-Веббера.
Пролиферативное заболевание мезангиальных клеток преимущественно выбирают из группы гломерулонефрит, диабетическая нефропатия, злокачественный нефросклероз, синдром тромботической микроангиопатии, отторжение трансплантата, гломерулопатия.
Применение соединений в соответствии с изобретением и/или их физиологически приемлемых солей и сольватов для получения лекарственного средства для лечения или предотвращения воспалительных заболеваний равным образом подпадает под объем правовой защиты в пределах объема настоящего изобретения. Примеры таких воспалительных заболеваний включают ревматоидный артрит, псориаз, контактный дерматит, отсроченная реакция гиперчувствительности и т.п.
Воспалительное заболевание преимущественно выбирают из группы
воспалительное заболевание кишечника, артрит, атеросклероз, астма, аллергии, воспалительные заболевания почек, множественный склероз, хроническое обструктивное заболевание легких, воспалительные заболевания кожи, заболевания пародонта, псориаз, стимулируемое Т-клетками иммунное заболевание.
Воспалительное заболевание кишечника предпочтительно выбирают из группы, включающей язвенный колит, болезнь Крона, неспецифический колит.
Стимулируемое Т-клетками иммунное заболевание предпочтительно выбирают из группы, включающей аллергический энцефаломиелит, аллергический неврит, отторжение трансплантата, реакция «трансплантата против хозяина», миокардит, тиреоидит, нефрит, системная красная волчанка, инсулинозависимый сахарный диабет
Заболевание артрит предпочтительно выбирают из группы, включающей ревматоидный артрит, остеоартрит, синдром Каплана, синдром Фелти, Синдром Шегрена, анкилозирующий спондилит, болезнь Стилла, хондрокальциноз, метаболический артрит, ревматическая атака, болезнь Рейтера, синдром Висслера.
Воспалительное заболевание почек предпочтительно выбирают из группы, включающей гломерулонефрит, повреждение гломерулярного фильтра, нефротический синдром, интерстициальный нефрит, волчаночный нефрит, синдром Гудпасчера, гранулематоз Вегенера, почечный васкулит, нефропатию IgA, идиопатическое заболевание почечных клубочков.
Воспалительное заболевание кожи предпочтительно выбирают из группы, включающей псориаз, атопический дерматит, контактная чувствительность, акне.
Равным образом оно охватывает применение соединений в соответствии с изобретением и/или их фармацевтически приемлемых солей и сольватов для получения лекарственного средства для лечения или предотвращения заболевания или состояний у млекопитающего, при этом согласно данному способу терапевтически эффективное количество соединения в соответствии с изобретением вводят больному млекопитающему, нуждающемуся в таком лечении. Терапевтическое количество варьируется в зависимости от конкретного заболевания и без излишних усилий может быть определено специалистом в данной области.
Настоящее изобретение также включает в себя применение соединений в соответствии с изобретением и/или их физиологически приемлемых солей и сольватов для получения лекарственного средства для лечения или предотвращения васкуляризации сетчатки глаза.
Равным образом оно охватывает применение соединений в соответствии с изобретением и/или их фармацевтически приемлемых солей для получения лекарственного средства для лечения и/или подавления заболевания вызванного опухолью у млекопитающего, при этом согласно данному способу терапевтически эффективное количество соединения в соответствии с изобретением вводят больному млекопитающему, нуждающемуся в таком лечении. Терапевтическое количество варьируется в зависимости от конкретного заболевания и без излишних усилий может быть определено специалистом в данной области.
Описанные соединения в соответствии с изобретением можно вводить в комбинации с другими лекарственными средствами, включая противораковые средства. Как используют в настоящем изобретении, термин «противораковое средство» относится к любому средству, которое вводят пациенту со злокачественным новообразованием для лечения рака.
Определенное выше противораковое лечение можно применять в виде монотерапии или дополнительно к описанным в настоящей заявке соединениям может включать в себя стандартное оперативное вмешательство или лучевую терапию или лекарственную терапию. Такая лекарственная терапия, например, химиотерапия или прицельная терапия, может включать одно или несколько, но предпочтительно одно из следующих противоопухолевых средств:
Алкилирующие средства
такие как алтретамин, бендамустин, бусульфан, кармустин, хлорамбуцил, хлорметин, циклофосфамид, дакарбазин, ифосфамид, импросульфан тозилат, ломустин, мельфалан, митобронитол, митолактол, нимустин, ранимустин, темозоломид, тиотепа, треосульфан, мехлороэтамин, карбоквон; апазиквон, фотемустин, глуфосфамид, палифосфамид, пипоброман, трофосфамид, урамустин, ТН-3024, VAL-0834;
Соединения платины
такие как карбоплатин, цисплатин, эптаплатин, гидрат мириплатина, оксалиплатин, лобаплатин, недаплатин, пикоплатин, сатраплатин; лобаплатин, недаплатин, пикоплатин, сатраплатин;
Средства, изменяющие ДНК
такие как амрубицин, бисантрен, децитабин, митоксантрон, прокарбазин, трабектедин, клофарабин;
амсакрин, бросталлицин, пиксантрон, ларомустин1,3;
Ингибиторы топоизомеразы
такие как этопозид, иринотекан, разоксан, собузоксан, тенипозид, топотекан, амонафид, белотекан, эллиптиния ацетат, ворелоксин;
Модификаторы микротрубочек
такие как кабазитаксел, доцетаксел, эрибулин, иксабепилон, паклитаксел, винбластин, винкристин, винорелбин, виндезин, винфлунин, фосбретабулин, тезетаксел;
Антиметаболиты
такие как аспарагиназа3, азацитидин, левофолинат кальция, капецитабин, кладрибин, цитарабин, эноцитабин, флоксуридин, флударабин, фторурацил, гемцитабин, меркаптопурин, метотрексат, неларабин, пеметрексед, пралатрексат, азатиоприн, тиогуанин, кармофур; доксифлуридин, элацитарабин, ралтитрексед, сапацитабин, тегафур2'3, триметрексат;
Противораковые антибиотики
такие как блеомицин, дактиномицин, доксорубицин, эпирубицин, идарубицин, левамизол, милтефозин, митомицин С, ромидепсин, стрептозоцин, валрубицин, зиностатин, зорубицин, даунуробицин, пликамицин; акларубицин, пепломицин, пирарубицин;
Гормоны/антагонисты
такие как абареликс, абиратерон, бикалутамид, бусерелин, калустерон, хлортрианизен, дегареликс, дексаметазон, эстрадиол, флуокортолон флуоксиместерон, флутамид, фулвестрант, гозерелин, гистрелин, лейпрорелин, мегестрол, митотан, нафарелин, нандролон, нилутамид, октреотид, преднизолон, ралоксифен, тамоксифен, тиротропин альфа, торемифен, трилостан, трипторелин, диэтилстильбэстрол; аколбифен, даназол, деслорелин, эпитиостанол, ортеронел, энзалутамид1'3;
Ингибиторы ароматазы
такие как аминоглутетимид, анастрозол, эксеместан, фадрозол, летрозол, тестолактон; форместан;
Низкомолекулярные ингибиторы киназ
такие как кризотиниб, дазатиниб, эрлотиниб, иматиниб, лапатиниб, нилотиниб, пазопаниб, регорафениб, руксолитиниб, сорафениб, санитиниб, вандетаниб, вемурафениб, босутиниб, гефитиниб, акситиниб; афатиниб, алисертиб, дабрафениб, дакомитиниб, динациклиб, довитиниб, энзастаурин, нинтеданиб, ленватиниб, линифаниб, линситиниб, маситиниб, мидостаурин, мотесаниб, нератиниб, орантиниб, перифосин, понатиниб, радотиниб, ригосертиб, типифарниб, тивантиниб, тивозаниб, траметиниб, пимазертиб, бриваниб аланинат, седираниб, апатиниб4, кабозантиниб S-малат1'3, ибрутиниб1'3, икотиниб4, бупарлисиб2, ципатиниб4, кобиметиниб1'3, иделалисиб1'3, федратиниб1, XL-6474;
Фотосенсибилизаторы
такие как метоксален3; порфимер натрия, талапорфин, темопорфин;
Антитела
такие как алемтузумаб, бесилесомаб, брентуксимаб ведотин, цетуксимаб, деносумаб, ипилимумаб, офатумумаб, панитумумаб, ритуксимаб, тозитумомаб, трастузумаб, бевацизумаб, пертузумаб2,3; катумаксомаб, элотузумаб, эпратузумаб, фарлетузумаб, могамулизумаб, нецитумумаб, нимотузумаб, обинутузумаб, окаратузумаб, ореговомаб, рамуцирумаб, рилотумумаб, силтуксимаб, тоцилизумаб, залутумумаб, занолимумаб, матузумаб, далотузумаб1,2,3, онартузумаб1'3, ракотумомаб1, табалумаб1'3, EMD-5257974, ниволумаб1'3;
Цитокины
такие как альдеслейкин, интерферон альфа3, интерферон альфа2а, интерферон альфа2b2,3; целмолейкин, тазонермин, тецелейкин, опрелвекин1,3, рекомбинантный интерферон бета-1а4;
Конъюгаты лекарственных препаратов
такие как денилейкин дифтитокс, ибритумомаб тиуксетан, йобенгуан I123, преднимустин, трастузумаб эмтансин, эстрамустин, гемтузумаб, озогамицин, афлиберцепт; цинтредекин бесудотокс, эдотреотид, инотузумаб озогамицин, наптумомаб эстафенатокс, опортузумаб монатокс, технеций (99mТс)
арцитумомаб1,3, винтафолид1,3;
Вакцины
такие как сипулейцел3, витеспен3, эмепепимут-S3, онкоВАКС4, риндопепимут3, троВакс4, MGN-16014, MGN-17034;
Прочие препараты
алитретиноин, бексаротен, бортезомиб, эверолимус, ибандроновая кислота, имиквимод, леналидомид, лентинан, метирозин, мифамуртид, памидроновая кислота, пэгаспаргаза, пентостатин, сипулейцел , сизофиран, тамибаротен, темсиролимус, талидомид, третиноин, висмодегиб, золедроновая кислота, вориностат; целекоксиб, циленгитид, энтиностат, этанидазол, ганетеспиб, идроноксил, инипариб, иксазомиб, лонидамин, ниморазол, панобиностат, перетиноин, плитидепсин, помалидомид, прокодазол, ридафоролимус, тасквинимод, телотристат, тимальфазин, тирапазамин, тоседостат, трабедерсен, убенимекс, вальсподар, гендицин4, пицибанил4, реолизин4, гидрохлорид ретаспимицина1,3, требананиб2,3, вирулизин4, карфилзомиб1,3, эндостатин4, иммукотел4, белиностат3, MGN-17034;
1 Предл. МНН (предложенное Международное Непатентованное Название)
2 Рекоменд. МНН (рекомендованное Международное Непатентованное Название)
3 Название в США (наименование препарата по Справочнику национальных непатентованных названий США)
4 МНН отсутствует
Доказательства действия фармакологических ингибиторов на пролиферацию/жизнеспособность опухолевых клеток in vitro
1.0 Предпосылки
В настоящем описании эксперимента раскрывается ингибирование пролиферации опухолевых клеток/жизнеспособность опухолевых клеток активными соединениями.
Клетки высевают приемлемой плотностью клеток в микротитрационные планшеты (96-луночного формата) и исследуемые вещества добавляют в виде серий концентраций. Через последующие четыре дня культивирования в содержащей сыворотку среде пролиферация опухолевых клеток/жизнеспособность опухолевых клеток может быть определена с помощью тест-системы аламаровый синий.
2.0. Процедура эксперимента
2.1. Клеточная культура
Например, коммерчески доступные линии клеток карциномы толстой кишки, линии клеток яичника, линии клеток предстательной железы или линии клеток молочной железы и т.д.
Клетки культивируют в среде. С интервалом в несколько дней, клетки отделяют от культуральной посуды с помощью раствора трипсина, и высевают в приемлемом разведении в свежую среду. Клетки культивируют при 37° по Цельсию и 10% СO2.
2.2. Высевание клеток
Определенное количество клеток (например, 2000 клеток) на культуру/лунку объемом 180 мкл культуральной среды высевают в микротитрационные планшеты (96-луночные клеточно-культуральные планшеты), используя многоканальную пипетку. Затем клетки культивировали в СО2 инкубаторе (37°С и 10% СО2).
2.3. Добавление исследуемых веществ
Исследуемые вещества растворяют, например, в ДМСО и затем используют в соответствующей концентрации (при необходимости в сериях разведений) в среде для культивирования клеток. Стадии разбавления могут быть адаптированы в зависимости от эффективности активных соединений и желаемого разброса концентраций. Среду для культивирования клеток добавляют к исследуемым веществам в соответствующих концентрациях. Добавление к клеткам исследуемых веществ можно осуществлять в тот же самый день, что и высевание клеток. Для этой цели в каждом случае 20 мкл раствора вещества из предварительно разбавленной пластины добавляют в культуры/лунки. Клетки культивируют в течение еще 4-х дней при 37° по Цельсию и 10% СО2.
2.4. Измерение цветной реакции
В каждом случае добавляют 20 мкл реагента аламаровый синий на лунку, и микротитрационные планшеты инкубируют, например, в течение еще семи часов в СO2 инкубаторе (при 37°С и 10% СO2). Планшеты измеряют в считывающем устройстве с флуоресцентным фильтром с длиной волны в 540 нм. Непосредственно перед измерением планшеты можно осторожно встряхнуть.
3. Оценка
Значение оптической плотности контрольной среды (отсутствие клеток и применяемых исследуемых веществ) вычитают из всех других значений оптической плотности. Контрольные варианты (клетки без исследуемого вещества) устанавливают равными 100 процентам, а все остальные значения оптической плотности устанавливают по отношению к ней (например, в % от контроля):
Подсчет:
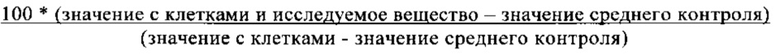
Значения IC50 (50% ингибирование) определяют при помощи статистических программ, таких как, например, RS1.

Определение ингибирования пролиферации ингибиторами метионинаминопептидазы 2 в тесте на пролиферацию БДУ (клеточный анализ)
Ингибирование пролиферации определяют включением бромдезоксиуридина (БДУ) в эндотелиальные клетки пупочной вены человека (ЭКПВЧ, PromoCell, С-12200). ЭКПВЧ культивируют при 37°С и 5% CO2 в базальной среде (PromoCell, С-22200) с добавлением смеси (PromoCell, С-39225). После отделения клеток при помощи трипсин/EDTA, определяют количество живых клеток, и клетки высевают плотностью 1000 клеток на полость в общем объёме 175 мкл (полости заранее покрывают или дополнительной культуральной средой в течение 1-2 часов при 37°С или посредством 1.5% желатина в течение 0.5-2 часов при 37°С). После культивирования в течение 24 часов, исследуемые вещества добавляют в различных концентрациях (например, конечные концентрации от 30 мкМ до 0.03 нм в 10-кратных стадиях разбавления) и объеме 25 мкл. Концентрацию ДМСО удерживают постоянной при 0.3%. После культивирования в течение в общем 48 или 72 часов добавляют 20 мкл бромдезоксиуридина (Roche, # 11647229001, разбавленный 1:1000 в культуральной среде, конечная концентрация 10 мкМ), и культивирование продолжают в течение еще от 20 до 24 часов. После инкубации с исследуемыми веществами в течение в общем 72 или 96 часов, культуральную среду удаляют, и иммуногистохимическое определение осуществляют для выявления включения БДУ (БДУ ELISA, Roche, # 11647229001). Таким образом, клетки обрабатывают фиксатором в течение 30 мин при комнатной температуре и затем инкубируют с анти-БДУ антителом, меченным пероксидазой (разбавлено 1:100 в буфере для разведения антител) в течение 60 мин при комнатной температуре. После трехкратного промывания посредством 1-кратно концентрированного буфера DPBS (Gibco, # 14200), ферментативную реакцию инициируют в растворе субстрата ТМВ. Цветное проявление останавливают через 15 мин добавлением 25 мкл 1 М раствора серной кислоты. Определение оптической плотности осуществляют в течение 5 мин путем измерения при длине волны 450 нм. Применяемые контрольные варианты представляют собой полости, содержащие обработанные посредством ДМСО клетки (100% контроль) или пустые полости (пустое значение). Чувствительность этого теста к ингибиторам метионинаминопептидазы проверяют и подтверждают при помощи ингибитора фумагиллин.
Измерение активности MetAP-2
Активность MetAP-2 определяют при помощи ферментативных реакций сочетания. В качестве субстрата используют Трипептид Met-Arg-Ser (MAS). Высвобожденный метионин сначала преобразуют в Metox и Н2О2 посредством L-аминооксидазы (ААО). Во второй стадии пероксидаза (POD) при помощи Н2О2 катализирует окисление лейко-красителя дианизидин до дианизидинаох, увеличение которого определяют фотометрически при 450 нм.
Активность MetAP-2 может быть записана непрерывно в качестве кинетики. Схема реакции показывает, что один моль дианизидинаох образуется на моль метионина. Поэтому ферментативную активность MetAP-2 можно подсчитать непосредственно как Д абсорбцию за единицу времени. Проверка активности MetAP-2 (моль Met/единицу времени) возможна при помощи коэффициент экстинкции дианизидинаох.
Изменение экстинкции за единицу времени изображают графически и подсчет наклона осуществляют в визуально линейной области реакции.
Активность соединений представлена в Таблице 1.
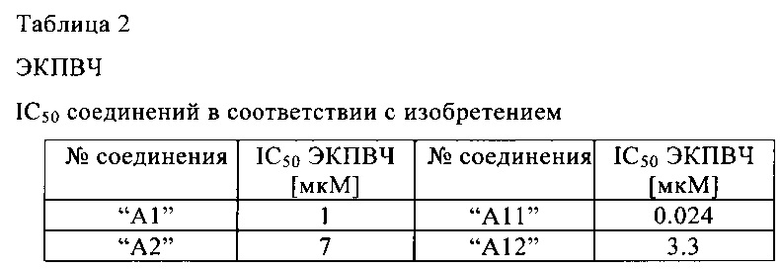
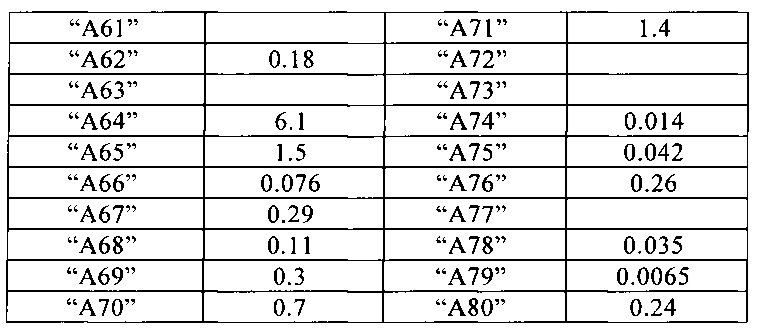
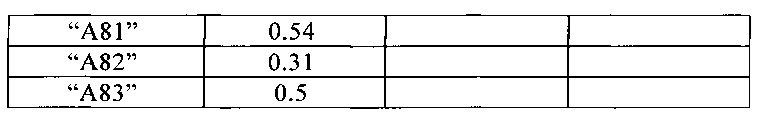
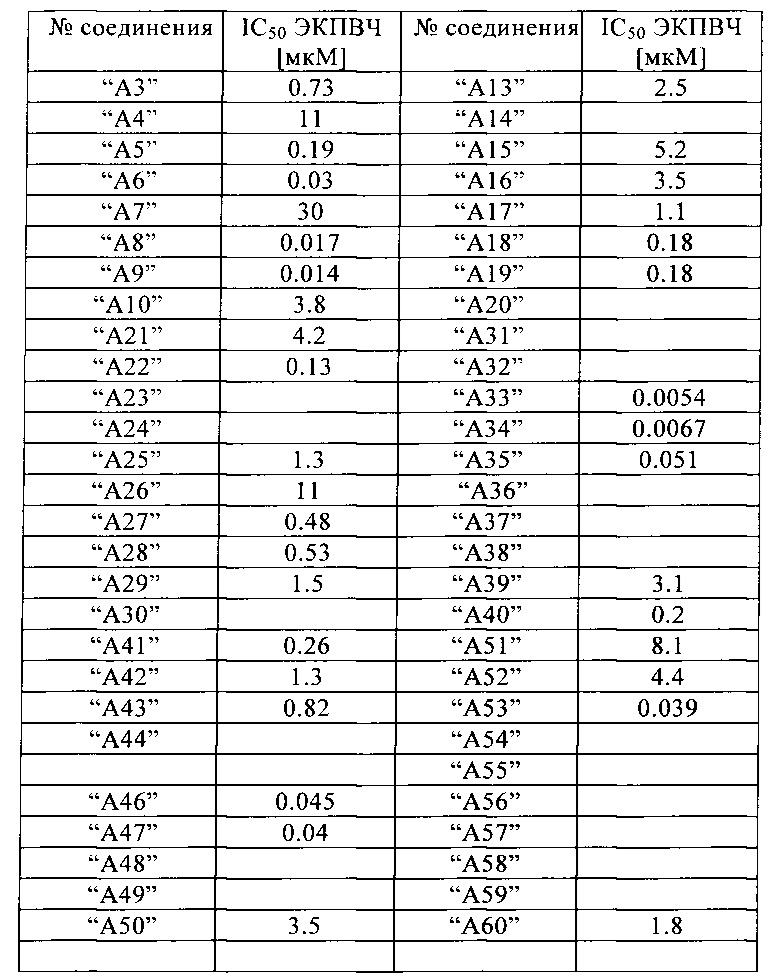
Пролиферация ЭКПВЧ, определенная количество посредством включения БДУ
ЭКПВЧ означает эндотелиальные клетки пупочной вены человека
Активность соединений представлена в Таблице 2.
Цель/Определение анализа
Пролиферацию ЭКПВЧ измеряют после 5-дневного инкубационного периода, используя встраивание БДУ в качестве меры активности клеточного цикла. Клетки инкубируют в присутствии или отсутствие исследуемых веществ. В течение последних от 18 до 24 часов инкубационного периода к среде добавляют БДУ. БДУ встраивается в ДНК, когда клетки проходят через S-фазу (синтез ДНК) клеточного цикла. Клетки фиксируют, и количество встроенного БДУ можно определить количественно, используя коммерчески доступную ELISA для выявления БДУ.
Этот анализ был разработан для скрининга исследуемых веществ для проекта MetAP2, но также может быть применен для оценки воздействия любого вещества, которое оказывает влияние на пролиферацию ЭКПВЧ.
Реагенты
EGM MV - среда для культивирования клеток
Трипсин/EDTA (0,5% /раствор 0,53 ммМ)
Забуференный фосфатом физраствор Дульбекко без Са и Mg
Клеточная пролиферация ELISA БДУ колориметрический
ДМСО
Референтные соединения
Эталон Эббота А-832234 MSC2129790
TNP-470 MSC1902850
Процедура
ЭКПВЧ как следует культивируют в среде EGM MV и применяют между пассажами 3 и 8.
День 1 - Пластинчатые клетки
Пипетируют 75 мкл/лунку питательной среды EGM MV (Promocell) в 96-луночный планшет, ряд Н лунок получают только среду, без клеток для холостого контрольного реагента.
Инкубируют планшет при 37°С при подготовке клеток.
Сбор ЭКПВЧ трипсином, как обычно:
Аспирируют культуральную среду, клеточный монослой промывают один раз при помощи 10 мл PBS, добавляют 2 мл раствора трипсина на колбу Т75 см и инкубируют при 37°С в течение 2-5 мин для отделения клеток.
Выполаскивают клетки из колбы посредством 10 мл EGM MV и переносят в центрифужную пробирку.
Центрифугируют 5 мин при 400 xg, ресуспендируют и подсчитывают. Регулируют концентрацию клеток до 1е4 клеток/мл.
В планшете, приготовленном с 75 мкл/лунку, пипетируют 100 мкл/лунку = 1000 клеток/лунку в 175 мкл/лунку общего объема.
Планшет инкубируют при 37°С в течение ночи.
День 2 - Добавление исследуемых веществ
В общем, исследуемые вещества доставляют диспенсарием при 10 мм в REMP пробирках.
Исследуемые вещества предварительно разбавляют в ДМСО и затем готовят рабочие разведения в культуральной среде для добавления в планшет с клетками.
Диапазон концентраций для исследуемых веществ составляет 30 мкМ, серийные 3-кратные разведения с 6-точечной кривой.
Референтные соединения -
MSC 1902850 TNP-270 начало при 30 нм (1:1000 предварительное разведение)
MSC 2129790 начало при 300 нм (1:100 предварительное
разведение)
Референтные соединения должны быть предварительно разведены в ДМСО для создания кривой концентраций, в которой ожидаемое ЕС50 упадет в середине 6-точечной кривой. 10 мМ маточный раствор референтных соединений предварительное разводят в ДМСО, и затем добавляют в планшет, как описано ниже.
Предварительное разведение исследуемых веществ в ДМСО:
В 96-луночном полипропиленовом планшете с круглым дном:
Строка А - помещают 20 мкл 10 мМ маточного раствора исследуемого вещества в ДМСО (или референтные соединения предварительно разведенные как указано выше).
Строка В-Н вводят 20 мкл ДМСО
Серийно разбавляют 3-кратно переносом 10 мкл из строки А в строку В, смесь и перенос 10 мкл в строку С, и т.д. до строки F.
Строка G является для 100 % = необработанной, только ДМСО. Это нейтральное референтное значение = значение в 0 % эффект в Assay Explorer.
Строка Н представляет собой холостой реагент без клеток, только среда. Это референтная шкала/тип ингибирования = значение в -100 % эффект в Assay Explorer.
Рабочие разведения в культуральной среде:
В 96-луночном полипропиленовом планшете с круглым дном:
Вводят 244 мкл культуральной среды/лунку.
Переносят 6 мкл разбавления ДМСО в лунки со средой для культивирования клеток = 1:41,6 разбавление = 8-кратная концентрация.
Переносят 25 мкл/лунку рабочего разведения в клеточные планшеты с 175 мкл, = 1:8 разбавление.
Из 10 мМ маточного раствора конечное разбавление составляет 1:333 (т.е. 41.6 х 8) для конечной концентрации в 30 мкМ в исследуемом планшете, все лунки содержат 0.3% ДМСО.
Планшет инкубируют при 37°С до 4 дня.
День 4 - добавление БДУ
Маточный раствор БДУ представляет собой 10 мМ в PBS (1000-кратный исходный раствор).
Готовят рабочее разведение 100 мкМ посредством его разведения 1:100 в культуральной среде. На каждый планшет требуется 2.2 мл. Применяют 22 мкл БДУ раствора в 2.2 мл среды EGM MV.
Пипетируют 20 мкл/лунку (1:10 разбавление). Конечная концентрация = 10 мкМ БДУ.
Инкубируют планшет в течение 18-24 ч 37°С.
День 5 - Фиксация, денатурирование, ELISA - следуйте инструкциям из набора со следующими изменениями в объеме:
Вытряхивают среду, слегка прижимают на бумажных полотенцах, чтобы удалить всю среду.
Добавляют 100 мкл раствора FixDenat из набора и инкубируют при комнатной температуре в течение 30 мин.
Вытряхивают FixDenat и слегка прижимают на бумажных полотенцах.
Недолгое время дают пластинам высохнуть на воздухе (1-2 мин), позволяя спирту в фиксаторе испариться.
Готовят рабочий раствор конъюгата анти-БДУ-пероксидазы каждый раз свежим разбавлением исходного раствора 1:100 в буфере для разбавления антител, поставляемом в наборе.
На каждый планшет требуется 5 мл, применяют 50 мкл в 5 мл буфера для разбавления антител.
Исходный раствор конъюгата анти-БДУ-пероксидазы изготавливают путем растворения лиофилизированного материала в 1.1 мл воды MilliQ. Исходный материал хранят при 4°С в течение нескольких недель, длительный срок -20°С.
Добавляют 50 мкл/лунку конъюгата анти-БДУ-пероксидазы и инкубируют 60-90 мин при комнатной температуре на встряхивающем устройстве для планшетов Eppendorf 300 об/мин.
Раствор антител вытряхивают, и планшет промывают 3х посредством 225 мкл/лунку промывочного раствора (поставляется в наборе или также можно использовать PBS с Ca/Mg).
Добавляют 100 мкл/лунку субстрата и инкубируют при комнатной температуре в течение 5-10 мин.
Добавляют 25 мкл/лунку 1 М H2SO4 останавливающего раствора и планшет считывают при 450 нм/референтное значение 690 нм в Tecan InfiniteM200.
Примечание:
Альтернативно может быть использована следующая смесь субстратов. Используют 100 мл/лунку и 50 мкл 1М H2SO4 останавливающего раствора. Длины волн для измерения, как указано выше.
Субстрат: каждый раз свежая смесь
Цитрат/фосфатный буфер рН 5 9 мл
1 мг/мл тетраметилбензидин в ДМСО 1 мл
К каждым 10 мл субстрата добавляют 2 мкл 30% Н2О2 непосредственно перед использованием

Смесь 243 мл лимонной кислоты + 257 мл двузамещенного фосфата Na до достижения рН 5.0
Доводят объем до 1000 мл с MilliQ водой 3,3',5,5'Тетраметилбензидин Merck VWR 1.08622 Структура планшета - Конечные концентрации
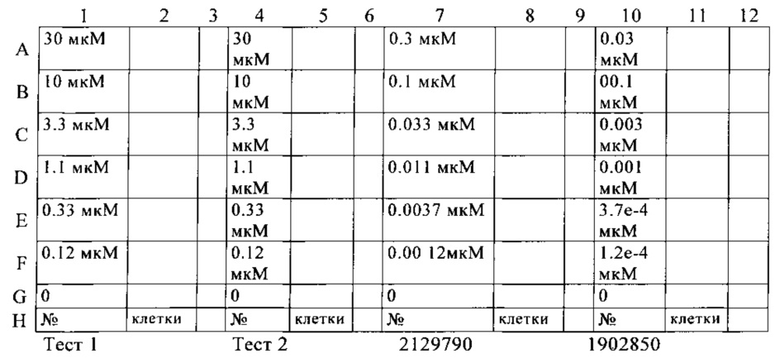
Все вещества прогоняют в трех экземплярах.
Статистические методы/Анализ данных
Референтные соединения прогоняют в каждом анализе. Ожидаемые значения являются следующими:
8е-10М (диапазон 2е-10М - 1е-9М) для MSC1902850A
2е-8М (диапазон 8е-9М - 6е-8М) для MSC2129790А
Фоновая активность - пустое значение или измерительная шкала = лунки без каких-либо клеток, должны быть 10% или меньше нейтрального референтного значения (необработанные клетки).
Данные анализируют, используя программу Assay Explorer. Вкратце, контрольную пробу вычитают из всех значений, тройные экземпляры усредняют и нормализуют для необработанных. ЕС50 определяют из общей сигмовидной кривой 4 параметров (уравнение Хилла у = (s0 - slnf) / (1 + ( х / AC50)∧nHill) + slnf) в Assay Explorer, Symyx).
Обработанные данные (ЕС50 или % эффекта, если нет ЕС50, если достигнуто, эффективность) загружаются непосредственно из Assay Explorer в MSRDB.
Соображения безопасности
Исследуемые вещества имеют неизвестную активностью и должны быть обработаны с обычными мерами предосторожности. Обязательно использовать перчатки и лабораторный халат. При работе с концентрированными маточными растворами в ДМСО, рекомендовано использование нитриловых, а не латексных перчаток.
Все загрязненные расходные материалы (наконечники, трубки, пластины) утилизируют в цитотоксических лабораторных корзинах для отходов, помеченных соответствующей наклейкой (2.29728.888).
Список необходимых химикатов, расходных материалов и оборудования
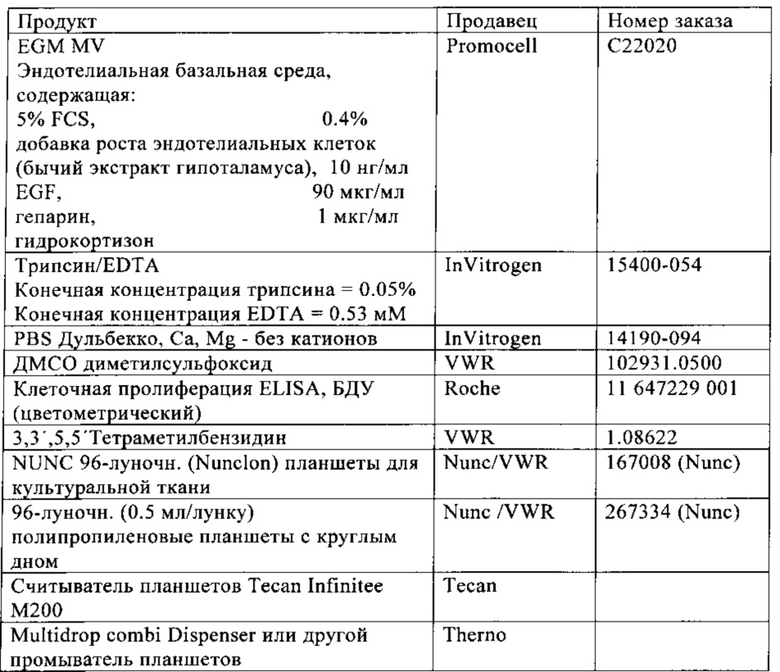

Образец растворителя:
Буфер: 3.954 г дигидрофосфата моногидрата натрия+ 6.024 г хлорида натрия + 950 мл сверхчистой воды рН устанавливают с применением 0.1 М NaOH или 0.1 М НСl.
Получение образца:
Образцы встряхивают при 37°С и 450 об/мин в течение 24 ч. Через приблизительно 7 ч, проверяют рН образцов и при необходимости регулируют.
Также проверяют, присутствует ли образец по-прежнему в избытке.
Непосредственно в конце 24 ч периода встряхивания, образцы снова проверяют относительно рН и осадка.
Блок сверхчистой воды: градиент MilliQ, ультратонкий фильтр, прибор: F3PN37462D
Встряхивающее устройство: TiMix control, Bühler
Инкубационный колпак: ТН 15 Bühler
Измеритель рН: прибор 766 Calimatic Knick: рН 1
Электрод рН: InLab 423 Mettler
Рацемические конечные продукты соединений в соответствии с изобретением или рацемические промежуточные продукты могут быть легко разделены как на аналитической, так и на препаративной шкале посредством хиральной ВЭЖХ или колонки SFC.
ЖХ-МС
колонка: Chromolith RP-18e 100-3 растворители:
А: вода + 0.05% муравьиная кислота
В: ацетонитрил + 0.05% муравьиная кислота
поток: 2.4 мл/мин
Градиент:
В: 0 -> 2.8 мин; 4% -> 100% В: 2.8 -> 3.3 мин; 100% время: 3.3 мин
* ЖХ-МС:
Колонка: XBridge С8, 3.5 мкМ, 4.6 х 50 мм; растворитель А: вода + 10 Мм NH4HCO3; Растворитель В: ACN; поток: 1 мл/мин; градиент: 0 мин: 5 % В, 8 мин 100 % В, 8.1 мин: 100 % В, 8.5 мин: 5% В, 10 мин 5% В.
Все приведенные выше и ниже температуры указаны в градусах Цельсия °С В последующих примерах "обычная обработка" обозначает: при необходимости добавляют воду, рН устанавливают, при необходимости, до значений от 2 до 10, зависимости от строения конечного продукта, смесь экстрагируют этилацетатом или дихлорметаном, фазы разделяют, органическую фазу высушивают над сульфатом натрия и упаривают, и остаток очищают при помощи хроматографии на силикагеле и/или кристаллизацией.
Схемы синтеза для получения соединений в соответствии с настоящим изобретением: а)
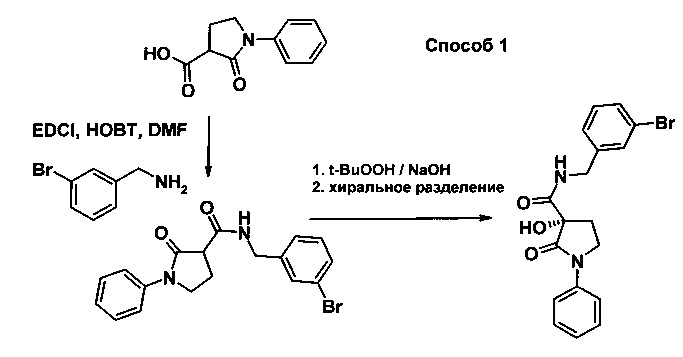
б)
в)
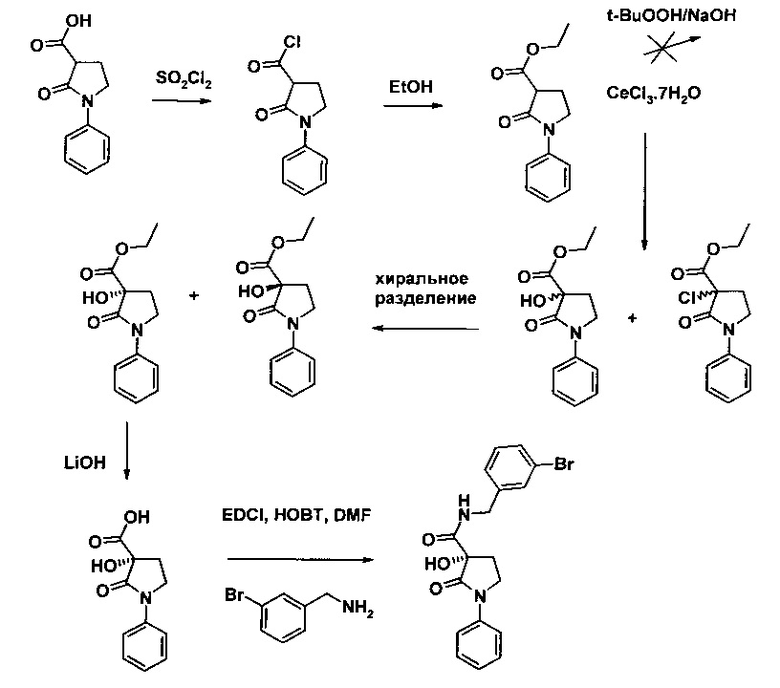
Способ 2
а) Способ 1: Кислоту преобразуют в соответствующий амид в амидном сочетании и после этого окисляют на углероде между двумя карбоксильными группами с применением третичного бутилгидропероксида в основной среде с получением спирта (с последующим разделением энантиомеров посредством хроматографии).
б) Способ 2: Альтернативно, было обнаружено, что при тех же самых окислительных условиях, которые описаны в способе 1 для амида, этиловый эфир исходной кислоты не может быть окислен. Тем не менее, это удается осуществить хлоридом церия. Производное хлора, полученное с 30%, может быть разделено на энантиомеры аналогично спиртам, а затем дериватизировано далее (другие реакции не показаны в настоящей заявке, однако затем имеются продуты, например, "А39", "А43м и "А61").
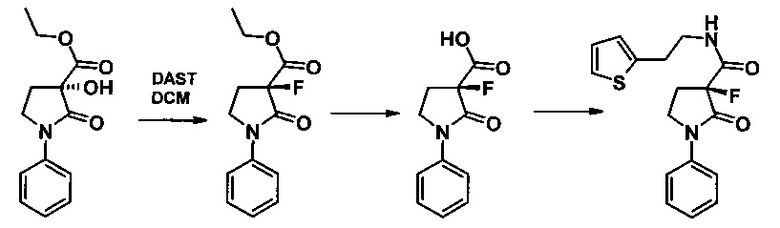
в) Тем не менее, применение фторида церия не обеспечивает аналогичное производное фтора. Реакция спиртового соединения с DAST (трифторид диэтиламиносеры) в дихлорметане приводит к целевому аналогу фтора. Тестирование подтверждает инверсию в центре асимметрии, которая ожидается из механистических соображений фторирования спиртов с использованием DAST.
г)
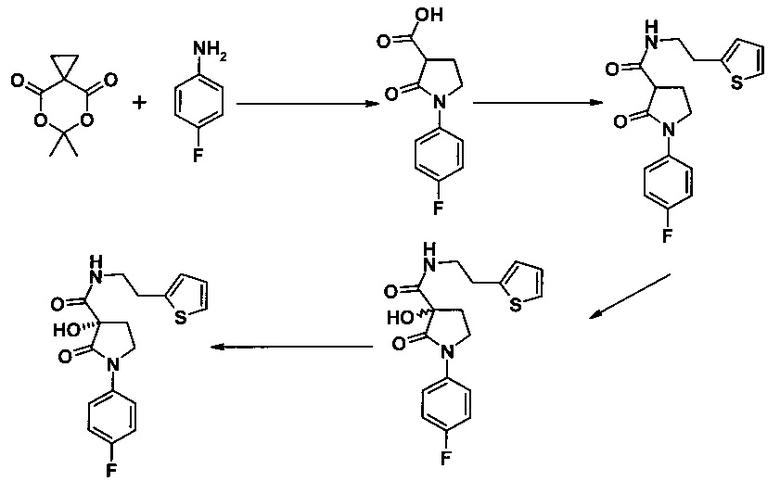
В г) показано, как могут быть получены N-ариллактамкарбоновые кислоты. Этот способ можно осуществить легко, если соединение азота является жидким. Установлено, что совместное плавление исходных веществ, если соединение азот-арил не является жидким, является невыгодным. Тем не менее, получают целевой продукт, если соединение азот-арил плавится и к этому расплаву добавляют сложный эфир дикарбоновой кислоты (кислота Мельдрума).
д)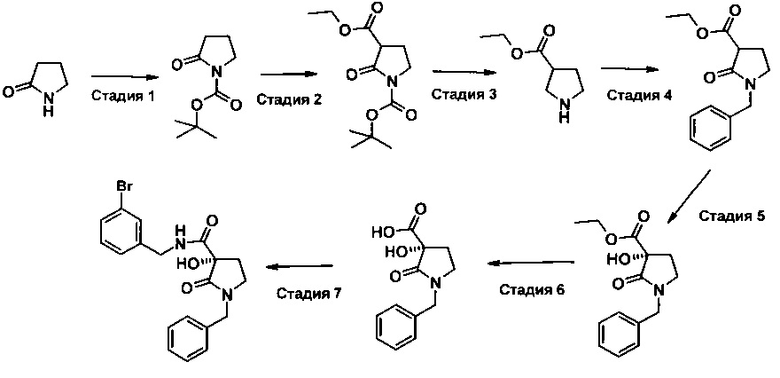 д) показан способ получения N-алкариллактамкарбоновой кислоты,
д) показан способ получения N-алкариллактамкарбоновой кислоты,
е)
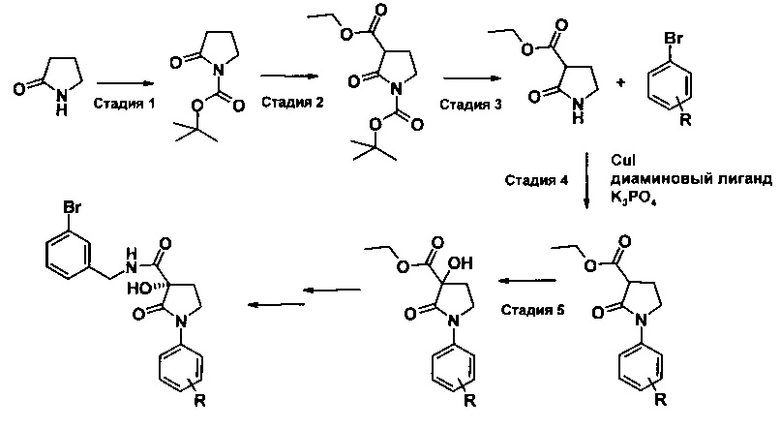
е) показан другой альтернативный способ, который осуществляют, чтобы сделать доступными арильные радикалы на лактаме азота, в котором аналогичное соединение азота не является жидким. В этом случае, лактам азота сочетают с арилгалогенидом, стадия, которую предпочтительно катализируют посредством соединений переходных металлов.
Пример 1
Синтез 3-хлор-5-фтор-бензиламида 3-гидрокси-1-(4-метансульфоксиминоил-фенил)-2-оксо-пирролидин-3-карбоновой кислоты ("А64")
1.1
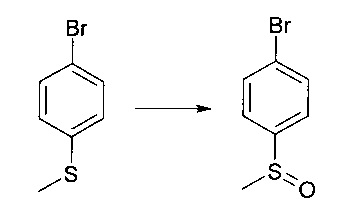
0.73 мл 30% раствора Н2О2 добавляют при 0°С к раствору 1 г 4-бромтиоанизола в 5 мл уксусной кислоты. Смесь перемешивают в течение 12 ч при КТ и обрабатывают посредством 10% раствора NaOH. Водную фазу экстрагируют этилацетатом. Органическую фазу промывают насыщенным раствором NaCl и сушат над Na2SO4. Удаление растворителя обеспечивает 0.97 г сырого продукта, который применяют в следующей стадии без дополнительной очистки.
1.2
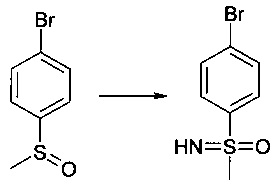
223 мг азида натрия добавляют по каплям при 0°С к раствору 900 мг 1-бром-4-метансульфинил-бензола в 18 мл хлороформа. Смесь перемешивают при 0° в течение 12 ч и добавляют ледяную воду. Обычная обработка обеспечивает 600 мг сырого продукта, который применяют в следующей стадии без дополнительной очистки.
1.3 253 мг 3-хлор-5-фтор-бензил амида 3-гидрокси-2-оксо-пирролидин-3-карбоновой кислоты (описано в WO 2013/149704), 359 мг карбоната калия, 382 мг N',N'-диметил-этан-1,2-диамина и 330 мг йодида меди(I) последовательно добавляют к раствору 200 мг сульфоксимина из стадии 1.2 в 12 мл дегазированного диоксана. Смесь подвергают реакции в течение 2 ч при 140 °С в микроволновой печи. Смесь фильтруют через целит, и растворители удаляют в вакууме. Препаративная ВЭЖХ обеспечивает 55 мг "А64" (диастереомерная смесь);
253 мг 3-хлор-5-фтор-бензил амида 3-гидрокси-2-оксо-пирролидин-3-карбоновой кислоты (описано в WO 2013/149704), 359 мг карбоната калия, 382 мг N',N'-диметил-этан-1,2-диамина и 330 мг йодида меди(I) последовательно добавляют к раствору 200 мг сульфоксимина из стадии 1.2 в 12 мл дегазированного диоксана. Смесь подвергают реакции в течение 2 ч при 140 °С в микроволновой печи. Смесь фильтруют через целит, и растворители удаляют в вакууме. Препаративная ВЭЖХ обеспечивает 55 мг "А64" (диастереомерная смесь);
'Н ЯМР 400 МГц, ДМСО-d6: δ [част. на млн] 8.79 (t, J = 6.40 Гц, 1H), 7.90-7.96 (m, 4Н), 7.26-7.29 (m, 1Н), 7.20 (s, 1Н), 7.10 (d, J = 9.60 Гц, 1Н), 6.87 (s, 1Н), 4.35-4.41 (m, 1Н), 4.20-4.27 (m, 2Н), 3.90-3.93 (m, 2Н), 3.04 (d, J = 0.80 Гц, 3Н), 2.58-2.62 (m, 1Н), 2.12-2.19 (m, 1Н).
Пример 2
Синтез 3,5-дифтор-бензиламида (S)-3-гидрокси-1-(1Н-индазол-5-ил)-2-оксо-пирролидин-3-карбоновой кислоты ("А75") и 3,5-дифтор-бензиламида (R)-3-гидрокси-1-(1Н-индазол-5-ил)-2-оксо-пирролидин-3-карбоновой кислоты
2.1

Раствор 11 г 6,6-диметил-5,7-диокса-спиро[2.5]октан-4,8-диона и 7 г 5-аминоиндазола в 50 мл ацетонитрила и 50 мл ДМФА перемешивают при 80°С в течение 12 ч.
Растворители удаляют, и обычная обработка обеспечивает 13 г 1 -(1Н-индазол-5-ил)-2-оксо-пирролидин-3-карбоновой кислоты.
2.2
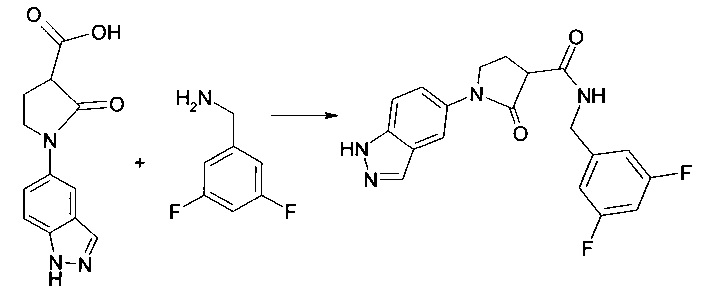
15 мл 4-Метилморфолина и 16 г HATU (3-оксид гексафторфосфат 1-[бис(диметиламино)метилен]-1Н-1,2,3-триазоло[4,5-b]пиридиния) добавляют к раствору 8.5 г 1-(1Н-индазол-5-ил)-2-оксо-пирролидин-3-карбоновой кислоты в 20 мл ДМФА. Раствор перемешивают в течение 20 минут при КТ и добавляют к раствору 6 г 3,5-дифторбензиламина в 20 мл ДМФА. Смесь перемешивают при 60 °С в течение 2 ч. Удаление растворителей и обычная обработка обеспечивают 9 г 3,5-дифтор-бензиламида 1-(1Н-индазол-5-ил)-2-оксо-пирролидин-3-карбоновой кислоты.
2.3

15.5 г магния монопероксифталата гексагидрата добавляют к раствору 8.5 г 3,5-дифтор-бензиламида 1-(1Н-индазол-5-ил)-2-оксо-пирролидин-3-карбоновой кислоты в 50 мл ДМФА. Суспензию желтого цвета перемешивают при 60 °С в течение 12 ч. После удаления растворителя и обычной обработки остаток очищают хроматографией (силикагель); выход: 5.1 г желтого масла 3,5-дифтор-бензиламида (S)-3-гидрокси-1-(1Н-индазол-5-ил)-2-оксо-пирролидин-3-карбоновой кислоты ("А75") и 3,5-дифтор-бензиламида (R)-3-гидрокси-1-(1Н-индазол-5-ил)-2-оксо-пирролидин-3-карбоновой кислоты.
2.4
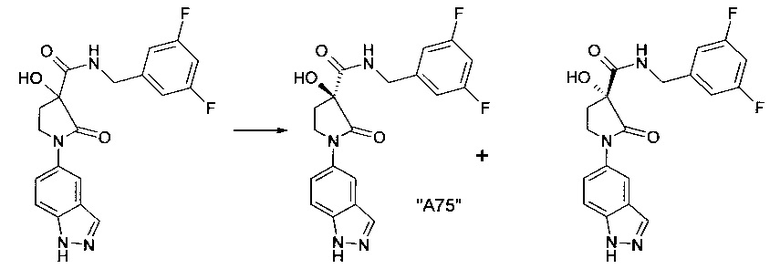
Разделение 5.1 г смесей энантиомеров осуществляют при помощи SF хроматографии.
Колонка: ChiralPAK AS-H
Элюент: СО2:метанол = 80:20
Длина волны: 220 нм
Поток: 100 мл/мин
Выход:
1.4 г 3,5-дифтор-бензиламида (S)-3-гидрокси-1-(1Н-индазол-5-ил)-2-оксо-пирролидин-3-карбоновой кислоты ("А75"),
1.3 г 3,5-дифтор-бензиламида (R)-3-гидрокси-1-(1Н-индазол-5-ил)-2-оксо-пирролидин-3-карбоновой кислоты ("А75");
"А75": ЖХ-МС 1.776 мин; [М+Н+] [387.1];
'Н ЯМР (500 МГц, ДМСО-d6) δ [част. на млн] 13.07 (s, 1H), 8.68 (t, J= 6.4 Гц, 1Н), 8.09 (d, J= 10.3 Гц, 1H), 7.91 (d, J= 1.6 Гц, 1H), 7.76 (dd, J= 9.0, 2.0 Гц, 1Н), 7.56 (t, J= 7.6 Гц, 1Н), 7.05 (tt, J = 9.4, 2.3 Гц, 1H), 7.03 - 6.97 (m, 2Н), 6.72 (s, 1Н), 4.42 (dd, J= 15.8, 6.8 Гц, 1H), 4.27 (dd, J = 15.8, 6.0 Гц, 1H), 3.96 - 3.87 (m, 2H), 2.63 (ddd, J= 12.0, 6.9, 4.9 Гц, 1H), 2.16 (dt, J = 12.9, 7.5 Гц, 1H).
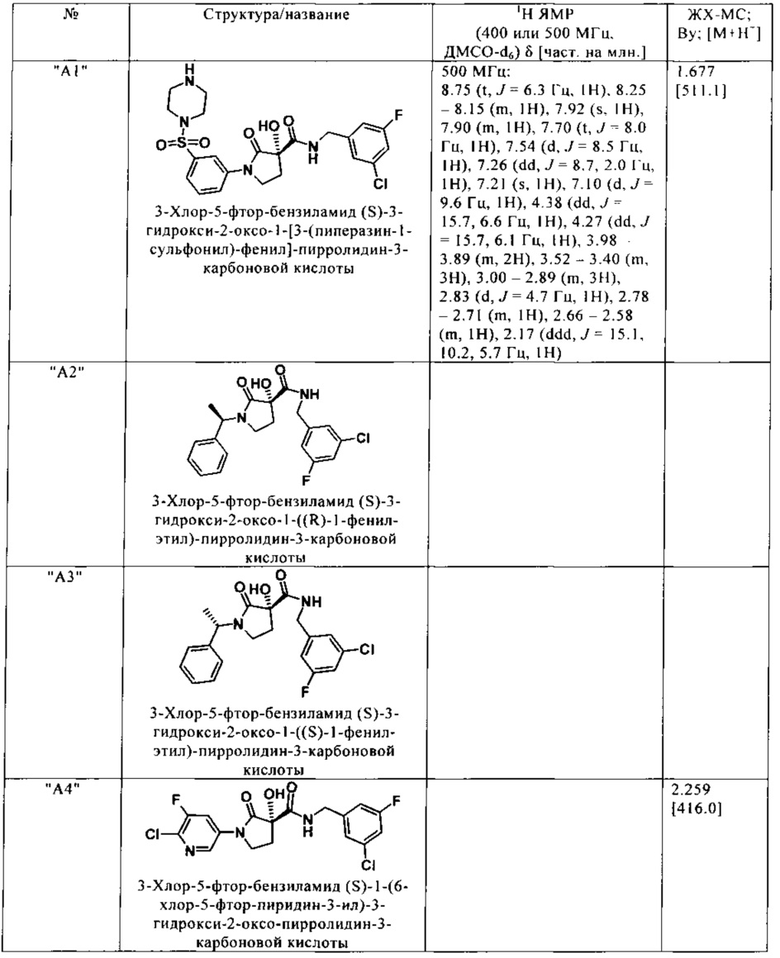
Нижеследующие соединения получают аналогичным образом.
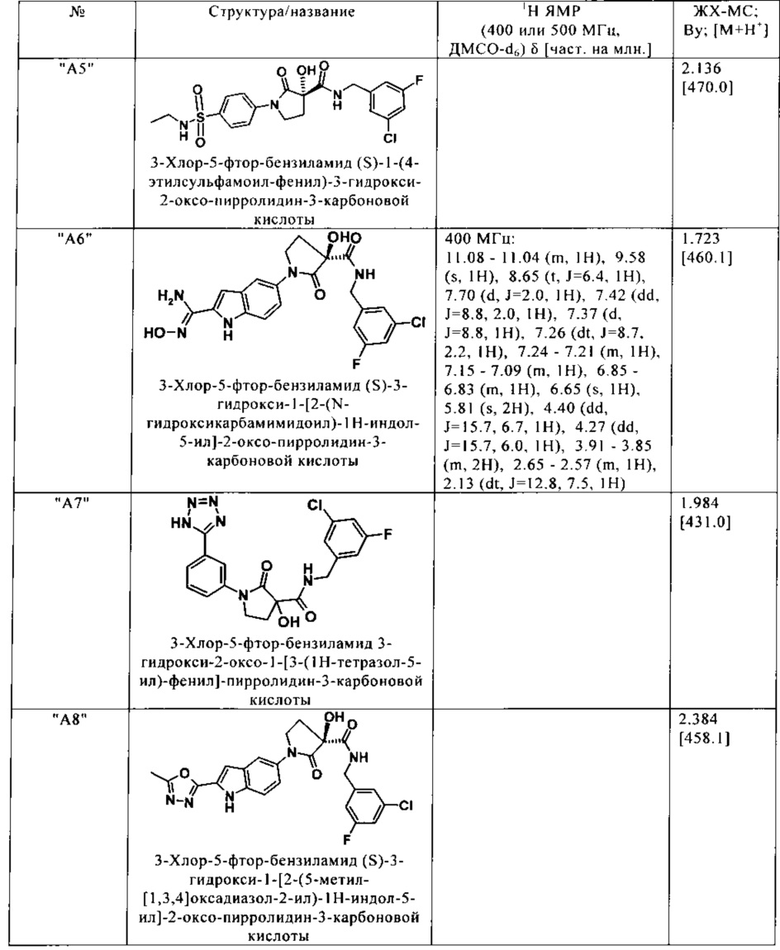
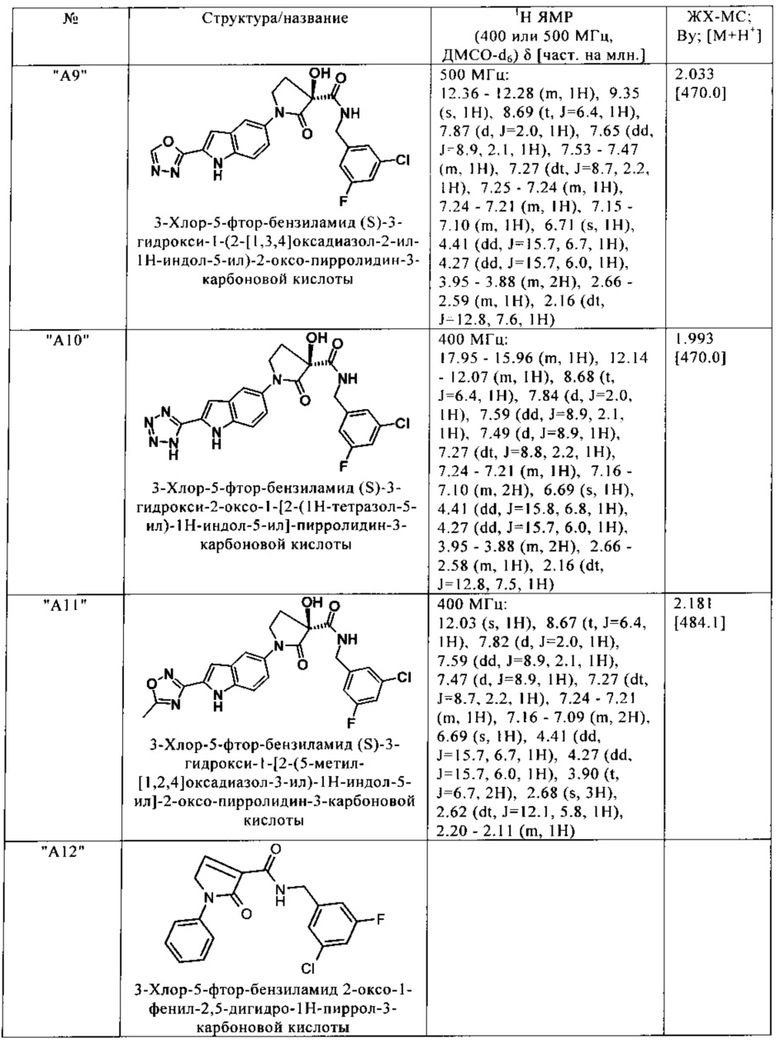
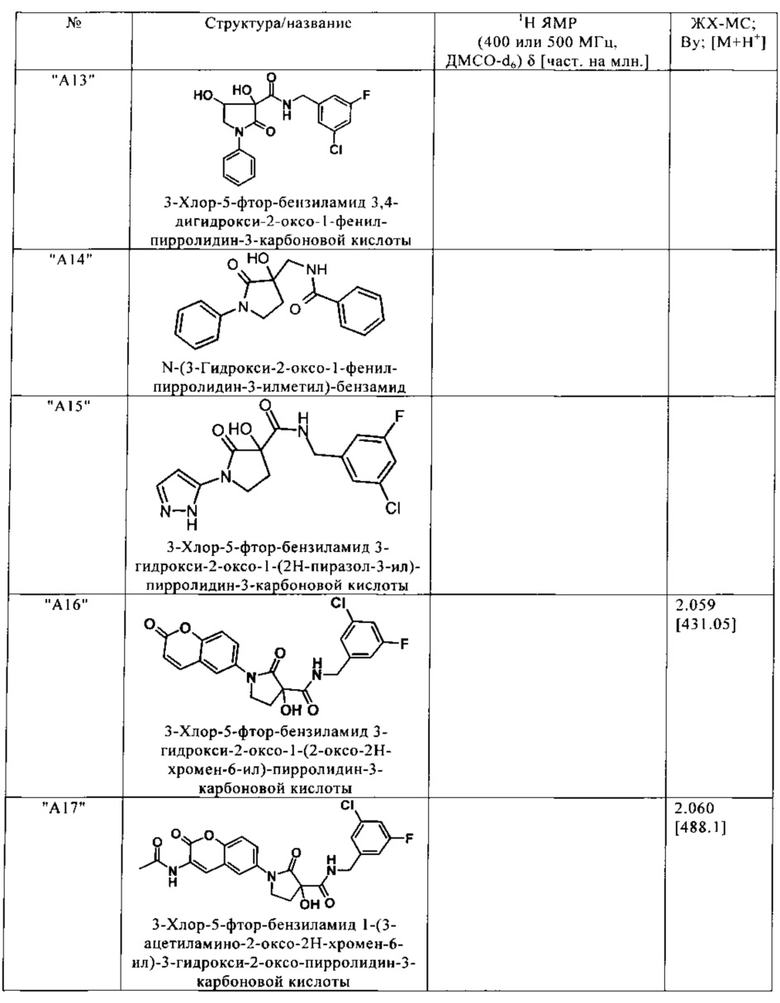
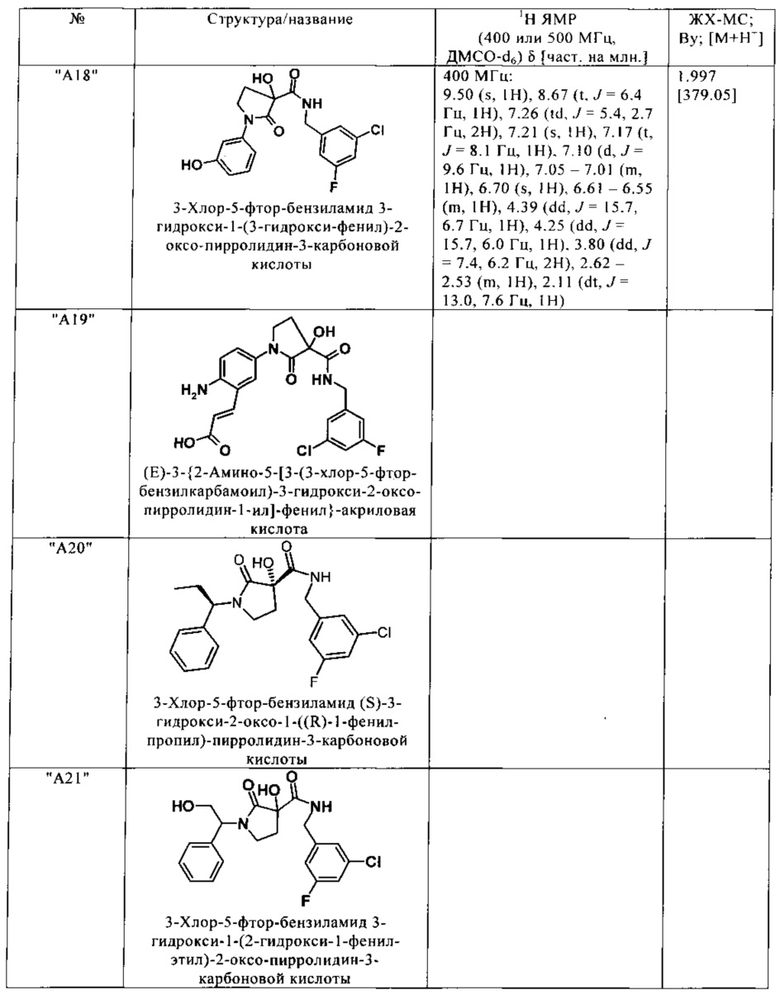
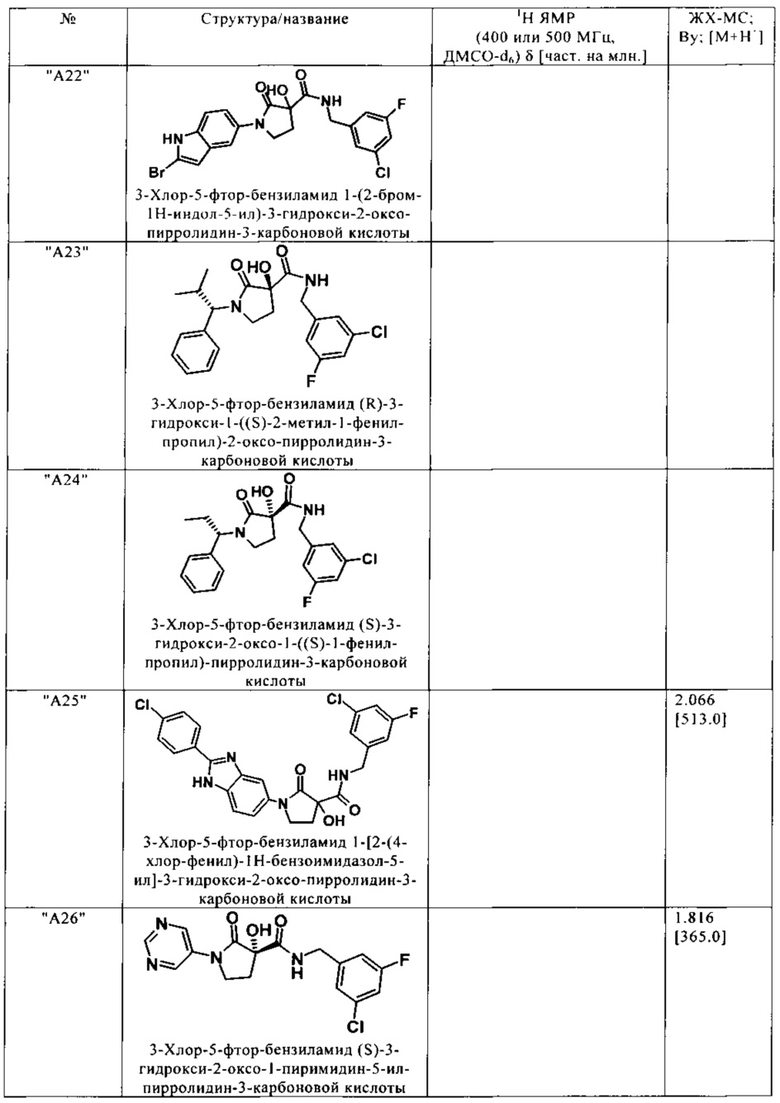
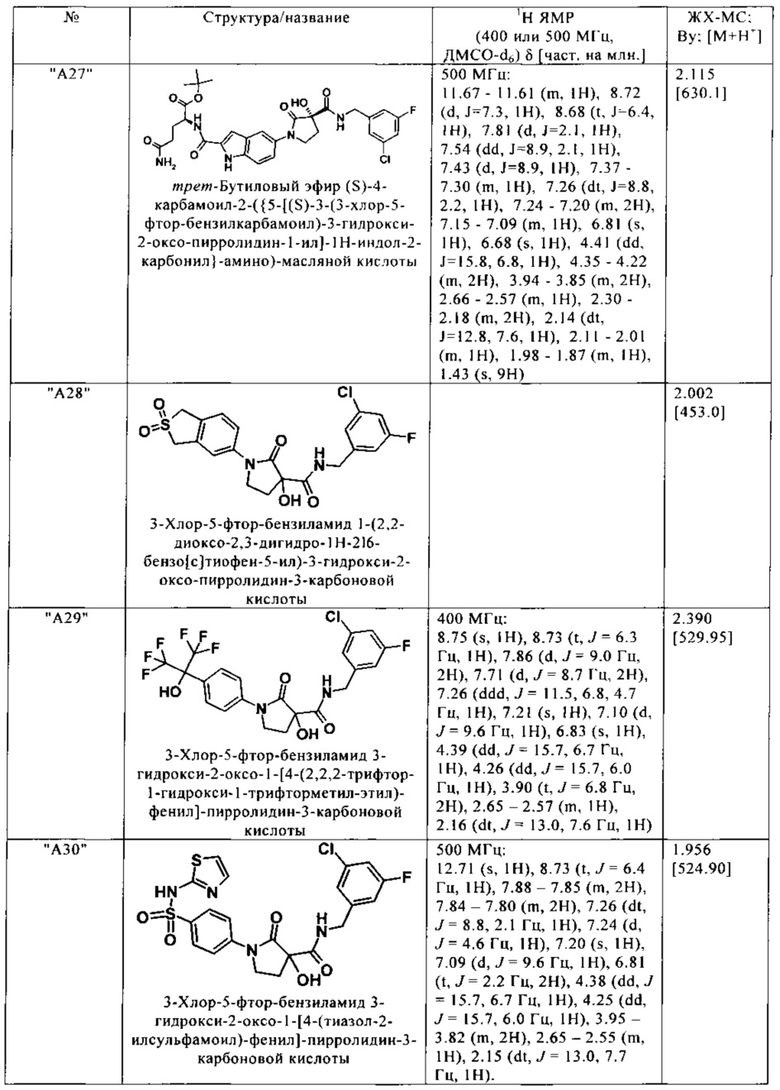
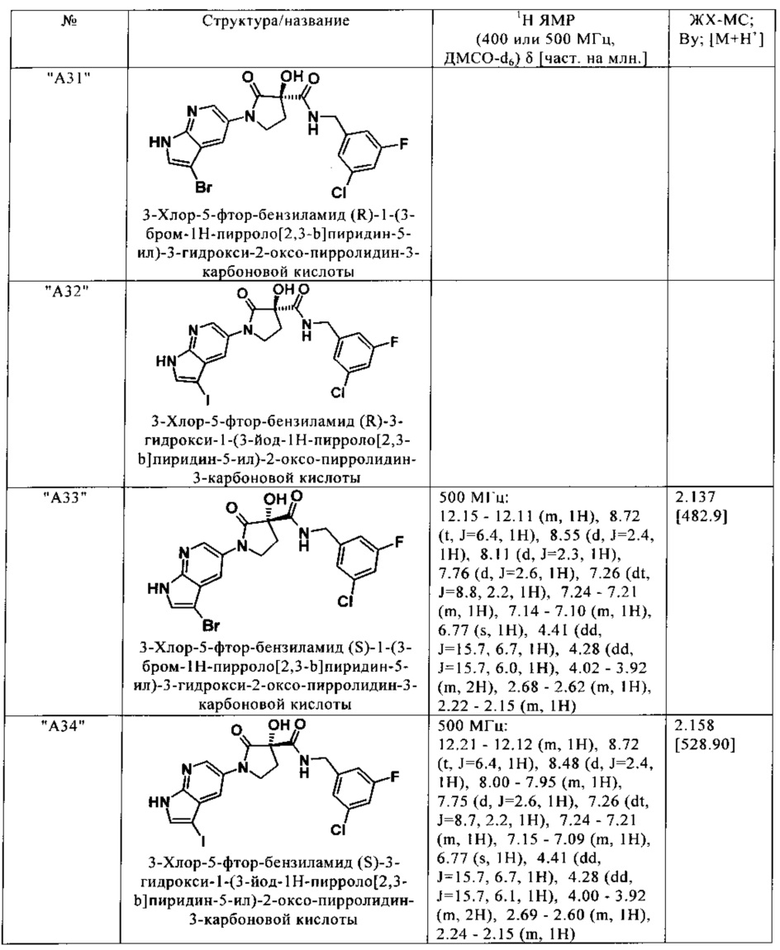
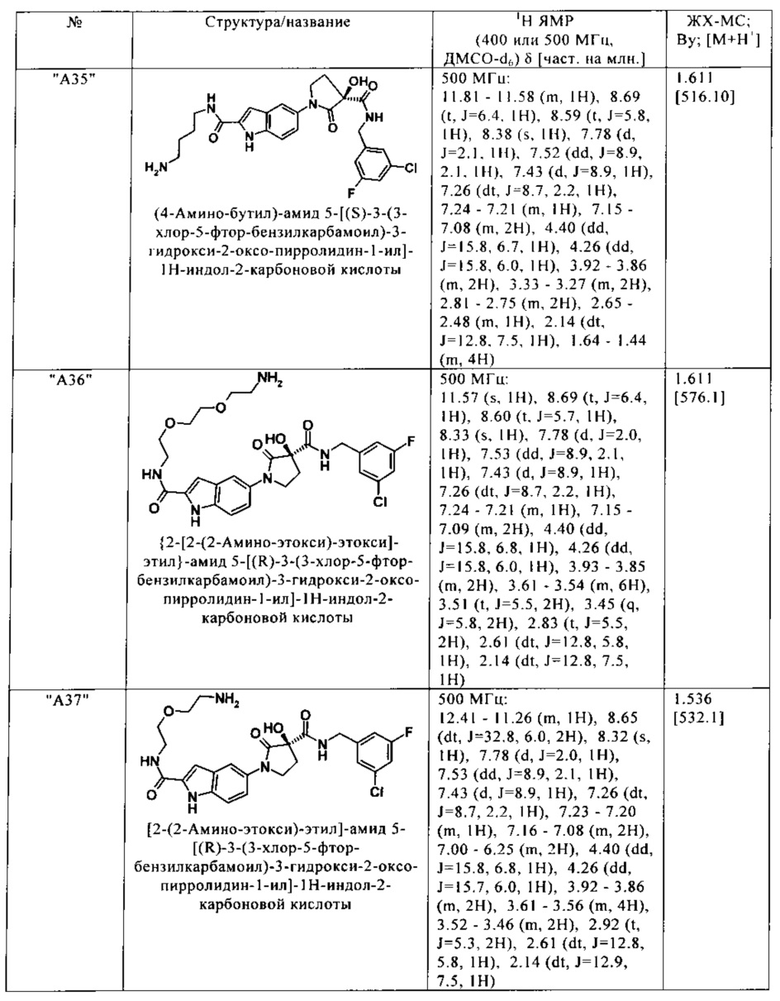
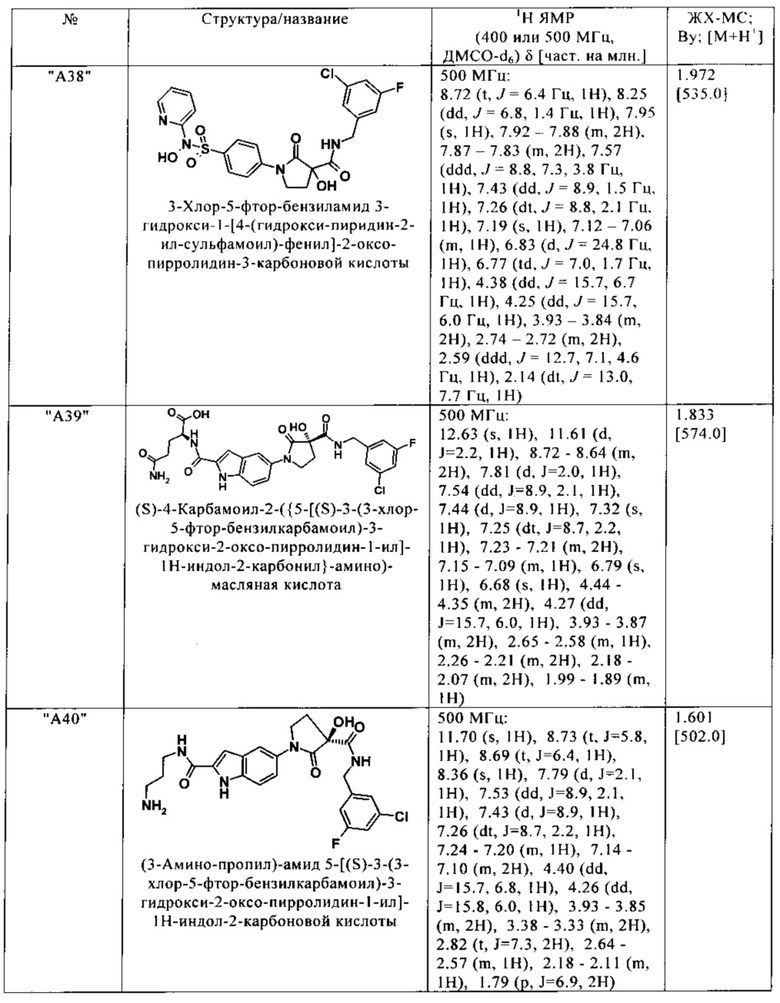
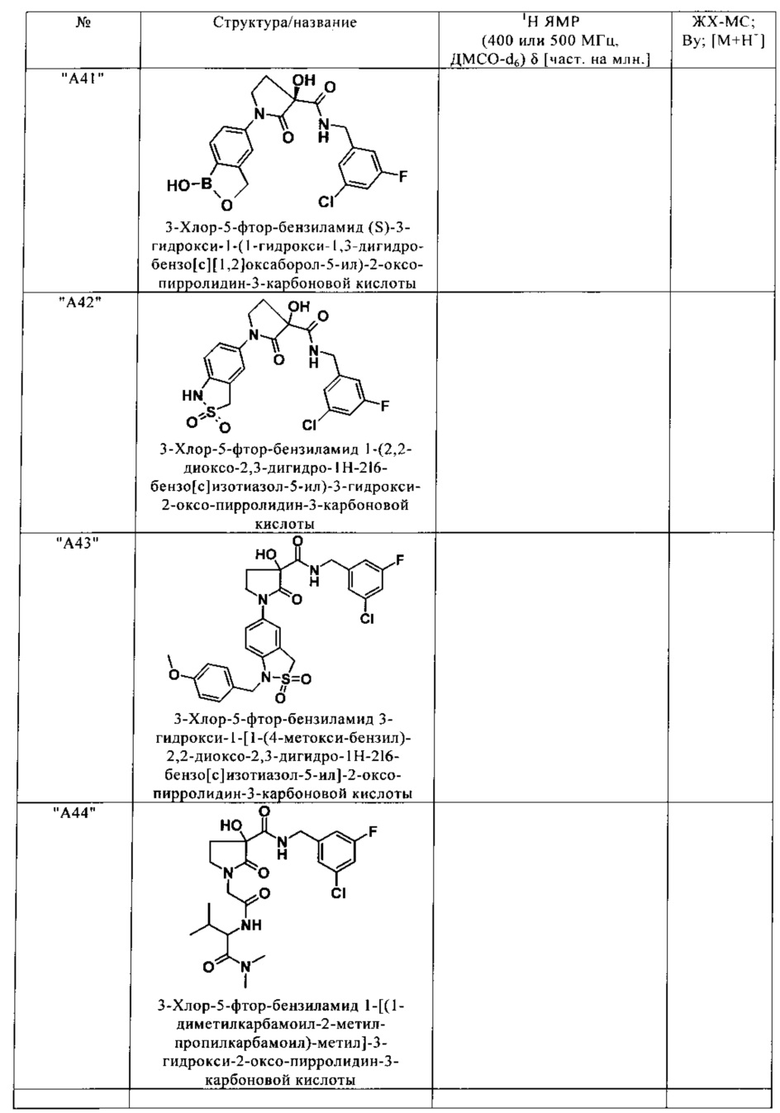
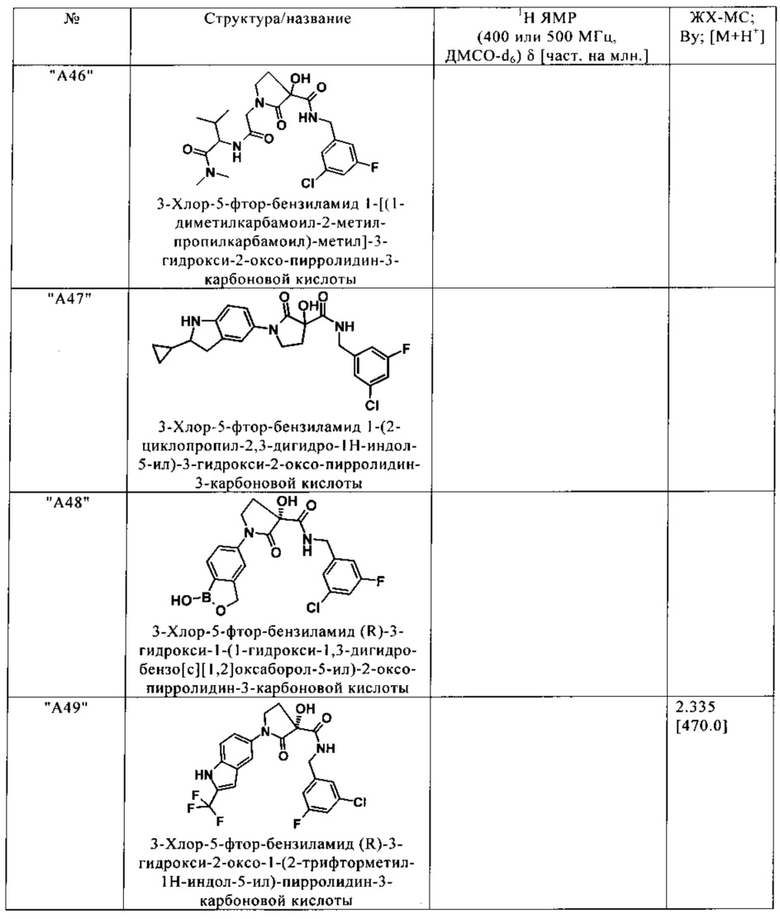
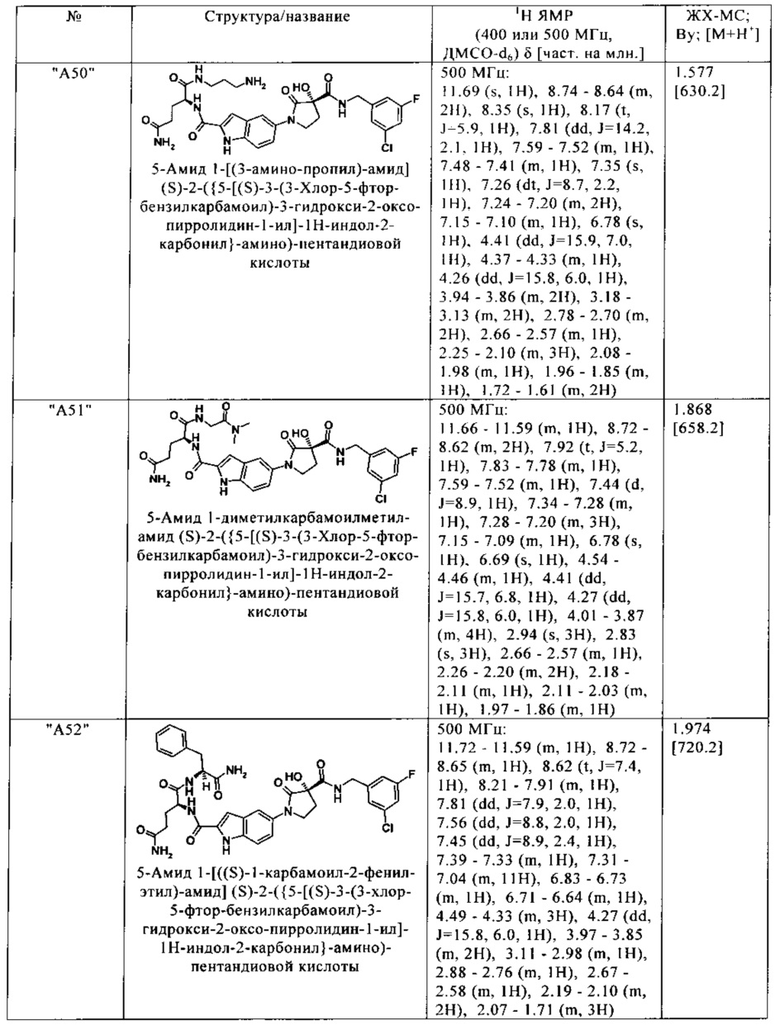
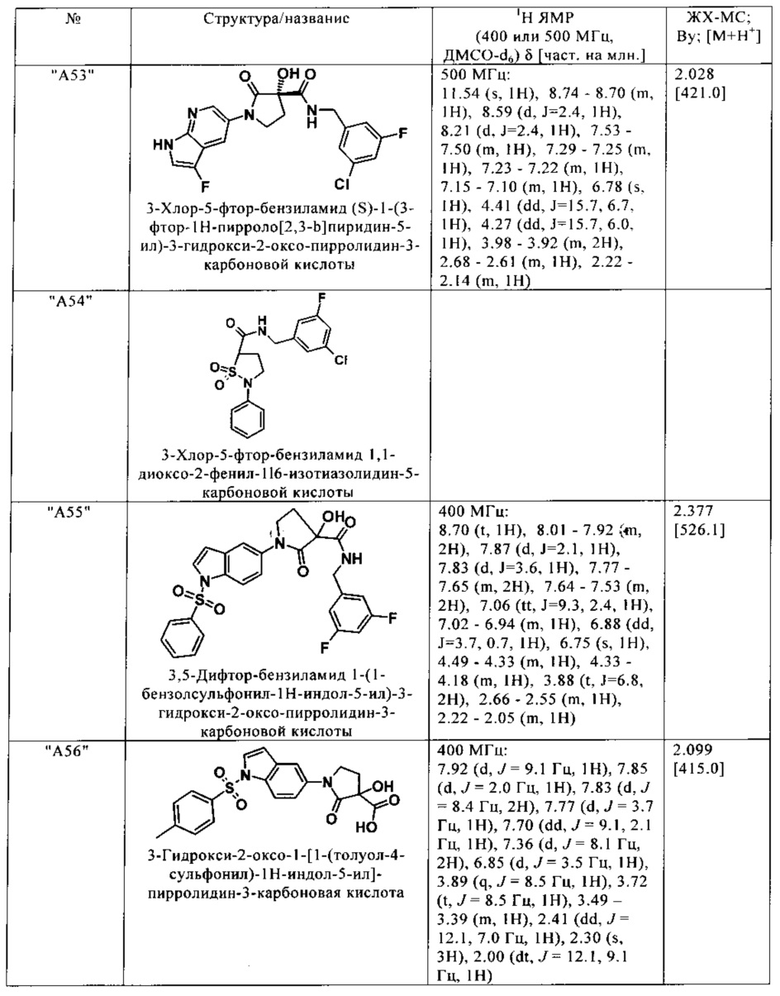
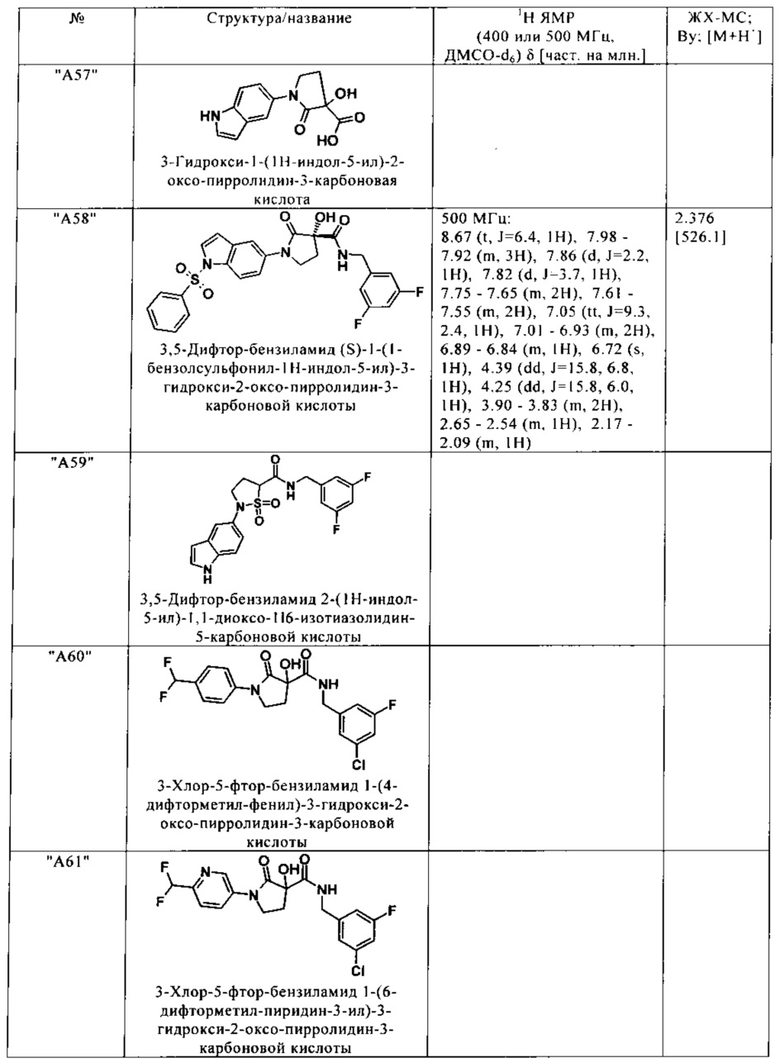
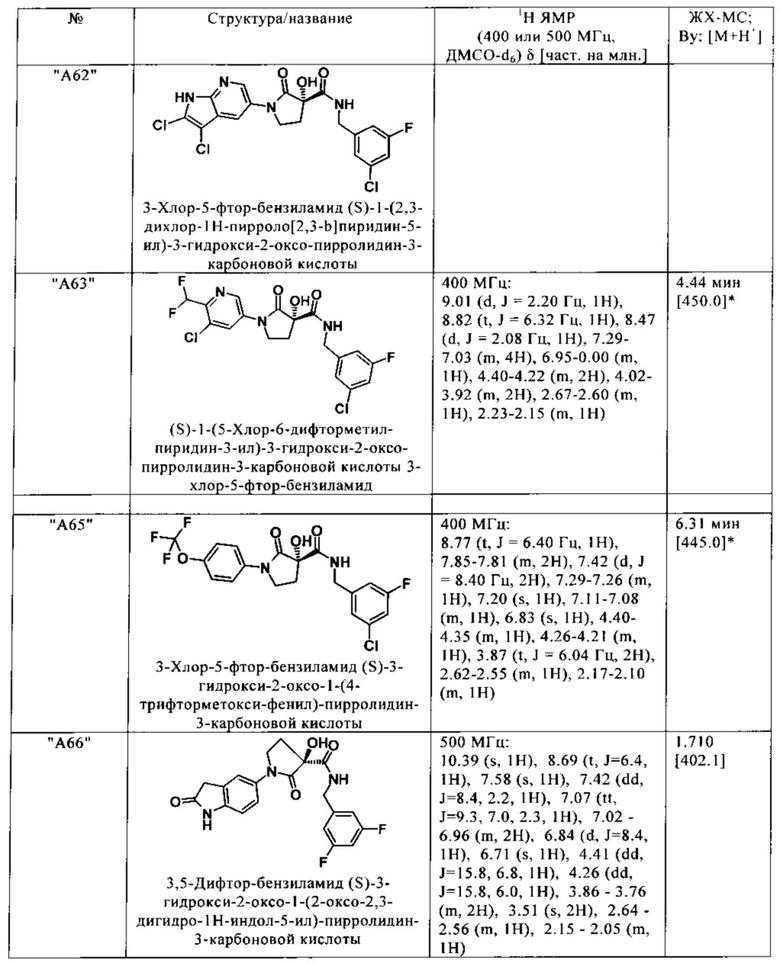
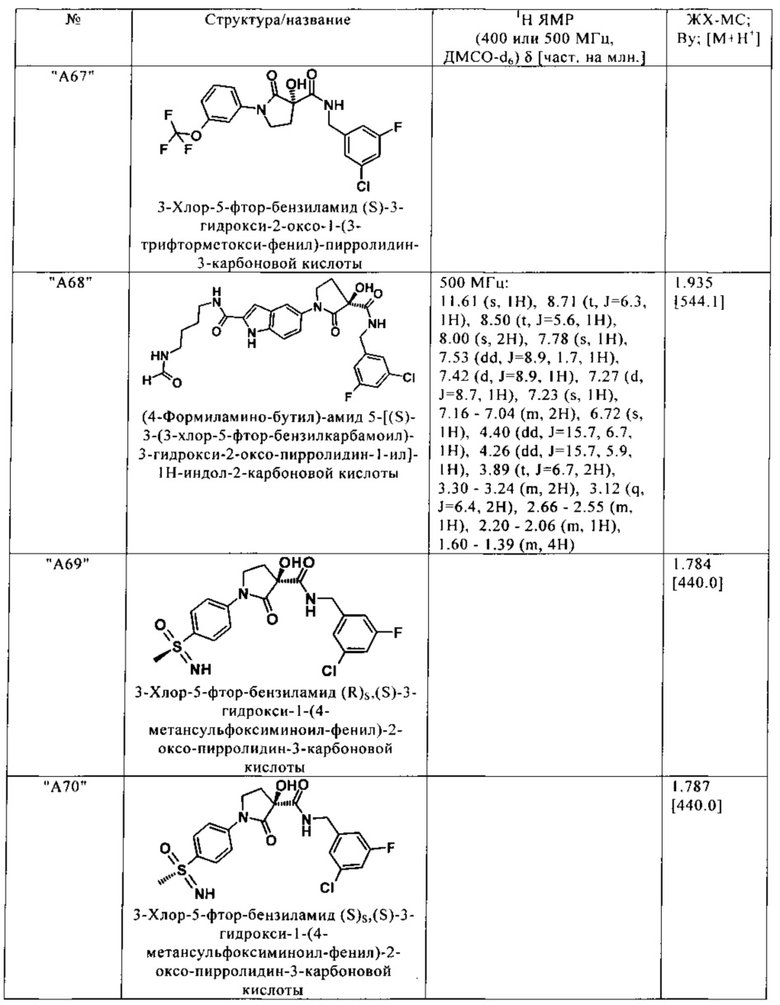
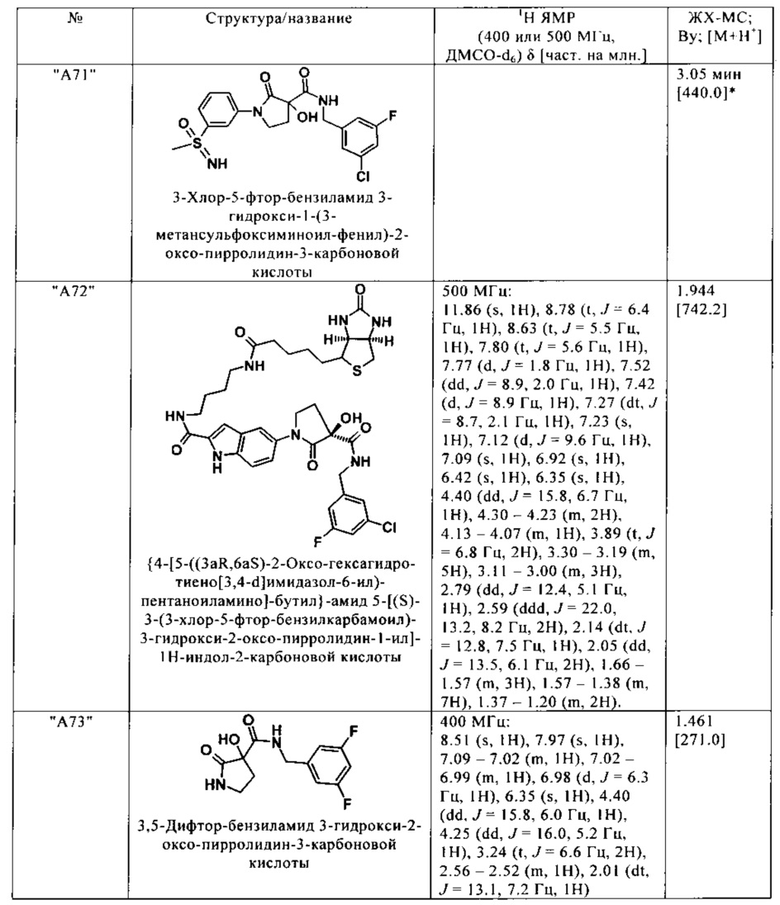
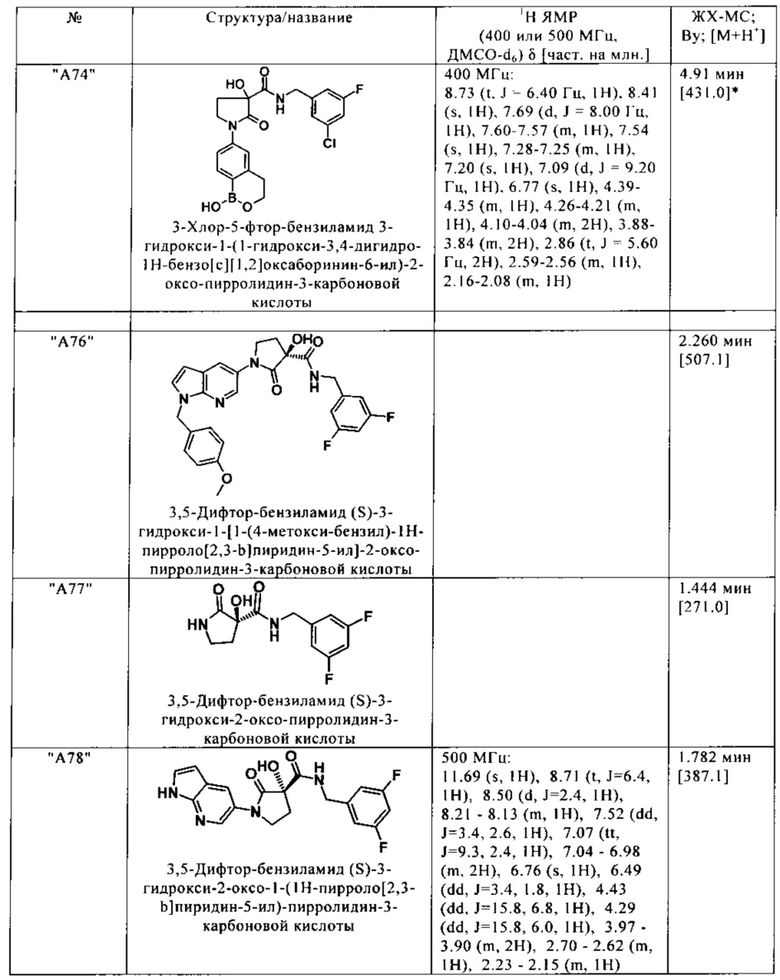
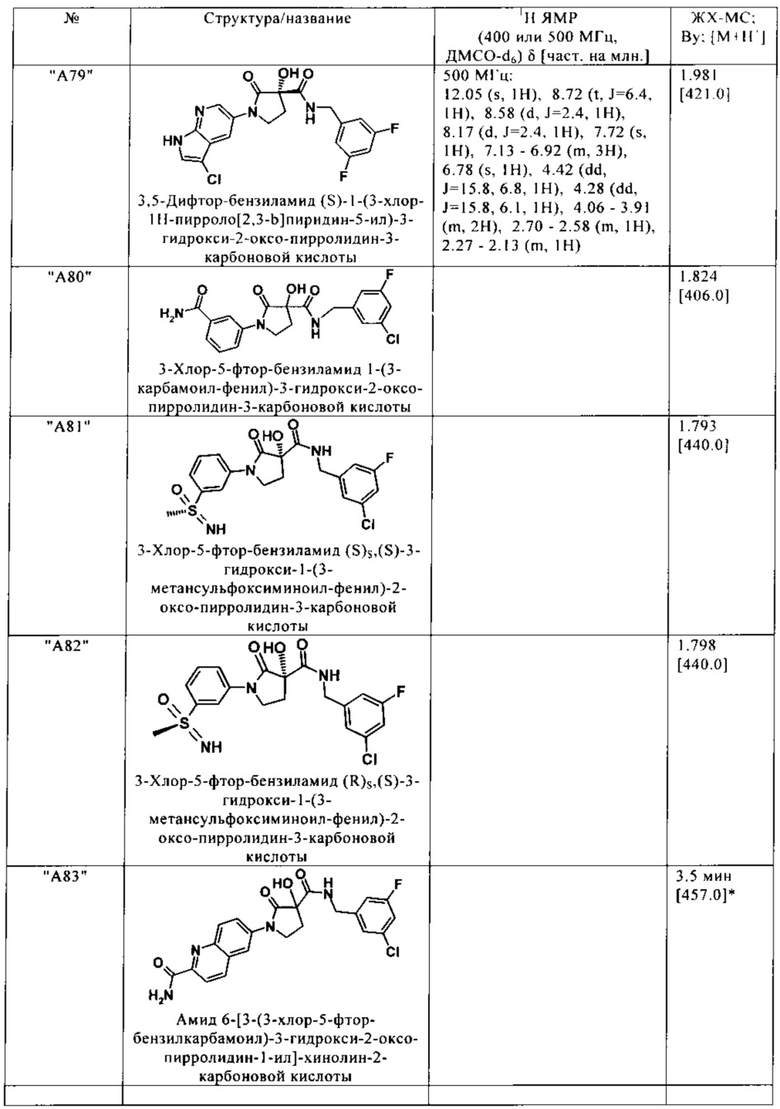
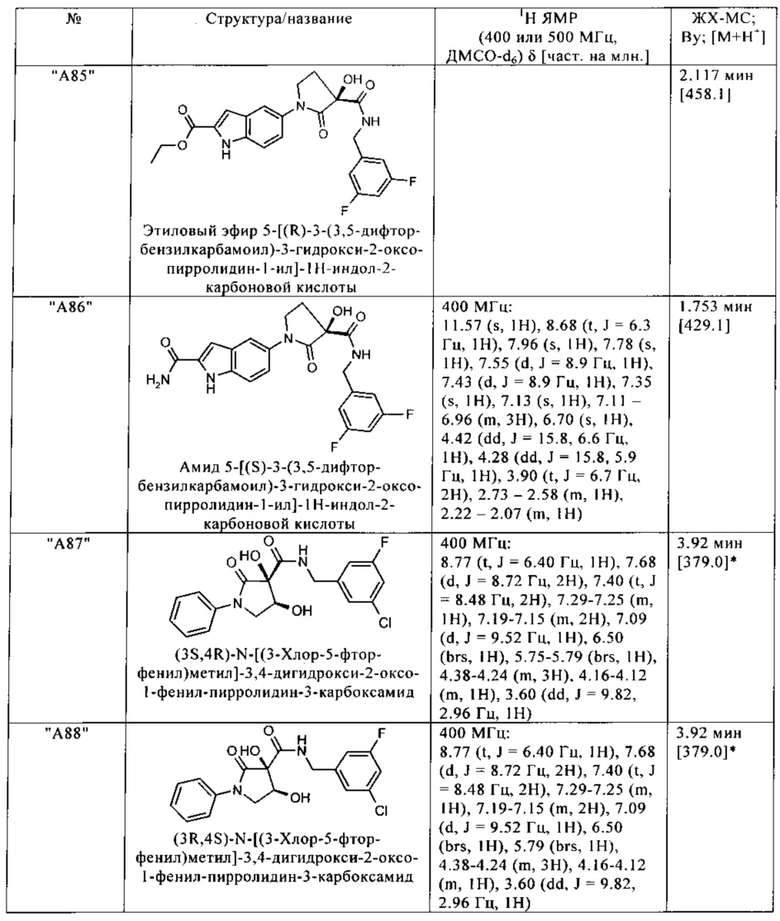
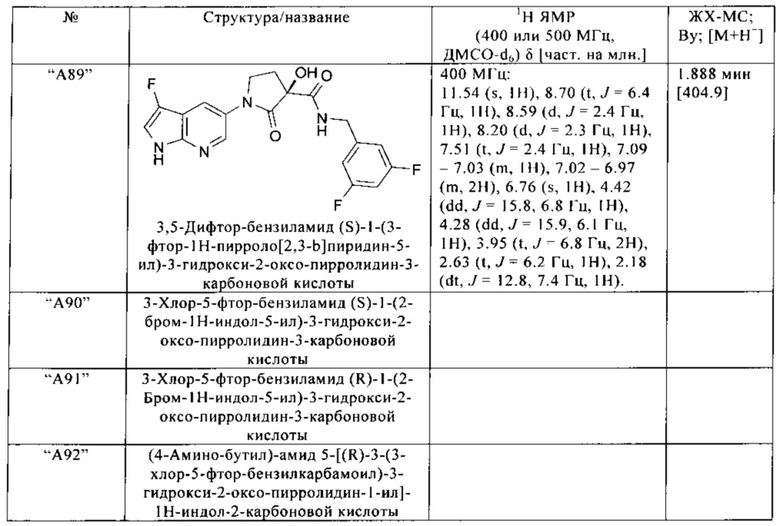
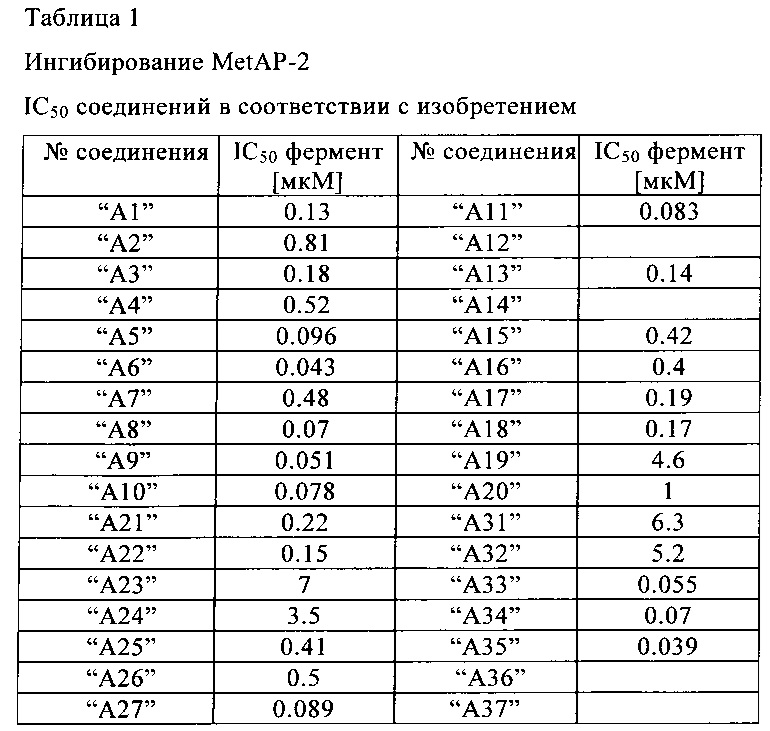

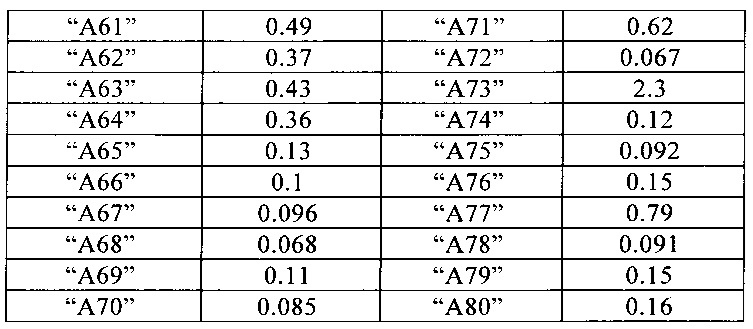
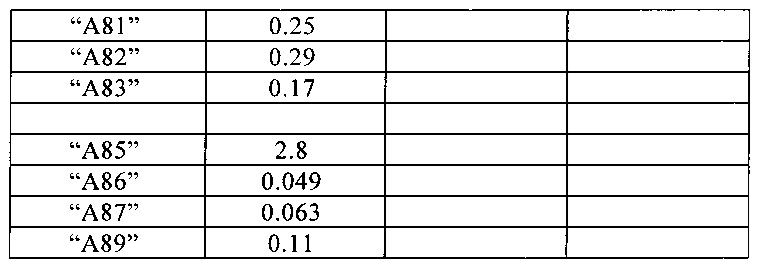
Сравнительные данные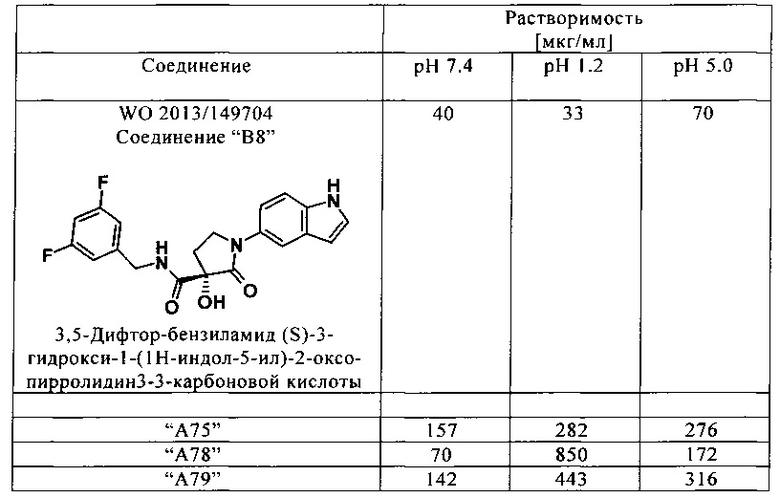
Соединения в соответствии с изобретением, такие как "А75", "А78" и "А79" демонстрируют более высокую растворимость по сравнению с соединением из известного уровня техники. Более высокая растворимость приводит к более высокой биодоступности при приеме соединений.
Нижеследующие примеры относятся к лекарственным средствам:
Пример А: Флаконы для инъекций
рН раствора 100 г активного соединения в соответствии с изобретением и 5 г гидрофосфата динатрия в 3 л бидистиллированной воды устанавливают до 6.5, с применением 2 н. соляной кислоты, стерильно фильтруют, переносят во флаконы для инъекций, лиофилизируют в стерильных условиях и запечатывают в стерильных условиях. Каждый флакон для инъекций содержит 5 мг активного соединения.
Пример Б: Суппозитории
Смесь 20 г активного соединения в соответствии с изобретением расплавляют со 100 г соевого лецитина и 1400 г масла какао, разливают в пресс-формы и дают остыть. Каждый суппозиторий содержит 20 мг активного соединения.
Пример В: Раствор
Раствор приготавливают из 1 г активного соединения в соответствии с изобретением, 9.38 г NaH2PO4 • 2 Н2O, 28.48 г Na2HPO4 • 12 Н2O и 0.1 г хлорида бензалкония в 940 мл бидистиллированной воды. рН раствора устанавливают до 6.8, объем раствора доводят до 1 л и стерилизуют путем облучения. Этот раствор можно применять в виде глазных капель.
Пример Г: Мазь
500 мг активного соединения в соответствии с изобретением смешивают с 99.5 г вазелина в асептических условиях.
Пример Д: Таблетки
Смесь 1 кг активного соединения в соответствии с изобретением, 4 кг лактозы, 1,2 кг картофельного крахмала, 0,2 кг талька и 0,1 кг стеарата магния спрессовывают для получения таблеток обычным способом таким образом, чтобы каждая таблетка содержала 10 мг активного соединения.
Пример Е: Драже
Таблетки спрессовывают аналогично примеру Д, и затем покрывают обычным способом покрытием из сахарозы, картофельного крахмала, талька, трагаканта и красителя.
Пример Ж: Капсулы
2 кг активного соединения в соответствии с изобретением помещают в твердые желатиновые капсулы обычным способом таким образом, чтобы каждая капсула содержала 20 мг активного соединения.
Пример 3: Ампулы
Раствор 1 кг активного соединения в соответствии с изобретением в 60 л бидистиллированной воды стерилизуют фильтрацией, переносят в ампулы, лиофилизируют в стерильных условиях и запечатывают в стерильных условиях. Каждая ампула содержит 10 мг активного соединения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОР СБОРКИ КАПСИДНОГО БЕЛКА, СОДЕРЖАЩИЙ N-ГЕТЕРОЦИКЛИЧЕСКОЕ ПЯТИЧЛЕННОЕ КОЛЬЦО, ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ | 2019 |
|
RU2802259C2 |
| Применение 6-фтор-3-триазеноиндолов для терапии инфекций, вызванных MRSA | 2019 |
|
RU2712265C1 |
| СОЕДИНЕНИЯ ХИНАЗОЛИНА | 2011 |
|
RU2530887C2 |
| Пангенотипичный ингибитор белка NS5A вируса гепатита С, фармацевтическая композиция и способы их получения и применения | 2019 |
|
RU2723482C1 |
| ФТАЛАЗИНОВЫЕ ПРОИЗВОДНЫЕ | 2014 |
|
RU2663623C2 |
| ПРОИЗВОДНЫЕ ИМИДАЗОПИРАЗИНОНА | 2014 |
|
RU2672885C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2006 |
|
RU2383545C2 |
| ПРИМЕНЕНИЕ 2,4,5-ТРИЗАМЕЩЕННЫХ 1,2,4-ТРИАЗОЛОНОВ В ПРОТИВОВИРУСНОЙ ТЕРАПИИ | 2021 |
|
RU2820287C1 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ГРИППА, ХАРАКТЕРИЗУЮЩИЙСЯ ТЕМ, ЧТО В НЕМ ОБЪЕДИНЕНЫ ИНГИБИТОР КЭП-ЗАВИСИМОЙ ЭНДОНУКЛЕАЗЫ И ЛЕКАРСТВЕННОЕ СРЕДСТВО ПРОТИВ ГРИППА | 2016 |
|
RU2745071C2 |
| БИЦИКЛИЧЕСКИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ПРОТИВОВОСПАЛИТЕЛЬНЫХ АГЕНТОВ | 2006 |
|
RU2426733C2 |
Изобретение относится к соединениям, представляющим собой производные пирролидинона, которые являются ингибиторами метионинаминопептидазы и могут быть использованы для лечения опухолевых новообразований. 2 н. и 2 з.п. ф-лы, 2 табл., 2 пр.
1. Соединение, выбранное из группы, включающей:
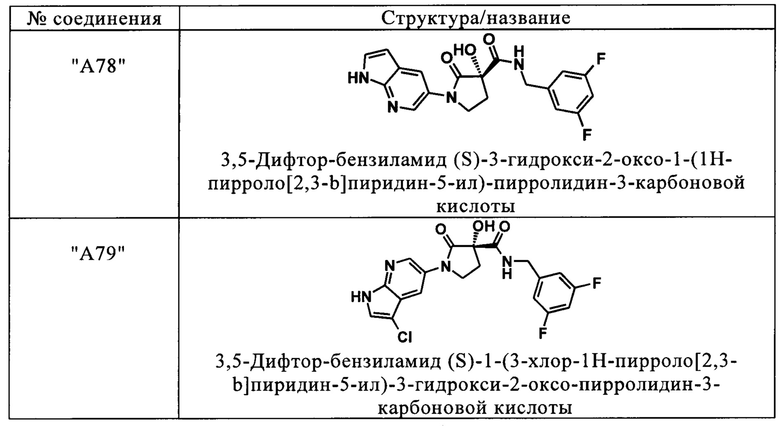
и его фармацевтически применимые соли.
2. Лекарственное средство, обладающее ингибирующим действием на метионинаминопептидазу MetAP-2, содержащее по меньшей мере одно соединение по п. 1 и/или его фармацевтически применимые соли и необязательно наполнители и/или вспомогательные средства.
3. Соединение по п. 1 и/или его фармацевтически применимые соли для применения для лечения заболеваний, отвечающих на ингибирование MetAP-2, выбранных из опухолевых новообразований, метастаз опухолей, пролиферативных заболеваний мезангиальных клеток, гемангиомы, пролиферативной ретинопатии, ревматоидного артрита, атеросклеротической неоваскуляризация, псориаза, глазной неоваскуляризации, остеопороза, диабетов и ожирения, лимфолейкоза, лимфомы, малярии и гипертрофии предстательной железы.
4. Соединение по п. 3, где опухолевое заболевание, отвечающее на ингибирование MetAP-2, выбирают из группы, включающей новообразования чешуйчатого эпителия, мочевого пузыря, желудка, почек, головы и шеи, пищевода, шейки матки, щитовидной железы, кишечника, печени, головного мозга, предстательной железы, мочеполовых путей, лимфатической системы, желудка, гортани, легкого, кожи, моноцитарный лейкоз, аденокарциному легкого, немелкоклеточную карциному легких, рак поджелудочной железы, глиобластому, рак молочной железы, острую миелоцитарную лейкемию, хроническую миелоцитарную лейкемию, острый лимфобластный лейкоз, хронический лимфолейкоз, лимфому Ходжкина, неходжкинскую лимфому.
| WO 2013149704 A1, 10.10.2013 | |||
| EA201300442 A1, 29.11.2013. |
Авторы
Даты
2019-07-17—Публикация
2015-07-10—Подача