Изобретение относится к области органической химии и может найти применение в аналитической химии и биологических исследованиях.
При изучении физиологически активных соединений необходимы их меченые аналоги.
Известно, что замена атомов соединений на их меченые аналоги не приводит к изменению каких-либо свойств исходного соединения (Evans Е.А. - Tritium and its compounds, London Butterworths, 1974, p. 48) [1].
Кроме того, показано, что реакции дейтерия и трития с веществами, нанесенными на поверхность катализатора, происходят с близкими скоростями и одинаковой селективностью, а отношение скоростей этих реакций приближается к единице (Золотарев Ю.А., Дадаян А.К., Кост Н.В., Воеводина М.Э., Соколов О.Ю., Козик B.C., Шрам С.И., Азев В.Н., Бочаров Э.В., Богачук А.П., Липкин В.М., Мясоедов Н.Ф. "Количественный анализ пептида HLDF-6-амида и его метаболитов в тканях лабораторных животных с использованием их меченных тритием и дейтерием производных" // Биоорганическая химия, 2015, Т. 41, №6, С. 644-656 и Zolotarev Yu.A., Dadayan А.K., Borisov Yu.A., Kozik V.S., Nazimov I.V., Ziganshin R.H., Bocharov E.V., Chizhov A.O., Myasoedov N.F. "New Development in the Solid-State Isotope Exchange with Spillover Hydrogen in Organic Compounds" // J. Phys.Chem. C., 2013, Vol. 117, P. 16878-16884) [2, 3].
Также в работе [1] показано, что в биологических исследованиях принципиально важную роль играет распределение трития в молекулах меченых препаратов. В работе подчеркивается, что при исследовании метаболизма лекарственных препаратов стабильность положения трития является одним из наиболее важных условий биологического эксперимента. Для каждого конкретного исследования требуется определенное распределение трития в молекулах меченых препаратов. Химически устойчивый связанный атом трития может стать подвижным при взаимодействии тритийсодержащего соединения с энзимом. В результате этого атом трития может быть потерян, несмотря на полную сохранность углеродного скелета молекулы. Если же тритий находится в другом фрагменте молекулы вещества, или в молекулах вещества их несколько, то вероятность получения более достоверных данных значительно повышается. При этом важно не только распределение трития, но даже и его стереохимическая конформация. Например, показано, что конверсия холестерина-4-14С-7α-3Н в холевую кислоту в организме крысы in vivo ведет к потере, по меньшей мере, 93% трития из положения 7. Однако при использовании 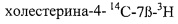 весь тритий оставался в холевой кислоте.
весь тритий оставался в холевой кислоте.
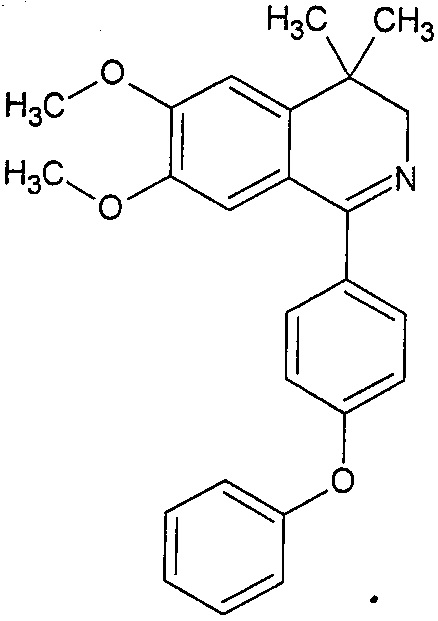
Известен 6,7-диметокси-4.4-диметил-1-(4-фенокси-фенил)-3Н-изохинолин формулы:
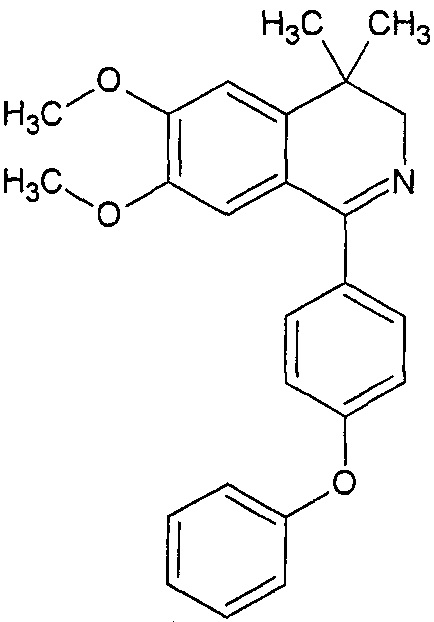
Установлено, что такие изохинолины увеличивают внутриклеточное поглощение доксорубицина в клетках MCF7 и усиливают антипролиферативный эффект доксорубицина с 5 до 95%. Считается, что подобные соединения классифицируются как ингибиторы Р-гликопротеина. [4] Colabufo N.A., Berardi F., Cantore M., Perrone M.G., Contino M., Inglese C., Niso M., Perrone R., Azzariti A., Simone G.M., Porcelli L., Paradiso A. "Small P-gp modulating molecules: SAR studies on tetrahydroisoquinoline derivatives" // Bioorg. Med. Chem., 2008, Vol. 16, №1, P. 362-373. Показано, что 6,7-диметокси-изохинолины имеют высокое сродство и селективность для рецепторов σ2. [5] Mach R.H., Huang Y., Freeman R.A., Wu L., Vangveravong S., Luedtke R.R. "Conformationally-flexible benzamide analogues as dopamine D3 and sigma 2 receptor ligands" // Bioorg.Med.Chem.Lett, 2004, Vol. 14, №1, P. 195-202. А эти рецепторы, по-видимому, участвуют в многочисленных фармакологических и физиологических функциях, а также модулируют ряд центральных нейромедиаторных систем. Исследования показывают, что эти рецепторы могут играть роль в патогенезе психических расстройств. [6] Mishina М., Ishiwata K., Ishii K., Kitamura S., Kimura Y., Kawamura K., Oda K., Sasaki Т., Sakayori О., Hamamoto M., Kobayashi S., Katayama Y. "Function of sigmal receptors in Parkinson's disease" // Acta. Neurol. Scand., 2005, Vol. 112, №2, P. 103-107. [7] Skuza G., Wedzony K. "Behavioral pharmacology of sigma-ligands" // Pharmacopsychiatry, 2004, Vol. 37, P. 183-188. Рецепторы σ2 (связанные с калиевыми каналами и высвобождением кальция) также участвуют в злокачественных опухолевых заболеваниях [4].
Однако меченный тритием 6,7-диметокси-4.4-диметил-1-(4-фенокси-фенил)-3Н-изохинолин не описан.
Техническим результатом, достигаемым настоящим изобретением, является расширение ассортимента меченых аналогов физиологически активных соединений.
Достигается указанный технический результат получением меченного тритием 6,7-диметокси-4.4-диметил-1-(4-фенокси-фенил)-3Н-изохинолина формулы:
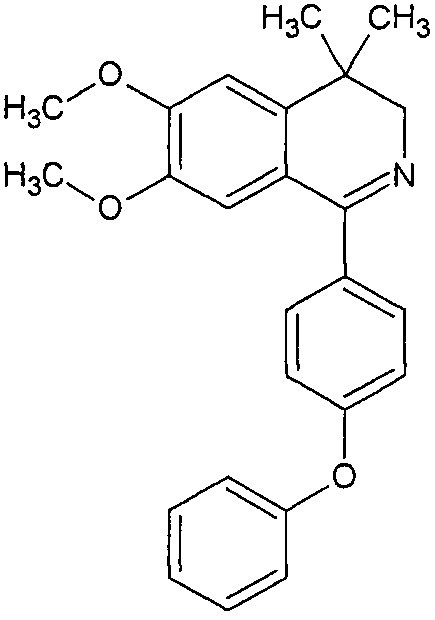
Ниже приведен пример реализации изобретения.
Пример 1.
Раствор 8 мг N-[2-(3,4-диметоксифенил)-2-метил-пропил]-4-фенокси-бензамина в 0.8 мл метанола упаривали в присутствии 90 мг катализатора Линдлара (Merck). После вакуумирования до давления 0.1 Па напускали газообразный тритий до давления 333 гПа и нагревали при 195°С в течение 15 мин. После удаления избыточного трития вакуумированием, вещество экстрагировали метанолом (5×1 мл) и смесью метанола с 1н НС1 (50:1) (5×1 мл). Фильтраты упаривали, лабильный тритий удаляли упариванием с метанолом (3×3 мл) и меченый препарат очищали хроматографическими методами. Выход меченого препарата составил 49%, молярная радиоактивность 140 Ки/ммоль.
Анализ и очистку меченого препарата проводили высокоэффективной жидкостной хроматографией на колонке 10×250 мм, Silasorb 300, 7 мкм, v-2.0 мл/мин, система хлороформ-триэтиламин-изо-пропанол (100:2.5:1), время удерживания - 10.14 мин (6,7-диметокси-4.4-диметил-1-(4-фенокси-фенил)-3Н-изохинолин); система хлороформ-изо-пропанол (100:1), время удерживания - 12.47 мин (N-[2-(3,4-диметоксифенил)-2-метил-пропил]-4-фенокси-бензамин); на колонке 4×150 мм, Kromasil C18, 7 мкм, v-0.8 мл/мин, система метанол-вода-триэтиламин (60:40:0.1), время удерживания - 5.75 мин (N-[2-(3,4-диметоксифенил)-2-метил-пропил]-4-фенокси-бензамин), система метанол-вода-трифторуксусная кислота (65:35:0.1), время удерживания - 3.90 мин (N-[2-(3,4-диметоксифенил)-2-метил-пропил]-4-фенокси-бензамин).
Для приема и обработки хроматографических данных использовалась система "МультиХром" (НТК "Амперсенд", Россия) на базе IBM PC/AT. Радиоактивность измеряли на сцинтилляционном счетчике с эффективностью регистрации трития 30% в диоксановом сцинтилляторе.
Для превращения меченного тритием N-[2-(3,4-диметоксифенил)-2-метил-пропил]-4-фенокси-бензамина в меченный тритием 6,7-диметокси-4.4-диметил-1-(4-фенокси-фенил)-3Н-изохинолин 1 мг меченного тритием N-[2-(3,4-диметоксифенил)-2-метил-пропил]-4-фенокси-бензамина растворяли в 0.15 мл ацетонитрила, при перемешивании добавляли 0.15 мл ацетонитрильного раствора POCl3 (100 мг/мл). Ампулу запаивали и продолжали перемешивание при 75°С в течение 105 мин. Затем реакционную смесь охлаждали до 5°С и добавляли 50 мкл 1 М Na2CO3, затем реакционную смесь упаривали и остаток экстрагировали 4 мл смеси хлороформа с водой (3:1). Хлороформный слой промывали водой (3×0.5 мл), упаривали и остаток очищали хроматографией.
Суммарный выход меченного тритием 6,7-диметокси-4,4-диметил-1-(4-фенокси-фенил)-3Н-изохинолина составил 41% с молярной радиоактивностью - 125 Ки/ммоль.
Таким образом, получен меченный тритием 6,7-диметокси-4,4-диметил-1-(4-фенокси-фенил)-3Н-изохинолин.
| название | год | авторы | номер документа |
|---|---|---|---|
| Синтез меченного тритием 6,7-диметокси-4,4-диметил-1-[4-(4-трифторметилфенокси)фенил]-3Н-изохинолина | 2019 |
|
RU2711646C1 |
| ПРОИЗВОДНЫЕ ПИРИДО(2,1-А)ИЗОХИНОЛИНА В КАЧЕСТВЕ ИНГИБИТОРОВ DPP-IV | 2002 |
|
RU2297417C2 |
| СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2004 |
|
RU2317985C1 |
| ПРОИЗВОДНЫЕ ПИПЕРАЗИНА | 1994 |
|
RU2124511C1 |
| Способ получения фенилэтиламинов или их солей | 1978 |
|
SU700061A3 |
| Способ получения производных тетрагидроизохинолина или их фармацевтически приемлемых кислотно-аддитивных солей | 1986 |
|
SU1598875A3 |
| ПРОИЗВОДНЫЕ АКРИДИНА, СПОСОБ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 1992 |
|
RU2119482C1 |
| Способ получения производных циклического амина или их кислотно-аддитивных солей | 1988 |
|
SU1561823A3 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ПРОЛЕКАРСТВО ИНГИБИТОРА ПРОТОННОГО НАСОСА | 1999 |
|
RU2232159C2 |
| МЕЧЕННЫЙ ТРИТИЕМ АЦИЛКОЕНЗИМ А | 2006 |
|
RU2305104C1 |
Изобретение относится к области органической химии и может найти применение в аналитичекой химии и биологических исследованиях. Задачей настоящего изобретения является получение меченного тритием 6,7-диметокси-4,4-диметил-1-(4-фенокси-фенил)-3Н-изохинолина формулы:
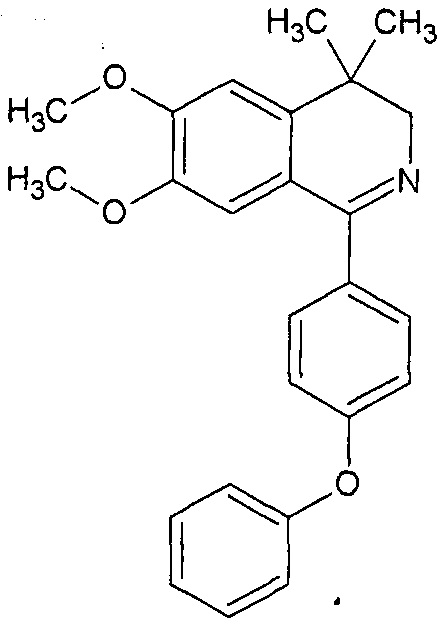 1 пр.
1 пр.
Меченный тритием 6,7-диметокси-4,4-диметил-1-(4-фенокси-фенил)-3Н-изохинолин формулы:
| Dezhu Wu et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Ведущий наконечник для обсадной трубы, употребляемой при изготовлении бетонных свай в грунте | 1916 |
|
SU258A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Brochmann -Hanssen E., S | |||
| W | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Приспособление для получения кинематографических стерео снимков | 1919 |
|
SU67A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Tetsuji Kametani et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
2019-07-19—Публикация
2019-04-08—Подача