Изобретение относится к медицине, а именно к фармакогенетике, клинической фармакологии, психиатрии, наркологии, и может быть использовано для подбора дозы антипсихотического лекарственного средства из группы производных фенотиазина трифлуоперазина у пациентов с любыми нозологиями.
Трифлуоперазин применяется для лечения расстройств, сопровождающихся развитием психотической симптоматикой, в том числе, включен в стандарты и протоколы лечения больных, страдающих алкогольной зависимостью, находящихся в состоянии актуализации патологического влечения. Трифлуоперазин обладает мощным антипсихотическим действием. Применение трифлуоперазина сопряжено с высоким риском развития нежелательных лекарственных реакций (острая дистония, дискинезии, кардиотоксичность и др.), что ограничивает его применение в клинике. В настоящее время есть достаточно большое количество данных о влиянии полиморфизмов генов, кодирующих элементы биотрансформации трифлуоперазина, на показатели его эффективности и безопасности.
Задачей изобретения является разработка способа, позволяющего прогнозировать и предупреждать развитие нежелательных лекарственных реакций терапии трифлуоперазином, либо наоборот, отсутствие ожидаемой эффективности терапии, посредством коррекции дозы препарата (либо рекомендации по его смене) в зависимости от наличия тех или иных полиморфизмов в генах, кодирующих изоферменты биотрансформации, принимающих участие в метаболизме трифлуоперазина.
Сущность изобретения состоит в расчете значения параметра Р, являющегося оценочной величиной выраженности изменения скорости биотрансформации трифлуоперазина, в зависимости от состояния генетического полиморфизма у каждого конкретного пациента. После проведения генотипирования по точкам, входящим в панель, разработанную нами, на основе имеющихся на сегодняшний день исследованиях уровня доказательности 3 выше и находящихся в открытом доступе в системе Medline, производится расчет значения параметра Р. В расчете используется следующий принцип: если ген кодирует основной изофермент биотрансформации трифлуоперазина CYP1A2 (Тау JK, Tan СН, Chong SA, Tan ЕС.Functional polymorphisms of the cytochrome P450 1A2 (CYP1A2) gene and prolonged QTc interval in schizophrenia. Send toProgNeuropsychopharmacolBiolPsychiatry. 2007 Aug 15;31 (6): 1297-302. Epub 2007 Jun 6.), то у пациента-гетерозиготы по функциональному полиморфизму данного гена отклонение в скорости биотрансформации будет принято на уровне 25%, а у мутантной гомозиготы 50%. Если имеются данные генотипирования по нескольким полиморфизмам одного гена, то полученные значения изменения скорости биотрансформации складываются друг с другом. Замедление биотрансформации имеет знак «-», ускорение знак «+». Если имеются нескольких изоферментов основного или альтернативного пути, то отклонение в скорости для каждого из изоферментов пути делится на количествоизоферментов, отвечающим за путь метаболизма. Данные процентные соотношения в отклонении скорости биотрансформации были выбраны на основании имеющихся на сегодняшний день мета-анализов авторитетных консорциумов по другим лекарственным средствам (напр. антидепрессантам).
При значении параметра Р в интервале [50;∞) (отклонении скорости биотрансформации трифлуоперазина на 50% и выше) дается рекомендация о замене лекарственного средства на то, в метаболизме которого не принимает участие изоферменты, активность которых нарушены. При значении параметра Р в интервале (-50;0) (замедлении скорости биотрансформации трифлуоперазина меньше, чем на 50%) дается рекомендация о понижении дозы. При значении параметра Р в интервале (0;50)(ускорении скорости биотрансформации трифлуоперазина меньше, чем на 50%) дается рекомендация о повышении дозы.
Использование изобретения позволяет получить следующий технический результат.
Предложенный способ оптимизации режима дозирования трифлуоперазина, основанный на анализе результатов генотипирования по полиморфным маркерам, способным оказывать влияние на изменение активности генов, кодирующих изоферменты биотрансформации трифлуоперазина, обладает высокой точностью, информативностью и объективностью, так как в основе лежит способ достоверной оценки генетического аппарата и алгоритмах, включенных в мета-анализы авторитетных консорциумов при расчете аналогичных показателей в отношении других лекарственных средств.
Предложенный способ является простым и доступным и может быть использован в медицинских учреждениях разного типа без применения специального оборудования, за исключения оборудования для проведения генотипирования.
Технический результат достигается за счет того, что авторами впервые определены степени выраженности отклонения в скорости биотрансформации трифлуоперазина в зависимости от состояния генетического аппарата, установлена достоверная связь между выраженностью данного отклонения и степенью изменения индивидуального ответа на трифлуоперазин, а также разработаны рекомендации по оптимизации режима дозирования трифлуоперазина в зависимости от степени выраженности данного отклонения.
Степени выраженности отклонения в скорости биотрансформации трифлуоперазина в зависимости от состояния генетического аппарата определены на основании анализа данных литературных источников, а также статистического и математического анализа большого количества клинического материала.
Способ осуществляется следующим образом. После получения результатов генотипирования по любым полиморфным маркерам генов CYP1A2 данные заносятся в таблицу Excel. Далее запускается разработанное нами программное обеспечение и в него загружается сформированный Excel-файл и программа автоматически рассчитывает искомые показатели с помощью нижеследующих формул:
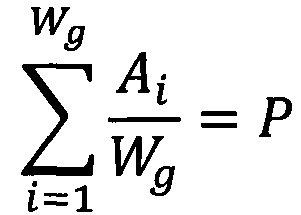
где:
Wg - количество полиморфизмов гена CYP1A2 (основного пути биотрансформации трифлуоперазина), данные которых были занесены в таблицу Excel;
Ai - изменение скорости биотрансформации трифлуоперазина, в зависимости от генотипа по каждому внесенному в таблицу Excel полиморфному маркеру гена CYP1A2.
По значению параметра «Результирующее изменение скорости биотрансформации трифлуоперазина» судят о рисках развития нежелательных лекарственных реакций и отсутствия терапевтической эффективности терапии трифлуоперазином.
При значении параметра Р в интервале [50;∞) (отклонении скорости биотрансформации трифлуоперазина на 50% и выше) дается рекомендация о замене лекарственного средства на то, в метаболизме которого не принимает участие изоферменты, активность которых нарушены. При значении параметра Р в интервале (-50;0) (замедлении скорости биотрансформации трифлуоперазина меньше, чем на 50%) дается рекомендация о понижении дозы. При значении параметра Р в интервале (0;50) (ускорении скорости биотрансформации трифлуоперазина меньше, чем на 50%) дается рекомендация о повышении дозы.
Предлагаемый способ апробирован на 13 пациентах с подтвержденным диагнозом «Психические и поведенческие расстройства, вызванные употреблением алкоголя. Синдром зависимости средней стадии, неосложненный. Воздержание в условиях, исключающих употребление психоактивных веществ (F 10.212)» согласно критериям МКБ-10. Пациенты находились на стационарном лечении в ГБУЗ «МНПЦ наркологии» ДЗМ в 2017 году. Возраст больных колебался от 18 до 55 лет; средний возраст составил 35,18±8,55 лет. Все пациенты были мужского пола.
Для купирования патологического влечения пациентам на 5-10 день пребывания в стационаре после купирования абстинентного синдрома назначался трифлуоперазин в форме драже (Трифтазин, производитель Дальхимфарм (Россия)) в период обострения патологического влечения. Подбор терапевтической дозы трифлуоперазина осуществлялся на основании оценки тяжести клинической картины обострения патологического влечения в соответствии со стандартами оказания наркологической медицинской помощи. Суточная дозировка оставалась неизменной на протяжении всего периода терапии, компонентном которой был трифлуоперазин. Суточные дозы трифлуоперазина представлены в таблице 1.
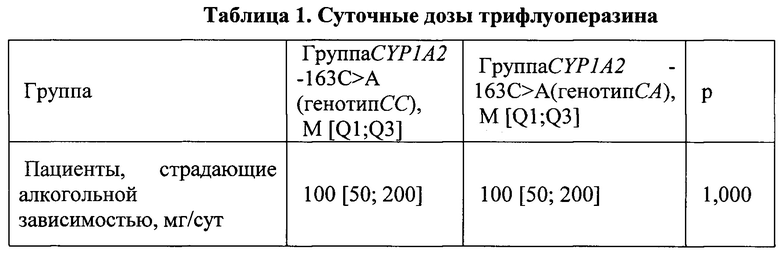
По результатам генотипирования CYP1A2 по полиморфному маркеру -163C>A(rs762551) у 13 пациентов, страдающих алкогольной зависимостью, были получены следующие данные:
Количество пациентов, являющихся носителем не мутантного гена СУР1А2(генотии СС) составило - 9 (69%);
Количество пациентов, являющихся гетерозиготными носителями полиморфизма -163С>Агена СYР1A2 (генотип СА) составило - 4 (31%).
Пациентов с мутантным генотипом АА обнаружено не было.
За время проведения исследования (5 дней терапии трифлуоперазином) у 6 пациентов было зафиксировано развитие дозозависимых нежелательных лекарственных реакций (холинолитические эффекты, дискинезия), при чем распределение по частоте встречаемости нежелательных реакций было следующим:
в группе пациентов с генотипом СС - 2 НЛР типа А (22,22%);
в группе пациентов с генотипом СА- 4 НЛР типа А (100%);
Статистический анализ, проведенный в программе STATISTICA 10.0 (StatSoft, USA), с помощью двустороннего критерия Фишера показал наличие статистически значимой разницы в частоте встречаемости дозозависимых НЛР у пациентов с разными генотипами (р=0,02098).
Расчет показателя Р для пациентов с генотипом СА показал, что скорость биотрансформации трифлуоперазина у данных пациентов замедлена на 25%, и была получены рекомендации о снижении дозы препарата.
В исследовании, проведенном нами, чувствительность методики составила 66,7%, а специфичность 100%. Невысокий показатель чувствительности обусловлен включением в исследование только одного полиморфизма. Вероятно, у пациентов с генотипом СС по полиморфному маркеру -163С>А, у которых развились НЛР типа А, имели место быть иные полиморфизмы гена CYP1A2, которые привели к накоплению препарата в плазме, что привело к развитию НЛР. Включение в панель генотипирования большего числа полиморфизмов обеспечит повышение чувствительности методики.
Изобретение относится к медицине, а именно к фармакогенетике, клинической фармакологии, психиатрии, наркологии, и может быть использовано для подбора дозы антипсихотического лекарственного средства трифлуоперазина у пациентов. Для этого осуществляют генотипирование с использованием полиморфных маркеров генов CYP1A2. Затем производят расчет значения параметра Р, являющегося оценочной величиной выраженности изменения скорости биотрансформации трифлуоперазина, в зависимости от состояния генетического полиморфизма у каждого конкретного пациента. При значении параметра Р в интервале [50;∞) (отклонении скорости биотрансформации трифлуоперазина на 50% и выше) дается рекомендация о замене лекарственного средства. При значении параметра Р в интервале (-50;0) (замедлении скорости биотрансформации трифлуоперазина меньше чем на 50%) дается рекомендация о понижении дозы. При значении параметра Р в интервале (0;50) (ускорении скорости биотрансформации трифлуоперазина меньше чем на 50%) дается рекомендация о повышении дозы. Способ обладает высокой точностью, информативностью и объективностью. 1 табл.
Способ оптимизации режима дозирования трифлуоперазином для лечения расстройств, сопровождающихся развитием психотической симптоматики, по результатам генотипирования с использованием полиморфных маркеров генов CYP1A2, отличающийся тем, что расчет результирующего изменения скорости биотрансформации трифлуоперазина (параметр Р) осуществляют по формуле
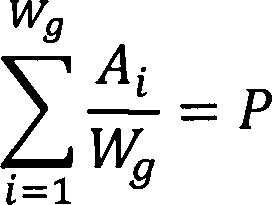 ,
,
где Wg - количество полиморфизмов гена CYP1A2 (основного пути биотрансформации трифлуоперазина);
Ai - изменение скорости биотрансформации трифлуоперазина в зависимости от генотипа по каждому полиморфному маркеру гена CYP1А2,
и если изменение определено как отклонение скорости биотрансформации трифлуоперазина на 50% и выше, рекомендуется замена лекарственного средства, если изменение определено как замедление скорости биотрансформации трифлуоперазина меньше чем на 50%, рекомендуется понижение дозы, если изменение определено как ускорение скорости биотрансформации трифлуоперазина меньше чем на 50%, рекомендуется повышение дозы.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОЦЕНКИ ЭФФЕКТИВНОСТИ ТЕРАПИИ ГАЛОПЕРИДОЛОМ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, СОПРОВОЖДАЮЩИХСЯ РАЗВИТИЕМ ПСИХОТИЧЕСКОЙ СИМПТОМАТИКИ | 2017 |
|
RU2643944C1 |
| US 20170147779 A1, 25.05.2017 | |||
| ДОКУКИНА Т.В | |||
| и др | |||
| Интерпретация результатов фармакогенетического тестирования у пациентов с психическим и поведенческими расстройствами при назначении психотропных лекарственных средств: учеб.-метод | |||
| пособие, Минск: Мисанта, 2016 | |||
| BOZINA N., BRADAMANTE V., LOVRIC M | |||
| Двигатель внутреннего горения | 1921 |
|
SU450A1 |
| Arh Hig Rada Toksikol, 2009, vol.60(2), pp.217-242 | |||
| SHIN J.G., SOUKHOVA N., FLOCKHART D.A | |||
| Двигатель внутреннего горения | 1921 |
|
SU450A1 |
| Drug Metab Dispos., 1999 Sep, 27(9), pp.1078-84. | |||
Авторы
Даты
2019-07-29—Публикация
2018-09-28—Подача