Настоящее изобретение относится к области микробиологии. Точнее, настоящее изобретение относится к характеризации популяции, по меньшей мере, одного микроорганизма с помощью масс-спектрометрии, и, в частности, масс-спектрометрии (MS) с времяпролетной матрично-активированной лазерной десорбцией/ионизацией, известной как MALDI-TOF.
В течение нескольких лет, метод MALDI-TOF использовали для проведения быстрой идентификации микроорганизма на уровне видов. Различные типы инструментов, которые подходят для этого вида характеризации, продаются заявителем, и также, в частности, Bruker Daltonics и Andromas.
Микроорганизм идентифицируется в MALDI-TOF по спектру наиболее распространенных белков в микроорганизме, по сравнению с эталонными данными для того, чтобы идентифицировать семейство, род, и обычно вид микроорганизма. Как правило, используемый протокол включает нанесение, по меньшей мере, части колонии микроорганизмов на пластину для MALDI, добавление матрицы, подходящей для метода MALDI, получение масс-спектра и идентификацию вида путем сравнения с эталонными данными, которые хранятся в базе данных.
В последнее время метод MALDI также используется для детекции феномена устойчивости микроорганизма к антибиотику, и, в частности, для идентификации фенотипа, который отвечает за гидролиз антибиотиков бета-лактамного типа, из-за секреции ферментов типа бета-лактамаз, и, в частности типа карбапенемаз. В этой связи могут быть упомянуты заявки US 2012/0196309 и WO 2012/023845. Характеризация устойчивости с помощью MALDI-TOF включает детекцию гидролизованной формы и/или потерю нативной формы бета-лактамного антибиотика после инкубации с указанным антибиотиком образца, который может содержать микроорганизм, способный продуцировать бета-лактамазы.
Хотя подготовка образца к нанесению не описывается подробно в этих патентных заявках, в общем, предполагается, что микроорганизм смешивают с антибиотиком заранее, а затем полученную смесь наносят на пластину MALDI или используют лизат микроорганизма(ов) (см. WO 2012/023845, в частности, пункт 15).
В документе WO 2012/113699 предусматривается применение масс-спектрометрии для того, чтобы оценить ингибирующее действие вещества на бета-лактамазы, при этом оценка, возможно, проводится в присутствии бактерий.
В следующих публикациях: (Hrabak, Walkova et al. 2011, Hooff, van Kampen et al. 2012, Hrabak, Studentova et al. 2012, Sparbier, Schubert et al. 2012) предлагается более подробное описание протоколов, которые будут осуществляться для подготовки образцов, при этом протоколы включают следующие стадии:
- подготовки инокулята, содержащего колонии микроорганизмов;
- центрифугирования инокулята;
- ресуспендирования бактериальных гранул с раствором антибиотика, с добавлением или без реагента для лизиса;
- инкубирования в течение от 30 минут до 3 часов;
- центрифугирования; и
- переноса 1 мкл супернатанта на пластину для MALDI и добавление 1 мкл матрицы, анализ с помощью MALDI-TOF масс-спектрометрии.
Подготовка образца для обнаружения устойчивости методом MALDI-TOF, таким образом, долгая и утомительная. На самом деле, процедура, используемая для детекции устойчивости по методу MALDI-TOF, влечет за собой необходимость подготовки инокулята с высокой концентрацией и/или одну или несколько стадий центрифугирования. Эти стадии требуют материалы, расходные материалы и специальное оборудование, и, таким образом, потребляют расходные материалы, время и опыт оператора. Кроме того, до начала подготовки такого типа трудно использовать метод MALDI-TOF рутинно для обнаружения устойчивости, учитывая, что проведение описания характеристик большого количества проб в день может быть не предусмотрено. Фактически часто возникает несоответствие между наличием инструмента для проведения идентификации феномена устойчивости методом MALDI-TOF и наличием образцов, полученных после обязательной стадии подготовки. Другая проблема заключается в том, что бактерии инкубируются с антибиотиком в объемах порядка 10 мкл - 50 мкл, что приводит к потенциально высокому риску снижения взаимодействий фермент-антибиотик. Как следствие, может быть снижение эффективности ферментной активности, которое может повлиять на чувствительность обнаружения и, таким образом, надежность метода, в частности, с микроорганизмами, которые, как известно, продуцируют или секретируют небольшие количества ферментов.
Детекция устойчивости к антимикробному агенту также описана в заявках WO 2011/045544 и US 2012/0196309, как проводимая с помощью других методов масс-спектрометрии, таких как тандемная масс-спектрометрия (MS-MS) и мониторинг множественных реакций (MRM). В таких условиях анализ с помощью масс-спектрометрии и, как следствие, с помощью ионизации осуществляется не на микроорганизме, а на белках, полученных после различных операций по очистке.
В контексте настоящего изобретения, авторы изобретения предлагают воплотить новый способ получения зоны характеризации для характеризации микроорганизма методом MALDI, который может быть использован для идентификации устойчивости к антибиотику и который прост в реализации. Кроме того, этот новый способ совместим с получением различных характеристик образца, присутствующего в зоне характеризации, по меньшей мере, одной, соответствующей определению устойчивости к антибиотику, и другой, зачастую, соответствующей идентификации микроорганизма.
Изобретение, таким образом, относится к способу характеризации образца, который содержит, по меньшей мере, один микроорганизм, с применением метода MALDI-TOF, который может быть использован для того, чтобы определить, является ли или нет популяция микроорганизма, устойчивой, по меньшей мере, к одному антимикробному агенту, и в течение относительно короткого периода времени, порядка от нескольких часов до одного часа или даже меньше.
Изобретение также относится к способу получения зоны характеризации аналитической пластины, для того, чтобы выполнять, по меньшей мере, одну характеризацию популяции, по меньшей мере, одного микроорганизма в присутствии, по меньшей мере, одного антимикробного агента, где указанная характеризация включает анализ методом масс-спектрометрии в ходе которого популяция, по меньшей мере, одного микроорганизма, нанесенная в аналитическую зону, подвергается по меньшей мере, одной стадии ионизации путем бомбардировки аналитической зоны лазерным лучом в соответствии с методом масс-спектрометрии с матричной лазерной десорбционной ионизацией, известной как MALDI;
способ получения аналитической зоны отличается тем, что включает последовательно следующие стадии:
- стадию, заключающуюся в предоставлении аналитической пластины для характеризации посредством метода MALDI, где пластина включает, по меньшей мере, одну аналитическую зону, несущую антимикробный агент;
- стадию нанесения популяции, по меньшей мере, одного микроорганизма на указанной аналитической зоне в контакте с антимикробным агентом;
- стадию инкубации, заключающуюся в поддержании аналитической пластины в условиях и в течение времени, достаточных для взаимодействия антимикробного агента и присутствующего микроорганизма; и
- стадию нанесения матрицы, которая пригодна для метода MALDI, на аналитическую зону.
Предпочтительно, в контексте процесса подготовки в соответствии с настоящим изобретением, наносится популяция одного микроорганизма, подлежащего характеризации. Таким образом, зона характеризации может быть затем использована для характеризации одного микроорганизма.
В соответствии с изобретением нанесенную популяцию микроорганизма(ов) получают без предварительной стадии контакта с антимикробным агентом, т.е. нанесенная популяция микроорганизма(ов), не смешена с антибактериальным агентом, присутствующим в зоне характеризации до нанесения.
Способ в соответствии с настоящим изобретением преимущественно проводят на популяции микроорганизма(ов), полученного после стадии концентрирования, обогащения и/или очистки и/или после роста на подходящей среде, в частности, гелевой среде, соответствующей колонии или фракции колонии.
В качестве примера, в контексте настоящего изобретения, антимикробный агент выбирают таким образом, чтобы сделать возможным детекцию устойчивости из-за выработки бета-лактамазы, и, в частности, из-за карбапенемазы.
Антимикробный агент, как правило, антибиотик, предпочтительно выбирают из числа пенициллинов, цефалоспоринов, цефамицинов, карбапенемов и монобактамов, и, в частности, из числа ампициллина, амоксициллина, тикарциллина, пиперациллина, цефалотина, цефуроксима, цефокситина, цефиксима, цефотаксима, цефтазидима, цефтриаксона, цефподоксима, цефепима, азтреонама, эртапенема, имипенема, меропенема и фаропенема.
Способ получения в соответствии с настоящим изобретением может включать стадию функционализации для получения аналитической пластины для характеризации с помощью метода MALDI, содержащей, по меньшей мере, одну аналитическую зону, несущую антимикробный агент, названной функционализированной зоной, где указанная стадия функционализации предпочтительно проводится путем нанесения водного раствора антимикробного агента с последующей сушкой.
Изобретение также относится к способу характеризации популяции, по меньшей мере, одного микроорганизма, где характеризация включает, по меньшей мере, определение присутствия или отсутствия популяции микроорганизма, который устойчив по меньшей мере, к одному антимикробному агенту.
Данный способ отличается тем, что включает последовательно следующие стадии:
- получение, по меньшей мере, одной зоны характеризации на аналитической пластине в соответствии со способом получения по изобретению;
- применение масс-спектрометрии с матрично-активированной лазерной десорбцией/ионизацией, известной как MALDI-TOF, чтобы проанализировать по меньшей мере однократно популяцию микроорганизма, нанесенного на зону характеризации для цели получения заключения, присутствует ли популяция микроорганизма, которая устойчива к антимикробному агенту, в зоне характеризации.
В частности, масс-спектрометрический анализ с помощью метода MALDI-TOF для цели получения заключения, присутствует ли популяция микроорганизма, которая устойчива к антимикробному агенту, в зоне характеризации, заключается в верификации наличия антимикробного агента и/или продуктов деградации антимикробного агента.
Преимущественно способ характеризации в соответствии с настоящим изобретением включает, по меньшей мере, две характеризации. В частности, характеризация дополнительно включает идентификацию семейства, рода или, предпочтительно, вида популяции микроорганизма, нанесенного на зону характеризации.
Предпочтительно, способ характеризации в соответствии с настоящим изобретением включает:
- определение семейства, рода, или, предпочтительно, вида популяции микроорганизма, нанесенного на зону характеризации путем проведения первого анализа методом масс-спектрометрии типа MALDI, соответствующего первой стадии ионизации зоны характеризации, и применение первой калибровки для анализа; и
- определение возможного присутствия в зоне характеризации популяции микроорганизма, который устойчив к антибактериальному агенту путем проведения второго анализа методом масс-спектрометрии с использованием метода MALDI-TOF, соответствующего второй стадии ионизации той же зоны характеризации, и применение второй калибровки для анализа.
В таких обстоятельствах, идентификация семейства, рода или, предпочтительно, вида популяции микроорганизма и определения возможного присутствия антимикробного агента предпочтительно касается одного и того же микроорганизма.
Изобретение также относится к способу характеризации популяции, по меньшей мере, одного микроорганизма, где характеризация включает, по меньшей мере:
- идентификацию семейства, рода или, предпочтительно, вида популяции микроорганизма, путем проведения первого анализа методом масс-спектрометрии с использованием метода MALDI, соответствующего первой стадии ионизации зоны характеризации, содержащей популяцию микроорганизма(ов), антимикробный агент и матрицу, подходящую для метода MALDI;
- определение присутствия популяции микроорганизма, который устойчив, по меньшей мере, к одному антимикробному агенту, путем проведения второго анализа методом масс-спектрометрии с использованием метода MALDI, соответствующего второй стадии ионизации зоны характеризации, включающей популяцию по меньшей мере одного микроорганизма, антимикробный агент и матрицу, подходящую для метода MALDI;
где способ отличается тем, что:
- первый анализ и второй анализ, соответственно, осуществляются с помощью отдельной первой стадии и отдельной второй стадии ионизации одной и той же зоны характеризации, включающей популяцию по меньшей мере одного микроорганизма, и антимикробный агент;
- первый анализ использует первую калибровку, а второй анализ использует вторую калибровку, которая отличается от первой калибровки.
Предпочтительно, нанесенная популяция включает один характеризуемый микроорганизм.
Способ характеризации этого вида предпочтительно использует способ получения зоны характеризации аналитической пластины в соответствии с настоящим изобретением.
В контексте данного изобретения, одна и та же зона характеризации и одна и та же популяция микроорганизма(ов) подвергается двум ионизациям подряд для того, чтобы получить две искомых характеризации: характеризации феномена устойчивости микроорганизма к антимикробному агенту, и идентификацию микроорганизма. Изобретение также относится к способу функционализации аналитической зоны аналитической пластины, адаптированной к методу MALDI, где способ функционализации аналитической зоны отличается тем, что включает:
- стадию функционализации аналитической зоны, для того, чтобы придать аналитической зоне способность принять антимикробный агент.
Стадия функционализации может быть реализована путем нанесения водного раствора антимикробного агента с последующей сушкой.
Изобретение также обеспечивает аналитическую пластину, предназначенную для приема популяции по меньшей мере одного микроорганизма, подлежащего характеризации на аналитической зоне масс-спектрометрией в соответствии с методом MALDI, где пластина отличается тем, что включает антимикробный агент, нанесенный, в частности, в форме твердого слоя на указанную аналитическую зону аналитической пластины, формируя тем самым функционализированную аналитическую зону. В частности, в аналитической пластине такого вида функционализированная аналитическая зона (или зоны), несущая (несущие) антимикробный агент, не включает микроорганизм в количестве, которое детектируется методом MALDI, и/или функционализированная аналитическая зона (или зоны) высушена.
Термин «высушенный», в частности, означает, что антимикробный агент находится не в растворе, а в виде твердого слоя, который сцеплен с аналитической зоной, на которую он нанесен. В частности, сохранение антимикробного агента в аналитической зоне, которая подвергается функционализации, может быть осуществлено электростатическим связыванием, ионным связыванием, ковалентным связыванием, аффинным связыванием, или фактически с помощью адгезивного агента. В частности, адгезивный агент может представлять собой полимер, который растворим в воде. Примером адгезивного агента, который может быть использован для иммобилизации антимикробного агента в аналитической зоне или зонах, который может быть упомянут, является гептакис (2,6-ди-О-метил)-β-циклодекстрин.
В конкретном воплощении, на аналитической пластине, предназначенной для получения популяции, по меньшей мере, одного микроорганизма, подлежащего характеризации, аналитическая зона или каждая аналитическая зона несет одиночный антимикробный агент.
Аналитическая пластина для приема популяции, по меньшей мере, одного микроорганизма в соответствии с настоящим изобретением может быть упакована в герметично закрытую упаковку. В частности, герметично закрытая упаковка может быть пригодна для защиты пластины от света и от влаги.
Функционализированная аналитическая зона (зоны) может быть получена путем нанесения водного раствора антимикробного агента, с последующей сушкой.
Пластины этого типа могут включать множество функционализованных аналитических зон, каждая из которых несет антимикробный агент, в частности, по меньшей мере первую функционализированную аналитическую зону, несущую первый антимикробный агент и вторую аналитическую зону, несущую второй антимикробный агент, который отличается от первого антимикробного агента.
Как правило, пластины этого вида включают, по меньшей мере, одну эталонную аналитическую зону, предназначенную для последующего приема популяции эталонного микроорганизма, и по этой причине поверхность эталонной аналитической зоны не содержит антимикробный агент.
Изобретение относится также к применению аналитической пластины в соответствии с изобретением, в способе характеризации в соответствии с настоящим изобретением.
Приведенное ниже описание, со ссылками на прилагаемые чертежи, способствует лучшему пониманию изобретения.
На фигуре 1 представлен схематический вид сверху пластины MALDI.
Фигуры 2-4 представляют собой масс-спектры, полученные в примерах с помощью метода MALDI-TOF. На этих фигурах шкала интенсивности является относительной шкалой со ссылкой на наиболее интенсивный пик спектра. В качестве примера, в выбранном диапазоне масс (в частности, от 200 m/z до 1200 m/z), если наиболее интенсивный пик составляет 100 мВ, то он принимается за 100% (как указано на левой стороне спектров). Менее интенсивные пики обозначены относительно наиболее интенсивного пика: таким образом, пик с интенсивностью 75 мВ достигает 75% от шкалы (на спектре, который содержит максимальную интенсивность пика 100 мВ). Как следствие, для того же спектра уровень интенсивности пиков между штаммами не может быть сравнен. В противоположность этому, эти спектры могут быть использованы для одного и того же штамма, чтобы сравнить интенсивности между нативным пиком антимикробного агента и продукта его деградации. Также возможно, для одного и того же штамма сравнивать интенсивность между нативным или гидролизованными пиками и контрольным пиком, который не был подвергнут изменениям, которые индуцируют биологическая/ферментативная активность тестируемого микроорганизма. Следующие пики: пик матрицы НССА, пик пептида или эталонной молекулы, добавленной к матрице, или, которая уже высушена в аналитической зоне, можно рассматривать в качестве контрольных пиков.
На фигуре 5 показан внешний вид аналитических зон (пятен), на которые был нанесен антибиотик, фаропенем, в присутствие и в отсутствие адгезивного агента (гептакис), до и после соскабливания с помощью инокуляционной петли.
На фигуре 6 показано изменение соотношения интенсивностей пиков нативного фаропенема и гидролизованного фаропенема, полученных методом MALDI-TOF по сравнению с контрольным пиком НССА в зависимости от соотношений [гептакис]/[фаропенем].
На фигуре 7 представлены масс-спектры, полученные во второй серии сбора данных в примере 5.
На фигуре 8 показано изменение в соотношениях интенсивностей 304/308 и 304/330 в зависимости от концентрации инокулята, используемого для двух штаммов, тестируемых в примере 5.
Фигура 9 представляет собой воплощение случая, дополненного, пластиной MALDI, которая может быть адаптирована к нанесению популяции микроорганизмов в жидком виде.
Аналитические пластины MALDI
Аналитическая пластина MALDI имеет по меньшей мере одну, а в общем случае множество аналитических зон. Аналитические зоны представлены в виде пятен, как правило, круглой формы. Для того, чтобы способствовать последующей ионизации по меньшей мере на уровне аналитической зоны или зон, поверхность пластины является проводящей. Например, аналитическая пластина этого вида образована полимером, таким как полипропилен, причем указанный полимер покрывают слоем нержавеющей стали. Полимер может содержать электропроводный материал, такой как сажа. В качестве примера, такая пластина может представлять собой пластину, представленную на рынке фирмой Shimadzu под названием «Fleximass™ DS disposable maldi targets)).
Широкий круг пластин для MALDI коммерчески доступен, среди них такие, как пластины Fleximass DS от bioMerieux (одноразового или многоразового использования) и пластины MALDI Biotarget от Bruker Daltonics. Пластины I такого вида, как правило, включают от 48 до 96 аналитических зон 1 или пятен, и, по меньшей мере, одну, или даже две или три эталонные аналитические зоны 2, размеры которых, как показано в примере на Фигуре 1, отличаются от аналитических зон.
В контексте настоящего изобретения термин «зона характеризации» используется для аналитической зоны, несущей антимикробный агент, популяцию микроорганизма(ов) и матрицу, пригодную для метода MALDI.
Функционализация аналитических зон
Термин «антимикробный агент» означает соединение, которое способно снижать жизнеспособность микроорганизма и/или снижать его рост или воспроизводство. Антимикробные агенты этого типа могут представлять собой антибиотики, когда они направлены против бактерий. Тем не менее, данное изобретение применимо для любого типа микроорганизмов из ряда бактерий, дрожжей, плесневых грибов, или паразитов, и, таким образом, к соответствующим антимикробным агентам.
Предпочтительно, если антимикробный агент представляет собой антитело, такое как бета-лактам, в частности, выбранный из числа пенициллинов, цефалоспоринов, цефамицинов, карбапенемов и монобактамов, и, в частности, из числа ампициллина, амоксициллина, тикарциллина, пиперациллина, цефалотина, цефуроксима, цефокситина, цефиксима, цефотаксима, цефтазидима, цефтриаксона, цефподоксима, цефепима, азтреонамома, эртапенема, имипенема, меропенема и фаропенема.
Карбапенемы используются, в частности, в качестве последнего средства для борьбы с грамотрицательными бактериями, таких как семейство Enterobacterium, Pseudomonas и Acinetobacter. Антибиотик этого типа, таким образом, наносят на аналитическую зону, когда есть подозрение, что присутствующий микроорганизм, является энтеробактерией или другим грамотрицательным видом, который может иметь устойчивость к карбапенемам.
Предпочтительно, чтобы он наносился из водного раствора антимикробного агента.
Буфер, подходящий для растворения антимикробного агента, а также для оптимизированной активности механизма в области целевой устойчивости, также может быть использован для приготовления раствора антимикробного агента. Также можно предусмотреть добавление солей цинка (в частности хлорида цинка или сульфатного типа) к антимикробному раствору для оптимизации активности металло-бета-лактамаз.
Капля, например, приблизительно от 1 до 2 микролитров, противомикробного раствора может быть нанесена таким образом, чтобы вся аналитическая зона была покрыта. Воду, содержащуюся в растворе, затем выпаривают, например, просто путем сушки в атмосферном воздухе и при температуре окружающей среды. В качестве примера, аналитическая пластина может быть оставлена при температуре, которая находится в диапазоне от 17°С до 40°С, и, в частности, при температуре окружающей среды (22°С). Кроме того, для того, чтобы ускорить сушку, можно перенести ее в термостатическую камеру, например, при 37°С.
Антимикробный агент наносится в водном растворе очень простым способом, это нанесение следует за операцией сушки. Таким образом, получают аналитическую зону, несущую антимикробный агент, которая называется функционализированной. Также возможно иммобилизовать антимикробный агент на аналитическую зону с помощью электростатической, ионной, ковалентной или аффинной связи, или с помощью адгезивного агента. Простое нанесение антимикробного агента не могло бы обеспечить его удовлетворительную иммобилизацию. В частности, если антимикробный агент не связывается в достаточной степени с зоной характеризации, это может привести к потере антимикробного агента при нанесении популяции микроорганизма(ов), что потребовало бы определенной сноровки со стороны оператора при нанесении, или, на самом деле, это может привести к потере антимикробного агента за счет отделения слоя при хранении пластины для MALDI для последующего использования. Кроме того, вместо простого нанесения, антимикробный агент мог бы быть связан с зоной анализа с помощью электростатических, ионных или ковалентных связей с использованием или без использования необязательно-специфического линкера или «плеча» (антитела, рекомбинантных фаговых белков), с помощью взаимодействия биотина/стрептавидина, уже привитых к поверхности аналитической зоны и антимикробного агента, или любым другим типом связи, адаптированным к природе антимикробного агента и к поверхности аналитической зоны, или с помощью адгезивного агента. Тем не менее, режим связывания или нанесения должен быть выбран таким образом, чтобы любое взаимодействие антимикробного агента с микроорганизмом не было нарушено, так как это может привести к маскировке феномена устойчивости. В частности, предпочтительно иммобилизовать антимикробный агент, с помощью адгезивного агента, а не за счет ковалентного связывания или аффинности связывания, для того, чтобы предотвратить изменения в конформации антимикробного агента и чтобы гарантировать, что он может получить надлежащий доступ к активному сайту фермента, который может продуцироваться микроорганизмом.
Когда адгезивный агент, т.е. агента, который прилипает к пластине, и, таким образом, улучшает иммобилизацию антимикробного агента к ней, используется, тогда наносится смесь адгезивного агента и антимикробного агента в водном растворе. В частности, адгезивный агент может представлять собой растворимый в воде полимер. Пример, который может быть упомянут в качестве адгезивного агента, который может быть использован для иммобилизации антимикробного агента в аналитической зоне или зонах, представляет собой гептакис (2,6-ди-О-метил)-β-циклодекстрин. Адгезивный агент должен быть выбран в зависимости от функции антимикробного агента, иммобилизуемого на аналитической зоне. В частности, его следует выбирать в зависимости от его массы, таким образом, чтобы его присутствие не искажало последующее обнаружение MALDI с целью определения наличия или отсутствия присутствующего антимикробного агента и/или продуктов его деградации. Специалист в данной области техники должен регулировать количество адгезивного агента, которое не должно быть слишком высоким, чтобы антимикробный агент являлся доступным для популяции микроорганизма, после нанесения последнего. В качестве примера с гептакис (2,6-ди-О-метил)-β-циклодекстрином, можно выбрать массовое соотношение гептакис (2,6-ди-О-метил)-β-циклодекстрина, к антимикробному агент от 1/20 до 1/2, предпочтительно от 1/10 до 1/5.
Специалист в данной области техники должен адаптировать количество антимикробного агента, нанесенного на аналитическую зону, как функцию антимикробного агента, о котором идет речь. На самом деле, в зависимости от степени ионизации молекулы, достаточное количество должно быть нанесено для того, чтобы была возможность детектировать пик(и), соответствующий антимикробному агенту, с помощью MALDI-TOF с интенсивностями выше фонового шума. В отличие от этого, слишком большое количество антимикробного агента может привести к риску маскировки обнаружения характеризуемого феномена возникновения устойчивости, так что уменьшение интенсивности пика, соответствующего нативному антимикробному агенту, может не наблюдаться. Избыток антимикробного агента может, в частности, компрометировать обнаружение бета-лактамазы с низкой активностью. Например, должно быть нанесено 0,04 г/м2 - 4 г/м2 антимикробного агента. С этой целью, раствор антимикробного агента в воде, в частности в сверхчистой воде, должен быть нанесен в концентрации от 0,1 мг/мл до 10 мг/мл. Например, в случае ампициллина может быть нанесен водный раствор, содержащий 1,7 мг/мл - 10 мг/мл ампициллина, а в случае фаропенема, может быть нанесен водный раствор, содержащий 0,1 мг/мл до 1 мг/мл фаропенема.
Зона характеризации предпочтительно должна нести один антимикробный агент, хотя применение множества антимикробных агентов на одной и той же аналитической зоны не исключается. Зона характеризации несущая множество антимикробных агентов могла бы быть использована для проверки наличия множества ферментов одновременно, и, таким образом, для различных феноменов устойчивости. Когда используется зона характеризации, несущая множество противомикробных агентов, агенты должны быть выбраны таким образом, что массы их нативной формы и/или продуктов их распада под действием фермента-мишени не перекрывали друг друга, так чтобы они могли детектироваться отдельно посредством MALDI-TOF. Например, можно внести еще один антимикробный агент, из того же семейства, или из другого семейства в дополнение к первому антимикробному агенту. Например, некоторые карбапенемы более приспособлены к выявлению конкретной карбапенемазы. Таким образом, можно предусмотреть наличие множества типов карбапенемов или других бета-лактамов на одной и той же зоне характеризации. В противоположность этому, если два антимикробных агента наносятся на одну и ту же зону, они должны быть выбраны таким образом, что их спектры активности не мешали друг другу, чтобы их можно было отдельно обнаружить с помощью MALDI-TOF.
Кроме того, можно внести еще одно соединение, в дополнение к антибактериальным агентам. С бета-лактамами также возможно нанесение ингибитора бета-лактамаз для того, чтобы охарактеризовать феномен ESBL (расширенный спектр бета-лактамаз), как применено, в частности, в заявке WO 2012/023845. В частности, может быть нанесено сочетание бета-лактама с ингибитором бета-лактамаз, таким как клавулановая кислота, сульбактам или разобактам. Если пластина MALDI содержит множество аналитических зон, по меньшей мере, две зоны, или даже более, предпочтительно несут различные антимикробные агенты. Также можно охарактеризовать несколько популяций микроорганизма(ов) с помощью одной пластины. Каждая из зон может нести отдельный антимикробный агент.Как правило, тем не менее, характеризации проводятся в двух повторах, так что одиночный антимикробный агент присутствует, по меньшей мере, в двух аналитических зонах, или даже в большем количестве зон.
Функционализированные пластины MALDI этого типа могут быть поставлены непосредственно потребителю, который в этом случае должен только нанести исследуемую популяцию микроорганизма(ов), а затем, после стадии инкубации, матрицу MALDI. Такие пластины могут быть реализованы в виде индивидуальных упаковок или упаковок, содержащих несколько пластин.
Подготовка и нанесение популяции микроорганизма(ов)
В контексте данного изобретения, популяция микроорганизма(ов) наносится на аналитическую зону Пластины MALDI, функционализированной с помощью антимикробного агента, для его характеризации.
Популяция микроорганизма(ов), может происходить из различных источников. Примеры источников микроорганизма(ов), которые могут быть упомянуты, представляют собой образцы биологического происхождения, в частности, животного или человеческого происхождения. Образец этого типа может соответствовать образцу биологической жидкости, цельной крови, сыворотки, плазме, мочи, цереброспинальной жидкости, или органической секреции, или образцу ткани или выделенных клеток. Этот образец может быть нанесен как есть или, что предпочтительнее, может быть подвергнут подготовке, включающей обогащение или концентрирование культуры и/или экстракцию, или стадию очистки с помощью способов, известных специалисту в данной области, перед нанесением на рассматриваемую аналитическую зону. Тем не менее, подготовка этого типа не должна быть лизисом, который может вызвать распад микроорганизмов и потерю их содержимого перед нанесением на аналитическую зону. Популяция микроорганизма(ов) может быть нанесена в виде инокулята. В контексте данного изобретения, популяция микроорганизма(ов), нанесенная на аналитическую зону, предпочтительно является популяцией живого микроорганизма(ов), хотя экстракция популяции микроорганизма(ов) из биологического образца с использованием детергента, который может повлиять на жизнеспособность, не исключена. Тем не менее, в таких условиях для того, чтобы провести немедленный тест популяции микроорганизма(ов) с помощью MALDI, может быть использован уже присутствующий запас активных ферментов, для характеризации популяции микроорганизмов(ов) путем обнаружения любого феномена устойчивости.
Источником популяции микроорганизма(ов), также может быть агропродовольственный продукт, такой как мясо, молоко, йогурт, и любой другой потребляемый продукт, который может быть загрязнен, или фактически может представлять собой косметический или фармацевтический продукт.И в этом случае продукт такого типа может быть подвергнут обогащению или приготовлению культуры, концентрированию и/или экстрагированию или стадии очистки для получения наносимой популяции микроорганизма(ов).
Как правило, источник микроорганизма(ов), предварительно может быть помещен в культуру в бульоне или на геле с тем, чтобы обогатить его микроорганизмами. Гелевые или бульонные носители этого типа хорошо известны специалистам в данной области. Обогащение на геле особенно выгодно, так как оно может быть использовано для получения колоний микроорганизмов, которые могут быть нанесены непосредственно на аналитическую зону.
В контексте настоящего изобретения, предпочтительно наносить на аналитическую зону клеточную среду, содержащую бактериальную популяцию, а не один или несколько белков, полученных после стадии экстракции или очистки, как в случае с методами MS/MS или MRM. Предпочтительно, если нанесенная популяция микроорганизмов содержит, по меньшей мере, 105 КОЕ микроорганизмов. Например, 105 КОЕ - 109 КОЕ микроорганизма может быть нанесено. Например, можно приступить непосредственно к нанесению биомассы, капнув суспензию микроорганизмов в сверхчистой воде или буфере. Может быть нанесена колония или фракция колонии микроорганизма.
Нанесенная популяция предпочтительно содержит один вид микроорганизма. Тем не менее, не исключается нанесение на аналитическую зону популяции, содержащей различные микроорганизмы. В этом случае, предпочтительно, чтобы было известно, что микроорганизмы будут развивать различные механизмы устойчивости, чтобы была возможность знать, какой микроорганизм представляет идентифицированную устойчивость.
В контексте данного изобретения не целесообразно проводить какую-либо подготовку наносимого образца. В частности, популяция микроорганизма(ов) наносится без предварительного контакта с антимикробным агентом. На самом деле в контексте настоящего изобретения нет необходимости проводить длительную и утомительную подготовку наносимого образца; наносимая популяция микроорганизма(ов), может быть получена без стадии центрифугирования.
Нанесение осуществляется таким образом, что популяция микроорганизма(ов) наносится на аналитическую зону единообразно. Для этой цели можно использовать процедуры, употребляемые для проведения стандартной идентификации микроорганизмов, описанные в руководствах для коммерческих инструментов MALDI-TOF, таких как инструмент VITEK® MS, выпускаемого фирмой bioMerieux.
Тем не менее, в дополнение к популяции микроорганизма(ов), также можно добавить соединение, о котором известно, что оно ускоряет ферментативную реакцию, встречающуюся в рассматриваемом механизме устойчивости. Это соединение может представлять собой цинк, например, в виде ZnCl2 или сульфата цинка, который, в частности, что является важным кофактором активности металло-бета-лактамаз. Это соединение уже может быть нанесено на аналитическую зону в комбинации с антибактериальным агентом или в любое другое время во время подготовки зоны характеризации.
Тот факт, что нанесенное вещество на аналитическую зону действительно содержит популяцию, по меньшей мере, одного микроорганизма может быть определен первоначально с помощью подходящего теста, в частности, на основании того факта, что оно является колонией, выделенной на геле. Предпочтительно, чтобы на аналитическую зону наносилась одна популяция одного микроорганизма.
Инкубация
После нанесения популяции микроорганизма(ов), аналитическую зону, несущую как антимикробный агент, так и популяцию характеризуемого микроорганизма, подвергают стадии инкубации, для того, чтобы обеспечить взаимодействие микроорганизма и антимикробного агента, и обеспечить, таким образом, в случае присутствия популяции микроорганизмов, которые устойчивы к антимикробному агенту, проявления реакции/феномена возникновения устойчивости. В частности, когда детектируемый феномен устойчивости обусловлен наличием фермента, вырабатываемого нанесенными микроорганизмами, инкубирование может быть осуществлено таким образом, чтобы позволить пройти ферментативной реакции.
В контексте данного изобретения, феномен, ответственный за устойчивость к антимикробному агенту, таким образом, происходит непосредственно на пластине MALDI, а не перед нанесением популяции микроорганизма(ов) уже в присутствии антимикробного агента на пластине MALDI, как это происходит в случае методов предшествующего уровня техники. Феномен, ответственный за устойчивость к антимикробному агенту, имеет место в минимальном объеме, соответствующем зоне характеризации. Таким образом, ограничиваются проблемы с разбавлением, обнаруженные в случае методов предшествующего уровня техники.
Условия и период инкубации должны быть адаптированы специалистом в данной области как функция характеризуемого феномена устойчивости.
В качестве примера, аналитическая пластина может быть оставлена при температуре, которая находится в диапазоне от 17°С до 40°С, и, в частности, при температуре окружающей среды (22°С). Кроме того, можно перенести ее в термостатическую камеру, например, при 37°С, с тем чтобы содействовать ферментативной реакции, которая может быть причиной этого феномена устойчивости.
Влажность воздуха должна быть адаптирована так, чтобы предотвратить высыхание присутствующих микроорганизмов, в частности, когда детектируемый феномен устойчивости использует реакцию гидролиза. Пластина может быть помещена в течение инкубации во влажную атмосферу, по меньшей мере, таким образом, чтобы количество влаги, предоставленное непосредственно нанесенным веществом, содержащим популяцию микроорганизма(ов), было достаточно.
В выбранных условиях время инкубации должно быть достаточным для того, чтобы обеспечить последующее обнаружение, с помощью МС MALDI-TOF, феномена устойчивости, который должен детектироваться, в частности, по ферментативной реакции феномена устойчивости, опосредованной ферментом. Инкубацию обычно проводят в течение не менее 5 мин, более предпочтительно в течение, по меньшей мере, 20 минут, а еще более предпочтительно в течение периода от 45 до 90 минут.
В контексте данного изобретения, было показано, что проведение стадии инкубации этого типа не оказывает никоим образом вредное воздействие на последующую идентификацию микроорганизма, если такая характеризация должна быть проведена в дополнение к обнаружению феномена устойчивости.
Нанесение матрицы MALDI
В общем, матрицы, используемые в методе MALDI, являются светочувствительными и кристаллизуются в присутствии популяции микроорганизма(ов), при сохранении целостности присутствующих молекул и микроорганизмов. Матрицы такого типа, в частности, пригодные для метода MS MALDI-TOF, хорошо известны и, например, состоят из соединения, выбранного из: 3,5-диметокси-4-гидроксикоричной кислоты, а-циано-4-гидроксикоричной кислоты, феруловой кислоты и 2,5-диоксибензойной кислоты. Специалистам в данной области известны многие другие соединения. Существуют также жидкие матрицы, которые не кристаллизуются ни при атмосферном давлении, ни под давлением. Может быть использовано любое другое соединение, которое может быть использовано для того, чтобы ионизировать молекулы, присутствующие в зоне характеризации под действием лазерного луча.
Для того чтобы получить матрицу, соединение этого типа растворяется, как правило, в воде, предпочтительно «сверхчистого» качества, или в смеси воды и органического растворителя (растворителей). Примерами органических растворителей, которые обычно используются и которые могут быть упомянуты, являются ацетон, ацетонитрил, метанол, и этанол. Иногда может быть добавлена трифторуксусная кислота (ТФУ). В качестве примера, один пример матрицы состоит из 20 мг/мл синаповой кислоты в смеси ацетонитрил/вода/TFA 50/50/0,1 (об./об.)). Органический растворитель, позволяет присутствующим гидрофобным молекулам, растворяться в растворе, хотя вода может быть использована для растворения гидрофильных молекул. Присутствие кислоты, такой как TFA, способствует ионизации молекул с помощью протонного захвата (Н+).
Раствор, образующий матрицу, наносят непосредственно на аналитическую зону, а затем покрывают популяцию микроорганизмов и антимикробного агента, присутствующих на ней.
Необязательно способ в соответствии с настоящим изобретением может также включать стадию кристаллизации матрицы, которая имеет место перед стадией ионизации зоны характеризации. Как правило, матрицу кристаллизуют, позволяя матрица высохнуть в окружающем воздухе. Растворитель в матрице таким образом, выпаривают, например, путем оставления аналитической пластины при температуре, которая, например находится, в диапазоне от 17°С до 30°С, и, в частности, при температуре окружающей среды (22°С) в течение нескольких минут, например в течение от 5 минут до 2 часов. Это испарение растворителя позволяет кристаллизоваться матрице, в которой распределены популяция микроорганизма(ов) и антимикробный агент.
Ионизация и получения масс-спектра
Популяция микроорганизма(ов), и антимикробный агент, помещенные в матрицу MALDI и образовавшие зону характеризации, подвергаются мягкой ионизации.
Лазерный луч, используемый для ионизации, может иметь любую длину волны, которая благоприятна для сублимации или испарения матрицы. Предпочтительно используют ультрафиолетовую длину волны, или даже инфракрасную длину волны. В качестве примера, эта ионизация может быть осуществлена с помощью азотного лазера, излучающего ультрафиолетовое (УФ) излучение при 337,1 нм.
В процессе ионизации, популяция микроорганизма(ов) и противомикробное средство подвергаются лазерному возбуждению. Матрица затем поглощает световую энергию, а восстановление этой энергии возгоняет матрицу, что приводит к тому, что молекулы, присутствующие в популяции микроорганизма(ов), и в антимикробном агенте десорбируются, и это приводит материал в состояние, которое называется плазма. В этой плазме происходит обмен зарядами между молекулами матрицы, микроорганизмов, и антимикробного агента. В качестве примера, протоны могут быть оторваны от матрицы и перенесены на белки, пептиды, и органические соединения, присутствующие в зоне характеризации. Эта стадия может быть использована для проведения мягкой ионизации присутствующих молекул, не вызывая их разрушение. Популяция микроорганизма(ов) и антимикробного агента затем высвобождает ионы различных размеров. После этого эти ионы ускоряются электрическим полем и свободно летят в трубке при пониженном давлении, известной как пролетная трубка. Давление, прилагаемое при ионизации и во время ускорения образованных ионов, как правило, находится в диапазоне от 10-6 до 10-9 миллибар [мбар]. Самые маленькие ионы поэтому «летят» быстрее, чем более крупные ионы, что позволяет им разделяться. Детектор расположен на конце пролетной трубки. Время пролета (TOF) ионов используется для вычисления их массы. Таким образом, получается масс-спектр, который представляет собой интенсивность сигнала, соответствующего числу ионизированных молекул одной и той же массы на заряд (m/z), в зависимости от соотношения m/z молекул, попадающих в детектор. Соотношение массы к заряду (m/z) выражается в Томсонах [Th]. После введения в масс-спектрометр, спектр зоны характеризации получают очень быстро, обычно менее чем за минуту.
Способ масс-спектрометрии MALDI-TOF, пригодный для применения в соответствии с настоящим изобретением, в частности, может включать следующие последовательные стадии для получения масс-спектра:
- обеспечения зоны характеризации, содержащей популяцию микроорганизма(ов) для изучения и, по меньшей мере, один антимикробный агент в матрице, адаптированной для MALDI-спектрометрии;
- необязательно, проведения кристаллизации матрицы, в которую помещены популяция микроорганизма(ов) и антимикробный агент;
- ионизации смеси популяции микроорганизма(ов) и антимикробного агента и матрицы с помощью лазерного луча;
- ускорения ионизированных молекул, полученного из-за разности потенциалов;
- осуществления свободного перемещения ионизированных и ускоренных молекулы в трубке при пониженном давлении;
- детекции, по меньшей мере, части ионизированных молекул на выходе из трубки таким образом, чтобы измерить время, которое у них заняло перемещение через трубку при пониженном давлении, и чтобы получить сигнал, соответствующий количеству ионизированных молекул, достигающих детектор в конкретный момент времени; и
- вычисления соотношения массы к заряду (m/z) детектируемых молекул таким образом, чтобы получить сигнал, соответствующий количеству ионизированных молекул одинаковой массы к заряду (m/z) как функцию соотношения m/z детектируемых молекул.
В общем, соотношение m/z рассчитывается с учетом первоначального калибровки масс-спектрометра, используемое в виде уравнения, связывающего соотношение массы к заряду (m/z) и время пролета ионизированных молекул в трубке при пониженном давлении.
Калибровка заключается в использовании молекулы или микроорганизма (в зависимости от характеризации), которые дают ионизированные молекулы, перекрывающие диапазон масс, соответствующих предусматриваемой характеризации. Соотношения m/z этих ионизированных молекул выполняют роль стандартов, позволяя прибору провести измерение масс должным образом.
Для идентификации микроорганизма калибровка может быть проведена с использованием штамма бактерий с ионизированными молекулами, которые имеют соотношения m/z, перекрывающие диапазон масс, используемых для идентификации (как правило, в диапазоне от 2000 дальтон (Да) до 20000 дальтон для дрожжей, плесени, бактерий, или паразитов). Для детекции сигналов, соответствующих антибактериальному агенту, калибровка может быть выполнена с использованием смеси пептидов малых масс. В контексте данного изобретения, например, может быть использован калибрант pepMIX 6 (LaserBio Labs), охватывающий диапазон масс от 350 Да до 1000 Да.
Для получения масс-спектра может быть использован любой тип масс-спектрометра MALDI-TOF. Спектрометры этого типа включают:
i) источник ионизации (в общем случае УФ-лазер) для ионизации смеси популяции микроорганизмов (ов) и антимикробного агента и матрицы;
ii) ускоритель ионизированных молекул, применяющий разность потенциалов;
iii) трубка с пониженным давлением, в которой движутся ионизированные и ускоренные молекулы;
iv) масс-анализатор, предназначенный для разделения молекулярных ионов, образующихся в зависимости от их соотношения массы к заряду (m/z); и
v) детектор, предназначенный для измерения уровня сигнала, выдаваемого непосредственно молекулярными ионами.
В контексте настоящего изобретения, анализ с помощью MALDI-TOF, предпочтительно представляет собой простой анализ MALDI-TOF, хотя анализ с помощью MALDI-TOF TOF не исключается. Анализ с помощью MALDI-TOF -TOF, хотя и является более сложным, может быть предусмотрен, в частности, с целью повышения чувствительности обнаружения, при определенных обстоятельствах, и это требует, инструмент, который подходит для анализа этого типа.
Обнаружение устойчивости к антимикробному агенту
Термин «устойчивость» означает явление, при котором микроорганизм не демонстрирует снижение его жизнеспособности или уменьшение его роста или его воспроизводства, когда подвергается воздействию концентрации антимикробного агента, которая признается в качестве эффективной против указанного микроорганизма при отсутствии устойчивости.
Механизм устойчивости может быть идентифицирован из масс-спектра, полученного для рассматриваемой зоны характеризации путем детекции на полученном масс-спектре пика с заданной массой или изменении в массовом пике по сравнению с эталонным масс-спектром, в частности, по сравнению с масс-спектром антимикробного агента, присутствующего в указанной зоне характеризации.
В контексте данного изобретения, было показано, что проведение масс-спектрометрии с помощью MALDI-TOF непосредственно на микроорганизме в присутствии антимикробного агента должно позволить обнаружить представляющие интерес молекулы, которые имеют отношение к определению устойчивости к указанному антимикробному агенту. Определение любой устойчивости популяции микроорганизма таким образом, может включать следующие стадии:
a1) получение эталонного масс-спектра, например, для антимикробного агента, и/или для продуктов его деградации; продукты деградации этого типа являются результатом феномена устойчивости и обусловлены, в частности, наличием деградирующего фермента;
b1) применение ионизации к популяции микроорганизма(ов) и антимикробному агенту, которые нанесены на аналитическую зону и нанесены в присутствии матрицы (соответствующей зоны характеризации в соответствии с изобретением);
c1) получение масс-спектра после этой ионизации, в диапазоне представляющих интерес масс, для определения устойчивости; и
d1) сравнение масс-спектра, полученного на стадии c1) с эталонным спектром и выведении из него наличия или отсутствия устойчивости.
В стадии d1), например, если, на масс-спектре, полученном на стадии c1), пик или пики с массой, характерной для антимикробного агента исчезли, и/или, если один или несколько из пиков с массой, характерной для одного или нескольких продуктов распада антимикробного агента, присутствуют, то можно сделать вывод о том, что присутствует микроорганизм, который устойчив к антибактериальному агенту. Например, интерпретация может быть выполнена из соотношения интенсивностей между пиком с характерной массой для антимикробного агента или одного из его продуктов деградации и пика с характерной массой для внешнего калибранта, или из соотношения интенсивностей между пиком с характерной массой для антимикробного агента, и пиком с характерной массой для продукта деградации антимикробного агента.
Кроме того, можно сравнить уровень интенсивности между пиком или пиками с характерной массой для антимикробного агента или пика или пиков с массой, характерной для одного или нескольких продуктов распада антимикробного агента и одного или нескольких пиков эталонного соединения, которое присутствует, и которое не было подвергнуто вариациям, индуцируемым тестируемой
биологической/ферментативной активностью. Примеры эталонных пиков, которые могут быть рассмотрены, являются один или несколько пиков матрицы MALDI, один или нескольких пиков пептида или эталонной молекулы, добавленных к матрице или, которые уже высушены на аналитической зоне, или один или несколько пиков, соответствующих молекуле присутствующего микроорганизма (например, метаболит), которая всегда присутствует и неизменна в нескольких видах.
При определении устойчивости, калибровка выполняется в диапазоне масс, соответствующих низким массам, как правило, в интервале от 200 дальтон до 1200 дальтон, а предпочтительно в диапазоне от 200 Да до 600 Да. Масс-спектр, полученный на стадии c1), также входит в этот диапазон масс. Для того, чтобы выполнить эту калибровку, два мкл калибровочного раствора, состоящего из смеси пептидов (рерМГХб, LaserBio Labs) и матрицы НССА, α-циано-4-гидроксикоричной кислоты, можно нанести, например, на зону эталонного анализа. До ионизации зон характеризации, на этой эталонной аналитической зоне ионизируется калибрант.Соотношения m/z ионизированных молекул калибранта затем выполняют роль стандартов, с тем чтобы, чтобы позволить используемому инструменту измерить массы соответствующим образом.
Способ в соответствии с изобретением, в частности, может быть использован для детекции устойчивости из-за способности микроорганизма секретировать фермент, который, как известно, деградирует антибиотики бета-лактамного типа, и, в частности, выбраны из числа пенициллиназ, цефалоспориназ, цефамициназ, и карбапенемаз. Изобретение также может применяться для обнаружения других феноменов устойчивости, основанных на деградации или ферментативной модификации, вызывающих изменение в массе антимикробного агента. В качестве примера, можно упомянуть механизмы устойчивости, такие как деградация макролидов эстеразами или деградация фосфомицина эпоксидазами, ацетилирование аминозидов, хлорамфеникола или фактически стрептограминов, фосфорилирование аминозидов, макролидов, рифампицина, и пептидных антибиотиков, гидроксилирование тетрациклина, аденилирование аминозидов и линкозамидов, АДФ-рибозилирование рифампицина и гликозилирование макролидов и рифампицина.
Термин «продукт деградации» включает любой продукт, соответствующий изменению химической структуры антимикробного агента вследствие действия присутствующего микроорганизма. В дополнение к механизмам деградации и ферментативной модификации, упомянутым выше, термин может также включать добавление группы, которая обнаруживается в MALDI-TOF, которая инактивирует антимикробный агент, или которая предотвращает его связывание со своей мишенью.
Способ этого типа для обнаружения устойчивости может быть выполнена с предварительно функционализированными пластинами MALDI с помощью коммерчески доступных инструментов MALDI-TOF. Только стадии калибровки и интерпретации необходимо адаптировать для того, чтобы сделать возможной детекцию устойчивости. В контексте настоящего изобретения теперь возможно детектирование устойчивости к антимикробным агентам, и, в частности, быстрое определение устойчивости к данному антибиотику в обычной манере, которое может иметь жизненно важное значение во многих клинических случаях.
Способ характеризации в соответствии с настоящим изобретением, который может быть использован для идентификации присутствия микроорганизма, который устойчив к антибиотикам, в очень короткий промежуток времени представляет особый интерес для экспресс-диагностики. Это особенно верно для обнаружения карбапенемаза-продуцирующих энтеробактерий (СРЕ). Способ в соответствии с изобретением, может быть использован для проведения экспресс-диагностики в условиях стационара, с тем, чтобы адаптировать лечение антибиотиками, которые вводят в быстром порядке.
Идентификация микроорганизма
Микроорганизмы, которые могут быть идентифицированы с помощью способа по изобретению, являются всеми видами микроорганизмов, болезнетворных или иных, которые встречаются как в промышленности, так и в клинических случаях, и которые могут демонстрировать феномен устойчивости к антимикробным агентам. Они могут являться предпочтительно бактериями, плесневыми грибами, дрожжами, или паразитами. Изобретение имеет особое применение к исследованию бактерий. Примерами микроорганизмов такого типа, которые могут быть упомянуты, являются грамположительные, грамотрицательные и микобактерии. Примерами родов грамотрицательных бактерий, которые могут быть упомянуты, являются: Pseudomonas, Escherichia, Salmonella, Shigella, Enterobacter, Klebsiella, Serratia, Proteus, Acinetobacter, Citrobacter, Aeromonas, Stenotrophomonas, Morganella, Enterococcus и Providencia, и, в частности, Escherichia coli, Enterobacter cloacae, Enterobacter aerogenes, Citrobacter sp., Klebsiella pneumoniae, Klebsiella oxytoca, Pseudomonas aeruginosa, Providencia rettgeri, Pseudomonas putida, Stenotrophomonas maltophilia, Acinetobacter baumanii, Comamonas sp., Aeromonas sp., Morganella morganii, Enterococcus sp., Proteus mirabilis, Salmonella senftenberg, Serratia marcescens, Salmonella typhimurium и т.д. Примеры родов грамположительных бактерий, которые могут быть упомянуты, являются: Enterococcus, Streptococcus, Staphylococcus, Bacillus, Listeria и Clostridium.
Эталонные спектры, полученные с помощью MALDI-TOF для микроорганизмов такого типа, которые соответствуют их основным белкам, являются доступными и хранятся в базах данных, прилагаемых к коммерческим инструментам MALDI-TOF, что позволяет идентифицировать присутствие таких микроорганизмов, которые будут определены путем сравнения.
Идентификация присутствия популяции микроорганизма, таким образом, может включать следующие стадии:
а2) получение эталонного масс-спектра, по меньшей мере, одного микроорганизма, и, как правило, для ряда микроорганизмов;
b2) применение ионизации к популяции микроорганизма(ов) и антимикробному агенту, нанесенному на аналитическую зону и в присутствии матрицы (соответствующей зоне характеризации в соответствии с изобретением);
с2) получение масс-спектра, полученного после этой ионизации, в диапазоне представляющих интерес масс, для идентификации микроорганизма; и
d2) сравнение масс-спектра, полученного на стадии с2) с эталонным спектром и установление на его основе семейства, рода или, что предпочтительнее, вида, по меньшей мере, одного микроорганизма.
При идентификации микроорганизмов, калибровка проводится в диапазоне масс, соответствующих большим массам, как правило, в диапазоне от 2000 Да до 20000 Да, а предпочтительно в диапазоне от 3000 Да до 17000 Да. Масс-спектр, полученный на стадии с2), также входит в этот диапазон масс.
Калибровка может быть выполнена путем размещения популяции эталонного микроорганизма в аналитической зоне, присутствующей на пластине и ее анализе с помощью MALDI-TOF. Например, эталонный микроорганизм этого типа может быть бактерией Е. coli. Для этой калибровки можно использовать процедуры, описанные для проведения стандартной идентификации микроорганизмов в инструкции по эксплуатации коммерческих инструментов MALDI-TOF, таких как инструмент VITEK® MS, выпускаемого фирмой  .
.
Можно использовать для калибровки две эталонные аналитические зоны: одну для идентификации микроорганизмов, а другую для характеризации устойчивости. Кроме того, можно использовать одну и ту же эталонную зону для выполнения обеих калибровок. В таких обстоятельствах, эталонная зона должна быть функционализирована с помощью антибактериального агента, устойчивость к которому должна быть изучена.
В контексте данного изобретения, предпочтительно, но не существенно, когда должны быть проведены обе следующие характеризации: определение устойчивости и идентификация микроорганизма, то устойчивость обнаруживается позже, то есть стадии ионизации и анализа, необходимые для детекции устойчивости, проводят на зоне характеризации после стадии, необходимой для идентификации микроорганизма.
Когда две характеризации выполняются на одной и той же зоне, это может быть осуществлено без удаления аналитической пластины из масс-спектрометра, используемого для анализа MALDI-TOF. Эта двойная характеризация, таким образом, может включать следующие стадии:
а3) получение эталонного масс-спектра 1, по меньшей мере, одного микроорганизма и, как правило, для ряда микроорганизмов, и масс-спектра 2 для антимикробного агента, и/или для продуктов его деградации;
b3) калибровки используемого масс-спектрометра при помощи калибранта, используемого для идентификации, который уже был нанесен на эталонную аналитическую зону;
с3) применение ионизации к популяции микроорганизма(ов) и антимикробного агента, нанесенных на аналитическую зону в присутствии матрицы (соответствующей зоне характеризации в соответствии с изобретением);
d3) получение масс-спектра, полученного после этой ионизации, в диапазоне представляющих интерес масс для идентификации микроорганизмов;
е3) калибровки масс-спектрометра, используемого во второй раз с помощью калибранта, используемого для обнаружения устойчивости, который уже был нанесен на эталонную аналитическую зону;
f3) применение ионизации снова к популяции микроорганизма(ов) и антимикробному агенту, нанесенных на аналитическую зону и приведенных во взаимодействие с матрицей (соответствующей зоне характеризации в соответствии с изобретением);
g3) получение масс-спектра, полученного после этой ионизации, в диапазоне представляющих интерес масс для определения устойчивости;
h3) сравнение масс-спектра, полученного на стадии d3) с эталонным спектром или спектром 1 и установление из него семейства, рода или, что предпочтительнее, вида по меньшей мере, одного присутствующего микроорганизма; и
i3) сравнения масс-спектра, полученного на стадии g3) с эталонным спектром 2 и установление из него присутствия или отсутствия устойчивости.
Стадии с3) и f3), таким образом, осуществляются на одной и той же зоне характеризации и, таким образом, на одной и той же популяции микроорганизма (ов), что, таким образом, означает, что стадии подготовки и манипуляции могут быть сокращены.
В контексте данного изобретения, одна и та же популяция микроорганизма(ов), и ее одиночный слой на одной аналитической зоне используются для получения зоны характеризации, к которой последовательно применяются две ионизации для проведения двух характеризаций (характеризация феномена устойчивости микроорганизма к антимикробному агенту и идентификация микроорганизма).
Фактически неожиданно было показано, что наличие антимикробного агента и проведение предварительной стадии инкубации, необходимой для обнаружения феномена устойчивости, никоим образом не препятствуют возможности идентификации микроорганизма.
Стадии сравнения h3) и i3) могут быть проведены в конце способа или после каждого случая рассматриваемого получения данных.
Предпочтительно, чтобы нанесенная популяция соответствовала популяции одного микроорганизма, и две характеризации: детекция устойчивости и идентификация микроорганизма, - относились к одному и тому же микроорганизму.
В заключение, изобретение может быть использовано для того, чтобы:
- быстро получать информацию из одной и той же зоны характеризации и, в частности, с одной стороны характеризовать феномен устойчивости к антимикробному агенту, а с другой стороны - идентифицировать микроорганизм;
- упрощение способов анализа MALDI-TOF без длительной и утомительной подготовки образца перед нанесением его на пластину MALDI для характеризации феномена устойчивости к антимикробному агенту;
- получения оптимального контакта непосредственно на пластине MALDI микроорганизма и антимикробного агента иногда оказывает положительное влияние на чувствительность обнаружения феномена устойчивости;
- достижение сокращения затрат времени и средств, что касается расходных материалов и ручной работы при проведении характеризации феномена устойчивости к антимикробному агенту с помощью MALDI-TOF; и
- достижение улучшенного отслеживания и лучшего управления анализируемыми образцами, учитывая, что нет необходимости в проведении предварительной инкубации в присутствии антимикробного агента перед его нанесением на пластинку MALDI.
Приведенные ниже примеры предназначены для иллюстрации изобретения, но они не ограничивают каким-либо образом. Анализы проводились с помощью инструмента VITEK® MS, выпускаемого фирмой  . Анализы проводились в каждом из приведенных ниже примеров в конце сбора данных. Получали спектры для всех зон характеризации, а затем анализировали:
. Анализы проводились в каждом из приведенных ниже примеров в конце сбора данных. Получали спектры для всех зон характеризации, а затем анализировали:
для идентификации спектр анализировали с помощью обработчика VITEK MS и базы данных V2.0.0, содержащихся в программном обеспечении Spectra Identifier версии 2.1.0;
для гидролиза пики спектров визуализировали с помощью программы для сбора данных Launchpad V2.8. Пример 1.
Предварительные эксперименты были проведены для того, чтобы показать, что с помощью MALDI-TOF возможно обнаружить пики антибиотиков бета-лактамного типа после нанесения на аналитическую зону пластины MALDI капли раствора, содержащего антибиотик, смешенного с соответствующей матрицей для метода MALDI. В настоящем эксперименте, аналитическую зону пластины MALDI (VITEK® MS одноразовые пластины ТО-430) обрабатывали бета-лактамным антибиотиком и тестировали для того, чтобы оценить способность антибиотиков расщепляться бета-лактамазой. Ампициллин использовали в качестве модели бета-лактамного антибиотика. Эксперимент проводился путем осуществления представленных ниже стадий:
- 2 мкл раствора ампициллина в концентрации 10 мг/мл в воде наносили в виде капли на аналитическую зону пластины MALDI. Пластину инкубировали при 37°С, до полного высыхания капли.
- 2 мкл рекомбинантной бета-лактамазы (бета-лактамаза Pseudomonas aeruginosa, Sigma-Aldrich партия L6170-550UN CAS: 9073-60-3.).
- 2 мкл рекомбинантной бета-лактамазы в концентрации 1 мг/мл в воде, которую использовали с добавлением цинка в виде сульфата цинка (0,76 миллимоль (мМ)) для стимуляции ферментативной активности, наносили на сухую аналитическую зону, несущую ампициллин. В тоже время осуществляли отрицательный контроль путем нанесения на другую аналитическую зону, обрабатываемую таким же образом амипициллином, 2 мкл капли воды с 0,76 мМ цинка, но без фермента.
- Пластину инкубировали при температуре окружающей среды в течение одного часа для проведения ферментативной реакции.
- 1 мкл матрицы НССА, альфа-циано-4 гидроксикоричной кислоты (матрицы VITEK MS СНСА, Biomerieux ссылка: 411071), наносили на аналитическую зону, уже содержащую ампициллин с или без рекомбинантной бета-лактамазы.
- масс-спектрометрический анализ MALDI-TOF проводили с помощью прибора VITEK® MS с использованием 2 мкл смеси НССА и рерМГХ 6 (приобретенной у LaserBio Labs), используемой в качестве калибранта, которые были нанесены на эталонную аналитическую зону, для того, чтобы откалибровать прибор для низких масс. Указанную смесь получали путем добавления одного объема pepMix6 (10Х) к 9 объемам НССА. Раствор pepMix6 (10Х) получали в разбавителе (трифторуксусной кислоте, 0,01% в сверхчистой воде), в соответствии с рекомендациями производителя. Пики получали для низкого диапазона масс от 200 Да до 1200 Да и изучали присутствие молекул, соответствующих нативной молекуле ампициллина или продуктам его деградации после гидролиза.
Все образцы анализировали на пластине в двух повторах.
На фигуре 2 представлена зависимость полученных масс-спектров и показано, что ампициллин не был стабильным на пластине, и что его эффективно деградирует бета-лактамаза после инкубации. Фактически на фигуре 2 наблюдали основной пик при 368,09 m/z, что соответствует гидролизованной форме ампициллина (вычисленная масса мононатриевой формы ампициллина, соответствующая 368,4 m/z) и полную потерю нативной формы при 372,09 m/z (масса, вычисленная для мононатриевой формы ампициллина, соответствующая 372,4 m/z) на верхнем спектре, соответствующая аналитической зоне с бета-лактамазой. В отличие от этого, для отрицательного контроля (нижний спектр), основной пик находился при 372,09 m/z, что соответствует мононатриевой нативной форме ампициллина. Незначительный спонтанный гидролиз ампициллина также наблюдался в отрицательном контроле. Это свидетельствует о том, что ферментативная реакция гидролиза бета-лактамов может детектироваться с помощью метода MALDI-TOF, с применением способа получения зоны характеризации в соответствии с настоящим изобретением.
Пример 2
Этот эксперимент был проведен с целью изучения деградации ампициллина различными штаммами бактерий после нанесения колоний непосредственно на аналитическую зону с ампициллином, который наносили в виде раствора и сушили, как описано в примере 1.
Бактериальные штаммы и их характеристики представлены в таблице 1 ниже.
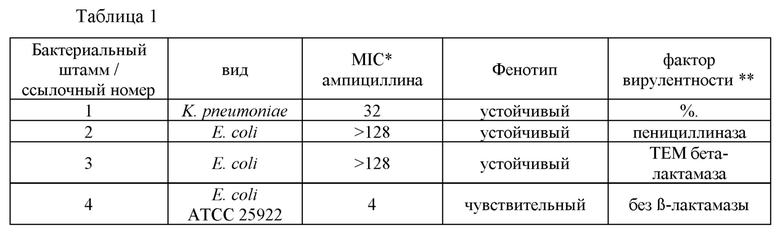
* MIC: минимальная ингибирующая концентрация штамма
** Фактор вирулентности: соответствует известному секретируемому ферменту
Тесты были реализованы путем выполнения представленных ниже стадий:
- 2 мкл водного раствора ампициллина в концентрации 10 мг/мл, с добавлением цинка (0,76 мМ), наносили на аналитические зоны пластины MALDI (так же, как в примере 1).
- Пластину инкубировали при 37°С до тех пор, пока капли осаждаемого раствора не высыхали полностью.
- Для каждого бактериального штамма, часть колонии полученной выращиванием в течение 24 ч на гелевой среде, наносили в двух повторах на аналитические зоны, несущие ампициллин. Каждое пятно было получено, как описано в процедуре VITEK® MS для идентификации микроорганизмов.
- Пластину инкубировали при комнатной температуре (20-25°С) в течение одного часа во влажной атмосфере. С этой целью, закрытый сосуд, содержащий воду, использовали в качестве инкубационной камеры для пластины.
- 1 мкл матрицы НССА добавляли к зонам анализа, несущим как антибиотик, так и бактерии.
- Масс-спектрометрический анализ MALDI-TOF проводили с помощью инструмента VITEK® MS, при этом пластину устанавливали в вакууме после помещения в камеру прибора, путем выполнения следующих двух стадий:
- первое получение данных спектра зон характеризации после калибровки инструмента по эталонной зоне, несущей нанесенный штамм Е. coli (Е-са1);
- второе получение данных с тех же зон характеризации после калибровки прибора по малым массам с помощью pepMIX 6 в качестве калибранта; это второе получение осуществляли непосредственно сразу после первого, без нарушения вакуума камеры, и без извлечения пластинки из прибора.
- Данные собирали и сравнивали с данными, содержащимися в базе данных с целью идентификации вида.
- Пики просматривали в диапазоне малых масс для обнаружения нативной или гидролизованный формы антибиотика.
Все образцы анализировали на пластине в двух повторах.
На фигуре 3 изображены масс-спектры, полученные во второй серии получения данных, и показано, что, устойчивые к ампициллину штаммы были способны гидролизовать ампициллин в используемых экспериментальных условиях, в то время как никакой деградации ампициллина не наблюдалось в случае штамма E.coli, АТСС 25922, который, как известно, чувствителен к ампициллину. Фактически, после второго получения данных при малых массах, основной пик при 372,15 m/z, соответствующий нативной форме ампициллина, наблюдали для чувствительного штамма и отрицательного контроля, в то время как для всех ампициллин-устойчивых штаммов, основной пик был расположен при 368,15 m/z, что соответствует гидролизованной форме ампициллина и исчезновению нативной формы.
После первого получения данных и получения соответствующего спектра, все штаммы бактерий могут быть идентифицированы с высокой степенью достоверности.
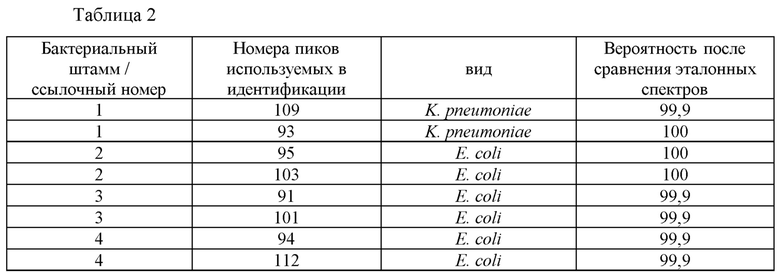
Как можно видеть в таблице 2 ниже, бактерии могут быть идентифицированы правильно с помощью MALDI-TOF из первой серии получения данных для всех зон характеризации с доверительным уровнем, который лежит в пределах 99,9%-100%, показывая, что условия эксперимента позволяют отличать различные виды.
Пример 3
Другие тесты были проведены для того, чтобы продемонстрировать, что определение вида и обнаружение продуцирования карбапенемазы было возможно осуществить с помощью одной и той же зоны характеризации. С этой целью использовали фаропенем в качестве модели антибиотика карбапена, и использовали протокол, идентичный протоколу в примере 2. Раствор фаропенема готовили в концентрации 0,5 мг/мл.
Используемые бактериальные штаммы подробно описаны ниже в таблице 3.

На фигуре 4 изображены масс-спектры, полученные в ходе второй серии получения данных, и показано, что активность карбапенемазы может быть обнаружена с помощью MALDI-TOF в этих условиях с помощью второй серии получения данных. Несмотря на то, что гидролизованные формы фаропенема не были обнаружены в этом эксперименте, можно было продемонстрировать потерю двух нативных форм фаропенема, из-за продуцирования бактериями карбапенемазы.
После получения данных в диапазоне малых масс, для чувствительного штамма основной пик наблюдался при 308,13 m/z с небольшим пиком при 330,13 m/z, что соответствует двум нативным формам фаропенема (соответствует рассчитанным массам 308,3 и 330,3 m/z). Эти два пика были потеряны, когда фаропенем инкубировали со штаммом S. marcescens, вырабатывающим карбапенемазу IMP-1.
После первого получения данных и спектров, оба штамма можно правильно идентифицировать с высокой степенью достоверности. Аналогичным образом, как в примере 2, наличие фаропенема в зонах характеризации не влияет на способность MALDI-TOF идентифицировать виды и возможность различать тип бактерий E.coli, от типа бактерий S. marcescens, как показано в результатах, полученных с помощью первой серии получения данных, представленных в таблице 4.
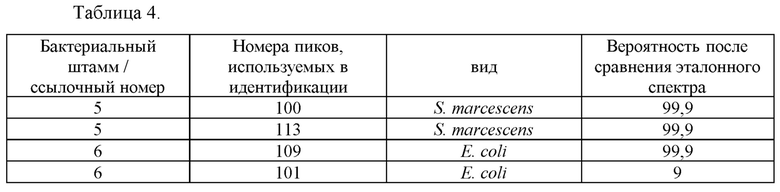
Пример 4
Этот тест был проведен с целью увеличения адгезии антибиотиков к аналитической зоне пластины MALDI. Фактически, сушка раствора антибиотика, нанесенного на пластину, приводила к образованию пленки, которая слабо сцеплена с поверхностью. Гептакис (2,6-ди-О-метил)-β-циклодекстрин (гептакис, Sigma-Aldrich исх Н0513) использовали для присоединения фаропенема к поверхности пластины MALDI.
Помимо своих адгезионных свойств, выбор использования гептакис был вызван его молекулярной массой 1331,36 г на моль (г.моль-1), которая не мешает пикам массы для фаропенема или для его гидролизованных продуктов. В ходе этого эксперимента, соотношения двух масс [гептакис]/[фаропенем] были испытаны с целью оценки адгезии сухого фаропенема и влияния гептакис на детекцию нативных пиков и гидролизованных пиков фаропенема.
Используемые бактериальные штаммы подробно описаны ниже в таблице 5.

Тесты были реализованы путем выполнения представленных ниже стадий:
- 2 раствора, содержащих смесь гептакис и фаропенема, и 1 раствор фаропенема без гептакис готовили в буфере NaCl (0,45%), дополненном цинком (сульфат цинка, 0,76 мМ). Конечные концентрации гептакис и фаропенема в этих растворах были следующими:
- 0 мг/мл гептакис и 1 мг/мл фаропенема;
- 0,1 мг/мл гептакис и 1 мг/мл фаропенема (массовое соотношение 1:10);
- 0,2 мг/мл гептакис и 1 мг/мл фаропенема (массовое соотношение 1: 5);
- 2 мкл каждого раствора наносили на аналитические зоны пластины MALDI (аналогично примеру 1);
- пластины инкубировали при комнатной температуре, до тех пор, пока капли осаждаемого раствора не высыхали полностью;
- для оценки адгезии, каждую аналитическую зону, функционализированую с помощью фаропенема или с помощью гептакис/фаропенема, соскабливали с помощью инокуляционной петли для того, чтобы имитировать нанесение колонии, и фотографировали данный слайд;
- для того чтобы оценить влияние концентрации гептакис на обнаружение пиков фаропенема, часть колонии получали после выращивания в течение 24 ч на гелевой среде, наносили в четырех повторах на аналитические зоны, несущие фаропенем отдельно или смеси фаропенема и гептакис;
- пластину инкубировали при 37°С в течение 2 ч во влажной атмосфере;
- 1 мкл матрицы НССА добавляли к аналитическим зонам, которые также несут антибиотик или смесь гептакис/антибиотик и бактерии;
- анализ с помощью масс-спектрометрии MALDI-TOF проводили с помощью инструмента VITEK® MS, с целью получения спектров с малой массой;
- были замечены пики нативной формы при 308,3 m/z (фаропенем + Na) и гидролизованной формы фаропенема при 304,3 m/z (гидролизованный фаропенем + Н), и пик для НССА при 212,03 m/z;
- для всех тестовых условий интенсивности трех пиков были записаны и были рассчитаны соотношения 308/212 и 304/212. Пик для НССА при 212 m/z использовали в этом примере в качестве контрольного пика неизменной интенсивности.
Все образцы анализировали на пластине в четырех повторах.
На фигуре 5 показан внешний вид аналитических зон (пятен) до и после соскабливания с помощью инокуляционной петли. На снимке показана хорошая дисперсия, после соскабливания смеси гептакис/фаропенем по всей поверхности пятна для соотношений [гептакис]/[фаропенема] 1/10 и 1/5, с хорошей стабильностью после соскабливания. Антибиотик, который высушили без гептакис, не был очень стабильным на поверхности слайда и пленка полностью или частично открепилась в ходе соскабливания инокуляционной петлей.
На фигуре 6 показано изменение соотношения интенсивностей пиков нативного фаропенема и гидролизованного фаропенема по сравнению с контрольным пиком НССА в зависимости от соотношений [гептакис]/[фаропенема], используемых при сушке антибиотика на слайде. Значения представляют собой среднее для четырех пятен. Для соотношений 1/10 и 1/5, детекция была сравнима с состоянием без гептакис, с дополнительным преимуществом воспроизводимости в присутствии гептакис.Фактически, существенная изменчивость, наблюдаемая в отсутствии гептакис (большая планка погрешности) была связана с полной или частичной потерей антибиотика на некоторых пятнах во время нанесения колонии. Что касается внешнего вида гидролизованного пика после инкубации с карбапенемаза КРС - продуцирующим штаммом, то мы наблюдали тот же феномен, т.е. хорошая детекция при соотношениях [гептакис]/[фаропенем] 1/10и 1/5.
Результаты этого эксперимента означают, что с помощью гептакис в подходящих концентрациях (0,1 мг/мл или 0,2 мг/мл для 1 мг/мл фаропенема) антибиотик может быть стабилизирован на слайде для хранения, обеспечивая при этом оптимизированное смешивание с бактериями в ходе нанесения колонии. При тех же концентрациях гептакис также может быть использован для улучшения воспроизводимости результатов между пятнами и не мешает обнаружению пиков или, фактически, реакции гидролиза фаропенема.
Пример 5
Этот тест был проведен для того, чтобы оценить возможность осуществления на функционализированной аналитической зоне пластины MALDI реакции гидролиза в жидком нанесении, т.е. в бактериальном инокуляте. На самом деле, проблемой, возникающей во время нанесения колонии, является отсутствие стандартизации в отношении количества нанесенных микроорганизмов, и изменчивость покрытия в зависимости от оператора. Таким образом, нанесение колонии на слайд для обычного применения при идентификации с помощью MALDI-TOF требует технической подготовки, и даже это не полностью устраняет риск изменчивости результатов из-за гетерогенных покрытий. Кроме того, бактериальный инокулят с известной концентрацией наносили на функционализованные аналитические зоны пластины MALDI.
Использованные бактериальные штаммы представлены в таблице 5 выше.
Испытания были реализованы путем выполнения представленных ниже стадий:
- 2 мкл раствора фаропенема при концентрации 1 мг/мл готовили в буфере NaCl (0,45%) с добавлением цинка (сульфат цинка, 0,76 мМ) наносили на аналитические зоны MALDI пластины и сушили при температуре окружающей среды;
- 2 мкл бактериальной инокулята в концентрации 3 единицы Мак Фарланда или 6 единиц Мак Фарланда применяли к функционализованным аналитическим зонам в четырех повторах;
- планшет инкубировали при 37°С в течение 2 ч во влажной атмосфере;
- к аналитическим зонам, несущим как антибиотик, так и бактерии, добавляли 1 мкл матрицы НССА;
- с помощью прибора VITEK® MS проводили два сбора данных масс-спектрометр ического анализа MALDI-TOF: один для спектров малых масс с целью наблюдения пиков фаропенема, а другой для спектров больших масс для идентификации (в соответствии с примером 2); и
- наблюдали пики для нативных форм при 308,3 m/z (фаропенем + Na) и при 330,3 m/z (фаропенем + 2Na), и пик для гидролизованной формы при 304,3 т/г(гидролизованный фаропенем+Н);
- для всех тестовых условий записывали интенсивности трех пиков и рассчитывали соотношения 304/308 и 304/330 для того, чтобы количественно оценить гидролиз фаропенема.
Все образцы анализировали на пластине в четырех повторах.
На фигуре 7 показана зависимость масс-спектров, полученных в ходе второй серии получения данных, и показано, что активность карбапенемазы может детектироваться с помощью MALDI-TOF после нанесения бактериального инокулята при силе 6 единиц Мак Фарленда. Фактически, можно было продемонстрировать потерю двух нативных форм и появление гидролизованного формы фаропенема из-за выработки бактериями карбапенемазы.
В полученных данных при малых массах у чувствительного штамма основной пик наблюдался при 308.03 m/z и наблюдался незначительный пик при 330.02 m/z, что соответствует двум нативным формам фаропенема (согласно рассчитанным массам 308,3 и 330,3 m/z). Эти два пика были потеряны при инкубации фаропенема со штаммом К. pneumoniae, продуцирующим карбапенемазу КРС, при этом наблюдалось появление пика при 304,06 m/z, который соответствует гидролизованной форме фаропенема (расчетная масса 304.03).
После первого получения данных и спектров, два штамма могут быть правильно идентифицированы с высокой степенью достоверности. Присутствие фаропенема в зонах характеризации и нанесение инокулята не влияет на способность идентификации видов с помощью MALDI-TOF, и не влияет на возможность различения бактерий типа Е. coli от бактерий типа К. pneumoniae, как можно видеть из результатов, полученных с помощью первой серии получения данных, представленной в таблице 6.

На фигуре 8 показано изменение отношения интенсивностей 304/308 и 304/330 в зависимости от концентрации инокулята, используемого для 2 тестируемых штаммов. Для штамма дикого типа, который не гидролизует антибиотик, не наблюдалось существенных различий 2 соотношений независимо от концентрации бактериального инокулята. Для штамма продуцирующего карбапенемазу типа КРС, значительное увеличение наблюдалось в обоих соотношениях, величина которых пропорциональна концентрации инокулята. Это увеличение соотношений привело к снижению интенсивности пиков нативных пиков и к увеличению интенсивности гидролизованного пика, как показано на фигуре 7.
Результаты этого эксперимента показывают, что нанесение инокулята также адаптировано к реакции гидролиза на пластине MALDI и к идентификации с помощью масс-спектрометрии MALDI-TOF. Кроме того, небольшие планки погрешности, наблюдаемые над средним для четырех нанесений, предполагают очень хорошую воспроизводимость результатов.
На фигуре 9 показано воплощение, включающее пластину MALDI, которая может быть адаптирована к нанесению популяции микроорганизмов в жидкой форме. Слайд пластины MALDI с аналитическими зонами, которые уже были покрыты высушенным антибиотиком помещали в галерею, внутри которой были сформированы множество лунок (12 в показанной модели). Шесть лунок, выровненных по одной оси, содержали контроль непрозрачности в обезвоженной форме, а остальные шесть лунок были пусты. Галерею, содержащую слайд, помещали в кассету с крышкой. Для хранения, эта кассета может, в частности, быть упакована в герметично запечатанном виде и защищена от света и влаги.
Протокол для применения этого продукта может быть описан в следующих стадиях:
- удалить крышку с кассеты;
- заполнить 12 лунок объемом 50 мкл - 100 мкл воды или физиологического буфера. Заполнение шести лунок, содержащих контроль непрозрачности, вызывало образование мутных растворов;
- подготовить инокулят в шести других лунках путем добавления колонии или части колонии для того, чтобы получить помутнение, сравнимое с контролем непрозрачности передней лунки;
- нанести 2 мкл каждого инокулята на аналитические зоны, несущие антибиотик;
- добавить воду к кассете при помощи пипетки для получения влажной атмосферы;
- заменить крышку и инкубировать при 37°С в течение 1 ч до 2 ч (или меньше);
- добавить 1 мкл матрицы НССА к аналитическим зонам, несущим как антибиотик, так и бактерии; и
- повторно заменить крышку слайда для анализа масс-спектрометрией MALDI-TOF.
Добавление контроля непрозрачности означает, что можно избежать приготовления инокулята с использованием устройства для измерения плотности или мутности, и возможно, таким образом, сэкономить время. Кроме того, измерительное устройство для рутинного применения, такое как денситометр, адаптировано для больших объемов (1-3 мл), что требует использования большого количества бактерий.
Инокулят также может быть получен с использованием твердого или жидкого экстракта бактерий, полученных непосредственно из биологического образца (например, из бактерий, извлеченных из гемокультуры).
Воплощение, представленное на фигуре 9, позволило протестировать шесть различных штаммов. Эта модель может быть адаптирована в зависимости от количества тестируемых штаммов, в частности, путем увеличения количества лунок.
Список литературы:
Hooff, G.P., J.J. van Kampen, R.J. Meesters, A. van Belkum, W.H. Goessens and T.M. Luider (2012). "Characterization of beta-lactamase enzyme activity in bacterial lysates using MALDI-mass spectrometry." J Proteome Res 11(1): 79-84.
Hrabak, J., V. Studentova, R. Walkova, H. Zemlickova, V. Jakubu, E. Chudackova, M. Gniadkowski, Y. Pfeifer, J.D. Perry, K. Wilkinson and T. Bergerova (2012). "Detection of NDM-1, VIM-1, КРС, OXA-48, and OXA-162 carbapenemases by matrix-assisted laser desorption ionization-time of flight mass spectrometry." J Clin Microbiol 50(7): 2441-2443.
Hrabak, J., R. Walkova, V. Studentova, E. Chudackova and T. Bergerova (2011). "Carbapenemase activity detection by matrix-assisted laser desorption ionization-time of flight mass spectrometry." J Clin Microbiol 49(9): 3222-3227.
Sparbier, K., S. Schubert, U. Weller, C. Boogen and M. Kostrzewa (2012). "Matrix-assisted laser desorption ionization-time of flight mass spectrometry-based functional assay for rapid detection of resistance against beta-lactam antibiotics." J Clin Microbiol 50(3): 927-937.
| название | год | авторы | номер документа |
|---|---|---|---|
| MALDI-TOF масс-спектрометрический способ определения устойчивости микроорганизмов к антибактериальным препаратам | 2020 |
|
RU2761096C2 |
| СПОСОБЫ РАЗДЕЛЕНИЯ, ХАРАКТЕРИСТИКИ И(ИЛИ) ИДЕНТИФИКАЦИИ МИКРООРГАНИЗМОВ С ПОМОЩЬЮ МАСС-СПЕКТРОМЕТРИИ | 2009 |
|
RU2519650C2 |
| СПОСОБ АНАЛИЗА ОТПЕЧАТКА С ИСПОЛЬЗОВАНИЕМ МАСС-СПЕКТРОМЕТРИИ | 2006 |
|
RU2417749C2 |
| Способ определения чувствительности неферментирующих бактерий к дезинфицирующим средствам с применением масс-спектрометрии | 2018 |
|
RU2709625C1 |
| Способ идентификации сероваров бактерий рода Leptospira методом MALDI-TOF масс-спектрометрии | 2017 |
|
RU2661108C1 |
| СПОСОБ АНАЛИЗА ПАНКРЕАТИТА И СОДЕРЖАЩИХ ЕГО КОМПОЗИЦИЙ | 2004 |
|
RU2359270C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ХАРАКТЕРИСТИК ПО МЕНЬШЕЙ МЕРЕ ОДНОГО МИКРООРГАНИЗМА С ПОМОЩЬЮ МАСС-СПЕКТРОМЕТРИИ | 2010 |
|
RU2604199C2 |
| Катионный пептид, проявляющий антибактериальные свойства | 2021 |
|
RU2778856C1 |
| СПОСОБ И СИСТЕМА ДЛЯ НЕРАЗРУШАЮЩЕГО IN OVO ОПРЕДЕЛЕНИЯ ПОЛА ПТИЦЫ | 2017 |
|
RU2756447C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 2011 |
|
RU2469315C1 |
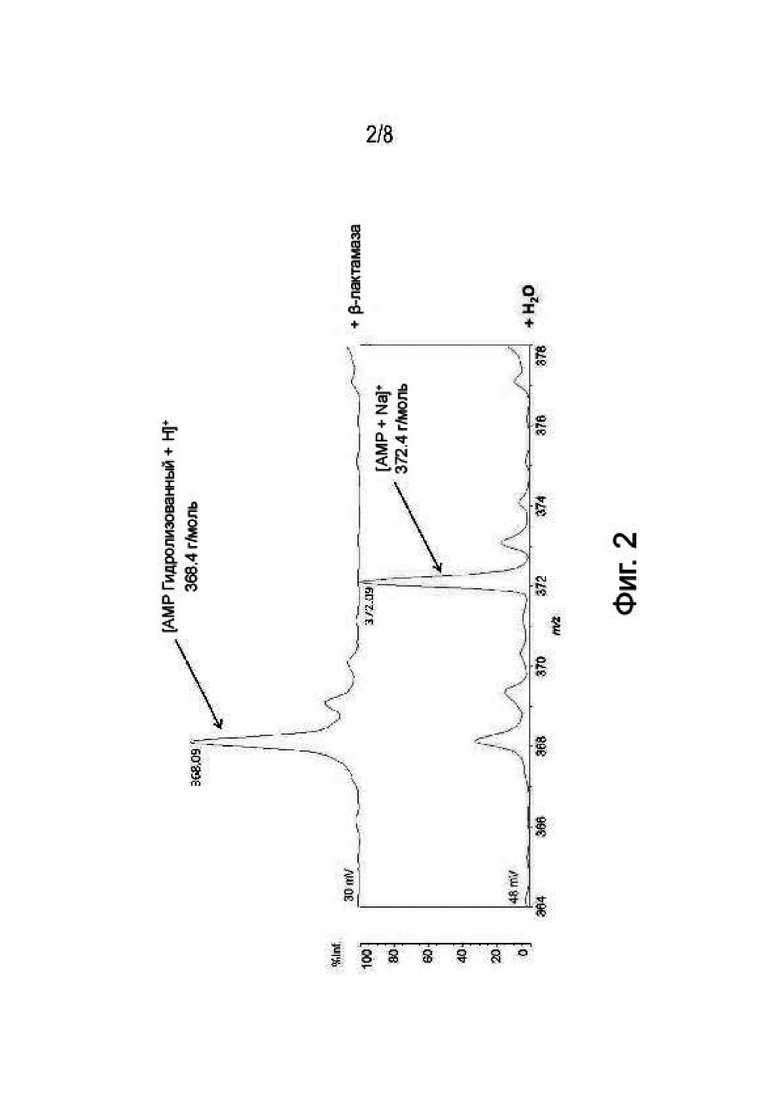
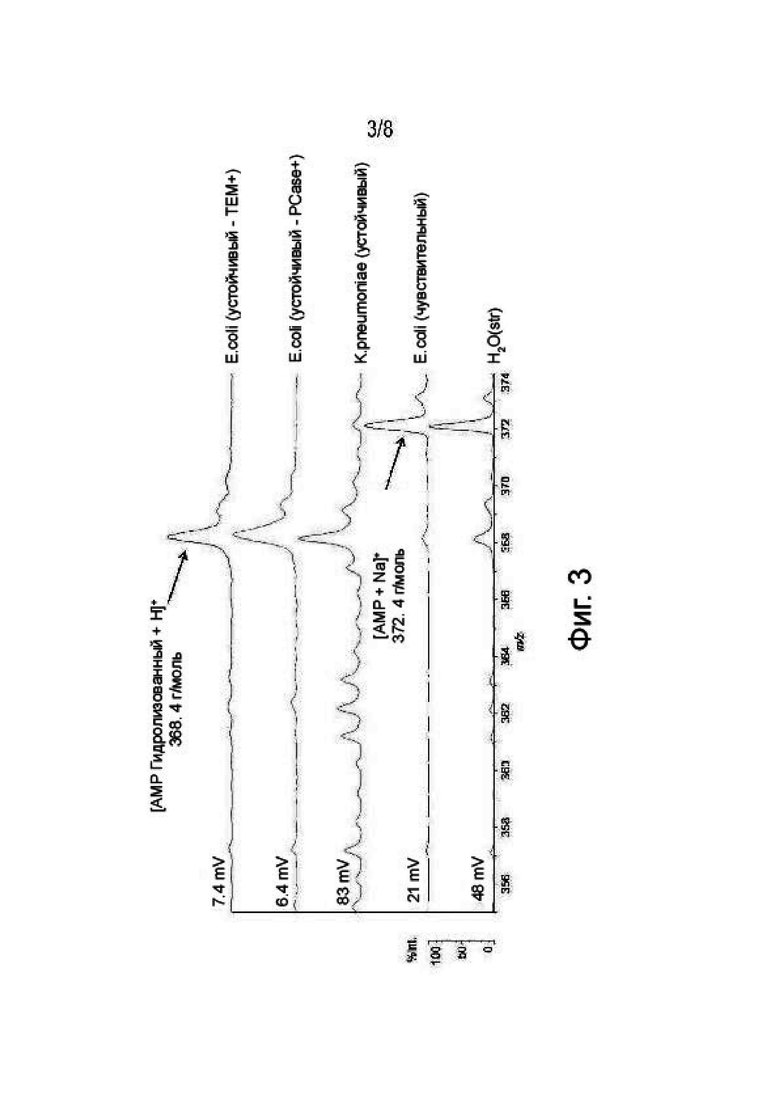

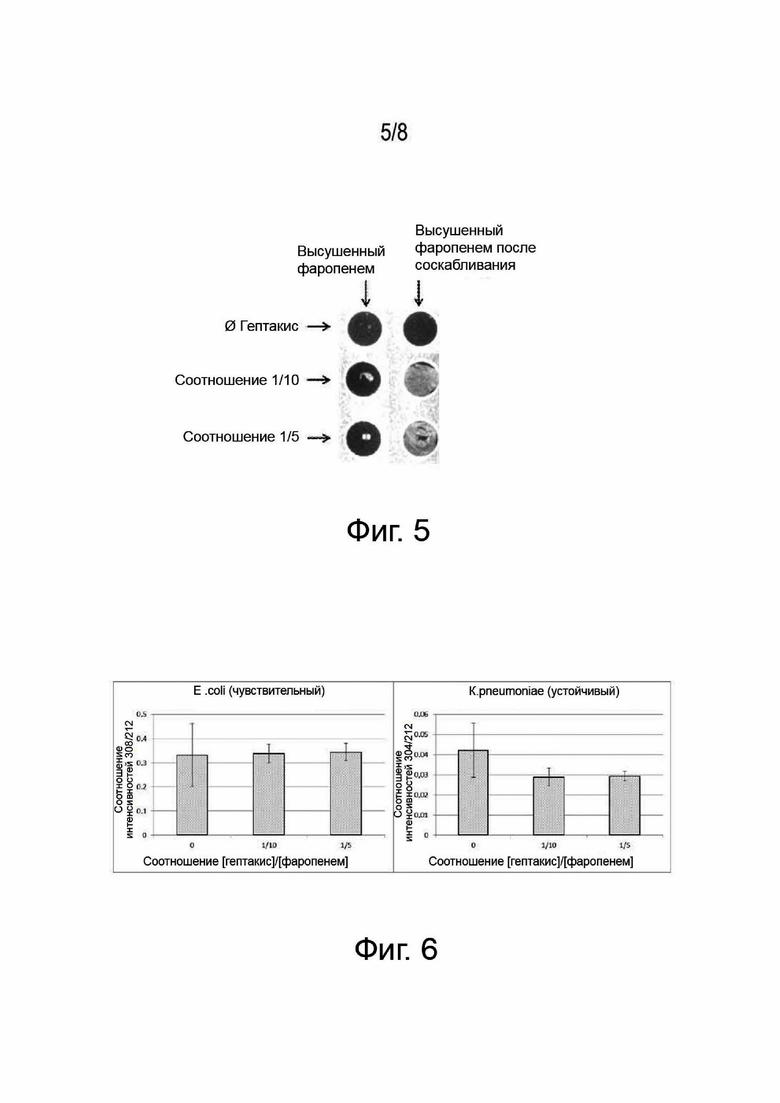
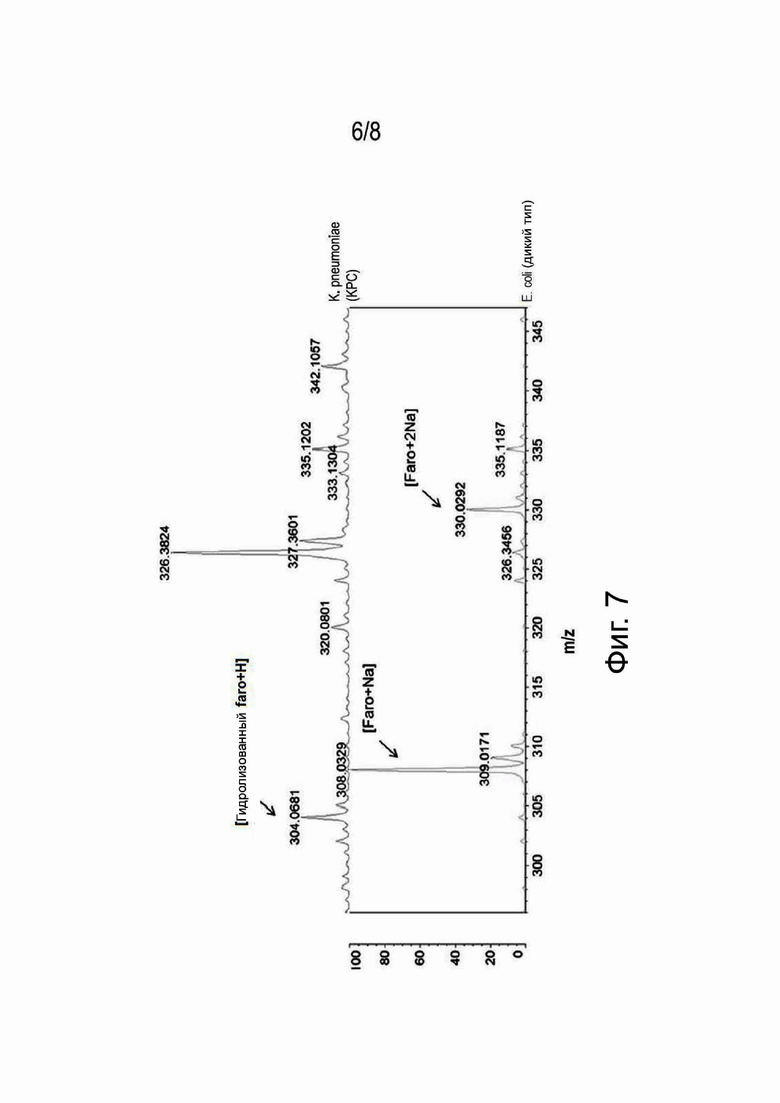
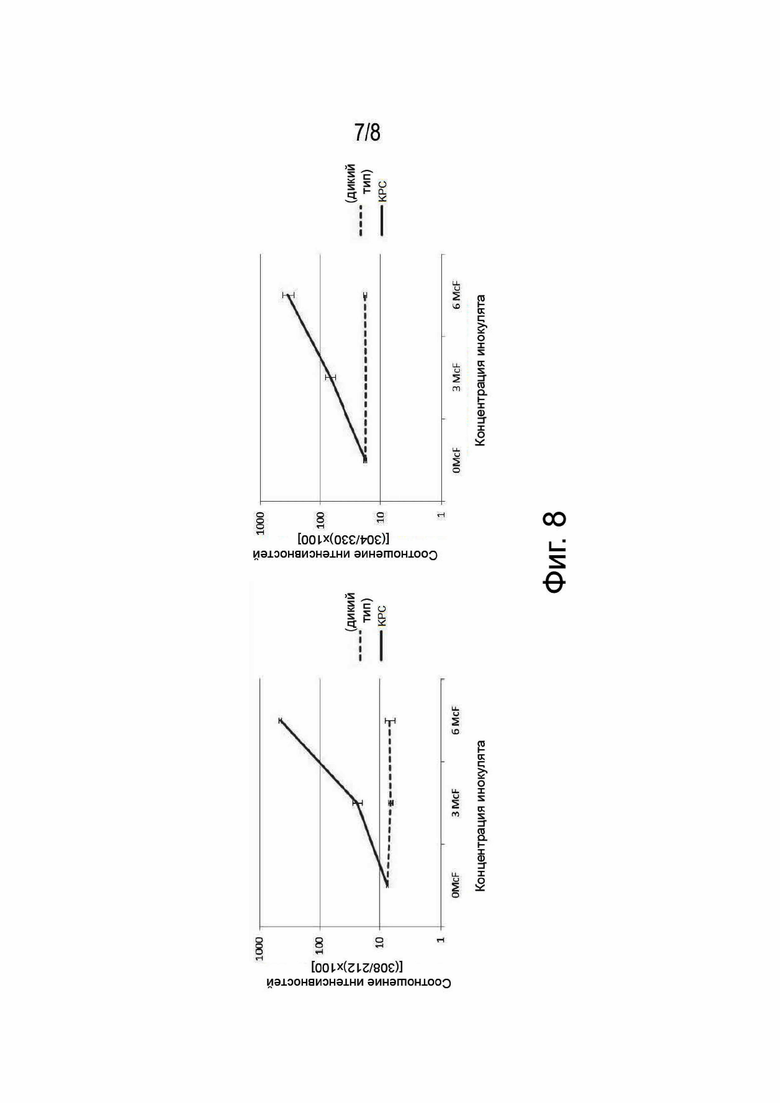
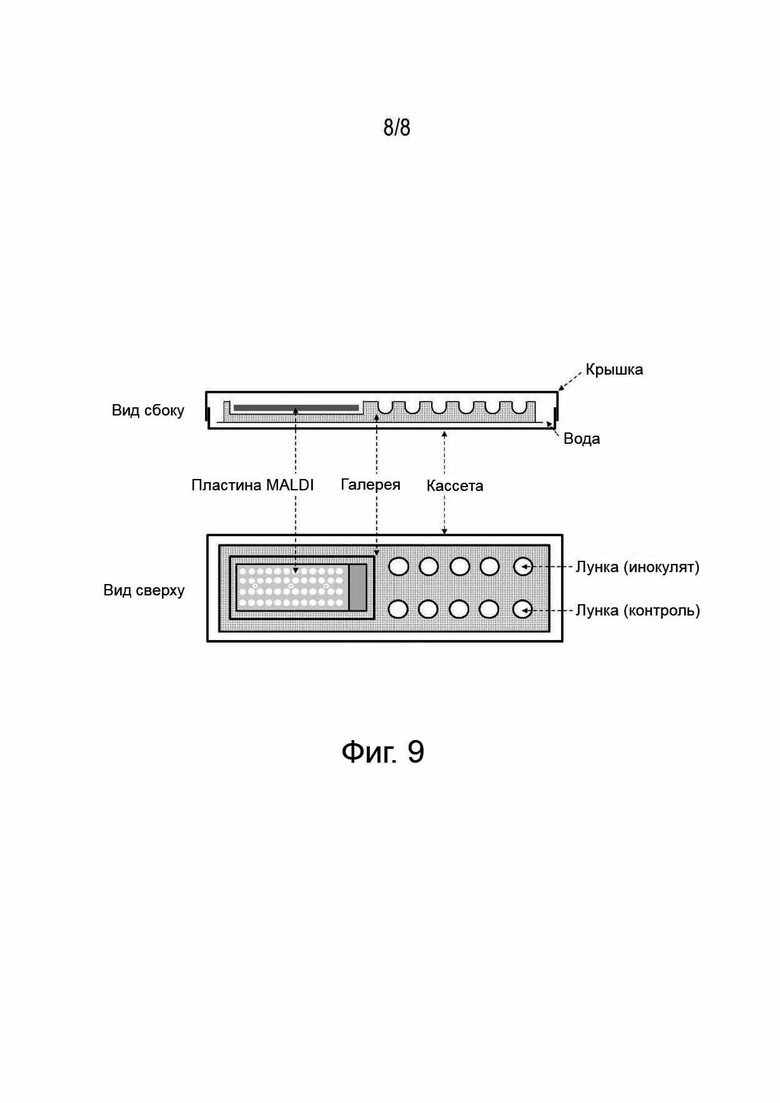
Группа изобретений относится к области биотехнологии. Предложен способ получения зоны характеризации аналитической пластины для проведения характеризации популяции микроорганизма в присутствии антимикробного агента методом MALDI, способ характеризации популяции микроорганизма (варианты), аналитическая пластина и средство для характеризации популяции микроорганизма, представляющее собой указанную пластину. Способ получения зоны характеризации включает предоставление аналитической пластины с содержащей антимикробный агент зоной, нанесение на нее популяции микроорганизма, инкубацию и нанесение на указанную зону пригодной для метода MALDI матрицы. Способ характеризации популяции микроорганизма в одном варианте включает подготовку зоны характеризации и верификацию присутствия антимикробного агента и/или продукта деградации антимикробного агента с помощью MALDI-TOF, а в другом варианте включает первый анализ зоны характеризации методом MALDI для идентификации семейства, рода или вида популяции микроорганизма и второй анализ зоны характеризации методом MALDI для определения присутствия популяции устойчивого к антимикробному агенту микроорганизма. Причём первый анализ и второй анализ осуществляют с помощью отдельных первой и второй стадий ионизации одной и той же зоны характеризации. Аналитическая пластина включает нанесенный в виде твердого слоя на аналитическую зону антимикробный агент. Изобретения обеспечивают простой в реализации способ получения зоны характеризации микроорганизма на аналитической пластине для идентификации его устойчивости к антибиотику и идентификации самого микроорганизма с помощью метода MALDI. 5 н. и 20 з.п. ф-лы, 6 табл., 5 пр., 9 ил.
1. Способ получения зоны характеризации аналитической пластины для проведения по меньшей мере одной характеризации популяции по меньшей мере одного микроорганизма в присутствии по меньшей мере одного антимикробного агента методом масс-спектрометрии с матрично-активированной лазерной десорбцией/ионизацией, известной как MALDI, который включает последовательно следующие стадии:
- стадию, заключающуюся в предоставлении аналитической пластины для характеризации с помощью метода MALDI, где пластина включает по меньшей мере одну функционализированную аналитическую зону, несущую антимикробный агент;
- стадию нанесения популяции по меньшей мере одного микроорганизма на указанную аналитическую зону с получением контакта с антимикробным агентом;
- стадию инкубации, состоящую в поддержании аналитической пластины в условиях и в течение времени, достаточного для того, чтобы позволить взаимодействовать присутствующим антимикробному агенту и микроорганизму; и
- стадию нанесения на аналитическую зону матрицы, которая пригодна для метода MALDI.
2. Способ получения по п. 1, отличающийся тем, что наносят популяцию одного характеризуемого микроорганизма.
3. Способ получения по п. 1 или 2, отличающийся тем, что нанесенную(ые) популяцию(ии) микроорганизма(ов) получают без предварительной стадии контакта с антимикробным агентом.
4. Способ получения по любому из пп. 1-3, отличающийся тем, что популяцию(ии) микроорганизма(ов) получают после стадии концентрирования, обогащения и/или очистки и/или популяция(ии) микроорганизма(ов) соответствует(ют) колонии или части колонии, полученной после роста на подходящей среде, в частности гелевой среде.
5. Способ получения по любому из пп. 1-4, отличающийся тем, что антимикробный агент выбран таким образом, чтобы позволить идентифицировать устойчивость микроорганизма из-за выработки бета-лактамазы, в частности карбапенемазы.
6. Способ получения по любому из пп. 1-5, отличающийся тем, что антимикробный агент представляет собой антибиотик, предпочтительно выбранный из пенициллинов, цефалоспоринов, цефамицинов, карбапенемов, монобактамов, в частности из числа ампициллина, амоксициллина, тикарциллина, пиперациллина, цефалотина, цефуроксима, цефокситина, цефиксима, цефотаксима, цефтазидима, цефтриаксона, цефподоксима, цефепима, азтреонама, эртапенема, имипенема, меропенема и фаропенема.
7. Способ получения по любому из пп. 1-6, отличающийся тем, что включает стадию функционализации для того, чтобы получить аналитическую пластину для характеризации с помощью метода MALDI, содержащей по меньшей мере одну аналитическую зону, несущую антимикробный агент, где указанную стадию функционализации предпочтительно проводят путем нанесения водного раствора антимикробного агента с последующей сушкой, чтобы сформировать функционализированную аналитическую зону.
8. Способ получения по любому одному из пп. 1-7, отличающийся тем, что функционализированная(ые) аналитическая(ие) зона(ы) несет(ут) один антимикробный агент.
9. Способ характеризации популяции по меньшей мере одного микроорганизма, где характеризация включает, по меньшей мере, определение присутствия или отсутствия популяции микроорганизма, который устойчив по меньшей мере к одному антимикробному агенту, отличающийся тем, что включает последовательно следующие стадии:
- подготовку по меньшей мере одной зоны характеризации аналитической пластины в соответствии со способом получения по любому из пп. 1-8;
- верификацию присутствия антимикробного агента и/или продукта деградации антимикробного агента с помощью времяпролетной масс-спектрометрии с матрично-активированной лазерной десорбцией/ионизацией, известной как MALDI-TOF, для того, чтобы иметь возможность сделать вывод, находится ли популяция микроорганизма, который устойчив к антимикробному агенту, в зоне характеризации.
10. Способ характеризации по п. 9, отличающийся тем, что характеризация дополнительно включает идентификацию семейства, рода или, что предпочтительнее, вида популяции микроорганизма, нанесенного на зону характеризации.
11. Способ характеризации по п. 9 или 10, отличающийся тем, что: идентифицируют семейство, род или, что предпочтительнее, вид популяции
микроорганизма, нанесенного на зону характеризации, путем проведения первого анализа масс-спектрометрией типа MALDI, соответствующего первой стадии ионизации зоны характеризации, и с использованием первой калибровки для анализа, и
определяют возможное присутствие в зоне характеризации популяции микроорганизма, который устойчив к антимикробному агенту, путем проведения второго анализа методом масс-спектрометрии с использованием метода MALDI-TOF, соответствующего второй стадии ионизации той же зоны характеризации, и с помощью второй калибровки для анализа, которая отличается от первой калибровки.
12. Способ характеризации по п. 10 или 11, отличающийся тем, что определение семейства, рода или, что предпочтительнее, вида популяции микроорганизма и определение того, возможно ли присутствие антимикробного агента, касается того же микроорганизма.
13. Способ характеризации популяции по меньшей мере одного микроорганизма, где характеризация включает по меньшей мере:
идентификацию семейства, рода или, что предпочтительнее, вида популяции микроорганизма путем проведения первого анализа методом масс-спектрометрии с использованием метода MALDI, соответствующего первой стадии ионизации зоны характеризации, включающей популяцию микроорганизма(ов), антимикробного агента и матрицы, подходящей для метода MALDI;
определение присутствия популяции микроорганизма, который устойчив по меньшей мере к одному антимикробному агенту, путем проведения второго анализа методом масс-спектрометрии с использованием метода MALDI, соответствующего второй стадии ионизации зоны характеризации, включающей популяцию по меньшей мере одного микроорганизма, антимикробный агент и матрицу, подходящую для метода MALDI,
отличающийся тем, что:
- первый анализ и второй анализ соответственно осуществляются с помощью отдельной первой стадии и отдельной второй стадии ионизации одной и той же зоны характеризации, включающей популяцию по меньшей мере одного микроорганизма и антимикробный агент;
- первый анализ использует первую калибровку, а второй анализ использует вторую калибровку, которая отличается от первой калибровки.
14. Способ характеризации по п. 13, отличающийся тем, что наносимая популяция включает один характеризуемый микроорганизм.
15. Способ характеризации по п. 13 или 14, отличающийся тем, что в нем используется способ получения зоны характеризации аналитической пластины по любому из пп. 1-8.
16. Аналитическая пластина для приема популяции по меньшей мере одного микроорганизма, подлежащего характеризации на аналитической зоне с помощью масс-спектрометрии с использованием метода MALDI, отличающаяся тем, что она включает антимикробный агент, который нанесен, в частности, в виде твердого слоя на указанную аналитическую зону аналитической пластины, образуя аналитическую зону, которая называется функционализированной.
17. Аналитическая пластина по п. 16, отличающаяся тем, что функционализированная аналитическая зона получена путем нанесения водного раствора антимикробного агента с последующей сушкой.
18. Аналитическая пластина по п. 16 или 17, отличающаяся тем, что антимикробный агент иммобилизован на аналитической зоне путем электростатического, ионного, ковалентного или аффинного связывания или, что предпочтительнее, с помощью адгезивного агента.
19. Аналитическая пластина по любому одному из пп. 16-18, отличающаяся тем, что пластина образована из полимера, который содержит электропроводный материал, покрытый слоем из нержавеющей стали.
20. Аналитическая пластина по любому из пп. 16-19, отличающаяся тем, что пластина содержит множество функционализованных аналитических зон, каждая из которых несет антимикробный агент.
21. Аналитическая пластина по любому из пп. 16-20, отличающаяся тем, что пластина содержит по меньшей мере первую функционализированную аналитическую зону, несущую первый антимикробный агент, и вторую функционализированную аналитическую зону, которая отличается от первой зоны, несущую второй антимикробный агент, который отличен от первого антимикробного агента.
22. Аналитическая пластина по любому из пп. 16-21, отличающаяся тем, что одна или каждая функционализированная аналитическая зона несет один антимикробый агент.
23. Аналитическая пластина по любому из пп. 16-22, отличающаяся тем, что она включает одну эталонную аналитическую зону, предназначенную для последующего приема популяции эталонного микроорганизма, и тем, что поверхность эталонной аналитической зоны свободна от антимикробного агента.
24. Аналитическая пластина по любому из пп. 16-23, отличающаяся тем, что она упакована в герметично закрытую упаковку.
25. Применение аналитической пластины по любому из пп. 16-24 в способе характеризации по любому из предыдущих пп. 9-15.
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
Авторы
Даты
2019-08-22—Публикация
2015-07-29—Подача