Изобретение относится к биотехнологии, в частности к генетической инженерии, и может быть использовано в ветеринарной практике для выявления генетического материала (ДНК) вируса герпеса крупного рогатого скота 4-го типа в пробах биоматериала от крупного рогатого скота для диагностики заболевания, а также для решения научно-исследовательских задач по изучению свойств возбудителя, изучения его роли в этиологии респираторных и гинекологических патологий телят и коров, по оценке эффективности диагностических, профилактических или лечебных препаратов против данного вируса.
Использование специфичных праймеров и зонда позволяет выявлять генетический материал вируса BHV-4 в исследуемых образцах методом полимеразной цепной реакции (ПЦР) с гибридизационно-флуоресцентной детекцией в режиме реального времени.
Вирус герпеса крупного рогатого скота 4-го типа (Bovine herpesvirus 4 (BHV-4)) относится к семейству Herpesviridae и имеет выраженные отличия от других герпесвирусов крупного рогатого скота. BHV-4 был выделен при разных клинических состояниях, а также у здоровых животных в разных странах и в основном связан с инфекциями репродуктивного тракта крупного рогатого скота, особенно в послеродовой период. Помимо крупного рогатого скота вирус был выявлен у других видов домашних и диких жвачных животных.
Изначально вирус делился на две группы, в соответствии с штаммами, выделенными от телят с респираторными заболеваниями в Венгрии в 1963 году и в США в 1971 году. Позднее был выявлен широкий спектр штаммов, которые показали вариабельность этого вируса и, следовательно, его сложность, как биологическом, так и эпидемиологическом отношении.
Изоляция вируса в культуре клеток является стандартным методом при диагностике болезней, вызванных BHV-4. Недостатком этого метода является длительность диагностики, обусловленная низкой скоростью размножения вируса в культуре до появления цитопатогенного эффекта, которая может продолжаться до 11 дней в зависимости от штамма вируса, культуры клеток и количества пассажей (Egyed L.,  A., Bartha A.,
A., Bartha A.,  S. Studies of in vivo distribution of bovine herpesvirus type 4 in the natural host. // J. Clin. Microbiol. - 1996. - 34. -P. 1091-1095.)
S. Studies of in vivo distribution of bovine herpesvirus type 4 in the natural host. // J. Clin. Microbiol. - 1996. - 34. -P. 1091-1095.)
Как альтернатива изоляции вируса в культуре клеток, в последнее десятилетие для выявления вируса BHV-4, применяется метод, основанный на полимеразной цепной реакции (ПЦР). Этот метод обладает рядом преимуществ, так как повышает точность выявления, сокращает сроки выявления, дает возможность обнаруживать и типировать возбудителя в исследуемом материале без выделения в культуре клеток. Кроме того, разные модификации ПЦР дают возможность проводить анализ в мультиплексном формате для определения всех групп вируса.
Известными аналогами являются ПЦР-тест-системы для детекции вируса: Boerner, В., Weigelt, W., Buhk, H-J., Castrucci, G., Ludwig, H.A sensitive and specific PCR/Southern blot assay for detection of bovine herpesvirus 4 in calves infected experimentally // J. Virol. Meth. - 1999 - 83, 169-180; Wellemberg G., Verstraten E.,  S., Verschuren S., Rijsewijk F., Peshev R., van Oirschot J. Detection of bovine herpesvirus 4 glycoprotein В and thymidine kinase DNA by PCR assays in bovine milk // J. Virol. Meth. - 2001. - 97. p. 101-112.; Herlekar D.A., Shashikant C.S., Gurjar A.A., Jayarao B.M. Presence of viral and bacterial organisms in milk and their association with somatic cell counts // J Dairy Sci. - 2013. - 96(10). - 6336-6346; Campos F.S., Franco A.C., Oliveira M.T., Firpo R., Strelczuk G., Fontoura F.E., Kulmann M.I., Maidana S., Romera S.A., Spilki F.R., Silva A.D.,
S., Verschuren S., Rijsewijk F., Peshev R., van Oirschot J. Detection of bovine herpesvirus 4 glycoprotein В and thymidine kinase DNA by PCR assays in bovine milk // J. Virol. Meth. - 2001. - 97. p. 101-112.; Herlekar D.A., Shashikant C.S., Gurjar A.A., Jayarao B.M. Presence of viral and bacterial organisms in milk and their association with somatic cell counts // J Dairy Sci. - 2013. - 96(10). - 6336-6346; Campos F.S., Franco A.C., Oliveira M.T., Firpo R., Strelczuk G., Fontoura F.E., Kulmann M.I., Maidana S., Romera S.A., Spilki F.R., Silva A.D.,  S.O., Roehe P.M. Detection of bovine herpesvirus 2 and bovine herpesvirus 4 DNA in trigeminal ganglia of naturally infected cattle by polymerase chain reaction. // Vet. Microbiol. - 2014. - 171(1-2). - p. 182-188. Однако они имеют электрофоретический режим регистрации результата.
S.O., Roehe P.M. Detection of bovine herpesvirus 2 and bovine herpesvirus 4 DNA in trigeminal ganglia of naturally infected cattle by polymerase chain reaction. // Vet. Microbiol. - 2014. - 171(1-2). - p. 182-188. Однако они имеют электрофоретический режим регистрации результата.
Наиболее близким аналогом (прототипом) является ПЦР-тест-система для выявления вируса BHV-4 по гену гликопротеина L в молоке (Herlekar D.A., Shashikant C.S., Gurjar А.А., Jayarao B.M. Presence of viral and bacterial organisms in milk and their association with somatic cell counts // J Dairy Sci. - 2013. - 96(10). - 6336-6346).
Однако вышеприведенные тест-системы (аналоги и прототип) имеют электрофоретический режим регистрации результата, что значительно увеличивает время проведения анализа, т.к. требуются дополнительные манипуляции, связанные с раститровкой ДНК исследуемой пробы или полученных в ходе ПЦР ампликонов, которые усложняют постановку анализа и могут приводить к появлению ложноположительных результатов. Стадия электрофореза ведет к резкому увеличению вероятности контаминации исследуемых проб продуктами амплификации.
Технической задачей изобретения являлась разработка набора специфичных олигонуклеотидных праймеров и зонда для идентификации генетического материала BHV-4 пробах биоматериала, сперме, молоке методом ПЦР с использованием гибридизационно-флуоресцентной детекции в режиме реального времени.
Поставленная задача решалась путем конструирования диагностических праймеров и флуоресцентно-меченого зонда на консервативном участке гена гликопротеина L (gL) генома вируса и оптимизации концентраций компонентов реакционной смеси и условий проведения ПЦР. Были рассчитаны пара праймеров и зонд для выявления генетического материала вируса. Для контроля амплификации были получены рекомбинантные плазмиды, несущие специфические участки ДНК-матрицы.
На начальном этапе был проведен анализ нуклеотидных последовательностей гликопротеина L разных штаммов вируса из базы данных NCBI (http://www.ncbi.nlm.nih.gov/) и определены наиболее консервативные участки.
Анализ свойств олигонуклеотидных праймеров и зондов проводился с использованием программы Vector NTI 9.0.0 (InforMax).
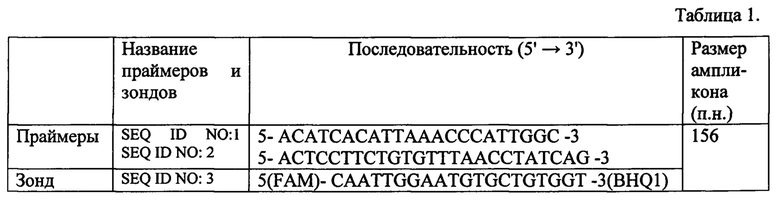
Для идентификации генетического материала вируса BHV-4 методом ПЦР в реальном времени были подобраны праймеры и зонд, представленные в таблице 1.
Пример 1. Проверка аналитической чувствительности набора праймеров и зонда.
Методом молекулярной трансформации компетентных бактериальных клеток Escherichia coli плазмидами pCR2.1, содержащими специфические ДНК вставки вируса BHV-4 для контроля амплификации были получены положительные контрольные образцы (ПКО).
Для проведения ПЦР в режиме реального времени в качестве анализируемых образцов использовали рекомбинантную плазмидную ДНК, включающую вставку ДНК, соответствующую детектируемому участку гена gL вируса BHV-4.
Для подтверждения специфичности полученного фрагмената ДНК определяли его нуклеотидную последовательность, для чего использовали набор реагентов BigDye® Terminator v3.1 Cycle Sequencing Kits (Applied Biosystems, США). Продукты секвенирующей реакции анализировали методом капиллярного электрофореза в автоматическом секвенаторе ABI PRISM® 3130×1 (Applied Biosystems/Hitachi, Япония). Полученную нуклеотидную последовательность сравнивали с последовательностями базы данных NCBI BLAST (http://www.ncbi.nlm.nih.gov/). Данный фрагмент ДНК, использованный для получения ПКО, являлся целевым и соответствовал участку гена gL вируса BHV-4.
Условия проведения амплификации оптимизировались по следующим параметрам: концентрация ионов магния в реакционной смеси; концентрация праймеров и зондов в реакционной смеси; температура отжига праймеров.
Оптимизированный состав реакционной смеси включал следующие компоненты: 10×Taq буфер без Mg2+ (ООО «Лаборатория Медиген», Россия) - конечная концентрация 1×; 100 mM раствор MgCl2 - конечная концентрация 3,3 mM; 5 mM раствор dNTP - конечная концентрация каждого 0,2 mM; смесь праймеров - конечная концентрация каждого 0,15 μМ; зонд - конечная концентрация 0,2 μМ; SmartTaq ДНК-полимераза - конечная концентрация 1,5 е.а; вода для ПЦР. Общий объем реакционной смеси составлял 30 мкл.
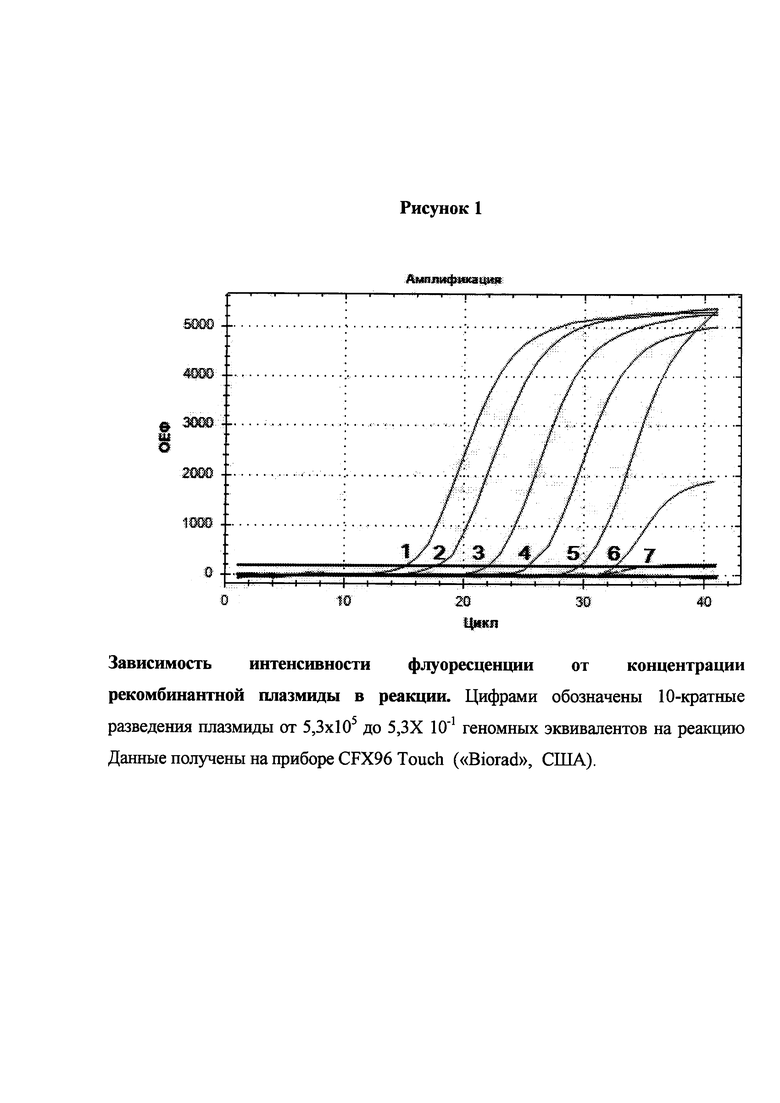
Аналитическую чувствительность метода определяли постановкой ПЦР «в реальном времени», где в качестве исследуемых образцов использовались 10-кратные разведения положительного контрольного образца с концентрацией 2,4 мкг/мл, что соответствует 5,3×1011 копий ДНК на 1 мл.
Результаты определения аналитической чувствительности приведены на рисунке 1.
За аналитическую чувствительность принимали последнее разведение ПКО, с которым результат ПЦР-анализа интерпретировался как положительный. Положительными считались образцы со значением Ct не превышающим 40.
По результатам исследований аналитическая чувствительность реакции составила 5,3×10 геномных эквивалентов на реакцию.
Пример 2. Определение специфичности ПЦР по заявленному способу.
Процедуру выделения ДНК из исследуемого материала проводили с использованием набора реагентов «Комплект для выделения ДНК/РНК из сыворотки или плазмы крови» (ООО «НПФ Литех», Россия) в соответствии с инструкцией по применению.
ПЦР в режиме реального времени проводили в реакционной смеси следующего состава (на 1 исследование):
ПЦР в режиме реального времени проводили в приборе Rotor Gene 6000 (Corbett Research, Австралия) по следующей программе (таблица 2).
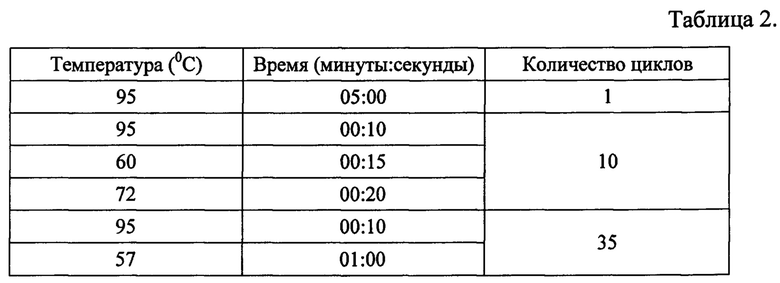
Измерение флуоресценции осуществляли при температуре 57°С.
Результаты опытов по определению специфичности реакции по заявленному способу представлены в таблице 3.
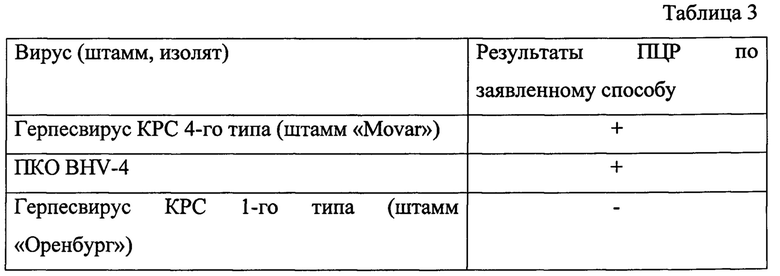

Таким образом заявленный способ обладает высокой специфичностью при выявлении ДНК вируса BHV-4.
Пример 3. Выявление ДНК вируса герпеса КРС 4-го типа в пробах биологического материала, полученного от больных и инфицированных животных.
Исследованию на вирус BHV-4 подвергают пробы лимфатических узлов, легких, трахеи от КРС с респираторными болезнями, внутренние органы аборт-плодов, амниотическую жидкость, плаценту, выделения из матки и влагалища при гинекологических болезнях, сперму быков-производителей и пробы молока при маститах.
Из органов и тканей вырезают кусочки размером 1×1×1 см, пробы молока, спермы и выделений берут в объеме не менее 1 мл.
Образцы молока, истечений, спермы используют для выделения ДНК без предварительной подготовки. Пробы органов и тканей перед исследованием растирают в отдельных фарфоровых ступках со стерильным песком пестиком, добавляют 5-10 мл стерильногофизиологического раствора и тщательно перемешивают. Смесь переносят в пластиковые пробирки емкостью 1,5 мл, центрифугируют при 10×103 об/мин в течение 5 минут. Для выделения ДНК используют 100 мкл осветленной надосадочной жидкости.
Дальнейшая процедура согласно примеру 2.
Всего предлагаемым способом было исследовано 18 образцов спермы быков-производителей, 46 проб молока, 112 проб внутренних органов КРС, 26 проб внутренних органов аборт-плодов и плаценты, 25 истечений из матки от абортировавших коров.
Результаты опытов по определению эффективности реакции при исследовании проб биоматериала от крупного рогатого скота по заявленному способу представлены в таблице 4.
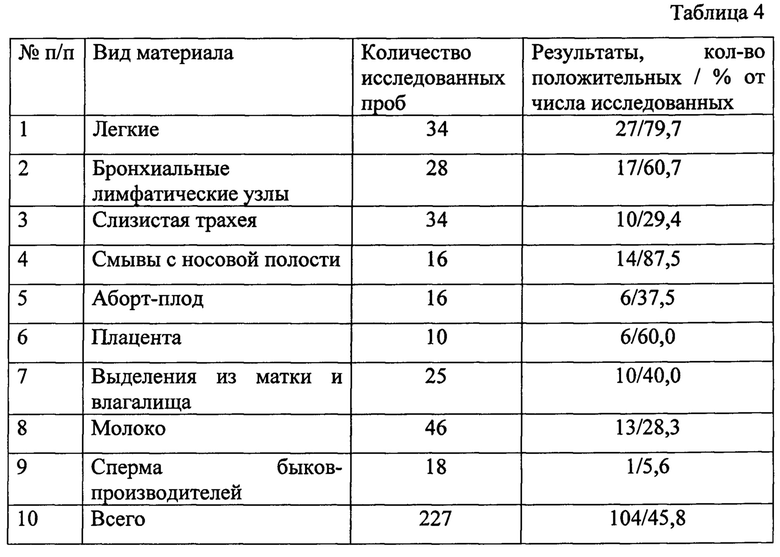
По заявленному способу количество положительных проб составило 45,8%.
Для подтверждения специфичности полученных фрагментов ДНК определяли их нуклеотидную последовательность как описано в примере 1. Результаты секвенирования показали, что все полученые ампликоны соответствуют исследованному участку гена гликопротеина L вируса BHV4.
Таким образом, предлагаемый способ обладает высокой чувствительностью (7,2×10 геномных эквивалентов на реакцию), специфичностью и эффективностью при выявлении ДНК вируса герпеса КРС 4-го типа атипичного в образцах биологического материала от крупного рогатого скота.

Изобретение относится к биотехнологии. Изобретение представляет собой набор олигонуклеотидных праймеров и зонда для выявления вируса герпеса крупного рогатого скота 4-го типа в пробах биоматериала от крупного рогатого скота, где праймеры имеют нуклеотидные последовательности SEQ ID NO: 1-5' acatcacattaaacccattggc 3', SEQ ID NO: 2-5' actccttctgtgtttaacctatcag 3', зонд имеет нуклеотидную последовательность SEQ ID NO: 3-5' caattggaatgtgctgtggt 3'. Изобретение позволяет идентифицировать генетический материал вируса герпеса крупного рогатого скота 4-го типа в пробах биоматериала от крупного рогатого скота 1 ил., 4 табл.
Набор олигонуклеотидных праймеров и зонда для выявления вируса герпеса крупного рогатого скота 4-го типа в пробах биоматериала от крупного рогатого скота, отличающиеся тем, что праймеры имеют нуклеотидные последовательности SEQ ID NO: 1-5' acatcacattaaacccattggc 3', SEQ ID NO: 2-5' actccttctgtgtttaacctatcag 3', зонд имеет нуклеотидную последовательность SEQ ID NO: 3-5' caattggaatgtgctgtggt 3'.
| Herlekar D.A., Shashikant C.S., Gurjar А.А., Jayarao B.M | |||
| Presence of viral and bacterial organisms in milk and their association with somatic cell counts, J Dairy Sci | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Способ изготовления искусственных пластических масс | 1925 |
|
SU6336A1 |
| СИНТЕТИЧЕСКИЕ ОЛИГОНУКЛЕОТИДЫ-ПРАЙМЕРЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ВЫЯВЛЕНИЯ ДНК ВИРУСА ИНФЕКЦИОННОГО РИНОТРАХЕИТА И ПУСТУЛЕЗНОГО ВУЛЬВОВАГИНИТА-ГЕРПЕСВИРУСА 1 ТИПА КРУПНОГО РОГАТОГО СКОТА | 2002 |
|
RU2241751C2 |
Авторы
Даты
2019-09-19—Публикация
2018-10-25—Подача