Изобретение относится к области медицинской биотехнологии и предназначено для получения моно- или поливалентных инактивированных (ИГВ) и живых (ЖГВ) гриппозных вакцин в целях иммунизации населения против потенциально пандемических вирусов гриппа А подтипа Н9. Полученный вакцинный штамм относится к семейству Orthomyxoviridae, род Influenza virus А.
Вирусы гриппа, циркулирующие среди животных, создают угрозу здоровью человека в случае непосредственного инфицирования и еще большую - при реассортации с вирусами человека, часто приводящей к возникновению особо патогенных вирусов с новыми антигенными свойствами.
Большинство вирусов диких птиц циркулируют и среди домашней птицы, вызывая у них заболевания разной степени тяжести, представляя угрозу для человека. Вирусы подтипа A/H9N2, как правило, являются вирусами с низкой патогенностью, вызывающие легкое и умеренное заболевание. Однако коинфекция с другими патогенами вызывает случаи тяжелых заболеваний и смертельные исходы [Dong G. et al., 2011]. Вирус A/H9N2 впервые был выделен из индейки в Висконсине в 1966 году [Gao Н. et al., 2015]. Начиная с 1990х вирус укоренился в странах Азии, Ближнего Востока и Северной Африки [Gu М., 2017]. На текущий момент вирус был детектирован у множества видов диких и домашних птиц во многих странах по всему миру и считается самым распространенным подтипом вируса гриппа среди домашней птицы [Li X. et al., 2018; Alexander D.J., 2007]. Вирусы подтипа A/H9N2 были обнаружены и у свиней, в организме которых может произойти реассортация с другими подтипами вирусов гриппа, что приведет к появлению потенциально пандемических вариантов вируса.
Также зарегистрированы случаи поражения людей вирусом подтипа A/H9N2 [Xu С. et al., 2018]. Генетический анализ вирусов подтипа A/H9N2, выделенных от домашней птицы, показал, что вирусы способны связываться и с α-2-6 сиалозидами, которые являются рецепторами человеческого типа, а также способны передаваться воздушно-капельным путем между хорьками, что является предпосылкой к передаче вируса от человека к человеку [Li X. et al., 2014]. Кроме того, недавние исследования показали, что вирусы A/H9N2 являются донором сегментов внутренних белков для таких высокопатогенных вирусов как A/H5N1, A/H7N9, A/H5N6 и A/H10N8 [Gu М., 2017; Wei Y., 2016]. Таким образом, распространение низкопатогенного вируса A/H9N2 у разных хозяев способствует появлению новых вариантов высокопатогенных вирусов. По всем этим факторам, а также из-за отсутствия иммунитета у популяции людей к вирусу данного подтипа, вирус A/H9N2 имеет пандемический потенциал [Longping V.Т. et al., 2014]
Необходимость разработки противопандемических мер, в том числе и для борьбы с вирусами птичьего гриппа, отражена в приказе Роспотребнадзора РФ [Приказ №40 от 28.12.2004]. В «Глобальном плане ВОЗ по подготовке к борьбе с гриппом» до начала пандемии национальным органам рекомендуется испытывать и лицензировать пандемические вакцины, а также поддерживать развитие производства и обмена прототипами сезонных и пандемических вакцин, для возможного целевого их применения. В связи с этим актуальными являются исследования по подготовке вакцинных препаратов против вирусов гриппа подтипов A/H9N2, а также испытания этих вакцинных препаратов на животных моделях.
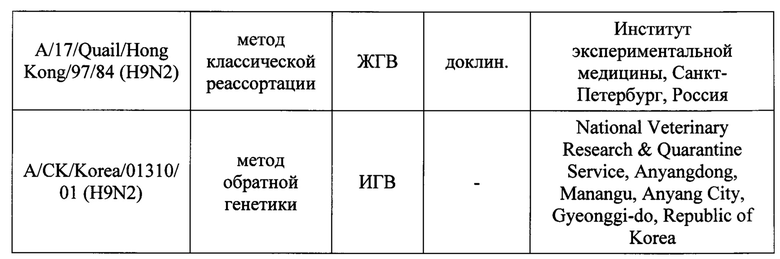
В настоящее время работы по созданию вакцин против пандемических вирусов гриппа подтипа A/H9N2 ведутся во всем мире, ряд вакцин находятся на различных стадиях доклинических [Desheva Y.A., 2015] и клинических испытаний [Karron R.A.,2009; Atmar R.L., 2011; Aichinger G., 2015; Nicholson K.G., 2009]. Это в основном инактивированные вакцины, полученные на основе штаммов, выделенных от человека. (Табл. 1)
В качестве донора генов внутренних белков для получения реассортанта на основе вируса A/H9N2 мы использовали разработанный в ФГБУ «НИИ гриппа» Минздрава России универсальный донор А/Гонконг/1/68/162/35 (H3N2) [Патент №2511431 от 25.07.2011], который ориентирован на получение реассортантных штаммов как для живой, так и для инактивированной гриппозных вакцин.
Задачей, на решение которой направлено заявляемое изобретение, было получение реассортанта на основе вируса гриппа A/H9N2 и донора генов внутренних белков A/Гонконг/1/68/162/35(H3N2) методом классической генетической реассортации, для производства инактивированных и живых гриппозных вакцин.
Получение штамма вируса гриппа RA-52 (A/HK/HK/6:2/2016 (H9N2))
Штамм вируса гриппа RA-52 (A/HK/HK/6:2/2016 (H9N2)) получен методом классической генетической реассортации штамма-донора А/Гонконг/1/68/162/35 (H3N2) и потенциально пандемического вируса A/Hong Kong/1073/99 (H9N2). При получении штамма было проведено 12 пассажей в 10-12 дневных развивающихся куриных эмбрионах. Селективными факторами для отбора необходимых клонов являлись пониженная температура (26°С) и присутствие гипериммунной сыворотки к штамму А/Гонконг/1/68/162/35 (H3N2).
Штамм представляет собой реассортант с формулой генома 6:2. Состав генома: 6 генов внутренних и неструктурных белков (РВ2, РВ1, PA, NP, М и NS) от вируса-донора А/Гонконг/1/68/162/35 (H3N2) и 2 гена (НА и NA) от вируса дикого типа.
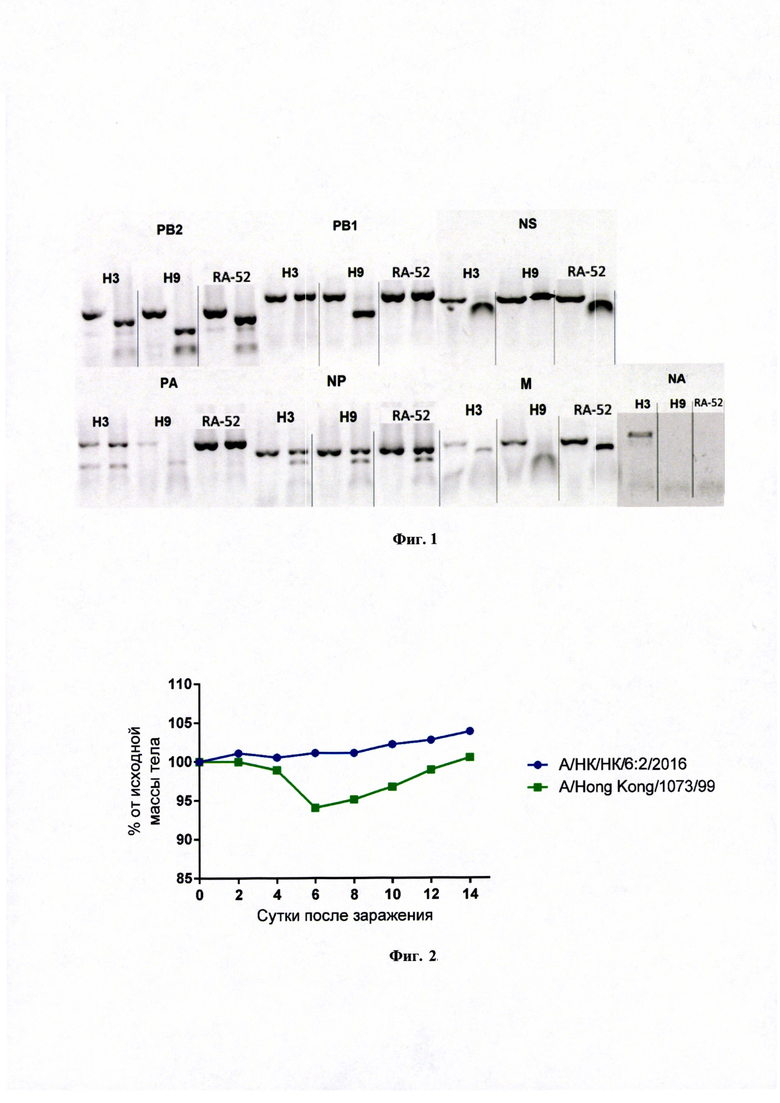
Подтверждение состава генома было выполнено с использованием рестрикционного анализа ДНК-копий сегментов РНК, полученных с помощью обратно-транскриптазной полимеразно-цепной реакции (ОТ-ПЦР). Полученные с помощью ОТ-ПЦР ДНК-копии сегментов РВ2, РВ1, PA, NP, М и NS вирусов А/Гонконг/1/68/162/35 и A/Hong Kong/1073/99 (H9N2) (обозначены на фиг. 1 как Н3 и Н9) обрабатывали эндонуклеазами рестрикции Bse3DI, MroNI, Ama87I, PstI, BslFI и BslFI соответственно. Принадлежность NA определяли методом ОТ-ПЦР с типоспецифичными праймерами к различным субтипам. Анализ ДНК-копий сегментов РНК (фиг. 1) показал, что реассортант RA-52 имеет состав генома 6:2.
Антигенное соответствие гемагглютинина родительскому штамму дикого типа у реассортанта RA-52 было подтверждено в реакции торможения гемагглютинации (РТГА) (табл. 2).
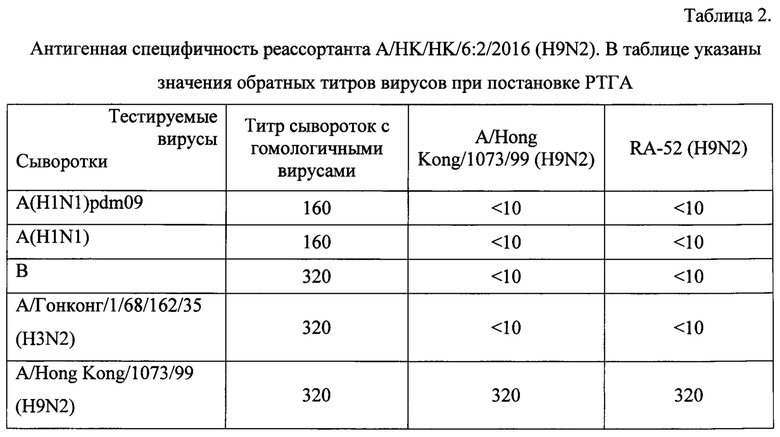
Показано, что вакцинный кандидат RA-52 антигенно идентичен родительскому штамму дикого типа.
Полногеномное секвенирование показало отсутствие у реассортанта RA-52 замен в нуклеотидной последовательности, по сравнению с родительскими штаммами. Нуклеотидные последовательности сегментов реассортанта RA-52 опубликованы в базе данных GISAID под номером EPI_ISL_321099.
Характеристика полученного штамма
Пример 1. Репродуктивные свойства штамма A/HK/HK/6:2/2016 (H9N2) (RA-52).
Штамм вируса гриппа RA-52 тестировали на инфекционную активность путем заражения развивающихся куриных эмбрионов 10-дневного возраста в соответствии с Методическими указаниями 3.3.2.1758-03 "Методы определения показателей качества иммунобиологических препаратов для профилактики и диагностики гриппа". Готовили десятикратные падающие разведения вируссодержащей аллантоисной жидкости. Каждым разведением начиная с 10-4 до 10-10 заражали по 3 куриных эмбриона. Инкубировали 48 часов при температуре 32°С. Наличие вируса определяли в РГА, инфекционную активность вируса рассчитывали по методу Рида и Менча.
Штамм вируса гриппа A/HK/HK/6:2/2016 (H9N2) показал высокую репродуктивную активность в РКЭ. Гемагглютинирующая активность реассортанта RA-52 составила 512-1024 ГАЕ/50 мкл с 0,5% взвесью куриных эритроцитов. Инфекционная активность в РКЭ составила - 8,5 lgЭИД50/0,2 мл.
Пример 2. Вакцинный штамм RA-52 обладает свойствами температурной чувствительности и холодоадаптированности.
Донор А/Гонконг/1/68/162/35 является универсальным, то есть обладает как высокой репродуктивностью, так и маркерами аттенуации - имеет температурочувствительный (ts) и холодоадаптированный (ca) фенотип. Реассортанты на основе донора А/Гонконг/1/68/162/35, также наследуют ts-, ca-фенотип.
Полученный реассортант наследовал от штамма-донора А/Гонконг/1/68/162/35 ts-, ca-фенотип - способность хорошо репродуцироваться при пониженной температуре и почти полную потерю способности к репродукции при повышенной температуре (табл. 3).
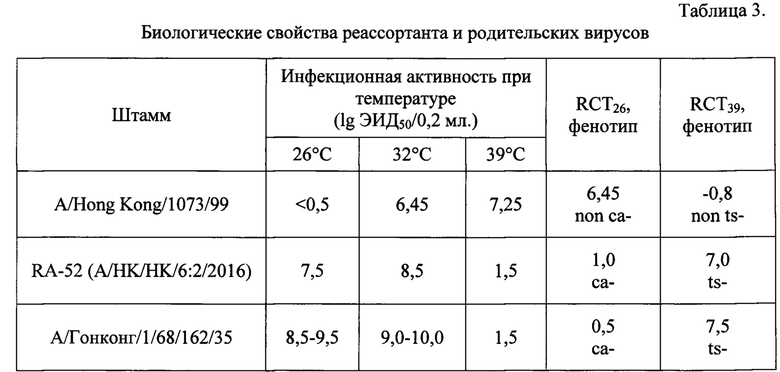
RCT (Reproductive capacity at different temperatures) - репродуктивная способность при различных температурах
ts - температурочувствительный фенотип (RCT39 более 5 lgЭИД50/0,2 мл)
ca - холодоадаптированный фенотип (RCT26 не более 3 lgЭИД50/0,2 мл)
Стабильность реассортанта проверяли 5-кратным пассированием при температуре 32°C в системе РКЭ. Степень температурочувствительности и холодоадаптированности, а также уровень репродукции реассортантного штамма не изменялись. Таким образом, реассортантный штамм удовлетворяет требованиям температурочувствительности и холодовой адаптации, предъявляемым к вакцинным штаммам для ЖГВ, и требованиям высокой репродуктивности для ИГВ.
Пример 3. Заявляемый вакцинный штамм RA-52 безопасен для мышей.
Тестирование штамма вируса гриппа RA-52 на специфическую безопасность проводили на линейных белых мышах Balb/c, самках, массой 18-20 г (16 шт.). В исследованиях использовали здоровых животных, на которых ранее не проводили какие-либо испытания. Испытания проводили в соответствии с методическими указаниями МУК 4.1/4.2.588-96.
Мышей инфицировали интраназально в дозе 6,5 lgЭИД50 на мышь, в объеме 50 мкл. В течение периода наблюдения (14 суток) у животных не наблюдалось потери массы тела (фиг. 2) и развития клинических симптомов инфекции. На 3-й и 6-е сутки после заражения у трех мышей проводили забор органов (легкие, носовые ходы) с целью индикации антигена и его накопления. Репродукцию вируса определяли по показателям титрования суспензии органов в культуре клеток MDCK. Результаты приведены в табл. 4.
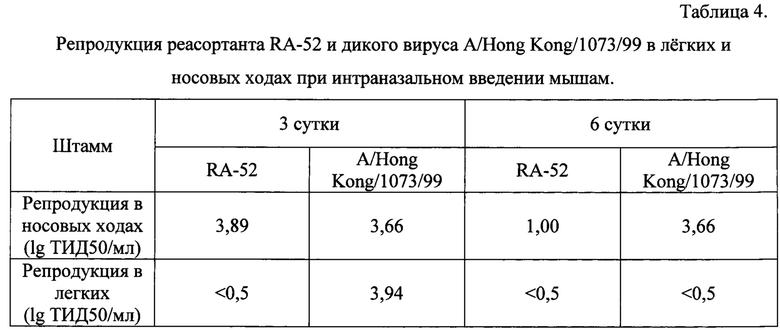
У мышей, инфицированных штаммом дикого типа, наблюдается репродукция вируса в носовых ходах как на 3-й, так и на 6-е сутки. В легких на 3-й сутки наблюдается высокий уровень репликации вируса. У мышей, инфицированных реассортантным штаммом, наблюдалось наличие вируса только в носовых ходах на 3-й и 6-е сутки, при этом уровень репликации вируса к 6-м суткам заметно снижался. В легких вирус не реплицируется, что подтверждает его аттенуированный фенотип. Полученные данные доказывают специфическую безопасность реассортантного штамма RA-52.
Пример 4. Вакцинный штамм RA-52 является иммуногенным для мышей.
На основе реассортантных штаммов были подготовлены кандидатные вакцинные препараты живой и инактивированной гриппозных вакцин (ЖГВ и ИГВ соответственно). Для получения ЖГВ накопленный вирусный материал реассортантного вируса разводили фосфатно-солевым буфером (ФСБ) до концентрации 6,5 lgЭИД50/50 мкл. ЖГВ вводили интраназально, в объеме 50 мкл. Для получения ИГВ вирусный материал инактивировали 0,02% формалином, затем очищали и концентрировали методом изопикнического центрифугирования в градиенте плотности сахарозы. Содержание гемагглютинина в вакцинном препарате оценивали методом электрофореза в полиакриламидном геле с последующей денситометрией. Доза ИГВ (250 мкл) содержала 10 мкг НА. В качестве адъюванта в одной из групп использовали полиоксидоний (ПО) - 200 мкг на дозу. ИГВ вводили внутримышечно (в верхнюю треть бедра задних конечностей).
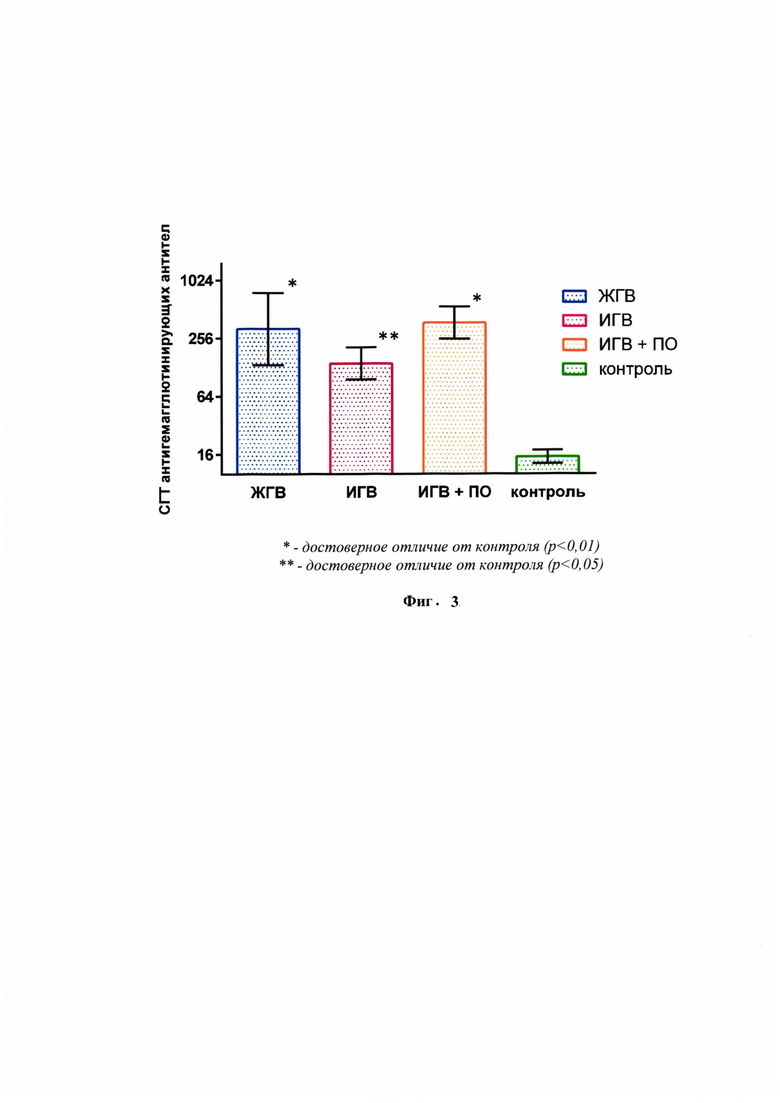
Препараты ЖГВ и ИГВ использовали для иммунизации мышей и исследования иммуногенности. Иммунизация была проведена двукратно с двухнедельным интервалом. Данные по содержанию антигемагглютинирующих антител к вирусам гриппа в сыворотках крови мышей, иммунизированных препаратами ЖГВ и ИГВ RA-52, демонстрируют достоверное (p<0,05) повышение уровня антигемагглютинирующих антител по сравнению с контрольными животными. Среднегеометрический титр (СГТ) антигемагглютинирующих антител в сыворотках после 2й иммунизации ЖГВ, ИГВ и ИГВ + ПО составил 320,139.3 и 367.6 соответственно (фиг. 3).
Полученные данные показывают, что после иммунизации мышей моновакцинами ЖГВ и ИГВ на основе реассортанта RA-52 формируются гемагглютинирующие антитела в титрах, превышающих защитные титры (защитный титр в РТГА ≥ 1:40). Таким образом, и живая и инактивированная моновакцины на основе полученного реассортанта RA-52, являются высоко иммуногенными.
Пример 5. Вакцинный штамм RA-52 обладает протективным действием для мышей.
Степень защиты, которую дают моновакцина ИГВ и ИГВ + ПО на основе реассортанта RA-52, в сравнении с контрольной группой, оценивали на самках мышей линии Balb/c на модели летального заражения. Мышей (по 5 в группе) через 2 недели после последней иммунизации заражали интраназально вирусом дикого типа A/Hong Kong/1073/99 (H9N2) в дозе 6,5 lgЭДИ50 на мышь. Далее на 3-й сутки после заражения у мышей проводили забор легких с целью индикации антигена и его накопления. Репродукцию вируса определяли по показателям титрования суспензии органов в культуре клеток MDCK. Результаты приведены в табл. 5.
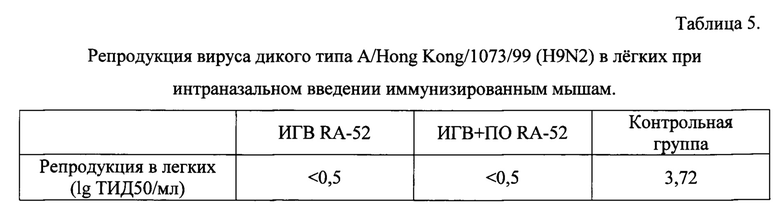
В легких мышей, иммунизированных ИГВ и ИГВ + ПО RA-52, вирус не реплицируется. В противоположность этому, в контрольной группе наблюдается высокий титр вируса в легких мышей. Эти данные свидетельствуют о том, что моновакцина ИГВ на основе реассортанта RA-52 обладает выраженным защитным действием против вируса гриппа A/Hong Kong/1073/99 (H9N2).
| название | год | авторы | номер документа |
|---|---|---|---|
| Штамм вируса гриппа A/UNL/HK/2:6/2017 (H5N8) для получения инактивированных и живых гриппозных вакцин | 2018 |
|
RU2702834C1 |
| Штамм вируса гриппа A/Shanghai/HK/6:2/2013 (H7N9) для получения инактивированных и живых гриппозных вакцин | 2017 |
|
RU2664460C1 |
| Штамм вируса гриппа А/Япония/ГК/6:2/2014 (H2N2) для получения инактивированных и живых гриппозных вакцин | 2017 |
|
RU2644670C1 |
| ШТАММ ВИРУСА ГРИППА А/Гонконг/1/68/162/35 (H3N2)-УНИВЕРСАЛЬНЫЙ ДОНОР ВНУТРЕННИХ ГЕНОВ ДЛЯ РЕАССОРТАНТОВ И РЕАССОРТАНТНЫЕ ШТАММЫ А/СПБ/ГК/09 (H1N1) И А/НК/Astana/6:2/2010 (H5N1), ПОЛУЧЕННЫЕ НА ЕГО ОСНОВЕ | 2011 |
|
RU2511431C2 |
| ШТАММ ВИРУСА ГРИППА ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ И ИНАКТИВИРОВАННОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2011 |
|
RU2464309C1 |
| Рекомбинантный штамм вируса гриппа A/PR8/HK-NS80E85A, экспрессирующий фрагменты антигенов ESAT-6 и Ag85A M.tuberculosis, для получения векторной вакцины против туберкулеза | 2018 |
|
RU2678175C1 |
| ШТАММ ВИРУСА ГРИППА А/17/MALLARD/НИДЕРЛАНДЫ/00/95(H7N3) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ И ПРОИЗВОДСТВА ИНАКТИВИРОВАННОЙ ГРИППОЗНЫХ ВАКЦИН | 2012 |
|
RU2507256C2 |
| ШТАММ ВИРУСА ГРИППА ГКВ 2389 ДЛЯ ПОЛУЧЕНИЯ ЖИВОЙ ИНТРАНАЗАЛЬНОЙ И ИНАКТИВИРОВАННОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2006 |
|
RU2318871C1 |
| РЕАССОРТАНТНЫЙ ШТАММ ВИРУСА ГРИППА RN9/13-HUMAN A(H6N9) ДЛЯ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К НЕЙРАМИНИДАЗЕ ПРИ ГРИППОЗНОЙ ИНФЕКЦИИ И ВАКЦИНАЦИИ | 2014 |
|
RU2587629C1 |
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА А(Н3N2)-А/8/Perth/16/2009 ДЛЯ ПРОИЗВОДСТВА ИНАКТИВИРОВАННОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2010 |
|
RU2458124C2 |
Изобретение относится к области биотехнологии. Изобретение представляет собой Influenzavirus А, подтип H9N2, штамм А/HK/HK/6:2/2016 (H9N2), депонированный в Государственную коллекцию вирусов ФГБУ «ФНИЦЭМ им. Н.Ф. Гамалеи» Минздрава России под №2884, для производства инактивированных и живых гриппозных вакцин против потенциально пандемического вируса гриппа A/H9N2. Изобретение позволяет усилить защитные действия вакцин против пандемического вируса гриппа А подтипа Н9. 3 ил., 5 табл., 5 пр.
Influenzavirus А, подтип H9N2, штамм А/HK/HK/6:2/2016 (H9N2), депонированный в Государственную коллекцию вирусов ФГБУ «ФНИЦЭМ им. Н.Ф. Гамалеи» Минздрава России под №2884, для производства инактивированных и живых гриппозных вакцин против потенциально пандемического вируса гриппа A/H9N2.
| ШТАММ ВИРУСА ГРИППА А/17/Ануи/2013/61 (H7N9) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ИНТРАНАЗАЛЬНОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2013 |
|
RU2563351C2 |
| ШТАММ ВИРУСА ГРИППА А/17/MALLARD/НИДЕРЛАНДЫ/00/95(H7N3) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ И ПРОИЗВОДСТВА ИНАКТИВИРОВАННОЙ ГРИППОЗНЫХ ВАКЦИН | 2012 |
|
RU2507256C2 |
Авторы
Даты
2019-10-11—Публикация
2018-12-21—Подача