Изобретение относится к области медицинской биотехнологии и касается создания рекомбинантного штамма, предназначенного для получения векторной вакцины против туберкулеза.
Из уровня техники известен рекомбинантный штамм вируса гриппа, экспрессирующий микобактериальный протективный антиген ESAT-6, предназначенные для профилактики и лечения туберкулеза (патент РФ №2318872, C12N 7/01, опубл. 10.03.2008 г.)
К его недостаткам можно отнести клеточную систему культивирования, которая уступает по урожайности системе развивающихся куриных эмбрионов (РКЭ), использующейся в настоящее время при производстве противогриппозных вакцин из живых холодоадаптированных вирусов гриппа. Кроме того, аттенуация (безопасность) штамма обеспечена единственным признаком - укорачиванием гена NS1, в отличие от полигенного признака аттенуации холодоадаптированных вирусов гриппа.
Также известен рекомбинантный штамм вируса гриппа ТВ-FLU ESAT6 2А AG85A, предназначенный для профилактики туберкулеза (Патент KZ А4 №28077, C12N 7/00, опубл. 15.01.2014 г.), который также обладает вышеперечисленными недостатками.
Задачей, на решение которой направлено заявляемое изобретение, являлось получение холодоадаптированного рекомбинантного вируса гриппа, экспрессирующего антигены ESAT-6 и Ag85A M.tuberculosis в составе укороченной рамки считывания NS1 и обладающего высокой репродуктивной активностью в системе РКЭ.
Новизной заявляемого рекомбинантного штамма является его холодоадаптированный фенотип, обеспечивающий дополнительную аттенуацию штамма, и способность штамма активно реплицироваться в системе РКЭ. Данные свойства рекомбинантного штамма были обеспечены за счет использования универсального донора внутренних генов А/Гонконг/1/68/162/35(H3N2) [Патент №2511431 от 25.07.2011], который ориентирован на получение штаммов, обладающих одновременно холодоадаптированным, температурочувствительным и высокорепродуктивным фенотипом.
Рекомбинантный штамм A/PR8/HK-NS80E85A относится к семейству Orthomyxoviridae, род Influenzavirus А, подтип H1N1. Штамм получен в апреле 2016 года методом обратной генетики, с помощью трансфекции клеток Vero набором из 8 плазмид на основе вектора pHW2000. Штамм прошел несколько пассажей в предельных разведениях в системе РКЭ, в результате которых был получен генетически стабильный вариант вируса.
Рекомбинантный штамм A/PR8/HK-NS80E85A является реассортантом с формулой генома 6:2. Состав генома: 2 гена (НА и NA) от вируса A/PR/8/34 (H1N1); 5 генов внутренних белков (РВ2, РВ1, PA, NP и М) от вируса А/Гонконг/1/68/162/35 (H3N2), 1 ген модифицированного неструктурного белка NS1 от вируса А/Гонконг/1/68/162/35(H3N2). Открытая рамка считывания NS1 укорочена до 80 аминокислот, после которых вставлена гетерологичная последовательность, кодирующая антиген ESAT6 (1-73) M.tuberculosis, отделенная глициновыми линкерами, после чего вставлен фрагмент антигена Ag85A (234-295) Рамка считывания NS1 терминирована кассетой из трех стоп-кодонов.
Рекомбинантный штамм A/PR8/HK-NS80E85A антигенно идентичен вирусу гриппа A/Puerto Rico/8/1934 (H1N1). Рекомбинантный штамм A/PR8/HK-NS80E85A (H1N1) является холодоадаптированным, аттенуированным и экспрессирует фрагменты антигенов ESAT-6 и Ag85A M.tuberculosis.
Рекомбинантный штамм A/PR8/HK-NS80E85A генетически стабилен и обладает высокой репродуктивной активностью в системе развивающихся куриных эмбрионов
Рекомбинантный штамм A/PR8/HK-NS80E85A стимулирует специфический противотуберкулезный CD4+ Т-клеточный ответ Th1 типа с образованием полифункциональных антиген-специфических Т-клеток при интраназальном введении мышам.
Рекомбинантный штамм A/PR8/HK-NS80E85A применим для получения интраназальной векторной вакцины против туберкулеза.
Рекомбинантный штамм A/PR8/HK-NS80E85A депонирован в Государственной коллекции вирусов Национального исследовательского центра эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи Министерства здравоохранения Российской Федерации под №2863.
Сущность изобретения поясняется чертежами, где
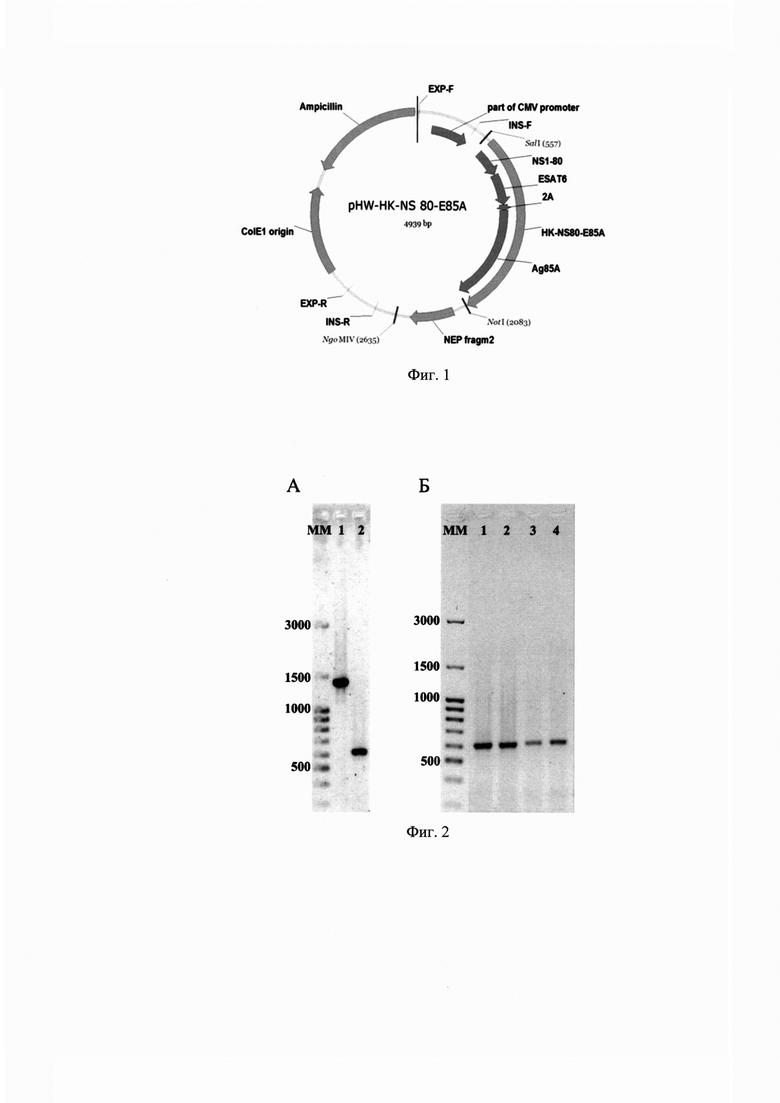
на Фиг. 1 представлена карта плазмиды pHW-HK-NS80-E85A, кодирующей модифицированный ген NS вируса А/Гонконг/1/68/162/35 (H3N2), в который после 80 аминокислотного остатка рамки NS1 были вставлены туберкулезные антигены Ag85A и ESAT-6;
на Фиг. 2 показана генетическая стабильность штамма A/PR8/HK-NS80-E85A. (А) ПЦР фрагменты гетерологичной вставки в гене NS в плазмиде pHW-HK-NS80-E85A (дорожка 1) и в гене NS штамма PR8/HK-NS80-E85A (дорожка 2). (Б) ПЦР фрагменты гетерологичной вставки в гене NS пассажных вариантов Е1-Е4 штамма PR8/HK-NS80-Е85А (дорожки 1-4, соответственно). ММ - маркер молекулярного веса, п.о.;
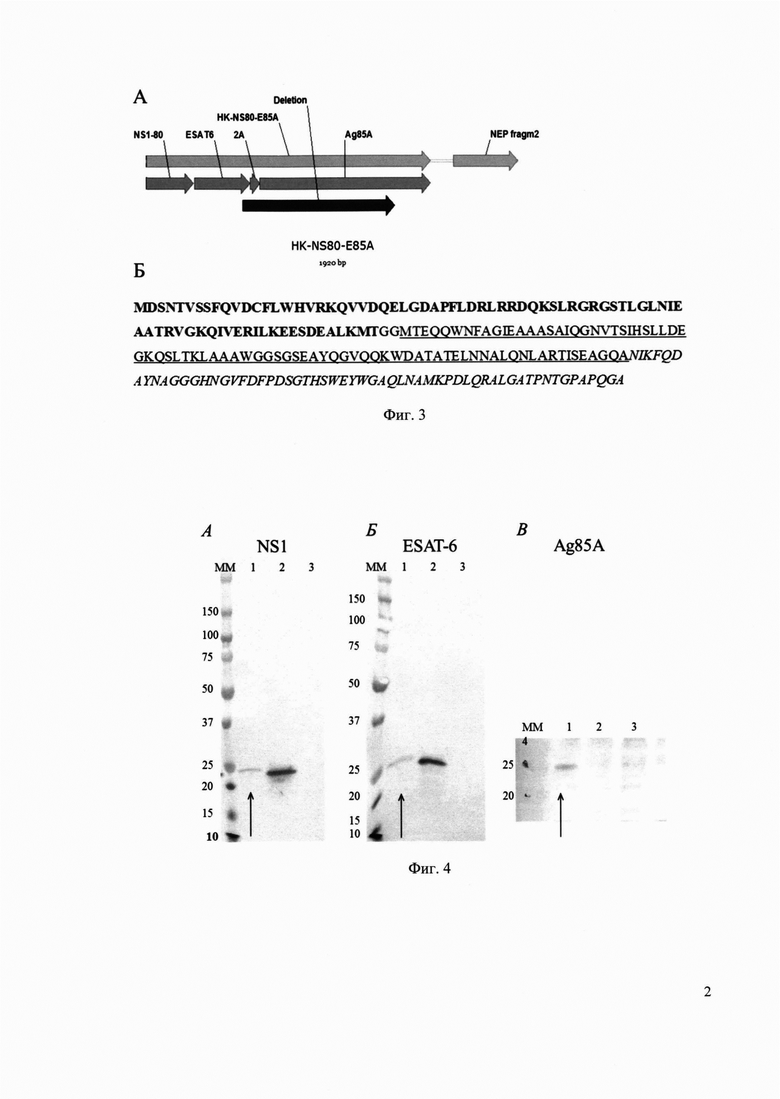
на Фиг. 3 приведен результат молекулярно-генетического анализа гена NS рекомбинантного вируса гриппа A/PR8/HK-NS80E85A. (А) Положение делении на карте гена NS в плазмиде pHW-HK-NS80-E85A. (Б) Последовательность химерного белка, кодируемого рамкой NS1 A/PR8/HK-NS80E85A. Фрагмент белка NS1 (а.к. 1-80) выделен жирным шрифтом, фрагмент антигена ESAT-6 (а.к. 1-73) подчеркнут, фрагмент антигена Ag85A выделен курсивом, не выделенные а.к. образуют линкер;
на Фиг. 4 показана экспрессия химерных белков при заражении клеток рекомбинантным вирусом A/PR8/HK-NS80-E85. Окрашивание на NS1 (A), ESAT6 (Б) и Ag85A (В). Номера дорожек и вес белков приведены в таблице 3;
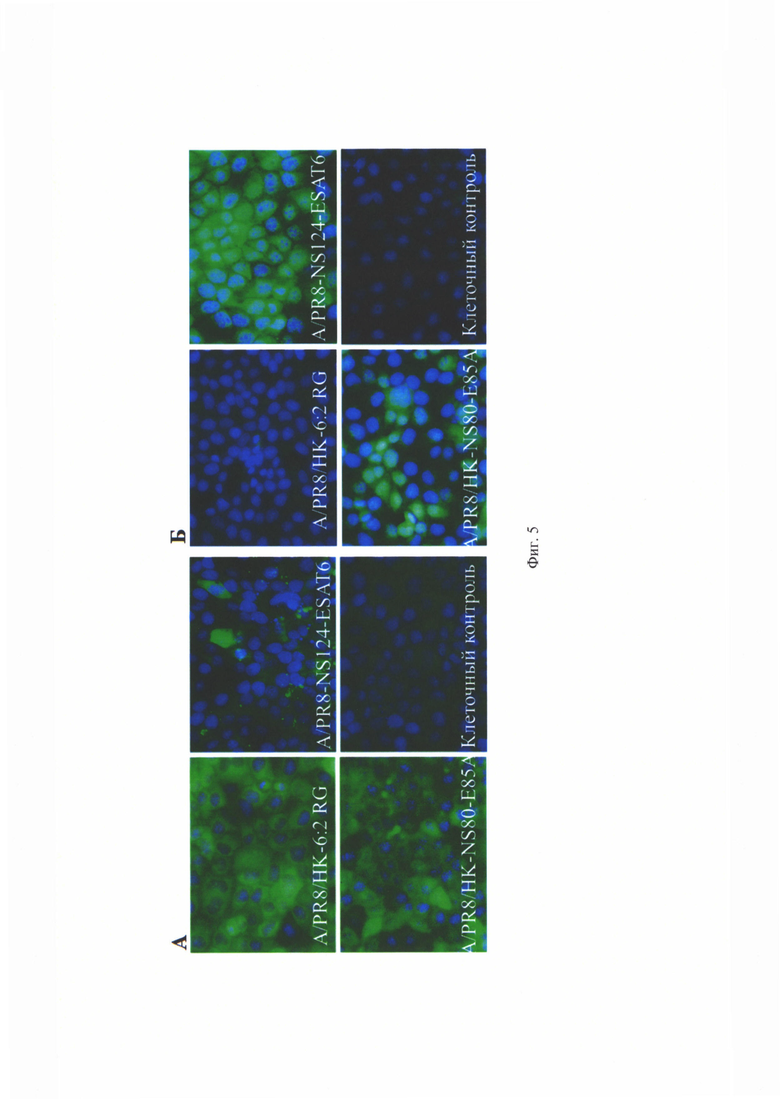
на Фиг. 5 показана экспрессия белка NS1(A) и антигена ESAT-6 (Б) при заражении клеток рекомбинантным вирусом A/PR8/HK-NS80-E85A;
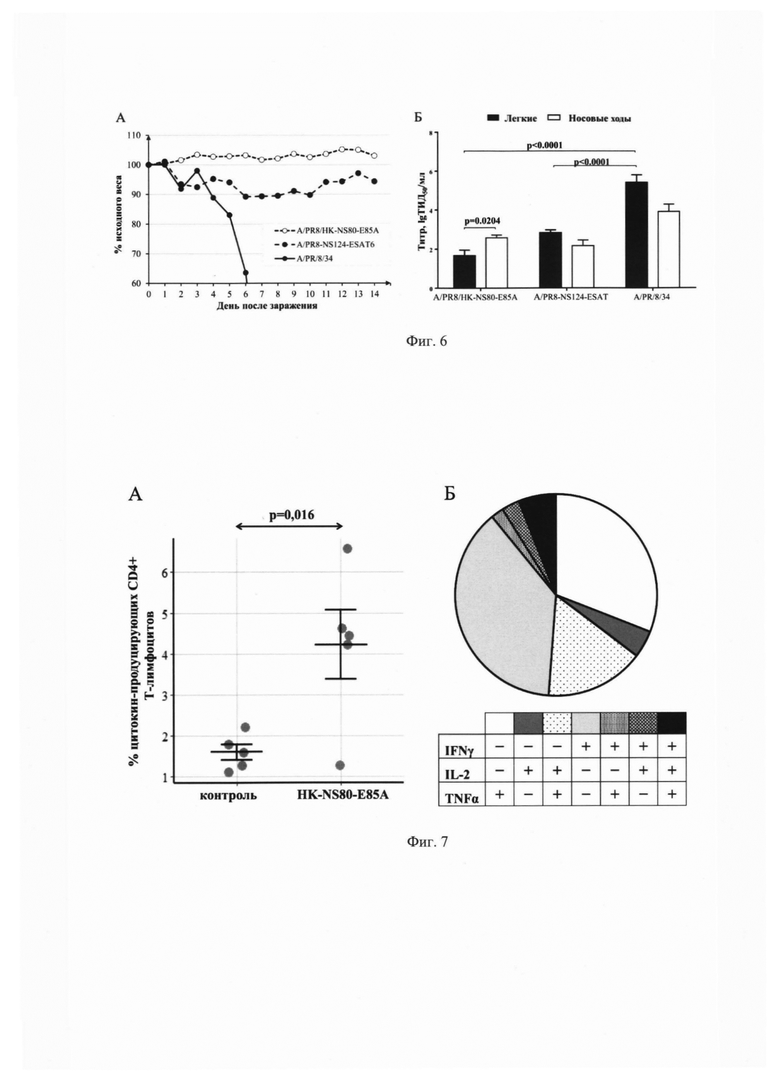
на Фиг. 6 проиллюстрирована безопасность штамма A/PR8/HK-NS80-E85A для мышей (А) График динамики веса мышей после заражения соответствующими вирусами. Потерю веса для каждого животного в % относительно исходного (день 0) определяли индивидуально, затем считали среднее по группе; (Б) Вирусная нагрузка в респираторном тракте мышей после заражения соответствующими вирусами. Значение р дано по результатам многофакторного дисперсионного анализа с последующими попарными сравнениями по методу Тьюкки с поправкой на множественность сравнений;
на Фиг. 7 проиллюстрировна индукция Т-клеточного ответа при иммунизации мышей рекомбинантным вирусом A/PR8/HK-NS80-E85A. (А) Относительное содержание цитокин-продуцирующих CD4+-Т-лимфоцитов (%) в спленоцитах мышей после и/н иммунизации рекомбинантным вирусом A/PR8/HK-NS80-E85A и контрольным вирусом без вставки A/PR8/HK-NS80 (контроль). Значение р критерия дано по результатам t-теста Стьюдента (Б) Доля антиген-специфических CD4+ Т-лимфоцитов, продуцирующих IFNγ, IL-2 и TNFα в различных сочетаниях после и/н иммунизации рекомбинантным вирусом A/PR8/HK-NS80-E85A.
Способ получения рекомбинантного вируса гриппа A/PR8/HK-NS80E85A
Рекомбинантный вирус гриппа A/PR8/HK-NS80E85A был получен из 8 плазмид методом обратной генетики в культуре клеток Vero и стабилизирован методом клонирования в предельных разведениях в развивающихся куриных эмбрионах (РКЭ). Использованные для трансфекции плазмиды кодировали гены НА и NA штамма A/PR/8/34 (H1N1), гены внутренних и неструктурных белков (РВ2, РВ1, PA, NP, М) вируса А/Гонконг/1/68/162/35 (H3N2), и модифицированный ген NS вируса А/Гонконг/1/68/162/35 (H3N2), в который после 80 аминокислотного остатка рамки NS1 были вставлены туберкулезные антигены Ag85A и ESAT-6 (Фиг. 1).
В результате серии последовательных пассажей в системе РКЭ материала трансфецированных клеток был получен вирус A/PR8/HK-NS80E85A, который характеризовался укороченной длиной гетерологичной вставки по сравнению со вставкой, закодированной в плазмиде pHW-HK-NS80-E85A, по результатам ОТ-ПЦР анализа. Для постановки ОТ-ПЦР анализа вирусную РНК выделяли с использованием набора RNEasy Mini Kit (Qiagen). Амплификацию фрагментов гена NS проводили методом ПЦР с обратной транскрипцией (ОТ-ПЦР) с использованием специально подобранных праймеров HK-NS1-226F (5'-ggattctgaaggaagaatccg) и PR8-NS1-523R (5'-tgacatcctcagcagtatgtcc) (Syntol, Россия) и набора реагентов Ambion AgPath-ID One Step RT-PCR (Thermo). Длину ПЦР-фрагментов определяли методом электрофореза в 1% агарозном геле при окрашивании бромистым этидием, документирование проводили с помощью системы ChemiDoc (Bio Rad). Результаты анализа длины вставки в гене NS вируса A/PR8/HK-NS80E85A и в гене NS, закодированном в плазмиде pHW-HK-NS80-Е85А, представлены на Фиг. 2А.
При последующих пассажах вируса A/PR8/HK-NS80E85A в системе РКЭ длина вставки не изменялась (Фиг. 2Б).
Последовательность модифицированного гена NS полученного рекомбинантного вируса гриппа A/PR8/HK-NS80E85A была определена методом секвенирования по Сенджеру. Секвенирование ПЦР-продуктов, полученных методом ОТ-ПЦР, проводили с помощью набора реагентов BigDye Terminator v3.1 Cycle Sequencing Kit (Applied Biosystems) на капиллярном секвенаторе ABI GA3130 (Applied Biosystems). Полученные последовательности анализировали с использованием программы Vector NTI (Invitrogen).
По результатам анализа было определено местоположение делеции в гене NS (Фиг. 3А). Было показано, что делеция не приводит к сдвигу рамки считывания NS1, и что гетерологичная вставка содержит участок 1-73 антигена ESAT-6 и участок 234-295 антигена Ag85A (Фиг. 3Б).
Ниже приведены примеры, подтверждающие заявленные свойства штамма A/PR8/HK-NS80E85A.
Характеристика полученного штамма
Пример 1. Репродуктивные свойства штамма A/PR8/HK-NS80E85A в системе РКЭ
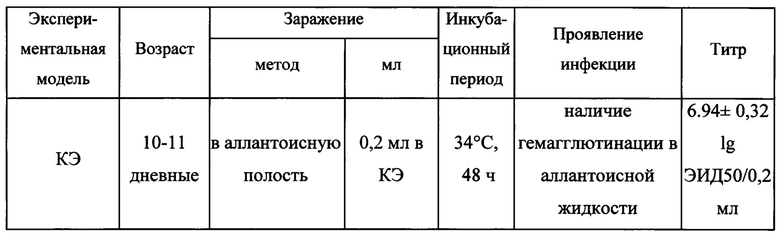
Штамм вируса гриппа A/PR8/HK-NS80E85A (H1N1) тестировали на инфекционную активность путем заражения РКЭ 10-дневного возраста. Готовили десятикратные падающие разведения вируссодержащей аллантоисной жидкости на фосфатно-солевом буфере с добавлением антибиотиков (100 ед/мл пенициллин, 100 мкг/мл стрептомицин, 5 мкг/мл амфотерицин В). Каждым разведением начиная с 10-8 до 10-2 заражали по 3 РКЭ вводя в аллантоисную полость 0,2 мл разведения. Эмбрионы инкубировали 48 часов при температуре 34°С. Наличие вируса в аллантоисной жидкости определяли в реакции гемагглютинации (РГА) с 0,5% суспензией куриных эритроцитов. Инфекционную активность вируса рассчитывали по методу Рида и Менча.
Репродуктивные свойства штамма представлены в таблице 1. Рекомбинантный вирус A/PR8/HK-NS80E85A показал высокую репродуктивную активность в РКЭ. Гемагглютинирующая активность рекомбинантного вируса A/PR8/HK-NS80E85A составляла от 1:16 до 1:64., инфекционная активность в РКЭ составила 6.94±0,32 lgЭИД50/0,2 мл.
Таблица 1 - Чувствительность к экспериментальной инфекции вируса гриппа A/PR8/HK-NS80E85A (H1N1)
Пример 2. Рекомбинантный вирус A/PR8/HK-NS80E85A является температурочувствительным и холодоадаптированным.
Температурочувствительный (ts-) и холодоадаптированный (са-)фенотипы являются маркерами аттенуации вирусов гриппа, используемых в качестве живых вакцин. Для определения фенотипа рекомбинантного вируса A/PR8/HK-NS80-E85A сравнивали показатели его инфекционной активности в РКЭ при различных температурах инкубации (табл. 2). Штамм A/PR8/HK-NS80-E85A обладает ts и са-фенотипом, так как разница в репродуктивной активности штамма при повышенной и оптимальной температурах (RCT39) составила более 5 lgЭИД50/мл, разница в репродукции при пониженной и оптимальной температурах RCT26 была менее 3 lgЭИД50/мл.
Таблица 2 - Инфекционная активность штамма PR8/HK-NS80-E85A при параллельном титровании в куриных эмбрионах при различных температурах

Пример 3. При заражении клеток MDCK рекомбинантным вирусом A/PR8/HK-NS80E85A происходит экспрессия туберкулезных антигенов ESAT-6 и Ag85A, сшитых с укороченным белком NS1
Экспрессия гетерологичных антигенов рекомбинантным векторным вакцинным штаммом обеспечивает презентацию антигенов иммунной системе и выработку иммунного ответа нужного типа. Экспрессию антигенов с модифицированной рамки считывания NS1 рекомбинантного вируса PR8/HK-NS80E85A оценивали в цитоплазме клеток MDCK через 6 часов после их заражения с помощью иммунофлуоресценции и Вестер-блот анализа.
Электрофорез и Вестерн-блот
Экспрессию модифицированного белка NS1 и антигенов ESAT-6 и Ag85A изучали через 6 часов после заражения клеток MDCK рекомбинантным штаммом A/PR8/HK-NS80-Е85А и контрольным вирусом A/PR8-NS124-ESAT6 (вирус со вставкой только антигена ESAT-6 из рабочей коллекции лаборатории векторных вакцин ФГБУ «НИИ гриппа»).
Культуру клеток MDCK (#FR-58, получены из коллекции IRR) растили в среде DMEM (Биолот) с 5% эмбриональной сывороткой Sus (Биолот) и 1% GlutaMAX (Gibco) при 37°С, 5% CO2. Суточный монослой клеток заражали вирусами в дозе 1-5 ТИД50/клетку и инкубировали при 34°С, 5% CO2 в течение 6 часов.
Для постановки Вестерн-блот клетки (≈1,2*106) снимали 0,25% трипсином-ЭДТА (Sigma) и ресуспендировали в 1X буфере Лэммли с β-меркаптоэтанолом (Bio-Rad). Затем проводили денатурирующий ЭФ образцов в 8-16% градиентном полиакриламидном геле, после чего белки переносили на нитроцеллулозную мембрану (Bio Rad). Мембрану блокировали 3% BSA (Amresco) в фосфатно-солевом буфере (PBS, Amresco), затем окрашивали антителами, разведенными в блокирующем буфере с добавлением 0,1% Tween-20 (Ferak Berlin). Использовали мышиные моноклональные антитела 1Н7 (ФГБУ «НИИ гриппа») против NS1 (1:5000), ab26246 (Abeam) против ESAT-6 (1:5000), и CSB-PA18279A0Rb (Cusabio) против Ag85A (1:500). В качестве вторичных антител были использованы меченые пероксидазой хрена Goat anti-mouse IgG(H+L) (G21040, Invitrogen) в разведении 1:2000 или Goat anti-rabbit IgG(H+L) (G21234, Invitrogen) в разведении 1:1000. Детекцию осуществляли с использованием Opti-4CN Substrate Kit (Bio Rad).
Результаты оценки экспрессии укороченного белка NS1 сшитого с участками антигенов ESAT-6 и Ag85A при заражении клеток MDCK вирусом A/PR8/HK-NS80-E85A иллюстрирует Фиг. 4. Результаты окрашивания окрашивания антителами против NS1 (А), ESAT-6 (Б) и Ag85 (В) лизатов клеток MDCK через 6 часов после заражения соответствующими вирусами. Дорожка 1 - клетки, зараженные вирусом A/PR8/HK-NS80-Е85А, дорожка 2 - клетки, зараженные вирусом A/PR8-NS124-ESAT6, дорожка 3 - незараженные клетки. ММ - маркер молекулярного веса, кДа. Стрелка отмечает лизат клеток, зараженных вирусом A/PR8/HK-NS80-E85A.
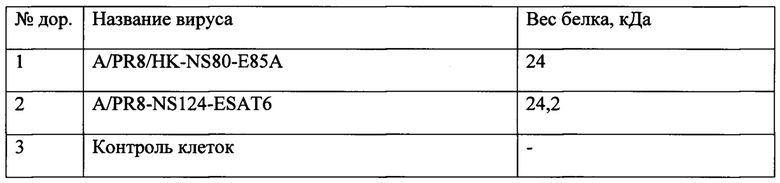
Приблизительная молекулярная масса антигенов NS1 и NS1 с гетерологичной вставкой по результатам теоретических расчетов с использованием сервера ExPASy ProtParam [51] приведена в таблице 3. По результатам Вестер-блот анализа видно, что собранный нами штамм экспрессирует туберкулезные антигены ESAT-6 и Ag85A, сшитые с гриппозным белком NS1. Молекулярный вес химерного белка схож с теоретически рассчитанным.
Таблица 3 - Приблизительная молекулярная масса химерных белков на основе NS1 и антигенов M.tuberculosis по результатам теоретических расчетов с использованием сервера ExPASy ProtParam
Иммунофлуоресценция
Экспрессию модифицированного белка NS1 и антигена ESAT-6 изучали через 6 часов после заражения клеток MDCK рекомбинантным штаммом A/PR8/HK-NS80-E85A и контрольными вирусами контрольными вирусами A/PR8/HK 6:2 RG (вирус без вставки) и A/PR8-NS124-ESAT6 (вирус со вставкой только антигена ESAT-6) из рабочей коллекции лаборатории векторных вакцин ФГБУ «НИИ гриппа»).
Для иммунофлуоресцентного окрашивания клетки фиксировали 4% параформальдегидом (Sigma) в PBS, пермеабилизировали 0,2% Triton Х-100 (Amresco) в PBS, блокировали 3% BSA в PBS. Антитела разводили в блокирующем буфере с добавлением 0,1% Tween-20. Окрашивание первичными антителами, проводили в течение ночи при +4°С, вторичными флуоресцентно-мечеными антителами в течение 1 ч при комнатной температуре. Окрашивание с помощью DAPI (4',6-diamidino-2-phenylindole, Serva) проводили, используя раствор 0,1 мкг/мл по 50 мкл на лунку. Использовали моноклональные мышиные антитела 1Н7 против NS1 (1:200) и поликлональные кроличьи антитела ab45073 (Abeam) против ESAT-6 (1:1000), в качестве вторичных антител использовали флуоресцентно меченые Goat Anti-Rabbit IgG H&L Alexa Fluor® 488 (ab150077, Abeam, 1:1000) и Goat Anti-Mouse pAb to MsIgG Alexa Fluor® 488 (ab150113, Abeam, 1:1000). Клетки фотографировали с использованием Cytell Cell Imaging System (GE Healthcare), с применением цифрового увеличения и увеличения объектива 10Х.
Результаты иммунофлуоресцентного анализа приведены на Фиг. 5. Показано, что клетки, зараженные вирусами, в отличие от незараженньгх клеток, экспрессируют вирусный белок NS1. Также показана экспрессия белка ESAT-6 при заражении вирусами A/PR8-NS124-ESAT6 и A/PR8/HK-NS80-E85A, о чем можно судить по свечению клеток, окрашенных на ESAT-6.
Пример 4. Рекомбинантный вирус A/PR8/HK-NS80E85A (H1N1) аттенуирован для лабораторных мышей
Тестирование рекомбинантного вируса гриппа A/PR8/HK-NS80E85A (H1N1) на безвредность для лабораторных животных проводили на линейных белых мышах BALB/c, самках, массой 18-20 г. В исследованиях использовали здоровых животных, на которых ранее не проводили какие-либо испытания. Вирус вводили интраназально в объеме 30 мкл по 5.0 lgЭИД50/мышь. Для определения безопасности полученного штамма проводили мониторинг массы тела животных в течение 14 дней после заражения (5 шт/группу) и оценивали вирусную нагрузку в респираторном тракте мышей на 3 день после заражения (3 шт/группу). В качестве контрольных вирусов использовали патогенный для мышей штамм A/PR/8/1934 (H1N1) и частично аттенуированный для мышей штамм A/PR8-NS124-ESAT6 (вирусы из коллекции лаборатории векторных вакцин ФГБУ «НИИ гриппа» Минздрава России).
В течение 14-дневного периода наблюдения после заражения все животные, зараженные вирусом A/PR8/HK-NS80E85A (H1N1) остались живы и ни у одного из них не были выявлены видимые признаки заболевания. Масса каждого животного в день окончания наблюдения не уменьшилась по сравнению с исходной. Таким образом, штамм A/PR8/HK-NS80-E85A был полностью аттенуирован, при этом мыши, зараженные патогенным штаммом A/PR/8/1934 (H1N1) в той же дозе, погибли к 8 суткам после заражения (Фиг. 6А).
Для определения вирусной нагрузки в респираторном тракте органы гомогенизировали в PBS с использованием Tissue Lyser (Qiagen, США). Вирусную нагрузку определяли по результатам титрования суспензии органов в культуре клеток MDCK в присутствии ТРСК-трипсина (2,5 мкг/мл) и амфотерицина В (2,5 мкг/мл). Зараженные клетки инкубировали при 34°С, 5% СО2 в течение 5 суток, результат оценивали в реакции гемагглютинации с 0,5% куриными эритроцитами, титр подсчитывали по методу Рида и Менча.
Титр неаттенуированного штамма A/PR/8/1934 (H1N1) в легких мышей составлял 5,42±0,38 lgТИД50/мл, что существенно превышало (р<0.001) вирусную нагрузку в легких мышей, зараженных частично аттенуированным вирусом A/PR8-NS124-ESAT6 (2,83±0,14 lgТИД50/мл) и полностью аттенуированным штаммом A/PR8/HK-NS80-E85A (1,67±0,29 lgТИД50/мл). При этом, штамм A/PR8/HK-NS80-E85A лучше размножался в носовых ходах мышей (2,58±0,14 lgТИД50/мл), чем в легких (р<0.05), что согласуется с его са-фенотипом (Фиг. 6Б).
Пример 5. Рекомбинантный вирус A/PR8/HK-NS80E85A стимулирует противотуберкулезный Т-клеточный ответ при иммунизации лабораторных мышей
Тестирование штамма вируса гриппа A/PR8/HK-NS80E85A (H1N1) на иммуногенность для лабораторных животных проводили на линейных черных мышах C57/black (5 мышей/группу). В исследованиях использовали здоровых животных, на которых ранее не проводили какие-либо испытания. Иммунизацию проводили интраназально по 5,0 lgЭИД50/мышь по 30 мкл/мышь вируса. Через 10 суток после иммунизации у мышей выделяли спленоциты. Гомогенизацию селезенки проводили при помощи пластиковых пестиков для ручной гомогенизации в микропробирках (Sarstedt, Германия). Гомогенаты органов фильтровали при помощи шприцевых фильтров 70 мкм в PBS с 2% FCS (Gibco, США). Отбирали 106 клеток в 100 мкл и стимулировали очищенным белком Ag85A (Novus Biologicals) в конечной концентрации 5 мкг/мл в присутствии костимулирующих антител к рецептору CD28 (Biolegend). После 12 часовой инкубации при 37°С, 5% CO2 в лунки добавляли брефельдин A (BD Biosciences). Для детекции живых клеток проводили окрашивание с помощью Zombie Red Fixable Viability kit (BioLegend). Для выделения популяции иммунных клеток использовали TruStain fcx CD 16/32 (BioLegend). Популяции лимфоцитов дифференцировали, используя антитела к поверхностным маркерам CD8-PE/Cy7, CD4-PerCp/Cy5.5 (BD Pharmingen), CD45-APC/Cy7 (BD Biosciences, США). Затем клетки фиксировали и пермеабелизировали с использованием набора реагентов Cytofix/Cytoperm Plus Fixation/Permebilization kit with BD Goldgi Stop (BD Biosciences), после чего окрашивали на внутриклеточные цитокины с использованием антител IFNγ-FITS, TNFα-Brilliant Violet 421, IL2-PE (BD Pharmingen). Результаты окрашивания детектировали на проточном цитометре BD FACSCanto II (BD Biosciences) и анализировали в программе Kaluza Analysis 1.05а.
Для оценки способности гриппозного вектора A/PR8/HK-NS80-E85A индуцировать противотуберкулезный Т-клеточный иммунный ответ была определена внутриклеточная продукция цитокинов CD4+ Т-клетками иммунизированных мышей. В качестве контрольной группы использовали мышей, иммунизированных «пустым» вектором A/PR8/HK-NS80 (вирус из рабочей коллекции лаборатории векторных вакцин ФГБУ «НИИ гриппа»).
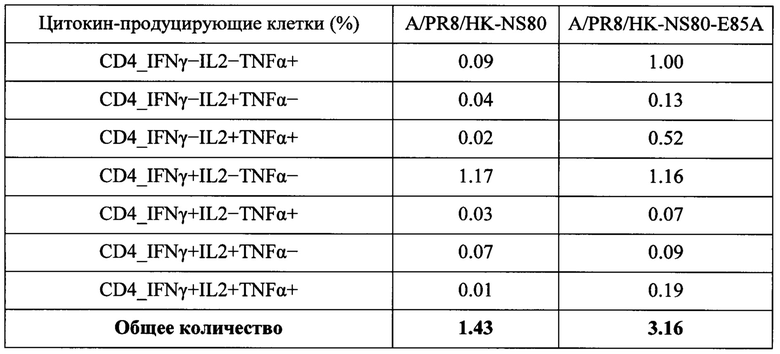
После однократной иммунизации рекомбинантным штаммом A/PR8/HK-NS80-Е85А доля цитокин-продуцирующих CD4+ Т-лимфоцитов в спленоцитах мышей при специфической стимуляции была достоверно выше, чем в контрольной группе животных (3.16±1.25 против 1.43±0.40; р=0.016, t-критерий Стьюдента, рис. 5А) (Фиг. 7А; табл. 4).
Далее была изучена функциональная активность CD4+ Т-клеток, способных под действием специфической стимуляции синтезировать IFN-γ, TNF-α и IL-2 или различные комбинации данных цитокинов. Среди популяции антиген-специфических CD4+ Т-клеток селезенки преобладали Т-клетки, секретирующие один цитокин (IFN-γ (36.85% от общего числа цитокин-продуцирующих CD4+-T-лимфоцитов), TNF-α (31.77%) или IL-2 (4.12%)). В то же время были обнаружены и полифункциональные антиген-специфические Т-клетки, продуцирующие два цитокина (IFN-γ и IL-2 (2.77%); IFN-γ и TNF-α (2.06%); TNF-α и IL-2 (16.32%)), а также минорная популяция тройных продуцентов, секретирующих IFN-γ, TNF-α и IL-2 (6.10%)) (Фиг. 7Б).
Таким образом, была продемонстрирована способность гриппозного вектора A/PR8/HK-NS80-E85A индуцировать специфический противотуберкулезный CD4+ Т-клеточный ответ у иммунизированных мышей линии C57/black при однократном интраназальном введении. Кроме того, обнаруженные полифункциональные Т-лимфоциты, благодаря более выраженной эффекторной функции по сравнению с Т-клетками, секретирующими только один цитокин, могут рассматриваться в качестве потенциального иммунологического маркера протективного иммунитета при туберкулезе.
Таблица 4 - Процентное содержание цитокин-продуцирующих CD4+-T-лимфоцитов
| название | год | авторы | номер документа |
|---|---|---|---|
| Рекомбинантный штамм вируса гриппа A/PR8-NS124-TB10.4-2A-HspX и способ специфической профилактики туберкулеза легких с использованием вакцины мукозального применения на его основе | 2019 |
|
RU2726106C1 |
| Рекомбинантный штамм вируса гриппа A/PR8-NS124-Luc и способ оценки поствакцинальных нейтрализующих антител с использованием биолюминесцентной детекции | 2019 |
|
RU2759054C2 |
| РЕКОМБИНАНТНЫЙ ВИРУС ГРИППА, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ПРОФИЛАКТИКИ COVID-19 И ГРИППА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2022 |
|
RU2802058C1 |
| АТТЕНУИРОВАННЫЕ ГРИППОЗНЫЕ ВЕКТОРЫ ДЛЯ ПРОФИЛАКТИКИ И/ИЛИ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ, А ТАКЖЕ ДЛЯ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2015 |
|
RU2628690C2 |
| Штамм вируса гриппа A/Shanghai/HK/6:2/2013 (H7N9) для получения инактивированных и живых гриппозных вакцин | 2017 |
|
RU2664460C1 |
| РЕКОМБИНАНТНЫЕ ШТАММЫ ВИРУСА ГРИППА, ЭКСПРЕССИРУЮЩИЕ МИКОБАКТЕРИАЛЬНЫЙ ПРОТЕКТИВНЫЙ АНТИГЕН ESAT-6, И ИХ ИСПОЛЬЗОВАНИЕ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2005 |
|
RU2318872C2 |
| Штамм вируса гриппа A/HK/HK/6:2/2016 (H9N2) для получения инактивированных и живых гриппозных вакцин | 2018 |
|
RU2702833C1 |
| Штамм вируса гриппа A/UNL/HK/2:6/2017 (H5N8) для получения инактивированных и живых гриппозных вакцин | 2018 |
|
RU2702834C1 |
| ШТАММ ВИРУСА ГРИППА А/Гонконг/1/68/162/35 (H3N2)-УНИВЕРСАЛЬНЫЙ ДОНОР ВНУТРЕННИХ ГЕНОВ ДЛЯ РЕАССОРТАНТОВ И РЕАССОРТАНТНЫЕ ШТАММЫ А/СПБ/ГК/09 (H1N1) И А/НК/Astana/6:2/2010 (H5N1), ПОЛУЧЕННЫЕ НА ЕГО ОСНОВЕ | 2011 |
|
RU2511431C2 |
| РЕКОМБИНАНТНАЯ ПРОТИВОГРИППОЗНАЯ ВАКЦИНА С ШИРОКИМ СПЕКТРОМ ЗАЩИТЫ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2017 |
|
RU2757013C2 |
Представленное изобретение относится к области медицинской биотехнологии. Методом обратной генетики получен рекомбинантный штамм вируса гриппа A/PR8/HK-NS80E85A, который является аттенуированным, холодоадаптированным, температурочувствительным и экспрессирует фрагменты антигенов ESAT6 и Ag85A М.tuberculosis. Рекомбинантный штамм A/PR8/HK-NS80E85A генетически стабилен и обладает высокой репродуктивной активностью в системе развивающихся куриных эмбрионов, а также стимулирует специфический противотуберкулезный CD4+ Т-клеточный ответ Th1 типа с образованием полифункциональных антиген-специфических Т-клеток при интраназальном введении мышам. Данный рекомбинантный штамм A/PR8/HK-NS80E85A депонирован в Государственной коллекции вирусов Национального исследовательского центра эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи Министерства здравоохранения Российской Федерации под №2863. Изобретение может быть использовано для получения векторной вакцины против туберкулеза. 7 ил., 4 табл., 5 пр.
Рекомбинантный штамм вируса гриппа A/PR8/HK-NS80E85A, семейство Orthomyxoviridae, род Influenzavirus А, подтип H1N1, кодирующий фрагменты антигенов ESAT-6 (1-73) и Ag85A (234-295) M. tuberculosis в составе открытой рамки считывания укороченного белка NS1 (1-80), депонированный в Государственной коллекции вирусов под №2863, предназначенный для получения интраназальной векторной вакцины против туберкулеза.
| ШТАММ ВИРУСА ГРИППА А/Гонконг/1/68/162/35 (H3N2)-УНИВЕРСАЛЬНЫЙ ДОНОР ВНУТРЕННИХ ГЕНОВ ДЛЯ РЕАССОРТАНТОВ И РЕАССОРТАНТНЫЕ ШТАММЫ А/СПБ/ГК/09 (H1N1) И А/НК/Astana/6:2/2010 (H5N1), ПОЛУЧЕННЫЕ НА ЕГО ОСНОВЕ | 2011 |
|
RU2511431C2 |
| US 0007988980 B2, 02.08.2011. | |||
Авторы
Даты
2019-01-23—Публикация
2018-03-16—Подача