Область техники, к которой относится изобретение
Изобретение относится к химической технологии, а именно к способу получения нового композиционного анодного материала для литий-ионных аккумуляторов ниобата титана TiNb2O7/C с улучшенными мощностными характеристиками.
Уровень техники
Технология хранения энергии на основе перезаряжаемых литий-ионных аккумуляторов (ЛИА) относится к наиболее актуальным направлениям современной науки и техники. По своим эксплуатационным характеристикам (удельная энергия, срок службы) они намного превосходят все другие виды аккумуляторов, что обеспечило их применение в различных беспроводных электронных устройствах, включая мобильные телефоны, персональные компьютеры и т.п. Распространение ЛИА в новые области, прежде всего, в современный электротранспорт, требует дальнейшего увеличения их емкостных и мощностных характеристик (работоспособности при высоких скоростях заряда и разряда), снижения скорости деградации при циклировании и хранении.
ЛИА состоят из положительного (катод) и отрицательного (анод) электродов, способных обратимо интеркалировать ионы лития и разделенных пористым сепаратором, пропитанным апротонным электролитом, который представляет собой раствор неорганической соли лития в органическом растворителе и обеспечивает перенос ионов Li+ между катодом и анодом. Перенос электронов осуществляется через внешнюю цепь, что сопровождается процессами окисления-восстановления ионов переходных металлов.
Свойства ЛИА в значительной степени зависят от свойств электродных материалов. Это стимулирует поиск новых и модифицирование уже используемых материалов. Материалы электродов должны обладать высокой электронной и ионной проводимостью, структурной устойчивостью к обратимой интеркаляции ионов лития, быть экологически безопасными. Улучшению мощностных характеристик материалов способствует повышение их дисперсности и электронно-ионной проводимости, что достигается путем катионного замещения и создания электронопроводящего углеродного покрытия. Потенциал окислительно-восстановительной пары электрода должен быть в пределах электрохимического окна стабильности электролита. В противном случае электрод вступает в реакцию с электролитом с образованием слоя интерфазы (solid electrolyte interface, SEI), что приводит к ухудшению его циклируемости.
Анодные материалы можно подразделить на 3 основные группы. К первой группе относят интеркаляционные аноды, которые обратимо внедряют в свою структуру ионы лития. Среди таких анодов наиболее широкое распространение получил графит из-за его дешевизны. Графит обладает теоретической удельной емкостью 372 мАч/г и высокой электронной проводимостью. Поскольку рабочий потенциал этого материала составляет 0,15-0,25 В относительно литиевого электрода, графит в ходе разряда реагирует с электролитом, образуя SEI, что приводит к деградации анода [1. An, S.J., Li, J., Daniel, C., Mohanty, D., Nagpure, S., Wood, D.L. The state of understanding of the lithium-ion-battery graphite solid electrolyte interphase (SEI) and its relationship to formation cycling // Carbon. - 2016. - V. 105. - P. 52-76]. Кроме того, графит не способен работать при высоких скоростях заряда/разряда [2. Guo, B., Wang, X., Fulvio, P., Chi, M., Mahurin, S., Sun, X., Dai, S. Soft-Templated Mesoporous Carbon-Carbon Nanotube Composites for High Performance Lithium-ion Batteries //Adv. Mater. - 2011. - V. 23. - P. 4661-4666].
К анодам второй группы относят элементы, которые образуют сплавы с литием (Si, Sn и др.). Такие аноды, как правило, обладают высокой удельной емкостью. Например, для кремния она составляет 4200 мАч/г, а для олова - 960 мАч/г [3. Zhang, C., Wang, F., Han, J., Bai, S., Tan, J., Liu, J., Li, F. Challenges and Recent Progress on Silicon-Based Anode Materials for Next-Generation Lithium-Ion Batteries // Small Struct. – 2021. – V. 2. - Nо 2100009]. Существенный недостаток этих анодов заключается в том, что они значительно изменяют свой удельный объем в ходе работы аккумулятора, что приводит к механическим повреждениям электрода.
К анодам третьей группы относят оксиды переходных металлов (MO, где M = Fe, Co, Ni, Cu), которые способны восстанавливаться до металла при разряде и регенерироваться обратно до оксида при заряде. Емкость анодных материалов на основе таких оксидов может достигать 600 - 700 мАч/г, однако они демонстрируют большую поляризацию, что уменьшает КПД аккумулятора, и достаточно высокий потенциал (~2 В), из-за чего аккумуляторы с таким анодом будут иметь низкую ЭДС [4. Poizot, P., Laruelle, S., Grugeon, S., Dupont, L., Tarascon, J.M. Nano-sized transition-metal oxides as negative-electrode materials for lithium-ion batteries // Nature. – 2000. – V. 407. P. 496-499].
Чтобы в аккумуляторе предотвратить образование solid electrolyte interface (SEI) на поверхности анода и, таким образом, увеличить его срок службы, предлагается использовать анодные материалы с рабочим напряжением чуть выше 1 В. Li4Ti5O12 со шпинельной структурой обладает удельной емкостью 175 мАч/г и рабочим потенциалом ~1,55 В, что предотвращает образование SEI. Это соединение отличается тем, что при интеркаляции оно практически не изменяет объем элементарной ячейки (ΔV=0,3%), чем обусловлена его высокая стабильность. К недостаткам этого материала относят его низкую электронную проводимость (~1·10-13 См/см) и низкий коэффициент диффузии ионов лития (1.6·10-11 см2/с), из-за чего Li4Ti5O12 поверхностно модифицируют электронопроводящими углеродными материалами и используют только в наноразмерном состоянии [5. Chen, Z., Li, H., Wu, L., Lu, X., Zhang, X. Li4Ti5O12 Anode: Structural Design from Material to Electrode and the Construction of Energy Storage Devices // Chem. Rec. - 2018. - V. 18. - P. 350-380]. Кроме того, Li4Ti5O12 обладает относительно низкой удельной емкостью в сравнении с графитом.
В качестве альтернативы Li4Ti5O12 в 2011 году был предложен ниобат титана TiNb2O7 [6. Han, J.-T., Huang, Y.-H., Goodenough, J.B. New Anode Framework for Rechargeable Lithium Batteries // Chem. Mater. - 2011. - V. 23. - P. 2027-2029]. Он обладает теоретической удельной емкостью 387,6 мАч/г, а его рабочий потенциал составляет 1,64 В. При интеркаляции ионов лития изменение объема элементарной ячейки составляет ~7,2%; фазовые изменения в ходе процессов заряда/разряда обратимы и слабо меняют его кристаллическую структуру. Недостатки TiNb2O7 аналогичны Li4Ti5O12: соединение имеет низкую электропроводность (10-9-10-11 См/см) и низкий коэффициент диффузии ионов лития (~1·10-15 см2/с) [7. Wang, H., Qian, R., Cheng, Y., Wu, H.-H., Wu, X., Pand, K., Zhang, Q. Micro/nanostructured TiNb2O7-related electrode materials for high-performance electrochemical energy storage: recent advances and future prospects // J. Mater. Chem. A. - 2020. - V. 8. - P. 18425-18463]. Поскольку TiNb2O7 обладает низким коэффициентом диффузии лития и изменяет удельный объем в большей степени, чем Li4Ti5O12, большинство работ направлено на получение этого соединения в высокодисперсном состоянии, чтобы сократить длину диффузионных путей и облегчить релаксацию искажений кристаллической структуры при изменении объема.
В Таблице 1 приведено сравнение основных характеристик наиболее перспективных на данный момент анодных материалов для ЛИА.
Таблица 1. Сравнительная характеристика анодных материалов для ЛИА
(В отн. Li+/Li)
(возможна кросс-туннельная диффузия внутри блока)
Фазовая диаграмма TiO2 – Nb2O5
В фазовой диаграмме TiO2 – Nb2O5 известно о существовании трех фаз: TiNb2O7, Ti2Nb10O29 и TiNb24O62. Все соединения характеризуются структурой кристаллографического сдвига. Они обладают рабочим потенциалом 1,6–1,8 В, структурной устойчивостью при циклировании и низкой электронной проводимостью. Значения теоретической удельной емкости составляют 387,6 мАч/г для TiNb2O7, 398 мАч/г для Ti2Nb10O29 и 401 мАч/г для TiNb24O62, однако содержание ниобия в двух последних соединениях заметно выше, что затрудняет их коммерциализацию из-за дороговизны ниобия [8. Hu, L., Luo, L., Tang, L., Lin, C., Li, R., Chen, Y. Ti2Nb2xO4+5x anode materials for lithium-ion batteries: a comprehensive review // J. Mater. Chem. A. - 2018. - V. 6. - P. 9799-9815].
Известно также соединение состава Ti2Nb2O9, которое отсутствует в фазовой диаграмме TiO2 – Nb2O5 [9. Patent US10651466B2. Active material, nonaqueous electrolyte battery, and battery pack. Заявка от 16.09.2014. Опубл. 08.09.2015]. Его получают из соединения состава KTiNbO5, которое синтезируют твердофазным способом из TiO2, Nb2O5 и K2CO3. Затем проводят обмен ионов K+ на H+ путем выдержки KTiNbO5 в 1М растворе соляной кислоте в течение 72 ч, заменяя раствор кислоты на новый через каждые 24 ч. Полученное соединение HTiNbO5 помещают в печь, заранее нагретую до 260–600°C, выдерживают в течение 2 ч, затем производят закалку и получают конечный продукт состава Ti2Nb2O9. Расчеты, проведенные в работе [10. Drozhzhin, O.A., Grigoryev, V.V., Alekseeva, A.M., Samigullin, R.R., Aksyonov, D.A., Boytsova, O.V., Chernyshov, D., Shapovalov, V.V., Guda, A.A., Soldatov, A.V., Stevenson, K.J., Antipov, E.V. Revisited Ti2Nb2O9 as an Anode Material for Advanced Li-Ion Batteries // ACS Appl. Mater. Interfaces – 2021. – V. 13. – P. 56366-56374], показали, что диффузия в нем является одномерной. Преимуществом Ti2Nb2O9 над TiNb2O7 считается меньшее содержание ниобия, однако метод его получения является многоступенчатым и включает использование жидких реагентов (кислоты), что требует последующей утилизации отходов.
Кристаллическая и электронная структура TiNb2O7
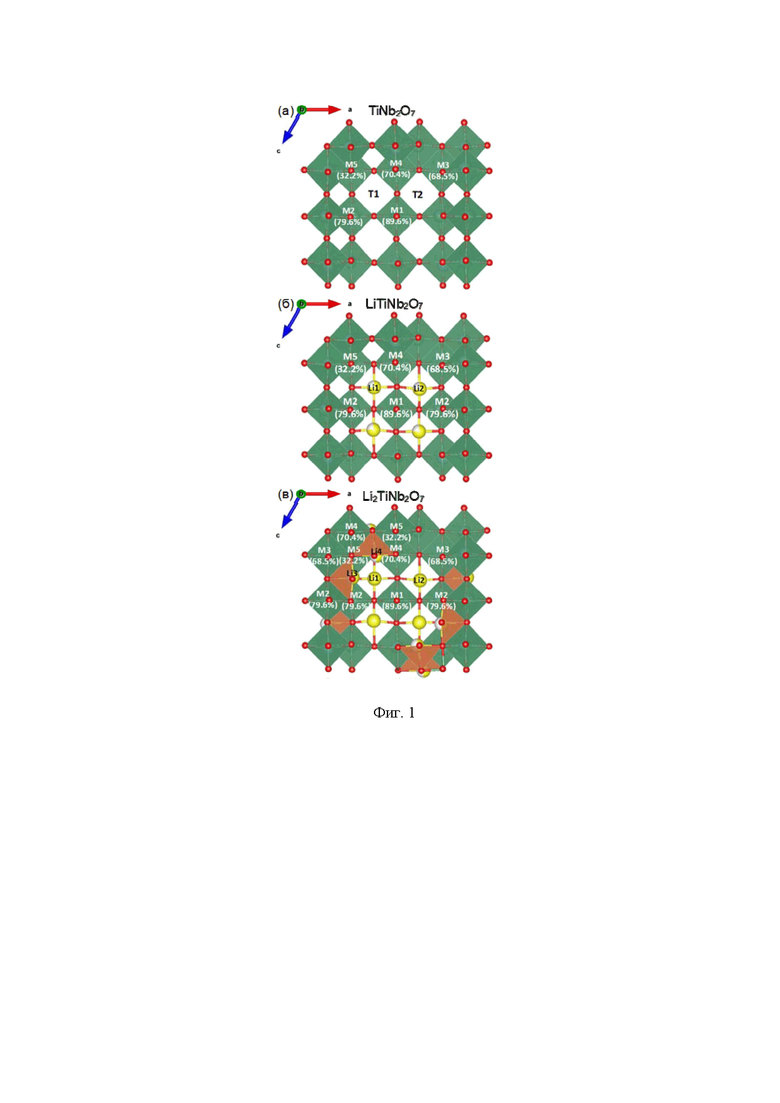
TiNb2O7 кристаллизуется в моноклинной сингонии с пространственной группой симметрии C2/m и параметрами элементарной ячейки: a = 20.351 Å, b = 3.801 Å, c = 11.882(2) Å, β = 120°19´, Z = 6 [11. Gasperin, M. Affinement de la structure de TiNb2O7 et repartition des cations // J. Solid State Chem. - 1984. - V. 53. - P. 144-147]. TiNb2O7 характеризуется структурой кристаллографического сдвига на основе структурного типа ReO3 и состоит из (3x3)∞ блоков октаэдров MO6 (M = Ti, Nb), соединенных вершинами и ребрами (Фиг. 1). Ранее предполагалось, что катионы титана и ниобия распределены статистически [12. Wadsley, A.D. Mixed Oxides of Titanium and Niobium. I. // Acta Cryst. - 1961. - V. 14. - P. 660-664]. Однако авторы [13. Cheetham, A.K., Von Dreele, R.B. The structures of some titanium-niobium oxides by powder neutron diffraction // Proc. R. Soc. Lond. A. - 1974. - V. 338. - P. 311-326] показали, что ионы Ti4+ предпочтительно занимают угловые позиции в 3×3 сечении блока, а ионы Nb5+, в первую очередь, занимают центральную и боковые позиции (позиции 3 и 5 на Фиг. 1).
В структуре TiNb2O7 имеет место преимущественно одномерная диффузия ионов лития вдоль оси b по туннелям между октаэдрами. (Фиг. 1). В отличие от одномерной диффузии лития, характерной для LiFePO4, в TiNb2O7 возможна кросс-туннельная диффузия в плоскости ac, которая ограничена плоскостями кристаллографического сдвига и возможна только в пределах 3x3 блока [14. Griffith, K.J., Seymour, I.D., Hope, M.A., Butala, M.M., Lamontagne, L.K., Preefer, M.B., Koçer, C.P., Henkelman, G., Morris, A.J., Cliffe, M.J., Dutton, S.E., Grey, C.P. Ionic and Electronic Conduction in TiNb2O7 // J. Am. Chem. Soc. - 2019. - V. 141. - P. 16706-16725]. Несмотря на то, что плоскости кристаллографического сдвига затрудняют диффузию лития в TiNb2O7, они обеспечивают устойчивость кристаллической решетки при интеркаляции ионов лития.
Согласно предложенному в литературе механизму интеркаляции [15. Yu, H., Lan, H., Yan, L., Qian, S., Cheng, X., Zhu, H., Long, N., Shui, M., Shu, J. TiNb2O7 hollow nanofiber anode with superior electrochemical performance in rechargeable lithium ion batteries // Nano Energy. - 2017. - V. 38. - P. 109-117], сначала литий заполняет одномерные туннели. Процесс протекает по однофазному механизму, переходя от состава TiNb2O7 к Li0.88TiNb2O7. После заполнения туннелей ионы лития мигрируют из туннелей в пустоты между внешними октаэдрами 3x3 блока, позволяя дальше внедряться ионам лития. Этот процесс протекает по механизму сосуществования двух фаз Li0.88TiNb2O7 и Li2.67TiNb2O7. Далее ионы лития из туннелей мигрируют в позиции между туннелями в сечении блока. В этой области процесс протекает по механизму твердых растворов до завершения интеркаляции лития.
В TiNb2O7 ионы Ti4+ и Nb5+ обладают d0 конфигурацией. Следовательно, это соединение является изолятором с шириной запрещенной зоны ~3 эВ. Валентная зона состоит из 2p состояний кислорода. Зона проводимости состоит из d-состояний титана и ниобия. Поскольку 3d-состояния титана и 4d-состояния ниобия перекрываются по энергии, сложно установить конкретные значения потенциалов пар Ti4+/Ti3+ и Nb5+/Nb4+. Поэтому утверждается, что при интеркаляции лития эти катионы восстанавливаются одновременно [16. Guo, B., Yu, X., Sun, X.-G., Chi, M., Qiao, Z.-A., Liu, J., Hu, Y.-S., Yang, X.-Q., Goodenough, J.B., Dai, S. A long-life lithium-ion battery with a highly porous TiNb2O7 anode for large-scale electrical energy storage // Energy Environ. Sci. - 2014. - V. 7. - P. 2220-2226].
При интеркаляции ионов лития электроны занимают d-состояния титана и ниобия в зоне проводимости. При этом электронная проводимость TiNb2O7 увеличивается почти на семь порядков и становится квазиметаллической. Однако при деинтеркаляции лития на внешней поверхности частиц образуется фаза с низкой электронной проводимостью, о чем свидетельствуют заметные омические потери во время заряда при отсутствии проводящих добавок в электроде [17. Lu, X., Jian, Z., Fang, Z., Gu, L., Hu, Y.-S., Chen, W., Wang, Z., Chen, L. Atomic-scale investigation on lithium storage mechanism in TiNb2O7 // Energy Environ. Sci. - 2011. - V. 4. - P. 2638-2644].
Повышение электронной проводимости исходного TiNb2O7 может быть достигнуто как за счёт создания электронопроводящего углеродсодержащего покрытия, так и путем допирования. Для этого используют различные углеродсодержащие соединения, в том числе, высокопроводящую сажу, углеродные нанотрубки и др. [18. Lin, C., Hu, L., Cheng, C., Sun, K., Guo, X., Shao, Q., Li, J., Wang, N., Guo, Z. Nano-TiNb2O7/carbon nanotubes composite anode for enhanced lithium-ion storage // Electrochim. Acta. - 2018. -V. 260. - P. 65-72], графен [19. Li, S., Cao, X., Schmidt, C. N., Xu, Q., Uchaker, E., Pei, Y., Cao, G. TiNb2O7/graphene composites as high-rate anode materials for lithium/sodium ion batteries // J. Mater. Chem. A. - 2016. - V. 4. - P. 4242-4251], восстановленный оксид графена [20. Niu, B., Zhao, P., Zhou, S., Li, Q., Li, Q., Wen, L., Liu, H., Liu, G. High-rate lithium storage of TiNb2O7/reduced graphene oxide // Ceram. Int. - 2021. - V. 47. - P. 1177-1183].
Способы получения TiNb2O7
В литературе описаны различные способы получения TiNb2O7, которые можно разделить на две основные группы: жидкофазные (гидро- и сольвотермальный синтез, соосаждение и золь-гель) и твердофазные. В большинстве работ TiNb2O7 получают растворными методами.
Гидротермальный синтез
Известен гидротермальный метод получения TiNb2O7 [21. Patent US10361429B2. Active substance used for nonaqueous electrolyte battery. Заявка от 26.03.2013. Опубл. 23.07.2019]. Метод включает в себя стадию смешения Ti(IV) и Nb(V)-содержащих реагентов в жидкой среде (вода, этанол или их смесь). Синтез проводят в автоклаве при 150–250°C в течение 1–100 ч. Полученный прекурсор отфильтровывают, промывают и сушат. Затем следует стадия отжига при 500–1200°C в течение 1–24 ч.
Недостатками гидротермального метода являются длительность его стадий и необходимость очистки прекурсора, что ведёт к удорожанию метода и необходимости утилизации жидких отходов.
Метод соосаждения
Известен метод получения TiNb2O7 путем соосаждения [22. Patent US10629901B2. Production method of battery active material, battery active material, nonaqueous electrolyte battery and battery pack. Заявка от 08.11.2013. Опубл. 21.04.2020], согласно которому смешивают кислые растворы солей Ti(IV) и Nb(V) (pH ≤ 5), затем к ним по каплям добавляют водный раствор аммиака для осаждения прекурсора. Далее следуют стадии фильтрации, промывки и сушки. Стадию отжига проводят при 635–1200°C в течение 0,5–12 ч.
Для предотвращения анизотропного роста частиц при отжиге было предложено измельчать прекурсор, полученный соосаждением, в шаровой мельнице [23. Patent US10170761B2. Active material, nonaqueous electrolyte battery, battery pack and battery module. Заявка от 19.03.2015. Опубл. 01.01.2019]. Согласно этому способу, стадию отжига проводят с быстрой скоростью нагрева (более 20°С/мин) и небольшой длительностью (1–60 мин).
Известна комбинация метода соосаждения с гидротермальным методом [24. Patent US9559357B2. Method for preparing a titanium and niobium mixed oxide by solvothermal treatment; electrode and lithium accumulator comprising said mixed oxide. Заявка от 17.10.2012. Опубл. 31.01.2017], в которой прекурсор, полученный соосаждением, подвергают сольвотермальной обработке в этаноле при 200–250°C в течение 2–10 ч. Полученный прекурсор промывают, сушат, затем измельчают в шаровой мельнице (300–500 об/мин, 15–120 мин) и отжигают при 700–1200°C в течение 0,5–2 ч.
Известен схожий метод получения TiNb2O7 [25. Patent US 10608250B2. Active material, active material composite material, electrode, secondary battery, battery pack, and vehicle. Заявка от 20.09.2017. Опубл. 31.05.2020], в котором продукт соосаждения подвергают гидротермальной обработке при 160–200°C в течение 5–10 ч. Полученный прекурсор подвергают сублимационной сушке (freeze-drying), а затем нагревают с высокой скоростью 100-500°С/мин и выдерживают при температуре 700-1100°C в течение 1–60 мин. Быстрый нагрев и отжиг проводят для того, чтобы предотвратить рост первичных частиц продукта.
Недостатком метода соосаждения является необходимость очистки прекурсора и утилизации жидких отходов.
Золь-гель метод
Известен золь-гель метод получения TiNb2O7 [26. Patent CA2810191C. Niobium oxide compositions and methods for using same. Заявка от 30.07.2010. Опубл. 12.06.2018]. Способ включает стадию получения раствора соли Nb(V) путем растворения Nb2O5 в HF, осаждение Nb(OH)5 путем добавления аммиака с повторным растворением осадка в лимонной кислоте. К раствору добавляют раствор Ti(OC3H7)4 в смеси этанола и воды. Полученную смесь перемешивают при 90°С до образования геля. Гель нагревают до 140°С, а затем отжигают при 900-1350°С.
Известен золь-гель метод получения TiNb2O7 [27. Patent US10056615B2. Active substance, nonaqueous electrolyte battery, and battery pack. Заявка от 20.09.2013. Опубл. 21.08.2018], в котором вместо того, чтобы растворять Nb2O5 в HF, используют готовую соль Nb(V). Согласно этому методу, соли Ti(IV) (например TiOSO4, (NH4)2TiO(C2O4)·H2O, Ti(OC3H7)4, TiCl4) и Nb(V) (например NbCl5, (NH4)Nb(C2O4)) смешивают, регулируя pH для облегчения гидролиза. Образовавшийся гель нагревают при 80°C для удаления растворителя. Полученный прекурсор отжигают при 700–1400°С в течение 1–24 ч. Допускается предварительное измельчение прекурсора в шаровой, вибрационной или бисерной мельнице.
Недостатками золь-гель методов является использование дорогих реагентов (органических солей титана и ниобия) и необходимость утилизации жидких отходов.
Твердофазный метод
Твердофазные методы синтеза отличаются большей простотой, дешевизной и легкой масштабируемостью. Однако образцы, полученные твердофазным методом, обычно обладают широким распределением по размеру частиц в пределах 0,1-10 мкм. Как правило, материал, полученный твердофазным методом, обладает неудовлетворительными свойствами (невысокая обратимая емкость, плохая циклируемость, низкая удельная емкость при высоких плотностях тока) и требует дальнейшего модифицирования.
Среди известных твердофазных методов синтеза следует выделить современный, сухой, энергетически эффективный и экологически чистый метод механохимически стимулированного твердофазного синтеза. Предварительная механическая активация (МА) позволяет производить смешение реагентов с одновременным измельчением, что способствует получению продукта в высокодисперсном состоянии. Для повышения кристалличности конечного продукта требуется стадия последующего отжига, однако ее продолжительность и температура при использовании МА существенно снижаются.
Известен твердофазный метод получения TiNb2O7 [28. Patent EP2696430B1. Negative electrode for battery, nonaqueous electrolyte battery and battery pack. Заявка от 29.10.2010. Опубл. 28.06.2017]. Согласно патенту, смесь TiO2 и Nb2O5 отжигают при 1000–1500°С в течение 10–40 ч.
Недостатками описанного метода является продолжительность синтеза и использование высоких температур.
Твердофазный метод с использованием механической активации (МА)
Известен твердофазный метод получения TiNb2O7 с применением предварительной механической обработки в шаровой мельнице [29. Patent US10096826B2. Active material, nonaqueous electrolyte battery, battery pack, and method of producing active material. Заявка от 26.10.2012. Опубл. 09.10.2018]. Согласно методу, смесь TiO2 и Nb2O5 измельчают в шаровой мельнице, затем проводят предварительный отжиг при температуре 1000°C в течение 12 ч (для удаления воды и органических примесей). Затем проводят повторный отжиг при 1350°C в течение 18 ч. Полученный продукт содержит примесные фазы: рутил TiO2, Ti2Nb10O29 и TiNb24O62. Утверждается, что при внедрении лития в фазу рутила увеличивается электронная проводимость, а наличие примесных фаз Ti2Nb10O29 и TiNb24O62 улучшает интеркаляционные свойства основного продукта. Согласно данному методу, содержание примесных фаз увеличивается, если после второго отжига продукт быстро охладить, вынув из печи. С другой стороны, содержание примесных фаз можно уменьшить при повторном отжиге продукта при 600°C в течение 24 ч. Однофазный образец получали двухстадийным отжигом при температуре 1000°C в течение 12 ч, а затем при 1100°C в течение 12 ч.
Недостатками описанного метода являются его многостадийность, продолжительность синтеза и использование высоких температур.
Твердофазный метод синтеза допированного TiNb2O7 с использованием МА
Известен твердофазный метод получения допированного TiNb2O7 с применением предварительной механической обработки в вибрационной мельнице [30. Patent CA3141700A1. Titanium-niobium oxides and electrodes and lithium-ion secondary cells employing titanium-niobium oxides. Заявка от 26.12.2019. Опубл. 01.07.2021]. Согласно этому методу, смесь оксидов Тi, Nb и источников допирующих элементов (ионов щелочных металлов до 0.30 ат.% и Al, Y, La, Ce, Pt, Sm) смешивают в вибрационной мельнице, после чего смесь отжигают при 1100°С в течение 2 ч. Утверждается, что добавление ионов щелочных металлов ускоряет протекание твердофазного синтеза, что позволяет уменьшить содержание побочных продуктов, таких как TiO2 и Ti2Nb10O29, но приводит к анизотропному росту частиц. Поэтому для подавления роста частиц TiNb2O7 добавляют такие элементы, как Al, Y, La, Ce, Pt, Sm.
Недостатками данного метода является наличие электрохимически неактивных элементов в продукте, что снижает удельную емкость анода.
Известен твердофазный метод получения допированного TiNb2O7 с применением предварительной механической обработки в шаровой мельнице [31. Patent US10957906B2. Electrode, secondary battery, battery pack, and vehicle. Заявка от 23.03.2018. Опубл. 30.08.2018]. Согласно методу, смесь оксидов Тi, Nb и источника ионов-заместителей M = Na, K, Ca, B, Co, Fe, Mn, Ni, Si, P, Mo подвергают механической обработке в шаровой мельнице в течение 1 ч, затем отжигают при 1000°С в течение 12 ч, после чего порошок измельчают в шаровой мельнице и повторно отжигают при 1100°С в течение 5 ч. Затем порошок измельчают молотковыми и валковыми мельницами, а потом измельчают во влажной шаровой мельнице в течение 3 ч. Полученный порошок подвергают отжигу при 1100°С в течение 1 ч, после чего производят закалку в жидком азоте. Для получения углеродного покрытия продукт диспергируют в насыщенном растворе сахарозы. Полученную смесь подвергают распылительной сушке, а затем проводят карбонизацию в потоке азота при 600°С в течение 2 ч.
Недостатками описанного метода являются его многостадийность и продолжительность синтеза.
Твердофазный метод синтеза допированного TiNb2O7/C с использованием МА
Наиболее близким по технической сущности является твердофазный метод получения допированного TiNb2O7 с применением предварительной механической обработки в шаровой мельнице [32. Patent US10944104B2. Electrode, secondary battery, battery pack, and vehicle. Заявка от 23.03.2018. Опубл. 31.08.2018]. Согласно методу, смесь оксидов Тi, Nb (в соотношении Ti/Nb = 1) и источника ионов-заместителей M = Na, K, Ca, B, Co, Fe, Mn, Ni, Si, P, Mo подвергают механической обработке в шаровой мельнице в течение часа, затем отжигают при 1000°С в течение 12 часов, после чего порошок измельчают в шаровой мельнице, добавляют Nb2O5 (до финальной стехиометрии TiNb1.95M0.05O7) и повторно отжигают при 1100°С в течение 5 часов. После этого проводят отжиг при температуре 500°С в течение 2 часов. Для получения углеродного покрытия продукт диспергируют в насыщенном растворе сахарозы. Полученную смесь подвергают распылительной сушке, а затем проводят карбонизацию в потоке азота при 600°С в течение 2 часов.
Недостатками описанного метода являются его многостадийность и продолжительность синтеза.
Сущность изобретения
Задача изобретения – разработка простого, быстрого и дешёвого способа получения высокодисперсного композиционного анодного материала TiNb2O7/С.
Поставленная задача решается благодаря тому, что в заявляемом способе реализуется получение высокодисперсного композиционного анодного материала TiNb2O7 с электронопроводящим углеродным покрытием, допированного ионами-заместителями, включающее измельчение, смешение и активацию реакционной смеси, содержащей оксиды титана и ниобия, а также один или несколько соединений переходных металлов, являющихся поставщиками ионов-заместителей, из числа оксидов, гидроксидов или солей; термическую обработку; охлаждение; диспергирование и поверхностное модифицирование углеродом, отличающийся тем, что исходные компоненты смешивают и активируют в механохимическом активаторе с удельной мощностью 10-80 Вт/г в течение 3-10 минут, после чего полученную смесь подвергают термической обработке при 900–1100°С в воздушной атмосфере, охлаждают до комнатной температуры и диспергируют с углеродом в механохимическом активаторе мощностью 10-80 Вт/г в течение 1-5 минут в инертной атмосфере, осуществляя поверхностное модифицирование.
При получении высокодисперсного композиционного анодного материала TiNb2O7/С, предпочтительно, в качестве соединений титана используют TiO2 (анатаз), а в качестве соединений ниобия – оксид ниобия Nb2O5. Синтез протекает по следующей реакции:

Предпочтительно, для поверхностного модифицирования углеродом используют высокопроводящую сажу в количестве 3-5 мол. %. Количество углерода в конечном композиционном анодном материале должно быть минимально возможным (3-5%), поскольку при его увеличении значительно снижается насыпная плотность и, как следствие, волюмометрическая плотность энергии.
Предпочтительно, введение ионов-заместителей M осуществляют с помощью соединений переходных металлов со степенью окисления 4+ из числа Ru, Zr, 5+ из числа V, Ta, 6+ из числа Mo, W в составе оксидов, гидроксидов или солей.
Предпочтительно, мольная концентрация иона-заместителя M составляет 1-5 мол.%, при этом M замещает либо ионы Ti4+, либо ионы Nb5+. Если мольная концентрация превышает 5 мол.%, то M образует примесную фазу, не оказывающую существенного влияния на электронную проводимость. Это ведет к снижению содержания активного компонента, что уменьшает удельную емкость.
Предпочтительно, для введения иона-заместителя V5+ добавляют оксид ванадия V2O5 в количестве 1-5 мол. %.
Предпочтительно, активированные смеси перед нагреванием прессуют.
Предпочтительно, термообработку осуществляют путем отжига на воздухе при температурах 900-1100°С со скоростью нагрева 10 град/мин и выдержкой 4-8 ч.
Существенными отличительными признаками заявляемого технического решения являются:
- исходные компоненты смешивают и активируют в механохимическом активаторе с удельной мощностью 10-80 Вт/г в течение 3-10 минут;
- полученную смесь подвергают термической обработке при 900–1100°С в воздушной атмосфере и выдержке 4-8 ч;
- охлаждают до комнатной температуры;
- диспергируют с углеродом в механохимическом активаторе мощностью 10-80 Вт/г в течение 1-5 минут в инертной атмосфере.
Совокупность существенных отличительных признаков позволяет решить поставленную задачу.
Одним из технических результатов, достигаемых в настоящем изобретении, является упрощение процесса синтеза и получение конечного продукта в высокодисперсном состоянии, что осуществляется за счёт проведения предварительной механической активации реагентов в высоконапряженных механохимических активаторах с удельной мощностью 10-80 Вт/г в течение 3-10 минут. Степень смешения и измельчения при этом существенно выше, чем в обычных шаровых мельницах. Указанные предельные условия являются оптимальными для измельчения и полной гомогенизации исходной смеси. При более высоких временах происходит процесс агломерации первичных частиц и увеличение степени загрязнения конечного продукта материалом мелющих тел. Процесс смешения и диспергирования проводят в атмосфере инертного газа для предотвращения взаимодействия реагентов с компонентами воздуха.
Другим техническим результатом, достигаемым в настоящем изобретении, является удешевление процесса получения композиционного анодного материала с углеродом за счёт понижения температуры, сокращения времени отжига и отсутствия необходимости использования жидких органических прекурсоров и дополнительного отжига для создания углеродной матрицы и сведения к минимуму количества отходов. При температурах ниже 900°С не достигается получение однофазного продукта, а при температурах выше 1100°С и продолжительности отжига более 8 ч происходит заметное увеличение размера частиц продукта вследствие спекания.
Еще одним техническим результатом, достигаемым в настоящем изобретении, является введение ионов-заместителей M в количестве 1-5 мол. %, что, наряду с углеродным покрытием, способствует повышению электронной проводимости анодного материала, улучшению его стабильности при циклировании и увеличению удельной емкости, в том числе при повышенных скоростях.
Описание полученных материалов
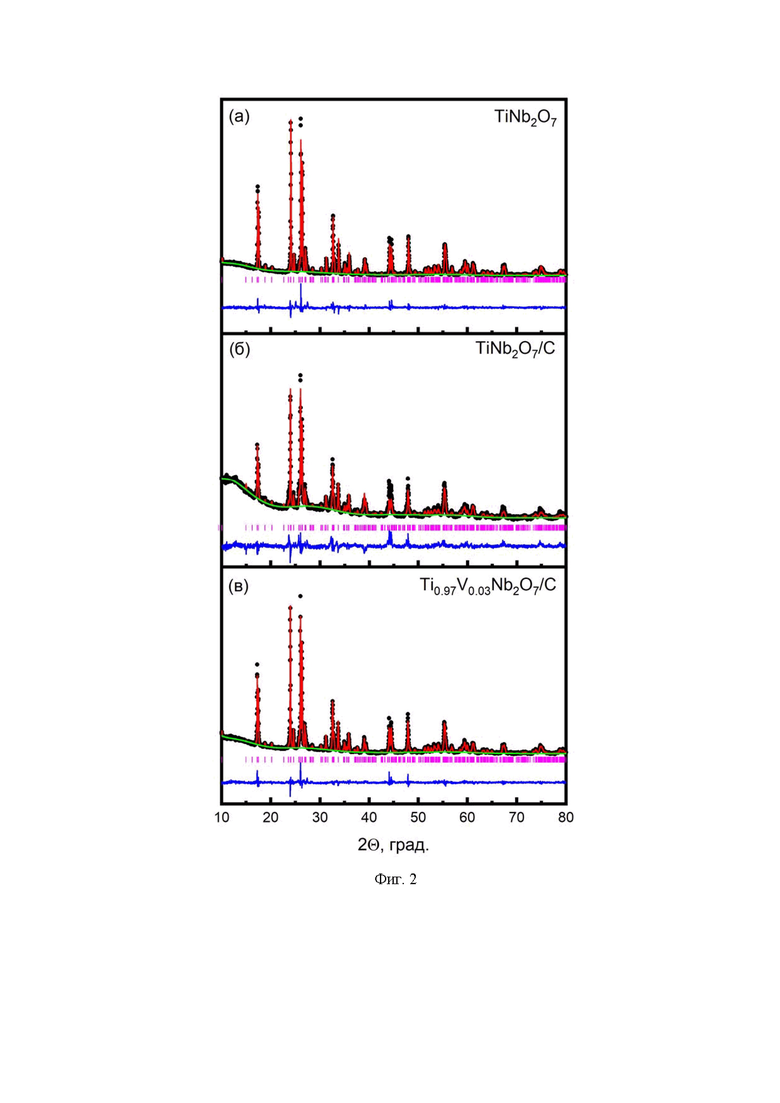
Образцы анодного материала TiNb2O7, композиционного анодного материала с углеродом TiNb2O7/С и TiNb2O7, допированного ионами-заместителями переходных металлов (например, V5+) были получены механохимически стимулированным твердофазным методом синтеза из оксидов титана и ниобия с добавлением углерода и оксида ванадия 5+. По данным рентгенофазового анализа, все полученные материалы являются однофазными (Фиг. 2). Рассчитанные параметры решетки представлены в Таблице 2. Из Таблицы следует, что для диспергированных с углеродом образцов параметры решетки немного увеличиваются, вероятно, из-за частичного восстановления ионов Ti4+ или Nb5+, поскольку диспергирование проводят в атмосфере аргона. Полученные параметры находятся в соответствии с литературными данными.
Таблица 2. Параметры решетки полученных продуктов

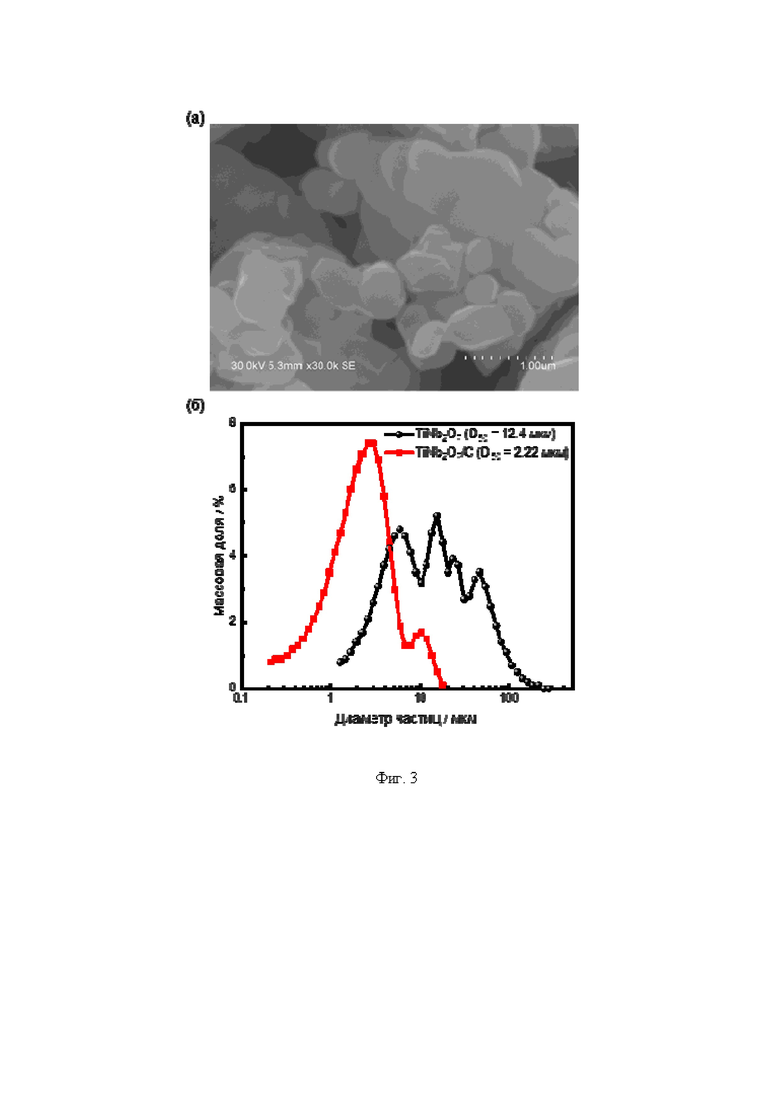
Средний размер частиц TiNb2O7 по данным сканирующей электронной микроскопии составляет 500 нм (Фиг. 3а). Гранулометрический анализ указывает, что для композиционного материала с углеродом характерно уменьшение среднего размера частиц от 12,4 мкм до 2,22 мкм и более узкое распределение частиц по размерам (Фиг. 3б).
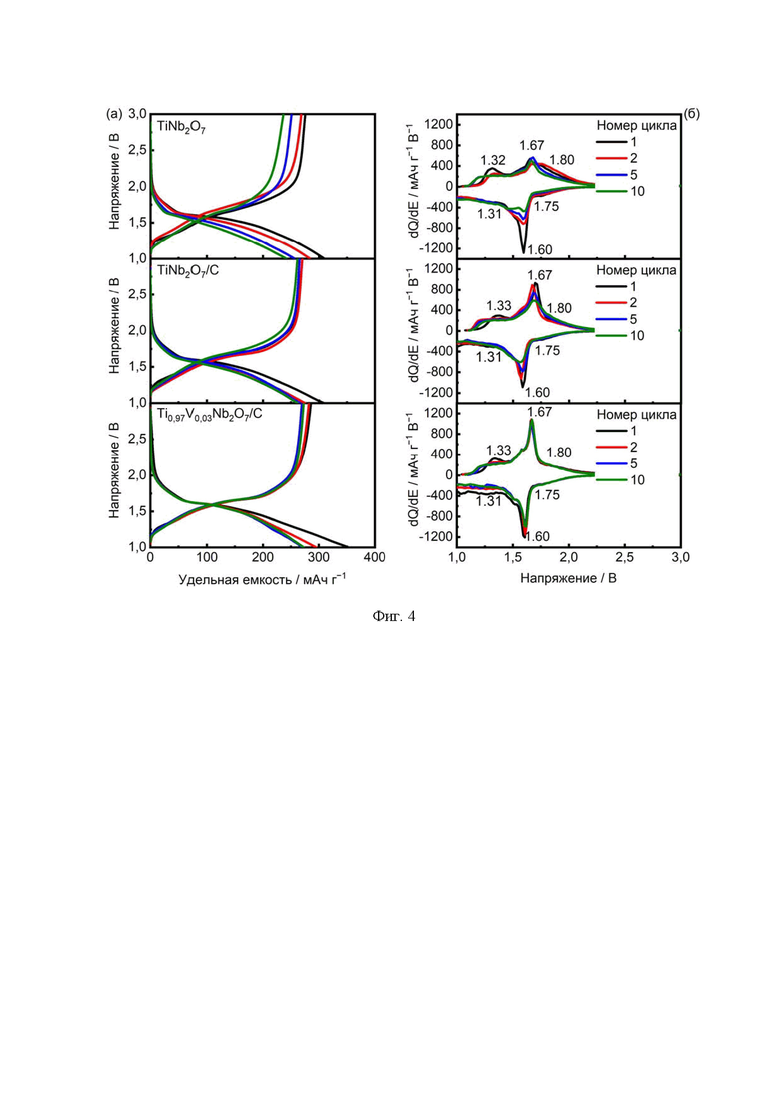
На Фиг. 4 приведены кривые циклирования полученных материалов. Циклирование проводили в гальваностатическом режиме в полуэлементах TiNb2O7+C / LiPF6+EC+DMC / Li со стекловолоконным сепаратором Whatman, Grade GF/C в интервале 1,0-3,0 В при скорости циклирования C/10 и температуре 20°C. Электроды готовили смешением активной составляющей анодного материала с углеродом (ФИЦ «Институт катализа им. Г.К. Борескова СО РАН», г. Омск). Общее содержание углерода в анодном материале составляло 10-20%. На зарядно-разрядных кривых наблюдается 3 участка. В области плато при 1,6 В интеркаляция/деинтеркаляция лития протекает по двухфазному механизму. На начальном и конечном участках кривой циклирования интеркаляция/деинтеркаляция лития протекает по механизму твердых растворов (Фиг. 4а). Поскольку 3d-состояния ионов титана и 4d-состояния ионов ниобия перекрываются по энергии, то соответственно перекрываются и пики на дифференциальных кривых, соответствующие окислительно-восстановительным парам Ti4+/Ti3+ и Nb5+/Nb4+ (Фиг. 4б). Согласно литературным данным [33. Tang, K., Mu, X., Aken, P.A., Yu, Y., Maier, J., “Nano-Pearl-String” TiNb2O7 as Anodes for Rechargeable Lithium Batteries // Adv. Energy Mater. - 2013. - V. 3. - P. 49-53.], широкий перекрывающийся пик при 1,70-1,80 В соответствует паре Ti4+/Ti3+; высокоинтенсивный пик при 1,58-1,66 В соответствует паре Nb5+/Nb4+, а пик при 1,28-1,35 В соответствует паре Nb4+/Nb3+.
На Фиг. 5 приведены значения удельной ёмкости полученных образцов в зависимости от номера цикла при скорости циклирования C/10 (C – теоретическая емкость, достигаемая за 1 ч). Наблюдается устойчивое циклирование диспергированных с углеродом образцов в течение 50 циклов. Обратимая удельная зарядная емкость составляет 276 мАч/г для TiNb2O7, 270 мАч/г для композита TiNb2O7/C и 286 мАч/г для допированного ванадием образца Ti0.97V0.03Nb2O7/C.
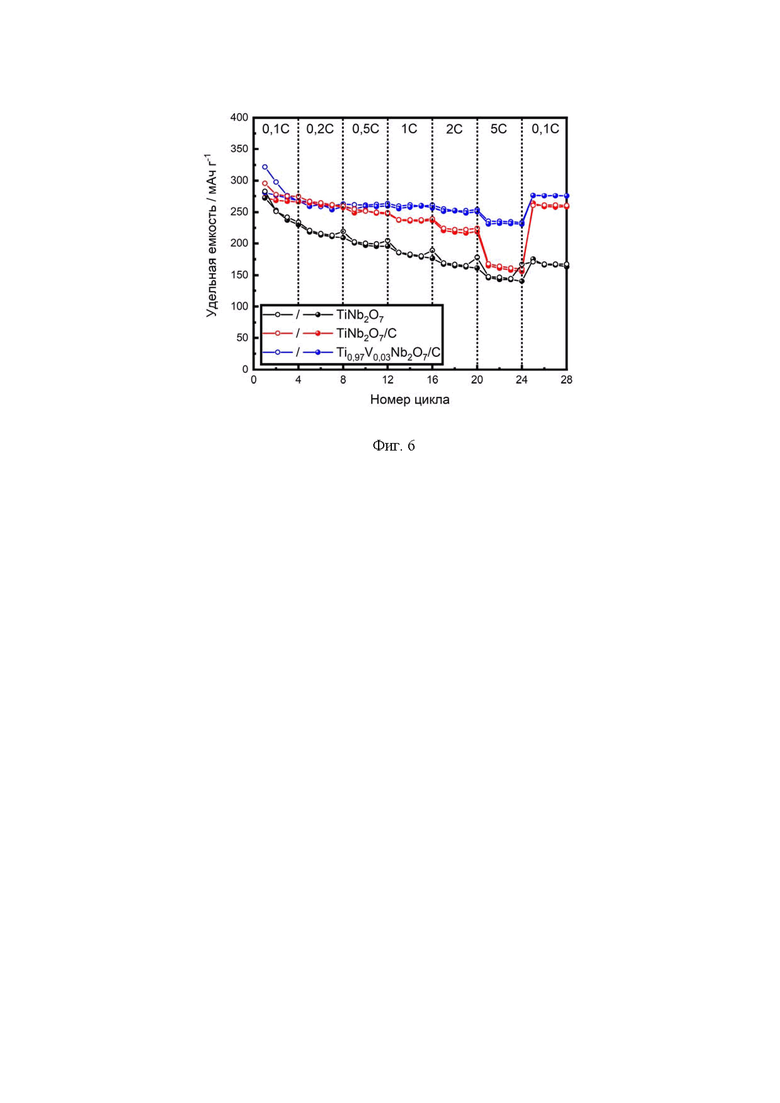
На Фиг. 6 представлена зависимость удельной разрядной ёмкости полученных образцов от скорости циклирования. При увеличении скорости циклирования от С/10 до 5С зарядная ёмкость сохраняется на уровне 143, 161 и 232 мАч/г для образцов TiNb2O7, TiNb2O7/C и Ti0.97V0.03Nb2O7/C соответственно. Данный эффект объясняется значительным увеличением электронной проводимости Ti0.97V0.03Nb2O7/C за счет создания электронопроводящего углеродного покрытия и зарядовой компенсации введенного иона-заместителя V5+ путем частичного восстановления ионов Ti4+ или Nb5+ и сокращения ширины запрещенной зоны благодаря примесным зонам ванадия [34. Liu, K., Wang, J.-A., Yang, J., Zhao, D., Chen, P., Man, J., Yu, X., Wen, Z., Sun, J. Interstitial and substitutional V5+-doped TiNb2O7 microspheres: A novel doping way to achieve high-performance electrodes // Chem. Eng. J. - 2021. - V. 407. - P. 127190].
Таким образом, преимущество данного технического решения заключается в совокупности подобранных оптимальных условий твердофазного механохимически стимулированного синтеза композиционного материала с высокопроводящим углеродным покрытием и допированного ионами переходных металлов, что позволяет создать простой, дешевый и безотходный способ получения высокодисперсного композиционного анодного материала Ti1-xMxNb2O7/C для литий-ионных аккумуляторов с улучшенными мощностными характеристиками.
Высокая дисперсность и сокращение времени синтеза достигаются путём применения в ходе синтеза МА. Модифицирование TiNb2O7 реализуется путем допирования ионами-заместителями и созданием электронопроводящего углеродного покрытия.
Технический результат, достигаемый благодаря заявляемому способу, заключается в получении высокодисперсного TiNb2O7/C и в улучшении его анодных характеристик при использовании в литий-ионных аккумуляторах, в частности, в достижении удельной разрядной емкости 194 мАч/г при скорости циклирования 5С, повышении устойчивости при циклировании, а также приводит к упрощению процесса синтеза и удешевлению получаемого продукта.
Примеры конкретного выполнения:
Пример 1. Для демонстрации оптимально подобранных условий синтеза получен TiNb2O7, не содержащий углерода и ионов-заместителей в своём составе. Для синтеза используют TiO2 (анатаз) и Nb2O5 в мольном соотношении 1:1. Реакционная смесь подвергается смешению, диспергированию и активации в механохимическом активаторе АГО-2 с удельной мощностью 60 Вт/г в течение 5 мин в атмосфере аргона, прессованию и последующей термической обработке на воздухе. Термическую обработку проводят при 1000°С в течение 4 ч. Удельная зарядная ёмкость полученного анодного материала составляет 276 мАч г-1 при скорости С/10 и 143 мАч г-1 при скорости 5С.
Пример 2. Для получения TiNb2O7/С, продукт, полученный в условиях примера 1, смешивали с углеродом в соотношении 95:5 и подвергали диспергированию в механохимическом активаторе АГО-2 с удельной мощностью 40 Вт/г в течение 3 мин в атмосфере аргона. Удельная зарядная ёмкость полученного анодного материала составляет 270 мАч г-1 при скорости С/10 и 161 мАч г-1 при скорости 5С.
Пример 3. Для получения Ti0.97V0.03Nb2O7 взята смесь TiO2, Nb2O5 и V2O5 в мольном соотношении 0.97:1:0.015. Допирование можно описать следующим квазихимическим уравнением:

Синтез Ti0.97V0.03Nb2O7 проводили в условиях примера 1. Для получения композита Ti0.97V0.03Nb2O7/C, полученный продукт диспергировали с углеродом в условиях примера 2. Удельная зарядная ёмкость полученного анодного материала составляет 286 мАч г-1 при скорости С/10 и 232 мАч г-1 при скорости 5С.
Пример 4. Для получения Ti0.99V0.01Nb2O7 взята смесь TiO2, Nb2O5 и V2O5 в мольном соотношении 0.99:1:0.005. Синтез Ti0.99V0.01Nb2O7 проводили в условиях примера 1. Для получения композита Ti0.99V0.01Nb2O7/C, полученный продукт диспергировали с углеродом в условиях примера 2. Удельная зарядная ёмкость полученного анодного материала составляет 284 мАч г-1 при скорости С/10 и 194 мАч г-1 при скорости 5С.
Пример 5. Для получения Ti0.95V0.05Nb2O7 взята смесь TiO2, Nb2O5 и V2O5 в мольном соотношении 0.95:1:0.025. Синтез Ti0.95V0.05Nb2O7 проводили в условиях примера 1. Для получения композита Ti0.95V0.05Nb2O7/C, полученный продукт диспергировали с углеродом в условиях примера 2. Удельная зарядная ёмкость полученного анодного материала составляет 259 мАч г-1 при скорости С/10 и 118 мАч г-1 при скорости 5С.
Пример 6. Для получения Ti0.97Mo0.03Nb2O7 взята смесь TiO2, Nb2O5 и MoO3 в мольном соотношении 0.97:1:0.03. Допирование можно описать следующим квазихимическим уравнением:
MoO3 → MoTi•• + 2OOX + ½ O2↑ + 2e'
Синтез Ti0.97Mo0.03Nb2O7 проводили в условиях примера 1. Для получения композита Ti0.97Mo0.03Nb2O7/C, полученный продукт диспергировали с углеродом в условиях примера 2. Удельная зарядная ёмкость полученного анодного материала составляет 272 мАч г-1 при скорости С/10 и 174 мАч г-1 при скорости 5С.
Краткое описание чертежей:
Сущность изобретения поясняется чертежами.
Фиг. 1 - Кристаллическая структура TiNb2O7: (а) с указанием имеющихся каналов, структурных позиций и их занятости, (б, в) то же для литированных материалов с разным содержанием лития.
Фиг. 2 - Дифрактограммы TiNb2O7 (а), TiNb2O7/С (б) и Ti0.97V0.03Nb2O7/C (в).
Фиг. 3 - Микрофотография TiNb2O7 (а) и распределение частиц по размерам (б).
Фиг. 4 - Зарядно-разрядные кривые TiNb2O7, TiNb2O7/С и Ti0.97V0.03Nb2O7/С.
Фиг. 5 - Зависимость удельной ёмкости TiNb2O7, TiNb2O7/С и Ti0.97V0.03Nb2O7/С от номера цикла при скорости циклирования С/10 в интервале 1,0 – 3,0 В.
Фиг. 6 - Зависимость удельной ёмкости TiNb2O7, TiNb2O7/С и Ti0.97V0.03Nb2O7/С от скорости циклирования в интервале 1,0 – 3,0 В.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения твердого электролита LiAlTi(PO) для твердотельных литий-ионных аккумуляторов | 2023 |
|
RU2821885C1 |
| Способ получения композиционного катодного материала на основе NaV(PO)F для натрий-ионных аккумуляторов | 2020 |
|
RU2747565C1 |
| АНОД ДЛЯ КАЛИЙ-ИОННЫХ АККУМУЛЯТОРОВ | 2020 |
|
RU2731884C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБКОГО АНОДНОГО МАТЕРИАЛА НА ОСНОВЕ МОДИФИЦИРОВАННОЙ УГЛЕРОДНОЙ ТКАНИ | 2024 |
|
RU2826545C1 |
| АНОДНЫЙ МАТЕРИАЛ ЛИТИЙ-ИОННОГО АККУМУЛЯТОРА НА ОСНОВЕ LiCrTiO СО СТРУКТУРОЙ ШПИНЕЛИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2558140C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОВЕРХНОСТНО-МОДИФИЦИРОВАННОГО КАТОДНОГО МАТЕРИАЛА СО СЛОИСТОЙ СТРУКТУРОЙ ДЛЯ ЛИТИЕВЫХ И ЛИТИЙ-ИОННЫХ АККУМУЛЯТОРОВ | 2006 |
|
RU2307429C1 |
| АНОДНЫЙ МАТЕРИАЛ ДЛЯ ЛИТИЙ-ИОННЫХ ХИТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2397576C1 |
| АНОДНЫЙ МАТЕРИАЛ ДЛЯ ЛИТИЙ- И НАТРИЙ-ИОННЫХ АККУМУЛЯТОРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2730001C1 |
| ГЕКСАФЕРРИТ СТРОНЦИЯ КАК КАТОДНЫЙ МАТЕРИАЛ ДЛЯ ЛИТИЕВОГО АККУМУЛЯТОРА | 2012 |
|
RU2510550C1 |
| Способ плазмоэлектрохимической переработки графита из использованных литий-ионных аккумуляторов | 2023 |
|
RU2825576C1 |

Изобретение относится к химической технологии и может быть использовано при создании литий-ионных аккумуляторов. Способ получения композиционного анодного материала TiNb2O7/C для литий-ионных аккумуляторов включает измельчение, тонкое смешение и активацию реакционной смеси, содержащей оксиды титана и ниобия, а также один или несколько соединений переходных металлов, являющихся поставщиками ионов-заместителей, из числа оксидов, гидроксидов или солей; термическую обработку; охлаждение; диспергирование и поверхностное модифицирование углеродом. Наличие ионов-заместителей и создание углеродсодержащего электронопроводящего поверхностного покрытия позволяют улучшить мощностные характеристики TiNb2O7. Технический результат заключается в получении с применением механической активации наноструктурированных композиционных материалов на основе Ti1-xMxNb2O7/C и в улучшении их мощностных характеристик при использовании в литий-ионных аккумуляторах. 7 з.п. ф-лы, 6 ил., 2 табл., 6 пр.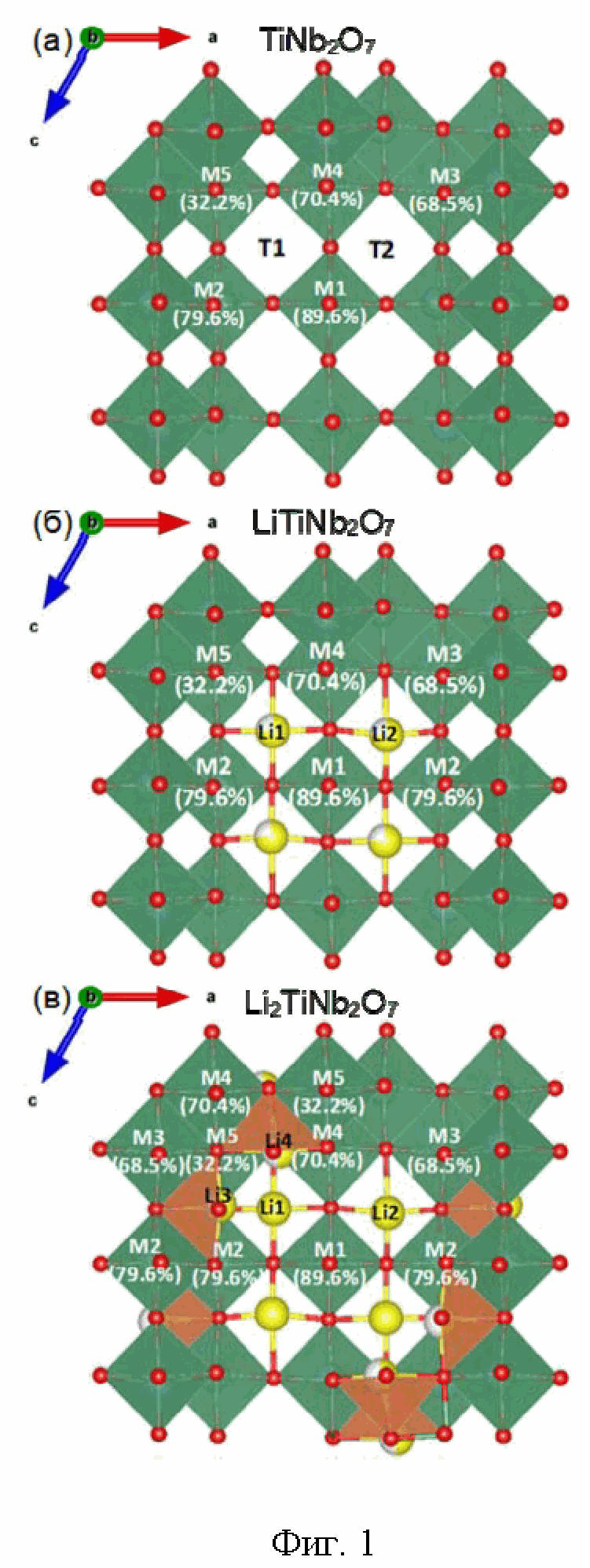
1. Способ получения композиционного анодного материала TiNb2O7/C для литий-ионных аккумуляторов, включающий измельчение, смешение и активацию реакционной смеси, содержащей оксиды титана и ниобия, а также один или несколько соединений переходных металлов, являющихся поставщиками ионов-заместителей, из числа оксидов, гидроксидов или солей; термическую обработку; охлаждение; диспергирование и поверхностное модифицирование углеродом, отличающийся тем, что исходные компоненты смешивают и активируют в механохимическом активаторе с удельной мощностью 10-80 Вт/г в течение 3-10 минут, после чего полученную смесь подвергают термической обработке при 900–1100°С в воздушной атмосфере, охлаждают до комнатной температуры и диспергируют с углеродом в механохимическом активаторе мощностью 10-80 Вт/г в течение 1-5 минут в инертной атмосфере, осуществляя поверхностное модифицирование.
2. Способ по п. 1, отличающийся тем, что в качестве соединений титана используют TiO2 анатаз, а в качестве соединений ниобия – оксид ниобия Nb2O5.
3. Способ по п. 1, отличающийся тем, что для поверхностного модифицирования углеродом используют высокопроводящую сажу в количестве 3-5 мол.%.
4. Способ по п. 1, отличающийся тем, что введение ионов-заместителей осуществляют с помощью соединений переходных металлов со степенью окисления 4+ из числа Ru, Zr, 5+ из числа V, Ta, 6+ из числа Mo, W в составе оксидов, гидроксидов или солей.
5. Способ по п. 1, отличающийся тем, что мольная концентрация ионов-заместителей составляет 1-5 мол.%.
6. Способ по п. 1, отличающийся тем, что для введения иона-заместителя V5+ добавляют оксид ванадия V2O5 в количестве 1-5 мол.%.
7. Способ по п. 1, отличающийся тем, что активированные смеси перед нагреванием прессуют.
8. Способ по п. 1, отличающийся тем, что термообработку осуществляют путем отжига на воздухе при температурах 900-1100°С со скоростью нагрева 10 град/мин и выдержкой 4-8 ч.
| US 10944104 B2, 09.03.2021 | |||
| Способ получения нанокомпозиционных катодов для литий-ионных аккумуляторов | 2015 |
|
RU2634306C2 |
| ЭЛЕКТРОДНЫЙ МАТЕРИАЛ ДЛЯ МЕТАЛЛ-ИОННЫХ АККУМУЛЯТОРОВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ЭЛЕКТРОД И АККУМУЛЯТОР НА ОСНОВЕ ЭЛЕКТРОДНОГО МАТЕРИАЛА | 2015 |
|
RU2619600C2 |
| US 10096826 B2, 09.10.2018 | |||
| US 10651466 B2, 12.05.2020. | |||
Авторы
Даты
2023-07-03—Публикация
2022-09-13—Подача