Область техники
Настоящее изобретение направлено на создание соединений с антибактериальным действием на основе фторированных производных салициловой кислоты. Указанные соединения могут быть использованы в клинической практике для лечения заболеваний мочеполовой системы и гнойно-воспалительных инфекций кожи и слизистых оболочек.
Уровень техники
Глобальные проблемы антибиотикорезистентности Neisseria gonorrhoeae и возбудителей бактериальных нозокомиальных (внутрибольничных) инфекций энтеробактерий, которые кроме различного спектра природной устойчивости, обладают способностью к формированию вторичной резистентности к антибактериальным препаратам разных классов, определяет необходимость поиска новых химических соединений, обладающих антибактериальной активностью. Соединения этого класса, проявляют широкий спектр разнообразной биологической активности, включая антибактериальную. Салициловую кислоту рекомендуют применять наружно в качестве отвлекающего, местно-раздражающего, противовоспалительного, кератопластического, кератолитического, подсушивающего и антисептического средства. Ее используют в монотерапии или в составе комбинированных препаратов при воспалительных, инфекционных и других поражениях кожи, включая ожоги, псориаз, экзему, дискератоз, ихтиоз, обыкновенные угри, бородавки, гиперкератоз, мозоли, омозолелость, жирную себорею, отрубевидный лишай, выпадение волос, потливость ног.
Для создания новых салицилатов большее значение должен иметь синтез полифторсодержащих производных. Как известно, введение атома фтора в молекулу органического соединения эффективно и успешно используют в медицинской химии для модуляции физико-химических и биологических свойств новых веществ при поиске лекарственных препаратов [D. O'Hagan. Fluorine in health care: Organofluorine containing blockbuster drugs // J. Fluor. Chem., 2010, Vol. 131, P. 1071-1081; P. Kirsch. Modern Fluoroorganic. Chemistry Synthesis, Reactivity, Applications. Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, 2004; E.A. Meyer, R.K. Castellano, F. Diederich. Interactions with Aromatic Rings in Chemical and Biological Recognition // Angew. Chemie Int. Ed., 2003, Vol. 42, P. 1210-1250]. Так, около 20% используемых фармацевтических препаратов имеют по крайней мере один атом фтора в структуре [Y. Zhou, J. Wang, Z. Gu, S. Wang, W. Zhu,  V.A. Soloshonok, K. Izawa, H. Liu. Next Generation of Fluorine-Containing Pharmaceuticals, Compounds Currently in Phase II-III Clinical Trials of Major Pharmaceutical Companies: New Structural Trends and Therapeutic Areas // Chem. Rev., 2016, Vol. 116, P. 422-518].
V.A. Soloshonok, K. Izawa, H. Liu. Next Generation of Fluorine-Containing Pharmaceuticals, Compounds Currently in Phase II-III Clinical Trials of Major Pharmaceutical Companies: New Structural Trends and Therapeutic Areas // Chem. Rev., 2016, Vol. 116, P. 422-518].
Успешная химическая модификация изначально довольно токсичной и неэффективной салициловой кислоты позволила получить целый ряд лекарственных препаратов, таких как салицилат натрия, метилсалицилат, троламин салицилат, салсалат, аспирин и др. Благодаря триаде противовоспалительного, жаропонижающего и анальгетического действия салицилаты имеют место в реестре клинически применяемых нестероидных противовоспалительных препаратов (НПВП) [S.C. Sweetman. Martindale: The Complete Drug Reference, Pharmaceutical Press, London - Chicago, 2009. pp. 20-25]. При этом установлено, что медные(II) комплексы салициловой и ацетилсалициловой кислот обладают более сильной противовоспалительной активностью в сочетании с низкой ульцерогенностью по сравнению со свободными лигандами [J.R.J. Sorenson, W. Hangarter, Treatment of rheumatoid and degenerative diseases with copper complexes // Inflammation, 1977, Vol. 2, P. 217-238; T. Jacka, C.C.A. Bernard, G. Singer. Copper salicylate as an anti-inflammatory and analgesic agent in arthritic rats // Life Sci., 1983, Vol. 32, P. 1023-1030; Z. Korolkiewicz,  I.
I.  P. Gorczyca,
P. Gorczyca,  The pharmacologic activity of complexes and mixtures with copper and salicylates or aminopyrine following oral dosing in rats // Agents Actions., 1989, Vol. 26, P. 355-359].
The pharmacologic activity of complexes and mixtures with copper and salicylates or aminopyrine following oral dosing in rats // Agents Actions., 1989, Vol. 26, P. 355-359].
Салицилат меди(II) входит в состав различных фармацевтических композиций, запатентованных для лечения инфекций кожи и слизистых оболочек [A.A. Shah. Compositions for treating skin and mucous membrane infections // Patent US 20190054011 Al, 2019; J. Spurge. Composition for treating skin lesions // Patent US 9107811 B2, 2015], включая вирусные инфекции, вызванные Herpes simplex [J. Spurge. Composition comprising synergistic combination of copper compound and hypericum perforatum extract for treating skin lesions // Patent US 20110064826 Al, 2011; J. Carter. Pharmaceutical composition comprising copper, salicylic acid, vitamin С and zinc for the treatment of different diseases such as bacterial or viral infection // PCT Int. Appl. WO 2002080942 Al, 2002]. Медный комплекс салициловой кислоты входит также в рецептуру, обладающую антибактериальным действием по отношению propionibacteriae [S. Scott, S.P. Jones. Antibacterial formulations against propionibacteriae comprising salicylic acid for treating acne // Patent GB 2463566 A, 2010], против грамотрицательных и грамположительных бактерий [P.W. Beerse, К.A. Biedermann, S.H. Page, M.J. Mobley, J.M. Morgan. Antimicrobial compositions for skin, comprising a benzoic acid analog and a metal salt // PCT Int. Appl. WO 2001028338 A2, 2001], против онихомикоза [К.Т. Zeiler. Antifungal nail composition containing a copper salt // PCT Int. Appl. WO 2002039963 A1, 2002]. Описан эффективный, простой, недорогой и безопасный способ для лечения розацеи, акне и бородавок различной этиологии путем местного применения металлокомплексов, включающих салицилаты цинка, магния, железа, меди и др. [W.L. Chiou. Compositions and methods for topical treatment of skin infection using polyvalent metal compounds // Patent US 20050123620 A1, 2005].
Смешанные Cu(II), Ni(II), Co(II) и Fe(II) комплексы салициловой кислоты с 8-гидроксихинолином, никотиновой кислотой, пиридином и β-пиколином показали выраженное антимикробное и фунгицидное действие [Y. Anjaneyulu, R.Y. Swamy, R.P. Rao. Studies on some mixed ligand complexes of copper(II) with 8-hydroxyquinoline and salicylic acids. Relation between stability constants and antimicrobial activity // Journal of the Indian Chemical Society, 1985, Vol. 62, Iss. 5, P. 346-351; C.P. Saxena, S.H. Mishra, P.V. Khadikar. Studies on the antifungal activity of some mixed ligand metallic complexes of salicylic acid // Current Science, 1979, Vol. 48, Iss. 1, P. 20-22]. При этом медные комплексы оказались наиболее активными.
Наиболее близким к нашему изобретению частично можно признать способ получения смешанных комплексов салицилатов меди(II) и марганца(II) с 2,2'-бипиридином или 1,10-фенантролином, заключающийся в получении соли путем взаимодействия салициловой кислоты и гидроксидов металлов при кипячении в этаноле. Выделенные и очищенные соли нагревают в этаноле с лигандами 2,2'-бипиридиновго типа с образованием целевых смешанных комплексов салицилатов переходных металлов. Синтезированные комплексы обладают способностью ингибировать патогенные дрожжи Candida albicans. При этом наибольшую anti-Candida активность показал марганцевый комплекс с 1,10-фенантролином [М. Geraghty, V. Sheridan, М. McCann, М. Devereux, V. McKee. Synthesis and anti-Candida activity of copper(II) and manganese(II) carboxylate complexes // Polyhedron, 1999, Vol. 18, P. 2931-2939] (прототип).
Недостатками метода являются:
- необходимость промежуточного выделения и очистки солей салицилатов;
- необходимость синтеза комплексов в органических растворителях;
- синтезированные комплексы на основе салициловой кислоты обладают только одним видом противогрибковой активности.
Данных о синтезе металлокомплексов на основе полифторсалициловых кислот и изучении их биоактивности в литературе не обнаружено.
Объект изобретения
Задача изобретения: синтезировать фторсодержащие соединения, имеющие высокую антибактериальную активность против ряда инфекций из доступных исходных материалов в мягких условиях с высокими выходами.
Поставленная задача решается путем получения на первой стадии солей переходных металлов при обработке водных растворов трифтор-(1а) и тетрафторсалициловых (1b) кислот водными растворами ацетата меди(II) или кобальта(II) в эквимолярном соотношении. Полученную реакционную массу перемешивают при комнатной температуре не менее 1 часа. Полученные соли (2а,b, 3) три- и тетрафторсалициловых кислот пригодны для проведения последующего синтеза без дополнительной очистки. Исходные три- (1а) и тетрафторсалициловые (1b) кислоты получают по методике, описанной в литературе [E.V. Shchegol'kov, I.V. Shchur, Y.V. Burgart, V.I. Saloutin, S.Y. Solodnikov, O.P. Krasnykh, M.A. Kravchenko. A convenient and efficient approach to polyfluorosalicylic acids and their tuberculostatic activity // Bioorg. Med. Chem. Lett., 2016, Vol. 26, P. 2455-2458].
На второй стадии полученные водные растворы солей (2а,b, 3b) смешивают с 1,10-фенантролином (4) и выдерживают реакционную массу при температуре 80-90°С не менее 2 часов. После охлаждения смеси до комнатной температуры выпавшие металлокомплексы (5а,b, 6) отфильтровывают и промывают водой и/или этиловым спиртом.
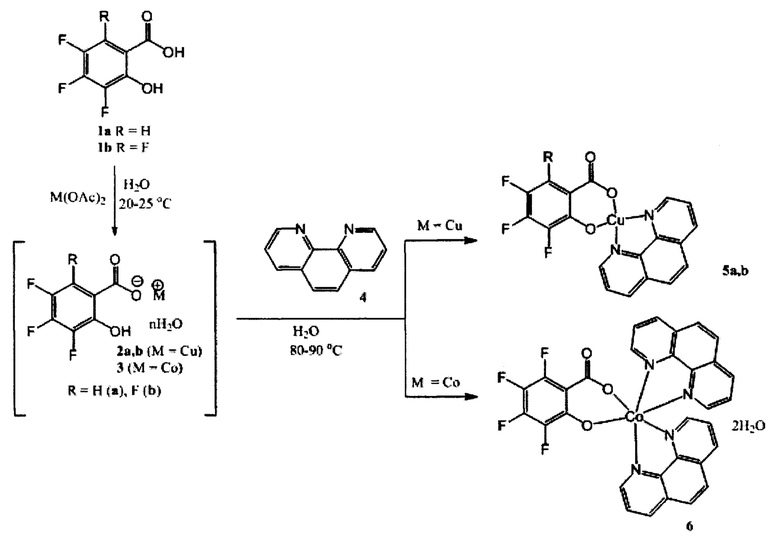
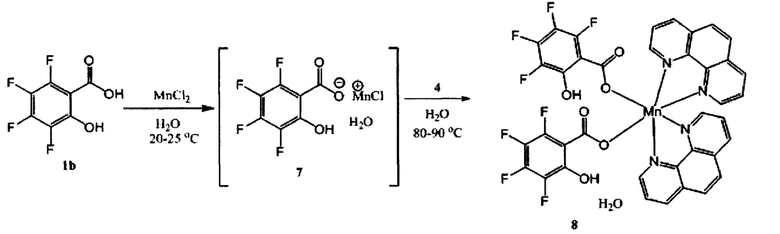
Синтез марганцевого металлокомплекса (8) основан на промежуточном получении марганцевой соли тетрафторсалциловой кислоты (7) из кислоты (1b) и хлорида марганца (II). Последующая обработка соли 1,10-фенантролином (4) при нагревании в воде приводит к целевому продукту (8). Процедура выделения и очистки комплекса (8) аналогична продуктам (5а,b, b).
Анализ целевых соединений проводят с использованием элементного анализа (C,H,N) на автоматическом анализаторе Perkin-Elmer РЕ-2400 Series II. Содержание фтора в комплексах определяют спектрофотометрическим методом.
ПРИМЕР 1
К раствору трифторсалициловой кислоты (1а) 0.96 г (5 ммоль) в 10 мл воды прибавляют раствор ацетата меди (II) моногидрата 1.00 г (5 ммоль) в 10 мл воды. Реакционную смесь перемешивают при комнатной температуре в течение 1 часа. К полученному водному раствору 3,4,5-трифторсалицилата меди (2а) добавляют 1.80 г (10 ммоль) 1,10-фенантролина (4) и реакционную массу нагревают при 80-90°С в течение 3 часов. Выпавший осадок фильтруют, промывают этанолом (20 мл) и водой (20 мл), высушивают. В результате получают 3,4,5-трифтор-2-гидроксибензоато-к2O-1,10-фенантролин-к2N меди(II) (5а) в виде сине-зеленого порошка. Выход 1.87 г (91%).
Т. пл. >250°С
Элементный анализ для C19H9CuF3N2O3 (433.82):
Вычислено (%): С, 52.60; Н, 2.09; N, 6.46; F, 13.14.
Найдено (%): С, 52.52; Н, 2.10; N, 6.60; F, 12.85.
ПРИМЕР 2
К раствору тетрафторсалициловой кислоты (1b) 1.05 г (5 ммоль) в 10 мл метанола прибавляют раствор ацетата меди (II) моногидрата 1.00 г (5 ммоль) в 10 мл воды. Реакционную смесь перемешивают при комнатной температуре в течение 1 часа. К полученному водному раствору 2,3,4,5-тетрафторсалицилата меди (2b) добавляют 1.80 г (10 ммоль) 1,10-фенантролина (4) и реакционную массу нагревают при 80-90°С в течение 3 часов. Выпавший осадок фильтруют, промывают этанолом (20 мл) и водой (20 мл), высушивают. В результате получают 2,3,4,5-тетрафтор-6-гидроксибензоато-к2O-1,10-фенантролин-к2N меди(II) (5b) в виде зеленого порошка. Выход 2.01 г (89%).
Т. пл. >250°С
Элементный анализ для C19H8CuF4N2O3 (451.82):
Вычислено (%): С, 50.51; Н, 1.78; N, 6.20; F, 16.82.
Найдено (%): С, 50.37; Н, 1.89; N, 6.23; F, 16.61.
ПРИМЕР 3
К раствору тетрафторсалициловой кислоты (1b) 1.05 г (5 ммоль) в 10 мл метанола прибавляют раствор ацетата кобальта (II) тетрагидрата 1.25 г (5 ммоль) в 10 мл воды. Реакционную смесь перемешивают при комнатной температуре в течение 3 часов. К полученному водному раствору 2,3,4,5-тетрафторсалицилата кобальта (3) добавляют 1.80 г (10 ммоль) 1,10-фенантролина (4) и реакционную массу нагревают при 80-90°С в течение 2 часов. Выпавший осадок фильтруют, промывают водой (20 мл) и высушивают. В результате получают 2,3,4,5-тетрафтор-6-гидроксибензоато-к2O-бис(1,10-фенантролин-к2N) кобальта(II) дигидрат (6) в виде желтого порошка. Выход 2.22 г (67%).
Т. пл. >250°С
Элементный анализ для C31H20CoF4N4O5 (663.45):
Вычислено (%): С, 56.12; Н, 3.04; N, 8.44; F, 11.45.
Найдено (%): С, 56.42; Н, 2.76; N, 8.53; F, 11.14.
ПРИМЕР 4
К раствору тетрафторсалициловой кислоты (1b) 1.05 г (5 ммоль) в 10 мл воды прибавляют раствор хлорида марганца (II) тетрагидрата 1.00 г (5 ммоль) в 10 мл воды. Реакционную смесь перемешивают при комнатной температуре в течение 1 часа. К полученному водному раствору 2,3,4,5-тетрафторсалицилата марганца (7) добавляют 1.80 г (10 ммоль) 1,10-фенантролина (4) и реакционную массу нагревают при 80-90°С в течение 3 часов. Выпавший осадок фильтруют, промывают этанолом (20 мл) и водой (20 мл), высушивают. В результате получают бис(2,3,4,5-тетрафтор-6-гидроксибензоато-к2O)-бис(1,10-фенантролин-k2N)марганца(II) гидрат (8) в виде светло-желтых кристаллов. Выход 2.93 г (69%).
Т. пл. 211-212°С
Элементный анализ для C38H18MnF8N4O7 (849. 48):
Вычислено (%): С, 53.73; Н, 2.14; N, 6.60; F, 17.89.
Найдено (%): С, 53.61; Н, 2.44; N, 6.77; F, 17.80.
Сведения, подтверждающие возможность осуществления изобретения
Список условных сокращений
АТСС - American Type Culture Collection (Американская коллекция типовых культур)
NCTC - National Collection of Type Cultures (Culture Collection of Puhlic Health England)
ГКПМ - Государственная коллекция патогенных микроорганизмов, Россия
SPEC - Спектиномицин (Spectinomycin), антибиотик класса аминоциклитолов. Механизм действия - ингибирует синтез белка в бактериальной клетке, путем связывания с 30S субъединицей рибосомы. Может нарушать функции и структуру 40 цитоплазматических мембран.
МИК - минимальная ингибирующая концентрация, мкг/мл
Контрольные штаммы:
Neisseria gonorrhoeae NCTC 12700/АТСС 49226;
Грамотрицательные штаммы (Энтеробактерии):
Escherichia coli АТСС 8739 (Е. coli)
Klebsiella pneumoniae АТСС 13883 (Kl. pneum.)
Citrobacter braakii ATCC 101/57 (C. braakii)
Shigella flexneri 1a8516 (Sh. flexneri)
Serratia marcescens ATCC 13880 (Ser. marces.)
Неферментатирующие грамотрицательные бактерии:
Pseudomonas aeruginosa ATCC 9027 (P. aerug.)
Грамположительные кокки:
Staphylococcus aureus ATCC 25923 / NCTC 12981 (F-49) (St. aureus)
Staphylococcus aureus MRSA NCTC 12493 (St. aureus MRSA) - штамм золотистого стафилококка резистентный к Метициллину - бета-лактамному антибиотику, пенициллинового ряда.
Изучение антибактериальной активности in vitro заявляемых соединений (5а,b, 6b, 8b).
Оценку чувствительности микроорганизмов к антимикробным препаратам проводят методом последовательных двукратных микроразведений - референсным методом, регламентированным международным стандартом ISO 20776-1:2006. В Российской Федерации действует Национальный Стандарт ГОСТ Р ИСО 20776-1-2010, идентичный международному стандарту. Растворитель химических соединений - ДМСО, разбавители дистиллированная стерильная вода (для инъекций), ростовая, среда. Критерии интерпретации результатов: новые химические соединения рассматривают перспективными для дальнейшего изучения, если значения МИК in vitro для контрольных штаммов не превышают 10-20 мкг/мл [Руководство по проведению доклинических исследований лекарственных средств. Часть первая / Под ред. А.Н. Миронова. - М.: Гриф и К, 2012. - 944 с. Порядок исследования при определении спектра антимикробного действия и активности нового соединения in vitro. С. 511-513].
Антибактериальную активность химических соединений в отношении облигатного патогена N. gonorrhoeae определяют методом двукратных серийных разведений в агаре (золотой стандарт). В качестве ростовой среды используют питательную среду - гонококковый агар с 1% ростовой добавкой (например, «Комплегон», Россия). Разведения химических соединений в агаре проводят в 24 луночных планшетах, рабочий объем лунки 2 мл. Для каждого химического соединения готовят не менее 12 точек двукратных серийных разведений: 250 мкг/мл - 0.122 мкг/мл. Посевная доза (конечная концентрация) инокулюма из суточной культуры N. gonorrhoeae - 105 КОЕ/мл. Инкубируют планшеты при условиях Т=37°С, [CO2=5%]. Оценку результатов проводят визуально через 18-24 часа, по отсутствию роста на агаре колоний N. gonorrhoeae [CLSI, 2014].
Исследование антибактериальной активности соединений против клинически значимых патогенных и условно-патогенных микроорганизмов осуществляют путем последовательного разбавления бульона Мюллера-Хинтон (например, Mueller Hinton Broth, Becton Dickinson, США). Двукратные серийные разведения химических соединений проводят в стерильных 96-луночных планшетах. Посевная доза соответствующих штаммов - 50 мкл инокулюма в концентрации 106 КОЕ/мл. Через 18-24 часа инкубации планшет в термостате при 37°С, проводят визуальную оценку результатов: по наличию лунок с ингибированием роста м/о (прозрачной ростовой средой). Концентрация химического соединения в первой лунке ингибирования роста соответствует МИК против данного штамма.
В качестве референтного соединения использовано лекарственное средство Спектиномицин (Sigma-Aldrich, USA) формулы (SPEC):
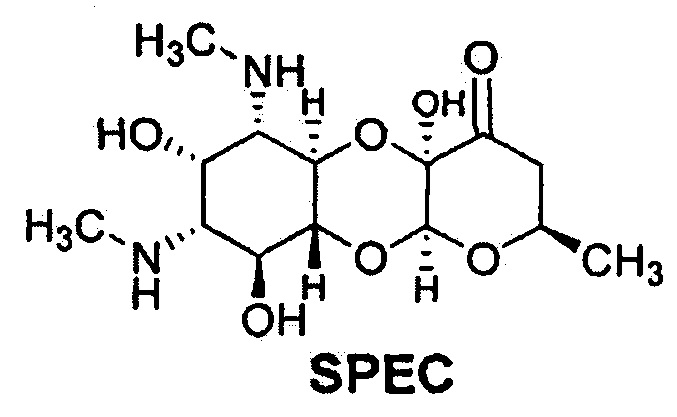
Спектиномицин применяют в медицинской практике для лечения острого гонококкового уретрита, простатита и проктита у мужчин, острого гонококкового цервицита и проктита у женщин, вызванных чувствительными штаммами Neisseria gonorrhoeae, при непереносимости или неэффективности бета-лактамных антибиотиков.
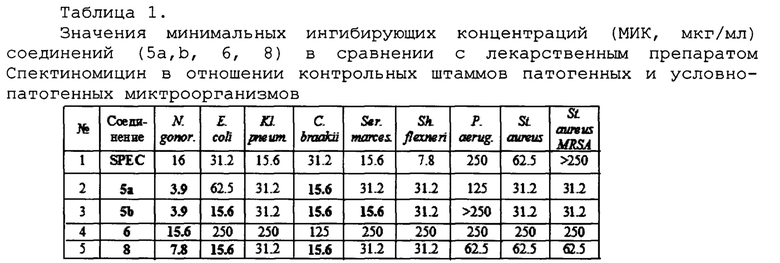
Для изучения антибактериальной активности соединений (5а,b, 6, 8) проводили определение МИК относительно референтных штаммов Neisseria gonorrhoeae NCTC12700 / АТСС49226 и других 8 патогенных и условно-патогенных клинически-значимых микроорганизмов из международной коллекции АТСС и российской коллекции ГКПМ. Результаты исследований представлены в таблице 1.
Соединения с общей формулой (I) проявили высокую активность в отношении Neisseria gonorrhoeae NCTC12700/ATCC49226. При этом соединение 5b показало активность на уровне референсного соединения Спектомицина, соединение 8 по этому виду активности превосходит препарат сравнения в 2 раза, а комплексы 5а, 5b и 6 - в 4 раза.
Соединение (5а) показало антибактериальную активность в отношении контрольного штамма энтеробактерий Citrobacter braakii АТСС 101/57, превосходящую действие Спектомицина в 2 раза.
Соединение (5b) показало антибактериальную активность в отношении контрольных штаммов энтеробактерий: Escherichia coli АТСС 8739, Citrobacter braakii АТСС 101/57, Serratia marcescens ATCC 13880, равную или превосходящую действие Спектомицина в 2 раза.
Соединение (8) показало антибактериальную активность в отношении контрольных штаммов энтеробактерий: Escherichia coli АТСС 8739, Citrobacter braakii АТСС 101/57, превосходящую действие Спектомицина в 2 раза.
Таким образом, нами предложен эффективный способ получения новых комплексов переходных металлов на основе полифторсалициловых кислот и 1,10-фенантролина, обладающих широким спектром антибактериальной активности в отношении кокковых инфекций. Преимуществом данного способа являются:
1. Доступность и низкая стоимость исходных реагентов.
2. Однореакторный способ получения, мягкие условия проведения реакции, не требующие дорогостоящего оборудования, использование воды в качестве растворителя.
3. Высокие выходы целевых комплексов (67-91%) и простота их очистки и выделения.
Наибольшим спектром активности обладает 2,3,4,5-тетрафтор-6-гидроксибензоато-к2O-1,10-фенантролин-к2N меди(II) (5b), в связи с чем это соединение наиболее перспективно для использования в клинической медицине для лечения заболеваний мочеполовой системы и гнойно-воспалительных инфекций кожи и слизистых оболочек.
Наличие причинно-следственной связи между совокупностью существенных признаков заявляемых объектов и достигаемых технических результатов показано в таблицах 2 и 3.
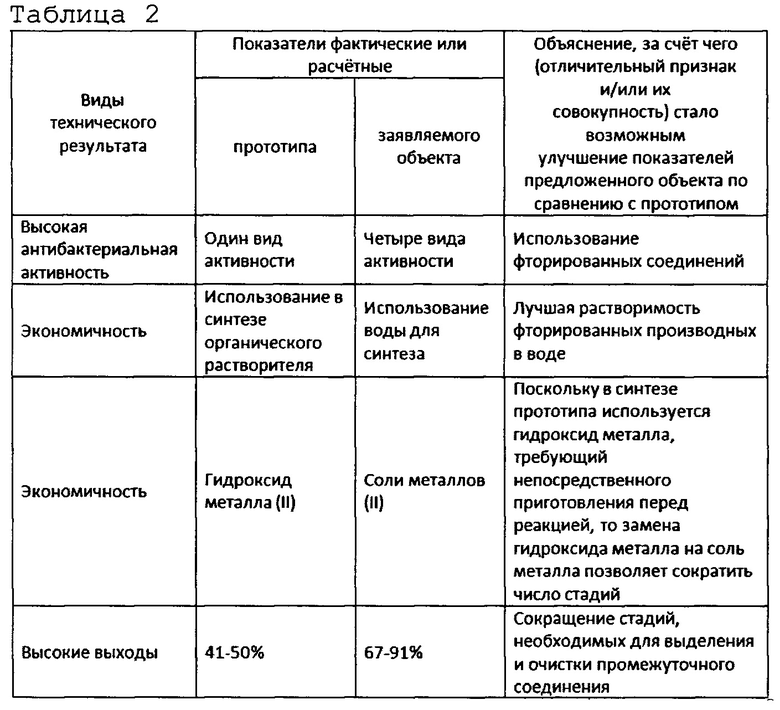
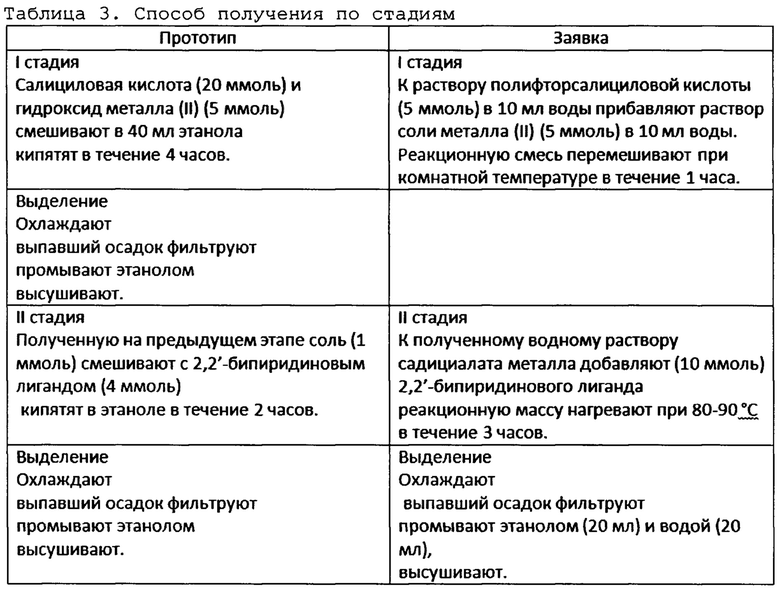
| название | год | авторы | номер документа |
|---|---|---|---|
| Смешанные металлокомплексы на основе 5-(4-метилфенил)-2,2'-бипиридина и (тетрафтор)салициловых кислот, обладающие антибактериальной и фунгистатической активностью | 2020 |
|
RU2737435C1 |
| 5-Арилзамещенный 4-(5-нитрофуран-2-ил)пиримидин, обладающий широким спектром антибактериальной активности, способ его получения и промежуточное соединение, обладающее широким спектром антибактериальной активности | 2016 |
|
RU2626647C1 |
| N-Арил-4-(5-нитрофуран-2-ил)-пиримидин-5-амины, проявляющие антибактериальную активность, и способ их получения | 2017 |
|
RU2642428C1 |
| Разнолигандные комплексы меди(II) с 1H-тетразол-5-уксусной кислотой и производными олигопиридина, проявляющие цитотоксичную активность | 2023 |
|
RU2818953C1 |
| Ди[(фуран-3-карбоксилато-О)-(2,9-диметил-1,10-фенантролин-N,N')-медь(II)], обладающий антипролиферативной и антимикобактериальной активностью | 2023 |
|
RU2815425C1 |
| Хиральные комплексы меди(II) с терпеновыми производными этилендиамина и их применение в качестве средства, обладающего антибактериальной и противогрибковой активностью | 2020 |
|
RU2756043C1 |
| Способ получения тетра-1,10-фенантролин-μ-фумарат-димеди(II) хлорида | 2019 |
|
RU2702119C1 |
| СЕЛЕКТИВНЫЕ АНТИБАКТЕРИАЛЬНЫЕ АГЕНТЫ, ПРЕДСТАВЛЯЮЩИЕ СОБОЙ 3-(АЗОЛ-1-ИЛ)-6-АМИНОЗАМЕЩЕННЫЕ 1,2,4,5-ТЕТРАЗИНЫ | 2017 |
|
RU2642882C1 |
| 4-ИЗОПРОПИЛ-6-R-ИМИДАЗО[1,2-b][1,2,4,5]ТЕТРАЗИН-3(4H)-ОНЫ, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ NEISSERIA GONORRHOEAE | 2020 |
|
RU2754554C1 |
| Фосфониевые соли на основе салициловой и ацетилсалициловой кислот, обладающие антибактериальной и антиоксидантной активностью" | 2019 |
|
RU2704025C1 |
Изобретение относится к новым металлокомплексам на основе полифторсалицилатов и 1,10-фенантролина общей формулы I
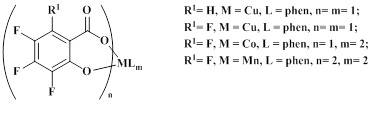 (I),
(I),
где R1 = H, F; M = Cu(II), Co(II), Mn(II); L = phen (1,10-фенантролин), n = 1-2, m = 1-2. Также предложен способ их получения. Соединения формулы (I) обладают широким спектром антибактериальной активности в отношении инфекций, вызванных гонококками и/или Escherichia coli, Citrobacter braakii, Staphylococcus aureus, Serratia marcescens. 2 н.п. ф-лы, 3 табл., 4 пр.
1. Металлокомплексы на основе полифторсалицилатов и 1,10-фенантролина общей формулы I, обладающих антибактериальной активностью:
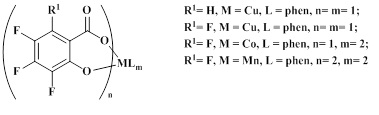 ,
,
где R1=H, F; M = Cu(II), Co(II), Mn(II); L = phen (1,10-фенантролин), n= 1-2, m = 1-2.
2. Способ получения металлокомплексов по п.1, содержащий следующие стадии:
- перемешивание при комнатной температуре водного раствора полифторсалициловой кислоты и соли металла, выбранной из группы, содержащей ацетат меди (II), ацетат кобальта (II), хлорид марганца (II), в эквимолярном соотношении, до выпадения промежуточного комплекса в виде осадка;
- смешивание полученного промежуточного комплекса с 1,10-фенантролином с последующим нагреванием при перемешивании при температуре по меньшей мере 80°С, не допуская кипения, до изменения цвета;
- охлаждение полученного металлокомплекса до выпадения осадка, фильтрация, промывание осадка этанолом, высушивание.
| GERAGHTY M | |||
| et al, Synthesis and anti-Candida activity of copper(II) and manganese(II) carboxylate comlexes, Polyhedron, 1999, v | |||
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| Приспособление для предохранения примуса или тому подобных ламп | 1924 |
|
SU2931A1 |
| SHCHEGOL'KOV E.V | |||
| et al, Polyfluorinated salicylic acid derivatives as analogs of known drugs: Synthesis, molecular docking and biological evaluation, Bioorg | |||
| Med | |||
| Chem., 2017, v | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| Огнетушитель | 0 |
|
SU91A1 |
Авторы
Даты
2019-11-20—Публикация
2019-06-20—Подача