Изобретение относится к синтезу новых химических соединений - хиральных комплексов меди(II) с терпеновыми производными этилендиамина, обладающих высокой антибактериальной и противогрибковой активностью.
Согласно литературным данным, металлокомплексные соединения являются перспективными антимикробными препаратами [Nasiri Sovari, S., Zobi, F. Recent Studies on the Antimicrobial Activity of Transition Metal Complexes of Groups 6–12. Chemistry, 2020, 2(2), 418–452. doi:10.3390/chemistry2020026; Frei, A. Metal Complexes, an Untapped Source of Antibiotic Potential? Antibiotics, 2020, 9(2), 90. https://doi.org/10.3390/antibiotics9020090]. Интерес исследователей к комплексным соединениям меди связан с тем фактом, что медь является важным биометаллом, который участвует во многих биохимических схемах. Целый ряд обзоров посвящен анализу результатов исследования комплексов меди в качестве потенциальных терапевтических агентов [Duncan, C., White, A. R. Copper complexes as therapeutic agents. Metallomics, 2012, 4(2), 127–138. https://doi:10.1039/c2mt00174h; Santini, C., Pellei, M., Gandin, V., Porchia, M., Tisato, F., Marzano, C. Advances in Copper Complexes as Anticancer Agents. Chem. Rev. 2014, 114, 815−862. https://dx.doi.org/10.1021/cr400135x].
Известны комплексы меди с органическими N-донорными лигандами: структура I [Abdel-Rahman, L.H., Adam, M.S.S., Abu-Dief, A.M. Synthesis, theoretical investigations, biocidal screening, DNA binding, in vitro cytotoxicity and molecular docking of novel Cu (II), Pd (II) and Ag (I) complexes of chlorobenzylidene Schiff base: Promising antibiotic and anticancer agents. Appl. Organom. Chem. 2018, 32, e4527. https://doi.org/10.1002/aoc.4527], структура II [Kalarani, R., Sankarganesh, M., Kumar, G. G. V., Kalanithi, M. Synthesis, spectral, DFT calculation, sensor, antimicrobial and DNA binding studies of Co(II), Cu(II) and Zn(II) metal complexes with 2-amino benzimidazole Schiff base. Journal of Molecular Structure, 2020, 127725. doi:10.1016/j.molstruc.2020.127725] и структура III [Satheesh, C.E., Kumar, P.R., Shivakumar, N., Lingaraju, K., Krishna, P.M., Rajanaika, H., Hosamani, A. Synthesis, structural characterization, antimicrobial and DNA binding studies of homoleptic zinc and copper complexes of NO Schiff bases derived from homoveratrylamine // Inorganica Chimica Acta. 2019. V. 495. 118929. https://doi.org/10.1016/j.ica.2019.05.028)], являются структурными аналогами полученных новых соединений, проявляют антибактериальную активность против грамположительных бактерий (например, Staphylococcus aureus), грамотрицательных бактерий (в частности Escherichia coli), противогрибковую – против мицелиальных грибков, грибков брожения, в том числе штамма Candida albicans.
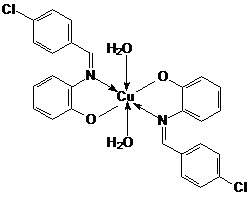 I
I 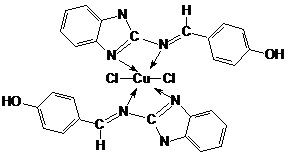 II
II  III
III
Изобретение направлено на расширение арсенала и получение новых медьсодержащих терпеновых производных этилендиамина, которые могут быть использованы в качестве средства, обладающего антибактериальной и противогрибковой активностью. Представленные соединения одни из первых металлсодержащих веществ среди соединений подобной структуры. В этом состоит технический результат.
Технический результат достигается тем, что новые хиральные комплексы меди(II) с терпеновыми производными получены в виде индивидуальных диастереомеров 1-4:

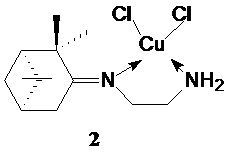


Полученные соединения 1-4 применяют в качестве антибактериального и противогрибкового средства.
Получение хиральных комплексов меди(II) с терпеновыми производными этилендиамина осуществляется следующим образом.
Лиганды - терпеновые производные этилендиамина - имеют комбинированную структуру: содержат хиральный терпеновый фрагмент - элемент, входящий в состав природных терпеноидов, и этилендиаминовый блок, отвечающий за хелатирование с металлом. Бифункциональность этилендиамина позволяет вводить с помощью классических методик органического синтеза (конденсация с карбонильными соединениями, последующее восстановление иминов и др.) необходимые структурные фрагменты, отвечающие за фармакофорные свойства, обеспечивающие гидрофильность (или гидрофобность), биодоступность препарата. Возможно введение различных по строению терпеноидных групп (например, борнановых – структура 1 и 4 или пинановых – структуры 2 и 3). Полученные лиганды являются универсальными, позволяющими получать на их основе хелатные металлокомплексы различных переходных металлов (медь, палладий, цинк, кобальт, никель и др.). Новые хиральные комплексы меди 1-4 получены в виде индивидуальных диастереомеров.
Ниже приведена схема 1, демонстрирующая получение новых соединений:
Схема 1

Реагенты и условия: i. H2N(CH2)2NMe2, PhH, 80 °C, 8 ч; ii. NaBH4, EtOH, 24 °C, 8 ч; iii. CuCl2×2H2O, MeOH, 24 °C, 8 ч.
(E,Z)-N1,N1-Диметил-N2-{(1R,4S)-2-оксо-1,7,7-триметилбицикло[2.2.1]гептан-3-илиден}этан-1,2-диамин (L1):
Раствор 0.56 г (3 ммоль) (-)-(1R,4S)-камфорхинона и 0.30 г (3 ммоль) N,N-диметилэтилендиамина в 20 мл абсолютного бензола кипятили 8 часов. Растворитель удаляли в вакууме, из остатка методом колоночной хроматографии на SiO2 (элюент – CHCl3-MeOH) выделили желтое маслообразное вещество, представляющее собой смесь изомеров (E)-L1 и (Z)-L1. Общий выход 0.59 г (84 %). ИК-спектр, ν, см-1: 1751 (С=О), 1672 (C=N). Спектр ЯМР 1Н (300 МГц, CDCl3, δ/м.д., J/Гц) для мажорного компонента (E)-1: 0.86 (с, 3Н, СH39), 0.99 (с, 3Н, СH38), 1.07 (с, 3Н, СH310), 1.49 (м, 1Н, Н5’), 1.58 (м, 1Н, Н6’), 1.82 (м, 1Н, Н6’’), 2.06 (м, 1H, Н5’’), 2.32 (с, 6Н, H13,14), 2.64 (м, 2Н, H12), 2.92 (д, 1Н, Н4, J 4.5), 3.66 (м, 2Н, H11). Спектр ЯМР 13С (75 МГц, CDCl3, δ, м.д.): 9.02 (С10), 17.71 (С8), 20.78 (С9), 23.75 (С5), 30.25 (С6), 44.19 (С7), 45.61 (2С13,14), 48.74 (С4), 52.12 (С11), 57.96 (С1), 59.30 (С12), 172.26 (С3), 205.94 (С2).
N1,N1-Диметил-N2-{(1R,2S,3R,4S)-2-окси-1,7,7-триметилбицикло[2.2.1]гептан-3-ил}этан-1,2-диамин (L2):
Раствор 0.50 г (2 ммоль) имина (смесь изомеров (E)-L1+(Z)-L1) в 10 мл абсолютного EtOН добавляли по каплям к интенсивно перемешиваемому раствору 0.32 г (8 ммоль) NaBH4 в 10 мл абсолютного EtOН в течение часа. Полученную суспензию перемешивали при комнатной температуре 8 часов. Реакционную смесь разбавили водой (10 мл), добавили 5%-ный водный раствор NaOH (15 мл) и диамин экстрагировали хлороформом. Органический раствор высушивали над K2CO3. Растворитель удаляли в вакууме, из остатка методом колоночной хроматографии на SiO2 (элюент CHCl3-MeOH) выделили соединение L2 в виде желтого масла. [α]D −8.7 (с 1; СНСl3). Выход 0.42 г (61 %). ИК-спектр, ν, см-1: 3208 шир. (OH, NH). Спектр ЯМР 1Н (300 МГц, CDCl3, δ/м.д., J/Гц): 0.78 (с, 3Н, СH39), 0.95 (с, 3Н, СH38), 1.06 (с, 3Н, СH310), 1.01 (м, 1Н, Н6’), 1.02 (м, 1Н, Н5’), 1.41 (м, 1Н, Н6’’), 1.62 д (1Н, Н4, J 4.2), 1.69 (м, 1H, Н5’’), 2.23 (с, 6Н, H13,14), 2.54 (м, 2Н, H12), 2.62 м (1Н, Н3), 2.84 (м, 2Н, H11), 3.45 д (1Н, Н2, J 7.0). Спектр ЯМР 13С (75 МГц, CDCl3, δ, м.д.): 11.54 (С10), 21.33 (С8), 21.90 (С9), 27.35 (С5), 33.17 (С6), 45.20 (2С13,14), 46.56 (С7), 48.14 (С4), 48.80 (С11), 52.45 (С1), 58.81 (С12), 66.65 (С2), 79.41 (С3).
Дихлоро{N1,N1-Диметил-N2-[(1R,2S,3R,4S)-2-окси-1,7,7-триметилбицикло[2.2.1]гептан-3-ил]этан-1,2-диамин-N1,N2,O}медь(II) (1):
К раствору CuCl2×2H2O (0.3 ммоль) в 5 мл МеОН прилили раствор лиганда L2 (0.3 ммоль) в 5 мл MeOH. Реакционную смесь перемешивали при комнатной температуре в течение 8 часов. После удаления растворителя и перекристаллизации из смеси ацетон – диэтиловый эфир получили комплекс меди 1 в виде кристаллов зеленого цвета. Выход 0.12 г (66 %). ИК-спектр, ν, см-1: 3228 шир. (OH), 3184 (NH). [α]D ‒207.1 (c 0.04, EtOH). Найдено, %: C 44.86; H 7.53; N 7.47. C14H28N2ОCuCl2. Вычислено, %: C 44.50; H 6.81; N 7.38. Спектры ЯМР 1Н и 13С синтезированных соединений регистрировали на спектрометре «Bruker Avance II 300» (300.17 и 75.5 МГц). Соотнесение сигналов 1H выполняли с помощью методики NOESY, соотнесение сигналов 13С – с помощью спектров ЯМР 13С в режиме J-модуляции и методик HSQC, HMBC. ИК-спектры диффузного отражения записывали на ИК-Фурье-спектрометре «Shimadzu IR Prestige 21» в таблетках с KBr (металлокомплексы) и в тонком слое (лиганды). Элементный анализ выполняли на автоматическом анализаторе «vario Micro cube» в режиме CHN. Протекание реакций контролировали с использованием метода ТСХ на пластинах «Sorbfil» (ООО «ИМИД»); продукты реакций обнаруживали обработкой пластин раствором нингидрина (3 г нингидрина, 50 мл EtOH) и парами йода. Температуры плавления определяли на приборе «Sanyo Gallenkamp MPD350» и не корректировали. Угол оптического вращения измеряли на автоматическом цифровом поляриметре Optical Activity polar 3001 (λ 589 нм).
В качестве стартового терпеноида для синтеза лигандов использовали (-)-(1R,4S)-камфорхинон оптической чистоты не менее 96 %. При конденсации камфорохинона с N,N-диметилэтилендиамином образуется смесь изомерных иминов (E)-L1+(Z)-L1 в мольном соотношении 2:1 с выходом 84 %. Состав и строение продуктов реакции подтверждены данными спектроскопии ЯМР. В спектрах NOESY мажорного компонента выявлено взаимодействие протонов Н11 этилендиаминового мостика с протоном H4 терпенового цикла. Этот факт подтверждает Е-конфигурацию C=N связи. При взаимодействии смеси иминокетонов (E)-L1 и (Z)-L1 с NaBH4 идет одновременное восстановление кратных связей C=O и C=N. Реакция идет стереоселективно с образованием единственного продукта - стереоизомера (1R,2S,3R,4S)-L2 с выходом 61 %. Относительная конфигурация вновь образующихся хиральных центров в положениях 2 и 3 терпенового цикла подтверждена на основании данных спектроскопии ЯМР и РСА комплексного соединения меди (1), полученного на основе этого лиганда.
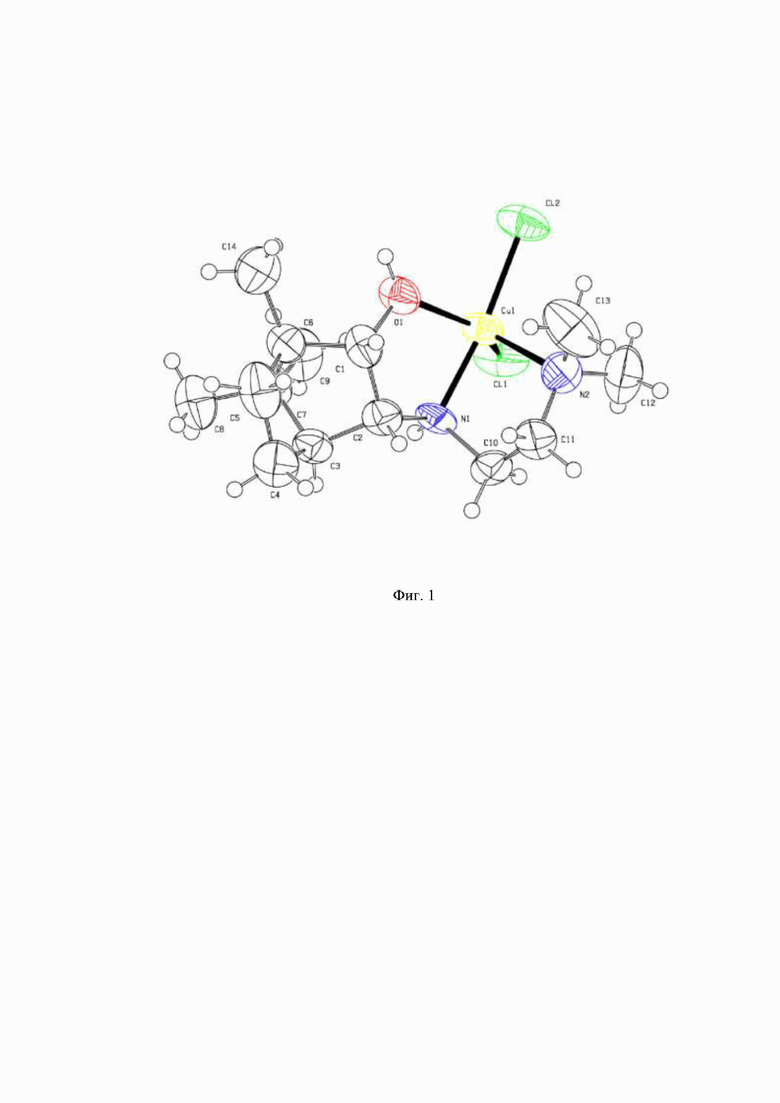
На фигуре 1 представлено соединение 1 по данным РСА в тепловых эллипсоидах 50% вероятности. Согласно данным РСА, комплексное соединение 1 кристаллизуется в нецентросимметричной пространственной группе, что подтверждает хиральность соединения. Центральный ион меди координирует два атома N, атом O группы OH тридентатного лиганда L2, а также два атома Cl (координационное число 5). В результате координационного взаимодействия иона Cu+2 с лигандом L2 замыкаются два пятичленных хелатных цикла CuC2N2 и CuC2NO. При этом происходит закрепление S-конфигурации хирального азота N1. Координационный полиэдр Cl2N2O имеет форму тригональной бипирамиды. Для синтеза комплексных соединений 2, 3 и 4 в качестве лигандов использовали терпеновые производные этилендиамина, синтез которых описан нами ранее в публикациях [Gur’eva Y.A., Alekseev I.N., Kutchin A.V., Zalevskaya O.A., Slepukhin P.A. Synthesis of new bidentate ligands-terpene derivatives of ethylenediamine and their palladium complexes // Russ. J. Org. Chem. 2016. V. 52. № 6. P. 781-784. doi: 10.1134/S107042801606004X; Gur’eva Y.A., Zalevskaya O.A., Alekseev I.N., Slepukhin P.A., Kutchin A.V. Synthesis of new chiral palladium complexes with multidentate camphor Schiff bases // Russ. J. Org. Chem. 2018. V. 54. № 9. P. 1285-1289. https://doi.10.1134/S1070428018090026; I.A. Dvornikova, E.V. Buravlev, L.L. Frolova, Yu.V. Nelyubina, I.Yu. Chukicheva, A.V. Kuchin. Synthesis of 1,2-diamine ligands based on natural monoterpenoids // Russ. J. Org. Chem. 2011. V. 47. № 8. P. 1130-1138].
Примеры, обосновывающие применение соединений 1-4 в качестве антибактериального и противогрибкового средства.
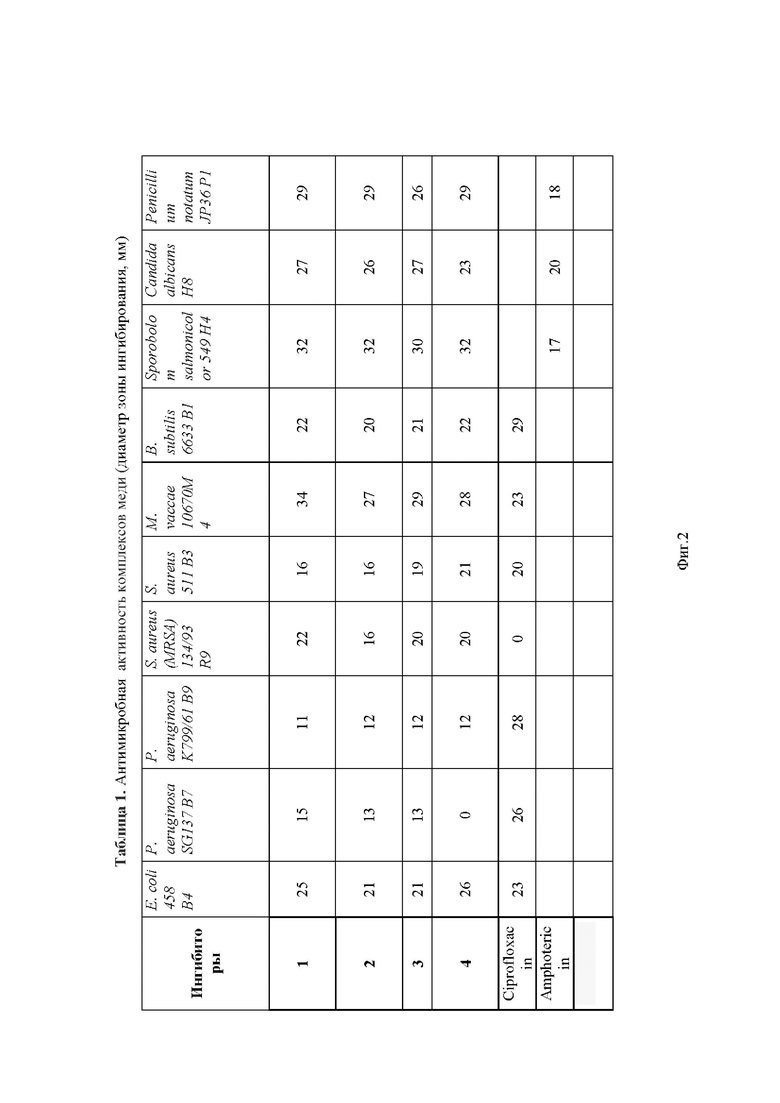
Исследована антибактериальная активность комплексов меди 1-4 в отношении штаммов грамм-отрицательных бактерий - Escherichia coli (E. Coli), Psevdomonas aeruginosa (P. Aeruginosa), грамм-положительных бактерий - Staphylococcus aureus (S. aureus), Mycobacterium vaccae (M. Vaccae), Bacillus subtilis (B. Subtilis) и противогрибковая активность в отношении штаммов грибов - Sporobolomyces salmonicolor (S. salmonicolor), Candida albicans (C. Albicans), Penicillium notatum (P. notatum).
Антибактериальную и противогрибковую активность препаратов определяли методом диффузии в агар (Agar diffusion assay) [Davis, W. W., Stout, T. R. Disc plate method of microbiological antibiotic assay. I. factors influencing variability and error. Applied Microbiology, 1971, 22, 659–665; Davis, W. W., Stout, T. R. Disc plate method of microbiological antibiotic assay. II. novel procedure offering improved accuracy. Applied Microbiology, 1971, 22, 666–670]. При изучении антибактериальной активности в качестве препарата сравнения использовали антибиотик ципрофлоксацина (Ciprofloxacin). При изучении антимикотической активности в качестве препарата сравнения использовали противогрибковый препарат амфотерицин (Amphotericin). В таблице 1 на фиг. 2 представлены полученные данные по антимикробной активности металлокомплексов 1-4.
Выявлена высокая антибактериальная активность комплексов меди 1-4 в отношении мультирезистентного штамма золотистого стафилококка S. aureus (MRSA), устойчивого в том числе к антибиотику сравнения – ципрофлоксацину. В отношении штамма S. aureus (511 B3) активность этих комплексов сопоставима с активностью ципрофлоксацина. Комплексные соединения меди 1-4 проявляет активность и в отношении мультирезистентного штамма P. Aeruginosa (SG137 B7). Комплексы меди 1-4 показали значительно более высокую противогрибковую активность в отношении штаммов Candida albicans, Sporobolomyces salmonicolor, Penicillium notatum по сравнению с активностью клинического противогрибкового препарата Амфотерицина.
| название | год | авторы | номер документа |
|---|---|---|---|
| Хиральные комплексы цинка с терпеновыми производными этилендиамина | 2022 |
|
RU2785281C1 |
| Хиральные трифторметилированные монотерпеновые тиоацетаты и тиолы пинанового ряда | 2020 |
|
RU2733369C1 |
| Хиральные трифторметилированные монотерпеновые тиоацетаты и тиолы на основе миртеналя | 2020 |
|
RU2743302C1 |
| (1-Бензил-1H-1,2,3-триазол-4-ил)метил (Z)-2-((3S,4S,8S,10S,11R,14S,16S)-16-ацетокси-3,11-дигидрокси-4,8,10,14-тетраметилгексадекагидро-17H-циклопента[a]фенантрен-17-илиден)-6-метилгепт-5-еноат, проявляющий антибактериальную и фунгицидную активность | 2022 |
|
RU2784215C1 |
| Хиральные монотерпеновые сульфинамиды | 2017 |
|
RU2646959C1 |
| Пинановые C,N-палладациклы, содержащие L-аминокислоты, и их применение в качестве средств, обладающих противоопухолевой активностью | 2022 |
|
RU2799205C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-КОМПЛЕКСОВ ДИХЛОРДИ-[(4-(БЕНЗИЛСУЛЬФАНИЛ)МЕТИЛ)-3,5-ДИМЕТИЛ-1Н-ПИРАЗОЛ]ПАЛЛАДИЯ(II) И ПЛАТИНЫ(II) | 2017 |
|
RU2672265C2 |
| N,N'-КОМПЛЕКС ДИБРОМДИ-[(4-(БЕНЗИЛСУЛЬФАНИЛ)МЕТИЛ)-3,5-ДИМЕТИЛ-1Н-ПИРАЗОЛ]ПАЛЛАДИЯ (II), ПРОЯВЛЯЮЩИЙ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2018 |
|
RU2703536C1 |
| Способ получения хиральных монотерпеновых сульфинамидов | 2017 |
|
RU2650681C1 |
| СПОСОБ БИОТРАНСФОРМАЦИИ РАСТИТЕЛЬНОГО МОНОТЕРПЕНОИДА (-)-ИЗОПУЛЕГОЛА ДЛЯ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ СОЕДИНЕНИЙ | 2022 |
|
RU2796679C1 |
Изобретение относится к новым химическим соединениям, а именно к хиральным комплексам меди(II) с терпеновыми производными этилендиамина в виде индивидуальных диастереомеров 1-4. Также предложено применение указанных соединений в качестве средства, обладающего антибактериальной и противогрибковой активностью. Технический результат состоит в расширении арсенала и получении новых медьсодержащих терпеновых производных этилендиамина, которые могут быть использованы в качестве антибактериальных и противогрибковых препаратов. 2 н.п. ф-лы, 2 ил.




1. Хиральные комплексы меди(II) с терпеновыми производными этилендиамина в виде индивидуальных диастереомеров 1-4:

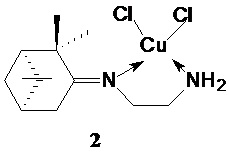

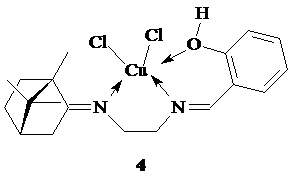
2. Применение хиральных комплексов меди(II) в виде индивидуальных соединений 1-4 по п. 1 в качестве средства, обладающего антибактериальной и противогрибковой активностью.
| KALARANI R | |||
| et al., Synthesis, spectral, DFT calculation, sensor, antimicrobial and DNA binding studies of Co(II), Cu(II) and Zn(II) metal complexes with 2-amino benzimidazole Schiff base, Journal of Molecular Structure, 11.01.2020, v | |||
| Устройство для получения рентгеновских изображений | 1925 |
|
SU1206A1 |
| Устройство для автоматического реверсивного управления двухфазным асинхронным серводвигателем | 1959 |
|
SU127725A1 |
| ABDEL-RAHMAN L.H | |||
| et al., Synthesis, theoretical | |||
Авторы
Даты
2021-09-24—Публикация
2020-10-15—Подача