Изобретение относится к области органической химии, а именно к новым индивидуальным соединениям класса 1,7-диазаспиро[4.4]нона-3,6,8-триена и к способу их получения, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем.
Известен структурный аналог заявленных соединений - 1,7-диазоспиро[4,4]нонан-2,6-дион, являющийся продуктом внутримолекулярной спиро-бис-гетероциклизации диметилового эфира 2-амино-2-(2-аминоэтил)глутаровой кислоты (Majer Z., Kajtar M., Tichy M., Blaha K. // Collect. Czech. Chem. Commun. 1982, 47(3), 950-960):
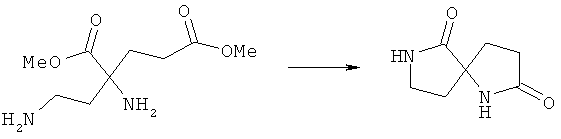
К недостаткам данного способа относится невозможность получения этил 1,6-диарил-4-ароил-3-гидрокси-2-оксо-8-фенил-1,7-диазаспиро[4.4]нона-3,6,8-триен-9-карбоксилатов.
Задачей изобретения является разработка простого способа синтеза не описанных в литературе этил 1,6-диарил-4-ароил-3-гидрокси-2-оксо-8-фенил-1,7-диазаспиро [4.4] нона-3,6,8-триен-9-карбоксилатов.
Поставленная задача осуществляется путем кипячения раствора 1-арил-4,5-диароил-1H-пиррол-2,3-дионов (Iа-г) с этиловым эфиром 3-амино-3-фенилпропеновой кислоты (II) в соотношении 1:1, по следующей схеме:
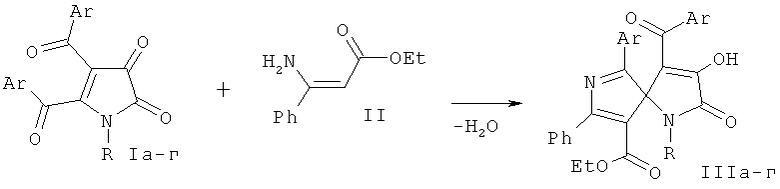
I, III: Ar-Ph, R=C6H4Ме-4 (а), C6H4OМе-4 (б); Ar=C6H4Me-4, R=C6H4Me-4 (в), C6H4OMe-4 (г).
Процесс ведут при температуре 79-80°С, а в качестве растворителя используют абсолютный бензол.
Из патентной и технической литературы не были выявлены способы получения замещенных этил 1,6-диарил-4-ароил-3-гидрокси-2-оксо-8-фенил-1,7-диазаспиро[4.4]нона-3,6,8-триен-9-карбоксилатов, имеющие сходные признаки с заявляемым способом, а именно не использовались исходные продукты, растворители, в которых проходит реакция, и интервал температур, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. Этил 4-бензоил-3-гидрокси-2-оксо-1-толил-6,8-дифенил-1,7-диазаспиро[4.4]нона-3,6,8-триен-9-карбоксилат (IIIa).
Раствор 1.0 ммоль 4,5-дибензоил-1-толил-1H-пиррол-2,3-диона (Ia) и 1.0 ммоль этилового эфира 3-амино-3-фенилпропеновой кислоты (II) в 20 мл абсолютного бензола кипятили в течение 2 ч, удаляли половину объема растворителя, разбавляли в два раза петролейным эфиром (Т.кип 40-70°С), охлаждали, образовавшийся осадок отфильтровывали и перекристаллизовывали из смеси бензола и этилацетата (1:1). Выход 71%, т.пл. 196-197°С. Соединение (IIIa) C36H28N2O5.
Найдено, %: С 75.99; Н 4.91; N 4.89.
Вычислено, %: С 76.04; Н 4.96; N 4.93.
Соединение (IIIa) - ярко-желтое кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, трудно растворимое в обычных органических растворителях, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В ИК-спектре соединения (IIIa), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний группы OH в виде широкого пика при 3265 см-1, сложноэфирной карбонильной группы при 1719 см-1, лактамной карбонильной группы при 1669 см-1, кетонной карбонильной группы при 1659 см-1 и связи C=N при 1640 см-1.
В спектре ПМР соединения (IIIa), записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец, присутствуют синглет протонов метильной группы при 2.21 м.д., триплет и мультиплет протонов метильной и метиленовой групп этоксикарбонильного заместителя при 1.14 и 4.14 м.д. соответственно, а также широкий сигнал протона группы OH при 12.73 м.д.
Пример 2. Этил 3-гидрокси-2-оксо-1,6-дитолил-4-толуоил-8-фенил-1,7-диазаспиро[4.4]нона-3,6,8-триен-9-карбоксилат (IIIв).
Раствор 1.0 ммоль 1-толил-4,5-дитолуоил-1H-пиррол-2,3-диона (Iа) и 1.0 ммоль этилового эфира 3-амино-3-фенилпропеновой кислоты (II) в 20 мл абсолютного бензола кипятили в течение 3 ч, удаляли половину объема растворителя, разбавляли в два раза петролейным эфиром (Т.кип 40-70°С), охлаждали, образовавшийся осадок отфильтровывали и перекристаллизовывали из смеси бензола и этилацетата (1:1). Выход 76%, т.пл. 215-216°С. Соединение (IIIв) C38H32N2O5.
Найдено, %: С 76.42; Н 5.39; N 4.67.
Вычислено, %: С 76.49; Н 5.41; N 4.69.
Соединение (IIIв) - ярко-желтое кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, трудно растворимое в обычных органических растворителях, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В ИК-спектре соединения (IIIв), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний группы ОН в виде широкого пика при 3269 см-1, сложноэфирной карбонильной группы при 1725 см-1, лактамной карбонильной группы при 1667 см-1, кетонной карбонильной группы и связи C=N при 1642 см-1.
В спектре ПМР соединения (IIIв), записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец, присутствуют три синглета протонов метильных групп при 2.21, 2.35 и 2.37 м.д., триплет и мультиплет протонов метильной и метиленовой групп этоксикарбонильного заместителя при 1.14 и 4.11 м.д. соответственно, а также широкий сигнал протона группы ОН при 12.61 м.д.
Соединения III (б, г) синтезировали аналогично.
Пример 3. Фармакологическое исследование этил 3-гидрокси-2-оксо-1,6-дитолил-4-толуоил-8-фенил-1,7-диазаспиро[4.4]нона-3,6,8-триен-9-карбоксилата (IIIв) и 3-гидрокси-2-оксо-6-толил-4-толуоил-1-(4-метоксифенил)-8-фенил-1,7-диазаспиро[4.4]нона-3,6,8-триен-9-карбоксилата (IIIг) на наличие анальгетической активности.
Анальгетическую активность соединений (IIIв, г) определяли на модели «уксусных корчей». Корчи вызывали введением внутрибрюшинно 0,75% раствора уксусной кислоты 0,25 мл на 10 г мыши. Все соединения вводились перорально в 2% крахмальной слизи в дозе 50 мг/кг (эталон сравнения - метамизол натрия) за 1 час до введения уксусной кислоты. Показатель - количество корчей в течение 10 минут от начала опыта. (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. Москва 2000. - С.239.) Статистическую обработку экспериментального материала проводили с использованием t критерия Стьюдента (М.Л.Беленький. Элементы количественной оценки фармакологического эффекта. - 2-е изд. - Л., 1963. - c.l52). Эффект считали достоверным при p<0,05.
Проведенные исследования показали (таблица), что соединения (IIIв, г) обладают анальгетической активностью. Данные о фармакологической активности аналогов заявляемых соединений в доступной литературе отсутствуют.
Предлагаемый способ прост в осуществлении, одностадиен и позволяет получить неописанные в литературе этил 1,6-диарил-4-ароил-3-гидрокси-2-оксо-8-фенил-1,7-диазаспиро[4.4]нона-3,6,8-триен-9-карбоксилаты (IIIа-г) с хорошими выходами, которые найдут применение в качестве исходных продуктов для синтеза гетероциклических систем и в фармакологии в качестве потенциальных лекарственных средств.
Изобретение относится к новым этил 1,6-диарил-4-ароил-3-гидрокси-2-оксо-8-фенил-1,7-диазаспиро[4.4]нона-3,6,8-триен-9-карбоксилатам формулы
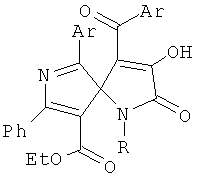
где Аr означает Ph, С6Н4Ме-4; R означает С6Н4Ме-4, С6Н4ОМе-4, которые проявляют анальгетическую активность. Соединения получают взаимодействием 1-арил-4,5-диароли-1Н-пиррол-2,3-диона с этиловым эфиром 3-амино-3-фенилпропеновой кислоты в соотношении 1:1 в среде кипящего абсолютного бензола с последующим выделением целевых продуктов. 2 н. и 2 з.п. ф-лы, 1 схема, 1 табл., 3 пр.
1. Этил 1,6-диарил-4-ароил-3-гидрокси-2-оксо-8-фенил-1,7-диазаспиро[4.4]нона-3,6,8-триен-9-карбоксилаты формулы
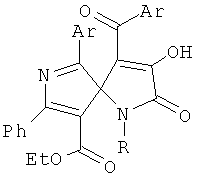
где Ar=Ph, C6H4Me-4; R=C6H4Me-4, C6H4OMe-4.
2. Способ получения этил 1,6-диарил-4-ароил-3-гидрокси-2-оксо-8-фенил-1,7-диазаспиро[4.4]нона-3,6,8-триен-9-карбоксилаты общей формулы

где Ar=Ph, С6Н4Ме-4; R=C6H4Me-4, С6Н4ОМе-4,
отличающийся тем, что 1-арил-4,5-диароли-1Н-пиррол-2,3-дионы подвергают взаимодействию с этиловым эфиром 3-амино-3-фенилпропеновой кислоты в соотношении 1:1 в среде кипящего абсолютного бензола с последующим выделением целевых продуктов.
3. Способ по п.2, отличающийся тем, что процесс ведут при температуре 79-80°С.
4. Способ по п.2 или 3, отличающийся тем, что в качестве растворителя используют абсолютный бензол.
| 0 |
|
SU336475A1 | |
| Ж | |||
| органической химии, т.47, выпуск 10, с.1572-1573. | |||
Авторы
Даты
2012-11-20—Публикация
2011-04-14—Подача