ОБЛАСТЬ ТЕХНИКИ
Описанное в данном документе относится к йогексолу, композиции, содержащей его, и способу его применения.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Йогексол является известным контрастным средством, имеющим следующую структуру:
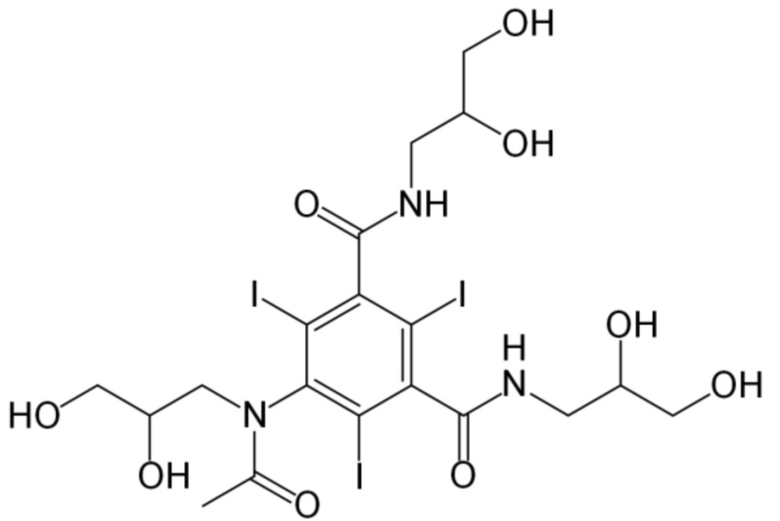
Растворы йогексола для перорального введения применимы в качестве контрастных средств для, например, визуализации органов брюшной полости посредством томографии. В данных целях целесообразно получать йогексол в твердой форме, который может быть разведен с получением контрастного раствора для перорального введения перед применением. Однако, несмотря на то, что йогексол легкорастворим в воде, частицы йогексола проявляют тенденцию к образованию больших, когезивных, липких агрегатов, которые растворяются очень медленно. Как правило, для полного растворения требуются длительное перемешивание или повышенные температуры, которые могут привести к разложению йогексола в небуферизованных системах. Поскольку твердый (например, порошкообразный) йогексол необходимо разводить при помощи перемешивания вручную композиции на основе твердого йогексола в соответствующем растворителе (например, воде или ароматизированном водном растворе) в кабинете врача или в учреждении визуализации, существует вероятность, что композиция на основе йогексола не полностью растворится при таких условиях, и поэтому пациент получит более низкую концентрацию и дозу контрастного средства на основе йогексола, чем необходимо для надлежащей визуализации. В связи с этим важно, чтобы йогексол был получен в такой форме, которая растворяется быстро и полностью под действием условий перемешивания вручную, чтобы пациент получил полную дозу йогексола с надлежащей концентрацией.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данном документе описаны композиции и способы применительно к йогексолу. В различных вариантах осуществления, описанных в данном документе, композиция на основе контрастного средства содержит частицы йогексола, которые в значительной степени растворяются в воде за приблизительно 60 секунд или менее при испытании с применением модифицированного способа 641 Фармакопеи Соединенных Штатов Америки, описанного в данном документе.
В некоторых вариантах осуществления композиция на основе контрастного средства содержит частицы йогексола, которые имеют одну или несколько следующих характеристик: насыпную плотность менее приблизительно 0,8 г/см3, расстояние между частицами более приблизительно 60% от насыпного объема и удельную площадь поверхности более приблизительно 0,8 м2/г.
В других вариантах осуществления композиция на основе контрастного средства содержит кристаллы йогексола с особой кристаллической структурой, например, демонстрирующие порошковую дифракционную рентгенограмму, по сути, как описано в данном документе и имеющую пики 2θ при приблизительно 7,6°, 16,2°, 19,9°, 20,8°, 22,3°, 29,8° и 30,7°.
В других вариантах осуществления композиция на основе контрастного средства содержит частицы йогексола, полученные посредством способа, включающего кристаллизацию йогексола из смеси растворителей, которая содержит спирт, алкилацетат и воду. Кристаллизацию осуществляют путем нагревания раствора йогексола в смеси растворителей (например, при температуре кипения) и при условиях интенсивного встряхивания (например, перемешивания).
В некоторых вариантах осуществления композиция на основе контрастного средства содержит частицы йогексола с распределением частиц по размеру, имеющим одну или несколько следующих характеристик: D90 не более приблизительно 40 мкм, D50 не более приблизительно 20 мкм и D10 не более приблизительно 10 мкм.
В некоторых вариантах осуществления композицию на основе контрастного средства получают путем высушивания распылением 30-40% (вес/вес) раствора йогексола. Температура на входе в распылительную сушилку находится в диапазоне приблизительно 220-255°C и температура на выходе находится в диапазоне приблизительно 95-115°C.
В некоторых вариантах осуществления способ получения кристаллов йогексола включает (a) нагревание раствора йогексола в растворителе, содержащем спирт, алкилацетат и воду до температуры кипения при встряхивании. Способ дополнительно включает (b) удаление одного или нескольких из спирта, алкилацетата и воды путем дистилляции раствора йогексола. Способ дополнительно включает (c) поддержание раствора йогексола при встряхивании и при температуре от 60°C вплоть до температуры кипения при атмосферном, пониженном или повышенном давлении, посредством чего получают суспензию кристаллов, по сути, на основе экзойогексола. Способ дополнительно включает (d) охлаждение суспензии из этапа (b) до приблизительно 40-50°C при встряхивании и (e) фильтрование и высушивание суспензии.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
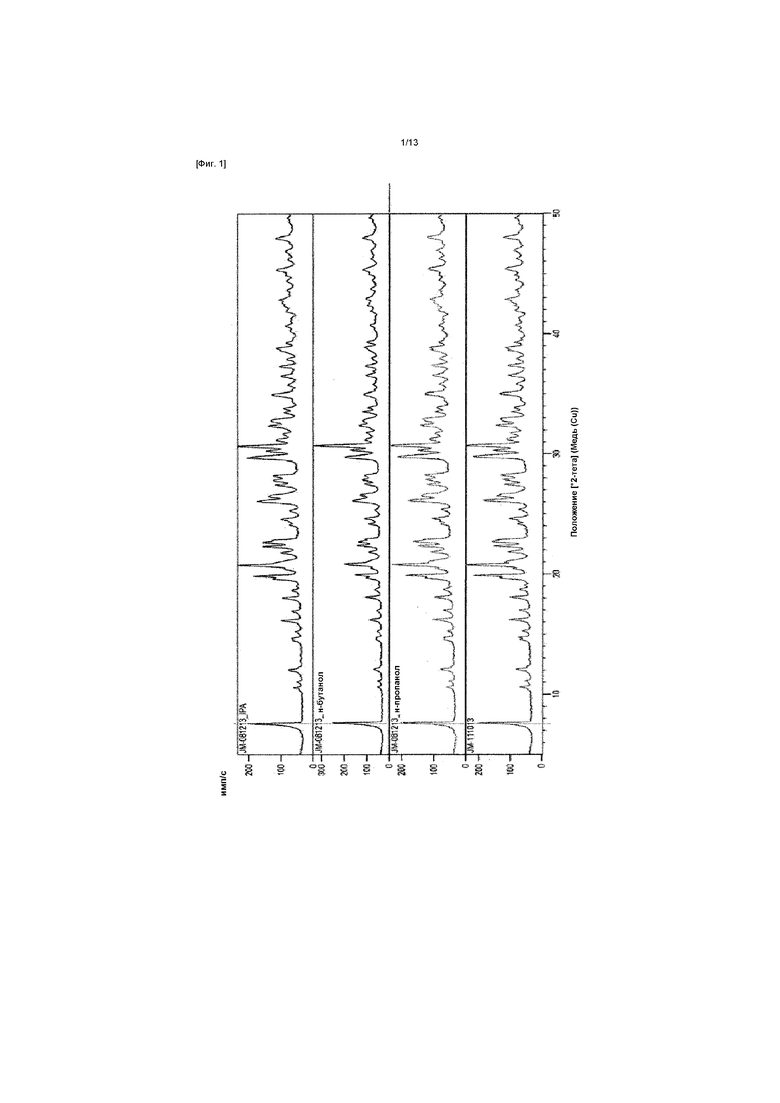
[Фиг. 1] ФИГ. 1 представляет собой сопоставление порошковых дифракционных рентгенограмм образцов JM-081213_IPA, JM-081213_н-бутанола, JM-081213_н-пропанола и JM-111013;
[Фиг. 2] ФИГ. 2 представляет собой SEM-изображение кристаллов йогексола, полученных способом кристаллизации по настоящему изобретению, с характеристическими размерами отдельных частиц приблизительно 0,5-3 мкм;
[Фиг. 3] ФИГ. 3 представляет собой SEM-изображение кристаллов йогексола, полученных способом кристаллизации по настоящему изобретению, демонстрирующее агломерацию кристаллов, образованных в областях с низкой интенсивностью перемешивания;
[Фиг. 4] ФИГ. 4 представляет собой SEM-изображение кристаллов йогексола, полученных без перемешивания в процессе кристаллизации;
[Фиг. 5] ФИГ. 5 представляет собой SEM-изображение кристаллов йогексола, демонстрирующее агломерацию частиц вследствие влияния влажности;
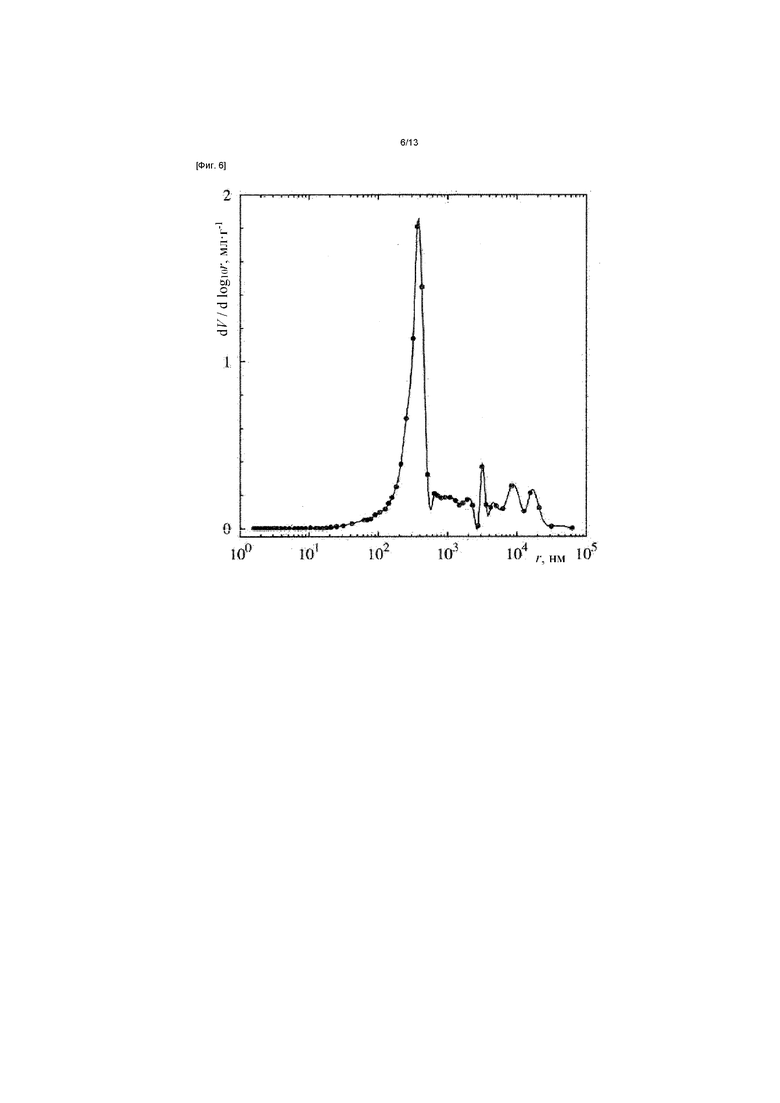
[Фиг. 6] ФИГ. 6 представляет собой график распределения по размерам открытых полостей в кристаллизированном йогексоле, полученный посредством ртутной порометрии - полости между агломератами имеют приблизительный размер от приблизительно 1 до приблизительно 100 мкм;
[Фиг. 7] ФИГ. 7 представляет собой SEM-изображение высушенного распылением йогексола, полученного посредством способа высушивания распылением по настоящему изобретению, с указанными характеристическими размерами;
[Фиг. 8] ФИГ. 8 представляет собой SEM-изображение высушенного распылением йогексола, полученного посредством обычных способов высушивания распылением, с указанными характеристическими размерами;
[Фиг. 9] ФИГ. 9A и 9B представляют собой SEM-изображения высушенного распылением йогексола, полученного посредством способов высушивания распылением по настоящему изобретению; на фиг. 9B показана поверхность среза одной из сферических частиц из фиг. 9A, что указано стрелкой;
ФИГ. 9C представляет собой SEM-изображение, иллюстрирующее дополнительные особенности поверхности среза частицы высушенного распылением йогексола из фиг. 9B;
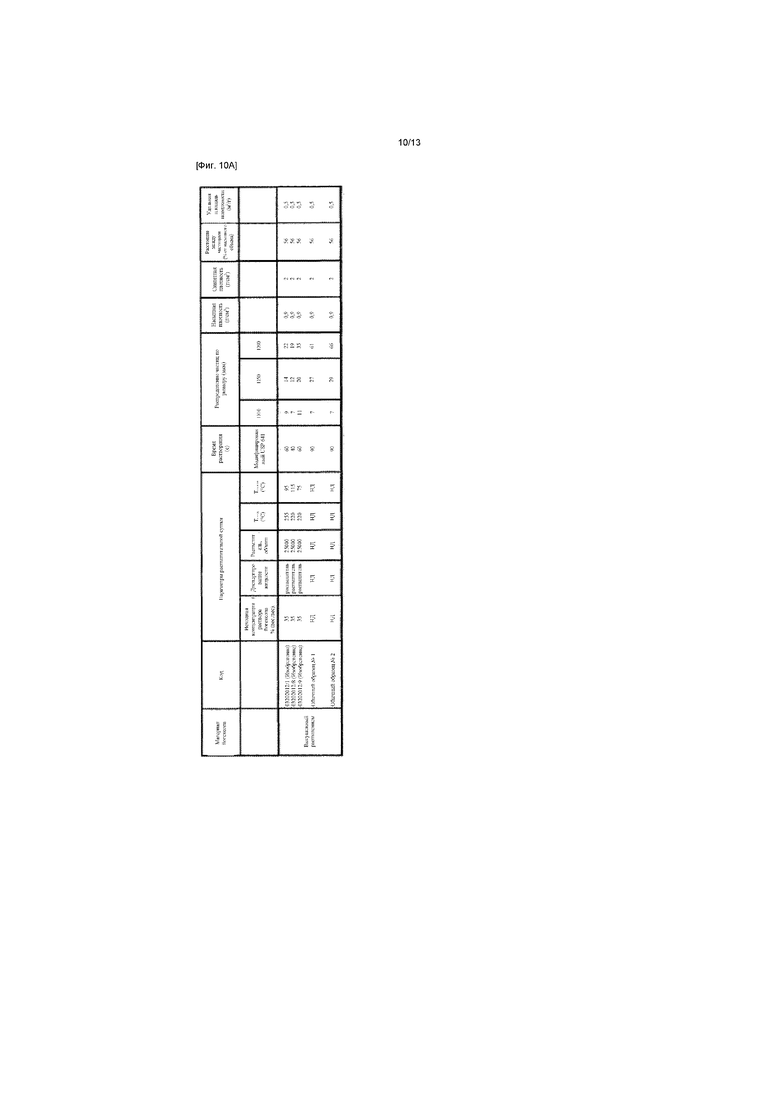
[Фиг. 10A] ФИГ. 10A представляет собой таблицу, иллюстрирующую влияние параметров высушивания распылением на время растворения и характеристики частицы;
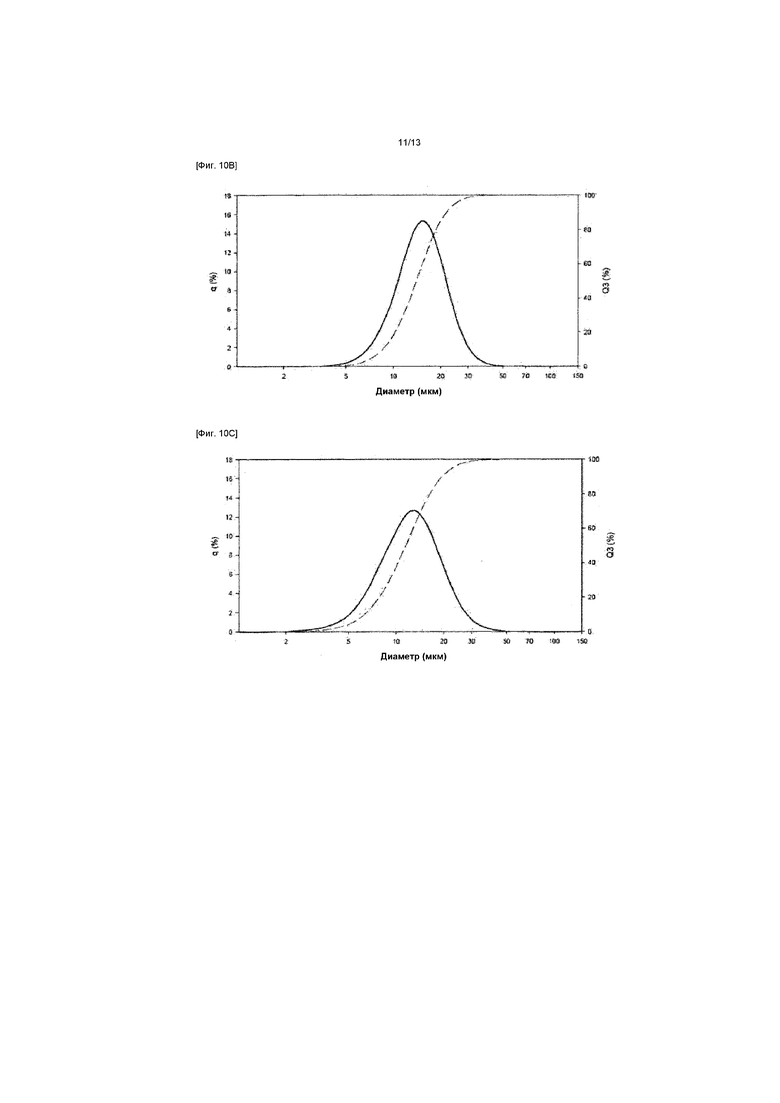
[Фиг. 10B] ФИГ. 10B представляет собой график распределения частиц по размеру для частиц с кодом 03202012/1 из ФИГ. 10A;
[Фиг. 10C] ФИГ. 10C представляет собой график распределения частиц по размеру для частиц с кодом 03202012/8 из ФИГ. 10A;
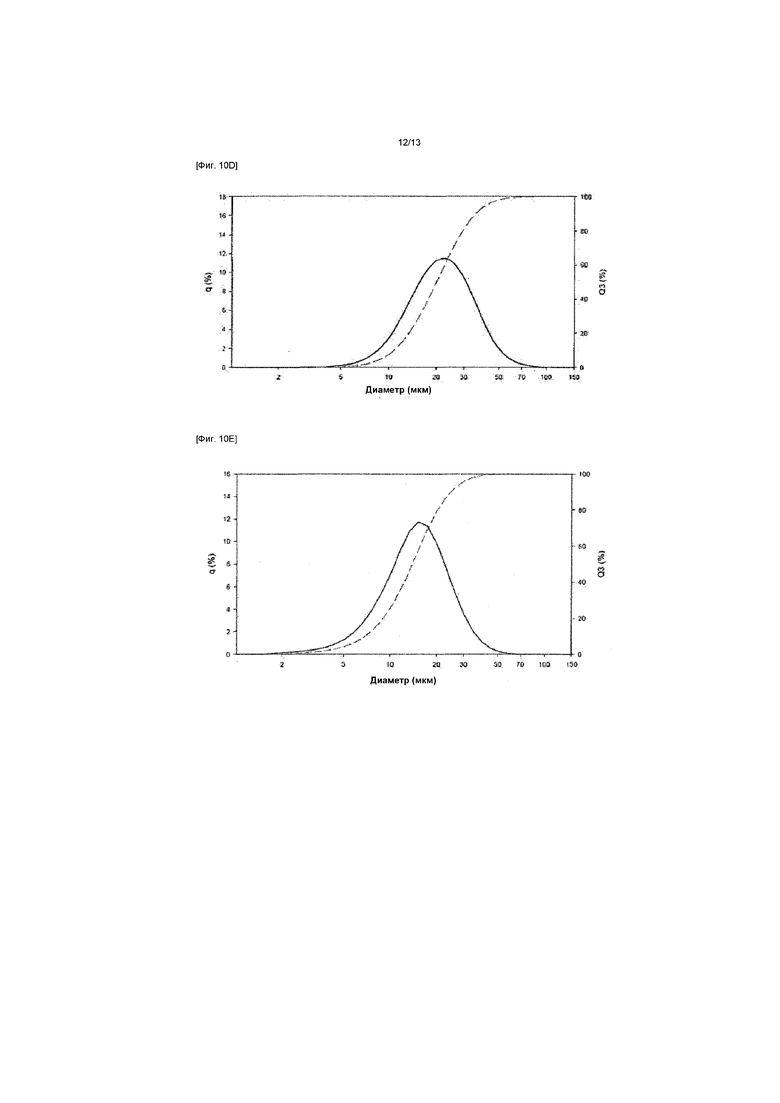
[Фиг. 10D] ФИГ. 10D представляет собой график распределения частиц по размеру для частиц с кодом 03202012/9 из ФИГ. 10A;
[Фиг. 10E] ФИГ. 10E представляет собой график распределения частиц по размеру для стандартного образца №1 из ФИГ. 10A и
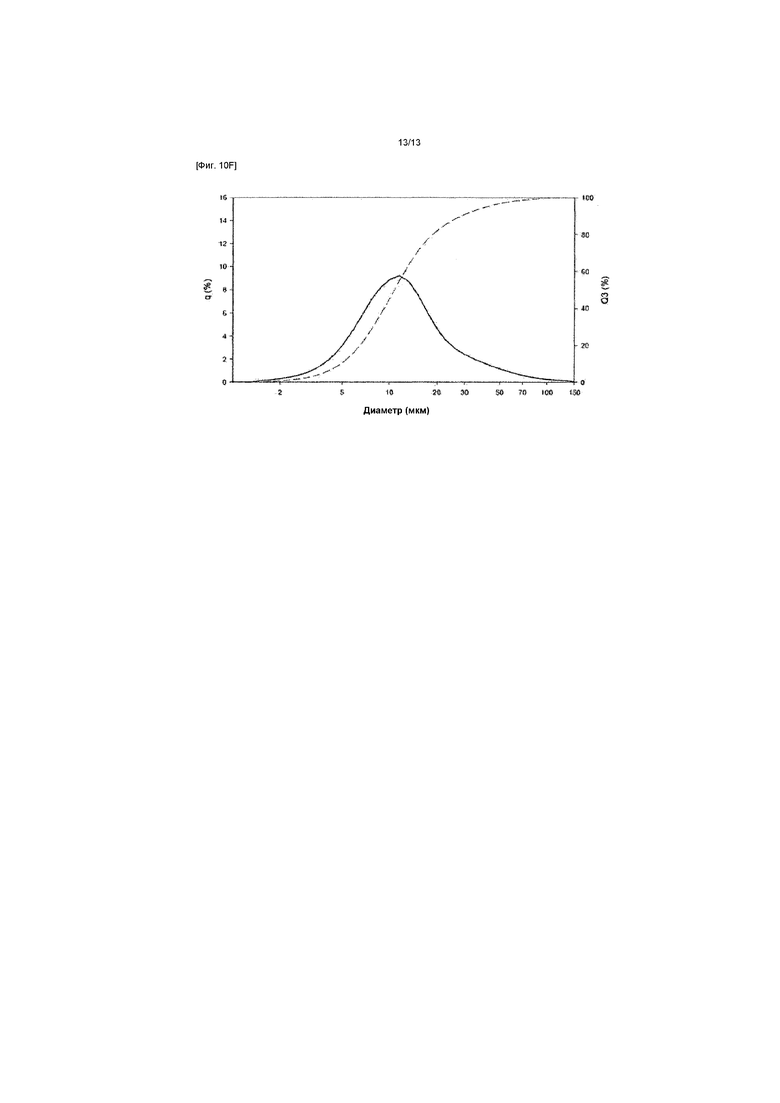
[Фиг. 10F] ФИГ. 10F представляет собой график распределения частиц по размеру для стандартного образца №2 из ФИГ. 10A.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Быстрорастворимые композиции на основе йогексола и их получение и применение предусматриваются в данном документе. Аспекты настоящего изобретения предусматривают композиции йогексола с конкретными характеристиками в отношении обеспечения быстрого растворения, включая, но без ограничения, распределение частиц по размеру, характеристики частицы, форму кристалла и/или т.п. Аспекты настоящего изобретения также предусматривают способы получения композиций быстрорастворимого йогексола посредством применения определенных условий кристаллизации или высушивания распылением. Все документы, патенты и патентные заявки, процитированные в данном документе, включены в данный документ посредством ссылок во всей их полноте для всех целей.
Применяемый в данном документе термин "Модифицированный способ 641 Фармакопеи Соединенных Штатов Америки" означает модифицированную форму стандартного способа 641 Фармакопеи Соединенных Штатов Америки, где модифицированный способ 641 Фармакопеи Соединенных Штатов Америки осуществляют следующим образом.
Помещают 1,8 г йогексола в виде частиц в тщательно очищенный закрытый стеклянной пробкой стеклянный цилиндр объемом 50 мл с соотношением размеров диаметра и высоты приблизительно 1:10.
В стеклянный цилиндр наливают 40 мл водопроводной воды, доведенной до 10°C (±2°C).
Сразу же начинают встряхивать стеклянный цилиндр и начинают регистрировать общее время.
Встряхивают стеклянный цилиндр движениями вверх и вниз, придерживаясь частоты 12-13 движений за 5 секунд.
Через 20 секунд наблюдают в течение 3 секунд за полнотой растворения.
Через 3 секунды оценивают, когда исчезают пузырьки, сравнивая с чистым растворителем.
Если растворился полностью, записывают "растворился за 20 секунд".
Если не растворился полностью, продолжают встряхивание в течение общего времени 30 с.
Повторяют оценку растворения через 30 секунд, 40 секунд, 1 мин и 1 мин 30 секунд.
Всегда повторяют оценку растворения с применением аналогичной процедуры.
Если растворился полностью в момент времени 1 мин 30 с, записывают "растворился NMT 1 мин. 30 с".
Если не растворился, записывают "не растворился за 1 мин 30 с".
Применяемый в данном документе термин "однократная доза" означает физически идентифицируемое, фиксированное количество йогексола, предусмотренное для применения. Однако, такая фиксированная "однократная доза" не должна содержать все количество, требуемое для нужд данной процедуры визуализации. Например, в данной процедуре визуализации может потребоваться более однократной дозы (например, могут быть объединены несколько однократных доз) или потребоваться менее однократной дозы (например, менее, чем полное количество йогексола, принятое после растворения в соответствующем растворителе).
Применяемый в данном документе термин "насыпная плотность" материала означает суммарную массу материала, деленную на суммарный объем, занимаемый материалом.
Применяемый в данном документе термин "расстояние между частицами" означает процент от "насыпного" объема частиц, который является свободным пространством. Расстояние между частицами может быть рассчитано из насыпной плотности и скелетной плотности. Как рассмотрено выше, насыпная плотность относится к плотности, определяемой путем деления веса образца на его измеренный объем, например, с применением способа USP <616>. Скелетную плотность, иногда называемую "истинной плотностью", определяют путем деления веса образца на его "истинный" объем, т.е. объем за исключением внутренних пустотных пространств и любой открытой пористости в образце (например, определенный при помощи методик вытеснения газом). Расстояние между частицами может быть рассчитано из насыпной плотности и скелетной плотности в соответствии с примерами из данного документа: если насыпная плотность конкретного образца йогексола составляет ~0,9 г/см3, то соответствующий "насыпной" объем для 1 г образца составляет 1,11 см3; и если скелетная плотность образца составляет ~2 г/см3, то соответствующий "скелетный" объем (т.е. объем с исключенной пористостью) для 1 г такого образца составляет 0,5 см3. Разность между "насыпным" объемом и "скелетным" объемом 0,61 см3 представляет собой объем свободного пространства (пористость) в частице. Расстояние между частицами представляет собой разность между "скелетным" объемом и насыпным объемом, деленную на "насыпной" объем и выражается в процентах (т.е. 0,61 см3/1,11 см3=55% в данном примере).
Применяемая в данном примере "удельная площадь поверхности" материала означает общую площадь поверхности материала на единицу массы материала.
Применяемый в данном документе термин "D90" материала в виде частиц означает величину диаметра частиц в материале, при которой приблизительно 90% частиц имеют диаметр ниже величины диаметра. Например, в образце с D90 20 мкм, 90% частиц в образце имеют диаметр 20 мкм или менее.
Применяемый в данном документе термин "D50" материала означает величину диаметра для частиц в материале, при которой приблизительно 50% частиц имеют диаметр ниже величины диаметра. Например, в образце с D50 10 мкм, 50% частиц в образце имеют диаметр 10 мкм или менее.
Применяемый в данном документе термин "D10" материала означает величину диаметра для частиц в материале, при которой приблизительно 10% частиц имеют диаметр ниже величины диаметра. Например, в образце с D10 5 мкм, 10% частиц в образце имеют диаметр 5 мкм или менее.
Применяемые в данном документе "функциональное вспомогательное вещество или добавка" означают вспомогательное вещество или добавку, которое повышает или усиливает свойства растворения композиции на основе йогексола, например, повышение растворимости или скорости растворения йогексола. Другими словами, скорость растворения композиции на основе йогексола с помощью функционального вспомогательного вещества или добавки сравнительно или значительно выше, чем у идентичной в остальном композиции на основе йогексола без функционального вспомогательного вещества или добавки. Например, если добавление конкретного вспомогательного вещества или добавки к композиции на основе контрастного средства уменьшает время растворения на приблизительно 10 или более секунд (например, как измерено посредством модифицированного способа 641 USP, описанного в данном документе и по сравнению с идентичным в остальном составом без вспомогательного вещества или добавки), то такое вспомогательное вещество или добавка будут считаться "функциональным вспомогательным веществом или добавкой". Примеры функциональных вспомогательных веществ и добавок включают без ограничения средства, улучшающие распадаемость таблеток (кроскармеллозу натрия, кросповидон, карбоксиметилкрахмал, крахмалгликолят натрия и т. д.), диспергирующие средства, бета-циклодекстрины и аналоги, средства, предотвращающие слипание (например, коллоидный диоксид кремния и т. д.), смазывающие вещества (например, стеарат магния, стеарилфумарат натрия, полиэтиленгликоли и т. д.) и прочие.
Применяемый в данном документе термин "нефункциональное вспомогательное вещество или добавка" означает вспомогательное вещество или добавку, которое не является функциональным вспомогательным веществом или добавкой (т.е. которое сравнительно или значительно не повышает или усиливает свойства растворения йогексола). Например, если добавление конкретного вспомогательного вещества или добавки к композиции на основе контрастного средства лишь незначительно уменьшает время растворения (например, на приблизительно 5 секунд или менее, как измерено посредством модифицированного способа 641 USP, описанного в данном документе и по сравнению с идентичным в других отношениях составом без вспомогательного вещества или добавки) или не изменяет время растворения, или увеличивает время растворения, то такие вспомогательное вещество или добавка будут считаться "нефункциональным вспомогательным веществом или добавкой". Как правило, неограничивающие примеры нефункциональных вспомогательных веществ или добавок включают вкусоароматические агенты (например, подсластители) или окрашивающие средства при условии, что такие вспомогательные вещества или добавки не усиливают растворение йогексола.
Применяемый в данном документе термин "стерильный" означает, что вещество и/или элемент были обработаны так, чтобы они не содержали и/или, как полагают, практически не содержали нежелательных микроорганизмов, таких как, но без ограничения, вирус, бактерия и/или подобные. Применяемый в данном документе термин "нестерильный" означает, что вещество и/или элемент не были обработаны так, чтобы они не содержали и/или, как полагают, практически не содержали нежелательных микроорганизмов, таких как, но без ограничения, вирус, бактерия и/или подобные.
Термин "приблизительно" при использовании вместе с числовой величиной означает числовую величину, плюс или минус вплоть до 15% от данной величины. Например, "приблизительно 100" означает от 85 до 115. В других вариантах осуществления термин "приблизительно" означает упоминаемое числовое значение, плюс или минус вплоть до 10% от данной упоминаемой числовой величины. Например, "приблизительно 100" означает от 90 до 110. В конкретных контекстах термин "приблизительно" применительно к ряду числовых величин относится к числовой величине, плюс или минус половина интервала (без перекрытия) между числовыми величинами в ряду.
В данном документе описаны композиции и способы применительно к йогексолу. В некоторых вариантах осуществления частицы йогексола по настоящему изобретению, например, однократная доза частиц йогексола, полученных согласно способам кристаллизации или высушивания распылением, описанным в данном документе, могут в значительной степени раствориться в воде за приблизительно 5 секунд, приблизительно 10 секунд, приблизительно 20 секунд, приблизительно 30 секунд, приблизительно 40 секунд, приблизительно 50 секунд, приблизительно 60 секунд, приблизительно 70 секунд, приблизительно 80 секунд или менее, чем приблизительно 90 секунд, включая все величины, диапазоны и поддиапазоны между ними при испытании с применением модифицированного способа 641 Фармакопеи Соединенных Штатов Америки. В некоторых вариантах осуществления настоящего изобретения композиция на основе контрастного средства включает частицы йогексола, которые в значительной степени растворяются в воде за приблизительно 60 секунд при испытании с применением модифицированного способа 641 Фармакопеи Соединенных Штатов Америки. В других вариантах осуществления частицы йогексола согласно настоящему изобретению в значительной степени растворяются за приблизительно 40 секунд при испытании с применением модифицированного способа 641 Фармакопеи Соединенных Штатов Америки.
Частицы йогексола согласно настоящему изобретению могут быть в кристаллической форме, в аморфной форме или их комбинациями. В некоторых вариантах осуществления композиция на основе контрастного средства по настоящему изобретению содержит, состоит преимущественно из или состоит из частиц йогексола, по сути, в кристаллической форме. Термин "по сути кристаллическая форма" относится к материалу, который является практически кристаллическим, но может содержать небольшие количества аморфного материала (например, менее приблизительно 1%, менее приблизительно 2%, менее приблизительно 3%, менее приблизительно 4%, менее приблизительно 5%, включая диапазоны и поддиапазоны между ними). В других вариантах осуществления композиция на основе контрастного средства по настоящему изобретению содержит, состоит преимущественно из или состоит из частиц йогексола, по сути, в аморфной форме. Аналогичным образом, термин "по сути, в аморфной форме" относится к материалу, который является преимущественно аморфным, но может содержать небольшие количества кристаллического материала (например, менее приблизительно 1%, менее приблизительно 2%, менее приблизительно 3%, менее приблизительно 4%, менее приблизительно 5%, включая диапазоны и поддиапазоны между ними). В конкретных вариантах осуществления кристаллическая форма йогексола представляет собой особую кристаллическую форму, описанную в данном документе.
В некоторых вариантах осуществления количество йогексола, предоставляемое пациенту для процедуры визуализации, может быть однократной дозой, более чем однократная доза или менее чем однократная доза в зависимости от выполняемой процедуры (например, рентгеноскопические процедуры, магниторезонансная визуализация и/или подобное). В некоторых вариантах осуществления количество йогексола в композиции на основе контрастного средства является однократной дозой. Например, однократная доза может составлять приблизительно 5 г, приблизительно 10 г, приблизительно 15 г или приблизительно 20 г с учетом всех величин, диапазонов и поддиапазонов между ними. В конкретных вариантах осуществления количество йогексола в однократной дозе составляет приблизительно 9,7 г.
В некоторых вариантах осуществления общее количество йогексола, предоставляемое пациенту, может составлять приблизительно 0,2 г, приблизительно 0,5 г, приблизительно 1,0 г, приблизительно 1,5 г, приблизительно 2 г, приблизительно 3 г, приблизительно 5 г, приблизительно 10 г, приблизительно 15 г, приблизительно 20 г, приблизительно 30 г, приблизительно 40 г, приблизительно 50 г, приблизительно 60 г, приблизительно 65 г, приблизительно 70 г, приблизительно 75 г, приблизительно 80 г, приблизительно 85 г, приблизительно 90 г, приблизительно 100 г с учетом всех величин, диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления количество йогексола составляет приблизительно 0,1 г. В некоторых вариантах осуществления количество йогексола находится в диапазоне от приблизительно 0,2 г до приблизительно 75 г. В некоторых вариантах осуществления количество йогексола составляет приблизительно 10 г, например, приблизительно 9,7 г.
В некоторых вариантах осуществления композиция на основе контрастного средства может практически не содержать фармацевтически приемлемые функциональные вспомогательные вещества, тогда как в других вариантах осуществления композиция на основе контрастного средства может включать одно или несколько фармацевтически приемлемых функциональных вспомогательных веществ.
В некоторых вариантах осуществления композиция на основе контрастного средства может включать по меньшей мере одно фармацевтически приемлемое нефункциональное вспомогательное вещество, тогда как в других вариантах осуществления композиция на основе контрастного средства вовсе не включает фармацевтически приемлемые нефункциональные вспомогательные вещества.
В некоторых вариантах осуществления композиция на основе контрастного средства практически не содержит фармацевтически приемлемые функциональные вспомогательные вещества. В некоторых вариантах осуществления композиция на основе контрастного средства включает по меньшей мере одно фармацевтически приемлемое нефункциональное вспомогательное вещество.
В некоторых вариантах осуществления композиция на основе контрастного средства практически не содержит фармацевтически приемлемые функциональные вспомогательные вещества и включает по меньшей мере одно фармацевтически приемлемое нефункциональное вспомогательное вещество.
В различных вариантах осуществления, описанных в данном документе, фармацевтически приемлемое нефункциональное вспомогательное вещество может быть выбрано из группы, состоящей из диспергирующих средств, разрыхлителей, покрытий, наполнителей, ароматизаторов, сорбентов, консервантов, подсластителей, окрашивающих средств, смачивающих средств, связующих веществ, средств, предотвращающих слипание, и их комбинаций при условии, что добавление таких вспомогательных веществ не повышает существенно растворение йогексола, как описано в данном документе.
Йогексол по настоящему изобретению может содержать экзоизомер йогексола (также называемый экзойогексолом), эндоизомер йогексола (также называемый эндойогексолом) и любую их комбинацию. В некоторых вариантах осуществления йогексол представляет собой, по сути, экзоизомер. В конкретных вариантах осуществления йогексол является кристаллическим и, по сути, экзоизомером.
В некоторых вариантах осуществления композиция на основе контрастного средства может быть нестерильной, тогда как в других вариантах осуществления композиция на основе контрастного средства может быть стерильной. В некоторых вариантах осуществления, в частности, если композиция на основе контрастного средства предназначена, например, для (но без ограничения) перорального введения, она может быть стерильной, даже если стерильность не является необходимой. В некоторых вариантах осуществления композиция на основе контрастного средства является нестерильной.
Частицы йогексола по настоящему изобретению могут иметь любую допустимую насыпную плотность, которая способствует быстрому растворению. В конкретных вариантах осуществления частицы йогексола могут иметь насыпную плотность приблизительно 0,9 г/см3, приблизительно 0,85 г/см3, приблизительно 0,8 г/см3, приблизительно 0,75 г/см3, приблизительно 0,7 г/см3, приблизительно 0,65 г/см3, приблизительно 0,6 г/см3, приблизительно 0,55 г/см3, приблизительно 0,5 г/см3, приблизительно 0,45 г/см3, приблизительно 0,4 г/см3, приблизительно 0,35 г/см3, приблизительно 0,3 г/см3, приблизительно 0,25 г/см3 или приблизительно 0,2 г/см3 с учетом всех величин, диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления частицы йогексола характеризуются насыпной плотностью менее приблизительно 1 г/см3. В некоторых вариантах осуществления частицы характеризуются насыпной плотностью менее приблизительно 0,8 г/см3. В некоторых вариантах осуществления частицы характеризуются насыпной плотностью менее приблизительно 0,6 г/см3. В некоторых вариантах осуществления частицы характеризуются насыпной плотностью от приблизительно 0,6 до приблизительно 0,2 г/см3.
Частицы йогексола могут иметь любое допустимое расстояние между частицами, которое способствует быстрому растворению. В некоторых вариантах осуществления частицы йогексола могут иметь расстояние между частицами приблизительно 50%, приблизительно 55%, приблизительно 60%, приблизительно 65%, приблизительно 70% приблизительно 75% приблизительно 80% приблизительно 85% приблизительно 90% приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% от насыпного объема с учетом всех величин, диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления частицы характеризуются расстоянием между частицами более приблизительно 40% от насыпного объема. В некоторых вариантах осуществления частицы характеризуются расстоянием между частицами более приблизительно 60% от насыпного объема. В некоторых вариантах осуществления частицы характеризуются расстоянием между частицами более приблизительно 70% от насыпного объема. В некоторых вариантах осуществления частицы характеризуются расстоянием между частицами от приблизительно 70 до приблизительно 95% от насыпного объема.
Частицы йогексола могут иметь любую допустимую удельную площадь поверхности, которая способствует быстрому растворению. В некоторых вариантах осуществления частицы йогексола могут иметь удельную площадь поверхности приблизительно 0,5 м2/г, 0,6 м2/г, приблизительно 0,7 м2/г, приблизительно 0,8 м2/г, приблизительно 0,9 м2/г, приблизительно 1 м2/г, приблизительно 1,5 м2/г, приблизительно 2,0 м2/г, приблизительно 2,5 м2/г, приблизительно 3 м2/г, приблизительно 3,5 м2/г, приблизительно 4,0 м2/г, приблизительно 4,5 м2/г, приблизительно 5,0 м2/г, приблизительно 5,5 м2/г, приблизительно 6,0 м2/г, приблизительно 6,5 м2/г, приблизительно 7,0 м2/г с учетом всех величин, диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления частицы имеют удельную площадь поверхности более приблизительно 0,5 м2/г. В некоторых вариантах осуществления частицы имеют удельную площадь поверхности более приблизительно 0,8 м2/г. В некоторых вариантах осуществления частицы имеют удельную площадь поверхности более приблизительно 4 м2/г. В некоторых вариантах осуществления частицы имеют удельную площадь поверхности от приблизительно 0,8 до приблизительно 5 м2/г.
В различных вариантах осуществления частицы йогексола по настоящему изобретению характеризуются двумя или более из следующих свойств: насыпной плотностью, расстоянием между частицами или удельной площадью поверхности, описанными в данном документе выше. В других вариантах осуществления частицы йогексола по настоящему изобретению характеризуются одним свойством из насыпной плотности, расстояния между частицами и удельной площади поверхности, как описано в данном документе выше. В некоторых вариантах осуществления частицы йогексола обладают одной или несколькими из следующих характеристик: насыпной плотностью менее приблизительно 0,8 г/см3; расстоянием между частицами более приблизительно 60% от насыпного объема и удельной площадью поверхности более приблизительно 0,8 м2/г.
В некоторых вариантах осуществления частицы характеризуются насыпной плотностью менее приблизительно 0,8 г/см3, расстоянием между частицами более приблизительно 60% от насыпного объема и удельной площадью поверхности более приблизительно 0,8 м2/г. В некоторых вариантах осуществления частицы характеризуются насыпной плотностью от приблизительно 0,6 до приблизительно 0,2 г/см3. В некоторых вариантах осуществления частицы характеризуются расстоянием между частицами от приблизительно 70 до приблизительно 95% от насыпного объема. В некоторых вариантах осуществления частицы имеют удельную площадь поверхности от приблизительно 0,8 до приблизительно 5 м2/г. В некоторых вариантах осуществления частицы характеризуются насыпной плотностью от приблизительно 0,6 до приблизительно 0,2 г/см3, расстоянием между частицами от приблизительно 70 до приблизительно 95% от насыпного объема и удельной площадью поверхности от приблизительно 0,8 до приблизительно 5 м2/г. В некоторых вариантах осуществления частицы характеризуются насыпной плотностью приблизительно 0,5 г/см³, расстояние между частицами составляет приблизительно 70% от насыпного объема и удельная площадь поверхности составляет приблизительно 4 м²/г.
В некоторых вариантах осуществления частицы йогексола содержат кристаллы йогексола, например, в форме порошка кристаллического йогексола. Такие кристаллы йогексола могут быть охарактеризованы посредством методик кристаллографии, таких как (но без ограничения) рентгенодифракционный анализ, дифракция нейтронов, дифракция электронов и/или подобные. В некоторых вариантах осуществления кристаллы йогексола могут быть охарактеризованы с помощью дифракционных рентгенограмм, или с помощью одного или нескольких параметров кристаллической решетки, или их комбинаций, например, как описано в данном документе.
В некоторых вариантах осуществления для кристаллов йогексола могут характеризоваться порошковой дифракционной рентгенограммой, практически идентичной приведенной на фигуре 1, например, с пиками 2θ при приблизительно 7,6°, приблизительно 10,6°, приблизительно 12,1°, приблизительно 16,2°, приблизительно 18,1°, приблизительно 19,7°, приблизительно 19,9°, приблизительно 20,8°, приблизительно 22,3°, приблизительно 22,7°, приблизительно 22,9°, приблизительно 26,1°, приблизительно 26,2°, приблизительно 29,8°, приблизительно 29,9°, приблизительно 30,3° и приблизительно 30,7°.
В некоторых вариантах осуществления кристаллы йогексола могут иметь следующие параметры элементарной ячейки при T=293K: a =14,722(3) Å, b=18,921(4) Å, c=9,295(2) Å, α=90°, β=91,281(3)°, γ=90° и моноклинная пространственная группа P21/c.
В некоторых вариантах осуществления кристаллы йогексола характеризуются порошковой дифракционной рентгенограммой с пиками 2θ при приблизительно 7,6°, 16,2°, 19,9°, 20,8°, 22,3°, 29,8° и 30,7°. Кроме того, в некоторых вариантах осуществления кристаллы йогексола имеют параметры элементарной ячейки при T=293K: a =14,722(3) Å, b=18,921(4) Å, c=9,295(2) Å, α=90°, β=91,281(3)°, γ=90° и моноклинная пространственная группа P21/c.
В некоторых вариантах осуществления кристаллы йогексола характеризуются порошковой дифракционной рентгенограммой с 2θ пиками при приблизительно 7,6°, 10,6°, 12,1°, 16,2°, 18,1°, 19,7°, 19,9°, 20,8°, 22,3°, 22,7°, 22,9°, 26,1°, 26,2°, 29,8°, 29,9°, 30,3° и 30,7°. Кроме того, в некоторых вариантах осуществления кристаллы йогексола имеют параметры элементарной ячейки при T=293K: a =14,722(3) Å, b=18,921(4) Å, c=9,295(2) Å, α=90°, β=91,281(3)°, γ=90° и моноклинная пространственная группа P21/c.
В некоторых вариантах осуществления кристаллы йогексола имеют параметры элементарной ячейки при T=293K: a =14,722(3) Å, b=18,921(4) Å, c=9,295(2) Å, α=90°, β=91,281(3)°, γ=90° и моноклинная пространственная группа P21/c.
В некоторых вариантах осуществления частицы йогексола могут быть агломератами из более мелких частиц, например, агломератами из более мелких непористых частиц.
В некоторых вариантах осуществления настоящего изобретения композиция на основе контрастного средства содержит частицы йогексола, полученные путем кристаллизации йогексола из смеси растворителей. В некоторых вариантах осуществления смесь растворителей может содержать один или несколько растворителей, выбранных из спирта, алкилового сложного эфира и воды. В конкретных вариантах осуществления смесь растворителей содержит спирт, алкиловый сложный эфир и воду. В некоторых вариантах осуществления стадия кристаллизации может быть осуществлена путем нагревания или кипячения с обратным холодильником смеси растворителей, как описано в данном документе. В других вариантах осуществления стадия кристаллизации может быть осуществлена путем нагревания или кипячения с обратным холодильником смеси растворителей с интенсивным перемешиванием.
В различных вариантах осуществления спирт может быть выбран из группы, состоящей из этанола, 2-пропанола, 1-пропанола, 1-бутанола и их комбинаций. В различных вариантах осуществления алкиловый сложный эфир может быть выбран из группы, состоящей из метилацетата, этилацетата, пропилацетата, изопропилацетата, бутилацетата и их комбинаций.
В различных вариантах осуществления смесь растворителей содержит один или несколько спиртов, описанных в данном документе и один или несколько алкиловых сложных эфиров, описанных в данном документе. В других вариантах осуществления смесь растворителей содержит один или несколько спиртов, описанных в данном документе, один или несколько алкиловых сложных эфиров, описанных в данном документе, и воду. В конкретных вариантах осуществления смесь растворителей содержит этанол и этилацетат. В других конкретных вариантах осуществления смесь растворителей содержит этанол, этилацетат и воду.
В некоторых вариантах осуществления смесь растворителей может содержать приблизительно 90% (вес/об.) спирта, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 98% любого из спиртов, описанных в данном документе, с учетом всех величин, диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления смесь растворителей может содержать приблизительно 95-97% (вес/об.) спирта. В конкретных вариантах осуществления смесь растворителей содержит приблизительно 95-97% (вес/об.) этанола.
В некоторых вариантах осуществления смесь растворителей может содержать менее приблизительно 1% (вес/об.) любого из алкиловых сложных эфиров, описанных в данном документе, или может содержать приблизительно 1%, приблизительно 1,5%, приблизительно 2%, приблизительно 2,5%, приблизительно 3%, приблизительно 4%, приблизительно 4,5%, приблизительно 5%, приблизительно 5,5%, приблизительно 6%, приблизительно 6,5%, приблизительно 7% алкилового сложного эфира, включая все промежуточные величины, диапазоны и поддиапазоны. В некоторых вариантах осуществления смесь растворителей может содержать приблизительно 2-5% (вес/об.) алкилового сложного эфира.
В некоторых вариантах осуществления смесь растворителей может содержать менее приблизительно 0,05% (вес/об.) воды или может содержать приблизительно 0,08%, приблизительно 0,1%, приблизительно 0,3%, приблизительно 0,5%, приблизительно 0,8%, приблизительно 1,2%, приблизительно 1,6%, приблизительно 1,8%, приблизительно 2%, приблизительно 2,2%, приблизительно 2,4%, приблизительно 2,8%, приблизительно 3%, приблизительно 3,5% воды с учетом всех величин, диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления смесь растворителей содержит приблизительно 0,1-2% (вес/об.) воды.
В конкретных вариантах осуществления смесь растворителей содержит приблизительно 95-97% этанола, приблизительно 2-5% алкилацетата и приблизительно 0,1-2% воды.
Способ может дополнительно включать удаление из раствора йогексола по меньшей мере части одного или нескольких из спирта, алкилацетата и воды. В некоторых вариантах осуществления удаление по меньшей мере части спирта, алкилацетата и/или воды может включать дистилляцию раствора йогексола. В некоторых вариантах осуществления дистилляция может представлять собой азеотропную дистилляцию. В некоторых вариантах осуществления способ дополнительно включает (b) удаление по меньшей мере части одного или нескольких из спирта, алкилацетата и воды путем дистилляции раствора йогексола. Дистилляция может быть осуществлена при атмосферном давлении или, в качестве альтернативы, при пониженном давлении или повышенном давлении (относительно атмосферного).
Способ может дополнительно включать поддержание раствора йогексола при встряхивании при температуре от приблизительно 40°C, приблизительно 45°C, приблизительно 50°C, приблизительно 55°C, приблизительно 60°C, приблизительно 65°C, приблизительно 70°C, приблизительно 75°C до температуры кипения с учетом всех величин, диапазонов и поддиапазонов между ними, посредством чего получают суспензию кристаллов, по сути, на основе экзойогексола. Температуру раствора йогексола, можно поддерживать при атмосферном давлении или, в качестве альтернативы, при пониженном или повышенном давлении относительно атмосферного давления. В некоторых вариантах осуществления способ дополнительно включает (c) поддержание раствора йогексола при встряхивании при температуре от 60°C вплоть до температуры кипения (при пониженном давлении, атмосферном давлении или повышенном давлении), посредством чего получают суспензию кристаллов, по сути, на основе экзойогексола.
Способ может дополнительно включать охлаждение суспензии из этапа (b) до приблизительно 30°C, приблизительно 35°C, приблизительно 40°C, приблизительно 45°C, приблизительно 50°C, приблизительно 55°C, приблизительно 60°C, включая все промежуточные величины, диапазоны и поддиапазоны. Способ может включать охлаждение суспензии при встряхивании или без него. В некоторых вариантах осуществления способ дополнительно включает (d) охлаждение суспензии из этапа (b) до приблизительно 40-50°C при встряхивании.
Способ может дополнительно включать обработку суспензии посредством одного или нескольких процессов, таких как без ограничения промывка, высушивание (включая вакуумную сушку), фильтрование и/или подобные. В некоторых вариантах осуществления способ дополнительно включает (e) фильтрование и высушивание суспензии. В некоторых вариантах осуществления с помощью дистилляции можно получить раствор (перед кристаллизацией), содержащий приблизительно 10% (вес/об.) йогексола, приблизительно 15%, приблизительно 18%, приблизительно 20%, приблизительно 22%, приблизительно 25%, приблизительно 27%, приблизительно 30%, приблизительно 35% йогексола, включая все величины, диапазоны и поддиапазоны между ними. В некоторых вариантах осуществления с помощью дистилляции можно получить раствор, содержащий приблизительно 20-25% (вес/об.) йогексола.
В некоторых вариантах осуществления с помощью дистилляции обеспечивают раствор перед кристаллизацией, содержащий приблизительно 20-25% (вес/об.) йогексола, приблизительно 95-97% спирта, приблизительно 2-5% алкилового сложного эфира и приблизительно 0,1-2% воды.
Способ может дополнительно включать поддержание раствора йогексола (как описано в данном документе) при встряхивании и при температуре от приблизительно 40°C до температуры кипения, от приблизительно 45°C, приблизительно 50°C, приблизительно 55°C, приблизительно 60°C, приблизительно 65°C, приблизительно 70°C, приблизительно 75°C до температуры кипения, включая все величины, диапазоны и поддиапазоны между ними, посредством чего получают суспензию кристаллов, по сути, на основе экзойогексола. В некоторых вариантах осуществления способ дополнительно включает (c) поддержание раствора йогексола (как описано в данном документе) при встряхивании и при температуре от 60°C вплоть до температуры кипения, посредством чего получают суспензию кристаллов, по сути, на основе экзойогексола.
Способ может дополнительно включать охлаждение суспензии из этапа (b) до приблизительно 30°C, приблизительно 35°C, приблизительно 40°C, приблизительно 45°C, приблизительно 50°C, приблизительно 55°C, приблизительно 60°C, включая все промежуточные величины, диапазоны и поддиапазоны при встряхивании. В некоторых вариантах осуществления способ дополнительно включает (d) охлаждение суспензии из этапа (b) до приблизительно 40-50°C при встряхивании.
Способ может дополнительно включать обработку суспензии посредством одной или нескольких обработок, таких как без ограничения промывка, высушивание (включая вакуумную сушку), фильтрование и/или подобные. В некоторых вариантах осуществления способ дополнительно включает (e) фильтрование и высушивание суспензии.
В некоторых вариантах осуществления настоящего изобретения композиция на основе контрастного средства включает частицы йогексола с конкретным распределением частиц по размеру, как описано в данном документе. Например, распределение частиц йогексола по размеру может иметь D90 приблизительно 10 мкм, приблизительно 11 мкм, приблизительно 12 мкм, приблизительно 13 мкм, приблизительно 14 мкм, приблизительно 15 мкм, приблизительно 16 мкм, приблизительно 17 мкм, приблизительно 18 мкм, приблизительно 19 мкм, приблизительно 20 мкм, приблизительно 21 мкм, приблизительно 22 мкм, приблизительно 23 мкм, приблизительно 24 мкм, приблизительно 25 мкм, приблизительно 26 мкм, приблизительно 27 мкм, приблизительно 28 мкм, приблизительно 29 мкм, приблизительно 30 мкм, приблизительно 31 мкм, приблизительно 32 мкм, приблизительно 33 мкм, приблизительно 34 мкм, приблизительно 35 мкм, приблизительно 36 мкм, приблизительно 37 мкм, приблизительно 38 мкм, приблизительно 39 мкм или приблизительно 40 мкм с учетом всех диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления распределение частиц по размеру имеет D90 не более приблизительно 40 мкм.
В некоторых вариантах осуществления распределение частиц по размеру имеет D50 приблизительно 5 мкм, приблизительно 6 мкм, приблизительно 7 мкм, приблизительно 8 мкм, приблизительно 9 мкм, приблизительно 10 мкм, приблизительно 11 мкм, приблизительно 12 мкм, приблизительно 13 мкм, приблизительно 14 мкм, приблизительно 15 мкм, приблизительно 16 мкм, приблизительно 17 мкм, приблизительно 18 мкм, приблизительно 19 мкм или приблизительно 20 мкм с учетом всех величин, диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления распределение частиц по размеру имеет D50 не более приблизительно 20 мкм.
В некоторых вариантах осуществления распределение частиц по размеру имеет D10 приблизительно 2 мкм, приблизительно 3 мкм, приблизительно 4 мкм, приблизительно 5 мкм, приблизительно 6 мкм, приблизительно 7 мкм, приблизительно 8 мкм, приблизительно 9 мкм, приблизительно 10 мкм или приблизительно 12 мкм с учетом всех величин, диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления распределение частиц по размеру имеет D10 не более приблизительно 11 мкм.
В некоторых вариантах осуществления композиция на основе контрастного средства содержит частицы йогексола с распределением частиц по размеру при наличии одной или нескольких из следующих характеристик: D 90, как описано в данном документе, D50, как описано в данном документе и D10, как описано в данном документе. В конкретном варианте осуществления композиция на основе контрастного средства содержит частицы йогексола с D90 не более приблизительно 40 мкм, D50 не более приблизительно 20 мкм и D10 не более приблизительно 10 мкм.
В некоторых вариантах осуществления композиция на основе контрастного средства может быть получена путем высушивания распылением раствора йогексола с применением конкретных условий высушивания распылением, которые обеспечивают частицы йогексола, которые быстро растворяются. Можно применять распылительную сушилку любой подходящей конфигурации, включая распылительные сушилки с распыляющим наконечником, центробежным распылителем, противоточной и прямоточной конфигурациями и т. д. В частности, температура на входе и на выходе из распылительной сушилки влияет на скорость растворения частиц йогексола, полученных таким образом. В таких вариантах осуществления температура на входе в распылительную сушилку (например, для водных растворов йогексола) может составлять приблизительно 200°C, приблизительно 210°C, приблизительно 215°C, приблизительно 220°C, приблизительно 230°C, приблизительно 240°C, приблизительно 245°C, приблизительно 250°C, приблизительно 255°C, приблизительно 260°C, приблизительно 270°C, приблизительно 280°C с учетом всех величин, диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления температура на входе в распылительную сушилку может находиться в диапазоне приблизительно 220-255°C. В некоторых вариантах осуществления температура на выходе из распылительной сушилки может составлять приблизительно 70°C, приблизительно 80°C, приблизительно 85°C, приблизительно 90°C, приблизительно 95°C, приблизительно 100°C, приблизительно 105°C, приблизительно 110°C, приблизительно 115°C, приблизительно 120°C, приблизительно 130°C, приблизительно 140°C с учетом всех величин, диапазонов и поддиапазонов между ними. В некоторых вариантах осуществления температура на выходе из распылительной сушилки может находиться в диапазоне приблизительно 95-115°C.
В некоторых вариантах осуществления композицию на основе контрастного средства получают путем высушивания распылением раствора йогексола. В некоторых вариантах осуществления температура на входе в распылительную сушилку находится в диапазоне приблизительно 220-255°C и температура на выходе находится в диапазоне приблизительно 95-115°C.
В некоторых вариантах осуществления высушивание распылением раствора йогексола может включать работу распылителя (например, центробежного распылителя) распылительной сушилки при RPM (количество оборотов в минуту) приблизительно 15000, приблизительно 20000, приблизительно 22000, приблизительно 24000, приблизительно 25000, приблизительно 26000, приблизительно 28000, приблизительно 30000, приблизительно 35000 и всех промежуточных величинах, диапазонах и поддиапазонах. В некоторых вариантах осуществления RPM распылителя составляет приблизительно 25000. В конкретных вариантах осуществления температура на входе и температура на выходе, а также режимы распылителя являются такими, как описано в данном документе.
В некоторых вариантах осуществления раствор йогексола может иметь концентрацию приблизительно 20% (вес/вес), приблизительно 25% (вес/вес), приблизительно 27% (вес/вес), приблизительно 29% (вес/вес), приблизительно 30% (вес/вес), приблизительно 31% (вес/вес), приблизительно 33% (вес/вес), приблизительно 35% (вес/вес), приблизительно 37% (вес/вес), приблизительно 39% (вес/вес), приблизительно 40% (вес/вес), приблизительно 41% (вес/вес), приблизительно 43% (вес/вес), приблизительно 45% (вес/вес), включая все промежуточные величины, диапазоны и поддиапазоны. В некоторых вариантах осуществления раствор йогексола имеет концентрацию приблизительно 30-40% (вес/вес).
Для высушивания распылением может быть использован любой подходящий растворитель, обеспечивающий растворение йогексола в данном процессе. Неограничивающий перечень подходящих растворителей для высушивания распылением йогексола включает воду и спирты, такие как этиловый спирт. В других вариантах осуществления могут применяться смеси из воды и органических растворителей (например, спиртов и/или алкилацетатов), в которых вода обеспечивает солюбилизацию йогексола, пока не будет высушена распылением.
В некоторых вариантах осуществления настоящего изобретения частицы йогексола получают путем высушивания распылением 30-40% (вес/вес) раствора йогексола. В некоторых вариантах осуществления температура на входе в распылительную сушилку находится в диапазоне приблизительно 220-255°C и температура на выходе находится в диапазоне приблизительно 95-115°C. В других вариантах осуществления высушенный распылением йогексол имеет распределение частиц по размеру, описанное в данном документе.
Различные варианты осуществления настоящего изобретения также включают кристаллы йогексола, полученные посредством любого способа получения кристаллов йогексола, описанного в данном документе.
Различные варианты осуществления настоящего изобретения также включают композицию на основе контрастного средства, включающую кристаллы йогексола, полученные посредством любого способа получения кристаллов йогексола, описанного в данном документе.
В некоторых вариантах осуществления способ получения йогексольного контрастного раствора может включать добавление фармацевтически приемлемого водного растворителя в емкость, содержащую любую композицию на основе контрастного средства, описанную в данном документе. В некоторых вариантах осуществления емкость может быть такой, как описана в заявке на патент США №13/934654, поданной 3 июля 2013 г., под названием "CONTAINER WITH CONCENTRATED SUBSTANCE AND METHOD OF USING THE SAME", полное раскрытие которой включено в данный документ посредством ссылки во всей ее полноте.
Способ может дополнительно включать встряхивание емкости таким образом, чтобы растворилось практически все контрастное средство на основе йогексола. В некоторых вариантах осуществления встряхивание может осуществляться в течение приблизительно 30 секунд, приблизительно 35 секунд, приблизительно 40 секунд, приблизительно 45 секунд, 50 секунд, в течение приблизительно 60 секунд, приблизительно 70 секунд, приблизительно 80 секунд, приблизительно 85 секунд, приблизительно 90 секунд, приблизительно 95 секунд, приблизительно 100 секунд, приблизительно 110 секунд, приблизительно 120 секунд, приблизительно 130 секунд, включая все промежуточные величины, диапазоны и поддиапазоны. В некоторых вариантах осуществления встряхивание может осуществляться в течение не более приблизительно 90 секунд. В некоторых вариантах осуществления встряхивание может осуществляться в течение не более приблизительно 60 секунд. В некоторых вариантах осуществления встряхивание может осуществляться в течение не более приблизительно 40 секунд. Встряхивание может предусматривать встряхивание вручную, автоматизированное встряхивание или любую их комбинацию. В конкретных вариантах осуществления встряхивание предусматривает встряхивание вручную.
В некоторых вариантах осуществления способ получения йогексольного контрастного раствора может включать добавление фармацевтически приемлемого водного растворителя в емкость, содержащую композицию на основе контрастного средства, которая включает частицы йогексола, которые могут в значительной степени растворяться в воде за приблизительно 5 секунд, приблизительно 10 секунд, приблизительно 20 секунд, приблизительно 30 секунд, приблизительно 40 секунд, приблизительно 50 секунд, приблизительно 60 секунд, приблизительно 70 секунд, приблизительно 80 секунд, включая все промежуточные величины, диапазоны и поддиапазоны при испытании с применением модифицированного способа 641 Фармакопеи Соединенных Штатов Америки. В некоторых вариантах осуществления способ получения йогексольного контрастного раствора включает (a) добавление фармацевтически приемлемого водного растворителя в емкость, содержащую композицию на основе контрастного средства, которая включает частицы йогексола, которые могут в значительной степени растворяться в воде за приблизительно 60 секунд при испытании с применением модифицированного способа 641 Фармакопеи Соединенных Штатов Америки.
Способ дополнительно может включать встряхивание емкости в течение не более приблизительно 30 секунд, приблизительно 35 секунд, приблизительно 40 секунд, приблизительно 45 секунд, 50 секунд, в течение приблизительно 60 секунд, приблизительно 70 секунд, приблизительно 80 секунд, приблизительно 85 секунд, приблизительно 90 секунд, приблизительно 95 секунд, приблизительно 100 секунд, приблизительно 110 секунд, приблизительно 120 секунд, приблизительно 130 секунд, включая все величины, диапазоны и поддиапазоны между ними. Встряхивание может предусматривать встряхивание вручную, автоматизированное встряхивание или любую их комбинацию. В некоторых вариантах осуществления способ дополнительно включает (b) встряхивание емкости в течение не более приблизительно 90 секунд, посредством чего растворяется практически все йогексольное контрастное средство. В некоторых вариантах осуществления этап (b) представляет собой встряхивание вручную. В некоторых вариантах осуществления емкость встряхивают вручную в течение не более приблизительно 60 секунд. В некоторых вариантах осуществления емкость встряхивают вручную в течение не более приблизительно 40 секунд.
Некоторые варианты осуществления настоящего изобретения направлены на введение йогексольного контрастного раствора нуждающемуся в этом пациенту, а именно, например, перед процедурой визуализации, проводимой пациенту. Введение может включать получение йогексольного контрастного раствора, как описано в данном документе, и введение йогексольного контрастного раствора пациенту, например, путем перорального введения.
В некоторых вариантах осуществления введение йогексольного контрастного раствора нуждающемуся в этом пациенту включает (a) добавление фармацевтически приемлемого водного растворителя в емкость, содержащую композицию на основе контрастного средства, включающую частицы йогексола, которые в значительной степени растворяются в воде за приблизительно 60 секунд при испытании с применением модифицированного способа 641 Фармакопеи Соединенных Штатов Америки. Введение дополнительно предусматривает (b) встряхивание емкости в течение не более 90 секунд, посредством чего растворяется практически все йогексольное контрастное средство. Введение дополнительно предусматривает введение пациенту контрастного раствора.
В различных вариантах осуществления процессы, описанные в данном документе, могут обеспечивать особые форму(формы) и размер(ы) частиц и распределение частиц йогексола по размеру, которые в свою очередь могут улучшать характеристики растворимости йогексола. Например, частицы йогексола, кристаллизированные согласно способам, описанным в данном документе, могут быть охарактеризованы как агломераты из более мелких кристаллов с высокой удельной площадью поверхности. Такая высокая удельная площадь поверхности может обеспечивать обширный контакт с растворителем в процессе восстановления композиций, содержащих такие формы йогексола, что приводит в результате к повышению скорости растворения без образования липких масс на основе йогексола в дистилляционном сосуде в ходе процесса растворения. Обычный высушенный распылением йогексол, из которого, как правило, образуются частицы сферической формы с низкой площадью поверхности, имеет более низкую (более медленную) скорость растворения по сравнению со скоростью растворения кристаллизированного или высушенного распылением йогексола согласно настоящему изобретению.
Различные варианты осуществления, раскрытые в данном документе, обеспечены для кристаллизации йогексола и преимущественного образования экзоизомеров. Другими словами, образованный йогексол, таким образом, содержит, по сути, экзоизомеры. Исходя из наблюдений (смотри примеры ниже), экзойогексол имеет более низкую тенденцию к поглощению влаги, чем йогексол природного происхождения, который, как правило, содержит как эндо-, так и экзоизомеры. Каждый поворотный изомер (экзо- и эндо-) может иметь различную кристаллическую структуру. Полагают, что такое различие может повлечь за собой разную степень водопроницаемости кристаллической решетки, что приводит в результате к более быстрому растворению изомера экзойогексола. Таким образом, в тех вариантах осуществления настоящего изобретения, в которых главным образом обеспечивается экзойогексол, может быть обеспечено более быстрое растворение по сравнению с обычными составами, содержащими смесь эндо- и экзойогексола.
В других вариантах осуществления, раскрытых в данном документе, соотношение эндо- и экзоизомеров йогексола в композиции может быть изменено путем изменения композиции смеси растворителей, применяемой в процессе кристаллизации, например, путем изменения соотношения, например, воды, этилацетата и этанола, применяемых при кристаллизации.
Обычно для получения и дозирования йодированного контрастного вещества требуется комбинация отдельных компонентов, для того чтобы получить разовую дозу (однократную дозу), которая доставляется пациенту. Такие компоненты включают без ограничения бутылку жидкости, концентрированное контрастное вещество, измерительное устройство, такое как шприц или другое измерительное устройство, и одну или две чаши для дозирования. Варианты осуществления, раскрытые в данном документе, могут быть применимы как часть автономного комплекта для перорального введения контрастного вещества, где все эти компоненты могут быть обеспечены как часть комплекта.
[0100] Композиции по настоящему изобретению могут быть разбавлены различными растворителями, которые обеспечивают стабильные растворы, пригодные для потребления человеком. Данные растворители могут включать, например, напитки, такие как лимонад (например, порошкообразный лимонад или другие смеси напитков с фруктовым ароматизатором), спортивные напитки (например, изотонические спортивные напитки), множество фруктовых соков, воду, молочную смесь и т. д. Такие ароматизированные растворители предназначены для улучшения соблюдения больным режима и схемы лечения (т. е. вероятности, что пациент допьет всю дозу) за счет маскировки любого отталкивающего или неприятного запаха йогексола.
ПРИМЕРЫ
Пример 1
Готовили четыре образца порошка из частиц йогексола согласно настоящему изобретению для дальнейшего структурного анализа (таблица 1)
Таблица 1
Сбор данных
Применяли два способа для определения характеристик кристаллов:
a) рентгенографический анализ порошка - измеряли небольшое количество всех четырех образцов;
b) рентгенографическое определение структуры - в образце JM-081213_н-бутанола находили подходящий монокристалл йогексола и непосредственно помещали на гониометрическую головку для определения структуры кристалла.
Результаты
Рентгенографический анализ порошка
Все четыре измеренных образца имели похожие порошковые рентгенограммы, показанные на ФИГ. 1. Число пиков для всех четырех образцов в диапазоне 2θ (5-20°, достоверно разделенные пики) является аналогичным, и положения пиков могут быть достоверно определены как приблизительно такие же в пределах погрешности эксперимента. Согласно рассматриваемым рентгенограммам все четыре образца, по-видимому, имеют практически одинаковую кристаллическую структуру (смотри ФИГ. 1), при этом они очень похожи на рентгенограмму порошка, полученную посредством расчета исходя из данных кристаллической структуры. Относительные интенсивности пиков являются похожими для образцов JM-081213_н-пропанол, JM-081213_IPA и JM-111013 и сравнимы с таковыми, рассчитанными исходя из данных кристаллической структуры.
Параметры элементарной ячейки для образца JM-111013
Автоматическое индексирование результатов, полученных с применением DICVOL04, показывает, что образованные кристаллы йогексола являются моноклинными с пространственной группой P21/c, и параметры элементарной ячейки уточняли методом наименьших квадратов для величин:
a=14,722(3) Å, α=90°
b=18,921(4) Å, β=91,281(3)°
c=9,295(2) Å, γ=90°
Объем: 2589(1) ų
Класс кристалла: моноклинный
Ячейка определена из: 107 отражений
Диапазон ячеек 2θ=5-60°
Температура: 293 K
Пример 2 - оценка разницы между временем растворения йогексольных веществ, полученных посредством разных методик выделения
Образцы
1) Кристаллизированный йогексол согласно настоящему изобретению - две партии, 03302012 и 01206013.
2) Обычный высушенный распылением йогексол - две партии, обозначенные как "Стандартные образцы №1 и №2".
4) Йогексол, высушенный распылением согласно настоящему изобретению - партия 03202012/1.
5) Йогексол, высушенный распылением согласно настоящему изобретению и согласно модифицированной процедуре, партия 03202012/8.
6) Йогексол, высушенный распылением согласно настоящему изобретению и согласно модифицированной процедуре, партия 03202012/9.
Материалы и устройство для испытания
20 унций (600 мл) модифицированного напитка в PET бутылке в виде продукта растворения йогексольного порошка для перорального приема; 50 мл стеклянный цилиндр для испытания; водопроводная вода.
Образцы подвергали испытанию с применением модифицированного способа <641> USP, описанного в данном документе.
Результаты
Таблица 4 Результаты
1 мин 30 с
1 мин 30 с
Йогексол, кристаллизированный согласно настоящему изобретению, образовывал очень мелкие частицы, агрегированные в кластер с очень большой площадью поверхности и расстоянием между частицами. Этот материал быстро растворялся.
Наихудшие результаты были получены для стандартного высушенного распылением йогексола, который обеспечивал неприемлемое время растворения - 1 мин 30 с. Данный материал имел меньшую площадь поверхности по сравнению с кристаллизированным йогексолом. Кроме того, порошок стандартно высушенного распылением йогексола после наливания воды в бутылку образовывал клееподобный слой, который прилипал ко дну и увеличивал время растворения.
Высушенный распылением материал готовили с применением различных режимов: режимов обычного высушивания распылением (температура на входе 255°C, на выходе 95°C) и модифицированных режимов высушивания распылением (температура на входе 220°C, на выходе 75°C; и температура на входе 220°C, на выходе 115°C). Наилучшие показатели обеспечивал один из модифицированных режимов высушивания распылением (температура на входе 220°C, на выходе 115°C), который обеспечивал более мелкие частицы йогексола. Улучшенный размер частицы получали посредством наличия более мелких частиц в целом (D50 приблизительно 16 микрон) и очень узкого диапазона распределения частиц по размеру, практически без частиц более 30 микрон. Для сравнения распределение частиц по размеру, полученное посредством обычных способов высушивания распылением, является намного более широким, со значительным количеством частиц, больших, чем 30 микрон и существенным количеством больших, чем 50 микрон.
Пример 3 - оценка морфологии частицы, скелетной, насыпной плотностей и удельных площадей поверхности полученного различным образом йогексола
Твердый йогексол получали посредством кристаллизации или посредством высушивания распылением. Было установлено, что способ получения твердой фазы определяет скорость растворения йогексола. Образцы идентифицированы как кристаллизированный йогексол или высушенный распылением йогексол. Каждый тип йогексола был представлен несколькими образцами. Некоторые образцы также выдерживали в лабораторной атмосфере (например, окружающей атмосфере) и затем анализировали.
Морфологию частицы оценивали посредством сканирующей электронной микроскопии (SEM) в сочетании с ионным микроскопом FIB-SEM Tescan Lyra3GU, оборудованным некоторым количеством детекторов EDS, EBSD, STEM, EBIC и TOF-SIMS. Вследствие непроводящей природы йогексола, он аккумулирует электрический заряд, который является причиной ухудшения изображений SEM. В связи с этим образцы йогексола покрывали тонким слоем платины с целью устранения электрических зарядов и посредством этого получали изображения SEM высокого качества.
Удельную площадь поверхности измеряли с помощью прибора для низкотемпературной адсорбции азота Pulse Chemisorb 2700.
Кристаллизированный йогексол
Изображения SEM показывают, что кристаллизированный йогексол образует агломераты частиц сферической/эллиптической формы, в которых характеристические размеры отдельных частиц составляют приблизительно 0,5-3 мкм, как показано на ФИГ. 2. Также, длинные кристаллы столбчатой формы наблюдали во всех образцах кристаллизированного йогексола (ФИГ. 3). Такие частицы столбчатой формы предположительно образовывались на краях кристаллизационного сосуда при низкой или нулевой интенсивности перемешивания. Данное предположение было подтверждено в ходе эксперимента кристаллизации без перемешивания, когда были получены длинные кристаллы столбчатой формы длиной вплоть до 100 мкм и диаметром 3-5 мкм (ФИГ. 4).
Образцы кристаллизированного йогексола также испытывали с помощью анализа SME в отношении влияния влажности воздуха (т.е., влажности воздуха окружающей среды/помещения). Образцы кристаллизированного йогексола выдерживали при влажности воздуха в течение 120 часов. После выдерживания наблюдали агломерацию первоначально отделенных частиц (ФИГ. 5).
Пористость частиц йогексола также изучали путем вдавливания ртути, а скелетную плотность определяли гелиевым пикнометром и посредством физической адсорбции азота.
Распределение частиц по размеру, полученное посредством ртутной порометрии (ФИГ. 6), показывает наличие пространств между агломератами и между частицами с характеристическими размерами, указанными выше (0,5-3 мкм). Полости между агломератами имели приблизительный размер между приблизительно 1 и приблизительно 100 мкм. После того так эти данные были получены посредством ртутной порометрии, размер полости можно было определить как радиус цилиндрической поры. Меньшие полости соответствовали расстояниям между частицами. Характерный максимум при 300 нм (смотри характерный пик на ФИГ. 6) соответствует размеру наиболее узкой области (окну), в которой соприкасаются три сферические частицы с радиусом приблизительно 3 мкм. При высоких давлениях наблюдали дополнительное увеличение количества вытесненной ртути. Этот результат исключает наличие очень малых открытых полостей или пор и поэтому предполагают, что такие малые частицы не являются пористыми.
Данные относительно удельной площади поверхности, которые оценивали с применением изотермы BET, подтверждают непористую природу/характер частиц. Измеренная величина удельной площади поверхности составляла приблизительно 2,8 м2/г, что согласуется с расчетом удельной площади поверхности гипотетического материала, который состоит из непористых сфер с радиусом 3 мкм. С учетом скелетной плотности кристаллизированного йогексола (2,097 г/см3), рассчитанная удельная площадь поверхности данного гипотетического материала составляет приблизительно 4 м2/г. Все данные, полученные с помощью анализа очевидно подтверждают вывод о том, что твердый материал кристаллизированного йогексола содержит агломераты, состоящие из малых непористых частиц и что общая удельная площадь представляет собой сумму внешних площадей поверхности этих частиц.
Высушенный распылением йогексол
Для оценки были выбраны три различных образца высушенного распылением йогексола:
1) высушенный распылением йогексол, полученный согласно настоящему изобретению с применением режимов высушивания распылением, описанных выше в примере 2 (партия номер 00405003);
2) обычный высушенный распылением йогексол (стандартный образец №2);
3) только что полученный высушенный распылением йогексол (партия номер 03202012/1) согласно настоящему изобретению получен при тех же условиях, которые применяли для образца номер 00405003, указанного выше.
Во всех образцах частицы представляют собой отдельные единицы без механической связи с другими частицами. Размеры частиц образцов 1) или 3) являются практически одинаковыми и демонстрируют два основных размера. Первая величина составляет приблизительно 10 мкм и вторая величина составляет приблизительно 25 мкм (смотри ФИГ. 7). Морфология поверхности частиц характеризуется наличием углублений и кратеров.
Для сравнения с образцами 1) и 3) образец стандартно высушенного распылением йогексола 2) (ФИГ. 8) является более однородным относительно распределения характеристических размеров частиц. Также, образец частиц 2) демонстрирует менее шероховатую поверхность (мелкие углубления и кратеры). Поверхность покрывается пленкой, аналогичной агломерированному кристаллизированному материалу, представленному на ФИГ. 5, т.е. после его выдерживания при влажности воздуха. Образец 2) также демонстрирует несколько мостиков между частицами.
С целью обнаружения возможных пор или полостей внутри частиц, одна выбранная сферическая частица образца 1) была разрезана при помощи пучка ионов. Анализ изображения SEM (смотри ФИГ. 9A-9C) не показывает никакой пористости. Кроме того, скелетная плотность (2,029 г/см3) практически тождественна величине, полученной для кристаллизированного йогексола, который, как рассмотрено выше, является очевидно непористым, и поэтому гипотетическое существование скрытой пористости в стандартно высушенном распылением йогексоле можно исключить. Удельная поверхность высушенных распылением йогексольных материалов в соответствии с данным исследованием оказалась менее 1 м2/г. Эту величину определяли с учетом предела обнаружения прибора и с применением способа, описанного в данном документе.
Сравнением определенных количеств азота, десорбированного из образцов, получен оценочный показатель, состоящий в том, что возможное значение удельной площади поверхности высушенного распылением йогексола в приблизительно 12-15 раз ниже, чем кристаллизированного йогексола. Эти результаты также сопоставимы с теоретическими величинами удельной площади поверхности, основанными на предположении, что частицы представляют собой простые геометрические тела с размерами согласно изображениям SEM.
Обсуждение величин удельной площади поверхности
Экспериментально полученные величины удельной площади поверхности являются очень низкими, что является типичным для от крупнопористых до непористых материалов. Величины экспериментальной удельной площади поверхности для всех образцовнаходятся в хорошем соответствии с предполагаемыми на основе анализа изображения SEM величинами (т.е. площадь поверхности частицы, рассчитанная на основе геометрической формы частицы, и при условии, что частицы не являются пористыми (подтверждено посредством ртутной порометрии, как рассмотрено выше)). Индивидуальные величины и сравнения количества десорбции азота для каждого образца обобщены в таблице 5.
Таблица 5 Величины удельной площади поверхности образцов йогексола
[м2/г]
[м2/г]
Ad/Ad(кристаллизированный)
a при условии, что сфера с диаметром 3 мкм
b при условии, что сферы двух размеров (10 мкм и 25 мкм) с одинаковой частой повторения
На основе всей информации, собранной в ходе испытания различных твердых форм йогексола, и на основе хорошего соответствия между предполагаемыми и измеренными величинами удельной поверхности считается, что частицы йогексола во всех рассмотренных формах являются непористыми.
Пример 4 - очистка йогексола
Водный раствор (2200 кг) с электропроводностью менее 5 мкСм/см, содержащий 426,0 кг неочищенного йогексола с менее чем 1,5% исходного вещества и менее чем 1,6% O-алкилированных соответствующих побочных продуктов, концентрируют при пониженном давлении до приблизительного веса 1000 кг. Добавляют 775 л этилацетата и удаляют часть воды посредством азеотропной дистилляция при пониженном давлении. Этилацетат частично (220 L) удаляют посредством дистилляции при пониженном давлении с последующим добавлением 1700 л этанола. Часть оставшегося этилацетата удаляют посредством азеотропной дистилляции бинарной этанол/этилацетатной азеотропной смеси. Полученный в результате этаноловый раствор йогексола с небольшими количествами этилацетата и воды выдерживали при температуре кипения и интенсивном перемешивании до образования крупных кристаллов. Суспензию интенсивно перемешивают в течение 48 часов. Смесь охлаждают до 40-50°C и продукт отфильтровывают, промывают и высушивают с использованием осушителя фильтра. Выход кристаллизированного йогексола составляет 320 кг с температурой плавления 246-254°C.
Пример 5 - характеристики частиц порошка йогексола
Три вида твердых форм йогексола были исследованы и получены следующим образом.
Кристаллизированный йогексол - кристаллизацией из органических растворителей, в итоге высушиванием и гельфильтрацией.
Высушенный распылением йогексол - высушиванием распылением из водного раствора.
Все формы йогексола исследовали в отношении следующих характеристик:
морфология частиц (агрегирование, агломерация, геометрические параметры, размер);
распределение частиц по размеру;
пористость;
удельная площадь поверхности;
насыпная и скелетная плотность;
степень кристаллизации;
гигроскопичность.
Параметры обобщены в следующей таблице 6.
Таблица 6 - Параметры
Степень кристаллизации - кристаллическая природа кристаллизированного йогексола была подтверждена с помощью XRPD. Высушенный распылением йогексол оказался фактически аморфным.
Морфология частицы - кристаллизированный йогексол образует агломераты частиц сферической/эллиптической формы с характеристическими размерами отдельных частиц приблизительно 0,5-3 мкм. Частицы организованы в агломераты со средней величиной D50 10 мкм.
Высушенный распылением йогексол образовывал сферические единицы с механической связью с другими частицами или без нее в зависимости от условий высушивания. Также, распределение частиц по размеру варьируется относительно D50 от 14 до 29 мкм. Все частицы характеризуются наличием углублений и кратеров.
Скелетная плотность, насыпная плотность - все формы йогексола в основном имеют одинаковую скелетную плотность, что свидетельствует о том, что масса внутреннего пространства частиц организована аналогичным образом. Кристаллизированный йогексол демонстрировал более низкую насыпную плотность, чем высушенный распылением йогексол. Неожиданно было установлено, что насыпная плотность имеет важную функцию в отношении характеристик растворения йогексола.
Пористость - все формы йогексола оказались непористыми. Удельные площади поверхности всех исследуемых форм являются сравнительно малыми вследствие отсутствия пор; однако, различие между кристаллизированным йогексолом и высушенным распылением йогексолом является существенным. Кристаллизированный йогексол имеет удельную площадь поверхности приблизительно 4 м2/г, при этом удельная площадь поверхности высушенного распылением йогексола составляет приблизительно 0,5 м2/г.
Время растворения - время, необходимое для полного растворения всех испытанных форм йогексола. Полученные величины варьируются от 30 до 90 секунд.
Пример 6 - влияние характеристик распылительной сушилки на распределение частиц по размеру для высушенного распылением йогексола
Смотри ФИГ. 10A для характеристик частиц высушенного распылением йогексола, полученного с различными параметрами высушивания распылением.
Tна входе(°C) - температура воздуха на входе в распылительную сушилку.
Tна выходе(°C) - температура воздуха на выходе из распылительной сушилки.
rpm распылителя - количество оборотов центробежного распылителя в минуту.
Исходная концентрация раствора йогексола % (вес/вес) - концентрация исходного раствора йогексола, закачанного в распылитель распылительной сушки.
ФИГ. 10B-10F иллюстрируют распределения частиц по размеру для полученных композиций йогексола для каждого исходного раствора йогексола, перечисленных в таблице ФИГ. 10A.
Несмотря на то, что различные варианты осуществления настоящего изобретения были описаны выше, следует понимать, что они представлены только в виде примера и не ограничены. Когда описанные выше способы и этапы указывают на некоторые события, происходящие в определенной последовательности, специалист в данной области техники, с учетом полезной информации из настоящего раскрытия, должен учитывать, что порядок определенных этапов можно модифицировать и что такие модификации находятся в соответствии с вариациями согласно настоящему изобретению. Кроме того, определенные этапы можно осуществлять одновременно c параллельным процессом, если это возможно, а также осуществлять последовательно, как описано выше. Варианты осуществления конкретно показаны и описаны, но следует понимать, что можно вносить различные изменения в форму и детали. Например, несмотря на то, что различные варианты осуществления были описаны при наличии конкретных материалов и/или комбинаций соединений, в других вариантах осуществления допустимы любые комбинации или подкомбинации любых материалов и/или соединений из любых вариантов осуществления, описанных в данном документе.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ ЛИНЕЗОЛИДА | 2018 |
|
RU2771279C2 |
| ТВЕРДЫЕ ГЕРБИЦИДНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ФЛУРОКСИПИР-МЕПТИЛ | 2015 |
|
RU2721264C2 |
| АНТАГОНИСТ РЕЦЕПТОРА CRF1, ЕГО ФАРМАЦЕВТИЧЕСКИЕ СОСТАВЫ И ТВЕРДЫЕ ФОРМЫ ДЛЯ ЛЕЧЕНИЯ ВРОЖДЕННОЙ ГИПЕРПЛАЗИИ НАДПОЧЕЧНИКОВ | 2019 |
|
RU2824490C2 |
| ОТВЕРЖДАЮЩАЯСЯ МНОГОКОМПОНЕНТНАЯ АКРИЛОВАЯ КОМПОЗИЦИЯ | 2014 |
|
RU2712216C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОЛИЗОВАННОГО КЕРАТИНСОДЕРЖАЩЕГО МАТЕРИАЛА С ВЫСОКОЙ СТЕПЕНЬЮ ПЕРЕВАРИВАЕМОСТИ | 2017 |
|
RU2736156C2 |
| ВЫСУШЕННЫЕ БИОЛОГИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2019 |
|
RU2810743C2 |
| ДЕАМОРФИЗАЦИЯ ВЫСУШЕННЫХ РАСПЫЛЕНИЕМ СОСТАВОВ ПОСРЕДСТВОМ СМЕШИВАНИЯ РАСПЫЛЕНИЕМ | 2014 |
|
RU2698331C2 |
| ПОЛУЧЕНИЕ ВЫСУШЕННЫХ ЧАСТИЦ, СОДЕРЖАЩИХ МЕНТОЛ | 2014 |
|
RU2665931C2 |
| КОМПОЗИЦИИ, КОРРИГИРУЮЩИЕ ВКУС КОНТРАСТНЫХ СРЕДСТВ | 2014 |
|
RU2683568C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОСАЖДЕННЫХ ДИОКСИДОВ КРЕМНИЯ | 2012 |
|
RU2605709C2 |







Изобретение относится к области медицины, а именно к контрастному средству, содержащему в качестве контрастного вещества частицы кристаллов йогексола (варианты), и к способу получения указанных частиц кристаллов йогексола. В первом варианте частицы кристаллов йогексола обладают насыпной плотностью менее 0,8 г/см3, свободным пространством между частицами более 60% от насыпного объема и удельной площадью поверхности более 0,8 м2/г. Во втором варианте частицы кристаллов йогексола характеризуются порошковой дифракционной рентгенограммой, имеющей пики 2θ при 7,6°, 16,2°, 19,9°, 20,8°, 22,3°, 29,8° и 30,7°. Изобретение обеспечивает повышение растворимости частиц йогексола. 3 н. и 12 з.п. ф-лы, 6 пр., 4 табл., 15 ил.
1. Контрастное средство, содержащее в качестве контрастного вещества частицы кристаллов йогексола, где указанные частицы обладают следующими характеристиками:
насыпной плотностью менее приблизительно 0,8 г/см3;
свободным пространством между частицами более 60% от насыпного объема и
удельной площадью поверхности более приблизительно 0,8 м2/г.
2. Контрастное средство по п.1, где количество йогексола находится в диапазоне от 0,2 до 75 г.
3. Контрастное средство по п.1, характеризующееся тем, что не содержит фармацевтически приемлемые функциональные вспомогательные вещества.
4. Контрастное средство по п.1, дополнительно содержащее по меньшей мере одно фармацевтически приемлемое нефункциональное вспомогательное вещество, выбранное из группы, состоящей из диспергирующих средств, разрыхлителей, покрытий, наполнителей, ароматизаторов, сорбентов, консервантов, подсластителей, окрашивающих средств, смачивающих средств, связующих веществ, средств, предотвращающих слипание, и их комбинаций.
5. Контрастное средство по п.1, где йогексол является экзоизомером.
6. Контрастное средство п.1, где частицы характеризуются насыпной плотностью менее 0,8 г/см3, свободным пространством между частицами более 60% от насыпного объема и удельной площадью поверхности более 0,8 м2/г.
7. Контрастное средство п.6, где указанные частицы характеризуются насыпной плотностью от 0,6 до 0,2 г/см3, свободным пространством между частицами от 70 до 95% от насыпного объема и удельной площадью поверхности от 0,8 до 5 м2/г.
8. Контрастное средство, содержащее в качестве контрастного вещества частицы кристаллов йогексола с порошковой дифракционной рентгенограммой, имеющей пики 2θ при 7,6°, 16,2°, 19,9°, 20,8°, 22,3°, 29,8° и 30,7°.
9. Контрастное средство по п.8, где указанные кристаллы йогексола характеризуются порошковой дифракционной рентгенограммой, имеющей пики 2θ при 7,6°, 10,6°, 12,1°, 16,2°, 18,1°, 19,7°, 19,9°, 20,8°, 22,3°, 22,7°, 22,9°, 26,1° и 26,2°, 29,8°, 29,9°, 30,3° и 30,7°.
10. Контрастное средство по п.8, где указанные кристаллы йогексола имеют параметры элементарной ячейки при T=293 K: a =14,722(3) Å, b=18,921(4) Å, c=9,295(2) Å, α=90°, β=91,281(3)°, γ=90° и моноклинная пространственная группа P21/c.
11. Контрастное средство по п.8, где указанные частицы йогексола растворяются в воде за 40 секунд при испытании с применением модифицированного способа 641 Фармакопеи Соединенных Штатов Америки, осуществление которого раскрыто в описании заявки.
12. Контрастное средство по п.8, где указанные частицы представляют собой агломераты из более мелких непористых частиц.
13. Контрастное средство по п.8, где частицы имеют следующие характеристики распределения частиц по размеру:
D90 от 10 до 40 мкм;
D50 от 5 до 20 мкм и
D10 от 2 до 11 мкм.
14. Способ получения частиц кристаллов йогексола, включающий:
кристаллизацию йогексола из смеси растворителей, содержащих спирт, алкилацетат и воду, где указанная кристаллизация включает:
(a) нагревание раствора йогексола в растворителе до температуры флегмы при встряхивании;
(b) удаление одного или нескольких из спирта, алкилацетата и воды путем дистилляции раствора йогексола и получение раствора йогексола, содержащего 20-25% вес./об. йогексола, 95-97% вес./об. спирта, 2-5% вес./об. алкилового сложного эфира, 0,1-2% вес./об. воды;
(c) поддержание раствора йогексола при встряхивании при температуре от 60°C вплоть до температуры флегмы, посредством чего получают суспензию кристаллов йогексола;
(d) охлаждение суспензии из этапа (b) до приблизительно 40-50°C при встряхивании;
(e) фильтрование и высушивание суспензии.
15. Способ по п.14, где йогексол является экзойогексолом.
| US 2013164224 A1, 27.06.2013 | |||
| EP 0919540 A1, 02.06.1999 | |||
| СПОСОБ ЙОДИРОВАНИЯ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ | 2009 |
|
RU2469997C2 |
| US 3368944 A, 13.02.1968 | |||
| WO 2007060380 A1, 31.05.2007 | |||
| Фармакопея Соединенных Штатов Америки | |||
| Монография: Йогексол, онлайн-ресурс: http://www.pharmacopeia.cn/v29240/usp29nf24s0_m41920.html | |||
| WO 2013007557 A1, 17.01.2013. | |||
Авторы
Даты
2020-01-17—Публикация
2015-03-04—Подача