Область техники
[0001] Настоящее изобретение относится к материалу, аккумулирующему NOx, способному эффективно накапливать оксиды азота (NOx) в области низких температур, и к способу очистки выхлопного газа с использованием материала, аккумулирующего NOx.
Уровень техники
[0002] Ожидается, что увеличение спроса на экономичные по потреблению топлива транспортные средства будет способствовать снижению температуры выхлопного газа. Кроме того, поставленная задача состоит в том, чтобы способствовать очистке вредных газовых компонентов при низких температурах. Также большой проблемой является управление выбросами NOx при температуре, меньшей 200°С, т.е. при той температуре, при которой каталитический нейтрализатор выхлопного газа только начинает проявлять свою активность.
[0003] Температурный диапазон, в котором функционирует обычный каталитический нейтрализатор выхлопного газа, составляет 250°С или более, и поэтому возникают трудности при нейтрализации NOx, образованных при недостаточном прогреве, например, при запуске двигателя. Соответственно, в качестве средства управления выбросами NOx при недостаточном разогреве, т.е. до тех пор, пока не будет достигнут температурный диапазон, в котором функционирует каталитический нейтрализатор, исследуется, например, способ, в котором материал для аккумулирования NOx помещен в первой половине каталитического нейтрализатора, что обеспечивает удержание NOx в материале для аккумулирования NOx в низкотемпературном диапазоне, в котором каталитический нейтрализатор еще не функционирует, и обеспечивает десорбцию NOx из материала для аккумулирования NOx в температурном диапазоне, в котором каталитический нейтрализатор проявляет активность, с последующей нейтрализацией выделившихся NOx.
[0004] Например, известен материал, способный аккумулировать NOx в низкотемпературном диапазоне: Ce1-xZrxO2. В этом материале десорбция поверхностного кислорода, сопровождающаяся восстановлением катиона Се, участвует в окислении NOx, и NOx удерживается в виде нитратной (нитритной) соли с Се в качестве катиона. Аккумулирующие свойства по NOx дополнительно улучшаются тем, что такой материал может служить подложкой для благородного металла, в том числе, Pt.
[0005] Кроме того, недавно было предложено использовать материал, полученный ионным обменом Pd на компаунде цеолита, например шабазит, что обеспечивает высокую способность к адсорбции NOx (см. «Низкотемпературный аккумулятор NO на основе цеолита с содержанием Pd для низкотемпературного управления выбросами дизельного двигателя», Catal Lett (2016) 146:1706-1711). В этом материале NO адсорбируется на молекулярном уровне к ионообменному катиону Pd и, тем самым, обеспечиваются высокие адсорбционные свойства по NOx в диапазоне низких температур.
[0006] С другой стороны, были проведены исследования аккумулирующих NOx материалов, не использующих каталитический металл платиновой группы, но использующих различные неметаллы, например, исследование Mn, имеющего высокую окислительную активность для NO, и было подтверждено, что сложный оксид, состоящий из MnOx и CeO2, изготовленный способом соосаждения, демонстрирует высокую аккумулирующую способность по NOx в температурном диапазоне 200°С или ниже.
Сущность изобретения
[Проблемы, которые должно решить данное изобретение]
[0007] Однако даже материал, указанный в не патентном документе 1, не является достаточно удовлетворительным применительно к аккумулирующим свойствам по NOx при низких температурах. Кроме того, в сложном оксиде, состоящем из MnOx и CeO2, существенным условием обеспечения эффективности является содержание переходного металла, например марганца, но поскольку указывается вредное воздействие такого переходного металла, необходим материал, который использует недорогой металл без использования переходного металла, и который временно удерживает NOx в области низких температур, равных 200°С или менее. Задача настоящего изобретения состоит в том, чтобы решить эти проблемы и предоставить материал для аккумулирования NOx, имеющий достаточную способность для аккумулирования NOx даже в области низких температур без использования переходного металла.
[Отличительные признаки для решения этих проблем]
[0008] Настоящее изобретение достигает вышеуказанной цели с помощью следующих средств.
[0009] <1> Материал для аккумулирования NOx, содержащий сложный оксид серебра и галлия.
<2> Материал для аккумулирования NOx по вышеуказанному пункту <1>, в котором сложный оксид дополнительно содержит алюминий.
<3> Материал для аккумулирования NOx по вышеуказанным пунктам <1> или <2>, в котором сложный оксид представляет собой сложный оксид типа делафоссит.
<4> Материал для аккумулирования NOx по вышеуказанным пунктам с <1> по <3>, в котором концентрация сложного оксида составляет 1,7 ммоль/г или более.
<5> Способ получения материала для аккумулирования NOx по любому из вышеуказанных пунктов с <1> по <4>, содержащий растворение солей металлов, составляющих сложный оксид, в растворителе и горячую сушку раствора.
<6> Способ по вышеуказанному пункту <5>, в котором молярное соотношение серебро : галлий или серебро : (галлий + алюминий) в сложном оксиде составляет от 2:8 до 7:3.
<7> Устройство для аккумулирования NOx, содержащее материал для аккумулирования NOx по любому из вышеуказанных пунктов с <1> по <4>.
<8> Способ очистки выхлопного газа, включающий в себя пропускание выхлопного газа, выпускаемого из двигателя внутреннего сгорания, через устройство для аккумулирования NOx по пункту <7> и последующее пропускание выхлопного газа через устройство очистки выхлопного газа, содержащее каталитический металл.
[Эффект изобретения]
[0010] В настоящем изобретении материал для аккумулирования NOx может обеспечить высокую способность аккумулирования NOx при низких температурах, в частности, при низкой температуре 200°С или меньше.
Краткое описание чертежей
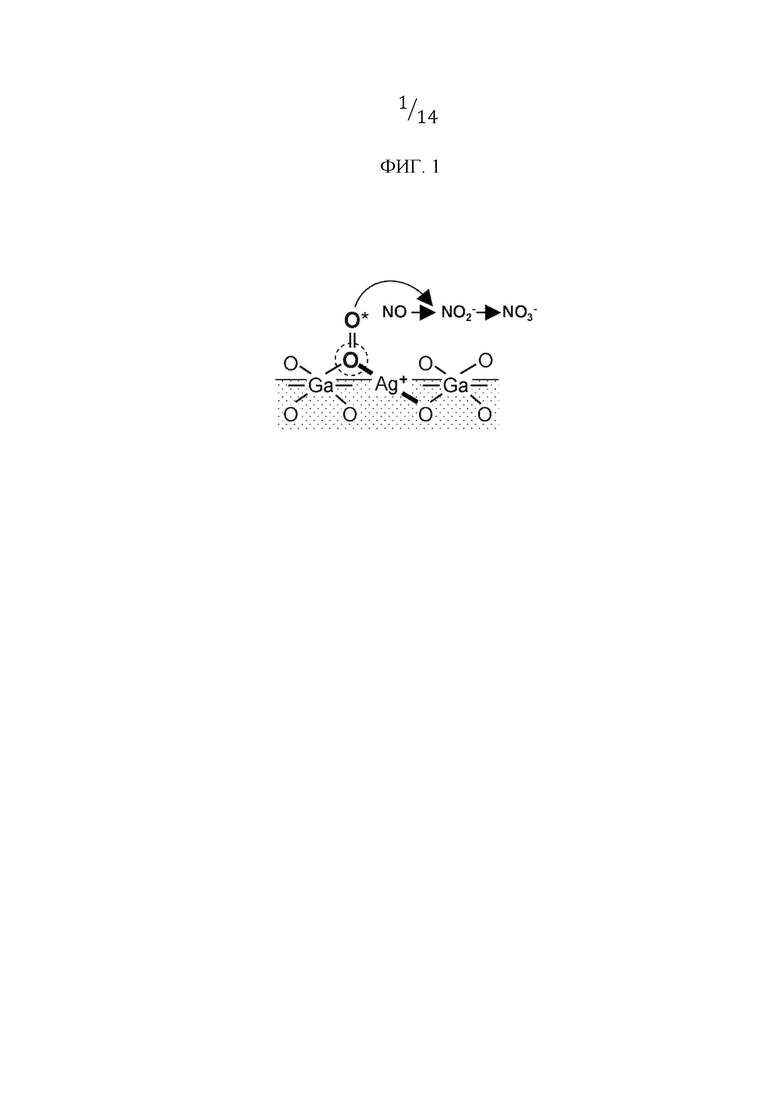
[0011] Фиг. 1 представляет собой схему, иллюстрирующую механизм реакции окисления NOx на материале для аккумулирования NOx согласно настоящему изобретению.
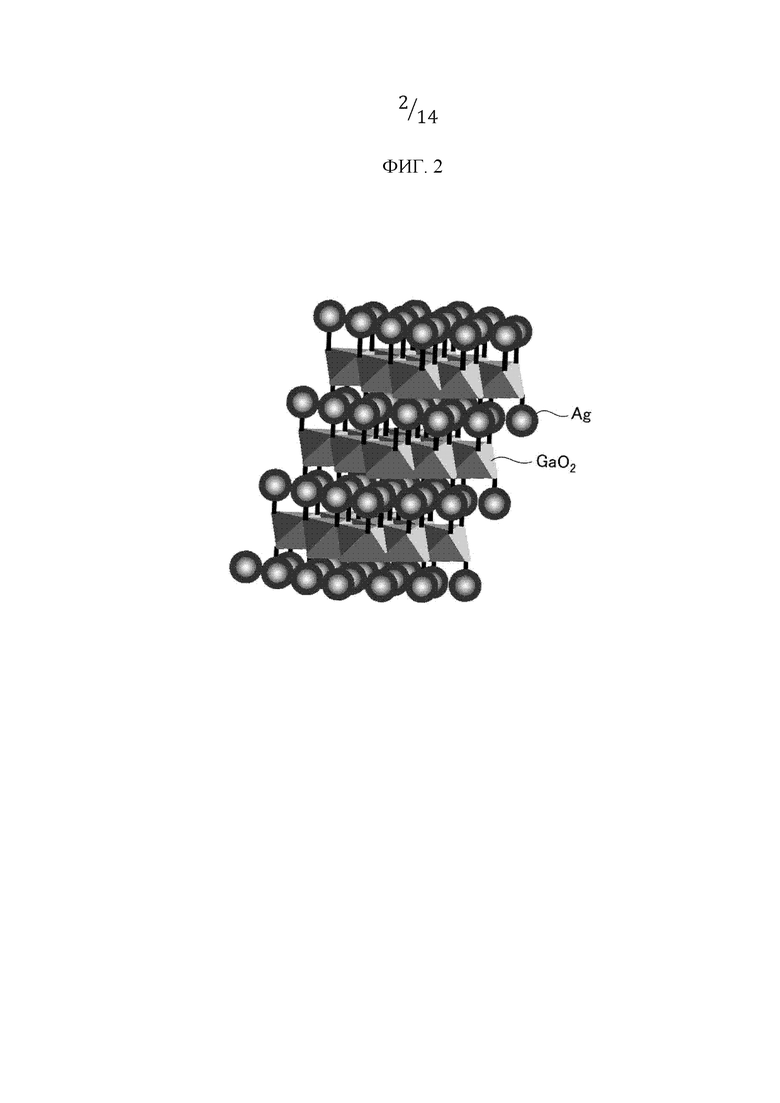
Фиг. 2 представляет собой принципиальную схему, иллюстрирующую структуру сложного оксида типа делафоссит.
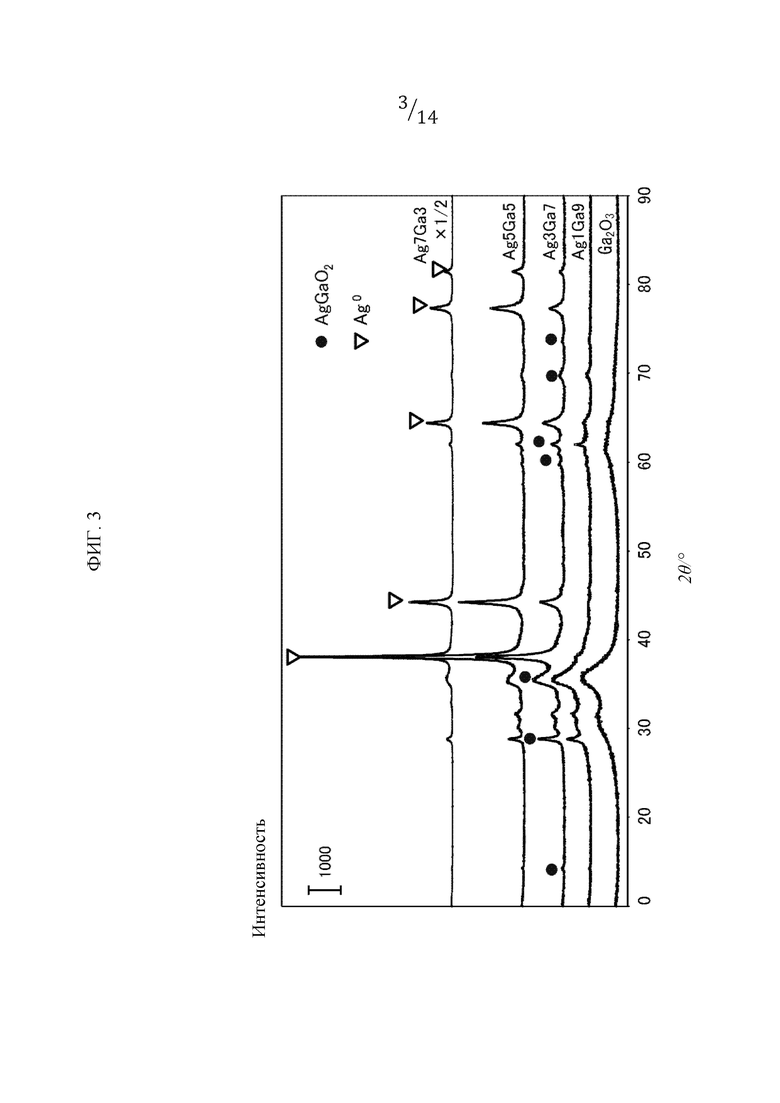
Фиг. 3 представляет собой дифракционную диаграмму XRD для каждого образца, полученного в «Примерах».
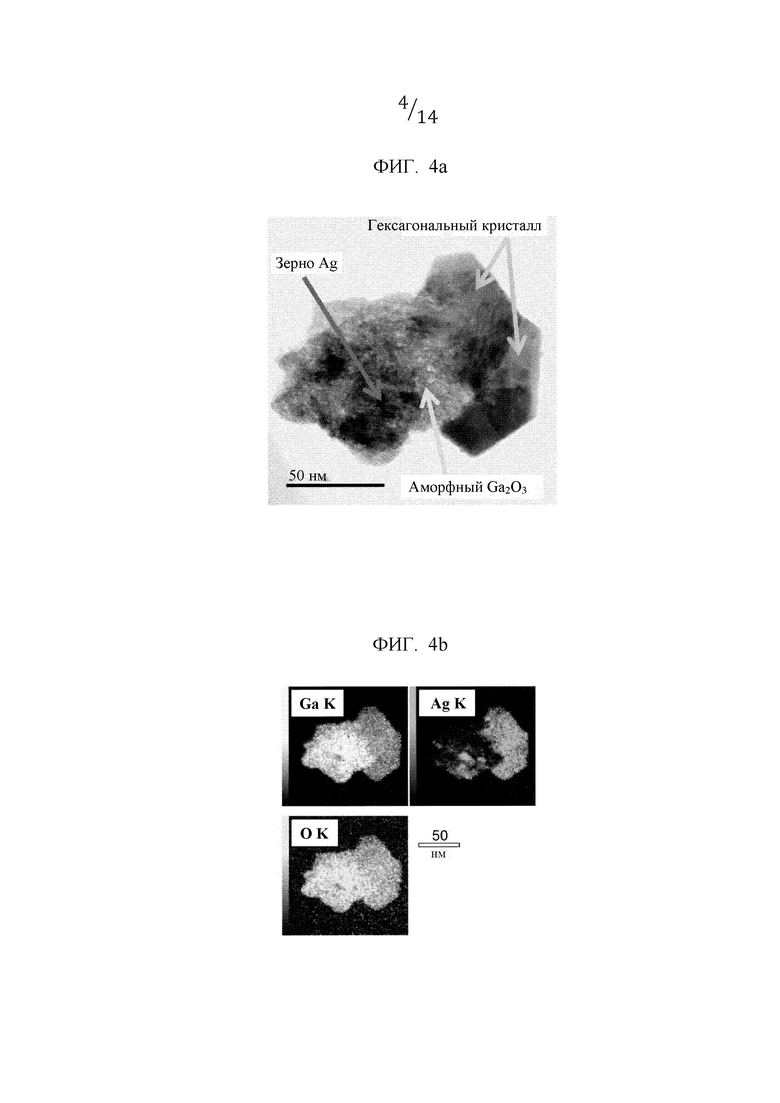
Фиг. 4а представляет собой изображение сложного оксида Ag3Ga7 (пример 1), полученное посредством технологии DF-STEM.
Фиг. 4b представляет собой картированное изображение сложного оксида Ag3Ga7 (пример 1), полученное посредством технологии EDS.
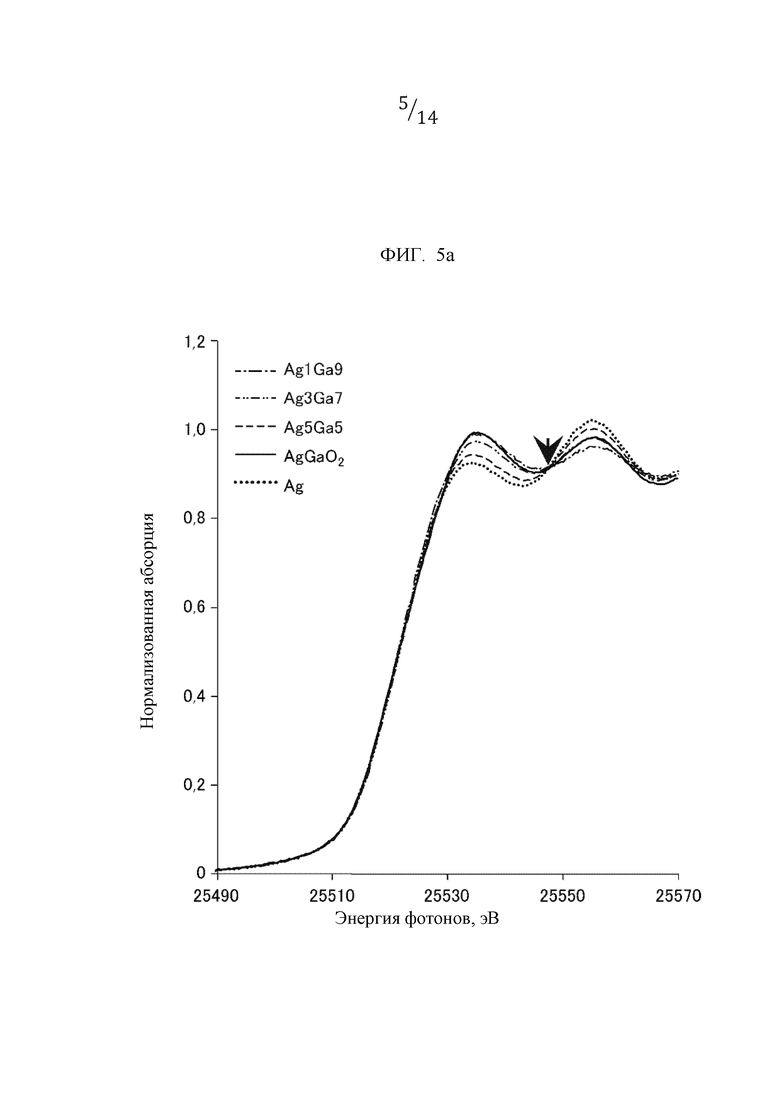
Фиг. 5а представляет собой график, иллюстрирующий результаты анализа по способу XAFS для каждого образца, полученного в примерах 1, 2 и 4, сравнительного образца AgGaO2 и медной фольги.
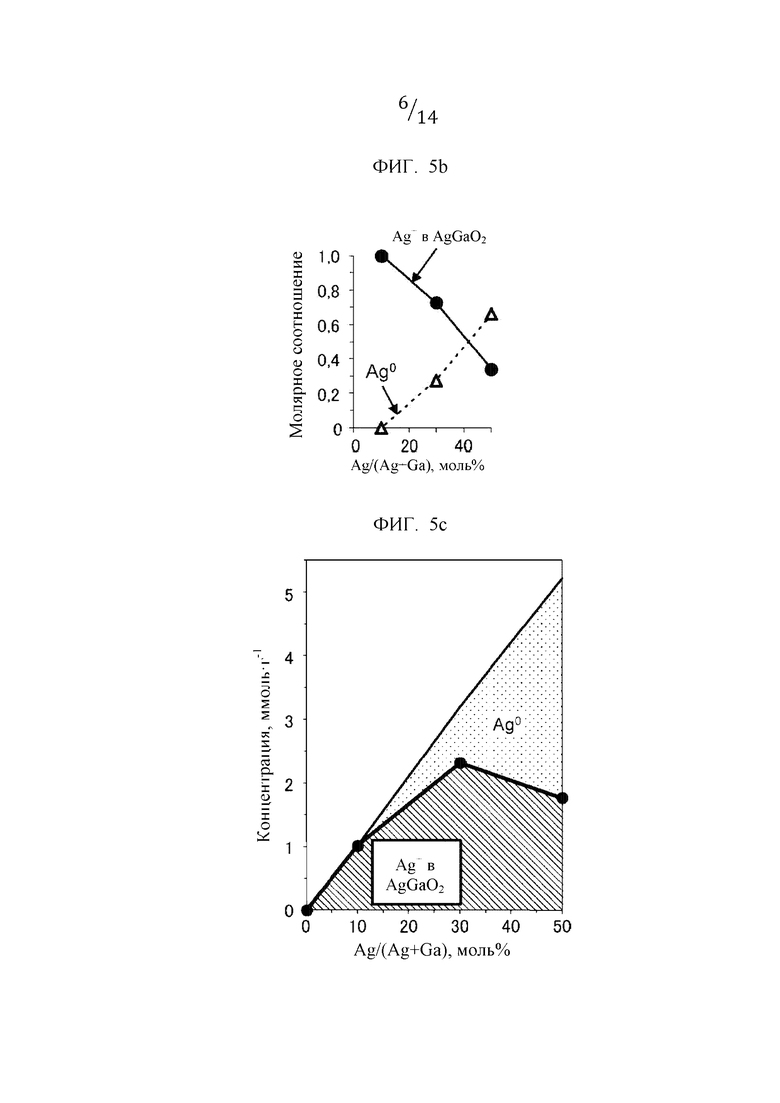
Фиг. 5b представляет собой график, иллюстрирующий результаты разделения формы волны между Ag0 и AgGaO2 в изобестической точке на фиг. 5а.
Фиг. 5с представляет собой график, иллюстрирующий количественные результаты для каждого компонента, изображенного на фиг. 5b.
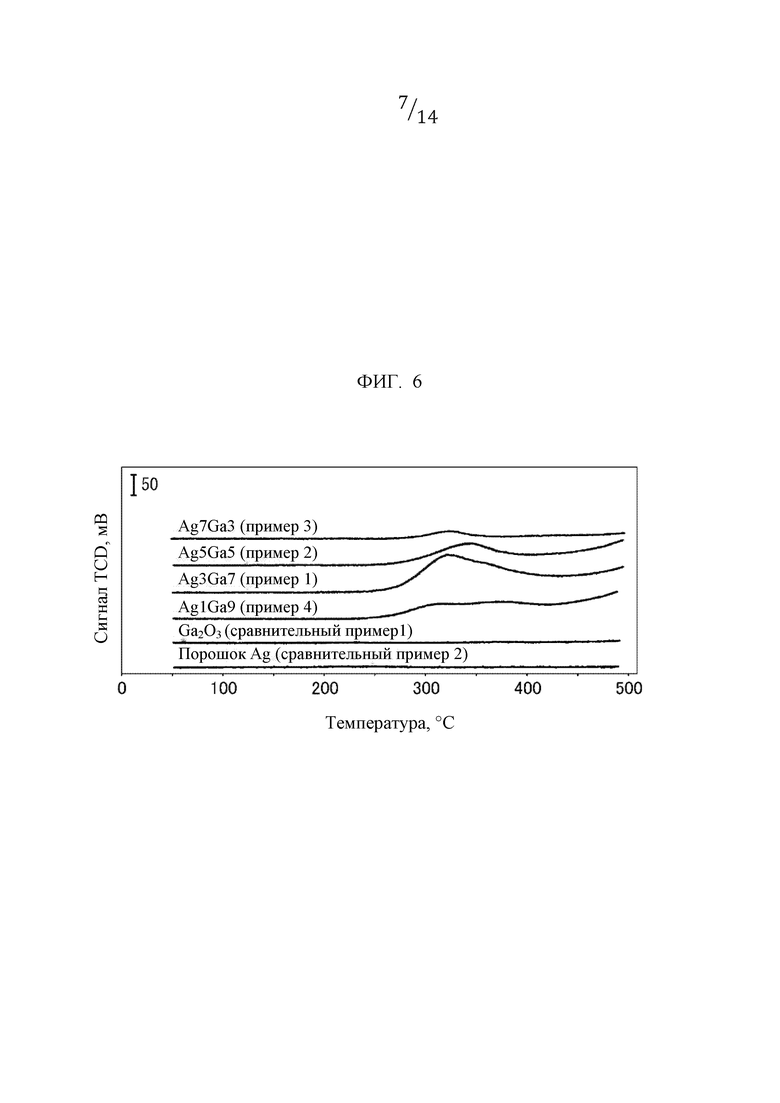
Фиг. 6 представляет собой график, иллюстрирующий профиль измерения способом ТПД для O2 для каждого образца, полученного в примерах с 1 по 4 и в сравнительных примерах 1 и 2.
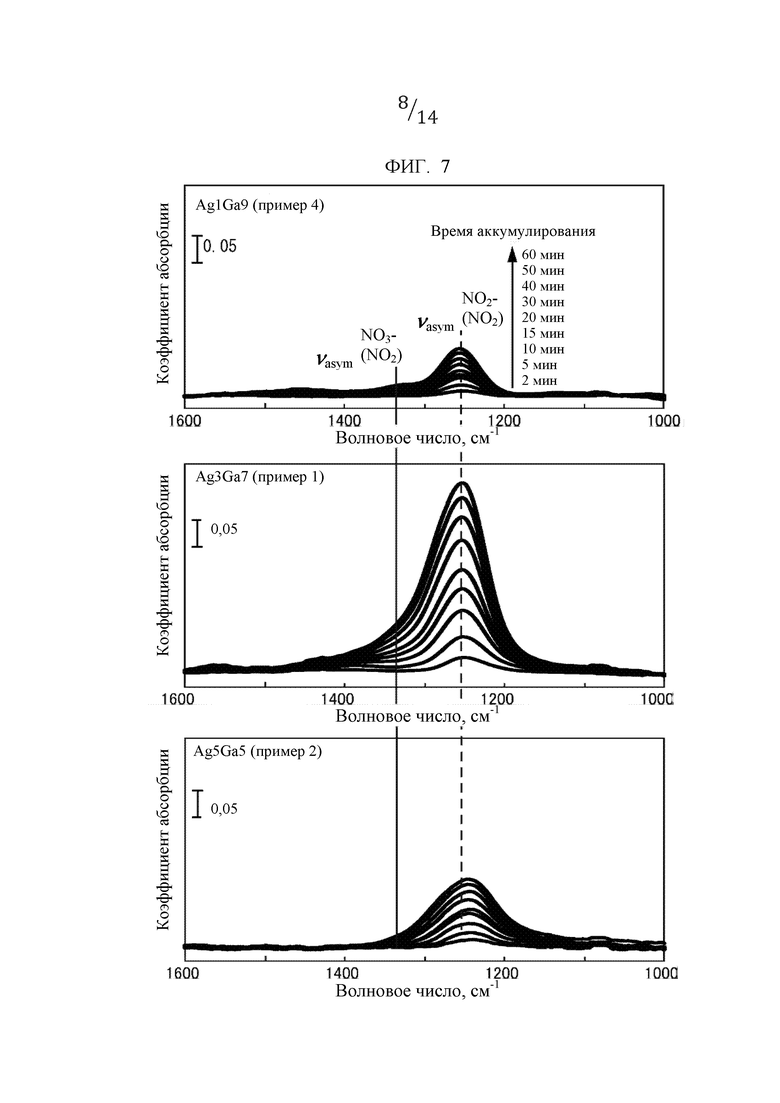
Фиг. 7 представляет собой график, иллюстрирующий результаты ИК-анализа для каждого образца, полученного в примерах 1, 2 и 4.
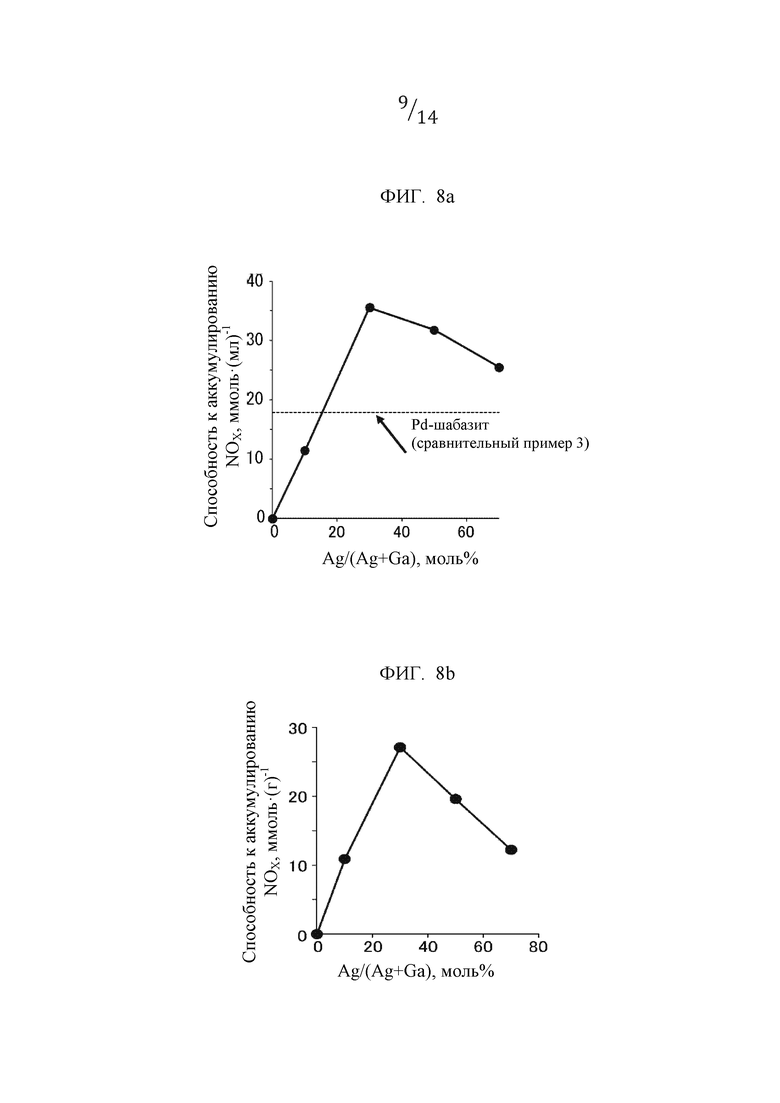
Фиг. 8а представляет собой график, иллюстрирующий количество аккумулированных NOx относительно объема каждого образца, полученного в примерах с 1 по 4 и в сравнительном примере 1.
Фиг. 8b представляет собой график, иллюстрирующий количество аккумулированных NOx относительно веса каждого образца, полученного в примерах с 1 по 4 и в сравнительном примере 1.
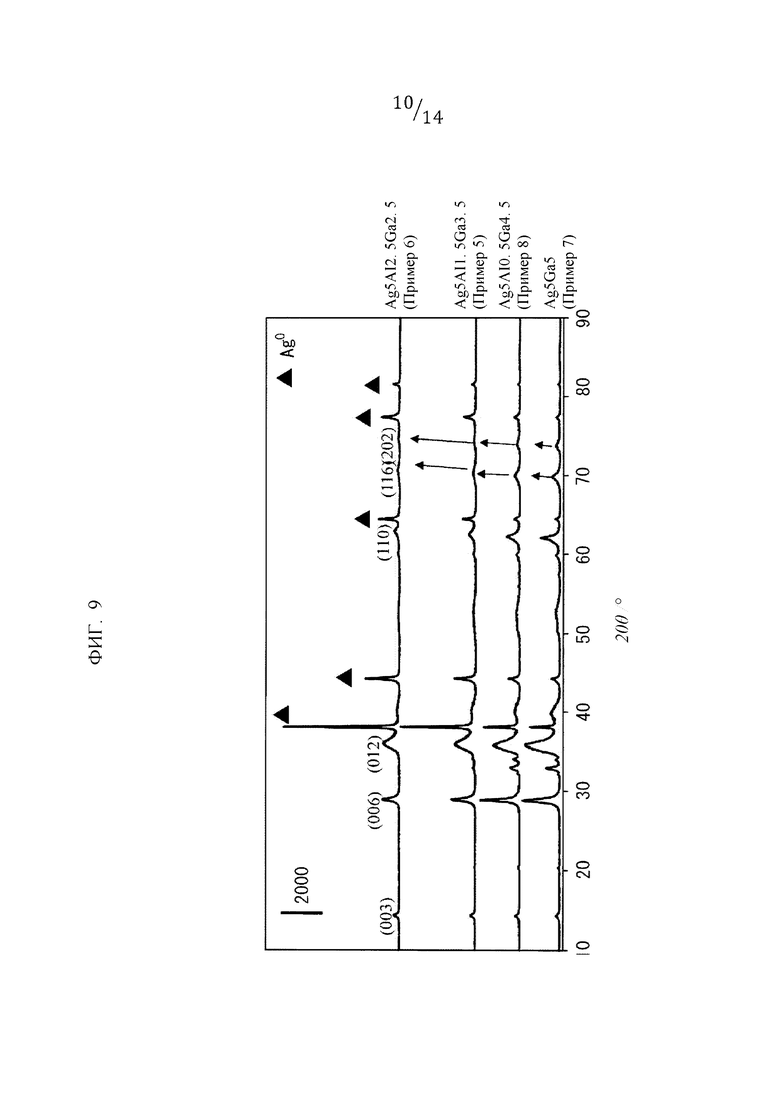
Фиг. 9 показывает дифракционную диаграмму XRD для каждого образца, полученного в «Примерах».
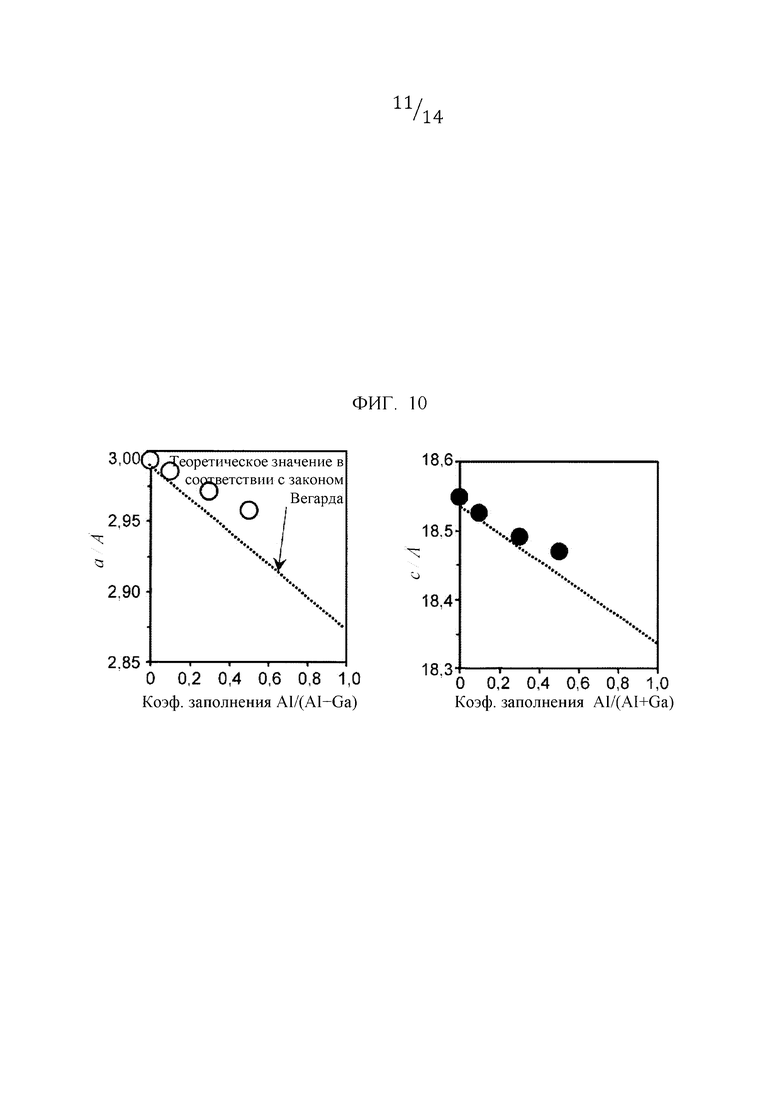
Фиг. 10 представляет собой график, иллюстрирующий соотношение между коэффициентом заполнения Al и длиной решетки.
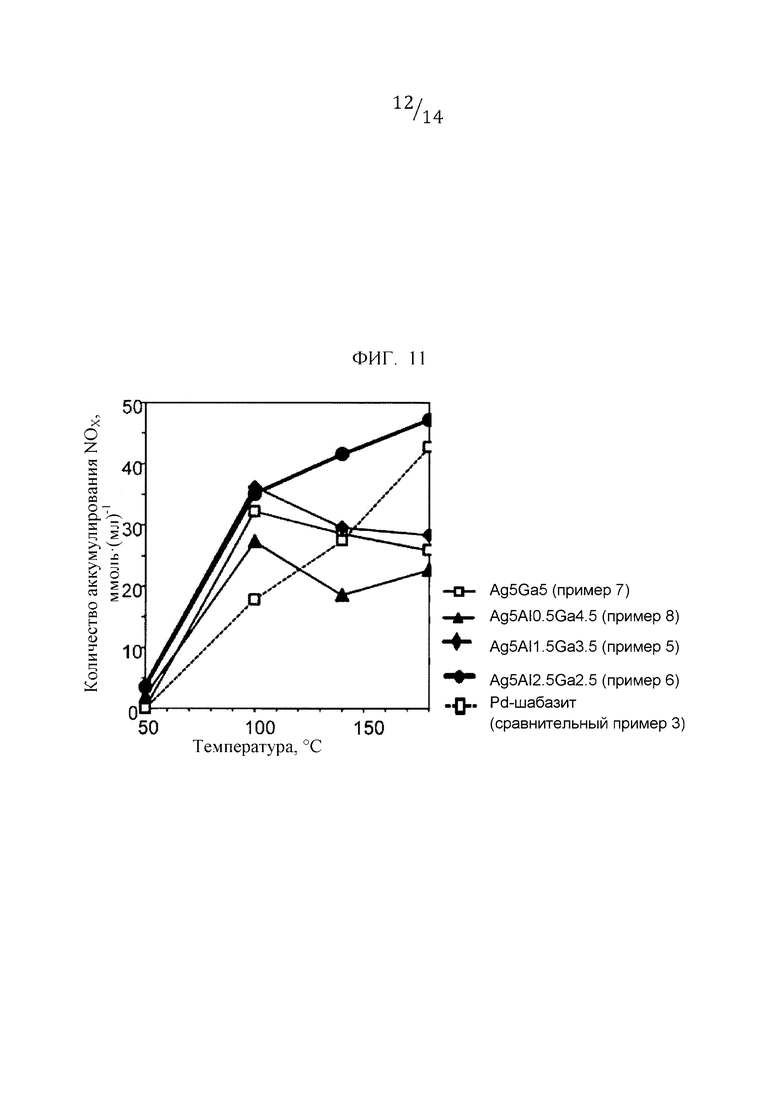
Фиг. 11 представляет собой график, иллюстрирующий соотношение между температурой и количеством накопления NOx.
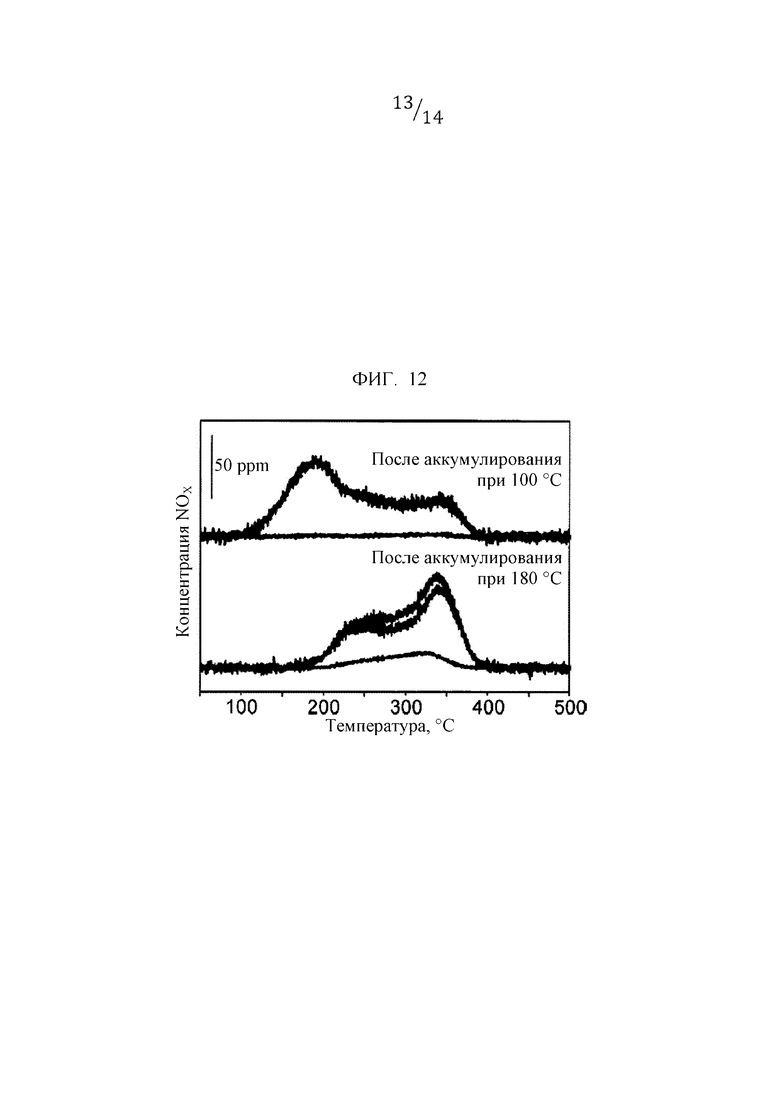
Фиг. 12 представляет собой график, иллюстрирующий профиль измерения способом ТПД для NOx.
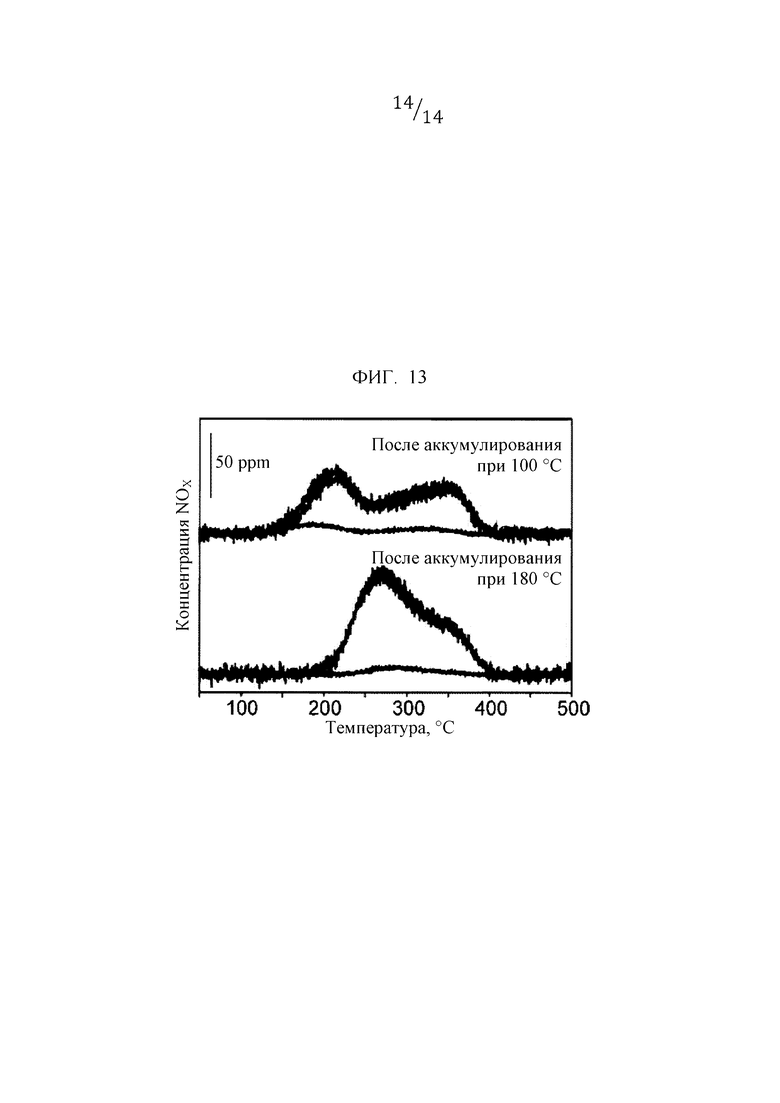
Фиг. 13 представляет собой график, иллюстрирующий профиль измерения способом ТПД для NOx.
Вариант осуществления изобретения
[0012] Вариант осуществления настоящего изобретения подробно раскрыт ниже. Тем не менее, настоящее изобретение не ограничено нижеследующими вариантами осуществления и может быть осуществлено посредством внесения в него различных модификаций в рамках сущности настоящего изобретения.
[0013] <Материал для аккумулирования NOx>
Материал для аккумулирования NOx согласно настоящему изобретению содержит сложный оксид серебра и галлия. Сложный оксид может дополнительно содержать алюминий. Алюминий замещаяет часть галлия в сложном оксиде серебра и галлия.
[0014] Как показано на фиг. 1, материал для аккумулирования NOx согласно настоящему изобретению содержит сложный оксид, в котором серебро (Ag) и галлий (Ga) растворены в твердом растворе, а участок Ag-O-Ga, сформированный в сложном оксиде, функционирует как низкотемпературный реакционный центр для аккумулирования NOx. Кроме того, предполагается, что кислород активируется на этом участке в области низких температур, а именно, в области низких температур 200°С или меньше, и активированный кислород оказывает влияние на образование нитритной соли (NO2-) и нитратной соли (NO3-) из NO, и в результате, NOx аккумулируется за счет окисления. Кроме того, сложный оксид может представлять собой сложный оксид, в котором часть галлия в сложном оксиде серебра и галлия замещена алюминием, и в данном случае предполагается, что кислород активируется на участке Ag-O-Ga(Al), и NOx аккумулируется за счет окисления.
[0015] В сложном оксиде серебра и галлия, содержащемся в материале для аккумулирования NOx согласно настоящему изобретению, молярное соотношение между серебром и галлием может составлять от 3:7 до 7:3 или от 4:6 до 6:4, а в сложном оксиде серебра, галлия и алюминия молярное соотношение между серебром и (галлий + алюминий) может составлять от 2:8 до 7:3. Сложный оксид предпочтительно представляет собой сложный оксид типа делафоссит. Фиг. 2 иллюстрирует схематическую структуру сложного оксида типа делафоссит. Структура типа делафоссит представлена AgGaO2 или AgAlxGa1-xO2 и состоит из одновалентного катиона Ag+, трехвалентного катиона Ga3+, Ag3+, и оксидного иона О-. В AgAlxGa1-xO2, х предпочтительно имеет значение от 0,1 до 0,9, более предпочтительно от 0,1 до 0,5. AgGa(Al)O2 образуется в виде слоистой структуры, в которой слой Ga(Al)O2 формируется за счет общих сторон октаэдра Ga(Al)O6, и слой Ag укладывается попеременно. За счет такой структуры, на поверхности оксида может существовать много участков Ag-O-Ga, и, поскольку такой участок функционирует как активный участок для реакции аккумулирования NOx, способность к аккумулированию NOx является высокой.
[0016] В материале для аккумулирования NOx, согласно настоящему
изобретению, концентрация сложного оксида серебра и галлия может составлять 1,0 ммоль/г или более и предпочтительно составляет 1,7 ммоль/г или более, или 1,8 ммоль/г или более. Кроме того, концентрация может составлять 2,4 ммоль/г или менее.
[0017] Материал для аккумулирования NOx, согласно настоящему изобретению, демонстрирует более высокую способность к аккумулированию NOx, чем компаунд, в котором палладий подвергается ионному обмену на компаунде цеолита, например на шабазите, обычно используемом в качестве материала для аккумулирования NOx в низкотемпературном диапазоне, в частности, в низкотемпературном диапазоне 200°С или менее, а также 100°С или менее.
[0018] <Способ производства материала для аккумулирования NOx>
Материал для аккумулирования NOx согласно настоящему изобретению может быть изготовлен любым способом, обычно используемым в качестве способа получения сложного оксида, и, в частности, может быть получен следующим способом согласно настоящему изобретению.
[0019] Способ производства материала для аккумулирования NOx согласно настоящему изобретению содержит этап растворения солей металлов, образующих сложный оксид, то есть, соли серебра, соли галлия и, если это требуется, соли алюминия, в растворителе, и этап горячей сушки раствора. В качестве соли серебра, соли галлия и соли алюминия возможно использование нитрата, карбоната и т.д., используемых в общем способе получения сложного оксида. В качестве растворителя возможно использование растворителя, способного растворять эти соли, например воду. Соль серебра и соль галлия предпочтительно смешивают в таком соотношении, чтобы молярное соотношение серебра и галлия Ag : Ga находилось в пределах от 2:8 до 7:3, от 3:7 до 7:3, или от 4:6 до 6:4, и в этом случае, часть галлия, то есть, от 10 до 90 моль % или от 10 до 50 моль %, может быть замещена алюминием.
[0020] Температура горячей сушки обычно равна 250°С или более, предпочтительно 300°С или более, и равна 600°С или менее, предпочтительно 400°С или менее. Горячая сушка может быть выполнена в воздухе или в кислороде, но предпочтительно выполняется в кислороде. Время горячей сушки может быть соответствующим образом определено в зависимости от температуры горячей сушки обычно составляет от 1 до 10 часов.
[0021] Горячая сушка предпочтительно выполняется в присутствии топлива. В качестве топлива могут быть использованы глицин, глюкоза, сахароза, мочевина, лимонная кислота, гидразин, карбогидразин, оксалилдигидразин, ацетилацетон, гексаметилентетрамин и т.д.
[0022] <Устройство для аккумулирования NOx>
Устройство для аккумулирования NOx согласно настоящему изобретению содержит вышеупомянутый материал для аккумулирования NOx. В устройстве для аккумулирования NOx согласно настоящему изобретению, материал для аккумулирования NOx может быть сконфигурирован с возможностью размещения в корпусе, или материал для аккумулирования NOx может быть расположен на опорной частице, а затем помещен в корпус.
[0023] Опорная частица содержит частицы оксида металла, например, оксида алюминия (Al2O3), оксида циркония (ZrO2), оксида церия (CeO2), оксида кремния (SiO2), оксида магния (MgO) и оксида титана TiO2 или их сложного оксида (например, сложный оксид оксида церия - оксида циркония (CeO2-ZrO2)). Среди них предпочтительными являются частицы оксида алюминия, оксида циркония и сложного оксида диоксида церия - диоксида циркония.
[0024] <Способ очистки выхлопного газа>
Способ очистки выхлопного газа, согласно настоящему изобретению, включает в себя обеспечение прохождения выхлопного газа, выпускаемого из двигателя внутреннего сгорания, через вышеуказанное устройство для аккумулирования NOx, и последующее прохождение выхлопного газа через устройство очистки выхлопного газа, содержащее каталитический металл.
[0025] Выхлопной газ, выходящий из двигателя внутреннего сгорания, сначала проходит через устройство для аккумулирования NOx и вступает во взаимодействие с материалом для аккумулирования NOx, и, тем самым, NOx в выхлопном газе может быть аккумулирован при низкой температуре, например, при запуске двигателя внутреннего сгорания, в частности, при низкой температуре 100°С. Затем, когда выхлопной газ достигает высокой температуры, аккумулированные NOx высвобождаются из материала для аккумулирования NOx, причем концентрация оксидов азота уменьшается в результате прохождения через устройство очистки выхлопного газа, содержащее каталитический металл, и, следовательно, происходит удаление вредного компонента из выхлопного газа.
[0026] В качестве каталитического металла в устройстве очистки выхлопного газа может быть использован один или несколько металлов, например, платина (Pt), родий (Rh), палладий (Pd), рутений (Ru), иридий (Ir) или осмий (Os).
[0027] Хотя это и не ограничивается особым образом, содержание каталитического металла относительно общего объема катализатора в устройстве очистки выхлопного газа обычно составляет соответственно от 0,5 до 10 г/л и предпочтительно составляет, например, от 0,5 до 7,0 г/л. Если количество нанесенного каталитического металла слишком мало, то каталитическая активность (в частности, каталитическая активность по окислению) за счет каталитического металла будет недостаточной, и с другой стороны, если количество нанесенного каталитического металла слишком велико, то каталитический металл, вероятно, подвергнется эффекту роста зерен, и в то же время это приведет к необоснованному росту стоимости.
[0028] Катализатор в устройстве очистки выхлопного газа может быть использован в виде гранулы сам по себе или может быть использован посредством размещения его на подложке. В качестве подложки может быть использована такая же подложка, которая используется в обычном известном каталитическом нейтрализаторе выхлопного газа. Например, подложка может предпочтительно представлять собой подложку, состоящую из термостойкого материала, имеющего пористую структуру. Термостойкий материал содержит термостойкий металл, например, таким материалом может быть кордиерит, карбид кремния (SiC), титанат алюминия, нитрид кремния и нержавеющая сталь, их сплав и т.д. Кроме того, подложка предпочтительно имеет сотовую структуру, форму пены, форму гранул и т.д. Кроме того, при выборе внешней формы подложки в целом, можно использовать цилиндрическую форму, эллиптическую цилиндрическую форму, многоугольную цилиндрическую форму и т.д.
ПРИМЕР
[0029] Пример 1 (сложный оксид Ag3Ga7):
2,55 г (15 ммоль) нитрата серебра (AgNO3), 14,0 g (35 ммоль) n-гидрата нитрата галлия (Ga(NO3)3⋅nH2O) и 1,41 г (19 ммоль) глицина помещают в мерный стакан объемом 200 мл и растворяют посредством добавления 10 мл дистиллированной воды. Полученный раствор помещают в муфельную печь, нагревают до 350°С при 5,4°С/мин и после этого сушат в воздухе при 350°С в течение 1 часа. Полученное твердое вещество помещают в ступку и размельчают, и полученный порошок затем обжигают при 500°С в течение 2 часов. Порошок спрессовывают и формуют при 2 т/см2 для получения гранулы диаметром (φ) от 1,0 до 1,7 мм. Таким образом, получают сложный оксид, изготовленный при соотношении долей серебра и галлия 3:7, и в настоящем описании он называется сложным оксидом Ag3Ga7.
[0030] Пример 2 (сложный оксид Ag5Ga5):
Гранулу изготавливают тем же способом, что и в примере 1, с использованием 4,25 г (25 ммоль) нитрата серебра (AgNO3), 10,0 г (25 ммоль) n-гидрата нитрата галлия (Ga(NO3)3⋅nH2O) и 1,41 г (19 ммоль) глицина.
[0031] Пример 3 (сложный оксид Ag7Ga3):
Гранулу изготавливают тем же способом, что и в примере 1, с использованием 5,95 г (35 ммоль) нитрата серебра (AgNO3), 6,0 г (15 ммоль) n-гидрата нитрата галлия (Ga(NO3)3⋅nH2O) и 1,41 г (19 ммоль) глицина.
[0032] Пример 4 (сложный оксид Ag1Ga9):
Гранулу изготавливают тем же способом, что и в примере 1, с использованием 0,85 г (5 ммоль) нитрата серебра (AgNO3), 18,0 г (45 ммоль) n-гидрата нитрата галлия (Ga(NO3)3⋅nH2O) и 1,41 г (19 ммоль) глицина.
[0033] Пример 5 (сложный оксид Ag5Al1.5Ga3.5):
Гранулу изготавливают тем же способом, что и в примере 1, с использованием 4,25 г (25 ммоль) нитрата серебра (AgNO3), 7,0 г (17,5 ммоль) n-гидрата нитрата галлия (Ga(NO3)3⋅nH2O), 2,81 г (7,5 ммоль) нонагидрата нитрата алюминия (Al(NO3)3⋅9H2O) и 0,62 г (8,3 ммоль) глицина.
[0034] Пример 6 (сложный оксид Ag5Al2.5Ga2.5):
Гранулу изготавливают тем же способом, что и в примере 1, с использованием 4,25 г (25 ммоль) нитрата серебра (AgNO3), 5,0 г (12,5 ммоль) n-гидрата нитрата галлия (Ga(NO3)3⋅nH2O), 4,69 г (12,5 ммоль) нонагидрата нитрата алюминия (Al(NO3)3⋅9H2O) и 0,62 г (8,3 ммоль) глицина.
[0035] Пример 7 (сложный оксид Ag5Ga5):
Гранулу изготавливают тем же способом, что и в примере 1, с использованием 4,25 г (25 ммоль) нитрата серебра (AgNO3), 10,0 г (25,0 ммоль) n-гидрата нитрата галлия (Ga(NO3)3⋅nH2O) и 0,62 г (8,3 ммоль) глицина.
[0036] Пример 8 (сложный оксид Ag5Al0.5Ga4.5):
Гранулу изготавливают тем же способом, что и в примере 1, с использованием 4,25 г (25 ммоль) нитрата серебра (AgNO3), 9,0 г (22,5 ммоль) n-гидрата нитрата галлия (Ga(NO3)3⋅nH2O), 0,94 г (2,5 ммоль) нонагидрата нитрата алюминия (Al(NO3)3⋅9H2O) и 0,62 г (8,3 ммоль) глицина.
[0037] Сравнительный пример 1 (Ga2O3):
Гранулу изготавливают тем же способом, что и в примере 1, с использованием 22,0 г (50 ммоль) n-гидрата нитрата галлия (Ga(NO3)3⋅nH2O) и 1,41 г (19 ммоль) глицина.
[0038] Сравнительный пример 2 (порошок Ag):
Был использован порошок серебра производства Wako Pure Chemical Industries, Ltd.
[0039] Сравнительный пример 3 (Pd-шабазит):
Был использован материал, полученный посредством осаждения 1% масс. палладия на шабазит (SiO2/Al2O3=13, удельная поверхность по способу БЭТ: 504 м2/г).
[0040] <Способ измерения и оценка>
Свойства полученных образцов были измерены с использованием следующих способов и оценены.
[0041] Рентгенодифракционный анализ (XRD)
Измерение проводилось с использованием прибора RINT2000 производства Rigaku Corporation с источником рентгеновского излучения CuKα (λ=1,5418 нм) для следующих условий: диапазон от 10 до 90 градусов, ширина шага 0,02 градусов, напряжение трубки 50 кВ и ток трубки 300 мА. Положение дифракционных пиков сравнивалось с известными данными из файла данных Международного центра дифракционных стандартов (JCPDS). Диаметр кристаллитов определяли по уравнению Шеррера.
[0042] (Анализ удельной площади поверхности)
Измерение проводили при 77 K способом адсорбции/десорбции азота с использованием прибора BELSORP-max-12-N-VP производства MicrotracBEL Corp. Образец для измерения подвергали вакуумной предварительной обработке в течение 3 часов при 250°С. Удельную площадь поверхности рассчитывали по прямой части f кривой БЭТ.
[0043] (Картированный анализ STEM-EDS)
Наблюдение проводили под просвечивающим сканирующим микроскопом (STEM) с использованием прибора JEM-1000 (ускоряющее напряжение: 200 кВ) производства JEOL Ltd. Образец в виде порошка диспергировали в этаноле, помещали каплями на медную сетку, а затем высушивали и измеряли.
[0044] (Анализ XAFS)
Анализ выполняли на экспериментальной станции BL07 в Центре исследования синхротронного света Кюсю. Спектр измеряли способом пропускания с использованием ионной камеры с помощью двухкристального спектрометра Si (220).
[0045] (Анализ способом ТПД для O2)
Для этих измерений был использован прибор Belcat А производства MicrotracBEL Corp. Точно взвесили 200 мг образца в виде порошка и поместили в измерительную трубку, 20% по объему O2/Не вливали со скоростью 30 мл/мин, и после этого подняли температуру до 500°С и поддерживали эту температуру в течение 10 минут, систему охлаждали до 50°С в такой же атмосфере. Газ в этой трубке был замещен газообразным Не при 50°С, затем Не вливали со скоростью 30 мл/мин, температуру подняли до 500°С, причем скорость нагревания образца была 10°С/мин, и проанализировали количество десорбции O2 способом TCD.
[0046] (ИК анализ)
Для этих измерений использовали инфракрасный спектрофотометр Jasco FT/IR-6200 производства JASCO Corp. Смешали в ступке образец и KBr с весовым соотношением 3:7, 12 мг точно взвесили и спрессовали в диск диаметром φ 8 мм, и использовали этот диск как образец. Для материала окна использовали CaF. Несколько раз выполняли следующую операцию предварительной обработки: операция обдува смесью газов, с составом O2 3%/Ar при общем расходе 200 мл/мин при 350°С в течение 5 минут с последующим введением смеси газов с составом Н2 5%/Ar в течение 10 минут. Смесь газов с составом O2 3%/Ar при таком же расходе охладили до температуры измерения, затем выполнили измерения фона, пропустили поток смеси газов с составом NO 400 мкг/г+O2 9%/Ar и измерили спектры после 2, 5, 10, 15, 20, 30, 40, 50 и 60 минут. Температуру измерения установили на 100°С и в диапазоне измерений от 1000 до 4000 см-1, собрали 128 сканирований в режиме накопления при разрешении 4 см-1.
[0047] (Анализ способом ТПД для NOx)
Поместили в проточный реактор 1 мл гранулированного катализатора и каждый газ при 180°С, 140°С и 100°С проанализировали при помощи анализатора FT-IR (SESAM-HL, BEST Instruments Co., Ltd.). После оценки указанных ниже характеристик аккумулирования NOx, образец нагрели со скоростью 20°С/мин в потоке N2 и проанализировали десорбцию видов NOx.
[0048] (Оценка характеристик аккумулирования NOx)
Поместили в проточный реактор 1 мл гранулированного образца, изготовленного по каждому из примеров и сравнительных примеров, и затем проанализировали переходное поведение каждого газа при 180°С, 140°С и 100°С с использованием анализатора FT-IR (SESAM-HL, BEST Instruments Co., Ltd.) и анализатора магнитного давления (Вех, BEST Instruments Co., Ltd.). После выполнения предварительной восстановительной обработки при 500°С в течение 5 минут в потоке Н2, переключили газ на O2 9%+CO2 10%+вода 10%/N2 в виде газа, и выполнили предварительную обработку при той же температуре в течение 5 минут. В той же окислительной атмосфере газ охладили до оценочной температуры, причем обедненный газ, показанный в приведенной ниже табл. 1, вводили со скоростью 1 л/мин в течение 15 минут, и количество аккумулированных NOx рассчитали на основе разницы с профилем NOx в холостой пробе, в которой отсутствовал катализатор.
[0049] <Результаты измерений>
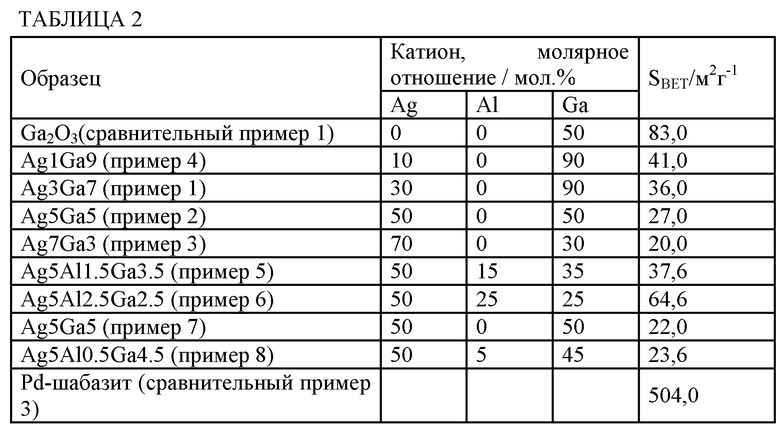
(Удельная площадь поверхности)
Соотношение состава и удельная площадь поверхности каждого из образцов, полученных в примерах и сравнительных примерах, показаны в табл. 2 ниже.
[0050] (Результаты структурного анализа способом XRD)
Диффракционная диаграмма XRD каждого образца показана на фиг. 3 и 9. Как показано на фиг. 3, были обнаружены дифракционные пики для оксида AgGaO2 типа делафоссит в образцах, кроме образца для Ga2O3. Кроме того, в сложном оксиде Ag3Ga7 (пример 1) интенсивность дифракции вышеупомянутого оксида была самой высокой. Дополнительно, как показано на фиг. 9, дифракционная линия металлического Ag была обнаружена на дифракционных диаграммах для всех продуктов, а также для AgAlxGa1-xO2 типа делафоссит, и для указанных продуктов было подтверждено, что это смесь обоих веществ. Более того, поскольку дифракционная линия для AgAlxGa1-xO2 сдвигается в сторону высокого угла при увеличении доли Al в составе, следует понимать, что была получена структура, в которой Ga замещен Al. Также предполагается, что с увеличением доли Al увеличивается содержание металлического крупнозернистого Ag.
[0051] Фиг. 10 иллюстрирует зависимость параметра решетки, вычисленного на основе показанного на фиг. 9 анализа коэффициента заполнения Al. Как длина оси а, так и длина оси с уменьшаются с увеличением доли Al, и поэтому обнаружено, что был получен оксид типа делафоссит, в котором часть Ga замещена Al. Однако результаты не полностью соответствовали теоретическим значениям согласно закону Вегарда, и это дает основания предполагать, что в части Al не было замещения, и оксид присутствовал в виде Al2O3 и т.д.
[0052] (Результаты структурного анализа с использованием STEM)
Фиг. 4а иллюстрирует изображение наблюдения, полученное при помощи DF-STEM для сложного оксида Ag3Ga7 (пример 1), а фиг. 4b иллюстрирует картированное изображение EDS для того же вещества. Можно подтвердить, что вместе с зернами Ag и Ga2O3 присутствует и гексагональный оксид, в котором распределение состава Ag, Ga и О является единообразным. Ожидается, что этот оксид представляет собой оксид AgGaO2 типа делафоссит, обнаруженный на дифракционной диаграмме XRD, показанной на фиг. 3.
[0053] (Результаты структурного анализа способом XAFS)
Фиг. 5а иллюстрирует результаты анализа способом XAFS для образцов из примеров 1, 2 и 4, образца из сравнительного примера 2, AgGaO2 в качестве контрольного образца и Ag. Спектр поглощения каждого образца изменяется через изобестическую точку в соответствии с разницей в отношении Ag/Ga, и это указывает на изменение вследствие разницы в отношении содержания двух компонентов Ag и AgGaO2.
[0054] Fig. 5b иллюстрирует результаты разделения формы волны в спектре по способу XAFS, показанном на фиг. 5а, в спектры для Ag0 и AgGaO2 и расчет каждой составляющей фракции. На основании результатов, представленных на фиг. 5b, количественно определили компонент Ag на массу материала. Способ количественного определения был следующим. В первую очередь AgGaO2 растворили в царской водке. После этого раствор выпаривали в ICP и количественно определили концентрацию Ag. Значение, показанное на фиг. 5с, можно получить путем умножения количественно определенной концентрации Ag на долю компонентов, рассчитанную в анализе способом XAFS.
[0055] В соответствии с показанным на фиг. 5с, следует понимать, что AgGaO2 содержится в наибольшем количестве в сложном оксиде Ag3Ga7 (пример 1). Из результатов, показанных на фиг. 5с, видно, что когда количество Ag равно 20 моль %, AgGaO2 присутствует в количестве 1,7 ммоль на грамм образца; когда количество Ag равно 10 моль %, AgGaO2 присутствует в количестве 1,0 ммоль на грамм образца; когда количество Ag равно 30 моль %, AgGaO2 присутствует в количестве 2,4 ммоль на грамм образца; и когда количество Ag равно 50 моль %, AgGaO2 присутствует в количестве 1,8 ммоль на грамм образца.
[0056] (Результаты анализа способом ТПД для O2)
Фиг. 6 иллюстрирует профиль измерения способом ТПД для O2. Как показано на фиг. 6, виды десорбции не были отмечены для Ga2O3 (сравнительный пример 1) и порошка Ag (сравнительный пример 2), но с другой стороны, пик десорбции кислорода был обнаружен вблизи значения 320°С в сложных оксидах, содержащих AgGaO2 (примеры с 1 по 4). Этот пик десорбции следует отнести к активному кислороду, десорбированному с участка Ag-O-Ga.
[0057] (Результаты анализа для адсорбции видов NOx при исследовании с использованием ИК излучения)
Фиг. 7 иллюстрирует результаты анализа посредством ИК излучения в среде, где NO и O2 были пропущены при 100°С относительно образцов согласно примерам 1, 2 и 4. Пик абсорбции, соответствующий нитритной соли (NO2-) и боковой выступ, соответствующий нитратной соли (NO3-) были обнаружены при 1,255 см-1. Эти результаты показывают, что газовая фаза NO была окислена кислородом и аккумулирована в виде нитритной соли и нитратной соли в образце.
[0058] (Результаты испытания аккумулирования NOx)
Фиг. 8а и 8b иллюстрируют количественные значения аккумулирования NOx при 100°С для каждого образца согласно примерам с 1 по 4 и сравнительным примерам 1 и 3. Фиг. 8а иллюстрирует количество аккумулирования NOx на единицу объема образца, а фиг. 8b иллюстрирует количество аккумулирования NOx на единицу веса образца. Взаимосвязь между количеством аккумулирования NOx на единицу объема или веса образца и долевым составом Ag показанная на фиг. 8а и 8b, демонстрирует тенденцию к увеличению количества аккумулирования NOx вследствие объединения Ag и Ga и обеспечивает явно выраженный пик при значении Ag/(Ag+Ga)=30 моль %. Выявлено, что образец, имеющий высокое значение аккумулирования (Ag3Ga7: пример 1, Ag5Ga5: пример 2, Ag7Ga3: пример 3), обеспечивает наличие множества эффективных участков для аккумулирования NOx и демонстрирует высокие характеристики в отношении количества аккумулирования на единицу объема по сравнению с Pd-шабазитом, который, как известно, обладает высокими низкотемпературными характеристиками для аккумулирования NOx (фиг. 8а). Кроме того, образец Ag1Ga9 (пример 4) также показал достаточное количество аккумулирования, хотя количество аккумулирования NOx было ниже, чем у Pd-шабазита. Порядок аккумулирования NOx на единицу веса применительно к композиции Ag/(Ag+Ga) полностью соответствовал порядку содержания AgGaO2 (фиг. 5с), и, следовательно, AgGaO2, как ожидается, обеспечивает реакцию аккумулирования.
[0059] На фиг. 11 показаны количества аккумулирования NOx при 50°С, 100°С, 140°С и 180°С для каждого образца согласно примерам с 5 по 8 и сравнительному примеру 3 (Pd-шабазит). По сравнению с Ag5Ga5 (пример 7) в Ag5Al0.5Ga4.5 (пример 8) количество аккумулированных NOx было ниже в области температур от 120 до 180°С, но количество аккумулированных NOx было выше при температуре 100°С или менее. В Ag5Al1.5Ga3.5 (пример 5) и Ag5Al2.5Ga2.5 (пример 6), где доля Al было еще больше, чем в Ag5Al0.5Ga4.5 (пример 8), количество аккумулированных NOx было выше, чем у Ag5Ga5 (пример 7) в области температур 140°С или менее. Кроме того, в Ag5Al2.5Ga2.5 (пример 6) количество аккумулированных NOx было выше, чем у Pd-шабазита (сравнительный пример 3) во всем температурном диапазоне 180°С или менее.
[0060] (Результаты анализа способом ТПД для NOx)
Фиг. 12 иллюстрирует профиль измерения способом ТПД для NOx для Ag5Ga5 (пример 7), а фиг. 13 иллюстрирует профиль измерения способом ТПД для NOx для Ag5Al2.5Ga2.5 (пример 6). В отношении обоих образцов были обнаружены виды NOx, демонстрирующие пик десорбции при 180°С, и виды NOx, испытывающие десорбцию в области более высоких температур. Исчезнувшие виды NOx, испытывающие десорбцию в области низких температур, были отнесены к соли нитрита (NO2-), имеющей низкую термическую стабильность, а виды NOx, испытывающие десорбцию в области высоких температур, были отнесены к соли нитрата (NO3-). С другой стороны, в профиле измерения способом ТПД для NOx после аккумулирования при 180°С, десорбция нитратной соли в области высокой температуры была преобладающей в обоих образцах.
[0061] Эти результаты показывают, что когда часть Ga замещается Al, при 180°С образуется большое количество нитратной соли, и предполагается, что причина этого заключается в том, что реакционная способность в оксиде или поверхностном кислороде была повышена, а степень превращения нитритной соли с низкой термостойкостью в нитратную соль с высокой термостойкостью тем самым была более ускорена, чем скорость десорбции азотистой кислоты.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2006 |
|
RU2370308C1 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА И СПОСОБ ВОССТАНОВЛЕНИЯ NO | 2005 |
|
RU2355470C2 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА И СПОСОБ ВОССТАНОВЛЕНИЯ NO | 2005 |
|
RU2386475C2 |
| КАТАЛИЗАТОР, НОСИТЕЛЬ КАТАЛИЗАТОРА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И СПОСОБ ОЧИСТКИ ОТХОДЯЩИХ ГАЗОВ ОТ ОКСИДОВ АЗОТА | 2001 |
|
RU2192307C1 |
| КАТАЛИЗАТОР ДЛЯ ОКИСЛЕНИЯ САЖИ | 2023 |
|
RU2832847C1 |
| Способ приготовления блочного катализатора | 2023 |
|
RU2825302C1 |
| СПОСОБ ПОЛУЧЕНИЯ И АКТИВАЦИИ ПОЛИМЕТАЛЛИЧЕСКИХ ЦЕОЛИТНЫХ КАТАЛИЗАТОРОВ, СОСТАВ И ПРИМЕНЕНИЕ КАТАЛИЗАТОРА ДЛЯ РАЗЛОЖЕНИЯ NO | 2002 |
|
RU2297278C2 |
| ТРОЙНОЙ КАТАЛИЗАТОР И ЕГО ПРИМЕНЕНИЕ В ВЫХЛОПНЫХ СИСТЕМАХ | 2016 |
|
RU2693482C2 |
| КАТАЛИЗАТОРЫ СКВ: ПЕРЕХОДНЫЙ МЕТАЛЛ/ЦЕОЛИТ | 2008 |
|
RU2506989C2 |
| ЧАСТИЦЫ ОКСИДА ЦЕРИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2746315C2 |
Изобретение относится к материалу, аккумулирующему NOx, способному эффективно накапливать оксиды азота (NOx) в области низких температур, и к способу очистки выхлопного газа с использованием материала, аккумулирующего NOx. Материал для аккумулирования NOx содержит сложный оксид серебра и галлия. Сложный оксид серебра и галлия предпочтительно представляет собой сложный оксид типа делафоссит. Сложный оксид получают посредством растворения соли серебра и соли галлия в растворителе и горячей сушки раствора, причем молярное соотношение серебро : галлий предпочтительно составляет от 2:8 до 7:3. Изобретение обеспечивает высокую способность аккумулирования NOx в области низких температур, в частности при низкой температуре 200°С или меньше. 4 н. и 4 з.п. ф-лы, 2 табл., 13 ил.
1. Материал для аккумулирования NOx, содержащий сложный оксид серебра и галлия, при этом молярное соотношение серебро : галлий в сложном оксиде серебра и галлия составляет от 3:7 до 7:3.
2. Материал для аккумулирования NOx по п. 1, в котором сложный оксид дополнительно содержит алюминий.
3. Материал для аккумулирования NOx по п. 1 или 2, в котором сложный оксид представляет собой сложный оксид типа делафоссит.
4. Материал для аккумулирования NOx по любому из пп. 1-3, в котором концентрация сложного оксида составляет от 1,7 ммоль/г до 2,4 ммоль/г.
5. Способ изготовления материала для аккумулирования NOx по любому из пп. 1-4, содержащий растворение солей металлов, составляющих сложный оксид, в растворителе и горячую сушку раствора.
6. Способ по п. 5, в котором молярное соотношение серебро : галлий или серебро : (галлий + алюминий) в сложном оксиде составляет от 2:8 до 7:3.
7. Устройство для аккумулирования NOx, содержащее материал для аккумулирования NOx по любому из пп. 1-4.
8. Способ очистки выхлопного газа, включающий в себя пропускание выхлопного газа, выпускаемого из двигателя внутреннего сгорания, через устройство для аккумулирования NOx по п. 7 и последующее пропускание выхлопного газа через устройство очистки выхлопного газа, содержащее каталитический металл.
| WO 2016079507 A1, 26.05.2016 | |||
| US 20060133977 A1, 22.06.2006 | |||
| WO 2016158642 A1, 06.10.2016 | |||
| КАТАЛИЗАТОР ДЛЯ ОЧИСТКИ ОТРАБОТАВШИХ ГАЗОВ И СПОСОБ ЕГО ПРОИЗВОДСТВА | 2010 |
|
RU2478427C1 |
| СПОСОБ УДАЛЕНИЯ NO И NO В ПРОЦЕССЕ ПОЛУЧЕНИЯ АЗОТНОЙ КИСЛОТЫ И УСТРОЙСТВО ДЛЯ ОСУЩЕСТВЛЕНИЯ ЭТОГО СПОСОБА | 2012 |
|
RU2600753C2 |
| US 6458741 B1, 01.10.2002 | |||
| WO 2017098518 A1, 15.06.2017 | |||
| JP 4277771 B2, 10.06.2009 | |||
| JP 2006297372 А, 02.11.2006 | |||
| CN 102482971 B, 29.10.2014. | |||
Авторы
Даты
2020-01-29—Публикация
2019-04-22—Подача