Перекрестная ссылка на родственную заявку
По настоящей заявке испрашивается приоритет в соответствии с 35 U.S.C. 119(е) предварительной патентной заявки США No. 61/985400, поданной 28 апреля 2014 г. Вышеупомянутая заявка включена в настоящее описание в качестве ссылки в полном объеме.
Уровень техники
Область техники
Настоящее изобретение относится к усовершенствованному способу получения соединений формулы (I), которые являются полезными в качестве ингибиторов PDE10. В частности, настоящее изобретение относится к усовершенствованному способу получения 1-(5-(4-хлор-3,5-диметоксифенил)фуран-2-ил)-2-этокси-2-(4-(5-метил-1,3,4-тиадиазол-2-ил)фенил)этанона (соединение 1001), который является полезным в качестве ингибитора PDE10.
Описание предшествующего уровня техники
Соединения формулы (I) являются известными и сильными ингибиторами PDE10:

где:
A представляет собой:
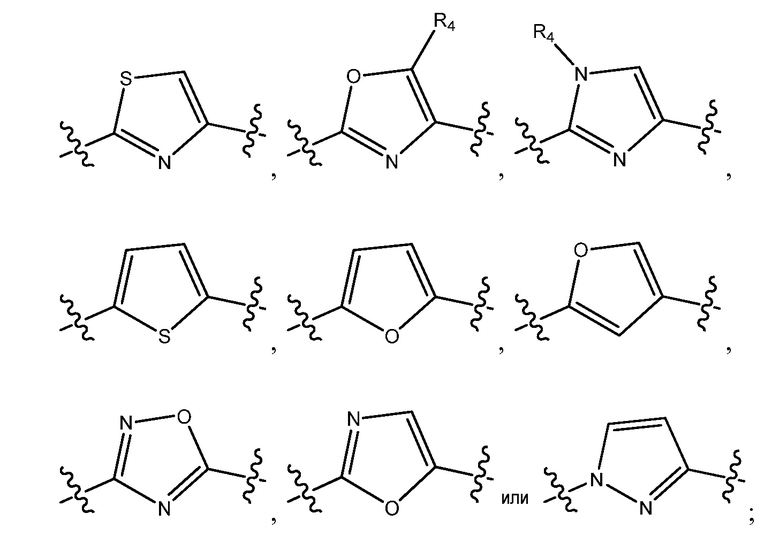
R1 представляет собой C1-6алкил, C1-6галогеналкил, C1-6аралкил, арил, -(CH2)nО(CH2)mCH3 или -(CH2)nN(CH3)2;
R2 представляет собой (i) замещенный или незамещенный арил или (ii) замещенный или незамещенный гетероциклил;
R3 представляет собой замещенный или незамещенный арил;
R4 представляет собой водород, C1-6алкил или C1-6галогеналкил;
n равно 1, 2, 3, 4, 5 или 6; и
m равно 0, 1, 2, 3, 4, 5 или 6.
Соединения формулы (II) являются известными и сильными ингибиторами PDE10:
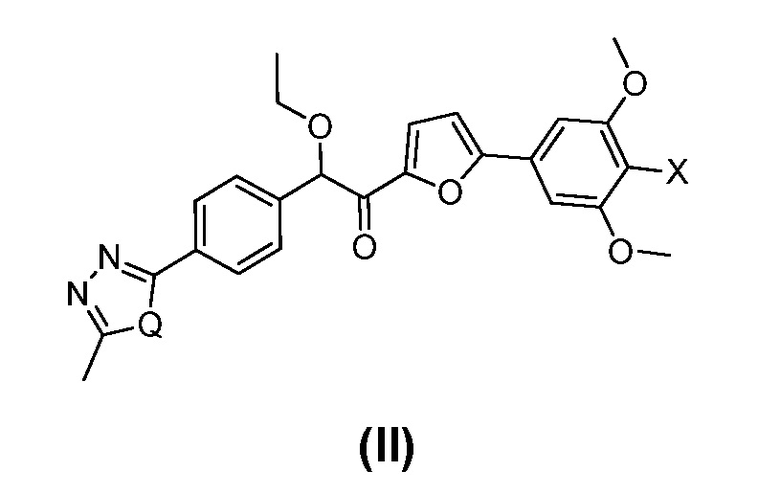
где:
Q представляет собой S или O; и
X представляет собой Cl или Br.
Соединения, имеющие структуру формулы (I), формулы (II), формулы (III) и соединение 1001 подпадают под действие ингибиторов PDE10, раскрытых в публикации международной заявки РСТ No. WO 2011/112828. Соединение 1001 (1-(5-(4-хлор-3,5-диметоксифенил)фуран-2-ил)-2-этокси-2-(4-(5-метил-1,3,4-тиадиазол-2-ил)фенил)этанон) конкретно раскрыто как соединение No. 65-10; Соединение 1002 (1-(5-(4-бром-3,5-диметоксифенил)фуран-2-ил)-2-этокси-2-(4-(5-метил-1,3,4-оксадиазол-2-ил)фенил)этанон) конкретно раскрыто как соединение No. 47-1; и Соединение 1003 (1-(5-(4-хлор-3,5-диметоксифенил)фуран-2-ил)-2-этокси-2-(4-(5-метил-1,3,4-оксадиазол-2-ил)фенил)этанон) конкретно раскрыто как соединение No. 63-1 в международной заявке РСТ No. WO 2011/112828. Соединения, имеющие структуру формулы (I), формулы (II), и соединения 1001-1003 могут быть получены в соответствии с общими способами, приведенными в публикации международной заявки РСТ No. WO 2011/112828, которая включена в настоящее описание в качестве ссылки.
Соединения формулы (II) и соединение 1001, в частности, имеют сложную структуру и их синтез является очень сложным. Известные методы синтеза сталкиваются с практическими ограничениями и не являются экономически выгодным для крупномасштабного производства. Существует необходимость в эффективном получении соединений формулы (II) и соединения 1001, в частности, с минимальным количеством стадий, хорошей химической чистотой и достаточным общим выходом. Известные способы получения соединений формулы (II) и соединения 1001, в частности, имеют ограниченный выход. Настоящее изобретение удовлетворяет этим потребностям и обеспечивает дополнительные связанные с этим преимущества.
Краткое описание
Настоящее изобретение относится к способу синтеза для получения соединений формулы (II), в частности, соединений 1001-1003, с использованием стадий синтеза, описанных в настоящем описании. Настоящее изобретение также относится к конкретным отдельным стадиям этого способа и конкретным отдельным промежуточным соединениям, используемым в этом способе.
В одном из вариантов осуществления предлагается способ получения соединения формулы (II):

где
Q представляет собой S или O,
X представляет собой Cl или Br, и
R1, R2 и R3 каждый независимо представляет собой C(1-6)алкил,
согласно следующей общей схеме (I):
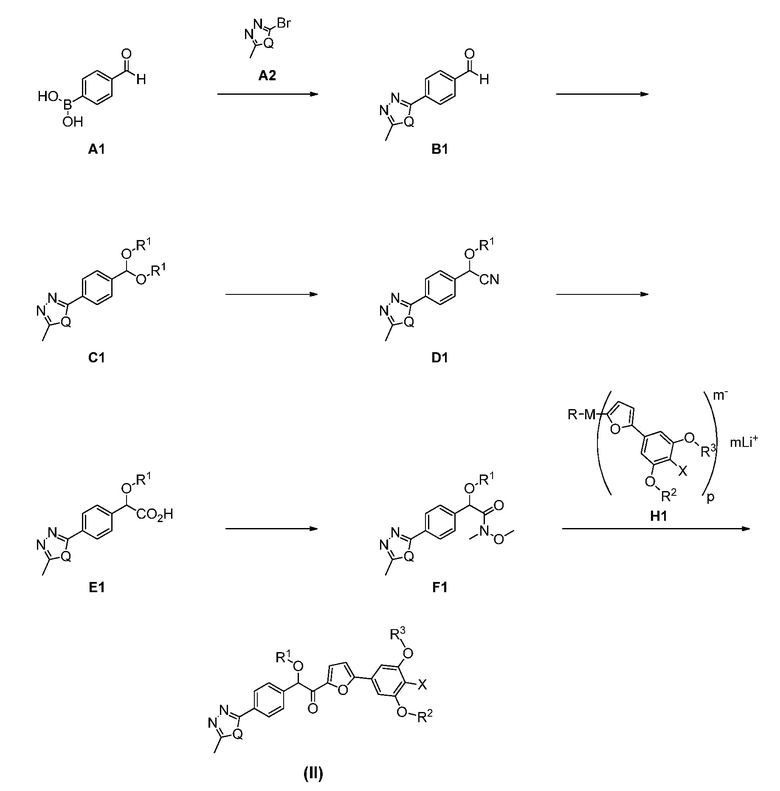
который включает:
преобразование бороновой кислоты A1 в карбальдегид B1 путем активации бороновой кислоты с активирующим веществом A2;
преобразование карбальдегида B1 в ацеталь C1 кислотным катализом с подходящим источником ортоформиата;
преобразование ацеталя C1 в нитрил D1 путем катализируемого цианирования с металлическим катализатором и источником цианида;
гидролиз D1 с подходящей кислотой с получением карбоновой кислоты E1;
преобразование карбоновой кислоты Е1 в амид F1 с подходящим основанием, подходящим связующим реагентом и источником амина;
преобразование амида F1 в соединение формулы (II) с анионным связующим реагентом, имеющим структуру H1,
где
M представляет собой металл I группы, металл II группы, Cu или Zn;
R, R2 и R3 каждый независимо представляет собой C(1-6)алкил;
m равно 1, 2, 3, или 4;
p равно 1, 2, 3, или 4; и
при необходимости, преобразование соединения формулы (II) в соль.
Другой аспект настоящего изобретения обеспечивает способ получения соединения формулы H1:
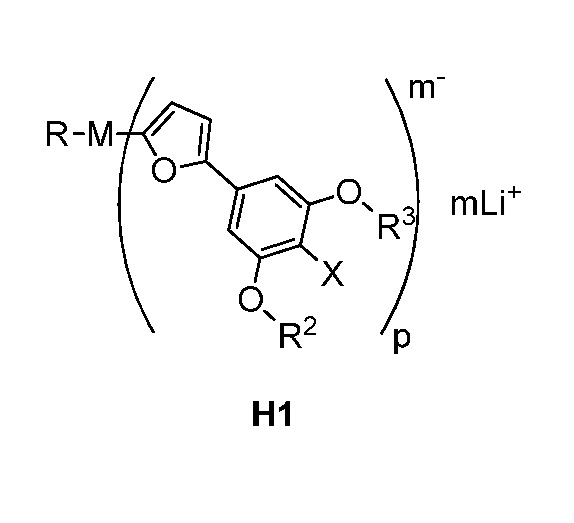
где
M представляет собой металл I группы, металл II группы, Cu или Zn,
R, R2 и R3 каждый независимо представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 1, 2, 3 или 4, и
p равно 1, 2, 3 или 4;
согласно следующей общей схеме (II):
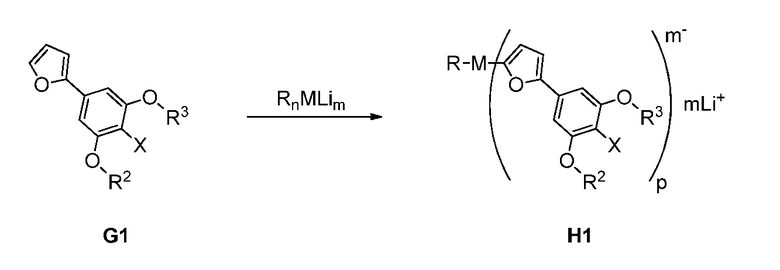
который включает:
получение в растворителе раствора литийалкильного металлического основания из Rn-Li и галогенида металла, содержащего M, где n равно 1, 2, 3 4 или 5; и
получение смешанного металл литиированного H1 из G1 и литийалкильного металлического основания.
В одном варианте осуществления предложен способ для получения соединения формулы (III):
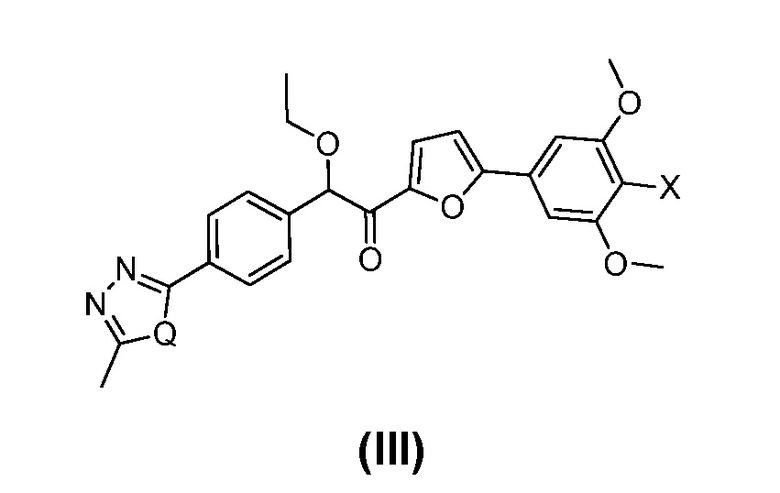
где Q представляет собой O или S и X представляет собой Cl или Br,
согласно следующей общей схеме (III):

который включает:
преобразование бороновой кислоты A1 в карбальдегид B1 путем активации бороновой кислоты с активирующим веществом A2;
преобразование карбальдегида B1 в ацеталь C1-1 кислотным катализом с подходящим источником ортоформиата;
преобразование ацеталя C1-1 в нитрил D1-1 путем катализируемого цианирования с металлическим катализатором и источником цианида;
гидролиз D1-1 с подходящей кислотой с получением карбоновой кислоты E1-1;
преобразование карбоновой кислоты Е1-1 в амид F1-1 с подходящим основанием, подходящим связующим реагентом и источником амина;
преобразование амида F1-1 в соединение формулы (III) с анионным связующим реагентом, имеющим структуру H1-1,
где
M представляет собой металл I группы, металл II группы, Cu или Zn;
R представляет собой C(1-6)алкил;
m равно 1, 2, 3 или 4;
p равно 1, 2, 3 или 4; и
при необходимости, преобразование соединения формулы (III) в соль.
Другой аспект настоящего изобретения относится к способу получения соединения формулы H1-1:
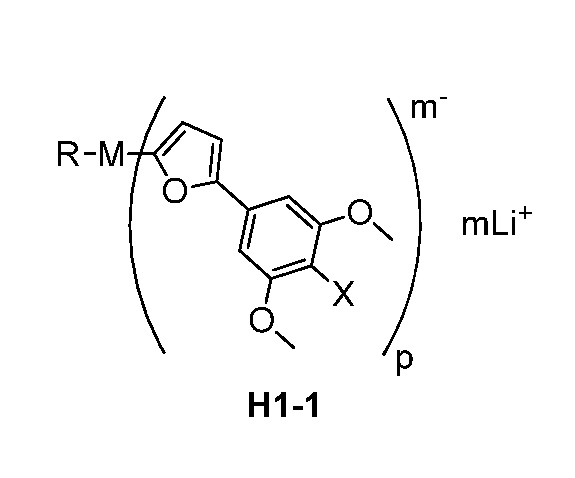
где
M представляет собой металл I группы, металл II группы, Cu или Zn,
R представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 1, 2, 3 или 4, и
p равно 1, 2, 3 или 4;
согласно следующей общей схеме (IV):
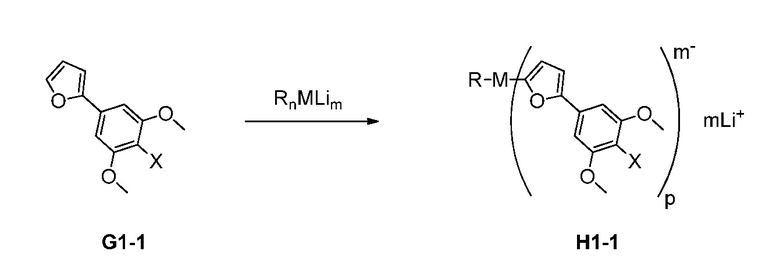
который включает:
получение в растворителе раствора литийалкильного металлического основания из Rn-Li и галогенида металла, содержащего M, где n равно 1, 2, 3 4, или 5; и
получение смешанного металл литиированного H1-1 из G1-1 и литийалкильного металлического основания.
Другой аспект настоящего изобретения относится к способу получения соединений 1001-1003, или их соли в соответствии с приведенной выше общей схемой (I).
Другой аспект настоящего изобретения относится к способу получения соединений 1001-1003 или их соли в соответствии с приведенной выше общей схемой (III).
Другой аспект настоящего изобретения относится к новым промежуточным соединениям, полезным для получения соединений формулы (II), формулы (III) или соединений 1001-1003.
В некоторых вариантах осуществления настоящее изобретение предоставляет промежуточное соединение, имеющее структуру формулы H1:

где
M представляет собой металл I группы, металл II группы, Cu или Zn,
R, R2 и R3 каждый независимо представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 1, 2, 3 или 4, и
p равно 1, 2, 3 или 4.
В некоторых вариантах осуществления настоящее изобретение предоставляет одно или несколько промежуточных соединений, выбранных из:

Эти и другие аспекты настоящего изобретения будут очевидны со ссылкой на следующее подробное описание. С этой целью в настоящем описании указаны различные ссылки, которые описывают более подробно определенную вспомогательную информацию, способы, соединения и/или композиции, и каждая из ссылок вводится в настоящее описание в качестве ссылки в полном объеме.
Подробное описание
Определения
Термины, специально не определенные в настоящем документе, имеют значения, которые дали бы им специалисты в данной области в свете раскрытия и контекста. Как, впрочем, используемые в настоящей заявке, если не указано иное, следующие термины имеют указанные значения:
"Амино" относится к -NH2 радикалу.
"Циано" относится к -CN радикалу.
"Гидрокси" или "гидроксил" относится к -OH радикалу.
"Имино" относится к =NH заместителю.
"Нитро" относится к -NО2 радикалу.
"Оксо" относится к =О заместителю.
"Тиоксо" относится к =S заместителю.
"C1-6алкил" означает неразветвленный или разветвленный, нециклический или циклический, ненасыщенный или насыщенный алифатический углеводородный радикал, содержащий от 1 до 6 атомов углерода. Типичные насыщенные неразветвленные алкилы включают метил, этил, н-пропил, н-бутил, н-пентил, н-гексил и тому подобное; в то время как насыщенные разветвленные алкилы включают изопропил, втор-бутил, изобутил, трет-бутил, изопентил и тому подобное. Типичные насыщенные циклические алкилы включают циклопропил, циклобутил, циклопентил, циклогексил и тому подобное; в то время как ненасыщенные циклические алкилы включают циклопентенил и циклогексенил и тому подобное.
Ненасыщенные алкилы содержат по меньшей мере одну двойную или тройную связь между смежными атомами углерода (обозначают как "алкенил" или "алкинил", соответственно). Типичные неразветвленные и разветвленные алкенилы включают, этиленил, пропиленил, 1-бутенил, 2-бутенил, изобутиленил, 1-пентенил, 2-пентенил, 3-метил-1-бутенил, 2-метил-2-бутенил, 2,3-диметил-2-бутенил и тому подобное; в то время как типичные неразветвленные и разветвленные алкинилы включают, ацетиленил, пропинил, 1-бутинил, 2-бутинил, 1-пентинил, 2-пентинил, 3-метил-1-бутинил, и тому подобное.
"C1-6алкилен" или "C1-6алкиленовая цепь" относится к прямой или разветвленной двухвалентной углеводородной цепи, присоединяющей остаток молекулы к радикалу, состоящей только из атомов углерода и водорода, которая является насыщенной или ненасыщенной (т.е. содержит одну или более двойных и/или тройных связей), и содержащей от одного до шести атомов углерода, например, метилен, этилен, пропилен, н-бутилен, этенилен, пропенилен, н-бутенилен, пропинилен, н-бутинилен и тому подобные. Алкиленовую цепь присоединяют к остатку молекулы через одинарную или двойную связь и к радикалу через одинарную или двойную связь. Положения присоединения алкиленовой цепи к остатку молекулы и к радикалу можно осуществлять через один атом углерода или любые два атома углерода в цепи.
"C1-6алкокси" относится к радикалу формулы -ORa, где Ra представляет собой алкильный радикал, как определено выше, например, метокси, этокси и тому подобные.
"Арил" относится к углеводородной кольцевой системе, содержащей водород, 6-18 атомов углерода и по меньшей мере одно ароматическое кольцо. Арильный радикал может представлять собой моноциклическую, бициклическую, трициклическую или тетрациклическую кольцевую систему, которая может содержать конденсированные или мостиковые кольцевые системы. Арильные радикалы включают, но ими не ограничиваются, арильные радикалы, полученные из ацеантрилена, аценафтилена, ацефенантрилена, антрацена, азулена, бензола, хризена, фторантена, флуорена, as-индацена, s-индацена, индана, индена, нафталина, феналена, фенантрена, плеиадена, пирена и трифенилена.
"C1-6аралкил" обозначает радикал формулы -Rb-Rc, где Rb представляет собой алкиленовую цепь, как определено выше, и Rc представляет собой один или более арильных радикалов, как определено выше, например, бензил, дифенилметил и тому подобные.
"Циклоалкил" или "карбоциклическое кольцо" относится к стабильному неароматическоу моноциклическому или полициклическому углеводородному радикалу, состоящему только из атомов углерода и водорода, который может содержать конденсированные или мостиковые кольцевые системы, имеющие от трех до пятнадцати атомов углерода, предпочтительно, имеющие от трех до десяти атомов углерода, и который может быть насыщенным или ненасыщенным и присоединенным к остатку молекулы одинарной связью. Моноциклические радикалы включают, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Полициклические радикалы включают, например, адамантил, норборнил, декалинил, 7,7-диметил-бицикло[2.2.1]гептанил и тому подобные.
"Гало" или "галоген" относится к брому, хлору, фтору или йоду.
"C1-6галогеналкил" относится к C1-6алкильному радикалу, как определено выше, который замещен одним или более галогеновыми радикалами, как определено выше, например, трифторметил, дифторметил, трихлорметил, 2,2,2-трифторэтил, 1,2-дифторэтил, 3-бром-2-фторпропил, 1,2-дибромэтил и тому подобные.
"Гетероцикл" или "гетероциклическое кольцо" означает любое 4-7-членное моноциклическое или 7-10-членное бициклическое, гетероциклическое кольцо, которое является насыщенным, ненасыщенным или ароматическим, и содержащее от 1 до 4 гетероатомов, независимо выбранных из азота, кислорода и серы, и где гетероатомы азота и серы, необязательно, могут быть окисленными, и гетероатом азота, необязательно, может быть четвертичным, включая бициклические кольца, в которых любой из указанных выше гетероциклов конденсирован с бензольным кольцом. Гетероцикл можно присоединять через любой гетероатом или атом углерода. Ароматический гетероцикл называется в настоящем документе как "гетероарил", и включает (но ими не ограничивается) фурил, бензофуранил, тиофенил, бензотиофенил, пирролил, индолил, изоиндолил, азаиндолил, пиридил, хинолинил, изохинолинил, оксазолил, изооксазолил, бензоксазолил, пиразолил, имидазолил, бензимидазолил, тиазолил, бензотиазолил, изотиазолил, пиридазинил, пиримидинил, пиразинил, триазинил, циннолинил, фталазинил, оксадиазолил, тиадиазолил, бензизоксазолил, триазолил, тетразолил, индазолил и хиназолинил. В дополнение к указанным выше гетероарилам, гетероциклы также включают морфолинил, пирролидинонил, пирролидинил, пиперидинил, пиперазинил и тому подобное. В дополнение, гетероциклы также включают бензотиофен-2-ил, 2,3-дигидробензо-1,4-диоксин-6-ил, бензо-1,3-диоксол-5-ил и тому подобные.
Термин "замещенный", как используется в настоящем описании (например, в контексте замещенного гетероциклила или замещенного арила), обозначает то, что по меньшей мере один атом водорода замещен заместителем. "Заместители" в контексте настоящего изобретения включают галоген, гидрокси, оксо, циано, нитро, имино, тиоксо, амино, алкиламино, диалкиламино, алкил, алкокси, алкилтио, галогеналкил, арил, аралкил, гетероарил, гетероарилалкил, гетероцикл и гетероциклалкил, а также -NRaRb, -NRaC(=O)Rb, -NRaC(=O)NRaNRb, -NRaC(=O)ORb, -NRaSO2Rb, -C(=O)Ra, -C(=O)ORa, -C(=O)NRaRb, -OC(=O)NRaRb, -ORa, -SRa, -SORa, -S(=O)2Ra, -OS(=O)2Ra, -S(=O)2ORa, =NSO2Ra и -SO2NRaRb. В изложенном выше Ra и Rb в данном контексте могут быть одинаковыми или различными и независимо представлять собой водород, алкил, галогеналкил, циклоалкил, арил, аралкил, гетероциклил. Кроме того, вышеуказанные заместители могут быть дополнительно замещены одним или несколькими из указанных выше заместителей.
Соединения по настоящему изобретению можно обычно использовать в виде свободной кислоты или свободного основания. Альтернативно, соединения по настоящему изобретению можно использовать в виде солей присоединения кислоты или основания. Соли присоединения кислоты свободных аминосоединений по настоящему изобретению можно получить способами, хорошо известными в данной области техники, и их можно получить из органических и неорганических кислот. Подходящие органические кислоты включают малеиновую, фумаровую, бензойную, аскорбиновую, янтарную, метансульфоновую, уксусную, трифторуксусную, щавелевую, пропионовую, винную, салициловую, лимонную, глюконовую, молочную, миндальную, коричную, аспарагиновую, стеариновую, пальмитиновую, гликолевую, глютаминовую и бензолсульфоновую кислоты. Подходящие неорганические кислоты включают хлороводородную, бромоводородную, серную, фосфорную и азотную кислоты. Соли присоединения основания включают те соли, которые образуются с карбоксилатным анионом, и включают соли, полученные с органическими и неорганическими катионами, такие как соли, выбранные из солей щелочных и щелочноземельных металлов (например, лития, натрия, калия, магния, бария и кальция), а также аммониевым ионом и его замещенными производными (например, дибензиламмоний, бензиламмоний, 2-гидроксиэтиламмоний и тому подобные). Таким образом, термин "фармацевтически приемлемая соль" формул (I), (II) и (III), как предполагается, охватывает любую и все приемлемые солевые формы.
Варианты осуществления изобретения
Как было упомянуто выше, настоящее изобретение относится к способу синтеза для получения соединений формулы (II) и формулы (III), в частности, соединений 1001-1003, с использованием стадий синтеза, описанных в настоящем описании. Настоящее изобретение также относится к конкретным отдельным стадиям этого способа и конкретным отдельным промежуточным соединениям, используемым в этом способе.
В схемах синтеза ниже, если не указано иное, то все группы заместителей в химических формулах, имеют значения, как в формуле (II). Реагенты, используемые в приведенных ниже примерах, могут быть получены либо так, как описано в настоящем документе, или, если не описано в настоящем документе, являются сами или коммерчески доступными или могут быть получены из коммерчески доступных материалов способами, известными в данной области техники. Некоторые исходные материалы, например, могут быть получены способами, описанными в публикации международной заявки РСТ WO 2011/112828.
Оптимальные условия реакции и время реакции могут изменяться в зависимости от конкретных используемых реагентов. Если не указано иное, растворители, температура, давление и другие условия реакции могут быть легко выбраны обычным специалистом в данной области. Как правило, ход реакции можно контролировать с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) или спектроскопией ядерного магнитного резонанса (ЯМР-спектроскопия), при необходимости, и промежуточные соединения и продукты могут быть очищены с помощью хроматографии и/или путем перекристаллизации или осаждения с или без обработки с углеродом.
В одном из вариантов осуществления настоящее изобретение относится к многостадийному способу синтеза для получения соединений формулы (II), и, в частности, соединений 1001-1003, как изложено в общих схемах (I) и (II). В одном из вариантов осуществления предложен способ получения соединения формулы (II):
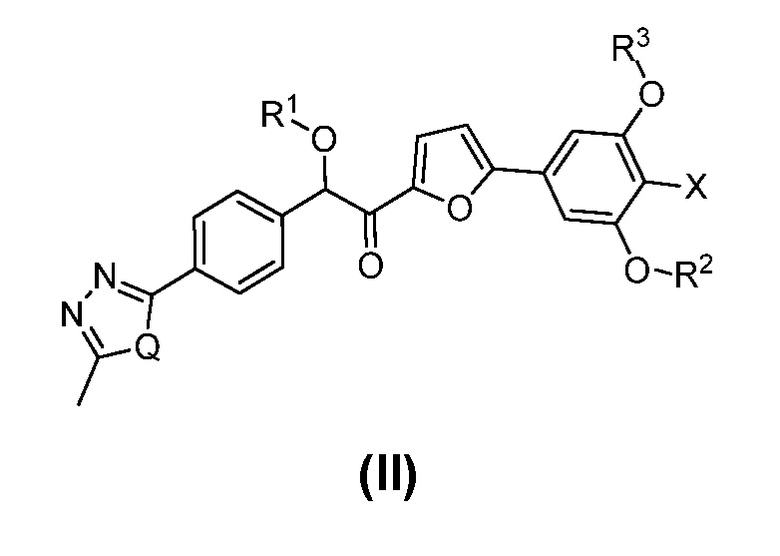
где
Q представляет собой S или O,
X представляет собой Cl или Br, и
R1, R2 и R3 каждый независимо представляет собой C(1-6)алкил,
согласно следующей общей схеме (I):
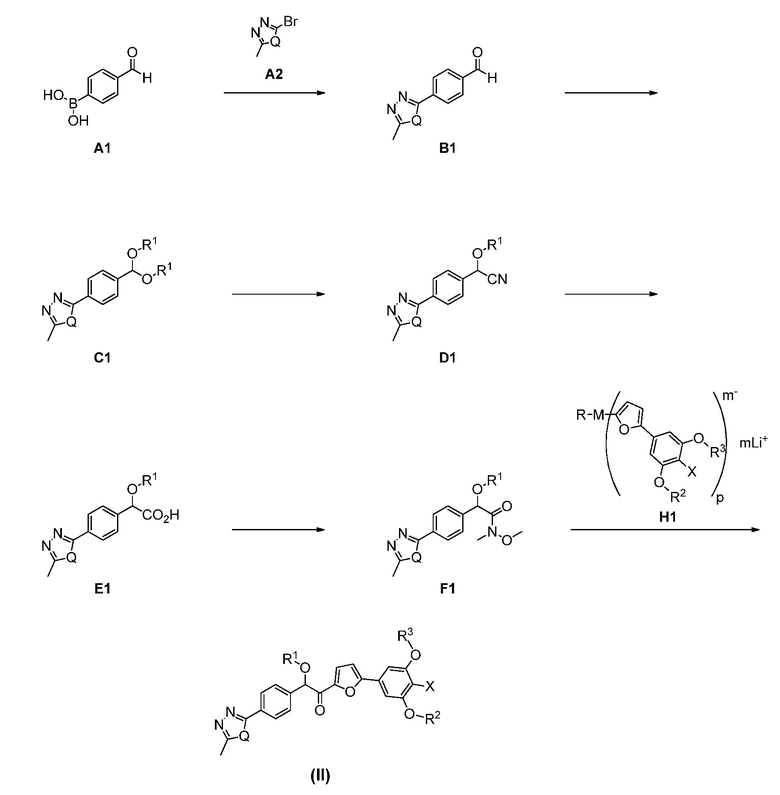
который включает:
преобразование бороновой кислоты A1 в карбальдегид B1 путем активации бороновой кислоты с активирующим веществом A2;
преобразование карбальдегида B1 в ацеталь C1 кислотным катализом с подходящим источником ортоформиата;
преобразование ацеталя C1 в нитрил D1 путем катализируемого цианирования с металлическим катализатором и источником цианида;
гидролиз D1 с подходящей кислотой с получением карбоновой кислоты E1;
преобразование карбоновой кислоты Е1 в амид F1 с подходящим основанием, подходящим связующим реагентом и источником амина;
преобразование амида F1 в соединение формулы (II) с анионным связующим реагентом, имеющим структуру H1,
где
M представляет собой металл I группы, металл II группы, Cu или Zn;
R, R2 и R3 каждый независимо представляет собой C(1-6)алкил;
m равно 1, 2, 3 или 4;
p равно 1, 2, 3 или 4; и
при необходимости, преобразование соединения формулы (II) в соль.
В дополнительных вариантах осуществления способа общей схемы (I) Q представляет собой O.
В дополнительных вариантах осуществления способа общей схемы (I) Q представляет собой S.
В дополнительных вариантах осуществления способа общей схемы (I) X представляет собой Cl.
В дополнительных вариантах осуществления способа общей схемы (I) X представляет собой Br.
В дополнительных вариантах осуществления способа общей схемы (I) M представляет собой металл II группы.
В дополнительных вариантах осуществления способа общей схемы (I) M представляет собой Mg.
В дополнительных вариантах осуществления способа общей схемы (I), R1 представляет собой метил, этил или пропил.
В дополнительных вариантах осуществления способа общей схемы (I), R1 представляет собой этил.
В дополнительных вариантах осуществления способа общей схемы (I), R2 представляет собой метил, этил или пропил.
В дополнительных вариантах осуществления способа общей схемы (I), R2 представляет собой метил.
В дополнительных вариантах осуществления способа общей схемы (I), R3 представляет собой метил, этил или пропил.
В дополнительных вариантах осуществления способа общей схемы (I), R3 представляет собой метил.
В дополнительных вариантах осуществления способа общей схемы (I), R представляет собой бутил. В дополнительных вариантах осуществления способа общей схемы (I) кислотный катализатор, используемый для образования ацеталя C1, представляет собой моногидрат пара-толуолсульфоновой кислоты.
В дополнительных вариантах осуществления способа общей схемы (I), подходящий источник ортоформиата представляет собой триэтилортоформиат.
В дополнительных вариантах осуществления способа общей схемы (I) металлический катализатор на стадии цианирования представляет собой соль кобальта.
В дополнительных вариантах осуществления способа общей схемы (I) металлический катализатор на стадии цианирования представляет собой CoCl2.
В дополнительных вариантах осуществления способа общей схемы (I) источник цианида представляет собой триметилсилил цианид.
В дополнительных вариантах осуществления способа общей схемы (I), подходящая кислота на стадии гидролиза представляет собой HCl.
В дополнительных вариантах осуществления способа общей схемы (I), подходящее основание на стадии амидирования представляет собой триэтиламин.
В дополнительных вариантах осуществления способа общей схемы (I), подходящий связующий реагент стадии амидирования представляет собой пропилфосфоновый ангидрид.
В дополнительных вариантах осуществления способа общей схемы (I) источник амина представляет собой гидрохлорид Ν,Ο-диметилгидроксиламина.
В дополнительных вариантах осуществления способа общей схемы (I) соединение формулы (II) представляет собой:

В дополнительных вариантах осуществления способа общей схемы (I) соединение формулы (II) представляет собой:

В дополнительных вариантах осуществления способа общей схемы (I) соединение формулы (II) представляет собой:
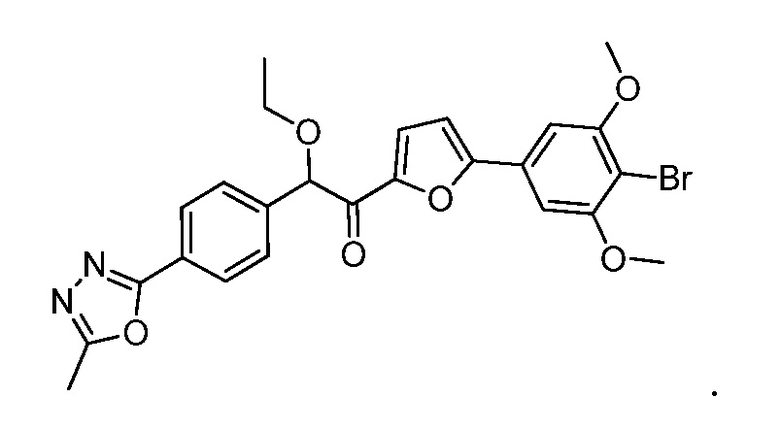
В другом варианте осуществления предложен способ получения соединения формулы H1:
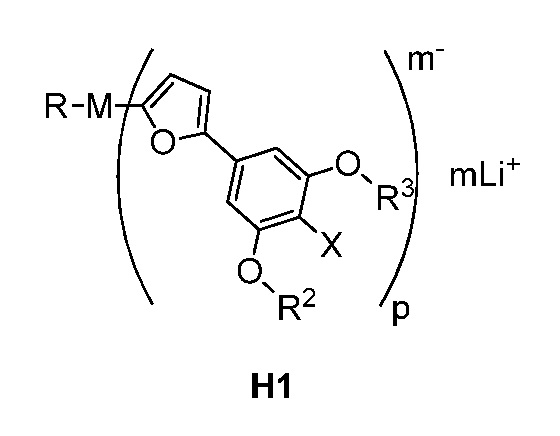
где
M представляет собой металл I группы, металл II группы, Cu или Zn,
R, R2 и R3 каждый независимо представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 1, 2, 3 или 4, и
p равно 1, 2, 3 или 4;
согласно следующей общей схеме (II):
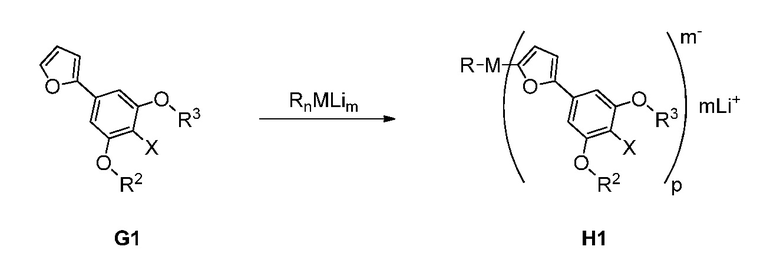
который включает:
получение в растворителе раствора литийалкильного металлического основания из Rn-Li и галогенида металла, содержащего M, где n равно 1, 2, 3 4 или 5; и
получение смешанного металл литиированного H1 из G1 и литийалкильного металлического основания.
В дополнительных вариантах осуществления способа общей схемы (II) R2 представляет собой метил, этил или пропил.
В дополнительных вариантах осуществления способа общей схемы (II) R2 представляет собой метил.
В дополнительных вариантах осуществления способа общей схемы (II) R3 представляет собой метил, этил или пропил.
В дополнительных вариантах осуществления способа общей схемы (II) R3 представляет собой метил.
В дополнительных вариантах осуществления способа общей схемы (II) R представляет собой бутил.
В дополнительных вариантах осуществления способа общей схемы (II) X представляет собой Cl.
В дополнительных вариантах осуществления способа общей схемы (II) X представляет собой Br.
В дополнительных вариантах осуществления способа общей схемы (II) M представляет собой металл (I) группы.
В дополнительных вариантах осуществления способа общей схемы (II) M представляет собой металл II группы.
В дополнительных вариантах осуществления способа общей схемы (II) M представляет собой Mg.
В дополнительных вариантах осуществления способа общей схемы (II) M представляет собой Cu.
В дополнительных вариантах осуществления способа общей схемы (II) M представляет собой Zn.
В дополнительных вариантах осуществления способа общей схемы (II) литийалкильное металлическое основание представляет собой литий алкилмагниевое основание.
В дополнительных вариантах осуществления способа общей схемы (II) литийалкильное металлическое основание представляет собой Bu4MgLi2.
В дополнительных вариантах осуществления способа общей схемы (II) соединение формулы H1 представляет собой соединение формулы H1-1:
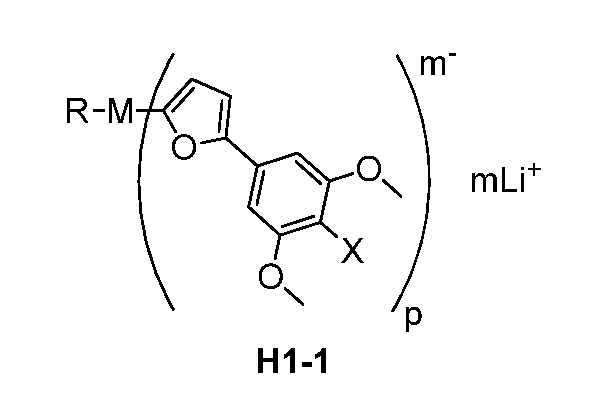
где
M представляет собой металл I группы, металл II группы, Cu или Zn,
R представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 1, 2, 3 или 4, и
p равно 1, 2, 3 или 4.
В дополнительных вариантах осуществления способа общей схемы (II) соединение формулы H1-1 представляет собой:
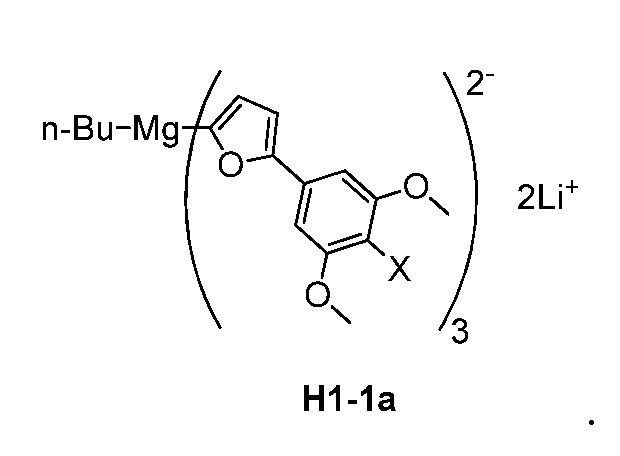
В дополнительных вариантах осуществления способа общей схемы (II) соединение формулы H1-1a представляет собой:
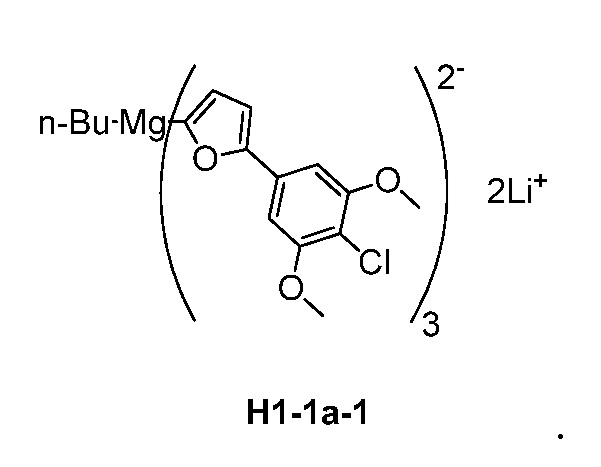
В одном из вариантов осуществления настоящее изобретение относится к многостадийному способу синтеза для получения соединений формулы (II) и, в частности, соединений 1001-1003, как изложено в общих схемах (III) и (IV). В одном из вариантов осуществления предложен способ получения соединения формулы (III):

где Q представляет собой S или O и X представляет собой Cl или Br,
согласно следующей общей схеме (III):
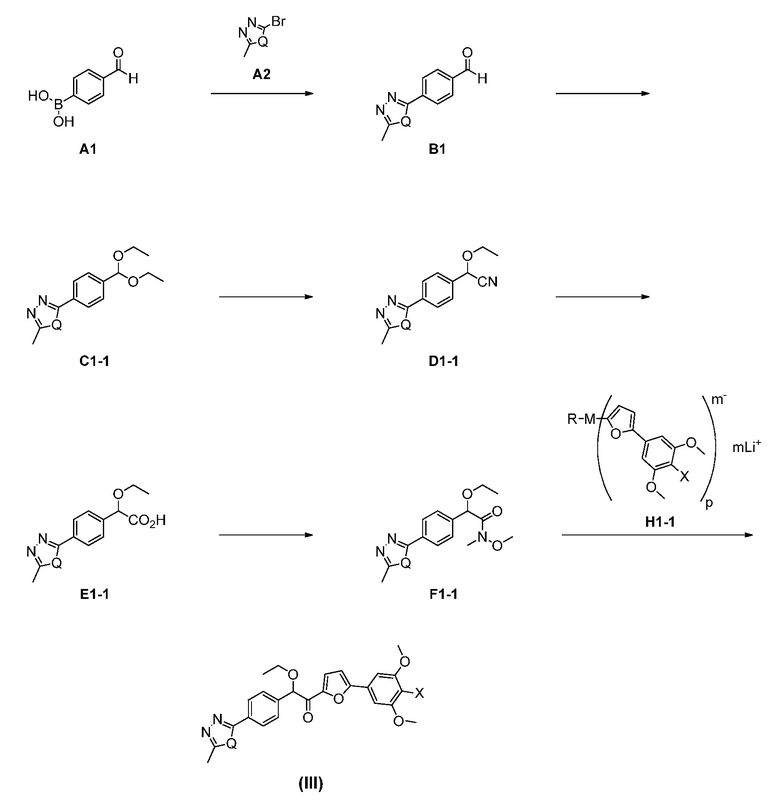
который включает
преобразование бороновой кислоты A1 в карбальдегид B1 путем активации бороновой кислоты с активирующим веществом A2;
преобразование карбальдегида B1 в ацеталь C1-1 кислотным катализом с подходящим источником ортоформиата;
преобразование ацеталя C1-1 в нитрил D1-1 путем катализируемого цианирования с металлическим катализатором и источником цианида;
гидролиз D1-1 с подходящей кислотой с получением карбоновой кислоты E1-1;
преобразование карбоновой кислоты Е1-1 в амид F1-1 с подходящим основанием, подходящим связующим реагентом и источником амина;
преобразование амида F1-1 в соединение формулы (III) с анионным связующим реагентом, имеющим структуру H1-1,
где
M представляет собой металл I группы, металл II группы, Cu или Zn;
R представляет собой C(1-6)алкил;
m равно 1, 2, 3 или 4;
p равно 1, 2, 3 или 4; и
при необходимости, преобразование соединения формулы (III) в соль.
В дополнительных вариантах осуществления способа общей схемы (III) Q представляет собой O.
В дополнительных вариантах осуществления способа общей схемы (III) Q представляет собой S.
В дополнительных вариантах осуществления способа общей схемы (III) X представляет собой Cl.
В дополнительных вариантах осуществления способа общей схемы (III) X представляет собой Br.
В дополнительных вариантах осуществления способа общей схемы (III), M представляет собой металл II группы.
В дополнительных вариантах осуществления способа общей схемы (III), M представляет собой Mg.
В дополнительных вариантах осуществления способа общей схемы (III), R представляет собой бутил.
В дополнительных вариантах осуществления способа общей схемы (III), кислотный катализатор, используемый для образования ацеталя C1-1, представляет собой моногидрат пара-толуолсульфоновой кислоты.
В дополнительных вариантах осуществления способа общей схемы (III), подходящий источник ортоформиата представляет собой триэтилортоформиат.
В дополнительных вариантах осуществления способа общей схемы (III), металлический катализатор на стадии цианирования представляет собой соль кобальта.
В дополнительных вариантах осуществления способа общей схемы (III), металлический катализатор на стадии цианирования представляет собой CoCl2.
В дополнительных вариантах осуществления способа общей схемы (III), источник цианида представляет собой триметилсилил цианид.
В дополнительных вариантах осуществления способа общей схемы (III), подходящая кислота на стадии гидролиза представляет собой HCl.
В дополнительных вариантах осуществления способа общей схемы (III), подходящее основание на стадии амидирования представляет собой триэтиламин.
В дополнительных вариантах осуществления способа общей схемы (III), подходящий связующий реагент стадии амидирования представляет собой пропилфосфоновый ангидрид.
В дополнительных вариантах осуществления способа общей схемы (III), источник амина представляет собой гидрохлорид Ν,Ο-диметилгидроксиламина.
В дополнительных вариантах осуществления способа общей схемы (III) соединение формулы (III) представляет собой:

В дополнительных вариантах осуществления способа общей схемы (III) соединение формулы (III) представляет собой:
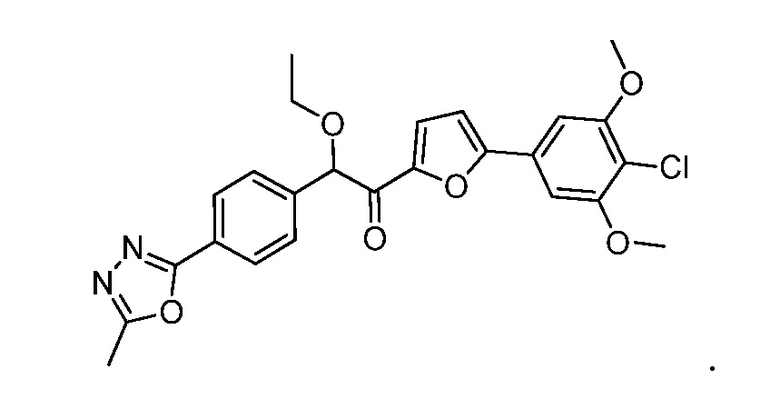
В дополнительных вариантах осуществления способа общей схемы (III) соединение формулы (III) представляет собой:
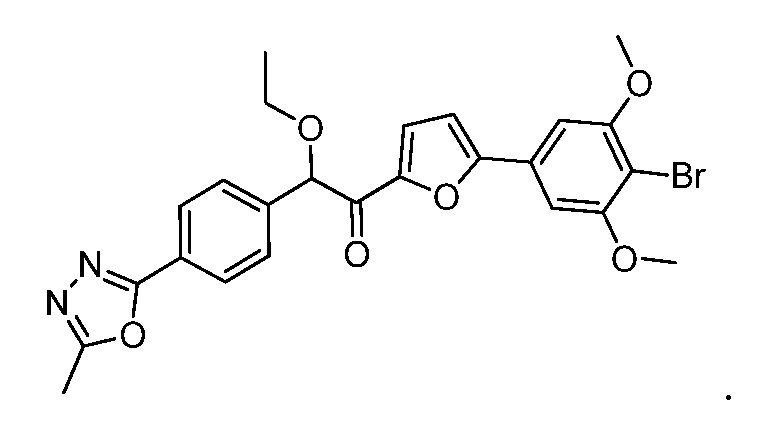
В другом варианте осуществления предложен способ получения соединения формулы H1-1:

где
M представляет собой металл I группы, металл II группы, Cu или Zn,
R представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 1, 2, 3 или 4, и
p равно 1, 2, 3 или 4;
согласно следующей общей схеме (IV):

который включает:
получение в растворителе раствора литийалкильного металлического основания из Rn-Li и галогенида металла, содержащего M, где n равно 1, 2, 3 4 или 5; и
получение смешанного металл литиированного H1-1 из G1-1 и литийалкильного металлического основания.
В дополнительных вариантах осуществления способа общей схемы (IV), X представляет собой Cl.
В дополнительных вариантах осуществления способа общей схемы (IV), X представляет собой Br.
В дополнительных вариантах осуществления способа общей схемы (IV), M представляет собой металл (I) группы.
В дополнительных вариантах осуществления способа общей схемы (IV), M представляет собой металл II группы.
В дополнительных вариантах осуществления способа общей схемы (IV), M представляет собой Mg.
В дополнительных вариантах осуществления способа общей схемы (IV), M представляет собой Cu.
В дополнительных вариантах осуществления способа общей схемы (IV), M представляет собой Zn.
В дополнительных вариантах осуществления способа общей схемы (IV), R представляет собой бутил.
В дополнительных вариантах осуществления способа общей схемы (IV), литийалкильное металлическое основание представляет собой литий алкилмагниевое основание.
В дополнительных вариантах осуществления способа общей схемы (IV), литийалкильное металлическое основание представляет собой Bu4MgLi2.
В дополнительных вариантах осуществления способа общей схемы (IV), соединение формулы H1-1 представляет собой соединение формулы H1-1a:
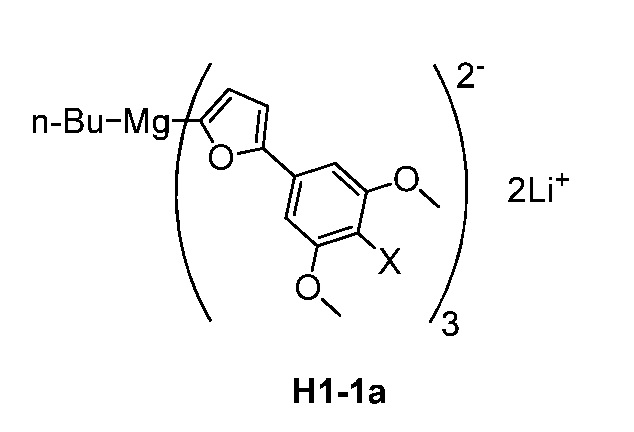
В дополнительных вариантах осуществления способа общей схемы (II) соединение формулы H1-1a представляет собой:

Дополнительные варианты осуществления настоящего изобретения относятся к отдельным стадиям многостадийных общих способов синтеза, описанных выше в (I)-(IV) и отдельным промежуточным соединениям, используемым в этих стадиях. Эти промежуточные соединения по настоящему изобретению подробно описаны ниже. Все группы заместителей в промежуточных соединениях, описанных ниже, являются такими, как определены в многостадийном способе выше.
Предпочтительные анионные связующие реагенты выбраны из соединения, имеющего структуру, соответствующую формуле H1:
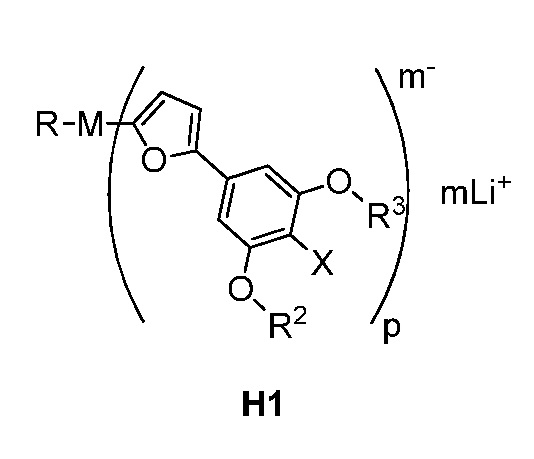
где
M представляет собой металл I группы, металл II группы, Cu или Zn,
R, R2 и R3 каждый независимо представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 1, 2, 3 или 4, и
p равно 1, 2, 3 или 4.
Предпочтительные анионные связующие реагенты выбраны из соединения, имеющего структуру, соответствующую формуле H1-1:

где
M представляет собой металл I группы, металл II группы, Cu или Zn,
R представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 1, 2, 3 или 4, и
p равно 1, 2, 3 или 4.
В другом варианте осуществления M представляет собой Mg.
Предпочтительные анионные связующие реагенты выбраны из соединения, имеющего структуру, соответствующую формуле H1-1a:
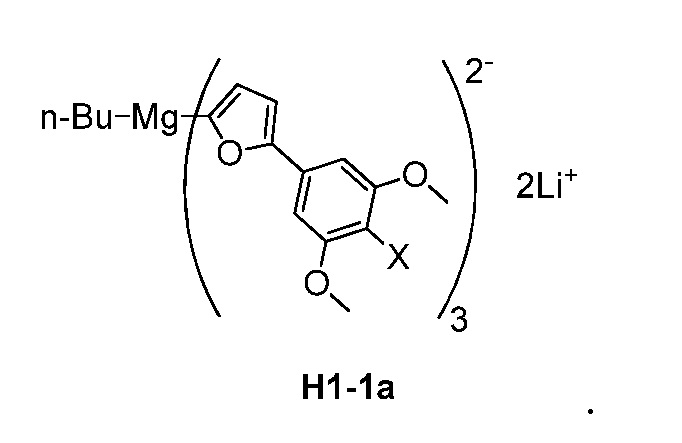
где X представляет собой Cl или Br.
В другом варианте осуществления X представляет собой Cl.
В другом варианте осуществления X представляет собой Br.
В другом варианте осуществления анионный связующий реагент имеет следующую структуру:

В другом варианте осуществления предпочтительное нитрильное промежуточное соединение имеет следующую структуру:
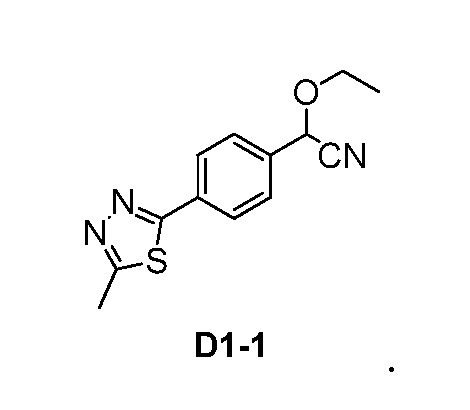
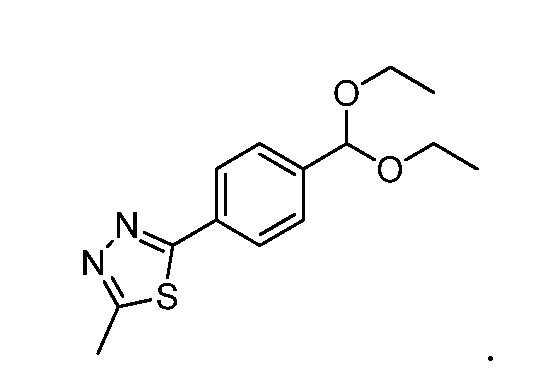
В еще одном варианте осуществления предпочтительное ацетальное промежуточное соединение имеет следующую структуру:
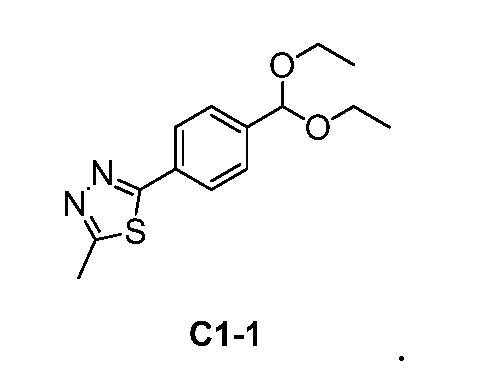
Примеры
Для того, чтобы настоящее изобретение могло быть более полно понято, приведены следующие примеры. Эти примеры приведены с целью иллюстрации вариантов осуществления настоящего изобретения и не должны истолковываться как ограничивающие объем изобретения каким-либо образом. Реагенты, используемые в приведенных ниже примерах, могут быть получены либо так, как описано в настоящем документе, или, если не описано в настоящем документе, являются либо коммерчески доступными или могут быть получены из коммерчески доступных материалов с помощью способов, известных в данной области техники.
Если не указано иное, растворители, температуры, давление и другие условия реакции могут быть легко выбраны средним специалистом в данной области. Как правило, ход реакции можно контролировать с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ), при желании, и промежуточные соединения и продукты могут быть очищены с помощью хроматографии и/или путем перекристаллизации или осаждения с обработкой или без обработки углеродом.
В одном из вариантов осуществления настоящее изобретение относится к многостадийному способу синтеза получения соединения 1001, как указано в примерах 1-8.
Пример 1
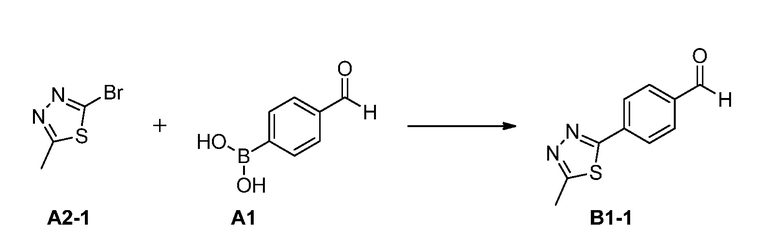
Смесь 2-бром-5-метил-1,3,4-тиадиазола A2-1 (13,1 г, 73,3 ммоль), (4-формилфенил)бороновой кислоты A1 (10,0 г, 66,7 ммоль), 2M K3PO4 (66,7 мл, 133,4 ммоль) в толуоле (150 мл) и этаноле (38 мл) нагревали до 55°С в атмосфере азота, затем дегазировали поочередно помещая под вакуумом и азотом три раза в течение нескольких минут каждый раз. Добавляли тетракис(трифенилфосфин)палладий (1,54 г, 1,33 ммоль) и затем смесь снова дегазировали. После нагревания в течение 18 часов при температуре 80°C и охлаждения до комнатной температуры, водный слой отделяли. Смесь промывали насыщенным солевым раствором и оставшийся органический слой уменьшали в объеме путем дистилляции. Добавление гептана обеспечило твердое вещество, которое собирали фильтрованием с получением 4-(5-метил-1,3,4-тиадиазол-2-ил)бензальдегида B1-1 в виде твердого вещества с выходом 85%.
Пример 2

B1-1 (1,05 г, 5,14 ммоль), EtOH (10 мл), CH(OEt)3 (1,1 эквив.) и моногидрат пара-толуолсульфоновой кислоты (5 моль%) нагревали при 67°C в течение 30 минут. Раствор охлаждали и добавляли насыщенный водный NaHCО3 (10 мл). Смесь переносили в делительную воронку с дихлорметаном (20 мл). Дополнительное количество воды растворило твердые частицы, и слои разделили. Органический слой концентрировали при пониженном давлении с получением смеси твердых веществ и масла. Смесь повторно растворяли в дихлорметане (10 мл) и раствор промывали водой (5 мл). Удаление растворителя дало C1-1a (1,29 г, выход 90%).
Пример 3
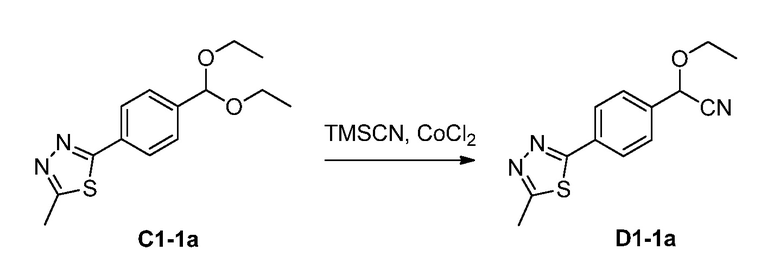
C1-1a (145 мг, 0,522 ммоль) перемешивали с TMSCN (100 мкл, 1,5 эквив.) и дихлорэтаном (1 мл), одновременно добавляли CoCl2(5 мг). Реакционную смесь нагревали при 60°С в течение 3,25 часов. Добавляли насыщенный водный раствор NaHCО3 (2 мл) и дихлорметан (5 мл). Слои разделяли и органический слой концентрировали при пониженном давлении с получением D1-1a в виде не совсем белого твердого вещества (104 мг, выход 77%).
Пример 4
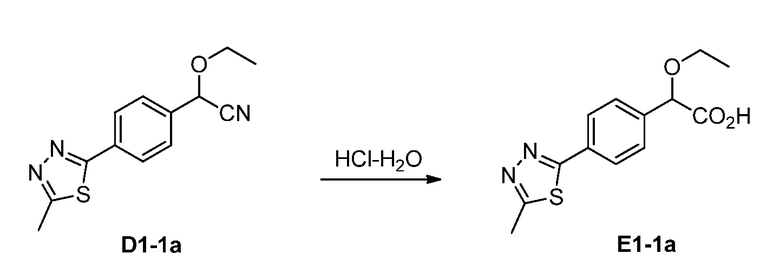
Смесь D1-1a (1,01 г, 3,90 ммоль), 1,2-дихлорэтана (5,0 мл), концентрированной HCl (2,0 мл) и воды (1,0 мл) нагревали до 70°C в течение 15 часов. После охлаждения до комнатной температуры, добавляли воду (1 мл). Органическую фазу отделяли и дополнительное количество воды (5 мл) добавляли к водному слою, затем экстрагировали дихлорметаном (2×10 мл). Первую органическую фазу объединяли с экстрактами дихлорметана, и смесь концентрировали при пониженном давлении с получением E1-1a в виде желтовато-коричневого твердого вещества (1,02 г, выход 94%).
Пример 5

В качестве альтернативы, стадии формирования E1-1a из B1-1a могут быть выполнены без выделения очищенных промежуточных соединений синтеза.
В реактор загружали В1-1а (100,4 г, 0,490 моль) с пара-толуолсульфоновой кислотой (каталитическое количество) и толуолом при комнатной температуре. Загружали этанол и триэтилортоформиат, с последующей промывкой толуолом. Загруженную смесь нагревали до температуры 45°С. Добавляли дополнительное количество пара-толуолсульфоновой кислоты (каталитическое количество), и нагревание продолжали в течение 2 часов. Добавляли безводный K2CO3 и смесь частично концентрировали в вакууме. Добавляли толуол и смесь снова частично концентрировали. Смесь фильтровали для удаления твердых веществ. Реактор и фильтр промывали толуолом.
К этому раствору загружали CoCl2 (каталитическое количество) и TMSCN при 20°С. Загруженную смесь нагревали при 75°С в течение ночи. К полученной смеси медленно загружали метил-трет-бутиловый эфир при 70-80°С. Загруженную смесь охлаждали до комнатной температуры, затем фильтровали и осадок промывали метил-трет-бутиловым эфиром и водой. Влажный отфильтрованный осадок сушили короткое время с получением 154,6 г D1-1a в виде влажного отфильтрованного осадка.
Влажный отфильтрованный осадок D1-1a загружали в реактор, затем концентрированную HCl и воду при температуре 20-25°С. Загруженную смесь нагревали до 60°С в течение 3,5 часов. Добавляли целит и ацетонитрил и смесь фильтровали через углерод Дарко G60 и целит. Фильтрат загружали в реактор и нагревали до 60-70°С. Медленно добавляли воду и затем охлаждали до 25°С. Твердое вещество собирали фильтрацией, промывали водой и сушили с получением 105 г E1-1а (выход 77%) в виде белого твердого вещества.
Пример 6
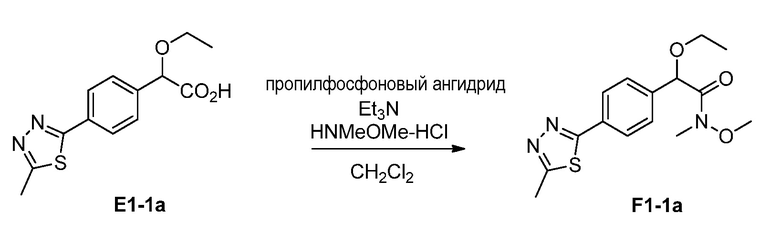
В реактор загружали E1-1a (117,2 г, 0,392 моль в виде гидрата, 6,3% воды) с гидрохлоридом Ν,Ο-диметилгидроксиламина (61,5 г, 1,5 эквив.) и дихлорметаном (936 мл). Смесь перемешивали с получением суспензии. Триэтиламин (272 мл) медленно загружали в течение 15 минут, результатом чего было небольшое выделение тепла. Пропилфосфоновый ангидрид (376 г в виде 50%-ного раствора в дихлорметане, 1,5 эквив.) медленно загружали в течение 1 часа. Загружали воду (470 мл) в течение 10 минут. Слои разделяли и водную фазу экстрагировали дихлорметаном. Органические фазы объединяли и промывали насыщенным раствором бикарбоната натрия, и 1 н раствором HCl. Партию концентрировали до некоторой степени при пониженном давлении. Добавляли изопропилацетат и смесь немного вновь концентрировали при пониженном давлении. Это повторяли дважды. Смесь нагревали, засевали при 50°С, добавляли гептан, затем смесь охлаждали до комнатной температуры. Твердое вещество собирали фильтрованием и промывали смесью изопропилацетат-гептан. F1-1a получали с выходом 88% и чистотой 99%.
Пример 7
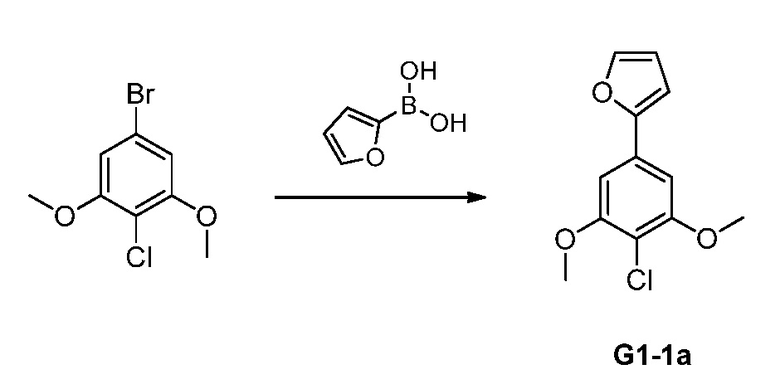
2-(4-Хлор-3,5-диметоксифенил)фуран G1-1a синтезировали в соответствии со способом, описанным в международной публикации заявки РСТ WO 2008/040669 следующим образом. В колбу, содержащую 3,5-диметокси-4-хлор-бромбензол (5 г, 20 ммоль), 2-фурилбороновую кислоту (2,45 г, 21,9 ммоль) и 2M Na2CO3 (25 мл) добавляли тетрагидрофуран (50 мл). Смесь дегазировали поочередно помещая под вакуум и азотом три раза в течение нескольких минут каждый. Добавляли тетракис(трифенилфосфин)палладий (0,46 г, 0,4 ммоль) и смесь снова дегазировали, затем нагревали при 60°C в течение 17 часов. Летучие вещества удаляли в вакууме, затем добавляли метанол (10 мл) и полученную суспензию перемешивали при 60°C в течение 2 часов. Смесь охлаждали до комнатной температуры, и собирали твердые вещества. Твердое вещество суспендировали в горячем метаноле, затем фильтровали и сушили с получением 2-(4-хлор-3,5-диметоксифенил)фурана (3,18 г, выход 67%).
Пример 8
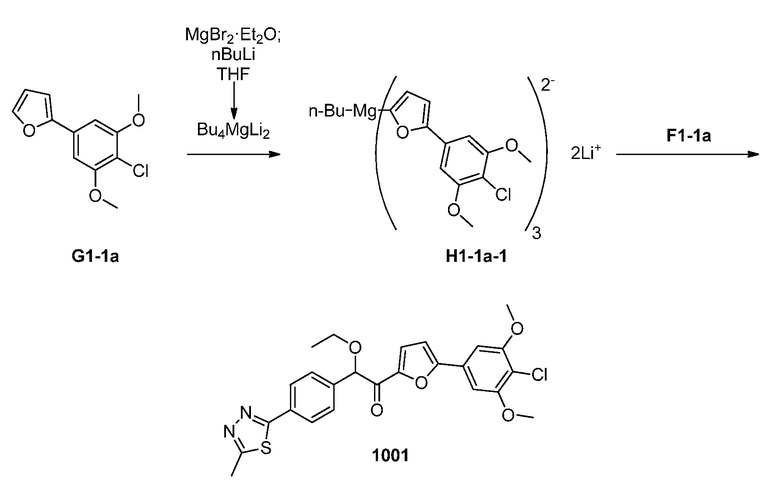
Все растворители дегазировали барботированием с N2 в течение как минимум 20 минут. Добавляли MgBr2⋅Et2O (3,91 г, 15,2 ммоль) к тетрагидрофурану (39,0 мл) в чистой сухой колбе (небольшой экзотермический эффект) с получением суспензии после охлаждения до комнатной температуры. Смесь охлаждали до -10°C и раствор н-BuLi (16,81 г, 2,62 М раствор в гексане) добавляли с помощью шприца в течение 34 минут. После перемешивания в течение 1 часа при -10°С, раствор G1-1а (11,61 г, 48,6 ммоль) в тетрагидрофуране (34,8 мл) добавляли в течение 60 минут при постоянной скорости. Раствор нагревали до комнатной температуры и хранили в атмосфере N2 в течение ночи.
В отдельную колбу добавляли раствор F1-1а (12,48 г, 38,9 ммоль) в толуоле (100,0 мл) и тетрагидрофуране (25,0 мл). Раствор охлаждали до -23°С и раствор аниона (полученный выше) добавляли в течение 2-х часов. Раствор уксусной кислоты (7,2 мл) в воде (67 мл) добавляли в течение 11 минут, в течение которых температура поднималась до -10°C. Реакционную смесь нагревали до 50°С и водную фазу удаляли. Добавляли воду (67 мл) и органическую фазу собирали и концентрировали при пониженном давлении. После хроматографии на силикагеле (70% изопропилацетат-гептан) получали 12,8 г соединения 1001 (выход 66%).
Пример 9
Синтез дополнительных репрезентативных соединений
Следующие репрезентативные соединения в таблице 1, синтезировали в соответствии с (i) вышеуказанными способами, путем выбора соответствующих исходных веществ и (ii) известными методами органического синтеза.


Следует принять во внимание, что, хотя конкретные варианты осуществления настоящего изобретения были описаны в настоящем документе в целях иллюстрации, различные модификации могут быть сделаны без отступления от сущности и объема настоящего изобретения. Соответственно, настоящее изобретение не ограничивается, за исключением прилагаемой формулы изобретения.
Все патенты США, опубликованные патентные заявки США, патентные заявки США, иностранные патенты, иностранные заявки на патент и непатентные публикации, упомянутые в настоящем описании, включены в настоящее описание в качестве ссылки, в полном объеме, в рамках, не противоречащих настоящему описанию.
Изобретение относится к области органической химии, а именно к способу получения соединения формулы (II), который включает преобразование бороновой кислоты A1 в карбальдегид B1 путем активации бороновой кислоты с активирующим веществом A2; преобразование карбальдегида B1 в ацеталь C1 кислотным катализом с источником ортоформиата; преобразование ацеталя C1 в нитрил D1 путем катализируемого цианирования с металлическим катализатором и источником цианида; гидролиз D1 с кислотой с получением карбоновой кислоты E1; преобразование карбоновой кислоты Е1 в амид F1 с основанием, связующим реагентом и источником амина; преобразование амида F1 в соединение формулы (II) с анионным связующим реагентом, имеющим структуру H1, где M представляет собой Mg; R, R2 и R3 каждый независимо представляет собой C(1-6)алкил; m равно 2; p равно 3; и при необходимости, преобразование соединения формулы (II) в соль. Также изобретение относится к промежуточным соединениям, соединению формулы Н1 и способу его получения, способу получения соединения формулы (III), частного случая соединения формулы (II). Технический результат: разработан новый способ получения соединений (II) и (III), полезных в качестве ингибитора PDE10. 9 н. и 59 з.п. ф-лы, 1 табл., 8 пр.
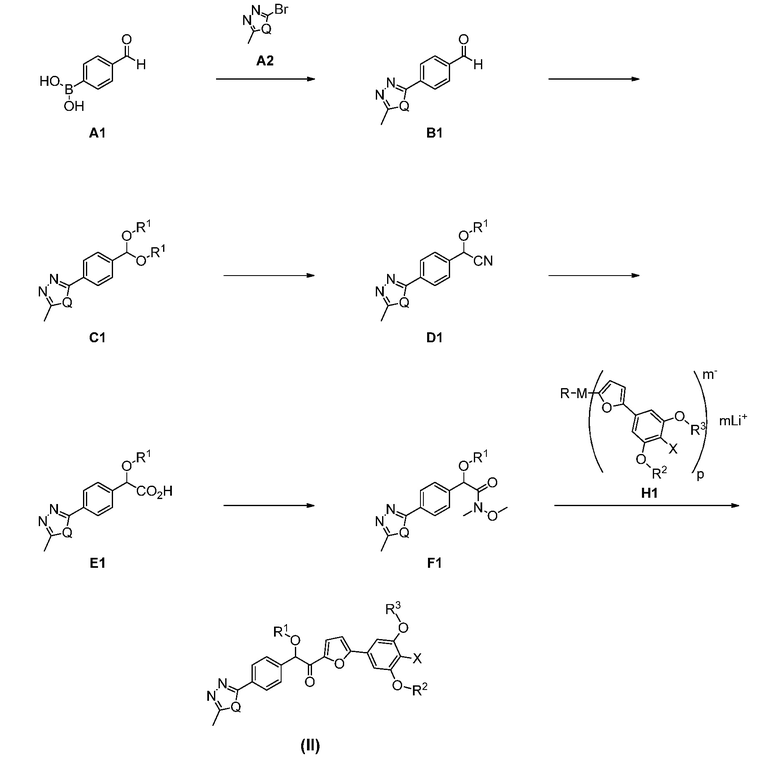
1. Способ получения соединения формулы (II):
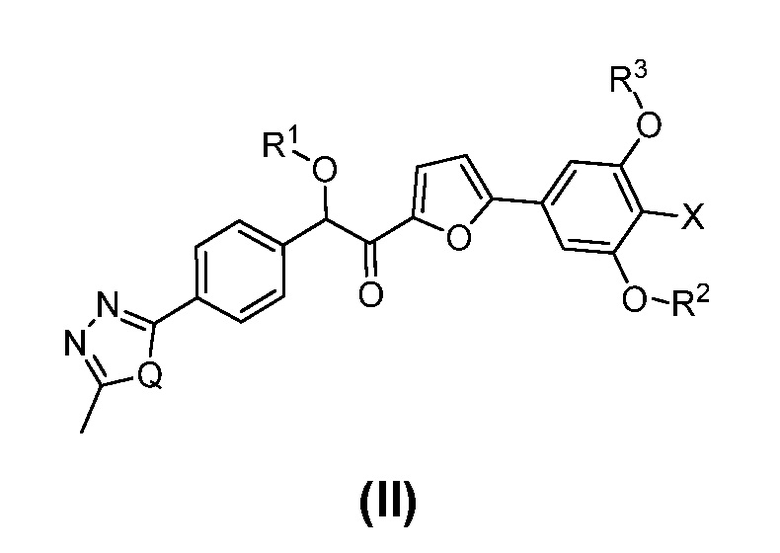
где
Q представляет собой S или O,
X представляет собой Cl или Br, и
R1, R2 и R3 каждый независимо представляет собой С(1-6)алкил,
согласно следующей общей схеме (I):

который включает:
преобразование бороновой кислоты A1 в карбальдегид B1 путем активации бороновой кислоты с активирующим веществом A2;
преобразование карбальдегида B1 в ацеталь C1 кислотным катализом с источником ортоформиата;
преобразование ацеталя C1 в нитрил D1 путем катализируемого цианирования с металлическим катализатором и источником цианида;
гидролиз D1 с кислотой с получением карбоновой кислоты E1;
преобразование карбоновой кислоты Е1 в амид F1 с основанием, связующим реагентом и источником амина;
преобразование амида F1 в соединение формулы (II) с анионным связующим реагентом, имеющим структуру H1,
где
M представляет собой Mg;
R, R2 и R3 каждый независимо представляет собой C(1-6)алкил;
m равно 2;
p равно3; и
при необходимости, преобразование соединения формулы (II) в соль.
2. Способ по п. 1, где Q представляет собой O.
3. Способ по п. 1, где Q представляет собой S.
4. Способ по любому из пп. 1-3, где X представляет собой Cl.
5. Способ по любому из пп. 1-3, где X представляет собой Br.
6. Способ по любому из пп. 1-5, где R1 представляет собой метил, этил или пропил.
7. Способ по любому из пп. 1-6, где R1 представляет собой этил.
8. Способ по любому из пп. 1-7, где R2 представляет собой метил, этил или пропил.
9. Способ по любому из пп. 1-8, где R2 представляет собой метил.
10. Способ по любому из пп. 1-9, где R3 представляет собой метил, этил или пропил.
11. Способ по любому из пп. 1-10, где R3 представляет собой метил.
12. Способ по любому из пп. 1-11, где R представляет собой бутил.
13. Способ по любому из пп. 1-12, где кислотный катализатор, используемый для образования ацеталя C1, представляет собой моногидрат пара-толуолсульфоновой кислоты.
14. Способ по любому из пп. 1-13, где источник ортоформиата представляет собой триэтилортоформиат.
15. Способ по любому из пп. 1-14, где металлический катализатор стадии цианирования представляет собой соль кобальта.
16. Способ по любому из пп. 1-15, где металлический катализатор стадии цианирования представляет собой CoCl2.
17. Способ по любому из пп. 1-16, где источник цианида представляет собой триметилсилил цианид.
18. Способ по любому из пп. 1-17, где кислота стадии гидролиза представляет собой HCl.
19. Способ по любому из пп. 1-18, где основание стадии амидирования представляет собой триэтиламин.
20. Способ по любому из пп. 1-19, где связующий реагент стадии амидирования представляет собой пропилфосфоновый ангидрид.
21. Способ по любому из пп. 1-20, где источник амина представляет собой гидрохлорид Ν,Ο-диметилгидроксиламина.
22. Способ по п.1, где соединение формулы (II) представляет собой:

23. Способ по п.1, где соединение формулы (II) представляет собой:

24. Способ по п.1, где соединение формулы (II) представляет собой:
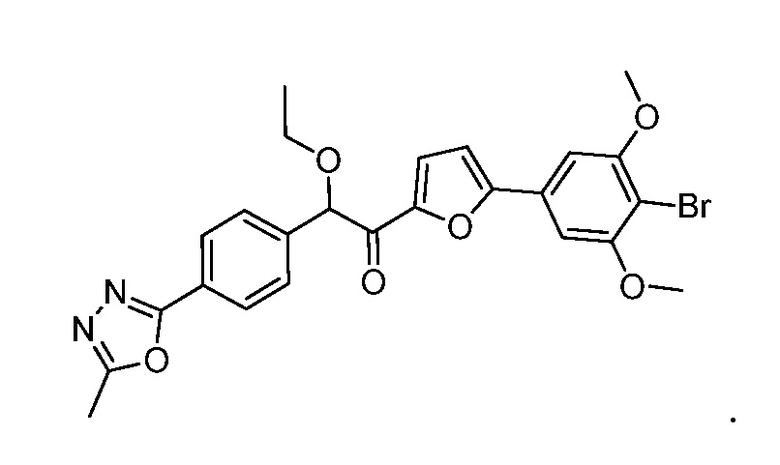
25. Способ получения соединения формулы H1:

где
M представляет собой Mg,
R, R2 и R3 каждый независимо представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 2, и
p равно 3;
согласно следующей общей схеме (II):
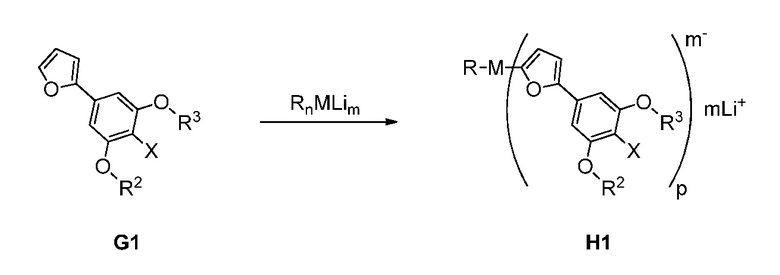
который включает:
получение в растворителе раствора литийалкильного металлического основания из Rn-Li и галогенида металла, содержащего M, где n равно 1, 2, 3 4 или 5; и
получение смешанного металл литиата H1 из G1 и литийалкильного металлического основания.
26. Способ по п. 25, где R2 представляет собой метил, этил или пропил.
27. Способ по п. 25 или 26, где R2 представляет собой метил.
28. Способ по любому из пп. 25-27, где R3 представляет собой метил, этил или пропил.
29. Способ по любому из пп. 25-28, где R3 представляет собой метил.
30. Способ по любому из пп. 25-29, где R представляет собой бутил.
31. Способ по любому из пп. 25-30, где X представляет собой Cl.
32. Способ по любому из пп. 25-31, где X представляет собой Br.
33. Способ по любому из пп. 25-32, где литийалкильное металлическое основание представляет собой литий алкилмагниевое основание.
34. Способ по любому из пп. 25-33, где литийалкильное металлическое основание представляет собой Bu4MgLi2.
35. Способ по любому из пп. 25-34, где соединение формулы H1 представляет собой:
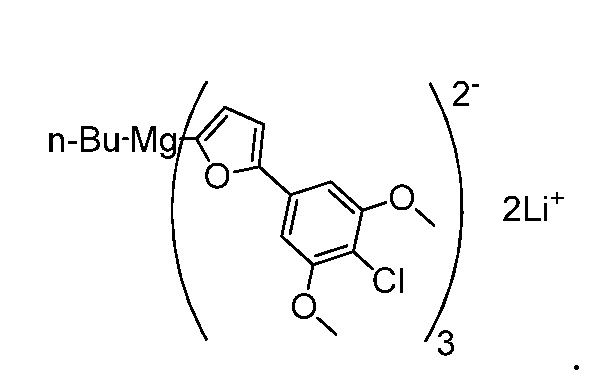
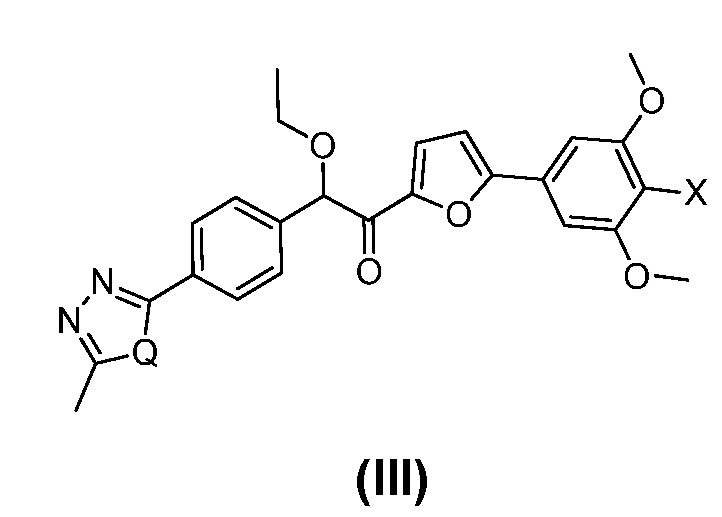
36. Способ получения соединения формулы (III):

где Q представляет собой S или O и X представляет собой Cl или Br,
согласно следующей общей схеме (III):
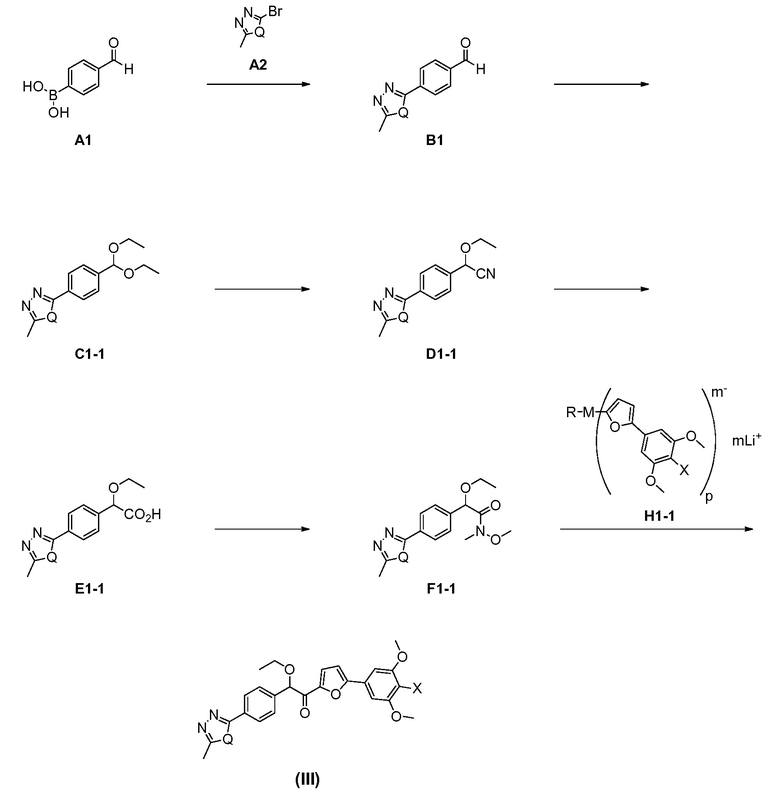
который включает:
преобразование бороновой кислоты A1 в карбальдегид B1 путем активации бороновой кислоты с активирующим веществом A2;
преобразование карбальдегида B1 в ацеталь C1-1 кислотным катализом с источником ортоформиата;
преобразование ацеталя C1-1 в нитрил D1-1 путем катализируемого цианирования с металлическим катализатором и источником цианида;
гидролиз D1-1 с кислотой с получением карбоновой кислоты E1-1;
преобразование карбоновой кислоты Е1-1 в амид F1-1 с основанием, связующим реагентом и источником амина;
преобразование амида F1-1 в соединение формулы (III) с анионным связующим реагентом, имеющим структуру H1-1,
где
M представляет собой Mg;
R представляет собой C(1-6)алкил;
m равно 2;
p равно 3; и
при необходимости, преобразование соединения формулы (III) в соль.
37. Способ по п. 36, где Q представляет собой O.
38. Способ по п. 36, где Q представляет собой S.
39. Способ по любому из пп. 36-38, где X представляет собой Cl.
40. Способ по любому из пп. 36-38, где X представляет собой Br.
41. Способ по любому из пп. 36-40, где R представляет собой бутил.
42. Способ по любому из пп. 36-41, где кислотный катализатор, используемый для образования ацеталя C1-1, представляет собой моногидрат пара-толуолсульфоновой кислоты.
43. Способ по любому из пп. 36-42, где источник ортоформиата представляет собой триэтилортоформиат.
44. Способ по любому из пп. 36-43, где металлический катализатор стадии цианирования представляет собой соль кобальта.
45. Способ по любому из пп. 36-44, где металлический катализатор стадии цианирования представляет собой CoCl2.
46. Способ по любому из пп. 36-45, где источник цианида представляет собой триметилсилил цианид.
47. Способ по любому из пп. 36-46, где кислота стадии гидролиза представляет собой HCl.
48. Способ по любому из пп. 36-47, где основание стадии амидирования представляет собой триэтиламин.
49. Способ по любому из пп. 36-48, где связующий реагент стадии амидирования представляет собой пропилфосфоновый ангидрид.
50. Способ по любому из пп. 36-49, где источник амина представляет собой гидрохлорид Ν,Ο-диметилгидроксиламина.
51. Способ по п. 36, где соединение формулы (III) представляет собой:
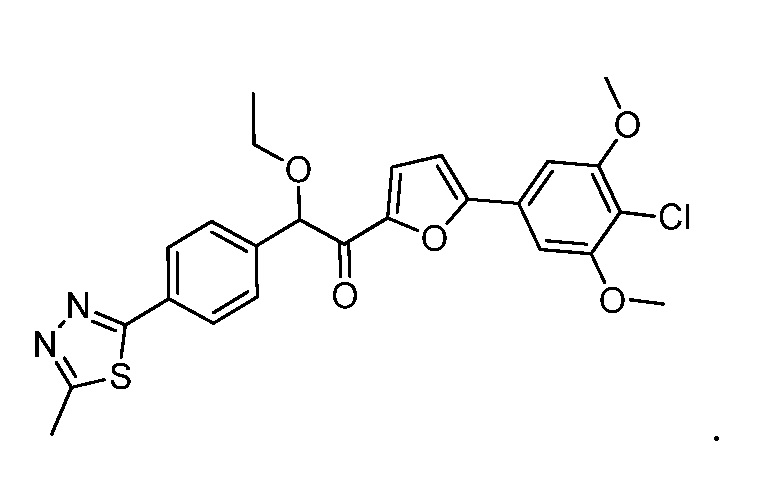
52. Способ по п. 36, где соединение формулы (III) представляет собой:
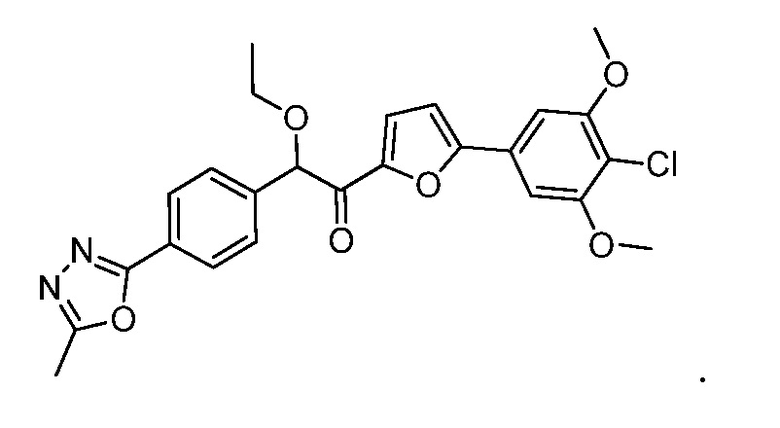
53. Способ по п. 36, где соединение формулы (III) представляет собой:

54. Способ получения соединения формулы H1-1:
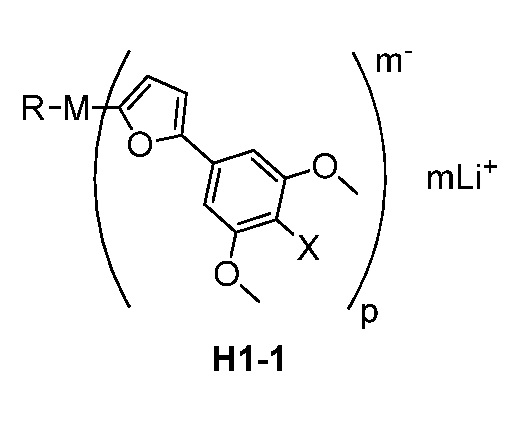
где
M представляет собой Mg,
R представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 2, и
p равно 3;
согласно следующей общей схеме (IV):
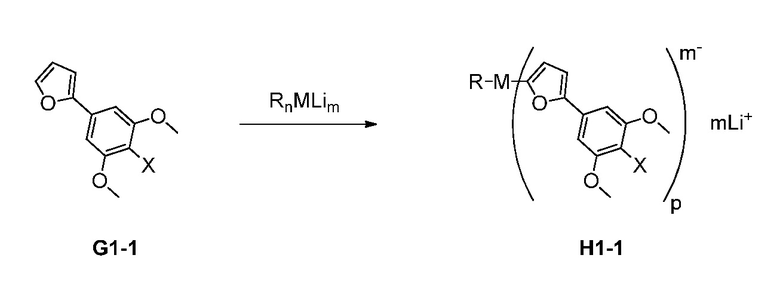
который включает:
получение в растворителе раствора литийалкильного металлического основания из Rn-Li и галогенида металла, содержащего M, где n равно 1, 2, 3 4 или 5; и
получение смешанного металл литиата H1-1 из G1-1 и литийалкильного металлического основания.
55. Способ по п. 54, где X представляет собой Cl.
56. Способ по п. 54, где X представляет собой Br.
57. Способ по любому из пп. 54-56, где R представляет собой бутил.
58. Способ по любому из пп. 54-57, где литийалкильное металлическое основание представляет собой литий алкилмагниевое основание.
59. Способ по любому из пп. 54-58, где литийалкильное металлическое основание представляет собой Bu4MgLi2.
60. Способ по любому из пп. 54-59, где соединение формулы H1-1 представляет собой:

61. Соединение, имеющее структуру формулы H1:
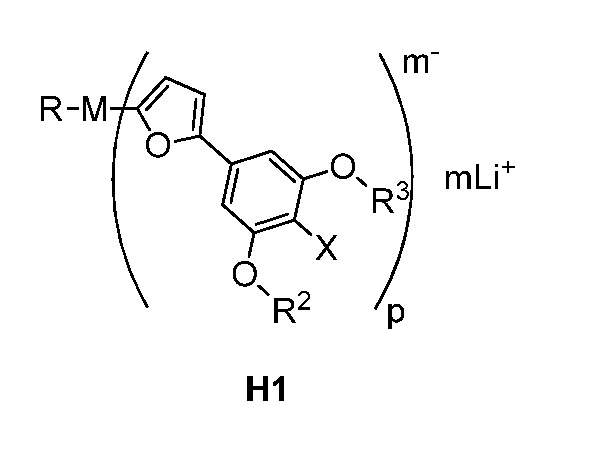
где
M представляет собой Mg R, R2 и R3 каждый независимо представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 2 и
p равно 3.
62. Соединение, имеющее структуру формулы H1-1:
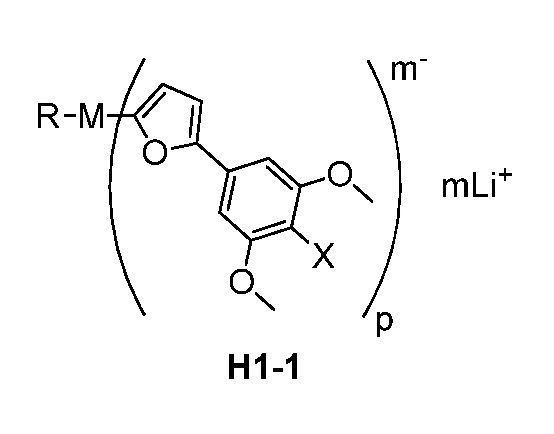
где
M представляет собой Mg,
R представляет собой C(1-6)алкил,
X представляет собой Cl или Br,
m равно 2, и
p равно 3.
63. Соединение, имеющее структуру формулы H1-1a:

где X представляет собой Cl или Br.
64. Соединение по любому из пп. 61-63, где X представляет собой Cl.
65. Соединение по любому из пп. 61-63, где X представляет собой Br.
66. Соединение по любому из пп. 61-64, имеющее следующую структуру:
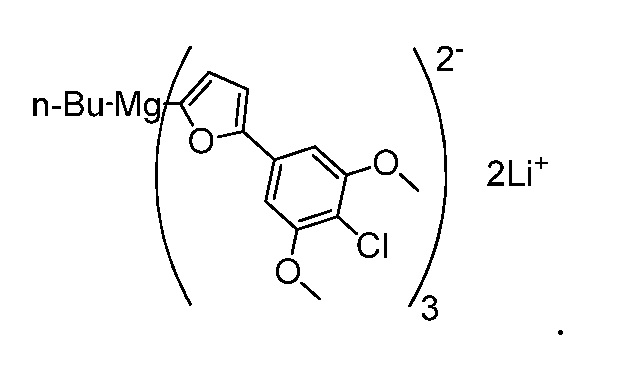
67. Соединение, имеющее следующую структуру:

68. Соединение, имеющее следующую структуру:
| RU 2012143610 A, 20.04.2014. |
Авторы
Даты
2020-04-15—Публикация
2015-04-24—Подача